Настоящее изобретение относится к анализу взаимодействий между молекулами.
Предшествующий уровень техники
Однонуклеотидные полиморфизмы (single nucleotide polymorphism, SNP) общепризнаны в качестве важной причины варьирования биологических функций. Хотя SNP могут оказывать важное влияние, наибольшее генетическое разнообразие наблюдается в некодирующих последовательностях ДНК. Кроме важности SNP в генетике человека, обнаружение SNP является важным также в области инфекционных заболеваний. Генотипирование является важным индикатором инфекций, вызываемых вирусом папилломы человека (HPV). В настоящее время семейство HPV содержит более тысячи генотипов, которые можно классифицировать в различные группы, включающие в себя важные для человека патогены (de Villiers et al, 2004). В частности, известно, что типы HPV высокого риска индуцируют рак шейки матки. Поэтому распознавание этих типов высокого риска требует надежных способов диагностики, делающих возможным наиболее адекватное лечение.
Анализы нуклеиновых кислот основаны на детекции специфических последовательностей ДНК или РНК. Целевые нуклеиновые кислоты, например полученные из клинических образцов, можно распознавать мечеными детекторными зондами. Специфичность анализа определяется специфичностью процесса гибридизации между мишенью и зондом. Однако обнаружение SNP требует максимального уровня специфичности. Кроме того, в настоящее время имеется много методик обнаружения SNP (например, гибридизация, секвенирование и масс-спектрометрический анализ), но ни один из них не объединяет эффективно высокую производительность и скрининг SNP с высокой плотностью. Тем не менее необходимость в таких способах растет.
Применение гранул (или микрогранул), таких как сферические гранулы, также обозначенные в данном описании как микросферы, в мультиплексном анализе было описано ранее, например, в Dunbar SA (Заявки на технологию под торговой маркой Luminex™(R) xMAP для быстрой высокопроизводительной мультиплексной детекции нуклеиновых кислот. Clin Chim Acta. 2005 Aug 15); [опубликовано в электронном виде до выхода из печати], Clin Chim Acta. 2006 Jan; 363(1-2):71-82, см.http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=pubmed&dopt=Abstract&list_uids=16102740&query h1=1) и веб-сайт информации о продуктах LuminexТМ (www.LuminexТМcorp.com). Система LuminexТМ представляет собой мультиплексную (матричную) технологию на основе гранул, которая оказалась очень эффективной для анализа множественных параметров или аналитов в одном образце (Dunbar et al, 2005). Она выдает результаты для многих биоаналитических форматов, включая анализы нуклеиновых кислот, анализы лиганд-рецепторных взаимодействий, иммуноанализы и ферментативные анализы.
Применение микроматриц на гранулах в жидкой фазе (liquid bead microarrays) для детекции HPV обсуждается в Wallace J et al, ("Facile, comprehensive, high-throughput genotyping of human genital papillomaviruses using spectrally addressable liquid bead microarrays." J Mol Diagn. 2005 Feb; 7(1)72-80).
Хотя протоколы и материалы для систем типа LuminexТМ известны и опубликованы и приведены на веб-сайте Luminex, существует дополнительная потребность в улучшении таких методик и материалов. Например, авторы изобретения обнаружили, что некоторые стандартные протоколы для применения микроматриц на гранулах в жидкой фазе не эффективны для разных SNP в маленьких мишенях или для систем, где имеются множественные точечные мутации, которые не всегда находятся в середине зонда. Для системы ТМАС, обычно используемой в Luminex, также рекомендуется постоянная длина зонда в пределах данной мультиплексной реакции. Более того, ТМАС является токсичной и нестабильной при повышенных температурах.
Настоящее изобретение направлено на такую потребность в улучшениях зонда и протокола, подходящих для применения с системами анализа на основе гранул, такими как Luminex.
Изложение сущности изобретения
Настоящее изобретение относится к способу детекции любого взаимодействия между зондом и целевой нуклеиновой кислотой, включающему следующие стадии:
1) денатурация любой двухцепочечной полинуклеиновой кислоты-мишени, присутствующей в образце;
2) гибридизация денатурированной мишени с зондом в условиях, которые позволяют осуществиться специфической гибридизации между зондом и мишенью;
3) возможно жесткая промывка;
4) добавление репортерной молекулы и инкубация с ней, делающие возможным детекцию связывания зонда с мишенью;
5) возможно промывка; и
6) детекция связывания зонда с мишенью,
где указанный способ включает одну или более из следующих дополнительных стадий:
а) поддержание температуры гибридизация после стадии гибридизации между зондом и мишенью после стадии (2);
б) применение стадии разведения-промывки сразу после стадии гибридизации (2);
в) поддержание температуры гибридизации во время любой жесткой промывки на стадии (3);
г) встряхивание или перемешивание при нагревании на стадии (2), например, с использованием термомиксера на стадии (2);
е) поддержание температуры гибридизации во время инкубации с репортерной молекулой на стадии (4);
В одном из аспектов температуру гибридизации поддерживают, начиная со стадии (2) до тех пор, пока не завершится реакция с репортерной молекулой на стадии (4).
В одном из аспектов осуществляют стадии (а) и (в), т.е. температуру гибридизации поддерживают после стадии гибридизации между зондом и мишенью и во время стадии жесткой промывки на стадии (3).
В другом аспекте зонд связывают с подложкой в виде частиц, такой как гранула.
Изобретение также относится к зонду, подходящему для связывания с подложкой в виде частиц, такой как гранула, содержащей:
а) связывающую группу (такую как группа NH2), которая делает возможным связывание (такое как ковалентное связывание) зонда с поверхностью подложки в виде частиц;
б) спейсер; и
в) мишень-специфическую олигонуклеотидную последовательность зонда,
где спейсер содержит:
1) олигонуклеотидный спейсер из по меньшей мере 15 нуклеотидов, такой как спейсер из повторов тимина или спейсер, содержащий повторяющийся блок TTG, между мишень-специфической последовательностью зонда и связывающей группой; и возможно
2) углеродный спейсер из 3-50 или 13-50 углеродных звеньев, соответственно С18-спейсера, между мишень-специфической последовательностью зонда и связывающей группой.
В одном из аспектов спейсер находится на 3′-конце мишень-специфической последовательности зонда.
В другом аспекте спейсер находится на 5′-конце мишень-специфической последовательности зонда.
Изобретение также относится к набору зондов, описанных в данной заявке, который содержит по меньшей мере две разные, мишень-специфические последовательности зонда, связанные с разными подложками в виде частиц, отличающимися друг от друга, например, благодаря разным меткам, таким как флуоресцентные метки или штрих-коды.
Изобретение также относится к набору от 2 до 1000, например от 2 до 50 разных мишень-специфических зондов, где каждый зонд содержит:
а) связывающую группу, которая делает возможным связывание зонда с твердой подложкой;
б) спейсер; и
в) мишень-специфическую олигонуклеотидную последовательность зонда,
где спейсер содержит один или оба из следующего:
1) углеродный спейсер из 13-50 углеродных звеньев между мишень-специфической последовательностью зонда и группой, связывающейся с подложкой; и
2) олигонуклеотидный спейсер из по меньшей мере 15 нуклеотидов между мишень-специфической последовательностью зонда и группой, связывающейся с подложкой, где этот олигонуклеотидный спейсер не гибридизуется с мишенью или с фланкирующим участком данной мишени.
Изобретение также относится к спейсерным последовательностям как таковым, как определено в любом аспекте данного изобретения.
Изобретение также относится к наборам, содержащим спейсерную молекулу по изобретению и подложку в виде частиц, такую как гранула.
Изобретение также относится к набору, содержащему спейсерную молекулу по изобретению и инструкции по связыванию с подложкой в виде частиц, такой как гранула.
Изобретение также относится к подложке в виде частиц, такой как гранула, связанной с зондом, как определено в данном описании.
Изобретение также относится к набору, содержащему подложку в виде частиц, такую как гранула, связанная со спейсерной молекулой по изобретению, и инструкции для применения в детекции молекулы-мишени.
Изобретение также относится к набору, содержащему подложку в виде частиц, такую как гранула, связанную с зондом по изобретению, и инструкции для применения в детекции молекулы-мишени.
Изобретение также относится к набору, содержащему зонд, где указанный зонд содержит:
а) связывающую группу, которая делает возможным связывание зонда с поверхностью подложки в виде частиц;
б) спейсер; и
в) мишень-специфическую олигонуклеотидную последовательность зонда,
где спейсер содержит один или оба из следующего:
1) углеродный спейсер из 13-50 углеродных звеньев между мишень-специфической последовательностью зонда и группой, связывающейся с подложкой; и
2) олигонуклеотидный спейсер из по меньшей мере 15 нуклеотидов между мишень-специфической последовательностью зонда и группой, связывающейся с подложкой;
и подложку в виде частиц, такую как полистирольные гранулы.
Изобретение также относится к набору, содержащему зонд, где указанный зонд содержит:
а) связывающую группу, которая делает возможным связывание зонда с поверхностью подложки в виде частиц;
б) спейсер; и
в) мишень-специфическую олигонуклеотидную последовательность зонда,
где спейсер содержит один или оба из следующего:
1) углеродный спейсер из 13-50 углеродных звеньев между мишень-специфической последовательностью зонда и группой, связывающейся с подложкой; и
2) олигонуклеотидный спейсер из по меньшей мере 15 нуклеотидов между мишень-специфической последовательностью зонда и группой, связывающейся с подложкой;
и инструкции по связыванию с подложкой в виде частиц, такой как полистирольные гранулы.
Графические материалы
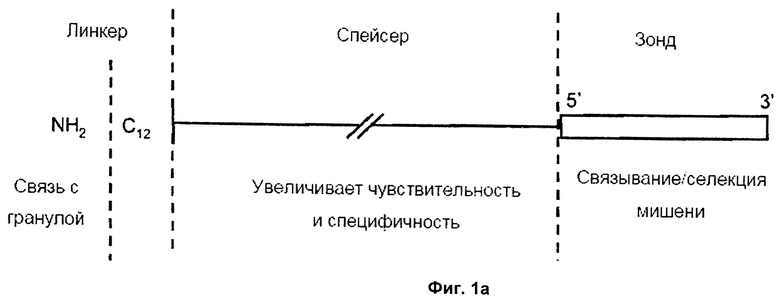
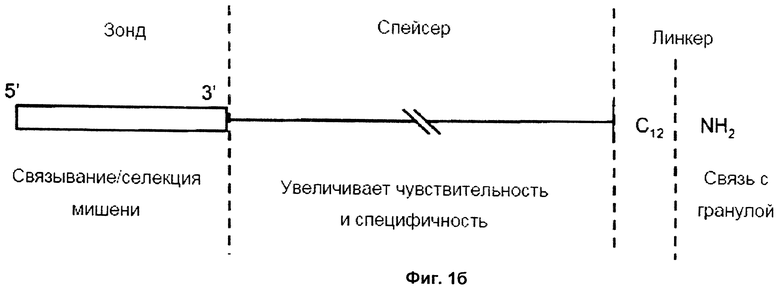
На Фиг.1а и 1б дана общая схема конструкции зонда и спейсера.
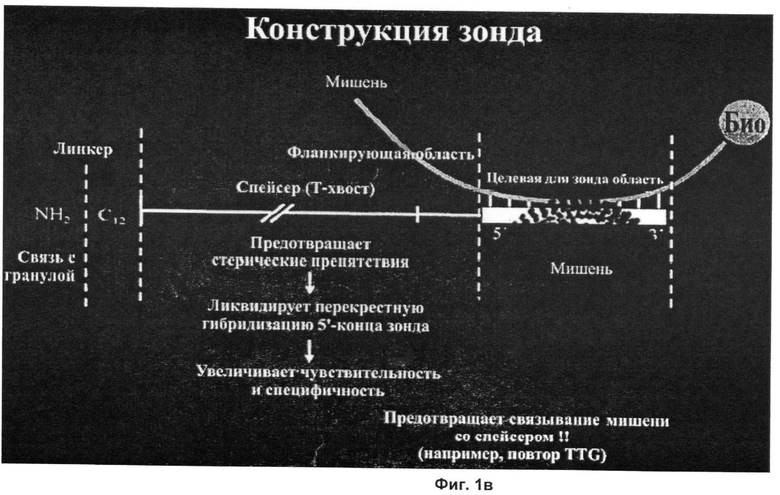
На Фиг.1в она дополнительно разработана.
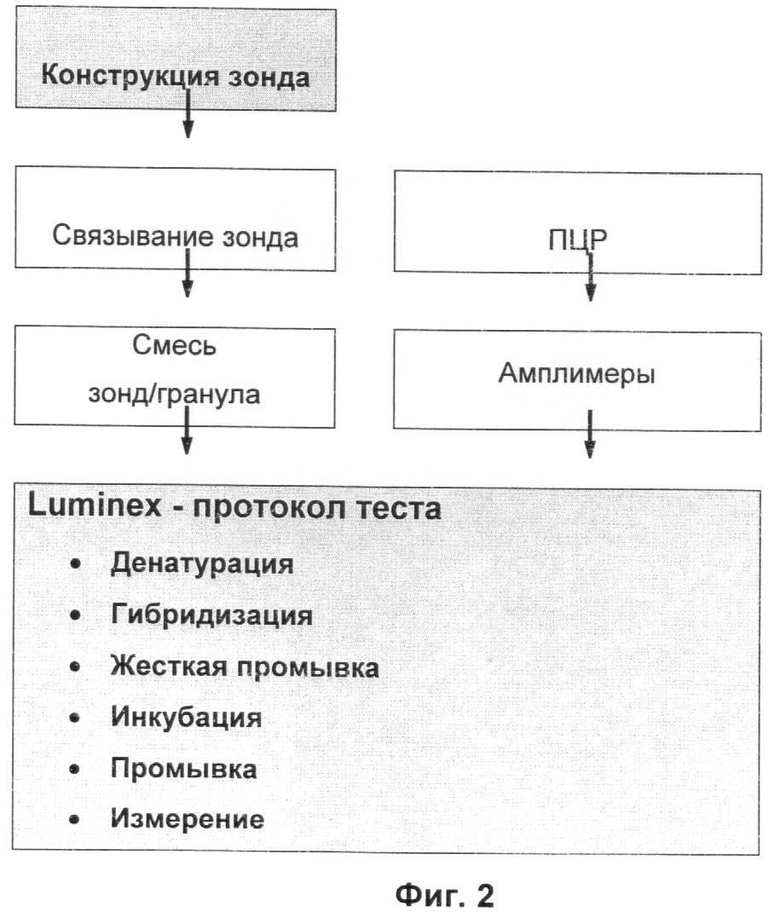
На Фиг.2 дана схема протокола анализа для системы детекции на основе гранул.
Подробное описание
В настоящем изобретении предложены улучшения в протоколах и реагентах, используемых в стандартном анализе на основе суспензии гранул для детекции нуклеиновых кислот, таком как анализ на основе Luminex™.
Подложки в виде частиц для применения в настоящем изобретении включают, в частности, гранулы, которые включают, например, сферические гранулы или цилиндрические гранулы. Гранулы можно обозначать также как микрогранулы или гранулы для применения в микрочипах. Описание данного изобретения в отношении гранул также применимо к другим подложкам в виде частиц для применения в данном изобретении.
Гранулы для применения в настоящем изобретении, которые включают описанные в данной заявке микросферы, соответственно представляют собой гранулы, которые подходят для применения в проточном цитометрическом анализе. Эти гранулы соответственно способны связываться с зондом для детекции взаимодействия между зондом и мишенью. В одном из аспектов гранулы мечены уникальной флуоресцентной молекулой или комбинацией молекул. Соответственно, мета на гранулах или в гранулах может быть идентифицирована с использованием лазерного возбуждения одного или более флуорохромов в грануле. В одном из аспектов гранула представляет собой полистирольную гранулу. В другом аспекте гранула представляет собой стеклянную гранулу.
Например, система Luminex хМАР включает 5,6 мкм полистирольные микросферы, которые окрашиваются внутри двумя спектрально различными флуорохромами (см. выше Dunbar et al). Такие гранулы подходят для применения в настоящем изобретении.
Другие системы мечения гранул для применения в данном изобретении включают в себя штрих-коды или цифровые голографические элементы, например меченые штрих-кодом цилиндрические гранулы от Illumina Inc. Штрих-коды или цифровые голографические элементы можно использовать в качестве альтернативы флуоресцентным меткам.
Например, система Illumina VeraCode включает цилиндрические стеклянные микрогранулы размером 240 мкм в длину на 28 мкм в диаметре, которые имеют встроенные в них цифровые голографические элементы для создания уникальных типов гранул. При возбуждении лазером каждая гранула VeraCode излучает уникальное кодовое изображение, которое может быть специфически обнаружено.
В одном из аспектов данного изобретения гранулы также могут иметь магнитные или парамагнитные свойства.
Обычно гранулы являются подходящими для применения в мультиплексной системе для одновременной детекции любого взаимодействия между множеством возможных мишеней и множеством зондов.
В примерах в данном описании использованы мишени, представляющие собой вирус папилломы человека (HPV), и зонды к нему, но разработанные принципы могут быть по существу использованы для детекции полинуклеиновой кислоты из любого источника.
Стандартные методики молекулярной биологии раскрыты в Sambrook et al, (Molecular Cloning. A Laboratory Manual. Cold Spring Harbour Press, third edition). Детали, например, принципов и параметров, относящихся к гибридизации между зондами и мишенью, и амплификации полинуклеиновой кислоты-мишени раскрыты в ЕР1012348, включенном в данное описание посредством ссылки.
Зонды
Зонд обычно содержит (1) связывающую группу (такую как группа NH2), которая делает возможным (соответственно ковалентное) связывание зонда с поверхностью гранулы, (2) спейсер, который служит для создания расстояния между поверхностью гранулы и специфической последовательностью зонда, и (3) мишень-специфическую олигонуклеотидную последовательность зонда (которую также можно обозначить в данном описании как мишень-специфическую последовательность зонда).
В одном из аспектов зонды имеют первичную аминогруппу, подходящую для связывания с карбоксильной группой на грануле или другой подложке.
В одном из аспектов изобретение относится к зондам, которые содержат специфические к мишени, представляющей собой HPV, последовательности зонда, такие как опубликованные наборы зондов SPF10 (см. ЕР1012348, включен в данное описание посредством ссылки), например, к HPV, или к любому зонду или комбинации зондов, описанному(ых) в данной заявке, в частности в Примере 13, возможно связанному(ых) с полиуглеродным повтором.
В одном из аспектов изобретение является подходящим для идентификации SNP, имеющих место в пределах короткого фрагмента целевой нуклеиновой кислоты, обычно фрагмента ДНК, амплифицированной из образца, такого как фрагмент длиной 20-50 оснований, такой как 20-30 оснований, такой как 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50 оснований.
В другом аспекте изобретение способно различать ошибочные спаривания, которые находятся в иных, чем середина зонда, положениях. В одном из аспектов изобретение можно использовать для различения ошибочных спариваний, которые находятся на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 оснований или даже более от центра зонда. В одном из аспектов изобретение можно использовать для различения ошибочных спариваний, которые находятся на 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 оснований или даже более от любого конца зонда, соответственно на 3-10 оснований.
Зонды по настоящему изобретению делают возможным различение мишени и не-мишени в сайтах, близких к концу зонда, что делает возможным зондирование коротких целевых фрагментов на присутствие множества разных SNP.
Спейсеры на основе атомов углерода и комбинации с олигонуклеотидными спейсерами
В одном из аспектов данного изобретения зонд содержит углеродный спейсер из 3-50 или 13-50 углеродных звеньев, в одном из аспектов С20-С50 спейсер, такой как С20-С40 спейсер или такой как С20-С30 спейсер, между мишень-специфической последовательностью зонда и связывающей группой. Можно использовать любой подходящий спейсер, такой как С13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или С50 спейсер. Соответствующий спейсер может быть выбран с использованием стандартных методов по эффекту на специфичность связывания и интенсивность сигнала для получения оптимального результата.
В одном из аспектов данного изобретения зонд содержит олигонуклеотидный спейсер, дополнительно к углеродному спейсеру, где олигонуклеотидный спейсер содержит по меньшей мере 15 нуклеотидов или по меньшей мере 20 нуклеотидов, таких как из 15-150 или 20-150 нуклеотидов, например 25-100 нуклеотидов, 30-75 нуклеотидов, включая 15-20, 20-25, 25-30, 30-35, 35-40, 40-45 и 45-50 нуклеотидов. Олигонуклеотидный спейсер может представлять собой, например, гомополимер или гетерополимер. В одном из аспектов олигонуклеотидный спейсер представляет собой политиминовый (поли-Т) спейсер или спейсер, содержащий другие подходящие повторяющиеся нуклеотидные звенья, такой как (TTG) повторяющийся спейсер, или поли-А (аденин) спейсер, или поли-G спейсер, или поли-С спейсер. Другие гетерополимерные спейсеры, которые могут быть подходящими, включают в себя повторы TTTG, AAG, AAC, AAAG или АААС. Разные спейсеры могут быть протестированы для оптимизации взаимодействий зонд-мишень с использованием рутинных способов, хорошо известных в данной области.
Таким образом, в одном из аспектов в данном изобретении в общем предложен зонд, содержащий как углеродный спейсер, так и олигонуклеотидный спейсер.
В одном из аспектов олигонуклеотидный спейсер находится между углеродным спейсером и специфической последовательностью зонда. В таком случае углеродный спейсер может быть короче в длину, чем 13 атомов углерода, таким как С12, или даже короче.
В одном из аспектов олигонуклеотидный спейсер выбран так, что он не гибридизуется с последовательностью-мишенью или фланкирующим участком данной последовательности-мишени. В одном из аспектов олигонуклеотидный спейсер выбран так, что он не гибридизуется с последовательностью-мишенью или с фланкирующим участком данной последовательности-мишени при использовании в описанном в данной заявке способе.
В одном из аспектов олигонуклеотидный спейсер выбран так, что участок спейсера, который фланкирует мишень-специфический зонд, не гибридизуется с последовательностью-мишенью или с фланкирующим участком данной последовательности-мишени. Это проиллюстрировано на Фиг.1в.
Полиуглеродные спейсеры раскрыты в Cowan et al (Transfer of a Mycobacterium tuberculosis genotyping method, Spoligotyping, from a reverse line-blot hybridization, membrane-based analysis to the Luminex multianalyte profiling system. J Clin Microbiol. 2004 Jan; 42(1):474-7) и Taylor et al (Taylor JD, Briley D, Nguyen Q, Long K, lannone MA, Li MS, Ye F, Afshari A, Lai E, Wagner M, Chen J, Weiner MP. Flow cytometric platform for high - throughput single nucleotide polymorphism analysis. Biotechniques. 2001 Mar; 30(3):661-6, 668-9).
Углеродные спейсеры представляют собой соответственно (СН2)n-спейсеры.
Олиго-спейсеры
Таким образом, в одном из аспектов в данном изобретении предложен зонд, содержащий только олигонуклеотидный спейсер между группой, связывающейся с гранулой, и мишень-специфической последовательностью зонда (т.е. в отсутствие углеродного спейсера).
В одном из аспектов этот спейсер содержит по меньшей мере 15 нуклеотидов или по меньшей мере 20 нуклеотидов. В одном из аспектов этот спейсер состоит из 15-150 или 20-150 нуклеотидов, например 25-100 нуклеотидов, 30-75 нуклеотидов, включая 15-20, 20-25, 25-30, 30-35, 35-40, 40-45 и 45-50 нуклеотидов.
Олигонуклеотидный спейсер может быть, например, гомополимером или гетерополимером. В одном из аспектов олигонуклеотидный спейсер представляет собой политиминовый спейсер (поли-Т) или спейсер, содержащий другие подходящие повторяющиеся нуклеотидные блоки, такой как спейсер, представляющий собой повторы (TTG), или спейсер, представляющий собой поли-А (аденин), или спейсер, представляющий собой поли-G, или спейсер, представляющий собой поли-С. Другие гетерополимерные спейсеры, которые могут быть подходящими, включают в себя повторы TTTG, AAG, ААС, AAAG или АААС. Разные спейсеры могут быть протестированы для оптимизации взаимодействий зонд - мишень с использованием рутинных способов, хорошо известных в данной области.
Таким образом, в одном из аспектов в данном изобретении предложен зонд, содержащий олигонуклеотидный спейсер между группой, связывающейся с гранулой, и мишень-специфической последовательностью зонда, где олигонуклеотидный спейсер представляет собой политиминовый (поли-Т) спейсер.
Таким образом, в одном из аспектов в данном изобретении предложен зонд, содержащий олигонуклеотидный спейсер между группой, связывающейся с гранулой, и мишень-специфической последовательностью зонда, где олигонуклеотидный спейсер представляет собой спейсер с повторами TTG или поли-А спейсер.
В одном из аспектов спейсер (либо углеродный+олигонуклеотидный спейсер, либо только олигонуклеотидный спейсер) находится на 3′-конце мишень-специфической последовательности зонда. В другом аспекте спейсер находится на 5′-конце мишень-специфической последовательности зонда.
В одном из аспектов олигонуклеотидный спейсер выбран так, что он не гибридизуется с последовательностью-мишенью или фланкирующим участком данной последовательности-мишени. В одном из аспектов олигонуклеотидный спейсер выбран так, что он не гибридизуется с последовательностью-мишенью или с фланкирующим участком данной последовательности-мишени при использовании в описанном в данной заявке способе.
В одном из аспектов олигонуклеотидный спейсер выбран так, что область спейсера, которая фланкирует мишень-специфический зонд, не гибридизуется с последовательностью-мишенью или с фланкирующим участком данной последовательности-мишени. Это проиллюстрировано на Фиг.1в.
В другом аспекте изобретение относится к набору зондов, содержащему по меньшей мере 2 зонда, соответственно включающему любой зонд или любые зонды по настоящему изобретению, где по меньшей мере один зонд связан с гранулой или спейсером через 5′-конец зонда и где по меньшей мере один зонд связан с гранулой или спейсером через 3′-конец зонда.
Спейсерные последовательности
Изобретение также относится к спейсерным последовательностям, подходящим для применения с жидкостными системами детекции на основе гранул. Спейсеры согласно изобретению могут представлять собой любые спейсеры, описанные в данной заявке. Спейсеры могут содержать, например, полиуглеродный повтор (например, С12-С30) и олигонуклеотидный повтор (например, поли-Т, или поли-(TTG), или поли-А длиной 15-150 или 20-150 нуклеотидов), связанные вместе и подходящие для присоединения к мишень-специфической последовательности зонда, или состоять из них.
Спейсеры по изобретению также могут содержать олигонуклеотидный повтор общей длиной 15-150, или 20-150, или 25-150 нуклеотидов или состоять из них.
Спейсеры соответственно содержат связывающую группу, такую как первичная аминогруппа, подходящая для присоединения к грануле.
Настоящее изобретение также относится к спейсерной молекуле по изобретению, связанной с гранулой.
Изобретение также относится к спейсерной молекуле по изобретению, связанной с мишень-специфической последовательностью зонда и, возможно, также связанной с гранулой.
Наборы
Изобретение также относится к набору, содержащему спейсерную молекулу по изобретению и подложку в виде частиц, такую как гранула.
Изобретение также относится к набору, содержащему спейсерную молекулу по изобретению и инструкции по связыванию с подложкой в виде частиц, такой как гранула.
Изобретение также относится к набору, содержащему спейсерную молекулу по изобретению, связанную с подложкой в виде частиц, такой как гранула, с инструкциями по связыванию с мишень-специфической последовательностью зонда.
Изобретение также относится к набору, содержащему зонд по настоящему изобретению, связанный с подложкой в виде частиц, такой как гранула, и инструкции по применению в детекции мишени.
Способ
Настоящее изобретение также относится к некоторым улучшениям способа, внесенным в существующие протоколы для детекции взаимодействий зонд - мишень на уровне нуклеиновой кислоты при использовании технологии на основе гранул.
Технологии на основе гранул, такие как технология Luminex, хорошо описаны в данной области и литературе. Гранулы, также обозначаемые как микросферы, соответственно представляют собой полистирольные гранулы, как описано в Dunbar et al и в ссылках там, которые все, таким образом, включены в данное описание посредством ссылки.
Общий способ по изобретению представляет собой стандартную схему детекции любого взаимодействия между зондом, соответственно таким зондом, как определено в данном описании, и целевой нуклеиновой кислотой. Этот способ соответственно содержит следующие стадии:
1) денатурация любой полинуклеиновой кислоты-мишени, присутствующей в образце;
2) гибридизация мишени с зондом в условиях, которые позволяют осуществиться специфической гибридизации между зондом и мишенью;
3) возможно жесткая промывка для удаления по существу всех несвязанных веществ;
4) добавление репортерной молекулы и инкубация с ней, чтобы сделать возможным детекцию связывания зонда с мишенью;
5) возможно промывка; и
6) детекция связывания зонда с мишенью.
Подробный пример такого протокола дан в содержащихся в данном описании примерах.
Общие стадии являются соответственно последовательными, но в одном из аспектов некоторые стадии можно осуществлять вместе, например зонд подвергают взаимодействию одновременно с мишенью и репортерной молекулой.
Специфическая гибридизация зонда с целевой нуклеиновой кислотой обычно означает, что указанный зонд формирует дуплекс с частью этой целевой области или со всей целевой областью в используемых экспериментальных условиях, и что в тех же условиях указанный зонд не образует дуплекс с другими областями полинуклеиновых кислот, присутствующих в анализируемом образце.
Жесткие условия промывки хорошо известны в данной области и включают, например, 3×SSC, 0,1% саркозила при 50°С и те условия, которые описаны в данной заявке в примерах.
Промывку на стадии (5) осуществляют в любых подходящих условиях, хорошо известных в данной области, что позволяет удалять избыток репортерной молекулы, например. В одном из аспектов изобретения промывку осуществляют в присутствии пониженной концентрации SSC по сравнению с концентрацией, используемой на стадии промывки, такой как по существу 2×SSC, 1,5×SSC или по существу 1×SSC.
Детекцию можно проводить любым подходящим способом, где в одном из аспектов данного изобретения для детекции взаимодействия мишени с зондом используют проточный цитометрический анализ на основе флуоресцентных свойств гранул, таких как система гранул Luminex, описанная в Dunbar (см. выше). В частности, в этой статье указано, например, что система Luminex хМАР включает 5,6 мкм полистирольные микросферы, которые окрашены внутри двумя спектрально различными флуорохромами. При использовании точных количеств каждого из этих флуорохромов создают матрицу, состоящую из разных наборов микросфер со специфическими спектральными адресами. Каждый набор микросфер может обладать отличающимся реагентом на своей поверхности. Поскольку наборы микросфер могут различаться их спектральными адресами, их можно объединять, что делает возможным, например, измерение 100 или более разных аналитов одновременно в одном реакционном сосуде. Третий флуорохром, связанный с репортерной молекулой, дает количественную оценку биомолекулярного взаимодействия, которое произошло на поверхности микросферы. Микросферы исследуют индивидуально в потоке быстро текущей жидкости при их прохождении мимо двух отдельных лазеров в анализаторе Luminex® 100™. Диодный красный лазер, работающий при 635 нм и 10 мВт, возбуждает два флуорохрома, содержащихся в микросферах; лазер на алюмоиттриевом гранате (YAG), работающий при 532 нм, 13 мВт, возбуждает репортерный флуорохром (R-фикоэритрин, Alexa 532 или Су3), связанный с поверхностью микросфер. Высокоскоростная обработка цифрового сигнала классифицирует микросферу на основании ее спектрального адреса и количественно характеризует реакцию на поверхности. Тысячи микросфер исследуют в секунду, что дает систему анализа, способную анализировать и регистрировать, например, 100 или более различных реакций в одном реакционном сосуде всего за несколько секунд на образец.
В одном из аспектов данного изобретения гранулы могут представлять собой парамагнитные гранулы. В одном из аспектов гранулы можно смешивать с мишенью и/или репортером с использованием механического перемешивания, основанного на магнитных свойствах гранул.
В одном из аспектов способ по изобретению включает поддержание температуры гибридизации после стадии гибридизации между зондом и мишенью после стадии (2). В одном из аспектов имеет место поддержание температуры гибридизации до по меньшей мере жесткой промывки на стадии (3). В одном из аспектов способ по изобретению включает поддержание температуры гибридизации во время инкубации с репортерной молекулой на стадии (4).
Как таковое, настоящее изобретение относится к процессу, описанному выше, детекции любого взаимодействия между зондом и целевой нуклеиновой кислотой, где температуру реакции гибридизации между мишенью и зондом поддерживают до тех пор, пока реакция с репортерной молекулой по существу не завершится.
В одном из аспектов способ по изобретению также включает применение стадии разведения-промывки сразу после стадии гибридизации (2). Такая стадия увеличивает объем реакции между мишенью и зондом и, по-видимому, снижает возможность неспецифической гибридизации. Разведение можно осуществлять с помощью буфера для промывки, используемого для удаления любых несвязавшихся веществ на стадии (2) этого способа.
В одном из аспектов способ по изобретению включает встряхивание или перемешивание при нагревании, например, с использованием термомиксера на стадии (2). Термомиксер обычно представляет собой любое устройство, которое обеспечивает перемешивание образца при заданной температуре. В данном описании перемешивание соответственно происходит при температуре гибридизации, обычно 50°С или выше, такой как 50-55°С, такой как 50°С, 52°С, 54°С и 55°С.
В одном из аспектов способ по изобретению включает промывку конечного комплекса зонд-мишень в 1×SSC перед детекцией сигнала после стадии (6). Такая промывка может быть осуществлена при комнатной температуре.
В одном из аспектов способ по изобретению включает встряхивание конечного комплекса зонд-мишень перед детекцией сигнала после стадии (6).
В другом аспекте этот способ включает дополнительную стадию связывания гранулы с зондом перед стадией (1). Таким образом, реакция между мишенью и зондом происходит в контексте твердой подложки.
В другом аспекте изобретение относится к способу, описанному выше, при котором зонд связан с гранулой, соответственно полистирольной гранулой, имеющей флуорохром.
В другом аспекте изобретение относится к способу, описанному выше, при котором по меньшей мере 2 зонда используют одновременно для детекции разных мишеней. Такие реакции обычно обозначают как мультиплексные реакции. В одном из аспектов зонды по настоящему изобретению, имеющие разные специфичности к мишеням, присоединены к гранулам, где каждая гранула является специфической для каждого типа конкретного зонда.
В другом аспекте изобретение относится к мультиплексной реакции, содержащей по меньшей мере 2 типа специфических зондов, где эти зонды присоединены к гранулам, которые соответственно мечены различными флуорохромами, и где длина зонда у разных зондов в мультиплексной реакции являются не одинаковой. Например, если определенный полинуклеотидный фрагмент (например, ДНК) будет подвергаться одновременному зондированию с использованием множественных специфических зондов разного типа, то в одном из аспектов настоящее изобретение не требует того, чтобы все зонды имели равную длину, и в одном из аспектов зонды различаются по длине.
В другом аспекте гибридизацию между зондом и мишенью осуществляют в присутствии цитрата натрия (SSC) или эквивалента, такого как 2-4×SSC или 3×SSC, соответственно для обеспечения ионной среды для того, чтобы происходили взаимодействия между зондом и мишенью.
Настоящее изобретение проиллюстрировано со ссылкой на следующие примеры, которые не ограничивают данное изобретение.
МАТЕРИАЛЫ И МЕТОДЫ
Стандартная процедура гибридизации (по стадиям) в соответствии с Wallace и др. (2005), см. выше, представляет собой нижеследующее:
1. Выбирают соответствующий набор микросфер, связанных с олигонуклеотидами.
2. Ресуспендируют микросферы с помощью встряхивателя и обработки ультразвуком в течение приблизительно 20 секунд.
3. Приготавливают рабочую смесь микросфер путем разведения исходных препаратов связанных микросфер до 150 микросфер на каждый набор в 1 мкл гибридизационного буфера 1,5×ТМАС (1×ТМАС=2 моль/л ТМАС / 0,15% саркозила / 75 ммоль/л Трис, 6 ммоль/л ЭДТА) (Примечание: для каждой реакции требуется 33 мкл рабочей смеси микросфер).
4. Перемешивают рабочую смесь микросфер с помощью встряхивателя и обработки ультразвуком в течение приблизительно 20 секунд.
5. В каждый образец или фоновую лунку добавляют по 33 мкл рабочей смеси микросфер.
6. В каждую фоновую лунку добавляют по 17 мкл dH2O.
7. В каждую лунку с образцом добавляют амплифицированную биотинилированную ДНК и dH2O до суммарного объема 17 мкл (Примечание: для детекции используют 7 мкл реакционной среды для ПЦР).
8. Среду в лунках осторожно перемешивают посредством пипетирования вверх-вниз несколько раз.
9. Инкубируют при 99°С в течение 5 минут для денатурации амплифицированной биотинилированной ДНК в термоциклере.
10. Инкубируют реакционный планшет при температуре гибридизации (55°С) в течение 15 минут.
11. Во время инкубации приготавливают фильтр-планшет путем промывания два раза ледяным 1×ТМАС. Затем каждую лунку фильтр-планшета заполняют ледяным 1×ТМАС.
12. Во время инкубации приготавливают свежую репортерную смесь путем разведения стрептавидин-R-фикоэритрина до 2 мкг/мл в 1× гибридизационном буфере ТМАС (Примечание: для каждой реакции требуется 75 мкл репортерной смеси) и помещают ее в термостат или водяную баню при температуре гибридизации.
13. Прекращают реакцию гибридизации путем переноса всей реакционной среды на фильтр-планшет, содержащий ледяной буфер для промывки.
14. После переноса фильтр-планшет два раза хорошо промывают ледяным 1×ТМАС буфером для промывки, чередуя с вакуумной фильтрацией.
15. Добавляют 75 мкл репортерной смеси в каждую лунку и перемешивают осторожно посредством пипетирования вверх-вниз несколько раз.
16. Планшет оставляют стоять в течение приблизительно 30 минут для достижения комнатной температуры.
17. Реакционный планшет инкубируют при температуре гибридизации в течение 30 минут.
18. Инкубацию прекращают посредством вакуумной фильтрации.
19. Промывают дважды 1×ТМАС буфером для промывки, чередуя с вакуумной фильтрацией.
20. Разбавляют реакционную среду 1×ТМАС буфером для промывки, чередуя с вакуумной фильтрацией.
21. Анализируют при комнатной температуре на анализаторе Luminex™100 в соответствии с руководством к системе.
[См. Фиг.2. Общая схема последовательности рабочих операций, как описано Wallace и др. (2005)]
Чувствительность и специфичность теста основаны на специфической гибридизации между последовательностями нуклеиновых кислот зонда и мишени. Поэтому гибридизация и промывка, а также инкубация с РЕ, по-видимому, являются критическими стадиями в процедуре. Протокол адаптировали для максимизации специфичности и чувствительности реакции путем оптимизации различных параметров, таких как температуры и кинетика диффузии. Эти адаптации указаны в оптимизированном протоколе гибридизации (см. ниже).
Материалы:
А. Буферы
рН 8,0 100 ×
Б. Гранулы
1. Используемые типы гранул представляют собой L100-C123-01 вплоть до L100-C172-01 (Luminex™Corp., Austin, ТХ).
В. Зонды (см. примеры)
1. Зонды получены от Eurogentec (Seraing, Бельгия)
Г. Оборудование
Методы и протоколы:
I. Связывание зонда
1. Нагревают свежую аликвоту обезвоженного порошка Pierce EDC (гидрохлорида 1-этил-3-(диметиламинопропил)карбодиимида) с -20°С до комнатной температуры.
2. Ресуспендируют аминозамещенный олигонуклеотид ("зонд" или "захватывающий" олиго) до 0,2 мМ (0,2 нмоль/мкл) в dH2O.
3. Ресуспендируют исходные микросферы с помощью встряхивателя и обработки ультразвуком в течение приблизительно 20 секунд.
4. Переносят 5,0×106 исходных микросфер в микроцентрифужную пробирку USA Scientific.
5. Осаждают исходные микросферы микроцентрифугированием при не менее 8000×g в течение 1-2 минут.
6. Удаляют супернатант и ресуспендируют осажденные микросферы в 50 мкл 0,1 М MES, pH 4,5 с помощью встряхивателя и обработки ультразвуком в течение приблизительно 20 секунд.
7. Приготавливают разведение (1:10) 0,2 мМ захватывающего олигонуклеотида в dH2O (0,02 нмоль/мкл).
8. Добавляют 2 мкл (0,04 нмоль) разбавленного (1:10) захватывающего олигонуклеотида к ресуспендированным микросферам и перемешивают с помощью встряхивателя.
9. Приготавливают свежий раствор 20 мг/мл EDC в dH2O. Растворяют 10 мг EDC в 500 мкл dH2O, максимально за 1 минуту перед применением. Аликвоты по 10 мг EDC (порошок) хранили сухими при -80°С, упакованными вместе с силикагелем.
10. Для каждой реакции добавляют последовательно по 2,5 мкл свежеприготовленного 20 мг/мл EDC к микросферам и перемешивают с помощью встряхивателя (Примечание: Аликвоту порошка EDC теперь следует отбросить).
11. Инкубируют в течение 30 минут при комнатной температуре в темноте.
12. Приготавливают второй свежий раствор 20 мг/мл EDC в dH2O.
13. Для каждой реакции добавляют последовательно по 2,5 мкл свежего 20 мг/мл EDC к микросферам и перемешивают с помощью встряхивателя (Примечание: Аликвоту порошка EDC теперь следует отбросить).
14. Инкубируют в течение 30 минут при комнатной температуре в темноте.
15. Добавляют 1,0 мл 0,02% Tween-20 к связанным микросферам.
16. Осаждают связанные микросферы микроцентрифугированием при не менее 8000×g в течение 1-2 минут.
17. Удаляют супернатант и ресуспендируют связанные микросферы в 1,0 мл 0,1%-ного додецилсульфата натрия с помощью встряхивателя.
18. Осаждают связанные микросферы микроцентрифугированием при не менее 8000×g в течение 1-2 минут.
19. Удаляют супернатант и ресуспендируют связанные микросферы в 100 мкл ТЕ, рН 8,0, с помощью встряхивателя и обработки ультразвуком в течение приблизительно 20 секунд.
20. Осаждают связанные микросферы микроцентрифугированием при не менее 8000×g в течение 1-2 минут.
21. Удаляют супернатант и ресуспендируют связанные микросферы в 100 мкл ТЕ, рН 8,0, с помощью встряхивателя и обработки ультразвуком в течение приблизительно 20 секунд.
22. Подсчитывают связанные микросферы с помощью гемоцитометра:
а. разбавляют ресуспендированные связанные микросферы 1:100 в dH2O;
б. тщательно перемешивают с помощью встряхивателя;
в. переносят 10 мкл в гемоцитометр;
г. подсчитывают микросферы в 4 больших квадратах решетки гемоцитометра;
д. микросферы/мкл=(сумма микросфер в 4 больших квадратах) ×2,5×100 (коэффициент разведения) (примечание: максимум составляет 50000 микросфер/мкл).
23. Хранят связанные микросферы охлажденными при 2-10°С в темноте.
II. Оптимизированный протокол гибридизации и промывки
1. Выбирают соответствующий набор микросфер, связанных с олигонуклеотидами.
2. Ресуспендируют микросферы с помощью встряхивателя и обработки ультразвуком в течение приблизительно 20 секунд.
3. Приготавливают рабочую смесь микросфер путем разведения исходных препаратов связанных микросфер до 150 микросфер каждого набора/мкл в гибридизационном буфере: 4,5×SSC / 0,15% саркозила (Примечание: для каждой реакции требуется 33 мкл рабочей смеси микросфер).
4. Перемешивают рабочую смесь микросфер с помощью встряхивателя и обработки ультразвуком в течение приблизительно 20 секунд.
5. В каждую лунку с образцом или фоновую лунку добавляют по 33 мкл рабочей смеси микросфер.
6. В каждую фоновую лунку добавляют по 17 мкл ТЕ, рН 8.
7. В каждую лунку с образцом добавляют амплифицированную биотинилированную ДНК и ТЕ, рН 8,0, до суммарного объема 17 мкл (Примечание: для детекции обычно достаточно 4 мкл из приблизительно 50 мкл реакционной смести для ПЦР).
8. Реакционную среду в лунках осторожно перемешивают посредством пипетирования вверх-вниз несколько раз.
9. Инкубируют при 95-100°С в течение 5 минут для денатурации амплифицированной биотинилированной ДНК в термоциклере.
10. Инкубируют реакционный планшет при 60°С в течение 3 минут в термоциклере.
11. Переносят реакционный планшет в термомиксер, предварительно нагретый до температуры гибридизации (Примечание: для одновременного переноса реакций в 8 лунок можно использовать 8-канальную пипетку).
12. Инкубируют реакционный планшет при температуре гибридизации в течение 15 минут и при 500 об/мин.
13. Во время инкубации приготавливают фильтр-планшет Millipore путем промывки дистиллированной водой. Затем в каждую лунку фильтр-планшета вносят 200 мкл буфера для промывки: 3×SSC /0,1% саркозила/ 1 мг/мл казеина при температуре гибридизации и помещают это в термостат при температуре гибридизации.
14. Во время инкубации приготавливают свежую репортерную смесь путем разведения стрептавидин-R-фикоэритрина до 2 мкг/мл в буфере для жесткой промывки: 3×SSC /0,1% саркозила/ 1 мг/мл казеина (Примечание: для каждой реакции требуется 75 мкл репортерной смеси) и помещают ее в термостат или водяную баню при температуре гибридизации.
15. Прекращают реакцию гибридизации путем переноса всей реакционной среды на фильтр-планшет, содержащий буфер для промывки, при температуре гибридизации.
16. После переноса фильтр-планшет промывают дважды 100 мкл буфера для жесткой промывки: 3×SSC /0,1% саркозила/ 1 мг/мл казеина, при температуре гибридизации, чередуя с вакуумной фильтрацией.
17. Добавляют 75 мкл репортерной смеси в каждую лунку и перемешивают осторожно посредством пипетирования вверх-вниз несколько раз.
18. Инкубируют реакционный планшет при температуре гибридизации в течение 15 минут.
19. Инкубацию прекращают с помощью вакуумной фильтрации.
20. Промывают дважды 100 мкл буфера для промывки: 1×SSC /0,1% саркозила/ 1 мг/мл казеина, при комнатной температуре, чередуя с вакуумной фильтрацией.
21. Разбавляют реакцию в 100 мкл буфера для промывки: 1×SSC /0,1% саркозила/ 1 мг/мл казеина, при комнатной температуре.
22. Анализируют 50 мкл при комнатной температуре на анализаторе Luminex™ 100 в соответствии с руководством к этой системе.
III. Считывание
Данные считывали с использованием программы Luminex™ 100 IS, версия 2.3.
Во время измерения использовали следующие параметры:
а. Объем образца: 50 мкл
б. Перерыв между образцами: 60 сек.
в. Температура нагревателя XY (°С): 35
г. Окно дискриминатора с двумя порогами:
1. Нижний предел: 8000
2. Верхний предел: 18500
д. Статистический параметр: медиана
IV. Обработка данных
1. Данные сохраняли в файле в формате raw CSV (разделенный запятыми *.csv), содержащем весь стандартный массив выходных данных, полученный программой Luminex™ 100 IS 2.3.
2. Полученные медианы сигналов переносили в файл Excel для вычисления отношения мишени к зонду и отношения сигнала к шуму (см. также методика и вычисления).
Настоящее изобретение относится к разным пунктам процедуры Luminex™, включая оптимизацию конструкции зонда и оптимизацию протокола тестирования.
В следующем тексте данные будут представлены в соответствии со схемой работы, как показано на Фиг.2.
Фиг.2. Общий схематический вид адаптированной схемы работы.
Представление результатов в примерах (методика и вычисления)
Примеры и соответствующие пункты формулы изобретения указаны и объяснены следующим образом. Результаты представлены в основном в виде таблиц, содержащих необработанные данные (MFI=медиана интенсивности флуоресценции), переменные (например, температура), зонды и мишени, как проанализировано, вычисления и примечания.
Вычисления включают отношение мишени к зонду (мишень/зонд в %) и отношение сигнала к шуму (сигнал/шум).
Отношение мишени к зонду вычисляют относительно зонда и выражают каждый сигнал в виде процента положительного контроля, который принимают за 100% (см. также пример Таблицы 12).
Отношение сигнала к шуму вычисляют относительно зонда. Каждый сигнал делят на медиану всех полученных сигналов (см. также пример Таблицы 13).
Как отношение мишени к зонду, так и отношение сигнала к шуму дают хороший общий показатель интенсивности и специфичности сигнала.
В некоторых примерах используют зонды из наборов зондов праймеров SPF10, описанных в ЕР1012348, который полностью включен в данное описание посредством ссылки. В этом патенте предложены технические предпосылки методик, используемых в настоящей заявке на патент.
Набор праймеров SPF10 образует небольшие амплимеры длиной лишь 65 п.н. с участком между праймерами, составляющим 22 нуклеотида. Это сильно ограничивает возможности расположения зондов, принимая во внимание различные ошибочные спаривания между всеми генотипами HPV.
Пример 1
Задача:
Исследовать, будет ли поддержание температуры гибридизации после стадии гибридизации оказывать значительный положительный эффект на специфичность сигнала.
Введение
После гибридизации между иммобилизованным на грануле зондом и денатурированной последовательностью-мишенью в растворе несвязавшееся вещество следует отмыть перед инкубацией с репортерным реагентом стрептавидин-R-фикоэритрином (РЕ). Это осуществляют с использованием фильтр-планшета (MSBVN12, Millipore), где гранулы и все прикрепившиеся молекулы отделяют от свободных молекул в растворе. Объем реакции маленький и поэтому подвержен быстрым изменениям температуры окружающей среды. Авторы изобретения исследовали эффект изменений температуры после температуры гибридизации.
Материалы и методы
Эффект инкубации при температуре ниже, чем температура гибридизации, на сигнал Luminex™ исследовали с использованием модельной системы SPF10.
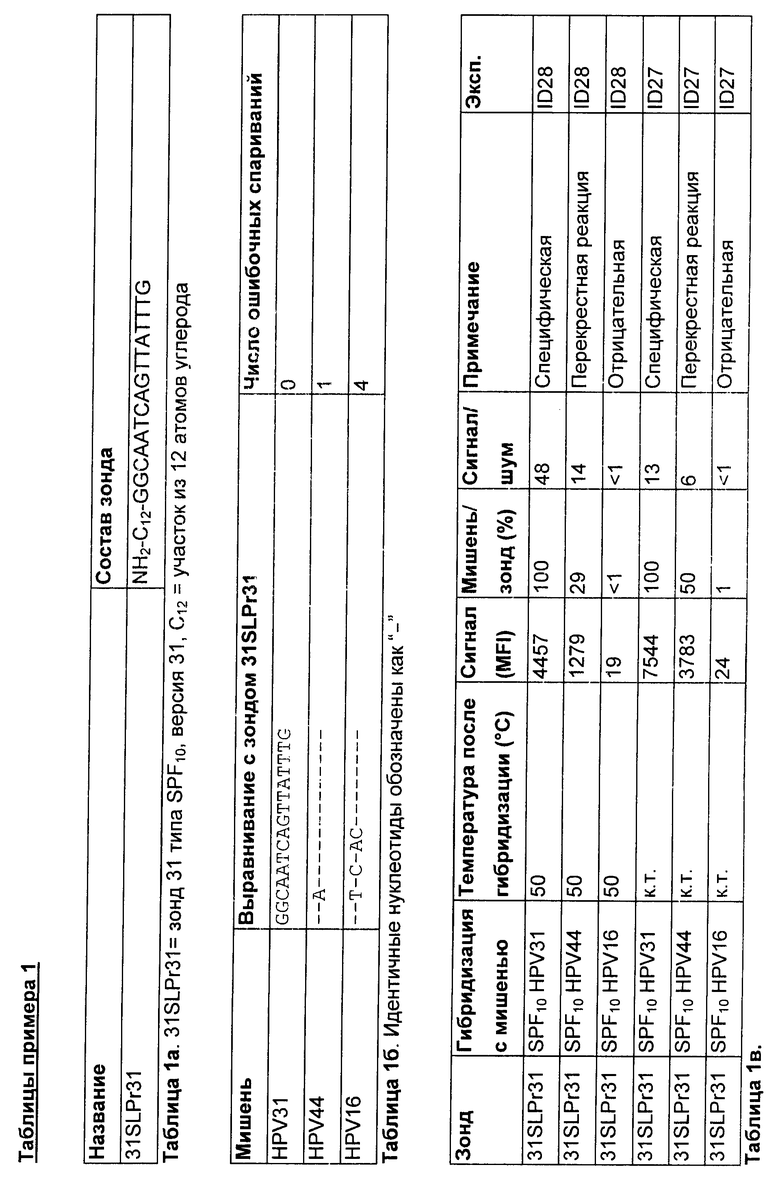
Использовали гранулу Luminex™, несущую зонд к HPV31 (зонд 31SLPr31, см. таблицу 1а). Указанный зонд является специфическим для идентификации последовательностей HPV31, амплифицированных с использованием набора праймеров SPF10. Для оценки любой перекрестной реактивности использовали амплимеры для HPV44 и HPV16. Последовательности-мишени HPV31 и HPV44 различаются по 1 положению, и последовательности-мишени последовательностей HPV31 и HPV16 различаются по 4 положениям (Таблица 1б).
Гибридизацию осуществляли при 50°С, и анализы проводили в двух повторностях. Затем один набор реакционных сред обрабатывали в соответствии со стандартным протоколом и гранулы немедленно промывали в фильтр-планшете при 4°С. Параллельный набор реакционных сред сначала инкубировали при комнатной температуре (к.т.) в течение 1 минуты перед началом такой же стандартной промывки при 4°С. В отличие от Wallace и др. (2005), буфер для промывки добавляли после переноса образцов в фильтр-планшет (см. также пример 2).
Результаты
Результаты показаны в таблице 1в. Как продемонстрировано, инкубация при к.т. в течение всего 1 минуты после гибридизации и перед жесткой промывкой вызывает увеличение сигнала, но также уменьшает специфичность (показано более высокими сигналами, наблюдающимися для HPV44). Это можно объяснить уменьшением жесткости, вызванным кратким падением температуры после гибридизации.
Заключение
Температуру реакционной смеси после стадии гибридизации следует поддерживать. После гибридизации гранулы следует промывать как можно быстрее без промедления для предотвращения снижения температуры.
Пример 2
Задача
Исследовать, будет ли разведение сразу после гибридизации оказывать значительный положительный эффект на специфичность сигнала.
Введение
Стандартная процедура анализа Luminex™ включает риск введения неспецифического связывания, если промывка не следует сразу после стадии гибридизации (см. также пример 1). Для минимизации этого риска исследовали разведение образца сразу после гибридизации.
Материалы и методы
Для исследования этого эффекта использовали смесь двух гранул Luminex™: одну гранулу, несущую зонд к HPV31 (название: 31 SLPr31, см. таблицу 2а), и другую гранулу, несущую HPV51 (название: 51SLPr2, см. таблицу 2а). Эти зонды являются специфическими для идентификации последовательностей HPV31 и HPV51, амплифицированных с использованием набора праймеров SPF10 соответственно. Для того чтобы наблюдать возможную перекрестную реактивность с 31 SLPr31, использовали амплимеры для HPV44 и HPV16. Последовательности-мишени HPV31 и HPV44 и 16 различаются по 1 положению и 4 положениям соответственно (Таблица 2б). Для того чтобы наблюдать возможную перекрестную реактивность с 51SLPr2, использовали амплимеры для HPV33 и HPV16. Каждая из последовательностей-мишеней HPV51 и HPV44 и 16 различается по 4 положениям (Таблица 2в).
Гибридизацию осуществляли при 50°С, используя стандартный протокол.
Затем первый набор реакций немедленно промывали в фильтр-планшете при 4°С без какой-либо дополнительной промывки. В отличие от Wallace и др. (2005), буфер для промывки добавляли после переноса образцов на фильтр-планшет.
Эффект дополнительной прямой и непрямой процедуры промывки разведением сразу после стадии гибридизации исследовали следующим образом. Для прямой и непрямой процедур использовали буфер для промывки (3×SSC /0,1% саркозила/ 1 мг/мл казеина. Это буфер для жесткой промывки) при 50°С.
Второй набор гранул промывали с использованием прямой процедуры. Прямая процедура включает в себя разведение гибридизационной смеси (50 мкл) 200 мкл буфера для промывки при температуре гибридизации в термоциклере с последующим переносом всего разбавленного образца на фильтр-планшет.
Третью реакцию гибридизации промывали с использованием непрямой процедуры. Непрямая процедура включает в себя разведение путем быстрого переноса 50 мкл гибридизационной смеси на фильтр-планшет, который уже содержит 200 мкл буфера для промывки при температуре гибридизации (см. также Wallace и др., 2005).
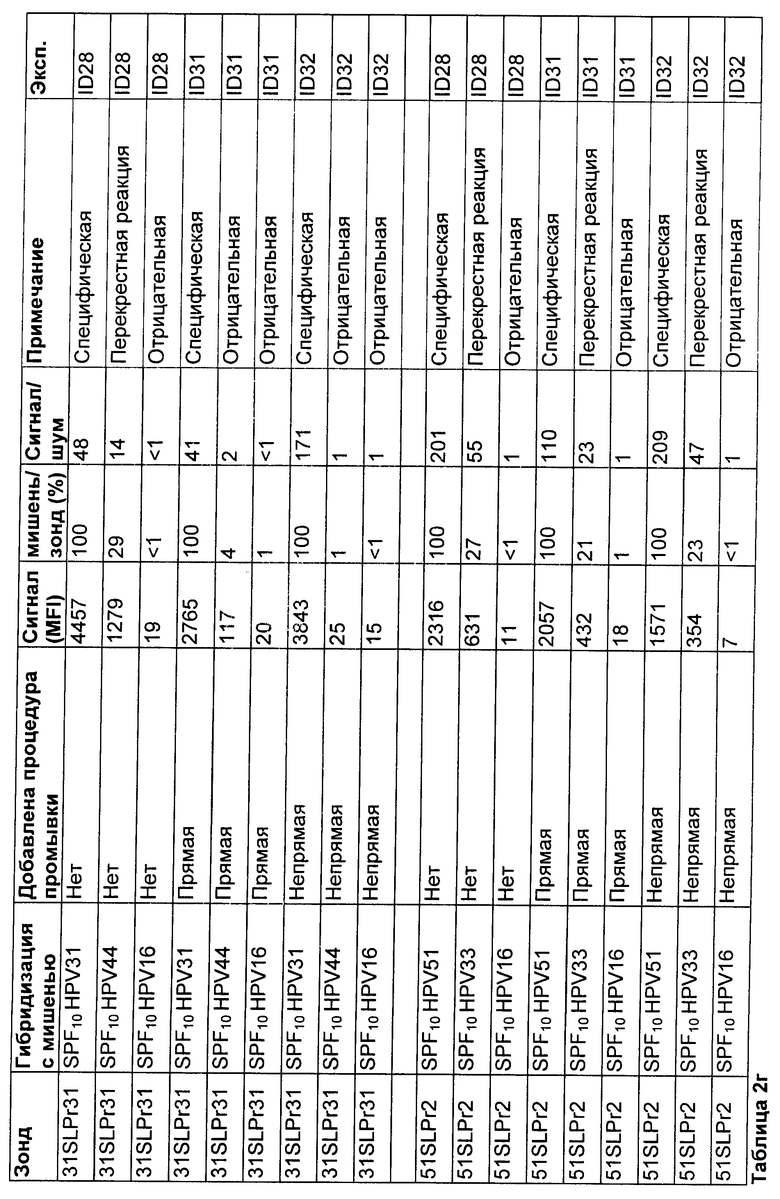
Результаты
Результаты показаны в таблице 2г. Обе дополнительные процедуры промывки приводят к уменьшению абсолютного сигнала по сравнению со стандартной процедурой, но в то же время специфичность сигнала значительно увеличивается. Значительных различий между процедурами прямой и непрямой промывки не было. На практике прямая промывка разведением в термоциклере является менее практичной, и поэтому процедура непрямой промывки разведением является предпочтительной.
Заключение
Применение дополнительной стадии разведения-промывки после гибридизации оказывает значительный положительный эффект на специфичность сигнала. По практическим соображениям процедура непрямой промывки разведением является предпочтительной.
Пример 3
Задача:
Исследовать, будет ли поддержание температуры гибридизации во время жесткой промывки перед инкубацией со стрептавидин-R-фикоэритрином оказывать значительный положительный эффект на специфичность сигнала.
Введение
Отрицательный эффект падения температуры после жесткой гибридизации, как описано выше, означает, что температура жесткой промывки может оказывать эффект сама по себе. Поэтому исследовали эффект температур жесткой промывки при 50°С, к.т. или 4°С.
Материалы и методы
Эффект разных температур буфера для жесткой промывки после стадии гибридизации перед инкубацией со стрептавидин-R-фикоэритрином исследовали с использованием модельной системы SPF10 следующим образом.
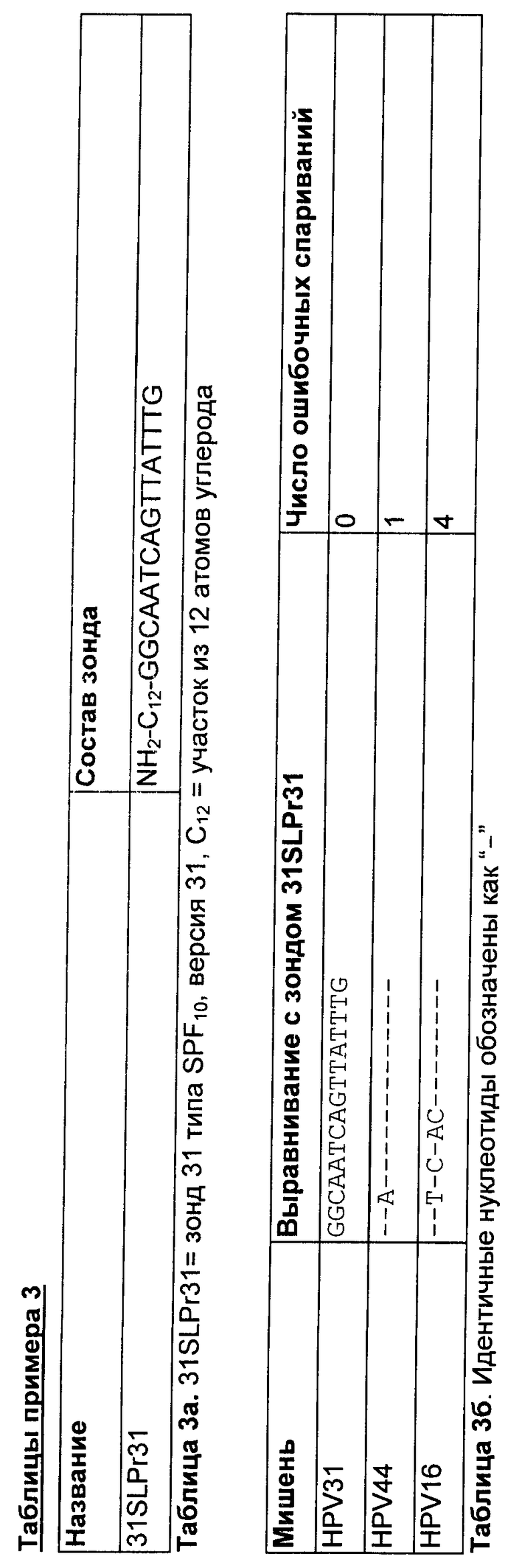
Для исследования этого эффекта использовали гранулу Luminex™, несущую зонд к HPV31 (название: 31SLPr31, см. таблицу 3а). Этот зонд является специфическим для идентификации последовательностей HPV31, амплифицированных с использованием набора праймеров SPF10. Для наблюдения возможной перекрестной реактивности с 31SLPr31 использовали амплимеры для HPV44 и HPV16. Последовательности-мишени HPV31 и HPV44 и 16 различаются по 1 положению и 4 положениям соответственно (Таблица 3б).
Гибридизацию осуществляли при 50°С. Затем набор реакций переносили на фильтр-планшет, содержащий буфер для промывки при 50°С, к.т. или 4°С соответственно.
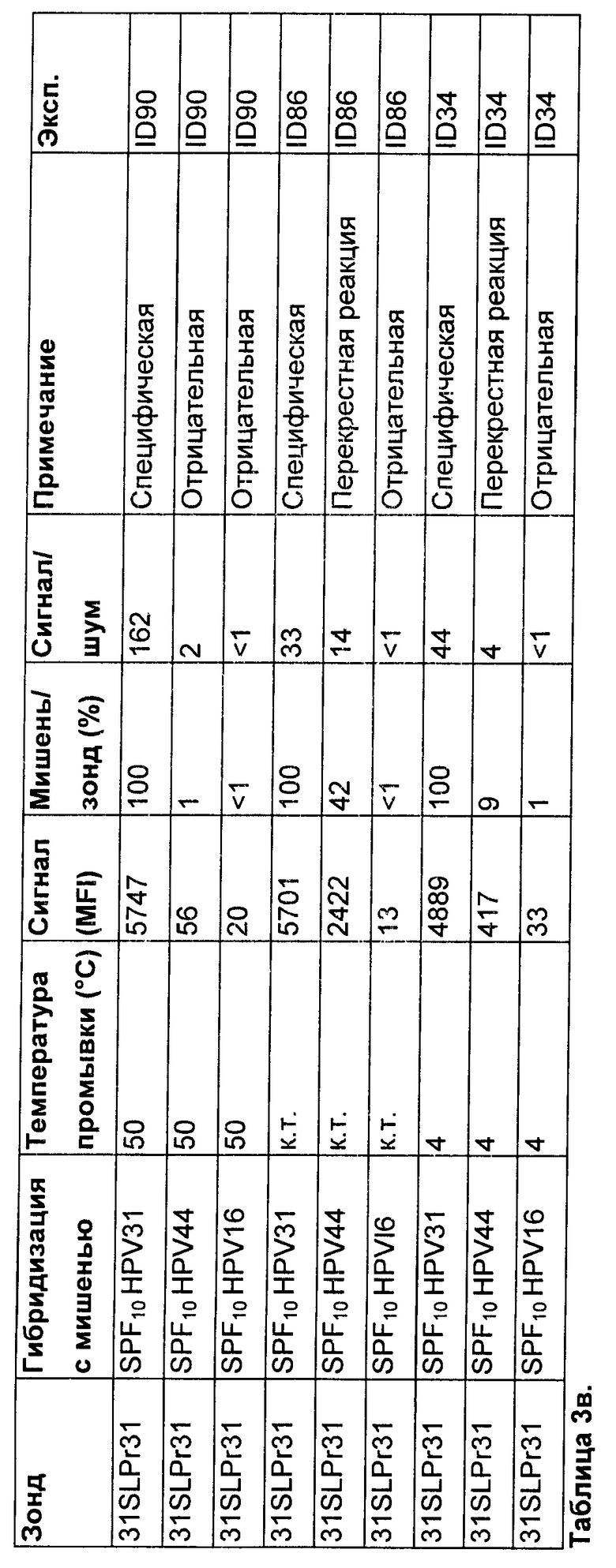
Результаты
Результаты показаны в таблице 3в. Абсолютные уровни сигнала из положительного контроля не отличаются между 50°С и к.т. и несколько снижены после промывки при 4°С. Однако промывка при 50°С приводит к значительному увеличению специфичности сигнала, тогда как промывка при к.т. или 4°С приводит к уменьшению специфичности сигнала. Поэтому процедура непрямой промывки разведением при температуре гибридизации 50°С является предпочтительной.
Заключение
Поддержание температуры гибридизации во время жесткой промывки перед инкубацией со стрептавидин-R-фикоэритрином оказывает значительный эффект на специфичность сигнала.
Пример 4
Задача:
Исследовать, будет ли применение термомиксера оказывать значительный положительный эффект на интенсивность сигнала.
Введение
На кинетику реакции гибридизации можно влиять путем перемешивания компонентов во время реакции.
Поэтому авторы изобретения исследовали эффект использования термомиксера во время гибридизации.
Материалы и методы
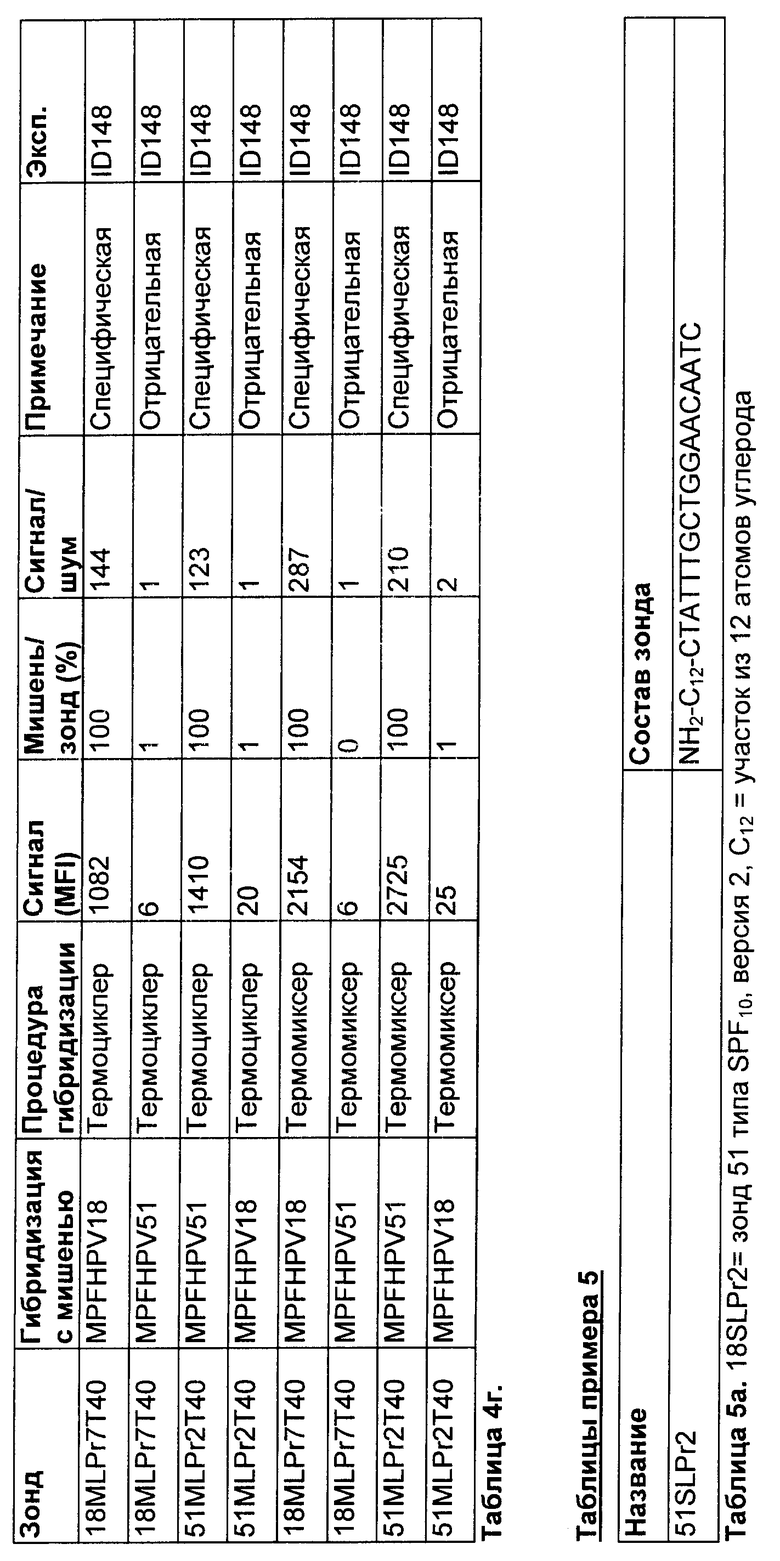
Эффект диффузионной кинетики с использованием термомиксера во время гибридизации исследовали с использованием модельной системы MPF следующим образом.
Использовали две гранулы Luminex™, несущие зонд либо для HPV18 (название: 18 MLPr7, см. таблицу 4а), либо для HPV51 (название: 51 MLPr2, см. таблицы 4а). Эти зонды являются специфическими для идентификации последовательностей HPV18 и HPV51, амплифицированных с использованием набора праймеров MPF.
Эти две гранулы смешивали и гибридизовали с использованием амплимеров MPF для HPV18 и HPV51.
Последовательности-мишени HPV18 и HPV51 различаются по 7 положениям (Таблица 4б и в). Реакции тестировали в двух повторностях.
Одну реакцию подвергали денатурации и гибридизации в термоциклере, без встряхивания (см. также Wallace и др., 2005).
Параллельную реакцию подвергали денатурации в термоциклере для денатурации и немедленно переносили в термомиксер для гибридизации. Гибридизацию осуществляли при 50°С.
Затем гранулы немедленно промывали в фильтр-планшете при 50°С с использованием оптимизированного протокола гибридизации и промывки.
Результаты
Результаты показаны в таблице 4г. Применение термомиксера значительно увеличивает абсолютный сигнал из положительного контроля, тогда как фон оставался неизменным. Это приводило к общему увеличению специфичности сигнала.
Эти результаты демонстрируют, что интенсивность сигнала будет увеличиваться (улучшаться) при использовании термомиксера.
Заключение
Применение термомиксера оказывает значительный положительный эффект на интенсивность и специфичность сигнала.
Пример 5
Задача:
Исследовать, будет ли инкубация со стрептавидин-R-фикоэритрином при температуре гибридизации оказывать значительный положительный эффект на интенсивность сигнала.
Введение
В общем, температура влияет на кинетику любой реакции, включая детекцию гибридов репортерным РЕ. Поэтому исследовали эффект температуры при инкубации с РЕ и последующей промывки.
Материалы и методы
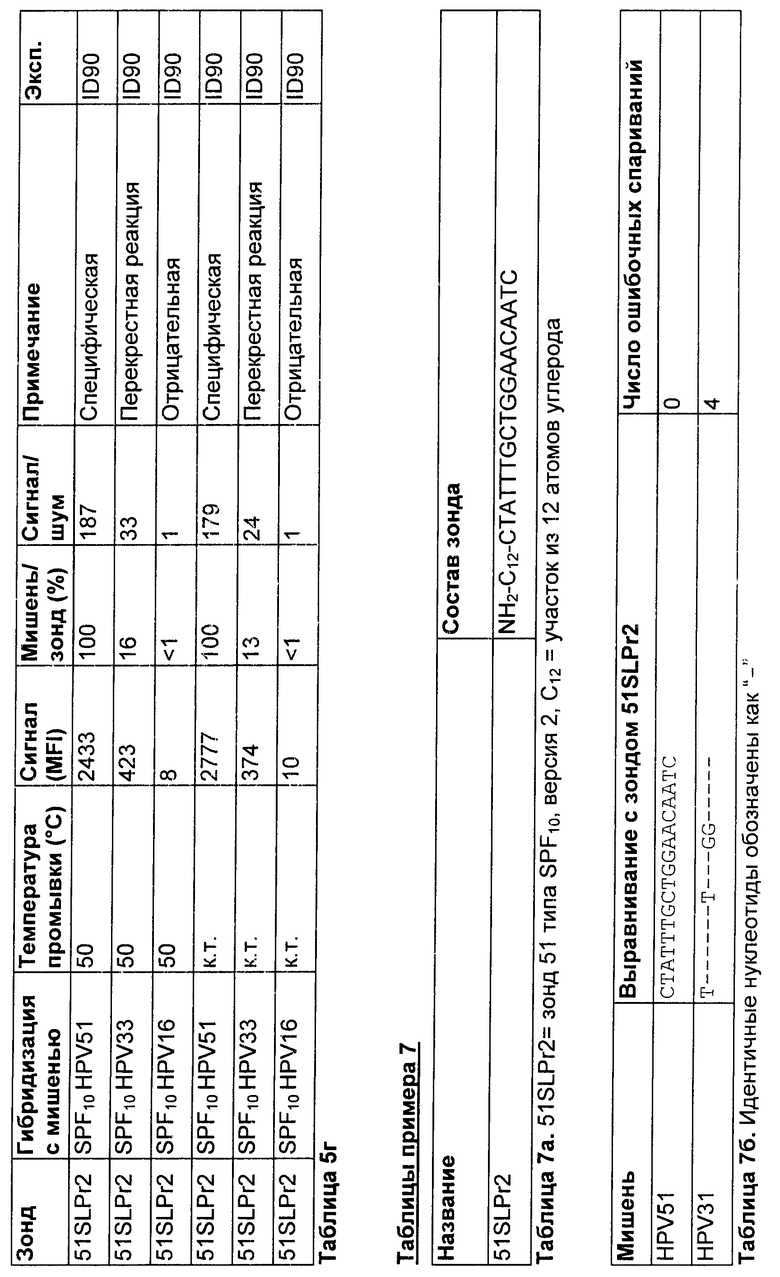
Использовали гранулы Luminex™, несущие зонд для HPV51 (название: 51SLPr2, см. таблицу 5а). Указанный зонд является специфическим для идентификации последовательностей HPV51, амплифицированных с использованием набора праймеров SPF10. Для наблюдения возможной перекрестной реактивности с этим зондом использовали амплимеры SPF10 для HPV33 и HPV16. Последовательности-мишени HPV51, HPV33 и HPV16 различаются по 4 положениям (Таблица 5б).
Гибридизацию осуществляли при 50°С в двух повторностях с использованием описанного в данной заявке оптимизированного протокола гибридизации и промывки. После жесткой промывки один набор реакций инкубировали с РЕ при 50°С (см. также Wallace и др., 2005), а другой набор инкубировали с РЕ при к.т. Затем гранулы промывали в фильтр-планшете при 50°С.
В другом эксперименте гибридизацию осуществляли при 50°С в двух повторностях с использованием оптимизированного протокола гибридизации и промывки. После жесткой промывки все реакции инкубировали с РЕ при 50°С (см. также Wallace и др., 2005). После инкубации с РЕ при 50°С один набор реакций промывали при 50°С (см. также Wallace и др., 2005), а параллельный набор промывали при к.т.
Результаты
Инкубация с РЕ при разных температурах оказывала значительный эффект, как показано в таблице 5с. Инкубация с РЕ при температуре гибридизации 50°С приводит к более высоким абсолютным сигналам по сравнению с инкубацией с РЕ при к.т. Однако специфичность сигнала существенно не отличалась.
Поэтому инкубация со стрептавидин-R-фикоэритрином при температуре гибридизации является предпочтительной. Напротив, промывка при к.т. или температуре гибридизации после инкубации не оказывала значительного эффекта, хотя это может быть более практичным в некоторых ситуациях.
Влияние температуры на стадию промывки после инкубации с РЕ не значительно. Как абсолютный сигнал, так и специфичность оказались не подвержены влиянию температуры промывки.
Заключение
Поддержание температуры гибридизации во время инкубации со стрептавидин-R-фикоэритрином оказывает значительный эффект на интенсивность сигнала, но не на специфичность сигнала.
Температура промывки после инкубации с РЕ не оказывает значительного эффекта.
Пример 6
Задача:
Исследовать, можно ли предотвратить засорение зонда Luminex™ для образцов конечной промывкой с использованием 1×SSC.
Введение
В оптимизированном протоколе гибридизации и промывки гибридизацию осуществляют в 3×SSC. При этой концентрации SSC вызывает такое засорение зонда Luminex™ для образцов, которое серьезно препятствует процессингу образцов. Поэтому исследовали эффект меньшей концентрации SSC для конечной промывки.
Результаты
Первоначально авторы изобретения пытались поддерживать концентрацию SSC как при гибридизации. Однако поскольку конечная промывка с использованием трехкратного SSC приводила к серьезному засорению зонда Luminex™ для образцов, невозможно было получить значимых данных. Просто осуществление этой стадии промывки 1×SSC приводило к значимым данным. Поэтому из-за отсутствия данных сравнение по данным невозможно было показать. Другие концентрации SSC не исследованы.
Заключение
Конечная промывка 1×SSC предотвращает засорение зонда Luminex™ для образцов.
Пример 7
Задача:
Исследовать, будет ли хранение образцов, которые готовы для измерения в течение по меньшей мере 4 суток после конечной промывки при 4°С оказывать какой-либо значительный эффект на сигнал.
Введение
Для увеличения гибкости схемы работы авторы изобретения проанализировали несколько стадий в отношении протокола тестирования прямой гибридизацией с использованием системы Luminex™. Одной из протестированных процедур является, в частности, хранение между двумя стадиями процедуры прямой гибридизации. Поэтому авторы изобретения исследовали эффект хранения при 4°С.
Материалы и методы
Эффект хранения при 4°С после процедуры конечной промывки исследовали с использованием модельной системы SPF10 следующим образом.
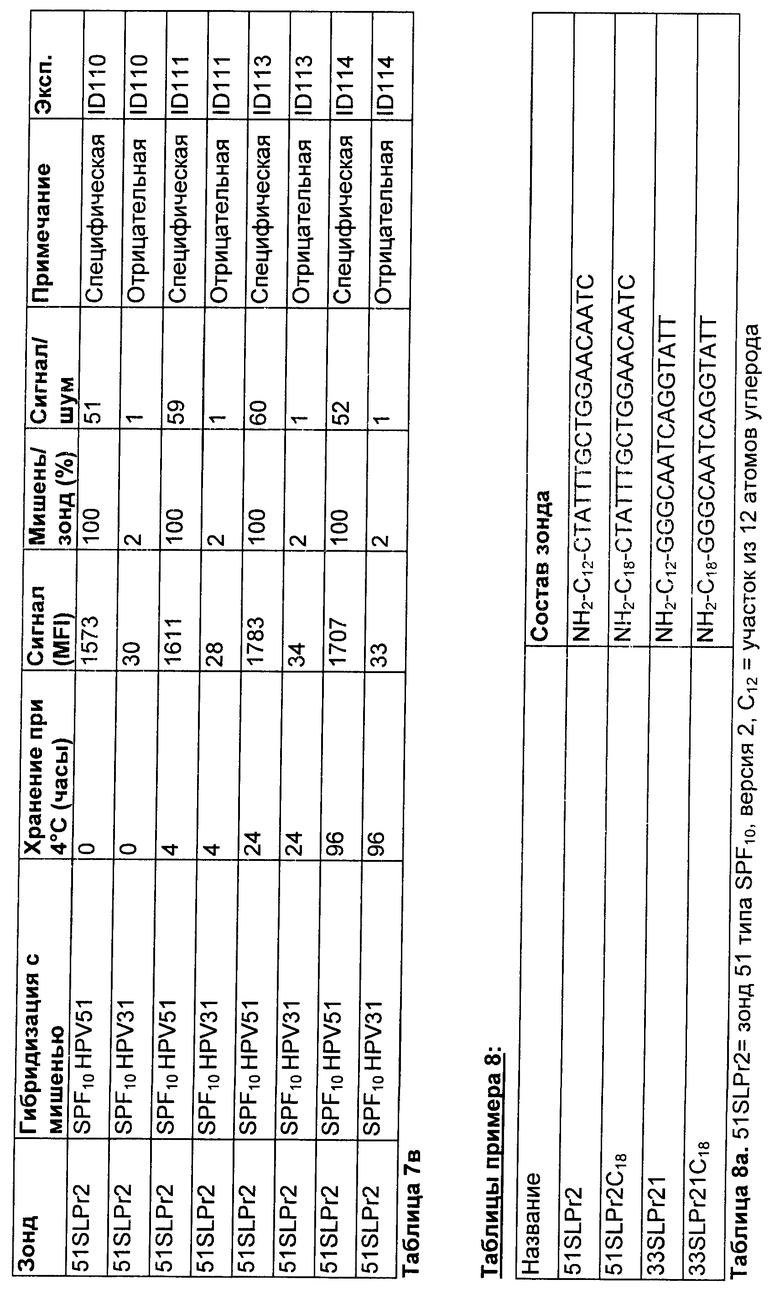
Для исследования этого эффекта использовали гранулы Luminex™, несущие зонд для HPV51 (название: 51SLPr2, см. таблицу 7а). Указанный зонд является специфическим для идентификации последовательностей HPV51, амплифицированных с использованием набора праймеров SPF10. Для наблюдения возможной перекрестной реактивности с 51SLPr2 использовали амплимеры для HPV31. Последовательности-мишени HPV51 и HPV31 различаются по 4 положениям (Таблица 7б).
После процедуры конечной промывки наборы реакций хранили при 4°С в течение 0, 4, 24 и 96 ч соответственно. Затем эти наборы реакций измеряли при к.т.
Результаты
Результаты показаны в таблице 7в. Как продемонстрировано, хранение после стадии конечной промывки не влияет на интенсивность или специфичность сигнала. Тем не менее, хранение, по-видимому, вносит незначительное улучшение в общую интенсивность сигнала с течением времени. Поэтому хранение после стадии конечной промывки может быть введено, при необходимости, в течение максимум 4 суток, при поддержании первоначального сигнала.
Заключение
Хранение после стадии конечной промывки не оказывает значительного влияния на интенсивность сигнала и специфичность сигнала, что повышает гибкость схемы работы.
Конструкция зонда (спейсера) - Введение
Ключевым принципом системы Luminex™ является иммобилизация специфического олигонуклеотидного зонда на поверхности микрогранулы, которая служит в качестве уникальной метки, благодаря цветовой композиции индивидуальных типов гранул.
В молекулярном масштабе гранула гораздо больше, чем специфический олигонуклеотидный зонд. Следовательно, специфическая последовательность зонда находится очень близко к поверхности гранулы Luminex™. Это расположение зонда может быть неоптимальным для кинетики гибридизации между иммобилизованным зондом и молекулами-мишенями в растворе из-за стерических препятствий и различных поверхностных эффектов гранулы, таких как гидрофобность поверхности.
Следующие примеры описывают множество подходов к изменению расположения зонда на поверхности гранулы для оптимизации кинетики гибридизации между зондом и мишенью.
Протестировали следующее варианты конструкции зонда:
1. Применение углеродного спейсера варьирующей длины.
2. Применение дополнительного олигонуклеотидного спейсера варьирующей длины.
3. Применение олигонуклеотидного спейсера варьирующего состава.
Зонд имеет три различных участка с разными функциями:
1. связывающую группу, такую как группа NH2, которая делает возможным ковалентное связывание зонда с поверхностью гранулы;
2. спейсер, который может служить (а) для создания расстояния между поверхностью гранулы и специфической последовательностью зонда и/или (б) для расположения специфического зонда в более гидрофильной среде; и
3. фактическую мишень-специфическую последовательность зонда: для этой части зонда применимы нормальные параметры в данной области, такие как состав и длина зонда.
Пример 8
Задача:
Определить эффект применения углеродного спейсера варьирующей длины.
Материалы и методы
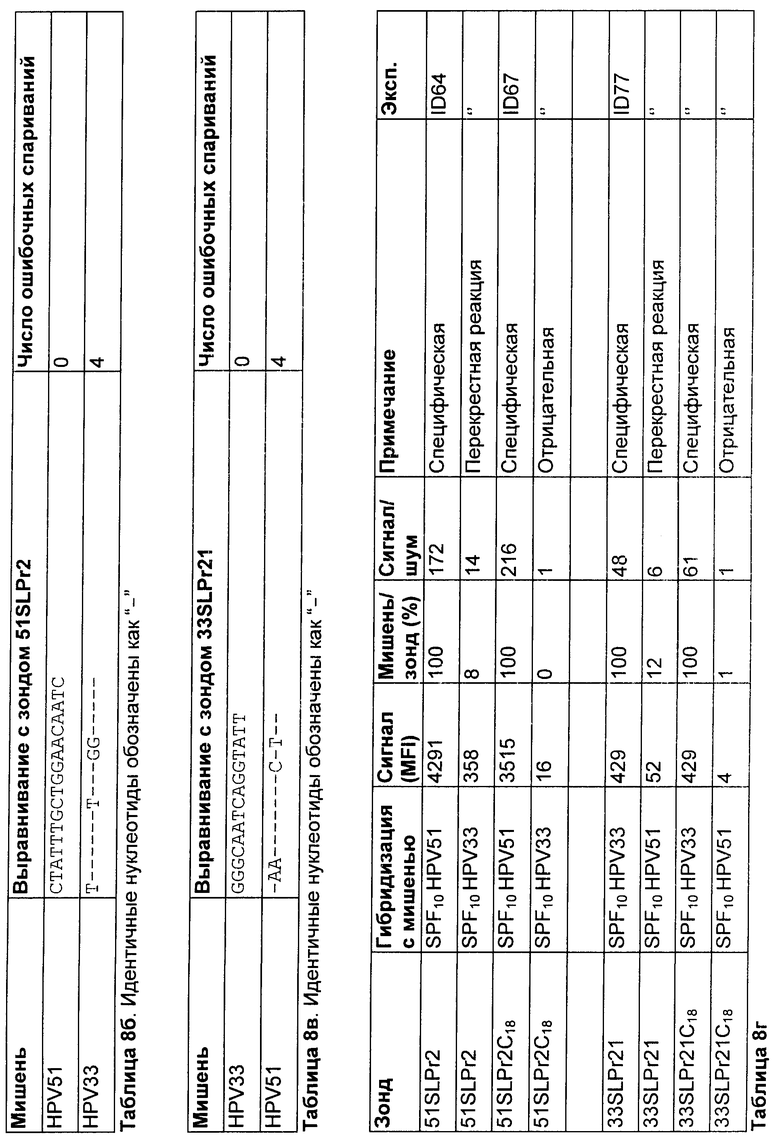
Использовали гранулы Luminex™, несущие зонд для HPV51 либо с С12спейсером (название: 51SLPr2, см. таблицу 8а), либо с С18спейсером (название: 51SLPr2C18, см. таблицу 8а). Эти зонды являются специфическими для идентификации последовательностей HPV51, амплифицированных с использованием набора праймеров SPF10. Для наблюдения возможной перекрестной реактивности с этими зондами использовали амплимеры для HPV33. Последовательности-мишени HPV51 и HPV33 различаются по 4 положениям (Таблица 8б).
Результаты
Результаты показаны в таблице 8в. С18спейсер приводил к уменьшению абсолютного сигнала, но специфичность была выше по сравнению с С12зондом. Этот феномен наблюдали не только для 51SLPr2C18, но также для других зондов с углеродным С18спейсером (например, 33SLPr21C18: Таблица 8а, в и г).
Заключение
Применение разных длин углеродного спейсера оказывает значительный эффект на специфичность сигнала. Что касается, например, 51SLPr2, то лучший зонд содержит углеродный С18спейсер.
Пример 9
Задача:
Определить эффект олигонуклеотидного спейсера варьирующей длины.
Материалы и методы
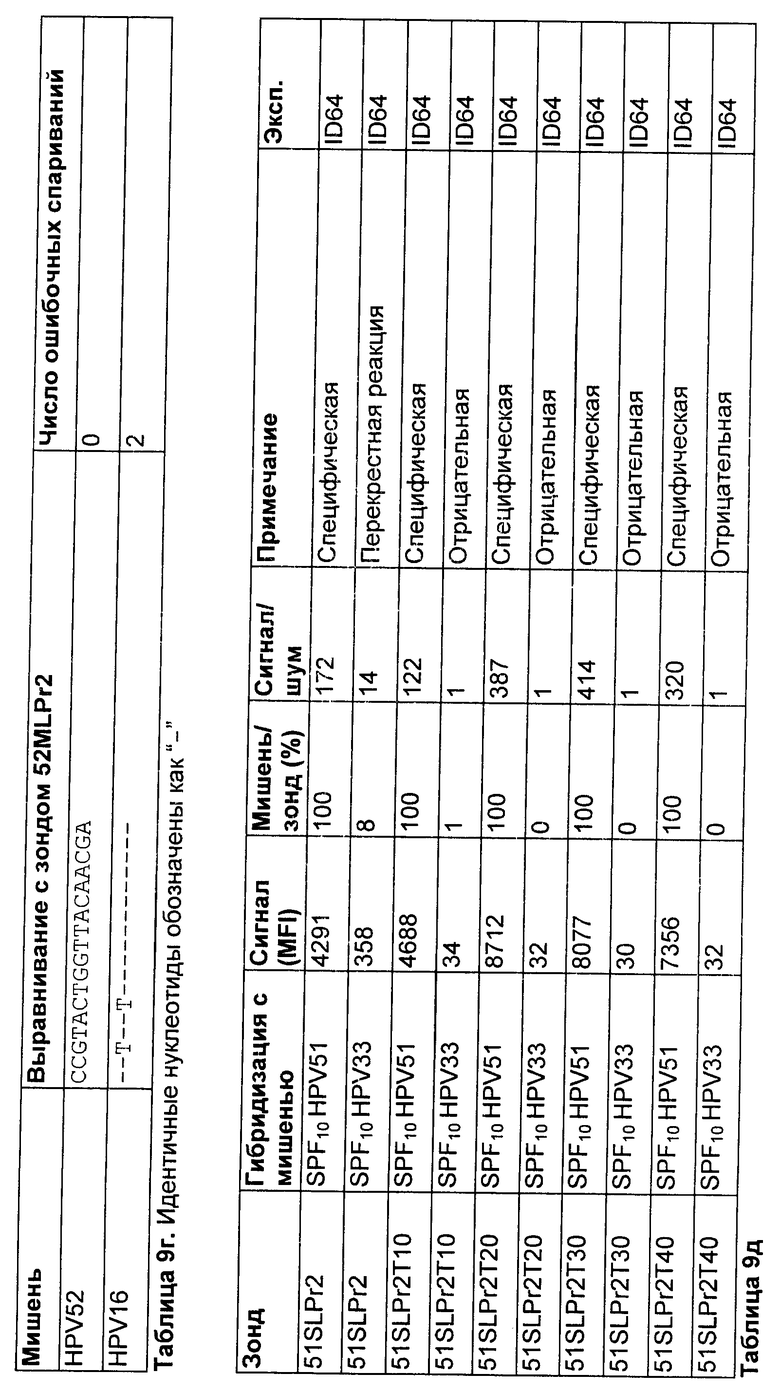
Использовали гранулы Luminex™, несущие зонд для HPV51 со спейсером из 0, 10, 20, 30 или 40 тиминов (название: 51SLPr2, 51SLPr2T10, 51SLPr2T20, 51SLPr2T30, 51SLPr2T40, см. таблицу 9a). Каждый тип гранул нес отдельный вариант зонда. Эти зонды являются специфическими для идентификации последовательностей HPV51, амплифицированных с использованием набора праймеров SPF10. Для наблюдения возможной перекрестной реактивности с этими зондами использовали амплимеры для HPV33. Последовательности-мишени HPV51 и HPV33 различаются по 4 положениям (Таблица 9с).
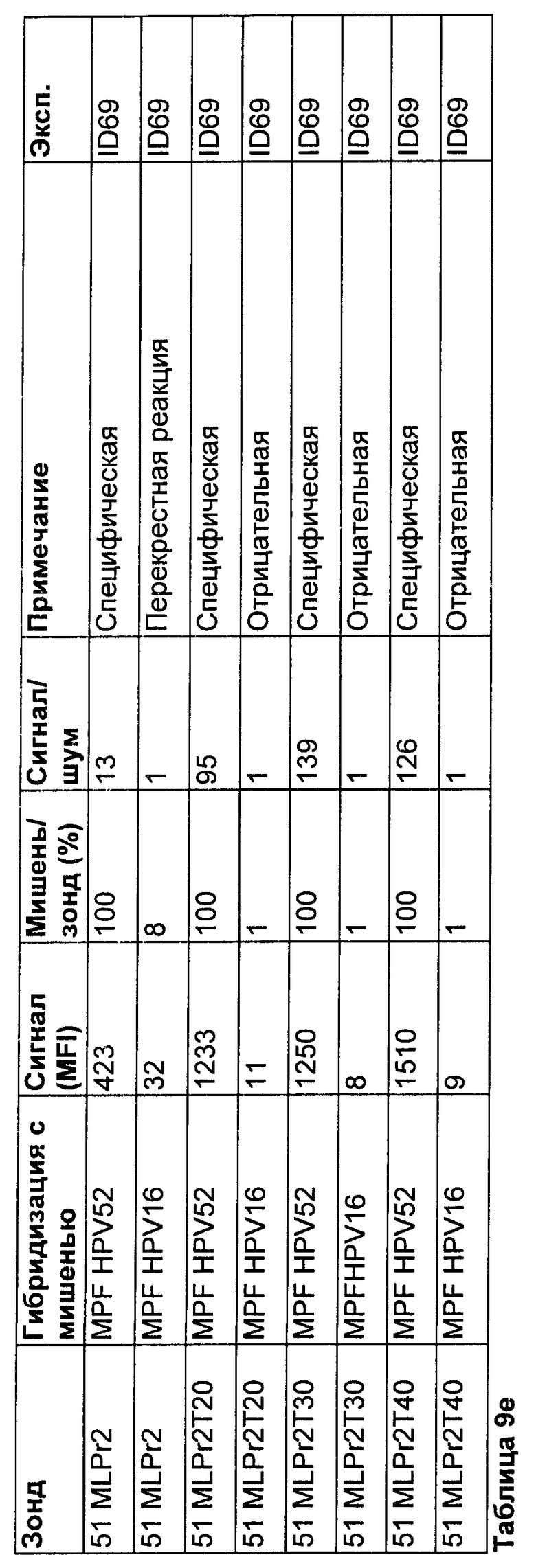
Этот эффект также исследовали следующим образом с использованием модельной системы MPF, помимо модельной системы SPF10. Использовали гранулы Luminex™, несущие зонд для HPV52 со спейсером, состоящим из 0, 20, 30 или 40 тиминов (название: 52MLPr2, 52MLPr2T20, 5MLPr2T30, 52MLPr2T40, см. таблицу 9б). Каждый тип гранул нес отдельный вариант зонда. Эти зонды являются специфическими для идентификации последовательностей HPV52, амплифицированных с использованием набора праймеров MPF. Для наблюдения возможной перекрестной реактивности с этими зондами использовали амплимеры для HPV16. Последовательности-мишени HPV52 и HPV16 различаются по 2 положениям (Таблица 9г).
Результаты
Результаты показаны в таблице 9д и 9е. Удлинение спейсера с использованием тиминового участка значительно увеличивает уровень абсолютного сигнала. Также значительно повышается специфичность по сравнению со спейсером без дополнительного тиминового спейсера. При сравнении спейсеров, имеющих разные длины, минимум 20 тиминовых остатков требуется для получения оптимального сигнала (например, 51SLPr2). В целом, зонды действуют лучше всего, когда они содержат спейсер из 40 нуклеотидов (например, 51SLPr2 и 52MLPr2). Поэтому эта длина спейсера является предпочтительной.
Заключение
Применение различных спейсеров оказывает значительный эффект не только на интенсивность сигнала, но и на специфичность. Что касается 51SLPr2Tn, то хороший зонд содержит спейсер из по меньшей мере 20 тиминовых нуклеотидов, увеличивающий как интенсивность, так и специфичность сигнала. В общем, спейсер с длиной по меньшей мере 40 нуклеотидов действует наилучшим образом.
Пример 10
Задача:
Определить, может ли применение модифицированного поли(Т) спейсера предотвращать ложноположительную реактивность.
Введение
Хорошо известно, что многие Taq ДНК-полимеразы добавляют дополнительный А-нуклеотид на 3′-конце синтезируемой цепи. Не известно, можно ли добавлять множественные А к 3′-концу, тем самым производя субпопуляцию молекул с олиго-А хвостом на 3′-конце.
Хотя такие молекулы будут представлять собой лишь очень малую долю от общего количества ПЦР-продукта, эти молекулы могут приводить к ложноотрицательному результату из-за высокой чувствительности данного способа детекции. Это происходит из-за гибридизации между такими олиго-А участками в ПЦР-продукте и поли(Т) спейсером зонда.
Этот артефакт ПЦР наблюдается в некоторых образцах, и его трудно воспроизвести на уровне ПЦР. Он, по-видимому, зависит от очень малых флуктуаций в реакционных условиях. На уровне детекции фон является очень воспроизводимым, т.е. ПЦР-продукт, генерирующий фон, будет делать это весьма воспроизводимым образом.
Этот артефакт ПЦР также может вызывать ложноположительные результаты в системе анализа с линейным зондом (LiPA), поскольку эта система также содержит зонды с Т-хвостами. В анализ LiPA это приводит к слабому равномерному (фоновому) сигналу со всех зондов, независимо от их специфической последовательности. Такие слабые фоновые считывания сигнала наблюдали также в системе Luminex™. Поэтому исследовали эффект модифицированного спейсера.
Материалы и методы
Использовали гранулы Luminex™, несущие зонд для HPV18 с использованием либо Т40 спейсера, либо модифицированного спейсера (TTG)13 (название: 18MLPr7T40 и 18MLPr7(TTG)13, см. таблицу 10а). Эти зонды являются специфическими для идентификации последовательностей HPV18, амплифицированных с использованием набора праймеров MPF. Триплет (TTG) выбрали в качестве альтернативного спейсера, поскольку он показывает одну из худших теоретических эффективностей связывания с поли(А).
Для наблюдения возможной перекрестной реактивности с 18MLPr7T40 и 18MLPr7(TTG)13 использовали амплимеры, происходящие из образцов, демонстрирующих этот ложноположительный фон (обозначены как nc8).
Результаты
Результаты показаны в таблице 10б.
Спейсер из 13 нуклеотидных триплетов "TTG" был отчетливо способен почти полностью элиминировать фоновой сигнал, который наблюдали для Т40 спейсера.
Заключение
Применение альтернативного спейсера на основе Т, такого как (TTG)13, оказывает значительный положительный эффект на специфичность сигнала, усираняющее ложноположительные сигналы, индуцированный А-обогащенными артефактами ПЦР.
Пример 11
Цель:
Исследовать, будет ли расположение спейсера на основе тимина либо на 5′-конце, либо на 3′-конце зонда исключать связывание с А-обогащенным участком мишени, фланкирующим сайт связывания мишени с зондом.
Введение
Известно, что ошибочные спаривания нуклеотидов в середине комплекса зонд/мишень оказывают большое влияние на энергию связывания. Ошибочные спаривания, близкие к концам участка связывания, являются более трудными для распознавания. В комбинации с положением А-обогащенных участков, фланкирующих участок связывания зонда с мишенью, это может наносить вред селективности зонда. Поэтому авторы изобретения исследовали влияние положения спейсера для минимизации его связывания с А-обогащенным участком мишени, фланкирующим сайт связывания мишени с зондом.
Материалы и методы
Эффект положения спейсера, расположенного между гранулой Luminex™ и специфической последовательностью зонда, либо на 5′-конце, либо на 3′-конце зонда, исследовали с использованием модельной системы MPF следующим образом.
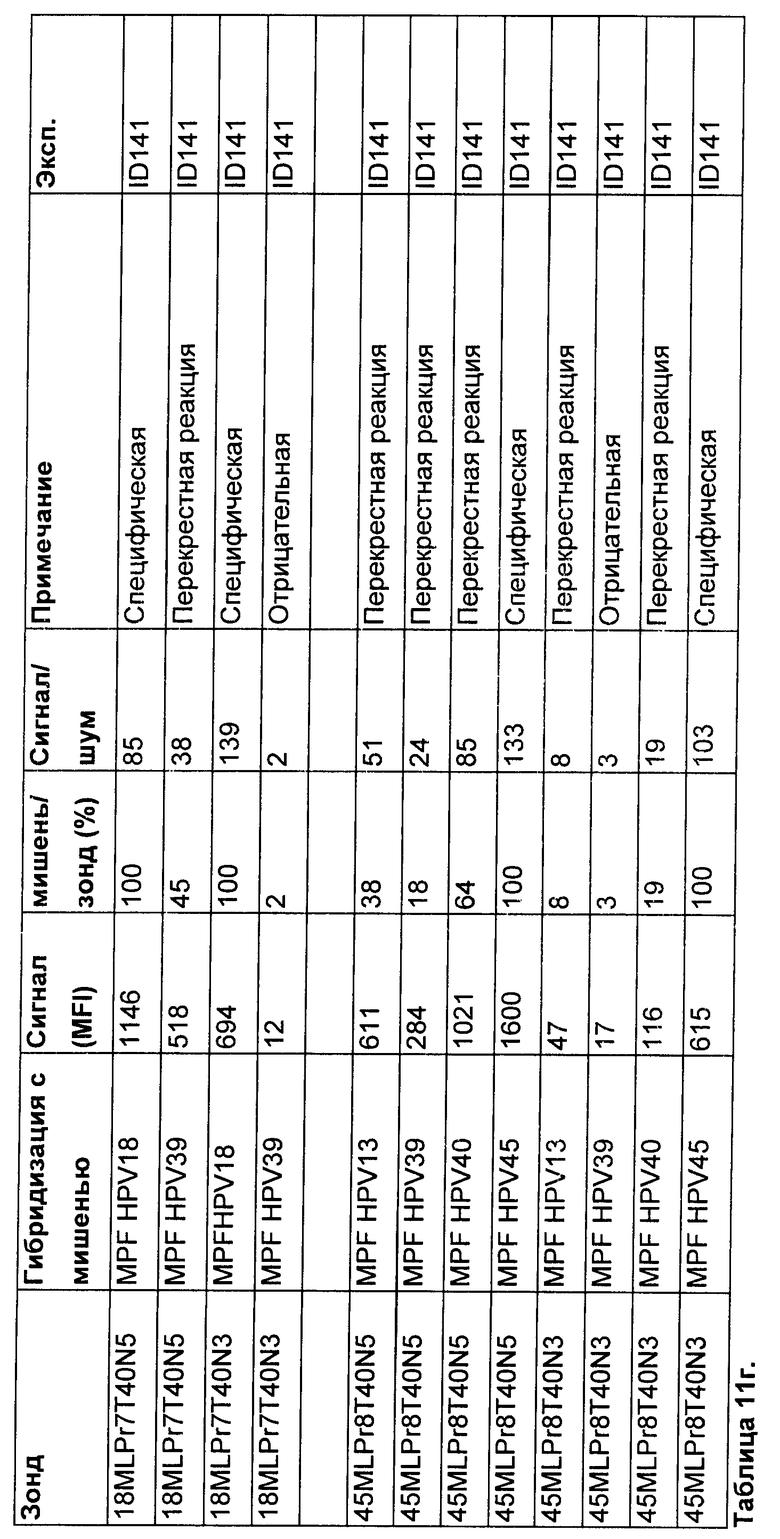
Для исследования этого эффекта использовали гранулы Luminex™, несущие зонд для HPV18 и HPV45 со спейсером на основе тимина (название: 18MLPr7T40N5, 18MLPr7T40N3, 45MLPr8T40N5 и 45MLPr8T40N3, см. таблицу 11а). Эти зонды являются специфическими для идентификации последовательностей HPV18 и HPV45, амплифицированных с использованием набора праймеров MPF соответственно. Для наблюдения возможной перекрестной реактивности с 18MLPr7T40n использовали амплимеры для HPV39. Последовательности-мишени HPV18 и HPV39 различаются по 2 положениям (Таблица 11б). Для наблюдения возможной перекрестной реактивности с 45 MLPr8T40n использовали амплимеры для HPV13, 39 и 40. Последовательности-мишени HPV45 и HPV13, 39 и 40 различаются по 3 положениям, 2 положениям и 1 положению соответственно (Таблица 11в).
Результаты
Результаты показаны в таблице 11г. Как продемонстрировано, спейсер на 3′-конце зонда вместо 5′-конца уменьшает его связывание с А-обогащенным участком мишени, фланкирующим сайт связывания мишени с зондом, влияя на энергию связывания (dG) и температуру плавления (Tms). Исключение этих неспецифических сигналов можно объяснить связыванием мишени со спейсером и зондом. Эти результаты позволяют предположить, что связывание мишени со спейсером может мешать специфичности зонда, что следует предотвращать. В принципе такой же механизм может иметь место при использовании спейсера из триплета нуклеотидов "TTG". Поэтому когда используют спейсер на основе тимина, стабильность гибрида зонд : мишень можно увеличить слабой перекрестной гибридизацией между спейсером и последовательностью, примыкающей к специфическому участку мишени, что приводит к ложноположительному сигналу, который следует учитывать при конструировании зонда.
Заключение
Положение спейсера на основе тимина либо на 5′-конце, либо на 3′-конце зонда может иметь значительный эффект в отношении связывания с А-обогащенным участком мишени, фланкирующим сайт связывания мишени с зондом.
Пример 12
Зонды для HPV, подходящие для применения в подходах на основе гранул, например для подходов на основе Luminex

В одном из аспектов данного изобретения любые 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21 или все 22 из всех указанных выше зондов можно использовать в мультиплексной реакции на основе гранул в идентичных условиях для одновременной детекции любой ДНК-мишени HPV, присутствующей в образце. Такие наборы гранул являются подходящими для применения в оптимизированной реакционной схеме, описанной выше. Может быть включен дополнительный полиуглеродный спейсер. Как таковое, изобретение относится к любому набору зондов, содержащему 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21 или все 22 из всех указанных зондов.
Общее заключение
Авторы изобретения предположили, что стерические препятствия и гидрофобное отталкивание приводят к субоптимальному различению ошибочного спаривания на концах гибрида. Кроме того, считают, что эти стерические препятствия уменьшают чувствительность, поскольку мишень связывается с зондом менее оптимальным образом. Так, было показано, что включение спейсера в конструкцию зонда предотвращает стерические препятствия и, следовательно, устраняет перекрестную гибридизацию и увеличивает чувствительность. Авторы изобретения наблюдали, что это действительно приводит к более высокой специфичности и чувствительности.
Хотя этот спейсер значительно увеличил эффективность зонда, некоторые перекрестные реакции все же наблюдались. Было обнаружено, что большинство этих перекрестных реакций имеют единственное ошибочное спаривание вблизи конца зонда (участок связывания мишени). Иногда такую перекрестную реакцию наблюдали в комбинации с А-обогащенным участком, фланкирующим участок связывания мишени с зондом. Поэтому авторы изобретения предположили, что такой А-обогащенный участок может связываться с частью Т-участка спейсера и тем самым увеличивать перекрестную реакцию. Первоначально авторы изобретения сконструировали зонд со спейсером на другом конце (3′ вместо 5′). Однако реконструирование спейсера с учетом последовательностей, фланкирующих участок связывания зонда, может быть альтернативой.
Авторы изобретения наблюдали, что в ПЦР иногда продуцируется искусственный продукт, который имеет тенденцию связываться со всеми зондами. Этот продукт может содержать множество остатков А на 3′-конце (это является известной активностью нескольких Taq-полимераз) и поэтому имеет повышенную аффинность к Т-спейсеру. Гибридизация А-Т может приводить к повышенной перекрестной реактивности, давая ложноположительные результаты гибридизации.
Для лучшего понимания этого феномена авторы изобретения сконструировали несколько зондов со спейсером, содержащим TTG-триплеты (например, (TTG)13). Авторы изобретения рассчитали, что этот триплет, в частности, будет наиболее отталкивающим и будет ослаблять связывание искусственного ПЦР-продукта с А-обогащенными участками, фланкирующими зондируемый участок мишени. Авторы изобретения наблюдали, что общая неспецифичность связывания этого искусственного ПЦР-продукта снижалась TTG-спейсером. TTG-спейсер также может уменьшать связывание фланкирующего участка зонда и увеличивать его специфичность.
В заключение:
- Стерические препятствия и гидрофобное отталкивание приводят к субоптимальному различению ошибочного спаривания на конце гибрида.
- Включение спейсера в конструкцию зонда предотвращает стерические препятствия и поэтому устраняет перекрестную гибридизацию, что приводит к более высокой специфичности и чувствительности.
- А-обогащенный участок, фланкирующий участок связывания мишени с зондом, может связываться с Т-участком спейсера и увеличивать перекрестную реакцию.
- Иногда ПЦР продуцирует искусственный продукт, содержащий на 3′-конце А-участки, которые имеют тенденцию связываться со всеми зондами.
- Этот продукт является А-обогащенным и поэтому имеет повышенную аффинность к Т-спейсеру.
- Этот феномен можно уменьшить с помощью TTG-спейсера, уменьшающего А-специфическое связывание участка, фланкирующего зонд, и увеличивающего его специфичность.










Изобретение относится к области биотехнологии, а именно к зонду для детекции и набору (варианты) для детекции целевой нуклеиновой кислоты, спейсеру, подходящему для присоединения к специфической к мишени последовательности зонда и способу детекции любого взаимодействия между заявленным зондом и целевой нуклеиновой кислотой. Зонд содержит: связывающую группу, которая делает возможным связывание зонда с поверхностью подложки в виде частиц; спейсер и мишень-специфическую олигонуклеотидную последовательность зонда. Спейсер содержит: олигонуклеотидный спейсер из по меньшей мере 20 нуклеотидов между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой, содержащий гомополимерный политиминовый спейсер или гетерополимерный спейсер из повторяющихся нуклеотидных звеньев, выбранных из группы, состоящей из TTG, TTTG, AAG, AAC, AAAG и АААС; и возможно углеродный спейсер из 12-30 углеродных звеньев между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой. Предложенное изобретение позволяет детектировать целевую нуклеиновую кислоту и увеличить соотношение сигнала к шуму в наборах. 7 н. и 18 з.п. ф-лы, 4 ил., 42 табл., 12 пр.
1. Зонд для детекции целевой нуклеиновой кислоты, подходящий для связывания с подложкой в виде частиц, содержащий:
а) связующую группу, которая делает возможным связывание зонда с поверхностью подложки в виде частиц;
б) спейсер и
в) мишень - специфическую олигонуклеотидную последовательность зонда,
где спейсер содержит:
1) олигонуклеотидный спейсер из по меньшей мере 20 нуклеотидов между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой, содержащий гомополимерный политиминовый спейсер или гетерополимерный спейсер из повторяющихся нуклеотидных звеньев, выбранных из группы, состоящей из TTG, TTTG, AAG, AAC, AAAG и АААС; и возможно
2) углеродный спейсер из 12-30 углеродных звеньев между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой.
2. Зонд по п.1, где спейсер включает как углеродный спейсер, так и олигонуклеотидный спейсер.
3. Зонд по п.1, где спейсер представляет собой олигонуклеотидный спейсер без углеродного спейсера и состоит из 25-150 нуклеотидов.
4. Зонд по п.1, где спейсер выбран таким образом, что он не гибридизуется с последовательностью - мишенью или фланкирующим участком данной мишени.
5. Зонд по п.1, где специфическая к мишени последовательность зонда является специфической к последовательности - мишени вируса папилломы человека.
6. Зонд по п.1, связанный с подложкой в виде частиц.
7. Зонд по п.6, где подложка представляет собой гранулу.
8. Зонд по п.6 или 7, где подложка выбрана из стекла или полистирола.
9. Зонд по п.1, где олигонуклеотидный спейсер содержит TTG-повторы.
10. Набор зондов по любому из пп.1-9 для детекции целевой нуклеиновой кислоты, содержащий по меньшей мере две разные специфические к мишени последовательности зондов, связанные с разными подложками в виде частиц, отличающимися друг от друга.
11. Набор зондов по п.10, где разные подложки в виде частиц мечены разными флуоресцентными молекулами.
12. Набор из 2-1000 разных специфических к мишени зондов для детекции целевой нуклеиновой кислоты, где каждый зонд содержит:
а) связующую группу, которая делает возможным связывание зонда с подложкой в виде частиц;
б) спейсер и
в) мишень - специфическую олигонуклеотидную последовательность зонда,
где спейсер содержит:
1) углеродный спейсер из 12-30 углеродных звеньев между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой; и
2) олигонуклеотидный спейсер из по меньшей мере 20 нуклеотидов между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой, содержащий гомополимерный политиминовый спейсер или гетерополимерный спейсер из повторяющихся нуклеотидных звеньев, выбранных из группы, состоящей из TTG, TTTG, AAG, AAC, AAAG и АААС, где олигонуклеотидный спейсер не гибридизуется с последовательностью - мишенью или фланкирующим участком данной мишени.
13. Набор по п.12, где олигонуклеотидный спейсер содержит TTG-повторы.
14. Спейсер, подходящий для присоединения к специфической к мишени последовательности зонда, содержащий углеродный спейсер из 12-30 звеньев и олигонуклеотид из по меньшей мере 20 нуклеотидов.
15. Набор для детекции целевой нуклеиновой кислоты, содержащий зонд, где указанный зонд содержит:
а) связующую группу, которая делает возможным связывание зонда с поверхностью подложки в виде частиц;
б) спейсер и
в) мишень - специфическую олигонуклеотидную последовательность зонда,
где спейсер содержит:
1) углеродный спейсер из 12-30 углеродных звеньев между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой; и
2) олигонуклеотидный спейсер из по меньшей мере 20 нуклеотидов между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой, содержащий гомополимерный политиминовый спейсер или гетерополимерный спейсер из повторяющихся нуклеотидных звеньев, выбранных из группы, состоящей из TTG, TTTG, AAG, AAC, AAAG и АААС, и подложку в виде частиц, такую как полистирольные гранулы.
16. Набор по п.15, где олигонуклеотидный спейсер содержит TTG-повторы.
17. Набор по п.15 или 16, содержащий набор из двух или более разных специфических к мишени последовательностей зондов для связывания с разными подложками в виде частиц, отличающимися друг от друга.
18. Набор для детекции целевой нуклеиновой кислоты, содержащий зонд, где указанный зонд содержит:
а) связующую группу, которая делает возможным связывание зонда с поверхностью подложки в виде частиц;
б) спейсер и
в) мишень - специфическую олигонуклеотидную последовательность зонда,
где спейсер содержит:
1) углеродный спейсер из 12-30 углеродных звеньев между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой; и
2) олигонуклеотидный спейсер из по меньшей мере 20 нуклеотидов между специфической к мишени последовательностью зонда и группой, связывающейся с подложкой, содержащий гомополимерный политиминовый спейсер или гетерополимерный спейсер из повторяющихся нуклеотидных звеньев, выбранных из группы, состоящей из TTG, TTTG, AAG, AAC, AAAG и АААС,
и инструкции по связыванию с подложкой в виде частиц, такой как полистирольные гранулы.
19. Набор по п.18, где олигонуклеотидный спейсер содержит TTG-повторы.
20. Набор по п.18 или 19, содержащий набор из двух или более разных специфических к мишени последовательностей зондов для связывания с разными подложками в виде частиц, отличающимися друг от друга.
21. Способ детекции любого взаимодействия между зондом по п.1 и целевой нуклеиновой кислотой, включающий следующие стадии:
1) денатурация любой двухцепочечной полинуклеиновой кислоты-мишени, присутствующей в образце;
2) гибридизация денатурированной мишени с зондом в условиях, которые позволяют осуществиться специфической гибридизации между зондом и мишенью;
3) (возможно жесткая промывка);
4) добавление репортерной молекулы и инкубация с ней, делающие возможным детекцию связывания зонда с мишенью;
5) (возможно промывка) и
6) детекция связывания зонда с мишенью, где указанный способ включает поддержание температуры гибридизации, начиная со стадии (2) до конца стадии (4).
22. Способ по п.21, где зонд связан с подложкой в виде частиц, такой как гранула.
23. Способ по п.21, где 2 или более разных зондов используют одновременно.
24. Способ по п.21, где длина специфической к мишени последовательности зонда разных специфических к мишени зондов является неидентичной.
25. Способ по любому из пп.21-24, где гибридизацию между зондом и мишенью осуществляют в ионной среде.
| XU HONGXIA et al | |||
| Multiplexed SNP genotyping using the Qbead system: a quantum dot-encoded microsphere-based assay// NUCLEIC ACIDS RESEARCH | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| KALLER M et al | |||
| Microarray-based AMASE as a novel approach for mutation detection// MUTATION RESEARCH | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| GUO Z et al | |||
| Direct fluorescence analysis of | |||
Авторы
Даты
2012-09-20—Публикация
2007-01-16—Подача