Изобретение относится к органической химии полимеров глицидилтриазолового ряда, конкретно к (со)полимерам N-глицидил-3-нитро-5-R-1,2,4-триазолов общей формулы
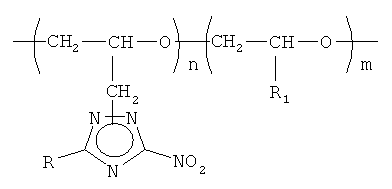
где R1=H, CH2N3, 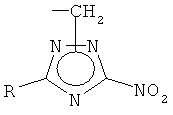 ;
;
R=H, СН3, С2Н5;
n=50÷100 мол.%;
m=0÷50 мол.%
и способам их получения.
Соединения вышеописанной формулы могут использоваться в качестве реагентов органического синтеза, компонентов газогенерирующих композиций, одними из основных требований которых являются высокая газопроизводительность (повышенные объем газов при сгорании и плотность) и высокая доля инертного азота.
Из уровня техники глицидильные полимеры и сополимеры с окисью этилена, с глицидилазидом, содержащие в качестве заместителя нитротриазольные фрагменты, их свойства и способ получения не обнаружены.
Аналогами заявляемых соединений являются поли-М-глицидил-4-фенил-1,2,3-триазол и его метил- и фторфенил производные (таблица 1) [Ji-Hye Jung, Yeong-Gweon Lim, Kyung-Hee Lee and Bon Tak Koo. Synthesis of glycidyl triazolyl polymers using click chemistry. - Tetrahedron Letters. - 48. - 2007. - P.6442-6448]. Общими недостатками аналогов являются низкий объем газов при сгорании, низкое содержание азота и недостаточно высокая плотность. Поли-N-глицидил-4-фенил-1,2,3-триазол и его метил- и фторфенил производные имеют объем газов при сгорании 811,15÷891,39 л/кг, содержат 19,17÷20,88% азота, плотность 1,23÷1,31 г/см3.
Наиболее близким структурным аналогом заявляемых (со)полимеров N-глицидил-3-нитро-5-R-1,2,4-триазолов является триазоловый полимер - N-глицидил-4-нитро-фенил-1,2,3-триазол (таблица 1), содержащий в качестве заместителя при циклическом атоме углерода 1,2,3-триазолового гетероцикла, нитрофенильный заместитель [Ji-Hye Jung, Yeong-Gweon Lim, Kyung-Hee Lee and Bon Tak Koo. Synthesis of glycidyl triazolyl polymers using click chemistry. - Tetrahedron Letters. - 48. - 2007. - P.6442-6448]. Недостатками данного соединения также являются низкий объем газов при сгорании 904,47 л/кг, низкое содержание азота 22,75% и недостаточно высокая плотность 1,36 г/см3.
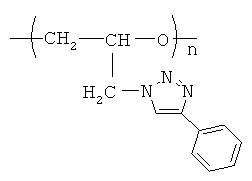
поли-N-глицидил-4-фенил-1,2,3-триазол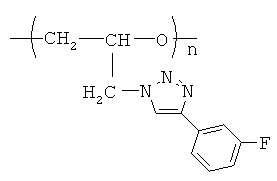
поли-N-глицидил-4-(3'-фторфенил)-1,2,3-триазол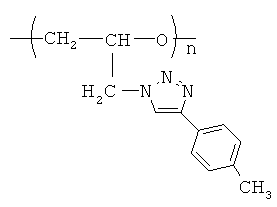
поли-N-глицидил-4-(4'-толил)-1,2,3-триазол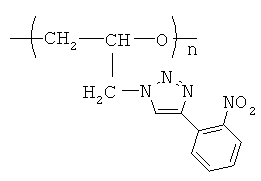
поли-N-глицидил-4-(2'-нитрофенил)-1,2,3-триазол
Способ получения вышеуказанных соединений является двухстадийным. На первой стадии полиэпихлоргидрин (ПЭХГ) растворяют в диметилформамиде (ДМФА) в течение 2-6 ч при температуре 100°С. Снижают температуру до 70°С и в реакционную смесь постепенно добавляют азид натрия (NaN3). Мольное соотношение ПЭХГ: NaN3=1,0:1,14-1,99. По окончании дозировки азида натрия температуру снова поднимают до 100°С и перемешивают реакционную смесь в течение 15 ч. Далее смесь охлаждают, твердые соли (NaCl и непрореагировавший NaN3) отфильтровывают, избыток ДМФА упаривают при 50°С под вакуумом, в смесь добавляют дихлорметан (ДХМ), проводят водные экстракции для удаления ДМФА и солей и обрабатывают 10% смесью ацетон/H2O или 10% метанол/Н2О. Раствор ДХМ высушивают сульфатом магния, затем пропускают через колонку, содержащую силикагель. Для удаления ДХМ полученный раствор нагревают при 50°С и затем сушат под вакуумом. Получают продукт полиглицидилазид [Е. Ahad. Synthesis and characterization of branched glycidyl azide polymer. DREV. Canada. 1991]. Полиглицидилазид также получают в среде диметилсульфоксида (ДМСО) при 100°С в течение 7 ч [Ji-Hye Jung, Yeong-Gweon Lim, Kyung-Hee Lee and Bon Tak Koo. Synthesis of glycidyl triazolyl polymers using click chemistry. - Tetrahedron Letters. - 48. - 2007. - P.6442-6448].
Вторая стадия основана на реакции 1,3-диполярного циклоприсоединения между азидогруппами полиглицидилазида и тройными связями соответствующих фенилацетиленов:
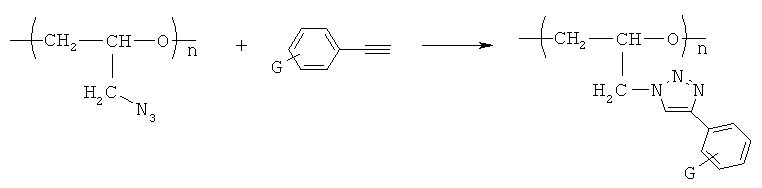
где G=Н; NO2; F; СН3.
В раствор полиглицидилазида в ДХМ добавляют водный раствор аскорбата натрия и меди (II) сернокислой 5-водной. В реакционную смесь добавляют фенилацетилены, замещенные различными заместителями (F, СН3, NO2), или незамещенный фенилацетилен. Смесь перемешивают при комнатной температуре в течение 8÷29 ч, выливают в ДХМ, отделяют органический слой и несколько раз промывают водой. Органический слой концентрируют, полученный раствор по каплям добавляют в пентан. Осадок отфильтровывают, высушивают под вакуумом и получают поли-N-глицидил-G-фенилтриазолы.
Недостатками способа получения поли-N-глицидил-G-фенилтриазолов является: многостадийность процесса (азидирование ПЭХГ; 1,3-диполярное циклоприсоединение); промежуточные и целевые продукты сложно выделяются с использованием большого числа различных реагентов (ПЭХГ, азид натрия, аскорбат натрия, медь (II) сернокислая 5-водная, незамещенные или замещенные фенилацетилены) и растворителей (ДМФА или ДМСО, ДХМ, ацетон или метанол); очистка промежуточных продуктов идет с использованием колонки, содержащей силикагель; использование высокотоксичного метанола и наличие в отходах токсичного и взрывоопасного азида натрия.
Техническая задача предлагаемого изобретения заключается в получении (со)полимеров N-глицидил-3-нитро-5-R-1,2,4-триазолов, обладающих высоким объемом продуктов при сгорании, высокой плотностью и содержанием азота и разработке способа их получения.
Поставленная техническая задача достигается тем, что в качестве таких соединений предлагаются (со)полимеры N-глицидил-3-нитро-5-R-1,2,4-триазолов общей формулы

где R1=H, CH2N3,  ;
;
R=H, СН3, С2Н5;
n=50÷100 мол.%;
m=0÷50 мол.%
и способы их получения:
1. Путем обработки натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной, где R=H, СН3, С2Н5 (со)полимерами глицидилхлорида общей формулы
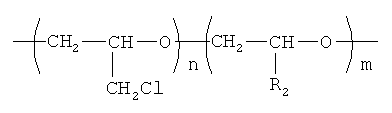
где R2=Н; CH2Cl;
n=50÷100 мол.%;
m=0÷50 мол.%,
в среде диметилформамида при температуре 95°÷135°С и мольном соотношении натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная:(со)полимер глицидилхлорида, равном 1,5:1,0, в течение 3-10 часов.
2. Путем обработки натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной, где R=H, СН3, C2H5 и азида натрия полимером глицидилхлорида общей формулы
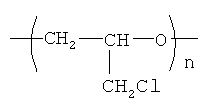
где n=100 мол.%,
в среде диметилформамида при температуре 95°÷135°С и мольном соотношении натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная : азид натрия : полиглицидилхлорид, равном 1,0-1,25:0,25-0,5:1,0 в течение 3÷10 часов.
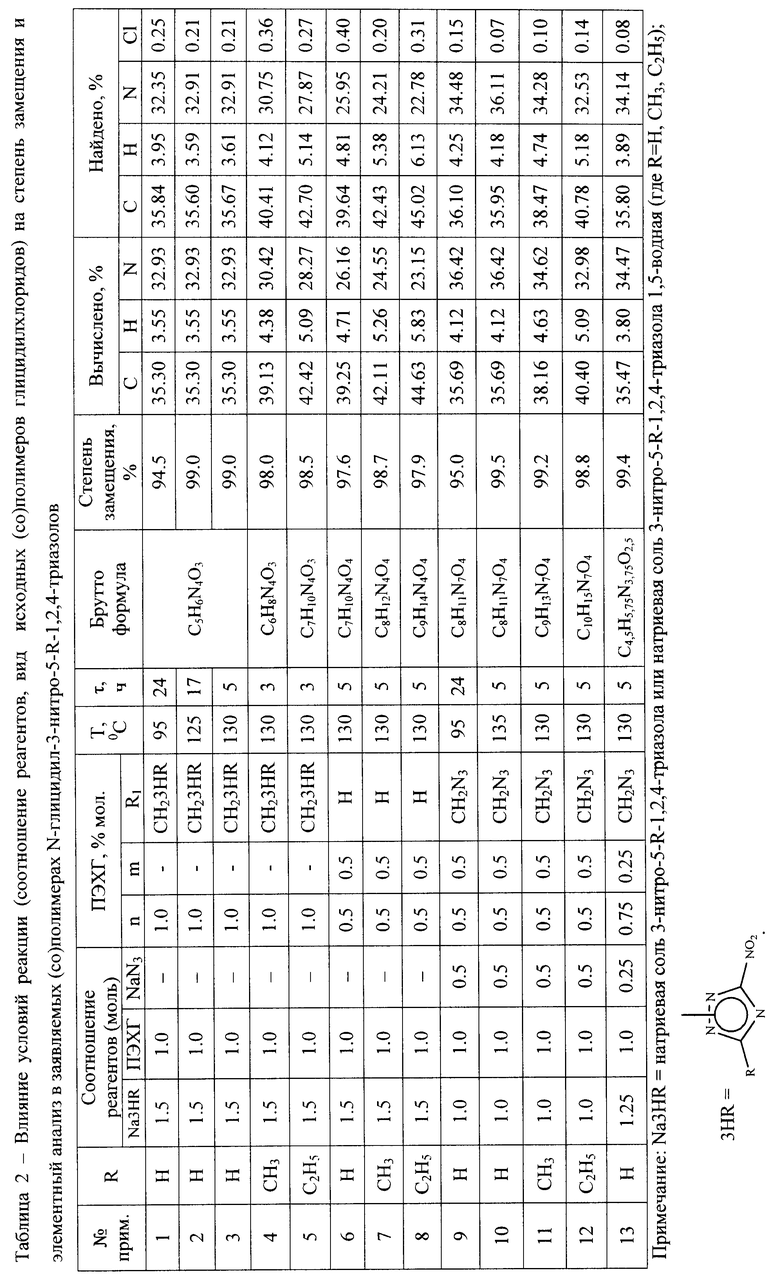
Синтез глицидилтриазоловых (со)полимеров, содержащих в качестве заместителей при атоме углерода гетероцикла NO2-группы вместо фенильных производных, обеспечивает комплекс существенных отличительных признаков настоящего изобретения (таблица 2):
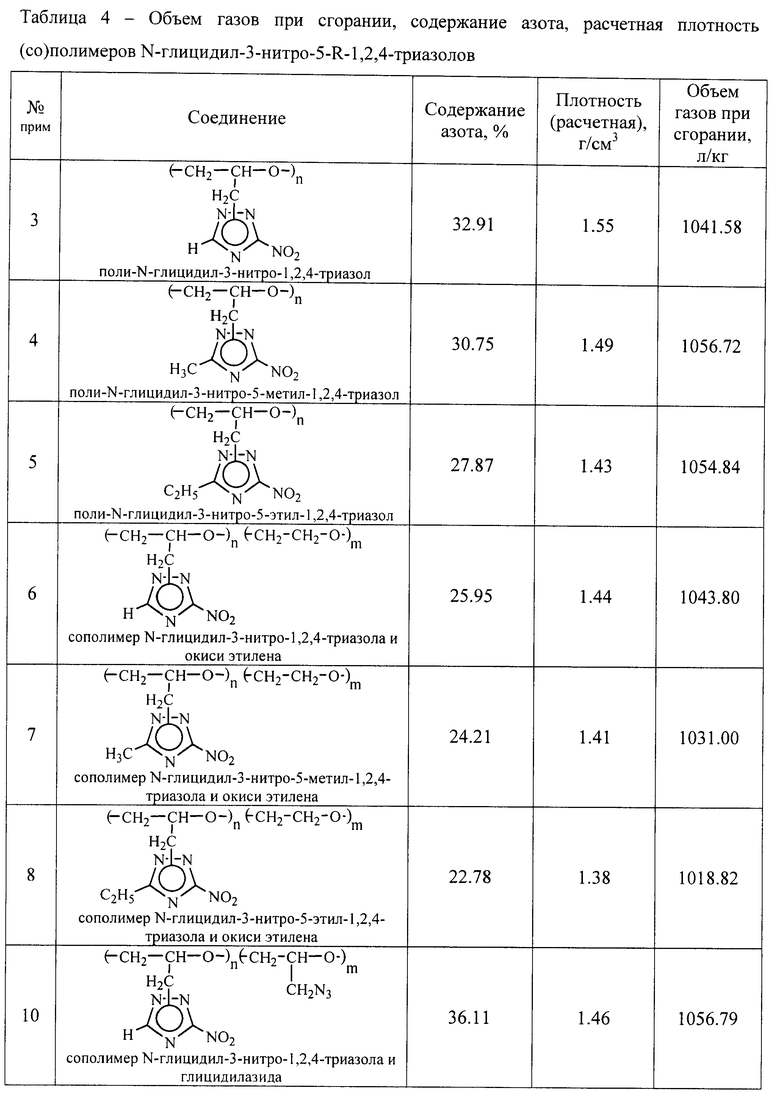
1. Все (со)полимеры N-глицидил-3-нитро-5-R-1,2,4-триазолов обеспечивают увеличение объема газов при сгорании на 14,0÷30,7% по сравнению со структурными аналогами.
2. Все (со)полимеры N-глицидил-3-нитро-5-R-1,2,4-триазолов имеют повышенную плотность. По сравнению с поли-N-глицидил-G-фенилтриазолами плотность увеличивается с 1,36 г/см3 до 1,38÷1,55 г/см3. Высокая плотность обеспечивает повышение производительности газогенератора с единицы объема.
3. Все (со)полимеры N-глицидил-3-нитро-5-R-1,2,4-триазолов имеют повышенное содержание азота. По сравнению с поли-N-глицидил-G-фенилтриазолами содержание азота увеличивается с 22,75% до 22,78÷36,11%.
4. По сравнению со способом получения поли-N-глицидил-G-фенилтриазолов сокращается количество стадий; количество реагентов и растворителей. В заявляемых условиях, при получении сополимеров N-глицидил-3-нитро-5-R-1,2,4-триазолов с глицидилазидом, азид натрия полностью расходуется, в реакционных смесях и маточных растворах после выделения целевых полимеров полностью отсутствует азид ион.
Таким образом, предлагаемые (со)полимеры N-глицидил-3-нитро-5-R-1,2,4-триазолов благодаря введению в их структуру 3-нитро-5-R-1,2,4-триазолов приобретают новые положительные свойства, что позволяет сделать вывод о соответствии заявляемых объектов критерию «изобретательский уровень».
Совокупность этих существенных признаков обеспечивает возможность использования заявляемых веществ в качестве компонентов газогенерирующих композиций.
Общий способ получения (со)полимеров N-глицидил-3-нитро-5-R-1,2,4-триазолов.
К раствору (со)полимера глицидилхлорида в диметилформамиде засыпают натриевую соль 3-нитро-5-R-1,2,4-триазола или натриевую соль 3-нитро-5-R-1,2,4-триазола 1,5-водную (в синтезе сополимеров с глицидилазидом дополнительно добавляют NaN3) и выдерживают при температуре 95÷135°С в течение 3÷10 ч. Охлажденную реакционную массу выливают при перемешивании в воду, выпавший продукт отделяют от маточного раствора, тщательно промывают дистиллированной водой, высушивают в вакууме.
Схема получения (со)полимеров N-глицидил-3-нитро-5-R-1,2,4-триазолов:
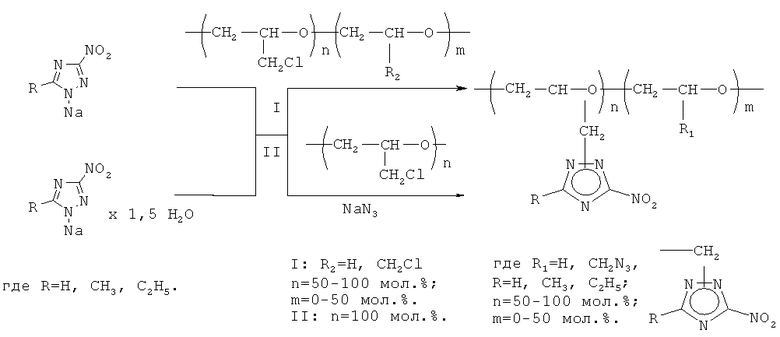
Соотношение реагентов, вид исходных (со)полимеров глицидилхлорида, температура, время реакции и степень замещения приведены для конкретных примеров в таблице 2.
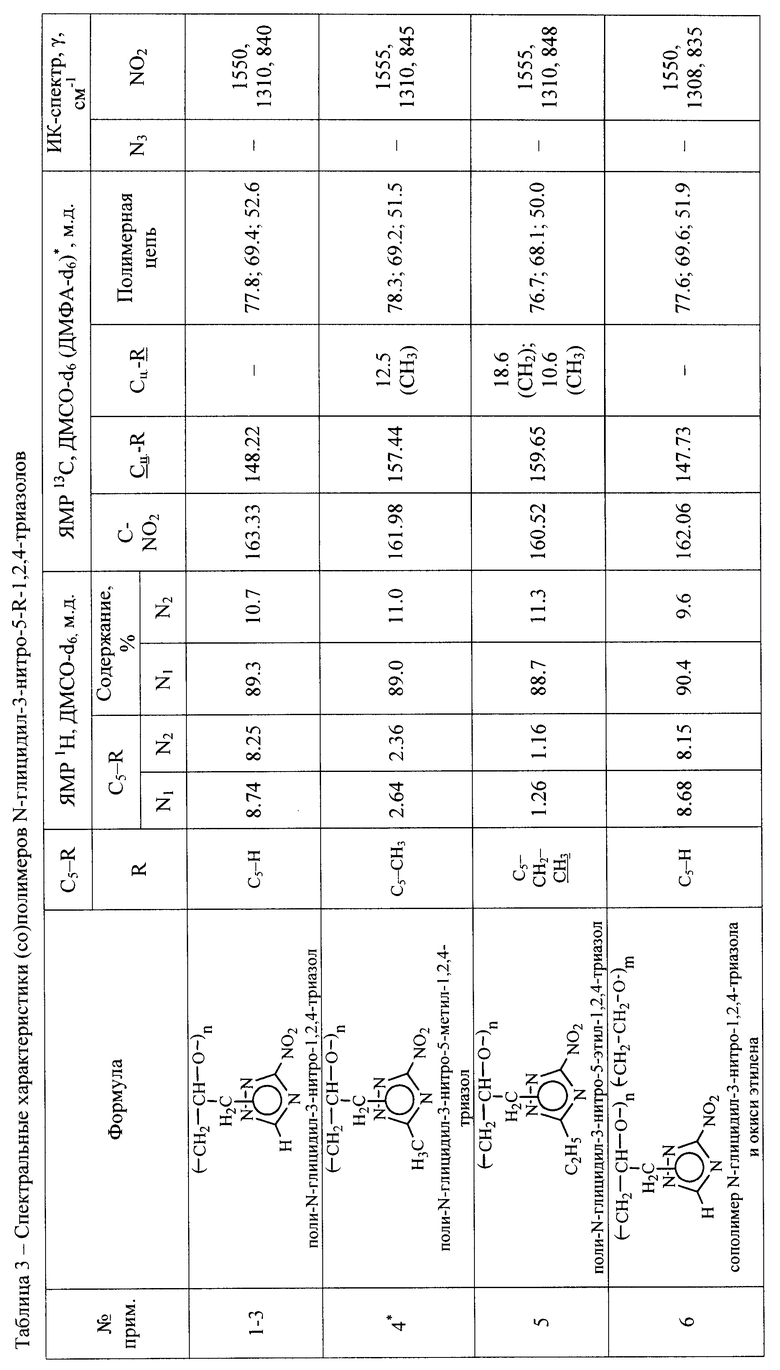
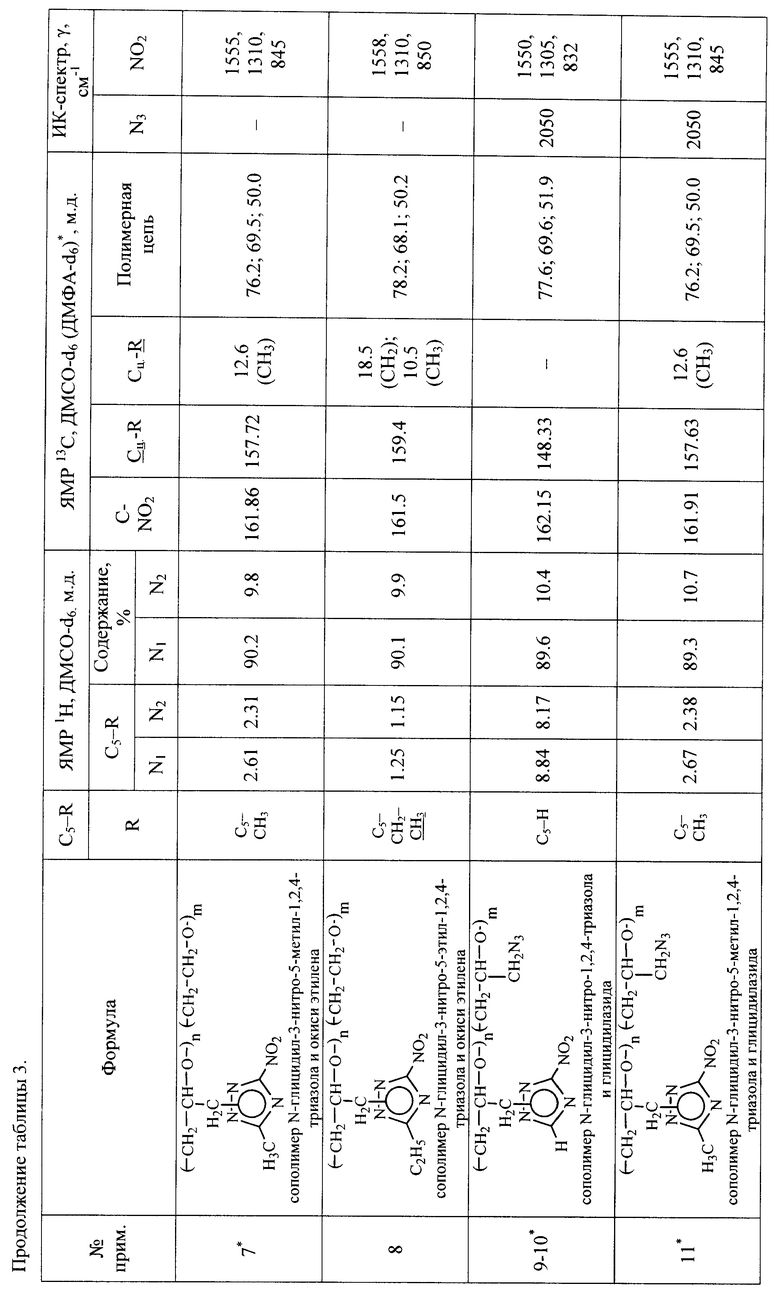
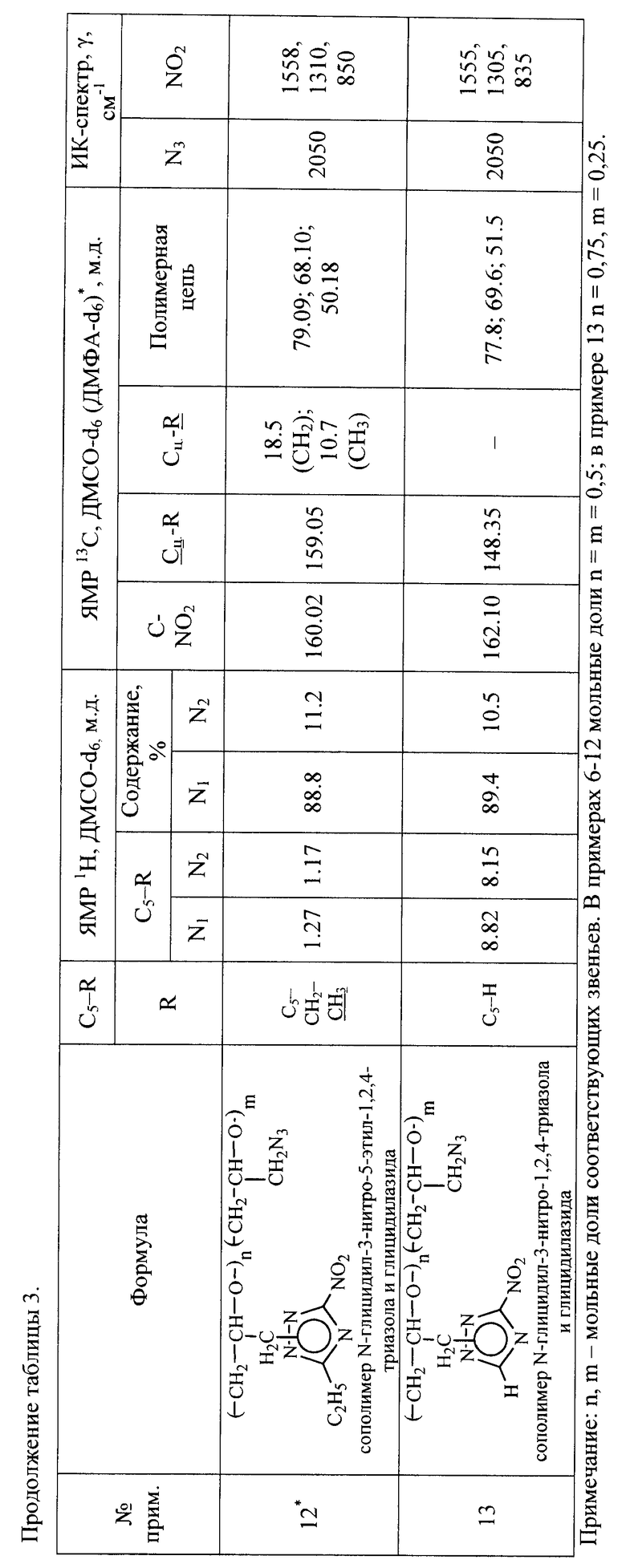
Все полученные (со)полимеры N-глицидил-3-нитро-5-R-1,2,4-триазолов идентифицированы их спектральными данными, приведенными в таблице 3, и элементным анализом, приведенным в таблице 2.
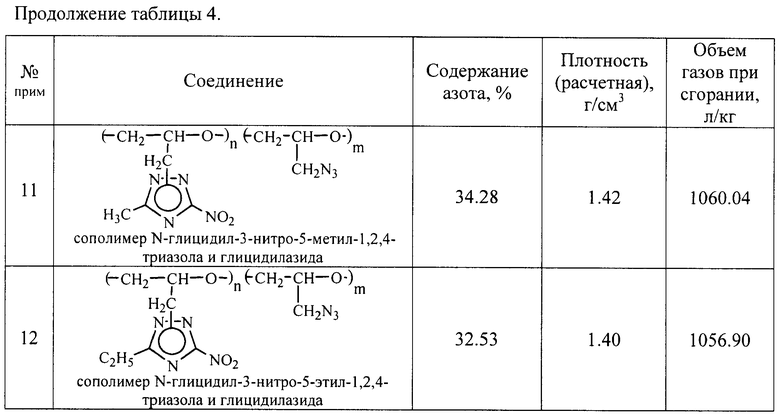
Объем газов при сгорании, содержание азота и расчетная плотность (со)полимеров N-глицидил-3-нитро-5-R-1,2,4-триазолов представлены в таблице 4.
Для получения (со)полимеров R-глицидил-3-нитро-5-R-1,2,4-триазолов необходимо
для реакции (I):
1. Реакцию проводить при температуре 95÷135°С. Снижение температуры ниже 95°С приводит к снижению степени замещения хлора, в (со)полимерах глицидилхлорида, на 3-нитро-5-R-1,2,4-триазольные фрагменты и увеличению продолжительности реакции, повышение температуры выше 135°С не рекомендуется с позиций технологичности метода получения.
2. Использовать мольное соотношение натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная : (со)полимеры глицидилхлорида, равное 1,5:1,0. Уменьшение мольного избытка натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной по отношению к (со)полимерам глицидилхлорида приводит к увеличению продолжительности реакции для достижения высокой степени замещения хлора на 3-нитро-5-R-1,2,4-триазольные фрагменты, а увеличение экономически нецелесообразно.
3. Реакцию проводить в течение 3÷10 часов. Сокращение времени реакции ниже 3 часов приводит к снижению степени замещения хлора, в (со)полимерах глицидилхлорида, на 3-нитро-5-R-1,2,4-триазольные фрагменты, увеличение времени реакции выше 10 часов экономически нецелесообразно, поскольку не приводит к повышению степени замещения.
для реакции (II):
1. Реакцию проводить при температуре 95÷135°С. Снижение температуры ниже 95°С приводит к снижению степени замещения хлора, в (со)полимерах глицидилхлорида, на 3-нитро-5-R-1,2,4-триазольные фрагменты и увеличению продолжительности реакции, повышение температуры выше 135°С не рекомендуется с позиций технологичности метода получения.
2. Использовать мольное соотношение натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная : азид натрия : (со)полимеры глицидилхлорида, равное 1,0-1,25:0,25-0,5:1,0. Уменьшение мольного избытка натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной по отношению к (со)полимерам глицидилхлорида приводит к увеличению продолжительности реакции для достижения высокой степени замещения хлора на 3-нитро-5-R-1,2,4-триазольные фрагменты, а увеличение экономически нецелесообразно.
3. Мольная доля глицидилазида регулируется дозировкой в реакционную смесь азида натрия. В реакционных смесях и маточных растворах после выделения целевых полимеров полностью отсутствует азид ион.
4. Реакцию проводить в течение 3÷10 часов. Сокращение времени реакции ниже 3 часов приводит к снижению степени замещения хлора, в (со)полимерах глицидилхлорида, на 3-нитро-5-R-1,2,4-триазольные фрагменты, увеличение времени реакции выше 10 часов экономически нецелесообразно, поскольку не приводит к повышению степени замещения.
Примеры конкретного получения заявляемых соединений приведены ниже.
Поли-N-глицидил-3-нитро-1,2,4-триазол
Пример 1
К раствору 0,1 моля полиглицидилхлорида (ПЭХГ) в 100 мл диметилформамида засыпают 0,15 моля натриевой соли 3-нитро-1,2,4-триазола и выдерживают при температуре 95°С 24 ч. Охлажденную реакционную массу выливают при перемешивании в воду, выпавший полимер отделяют от маточного раствора, тщательно промывают дистиллированной водой, высушивают в вакууме. Степень замещения 94,5%.
Пример 2
Проводят аналогично примеру 1, но используют натриевую соль 3-нитро-1,2,4-триазола 1,5-водную, реакционную смесь выдерживают при температуре 125°С в течение 17 ч. Степень замещения 99,0%.
Пример 3
Проводят аналогично примеру 1, но реакционную смесь выдерживают при температуре 130°С в течение 5 ч. Степень замещения 99,0%.
Поли-N-глицидил-3-нитро-5-метил-1,2,4-триазол
Пример 4
Проводят аналогично примеру 3, но используют 28,5 мл диметилформамида, 0,15 моля натриевой соли 3-нитро-5-метил-1,2,4-триазола и реакционную смесь выдерживают при температуре 130°С в течение 3 ч. Степень замещения 98,0%.
Поли-R-глицидил-3-нитро-5-этил-1,2,4-триазол
Пример 5
Проводят аналогично примеру 4, но используют 0,15 моля натриевой соли 3-нитро-5-этил-1,2,4-триазола и реакционную смесь выдерживают при температуре 130°С в течение 3 ч. Степень замещения 98,0%.
Сополимер N-глицидил-3-нитро-1,2,4-триазола и окиси этилена
Пример 6
Проводят аналогично примеру 3, но используют 0,1 моля сополимера глицидилхлорида (50 мол.%) и окиси этилена (50 мол.%) и реакционную смесь выдерживают при температуре 130°С в течение 5 ч. Степень замещения 97,6%.
Сополимер N-глицидил-3-нитро-5-метил-1,2,4-триазола и окиси этилена
Пример 7
Проводят аналогично примеру 6, но используют 0,15 моля натриевой соли 3-нитро-5-метил-1,2,4-триазола и реакционную смесь выдерживают при температуре 130°С в течение 5 ч. Степень замещения 98,7%.
Сополимер N-глицидил-3-нитро-5-этил-1,2,4-триазола и окиси этилена
Пример 8
Проводят аналогично примеру 6, но используют 0,15 моля натриевой соли 3-нитро-5-этил-1,2,4-триазола и реакционную смесь выдерживают при температуре 130°С в течение 5 ч. Степень замещения 97,9%.
Сополимер N-глицидил-3-нитро-1,2,4-триазола и глицидилазида
Пример 9
Проводят аналогично примеру 1, но используют 0,1 моля натриевой соли 3-нитро-1,2,4-триазола, 0,05 моля азида натрия и реакционную смесь выдерживают при температуре 95°С в течение 24 ч. Степень замещения 95,0%.
Пример 10
Проводят аналогично примеру 3, но используют 0,1 моля натриевой соли 3-нитро-1,2,4-триазола, 0,05 моля азида натрия и реакционную смесь выдерживают при температуре 135°С в течение 5 ч. Степень замещения 99,5%.
Сополимер N-глицидил-3-нитро-5-метил-1,2,4-триазола и глицидилазида
Пример 11
Проводят аналогично примеру 3, но используют 0,1 моля натриевой соли 3-нитро-5-метил-1,2,4-триазола 1,5-водной и 0,05 моля азида натрия, реакционную смесь выдерживают при температуре 130°С в течение 5 ч. Степень замещения 99,2%.
Сополимер N-глицидил-3-нитро-5-этил-1,2,4-триазола и глицидилазида
Пример 12
Проводят аналогично примеру 3, но используют 0,1 моля натриевой соли 3-нитро-5-этил-1,2,4-триазола и 0,05 моля азида натрия, реакционную смесь выдерживают при температуре 130°С в течение 5 ч. Степень замещения 98,8%.
Сополимер N-глицидил-3-нитро-1,2,4-триазола и глицидилазида
Пример 13
Проводят аналогично примеру 3, но используют 0,125 моля натриевой соли 3-нитро-1,2,4-триазола, 0,025 моля азида натрия и реакционную смесь выдерживают при температуре 130°С в течение 5 ч. Степень замещения 99,4%.
| название | год | авторы | номер документа |
|---|---|---|---|
| 1,4-ДИАЛКИЛ-3-НИТРО-5-R-1,2,4-ТРИАЗОЛИЕВЫЕ СОЛИ ДИНИТРАМИДА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2408588C2 |
| 2-(5-НИТРОНИЛФУРАН-2-ИЛ)-5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-А]ПИРИМИДИН-7(4Н)-ОН И ЕГО СОЛИ | 2018 |
|
RU2716715C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ 3,5-ДИНИТРО-1,2,4-ТРИАЗОЛА | 2000 |
|
RU2174120C1 |
| СПОСОБ ПОЛУЧЕНИЯ R-МЕТИЛПРОИЗВОДНЫХ 3,5-ДИАМИНО-1,2,4-ТРИАЗОЛА | 2005 |
|
RU2292340C1 |
| АЗОЛОАЗИНИЕВЫЕ СОЛИ ФТОРХИНОЛОНОВ, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНЫМ И ПРОТИВОВИРУСНЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2547835C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ БИС[ДИАЛКОКСИФОСФОРИЛ]АЦЕТАМИДИНОВ | 2009 |
|
RU2415861C1 |
| ПРОИЗВОДНОЕ АЛЬФА-АМИНОГИДРОКСАМОВОЙ КИСЛОТЫ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2265592C2 |
| СЕЛЕКТИВНЫЕ ПРОТИВОТУБЕРКУЛЕЗНЫЕ АГЕНТЫ, ПРЕДСТАВЛЯЮЩИЕ СОБОЙ ЗАМЕЩЕННЫЕ 7-АРИЛ(ГЕТЕРИЛ)-6-КАРБЭТОКСИ-4,7-ДИГИДРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНЫ ИЛИ ЗАМЕЩЕННЫЕ 7-АРИЛ(ГЕТЕРИЛ)-4,7-ДИГИДРО-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ АДДИТИВНЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 7-АРИЛ(ГЕТЕРИЛ)-6-КАРБЭТОКСИ-5-МЕТИЛ-4,7-ДИГИДРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИНОВ | 2007 |
|
RU2360905C2 |
| ПРОИЗВОДНОЕ 2-ЗАМЕЩЕННОГО САХАРИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ ИНГИБИТОРНУЮ АКТИВНОСТЬ ПРОТИВ ЭЛАСТАЗЫ | 1992 |
|
RU2101281C1 |
| ИНСЕКТИЦИДНЫЕ ИЗОКСАЗОЛИНЫ | 2007 |
|
RU2452736C2 |
Изобретение относится к органической химии полимеров глицидилтриазолового ряда. Предложены (со)полимеры N-глицидил-3-нитро-5-R-1,2,4-триазолов общей формулы I, где R1=H, CH2N3,  ; n=50÷100 мол.%; m=0÷50 мол.%. Предложены также варианты способа получения предложенных соединений: для получения соединения формулы I, где R1=H или
; n=50÷100 мол.%; m=0÷50 мол.%. Предложены также варианты способа получения предложенных соединений: для получения соединения формулы I, где R1=H или  - обработка натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной, где R=H, СН3, С2Н5 (со)полимерами глицидилхлорида общей формулы II при мольном соотношении (натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная): ((со)полимер глицидилхлорида)=1,5:1,0, а для получения соединения формулы I, где R1=CH2N3 - обработка натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной, где R=H, СН3, С2Н5 и азида натрия полимером глицидилхлорида общей формулы II при мольном соотношении (натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная):(азид натрия):((со)полимер глицидилхлорида)=(1,0-1,25):(0,25-0,5):1,0. Обработку проводят в среде диметилформамида при температуре 95÷135°C в течение 3÷10 часов. Технический результат - предложенные (со)полимеры обладают высоким объемом продуктов при сгорании, высокой плотностью и содержанием азота и могут использоваться в качестве компонентов газогенерирующих композиций и реагентов органического синтеза. 3 н.п. ф-лы, 4 табл., 13 пр.
- обработка натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной, где R=H, СН3, С2Н5 (со)полимерами глицидилхлорида общей формулы II при мольном соотношении (натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная): ((со)полимер глицидилхлорида)=1,5:1,0, а для получения соединения формулы I, где R1=CH2N3 - обработка натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной, где R=H, СН3, С2Н5 и азида натрия полимером глицидилхлорида общей формулы II при мольном соотношении (натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная):(азид натрия):((со)полимер глицидилхлорида)=(1,0-1,25):(0,25-0,5):1,0. Обработку проводят в среде диметилформамида при температуре 95÷135°C в течение 3÷10 часов. Технический результат - предложенные (со)полимеры обладают высоким объемом продуктов при сгорании, высокой плотностью и содержанием азота и могут использоваться в качестве компонентов газогенерирующих композиций и реагентов органического синтеза. 3 н.п. ф-лы, 4 табл., 13 пр.
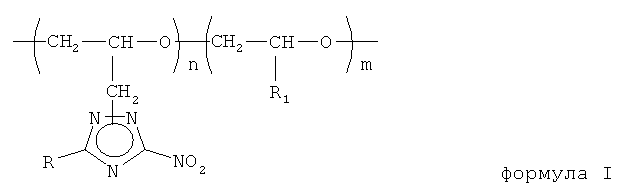

1. (Со)полимеры N-глицидил-3-нитро-5-R-1,2,4-триазолов общей формулы

где R1 - H, CH2N3, 
R - H, СН3, С2Н5;
n=50÷100 мол.%;
m=0÷50 мол.%.
2. Способ получения (со)полимеров N-глицидил-3-нитро-5-R-1,2,4-триазолов общей формулы

где R1 - H, 
R - H, CH3, C2H5,
n=50÷100 мол.%;
m=0÷50 мол.%,
заключающийся в обработке натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной, где R - H, СН3, С2Н5, (со)полимерами глицидилхлорида общей формулы

где R2 - H; CH2Cl;
n=50÷100 мол.%;
m=0÷50 мол.%,
в среде диметилформамида при температуре 95°÷135°C и мольном соотношении натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная:(со)полимер глицидилхлорида, равном 1,5:1,0, в течение 3-10 ч.
3. Способ получения (со)полимеров N-глицидил-3-нитро-3-R-1,2,4-триазолов общей формулы

где R1 - CH2N3;
R - H, СН3, С2H5;
n=50÷100 мол.%;
m=0÷50 мол.%,
заключающийся в обработке натриевой соли 3-нитро-5-R-1,2,4-триазола или натриевой соли 3-нитро-5-R-1,2,4-триазола 1,5-водной, где R - H, СН3, С2Н5, и азида натрия полимером глицидилхлорида общей формулы

где n=100 мол.%,
в среде диметилформамида при температуре 95°÷135°С и мольном соотношении натриевая соль 3-нитро-5-R-1,2,4-триазола или натриевая соль 3-нитро-5-R-1,2,4-триазола 1,5-водная:азид натрия:полиглицидилхлорид, равном 1,0-1,25:0,25-0,5:1,0, в течение 3÷10 ч.
| Ji-Hye Jung et al | |||
| Synthesis of glycidyl triazolyl polymers using click chemistry// Tetrahedron Letters | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРОВ ВИНИЛНИТРОТРИАЗОЛОВ | 2002 |
|
RU2261873C2 |
| RU 97116160 A, 20.07.1999. | |||
Авторы
Даты
2012-09-27—Публикация
2010-10-07—Подача