Изобретение относится к катализаторам низкотемпературного окисления монооксида углерода (CO), способам их приготовления и способу окисления CO с целью защиты окружающей среды от загрязнений CO.
Монооксид углерода является чрезвычайно токсичным газом, поскольку он связывается с гемоглобином крови прочнее и в 200-300 раз быстрее, чем кислород. При этом образуется карбоксигемоглобин, который блокирует процессы транспортировки кислорода и клеточного дыхания. При нахождении человека в закрытых производственных и жилых помещениях, например, производственные цеха, овощехранилища, подводные лодки, космические станции, в которых может накапливаться CO, может наступить отравление так называемым «угарным» газом - CO. Известно, что среднесуточное выделение CO человеком составляет 780 мг. При этом ПДК по CO составляет 5 мг/м3. Концентрация CO в воздухе более 0.1% (1250 мг/м3) приводит к смерти в течение 1 ч. Поэтому необходима очистка воздуха производственных и жилых помещений от монооксида углерода.
Решение этой проблемы в основном связывают с каталитическими методами обезвреживания. Отличительная особенность окисления CO в закрытых помещениях состоит в том, что концентрация CO невелика и изменяется в пределах 100÷1000 ppm, при этом окисление должно протекать при температуре и влажности окружающего воздуха. Эти условия накладывают определенные требования к каталитическим системам и методам их тестирования. В частности, катализаторы должны устойчиво работать при низкой (комнатной) температуре и влажности окружающего воздуха.
Одним из возможных подходов является использование благородных металлов (Pd, Ag, Au), нанесенных на различные носители. В последнее время особое внимание уделяется Au-содержащим системам, среди которых, по данным [М.Haruta, N.Yamada, T.Kobayashi, S.Iijima, J. Catal. 115 (1989) 301], Au/Fe2O3, Au/Co3O4 и Au/TiO2 проявляют высокую активность в окислении CO при комнатной температуре. Согласно [М.Khoudiakov, M.C.Gupta, S.Deevi, Au/Fe2O3 nanocatalysts for CO oxidation: A omparative study of deposition-precipitation and coprecipitation techniques. Appl. Catal. A: General 291 (2005) 151-161], катализатор состава: 2.5 ат.% Au/Fe2O3, полученный соосаждением золота и железа, в исходном состоянии показал высокую активность в окислении CO при ~30°C; однако после 10 мин работы наблюдается снижение его активности; кроме того, термическая обработка катализатора при 350°С также приводит к снижению активности катализатора, но стабильность повышается.
Помимо Au-содержащих катализаторов, активность в низкотемпературном окислении CO проявляют и Pd-содержащие катализаторы. В зависимости от природы носителя температура (Т50), отвечающая 50% конверсии CO увеличивается в ряду: CeO2(45°С)<ZrO2(165°С)<TiO2(185°С)<Al2O3(205°С)<SiO2(255°C). По мнению авторов [M.-F.Luo, Z.-Y.Hou, Х.-Х.Yuan, X.-M.Zheng. Characterization study of CeO2 supported Pd catalyst for low-temperature carbon monoxide oxidation, Catal. Lett. - 1998. - V.50. - P.205-209], активность в окислении CO определяется наличием металлического палладия, а частицы PdO имеют невысокую активность, соответственно они заключили, что достаточно наносить не более 2 мас.% Pd для формирования активных центров для окисления CO; последующее увеличение содержания Pd приводит лишь к тому, что избыточный палладий образует объемные частицы PdO, дающие незначительный вклад в активность. Анализ результатов показывает, что при прочих равных условиях Pd-содержащие катализаторы оказались менее активны по сравнению с Au-содержащими. Если принять во внимание тот факт, что Au-содержащие катализаторы являются более активными, если они не подвергнуты термической обработке или высушены при невысокой температуре, то это дает основание полагать, что присутствующие OH группы могут оказывать влияние на активность в реакции окисления CO.
Действительно, согласно результатам работы [Botao Qiao, Lequan Liu, Juan Zhang, Youquan Deng, Preparation of highly effective ferric hydroxide supported noble metal catalysts for CO oxidations: From gold to palladium, J. Catal. - 2009. - V.261. - P.241-244], использование в качестве носителей гидроксидов Al(ОН)x, Fe(OH)x и Co(OH)x для получения Pd(Au) - нанесенных катализаторов позволило повысить их активность в окислении CO: Т50 для 4.0 мас.% Pd/Al(OH)x и Pd/Co(OH)x составляет >140 и 78°С, соответственно. При нанесении Pd(Au) на Fe(OH)x наблюдается самая высокая активность: Т50 для Pd/Fe(OH)x с содержанием Pd, равным 0.3, 1.1, 4.1 и 8.3 мас.%, составляет 17, 3, -24 и -28°С, соответственно. Оказалось, что в этом случае активность Pd/Fe(OH)x сопоставима с активностью Au/Fe(OH)x катализатора при близком содержании благородного металла. Исследование стабильности показало, что на 4.1% Pd/Fe(OH)x катализаторе полная конверсия CO сохраняется в течение 10 ч при 0°С и 210 ч при 20°С. Однако приведенные данные по активности относятся к окислению CO в «сухой» смеси, не содержащей паров воды. В то же время известно [Н.Н.Kung, M.C.Kung, C.K.Costello, Supported Au catalysts for low temperature CO oxidation, // J. Catal. 216 (2003) 425-432], что наличие воды оказывает негативное влияние на активность катализаторов; одной из возможных причин дезактивации катализатора может быть превращение промежуточных веществ - бикарбонатов в неактивные карбонаты, которые блокируют активные поверхностные центры. Поэтому особый интерес представляют катализаторы, работающие эффективно в окислении CO при комнатной температуре и соответствующей влажности.
Наиболее близким к заявляемому по технической сущности является катализатор окисления CO на основе палладийсодержащего компонента, нанесенного на оксид алюминия, описанный в [SU №1833204, 1993].
Катализатор, содержащий 2-3 мас.% Pd/Al2O3, получают пропиткой оксида алюминия предварительно избыточным раствором диметилформамида в течение 2-х ч и последующей его декантацией, затем избыточным раствором хлорида палладия, содержащего щавелевую кислоту, с последующей декантацией или фильтрацией, после чего катализатор заливают дистиллированной водой и нагревают на водяной бане при 100°С в течение 2-х ч, затем отфильтровывают, промывают и сушат.
Каталитические свойства катализатора в реакции окисления монооксида углерода оценивали по степени превращения CO при комнатной температуре: конверсия CO составляет 75% в области концентраций CO, близких ПДК.
Недостатками известного катализатора является высокое содержание палладия, неэффективность его нанесения на носитель, включающее декантацию или фильтрацию избыточного раствора хлорида палладия; использование хлорсодержащего предшественника; относительно невысокая степень превращения CO. Нет информации о присутствии паров воды в реакционной смеси.
Задача изобретения - разработать катализатор, обеспечивающий полное окисление монооксида углерода CO при комнатной температуре и соответствующей влажности.
Для решения поставленной задачи предложен катализатор окисления монооксида углерода, содержащий палладий, нанесенный на носитель, при этом носитель представляет собой оксидную железосодержащую композицию.
Носитель представляет собой FeOOH, характеризующийся удельной поверхностью, равной (250±20) м2/г, и влагоемкостью - (0.70±0.05) мл/г.
Носитель представляет собой Fe2O3, характеризующийся удельной поверхностью, равной (50±5) м2/г, и влагоемкостью - (0.53±0.05) мл/г.
Содержание палладия составляет 0.25÷1.0 мас.%.
Задача решается также способом приготовления катализатора окисления монооксида углерода, который осуществляют пропиткой носителя по влагоемкости вначале раствором диметилформамида, а затем раствором, содержащим соль палладий, с последующими стадиями фильтрации, промывки и сушки, при этом носитель представляет собой оксидную железосодержащую композицию состава FeOOH, характеризующуюся удельной поверхностью, равной (250±20) м2/г, и влагоемкостью - (0.70±0.05) мл/г или Fe2O3, характеризующуюся удельной поверхностью, равной (50±5) м2/г, и влагоемкостью - (0.53±0.05) мл/г.
Железосодержащий носитель готовят осаждением раствора азотнокислого железа водным раствором аммиака при pH 8.5±0.1 и комнатной температуре с последующей выдержкой при указанных условиях в течение 2 ч, фильтрацией, промывкой, сушкой при комнатной температуре, затем при 110°С в течение 12-14 ч, получая FeOOH с удельной поверхностью, равной (250±20) м2/г, и влагоемкостью - (0.70±0.05) мл/г; а термическая обработка его при 450±20°С позволяет получать Fe2O3 с удельной поверхностью, равной (50±5) м2/г, и влагоемкостью - (0.53±0.05) мл/г.
Катализатор готовят нанесением Pd-содержащего активного компонента на железосодержащий носитель, который готовят пропиткой FeOOH с удельной поверхностью, равной (250±20) м2/г, по влагоемкости, равной (0.70±0.05) мл/г, или Fe2O3 с удельной поверхностью, равной (50±5) м2/г, по влагоемкости, равной (0.53±0.05) мл/г, вначале раствором диметилформамида с последующей сушкой при 100°С, 2 ч, затем раствором, содержащим азотнокислый палладий в пересчете на Pd (0.5-1.0) мас.%, с последующей обработкой раствором формиата натрия при 80°С, фильтрацией, промывкой и сушкой.
Задача решается также способом окисления монооксида углерода в присутствии описанного выше катализатора. Концентрация монооксида углерода в реакционной смеси составляет не выше 100 ppm.
Окисление монооксида углерода ведут в присутствии воды в реакционной смеси, соответствующей давлению паров при температуре 20°С.
Окисление монооксида углерода можно проводить также в отсутствии воды в реакционной смеси.
Отличительными признаками предлагаемого катализатора являются
1. Содержание Pd-содержащего активного компонента и носитель катализатора, который представляет собой либо гидроксид железа - FeOOH с удельной поверхностью, равной (250±20) м2/г, и влагоемкостью - (0.70±0.05) мл/г, либо оксид железа - Fe2O3 с удельной поверхностью, равной (50±5) м2/г, и влагоемкостью -(0.53±0.05) мл/г.
Тестирование катализаторов в реакции окисления CO проводят в автоматизированной установке с проточным реактором и масс-спектрометрическим анализом газовой смеси с помощью квадрупольного масс-спектрометра (Stanford Research Systems, QMS 200 Gas Analyzer) при комнатной температуре в отсутствии и в присутствии воды. На исходный катализатор фракции 0.25-0.5 мм, охлажденный до температуры 20°С, подают реакционную смесь со скоростью 500 см3/мин, содержащую:
1) 100 ppm CO, 1.0 об.% O2, 0.5 об.% Ne, баланс - гелий;
2) 100 ppm CO, 1.0 об.% O2, 0.5 об.% Ne, H2O, соответствующая давлению паров при температуре 20°C, баланс - гелий.
Объемная скорость подачи реакционной смеси составляет 24000 ч-1. В ходе реакции следят за концентрациями CO, O2 и CO2. Измерение концентраций в каждой точке проводят с частотой 0.34 Hz.
Сущность предлагаемого изобретения иллюстрируется следующими примерами, показывающими изменение активности (температур достижения соответствующих степеней превращения монооксида углерода) в зависимости от содержания палладия в катализаторе, природы носителя, способа их приготовления и окисления CO в отсутствии и в присутствии воды в реакционной смеси.
Основные характеристики катализаторов и значения конверсии CO приведены на Фиг.1-7.
Примеры 1-7 иллюстрируют состав и способ получения катализаторов, представляющих собой Pd-содержащий активный компонент, нанесенный на железосодержащий носитель, представляющий собой либо Fe(OH)x с удельной поверхностью, равной (250±20) м2/г, и влагоемкостью - (0.70±0.05) мл/г; либо Fe2O3 с удельной поверхностью, равной (50±5) м2/г, и влагоемкостью - (0.53±0.05) мл/г, при этом реакцию окисления монооксида углерода проводят при комнатной температуре и объемной скорости подачи реакционной смеси, равной 24000 ч-1, в отсутствии и в присутствии воды, соответствующей давлению паров при температуре 20°C.
Пример 1.
В реактор заливают 500 мл дистиллированной воды, устанавливают pH-метр и при комнатной температуре дозируют смешанный раствор азотнокислого железа, содержащего 100 г Fe2O3, со скоростью 30 мл/мин, одновременно добавляя 940 мл раствора NH4OH для поддержания pH осаждения, равным 8,5. Полученную суспензию выдерживают при указанных условиях в течение 2 ч, после чего фильтруют и промывают дистиллированной водой. Полученный осадок сушат на воздухе, затем при 110°С в течение 12-14 ч. Полученный носитель имеет состав FeOOH с удельной поверхностью, равной 245 м2/г, и влагоемкостью - 0.67 мл/г.
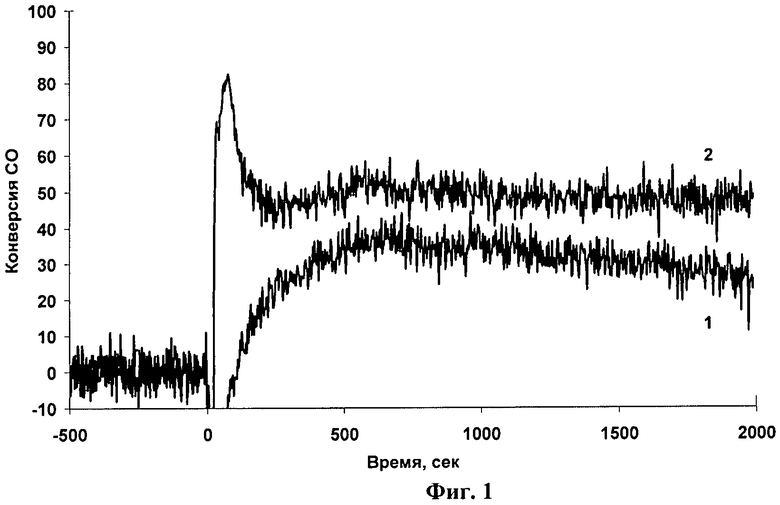
Навеску Fe(OH)x, равную 2,173 г, пропитывают по влагоемкости вначале 1,4 мл раствора деметилформамида, сушат при 100°С, 2 ч, затем раствором азотнокислого палладия, содержащего 0,0362 г Pd(NO3)2, с последующей обработкой раствором формиата натрия при 80°С, фильтрацией, промывкой дистиллированной водой и сушкой при комнатной температуре. Катализатор имеет состав: 0.25 мас.% Pd/FeOOH; каталитические свойства катализатора показаны на Фиг.1
Пример 2.
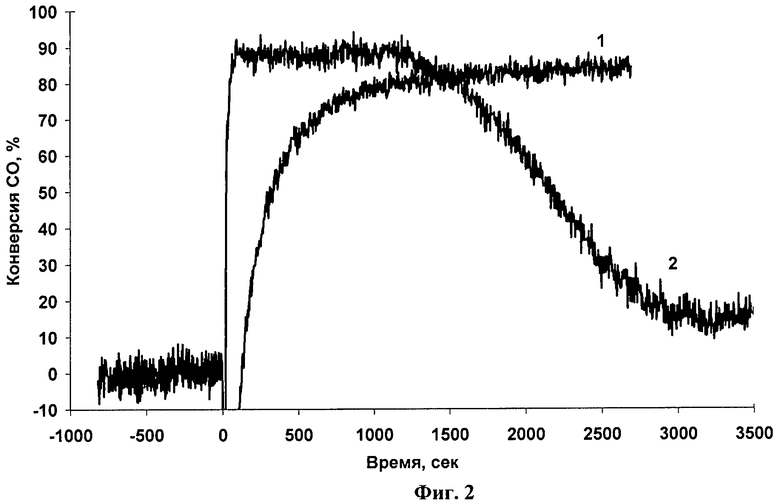
Аналогичен примеру 1. Отличие состоит в том, что навеску Fe(OH)x, равную 3,488 г, пропитывают по влагоемкости вначале 2,3 мл раствора деметилформамида, сушат при 100°С, 2 ч, затем раствором азотнокислого палладия, содержащего 0,0623 г Pd(NO3)2. Катализатор имеет состав: 0.5 мас.% Pd/FeOOH; каталитические свойства катализатора показаны на Фиг.2.
Пример 3.
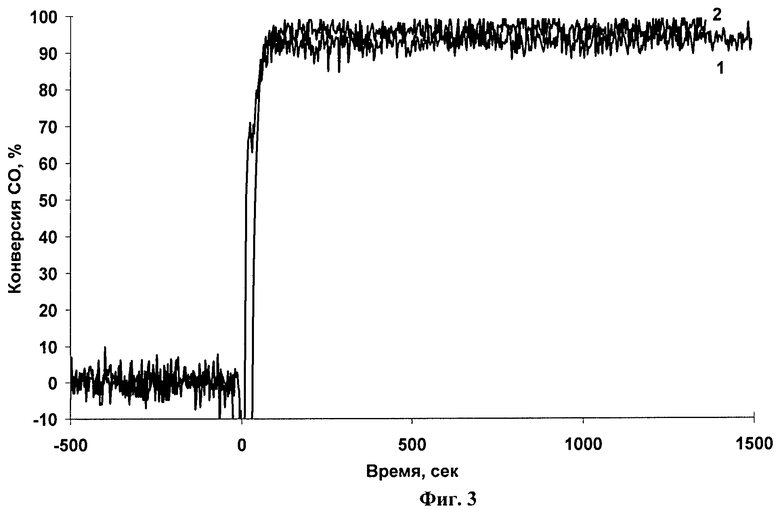
Аналогичен примеру 1. Отличие состоит в том, что навеску Fe(OH)x, равную 1,883 г, пропитывают по влагоемкости вначале 1,3 мл раствора деметилформамида, сушат при 100°С, 2 ч, затем раствором азотнокислого палладия, содержащего 0,1331 г Pd(NO3)2. Катализатор имеет состав: 1.0 мас.% Pd/FeOOH; каталитические свойства катализатора показаны на Фиг.3.
Пример 4.
В реактор заливают 500 мл дистиллированной воды, устанавливают рН-метр и при комнатной температуре дозируют смешанный раствор азотнокислого железа, содержащего 100 г Fe2O3, со скоростью 30 мл/мин, одновременно добавляя 940 мл раствора NH4OH для поддержания рН осаждения равным 8,5. Полученную суспензию выдерживают при указанных условиях в течение 2 ч, после чего фильтруют и промывают дистиллированной водой. Полученный осадок сушат на воздухе, затем при 110°С в течение 12-14 ч и прокаливают при 450°С в течение 4-х ч. Полученный носитель имеет состав Fe2O3 с удельной поверхностью, равной 50 м2/г, и влагоемкостью - 0.51 мл/г.
Навеску Fe2O3, равную 1,874 г, пропитывают по влагоемкости вначале 0,95 мл раствора деметилформамида, сушат при 100°С, 2 ч, затем раствором азотнокислого палладия, содержащего 0,0127 г Pd(NO3)2, с последующей обработкой раствором формиата натрия при 80°С, фильтрацией, промывкой дистиллированной водой и сушкой при комнатной температуре. Катализатор имеет состав: 0.1 мас.% Pd/Fe2O3; каталитические свойства катализатора показаны на Фиг.4.
Пример 5.
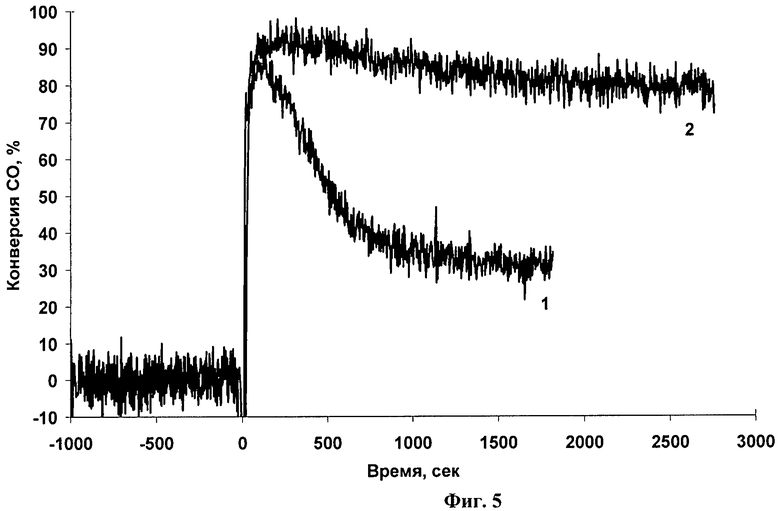
Аналогичен примеру 4. Отличие состоит в том, что навеску Fe2O3, равную 1,872 г, пропитывают по влагоемкости вначале 0,93 мл раствора деметилформамида, сушат при 100°С, 2 ч, затем раствором азотнокислого палладия, содержащего 0,0315 г Pd(NO3)2. Катализатор имеет состав: 0.25 мас.% Pd/Fe2O3; каталитические свойства катализатора показаны на Фиг.5.
Пример 6.
Аналогичен примеру 4. Отличие состоит в том, что навеску Fe2O3, равную 2,002 г, пропитывают по влагоемкости вначале 1,0 мл раствора деметилформамида, сушат при 100°С, 2 ч, затем раствором азотнокислого палладия, содержащего 0,069 г Pd(NO3)2. Катализатор имеет состав: 0,5 мас.% Pd/Fe2O3; каталитические свойства катализатора показаны на Фиг.6.
Пример 7.
Аналогичен примеру 4. Отличие состоит в том, что навеску Fe2O3, равную 2,369 г, пропитывают по влагоемкости вначале 1,2 мл раствора деметилформамида, сушат при 100°С, 2 ч, затем раствором азотнокислого палладия, содержащего 0,1613 г Pd(NO3)2. Катализатор имеет состав: 1.0 мас.% Pd/Fe2O3; каталитические свойства катализатора показаны на Фиг.7.
Показатели окисления CO по всем примерам приведены на Фиг.1-7.
Фиг.1. Зависимость конверсии CO от времени для 0.25 мас.% Pd/Fe(OH)x катализатора при 20°С в отсутствии (1) и присутствии (2) воды.
Фиг.2. Зависимость конверсии CO от времени для 0.5 мас.% Pd/Fe(OH)x катализатора при 20°С в отсутствии (1) и присутствии (2) воды.
Фиг.3. Зависимость конверсии CO от времени для 1.0 мас.% Pd/Fe(OH)x катализатора при 20°С в отсутствии (1) и присутствии (2) воды.
Фиг.4. Зависимость конверсии CO от времени для 0.1 мас.% Pd/Fe2O3 катализатора при 20°С в отсутствии (1) и присутствии (2) воды.
Фиг.5. Зависимость конверсии CO от времени для 0.25 мас.% Pd/Fe2O3 катализатора при 20°С в отсутствии (1) и присутствии (2) воды.
Фиг.6. Зависимость конверсии CO от времени для 0.5 мас.% Pd/Fe2O3 катализатора при 20°С в отсутствии (1) и присутствии (2) воды.
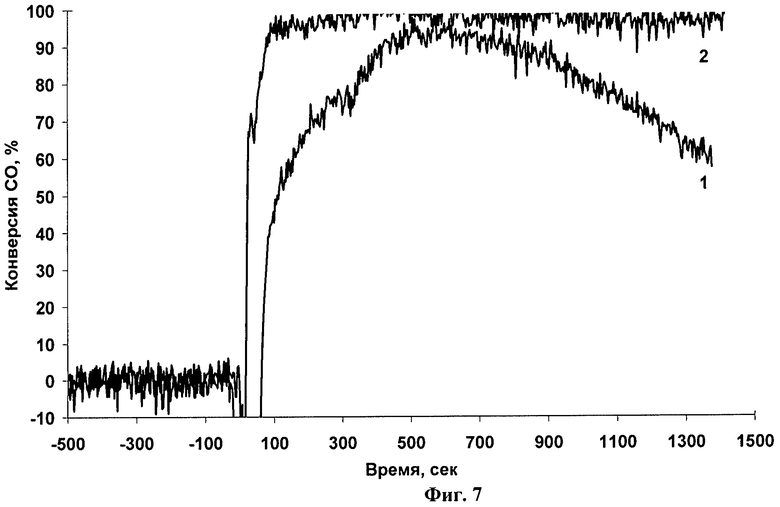
Фиг.7. Зависимость конверсии CO от времени для 1.0 мас.% Pd/Fe2O3 катализатора при 20°С в отсутствии (1) и присутствии (2) воды.
Как видно из приведенных примеров и Фиг., предлагаемые Pd/FeOOH и Pd/Fe2O3 катализаторы позволяют решить задачу эффективного окисления CO при его концентрации в реакционной смеси, равной 100 ppm, если содержание Pd составляет 0.5-1.0 мас.% в катализаторе Pd/FeOOH; или 0.25-1.0 мас.% в катализаторе Pd/Fe2O3, причем катализаторы Pd/FeOOH работают эффективно как в отсутствии, так и в присутствии паров воды, особенно катализатор 1.0 мас.% Pd/FeOOH.
Катализаторы Pd/Fe2O3 работают более эффективно в присутствии паров воды: на 0.5 мас.% Pd/Fe2O3 катализаторе конверсия CO достигает 100%; а в отсутствии воды в реакционной смеси конверсия CO составляет 95-97%, а после 30 мин работы катализатора она постепенно снижается до 40%.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР, СПОСОБ ПРИГОТОВЛЕНИЯ НОСИТЕЛЯ, СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА И СПОСОБ ОКИСЛЕНИЯ МОНООКСИДА УГЛЕРОДА | 2011 |
|
RU2446878C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ БИМЕТАЛЛИЧЕСКОГО КАТАЛИЗАТОРА (ВАРИАНТЫ) И ЕГО ПРИМЕНЕНИЕ ДЛЯ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2010 |
|
RU2428769C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И СПОСОБ ОЧИСТКИ ОТХОДЯЩИХ ГАЗОВ ОТ ОКСИДОВ АЗОТА | 2012 |
|
RU2480281C1 |
| КАТАЛИЗАТОР НИЗКОТЕМПЕРАТУРНОГО ОКИСЛЕНИЯ МОНООКСИДА УГЛЕРОДА И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2014 |
|
RU2557229C1 |
| КАТАЛИЗАТОР ДЛЯ ИЗБИРАТЕЛЬНОГО ОКИСЛЕНИЯ МОНООКСИДА УГЛЕРОДА В СМЕСИ С АММИАКОМ И СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2013 |
|
RU2515529C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ, СПОСОБ СЕЛЕКТИВНОГО ОКИСЛЕНИЯ МОНООКСИДА УГЛЕРОДА, КАТАЛИЗАТОР СЕЛЕКТИВНОГО ОКИСЛЕНИЯ МОНООКСИДА УГЛЕРОДА, СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2724109C1 |
| Катализатор жидкофазного селективного гидрирования ацетиленовых углеводородов и способ его получения | 2020 |
|
RU2738233C1 |
| КАТАЛИЗАТОР ДЛЯ ИЗБИРАТЕЛЬНОГО ОКИСЛЕНИЯ МОНООКСИДА УГЛЕРОДА В СМЕСИ С АММИАКОМ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2515514C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА | 2017 |
|
RU2653360C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ НАНЕСЕННЫХ ПОЛИМЕТАЛЛИЧЕСКИХ КАТАЛИЗАТОРОВ (ВАРИАНТЫ) | 2005 |
|
RU2294240C2 |


Изобретение относится к катализаторам низкотемпературного окисления монооксида углерода (CO) и способу окисления CO с целью защиты окружающей среды от загрязнений CO. Описаны катализатор окисления монооксида углерода, содержащий палладий, нанесенный на оксидную железосодержащую композицию, и способ его приготовления, в результате которого получают оксидную железосодержащую композицию, которая представляет собой FeOOH, характеризующийся удельной поверхностью, равной (250±20) м2/г, и влагоемкостью - (0.70±0.05) мл/г, или Fe2O3, характеризующийся удельной поверхностью, равной (50±5) м2/г, и влагоемкостью - (0.53±0.05) мл/г. Содержание палладия составляет 0.25-1.0 мас.%. Окисление монооксида углерода проводят в присутствии или отсутствии воды в реакционной смеси с использованием описанного выше катализатора, концентрация монооксида углерода в реакционной смеси составляет не выше 100 ppm. Технический результат - полное окисление монооксида углерода при комнатной температуре и соответствующей влажности. 3 н. и 5 з.п. ф-лы, 7 пр., 7 ил.
1. Катализатор низкотемпературного окисления монооксида углерода, содержащий палладий, нанесенный на носитель, отличающийся тем, что носитель представляет собой оксидную железосодержащую композицию, содержание палладия составляет 0,25÷1,0 мас.%.
2. Катализатор по п.1, отличающийся тем, что носитель представляет собой FeOOH, характеризующийся удельной поверхностью, равной (250±20) м2/г, и влагоемкостью - (0,70±0,05) мл/г.
3. Катализатор по п.1, отличающийся тем, что носитель представляет собой Fe2O3, характеризующийся удельной поверхностью, равной (50±5) м2/г, и влагоемкостью - (0,53±0,05) мл/г.
4. Способ приготовления катализатора низкотемпературного окисления монооксида углерода, содержащий палладий и носитель, пропиткой носителя по влагоемкости вначале раствором диметилформамида, а затем раствором, содержащим соль палладий, с последующими стадиями фильтрации, промывки и сушки, отличающийся тем, что носитель представляет собой оксидную железосодержащую композицию состава FeOOH, характеризующуюся удельной поверхностью, равной (250±20) м2/г, и влагоемкостью - (0,70±0,05) мл/г или Fe2O3, характеризующуюся удельной поверхностью, равной (50±5) м2/г, и влагоемкостью - (0,53±0,05) мл/г, при этом получают катализатор с содержанием палладия 0,25÷1,0 мас.%, а содержание палладия составляет 0,25÷1,0 мас.%.
5. Способ окисления монооксида углерода в присутствии катализатора при комнатной температуре, отличающийся тем, что его осуществляют в присутствии катализатора по любому из пп.1-3 или полученного по п.4.
6. Способ по п.5, отличающийся тем, что концентрация монооксида углерода в реакционной смеси составляет не выше 100 млн-1.
7. Способ по п.5, отличающийся тем, что окисление монооксида углерода ведут в присутствии воды в реакционной смеси, соответствующей давлению паров при температуре 20°C.
8. Способ по п.5, отличающийся тем, что окисление монооксида углерода можно проводить в отсутствии воды в реакционной смеси.
| SU 18332204 A3, 07.08.1993 | |||
| КАТАЛИЗАТОР ОКИСЛИТЕЛЬНОЙ ОЧИСТКИ ГАЗОВ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2006 |
|
RU2311957C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПАЛЛАДИЕВОГО КАТАЛИЗАТОРА НА АКТИВНОМ ОКСИДЕ АЛЮМИНИЯ ДЛЯ НИЗКОТЕМПЕРАТУРНОГО ОКИСЛЕНИЯ ОКСИДА УГЛЕРОДА | 2007 |
|
RU2339446C1 |
| JP 53093191 A, 15.08.1978 | |||
| US 20109316547 A1, 16.12.2010. | |||
Авторы
Даты
2012-10-20—Публикация
2011-09-19—Подача