Изобретение относится к способу получения нанесенных металлических катализаторов. Катализаторы могут быть использованы в различных областях катализа, например, для проведения процессов каталитической окислительной конверсии углеводородов и кислородсодержащих органических соединений, гидрирования оксидов углерода и ненасыщенных углерод-углеродных и углерод-гетероатомных связей в органических субстратах, процессах гидрокрекинга углеводородов. В частности, такие реакции, как паровая и углекислотная конверсии, парциальное окисление или автотермический реформинг углеводородов с получением синтез-газа лежат в основе большинства крупнотоннажных процессов химической и нефтехимической промышленности. Усовершенствование таких катализаторов и оптимизация параметров проведения этих процессов всегда имеют стратегическое значение, способствуя ресурсо- и энергосбережению.
Многие из этих каталитических процессов протекают при довольно высоких температурах, часто выше 600°С. При этих температурах для сохранения стабильной структуры катализатора необходимо использовать носители, предварительно прокаленные при высоких температурах (зачастую на 50-100°С превышающих рабочую температуру целевого процесса). Такие носители обычно характеризуются невысокой удельной поверхностью, часто не превышающей пары десятков квадратных метров на грамм, а также большими размерами гранул и развитой макропористостью для предотвращения нежелательных гидродинамических эффектов. В этой связи нанесение достаточно больших количеств активного металла равномерно по поверхности такого рода носителей связано с технологическими трудностями, а придание высокой дисперсности нанесенному активному компоненту в получаемых катализаторах становится весьма проблематичным.
В рамках известных и широкоиспользуемых методов приготовления таких катализаторов не представляется возможным легко преодолеть эти проблемы. Так, подходы, в основе которых лежит адсорбция предшественников металлов на поверхности подложки, оказываются нетехнологичными из-за неприемлемо низкой адсорбционной емкости указанных носителей.
В свою очередь, применение метода пропитки по влагоемкости, заключающегося в приготовлении и пропитке носителя водным раствором соли наносимого металла, взятым в объеме, равном объему пор пропитываемого носителя, затруднено малым объемом приготавливаемого раствора. По этой причине зачастую проводят многократную пропитку, что осложняет и удлиняет процесс нанесения. При этом, чтобы избежать перерастворения соли металла, нанесенной на предыдущем этапе, часто требуется проведение процедуры прокаливания, позволяющей зафиксировать нанесенный металл по поверхности носителя в нерастворимой форме. Это в свою очередь кратно увеличивает энергопотребление и, соответственно, себестоимость производимого катализатора. В целом, пропиточные методы в большинстве случаев приводят к неравномерному распределению металла по поверхности зерен носителя, большим размерам частиц наносимого металла и, как следствие, - к низкой активности катализатора.
Приготовление катализаторов методом пропитки избытком раствора также дает неудовлетворительные результаты, аналогичные таковым по методу пропитки по влагоемкости, поскольку ему свойственны описанные выше недостатки.
С рядом проблем сопряжено и использование другого известного метода приготовления - метода осаждения, когда соль наносимого металла растворяют в большом объеме растворителя, значительно превышающем объем взятого носителя, помещают туда носитель и постепенно при перемешивании добавляют раствор вещества-осадителя, за счет чего происходит осаждение нерастворимых соединений металла на поверхность носителя. Недостатком такого метода, в первую очередь, являются значительные потери наносимого металла, так как существенная его часть осаждается не на носитель, а в объеме раствора вне зерен носителя из-за быстрого роста и агрегации осаждаемых металлсодержащих частиц. Это делает указанный метод совершенно непригодным для приготовления катализаторов на основе массивных блочных носителей сетчатой, пеноподобной и сотовой структуры, отличающихся огромным объемом макропор, в которых невозможно обеспечить достаточно быстрое смешение растворов предшественника металла и осаждающего агента.
Настоящее изобретение предлагает простой и технологичный способ приготовления высокодисперсных металлических катализаторов на основе благородных металлов, в частности рутениевых, платиновых, родиевых и палладиевых, нанесенных на оксидные носители с низкой удельной поверхностью и различной формой (зерна, экструдаты разнообразной геометрии, блоки пеноподобной, сотовой или сетчатой структуры), который заключается в гидролитическом зарождении и росте наночастиц оксидов этих металлов на поверхности различных оксидных носителей в кинетически затрудненных в отношении гомогенного гидролиза системах типа "комплекс металла + щелочной агент". Сущность метода состоит в подборе в качестве предшественников активного компонента таких комплексов металла, у которых лигандное замещение во внутренней сфере центрального атома происходит очень медленно, поэтому гидролиз этих комплексов протекает в гомогенных условиях с низкой скоростью, но резко ускоряется на границе раздела "раствор-оксидный носитель" под влиянием силовых полей поверхности носителя и носит автокаталитический характер. Вследствие этого доминирующим механизмом формирования катализатора становится гетерогенное зарождение и рост частиц гидроксидов и оксидов благородных металлов непосредственно на поверхности носителя, а вклад гомогенного зарождения частиц осадков с последующим их ростом и выпадением в объеме раствора вне зерен носителя оказывается ничтожно малым.
Наиболее близким техническим решением к заявляемому является способ приготовления катализатора путем нанесения металлов на керамику, пластмассы, металлы, композитные материалы, оксиды переходных металлов, углеродный материал, включающий последовательные стадии нанесения предшественников, несущих катионную и анионную часть (RU 2294240, B01J 23/56, С07B 33/00, 27.02.2007), выбранный в качестве прототипа. Суть одного из вариантов способа приготовления состоит в том, что исходный носитель обрабатывают растворами кислот, оснований или солей таким образом, что на носителе осаждаются малорастворимые координационные соединения, состоящие из комплексного катиона и комплексного аниона металла. Далее проводят разложение нанесенных комплексных солей до металлов различными способами: органическими или неорганическими восстановителями в водных средах или газообразными восстановителями, либо термическим разложением нанесенной фазы в инертной или окислительной по отношении к образующимся металлам атмосфере. Например, Rh содержащие частицы, нанесенные на низкоповерхностный носитель ZrO2, в катализаторе, приготовленном в соответствии с этим способом (Е.М. Чуракова и др. Биметаллические катализаторы Rh-Co/ZrO2 паровой конверсии этанола в водородсодержащий газ // Кинетика и катализ, 2010, том 51, №6, сс. 923-928) имели размер около 100 нм.
Недостатками указанного в прототипе метода приготовления катализаторов являются:
- технологическая сложность вследствие многостадийности процесса нанесения активного компонента на носители с низкой удельной поверхностью,
- грубая дисперсность и широкое распределение по размерам частиц нанесенного активного компонента, что снижает степень использования поверхности дорогостоящих металлов.
Изобретение решает задачу создания простого в технологическом отношении способа приготовления высокодисперсных катализаторов на основе благородных металлов.
Катализатор готовят гидролитическим осаждением оксидов благородных металлов на носитель, характеризующийся широким диапазоном вариации химического состава, пористости и морфологии частиц, помещая носитель в метастабильный водный раствор, содержащий соль или комплекс наносимого металла и гидролизующий агент, при температуре, которая способствуют ускорению гидролиза соединений благородного металла и количественному закреплению оксидов металла на носителе, с последующим извлечением носителя с нанесенными оксидами металла из раствора, сушкой на воздухе и восстановлением.
В качестве исходных соединений для приготовления растворов осаждения используют галогенидные соли и комплексы благородных металлов, преимущественно платины, рутения или родия. В качестве галогенид-иона выступают хлорид-ионы.
В качестве гидролизующих агентов для приготовления растворов осаждения используют гидроксиды, гидрокарбонаты или карбонаты щелочных металлов.
Активный компонент наносят в количестве 0,1-3,0 мас. %.
В качестве носителей используют оксиды трудновосстанавливающихся элементов, такие как: оксиды алюминия, циркония, церия, алюмосиликаты и сплавы алюминия, железа, никеля, хрома. Носитель может быть выполнен в виде порошков, гранул, экструдатов или блоков различной формы и геометрии, блоки могут быть выполнены на основе стеклоткани, пенометалла или пенокерамики. В качестве носителей используют композиционные оксид-оксидные или металл-оксидные блочные носители различной формы и геометрии.
Температура, которая способствует ускорению гидролиза соединения благородного металла и количественному закреплению оксида металла на носителе, не превышает 100°C, преимущественно 20-80°С.
Катализатор сушат при температуре выше 70°C, преимущественно 100-120°С.
Восстановление оксида металла проводят при температуре выше 20°C, преимущественно 200-400°С.
Способ предполагает последовательное осуществление перечисленных ниже процедур:
- пропитки носителя при комнатной температуре избытком метастабильного водного раствора хлорида благородного металла и щелочного агента (например, гидроокись, карбонат и/или гидрокарбонат щелочного металла),
- последующего нагревания этого раствора с помещенным в него носителем до оптимальной температуры протекания реакции автокаталитического осаждения оксида металла на носитель и поддержания этой температуры в течение периода, необходимого для полного осаждения,
- извлечения носителя из пропиточного раствора и его отмывки от растворимых продуктов реакции декантацией горячей водой,
- удаления воды сушкой образцов на воздухе при температуре выше 70°C,
- восстановления нанесенного оксида металла до высокодисперсных металлических частиц в токе водорода при 200-400°C.
Технический результат предлагаемого подхода - возможность равномерного распределения активного компонента катализатора по внутренней поверхности массивных пористых носителей и высокая дисперсность наночастиц указанных металлов при их нанесении на оксидные носители с низкой удельной поверхностью и, как следствие, - высокая активность получаемого катализатора.
Отличительным признаком настоящего изобретения по сравнению с прототипом является то, что выпадения осадков оксидов металлов из приготовленных растворов осаждения при комнатной температуре не происходит длительное время, несмотря на присутствие гидролизующих агентов. С заметной скоростью их осаждение протекает только после добавления носителя благодаря снижению энергии Гиббса гетерогенного образования зародышей гидроксидов этих металлов на поверхности носителя (при традиционном осаждении гидролиз протекает быстро, и энергия Гиббса гомогенного зародышеобразования достаточно мала, поэтому кристаллиты осаждаемого вещества легко образуются непосредственно в объеме раствора, что приводит к нежелательной сегрегации частиц носителя и осажденных предшественников активного компонента). Ускорение процесса гетерогенного гидролиза соли металла и, соответственно, процесса нанесения металла на поверхность оксидного носителя осуществляется также за счет нагревания раствора или изменения состава электролитного фона. В отличие от прототипа предлагаемый метод позволяет достигать высокой дисперсности (1-3 нм) частиц благородных металлов, преимущественно Rh, Pt, Ru и Pd, даже на носителях с низкой удельной поверхностью (2-157 м2/г) и обеспечивает равномерное распределение металлов в порах указанных выше носителей, даже если они используются в виде объемных блоков сетчатой, пенообразной или сотовой структуры.
Сущность изобретения иллюстрируется примерами.
Примеры 1-14, приведены для иллюстрации заявленного способа и проведено сравнение с прототипом (пример 15)
Краткое описание состава приготовленных катализаторов и информация о соответствующих им средним размерам частиц нанесенных металлов приведены в Таблице.
Средний размер частиц нанесенных металлов вычисляли по результатам хемосорбции CO.
Пример 1
Синтез катализатора 1 мас. % Rh/ZrC2
Готовят раствор родия смешением 30 мл H2O, 1.00 мл 0.1 М RhCl3 и 1.50 мл 1 М Na2CO3 (мольное отношение Cl/Na=1:10). (Отдельный эксперимент показал, что такой раствор стабилен при комнатной температуре, по крайней мере, в течение 20 ч) При перемешивании к раствору добавляют 1.00 г порошкообразного ZrO2 (фракция <0.1 мм, удельная поверхность, SБЭТ=10.4 м2/г). В последующие 20 мин видимых изменений в полученной суспензии не наблюдается. После этого суспензию нагревают при 80°C в течение 1 ч, в результате чего родий количественно осаждается на носитель в виде оксида. Носитель с нанесенными соединениями родия отфильтровывают и тщательно промывают дистиллированной водой до величины pH промывных вод 6-7. Отфильтрованный рассол проверяют на реакцию с NaBH4, убеждаясь в отсутствии в нем ионов родия (их примесь дает серое опалесцирующее окрашивание пробы вследствие образования золей металла).
Образец с нанесенными соединениями родия сушат при 80°C на воздухе, затем помещают в проточный реактор и нагревают сначала в токе азота при 100°C (30 мин), а затем в токе водорода поднимают температуру со скоростью 50°/10 мин до 250°C и в этих условиях выдерживают образец 30 мин. По окончании процедуры восстановления реактор охлаждают, продувают азотом, пассивируют катализатор многократным введением малых порций воздуха и извлекают из реактора.
Дисперсность металла в катализаторе, CO/Rh=1.05.
Пример 2
Синтез катализатора 1 мас. % Ph/α-Аl2О3
Катализатор готовят по методике, изложенной в Примере 1, за исключением того, что для приготовления раствора осаждения берут 1.50 мл 0.1 М Na2CO3 (мольное отношение Cl/Na=1:1), а в качестве носителя используют сфероподобные экструдаты, сформированные из α-Al2O3 (фракция <2 мм, SБЭТ=4.0 м2/г).
Дисперсность металла в катализаторе, CO/Rh=0.17.
Пример 3
Синтез катализатора 1 мас. % Rh/Ce2
Катализатор готовят по методике, изложенной в Примере 2, за исключением того, что в качестве носителя используют порошок CeO2 (фракция <0.1 мм, SБЭТ=65 м2/г).
Дисперсность металла в катализаторе, CO/Rh=1.67.
Пример 4
Синтез катализатора 1 мас. % Rh/Ce0.75Zr0.25O2
Катализатор готовят по методике, изложенной в Примере 2, за исключением того, что в качестве носителя используют порошок соосажденного смешанного оксида СеO2+ZrO2 (мольное соотношение 3:1), прокаленного 0.5 ч при 800°C на воздухе (фракция 0.2-0.5 мм, SБЭT=73 м2/г).
Дисперсность металла в катализаторе, CO/Rh=1.32.
Пример 5
Синтез катализатора 1 мас. % Rh/Се0.75Zr0.25O2/кордиерит
Катализатор готовят по методике, изложенной в Примере 4, за исключением того, что в качестве носителя используют кордиеритовый блок (толщина стенки - 0.165 мм, плотность каналов - 62 канала на см2) с нанесенным на стенки его каналов слоя Ce0.75Zr0.25O2 (вес блочного носителя - 13.34 г, содержание Ce0.75Zr0.25O2 - 7.5 мас. %), причем циркуляцию подщелоченного раствора родия через каналы носителя осуществляют периодическим переворачиванием герметично укупоренного термостатированного сосуда, в который помещены раствор и носитель. Содержание Rh в катализаторе - 1 мас. % в пересчете на массу Ce0.75Zr0.25O2.
Дисперсность металла в катализаторе, CO/Rh=1.21.
Пример 6
Синтез катализатора 1 мас. % Rh/Ce0.75Zr0.25O2
Катализатор готовят по методике, изложенной в Примере 4, за исключением того, что в качестве щелочного агента используют Cs2CO3 (мольное отношение Cl/Cs=1:1), а осаждение полностью завершается уже при 20°С. Дисперсность металла в катализаторе, CO/Rh=1.90.
Пример 7
Синтез катализатора 1 мас. % Rh/Ce0.75Zr0.25O2
Катализатор готовят по методике, изложенной в Примере 6, за исключением того, что восстановление катализатора в токе H2 проводят при 600°C в течение 2 ч.
Дисперсность металла в катализаторе, CO/Rh=1.27.
Пример 8
Синтез катализатора 1 мас. % Rh/Al2O3@Ce0.75Zr0.25O2.
Катализатор готовят по методике, изложенной в Примере 2, за исключением того, что в качестве носителя используют порошок соосажденного трехкомпонентного смешанного оксида Al2O3+CeO2+ZrO2 (мольное соотношение 1:0.75:0.25), прокаленного 0.5 ч при 800°C на воздухе (фракция 0.2-0.5 мм, SБЭТ=157 м2/г).
Дисперсность металла в катализаторе, CO/Rh=1.51.
Пример 9
Синтез катализатора 2 мас. % Rh/Al2O3@Се0.75Zr0.25O2/фехралой
Катализатор готовят по методике, изложенной в Примере 5, за исключением того, что в качестве носителя используют высокоячеистый пеноматериал из фехралоя (сплав Fe-Cr-Al, размер пор - 2 мм) с нанесенным на его поверхность слоем трехкомпонентного смешанного оксида Al2O3+CeO2+ZrO2 (мольное соотношение 1:0.75:0.25) (вес блочного носителя - 7.48 г, содержание Al2O3@Ce0.75Zr0.25O2 - 13.1 мас. %),. Содержание Rh в катализаторе - 2 мас. % в пересчете на массу Al2O3@Ce0.75Zr0.25O2.
Дисперсность металла в катализаторе, CO/Rh=1.21.
Пример 10
Синтез катализатора 1.9 мас. % Pt/Ce0.75Zr0.25O2
К 0.98 г порошка соосажденного смешанного оксида СеО2+ZrO2 (мольное соотношение 3:1), прокаленного 0.5 ч при 800°C на воздухе (фракция 0.2-0.5 мм, SБЭТ=73 м2/г), приливают раствор, содержащий 10 мл H2О+0.97 мл 0.1 М H2PtCl6+0.165 мл 1 М Na2CO3+0.100 мл 1 М NaOOCH. (Отдельный эксперимент показал, что в отсутствие носителя такой раствор стабилен при комнатной температуре, по крайней мере, в течение 20 ч и при нагревании при 80°C в течение 1 ч). Полученную суспензию сначала перемешивают 15 мин при 20°C (видимых изменений в полученной суспензии не наблюдается), затем еще 15 мин при 60°C (раствор обесцвечивается) и 20 мин при 80°С. В результате платина полностью осаждается на носитель (согласно отрицательной реакции фильтрата с NaBH4).
Носитель с нанесенными соединениями платины отфильтровывают и тщательно промывают дистиллированной водой до величины pH промывных вод 6-7. Сушку и восстановление образца водородом осуществляют согласно Примеру 1.
Дисперсность металла в катализаторе, СО/Pt=0.59.
Пример 11
Синтез катализатора 1.9 мас. % Pt/Ce0.75Zr0.25O2
К 0.98 г порошка соосажденного смешанного оксида CeO2+ZrO2 (мольное соотношение 3:1), прокаленного 0.5 ч при 800°C на воздухе (фракция 0.2-0.5 мм, SБЭТ=73 м2/г), приливают охлажденный до 5°C раствор, содержащий 10 мл H2О+0.97 мл 0.1 М H2PtCl4+0.194 мл 1 М Na2CO3. (Отдельный эксперимент показал, что в отсутствие носителя такой раствор стабилен при указанной температуре, по крайней мере, в течение 2 ч). Полученную суспензию перемешивают 15 мин при 5°C, в результате чего раствор обесцвечивается, и платина полностью осаждается на носитель (согласно отрицательной реакции фильтрата с NaBH4).
Носитель с нанесенными соединениями платины отфильтровывают и тщательно промывают дистиллированной водой до величины pH промывных вод 6-7. Сушку и восстановление образца водородом осуществляют согласно Примеру 1.
Дисперсность металла в катализаторе, CO/Pt=0.62.
Пример 12
Синтез катализатора 1 мас. % Ru/Ce0.75Zr0.25O2
Предварительно готовят рутениевый комплекс смешением 0.241 мл 0.41 М Ru(OH)Cl3 в растворе 0.82 М HCl и 0.494 мл 0.1 М N2H4×2HCl с последующим нагреванием смеси до кипения, упариванием досуха и прокаливанием при 210°C в течение 10 мин. Полученное соединение растворяют в 10 мл воды, подщелачивают добавкой 1.96 мл 0.1 М Na2CO3 и раствор приливают к 0.99 г порошка смешанного оксида СеO2+ZrO2, идентичного таковому в Примере 4. Суспензию перемешивают 30 мин при 20°C, затем еще 30 мин при 60°C до полного осаждения рутения.
Сушку и восстановление образца водородом осуществляют согласно Примеру 1.
Дисперсность металла в катализаторе, CO/Ru=0.81.
Пример 13
Синтез катализатора 3 мас. % Pd/ZrO2.
Предварительно готовят раствор H2PdCl4 растворением 0.1002 г PdCl2 (содержание Pd - 59.9 мас. %) в 1.15 мл 1.0 HCl при слабом нагревании, затем полученный раствор доводят водой до 5 мл. Раствор H2PdCl4 при интенсивном перемешивании приливают к 20 мл водного раствора Na2CO3, содержащего 0.6 г Na2CO3 (на сухой вес). В приготовленный таким образов щелочной раствор палладия добавляют 1.94 г порошка ZrO2 (по Примеру 1)) и размешивают 1 ч при 20°C, затем еще 30 мин при 60°C до полного осаждения палладия.
Сушку и восстановление образца водородом осуществляют согласно Примеру 1.
Дисперсность металла в катализаторе, CO/Pd=0.39.
Пример 14
Синтез катализатора 0.1 мас. % Pd/α -Al2O3
0.167 мл раствора H2PdCl4, приготовленного по Примеру 13, при интенсивном перемешивании приливают к 20 мл водного раствора Na2CO3, содержащего 0.02 г Na2CO3 (на сухой вес). В приготовленный таким образов щелочной раствор палладия добавляют 2.0 г порошка α-Al2O3 (фракция <0.1 мм, SБЭТ=4.0 м2/г) и размешивают 1 ч при 20°С, затем еще 30 мин при 60°С до полного осаждения палладия.
Сушку и восстановление образца водородом осуществляют согласно Примеру 1.
Дисперсность металла в катализаторе, CO/Pd=0.83.
Пример 15 (Сравнительный, согласно прототипу).
Получение образца 1 мас. % Rh/ZrO2.
К 1.5 мл H2O добавляют 0.1 мл 0.1 М [Rh(NH3)6]Cl3 и добавляют 0.2 г ZrO2 (удельная поверхность 10.4 м2/г). Далее образец перемешивают на воздухе при 80°C до испарения всего количества воды и затем в течение 1 ч при 110°C. Далее к 1.5 мл добавляют 0.1 мл 0.1 М (NH4)3[Rh(NO2)6] после чего в раствор помещают высушенный на первом этапе ZrO2 с нанесенной солью. Далее образец перемешивают на воздухе при 80°C до испарения всего количества воды и затем в течение 1 ч при 110°C.
Процесс приготовления завершают процедурой восстановления в водороде при 400°C в течение 1 ч.
Дисперсность металла в катализаторе, CO/Rh=0.027.
Текстурные характеристики оксидных носителей, использованных для приготовления катализаторов, определяли по данным адсорбции N2 при 77К на приборе ASAP 2400 (Micrometritics). Образцы предварительно прокаливали при 573К до остаточного давления 10-3 мм рт.ст. Из начального участка изотермы адсорбции N2 в области Р/Р0=0.05-0.2 вычисляли величину удельной поверхности по БЭТ (SBET). Объем мезопор (Vмe) вычисляли по десорбционной (BJH cum. des.) ветви гистерезиса капиллярной конденсации азота в соответствии с BJH моделью [Е.Р. Barrett, L.G. Joyner, P.P. Halenda, J. Amer. Chem. Soc. 73, 373 (1951)]. Средний диаметр пop (Dпop) вычисляли по модели БЭТ как Dпор=4VΣ/SБЭТ.
Среднеповерхностный размер частиц металла в катализаторах, приготовленных согласно Примерам 1-13, определен методом хемосорбции CO (импульсное CO-титрование).
CO-титрование образцов катализаторов осуществляли при 20-25°С на проточной установке, собранной на базе хроматографа. Навеску катализатора помещали в U-образный стеклянный реактор, служащий одной из колонок хроматографа, и восстанавливали в токе H2 в течение 1 ч при 120°C. Затем реактор охлаждали до комнатной температуры и импульсами (фиксированными порциями) вводили CO в поток H2. В этих условиях молекулы CO прочно адсорбируются только на поверхности нанесенного металла, а их адсорбция на носителе пренебрежимо мала. Концентрацию CO на выходе из реактора определяли с помощью катарометра. Титрование прекращали при полном насыщении поверхности образца адсорбатом.
Дисперсность частиц нанесенных металлов, определяемую как количество поверхностных атомов металла к общему количеству атомов металла в катализаторе, вычисляли по количеству СО, хемосорбированного образцом. Предварительные исследования, направленные на сопоставление хемосорбционных и электронно-микроскопических данных, позволили сделать вывод, что один поверхностный атом Pt и Ru связывает одну молекулу CO, а один поверхностный атом Rh связывает примерно 1.5 молекул CO. При пересчете дисперсности металла на среднеповерхностный размер (ds) его частиц использовали формулы:
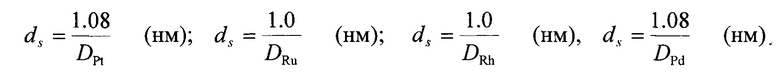
Результаты определения среднеповерхностных размеров частиц палладия в приготовленных образцах катализаторов приведены в Таблице.
Как видно из примеров и Таблицы, предлагаемое изобретение позволяет получать высокодисперсные, с размерами частиц активного компонента 1-3 нм, катализаторы на основе благородных металлов, нанесенных на оксидные носители, которые обладают низкой удельной поверхностью и различной формой частиц (зерна, экструдаты и блоки различной геометрии).

* В пересчете на Ce0.75Zr0.25O2 (Пример 5) или Al2O3@Ce0.75Zr0.25O2 (Пример 9).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ ПЛАТИНО-РУТЕНИЕВЫХ ЭЛЕКТРОКАТАЛИЗАТОРОВ | 2010 |
|
RU2446009C1 |
| КАТАЛИЗАТОР ГИДРИРОВАНИЯ РАСТИТЕЛЬНЫХ МАСЕЛ И ЖИРОВ, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ГИДРИРОВАНИЯ | 2009 |
|
RU2414964C1 |
| ПАЛЛАДИЕВЫЙ КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ЯНТАРНОЙ КИСЛОТЫ | 2015 |
|
RU2603777C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОБЕЗВРЕЖИВАНИЯ ГАЗОВЫХ ВЫБРОСОВ (ВАРИАНТЫ) | 2008 |
|
RU2388532C1 |
| ПАЛЛАДИРОВАННЫЕ НАНОТРУБКИ ДЛЯ ГИДРИРОВАНИЯ РАСТИТЕЛЬНЫХ МАСЕЛ, СПОСОБ ИХ ПРИГОТОВЛЕНИЯ И СПОСОБ ЖИДКОФАЗНОГО ГИДРИРОВАНИЯ | 2010 |
|
RU2438776C1 |
| СОСТАВ И СПОСОБ ПРИГОТОВЛЕНИЯ НОСИТЕЛЯ И КАТАЛИЗАТОРА ГЛУБОКОЙ ГИДРООЧИСТКИ УГЛЕВОДОРОДНОГО СЫРЬЯ | 2012 |
|
RU2569682C2 |
| КАТАЛИТИЧЕСКИЙ НЕЙТРАЛИЗАТОР И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ (ВАРИАНТЫ) | 2000 |
|
RU2262983C2 |
| НАНОСТРУКТУРИРОВАННЫЙ КАТАЛИЗАТОР ДЛЯ ДОЖИГАНИЯ МОНООКСИДА УГЛЕРОДА | 2012 |
|
RU2500469C1 |
| КАТАЛИЗАТОР (ВАРИАНТЫ), СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2003 |
|
RU2248932C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ОКСИДНО-ПОЛИМЕТАЛЛИЧЕСКИХ КАТАЛИЗАТОРОВ НА ОСНОВЕ ЖАРОПРОЧНЫХ СПЛАВОВ ДЛЯ ПАРЦИАЛЬНОГО ОКИСЛЕНИЯ УГЛЕВОДОРОДОВ В СИНТЕЗ-ГАЗ | 2013 |
|
RU2552639C1 |
Изобретение относится к области приготовления катализаторов, которые могут быть использованы в процессах окислительной конверсии углеводородов и селективного окисления кислородсодержащих органических соединений, гидрирования оксидов углерода и ненасыщенных углерод-углеродных и углерод-гетероатомных связей в органических субстратах, гидрокрекинга углеводородов. Катализатор готовят гидролитическим осаждением оксидов платины, рутения или родия на носитель, помещая носитель в метастабильный водный раствор, содержащий хлорсодержащие соль или комплекс платины, рутения или родия и гидролизующий агент при температуре ниже 100°C, которая способствуют ускорению гидролиза соли или комплекса платины, рутения или родия и количественному закреплению оксидов металла на носителе, с последующим извлечением носителя с нанесенными оксидами платины, рутения или родия из раствора, сушкой на воздухе и восстановлением. Технический результат заключается в получении катализатора с высокой дисперсностью частиц активного компонента. 10 з.п. ф-лы, 1 табл., 15 пр.
1. Способ приготовления катализатора нанесением благородных металлов на носитель, отличающийся тем, что катализатор готовят гидролитическим осаждением оксидов платины, рутения или родия на носитель, помещая носитель в метастабильный водный раствор, содержащий хлорсодержащие соль или комплекс платины, рутения или родия и гидролизующий агент при температуре ниже 100°C, которая способствуют ускорению гидролиза соли или комплекса платины, рутения или родия и количественному закреплению оксидов металла на носителе, с последующим извлечением носителя с нанесенными оксидами платины, рутения или родия из раствора, сушкой на воздухе и восстановлением.
2. Способ по п. 1, отличающийся тем, что в качестве гидролизующих агентов для приготовления растворов осаждения используют гидроксиды, гидрокарбонаты или карбонаты щелочных металлов.
3. Способ по п. 1, отличающийся тем, что активный компонент наносят в количестве 0,1-3,0 мас. %.
4. Способ по п. 1, отличающийся тем, что в качестве носителей используют оксиды трудновосстанавливающихся элементов.
5. Способ по п. 1, отличающийся тем, что в составе носителей используют оксиды алюминия, циркония, церия, алюмосиликаты и сплавы алюминия, железа, никеля, хрома.
6. Способ по 1, отличающийся тем, что носитель может быть выполнен в виде порошков, гранул, экструдатов или блоков различной формы и геометрии.
7. Способ по п. 6, отличающийся тем, что блоки могут быть выполнены на основе стеклоткани, пенометалла или пенокерамики.
8. Способ по п. 1, отличающийся тем, что в качестве носителей используют композиционные оксид-оксидные или металл-оксидные блочные носители различной формы и геометрии.
9. Способ по п. 1, отличающийся тем, что температура, которая способствует ускорению гидролиза соединения благородного металла и количественному закреплению оксидов платины, рутения или родия на носителе, не превышает 100°C, преимущественно 20-80°C.
10. Способ по п. 1, отличающийся тем, что катализатор сушат при температуре выше 70°C, преимущественно 100-120°C.
11. Способ по п. 1, отличающийся тем, что восстановление оксида металла проводят при температуре выше 20°C, преимущественно 200-400°C.
| ПАЛЛАДИЕВЫЙ КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ЯНТАРНОЙ КИСЛОТЫ | 2015 |
|
RU2603777C1 |
| US 20120065443 A1, 15.03.2012 | |||
| СПОСОБ ПРИГОТОВЛЕНИЯ НАНЕСЕННЫХ ПОЛИМЕТАЛЛИЧЕСКИХ КАТАЛИЗАТОРОВ (ВАРИАНТЫ) | 2005 |
|
RU2294240C2 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И ПРОЦЕСС ГИДРОДЕОКСИГЕНАЦИИ КИСЛОРОДОРГАНИЧЕСКИХ ПРОДУКТОВ БЫСТРОГО ПИРОЛИЗА БИОМАССЫ | 2007 |
|
RU2335340C1 |
Авторы
Даты
2018-05-08—Публикация
2017-06-26—Подача