Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для диагностических целей при гриппозной инфекции, а также для оценки иммуногенности при вакцинации гриппозными вакцинами.
Современная эпидемическая ситуация по гриппу характеризуется одновременной циркуляцией сразу нескольких вариантов вируса семейства Orthomyxoviridae, рода Influenzavirus A(H1N1), A(H3N2) и В. Традиционно иммуногенность гриппозных вакцин оценивается по формированию после прививки антител к гемагглютинину (HA) в сыворотке крови [Приказ №156/29 МЗ РФ 07.05.1998]. Иммунитет к нейраминидазе (NA) является одним из факторов защиты против инфекции вирусами гриппа A. Для определения антител к нейраминидазе вируса гриппа ранее применялись реассортантные штаммы на основе вируса гриппа A/лошадь/Прага/1/56(H7M7), содержащие нейраминидазу эпидемических вирусов человека A(H1N1) и A(H3N2) [Вопр. вирусологии. - 1985. - №1. - стр.35-39]. При этом использовался тест ингибирования элюции, основанный на блокировании антителами сиалидазной активности NA, что препятствовало разрушению агглютинации эритроцитов, вызванной вирусом гриппа.
Известен реассортантный штамм RN1/09-swine A(H7N1), применяющийся для выявления антител к нейраминидазе подтипа N1 в твердофазном тесте ингибирования сиалидазной активности [Influenza and other respiratory viruses. - 2011. - Vol.5. - Suppl.2. - P. 370-372].
Задачей, на решение которой направлено заявляемое изобретение, является получение реассортантного штамма для определения антител в твердофазном тесте ингибирования сиалидазной активности нейраминидазы подтипа N2. Для этих целей использовали методы классической генетической реассортации в развивающихся куриных эмбрионах (КЭ) вируса A/лошадь/Прага/1/1956(H7N7) и вакцинного штамма A/17/утка/Потсдам/86/92 (H5N2), содержащего нейраминидазу N2 от донора аттенуации A/Ленинград/134/17/1957(H2N2). Для отбора клонов с нужными свойствами и составом генома проводили ряд селективных пассажей при пониженной до 25°C температуре в присутствии поликлональных антител к гемагглютинину вируса гриппа H5.
Вакцинный штамм A/17/утка/Потсдам/86/92(Н5N2), являющийся реассортантом на основе холодоадаптированного донора аттенуации A/Ленинград/134/17/57(H2N2) с формулой генома 7:1, унаследовавшим 6 генов внутренних и неструктурных белков и ген NA от донора аттенуации, а ген HA - от вируса гриппа птиц A/утка/Потсдам/1806-4/86(H5N2) [Патент №2318871. - Б.И. №7, 10.03.2008], был получен из коллекции отдела вирусологии НИИЭМ СЗО РАМН.
Вирус A/лошадь/Прага/1/1956(H7M7) был предоставлен центром по контролю и предупреждению заболеваний США (Атланта, Джорджия).
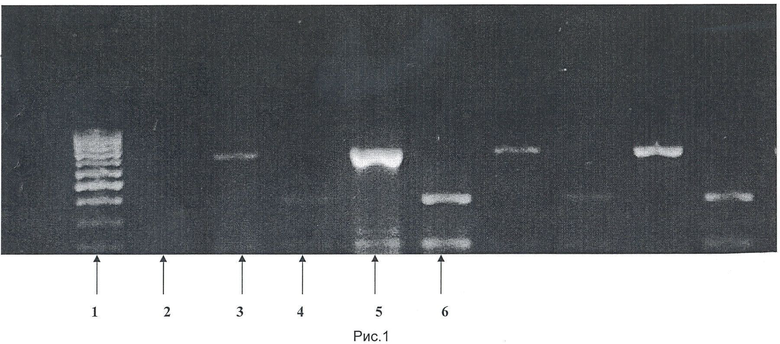
Реассортант RN2/57-human A(H7N2) унаследовал ген NA от штамма Ленинград/134/17/57(Н2N2). На рис.1 представлен пример анализа гена NA при помощи полимеразной цепной реакции (ПЦР) с праймерами, специфичными для нейраминидазы подтипа N2, и последующей обработки фрагментов ДНК эндонуклеазой рестрикции Tru9 I. Дорожки имеют следующее соответствие: 1 -ДНК-маркер (100 bp), 2 - ПЦР с РНК штамма A/лошадь/Прага/1/1956(H7N7), 3 - ПЦР с РНК штамма A/17/утка/Потсдам/86/92(H5N2), 4 - рестрикция ДНК-амплификата гена NA штамма A/17/утка/Потсдам/86/92(H5N2), 5 - ПЦР с РНК штамма RN2/57-human A(H7N2), 6 - рестрикция ДНК-амплификата гена NA штамма RN2/57-human A(H7N2). Наличие амплификации РНК реассортанта RN2/57-human A(H7N2) (5-я дорожка) с праймерами N2 подобно родительскому штамму A/17/утка/Потсдам/86/92(H5N2) (3-я дорожка) и подтверждение специфичности данной амплификации рестрикцией (6-я и 4-я дорожки) свидетельствуют об идентичности гена NA реассортанта RN2/57-human A(H7N2) и штамма A/Ленинград/134/17/57(H2N2).
ПЦР-рестрикционный анализ шести генов негликозилированных белков [J. Virol. Method. - 1995. - №55. - Р.445-446] показал, что все они также были унаследованы от аттенуированного донорского штамма A/Ленинград/134/17/57(H2N2). Принадлежность гемагглютинина реассортанта родительскому штамму A/лошадь/Прага/1/56(H7N7) подтверждена в реакции торможения гемагглютинации (РТГА).
Наличие нейраминидазы вируса гриппа N2 делает возможным применение указанного штамма для выявления перекрестно-реагирующих антител к нейраминидазе этого подтипа у лиц, перенесших инфекцию или прошедших вакцинацию гриппозными вакцинами.
Штамм депонирован в Государственной коллекции вирусов Научно-исследовательского института вирусологии им. Д.И.Ивановского Российской Академии Медицинских Наук под №ГКВ 2475.
Морфология штамма - полиморфная, типичная для вируса гриппа.
ХАРАКТЕРИСТИКА ПОЛУЧЕННОГО ШТАММА.
Инфекционная активность реассортантного штамма RN2/57-human A(H7N2) при репродукции в развивающихся куриных эмбрионах при 33°C в течение 48 часов - 6,3 lg ЭИД50/0,2 мл.
Гемагглютинирующая активность - 1:320.
Паспорт на реассортантный штамм RN2/57-human A(H7N2) прилагается.
ПАСПОРТ ШТАММА
вируса гриппа RN2/57-human A(H7N2)
1. Название штамма - RN2/57-human A(H7N2) [A/лошадь/Прага/1/1956(H7)-A/Ленинград/134/17/1957(N2)]
2. Серия - серия 1
3. Метод получения - реассортация
4. Характеристика родительских вирусов:
а) вирус гриппа лошади - A/лошадь/Прага/1/1956(Н7N7);
б) вакцинный штамм A/17/утка/Потсдам/86/92(Н5N2), содержащий ген НА апатогенного вируса гриппа птиц А/утка/Потсдам/1402-6/1986(H5N2), остальные 7 сегментов РНК донора аттенуации А/Ленинград/134/17/1957(H2N2)
5. Количество пассажей - 6 в процессе рекомбинации; 3 накопительных пассажа в системе развивающихся куриных эмбрионов
6. Характеристика штамма до лиофилизации:
а) оптимальные условия репродукции - 33°С, 48 часов;
б) гемагглютинирующая активность 1:512;
в) инфекционная активность 8,3 lg ЭИД50/0,2 мл;
г) чувствительность к ингибиторам: ингибиторорезистентный;
д) структура генома реассортанта:
- гены от вируса гриппа лошади: НА
- гены от вакцинного штамма (т.е. от донора аттенуации A/Ленинград/134/17/1957(H2N2)) - PB2, PB1, PA, NP, M, NS и NA
7. Характеристика штамма после лиофилизации:
а) дата лиофилизации: 24.12.2009;
б) объем материала в ампуле: 1 мл;
в) инфекционная активность - 6,3 lgЭИД50/0,2 мл;
г) гемагглютинирующая активность -1:320
8. Антигенная специфичность:
а) гемагглютинина - идентичен вирусу A/лошадь/Прага/1/1956(Н7N7) по данным РТГА с крысиной антисывороткой и ПЦР-рестриктазного анализа ДНК-копий гена;
б) нейраминидазы - идентична вирусу A/17/утка/Потсдам/86/92(Н5N2) (т.е. донору аттенуации A/Ленинград/134/17/1957(H2N2)) по данным ПЦР-рестриктазного анализа ДНК-копий гена
9. Бактериологический контроль лиофилизированного материала: дата проведения - 13.01.2010 - стерилен
Назначение полученного штамма - качественное и количественное определение антител к NA подтипа N2 в сыворотках крови.
1. Штамм может применяться для выявления антинейраминидазных антител в тесте ингибирования сиалидазной активности NA.
Методика такого выявления основана на определении титра антинейраминидазных ингибирующих антител, представляющих собой величину, обратную последнему разведению тестируемой сыворотки, в котором еще наблюдается блокирование сиалидазной активности NA диагностического штамма RN2/57-human A(H7N2). Сиалидазная активность NA определяется по отношению к натуральному субстрату (фетуин) с последующим узнаванием демаскированных полисахаридов пероксидазно-меченным лектином.
Для получения иммунных сывороток мышей иммунизируют живым или убитым вирусом гриппа различными способами (интраназально, внутримышечно, интраперитонеально). Эвтаназию проводят согласно «Правилам проведения работ с использованием экспериментальных животных». Взятие крови осуществляется из подключичной артерии, сыворотки крови отбираются после центрифугирования и хранятся при - 20°C.
Пример выполнения эксперимента
Мышам линии СВА вводили интраназально однократно реассортантный штамм A/17/утка/Потсдам/86/92(Н5N2) в дозе 106,5 ЭИД50/0,05 мл. Сыворотки крови иммунизированных мышей были получены через 21 день после инокуляции. Показано, что однократная интраназальная иммунизация стимулировала выработку сывороточных антител как к гемагглютинину, так и нейраминидазе штамма (табл.1). Так, в РТГА и ИФА с очищенным белком титры антител к НА в группе, получившей препарат плацебо, не превышали порога чувствительности методов, в то время как соответствующие титры среди вакцинированных мышей были статистически значимо выше порогового значения. Титры антинейраминидазных антител в группе иммунизированных животных (Me=78,8) также выявлялись на статистически значимо более высоком уровне, чем среди интактных мышей (Me=13,9): выборочные статистики критерия Манна-Уитни и достигнутый уровень значимости составили U=4,0; Z=-2,142, р=0,03. Наибольшая корреляция прослеживалась для данных ИФА с очищенным НА A/17/утка/Потсдам/86/92(Н5N2) и твердофазной РИНА с диагностическим реассортантом RN2/57-human A(H7N2), для которых коэффициент ранговой корреляции Спирмена равнялся rs=0,51, но из за малого объема выборки (n=14) связь все же не являлась статистически значимой (р=0,06).
2 Средний титр в группе вакцинированных выше, чем среди получивших препарат плацебо (одновыборочный t-тест: t13=9,436, р<0,0001);
3 Титры в группе вакцинированных в среднем выше, чем среди получивших препарат плацебо (тест Манна-Уитни: U=4,0; Z=-2,142, р=0,03).
2. Штамм может применяться для выявления антинейраминидазных антител в тесте ингибирования сиалидазной активности NA в сыворотках крови волонтеров, иммунизированных ЖГВ.
У обследуемых волонтеров отбираются пробы крови из пальца до и после вакцинации. Полученные после центрифугирования сыворотки крови хранятся при -20°C.
Пример выполнения эксперимента
С целью клинического изучения моновалентной ЖГВ A/17/утка/Потсдам/86/92(Н5N2) волонтерам в возрасте от 21 до 49 лет вводили препарат двукратно интраназально с интервалом в 21 день в дозе 106,9 или 108,3 ЭИД50/0,5 мл. Антитела в сыворотках крови добровольцев определяли при помощи реакции микронейтрализации и твердофазной реакции ингибирования нейраминидазной активности. Двукратная прививка как пониженной, так и повышенной дозой аттенуированного штамма A/17/утка/Потсдам/86/92(Н5N2) не только эффективно стимулировала выработку нейтрализующих антител, но также привела к статистически значимому увеличению титров антинейраминидазных антител к гомологичному антигену (табл.2). Процент совпадения результатов двух тестов в плане выявления/не выявления сероконверсий в одних и тех же парах сывороток крови вакцинированных повышенной дозой аттенуированного вируса волонтеров составил 73,2%; у 19,5% достоверные приросты сывороточных антител выявлялись только в реакции микронейтрализации; 7,3% привитых лиц демонстрировали иммунный ответ исключительно к NA вакцинного штамма.
Результаты экспериментов наглядно демонстрируют пригодность заявляемого реассортантного штамма для выявления антител к нейраминидазе N2 вируса гриппа, благодаря чему этот штамм может быть использован для диагностики, при изучении иммуногенности гриппозной вакцины, для анализа фоновых значений антинейраминидазных антител в популяции в целом.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕАССОРТАНТНЫЙ ШТАММ ВИРУСА ГРИППА RN 1/09-SWINE A(H7N1) ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К НЕЙРАМИНИДАЗЕ ПРИ ГРИППОЗНОЙ ИНФЕКЦИИ И ВАКЦИНАЦИИ | 2010 |
|
RU2428476C1 |
| Реассортантный штамм вируса гриппа RN2/66-human A(H7N2) для определения антител к нейраминидазе при гриппозной инфекции и вакцинации | 2016 |
|
RU2625024C1 |
| РЕАССОРТАНТНЫЙ ШТАММ ВИРУСА ГРИППА RN9/13-HUMAN A(H6N9) ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К НЕЙРАМИНИДАЗЕ ПРИ ГРИППОЗНОЙ ИНФЕКЦИИ И ВАКЦИНАЦИИ | 2014 |
|
RU2587629C1 |
| ШТАММ ВИРУСА ГРИППА ГКВ 2389 ДЛЯ ПОЛУЧЕНИЯ ЖИВОЙ ИНТРАНАЗАЛЬНОЙ И ИНАКТИВИРОВАННОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2006 |
|
RU2318871C1 |
| Реассортантный штамм вируса гриппа RN2/14-human A(H6N2) для определения антител к нейраминидазе при гриппозной инфекции и вакцинации | 2019 |
|
RU2716416C1 |
| ШТАММ ВИРУСА ГРИППА ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ И ИНАКТИВИРОВАННОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2011 |
|
RU2464309C1 |
| ШТАММ ВИРУСА ГРИППА А/17/MALLARD/НИДЕРЛАНДЫ/00/95(H7N3) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ И ПРОИЗВОДСТВА ИНАКТИВИРОВАННОЙ ГРИППОЗНЫХ ВАКЦИН | 2012 |
|
RU2507256C2 |
| ШТАММ ВИРУСА ГРИППА А/17/Ануи/2013/61 (H7N9) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ИНТРАНАЗАЛЬНОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2013 |
|
RU2563351C2 |
| РЕАССОРТАНТНЫЙ ШТАММ ВИРУСА ГРИППА А/17/СЕРЕБРИСТАЯ ЧАЙКА/САРМА/06/887 (H6N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2015 |
|
RU2606026C1 |
| ШТАММ ВИРУСА ГРИППА А(НINI) ДЛЯ ПОЛУЧЕНИЯ ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЕТЕЙ | 1991 |
|
RU2031941C1 |
Изобретение относится к области биотехнологии, вирусологии и медицине. Диагностический штамм вируса гриппа RN2/57-human A(H7N2) получен путем скрещивания апатогенного вируса гриппа лошадей А/лошадь/Прага/1/1956(H7N7) с холодоадаптированным вакцинным штаммом A/17/yткa/Пoтcдaм/86/92(H5N2) на основе донора аттенуации А/Ленинград/134/17/57(Н2М2). Штамм содержит нейраминидазу вируса гриппа подтипа N2 А/Ленинград/134/17/1957(H2N2) и гемагглютинин вируса гриппа лошадей А/лошадь/Прага/1/1956(Н7М7). Штамм RN2/57-human A(H7N2) активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 33°С, что позволяет накапливать вирусный материал для последующей очистки и концентрации. Изобретение может применяться для выявления антител к нейраминидазе N2 вируса гриппа в сыворотках подопытных животных и волонтеров с использованием твердофазного теста ингибирования сиалидазной активности нейраминидазы (фетуин-лектинового). 1 ил., 2 табл.
Штамм вируса гриппа RN2/57-human A(H7N2), депонированный в Государственной коллекции вирусов Научно-исследовательского института вирусологии им. Д.И. Ивановского Российской академии медицинских наук под №2475, для выявления антител к нейраминидазе N2 вируса гриппа.
| ШТАММ ВИРУСА ГРИППА ГКВ 2389 ДЛЯ ПОЛУЧЕНИЯ ЖИВОЙ ИНТРАНАЗАЛЬНОЙ И ИНАКТИВИРОВАННОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2006 |
|
RU2318871C1 |
| KZ 22286 A4, 15.02.2010 | |||
| ШТАММ ВИРУСА ГРИППА ПТИЦ A/Goose/Krasnoozerskoye/627/05 СУБТИП Н5N1 ДЛЯ ИЗУЧЕНИЯ АКТИВНОСТИ ЛЕЧЕБНЫХ И ПРОФИЛАКТИЧЕСКИХ ПРЕПАРАТОВ ПРОТИВ ВИРУСА ГРИППА | 2008 |
|
RU2366709C1 |
Авторы
Даты
2012-10-20—Публикация
2011-06-16—Подача