Область техники, к которой относится изобретение
Настоящее изобретение относится к композициям для применения в способах лечения воспалительных нарушений и способам получения композиций.
Уровень техники
Существует много болезней/нарушений, являющихся по своей природе воспалительными. Воспалительные нарушения, которые поражают население, включают астму, воспалительную болезнь кишечника, ревматоидный артрит, остеоартрит, ринит, конъюнктивит и дерматит.
Обычно воспаление вызывает боль. Боль из-за воспаления возникает по многим причинам, таким как инфекция, оперативное вмешательство или другие травмы. Кроме того, некоторые болезни, включая злокачественные и сердечно-сосудистые болезни, как известно несут дополнительные воспалительные компоненты в совокупность симптомов пациента.
Астма является болезнью дыхательных путей, включающей и воспаление, и бронхостеноз. Схема лечения астмы зависит от тяжести протекания. Вялая форма болезни либо не лечится, либо лечится ингаляцией β-агонистов, которые воздействуют на бронхостеноз, тогда как пациенты с более тяжелой формой астмы обычно лечатся регулярным ингалированием кортикостероидов, которые в большей степени являются противовоспалительными по своей природе. Новая профилактическая терапия астмы действует блокированием продуцирования вызывающих воспаление лейкотриенов и цитокинов ингибированием энзима 5-липоксигеназы.
Аллергический и неаллергический риниты являются обычной болезнью, поражающей около 30% населения. Ринит оказывает влияние на качество жизни. Действительно, полагают, что ринит оказывает больше влияние на качество жизни, чем, например, астма.
Сенная лихорадка и продолжительный аллергический ринит характеризуются чиханием, ринореей, заложенностью носа, конъюнктивитом и фарингитом. При продолжительном рините часто заметна хроническая закупорка носовых ходов и может доходить до закупорки евстахиевой трубы.
Оральное или местное применение антигистаминов является первым этапом лечения и стероидов - вторым этапом лечения ринита. Для большинства пациентов местное применение кортикостероидов и антигистаминных препаратов пролонгированного действия обеспечивает купирование приступа. Антигистамины также могут воздействовать не иммунологическим путем (non-IgE) на опосредованные аллергические реакции, такие как неаллергический ринит, астма напряжения, холодовая крапивница и неспецифическая бронхиальная гиперреактивность.
Основные клинические эффекты антигистаминов включают уменьшение чихания и ринореи. Однако заложенность носа представляется менее подверженной воздействию. Местное применение антигистаминов (таких как азеластин и левокабастин) обладает преимуществами, включающими быстрое действие и меньшее количество побочных эффектов.
Боль при воспалении может быть снижена ингибированием энзима циклооксигеназы (СОХ). Энзим СОХ существует в двух формах, одна из которых в основном проявляется во многих клетках и тканях (СОХ-1) и другая, которую вызывают раздражители, способствующие воспалению, такие как цитокины, при воспалительной реакции (СОХ-2).
СОХ метаболизируют арахидоновую кислоту в неустойчивый промежуточный простагландин H2(PGH2). PGH2 далее метаболизируется в другие простагландины, включающие PGE2 PGF2α, PGD2 простациклин и тромбоксан А2. Известно, что метаболиты арахидоновой кислоты обладают выраженной физиологической и патофизиологической активностью, включающей эффекты, способствующие воспалению. В частности, известно, что PGE2 является сильным медиатором воспаления и также вызывает жар и боль. В результате были разработаны многочисленные медикаменты для ингибирования образования PGE2, включая "NSAIDs" (нестероидные противовоспалительные медикаменты) и "коксибы" (селективные ингибиторы СОХ-2).
Указанные медикаменты преимущественно действуют путем ингибирования СОХ-1 и/или СОХ-2, снижая, таким образом, образование PGE2. Лейкотриены (LTs) образуются из арахидоновой кислоты рядом энзимов, отличающихся от энзимов пути метаболизма СОХ/PGES. Ключевым энзимом в биосинтезе лейкотриена является 5-липоксигеназа (5-LO), которая в двухстадийной реакции катализирует образование LТА4 из арахидоновой кислоты. Лейкотриен А4 может быть далее метаболизирован в лейкотриен В4, реакция катализируется LTA4-гидролазой. Клеточный биосинтез лейкотриена зависит от белка (FLAP), активирующего 5-липоксигеназу, мембранного белка, который связывает арахидоновую кислоту и облегчает реакцию 5-липоксигеназы. Известно, что лейкотриен В4 является сильным медиатором воспаления, тогда как цистеинилсодержащие лейкотриены C4, D4 и Е4 (CysLTs) являются очень сильнодействующим бронхоконстриктором и медиаторами воспаления, что было учтено в патологии астмы и воспаления. Следовательно, поставляемые 5-LO ингибиторы и антагонисты рецепторов 1 и 2 цистеинилсодержащего лейкотриена представляют два новых класса противовоспалительных препаратов, тогда как разработка поставляемых ингибиторов FLAP, лейкотриена А4 гидролазы, антагонистов рецепторов лейкотриена B4 может обеспечить новые классы противовоспалительных препаратов.
Фосфодиэстераза 4 типа (PDE4) играет важную роль в модулировании активности клеток, которые участвуют в воспалительном процессе, встречающемся при хроническом обструктивном заболевании легких (COPD) и астме. Ингибиторы PDE4 представляют новый класс медикаментов, которые могут ингибировать бронхостеноз, а также ингибировать воспалительную активность клеток (включая ингибирование выработки лейкотриенов).
Липосомы (также известные как липидные везикулы) являются коллоидными частицами, которые образуются из полярных липидных молекул, получаемых из натуральных источников или химическим синтезом. Указанные сферические закрытые структуры, состоящие из искривленных двойных липидных слоев, обычно применяют для включения медикаментов, которые обычно бывают цитотоксичными, для снижения токсичности и/или увеличения эффективности. Включенные в липосомы лекарственные формы обычно поставляют в сухой форме (например, лиофилизированными), которые затем восстанавливают водным раствором непосредственно перед приемом. Это делают для минимизирования возможности потери, например, цитотоксичного медикамента в водном растворе и снижения эффекта включения в липосому.
Липосомы также были применены для инкапсулирования различных лекарственных веществ для введения через нос для улучшения биодоступности или в качестве адъюванта. Медикаменты, которые можно упомянуть, включают столбнячный анатоксин, инсулин, десмопрессин и димедрол (см. Türker et al., Review Article: Nasal Route and Drug Delivery Systems, Pharm. World Sci., 2004; 26, 137-142 и ссылки, указанные в статье), а также ципрофлоксацин, СМ3 и сальбутамол (см. Desai et al, A Facile Method of Delivery of Liposomes by Nebulization, J. Control. Release, 2002; 84, 69-78).
Цетиризин, включенный в липосому, применяли локально для оценки периферической антигистаминной активности и системной резорбции на кроликах (Elzainy et al., Cetirizine from Topical Phosphatidylcholine-Hydrogenated Liposomes, The AAPS Journal, 2004; 6, 1-7, см. также Drug Development and Industrial Pharmacy, 2005; 31, 281-291).
Гомогенные фармацевтические композиции, содержащие цетиризин и полярную липидную липосому, раскрыты в WO 2005/107711.
Было изучено липофильное поведение цетиризина в водных буферных фосфатидилхолин (лецитин) липосомных системах (Plemper van Balen G et al., Lipophilicity behaviour of the zwitterionic antihistamine cetirizine in phosphatidylcholine liposomes/water systems, Pharm. Res. 2001; 18, 694-701).
Примеры других рецептур, включающих inter alia инкапсулированные в липосому активные ингредиенты, рассмотрены в US 4427649, US 5569464, EP 0249561, WO 00/38681, US 4839175 и WO 98/00111.
Раскрытие изобретения
Неожиданно нами было обнаружено, что раздражение, которое может быть вызвано применением (например, назальным) некоторых противовоспалительных и/или антигистаминных активных ингредиентов, может быть снижено путем применения гомогенных фармацевтических композиций, включающих указанные активные ингредиенты, полярную липидную липосому и фармацевтически приемлемый носитель.
В соответствии с настоящим изобретением предложена гомогенная фармацевтическая композиция, пригодная для лечения воспалительных нарушений, включающая противовоспалительный и/или антигистаминный активные ингредиенты, полярную липидную липосому и фармацевтически приемлемый носитель при условии, что активный ингредиент не является цетиризином, указанные композиции здесь и далее именуются как "композиции изобретения".
Специалисту в данной области техники понятно, что противовоспалительный и/или антигистаминный активные ингредиенты применяют в композициях изобретения в фармакологически эффективных количествах (vide infra).
Термин "фармакологически активное количество" относится к количеству противовоспалительного и/или антигистаминного активного ингредиента, которое способно произвести желаемый терапевтический эффект при лечении пациента, при получении одного или в комбинации с другим активным ингредиентом. Указанный эффект может быть объективным (т.е. измеримым при помощи теста или маркера) или субъективным (т.е. субъект обозначает симптомы, восприятие эффекта).
Под "фармацевтическими композициями" подразумеваются композиции, которые являются подходящими для прямого применения к млекопитающим, особенно к человеку. В этом отношении термин предназначен для включения рецептур, которые содержат только такие компоненты, которые рассматриваются в известном уровне техники как подходящие для применения к млекопитающим, особенно к человеку.
В контексте настоящего изобретения термин также может означать композиции изобретения, находящиеся в форме жидкости, годной к применению прямо с полки, а не рецептуры, в которых медикамент инкапсулирован внутрь липосом, требующие восстановления незадолго перед применением для исключения потери медикамента из липосом в водный носитель.
Под "гомогенными" подразумеваются не только композиции изобретения, содержащие липосомы, равномерно диспергированные в водном носителе, но также в которых активный ингредиент распределен по всей композиции. Это означает, что после образования смеси, включающей липосомы и медикаменты в водной среде, медикамент, который не инкапсулирован в липосому, не удаляется при последующем образовании липосомы. Это может привести в случае некоторых композиций изобретения к по существу одинаковой концентрации активного компонента в подходящей водной среде вне зависимости, находится ли указанная среда внутри или вне структур липосом. Под "по существу одинаковая" подразумевается, что концентрация может меняться на около ±50%, например, на около ±40%, предпочтительно около ±30%, более предпочтительно около ±20% и особенно около ±10% (при сравнении концентраций внутри и вне структур липосом) при комнатной температуре и атмосферном давлении. Изменение концентрации медикамента может быть измерено стандартным способом, известным специалисту в данной области техники, таким как 31Р-ЯМР. Например, стандартным in situ способом зондирования или может быть применен способ, который включает отделение фракции липосомы от свободного водного носителя и измерение количества/концентрации медикамента, связанного с каждой фракцией. Отделение может быть выполнено центрифугированием, диализом, ультрафильтрацией или гель-фильтрацией.
Предпочтительно, чтобы композиции изобретения, кроме того, включали фармацевтически приемлемый буфер, способный обеспечить рН от около рН 4 (например, 4,0) до около рН 8 (например, 8,0), предпочтительно от около рН 5 (например, 5,0) до около рН 7 (например, 7,0). Подходящие буферы включают такие, которые не повлияют на образование липосом, такие как фосфат (например, динатрий фосфат или фосфорная кислота плюс основание), цитрат (например, цитрат натрия или лимонная кислота плюс основание) или ацетатный буфер (например, ацетат натрия или уксусная кислота плюс основание), которые способны поддерживать рН в пределах, указанных выше. Буферы могут быть применены в количествах, которые подходят для обеспечения вышеуказанных эффектов, и понятны специалисту в данной области техники. Подходящие количества находятся, например, в ряду около 1 - 30 мг/мл.
Термин "воспалительное нарушение", понятный специалисту в данной области техники, включает любые условия, характеризуемые локализованной или системной защитной реакцией, которая может быть вызвана физической травмой, инфекцией, хроническими болезнями, такими как вышеуказанные и/или химические, и/или физиологические реакции на внешние раздражители (например, как часть аллергической реакции). Любая подобная реакция, которая может служить для разрушения, разбавления или изолирования и вредоносного фактора и раневой ткани, может выражаться, например, в повышенной температуре тела, опухоли, боли, покраснении, дилатации кровеносных сосудов и/или усилении кровотока, инвазии лейкоцитов в пораженный участок, потере функции и/или любых других симптомах, которые связаны с условиями воспаления.
Следует понять, что этот термин включает любые воспалительные болезни, нарушения или условия, в том числе условия, содержащие воспалительный компонент с ними связанный, и/или условия, характеризуемые воспалением, такие как симптомы, включая среди прочих острые, хронические, язвенные, специфические и некротические воспаления и другие формы воспаления, известные специалисту в данной области. Таким образом, термин для целей настоящего изобретения также включает боль при воспалении, боль в общем и/или жар.
Соответственно, композиции изобретения могут быть полезньми при лечении астмы, хронического обструктивного заболевания легких, фиброза легких, воспалительного заболевания кишечника, синдрома раздраженного кишечника, боли при воспалении, жара, мигрени, головной боли, поясничной боли, фибромиалгии, миофасциальных нарушений, вирусных инфекций (например, гриппа, простуды, опоясывающего герпеса, гепатита С и СПИДа), бактериальных инфекций, грибковых инфекций, дисменореи, ожогов, при хирургических и зубных процедурах, злокачественных опухолях (например, рака молочной железы, колоректальный, простаты), синдрома гиперпростагландина Е, классического синдрома Бартера (Bartter), атеросклероза, подагры, артрита, остеоартрита, болезни Стилла, ревматоидного артрита, жара, болезни Бехтерева, лимфогранулематоза, системной красной волчанки, васкулита, панкреатита, нефрита, бурсита, конъюнктивита, ирита, склерита, увеита, заживлении ран, дерматита, экземы, псориаза, удара, сахарного диабета, болезни Альцгеймера, множественного (рассеянного) склероза, аутоимунных болезней, аллергических болезней, ринита, язв, коронарной болезни, саркоидоза и любых других болезней с воспалительным компонентом.
Композиции изобретения особенно полезны в лечении ринита, мигрени, острой боли, хронической боли и астмы. Термин "ринит" включает любую ирритацию и/или воспаление носа, вне зависимости аллергические или нет, включая сезонный ринит (например, вызванный внешними факторами, такими как пыльца; сенная лихорадка) и/или постоянный ринит (например, вызванный клещевым аллергеном домашней пыли, домашним грибком и т.д.), так же как и их симптомы.
Термин "противовоспалительный и/или антигистаминный активный ингредиент" включает любое вещество вне зависимости природное или синтетическое с соответствующими противовоспалительными и/или антигистаминными свойствами. Класс противовоспалительных соединений включает стероидные противовоспалительные медикаменты (кортикостероиды) и нестероидные противовоспалительные медикаменты (NSAIDs), последние из которых включают ингибиторы СОХ, ингибиторы PDE4 и модификаторы лейкотриенов (например, ингибиторы 5-липогеназы, ингибиторы FLAP, гидролазы LTA4, антагонисты LTB4 рецепторов и CysLT (т.е. CysLT1 и CysLT2) рецепторов), тогда как класс антигистаминных соединений включает антагонисты H1 рецепторов. В контексте настоящего изобретения термин "противовоспалительный и/или антигистаминный активный ингредиент" также включает средства против мигрени, опиоиды и их аналоги.
Предпочтительные активные ингредиенты композиций изобретения включают антигистаминные ингредиенты, кортикостероиды и модификаторы лейкотриенов.
Средства против мигрени, которые могут быть упомянуты, включают алмотрипан, дигидроэрготамин, элетрипан, эрготамин, пиретрум девичий, фроватриптан, ипразохром, метисергид, наратриптан, пизотифен, ризатриптан, суматриптан, золмитриптан и обычно применяемые соли этих веществ.
Опиоиды и их аналоги, которые могут быть упомянуты, включают альфентанил, анилеридин, безитрамид, бупренорфин, буторфанол, карфентанил, кодеин, декстроморамид, декстропропоксифен, дезоцин, диаморфин, дигидрокодеин, дипипанон, эмбутрамид, этогептазин, этилморфин, эторфин, фентанил, гидрокодон, гидроморфин, кетобемидон, левацетилметадол, левометадон, левофанол, лофексидин, мептазинол, метадон, морфин, налбуфин, налтрексон, никоморфин, опиум, оксикодон, оксиморфон, папаверетум, пентазоцин, петидин, пентазоцин, феноперидин, фолкодин, пиритрамид, ремифентанил, суфентанил, тилидин, трамадол и обычно применяемые соли этих веществ.
Стероидные противовоспалительные вещества, которые могут быть упомянуты, включают алклометазон, беклометазон, бетаметазон, будезонид, циклезонид, клобетазол, клобетазон, дефлазакорт, дексаметазон, дифлокортолон валерат, флуоцинолон ацетонид, флуоцинонид, флуокортолон, флупредниден, флурометолон, флутиказон, халцинонид, гидрокортизон, метилпреднизолон, мометазон, преднизолон, римексолон, триамцинолон и обычно применяемые соли этих веществ. Предпочтительные стероидные противовоспалительные вещества будезонид и флутиказон (например, последнее в форме соли, такой как пропионат).
NSAIDs (включая ингибиторы СОХ), которые могут быть упомянуты, включают ацеклофенак, ацемеацин, ацетанилид, алклофенак, алминопрофен, алоксиприн, аминопирин, аминопропилон, ампироксикам, амтолметин гуацил, амил салицилат, аспирин, азапропазон, бендазак, беноксапрофен, бензидамин, бета-аминопропионитрил, борнил салицилат, бромофенак, буфексамак, бумадизон, бутибуфен, карбасалат, карпрофен, целекоксиб, клофексамид, клофезон, клониксин, декскетопрефен, диклофенак, дифлунизал, дипирон, дроксикам, элтенак, эпиризол, этодолак, этензамид, этил салицилат, этофенамат, эторикоксиб, фелбинак, фенбуфен, фенопрефен, фентиазак, фепрадинол, фепразон, флоктафенин, флуфенамовая кислота, флуниксин, флуноксапрофен, флурбипрофен, фосфосал, фурпрофен, глафенин, глукаметацин, гликоль салицилат, ибупрофен, ибупроксам, индометацин, кетопрофен, кеторолак, лизин аспирин, мефенамовая кислота, мелоксикам, метил бутенизалицилат, метил салицилат, набуметон, напроксен, недокромил, нифеназон, нифлумовая кислота, нимесулид, оксапрозин, оксифенбутазон, парацетамол, парекоксиб, фенацетин, феназон, фенилбутазон, пиколамин салицилат, пикетопрофен, пироксикам, пранопрофен, проглуметацин, пропацетамол, пропифеназон, проказон, рамифеназон, рофекоксиб, саламидацетиловая кислота, салициламид, саликс, салол, салсалат, хромогликат натрия, салицилат, тиосалицилат, сулиндак, супрофен, суксибузон, тенидап, теноксикам, тетридамин, турфил салицилат, тиапрофеновая кислота, тиарамид, тиноридин, толфенамовая кислота, толметин, трисалипилат, троламин салицилат, уфенамат, валдекоксиб, ведапрофен, залтопрофен и обычно применяемые соли этих веществ.
Специфические ингибиторы PDE4, которые могут быть упомянуты, включают циломиласт, рофлумиласт, тетомиласт, пикламиласт, так же как
(аа) СР-671305, (+)-2-[4-({[бензо[1,3]диоксол-5-илокси)-пиридин-3-карбонил]-амино}-метил)-3-фтор-фенокси]-пропионовая кислота,
(bb) SCH351591, N-(3,5-дихлор-1-оксидо-4-пиридинил)-8-метокси-2-(трифторметил)-5-хинолинкарбоксамид,
(cc) KF 19514, 5-фенил-3-(3-пиридил)метил-3H-имидазо(4,5-с)(1,8)-нафтиридин-4(5Я)-он,
(dd) AWD 12-281, N-(3,5-дихлорпирид-4-ил)-(1-(4-фторбензил)-5-гидрокси-индол-3-ил)глиоксиловой кислоты амид,
(ее) D 22888, 1-этил-8-метокси-3-метил-5-пропилимидазо(1,5-а)пиридо(3,2-е)пиразинон,
(ff) YM976, 4-(3-хлорфенил)-1,7-диэтилпиридо[2,3-d]пиридин-2(1H)-он,
(gg) NVP-ABE171, 4-(8-бензо[1,2,5]оксадиазол-5-ил[1,7]нафтиридин-6-ил)-бензойная кислота,
(hh) CI-1044, N-(9-амино-4-оксо-1-фенил-3,4,6,7-тетрагидро(1,4)диазепино-(6,7,1-hi)индол-3-ил)никотинамид,
(ii) SB 207499, с-4-циано-4-(3-циклопентилокси-4-метоксифенил)-1-циклогексанкарбоновая кислота,
(jj) CC-100004, YM-64227, BAY 19-8004 и GRC 3886,
и обычно применяемые соли этих веществ.
Антагонисты CysLT1 и CysLT2 рецепторов, которые могут быть упомянуты, включают абулукаст, циналукаст, иралукаст, монтелукаст, побилукаст, пранлукаст, сулукаст, томелукаст, верлукаст, зафирлукаст,
(I) BAY-u9773
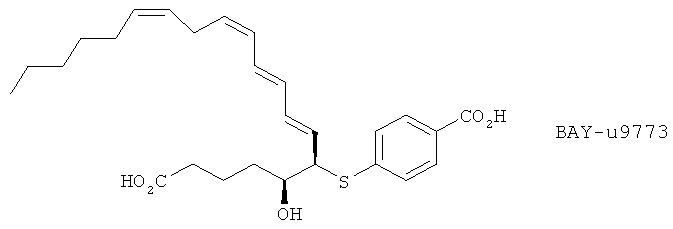
(II) MK571
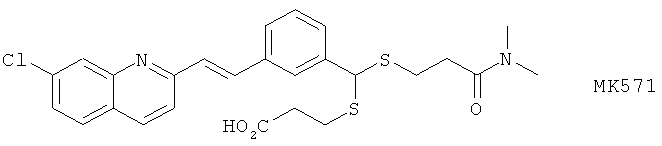
и обычно применяемые соли этих веществ. Предпочтительные антагонисты CysLT рецепторов, которые могут быть упомянуты, включают монтелукаст.
Ингибиторы 5-липоксигеназы, которые могут быть упомянуты, включают следующее.
(1) Зилеутон (синонимы: А-64077, АВТ 077, Zyflo®), описанный, например, в ЕР 0279263, US 4873259, Int. J. Immunopharmacol. 14, 505 (1992), Br. J. Cancer 74, 683 (1996) и Am. J. Resp.Critical Care Med. 157, Part 2,1187 (1998)
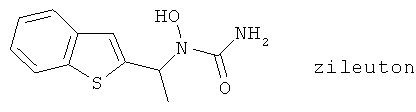
(2) А-63162, описанный, например, в Anticancer Res. 14, 1951 (1994)

(3) A-72694
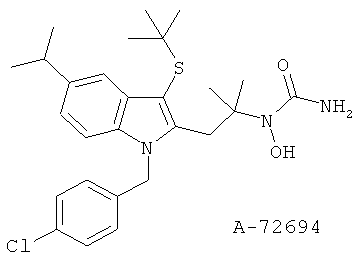
(4) А-78773, описанный, например, в Curr. Opin. Invest. Drugs 2, 69 (1993)
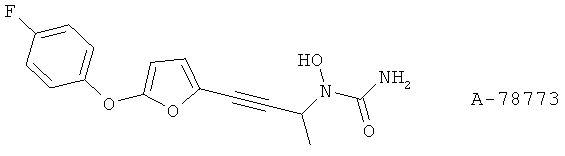
(5) А-79175 (R-энантиомер А-78773), описанный, например, в Carcinogenesis 19, 1393 (1998) и J. Med Chem. 40, 1955 (1997)
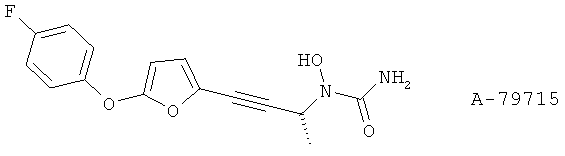
(6) A-80263
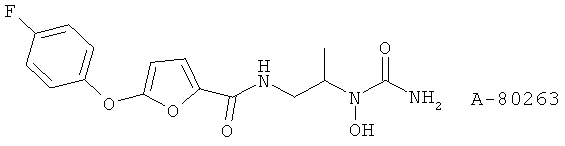
(7) A-81834
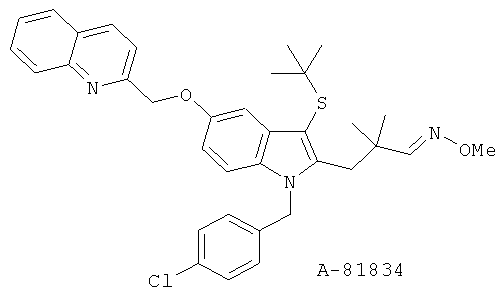
(8) A-93178
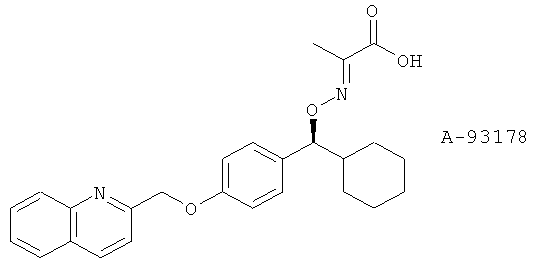
(9) А-121798, описанный, например, в 211th Am. Chem. Soc. Meeting. 211: abstr. 246, 24 March 1996.
(10) Атрелеутон (синонимы АВТ-761 и А-85761), описанный, например, в Ехр. Opin. Therap. Patents 5 127 (1995)
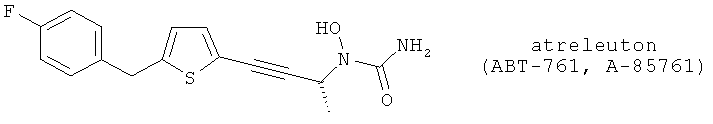
(11) MLN-977 (синонимы LPD-977 и CMI-977), описанный, например, в Сиrr. Opin. Anti-Inflamm. & Immunomod. Invest. Drugs 1, 468 (1999). Указанное, так же как и подобные соединения, описано в US 5703093
(12) CMI-947, описанный, например, в 215th Am. Chem. Soc. Meeting. 215: abstr. MEDI 004, 29 March 1998. Указанное, так же как и подобные соединения, описано в US 5792776

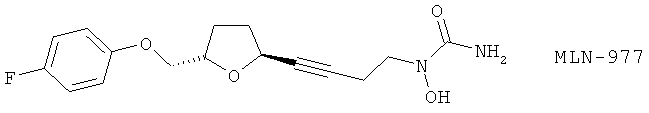
(13) CMI-568, описанный, например, в 211th Am. Chem. Soc. Meeting. 211: abstr. 20524 March 1996
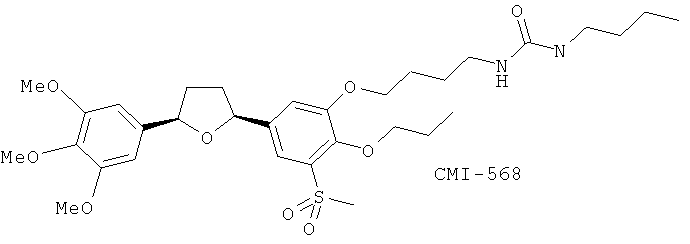
(14) LDP 392 (синоним СМI 392), описанный, например, в Pharmacol. Res. 44, 213 (2001)
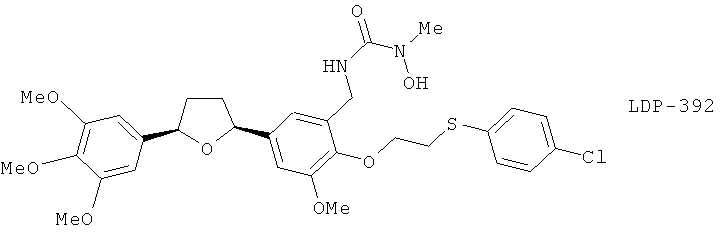
(15) Линетастин (синонимы: линмзоласт, ТМK 688, YM 257), описанный, например, в Int. J. Immunopharmacol. 22, 123 (2000)
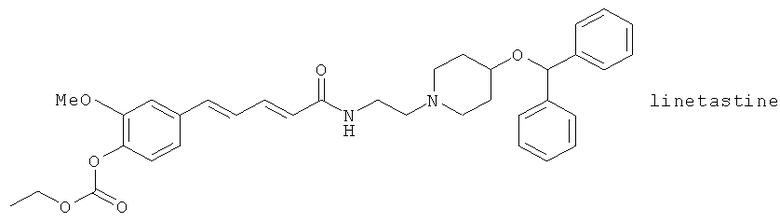
(16) Лонапален (синоним: RS 43179), описанный, например, в Pharm. Res. 9, 1145 (1992)
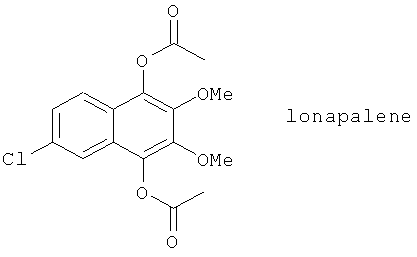
(17) LY-221068, описанный, например, в Ann. N.Y. Acad. Sci. (Immunosuppressive and Antiinflammatory Drugs) 696, 415 (1993)

(18) LY 269415, описанный, например, в Agents and Actions 42, 67 (1994)
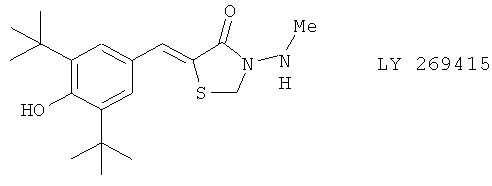
(19) Ингибиторы 5-LO с антагонистической активностью к H1 рецепторам гистамина, описанные, например, в Bioorg. Med. Chem. Lett. 14, 2265 (2004), такие как следующие соединения
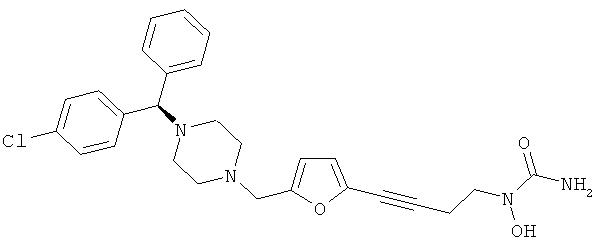
(20) BF-389

(21) BIL 226 и BIL 357, описанные, например, в J.Pharmacol. Exp. Therap.265, 483(1993)
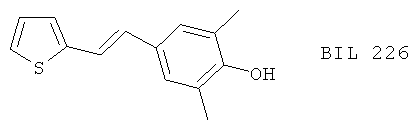
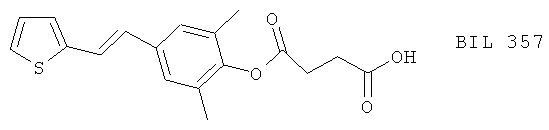
(22) BU 4601A, BU 4601В и BU 4601C, описанные, например, в J.Antibiotics 46, 705 (1993)
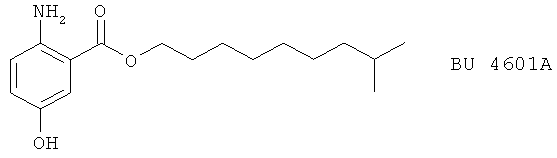
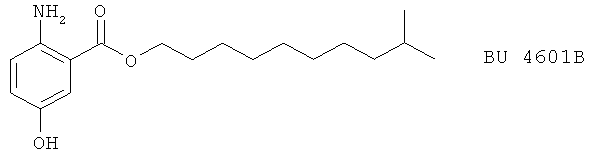

(23) BW 755C, описанный, например, в J. Pharm. Exp. Therap. 277, 17 (1996)
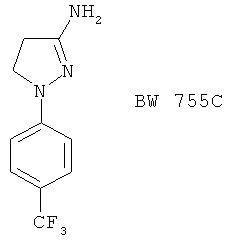
(24) BW-A4C, описанный, например, в Eur. J. Biochem. 267, 3633 (2000)
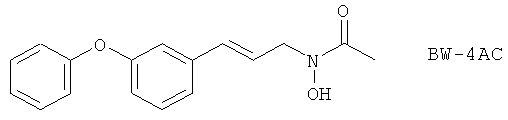
(25) BWB 70C, описанный, например, в Br. J. Pharmacol. 108 (Suppl), 186P (1993)
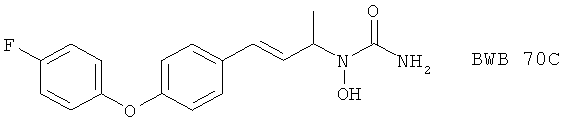
(26) CBS 1108
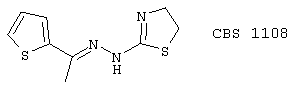
(27) CGS 26529, описанный, например, в Inflamm. Res. 44 (Suppl. 2) 147 (1995)
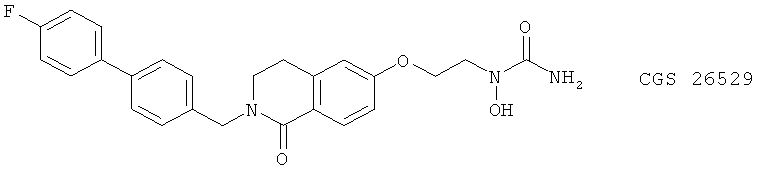
(28) CGS 25667, CGS 25997 и CGS 25998, описанные, например, в J. Med. Chem. 38, 68 (1995)

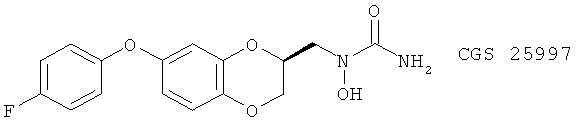
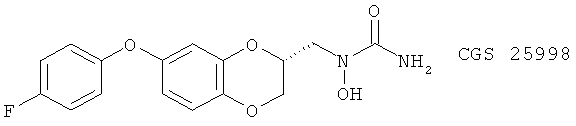
(29) CGS-23885, описанный, например, в J. Med. Chem. 36,3580 (1993)
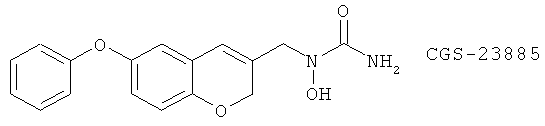
(30) CI-986
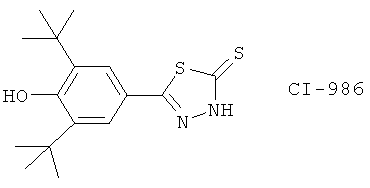
(31) CT 3 (синонимы: аджумелиевая кислота, DMH-11C, HU 239), описанный, например, в J. Med Chem. 35, 3153 (1992)
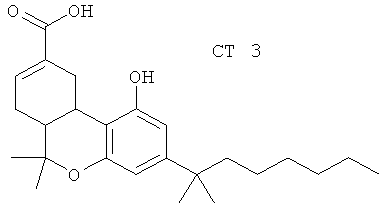
(32) CV 6504, описанный, например, в Ann. Oncol. 11,1165 (2000)
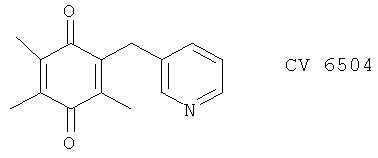
(33) Дарбуфелон (синонимы: CI-1004, PD 136095-0073) и его аналоги, описанные, например, в Arthritis and Rheumatism 42 (Suppl.) 404 (1999), ibid 42 (Suppl.) 81 (plus poster) (1999) и J. Med. Chem. 37, 322 (1994)
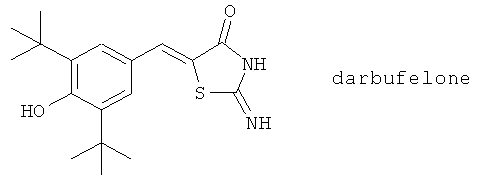
(34) Доцебенон (синоним АА861) и его аналоги, описанные, например, в Int. Arch. Allergy and Immunol. 100, 178 (1993) и Biochim. Biophys. Acta 713, 470 (1982)
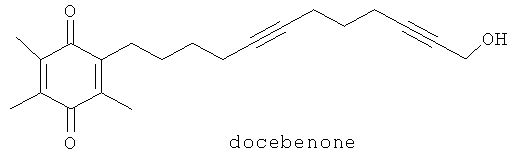
(35) DUP 654, описанный, например, в J. Med. Chem. 33, 360 (1990)
(36) ХА 547, описанный, например, в BTG International Inc. Company Communication 15 Oct 1999, и Bioorg. Med. Chem. 3, 1255 (1995).
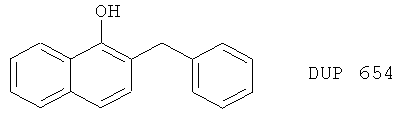
(37) E-3040
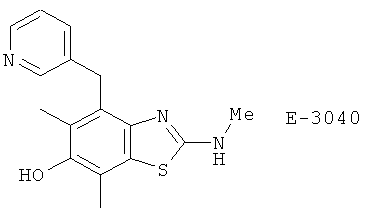
(38) E 6080, описанный, например, в Res. Commun. Mol. Pathol. Pharmacol. 86, 75 (1994)
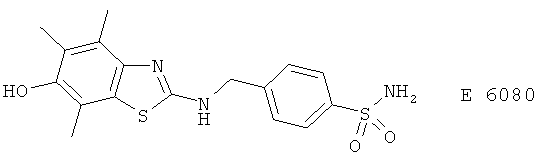
(39) E 6700
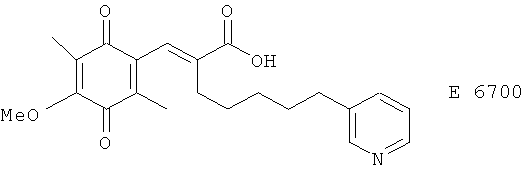
(40) Эпокарбозолин А, соединение, выделенное из Streptomyces anulatus T688-8 и описанное, например, в J. Antibiotics 46, 25 (1993)
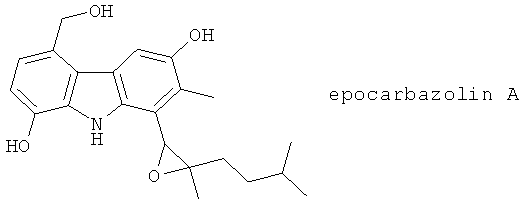
(41) ER 34122, описанный, например, в Inflamm. Res. 47, 375 (1998)
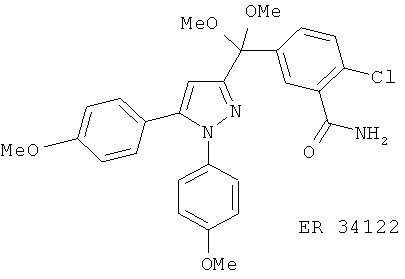
(42) ETH 615, описанный, например, в Ехр. Dermatol. 2, 165 (1993)
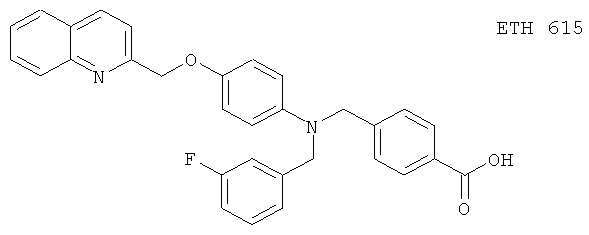
(43) F 1322, описанный, например, в XV International Congress of Allergology and Clinical Immunology (Suppl 2) 325 (1994)
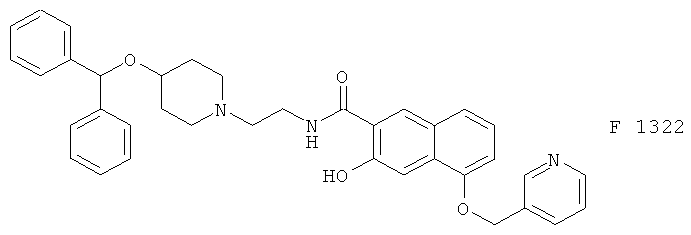
(44) Флезаластин (синонимы: D 18024, IDB 18024), описанный, например, в Allergy (Suppl.) 47, 47 (1992)

(45) Азеластин, описанный, например, в Int. Arch. Allergy and Applied Immunol. 90, 285 (1989)
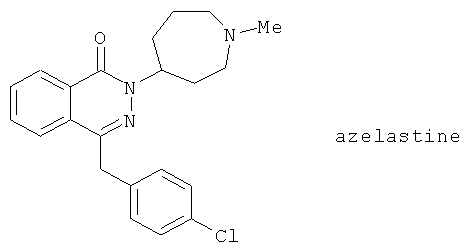
(46) FPL 62064, описанный, например, в Agents and Actions 30, 432 (1990)
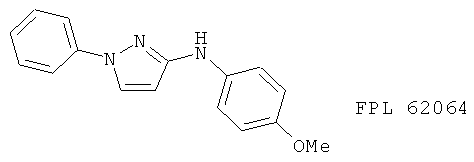
(47) FR 110302, описанный, например, в Am. Rev. Resp.Dis. 145, A614 (1992)
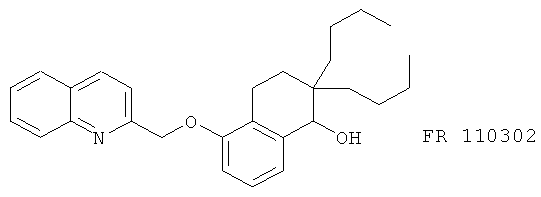
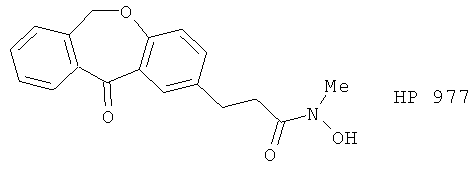
(48) HP 977 и Р 10294, описанные, например, в J. Med. Chem. 39, 246 (1996)
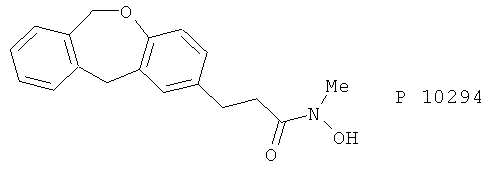
(49) P-8977
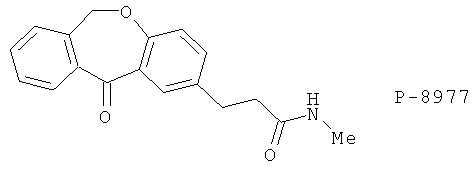
(50) НХ-0835, описанный, например, в Rinsho Iyaku. 11, 1577 & 1587 (1995)

(51) НХ-0836, описанный, например, в J. Med. Chem. 36 3904 (1993)
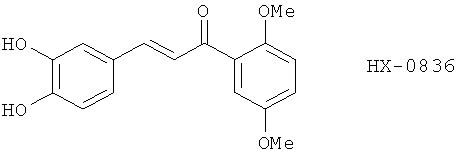
(52) Следующее соединение, описанное в Bioorg. Med. Chem. Lett. 6, 93 (1996)
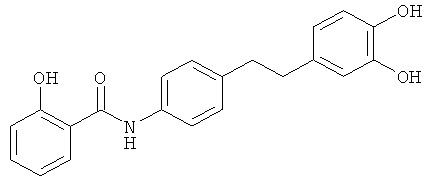
(53) Икодулиний (синонимы: CBS 113А, икодулин), описанный, например, в Arzneimittel-Forschung (Drug Research) 39, 1242 & 1246 (1989)
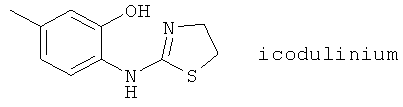
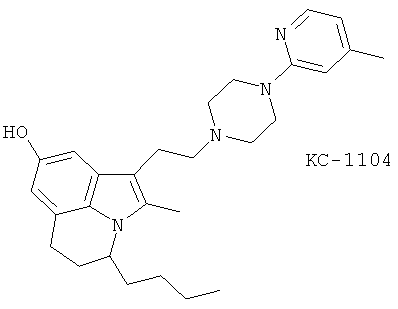
(54) KC-11404, описанный, например, в Eur. Resp. J. 7 (Suppl. 18), 48 (1994)
(55) KC-11425
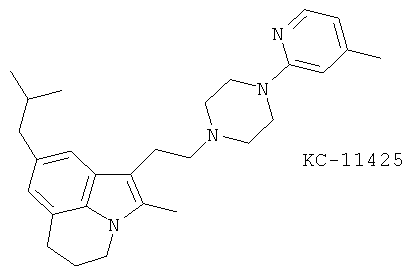
(56) KME 4
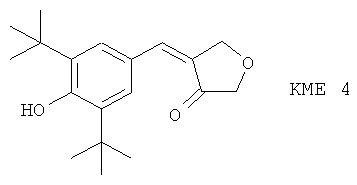
(57) L 651392, описанный, например, в Adv. Prostaglandin, Thromboxane and Leukotriene Res. 17, 554 (1987)

(58) L 651896
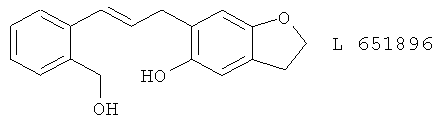
(59) L 652343

(60) L 653150
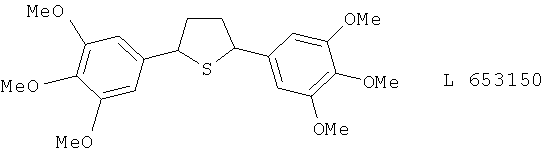
(61) L-656224, описанный, например, в J. Gastroenterol. Hepatol. 11, 922 (1996)

(62) L-702539, описанный, например, в J. Med. Chem. 37, 512 (1994)

(63) L-670630
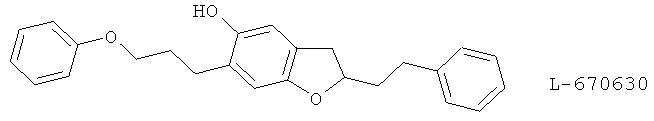
(64) L-691816, описанный, например, в Curr. Opin. Invest. Drugs 2, 683 (1993)
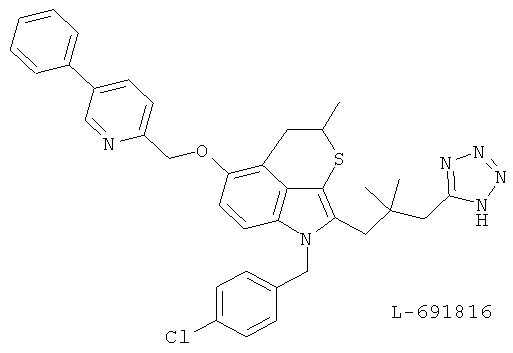
(65) L 699333, описанный, например, в J. Med. Chem. 38, 4538 (1995)
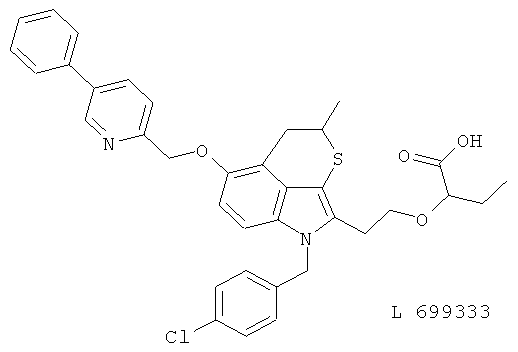
(66) L 739010
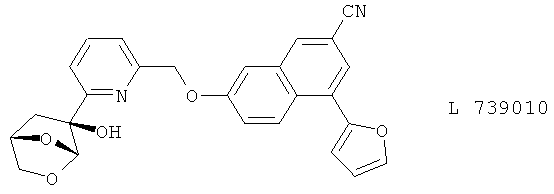
(67) Лагунамицин, описанный, например, в J. Antibiotics 46, 900 (1993)

(68) Ликофелон (синоним: ML 3000), описанный, например, в Eur. J. Pharm. 453, 131 (2002) и J. Med. Chem. 37, 1894 (1994)
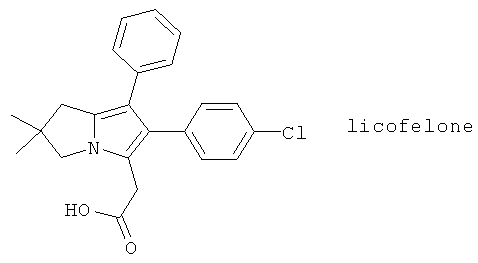
(69) PD 145246
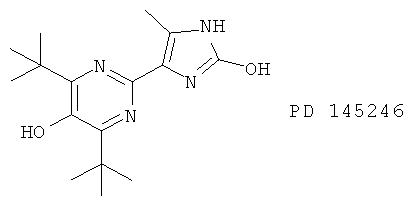
(70) R 840 (синоним: S 26431)
(71) R 68151, описанный, например, в Arch. Dermatol. 128, 993 (1992)

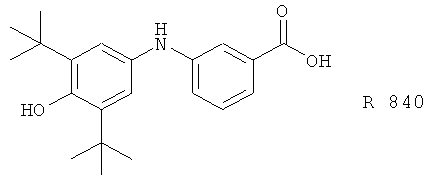
(72) R 85355, описанный, например, в Skin Pharmacol. 9, 307 (1996)
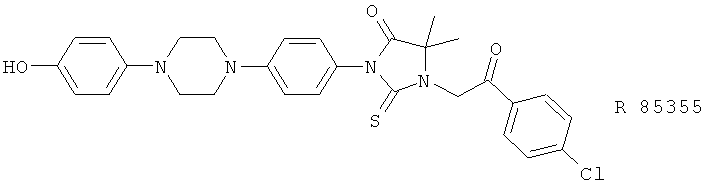
(73) REV 5901 (синонимы: PF 5901, Ревлон 5901, RG 5901), описанный, например, в J. Allergy Clin. Immunol. 91, 214 (1993)
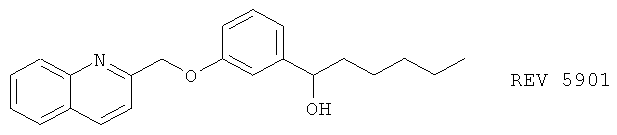
(74) RWJ 63556, описанный, например, в 214th Am. Chem. Soc. Nat. Meeting, abstr. MEDI 091 (1997)
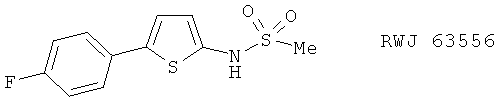
(75) S 19812, описанный, например, в Mediators of Inflammation 8 (Suppl. 1), 134 & 135 (1999)

(76) SC 45662, описанный, например, в J. Allergy and Clin. Immunol. 89, 208 (1992)

(77) SC-41661A
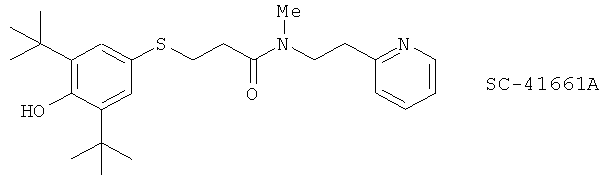
(78) SCH 40120
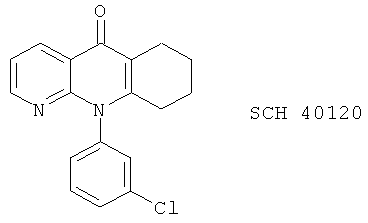
(79) SKF-86002
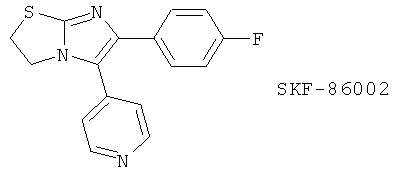
(80) SKF 104351 и SKF 105809
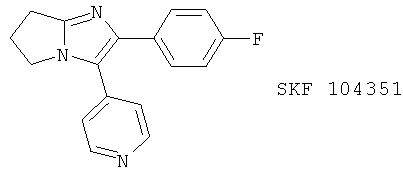
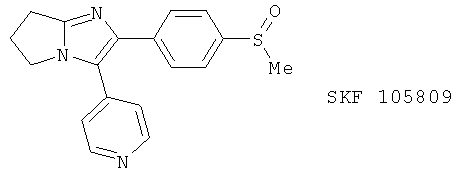
(81) SKF-107649, описанный, например, в J. Med. Chem. 39, 5035 (1996)
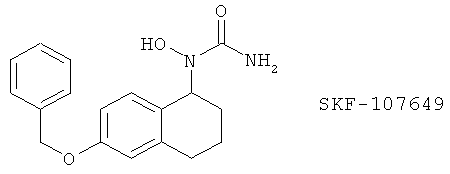
(82) T0757 и Т0799, описанные, например, в Jap. J. Pharmacol. 66, 363 (1994)
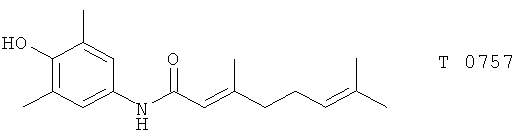
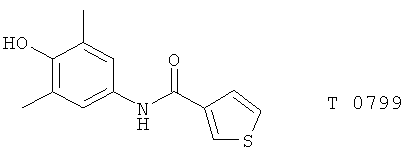
(83) ТА 270, описанный, например, в Naunyn-Schmiedeberg′s Arch. Pharmacol. 358 (Suppl. 2) 737 (1998)

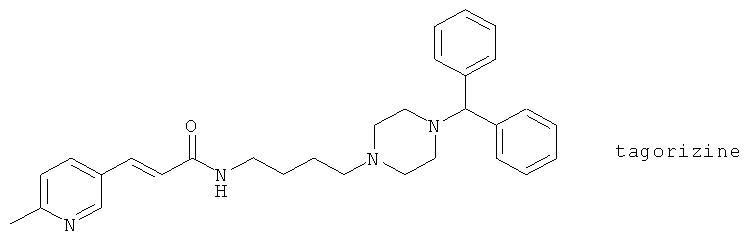
(84) Тагоризин (синоним: AL 3264), описанный, например, в Jap. J. Pharmacol. 65, 19 (1994) и ibid. 64 (Suppl. 1), 312 (1994)
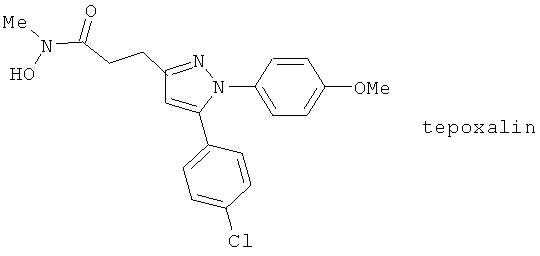
(85) Тепоксалин (синонимы: ORF 20485, RWJ 20485), описанный, например, в J. Pharmacol. Exp. Therap. 271, 1399 (1994)
(86) UPA 780, описанный, например, в Inflamm. Res. 44 (Suppl. 3), 273 (1995)
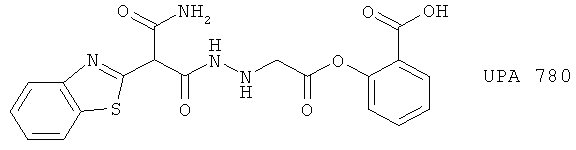
(87) VUFB 19363
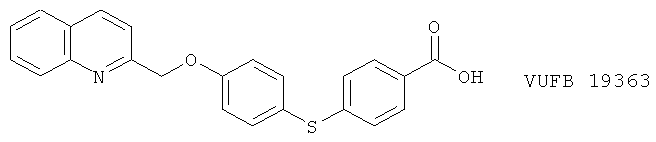
(88) VZ 564, описанный, например, в Arzneimittel-Forschung (Drug Research) 25, 155 (1995)
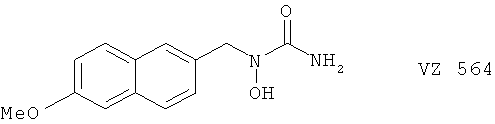
(89) Следующее соединение, описанное в J. Med. Chem. 40, 819 (1997)
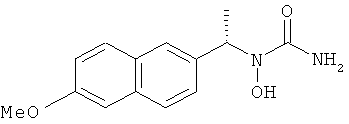
(90) WAY 120739
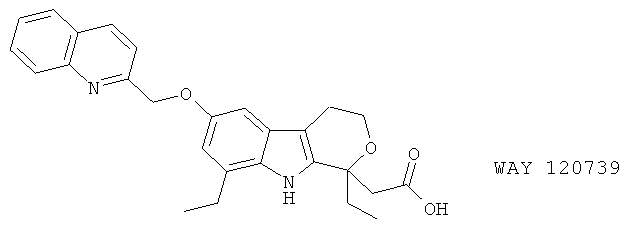
(91) WAY 121520, описанный, например, в Agents and Actions 39 (Spec. issue C1) C30 (1993) и Ехр. Opin. Invest. Drugs 6, 279 (1997)

(92) WAY-126299A, описанный, например, в Inflamm. Res. 44 (Suppl. 2), 170 (1995)
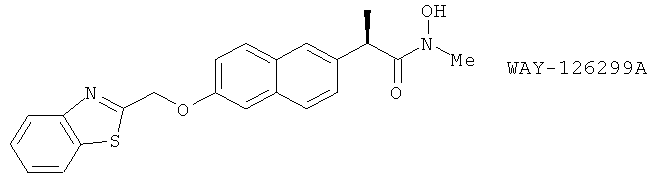
(93) WAY-125007, описанный, например, в WO 04/004773

(94) WHIP 97, описанный, например, в 216th Am. Chem. Soc. Nat. Meeting, abstr. MEDI 363 (1998)
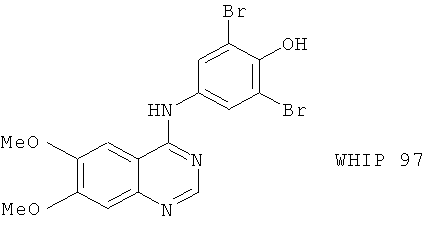
(95) WY 28342, описанный, например, в J. Med. Chem. 38, 1473 (1995)
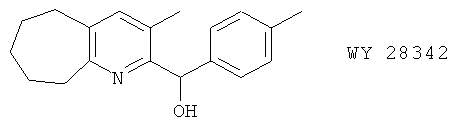
(96) WY 50295 (S-энантиомер WY 49232), описанный, например, в Eur. J. Pharmacol. 236, 217 (1993)
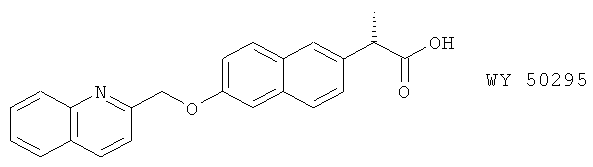
(97) ZD 2138 (синоним: ICI D 2138), описанный, например, в Asthma 95: Theory to Treatment 15 (1995) и Trends in Pharm. Sci. 13, 323 (1992)
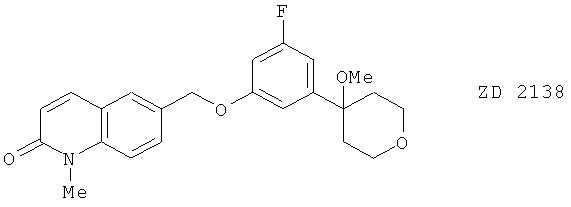
(98) ZM 230487 (синоним: ICI 230487), описанный, например, в Inpharma 660, 9 (1994)

(99) ZD 4007 and ZD 4407, описанный, например, в ЕР 0623614

(100) ZD 7717, описанный, например, в ЕР 0462813
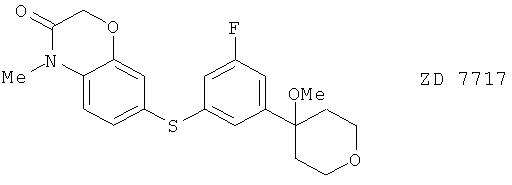
(101) ZM-216800
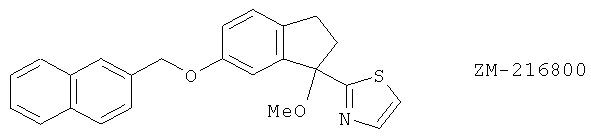
(102) CJ-12,918 и его аналоги, описанные, например, в Bioorg. Med. Chem. 11, 3879 (2003)
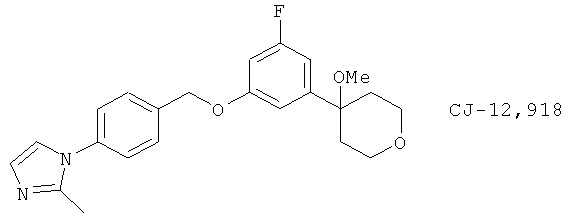
(103) Соединения, описанные в качестве смешанных ингибиторов 5-LO/СОХ-2 в Bioorg. Med. Chem. Lett. 12, 779 (2002), так же как и следующие соединения
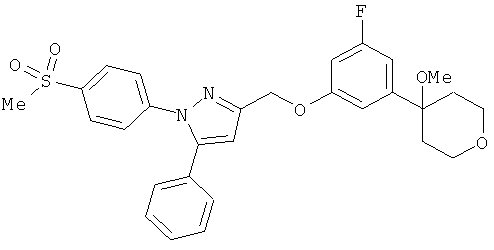
(104) АKВА (ацетил-11-кето-β-босвелловая кислота), описанная, например, в Br. J. Pharmacol. 117, 615 (1996) и Eur. J. Biochem. 256, 364 (1998)
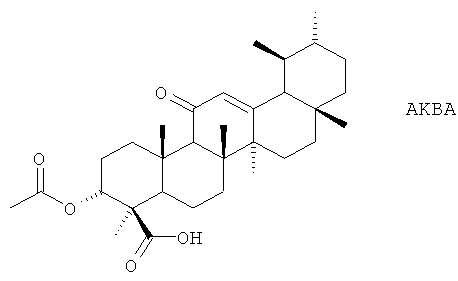
(105) Соединения, описанные в качестве двойных ингибиторов 5-LO и СОХ в Eur. J. Med. Chem. 22, 147 (1997) и Arzneimittel-Forschung (Drug Research) 35, 1260 (1985), такие как 2-ацетилтиофен-2-тиазолилгидразон (CBS-1108) и N-фенилбензамидразон

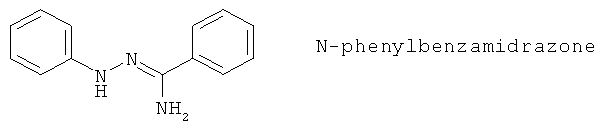
(106) Босвеллин (экстракт Boswellia serrata), описанный, например, в Fifth Chemical Congress of North America, Abstract 01/1351 (1997) и ibid. Abstract 01/1350 (1997).
(107) 2,4,6-Трийодфенол, описанный в качестве ингибитора 5-LO, например, в US 5985937.
(108) Никаравен, описанный, например, в Curr. Opin. Invest. Drugs 4, 83 (2003)
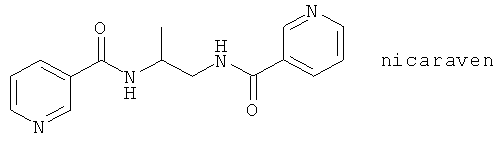
(109) Тенидап, описанный, например, в ЕР 0156603, US 4556672, Arthritis Rheum. 31, Suppl. S52 (1988) и Р. Katz et al., ibid. S52
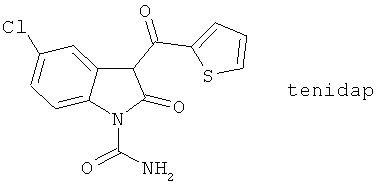
(110) Циклические гидразиды, представленные как ингибиторы 5-LO в J. Med. Chem. 39, 3938 (1996), такие как фенидон, 1-фенил-2H-тетрагидропиридазин-3-он и 1-фенилпергидро-1,2,4-тетрагидропиридазин-3-он
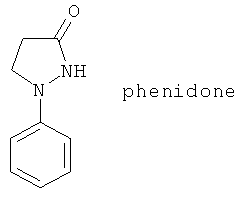


(111) ICI 207968, описанный, например, в J. Med. Chem. 34, 1028 (1991)
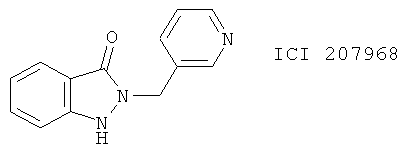
(112) ICI 211965 и другие (метоксиалкил)тиазолы, описанные, например, в J. Med. Chem. 34, 2176 (1991)
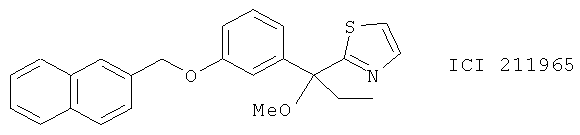
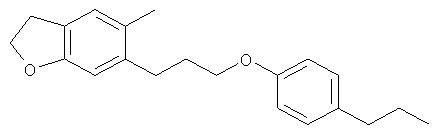
(113) 2,3-Дигидро-5-бензофуранолы, описанные в J. Med. Chem. 32, 1006 (1989), такие как следующие соединения
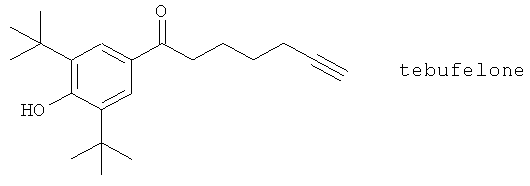
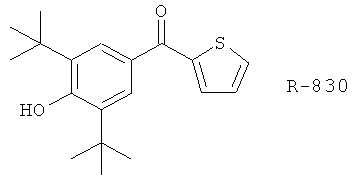
(114) Производные 2,6-ди-трет-бутилфенола, описанные в Bioorg. Med. Chem. 11, 4207 (2003), такие как тебуфелон, R-830 и S2474.
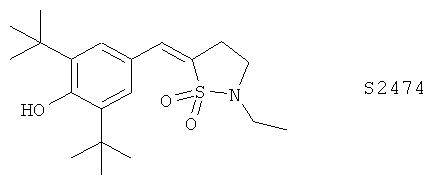
(115) 7-трет-Бутил-2,3-дигидро-3,3-диметилбензофураны, описанные в качестве ингибиторов 5-LO/СОХ-2 в J. Med. Chem. 41,1112 (1998), такие как PGV-20229
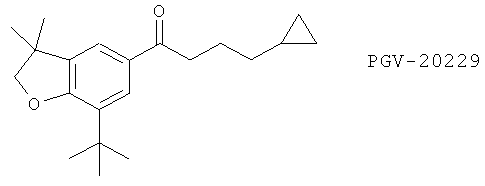
(116) Соединения, описанные как двойные ингибиторы 5-LO/СОХ в Eur. J. Med. Chem. 35, 1897 (2003), такие как следующие соединения
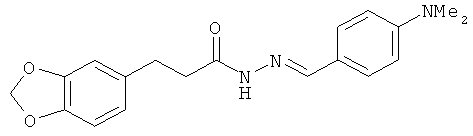
(117) Хеленалин, сесквитерпеновый лактон, который может быть выделен из некоторых представителей растений семейства Asteraceae, описанные, например, в Biochem. Pharm. 62, 903 (2001).
(118) AS-35, (9-[(4-ацетил-3-гидрокси-2-n-пропилфенокси)метил]-3-(1H-тетразол-5-ил)-4H-пиридо[1,2-а]пиримидин-4-он), описанный, например, в Int. J. Immunopharmacol. 22, 483 (2000)

(119) Магнолол, описанный, например, в Planta Medica 65, 222 (1999)

(120) Хонокиол, заимствованный из китайской традиционной медицины и описанный, например, в Arch. Allergy and lmmunol. 110, 278 (1996)

(121) Хрисаробин
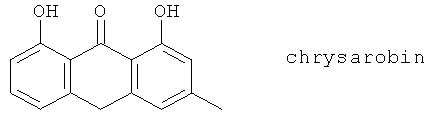
(122) Е-3040
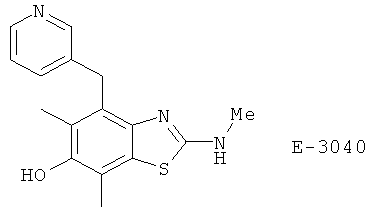
(123) Флобуфен, описанный, например, в Chirality 16, 1 (2004)
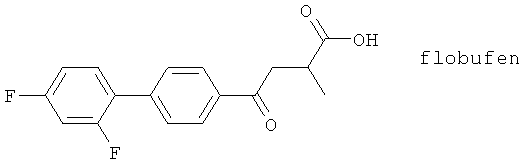
(124) YPE-01, описанный, например, в Eur. J. Pharmacol. 404, 375 (2000)
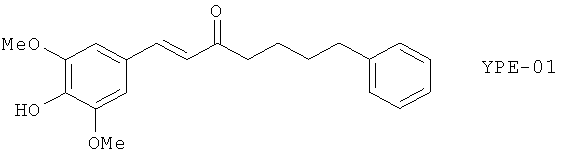
(125) BW-A137C
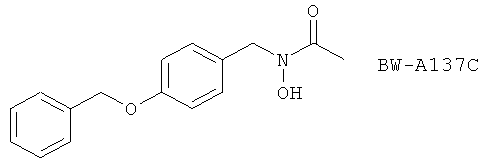
(126) LY-233569
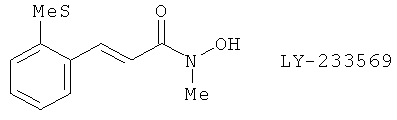
(127) PD-138387
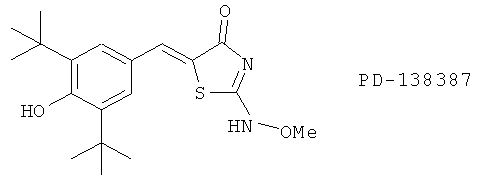
(128) SB-210661

(129) DuP-983
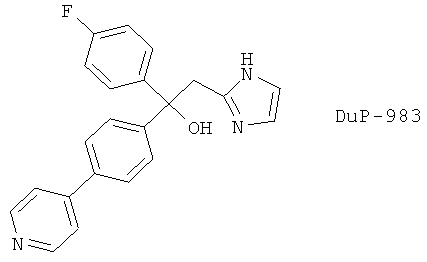
(130) BTS-71321

(131) Пирипост, описанный, например, в Toxicon. 24, 614 (1986).
(132) МK-866, описанный, например, в Eur J Pharmacol 205, 259 (1991).
(133) UCB 62045, описанный, например, в Chest 123, 371S (2003).
(134) ONO-LP-049, описанный, например, в J. Immunol. 140, 2361 (1988).
(135) 3323W, L-697198, L-7080780, FR-122788, CMI-206, FPL-64170, PD-089244 и обычно применяемые соли этих соединений.
Предпочтительные ингибиторы 5-липогеназы включают зилеутон или более точно азеластин.
Другие специфические ингибиторы 5-LO, которые могут быть упомянуты, включают ингибиторы, описанные в обзорных статьях Prog. Med. Chem., G. P. Ellis and D. K. Luscombe, Elsevier 29,1 (1992) и J. Med. Chem. 14, 2501 (1992).
Специфические ингибиторы FLAP, которые могут быть упомянуты, включают следующие.
(a) L-674,573 и соответствующие ингибиторы FLAP (например, L-655,238), описанные, например, в Mol. Pharmacol. 40, 22 (1991)

(b) L-674,636, описанный, например, в J. Med. Chem. 38, 4538 (1995)
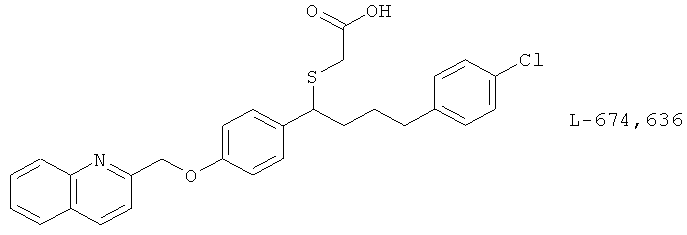
(с) L-689,037 и фотоаффинные аналоги [125I]-669,083 и [125I]-691,678, описанные, например, в Mol. Pharmacol. 41, 267 (1992)
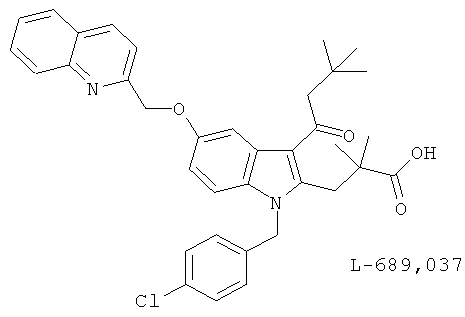
(d) L-705,302, описанный, например, в J. Med. Chem. 38, 4538 (1995)
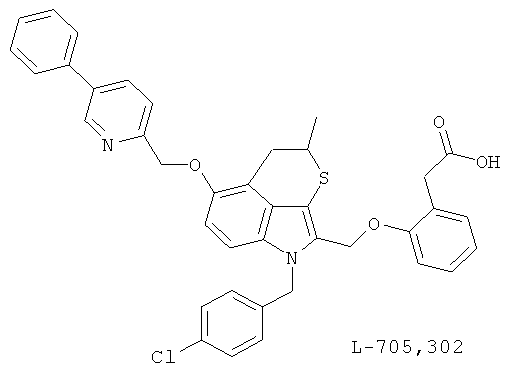
(е) МK-886 (синонимы: L663536, МK 0886), описанный, например, в US 5081138, Am. Rev. Resp. Dis. 147. 839 (1993), Eur. J. Pharmacol. 267, 275 (1994), The Search for Anti-Inflammatory Drug. 233 (1995) Eds.: V.J.Merluzzi and J. Adams, Boston, Birkhauser
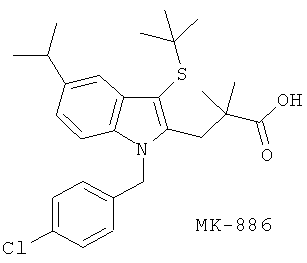
(f) Соединения, структурно родственные с МK-886, описанные, например, в WO 93/16069, US 5308850 and WO 94/13293.
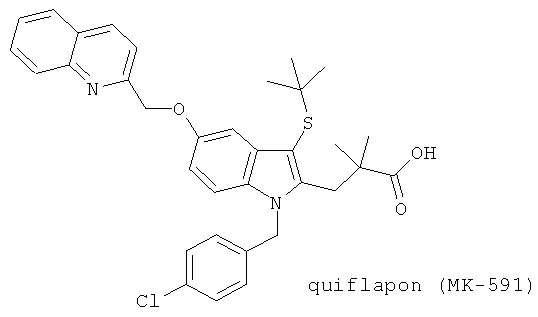
(g) Кифлапон (синонимы: MK-591, L 686708), описанный, например, в J. Physiol. Pharmacol. 70, 799 (1992) и J. Lipid Mediators 6, 239 (1993)
(h) BAY X 1005, описанный, например, в Thorax 52, 342 (1997)
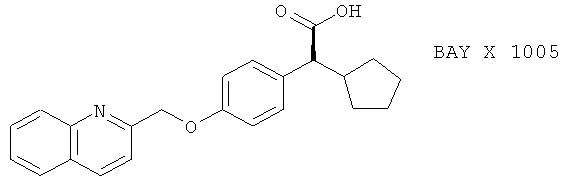
(i) BAY Y 105, описанный, например, в Arthritis and Rheumatism 39, 515 (1996) и Drug & Market Devel. 7, 177 (1996)
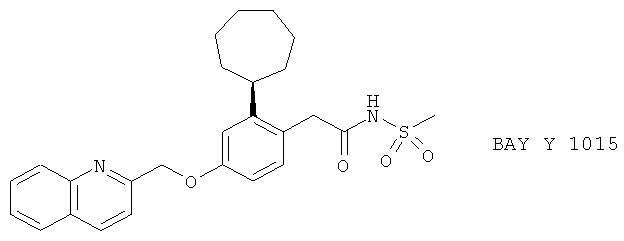
(j) VML 530 (синоним: АВТ 080), описанный, например, в Pharmacologist 39, 33 (1997)
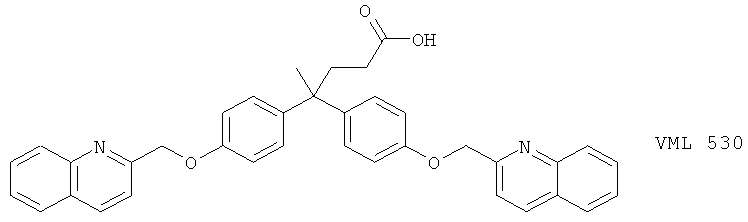
и обычно применяемые соли этих соединений.
Ингибиторы LTA4-гидролазы, которые могут быть упомянуты, следующие.
(А) Соединения, представленные как ингибиторы LTA4-гидролазы в US 5455271 и WO 94/00420, например
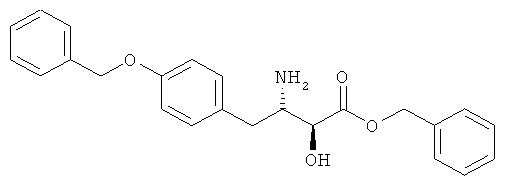
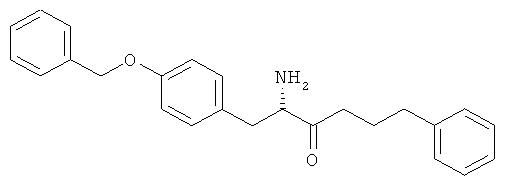
(В) Соединения, представленные как ингибиторы LTA4-гидролазы в J. Med. Chem. 36, 211 (1993) и J. Am. Chem. Soc. 114, 6552 (1992), такие как следующие соединения
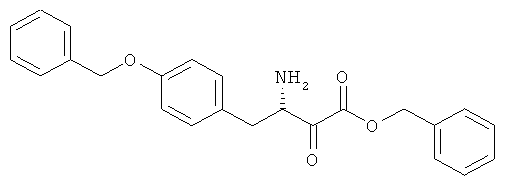
(C) Соединения, которые определяются способом, в соответствии с пунктом 24 формулы изобретения WO 00/50577.
(D) Соединения, представленные как ингибиторы LТА4-гидролазы в US 6506876, такие как SC-56938

(Е) Аналоги SC-56938, описанные, например, в Bioorg. Med. Chem. Lett. 12, 3383 (2002).
(F) Соединения, представленные как ингибиторы LTA4-гидролазы в US 5719306, например
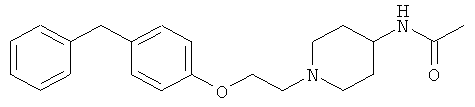
(G) Соединения, представленные как ингибиторы LTA4-гидролазы в WO 96/11192, такие как
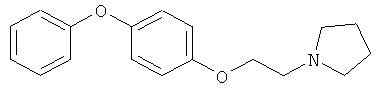
(Н) Соединения, представленные как ингибиторы LTA4-гидролазы в US 6265433 и WO 98/40364, например
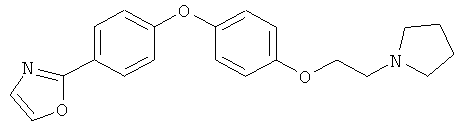
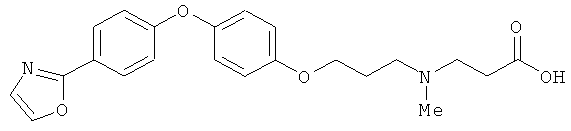
(I) Соединения, представленные как ингибиторы LTA4-гидролазы в US 6506876 и WO 96/10999, такие как
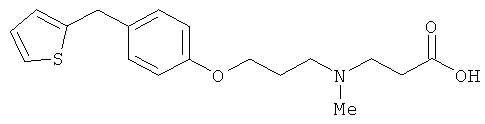
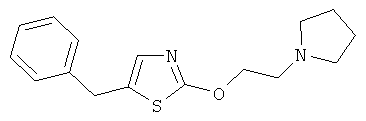
(J) Соединения, представленные как ингибиторы LTA4-гидролазы в WO 98/40370, такие как
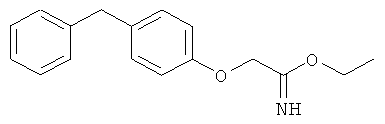
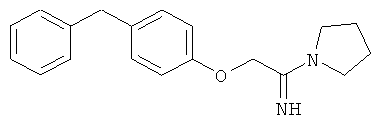
(K) Соединения, представленные как ингибиторы LТА4-гидролазы в WO 98/40354.
(L) Соединения (3-оксиранилблензойные кислоты), представленные как ингибиторы LTA4-гидролазы в ЕР 0360246, такие как
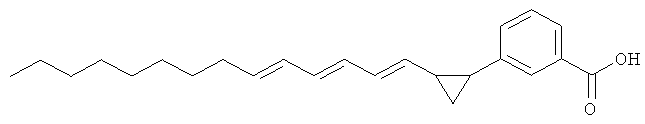
(М) Производные 20,20,20-трифторлейкотриена В4, описанные, например, в JP 01211549 А2, такие как следующие соединения
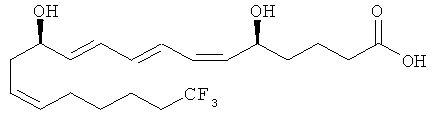
(N) Соединения, представленные как ингибиторы LTA4-гидролазы в ЕР 1165491 и WO 00/059864, такие как 2-амино-6-(4-бензилфенокси)гексановая кислота
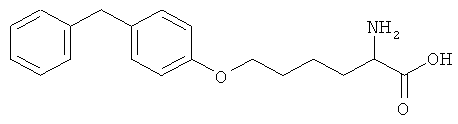
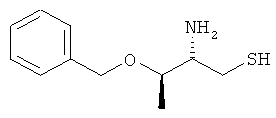
(О) Соединения, представленные как ингибиторы LTA4-гидролазы в US 6436973 и WO 00/017133, такие как (2S,3R)-2-амино-3-(бензилокси)бутан-1-тиол
(Р) Соединения, представленные как ингибиторы LTA4-гидролазы в Bioorg. Med. Chem. 3, 969 (1995), такие как
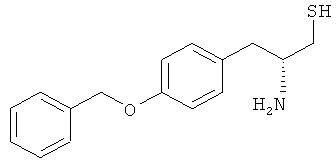
(Q) [4-(ω-Арилалкил)фенил]алкановые кислоты, представленные как ингибиторы LTA4-гидролазы в DE 4121849 А1, такие как
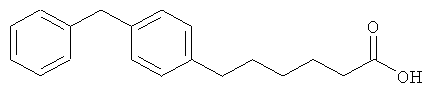
(R) Аралкилтиенилалканоаты, представленные как ингибиторы LTA4-гидролазы в DE 4118173 А1, такие как

(S) ω-[(4-Арилалкил)тиен-2-ил]алканоаты, представленные как ингибиторы LTA4-гидролазы в DE 4118014 А1, такие как:
 .
.
(Т) Соединения, представленные как ингибиторы LTA4-гидролазы в J. Med. Chem. 35, 3156 (1992), такие как RP64966
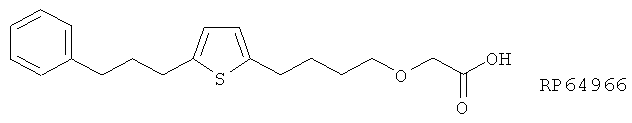
(U) Соединения, структурно связанные с RP66153 и описанные в J. Med. Chem. 35, 3170 (1992).
(V) 2-Гидроксифенилзамещенные изоксазолы, представленные как ингибиторы LTA4-гидролазы в DE 4314966 А1, такие как

(W) Бестатин, описанный, например, в J. Nat. Cancer Institute 95, 1053 (2003)

(X) SC-22716 (1-[2-(4-Фенилфенокси)этил]пирролидин), описанный, например, в J. Med. Chem. 43, 721 (2000)
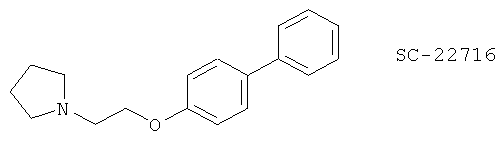
(Y) SC57461A, описанный, например, в J. Med. Chem. 45, 3482 (2002) и Curr. Pharm. Design 7, 163 (2001)
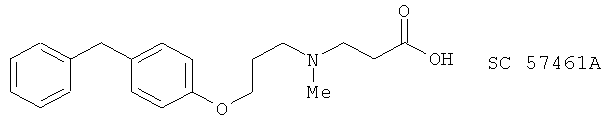
(Z) Имидазопиридины и пурины, представленные как ингибиторы LTA4-гидролазы в Bioorg. Med. Chem. Lett. 13, 1137 (2003).
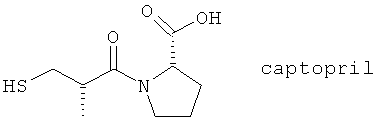
(АА) Каптоприл, описанный, например, в FASEB Journal 16, 1648 (2002)
(АВ) Производные гидроксамой кислоты, представленные как ингибиторы LTA4-гидролазы в WO 99/40910, такие как
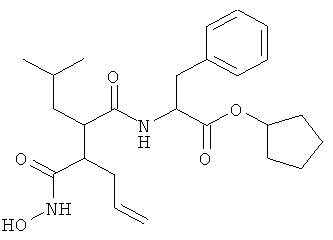
(AC) AB5366, описанный, например, в JP 11049675 А2.
(AD) SA6541, описанный, например, в WO 96/27585, Life Sci. 64, PL51-PL56 (1998) и Eur. J. Pharmacol. 346, 81 (1998)
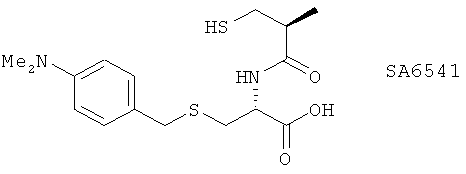
(АЕ) Соединения, содержащие N-меркаптоацилпролины, представленные как ингибиторы LTA4-гидролазы в JP 10265456 А2, такие как
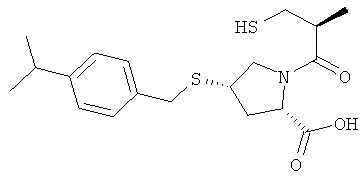
(AF) Амфотерицин В, описанный, например, в Prostaglandins, Leukotrienes and Essential Fatty Acids 58, 105 (1998)

(AG) 14,15-Дегидролейкотриен А4, описанный, например, в Biochem. J. 328, 225 (1997).
(АН) 8(S)-Амино-2(R)-метил-7-оксононановая кислота, вырабатываемая Streptomyces diastaticus и описанная, например, в J. Natural Products 59, 962 (1996)
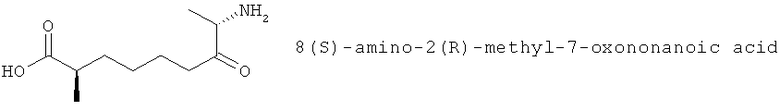
(AI) Пептид келаторфан, содержащий гидроксамовую кислоту, описанный, например, в Bioorg. Med. Chem. Lett. 5,2517 (1995).
(AJ) Амино гидроксамовые кислоты, представленные как ингибиторы LTA4-гидролазы в Bioorg. Med. Chem. 3, 1405 (1995), такие как
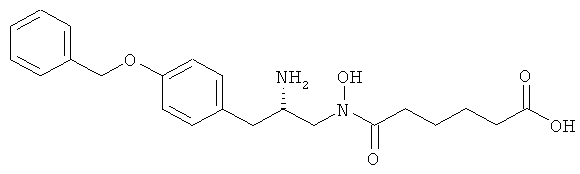
(AK) α-Кето-β-амино эфиры и тиоамины, представленные как ингибиторы LTA4-гидролазы в J. Pharmacol. Exp.Therap. 275, 31 (1995).
(AL) N-(Фенилбутаноил)лейцины, представленные как ингибиторы LTA4-гидролазы в JP 05310668 А2
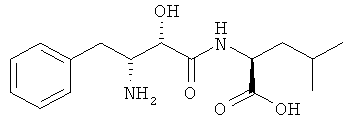
и обычно применяемые соли этих соединений.
Другие специфические ингибиторы LTA4-гидролазы, которые могут быть упомянуты, включают ингибиторы, описаны в обзорных статьях Curr. Pharm. Design 7, 163 (2001) и Curr. Med. Chem. 4,67 (1997).
Антагонисты LTB4 рецепторов (например, BLT1), которые могут быть упомянуты, включают следующие.
(i) Соединения, представленные как антагонисты LTB4 рецепторов в US 6291530, такие как (Е)-[5-(2-диэтилкарбамоил-1-метилвинил)-2-(2,6-дифтор-бензилокси) фенокси]уксусная кислота
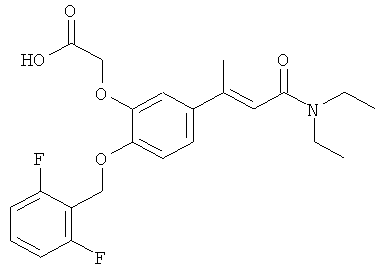
(ii) Соединения, представленные как антагонисты LTB4 рецепторов в US 2002/0128315, такие как 4-амидинофенильный эфир 4-(4-фенилпиперидинилметил)бензойной кислоты и 4-амидинофенильный эфир 4-(2-фенилимидазолилметил)бензойной кислоты
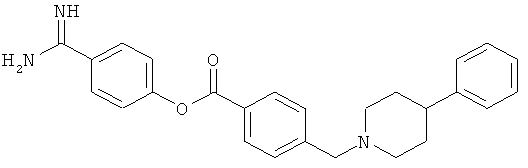
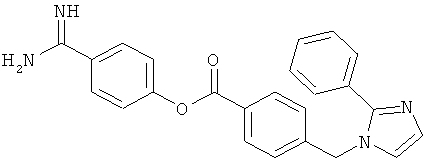
(iii) Соединения, представленные как антагонисты LTB4 рецепторов в US 2004/0053962, такие как 2-(2-пропил-3-(3-(2-этил-4-(4-фторфенил)-5-гидроксифенокси)пропокси)фенокси)бензойная кислота:
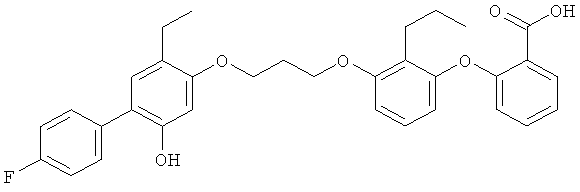
(iv) BIIL, описанный, например, в J. Pharmacol. Exp.Therap. 297, 458 (2001) и WO 02/055065
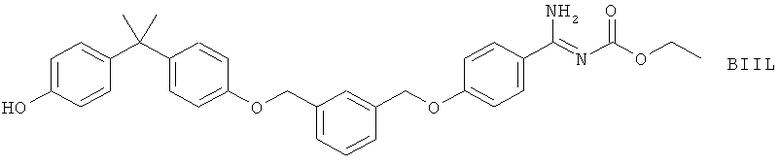
(v) CP 105696 и СР 195543, описанные, например, в J. Pharmacol. Exp. Therap. 285, 946 (1998)
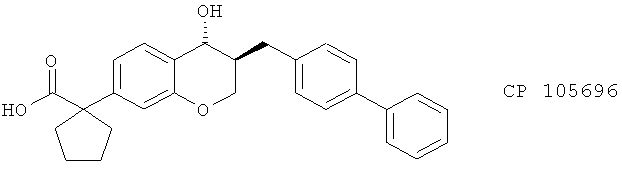
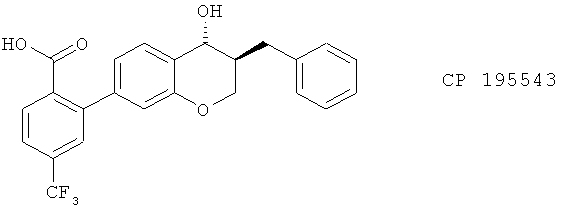
(vi) LY 210073
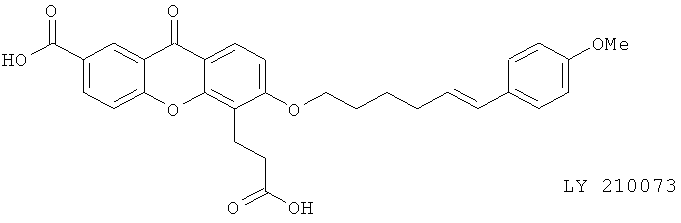
(vii) LY 223982 (синонимы: CGS 23131, SKF 107324)
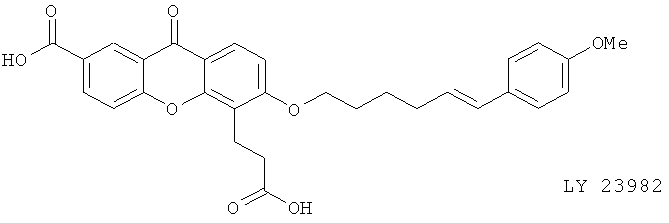
(viii) LY 255283 (синонимы: CGS 23356, LY 177455), описанный, например, в Eur. J. Pharmacol. 223, 57 (1992)
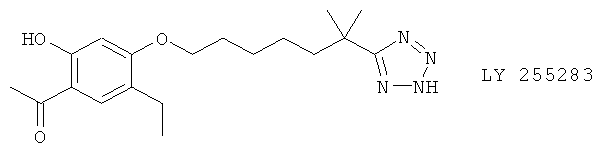
(ix) LY 292728
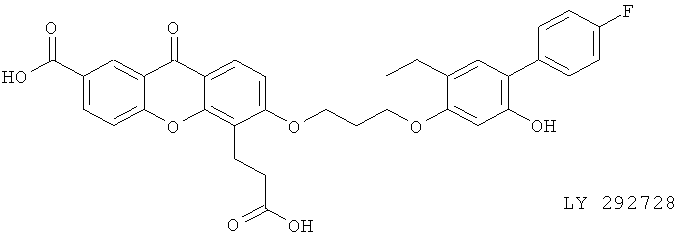
(x) LY 293111 (синоним: VML 295), описанный, например, в Drugs of the Future 21, 610 (1996), Clin. Cancer Res. 8, 3232 (2002) и WO 01/085166
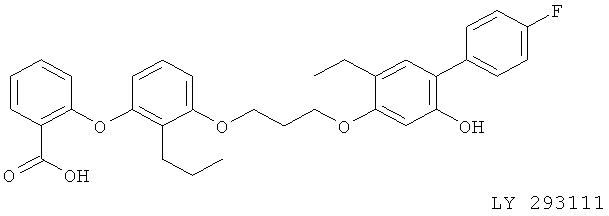
(xi) LTB 019.
(xii) Моксилубант (синоним: CGS 25019C), описанный, например, в Exp. Opin. Therap. Patents 5, 127 (1995)
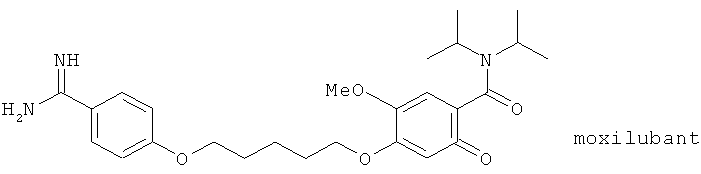
(xiii) Олопатидин (синонимы: аллелок, ALO 4943A, KW 4679, патанол®), описанный, например, в Drugs of the Future 18, 794 (1993)
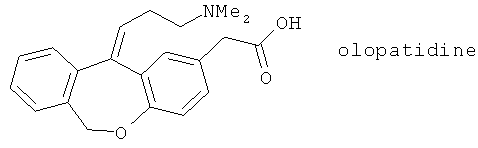
(xiv) ONO 4057 (синоним: LB 457), описанный, например, в Gastroenterology 110 (Suppl.), 110 (1996)
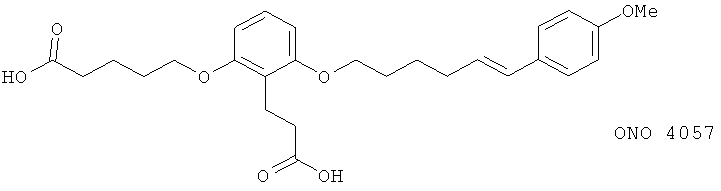
(xv) Онтазоласт (синоним: BIRM 270), описанный, например, в J. Pharm. Exp. Therap. 271, 1418 (1994)
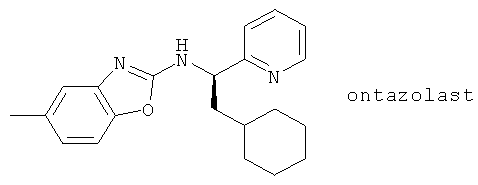
(xvi) PF 10042, описанный, например, в Eur. J. Pharmacol. - Enviromental Toxicology и Pharmacology Section 293, 369 (1995)
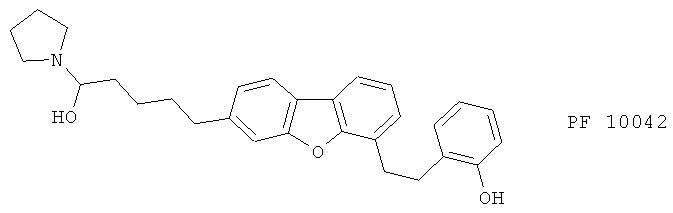
(xvii) RG 14893, описанный, например, в Pharmacologist 34, 205 (1992)
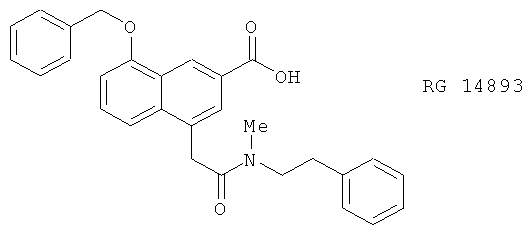
(xviii) RO 254094, описанный, например, в ISSX Proceedings 6, 232 (1994)
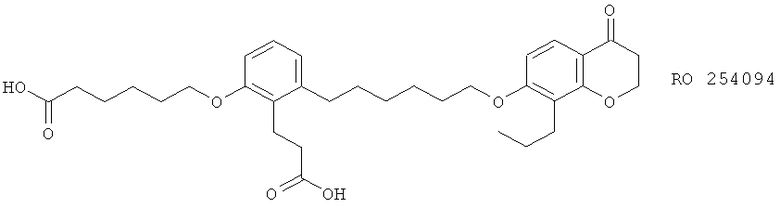
(xix) RP 66153

(xx) RP 66364

(xxi) RP 69698
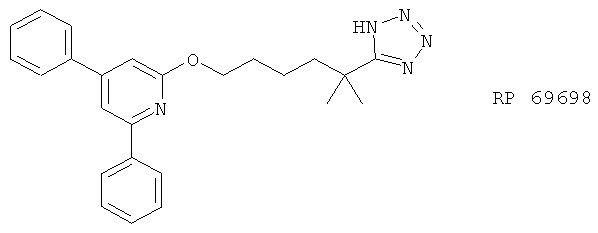
(xxii) SB 201146, описанный, например, в Thorax 53, 137 (1998)
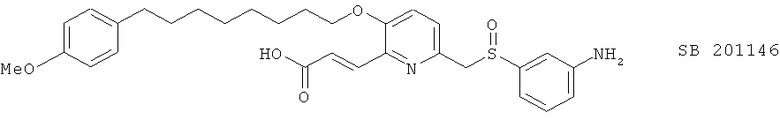
(xxiii) SB 201993, описанный, например, в J. Med. Chem. 36, 2703 (1993)
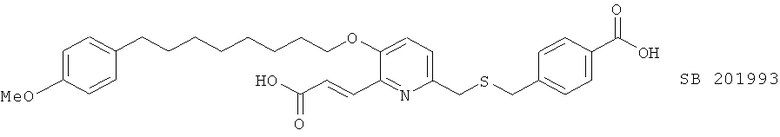
(xxiv) SC 41930, описанный, например, в J. Pharmacol. Exp. Therap. 269, 917 (1994)

(xxv) SC 50605
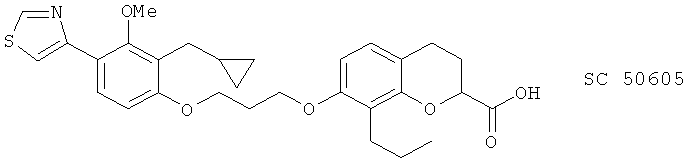
(xxvi) SC 51146
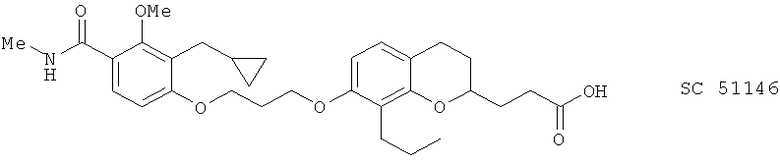
(xxvii) SC 53228, описанный, например, в Inflammation Res. 44 (Suppl. 2), 143 (1995)
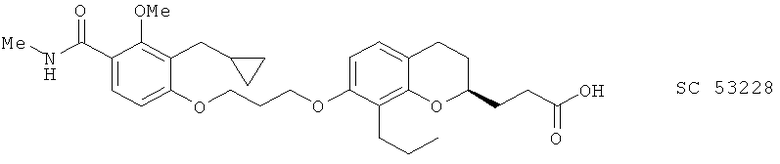
(xxviii) Тиколубант (синоним: SB 209247), описанный, например, в Adv. Prostaglandin Thromboxane and Leukotriene Res. 23, 275 (1995)
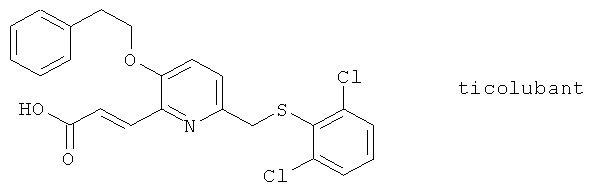
(xxix) U 75302 (синонимы: U 75485, U 77692, U 78489), описанный, например, в Adv. Prostaglandin Thromboxane and Leukotriene Res. 23, 275 (1995)
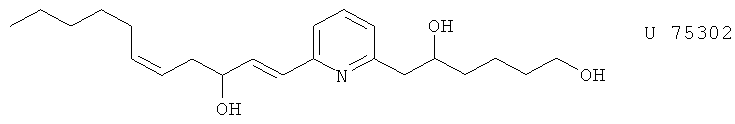
(xxx) VM 301 (синонимы: OAS 1000, псевдоптерозин А метиловый эфир), описанный, например, в Inflammation Res. 44, (Suppl. 3) 268 (1995).
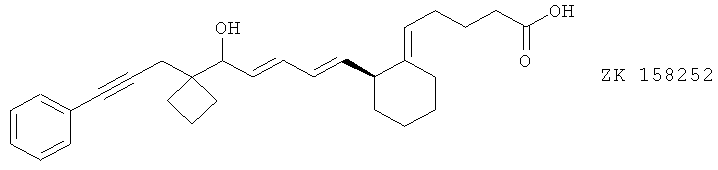
(xxxi) ZD 158252, описанный, например, в Inpharma 1094, 9 (1997).
(xxxii) ZK 158252, описанный, например, в Inpharma 1094, 9 (1997)
(xxxiii) U-75509, описанный, например, в Am. J. Physiol. Heart Circ. Physiol. 2004, Mar 11 [Электронная версия опубликована ранее].
(xxxiv) CP-105,696, описанный, например, в Br. J. Pharmacol. 139, 388 (2003).
(xxxv) LY293111, описанный, например, в Clin. Cancer Res. 8, 3232 (2002),
и обычно применяемые соли этих соединений.
Антагонисты рецепторов H1 гистамина, которые могут быть упомянуты, включают акривастин, алимемазин, анатозолин, астемизол, азатадин, азеластин, бамипин, бепотастин, бромазин, бромофенирамин, буклизин, карбиноксамин, хлорциклизин, хлорпирамин, хлорфенамин, циннаризин, клемастин, клемизол, клоцинизин, циклизин, ципрогептадин, депропин, деслоратадин, дексхлорфенирамин, дименоидринат, диметинден, диметотиазин, дифенгидрамин, пифенилпиралин, доксиламин, эбастин, эмбрамин, эмедастин, эпинастин, фексофенадин, флунаризин, гомохлорциклизин, гидроксизин, изотифендил, левокарбастин, лоратидин, мебгидролин, меклозин, мепирамин, мекитазин, метдилазин, мизоластин, ниапразин, олопатадин, оксатомид, оксомемазин, фениндамин, фенирамин, фенилтолоксамин, пиметиксен, пипингидринат, прометазин, пропиомазин, кифенадин, рупутадин, сетастин, терфенадин, тенилдиамин, тиэтилперазин, тонзиламин, толпропамин, триметобензамин, триэленамин, трипролидин, тритокалин и обычно применяемые соли этих соединений.
Активные компоненты могут быть применены в комбинации.
Любые фармацевтически пригодные соли противовоспалительных и/или антигистаминных активных компонентов, так же как в форме их свободных оснований могут применяться при приготовлении композиций изобретения. Предпочтительные соли включают ацетаты, ацетонаты, соли алюминия, соли аммония, соли аргинина, бромиды, бутираты, соли кальция, хлориды, соли холина, цитраты, соли диэтаноламина, соли диэтиламина, дипропионаты, эмбонаты, соли этаноламина, соли диэтилендиамина, формиаты, фумараты, фуораты, гидробромиды, гидрохлориды, соли имидазола, лактаты, соли лизина, соли магния, малаты, малеаты, малонаты, соли меглумина, мезилаты, соли морфолина, нитраты, фосфаты, соли пиперазина, соли калия, пропионаты, соли натрия, сукцинаты, сульфаты, тартраты, соли теоклата, пара-толуолсульфонаты, соли триэтаноламина, валераты и т.д. и/или описанные в “Handbook of Pharmaceutical Salts", Eds. Stahl and Wermuth, Wiley, 2002, Chapter 12.
Количество противовоспалительных и/или антигистаминных активных компонентов или их солей, которые могут быть применены для получения композиций изобретения, может быть определено медиком или специалистом в данной области техники, в отношении того, что будет наиболее подходящим для отдельного пациента. Желательно изменять в зависимости от природы применяемого активного ингредиента, тяжести заболевания, которое следует излечить, так же как особенности, возраст, вес, работу почек, печени и реакцию отдельного пациента, подвергнутого лечению. Однако предпочтительно, чтобы композиции изобретения содержали противовоспалительные и/или антигистаминные медикаменты или их соли в количестве около 0,1-200 мг/мл, в пересчете на свободное основание.
Общее количество активного ингредиента, который может присутствовать, может быть достаточным для обеспечения суточной дозы за одноразовый прием, подходящей для активного применяемого(ых) ингредиента(ов). Например, это может составлять около 20 µг - 200 мг. Для специалиста в данной области техники понятно, что композиции изобретения могут приниматься единовременно или несколько раз в день для обеспечения указанной суточной дозы. Предпочтительный диапазон включает около 0,1-100 (например, около 70) мг/мл и более точно около 0,2-50 мг/мл.
Вышеуказанные дозировки являются характерными для среднего пациента, конечно, могут существовать индивидуальные случаи, когда необходимы более высокие или более низкие дозы, что находится в рамках притязаний настоящего изобретения.
Термин "липосома", как легко понятно специалисту в данной области техники, включает структуру, состоящую из одной или более концентрических сфер полярных липидных двойных слоев, разделенных отделениями с водой или водным буфером.
Липосомы могут быть получены различными способами с применением растворителей, пониженного давления, двухфазного синтеза, лиофилизации, обработки ультразвуком и т.д., описанными, например, в Liposome Drug Delivery Systems, Betageri G V et al., Technomic Publishing AG, Basel, Switzerland, 1993, подходящие раскрытия из которого включены в описание ссылкой.
Термин "полярный липид", как легко понятно специалисту в данной области техники, включает любой липид с полярной концевой группой и двумя остатками жирных кислот, способный образовывать липосомы.
Полярные липиды, такие как описанные далее, могут быть природными и/или синтетическими/полусинтетическими. Смеси природных и синтетических/полусинтетических полярных липидов также могут быть применены в композициях изобретения.
Полярные липиды, которые могут быть применены в композициях изобретения, могут быть таким образом на основе, например, фосфолипидов и, в частности, фосфатидилхолина (PC), фосфатидилглицерина (PG), фосфатидилинозитола (PI), фосфатидной кислоты (РА), фосфатидилсерина (PS) и их смесей.
Фосфолипиды, которые могут быть применены в композициях изобретения, включают полярные и неполярные группы, связанные с основной цепью с гидроксильными группами, такими как глицерин.
Фосфолипиды также могут быть представлены общей формулой I
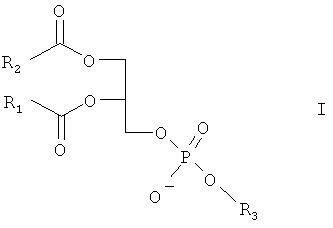
где R1 и R2 независимо представляют насыщенную или ненасыщенную (например, алкенильную), разветвленную или с прямой цепью алкильную группу с 7-23 атомами углерода, предпочтительно 11-19 атомами углерода; и R3 представляет амидную или сложноэфирную группу, такую как
-СН2-СН(ОН)-CH2OH (фосфатидилглицерин),
-СН2-СН2-N(СН3)3 (фосфатидилхолин),
-CH2-CH2-NH2 (фосфатидилэтаноламин),
-Н (фосфатидная кислота) или
-CH2-CH(NH2)-COOH (фосфатидилсерин).
Фосфолипид может быть натуральным. Природные фосфолипиды являются предпочтительно мембранными липидами, полученными из различных источников растительных (например, семян рапса, подсолнечника и т.д., предпочтительно сои) и животных (например, яичного желтка, коровьего молока и т.д.).
Фосфолипиды из сои, основного источника растительных фосфолипидов, обычно получаются из побочных продуктов (т.е. лецитинов) при очистке сырого соевого масла рафинированием. Лецитины далее перерабатывают и очищают другими физическими операциями, такими как фракционированием и/или хроматографией. Другие фосфолипиды могут быть получены, например, прессованием подходящих семян и зерен с последующей экстракцией растворителем и затем дальнейшей переработкой, как описано выше. Природные фосфолипиды, которые могут быть упомянуты, включают, например, такие, которые доступны под торговой маркой Lipoid S75, Lipoid S100 и Lipoid S75-3N (Lipoid GmbH, Germany), которые все являются смесями нескольких различных фосфолипидов, найденных в сое.
Фосфолипиды альтернативно могут быть синтетическими или полусинтетическими (т.е. полученными химическим синтезом). Например, многостадийный химический синтетический подход может быть применен для получения ключевых промежуточных фосфолипдов, 1,2-диацилглицерин, из (S)-1,2-изопропилиденглицерина, последний образует глицериновую цепь, характерную для фосфолипидов.
1,2-Диацетилированные фосфолипиды затем могут быть получены, когда соответствующие полярные концевые группы присоединяются химическим синтезом к промежуточному 1,2-диацилглицерину. Однако обычно глицерин и жирные кислоты, применяемые на различных стадиях синтеза, могут быть и натуральными и синтетическими. Синтетические и/или полусинтетические фосфолипиды, которые могут быть упомянуты, включают дилаурилфосфатидилхолин (DLPC), димиристолфосфатидилхолин (DMPC), дипальмитоилфосфатидилхолин (DPPC), дилаурилфосфатидилглицерин (DLPG), димиристолфосфатидилглицерин (DMPG), диолеоилфосфатидилхолин (DOPC) и дилеоилфосфатидилглицерин (DOPG).
Полярный липид альтернативно может содержать или более предпочтительно состоять из гликолипида. В контексте настоящего изобретения термин "гликолипид" обозначает соединение, содержащее один или более остатков моносахарида, связанных гликозидной связью с гидрофобной частью, такой как ацилглицерин, сфингоид или перамид (N-ацилсфингоид).
Гликолипид может быть гликоглицеролипидом. В контексте настоящего изобретения термин "гликоглицеролипид" обозначает гликолипид, содержащий один или более глицериновых остатков. В соответствии с предпочтительным аспектом изобретения гликоглицеролипид содержит или состоит из галактоглицеролипида, более предпочтительно из дигалактозилдиацилглицерина общей формулы II
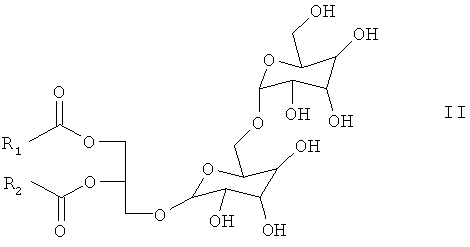
где R1 и R2 определены выше.
Альтернативно гликолипид может быть гликосфинголипидом. В контексте настоящего изобретения термин "гликосфинголипид" обозначает липид, содержащий, по меньшей мере, один моносахаридный остаток и либо сфингоид, либо церамид. Термин может таким образом включать нейтральные гликосфинголипиды, такие как моно- и олигогликозилсфингоиды, так же как олиго- и более предпочтительно моногликозилцерамиды. Термин дополнительно включает кислые гликосфинголипиды, такие как сиалогликосфинголипиды, уроногликосфинголипиды, сульфогликосфинголипиды, фосфогликосфинголипиды и фосфоногликосфинголипиды.
Сфинголипид может быть церамидом, моногексозилцерамидом, дигексозилцерамидом, сфингомиелином, лизосфингомиелином, сфингозином или их смесью. Предпочтительно гликосфинголипид является сфингомиелином или продуктами, полученными из него. Содержание сфингомиелина предпочтительно определяют хроматографическими способами. Сфингомиелин может быть выделен из молока, предпочтительно коровьего молока, головного мозга, яичного желтка или эритроцитов крови животных, предпочтительно овец. Для исключения неопределенности изобретение включает синтетические и полусинтетические сфинголипиды.
Альтернативно гликолипид может быть гликофосфатидилинозитом. В контексте настоящего изобретения термин "гликофосфатидилинозит" обозначает гликолипид, содержащий сахариды, связанные гликозидной связью с инозитной частью фосфатидилинозитов.
Предпочтительные гликолипиды включают дигалактозилдиацилглицерин (DGDG).
Предпочтительно, чтобы полярный липид был на основе фосфолипида и более предпочтительно фосфолипида, полученного из сои (например, Lipoid S100, Lipoid S75 или Lipoid S75-3N).
Предпочтительными полярными липидами (такие как фосфолипиды) являются такими, которые набухают в заметной степени в воде, и/или такие, которые способны самопроизвольно образовывать липосомы.
Если полярный (например, фосфо-) липид самопроизвольно не набухает в воде, специалист в данной области техники понимает, что тем не менее возможно получить липосомы добавлением более полярного, набухаемого (например, фосфо-) липида, такого как анионный (например, фосфо-) липид (например, фосфатидилглицерин).
Образование липосомы может быть выполнено при температуре выше около 0°С (например, комнатной температуре), если температура фазового перехода ацильной цепи (плавление цепи; переход состояния кристаллов гель-жидкость) ниже точки плавления воды.
Вне зависимости, какое липидное вещество (или их комбинация) применяется, подходящее общее количество/концентрация липида(ов), которые могут быть применены в получении композиции изобретения, составляет около 10-120 мг/мл. Композиции изобретения, которые могут быть упомянуты, включают те, в которых, когда полярный липид включает фосфолипид (либо в комбинации с другим липидом или иначе), количество фосфолипида(ов) в композиции составляет около 10 (например, около 17, например, 20) - 120 мг/мл, более предпочтительно около 25 (например, около 35) - 100 (например, около 70, например, около 50, например, около 40) мг/мл. Обычные диапазоны, которые могут быть упомянуты, включают около 25 (например, 27) - 50 мг/мл (например, 45 или более точно 35 мг/мл). Кроме того, общее количество фосфолипида (когда полярный липид содержит фосфолипид) предпочтительно находится в диапазоне около 10-80 мг (например, около 17 (например, 20) мг - 70 (например, 40) мг).
Композиции изобретения могут также содержать антиоксидант, такой как α-токоферол, аскорбиновая кислота, бутилированный гидроксианизол, бутилированный гидрокситолуол, лимонная кислота, фумаровая кислота, яблочная кислота, монотиоглицерин, пропионовая кислота, пропил галлат, аскорбат натрия, бисульфит натрия, метабисульфит натрия, метабисульфит калия, сульфит натрия, винная кислота или витамин Е. Предпочтительные антиоксиданты включают бутилированный гидрокситолуол, α-токоферол, аскорбиновую кислоту и бутилированный гидроксианизол. В соответствии с изобретением может быть применен хелатирующий агент для уменьшения катализируемого ионами металлов окисления фосфолипида и/или активного ингредиента(ов).
Примерами полезных хелатирующих агентов являются этилендиаминтетрауксусная кислота (EDTA) и ее соли (например, натрий или калий EDTA), этилендиаминтриуксусная кислота и диэтилентриаминпентауксусная кислота (DTPA). Также можно применять другие агенты для защиты от окисления композиции изобретения, в частности любые остатки ненасыщенных жирных кислот, которые могут в них присутствовать. Предпочтительные хелатирующие агенты включают EDTA и ее соли.
Композиция изобретения может включать один или более консервантов. Примерами обычных консервантов для жидких фармацевтических композиций являются хлорид бензалкония, бензойная кислота, бутилированный гидроксианизол, бутилпарабен, хлорбутанол, этилпарабен, метилпарабен, пропилпарабен, феноксиэтанол или фенилэтиловый спирт. Предпочтительный консервант включает хлорид бензалкония. Другие консерванты, которые могут быть упомянуты, включают сорбиновую кислоту.
Для удержания композиции изобретения на месте применения она также может содержать загуститель, такой как, например, гидрофильные полимеры типа полиэтиленгликоля или сшитого поливинилпирролидона, и/или, например, производные целлюлозы, такие как гидроксипропилметилцеллюлоза. Загустители также могут выступать в роли защитных коллоидов для физической стабилизации композиции изобретения до применения. Предпочтительные защитные коллоиды включают гидроксипропилметилцеллюлозу и более точно полиэтиленгликоль.
Композиции изобретения также могут содержать отдушки (например, порошки с запахом лимона, ментола или мяты перечной) и/или подсластители (например, неогесперидин).
Композиции изобретения также могут содержать агенты, модифицирующие тоничность, такие как хлорид натрия, хлорид калия, глицерин, глюкоза, гекстроза, сахароза, манит и т.д.
Необязательные добавки, включающие буферирующие вещества, консерванты, загустители, антиоксиданты, агенты, модифицирующие тоничность, и хелатирующие агенты, следует выбирать с учетом их свойств и применяемых количеств, стараясь минимизировать их отрицательный эффект на стабильность липосомы. Для определенной добавки это может быть установлено простым экспериментированием, известным специалисту в данной области техники. Подходящие количества указанных ингредиентов, однако, находятся в диапазоне около 0,01-10 мг/мл. Предпочтительно, чтобы композиции изобретения содержали, по меньшей мере, один консервант, антиоксидант, хелатирующий агент, буферирующий агент и/или загуститель. Подходящие количества любого/всех необязательных добавок составляют около 0,02-5 (например, около 3) мг/мл (например, около 0,1-2 мг/мл).
Также предложен способ получения композиций изобретения. Неожиданно было обнаружено, что липосомы могут быть получены прямым набуханием полярных липидов в водной среде без добавления любых других наполнителей, таких как заряженные липиды и/или сурфактанты и т.д., которые обычно необходимы.
В соответствии с дальнейшим аспектом изобретения предложен способ получения композиций изобретения, который включает:
(a) совместное смешивание (i) полярного липида или смеси полярных липидов, которые являются набухаемыми в водной среде, (ii) водной фазы и (iii) противовоспалительного и/или антигистаминного активного ингредиента; и
(b) гомогенизацию препарата.
Водная фаза, применяемая ранее на стадии (а), включает воду или воду, в которой растворено еще что-то (т.е. водный раствор). Водный раствор может содержать, например, буфер (vide infra). Водные растворы также могут содержать противовоспалительный и/или антигистаминный активный ингредиент (т.е. вышеуказанный компонент (iii)), в этом случае полярный липид или смесь полярных липидов добавляют к водному раствору противовоспалительного и/или антигистаминного активного ингредиента на вышеуказанной стадии (а).
Стадию (а) вышеуказанного способа предпочтительно выполняют с подходящим размешиванием (например, перемешиванием).
Предпочтительно рН препарата регулируют, например, до стадии гомогенизации (b) до желаемого значения в диапазоне около рН 4 (например, 4,0) - рН 8 (например, 8,0), предпочтительно около рН 5 (например, 5,0) - рН 7 (например, 7,0) добавлением кислоты или основания (например, соляной кислоты или гидроксида натрия подходящей концентрации (например, 1М)).
Предпочтительно воду, физиологический раствор или буферный раствор добавляют, например, до стадии гомогенизации (b) и/или после вышеуказанной стадии регулирования рН к препарату для получения желаемого финального объема партии.
Растворы/жидкости могут быть продуты азотом или аргоном на подходящей стадии вышеуказанного способа при необходимости.
В контексте настоящего изобретения липид может быть признан набухающим в водной среде, если при помещении в указанную среду он набухает в заметной степени.
Буферы предпочтительно могут быть добавлены к водному раствору медикамента (и/или медикамент может быть добавлен к водному буферному раствору) до добавления липида.
Образование липосом изобретения может быть облегчено самопроизвольным набуханием полярного липида в воде, образуя плоскую жидкокристаллическую фазу с максимальным содержанием воды около 35% масс. или выше в зависимости от природы полярного липида. В зависимости от применяемых липида или смеси липидов и других условий самопроизвольное образование липосом может быть достигнуто при добавлении избытка воды к указанной плоской фазе. Если самопроизвольное образование не достигается, образование липосом может быть достигнуто стадией механического диспергирования (т.е. стадией гомогенизации (b) вышеуказанного способа) плоской жидкокристаллической фазы в избытке воды.
Способы гомогенизации/диспергирования включают энергичное механическое перемешивание или высокоскоростную гомогенизацию, например, при помощи Ultra Turrax® (Jankel & Kuhnke, Germany). Могут также выполняться встряхивание, встряхивание с перемешиванием и раскатывание, как часть стадии гомогенизации вышеуказанного способа.
Гомогенный гранулометрический состав липосом изобретения может оказаться необходимым и может быть получен экструзией через мембранный фильтр, такой как выполненный из поликарбоната с размером пор около 100 нм. Мембранные фильтры могут быть поставляемыми Avestin Inc., Canada.
Пониженный средний размер липосом и суженный гранулометрический состав также предпочтительно могут быть получены, когда дисперсию липосомы подвергают гомогенизации при высоком давлении подходящим гомогенизатором (Rannie APV, type 7.30 VH, Rannie AS, Denmark), например, при около 300-1000 бар, например, около 400-900 бар, например, около 500-800 бар за около 4-8 (например, 7, например, 6) циклов. Установлено, что присутствие некоторых активных ингредиентов приводит к снижению размера липосомы. Липосомы меньшего размера обычно предпочтительны, поскольку они более стабильны физически и благодаря их большему отношению площадь поверхности/объем легче резорбируются слизистой оболочкой.
Предпочтительно, чтобы диаметр липосом в композициях изобретения был менее 200 нм (например, около 40-100 нм), при измерении, например, лазерной дифракцией или динамическим рассеянием света, например, как описано далее.
Кроме того, вышеуказанный способ получения композиций изобретения обычно не требует общепринятой обработки органическим растворителем, таким как хлороформ или дихлорметан. Однако, если применяют два или более мембранных липидов может быть подходящим и/или необходимым обрабатывать их органическим растворителем до добавления водного растворителя. Например, липиды могут быть растворены в летучем растворителе или смеси растворителей, таких как хлороформ или хлороформ/метанол.
Раствор затем может быть помещен в круглодонную колбу для удаления растворителя в вакуумном роторном испарителе. Избыточный объем водного буфера, содержащего медикамент, затем может быть добавлен к тонкой сухой пленке липидов, который может быть оставлен для набухания для образования липосом. В других случаях, если активный ингредиент существенно нерастворим в воде и/или фосфолипиде, может быть необходимым растворить его и фосфолипид в органическом растворителе перед добавлением водной фазы. Вновь органический растворитель может быть удален (например, в вакууме) до добавления водной фазы.
Композиции изобретения применимы в лечении всех симптомов, при которых, как известно, соответствующие активные ингредиенты эффективны, например симптомы, специально отмеченные для интересующих активных ингредиентов в Martindale "The Complete Drug Reference", 34th Edition, Royal Pharmaceutical Society (2005).
В соответствии с дальнейшим аспектом изобретения предложен способ лечения воспалительных нарушений (и/или мигрени или боли (например, острой боли) соответственно), включая назначение фармакологически эффективных количеств композиции изобретения индивиду, страдающему или чувствительному к указанным нарушениям.
Для исключения разночтений "лечение" включает терапевтическое лечение, так же как симптоматическое лечение, профилактику или диагностику состояния.
Хотя композиции изобретения могут вводиться любым известным путем, включая парентеральный, локальный и/или оральный, они могут быть введены нормально через слизистую оболочку и более точно через нос, глаза и легкие. Например, композиции изобретения могут быть введены при помощи назального аэрозоля, капель для носа и/или глазных капель. Также возможно вводить композиции изобретения в виде мелкого аэрозоля в легкие путем пульверизации. Для введения в нос могут быть применены любые подходящие устройства известного уровня техники для получения аэрозоля водной дисперсии липосом.
Указанные рецептуры могут быть приготовлены в соответствии со стандартной и/или фармацевтически приемлемой практикой.
Там где применяется слово "около" в описании в контексте размеров (например, значения рН, размеров, температуры, давления и т.д.) и количества (например, количества, веса и/или концентраций индивидуальных составляющих в композиции или компонента композиции, пропорций медикамента внутри/вне структур липосом, абсолютной дозы активного ингредиента и т.д.), понятно, что указанные переменные являются приблизительными и как таковые могут меняться на ±10%, например, ±5% и предпочтительно ±2% (например, ±1%) от чисел указанных в описании.
Композиции изобретения и вышеуказанный способ, который применяют для их приготовления, обладают преимуществами, указанными выше. В частности, композиции изобретения могут снизить показатель нежелательных неприятных побочных эффектов (в частности, раздражение), которые часто наблюдаются при, например, назальном введении рецептур.
Композиции изобретения несложны в изготовлении и дают возможность получения рецептур на основе липосом, которые находятся в форме, готовой к употреблению, устраняя необходимость разбавления перед введением.
Композиции изобретения также могут иметь преимущество в том, что они могут быть получены с применением признанных фармацевтических способов переработки и материалов, принятых для применения пищевых или фармацевтических продуктов или подобного регулятивного статуса.
Композиции изобретения также могут иметь преимущество в том, что могут быть более эффективными, менее токсичными, более длительного действия, более сильнодействующими, дающими меньше побочных эффектов, легче адсорбируемыми и/или с лучшим фармокинетическим профилем, и/или с другими полезными фармакологическими, физическими или химическими свойствами по сравнению с фармацевтическими композициями известного уровня техники при лечении ринита или другим образом.
Изобретение иллюстрируется следующими примерами.
Общая процедура. Ссылки на веса и объемы приведены далее в таблицах. Буферный раствор готовят растворением безводной лимонной кислоты и твердого гидроксида натрия в 160 мл воды (80% общего объема партии) в 200 мл мерной колбе. Добавляют взвешенное количество активного агента и растворяют при перемешивании магнитной мешалкой. Отдельно взвешивают фосфолипид и добавляют к раствору. Перемешивание продолжают до образования хорошо диспергированной суспензии, рН которой доводят до 5,0±0,1 1,0 М NaOH и/или 1,0 М НСl. Объем препарата доводят до конечного объема партии в 200 мл. Препарат помещают в гомогенизатор высокого давления (Rannie APV, type 7.30 VH, Rannie AS, Denmark) и гомогенизируют при 500-800 бар за 5 циклов.
Аликвоты полученной таким образом композиции удаляют из приемника и помещают в ампулы.
Вышеуказанная процедура применяется для приготовления конечной композиции, как отмечается далее примерами 1-8. При необходимости количества компонентов соответственно увеличиваются (например, в примерах 1-8 умножены на 200). Процедура для примера 9 описана ниже отдельно.
Пример 1
Пример 2
Пример 3
Пример 4
Пример 5
Пример 6
Пример 7
Пример 8
Пример 9
Коммерчески доступный назальный антигистамин азеластин (зарегистрированный под следующими торговыми названиями Azelvin®, Azosin®, Astelin®, Lastin® и Rhinolast®) используют в количествах и на стадиях, отмеченных далее.
1. 160 мл раствора азеластина для назального введения (Lastin®), содержащего 0,9 мг/мл азеластина, помещают в 200 мл мерную колбу.
2. Добавляют 7 г соевого фосфолипида (Lipoid S100; Lipoid GmbH, Germany) и смесь оставляют на ночь для набухания.
3. Объем доводят до 200 мл добавлением раствора азеластина (смотри стадию 1 выше).
4. Контролируют значение рН.
5. Раствор гомогенизируют за 7 циклов при 800 бар, как описано выше в общей процедуре.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РИНИТА И РОДСТВЕННЫХ ЗАБОЛЕВАНИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2006 |
|
RU2444351C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЛИПИДЫ, КОТОРЫЕ НЕСУТ ПОЛЯРНЫЙ И НЕПОЛЯРНЫЙ ФРАГМЕНТ | 2002 |
|
RU2294738C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЦИКЛОСПОРИН | 2006 |
|
RU2421209C2 |
| ВЫСУШЕННЫЕ ВОССТАНОВЛЕННЫЕ ВЕЗИКУЛЫ ДЛЯ ФАРМАЦЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2007 |
|
RU2443412C2 |
| ИНГИБИТОРЫ ЛЕЙКОТРИЕН А4-ГИДРОЛАЗЫ | 2014 |
|
RU2690489C2 |
| СРЕДСТВО НА ОСНОВЕ БИСНАФТАЗАРИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2669374C2 |
| ЛИПОСОМАЛЬНЫЙ ПРЕПАРАТ ДЛЯ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ | 2017 |
|
RU2756755C2 |
| ИНГИБИТОРЫ ЛЕЙКОТРИЕН А4-ГИДРОЛАЗЫ | 2014 |
|
RU2696559C2 |
| ФОСФОЛИПИДНАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ | 1994 |
|
RU2119791C1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ TUSC2-ИММУНОТЕРАПИИ | 2017 |
|
RU2755903C2 |
Изобретение относится к гомогенной фармацевтической композиции для лечения воспалительных нарушений, которая содержит смесь стероидного противовоспалительного или антигистаминного активного ингредиента в фармацевтически приемлемом водном носителе с липосомой. В качестве стероидного противовоспалительного ингредиента используется будезонид или флутиказон или их фармацевтически приемлемая соль, а антигистаминным препаратом является азеластин или его фармацевтически приемлемая соль, при этом концентрация активного ингредиента в водном носителе является по существу одинаковой внутри и снаружи липосомных структур и варьирует ±20% при сравнении концентрации активного ингредиента внутри и снаружи липосомных структур. Полярный липид является набухаемым в воде и представляет собой фосфолипид или гликосфинголипид. Изобретение также относится к способу получения композиции, который заключается в совместном смешивании полярного липида, водной фазы и указанного активного ингредиента и гомогенизации смеси. Изобретение также относится к способу лечения воспалительных нарушений, который включает введение заявленной композиции индивиду, страдающему от или чувствительному к указанным нарушениям. Изобретение обеспечивает уменьшение раздражения, например, при назальном введении композиции. 4 н. и 48 з.п. ф-лы, 9 пр.
1. Гомогенная фармацевтическая композиция для лечения воспалительных нарушений, содержащая смесь стероидного противовоспалительного или антигистаминного активного ингредиента в фармацевтически приемлемом водном носителе и липосому, полученную из полярного липида, который является набухающим в водной среде и выбран из группы, состоящей из дилаурилфосфатидилхолина, димиристолфосфатидилхолина, дипальмитоилфосфатидилхолина, дилаурилфосфатидилглицерина, димиристолфосфатидилглицерина, диолеоилфосфатидилхолина, диолеоилфосфатидилглицерина или моногликозилсфингоида, олигогликозилсфингоида, олигогликозилцерамида, моногликозилцерамида, сиалогликосфинголипида, уроногликосфинголипида, сульфогликосфинголипида, фосфогликосфинголипида, фосфоногликосфинголипида, церамида, моногексозилцерамида, дигексозилцерамида, сфингомиелина, лизосфингомиелина, сфингозина или их смеси,
причем стероидный противовоспалительный ингредиент выбирают из будезонида и флутиказона или их фармацевтически приемлемой соли, а антигистаминным препаратом является азеластин или его фармацевтически приемлемая соль и концентрация активного ингредиента в водном носителе является по существу одинаковой внутри и снаружи липосомных структур и варьирует ±20% при сравнении концентрации активного ингредиента внутри и снаружи липосомных структур,
а полярная липидная липосома получена путем
(a) совместного смешивания (i) указанного полярного липида или смеси полярных липидов, которые являются набухаемыми в водной среде, (ii) водной фазы, (iii) указанных противовоспалительного или антигистаминного активного ингредиента; и
(b) гомогенизации смеси.
2. Композиция по п.1, где полярный липид или смесь полярных липидов добавляют в водный раствор противовоспалительного и/или антигистаминного активного ингредиента на стадии (а).
3. Композиция по пп.1 и 2, где перед стадией гомогенизации рН доводят до желаемого значения добавлением кислоты или основания.
4. Композиция по пп.1 и 2, где перед стадией гомогенизации добавляют воду, изотонический раствор или буферный раствор к препарату для получения желаемого конечного объема партии.
5. Композиция по п.3, где перед стадией гомогенизации добавляют воду, изотонический раствор или буферный раствор к препарату для получения желаемого конечного объема партии.
6. Композиция по п.5, где добавление воды, изотонического раствора или буфера происходит после этапа доведения рН.
7. Композиция по п.1, где, по меньшей мере, один из растворов/жидкостей продувают азотом и/или аргоном.
8. Композиция по п.2, где водный раствор активного ингредиента получают либо добавлением буфера к водному раствору активного ингредиента, либо добавлением активного ингредиента к водному раствору липида.
9. Композиция по п.1, где, если применяются полярные липиды, то они предварительно обрабатываются органическим растворителем.
10. Композиция по п.1, где, если активный ингредиент недостаточно растворим в воде, то он предварительно обрабатывается органическим растворителем (совместно с липидом).
11. Композиция по п.1, где стадия (b) гомогенизации включает энергичное перемешивание, высокоскоростную гомогенизацию, встряхивание, встряхивание с перемешиванием и/или растирание.
12. Композиция по п.1, где способ ее получения включает дополнительную стадию снижения размера липосомы.
13. Композиция по п.12, где стадия снижения размера липосомы включает экструзию через мембранный фильтр.
14. Композиция по любому из пп.1, 2 или 13, где стадии гомогенизации и/или снижения размера включают гомогенизацию при высоком давлении.
15. Композиция по п.1, которая дополнительно содержит фармацевтически приемлемый буфер, способный обеспечивать рН в интервале 4-8.
16. Композиция по п.15, в которой значение рН равно 5-7.
17. Композиция по п.15 или 16, в которой буфером является фосфатный, цитратный или ацетатный буфер.
18. Композиция по п.17, в которой буфером является двузамещенный фосфат натрия, двузамещенный фосфат калия, однозамещенный фосфат натрия, однозамещенный фосфат калия, фосфорная кислота плюс основание, цитрат натрия, лимонная кислота плюс основание, ацетат натрия или уксусная кислота плюс основание.
19. Композиция по п.15, в которой количество буфера находится в диапазоне 1-30 мг/мл.
20. Композиция по п.1, в которой полярная липидная липосома образована из полярного липида, который является природным, синтетическим/полусинтетическим или включает смесь обоих.
21. Композиция по п.1, в которой фосфолипид представляет собой Lipoid S75, Lipoid S100 и/или Lipoid S75-3N.
22. Композиция по п.1, в которой количество применяемого для образования липосом полярного липида находится в диапазоне 10-120 мг/мл.
23. Композиция по п.1, в которой количество фосфолипида в композиции составляет 17-70 мг/мл.
24. Композиция по п.22, в которой количество полярного липида составляет 20-40 мг/мл.
25. Композиция по любому из предшествующих пунктов, которая дополнительно содержит антиоксидант.
26. Композиция по п.25, в которой антиоксидантом является α-токоферол, аскорбиновая кислота, бутилированный гидроксианизол, бутилированный гидрокси-толуол, лимонная кислота, фумаровая кислота, яблочная кислота, монотиоглицерин, пропионовая кислота, пропил галлат, аскорбат натрия, бисульфит натрия, метабисульфит натрия, метабисульфит калия, сульфит натрия, винная кислота и/или витамин Е.
27. Композиция по п.1, которая дополнительно содержит хелатирующий агент.
28. Композиция по п.27, в которой хелатирующим агентом является этилендиаминтетрауксусная кислота (и/или ее соли), этилендиаминтриуксусная кислота и/или диэтилентриаминпентауксусная кислота.
29. Композиция по п.1, которая дополнительно содержит консервант.
30. Композиция по п.29, в которой консервантом является хлорид бензалкония, бензойная кислота, бутилированный гидроксианизол, бутапарабен, хлорбутанол, этилпарабен, метилпарабен, пропилпарабен, феноксиэтанол и/или фенилэтиловый спирт.
31. Композиция по любому из предшествующих пунктов, которая дополнительно содержит загуститель.
32. Композиция по п.31, в которой загустителем является полиэтиленгликоль, сшитый поливинилпирролидон и/или гидроксипропилметил целлюлоза.
33. Композиция по п.1, в которой диаметр липосом равен менее 200 нм.
34. Композиция по п.33, в которой диаметр составляет 40-100 нм.
35. Способ получения композиции по любому из предыдущих пунктов, который включает:
(a) совместное смешивание (i) полярного липида или смеси полярных липидов, которые являются набухаемыми в водной среде, (ii) водной фазы и (iii) стероидного противовоспалительного или антигистаминного активного ингредиента, определенных в п.1; и
(b) гомогенизацию препарата.
36. Способ по п.35, в котором полярный липид или смесь полярных липидов добавляют в водный раствор противовоспалительного и/или антигистаминного активного ингредиента на стадии (а).
37. Способ по пп.35 и 36, в котором перед стадией гомогенизации рН доводят до желаемого значения добавлением кислоты или основания.
38. Способ по п.35, в котором перед стадией гомогенизации добавляют воду, изотонический раствор или буферный раствор к препарату для получения желаемого конечного объема партии.
39. Способ по п.38, в котором перед стадией гомогенизации добавляют воду, изотонический раствор или буферный раствор к препарату для получения желаемого конечного объема партии.
40. Способ по пп.39 и 40, в котором добавление воды, изотонического раствора или буферного раствора происходит после этапа доведения рН.
41. Способ по п.35, в котором, по меньшей мере, один из растворов/жидкостей продувают азотом и/или аргоном.
42. Способ по п.36, в котором водный раствор активного ингредиента получают либо добавлением буфера к водному раствору активного ингредиента, либо добавлением активного ингредиента к водному раствору липида.
43. Способ по п.35, в котором стадия (b) гомогенизации включает энергичное перемешивание, высокоскоростную гомогенизацию, встряхивание, встряхивание с перемешиванием и/или растирание.
44. Способ по п.35, который включает дополнительную стадию снижения размера липосом.
45. Способ по п.44, в котором стадия снижения размера включает экструзию через мембранный фильтр.
46. Способ по п.1 или 44, в котором стадии гомогенизации и/или снижения размера включают гомогенизацию при высоком давлении.
47. Способ лечения воспалительных нарушений, включающий введение композиции по любому из пп.1-34, индивиду, страдающему от или чувствительному к указанным нарушениям.
48. Применение композиции по любому из пп.1-34 для изготовления медикамента для лечения воспалительных нарушений, которое включает введение композиции индивиду, страдающему от или чувствительному к указанным нарушениям.
49. Способ по п.47, в котором воспалительным нарушением является ринит.
50. Применение по п.48, при котором воспалительным нарушением является ринит.
51. Способ по п.47, в котором воспалительным нарушением является астма.
52. Применение по п.48, при котором воспалительным нарушением является астма.
| K.IWANAGA et al., Usefulness of liposomes as an dosage formulation for topical drug application., Biol | |||
| Pharm | |||
| Bull., 2000, N.23, V.3, p.p.323-326 | |||
| US 4839175 A, 13.06.1989 | |||
| E.Abber A.W | |||
| et al., Hydroxyzine from topical phospholipid liposomal formulations: evaluation of antihistaminic activity and systemic absorbtion in a rabbit model., Aaps |
Авторы
Даты
2012-12-10—Публикация
2006-06-08—Подача