Изобретение относится к ионогенным мономерам и способу их получения, которые могут быть использованы для синтеза водорастворимых полиэлектролитов.
Известны мономерные системы производных диаллиламина и четвертичных аммониевых оснований диаллильной природы, полученные на основе хлористого аллила и производных диаллиламина [1-4], на основе которых были получены полиэлектролиты с невысокими значениями молекулярных масс. В работе [5] авторами было показано, что основные и кислые аминокислоты не реагируют с бромистым аллилом и не образуют продукты замещения.
В качестве наиболее близкого аналога принят патент США №3457302, из которого известен N,N-диаллилглицин (C8H13NO2) и его способ получения третичной аминокислоты, синтезированный взаимодействием 0.8-1.2 моля щелочи на моль галоидзамещенной карбоновой кислоты в полярном растворителе. Смесь 18.9 ч. хлоруксусной кислоты и 58.2 ч. диаллиламина нагревают в атмосфере азота при 100°С в течение 16 часов, охлаждают до 20°С, прибавляют раствор 11.2 ч. KОН в 200 ч. МеОН, встряхивают 5 мин, фильтруют, фильтрат упаривают в вакууме, остаток растворяют в 300 ч. СНСl3, фильтруют и получают диаллилглицин.
Недостатком метода получения являются необходимость проведения реакции в атмосфере азота при 100°С в течение 16 часов, затем обработки метиловым раствором едкого калия, после добавления раствора щелочи, фильтрат необходимо упаривать в вакууме и остаток растворять в хлороформе.
Задачей изобретения является синтез мономера диаллильной природы, в молекулах которых содержатся как отрицательно заряженные, так и положительно заряженные функциональные группы, которые способны вступать в реакции радикальной полимеризации для получения новых полиэлектролитов с регулируемым кислотно-основным и гидрофильно-гидрофобным балансом, а также упрощение способа. Поставленная задача решается получением нового мономера формулы (C10H15NO4):
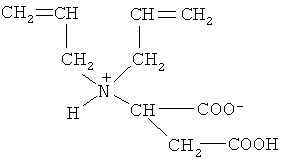
имеющий элементный состав (табл.1).
Элементный состав N,N-диаллиласпарагиновой кислоты (ДААсК).
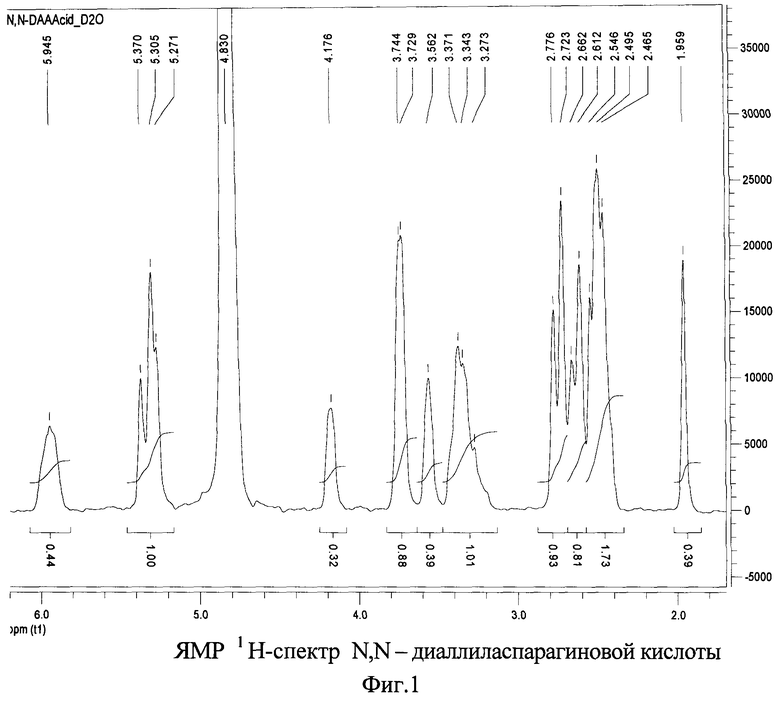
Структура синтезированного мономера- N,N- диаллиламиноэтановой кислоты подтвержден 1Н-ЯМР спектроскопией (фиг.1, табл.2).
Данные 1Н-ЯМР спектроскопии в D2O.
Сущность способа заключается в том, что в водно-спиртовом растворе α-аспарагиновую кислоту превращают в натриевую соль воздействием раствора щелочи, затем при температуре 0-5°С прикалывают хлористый аллил в течение 15-30 мин, температуру синтеза доводят до 60-75°С и синтез проводят при данной температуре в течение 3-5 часов, что приводит к получению N,N-диаллиласпарагиновой кислоты (ДААсК). После окончания реакции реакционную смесь постепенно вливают в сухой ацетон порциями. N,N-диаллиласпарагиновая кислота в виде хлопьев собирается на поверхности ацетона, при этом соли выпадают в осадок. Хлопья отсасывают на воронке Бюхнера, тщательно промывают сухим ацетоном, затем в эксикаторе сушат над оксидом фосфора (V) до постоянного веса.
Пример 1. В четырехгорлую колбу, снабженную мешалкой, термометром, капельной воронкой и обратным холодильником с насадкой для использования сухого льда в ацетоне, вносят 21.42 г (1 моль) α-аспарагиновой кислоты, растворяют в 45 мл воды и добавляют 45 мл изопропилового спирта, затем прикалывают 8 мл 50%-ного раствора гидроксида натрия. Реакционную смесь охлаждают до 0°С, для отвода избыточного тепла используют водяную баню со льдом. Затем прикалывают медленно 16.32 мл (2 моль) хлористого аллила в течение 15 мин. После добавления 16 мл 50%-ного раствора гидроксида натрия реакционную массу медленно подогревают до 60°С, выдерживают в течение 3 часов. После окончания реакции реакционную смесь постепенно вливают в сухой ацетон порциями. N,N-диаллиласпарагиновая кислота в виде хлопьев собирают на поверхности ацетона, при этом соли выпадают в осадок. Хлопья отсасывают на воронке Бюхнера, тщательно промывают сухим ацетоном, затем в эксикаторе сушат над оксидом фосфора (V) до постоянного веса. N,N-диаллиласпарагиновая кислота - мономер светло-желтого цвета. Мономер плавится с разложением при 292±2°С (Тпл α-аминоаспарагиновой кислоты 270°С с разложением). Выход мономера 65%.
Пример 2. В четырехгорлую колбу, снабженную мешалкой, термометром, капельной воронкой и обратным холодильником с насадкой для использования сухого льда в ацетоне, вносят 21.42 г (1 моль) α-аспарагиновой кислоты, растворяют в 45 мл воды и добавляют 45 мл изопропилового спирта, затем прикалывают 8 мл 50%-ного раствора гидроксида натрия. Реакционную смесь охлаждают до 5°С, для отвода избыточного тепла используют водяную баню со льдом. Затем прикалывают медленно 16.32 мл (2 моль) хлористого аллила в течение 15 мин. После добавления 16 мл 50%-ного раствора гидроксида натрия реакционную массу медленно подогревают до 60°С, выдерживают в течение 3 часов. После окончания реакции реакционную смесь постепенно вливают в сухой ацетон порциями. N,N-диаллиласпарагиновая кислота в виде хлопьев собираются на поверхности ацетона, при этом соли выпадают в осадок. Хлопья отсасывают на воронке Бюхнера, тщательно промывают сухим ацетоном, затем в эксикаторе сушат над оксидом фосфора (V) до постоянного веса. N,N-диаллиласпарагиновая кислота - мономер светло-желтого цвета. Мономер плавится с разложением при 292±2°С (Тпл α-аспарагиновой кислоты 270°С с разложением). Выход мономера 55%.
Пример 3. В четырехгорлую колбу, снабженную мешалкой, термометром, капельной воронкой и обратным холодильником с насадкой для использования сухого льда в ацетоне, вносят 21.42 г (1 моль) α-аспарагиновой кислоты, растворяют в 45 мл воды и добавляют 45 мл изопропилового спирта, затем прикалывают 8 мл 50%-ного раствора гидроксида натрия. Реакционную смесь охлаждают до 5°С, для отвода избыточного тепла используют водяную баню со льдом. Затем прикалывают медленно 16.32 мл (2 моль) хлористого аллила в течение 30 мин. После добавления 16 мл 50%-ного раствора гидроксида натрия реакционную массу медленно подогревают до 75°С, выдерживают в течение 5 часов. После окончания реакции реакционную смесь постепенно вливают в сухой ацетон. N,N-диаллиласпарагиновая кислота в виде хлопьев собираются на поверхности ацетона, при этом соли выпадают в осадок. Хлопья отсасывают на воронке Бюхнера, тщательно промывают сухим ацетоном, затем в эксикаторе сушат над оксидом фосфора (V) до ···постоянного веса. N,N-диаллиламиноэтановая кислота - мономер светло-желтого цвета. Мономер плавится с разложением при 292±2°С (Тпл α-аспарагиновой кислоты 270°С с разложением). Выход мономера 65%.
Пример 4. В четырехгорлую колбу, снабженную мешалкой, термометром, капельной воронкой и обратным холодильником с насадкой для использования сухого льда в ацетоне, вносят 21.42 г (1 моль) α-аспарагиновой кислоты, растворяют в 45 мл воды и добавляют 45 мл изопропилового спирта, затем прикалывают 8 мл 50%-ного раствора гидроксида натрия. Реакционную смесь охлаждают до 0°С, для отвода избыточного тепла используют водяную баню со льдом. Затем прикалывают медленно 16.32 мл (2 моль) хлористого аллила в течение 30 мин. После добавления 16 мл 50%-ного раствора гидроксида натрия реакционную массу медленно подогревают до 75°С и выдерживают в течение 5 часов. После окончания реакции реакционную смесь постепенно вливают в сухой ацетон порциями. N,N-диаллиласпарагиновая кислота в виде хлопьев собираются на поверхности ацетона, при этом соли выпадают в осадок. Хлопья отсасывают на воронке Бюхнера, тщательно промывают сухим ацетоном, затем в эксикаторе сушат над оксидом фосфора (V) до постоянного веса. N,N-диаллиласпарагиновая кислота - мономер светло-желтого цвета. Мономер плавится с разложением при 292±2°С (Тпл α-аспарагиновой кислоты 270°С с разложением). Выход мономера 75%.
Ниже приводимыми примерами подтверждаем возможность получения водорастворимого полиэлекторлита из N,N-диаллиласпарагиновой кислоты путем реакции радикальной полимеризации в присутствии персульфата аммония в качестве радикального инициатора.
Пример 1. В одногорлую колбу, снабженную мешалкой, термометром, обратным холодильником, помещают 1.55 г (1 моль) N,N-диаллиласпарагиновой кислоты, 10 мл бидистиллированной воды и 5.0·10-3моль/л (0.00114 г) персульфата аммония (ПСА). Реакционную смесь нагревали при температуре 80°С в течение 8 часов. После окончания реакции реакционную смесь постепенно вливают в сухой ацетон порциями. Поли-N,N-диаллиласпарагиновая кислота в виде хлопьев выпадает в осадок. Хлопья отфильтровывают на воронке Бюхнера, тщательно промывают сухим ацетоном, затем в эксикаторе сушат над оксидом фосфора (V) до постоянного веса. Поли-N,N- диаллиласпарагиновая кислота - полимер светло-желтого цвета с разложением при 330±2°С. Выход полимера 65%, ηприв.=0.15 дл/г (0.5 N растворе NaCl).
Пример 2. В одногорлую колбу, снабженную мешалкой, термометром, обратным холодильником, помещают 3.10 г (2 моль) N,N-диаллиласпарагиновой кислоты, 10 мл бидистиллированной воды и 1.0·10-2 моль/л (0.00228 г) персульфата аммония (ПСА). Реакционную смесь нагревали при температуре 60°С в течение 5 часов. После окончания реакции реакционную смесь постепенно вливают в сухой ацетон порциями. Поли-N,N-диаллиласпарагиновая кислота в виде хлопьев выпадает в осадок. Хлопья отфильтровывают на воронке Бюхнера, тщательно промывают сухим ацетоном, затем в эксикаторе сушат над оксидом фосфора (V) до постоянного веса. Поли-N,N- диаллиласпарагиновая кислота - полимер светло-желтого цвета с разложением при 330±2°С. Выход полимера 70%, ηприв.=0.19 дл/г (0.5 N растворе NaCl).
Пример 3. В одногорлую колбу, снабженную мешалкой, термометром, обратным холодильником, помещают 3.10 г (2 моль) N,N-диаллиласпарагиновой кислоты, 10 мл бидистиллированной воды и 1.0·10-2 моль/л (0.00228 г) персульфата аммония (ПСА). Реакционную смесь нагревали при температуре 80°С в течение 8 часов. После окончания реакции реакционную смесь постепенно вливают в сухой ацетон порциями. Поли-N,N-диаллиласпарагиновая кислота в виде хлопьев выпадает в осадок. Хлопья отфильтровывают на воронке Бюхнера, тщательно промывают сухим ацетоном, затем в эксикаторе сушат над оксидом фосфора (V) до постоянного веса. Поли-N,N- диаллиласпарагиновая кислота - полимер светло-желтого цвета с разложением при 330±2°С. Выход полимера 70%, ηприв.=0.25 дл/г (0.5 N растворе NaCl).
Технический результат изобретения заключается в синтезе мономера диаллильной природы, который обладает высокой активностью в реакциях радикальной полимеризации, в молекулах которых содержатся как отрицательно заряженные, так и положительно заряженные функциональные группы, для получения новых полиэлектролитов с регулируемым кислотно-основным и гидрофильно-гидрофобным балансом, используемых в качестве флокулянтов, коагулянтов, структураторов почв, пролонгаторов лекарственных средств и упрощении способа, за счет снижения температуры реакции, уменьшения времени синтеза, применения в качестве исходных реагентов менее вредных веществ.
ЛИТЕРАТУРА
1. Мацоян С.Г., Погосян Г.М., Джагамян А.О., Мушегян А.А. Исследование в области циклической полимеризации и сополимеризации. 13. Изучение циклической полимеризации N-замещенных диаллиламинов.// Высокомолекул. соединения. 1963. Т.5. №6. С.854-860.
2. Hoover M.F. Cationic Quartemery Polyelectrolytes-A Literature Review. // J. Macromol. Sci.-Chem, 1970. A4(6). P 1293-1300.
3. Lancaster L.E., Basset L., Panzer H.P. The Structure of Poly(Diallyl dimethylammonium) Chloride by 13C-NMR spectroscopy. // J. Polym. Sci. 1976. V.14. P.549-554.
4. Johns S.R., Willing R.L., Middleton S., Ong A.K. Cyclopoplymerization. VII. The 13C-NMR Spectra of Cyclopolymers obtained from N,N-Diallylamines. // J. Macromol. Sci.-Chem., A, 1976. V.10. №5. P.875-891.
5. Канао С., Сакаери Я. «Якугаку дзасси, Yakugaku zasshi, J. Phrmac. Soc. Japan» 1966, 86, №1161105-1108, РЖХ, 23Ж670, 1967.
6. Патент США №3457302 «Способ получения третичных аминокислот», РЖХ, 13Н355 П., 1970.
| название | год | авторы | номер документа |
|---|---|---|---|
| N, N-ДИАЛЛИЛВАЛИН | 2013 |
|
RU2533835C1 |
| N,N-ДИАЛЛИЛАМИНОЭТАНОВАЯ КИСЛОТА И СПОСОБ ПОЛУЧЕНИЯ | 2010 |
|
RU2458045C2 |
| N, N-ДИАЛЛИЛЛЕЙЦИН | 2013 |
|
RU2529028C1 |
| Способ получения N,N-диаллилглутаминовой кислоты | 2021 |
|
RU2781156C1 |
| ПОЛИ-N,N-ДИАЛЛИЛАСПАРАГИНОВАЯ КИСЛОТА | 2011 |
|
RU2476450C2 |
| Поли-N,N- диаллилглутаминовая кислота | 2021 |
|
RU2772216C1 |
| ПОЛИ-N, N-ДИАЛЛИЛАМИНОЭТАНОВАЯ КИСЛОТА | 2010 |
|
RU2439086C1 |
| ПОЛИ-N,N-ДИАЛЛИЛВАЛИН | 2013 |
|
RU2533889C1 |
| ПОЛИ-N, N-ДИАЛЛИЛЛЕЙЦИН | 2013 |
|
RU2529192C1 |
| Поли-N,N-диаллил-п-аминобензойная кислота | 2015 |
|
RU2610543C1 |
Изобретение относится к области химии, конкретно к N,N-диаллиласпарагиновой кислоте формулы
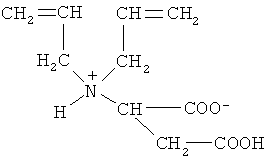
которая может найти применение в качестве исходного соединения (мономера) для получения новых полиэлектролитов с регулируемым кислотно-основным и гидрофильно-гидрофобным балансом, используемых в качестве флокулянтов, коагулянтов и т.д. Изобретение относится также к способу получения N,N-диаллиласпарагиновой кислоты взаимодействием натриевой соли α-аспарагиновой кислоты в водно-спиртовом растворе с хлористым аллилом. 2 н.п. ф-лы, 1 ил., 2 табл., 7 пр.
1. N,N-диаллиласпарагиновая кислота следующей формулы:
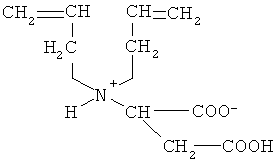 .
.
2. Способ получения N,N-диаллиласпарагиновой кислоты по п.1, заключающийся в том, что реакцию ведут взаимодействием натриевой соли α-аспарагиновой кислоты в водно-спиртовом растворе с хлористым аллилом.
| US 3457302, 22.07.1969 | |||
| N.SAKAI et al, Practical Synthesis of Natural Amino Acid Derivatives: Hf(OTf)-Catalyzed Mannich-Type Reaction of Ketene Silyi Acetals or Enol Silyi Ethers with N,O-Acetals as a Glycine Cation Equivalent, SYNLETT, 2009, No.9, 1449-1452 | |||
| C.A.FALER et al, Substituted azabicyclo[3.1.0]hexan-l-ols from aspartic and |
Авторы
Даты
2013-01-27—Публикация
2010-07-27—Подача