ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соединениям, которые можно использовать в качестве ингибиторов протеинкиназ. Данное изобретение также относится к фармацевтически приемлемым композициям, содержащим соединения данного изобретения, а также к способам применения данных композиций для лечения разных нарушений. Изобретение также относится к способам получения соединений настоящего изобретения.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Разработке новых терапевтических средств в последнее время в значительной мере способствует более глубокое понимание структуры ферментов и других биомолекул, связанных с заболеваниями. Важным классом ферментов, подвергающихся интенсивным исследованиям, являются протеинкиназы. Протеинкиназы составляют большое семейство структурно родственных ферментов, которые отвечают за регуляцию ряда процессов передачи сигнала внутри клетки (см. Hardie, G and Hanks, S. The Protein Kinase Facts Book, I and II, Academic Press, San Diego, CA: 1995). Консервативность структуры и каталитической функции протеинкиназ позволяет предположить, что они эволюционируют из общего гена-предшественника. Почти все киназы содержат подобные каталитические домены из 250-300 аминокислот. Киназы можно подразделить на семейства в зависимости от субстратов, которые они фосфорилируют (например, протеин-тирозин, протеин-серин/треонин, липиды и др.). Идентифицированы мотивы последовательностей, которые в основном соответствуют каждому из указанных семейств протеинкиназ (см., например, Hanks, S. K., Hunter, T., FASEB J. 1995, 9, 576-596; Knighton et al., Science 1991, 253, 407-414; Hiles et al., Cell 1992, 70, 419-429; Kunz et al., Cell 1993, 73, 585-596; Garcia-Bustos et al, EMBO J 1994, 13, 2352-2361).
Как правило, протеинкиназы опосредуют внутриклеточную передачу сигнала, обеспечивая перенос фосфорила с трифосфата нуклеозида на белковый акцептор, участвующий в сигнальном пути. Указанные события фосфорилирования действуют как молекулярные переключатели, которые могут модулировать или регулировать целевую биологическую функцию белка. В конечном счете, события фосфорилирования инициируются в ответ на ряд внеклеточных и других стимулов. Примеры таких стимулов включают в себя стрессовые сигналы, связанные с воздействием окружающей среды и химических веществ (такие как шок, тепловой шок, воздействие ультрафиолетового облучения, бактериального эндотоксина и H2O2), цитокины (например, интерлейкин-1 (IL-1) и фактор некроза опухоли-альфа (TNF-α) и факторы роста (например, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) и фактор роста фибробластов (FGF)). Внеклеточные стимулы могут воздействовать на один или несколько клеточных ответов, связанных с клеточным ростом, миграцией, дифференциацией, секрецией гормонов, активацией факторов транскрипции, сокращением мышц, метаболизмом глюкозы, регуляцией синтеза белка, выживанием и регуляцией клеточного цикла.
Многие заболевания связаны с аномальными клеточными ответами, которые инициируются описанными выше событиями, опосредуемыми протеинкиназами. Данные заболевания включают в себя, без ограничения, рак, аутоиммунные заболевания, воспалительные заболевания, заболевания костей, метаболические заболевания, неврологические и нейродегенеративные заболевания, сердечно-сосудистые заболевания, аллергию и астму, болезнь Альцгеймера и гормональные заболевания. Соответственно, в области медицинской химии большое внимание уделяется поиску ингибиторов протеинкиназ, которые можно использовать в качестве эффективных терапевтических средств.
Polo-подобные киназы (Plk) принадлежат к семейству серин/треонин-киназ, которое является высококонсервативным среди разных видов, варьирующих от дрожжей до человека (обзор можно найти в Lowery DM et al., Oncogene 2005, 24; 248-259 ). Киназы Plk играют несколько ролей в клеточном цикле, в том числе, они регулируют вступление клетки в митоз и развитие митоза.
Plk1 является наиболее хорошо охарактеризованным членом семейства Plk. Plk1 экспрессируется в широком ряде тканей, причем чаще всего он встречается в тканях с высоким митотическим индексом. Уровни белка Plk1 увеличиваются и достигают пика при митозе (Hamanaka, R et al., J Biol Chem 1995, 270, 21086-21091). Все описанные субстраты Plk1 представляют собой молекулы, которые заведомо регулируют вступление в митоз и развитие митоза, они включают в себя CDC25C, циклин B, p53, APC, BRCA2 и протеасомы. Повышающая регуляция Plk1 наблюдается при многих типах рака, причем уровни экспрессии коррелируют с тяжестью заболевания (Macmillan, JC et al., Ann Surg Oncol 2001, 8, 729- 740). Plk1 является онкогеном и может трансформировать клетки NIH-3T3 (Smith, MR et al., Biochem Biophys Res Commun 1997, 234, 397-405). Элиминация или ингибирование Plk1 под действием siРНК, антисмысловых последовательностей, в результате микроинъекции антител или трансфекции доминантной конструкции Plk1 отрицательного направления в клетки уменьшает пролиферацию и жизнеспособность опухолевых клеток in vitro (Guan, R et al., Cancer Res 2005, 65, 2698-2704; Liu, X et al., Proc Natl Acad Sci U S A 2003, 100, 5789-5794, Fan, Y et al., World J Gastroenterol 2005, 11, 4596-4599; Lane, HA et al., J Cell Biol 1996, 135, 1701-1713). У опухолевых клеток с элиминацией Plk1 наблюдаются активация контрольных точек веретена, а также дефекты в формировании веретена, выравнивании и разделении хромосом и цитокинезе. Опубликованные данные свидетельствуют об утрате жизнеспособности вследствие индукции апоптоза. И наоборот, описано, что нормальные клетки сохраняют жизнеспособность при элиминации Plk1. Нокдаун Plk1 в результате применения siРНК или доминантных отрицательных конструкций in vivo приводит к ингибированию роста или регрессии опухолей у моделей с ксенотрансплантатами.
Как правило, Plk2 экспрессируется во время фазы G1 клеточного цикла и в процессе интерфазы локализуется в центросоме. Мыши с нокаутом Plk2 развиваются нормально, способны к деторождению и имеют нормальный коэффициент выживаемости, который, однако, приблизительно на 20% ниже, чем у мышей дикого типа. Клетки животных с нокаутом проходят клеточный цикл медленнее, чем клетки нормальных мышей (Ma, S et al., Mol Cell Biol 2003, 23, 6936-6943). Элиминация Plk2 под действием siРНК или трансфекция неактивных мутантных генов киназы в клетки блокирует дупликацию центриолей. Понижающая регуляция Plk2 также делает опухолевые клетки чувствительными к таксолу и инициирует митотическую катастрофу, отчасти путем подавления ответа p53 (Burns TF et al., Mol Cell Biol 2003, 23, 5556-5571).
Экспрессия Plk3 происходит на протяжении всего клеточного цикла и увеличивается от фазы G1 до митоза. Повышающая регуляция экспрессии наблюдается в интенсивно пролиферирующих клетках опухолей яичников и рака молочной железы и связана с худшим прогнозом (Weichert, W et al., Br J Cancer 2004, 90, 815-821; Weichert, W et al., Virchows Arch 2005, 446, 442-450). Полагают, что помимо регуляции митоза Plk3 участвует во фрагментации комплекса Гольджи в процессе клеточного цикла и в ответе, связанном с повреждением ДНК. Показано, что ингибирование Plk3 в результате экспрессии доминантной отрицательной последовательности инициирует p53-независимый апоптоз после повреждения ДНК и подавляет образование колоний опухолевыми клетками (Li, Z et al., J Biol Chem 2005, 280, 16843-16850.
Plk4 по структуре отличается от других членов семейства Plk. Элиминация данной киназы приводит к апоптозу раковых клеток (Li, J et al., Neoplasia 2005, 7, 312-323). Мыши с нокаутом Plk4 останавливаются на стадии развития E7.5 с высокой фракцией клеток, находящихся в митозе и содержащих частично сегрегированные хромосомы (Hudson, JW et al., Current Biology 2001, 11, 441-446).
Молекулы семейства протеинкиназ участвуют в росте, пролиферации и выживании опухолевых клеток. Соответственно, существует настоятельная потребность в разработке соединений, которые можно использовать в качестве ингибиторов протеинкиназ. Существуют четкие доказательства того, что участие киназ Plk является необходимым для клеточного деления. Блокада клеточного цикла является клинически проверенным способом ингибирования пролиферации и жизнеспособности опухолевых клеток. Следовательно, желательно разработать соединения, которые можно использовать в качестве ингибиторов семейства протеинкиназ Plk (например, Plk1, Plk2, Plk3 и Plk4) и которые способны ингибировать пролиферацию и уменьшать жизнеспособность опухолевых клеток, в особенности, поскольку в медицине существует настоятельная потребность в разработке новых способов лечения рака, в том числе с использованием пероральных лекарственных средств.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Соединения данного изобретения, а также их фармацевтически приемлемые композиции можно использовать в качестве ингибиторов протеинкиназ. В некоторых воплощениях данные соединения можно использовать в качестве ингибиторов протеинкиназ PLK; в некоторых воплощениях - в качестве ингибиторов протеинкиназ PLK1. Такие соединения представляют собой соединения формулы I, описанные в данном документе, или их фармацевтически приемлемые соли.
Указанные соединения и их фармацевтически приемлемые композиции можно использовать для лечения или профилактики ряда заболеваний, нарушений или состояний, включающих в себя, без ограничения, аутоиммунное, воспалительное, пролиферативное или гиперпролиферативное заболевание, нейродегенеративное заболевание или заболевание, опосредованное иммунной системой. Соединения, предлагаемые в данном изобретении, также можно использовать для исследования киназ в биологических и патологических процессах; для исследования путей внутриклеточной передачи сигнала, опосредованных такими киназами; и для сравнительной оценки новых ингибиторов киназ.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение предлагает соединение формулы I
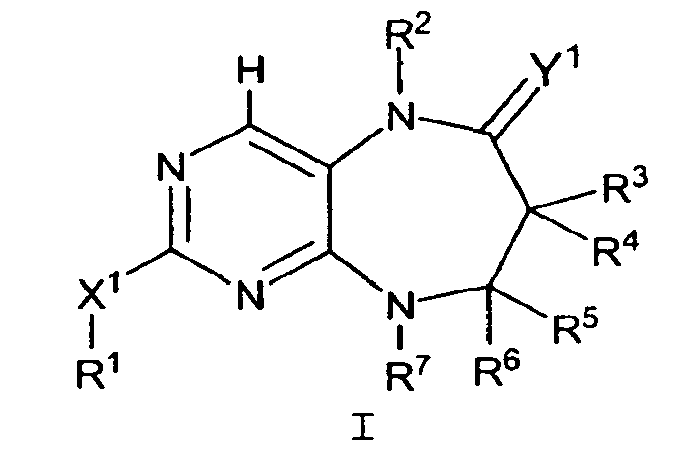
где
X1 обозначает связь, O, NR8, S, SO или SO2;
Y1 обозначает O или NR9;
R1 обозначает H, С1-10алифатический фрагмент, С3-10циклоалифатический фрагмент, С6-10арил, 5-10-членный гетероарил или 3-10-членный гетероциклил; где указанный R1 необязательно замещен 0-5 J1; при условии, что если X1 обозначает связь, R1 не обозначает H; R2 обозначает H, С1-10алифатический фрагмент, -(С1-10алифатический фрагмент)-(C3-10циклоалифатический фрагмент), C3-8циклоалифатический фрагмент, галогенC1-4алифатический фрагмент; где указанный R2 необязательно замещен 0-4 J2;
каждый из R3, R4, R5 и R6 независимо обозначает H, С1-10алифатический фрагмент, C3-10циклоалифатический фрагмент, C6-10арил или 5-10-членный гетероарил; где каждый R3, R4, R5 и R6 необязательно и независимо замещен 0-5 J3, J4, J5 и J6 соответственно; и
R7 обозначает H, C(O)R, C(O)OR или C(O)NRR', C1-10алифатический фрагмент, C3-10циклоалифатический фрагмент, C6-10арил, 5-10-членный гетероарил, 3-10-членный гетероциклил, -(С1-6алифатический фрагмент) -(C3-10циклоалифатический фрагмент), -(C1-6алифатический фрагмент)-(С6-10арил), или -(С1-6алифатический фрагмент)-(5-10-членный гетероарил); где указанный R7 необязательно замещен 0-5 J7; или
R3 и R4 вместе с атомом углерода, к которому они присоединены, необязательно образуют 3-8-членный насыщенный или частично ненасыщенный моноциклический фрагмент, содержащий 0-4 гетероатомов, независимо выбранных из O, N и S; причем указанный моноциклический фрагмент, образованный R3 и R4, необязательно замещен 0-4 J34;
R5 и R6 вместе с атомом углерода, к которому они присоединены, необязательно образуют 3-8-членный насыщенный или частично ненасыщенный моноциклический фрагмент, содержащий 0-4 гетероатомов, независимо выбранных из O, N и S; причем указанный моноциклический фрагмент, образованный R5 и R6, необязательно замещен 0-4 J56;
R3 и R5 вместе с атомами углерода, к которым они присоединены, необязательно образуют 3-8-членный насыщенный или частично ненасыщенный моноциклический фрагмент, содержащий 0-4 гетероатомов, независимо выбранных из O, N и S; причем указанный моноциклический фрагмент, образованный R3 и R5, необязательно замещен 0-4 J35;
R3 и R7 вместе с атомами, к которым они присоединены, необязательно образуют 4-8-членный насыщенный или частично ненасыщенный моноциклический фрагмент, содержащий 0-4 гетероатомов, независимо выбранных из O, N и S; причем указанный моноциклический фрагмент, образованный R3 и R7, необязательно замещен 0-4 J37;
R5 и R7 вместе с атомами, к которым они присоединены, необязательно образуют 3-8-членный насыщенный или частично ненасыщенный моноциклический фрагмент, содержащий 0-4 гетероатомов, независимо выбранных из O, N и S; причем указанный моноциклический фрагмент, образованный R5 и R7, необязательно замещен 0-4 J57;
R8 обозначает H, С1-6алифатический фрагмент, C3-8циклоалифатический фрагмент, C(O)R, C(O)OR или C (O)NRR';
R9 обозначает H или незамещенный С1-6алифатический фрагмент; или
R2 и R9, вместе с атомами, к которым они присоединены, необязательно образуют 5-8-членный ароматический или неароматический моноциклический фрагмент, содержащий 2-4 гетероатомов, независимо выбранных из O, N и S; причем указанный моноциклический фрагмент, образованный R2 и R9, необязательно замещен 0-4 J29;
каждый J1 независимо обозначает C1-6галогеналкил, галоген, NO2, CN, Q или -Z-Q; или два J1 вместе могут необязательно образовывать =O;
Z обозначает C1-6алифатический фрагмент, необязательно замещенный 0-3 заместителями, выбранными из -NR-, -О-, -S-, -C(O)-, -C(=NR)-, -C(=NOR)-, -SO- или -SO2-; причем каждый Z необязательно замещен 0-2 JZ;
Q обозначает H; C1-6алифатический фрагмент; 3-8-членный ароматический или неароматический моноциклический фрагмент, содержащий 0-3 гетероатомов, независимо выбранных из O, N и S; или 8-12-членную ароматическуюй или неароматическую бициклическую систему, содержащую 0-5 гетероатомов, независимо выбранных из O, N и S; каждый Q необязательно замещен 0-5 JQ;
каждый J2 обозначает галоген или галогенC1-4алифатический фрагмент;
каждый из J3, J4, J5 и J6 независимо обозначает C1-6алифатический фрагмент, C3-6циклоалифатический фрагмент или -(C1-4алкил)n-V1;
где n равен 0 или 1;
V1 обозначает галоген(C1-4алифатический фрагмент), -O(галогенC1-4алифатический фрагмент), галоген, NO2, CN, OH, OR", SH, SR", NH2, NHR", N(R")2, COH, COR", CO2H, CO2R", CONH2, CONHR", CONR"2, OCOR", OCONH2, OCONHR", OCON(R")2, NHCOR", NR"COR", NHCO2R", NR"CO2R", NHCO2H, NR"CO2H, NHCONH2, NHCONHR", NHCON(R")2, SO2NH2, SO2NHR", SO2N(R")2, NHSO2R", NR"SO2R"; или
V1 обозначает циклическую группу, выбранную из C3-6циклоалифатического фрагмента, фенила, 5-6-членного гетероарила или 3-6-членного гетероциклила; где указанная циклическая группа необязательно замещена 0-3 Jv;
R" обозначает незамещенный С1-4алифатический фрагмент;
или два из тех же J3, J4, J5 или J6, связанные с одним атомом, вместе могут необязательно образовывать =O;
каждый Jz и Jv независимо обозначает галоген, C1-6алифатический фрагмент, C3-6циклоалифатический фрагмент, NO2, CN, -NH2, -NH(C1-4алифатический фрагмент), -N(C1-4алифатический фрагмент)2, -OH, -O(C1-4алифатический фрагмент), -CO2H, -CO2(C1-4алифатический фрагмент), -O (галогенC1-4алифатический фрагмент) или галоген(С1-4алифатический фрагмент);
каждый из JQ, J7, J29, J34, J56, J35, J37 и J57 независимо обозначает M или -Y-M;
каждый Y независимо обозначает незамещенный С1-6алифатический фрагмент, необязательно замещенный 0-3 заместителями, выбранными из -NR-, -O-, -S-, -C(O)-, -SO- или -SO2-;
каждый M независимо обозначает H, C1-6алифатический фрагмент, C3-6циклоалифатический фрагмент, галоген(С1-4алифатический фрагмент), -О(галогенC1-4алифатический фрагмент), 3-6-членный гетероциклил, галоген, NO2, CN, OH, OR', SH, SR', NH2, NHR', N(R')2, COH, COR', CO2H, CO2R', CONH2, CONHR', CONR'2, OCOR', OCONH2, OCONHR', OCON(R')2, NHCOR', NR'COR', NHCO2R', NR'CO2R', NHCO2H, NR'CO2H, NHCONH2, NHCONHR', NHCON(R')2, SO2NH2, SO2NHR', SO2N(R')2, NHSO2R' или NR'SO2R';
R обозначает H или незамещенный C1-6алифатический фрагмент;
R' обозначает незамещенный С1-6алифатический фрагмент; или две группы R', вместе с атомом, к которому они присоединены, образуют незамещенный 3-8-членный насыщенный или частично ненасыщенный моноциклический фрагмент, содержащий 0-1 гетероатом, независимо выбранных из O, N и S.
В одном воплощении R1 обозначает H, С1-10алифатический фрагмент, C3-10циклоалифатический фрагмент, C6-10арил, 5-10-членный гетероарил или 3-10-членный гетероциклил; где указанный R1 необязательно замещен 0-5 J1; при условии, что если X1 обозначает связь, R1 не обозначает H; а другие переменные имеют указанные в данном описании определения.
В другом воплощении R7 обозначает H, C(O)R, C(O)OR или C(O)NRR', С1-10алифатический фрагмент, C3-10циклоалифатический фрагмент, C6-10арил, 5-10-членный гетероарил, 3-10-членный гетероциклил, -(С1-6алифатический фрагмент)-(C3-10циклоалифатический фрагмент), -(С1-6алифатический фрагмент)-(C6-10арил), -(С1-6алифатический фрагмент)-(5-10-членный гетероарил) или - (С1-6алифатический фрагмент)-(3-6-членный гетероциклил); где указанный R7 необязательно замещен 0-5 J7; а другие переменные имеют указанные в данном описании определения.
В другом воплощении Q обозначает H; C1-6алифатический фрагмент; 3-8-членный ароматический или неароматический моноциклический фрагмент, содержащий 0-3 гетероатомов, независимо выбранных из O, N и S; или 7-12-членный ароматический или неароматический бициклический фрагмент, содержащий 0-5 гетероатомов, независимо выбранных из O, N и S; причем каждый Q необязательно замещен 0-5 JQ; а другие переменные имеют указанные в данном описании определения.
В другом воплощении каждый M независимо обозначает H, C1-6алифатический фрагмент, C3-6циклоалифатический фрагмент, галоген(C1-4алифатический фрагмент), -О(галогенC1-4алифатический фрагмент), 3-6-членный гетероциклил, C6-10арил, галоген, NO2, CN, OH, OR', SH, SR', NH2, NHR', N(R')2, COH, COR', CO2H, CO2R', CONH2, CONHR', CONR'2, OCOR', OCONH2, OCONHR', OCON(R')2, NHCOR', NR'COR', NHCO2R', NR'CO2R', NHCO2H, NR'CO2H, NHCONH2, NHCONHR', NHCON(R')2, SO2NH2, SO2NHR', SO2N(R')2, NHSO2R' или NR'SO2R' или два M вместе могут необязательно образовывать =O; а другие переменные имеют указанные в данном описании определения.
Соединения данного изобретения описаны в общих чертах выше и дополнительно иллюстрируются классами, подклассами и видами, раскрытыми в данном описании. Если не указано иначе, в настоящем документе используются нижеследующие определения. В целях данного изобретения химические элементы идентифицируют в соответствии с периодической таблицей элементов, версия CAS, Руководство по химии и физике, 75-е издание. Кроме того, общие принципы органической химии описаны в "Organic Chemistry", Thomas Sorrell, University Science Books, Sausalito: 1999, и "March's Advanced Organic Chemistry", 5th Ed., Ed.: Smith, M. B. and March, J., John Wiley & Sons, New York: 2001, полное содержание которых включено в данное описание в качестве ссылки.
В данном описании указанный интервал числа атомов включает в себя целые значения. Например, группа, содержащая 1-4 атомов, может иметь 1, 2, 3 или 4 атомов. Как указано в данном описании, соединения настоящего изобретения необязательно могут быть замещены одним или несколькими заместителями, как иллюстрируется в общих чертах выше или как разъясняется на примерах конкретных классов, подклассов и видов данного изобретения. Следует понимать, что фраза "необязательно замещенный" используется как взаимозаменяемая с фразой "замещенный или незамещенный". Как правило, термин "замещенный", используемый ли вместе с термином "необязательно", или без него, относится к замещению радикалов водорода заданной структуры радикалом указанного заместителя. Если не указано иначе, необязательно замещенная группа может иметь заместитель в каждом замещаемом положении, и если в заданной структуре несколько положений замещены несколькими заместителями, выбранными из указанных групп, заместители во всех положениях могут быть одинаковыми или разными. Предпочтительно в объем данного изобретения входят сочетания заместителей, обеспечивающие образование стабильных или химически возможных соединений.
Термин "стабильный" в соответствии с настоящим описанием относится к соединениям, которые практически не изменяются под воздействием условий, используемых для их получения, детекции, выделения, очистки или применения с одной или несколькими целями, раскрытыми в данном документе. В других воплощениях стабильное или химически возможное соединение представляет собой соединение, которое практически не изменяется при хранении в течение, по меньшей мере, недели при 40°C или менее, в отсутствие влаги или других реакционно-способных условий.
Термин "алифатический фрагмент" или "алифатическая группа" в данном описании относится к линейной (т. е., неразветвленной) или разветвленной, замещенной или незамещенной углеводородной цепи, которая содержит один или несколько элементов ненасыщенности и имеет одну точку присоединения к остальной части молекулы.
Если не указано иначе, алифатические группы содержат 1-20 алифатических атомов углерода. В некоторых воплощениях алифатические группы содержат 1-10 алифатических атомов углерода. В других воплощениях алифатические группы содержат 1-8 алифатических атомов углерода. В следующих воплощениях алифатические группы содержат 1-6 алифатических атомов углерода, и в очередных алифатических группах содержатся 1-4 алифатических атомов углерода. Подходящие алифатические группы включают в себя, без ограничения, линейные или разветвленные, замещенные или незамещенные алкильные, алкенильные или алкинильные группы. Конкретные примеры включают в себя, без ограничения, метил, этил, изопропил, н-пропил, втор-бутил, винил, н-бутенил, этинил и трет-бутил.
Термин "циклоалифатический фрагмент" (или "карбоцикл", или "карбоциклил", или "циклоалкил") относится к моноциклическому C3-C8 углеводороду, или бициклическому C8-C12 углеводороду, или бициклическому C7-C12 углеводороду, который является полностью насыщенным или содержит одну или несколько единиц ненасыщенности, но который не является ароматическим и имеет одну точку присоединения к остальной части молекулы, где каждый цикл указанной бициклической системы содержит 3-7 членов. Подходящие циклоалифатические группы включают в себя, без ограничения, циклоалкильные и циклоалкенильные группы. Конкретные примеры включают в себя, без ограничения, циклогексил, циклопропенил и циклобутил.
Термин "гетероцикл", "гетероциклил" или "гетероциклический" в данном описании относится к неароматическим, моноциклическим, бициклическим или трициклическим системам, в которых один или несколько членов цикла представляют собой независио выбранные гетероатомы. В некоторых воплощениях "гетероцикл", "гетероциклил" или "гетероциклическая" группа содержит от трех до четырнадцати циклических членов, среди которых один или несколько представляют собой гетероатом, независимо выбранный из кислорода, серы, азота или фосфора, а каждый цикл в системе содержит от 3 до 7 циклических членов. В некоторых воплощениях циклическая система содержит 1-4 гетероатомов.
Подходящие гетероциклы включают в себя, без ограничения, 3-1H-бензимидазол-2-он, 3-(1-алкил)-бензимидазол-2-он, 2-тетрагидрофуранил, 3-тетрагидрофуранил, 2-тетрагидротиофенил, 3-тетрагидротиофенил, 2-морфолин, 3-морфолин, 4-морфолин, 2-тиоморфолин, 3-тиоморфолин, 4-тиоморфолин, 1-пирролидинил, 2-пирролидинил, 3-пирролидинил, 1-тетрагидропиперазинил, 2- тетрагидропиперазинил, 3-тетрагидропиперазинил, 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 1-пиразолинил, 3-пиразолинил, 4-пиразолинил, 5-пиразолинил, 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 4-пиперидинил, 2-тиазолидинил, 3-тиазолидинил, 4-тиазолидинил, 1-имидазолидинил, 2-имидазолидинил, 4-имидазолидинил, 5-имидазолидинил, индолинил, тетрагидрохинолинил, тетрагидроизохинолинил, бензотиолан, бензодитиан и 1,3-дигидро-имидазол-2-он.
Циклические группы (например, циклоалифатические и гетероциклические) могут быть линейно сопряженными, соединенными через мостик или спироциклическими.
Термин "гетероатом" обозначает один или несколько из атомов кислорода, серы, азота, фосфора или кремния (в том числе любую окисленную форму азота, серы, фосфора или кремния; четвертичную форму любого основного азота или замещаемый атом азота гетероциклической группы, например, N (как в 3,4-дигидро-2Н-пирролиле), NH (как в пирролидиниле) или NR+ (как в N-замещенном пирролидиниле)).
Термин "ненасыщенный" в данном описании означает, что фрагмент содержит один или несколько элементов ненасыщенности.
Термин "неароматический" в данном описании относится к циклам, которые являются либо насыщенными, либо частично ненасыщенными.
Термин "алкокси" или "тиоалкил" в данном описании относится к алкильной группе, определенной выше, присоединенной через атом кислорода ("алкокси") или серы ("тиоалкил").
Термины "галогеналкил", "галогеналкенил", "галогеналифатический фрагмент" и "галогеналкокси" обозначают алкил, алкенил или алкокси, в зависимости от обстоятельств, замещенные одним или несколькими атомами галогена. Термин "галоген" обозначает F, Cl, Br или I.
Термин "арил", используемый в применении к отдельной группе или к группе, являющейся частью более крупного фрагмента, такого как "аралкил", "аралкокси" или "арилоксиалкил", относится к моноциклическим, бициклическим и трициклическим системам, содержащим всего от пяти до четырнадцати циклических членов, причем, по меньшей мере, один цикл в системе является ароматическим, и каждый цикл системы содержит от 3 до 7 циклических членов. Термин "арил" может использоваться как взаимозаменяемый с термином "арильный цикл".
Термин "гетероарил", используемый в применении к отдельной группе или к группе, являющейся частью более крупного фрагмента, такого как "гетероаралкил" или "гетероарилалкокси", относится к моноциклическим, бициклическим и трициклическим системам, содержащим всего от пяти до четырнадцати циклических членов, причем, по меньшей мере, один цикл в системе является ароматическим, по меньшей мере, один цикл в системе содержит один или несколько гетероатомов, и каждый цикл системы содержит от 3 до 7 циклических членов. В некоторых воплощениях циклическая система содержит 1-4 гетероатомов. Термин "гетероарил" можно использовать как взаимозаменяемый с терминами "гетероарильный цикл" или "гетероароматический фрагмент". Подходящие гетероарильные циклы включают в себя, без ограничения, 2-фуранил, 3-фуранил, N-имидазолил, 2-имидазолил, 4-имидазолил, 5-имидазолил, бензимидазолил, 3-изоксазолил, 4-изоксазолил, 5-изоксазолил, 2-оксазолил, 4-оксазолил, 5-оксазолил, N-пирролил, 2-пирролил, 3-пирролил, 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, пиридазинил (например, 3-пиридазинил), 2-тиазолил, 4-тиазолил, 5-тиазолил, тетразолил (например, 5-тетразолил), триазолил (например, 2-триазолил и 5-триазолил), 2-тиенил, 3-тиенил, бензофурил, бензотиофенил, индолил (например, 2-индолил), пиразолил (например, 2-пиразолил), изотиазолил, 1,2,3-оксадиазолил, 1,2,5-оксадиазолил, 1,2,4-оксадиазолил, 1,2,3-триазолил, 1,2,3-тиадиазолил, 1,3,4-тиадиазолил, 1,2,5-тиадиазолил, пуринил, пиразинил, 1,3,5-триазинил, хинолинил (например, 2-хинолинил, 3-хинолинил, 4-хинолинил) и изохинолинил (например, 1-изохинолинил, 3-изохинолинил или 4-изохинолинил).
Термины "защищающая группа" и "защитная группа" в данном описании являются взаимозаменяемыми и относятся к средству, используемому для временной блокировки одной или нескольких целевых функциональных групп в соединении с несколькими реакционно-способными центрами. В некоторых воплощениях защитная группа должна удовлетворять одному или нескольким из нижеследующих требований или всем нижеследующим требованиям: a) она должна быть способной селективно присоединяться к функциональной группе с хорошим выходом и с получением защищенного субстрата, b) который является стабильным в условиях реакций, проводимых по одной или нескольким другим реакционно-способным группам; и c) который можно селективно удалить с хорошим выходом с помощью реагентов, которые не оказывают воздействия на регенерируемую функциональную группу, с которой удаляют защиту. Специалистам в данной области известно, что в некоторых случаях реагенты не взаимодействуют с другими реакционно-способными группами соединения. В других случаях реагенты могут взаимодействовать с другими реакционно-способными группами соединения. Примеры защитных групп подробно описаны в Greene, T. W., Wuts, P. G in "Protective Groups in Organic Synthesis", Third Edition, John Wiley & Sons, New York: 1999 (а также в других изданиях данной книги), полное содержание которой включено в настоящее описание в качестве ссылки. Термин "защитная группа для азотсодержащих групп" в данном описании относится к средствам, используемым для временной блокировки одной или нескольких целевых азотсодержащих реакционно-способных групп в полифункциональном соединении. Предпочтительные защитные группы для азотсодержащих групп также обладают указанными выше характеристиками, а некоторые примеры защитных групп для азотсодержащих групп также подробно описаны в главе 7 Greene, T. W., Wuts, P. G in "Protective Groups in Organic Synthesis", Third Edition, John Wiley & Sons, New York: 1999, полное содержание которой включено в настоящее описание в качестве ссылки.
В некоторых воплощениях алкильная или алифатическая цепь может быть необязательно замещена другим атомом или другой группой. Это означает, что метиленовый элемент алкильной или алифатической цепи необязательно замещен указанными другими атомом или группой. Примеры таких атомов или групп включают в себя, без ограничения, -NR-, -O-, -C(O)-, -C(=N-CN)-, -C(=NR)-, -C(=NOR)-, -S-, -SO- или -SO2-. Данные атомы или группы могут быть объединены с образованием более крупных фрагментов. Примеры таких фрагментов включают в себя, без ограничения, -OC(O)-, -C(O)CO-, -CO2-, -C(O)NR-, -C(=N-CN), -NRCO-, -NRC(O)O-, -SO2NR-, -NRSO2-, -NRC(O)NR-, -OC(O)NR- и -NRSO2NR-, где R имеет указанное в данном описании определение.
Если не указано иначе, необязательные замены приводят к получению химически стабильного соединения. Необязательные замены можно осуществлять как внутри цепи, так и на любом конце цепи; т.е. в точке присоединения и/или на свободном конце. Две необязательные замены могут находиться по соседству внутри цепи, если в результате образуется химически стабильное соединение. Необязательные замены также могут осуществляться с полной заменой всех атомов углерода в цепи. Например, алифатический фрагмент C3 может быть необязательно замещен -NR-, -C(O)- и -NR- с получением -NRC(O)NR- (мочевина).
Если не указано иначе, при осуществлении замены по свободному концу, заменяемый атом связан с H на свободном конце. Например, если -CH2CH2CH3 необязательно замещен -О-, полученное соединение может представлять собой -OCH2CH3, -CH2OCH3 или -CH2CH2OH.
Если не указано иначе, также подразумевается, что изображенные в данном описании структуры включают в себя все изомерные формы (например, энантиомерные, диастереомерные, геометрические, конформационные и поворотные изомеры). Например, в объем данного изобретения входят R- и S-конфигурации по каждому асимметрическому центру, (Z)- и (E)-изомеры по двойной связи, а также (Z) и (E) конформационные изомеры. Специалистам в данной области известно, что заместитель может свободно вращаться вокруг любой связи, допускающей такое вращение. Например, заместитель, изображаемый 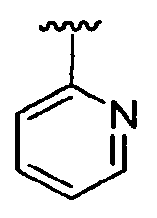 также может представлять собой
также может представлять собой 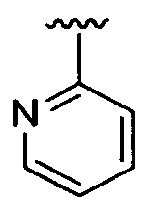 .
.
Следовательно, в объем данного изобретения входят индивидуальные стереохимические изомеры, а также смеси энантиомеров, диастереомеров, геометрических, конформационных или поворотных изомеров.
Если не указано иначе, все таутомерные формы описываемых соединений входят в объем данного изобретения.
Кроме того, если не указано иначе, также подразумевается, что изображенные в данном описании структуры включают в себя соединения, которые отличаются только присутствием одного или нескольких атомов, обогащенных одним изотопом. Например, в объем настоящего изобретения входят соединения, имеющие структуру настоящего изобретения, но содержащие вместо водорода дейтерий, или тритий, или углерод, обогащенный изотопами 13C или 14C. Такие соединения можно использовать в биологических анализах, например, в качестве аналитических инструментов или зондов.
Соединения данного изобретения могут существовать в свободной форме, пригодной для лечения, или, когда это целесообразно, в виде фармацевтически приемлемой соли.
В данном описании термин "фармацевтически приемлемая соль" относится к солям соединения, которые в рамках вынесенного медицинского заключения подходят для применения в контакте с тканями людей и низших животных, не вызывая излишних токсичности, раздражения, аллергического ответа и т.п. и обладая приемлемым соотношением польза/риск.
Фармацевтически приемлемые соли хорошо известны в данной области. Например, S. M. Berge et al. подробно описывают фармацевтически приемлемые соли в J. Pharmaceutical Sciences, 1971, 66, 1-19, включенной в данное описание в качестве ссылки. Фармацевтически приемлемые соли соединений данного изобретения включают в себя соли подходящих неорганических и органических кислот и оснований. Данные соли можно получить in situ в процессе конечного выделения и очистки соединений. Кислотно-аддитивные соли можно получить путем 1) взаимодействия очищенного соединения в виде свободного основания с подходящей органической или неорганической кислотой и 2) выделения полученной соли.
Примерами фармацевтически приемлемых нетоксичных кислотно-аддитивных солей являются соли аминогруппы, полученные с использованием неорганических кислот, таких как хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и хлорная кислота, или органических кислот, таких как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или с помощью других известных в данной области методов, таких как ионный обмен. Другие фармацевтически приемлемые соли включают в себя адипаты, альгинаты, аскорбаты, аспартаты, бензолсульфонаты, бензоаты, бисульфаты, бораты, бутираты, камфораты, камфорсульфонаты, цитраты, циклопентанпропионаты, диглюконаты, додецилсульфаты, этансульфонаты, форматы, фумараты, глюкогептонаты, глицерофосфаты, гликоляты, глюконаты, гемисульфаты, гептаноаты, гексаноаты, гидроиодиды, 2-гидроксиэтансульфонаты, лактобионаты, лактаты, лаураты, лаурилсульфаты, малаты, малеаты, малонаты, метансульфонаты, 2-нафталинсульфонаты, никотинаты, нитраты, олеаты, оксалаты, пальмитаты, пальмоаты, пектинаты, персульфаты, 3-фенилпропионаты, фосфаты, пикраты, пивалаты, пропионаты, салицилаты, стеараты, сукцинаты, сульфаты, тартраты, тиоцианаты, п-толуолсульфонаты, ундеканоаты, валераты и т.п. Соли, полученные с использованием подходящих оснований, включают в себя соли щелочных металлов, щелочноземельных металлов, аммония и N+(С1-4алкил)4. Данное изобретение также охватывает соединения, полученные в результате преобразования основной азотсодержащей группы, входящей в состав раскрытых в данном описании соединений, в четвертичное основание. Путем образования четвертичного основания можно получить водо- или маслорастворимые или -диспергируемые продукты.
Основно-аддитивные соли можно получить путем 1) взаимодействия очищенного соединения в кислой форме с подходящим органическим или неорганическим основанием и 2) выделения полученной соли. Основно-аддитивные соли включают в себя соли щелочных и щелочноземельных металлов. Примеры солей щелочных и щелочноземельных металлов включают в себя соли натрия, лития, калия, кальция, магния и т.п. Другие фармацевтически приемлемые соли включают в себя, если это целесообразно, соли, образованные нетоксичными катионами аммония, четвертичного аммония и амина и такими противоионами, как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, низший алкилсульфонат и арилсульфонат. Другие кислоты и основания, которые сами по себе не являются фармацевтически приемлемыми, можно использовать для получения солей, применяющихся в качестве промежуточных продуктов при получении соединений данного изобретения и их фармацевтически приемлемых кислотно- или основно-аддитивных солей.
В данном описании используются следующие сокращения:
В одном аспекте данного изобретения X1 обозначает O, NR8 или S. В некоторых воплощениях X1 обозначает NR8. В других аспектах Y1 обозначает О.
В другом аспекте данного изобретения R1 обозначает необязательно замещенный C6-10арил или необязательно замещенный 5-10-членный гетероарил.
В одном воплощении R1 необязательно замещен C6-10арилом, таким как фенил.
В одном воплощении R1 необязательно замещен J1, где J1 обозначает -H, -O-C1-6алкил, галоген или -C(O)N(R)(Q), где R обозначает -H.
В одном воплощении R1 необязательно замещен J1, где J1 обозначает -H, -OCH3, галоген или -C(O)N(R)(Q), где R обозначает -H.
В одном воплощении J1 обозначает -OCH3 или -C(O)N(R)ZQ, где Z обозначает С1-6алифатический фрагмент, а Q обозначает 3-8-членный ароматический или неароматический моноциклический фрагмент, содержащий 1-3 гетероатомов, независимо выбранных из O, N и S; или 8-12-членный ароматический или неароматический бициклический фрагмент, содержащий 1-5 гетероатомов, независимо выбранных из O, N и S; а Q необязательно замещен 0-5 JQ. В некоторых воплощениях Z обозначает C1-6алкил, а в более конкретных воплощениях Z обозначает -CH2-.
В одном воплощении J1 обозначает -OCH3 или -C(O)N(R)ZQ, где Z обозначает C1-6алифатический фрагмент, а Q обозначает 5-6-членный ароматический фрагмент, содержащий 1 гетероатом, выбранный из О и N (например, пиридин); где Q необязательно замещен 0-5 JQ. В некоторых воплощениях Z обозначает C1-6алкил, а в более конкретных воплощениях Z обозначает -CH2-.
В некоторых воплощениях Z обозначает C1-6алкил, а в более конкретных воплощениях Z обозначает -CH2-.
В одном воплощении J1 обозначает -OCH3 или -C(O)N(R)(Q), где R обозначает -H, а Q обозначает C1-6алкил, 3-6-членный циклоалкил, 7-12-членную неароматическую бициклическую систему или 8-12-членную неароматическую бициклическую систему, где каждый Q замещен 0-5 JQ.
В одном воплощении J1 обозначает -OCH3 или -C(O)N(R)(Q), где R обозначает -H, а Q обозначает 3-6-членный циклоалкил, где каждый Q замещен 0-5 JQ.
В одном воплощении J1 обозначает -OCH3 или -C(O)N(R)(Q), где R обозначает -H, а Q обозначает циклогексил, где каждый Q замещен 0-5 JQ.
В одном воплощении J1 обозначает -OCH3 или -C(O)N(R)(Q), где R обозначает -H, а Q обозначает C6-10арил или 5-10-членный гетероарил, содержащий 0-5 гетероатомов, независимо выбранных из O, N и S; где каждый Q замещен 0-5 JQ.
В одном воплощении J1 обозначает -OCH3 или -C(O)N(R)(Q), где R обозначает -H, а Q обозначает 3-8-членный гетероциклический фрагмент, содержащий 1 или 2 гетероатома, независимо выбранных из O, N и S; где каждый Q замещен 0-5 JQ.
В одном воплощении J1 обозначает Q, а Q обозначает:
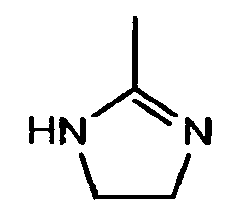
где Q замещен 0-5 JQ.
В одном воплощении Q замещен 0, 1 или 2 JQ.
В одном воплощении каждый JQ независимо обозначает F, -OH, - OR' или -OC(O)R'.
В одном воплощении каждый R' независимо обозначает C1-6алифатический фрагмент, где алифатический фрагмент является линейным.
В одном воплощении каждый R' независимо обозначает С1-6алкил, где алкил является линейным.
В одном воплощении R' обозначает CH3.
В другом аспекте R2 обозначает необязательно замещенный С1-10алифатический фрагмент или необязательно замещенный C3-10циклоалифатический фрагмент.
В некоторых воплощениях R3 и R4 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенный 3-6-членный моноциклический фрагмент.
В других воплощениях R3 и R5 вместе с атомами углерода, к которым они присоединены, образуют необязательно замещенный 3-6-членный моноциклический фрагмент.
В следующих воплощениях R3, R4, R5 и R6 независимо обозначают необязательно замещенную группу, выбранную из H, C1-10алифатического фрагмента, С3-10циклоалифатического фрагмента, С6-10арила или 5-10-членного гетероарила. В некоторых воплощениях каждый R3 и R4 независимо обозначает H, C1-6алифатический фрагмент или C3-8циклоалифатический фрагмент. В некоторых воплощениях один из R3 и R4 обозначает H, а другой обозначает С1-6алифатический фрагмент или C3-8циклоалифатический фрагмент.
В одном воплощении каждый из R3 и R4 независимо обозначает H или C1-3алкил, или R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют необязательно замещенный 3-4-членный моноциклический фрагмент.
В одном воплощении один из R3 и R4 обозначает H, а другой обозначает этил или (S)-метил.
В одном воплощении один из R3 и R4 обозначает H, а другой обозначает (R)-метил.
В одном воплощении каждый из R3 и R4 обозначает метил.
В одном воплощении R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют незамещенный 3-4-членный моноциклический фрагмент.
В одном воплощении R3 и R4 вместе с атомами углерода, к которым они присоединены, образуют незамещенный 3-членный моноциклический фрагмент.
В одном воплощении R5 обозначает H.
В одном воплощении R6 обозначает H.
В некоторых воплощениях J3 и J4 независимо обозначают галоген.
В других воплощениях R5 и R7 вместе с атомами углерода, к которым они присоединены, образуют необязательно замещенный 3-6-членный насыщенный или частично ненасыщенный моноциклический фрагмент.
В одном аспекте данного изобретения R7 обозначает необязательно замещенную группу, выбранную из С1-10алифатического фрагмента, C3-10циклоалифатического фрагмента, С6-10арила, 5-10-членного гетероарила и 3-10-членного гетероциклила. В некоторых аспектах R7 обозначает необязательно замещенную группу, выбранную из С1-10алифатического фрагмента, C3-6циклоалифатического фрагмента, фенила, 5-членного гетероарила, 2-пиридила, 3-пиридила, 4-пиридила, 2,5-пиридазинила, 3,5-пиримидила и 3-8-членного гетероциклила. В других аспектах R7 не обозначает 3-амино-2,4-пиримидин.
В одном воплощении R8 обозначает H.
В одном аспекте данное изобретение предлагает соединение формулы II
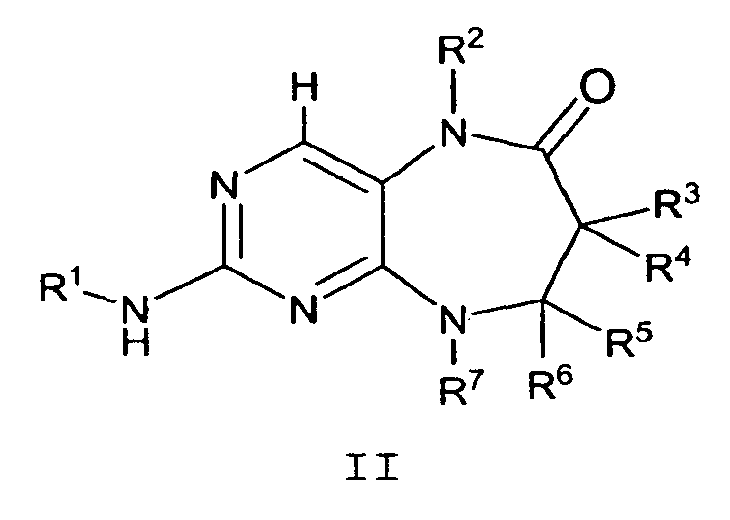
где
R1 обозначает необязательно замещенный C6-10арил или необязательно замещенный 5-10-членный гетероарил;
R2 обозначает H или необязательно замещенную группу, выбранную из С1-10алифатического фрагмента и C3-10циклоалифатического фрагмента;
каждый R3, R4, R5 и R6 независимо обозначает H, C1-10алифатический фрагмент или C3-10циклоалифатический фрагмент; где каждый R3, R4, R5 и R6 необязательно замещен 0-5 J3, J4, J5 и J6 соответственно; или
R3 и R4 вместе с атомом углерода, к которому они присоединены, могут образовывать необязательно замещенный 3-6-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R3 и R5 вместе с атомами углерода, к которым они присоединены, могут образовывать необязательно замещенный 3-6-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R5 и R7 вместе с атомами, к которым они присоединены, могут образовывать необязательно замещенный 3-6-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R2 и R9 вместе с атомами, к которым они присоединены, могут образовывать необязательно замещенный 5-8-членный насыщенный или частично ненасыщенный моноциклический фрагмент.
В другом аспекте данное изобретение предлагает соединение формулы III
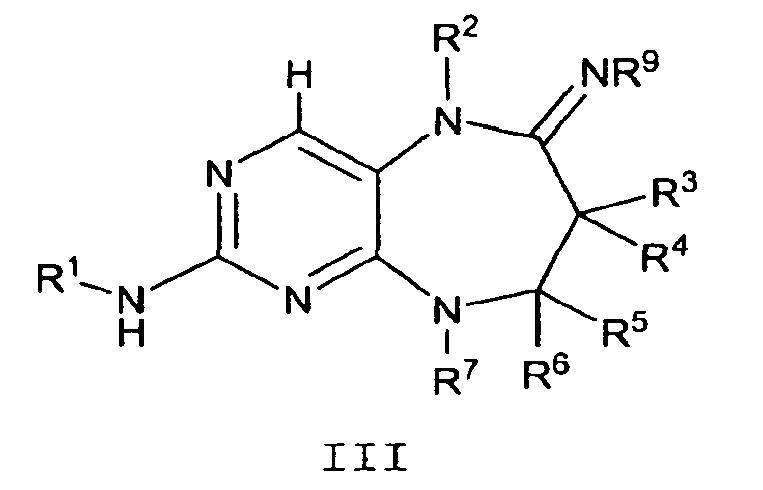
где
R1 обозначает необязательно замещенный C6-10арил или необязательно замещенный 5-10-членный гетероарил;
R2 обозначает H или необязательно замещенную группу, выбранную из С1-10алифатического фрагмента и C3-10циклоалифатического фрагмента;
каждый R3, R4, R5 и R6 независимо обозначает H, C1-10алифатический фрагмент или C3-10циклоалифатический фрагмент; где каждый R3, R4, R5 и R6 необязательно замещен 0-5 J3, J4, J5 и J6 соответственно; или
R3 и R4 вместе с атомом углерода, к которому они присоединены, могут образовывать необязательно замещенный 3-6-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R3 и R5 вместе с атомами углерода, к которым они присоединены, могут образовывать необязательно замещенный 3-6-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R5 и R7 вместе с атомами, к которым они присоединены, могут образовывать необязательно замещенный 3-6-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R2 и R9 вместе с атомами, к которым они присоединены, могут образовывать необязательно замещенный 5-8-членный насыщенный или частично ненасыщенный моноциклический фрагмент.
В некоторых воплощениях каждый из J3, J4, J5 и J6 независимо обозначает C1-6алифатический фрагмент, C3-6циклоалифатический фрагмент или -(С1-4алкил)n-V1; где
n равен 0 или 1;
V1 обозначает галоген(С1-4алифатический фрагмент), -О(галогенC1-4алифатический фрагмент), галоген, NO2, CN, OH, OR", SH, SR", NH2, NHR", N(R")2, COH, COR", CO2H, CO2R", CONH2, CONHR", CONR"2, OCOR", OCONH2, OCONHR", OCON(R")2, NHCOR", NR"COR", NHCO2R", NR"CO2R", NHCO2H, NR"CO2H, NHCONH2, NHCONHR", NHCON(R")2, SO2NH2, SO2NHR", SO2N(R")2, NHSO2R", NR"SO2R";
R" обозначает незамещенный C1-4алифатический фрагмент;
или два указанных J3, J4, J5 или J6, связанных с одним атомом, могут необязательно образовывать =O.
В некоторых воплощениях переменные имеют значения, указанные в настоящем описании.
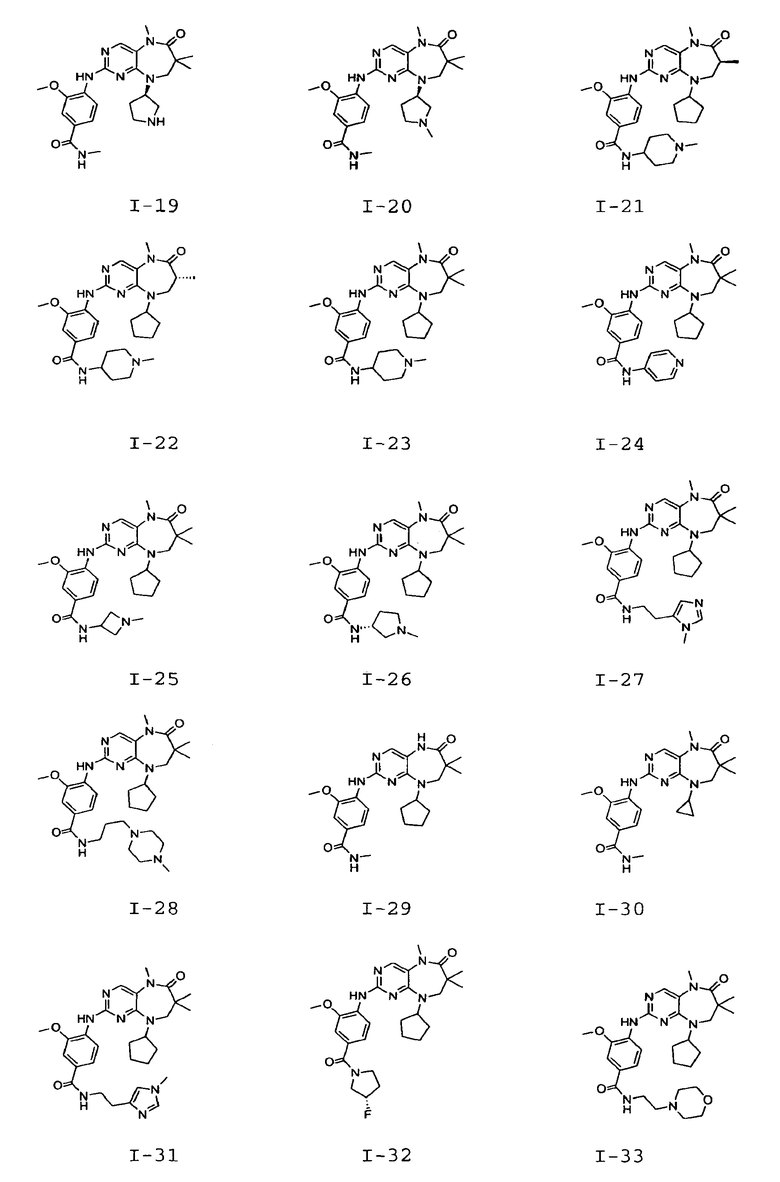
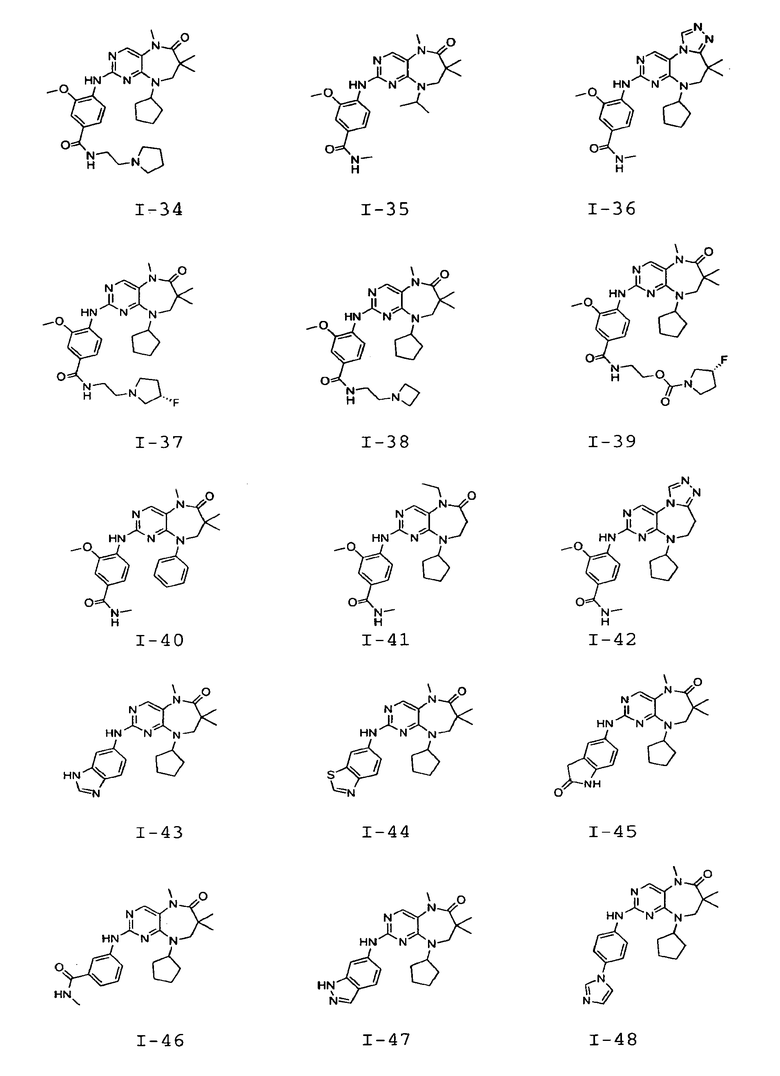
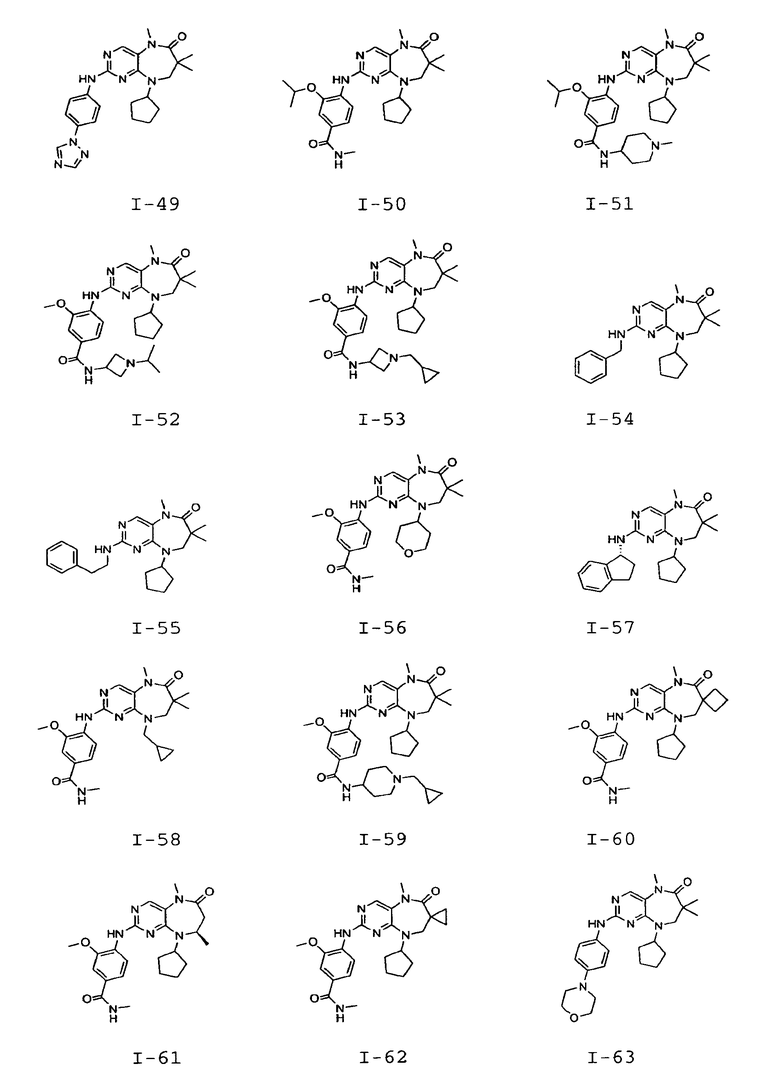
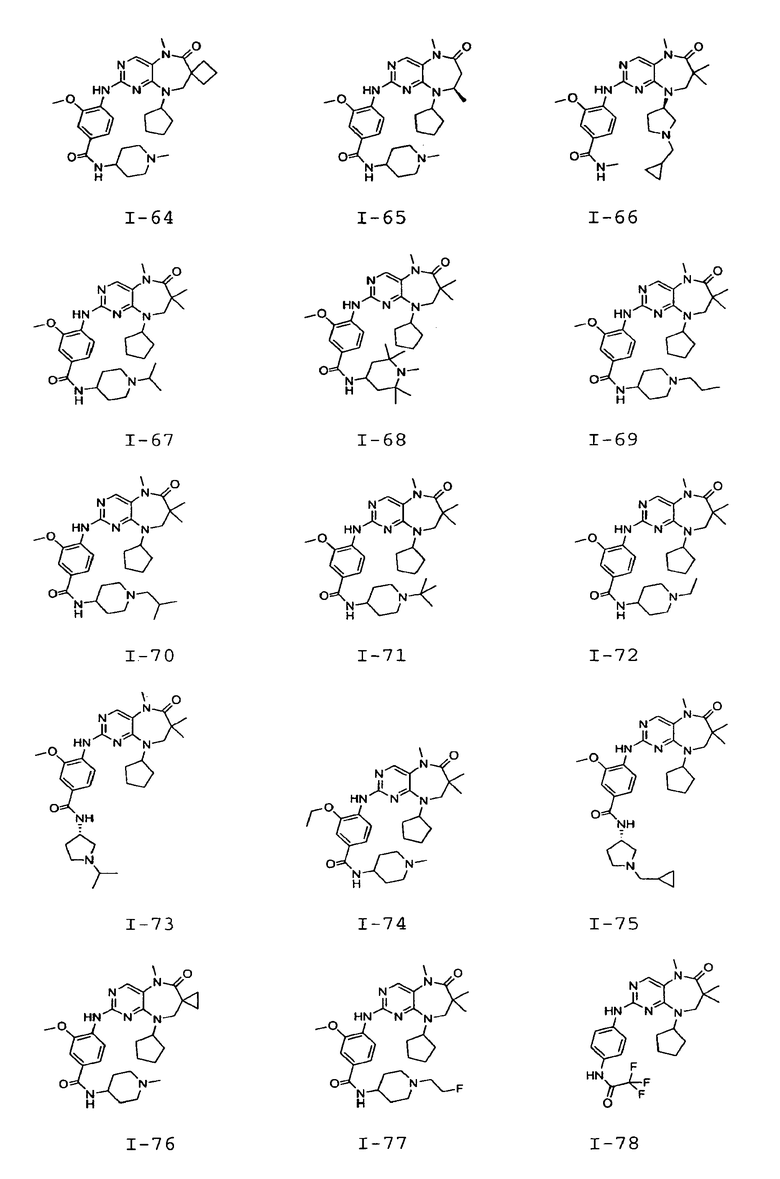
В некоторых воплощениях соединения данного изобретения имеют структуры, представленные в таблице 1.
Таблица 1
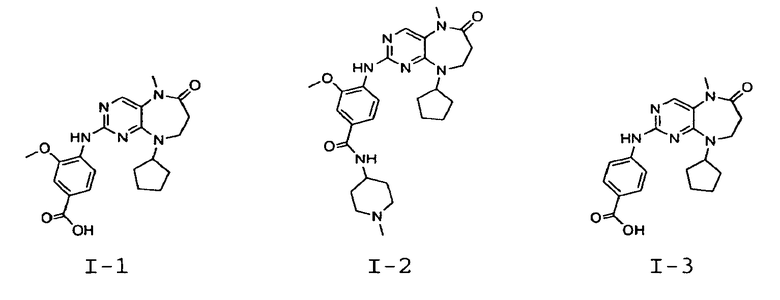
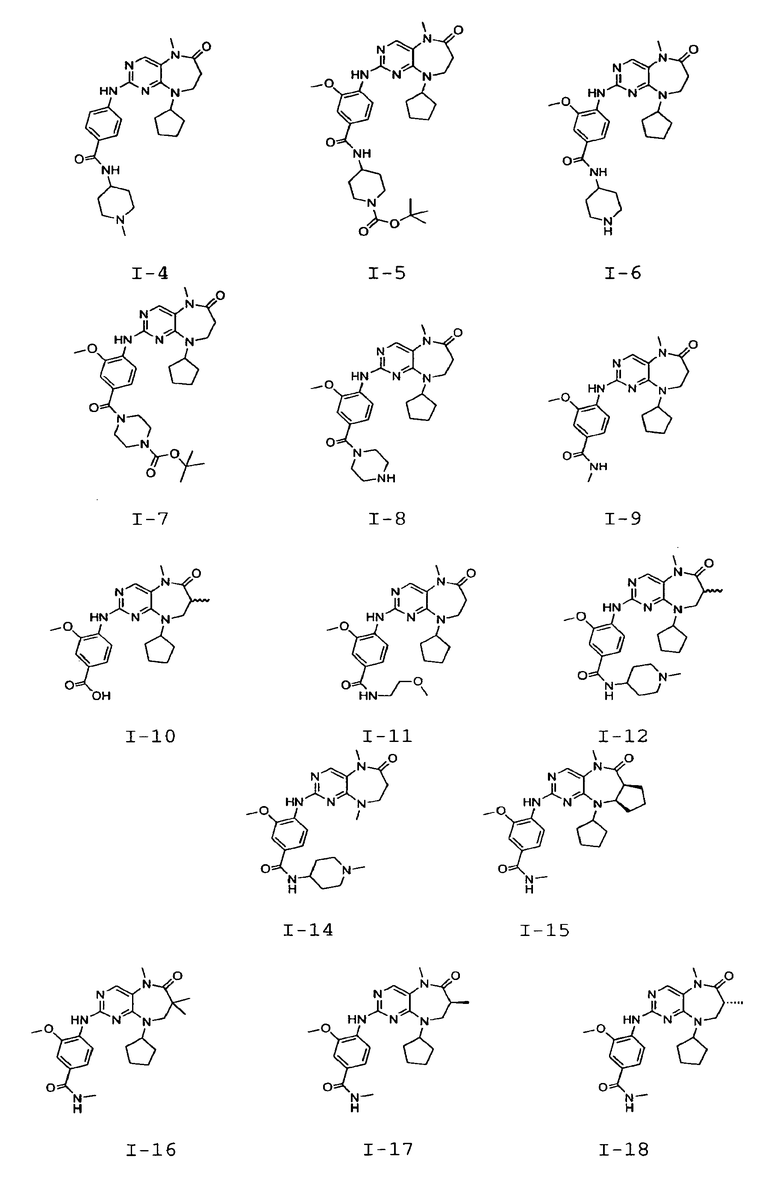
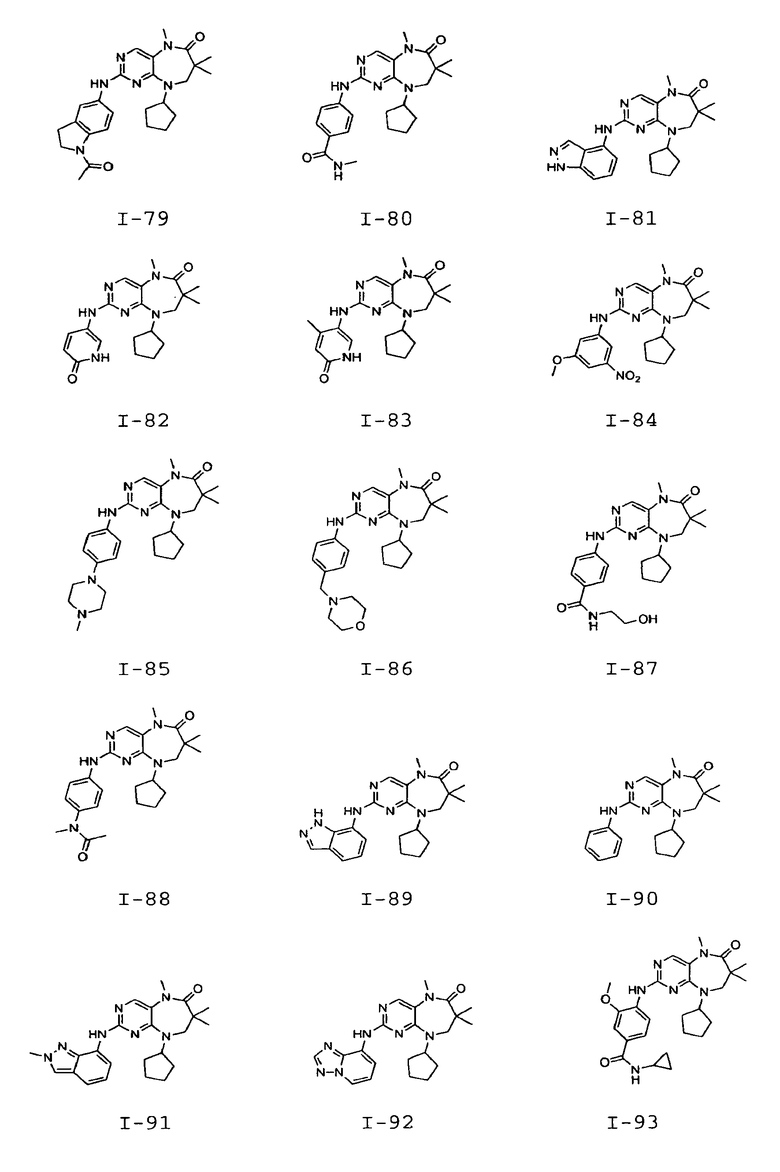
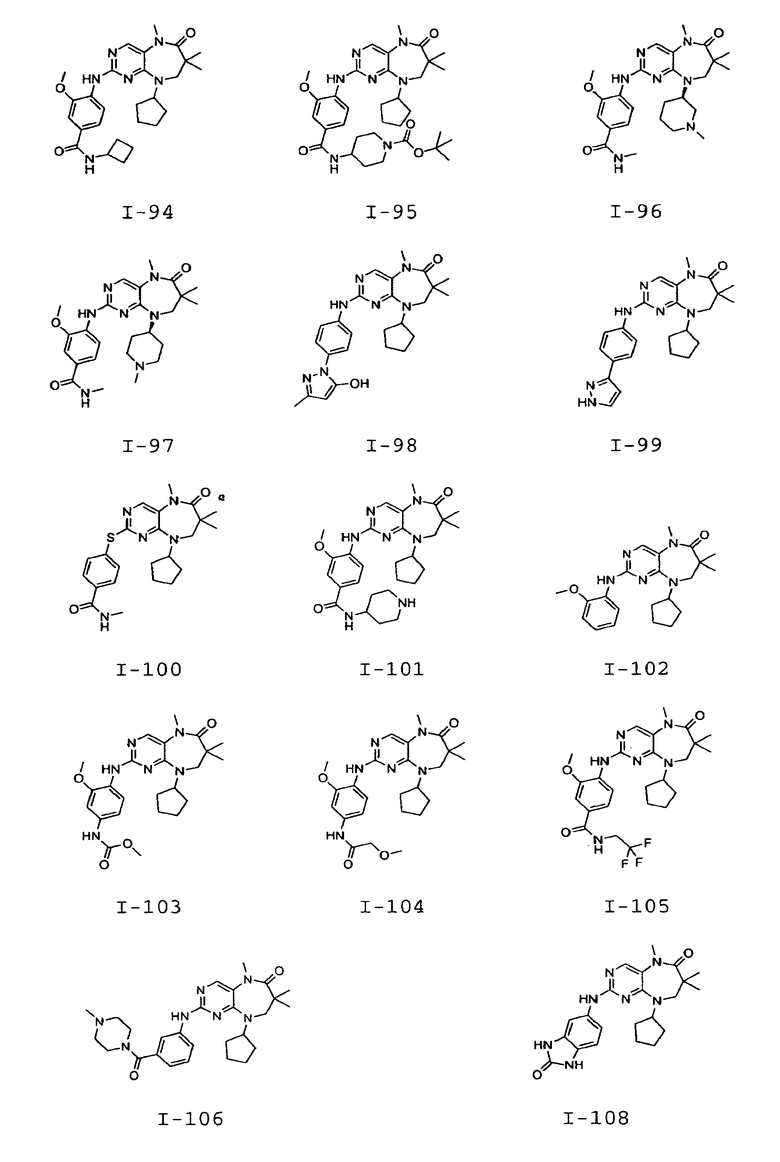
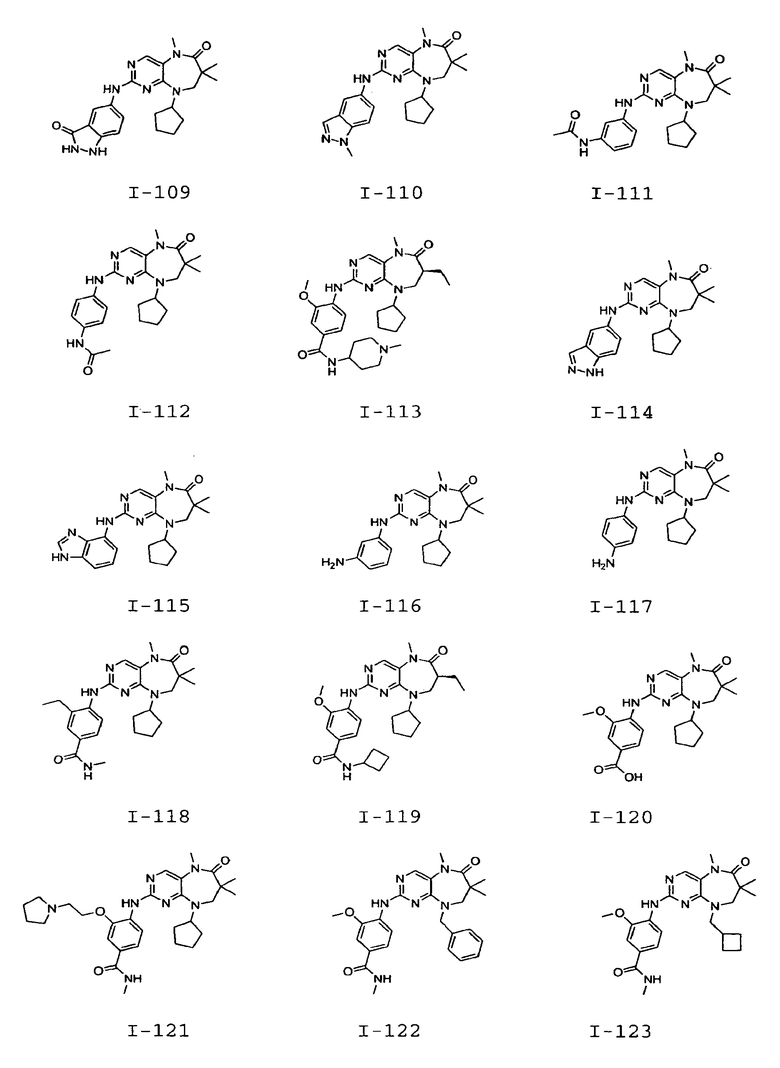
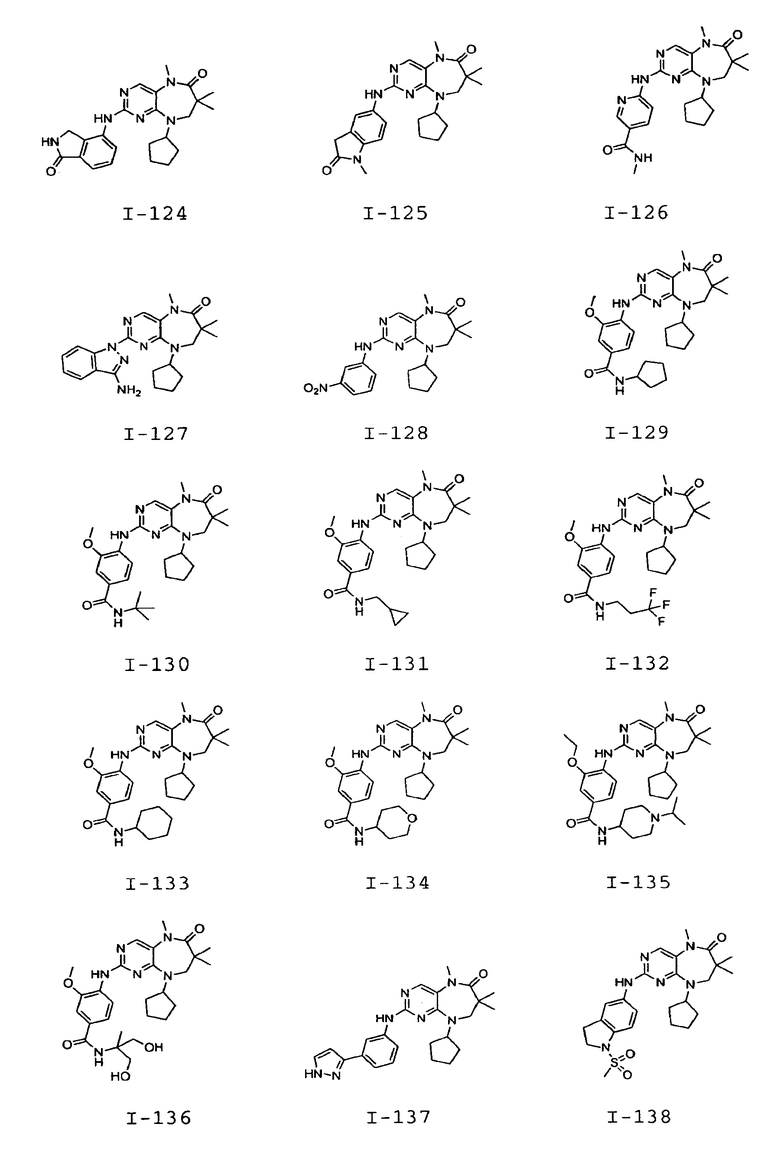
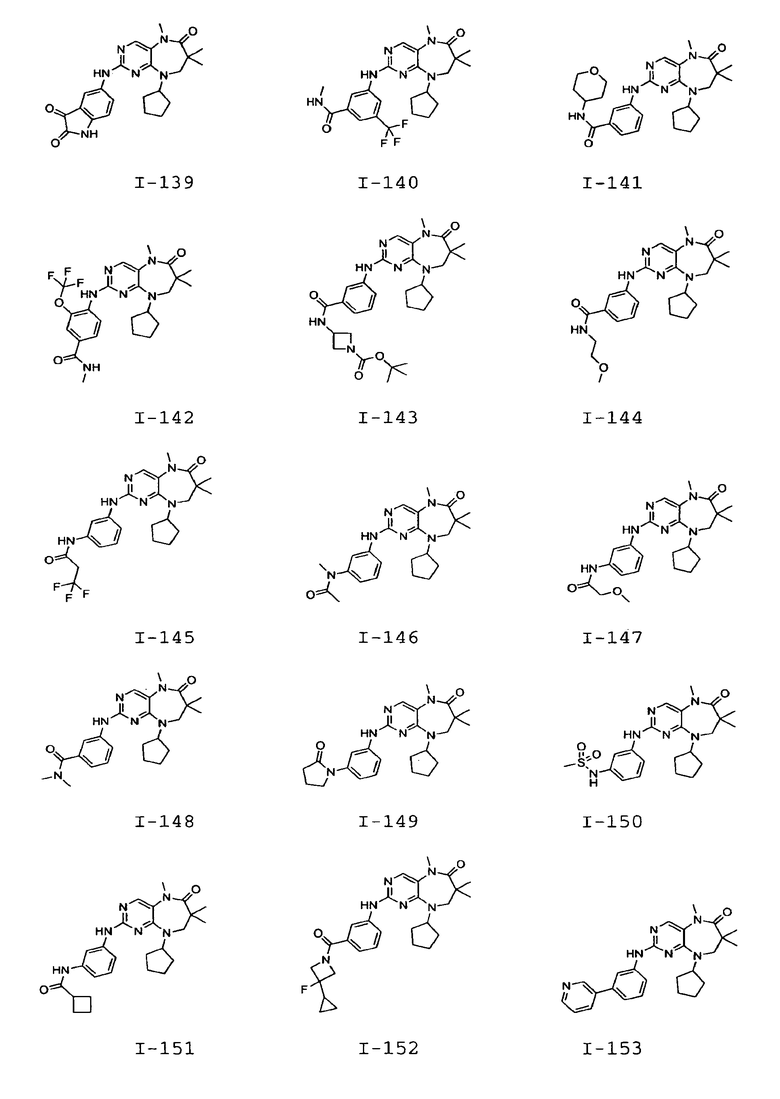
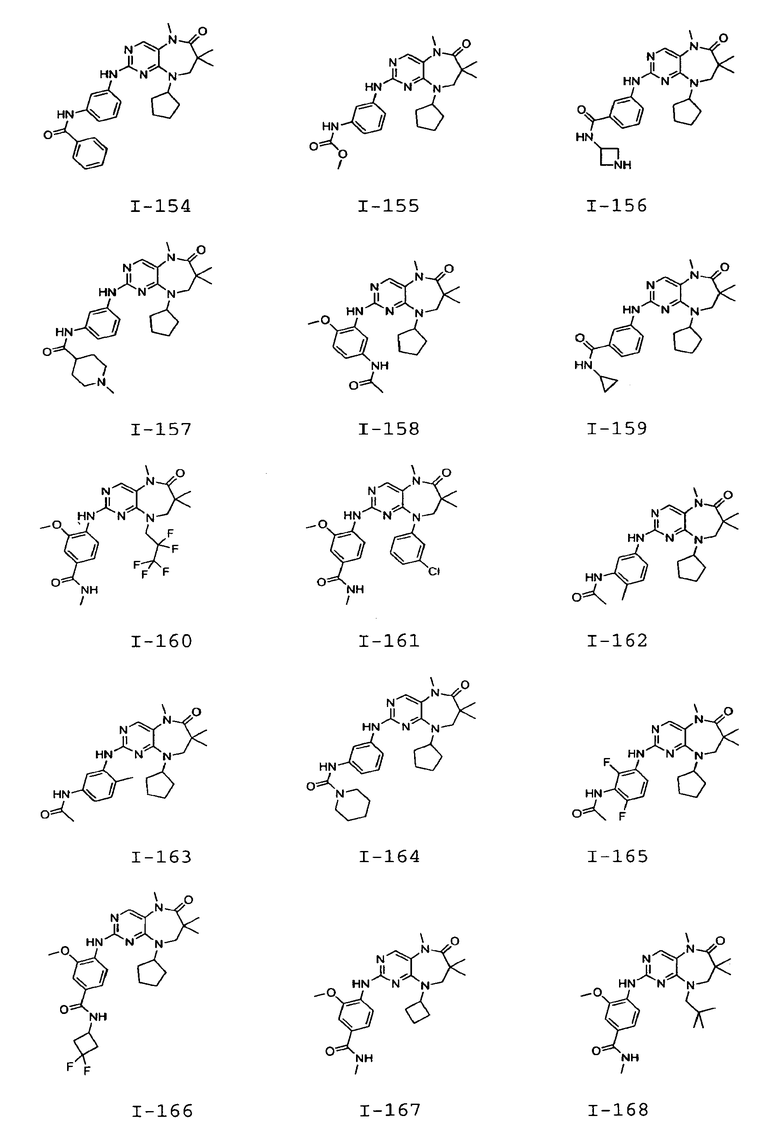
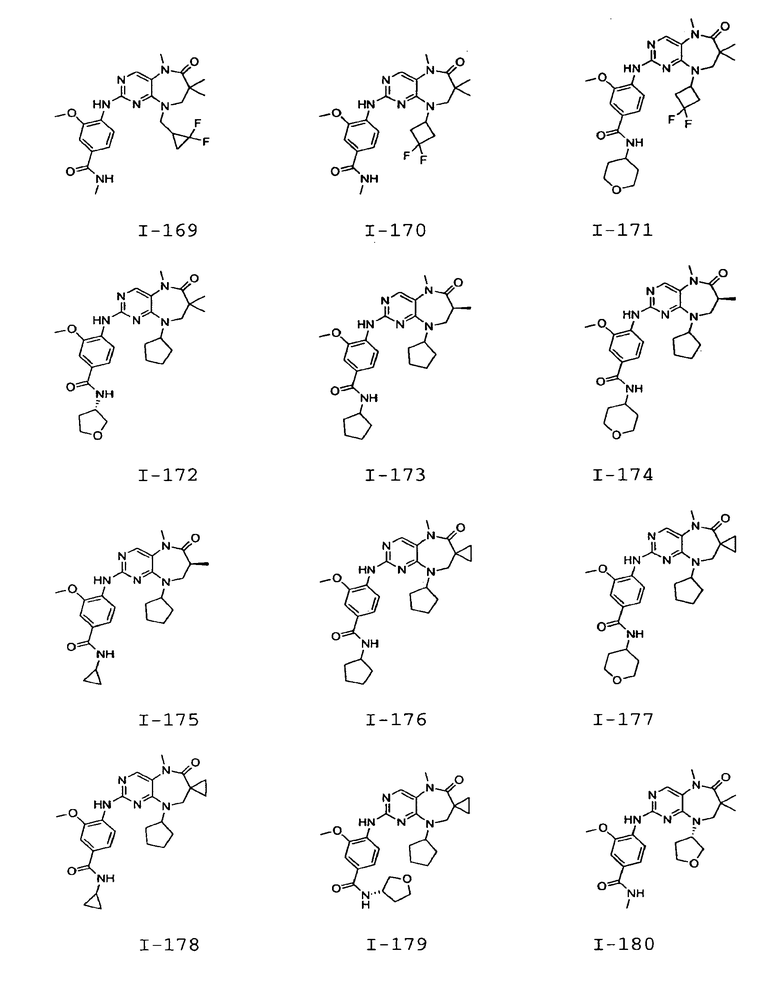
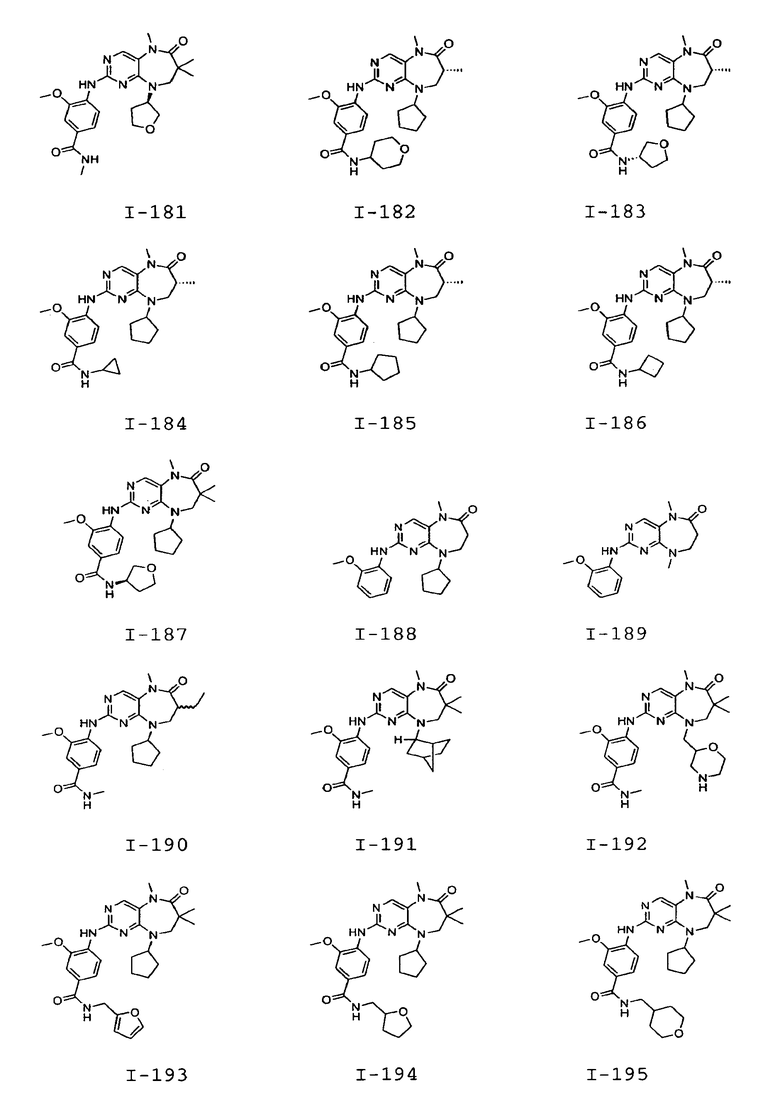
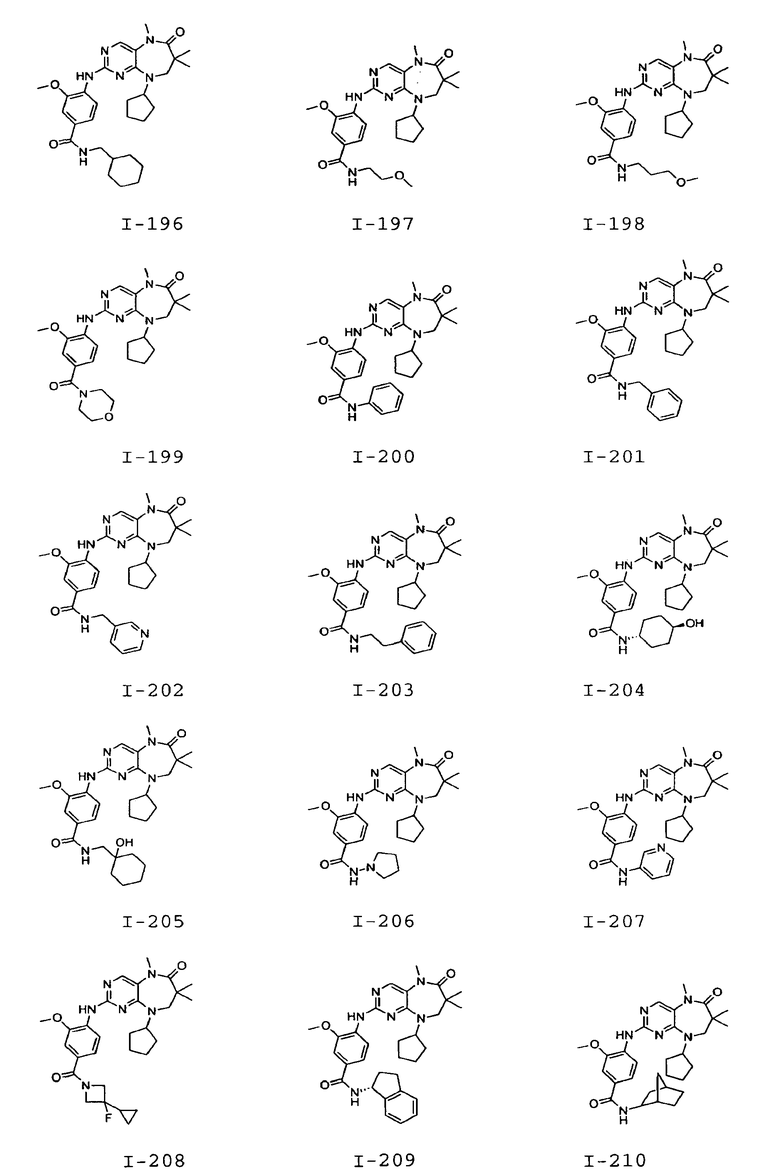
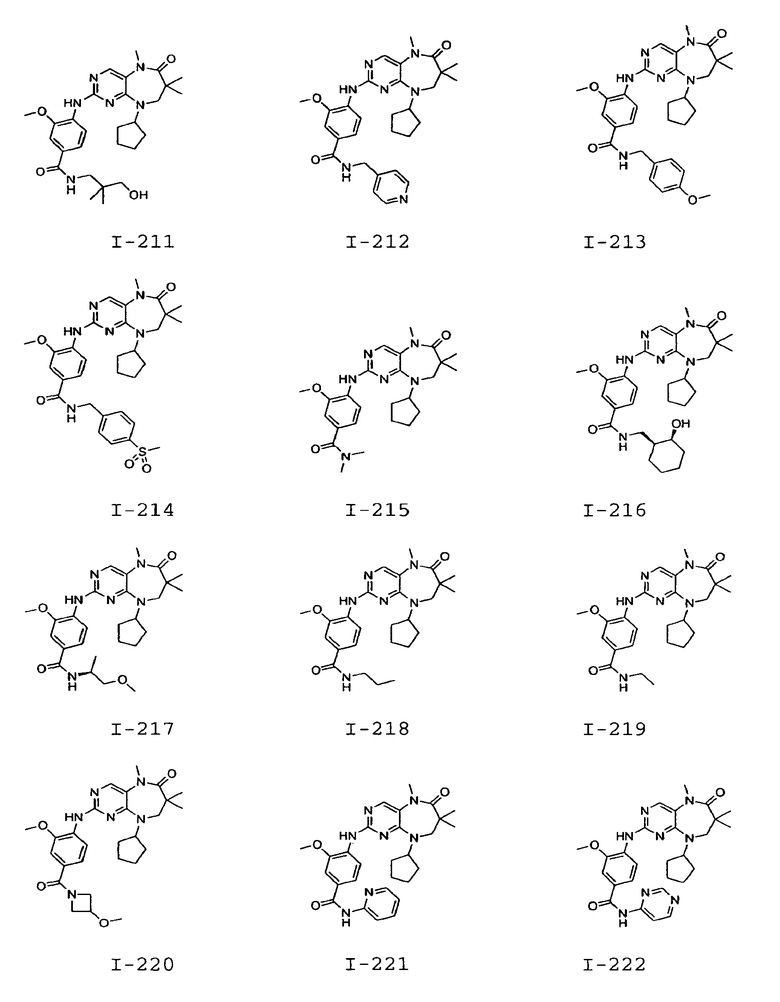
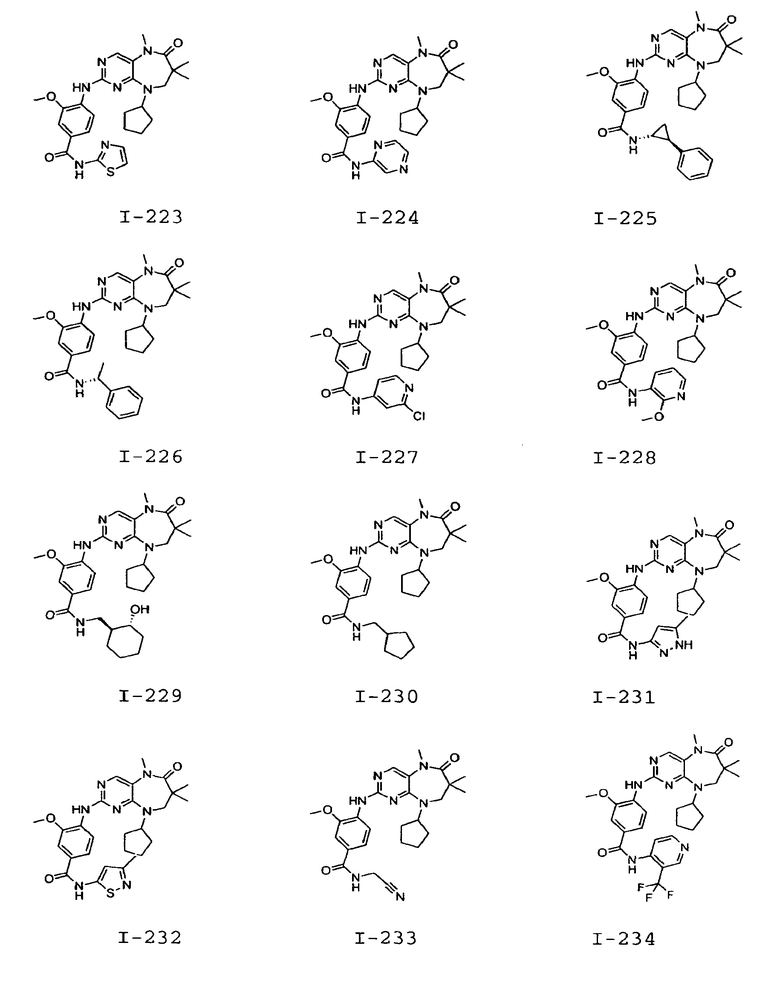
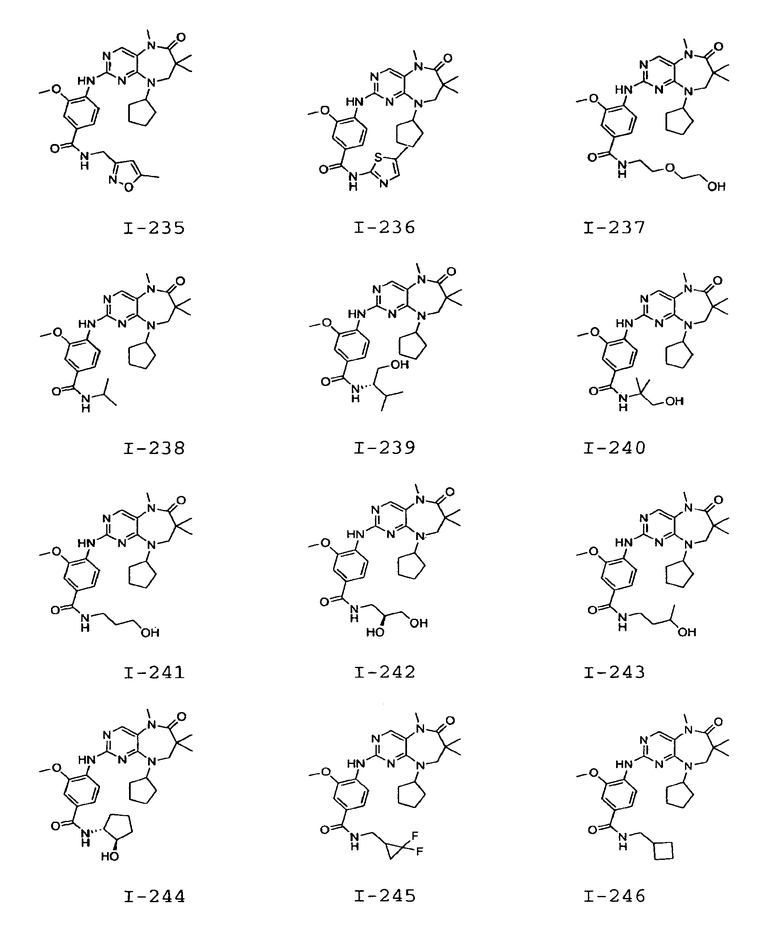
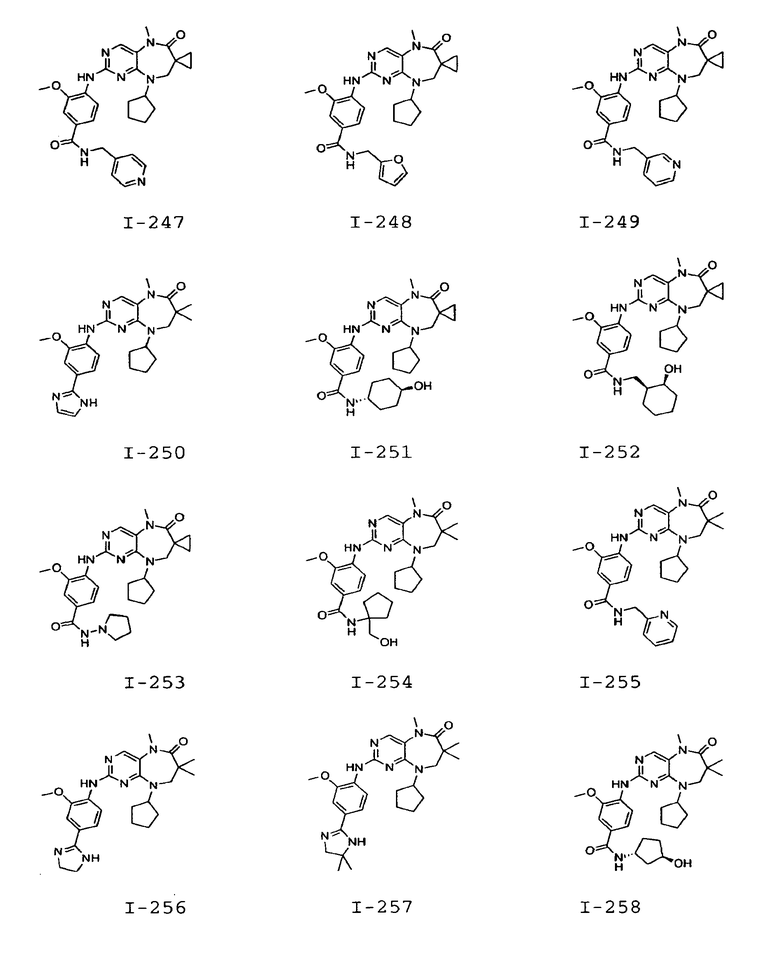
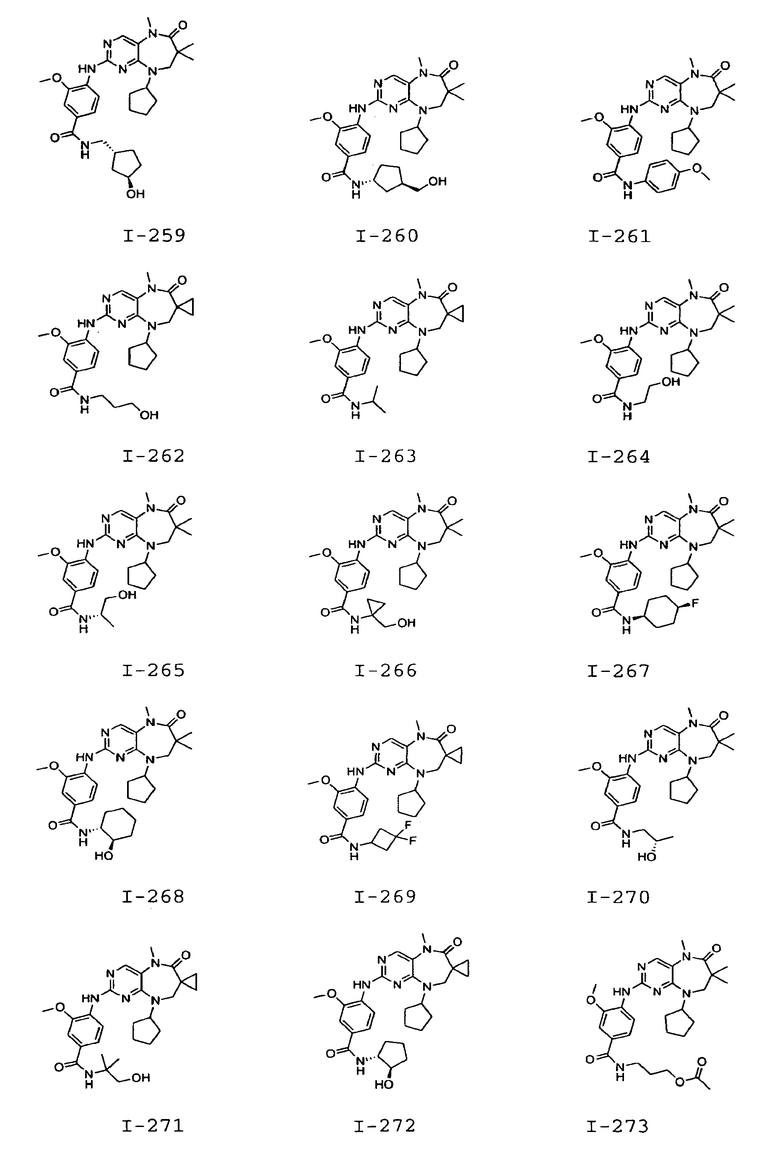
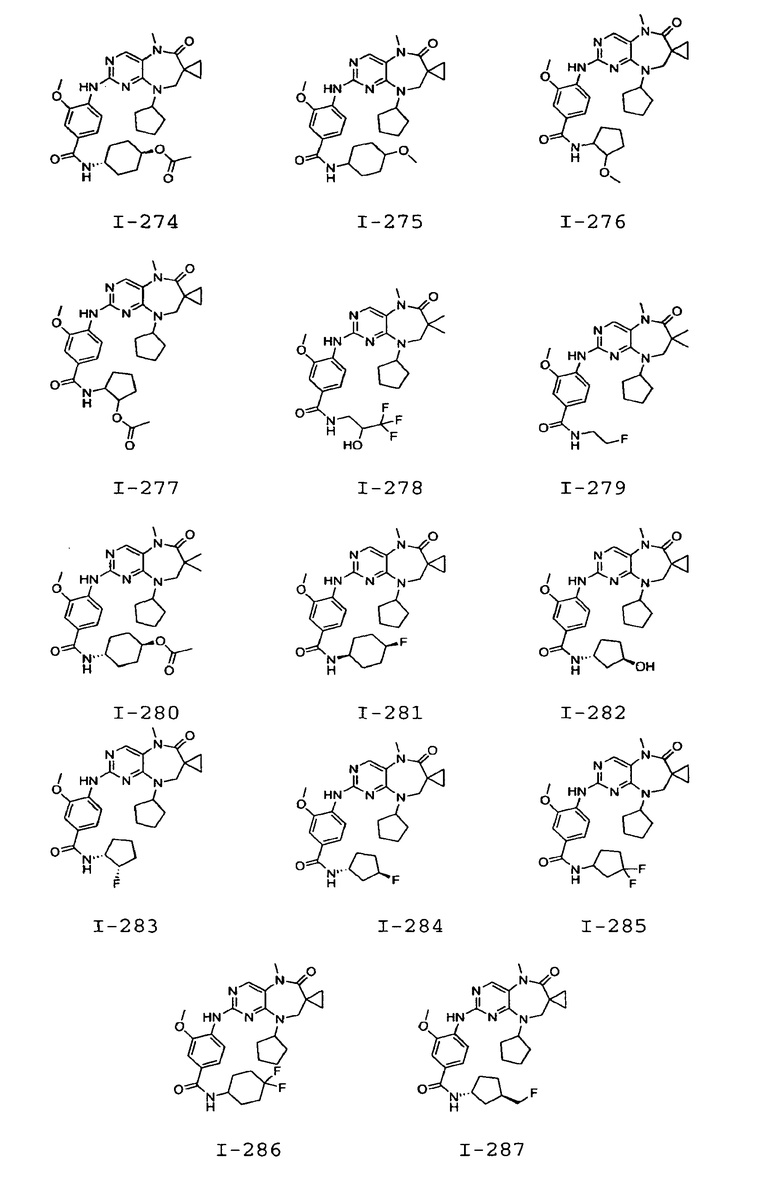
Общие способы синтеза
Как правило, соединения данного изобретения можно получить с помощью способов, изображенных на приведенных ниже общих схемах и описанных в нижеследующих примерах получения. Если не указано иначе, все переменные в нижеследующих схемах имеют значения, указанные в данном описании.
Схема 1
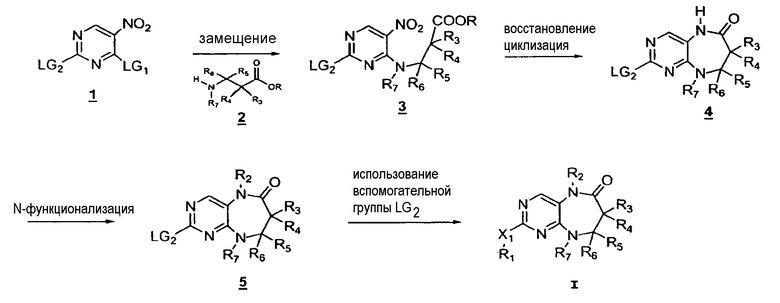
На приведенной выше схеме 1 показан общий способ синтеза соединений формулы I, где Y1 = О. Исходное вещество 1 (где LG1 и LG2 могут представлять собой, без ограничения, атомы хлора) взаимодействует со сложным β-аминоэфиром 2 с получением аддукта 3. Восстановление нитрогруппы с последующей конденсацией с циклизацией дает бициклическое соединение 4. На данной стадии амид N-H можно функционализировать с получением соединения 5. LG2 в конечном счете можно использовать в качестве вспомогательной группы для получения соединений формулы I. На данной последней стадии LG2 можно, например, заместить аминами или подвергнуть катализируемым палладием реакциям присоединения, известным специалистам в данной области (таким как реакции Сузуки и Стилла).
Альтернативно, соединение формулы 3 после восстановления нитрогруппы вначале можно функционализировать с получением соединения формулы 3-b;
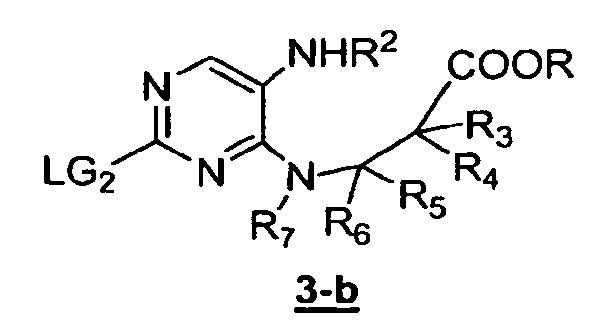
которое затем можно подвергнуть циклизации с получением соединения формулы 5.
Схема 2
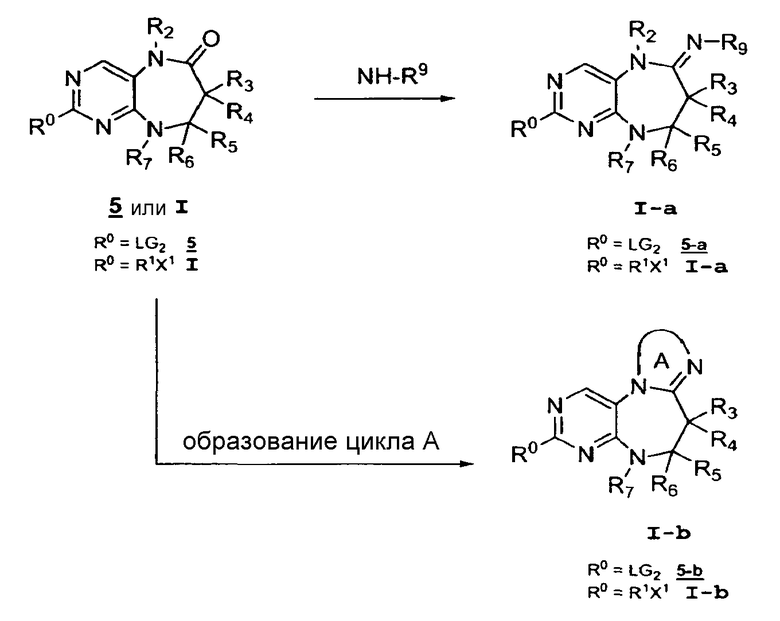
На приведенной выше схеме 2 изображен способ синтеза соединений данного изобретения, в которых Y1 обозначает NR9. Лактамную функциональную группу в соединении 5 или I (в соединении 5 LG2 еще присутствует, а в соединении I она уже дериватизирована с получением R1X1) можно превратить в амидиновую группу (с получением либо соединения 5-a, в котором LG2 еще присутствует, либо соединения I-a, в котором она уже дериватизирована с получением R1X1).
Альтернативно, на приведенной выше схеме 2 также изображен способ синтеза соединений данного изобретения, в которых Y1 = N, а R2 и R9 вместе образуют цикл A. Лактамную функциональную группу в соединении 5 или I (в соединении 5 LG2 еще присутствует, а в соединении I она уже дериватизирована с получением R1X1) посредством многостадийного процесса циклизации можно превратить в цикл А (с получением либо соединения 5-b, в котором LG2 еще присутствует, либо соединения I-b, в котором она уже дериватизирована с получением R1X1).
Схема 3
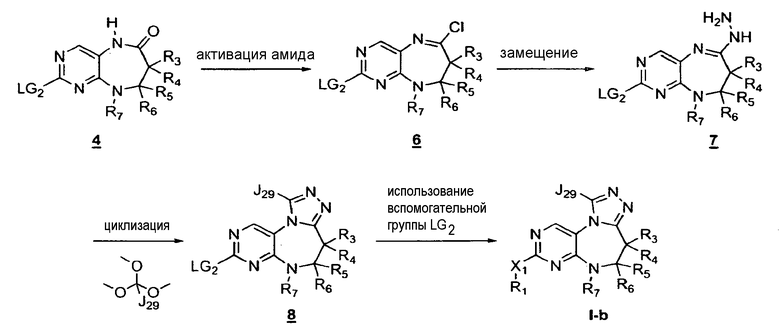
На приведенной выше схеме 3 показан общий способ синтеза соединений данного изобретения, в которых Y1 обозначает NR9, а R2 и R9 вместе образуют триазольный цикл. Активация лактамной функциональной группы в соединении 4 с последующим замещением гидразином приводит к получению промежуточных соединений формулы 1. Соединения формулы I-b в конечном счете получают путем циклизации производных 7 с последующим замещением HX1-R1.
Схема 4
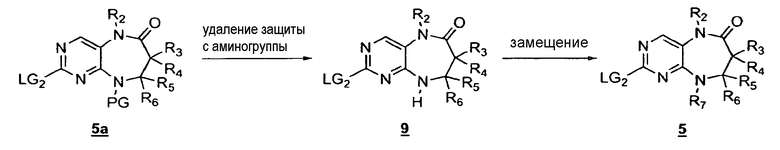
На приведенной выше схеме 4 показан другой общий способ синтеза соединений 5 данного изобретения. Соединения формулы 5a, содержащие защищенную аминогруппу, можно получить с помощью описанного выше способа (см. соединение 5, схема 1). Удаление защиты с аминогрупп соединения 5a и последующее замещение свободных аминов 9 желательными R7-галогенидами можно проводить с помощью хорошо известных в данной области способов.
Соответственно, данное изобретение также предлагает способ получения соединения данного изобретения.
Одно воплощение данного изобретения предлагает способ получения соединения формулы I
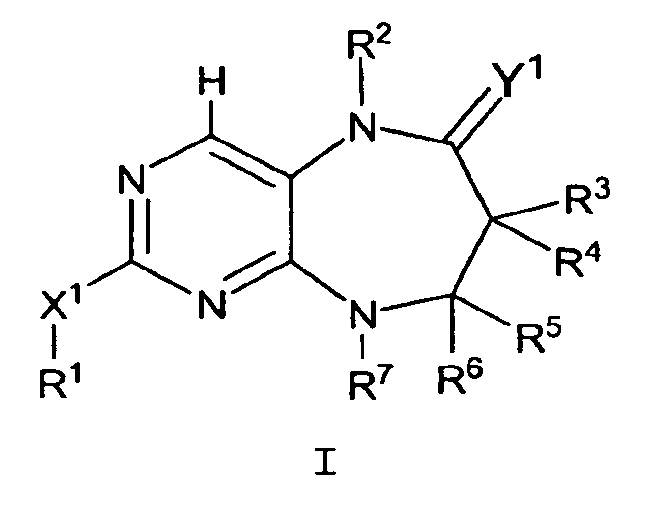
где
Y1 обозначает O, а X1, R1, R2, R3, R4, R5, R6 и R7 имеют указанные в данном описании определения;
включающий в себя взаимодействие соединения формулы 5;
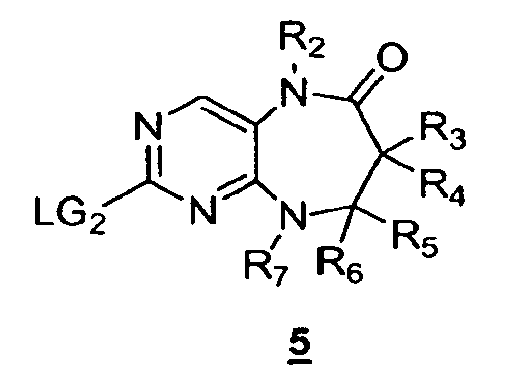
где
R2, R3, R4, R5, R6 и R7 имеют указанные в данном описании определения, а LG2 обозначает подходящую уходящую группу, такую как галоген, с X1R1 в подходящих условиях с получением соединения формулы I. Замену LG2 на X1R1 можно осуществить с помощью ряда способов, известных специалистам в данной области. Например, если X1 обозначает NHR8, O или S, то замену LG2 на X1R1 можно проводить в подходящих условиях в присутствии подходящих основания или кислоты и растворителя. Подходящие реакции замещения известны специалистам в данной области, они описаны в ряде источников, например, в "March's Advanced Organic Chemistry". Серосодержащий линкер (где X1 обозначает S) можно окислить в подходящих условиях с получением соединений, в которых X1 обозначает SO или SO2. Соединения формулы I, где X1 обозначает связь, а R1 связан с X1 через атом углерода, можно получить в подходящих условиях перекрестного сочетания. В указанных реакциях перекрестного сочетания одно из исходных веществ представляет собой R1, связанный с группой, способной участвовать в перекрестном сочетании. Данное исходное вещество может взаимодействовать с соединениями формулы 5 в условиях перекрестного сочетания с получением соединений формулы I, в которых X1 обозначает связь, а R1 связан с X1 через атом углерода.
Термин "реакция перекрестного сочетания" в данном описании относится к реакции, в которой углерод-углеродная связь образуется с помощью металлического катализатора. Обычно один из атомов углерода связан с функциональной группой ("группа, способная участвовать в перекрестном сочетании"), а другой атом углерода связан с галогеном. Примеры реакций перекрестного сочетания включают в себя, без ограничения, реакции сочетания Сузуки, реакции сочетания Стилла и реакции сочетания Негиши.
Термин "группа, способная участвовать в перекрестном сочетании" в данном описании относится к функциональной группе, способной взаимодействовать с другой функциональной группой (например, галогеном) в реакции перекрестного сочетания с образованием углерод-углеродной ("C-C") связи. В некоторых воплощениях связь C-C образуется между двумя ароматическими группами.
Термин "условия перекрестного сочетания" в данном описании относится к химическим условиям (таким как температура, время реакции, объем необходимого растворителя), обеспечивающим протекание реакции перекрестного сочетания.
Примеры групп, способных участвовать в перекрестном сочетании, и соответствующих им условий перекрестного сочетания включают в себя, без ограничения, бороновые кислоты и эфиры бороновых кислот, используемые в условиях реакции сочетания Сузуки, SnBu3, используемый в условиях реакции сочетания Стилла, и ZnX, используемый в условиях реакции сочетания Негиши.
Все три типа условий сочетания обычно включают в себя применение катализатора, подходящего растворителя и, необязательно, основания. Условия реакции сочетания Сузуки включают в себя применение палладиевого катализатора и подходящего растворителя. Примеры подходящих палладиевых катализаторов включают в себя, без ограничения, PdCl2(PPh3)2, Pd(Ph3)4 и PdCl2(dppf). Подходящие основания включают в себя, без ограничения, K2CO3 и Na2CO3. Подходящие растворители включают в себя, без ограничения, тетрагидрофуран, толуол и этанол.
Условия реакции сочетания Стилла включают в себя применение катализатора (обычно палладия, но иногда и никеля), подходящего растворителя и других необязательных реагентов. Примеры подходящих катализаторов включают в себя, без ограничения, PdCl2(PPh3)2, Pd(Ph3)4 и PdCl2(dppf). Подходящие растворители включают в себя, без ограничения, тетрагидрофуран, толуол и диметилформамид.
Условия реакции сочетания Негиши включают в себя применение катализатора (палладия или никеля) и подходящего растворителя. Примеры подходящих катализаторов включают в себя, без ограничения, Pd2(dba)3, Ni(PPh3)2Cl2, PdCl2(PPh3)2 и Pd(Ph3)4. Подходящие растворители включают в себя, без ограничения, тетрагидрофуран, толуол и диметилформамид.
Условия реакций Сузуки, Стилла и Негиши известны специалистам в данной области и описаны более подробно в ряде источников, в том числе в "March's Advanced Organic Chemistry".
Как известно специалистам в данной области, группы, способные участвовать в перекрестном сочетании, образуются из предшественников групп, способных участвовать в реакции сочетании. Предшественник группы, способной участвовать в реакции сочетании, представляет собой реагент или группу реагентов, используемых для получения группы, способной участвовать в перекрестном сочетании. Примеры включают в себя, без ограничения, бис(пинаколато)диборан, используемый для получения эфиров бороновых кислот, триметилбораты, используемые для получения бороновых кислот, Bu3SnCl, используемый для получения станнанов, и ZnCl2, используемый для получения цинкатов в реакциях сочетания Негиши. Примеры подходящих условий получения групп, способных участвовать в перекрестном сочетании, включают в себя, без ограничения, применение палладийсодержащих катализаторов для получения эфиров бороновых кислот; применение условий гидролиза эфиров бороновых кислот для получения бороновых кислот; применение двустадийного процесса, включающего в себя: 1) галоген-металлический обмен с последующим 2) трансметаллированием с использованием Bu3SnCl, для получения станнанов; и применение двустадийного процесса, включающего в себя: 1) галоген-металлический обмен с последующим 2) добавлением ZnCl2, для получения цинкатов.
Другое воплощение предлагает способ получения соединения формулы 5, включающий в себя взаимодействие соединения формулы 4
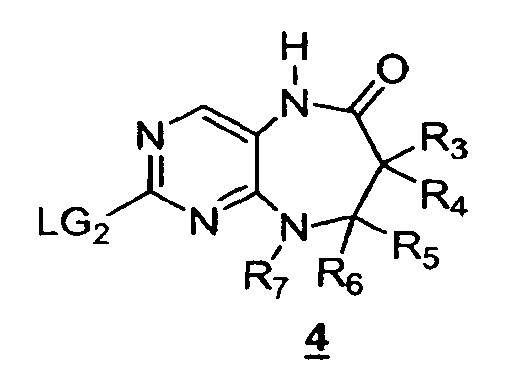
где R3, R4, R5, R6 и R7 имеют указанные в данном описании определения, а LG2 обозначает подходящую уходящую группу, такую как галоген;
с R2-LG3, где LG3 представляет собой уходящую группу, способную замещаться NH-амидом. Примеры уходящих групп включают в себя, без ограничения, галоген, тозилат и мезилат.
Другое воплощение предлагает способ получения соединения формулы 4, включающий в себя двустадийный процесс взаимодействия соединения формулы 3.
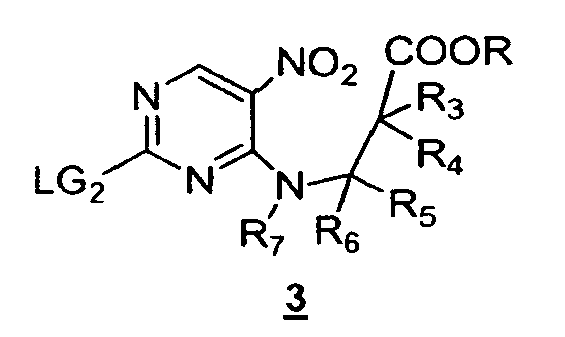
Первая стадия включает в себя восстановление нитрогруппы в подходящих условиях, например, с применением порошкообразного железа, SnCl2, порошкообразного цинка, смесей индий/HCl или H2/Pd с получением соединения формулы 3-a:
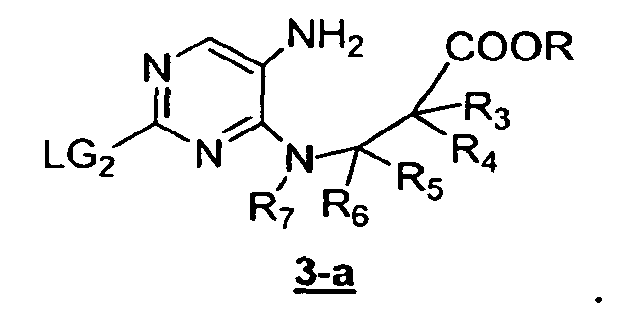
Вторая стадия включает в себя циклоконденсацию амина с эфиром карбоновой кислоты формулы 3-a, приводящую к получению соединения формулы 4. Циклоконденсацию обычно проводят в присутствии кислоты или основания. В некоторых воплощениях указанный двустадийный процесс проводят in situ. Примером условий in situ является обработка нитросодержащего соединения порошкообразным железом в ледяной уксусной кислоте.
В другом аспекте данное изобретение предлагает альтернативный способ получения соединений формулы 5. Вместо непосредственной циклизации соединения формулы 3-a с получением соединения формулы 4, аминосодержащее промежуточное соединение можно вначале функционализировать с получением соединения формулы 3-b
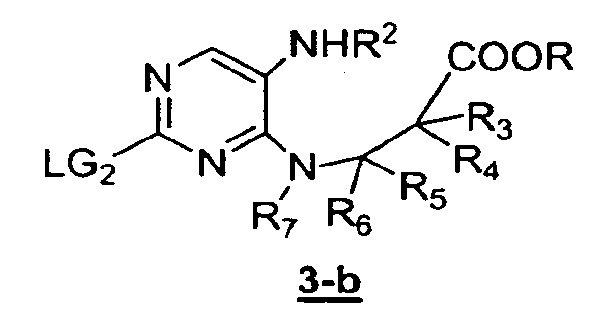
в подходящих условиях, известных специалистам в данной области. Например, аминогруппу можно подвергнуть взаимодействию с R2-LG3, где LG3 представляет собой уходящую группу, способную замещаться амином. Примеры уходящих групп включают в себя, без ограничения, галоген, тозилат и мезилат.
Затем данное соединение можно подвергнуть циклизации в подходящих условиях циклоконденсации с получением соединения формулы 5.
В другом воплощении данное изобретение предлагает способ получения соединения формулы 3, включающий в себя взаимодействие соединения формулы 2
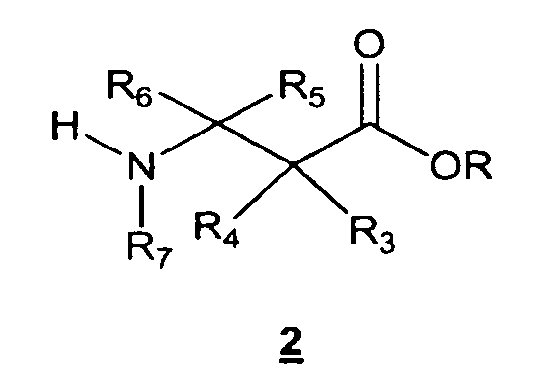
с соединением формулы 1
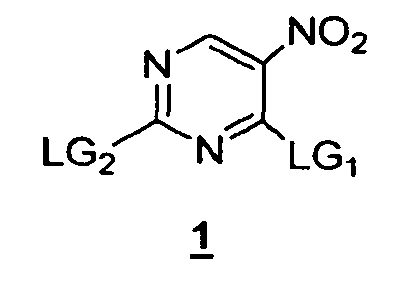
в подходящих условиях замещения с получением соединения формулы 3. Подходящие условия замещения обычно включают в себя применение подходящего растворителя и подходящих основания или кислоты. Примеры подходящих условий замещения включают в себя, без ограничения, применение K2CO3 и ацетона, основание Хунига/THF.
В другом аспекте данное изобретение предлагает способ получения соединения формулы I, где Y1 обозначает NR9. Одно воплощение включает в себя взаимодействие соединения формулы I, в котором Y1 обозначает O, а X1, R1, R2, R3, R4, R5, R6 и R7 имеют указанные в данном описании определения; в подходящих условиях, известных в данной области, обеспечивающих превращение амидов в амидины, с получением соединения формулы I, в котором Y1 обозначает NR9 (показанного на схеме II как I-a). Подходящие условия обычно включают в себя применение амина (R1-NHR9), подходящего растворителя и активированного промежуточного соединения, полученного из амида (например, тиоамида полученного в результате взаимодействия амида с реагентом Лоуссона).
В другом аспекте соединение формулы 5 можно подвергнуть воздействию условий, подобных используемым для превращения амида, с получением соединения формулы 5-a. Группу LG2 в соединениях 5-a или 5-b можно использовать в качестве вспомогательной группы для получения соединений данного изобретения. На данной последней стадии LG2 можно, например, заменить аминами или подвергнуть реакциям сочетания, катализируемым палладием (например, Сузуки, Стилла).
В некоторых воплощениях соединения формулы I или 5, в которых Y1 обозначает O, а X1, R1, R2, R3, R4, R5, R6 и R7 имеют указанные в данном описании определения, можно превратить в циклические амидины, где R2 и R9 вместе образуют цикл A. Указанные циклические амидины (показанные на схеме II как I-b) можно получить посредством многостадийного процесса циклизации. Цикл A может варьировать по размеру (например, он может быть 5-8-членным) и по степени ненасыщенности. Например, цикл A можно получить с помощью способов, подобных описанным в: J. Am. Chem. Soc, 103 (14), 4186-4194, 1981; J. Het. Chem., 19(1), 193-200, 1982; Angew. Chem., 43(4), 478-482, 2004; Scientia Pharm., 57(1), 27-38, 1989; Tetrahedron Lett., 16(2), 449-469, 2005; J. Org. Chem., 59 (17), 5084-5087, 1994. Группу LG2 в соединениях 5-a или 5-b можно использовать в качестве вспомогательной группы для получения соединений данного изобретения. На данной последней стадии LG2 можно, например, заменить аминами или подвергнуть реакциям сочетания, катализируемым палладием (например, Сузуки, Стилла).
В другом аспекте данное изобретение предлагает соединения, которые являются ингибиторами протеинкиназ и, следовательно, наряду с другими применениями, описанными в данном документе, могут использоваться для лечения заболеваний, нарушений и состояний. В другом аспекте настоящее изобретение предлагает фармацевтически приемлемые композиции, где указанные композиции содержат одно из описанных в данном документе соединений и необязательно фармацевтически приемлемые носитель, адъювант или среду. В некоторых воплощениях указанные композиции также необязательно содержат одно или несколько других терапевтических средств.
Настоящее изобретение предлагает соединения и композиции, которые можно использовать в качестве ингибиторов протеинкиназ. В некоторых воплощениях протеинкиназы представляют собой PLK. В некоторых воплощениях PLK1.
Как ингибиторы протеинкиназ соединения и композиции данного изобретения в особенности подходят для лечения или уменьшения тяжести заболевания, состояния или нарушения, в развитии которого участвует протеинкиназа. В одном аспекте настоящее изобретение предлагает способ лечения или уменьшения тяжести заболевания, состояния или нарушения, где протеинкиназа участвует в развитии болезненного состояния. В другом аспекте настоящее изобретение предлагает способ лечения или уменьшения тяжести опосредованного киназой заболевания, состояния или нарушения, где ингибирование ферментативной активности вносит вклад в лечение заболевания. В другом аспекте настоящее изобретение предлагает способ лечения или уменьшения тяжести заболевания, состояния или нарушения с помощью соединения, которое ингибирует ферментативную активность путем связывания с протеинкиназой. В другом аспекте настоящее изобретение предлагает способ лечения или уменьшения тяжести опосредованного киназой заболевания, состояния или нарушения путем ингибирования ферментативной активности киназы с помощью ингибитора протеинкиназы.
В некоторых воплощениях, указанный ингибитор протеинкиназы представляет собой ингибитор PLK.
В одном аспекте настоящее изобретение относится к способу ингибирования активности протеинкиназы у пациента, данный способ включает в себя введение пациенту соединения формулы I или композиции, содержащей указанное соединение.
В некоторых воплощениях указанный способ используют для лечения или профилактики состояния, выбранного из аутоиммунных заболеваний, воспалительных заболеваний, пролиферативных и гиперпролиферативных заболеваний, заболеваний, опосредованных иммунной системой, заболеваний костей, метаболических заболеваний, неврологических и нейродегенеративных заболеваний, сердечно-сосудистых заболеваний, гормональных заболеваний, аллергий, астмы и болезни Альцгеймера. В некоторых воплощениях указанная протеинкиназа представляет собой PLK. В других воплощениях указанное состояние выбрано из пролиферативного нарушения и нейродегенеративного нарушения.
В зависимости от конкретных подлежащих лечению или профилактике состояний, опосредуемых протеинкиназами, вместе с ингибиторами настоящего изобретения можно вводить другие лекарственные средства, которые обычно используют для лечения или профилактики данных состояний. Например, для лечения пролиферативных заболеваний ингибиторы протеинкиназ данного изобретения можно объединять с химиотерапепевтическими или другими антипролиферативными средствами.
В рамках множественного режима дозирования указанные другие средства можно вводить отдельно от соединения или композиции, содержащих ингибитор протеинкиназы. Альтернативно данные средства в смеси с ингибитором протеинкиназы могут входить в состав одной композиции и являться частью одной лекарственной формы.
Как ингибиторы протеинкиназ соединения и композиции данного изобретения также можно использовать в биологических образцах. Один аспект данного изобретения относится к способу ингибирования активности протеинкиназы в биологическом образце, причем данный способ включает в себя приведение в контакт указанного биологического образца с соединением формулы I или с композицией, содержащей указанное соединение. Термин "биологический образец" в данном описании относится к in vitro или ex vivo образцу, включающему в себя, без ограничения, клеточные культуры и их экстракты; биопсийные образцы, полученные от млекопитающего, или их экстракты; а также кровь, слюну, мочу, фекалии, семенную жидкость, слезы или другие жидкости организма и их экстракты.
Ингибирование активности протеинкиназы в биологическом образце осуществляют с разными целями, известными специалистам в данной области. Примеры таких целей включают в себя, без ограничения, переливание крови, трансплантацию органов и хранение биологического образца.
Другой аспект данного изобретения относится к исследованию роли протеинкиназ в биологических и патологических явлениях; к исследованию путей внутриклеточной передачи сигнала, опосредованных такими протеинкиназами; и к сравнительному анализу новых ингибиторов протеинкиназ. Примеры таких способов применения включают в себя, без ограничения, биологические анализы, такие как ферментативные анализы и клеточные анализы.
Активность соединений, связанную с ингибированием протеинкиназ, можно анализировать in vitro, in vivo или в клеточной линии. In vitro анализы включают в себя анализы ингибирования, либо киназной активности, либо АТФ-азной активности активированной киназы. Другие анализы in vitro позволяют количественно определять способность ингибитора связываться с протеинкиназой, которую измеряют либо путем радиоактивного мечения ингибитора перед связыванием с последующим выделением комплекса ингибитор/киназа и определением связанной радиоактивной метки, либо путем анализа конкурентного связывания, в котором новые ингибиторы инкубируют с киназой, связанной с известными радиоактивномеченными лигандами. Условия анализов соединений, используемых в данном изобретении в качестве ингибиторов PLK1, PLK2, PLK3 и PLK4 подробно описаны ниже в разделе Примеры.
В одном аспекте данное изобретение предлагает соединения, которые можно использовать для лечения заболеваний, нарушений и состояний, характеризующихся избыточной или аномальной пролиферацией клеток. Такие заболевания включают в себя пролиферативные или гиперпролиферативные заболевания и нейродегенеративные заболевания.
Примеры пролиферативных и гиперпролиферативных заболеваний включают в себя, без ограничения, рак.
Термин "рак" включает в себя, без ограничения, следующие раковые заболевания: рак молочной железы; рак яичника; рак шейки матки; рак простаты; рак яичка, рак мочеполового тракта; рак пищевода; рак гортани, глиобластому; нейробластому; рак желудка; рак кожи, кератоакантому; рак легких, эпидермоидный рак, крупноклеточный рак, мелкоклеточный рак, аденокарциному легких; рак кости; рак толстой кишки; рак толстой и прямой кишки; аденому; рак поджелудочной железы, аденокарциному; рак щитовидной железы, фолликулярную карциному, недифференцированную карциному, папиллярную карциному; семиному; меланому; саркому; рак мочевого пузыря; рак печени и желчных протоков; рак почки; миелоидные нарушения; лимфоидные нарушения, болезнь Ходжкина, лейкоз ворсистых клеток; рак щечного кармана и глотки (полости рта), губы, языка, рта, глотки; рак тонкого кишечника; рак толстой и прямой кишки, рак толстой кишки, рак прямой кишки; рак мозга и центральной нервной системы; хронический миелоидный лейкоз (CML) и лейкоз. Термин "рак" включает в себя, без ограничения, следующие раковые заболевания: миелому, лимфому или раковое заболевание, выбранное из рака желудка, почек, или следующие раковые заболевания: рак головы и шеи, рак ротоглоточной области, немелкоклеточный рак легких (NSCLC), рак эндометрия, гепатокарциному, неходжкинскую лимфому и рак легких.
Во избежание сомнений следует отметить, что термин "рак" также включает в себя, без ограничений: эпидермоидные раковые заболевания ротовой полости: щечного кармана, губ, языка, рта, глотки; раковые заболевания сердца: такие как саркома (ангиосаркома, фибросаркома, рабдомиосаркома, липосаркома), миксома, рабдомиома, фиброма, липома и тератома; раковые заболевания легких: бронхогенный рак (плоскоклеточный или эпидермоидный, недифференцированный мелкоклеточный, недифференцированный крупноклеточный, аденокарцинома), альвеолярный (бронхиолярный) рак, бронхиальная аденома, саркома, лимфома, хондроматозная гамартома, мезотелиома; раковые заболевания желудочно-кишечного тракта: рак пищевода (плоскоклеточная карцинома, рак гортани, аденокарцинома, лейомиосаркома, лимфома), рак желудка (карцинома, лимфома, лейомиосаркома), рак поджелудочной железы (аденокарцинома протоков, инсулинома, глюкагонома, гастринома, карциноидные опухоли, випома), рак тонкой кишки или тонкого кишечника (аденокарцинома, лимфома, карциноидные опухоли, саркома Капоши, лейомиома, гемангиома, липома, нейрофиброма, фиброма), рак толстой кишки или толстого кишечника (аденокарцинома, тубулярная аденома, ворсинчатая аденома, гамартома, лейомиома), рак толстой кишки, рак толстой и прямой кишки, рак ободочной и прямой кишки; рак прямой кишки, раковые заболевания мочеполового тракта: рак почек (аденокарцинома, опухоль Вильмса [нефробластома], лимфома, лейкоз), рак мочевого пузыря и уретры (плоскоклеточная карцинома, переходно-клеточная карцинома, аденокарцинома), рак простаты (аденокарцинома, саркома), рак яичек (семинома, тератома, эмбриональная карцинома, тератокарцинома, хориокарцинома, саркома, интерстициально-клеточная карцинома, фиброма, фиброаденома, аденоматоидные опухоли, липома); раковые заболевания печени: гепатома (гепатоцеллюлярная карцинома), холангиокарцинома, гепатобластома, ангиосаркома, гепатоцеллюлярная аденома, гемангиома, рак желчных протоков; раковые заболевания костей: остеогенная саркома (остеосаркома), фибросаркома, злокачественная фиброзная гистиоцитома, хондросаркома, саркома Юинга, злокачественная лимфома (ретикулоклеточная саркома), множественная миелома, злокачественная гигантоклеточная хордома, остеохронфрома (костно-хрящевой экзостоз), доброкачественная хондрома, хондробластома, хондромиксоидная фиброма, остеоид-остеома и гигантоклеточные опухоли; раковые заболевания нервной системы: рак черепа (остеома, гемангиома, гранулома, ксантома, деформирующий остит), рак мозговой оболочки (менингиома, менингиосаркома, глиоматоз), рак мозга (астроцитома, медуллобластома, глиома, эпендимома, герминома [пинеалома], полиморфная глиобластома, олигодендроглиома, шваннома, ретинобластома, наследственные опухоли), нейрофиброма спинного мозга, менингиома, глиома, саркома); гинекологические раковые заболевания: рак матки (карцинома эндометрия), рак шейки матки (карцинома шейки матки, предопухолевая дисплазия шейки матки), рак яичников (карцинома яичников [серозная цистаденокарцинома, слизеобразующая цистаденокарцинома, неклассифицированная карцинома], гранулозо-текально-клеточные опухоли, опухоли из клеток Сертоли-Лейдига, дисгерминома, злокачественная тератома), рак наружных женских половых органов (плоскоклеточная карцинома, внутриэпителиальная карцинома, аденокарцинома, фибросаркома, меланома), рак влагалища (светлоклеточная карцинома, плоскоклеточная карцинома, ботриоидная саркома (эмбриональная рабдомиосаркома), рак фаллопиевых труб (карцинома), рак молочной железы; гематологические раковые заболевания: рак крови (миелоидный лейкоз [острый и хронический], острый лимфобластный лейкоз, хронический лимфолейкоз, миелопролиферативные заболевания, множественная миелома, миелодиспластический синдром), болезнь Ходжкина, неходжкинская волосатоклеточная лимфома [злокачественная лимфома]; лимфоидные нарушения; раковые заболевания кожи: злокачественная меланома, базально-клеточная карцинома, плоскоклеточная карцинома, саркома Капоши, кератоакантома, диспластические невоидные опухоли родинок, липома, ангиома, дерматофиброма, келоиды, псориаз, раковые заболевания щитовидной железы: папиллярная карцинома щитовидной железы, фоликулярная карцинома щитовидной железы; медуллярная карцинома щитовидной железы, недифференцированный рак щитовидной железы, множественная эндокринная неоплазия типа 2A, множественная эндокринная неоплазия типа 2B, семейный медуллярный рак щитовидной железы, феохромоцитома, параганглиома; и раковые заболевания надпочечников: нейробластома. Таким образом, термин "раковая клетка" в данном описании включает в себя клетку, участвующую в одном из вышеуказанных состояний.
В некоторых воплощениях соединения данного изобретения можно использовать для лечения рака, такого как рак толстой и прямой кишки, щитовидной железы, молочной железы и легкого; миелопролиферативных нарушений, таких как истинная полицитемия, тромбоцитемия, миелоидная метаплазия с миелофиброзом, хронический миелолейкоз, хронический миеломоноцитарный лейкоз, гиперэозинофильный синдром, ювенильный миеломоноцитарный лейкоз и системный мастоцитоз.
В некоторых воплощениях соединения данного изобретения можно использовать для лечения гематопоэтических нарушений, таких как острый миелобластный лейкоз (AML), хронический миелолейкоз (CML), острый промиелоцитарный лейкоз (APL) и острый лимфолейкоз (ALL).
Примеры нейродегеративных заболеваний включают в себя, без ограничения, болезнь Альцгеймера.
Другой аспект данного изобретения предлагает способ лечения или уменьшения тяжести заболевания, выбранного из пролиферативного, или гиперпролиферативного заболевания, или нейродегеративного заболевания, включающий в себя введение эффективного количества соединения или фармацевтически приемлемой композиции, содержащей соединение, субъекту, нуждающемуся в таком введении.
В некоторых воплощениях "эффективное количество" соединения или фармацевтически приемлемой композиции представляет собой количество, эффективное для лечения указанного заболевания. Соединения и композиции в соответствии со способом настоящего изобретения можно вводить в любом количестве и с помощью любого способа введения, обеспечивающих эффективное лечение или уменьшение тяжести указанного заболевания.
В некоторых воплощениях указанное заболевание представляет собой состояние, опосредованное протеинкиназой. В некоторых воплощениях указанное заболевание представляет собой PLK-опосредованное заболевание.
Термин "состояние, опосредованное протеинкиназой" в данном описании относится к любому заболеванию или другому болезнетворному состоянию, в развитии которого участвует протеинкиназа. Такие состояния включают в себя, без ограничения, аутоиммунные заболевания, воспалительные заболевания, пролиферативные и гиперпролиферативные заболевания, иммунологические заболевания, заболевания костей, метаболические заболевания, неврологические и нейродегенеративные заболевания, сердечно-сосудистые заболевания, гормональные заболевания, аллергии, астму и болезнь Альцгеймера.
Термин "PLK-опосредованное состояние" в данном описании относится к любому заболеванию или другому болезнетворному состоянию, в развитии которого участвует PLK. Такие состояния включают в себя, без ограничения, пролиферативное или гиперпролиферативное заболевание или нейродегеративное заболевание.
В другом аспекте настоящее изобретение предлагает фармацевтически приемлемые композиции, которые содержат любое из описанных в данном документе соединений и необязательно фармацевтически приемлемые носитель, адъювант или среду.
В некоторых воплощениях указанные композиции необязательно дополнительно содержат одно или несколько других терапевтических средств.
Например, для лечения пролиферативных заболеваний и рака соединения данного изобретения можно объединять с химиотерапевтическими или другими антипролиферативными средствами.
Примеры известных химиотерапевтических средств включают в себя, без ограничения, GleevecTM, адриамицин, дексаметазон, винкристин, циклофосфамид, фторурацил, топотекан, таксол, интерфероны и производные платины.
Другие примеры средств, с которыми можно сочетать ингибиторы данного изобретения, включают в себя, без ограничения: средства против болезни Альцгеймера, такие как Aricept® и Excelon®; средства против болезни Паркинсона, такие как L-DOPA/карбидопа, энтакапон, ропинрол, прамипексол, бромкриптин, перголид, тригексефендил и амантадин; средства против рассеянного склероза (MS), такие как бета-интерферон (например, Avonex® и Rebif®), Copaxone® и митоксантрон; средства против астмы, такие как альбутерол и Singulair®; средства против шизофрении, такие как зипрекса, риспердал, сероквел и галоперидол; противовоспалительные средства, такие как кортикостероиды, блокаторы TNF, IL-1 RA, азатиоприн, циклофосфамид и сульфасалазан; иммуномодулирующие и иммуносупрессивные средства, такие как циклоспорин, такролимус, рапамицин, микофенолята мофетил, интерфероны, кортикостероиды, циклофосфамид, азатиоприн и сульфасалазин; нейротрофические факторы, такие как ингибиторы ацетилхолинэстеразы, ингибиторы MAO, интерфероны, противосудорожные средства, блокаторы ионных каналов, рилузол и противопаркинсонические средства; средства против сердечно-сосудистых заболеваний, такие как бета-блокаторы, ингибиторы ACE, диуретики, нитраты, блокаторы кальциевых каналов и статины; средства против заболеваний печени, такие как кортикостероиды, холестирамин, интерфероны и противовирусные средства; средства против заболеваний крови, такие как кортикостероиды, противолейкемические средства и факторы роста; и средства против иммунодефицитных состояний, такие как гамма-глобулин.
Как указано в данном описании, фармацевтически приемлемые композиции настоящего изобретения дополнительно содержат фармацевтически приемлемые носители, адъюванты или среды, которые в соответствии с данным описанием включают в себя все и любые растворители, разбавители или другие жидкие среды, средства, облегчающие диспергирование или суспендирование, поверхностно-активные вещества, изотонические средства, загущающие или эмульгирующие средства, консерванты, твердые связующие средства, смазывающие средства и т.п., подходящие для конкретной желательной лекарственной формы. В Remington's Pharmaceutical Sciences, Sixteenth Edition, E. W. Martin (Mack Publishing Co., Easton, Pa., 1980) описаны разные носители, используемые для получения фармацевтически приемлемых композиций, а также известные способы получения таких композиций. Все традиционные среды-носители входят в объем настоящего изобретения за исключением сред, не совместимых с соединениями данного изобретения, например, в результате вызываемых ими нежелательных биологических эффектов или взаимодействия с любым другим компонентом (компонентами), приводящего к вредным последствиям.
Некоторые примеры веществ, которые могут служить фармацевтически приемлемыми носителями, включают в себя, без ограничения, ионообменные вещества, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как человеческий сывороточный альбумин, забуферивающие вещества, такие как фосфаты, глицин, сорбиновая кислота или сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, вода, соли или электролиты, такие как протаминсульфат, гидрофосфат динатрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный оксид кремния, трисиликат магния, поливинилпирролидон, полиакрилаты, воски, блок-полимеры полиэтилен-полиоксипропилен, ланолин, сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлоза и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; наполнители, такие как кокосовое масло и свечные воски; масла, такие как арахисовое масло, хлопковое масло; сафлоровое масло; кунжутное масло; оливковое масло; кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль или полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; забуферивающие средства, такие как гидроксид магния и гидроксид алюминия; альгиновая кислота; апирогенная вода; изотонический физиологический раствор; раствор Рингера; этиловый спирт и растворы фосфатного буфера, а также другие нетоксичные совместимые смазывающие средства, такие как лаурилсульфат натрия и стеарат магния, кроме того, в соответствии с рекомендациями специалиста в состав композиций также могут быть введены красители, средства, регулирующие высвобождение, покрытия, подсластители, ароматизаторы и отдушки, консерванты и антиоксиданты.
На основе ингибиторов протеинкиназ или их фармацевтических солей можно получить фармацевтические композиции для введения животным или людям. Данные фармацевтические композиции, содержащие ингибитор проинкиназы в количестве, эффективном для лечения или профилактики состояния, опосредованного протеинкиназой, и фармацевтически приемлемый носитель, составляют другое воплощение настоящего изобретения. В некоторых воплощениях указанное протеинкиназа-опосредованное состояние представляет собой PLK-опосредованное состояние.
Точное, требующееся для лечения количество соединения варьирует от субъекта к субъекту в зависимости от вида, возраста, общего состояния субъекта, тяжести инфекции, конкретного средства, способа его введения и т.п. Для простоты введения и единообразия дозирования композиции на основе соединений данного изобретения предпочтительно получают в виде стандартных лекарственных форм. Выражение "стандартная лекарственная форма" в данном описании относится к физически дискретной единице средства, подходящей для лечения пациента. Однако следует понимать, что общая дневная доза соединений и композиций настоящего изобретения устанавливается лечащим врачом в рамках обоснованного медицинского заключения. Конкретный уровень эффективной дозы для конкретного пациента или организма зависит от ряда факторов, включающих в себя вид нарушения, подлежащего лечению, и тяжесть нарушения; активность конкретного используемого соединения; вид конкретной используемой композиции; возраст, массу тела, общее состояние здоровья, пол и диету пациента; время введения, способ введения и скорость экскреции конкретного используемого соединения; длительность лечения; лекарственные средства, применяющиеся в сочетании или совместно с конкретным используемым соединением, а также подобные факторы, хорошо известные в области медицины. Термин "пациент" в данном описании относится к животному, предпочтительно млекопитающему, наиболее предпочтительно, человеку.
Фармацевтически приемлемые композиции данного изобретения можно вводить людям и другим животным перорально, ректально, парентерально, интрацистернально, интравагинально, внутрибрюшинно, местно (например, в виде порошков, мазей или капель), трансбуккально, например, в виде перорального или назального спрея и т.п., в зависимости от тяжести инфекции, подлежащей лечению. В некоторых воплощениях, чтобы получить желательный терапевтический эффект, соединения данного изобретения вводят перорально или парентерально в дозах, составляющих приблизительно от 0,01 мг/кг до 50 мг/кг, предпочтительно приблизительно от 1 мг/кг до 25 мг/кг массы тела субъекта в день, один или несколько раз в день. В предпочтительном воплощении соединения данного изобретения вводят перорально.
Жидкие дозировочные формы для перорального введения включают в себя, без ограничения, фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. Помимо активного соединения жидкие дозировочные формы могут содержать инертные разбавители, обычно используемые в данной области, такие как, например, вода или другие растворители, солюбилизирующие средства и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в особенности, хлопковое, арахисовое, кукурузное, зародышевое, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и эфиры жирных кислот и сорбитана, а также их смеси. Кроме инертных разбавителей пероральные композиции могут содержать адъюванты, такие как увлажняющие средства, эмульгирующие и суспендирующие средства, подслащивающие средства, отдушки и ароматизирующие средства.
Препараты для инъекций, например, стерильные водные или масляные суспензии для инъекций, можно получить в соответствии с известными в данной области способами, с использованием подходящих диспергирующих или увлажняющих средств и суспендирующих средств. Стерильный препарат для инъекций также может представлять собой инъецируемый стерильный раствор, суспензию или эмульсию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, раствор в 1,3-бутандиоле. К пригодным для использования приемлемым средам и растворителям относятся вода, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды часто используют стерильные жирные масла. Для данной цели можно использовать любое легкое жирное масло, в том числе моно- или диглицериды. Для получения инъецируемых препаратов также можно использовать жирные кислоты, такие как олеиновая кислота.
Композиции для инъекций можно стерилизовать, например, путем фильтрации через фильтр, удерживающий бактерии, или путем использования стерилизующих средств в составе стерильных твердых композиций, которые перед применением можно растворить или диспергировать в стерильной воде или другой среде для инъекций.
Чтобы продлить эффект соединения настоящего изобретения, зачастую желательно замедлить абсорбцию соединения при подкожной или внутримышечной инъекции. Это можно осуществить путем применения жидкой суспензии кристаллического или аморфного вещества с плохой растворимостью в воде. Скорость абсорбции соединения завит от скорости его растворения, которая в свою очередь может зависеть от размера и формы кристаллов. Альтернативно, замедленную абсорбцию парентерально вводимого соединения можно достичь путем растворения или суспендирования соединения в масляной среде. Инъецируемые депо получают путем заключения матриц, содержащих соединения, в микрокапсулы из биоразрушаемых полимеров, таких как полилактид-полигликолид. Скорость высвобождения соединения зависит от соотношения соединения к полимеру и природы конкретного используемого полимера. Примеры других биоразрушаемых полимеров включают в себя сложные поли(ортоэфиры) и поли(ангидриды). Композиции инъецируемых депо также получают путем улавливания соединения в липосомах или микроэмульсиях, совместимых с тканями организма.
Композиции для ректального или вагинального введения предпочтительно представляют собой свечи, которые можно получить путем смешивания соединений данного изобретения с подходящими нераздражающими наполнителями или носителями, такими как кокосовое масло, полиэтиленгликоль или свечной воск, которые при температуре окружающей среды находятся в твердом виде, а при температуре организма являются жидкими, и, следовательно, плавятся в прямой кишке или вагинальной полости, высвобождая активное соединение.
Твердые дозировочные формы для перорального введения включают в себя капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых дозировочных формах активное соединение находится в смеси, по меньшей мере, с одним инертным, фармацевтически приемлемым наполнителем или носителем, таким как цитрат натрия или фосфат дикальция и/или a) наполнителями или разбавителями, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота, b) связующими средствами, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и гуммиарабик; c) средствами, удерживающими влагу, такими как глицерин, d) дезинтегрирующими средствами, такими как агар-агар, карбонат кальция, картофельный крахмал или крахмал из кассавы, альгиновая кислота, некоторые силикаты и карбонат натрия, e) средствами, замедляющими растворение, такими как парафин, f) ускорителями абсорбции, такими как соединения четвертичного аммония, g) увлажняющими средствами, такими как, например, цетиловый спирт и моностеарат глицерина, h) абсорбентами, такими как каолин и бентонитовая глина, и i) смазывающими средствами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия, а также с их смесями. В случае капсул, таблеток и пилюль лекарственная форма также может содержать забуферивающие средства.
Твердые композиции подобного типа, содержащие такие наполнители, как лактоза или молочный сахар, высокомолекулярные полиэтиленгликоли и т.п., также можно использовать в качестве наполнителей мягких и твердых желатиновых капсул. Такие твердые лекарственные формы, как таблетки, драже, капсулы, пилюли и гранулы, могут иметь покрытия и оболочки, например, энтеросолюбильные покрытия или другие покрытия, хорошо известные в области фармацевтики. Композиции энтеросолюбильных покрытий могут необязательно содержать замутняющие средства и могут обеспечивать высвобождение активного ингредиента (ингредиентов) только, или предпочтительно, в определенной части кишечного тракта, необязательно, в замедленной манере. Примеры пригодных к использованию заключенных композиций содержат полимерные вещества и воски. Твердые композиции подобного типа, содержащие такие наполнители, как лактоза или молочный сахар, высокомолекулярные полиэтиленгликоли и т.п., также можно использовать в качестве наполнителей мягких и твердых желатиновых капсул.
Активные соединения также могут быть заключены в микрокапсулы с использованием одного или нескольких наполнителей, как указано выше. Такие твердые лекарственные формы, как таблетки, драже, капсулы, пилюли и гранулы, могут иметь покрытия и оболочки, например, энтеросолюбильные покрытия, покрытия, обеспечивающие контролируемое высвобождение, или другие покрытия, хорошо известные в области фармацевтики. В таких твердых лекарственных формах активное соединение может находиться в смеси, по меньшей мере, с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие лекарственные формы в рамках обычной практики также могут содержать другие вещества, отличные от инертных разбавителей, например, смазывающие средства для таблетирования, а также другие вспомогательные средства, используемые при таблетировании, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль лекарственные формы также могут содержать забуферивающие средства. Такие композиции могут необязательно содержать замутняющие средства и могут обеспечивать высвобождение активного ингредиента (ингредиентов) только, или предпочтительно, в определенной части кишечного тракта, необязательно, в замедленной манере. Примеры пригодных к использованию заключенных композиций содержат полимерные вещества и воски.
Лекарственные формы для местного или трансдермального введения соединения данного изобретения включают в себя мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, лекарственные формы для ингаляций или пластыри. Активный компонент смешивают в стерильных условиях с фармацевтически приемлемым носителем и, при необходимости, с любыми желательными консервантами или буферами. В объем данного изобретения также входят офтальмические композиции, ушные капли и глазные капли. Кроме того, настоящее изобретение охватывает применение пластырей для трансдермального введения, дополнительное преимущество которых заключается в обеспечении контролируемой доставки соединения в организм. Такие лекарственные формы можно получить путем растворения или диспергирования соединения в подходящей среде. Для увеличения проникновения соединения через кожу также можно использовать усилители абсорбции. Скорость абсорбции можно контролировать либо путем использования мембраны, регулирующей скорость проникновения, либо путем диспергирования соединения в полимерном матриксе или геле.
В состав композиций для лечения или профилактики вышеуказанных нарушений помимо соединений данного изобретения могут входить их фармацевтически приемлемые производные или лекарственные формы.
Соединения данного изобретения также могут существовать в виде фармацевтически приемлемых производных.
"Фармацевтически приемлемое производное" представляет собой аддукт или производное, которое при введении пациенту, нуждающемуся в этом, способно образовывать, непосредственно или косвенно, соединение, описанное в данном документе выше, или его метаболит, или остаток. Примеры фармацевтически приемлемых производных включают в себя, без ограничения, сложные эфиры и соли таких сложных эфиров.
"Фармацевтически приемлемые производные или пролекарственные формы" представляют собой любые фармацевтически приемлемые сложные эфиры, соли сложных эфиров или другие производные соединений данного изобретения, которые при введении реципиенту способны предоставлять, непосредственно или косвенно, соединение данного изобретения, или его метаболит, или остаток, обладающий ингибиторной активностью. Особенно предпочтительные производные или пролекарственные формы способны повышать биодоступность соединений данного изобретения при введении пациенту (например, путем увеличения поступления в кровь перорально вводимого соединения) или увеличивать доставку исходного соединения в биологический компартмент (например, мозг или лимфатическую систему) по сравнению с исходными формами.
Фармацевтически приемлемые пролекарственные формы соединений данного изобретения включают в себя, без ограничения, сложные эфиры, сложные эфиры аминокислот, эфиры фосфорной кислоты, соли металлов и эфиры сульфокислот.
Фармацевтически приемлемые носители, которые можно использовать в указанных фармацевтических композициях, включают в себя, без ограничения, ионообменные смолы, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как человеческий сывороточный альбумин, забуферивающие средства, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как протаминсульфат, гидрофосфат динатрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный оксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, карбоксиметилцеллюлоза натрия, полиакрилаты, воски, блок-полимеры полиэтилен-полиоксипропилен, полиэтиленгликоль и ланолин.
Композиции настоящего изобретения можно вводить перорально, парентерально, в виде спрея для ингаляции, местно, ректально, назально, трансбуккально, вагинально или посредством имплантируемого резервуара. Термин "парентеральный" в данном описании включает в себя, без ограничения, подкожный, внутривенный, внутримышечный, внутрисуставный, внутрисиновиальный, надчревный, интратекальный, внутрипеченочный, в участок повреждения и внутричерепной способы инъекции или инфузии. Предпочтительно композиции вводят перорально, внутрибрюшинно или внутривенно.
Стерильные инъецируемые формы композиций данного изобретения могут представлять собой водные или масляные суспензии. Такие суспензии могут быть получены с помощью известных в данной области способов с использованием подходящих диспергирующих или увлажняющих и суспендирующих средств. Стерильный инъецируемый препарат также может представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, раствор в 1,3-бутандиоле. К пригодным для использования приемлемым средам и растворителям относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды часто используют стерильные жирные масла. Для данной цели можно использовать любое легкое жирное масло, в том числе моно- или диглицериды. Для получения инъецируемых препаратов также можно использовать жирные кислоты, такие как олеиновая кислота, и ее глицеридные производные, например, природные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно их полиоксиэтилированные производные. Указанные масляные растворы или суспензии также могут содержать длинноцепочечный спирт в качестве разбавителя или диспергирующее средство, такое как карбоксиметилцеллюлоза, или подобное диспергирующее средство, обычно используемое для получения фармацевтически приемлемых лекарственных форм, включающих в себя эмульсии и суспензии. Для получения композиций также можно использовать поверхностно-активные вещества, такие как Tweens, Spans, а также другие эмульгирующие средства или усилители биодоступности, которые традиционно используются в производстве фармацевтически приемлемых твердых, жидких или других лекарственных форм.
Фармацевтические композиции данного изобретения можно вводить перорально в виде любой перорально приемлемой лекарственной формы, включающей в себя, без ограничения, капсулы, таблетки, водные суспензии или растворы. В случае таблеток для перорального применения традиционно используемые носители включают в себя, без ограничения, лактозу и кукурузный крахмал. Кроме того, обычно добавляют смазывающие средства, такие как стеарат магния. Для получения капсульных форм для перорального введения используют такие разбавители, как лактоза и сухой кукурузный крахмал. В случае водных суспензий для перорального применения активный ингредиент объединяют с эмульгирующими и суспендирующими средствами. При желании также могут быть добавлены некоторые подслащивающие, ароматизирующие или окрашивающие средства.
Альтернативно, фармацевтические композиции данного изобретения можно вводить ректально в виде свечей. Такие свечи можно получить путем смешивания средства с подходящим нераздражающим наполнителем, который при комнатной температуре находится в твердом виде, а при ректальной температуре является жидким и, следовательно, плавится в прямой кишке, высвобождая лекарственное средство. Такие вещества включают в себя, без ограничения, кокосовое масло, пчелиный воск и полиэтиленгликоли.
Фармацевтические композиции данного изобретения также можно вводить местно, особенно, если мишенью для лечения являются участки или органы, легко доступные для местного нанесения, как в случае заболеваний глаз, кожи или нижнего кишечного тракта. Подходящие местные композиции можно легко получить для каждого из указанных участков или органов.
Для местного применения на нижнем кишечном тракте можно использовать композиции ректальных свечей (описанные выше) или подходящие композиции клизм. Для местного применения также можно использовать пластыри для трансдермального введения.
Фармацевтические композиции для местного применения могут находиться в виде подходящей мази, содержащей активный компонент, суспендированный или растворенный в одном или нескольких носителях. Носители для местного введения соединений данного изобретения включают в себя, без ограничения, минеральное масло, жидкий вазелин, белый вазелин, пропиленгликоль, полиоксиэтилен, полиоксипропиленовое соединение, эмульгирующий воск и воду. Альтернативно фармацевтические композиции можно получить в виде подходящего лосьона или крема, содержащем активные компоненты, суспендированные или растворенные в одном или нескольких фармацевтически приемлемых носителях. Подходящие носители включают в себя, без ограничения, минеральное масло, моностеарат сорбитана, полисорбат 60, воскообразные цетиловые сложные эфиры, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
Фармацевтические композиции для офтальмического применения можно получить в виде тонкодисперсных суспензий в изотоническом стерильном физиологическом растворе с доведенным pH, или, предпочтительно, в виде растворов в изотоническом стерильном физиологическом растворе с доведенным pH, в присутствии или отсутствие консерванта, такого как хлорид бензилалкония. Альтернативно фармацевтические композиции для офтальмического применения можно получить в виде мази, такой как вазелин.
Фармацевтические композиции данного изобретения также можно вводить посредством назального аэрозоля или ингаляции. Такие композиции получают с помощью способов, хорошо известных в области фармацевтики, они могут быть получены в виде растворов в физиологическом растворе с использованием бензилового спирта или других подходящих консервантов, усилителей абсорбции для повышения биодоступности, фторуглеродов и/или других традиционных солюбилизирующих или диспергирующих средств.
Количество ингибитора протеинкиназы, которое может быть объединено с веществами-носителями с получением стандартной лекарственной формы, варьирует в зависимости от хозяина, подвергающегося лечению, и конкретного способа введения. Предпочтительно композиции получают таким образом, чтобы пациенту, получающему данные композиции, можно было ввести дозу ингибитора, находящуюся в интервале 0,01-100 мг/кг массы тела/день.
Следует понимать, что конкретные доза и режим лечения для какого-либо конкретного пациента зависят от ряда факторов, включающих в себя активность конкретного используемого соединения, возраст, массу тела, общее состояние здоровья, пол, диету, продолжительность введения, скорость экскреции, сочетание лекарственных препаратов и заключение лечащего врача, а также от тяжести конкретного заболевания, подлежащего лечению. Количество ингибитора зависит от конкретного соединения, входящего в состав композиции.
В соответствии с другим воплощением данное изобретение предлагает способы лечения или профилактики состояния, опосредованного протеинкиназой (в некоторых воплощениях состояния, опосредованного PLK), включающие в себя стадию введения пациенту одной из вышеописанных фармацевтических композиций. Термин "пациент" в данном описании относится к животному, предпочтительно, к человеку.
В некоторых воплощениях указанный способ используют для лечения или профилактики состояния, выбранного из пролиферативного нарушения, такого как рак, нейродегенеративного нарушения, аутоиммунного нарушения, воспалительного нарушения и иммунологического нарушения. В некоторых воплощениях указанный способ используют для лечения или профилактики состояния, выбранного из раковых заболеваний, таких как раковые заболевания молочной железы, толстой кишки, простаты, кожи, поджелудочной железы, мозга, мочеполового тракта, лимфатической системы, желудка, гортани и легкого, в том числе аденокарцинома легкого и мелкоклеточный рак легкого; инсульта, диабета, миеломы, гепатомегалии, кардиомегалии, болезни Альцгеймера, кистозного фиброза и вирусного заболевания, или любого описанного выше конкретного заболевания.
Как правило, соединения данного изобретения можно получить с помощью способов, известных специалистам в данной области. Данные соединения можно анализировать известными способами, включающими в себя, без ограничения, методы ЖХМС (жидкостная хроматография - масс-спектрометрия) и ЯМР (ядерный магнитный резонанс). Соединения данного изобретения также можно тестировать в соответствии с данными примерами. Следует понимать, что приведенные ниже конкретные условия являются только примерами и не предназначаются для ограничения диапазона условий, используемых для получения, анализа или тестирования соединений данного изобретения. Зато данное изобретение также включает в себя известные специалистам в данной области условия получения, анализа и тестирования соединений данного изобретения.
ПРИМЕРЫ
В данном описании термин "вр. уд. (мин)" относится к времени удерживания соединения на колонке ВЭЖХ, измеряемому в минутах. Если не указано иначе, для определения приведенного времени удерживания используют следующие условия ВЭЖХ:
Колонка: колонка ACE C8, 4,6×150 мм
Градиент: 0-100% ацетонитрил+метанол 50:50 (20 мM трис-фосфат)
Скорость потока: 1,5 мл/минуту
Детекция: 225 нм
Анализ образцов методом масс-спектрометрии проводят на масс-спектрометре MicroMass в одном режиме с ионизацией электрораспылением. Образцы вводят в масс-спектрометр после хроматографии.
Спектры 1H-ЯМР регистрируют при 400 мГц с помощью прибора Bruker DPX 400. Нижеследующие соединения формулы I получают и анализируют с помощью описанных ниже способов.
Соединения от I-1 до I-273 и от I-278 до I-282 получают и характеризуют с помощью способов, описанных в приведенных ниже примерах.
Пример 1:
4-(9-Циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензойная кислота (I-1)
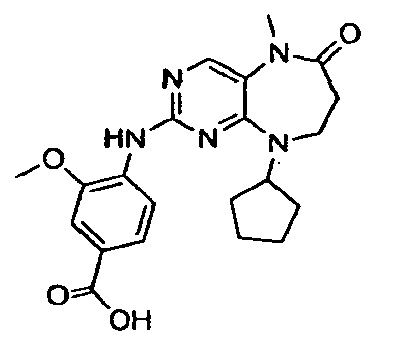
Способ A: Метил 3-(N-циклопентил-N-(2-хлор-5-нитропиримидин-4-ил)амино)пропионат
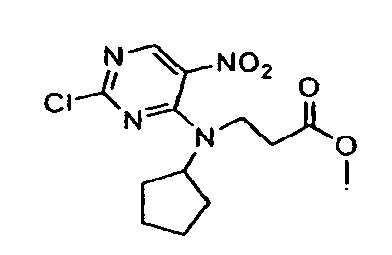
Метил 3-(циклопентиламино)пропаноат (1,78 г, 10,4 ммоль) и карбонат калия (1,52 г, 11,0 ммоль) в ацетоне (25 мл) перемешивают при 0°C в процессе добавления раствора 2,4-дихлор-5-нитропиримидина (2,04 г, 10,4 ммоль) в ацетоне (15 мл). Смесь перемешивают при температуре окружающей среды в течение ночи, концентрируют и разбавляют смесью этилацетат/вода. Смесь экстрагируют ×3 этилацетатом, сушат над сульфатом магния и концентрируют, получая янтарное масло, которое отверждается при стоянии. После флэш-хроматографии на силикагеле с использованием в качестве элюента смеси 30% этилацетат/бензин получают метил 3-(N-циклопентил-N-(2-метил-5-нитропиримидин-4-ил)амино)пропионат в виде бледно-желтого твердого вещества (2,24 г, 65%). ЯМР CDCl3 1,50-2,07 (8H, м), 2,70-2,82 (2H, м), 3,65-3,90 (6H, м), 8,72 (1H, с).
Способ B: 2-Хлор-9-циклопентил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он
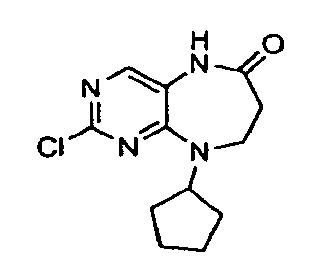
Метил 3-(N-циклопентил-N-(2-хлор-5-нитропиримидин-4-ил)амино)пропионат (2,0 г, 6,1 ммоль) в ледяной уксусной кислоте порциями обрабатывают порошком железа (0,7 г, 12,4 ммоль) при температуре 70°С в течение 6 часов. Смесь концентрируют, перетирают с дихлорметаном и фильтруют. Фильтрат абсорбируют на силикагеле и экстрагируют этилацетатом с применением аппарата Сокслета в течение 7 часов. Экстракт концентрируют до получения черного масла и перетирают с метанолом с получением бледно-коричневых кристаллов 2-хлор-9-циклопентил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-она (499 мг, 31%). ЯМР 1,46-1,58 (4H, м), 1,60-1,72 (2H, м), 1,75-1,85 (2H, м), 2,64 (2H, д), 3,55 (2H, д), 4,92-5,03 (1H, м), 7,83 (1H, с), 9,72 (1H, с).
Способ C: 2-Хлор-9-циклопентил-8,9-дигидро-5-метил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он
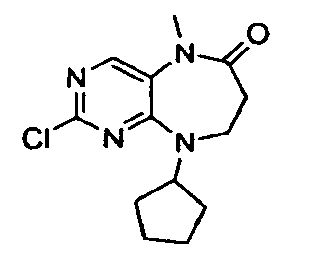
2-Хлор-9-циклопентил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (474,7 мг, 1,78 ммоль) и метилиодид (0,122 мл, 1,96 ммоль) в DMA (4,5 мл) перемешивают при температуре -10°C и обрабатывают 60% дисперсией гидрида натрия в масле (75 мг, 1,87 ммоль). Смесь нагревают до 0°С в течение 20 мин, затем до 20°С в течение 40 мин. Добавляют еще 0,12 мл метилиодида и 8 мг гидрида натрия, после чего смесь перемешивают при температуре окружающей среды в течение ночи. Затем добавляют лед и смесь концентрируют при пониженном давлении. Остаток масла обрабатывают по каплям водой (6 мл), фильтруют и полученное светло-коричневое твердое вещество сушат в высоком вакууме при температуре 60°С (486 мг, 98%). ЯМР ДМСО D6 1,45-1,72 (6H, м), 1,76-1,91 (2H, м), 2,61 (2H, д), 3,18 (3H, с), 3,64 (2H, д), 4,65-4,74 (1H, м), 8,15 (1H, с).
Способ D: 4-(9-Циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензойная кислота (I-1)
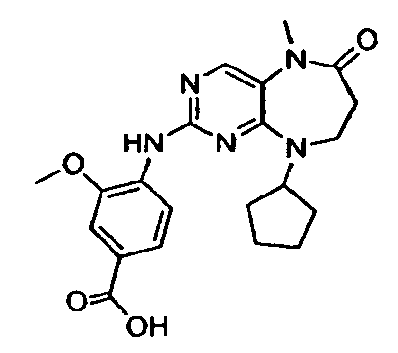
2-Хлор-9-циклопентил-8,9-дигидро-5-метил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (150 мг, 0,536 ммоль) в этаноле (2,25 мл) и воде (9 мл) обрабатывают концентрированной HCl (0,088 мл) и 4-амино-3-метоксибензойной кислотой (134 мг, 0,804 ммоль). Смесь перемешивают при 90°С в течение 24 часов, концентрируют, остаток перетирают со смесью метанол/эфир, фильтруют, твердый остаток промывают этанолом, затем эфиром и получают 4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b] [1,4]диазепин-2-иламино)-3-метоксибензойную кислоту в виде светло-коричневого порошка (185,5 мг, 84%). ЯМР ДМСО D6 1,51-1,79 (6H, м), 1,82-1,93 (2H, м), 2,70-2,75 (2H м), 3,18 (3H, с), 3,72-3,78 (2H, м), 3,98 (3H, с), 4,81-4,93 (1H, м), 7,57-7,64 (2H, м), 8,15-8,22 (2H, м), 9,46 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 6,57.
Пример 2:
Способ E: 4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид(1-2)
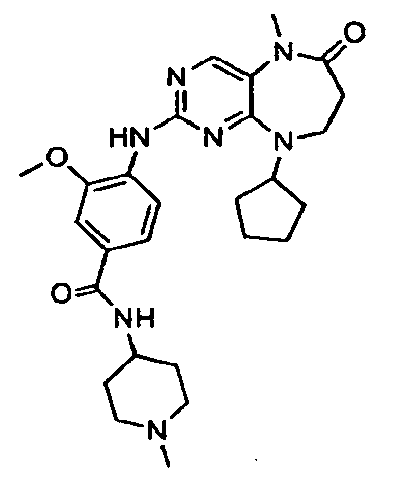
Циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензойную кислоту (150 мг, 0,365 ммоль) в дихлорметане (5 мл) обрабатывают диизопропилэтиламином (0,127 мл, 0,73 ммоль) и TBTU (127 мг, 0,394 ммоль). Смесь перемешивают в течение 25 мин, затем обрабатывают 4-амино-l-метилпиперидином (52 мг, 0,453 ммоль) и перемешивают в течение ночи. Смесь разбавляют этилацетатом, промывают водным раствором гидрокарбоната натрия, ×2 0,02 M раствором гидроксида натрия, насыщенным соляным раствором, сушат над сульфатом магния и концентрируют. После перетирания со смесью этилацетат/эфир получают 4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(l-метилпиперидин-4-ил)бензамид в виде бесцветного твердого вещества (132 мг, 71%). ЯМР ДМСО D6 1,50-2,08 (14H, м), 2,21 (3H, с), 2,55-2,65 (2H, м), 2,77-2,87 (2H, м), 3,21 (3H, с), 3,60-3,70 (2H, м), 3,70-3,82 (1H, м), 3,98 (3H, с), 4,80-4,90 (1H, м), 7,42-7,52 (2H, м), 7,75 (1H, с), 8,10-8,18 (2H, м), 8,40 (1H, д); ВЭЖХ вр. уд. (мин): 9,60.
Пример 3:
4-(9-Циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)бензойная кислота(I-3)
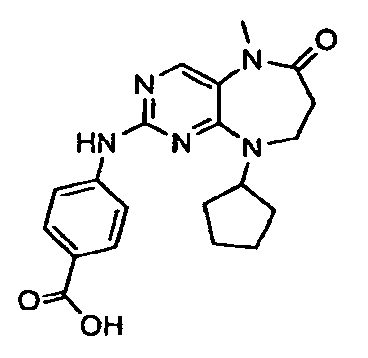
Получают из 2-хлор-9-циклопентил-8,9-дигидро-5-метил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-она и 4-аминобензойной кислоты по способу D. ЯМР ДМСО D6 1,59-1,80 (6H, м), 1,90-1,98 (2H, м), 2,70-2,75 (2H м), 3,18 (3H, с), 3,71-3,75 (2H, м), 4,91 (1H, м), 7,77 (2H, д), 7,94 (2H, д), 8,17 (1H, с), 10,65 (1H, ушир.с). ВЭЖХ вр. уд. (мин): 6,39.
Пример 4:
4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-метилпиперидин-4-ил)бензамид (1-4)
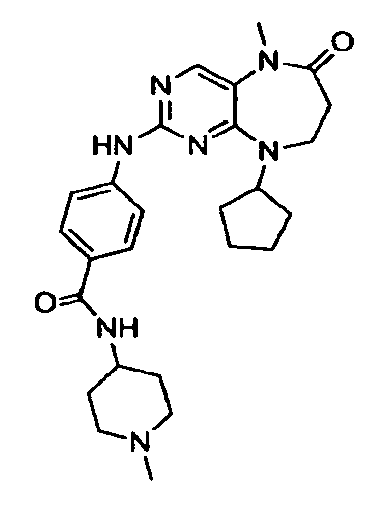
Получают из соединения I-3 и 4-амино-1-метилпиперидина по способу E.
ЯМР ДМСО D6 1,62-2,05 (14H, м), 2,23 (3H, с), 2,60-2,68 (2H, м), 2,77-2,86 (2H, м), 3,23 (3H, с), 3,65-3,70 (2H, м), 3,78 (1H, м), 4,91 (1H, м), 7,76-7,85 (4H, м), 8,00 (1H, д), 8,11 (1H, с), 9,50 (1H, c); ВЭЖХ вр. уд. (мин): 7,50.
Пример 5:
4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H- пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-[1-(трет-бутоксикарбонил)пиперидин-4-ил]бензамид (I-5).
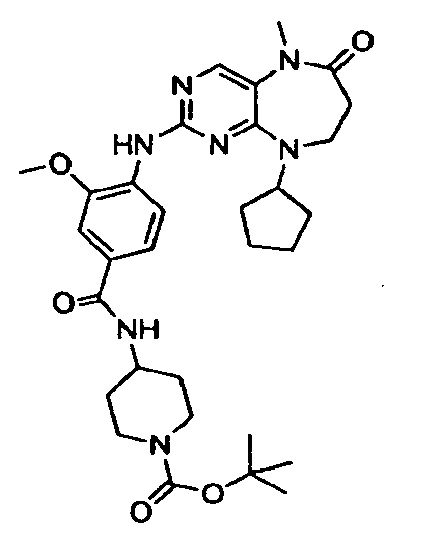
Получают из соединения I-1 и 4-амино-1-(трет-бутоксикарбонил )пиперидина по способу E. ЯМР ДМСО D6 1,41 (9H, с), 1,37-1,98 (14H, м), 2,57-2,63 (2H, м), 2,80 (2H, м), 3,17 (3H, с), 3,61-3,69 (2H, м), 3,91 (3H, с), 3,97 (1H, м), 4,83 (1H, м), 7,47-7,52 (2H, м), 8,07-8,15 (3H, м), 8,27 (1H, м); ВЭЖХ вр. уд. (мин): 10,07.
Пример 6:
Способ F: 4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиперидин-4-ил)бензамид (I-6)
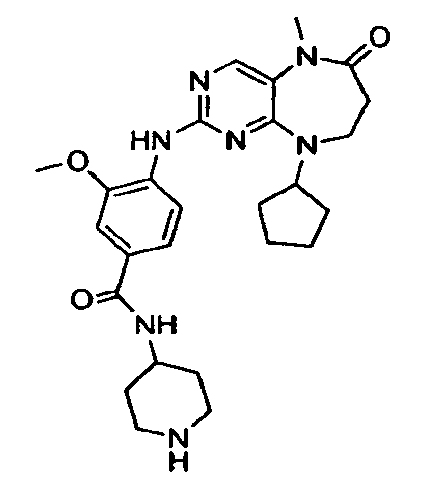
К раствору 4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-[1-(трет-бутоксикарбонил)пиперидин-4-ил]бензамид (I-5) (72 мг, 0,12 ммоль) в дихлорметане (3 мл) добавляют трифторуксусную кислоту при температуре 0°С. Реакционную смесь перемешивают в течение 30 минут при температуре 0°С, в течение 60 минут при комнатной температуре, затем растворители выпаривают. Остаток перетирают в диэтиловом эфире, твердое вещество фильтруют и получают соль TFA обозначенного соединения в виде твердого грязно-белого вещества (70 мг, 95%). ЯМР ДМСО D6 1,55-2,04 (14H, м), 2,62-2,70 (2H, м), 2,98-3,08 (2H, м), 3,19 (3H, с), 3,40-3,48 (2H, м), 3,65-3,71 (2H, м), 3,97 (3H, с), 4,09 (1H, м), 4,89 (1H, м), 7,49-7,56 (2H, м), 8,10 (1H, с), 8,19 (1H, д), 8,30-8,40 (2H, д), 8,60-8,69 (2H, м); ВЭЖХ вр. уд. (мин): 7,53.
Пример 7:
4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксифенил-(4-трет-бутоксикарбонилпиперазин-1-ил)метанон (I-7)
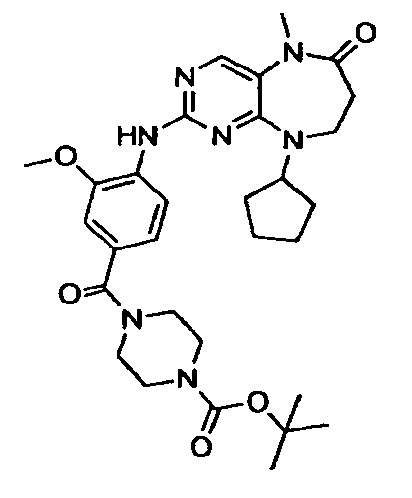
Получают из соединения I-1 и N-трет-бутоксикарбонилпиперазины по способу E. ЯМР ДМСО D6 1,41 (9H, с), 1,55-1,95 (10H, м), 2,57-2,62 (2H, м), 3,18 (3H, с), 3,27-3,63 (8H, м), 3,90 (3H, с), 4,80 (1H, м), 6,96 (1H, д), 7,05 (1H, с), 7,72 (1H, с), 8,07 (1H, с), 8,30 (1H, д); ВЭЖХ вр. уд. (мин): 9,98.
Пример 8:
4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метилоксифенил(пиперазин-1-ил)метанон (I-8 )
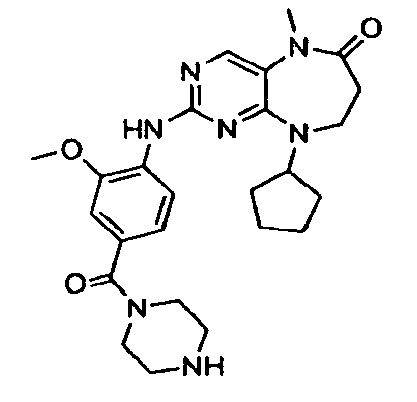
Получают из соединения I-7 по способу F. ЯМР ДМСО D6 1,50-1,91 (8H, м), 2,65-2,73 (2H, м), 3,15-3,22 (7H, м), 7,63-7,70 (6H, м), 3,94 (3H, с), 4,80 (1H, м), 7,12 (1H, д), 7,20 (1H, с), 8,04 (1H, д), 8,10 (1H, с), 9,02-9,11 (2H, м). ВЭЖХ вр. уд. (мин): 7,81.
Пример 9:
4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино-3-метокси-N-метилбензамид(I-9).
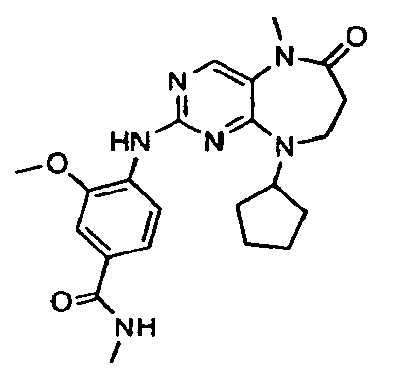
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,62-1,73 (6H, м), 1,92-1,97 (2H, м), 2,58-2,60 (2H, м), 2,78-2,80 (3H, м), 3,17 (3H, с), 3,62-3,64 (2H, м), 3,94 (3H, с), 4,82 (1H, м), 7,46-7,50 (2H, м), 7,73 (1H, с), 8,08 (1H, с), 8,35 (1H, м), 8,38 (1H, м); ВЭЖХ вр. уд. (мин): 8,45; МС (ES+) 425, (ES-) 423.
Пример 10:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензойная кислота(I-10)
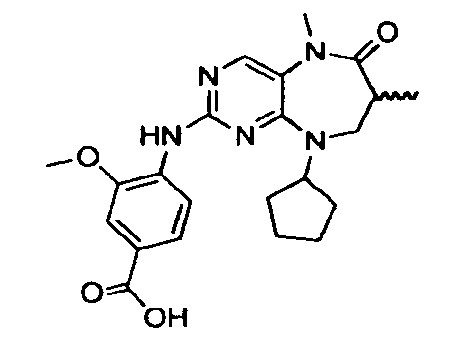
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,08 (3H, д), 1,48-1,86 (7H, м), 1,98-2,10 (1H, м), 2,90-3,00 (1H, м), 3,20 (3H, с), 3,37 (1H, д), 3,56 (1H, т), 3,95 (3H, с), 4,72-4,85 (1H, м), 7,56 (1H, с), 7,60 (1H, д), 8,13 (1H, с), 8,31 (1H, д), 8,66 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 7,47; МС (ES+) 426, (ES-) 424.
Пример 11:
4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(2-метоксиэтил)бензамид (I-11)
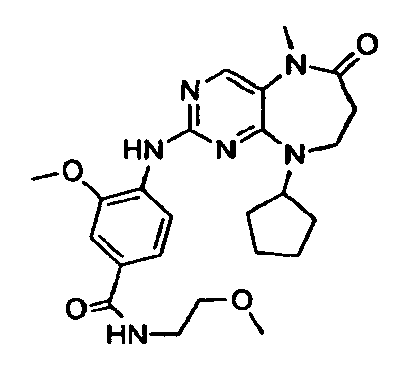
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,62-1,73 (6H, м), 1,90-2,0 (2H, м), 2,54-2,60 (2H, м), 3,17 (3H, с), 3,25 (3H, с), 3,42-3,46 (4H, м), 3,62-3,64 (2H, м), 3,95 (3H, с), 4,82 (1H, м), 7,49-7,52 (2H, м), 7,74 (1H, с), 8,09 (1H, с), 8,41 (2H, м); ВЭЖХ вр. уд. (мин): 8,65; МС (ES+) 469, (ES-) 467.
Пример 12:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо [4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид (I-12).
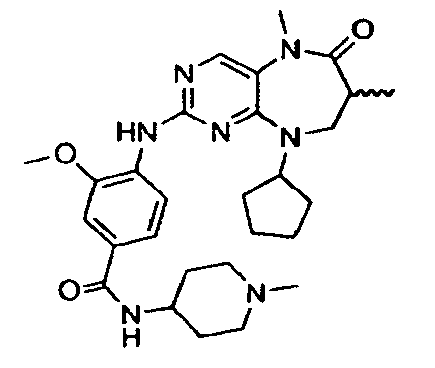
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,03 (3H, д), 1,50-2,15 (14H, м), 2,18 (3H, с), 2,76-2,90 (3H, м), 3,20 (3H, с), 3,28-3,48 (2H, м), 3,70-3,80 (1H, м), 3,98 (3H, с), 7,49-7,52 (2H, м), 7,74 (1H, с), 8,05-8,12 (2H, м), 8,40 (1H, д); ВЭЖХ вр. уд. (мин): 8,95; МС (ES+) 522, (ES-) 520.
Пример 13:
Способ G: Этил 4-(9-циклопентил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)пиперидин-1-карбоксилат (I-13)
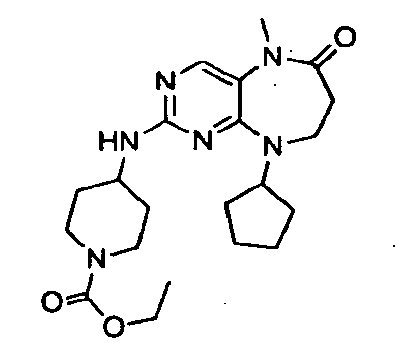
2-Хлор-9-циклопентил-8,9-дигидро-5-метил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (100 мг, 0,357 ммоль) и этил 4-аминопиперидин-1-карбоксилат (129 мкл, 0,714 ммоль) в изопропиловом спирте (2 мл) нагревают при температуре 90°С в течение 24 часов. Затем добавляют диизопропилэтиламин (125 мкл, 0,714 ммоль) и реакционную смесь нагревают при температуре 105°С в течение еще 24 часов. Неочищенную смесь концентрируют в вакууме и очищают методом препаративной ВЭЖХ на обращенной фазе [Waters Sunfire C18, 10 мкм, 100 A колонка, градиент 10% - 95% B (растворитель A: 0,05% TFA в воде; растворитель B: CH3CN) в течение 16 минут со скоростью 25 мл/мин] с получением указанного в заголовке соединения (18 мг) в виде порошка грязно-белого цвета. ЯМР ДМСО D6 1,20 (3H, т), 1,28-1,91 (14H, м), 2,80-2,96 (2H, м), 3,11 (3H, с), 3,50-3,58 (2H, м), 3,70-3,85 (1H, м), 3,90-3,98 (2H, м), 4,03 (2H, кв.), 4,60-4,70 (1H, м), 6,65 (1H, ушир.с), 7,88 (1H, с); ВЭЖХ вр. уд. (мин): 8,09; МС (ES+) 417, (ES-) 415.
Пример 14:
4-(6,7,8,9-тетрагидро-5,9-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид(I-14).
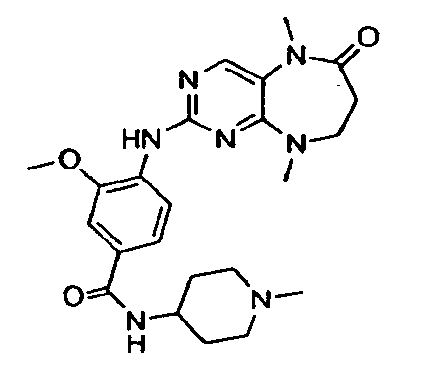
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,65-1,67 (2H, м), 1,83-1,85 (2H, м), 2,33-2,36 (3H, м), 2,50-2,53 (2H, м), 2,60-2,63 (2H, м), 3,07 (3H, с), 3,18 (3H, с), 3,29 (3H, с), 3,69-3,71 (2H, м), 3,94 (3H, с), 7,48-7,53 (2H, м), 7,75 (1H, с), 8,11 (2H, м), 8,46 (1H, м); ВЭЖХ вр. уд. (мин): 6,75; МС (ES+) 454, (ES-) 452.
Пример 15:
4-((3aR,10aS)-4-циклопентил-9-метил-10-оксо-1,2,3,3a,4,9,10,10a-октагидро-4,5,7,9-тетрааза-бензо[f]азулен-6-иламино)-3-метокси-N-метилбензамид (I-15)
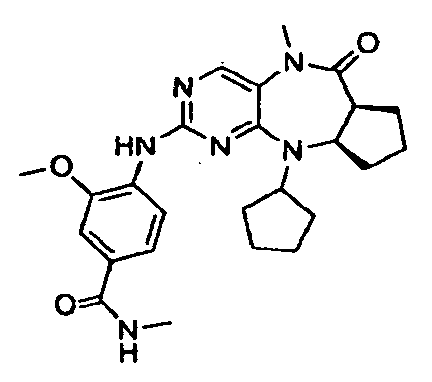
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,40-1,60 (9H, м), 1,66-1,69 (2H, м), 1,79 (1H, м), 1,86-1,87 (2H, м), 2,04 (1H, м), 2,15 (1H, м), 2,80 (3H, д), 3,20 (3H, с), 3,92 (3H, с), 4,14 (1H, м), 7,55 (1H, д), 7,57 (1H, с), 7,95 (1H, д), 8,22 (1H, с), 8,44 (1H, д), 8,95 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,45; МС (ES+) 465, (ES-) 463.
Пример 16:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-16)
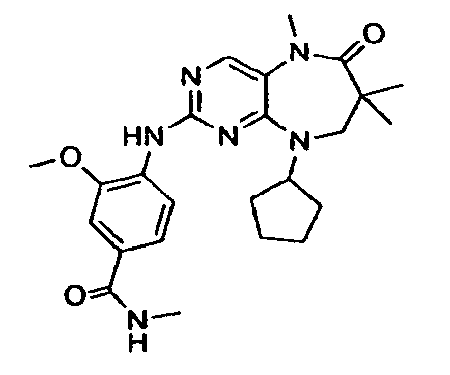
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,62-1,65 (4H, м), 1,74 (2H, м), 1,88 (2H, м), 2,79 (3H, д), 3,19 (3H, с), 3,36-3,40 (2H, м), 3,94 (3H, с), 5,18 (1H, м), 7,45-7,50 (2H, м), 7,68 (1H, с), 7,99 (1H, с), 8,30 (1H, м), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 9,23; МС (ES+) 453, (ES-) 451.
Пример 17:
4-((S)-9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-17)
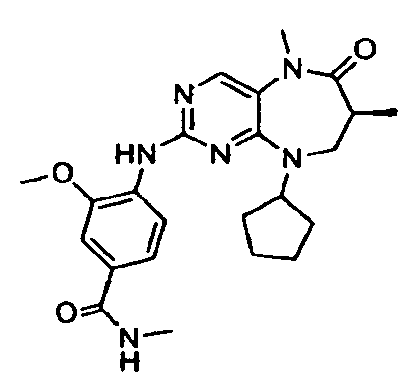
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,03-1,07 (3H, м), 1,55-1,61 (4H, м), 1,70-1,78 (4H, м), 1,99 (1H, м), 2,80 (3H, м), 3,18 (3H, с), 3,56-3,61 (2H, м), 3,94 (3H, с), 4,80 (1H, м), 7,50-7,52 (1H, м), 7,58 (1H, м), 8,07-8,10 (1H, м), 8,13 (1H, ушир.с), 8,47 (1H, м), 9,25 (1H, ушир.с);. ВЭЖХ вр. уд. (мин): 8,92; МС (ES+) 439. (ES-) 437.
Пример 18:
4-((R)-9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-18)
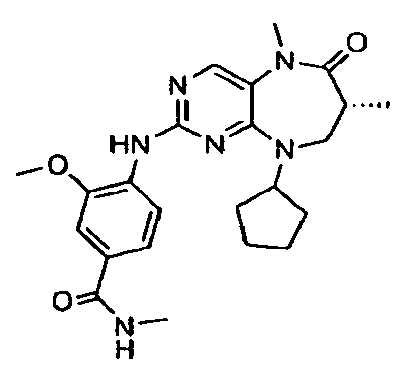
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,03-1,07 (3H, м), 1,56-1,60 (4H, м), 1,72-1,78 (4H, м), 1,98 (1H, м), 2,80 (3H, м), 3,19 (3H, м), 3,57-3,63 (2H, м), 3,94 (3H, с), 4,81 (1H, м), 7,50-7,53 (1H, м), 7,60 (1H, м), 8,06 (1H, д), 8,15 (1H, м), 8,50 (1H, д), 9,49 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,92; МС (ES+) 439, (ES-) 437.
Пример 19:
4-(6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-9-((R)-пирролидин-3-ил)-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-19)
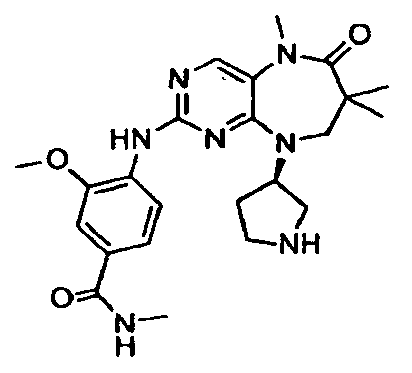
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,118 (3H, с), 1,124 (3H, с), 2,04 (1H м), 2,27 (1H, м), 2,80 (3H, д), 3,11-3,28 (5H, м), 3,40-3,56 (4H, м), 3,93 (3H, с), 5,42 (1H, квинт.), 7,53-7,57 (2H, м), 8,10 (1H, с), 8,17 (1H, д), 8,39 (1H, кв.), 8,55 (1H, ушир.с), 9,05 (1H, ушир.с), 9,12 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 6,14; МС (ES+) 454, (ES-) 452.
Пример 20:
4-(6,7,8,9-тетрагидро-5,7,7-триметил-9-((R)-1-метилпирролидин-3-ил)-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-20)
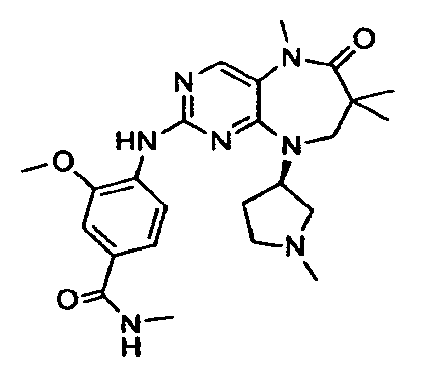
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11-1,15 (6H, м), 2,00-2,41 (2H м), 2,80 (3H, д), 2,85-2,95 (3H, м), 3,10-3,40 (5H, м), 3,51-3,80 (4H, м), 3,93 (3H, с), 5,36-5,60 (1H, м), 7,56-7,59 (2H, м), 8,04-8,13 (2H, м), 8,46 (1H, м), 8,93-9,13 (1H, ушир.с), 10,38-10,77 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 7,25; МС (ES+) 468, (ES-) 466.
Пример 21:
4-((S)-9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид (I-21)
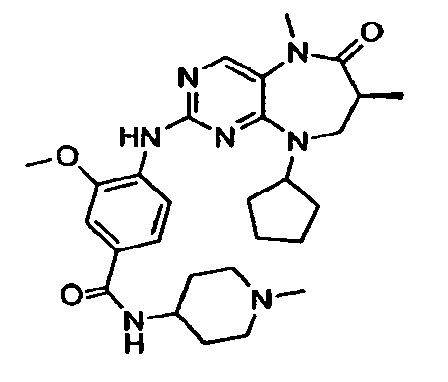
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,06-1,07 (3H, д), 1,56-2,03 (14H, м), 2,70 (3H, д), 3,09 (3H, м), 3,19 (3H, с), 3,58-3,64 (2H, м), 3,95 (3H, с), 4,04 (1H, м), 4,84 (1H, м), 7,56-7,64 (2H, м), 8,08 (1H, д), 8,22 (1H, с), 8,59 (1H, д), 9,61 (1H, ушир.c), 10,77 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 9,00; МС (ES+) 522, (ES-) 520.
Пример 22:
4-((R)-9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид (I-22)
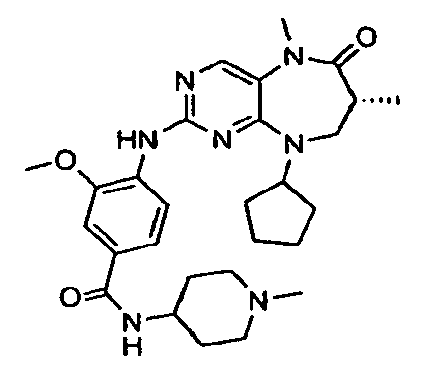
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,06-1,07 (3H, д), 1,56-1,98 (14H, м), 2,71 (3H, д), 3,02-3,08 (3H, м), 3,19 (3H, с), 3,58-3,64 (2H, м), 3,95 (3H, с), 4,05 (1H, м), 4,83 (1H, м), 7,57-7,64 (2H, м), 8,09 (1H, м), 8,23 (1H, с), 8,60 (1H, д), 9,64 (1H, ушир.с), 10,81 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 9,11; МС (ES+) 522, (ES-) 520.
Пример 23:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид (I-23)
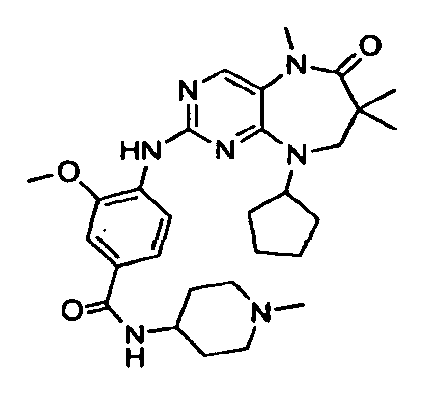
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,20 (6H, с), 1,55-2,08 (12H, м), 2,70 (3H, с), 3,00-3,14 (2H, м), 3,52 (3H, с), 3,50-3,85 (4H, м), 3,96 (3H, с), 3,98-4,08 (1H, м), 5,07-5,18 (1H, м), 7,56 (1H, д), 7,65 (1H, с), 8,07 (1H, д), 8,10 (1H, с), 8,57 (1H, д), 9,50 (1H, ушир.с), 10,60 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,55; МС (ES+) 536, (ES-) 534.
Пример 24:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-илaминo)-3-метокси-N-(пиридин-4-ил)бензамид (I-24)
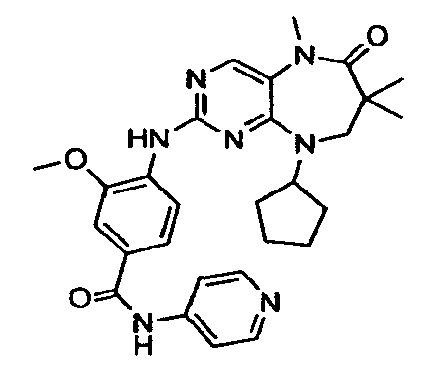
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,20 (6H, с), 1,55-1,90 (8H, м), 3,19 (3H, с), 3,50-3,60 (2H, м), 4,04 (3H, с), 5,13-5,22 (1H, м), 7,85 (1H, д), 7,90 (1H, с), 8,11 (1H, с), 8,31 (1H, д), 8,45 (2H, д), 8,77 (2H, д), 9,18 (1H, ушир.с), 11,78 (1H, C); ВЭЖХ вр. уд. (мин): 9,94; МС (ES+) 516, (ES-) 514.
Пример 25:
Способ H: 4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилазетидин-3-ил)бензамид (I-25)
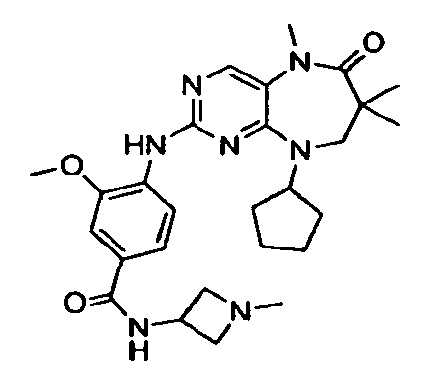
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(азетидин-3-ил)-3-метоксибензамид (69 мг, 0,14 ммоль) растворяют в метаноле (1,5 мл), затем последовательно добавляют 37% водный раствор формальдегида (66 мкл, 0,84 ммоль) и цианоборгидрид натрия (26 мг, 0,42 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение 2 часов. Неочищенную смесь разбавляют 2 н. HCl, затем подщелачивают насыщенным раствором NaHCO3. Смесь дважды экстрагируют этилацетатом. Объединенные органические фазы сушат (MgSО4) и концентрируют в вакууме. После кристаллизации из этилацетата получают указанное в заголовке соединение (33 мг) в виде белого твердого вещества. ЯМР ДМСО D6 1,10 (6H, с), 1,55-1,69 (4H, м), 1,69-1,80 (2H, м), 1,82-1,95 (2H, м), 2,28 (3H, с), 3,01 (2H, т), 3,38 (2H, с), 3,57 (2H, т), 3,95 (3H, с), 4,39-4,50 (1H, м), 5,12-5,25 (1H, м), 7,43-7,52 (2H, м), 7,71 (1H, с), 8,00 (1H, с), 8,38 (1H, д), 8,63 (1H, д); ВЭЖХ вр. уд. (мин): 9,60; МС (ES+) 508, (ES-) 506.
Пример 26:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((R)-1-метилпирролидин-3-ил)бензамид (I-26)
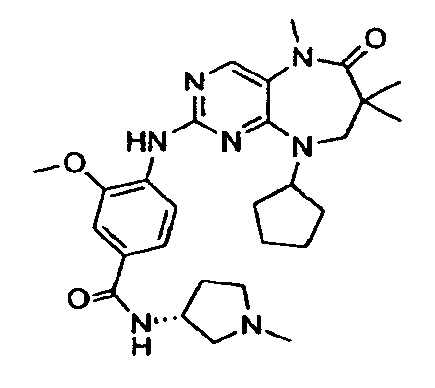
Получают по способу H, используя подходящие реагенты. ЯМР ДМСО D6 1,01 (6H, с), 1,52-1,94 (9H, м), 2,12-2,20 (1H, м), 2,27 (3H, с), 2,35-2,42 (1H, м), 2,8-2,68 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,36-4,47 5,13-5,26 (1H, м), 7,46-7,56 (2H, м), 7,69 (1H, с), 7,99 (1H, с), 8,33-8,41 (2H, м); ВЭЖХ вр. уд. (мин): 9,71; МС (ES+) 522, (ES-) 520.
Пример 27:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(2-(1-метил-1H-имидазо-5-ил)этил)бензамид (I-27)
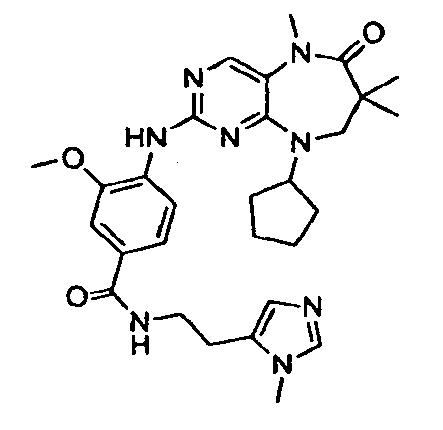
Получают по способу E, используя подходящие реагенты. ЯМР ДМСО D6 1,01 (6H, с), 1,55-1,94 (8H, м), 2,77-2,85 (2H, м), 3,20 (3H, с), 3,38 (2H, с), 3,45-3,50 (2H, м), 3,58 (3H, с), 5,15-5,25 (1H, м), 6,73 (1H, с), 7,45-7,55 (2H, м), 7,70 (1H, с), 7,99 (1H, с), 8,49 (1H, д), 8,55-8,59 (1H, м); ВЭЖХ вр. уд. (мин): 9,10; МС (ES+) 547, (ES-) 545.
Пример 28:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(3-(4-метилпиперазин-1-ил)пропил)бензамид (I-28)
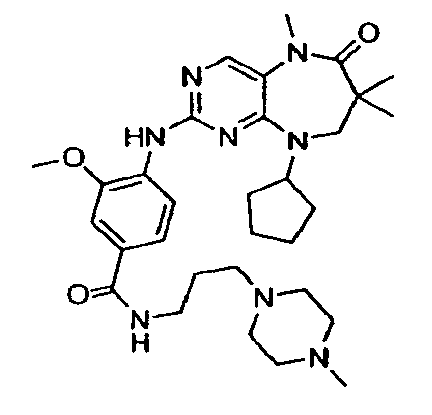
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,53-1,95 (12H, м), 2,15 (3H, с), 2,20-2,45 (8H, м), 3,19 (3H, с), 3,22-3,30 (2H, м), 3,38 (2H, с), 3,94 (3H, с), 5,10-5,21 (1H, м), 7,48 (1H, д), 7,49 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,30-8,40 (2H, м); ВЭЖХ вр. уд. (мин): 9,37; МС (ES+) 579, (ES-) 577.
Пример 29:
4-(9-циклопентил-6,7,8,9-тетрагидро-7,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-29)
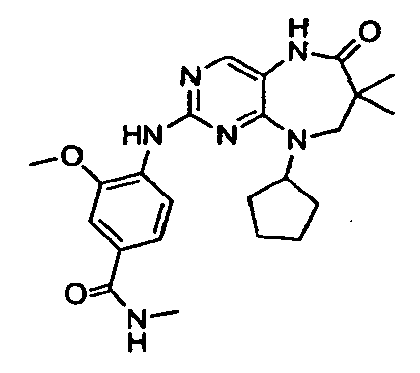
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,59-1,60 (4H, м), 1,75-1,82 (4H, м), 2,80 (3H, д), 3,45 (2H, м), 3,93 (3H, с), 5,21 (1H, м), 7,48 (1H, м), 7,56 (1H, с), 7,79 (1H, с), 8,05 (1H, м), 8,44 (1H, м), 9,00 (1H, очень ушир.c), 9,76 (1H, с); ВЭЖХ вр. уд. (мин): 8,97; МС (ES+) 439, (ES-) 437.
Пример 30:
4-(9-циклопропил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-30)
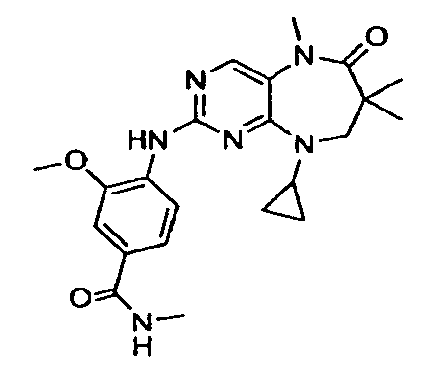
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,83 (2H, м), 0,96 (2H, кв.), 1,16 (6H, с), 2,79 (3H, д), 3,09 (1H, м), 3,17 (3H, с), 3,71 (2H, с), 3,96 (3H, с), 7,52-7,56 (2H, м), 8,12 (1H, с), 8,38 (1H, кв.), 8,53 (1H, д), 9,12 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,26; МС (ES+) 425, (ES-) 423.
Пример 31:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(2-(1-метил-lH-имидазо-4-ил)этил)бензамид (I-31)
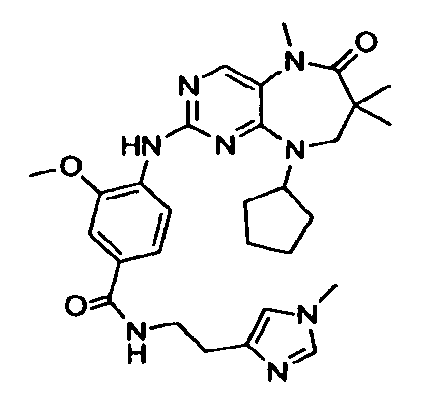
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,55-1,68 (4H, м), 1,70-1,78 (2H, м), 1,83-1,93 (2H, м), 2,70 (2H, т), 3,19 (3H, с), 3,39 (2H, с), 3,93-3,51 (2H, м), 3,60 (3H, с), 3,95 (3H, с), 5,14-5,25 (1H, м), 6,91 (1H, с), 7,43-7,52 (3H, м), 7,65 (1H, с), 7,99 (1H, с), 8,37 (1H, д), 8,41-8,46 (1H, м); ВЭЖХ вр. уд. (мин): 9,16; МС (ES+) 547, (ES-) 545.
Пример 32:
9-Циклопентил-2-[4-((S)-3-фтор-пирролидин-1-карбонил)-2-метоксифениламино]-5,7,7-триметил-5,7,8,9-тетрагидропиримидо[4,5-b][1,4]диазепин-6-он (I-32)
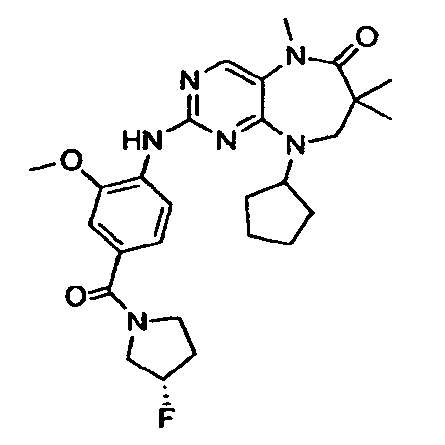
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,60-2,27 (10H, м), 3,25 (3H, с), 3,43 (2H, с), 3,65-3,90 (4H, м), 3,98 (3H, с), 5,18-5,29 (1H, м), 5,30-5,53 (1H, м), 7,15-7,25 (2H, м), 7,73 (1H, с), 8,03 (1H, с), 8,39 (1H, д); ВЭЖХ вр. уд. (мин): 9,67; МС (ES+) 411, (ES-) 409.
Пример 33:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(2-морфолиноэтил)бензамид (I-33)
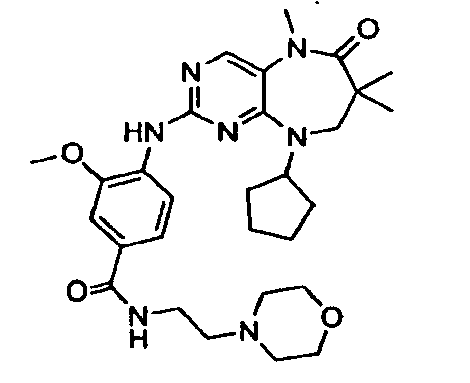
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,55-1,92 (8H, м), 2,38-2,52 (6H, м), 3,19 (3H, с), 3,38 (2H, с), 3,36-3,44 (2H, м), 3,54-3,63 (4H, м), 3,94 (3H, с), 5,12-5,22 (1H, м), 7,45 (1H, д), 7,49 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,26 (1H, ушир.с), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 9,26; МС (ES+) 552, (ES-) 550.
Пример 34:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(2-(пирролидин-1-ил)этил)бензамид (I-34)
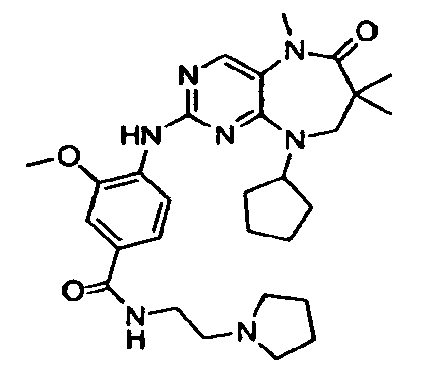
Получают по способу E, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,55-1,93 (12H, м), 2,52-2,73 (6H, м), 3,19 (3H, с), 3,39 (2H, с), 2,28-2,46 (2H, м), 3,95 (3H, с), 5,13-5,22 (1H, м), 7,43-7,50 (2H, м), 7,69 (1H, с), 7,99 (1H, с), 8,34-8,42 (2H, м); ВЭЖХ вр. уд. (мин): 9,17; MS (ES+) 536, (ES-) 534.
Пример 35:
4-(6,7,8,9-тетрагидро-9-изопропил-5,7,7-триметил-6-оксо-5H- пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-35)
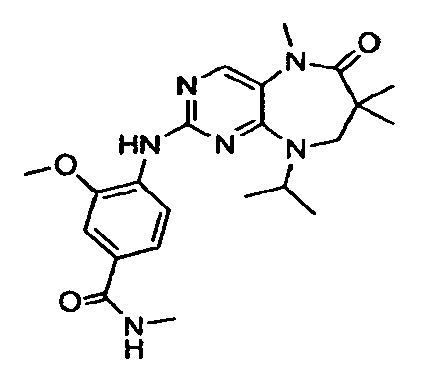
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 1,23 (6H, д), 2,80 (3H, д), 3,18 (3H, с), 3,50 (2H, с), 3,95 (3H, с), 5,09 (1H, гепт.), 7,53 (1H, дд), 7,57 (1H, д), 8,01 (1H, с), 8,07 (1H, д), 8,41 (1H, кв.), 9,15 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 8,63; МС (ES+) 527. (ES-) 525.
Пример 36:
4-(6-Циклопентил-4,4-диметил-5,6-дигидро-4H-2,3,6,7,9,10b-гексаазабензо[e]азулен-8-иламино)-3-метокси-N-метилбензамид (I-36)
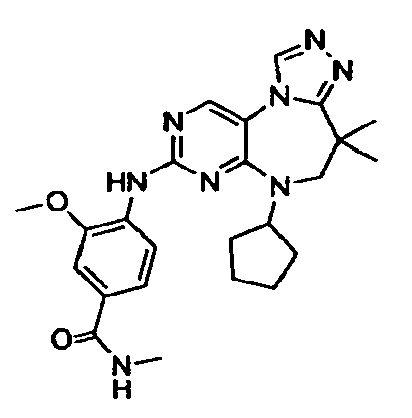
Способ I: 8-Хлор-6-Циклопентил-4,4-диметил-5,6-дигидро-4H- 2,3,6,7,9,10b-гексаазабензо[e]азулен
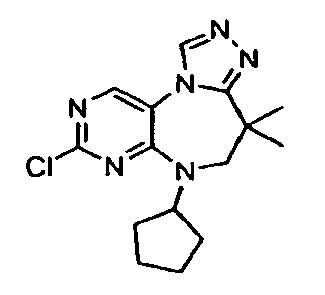
2-Хлор-9-циклопентил-8,9-дигидро-7,7-диметил-5H-пиримидо[4,5-b](1,4]диазепин-6(7H)-он (0,21 г, 0,73 ммоль) в оксихлориде фосфора (6 мл) нагревают при температуре 110°С в течение 4 часов. Реакционную смесь концентрируют в вакууме и перерастворяют в дихлорметане (4 мл). Полученный раствор по капле добавляют к 1M раствору гидразина в тетрагидрофуране (7,27 мл, 7,27 ммоль). Реакционную смесь перемешивают в течение ночи при комнатной температуре. Затем добавляют насыщенный раствор NaHCO3 и смесь экстрагируют этилацетатом. Органический слой сушат (MgSO4), фильтруют и концентрируют в вакууме. Полученную смесь растворяют в триметилортоформиате (4 мл) и нагревают до 110°С в течение 90 минут. Реакционную смесь упаривают в вакууме, очищают методом хроматографии на силикагеле, элюируя этилацетатом, и получают указанное в заголовке соединение в виде не совсем белого твердого вещества. (0,16 г, выход 69%). ЯМР ДМСО D6 1,37 (6H, с), 1,52-1,88 (8H, м), 3,44 (2H, с), 5,23 (1H, квинт.), 8,56 (1H, с), 9,02 (1H, с); МС (ES+) 319.
4-(6-Циклопентил-4,4-диметил-5,6-дигидро-4H-2,3,6,7,9,10b-гексаазабензо[e]азулен-8-иламино)-3-метокси-N-метилбензамид (I-36)
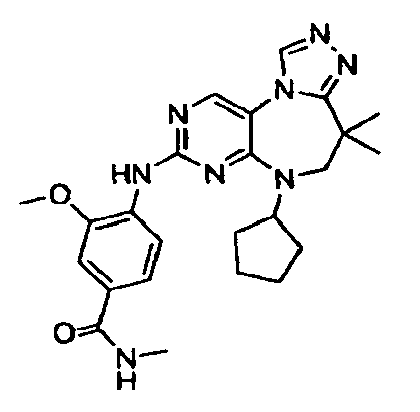
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,41 (6H, с), 1,55-1,90 (8H, м), 2,80 (3H, д), 3,50 (2H, с), 3,94 (3H, с), 5,27 (1H, квинт.), 7,51 (1H, дд), 7,57 (1H, д), 8,08 (1H, д), 8,47 (1H, кв.), 8,51 (1H, с), 8,97 (1H, ушир.с), 9,12 (1H, с); ВЭЖХ вр. уд. (мин): 8,54; МС (ES+) 463, (ES-) 461.
Пример 37:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2-((S)-3-фторпирролидин-1-ил)этил)-3-метоксибензамид (I-37)
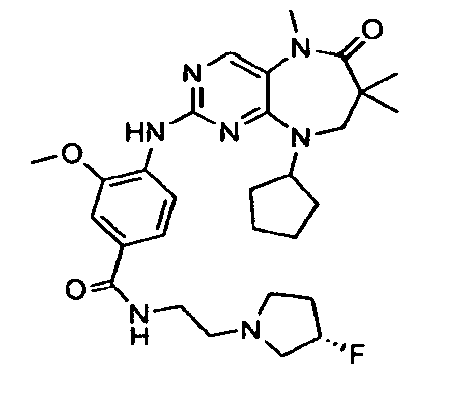
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,16 (6H, с), 1,62-2,04 (9H, м), 2,08-2,50 (2H, м), 2,60-3,00 (5H, м), 3,25 (3H, с), 3,43-3,48 (2H, м), 3,44 (2H, с), 4,00 (3H, с), 5,17-5,38 (2H, м), 7,51 (1H, д), 7,56 (1H, с), 7,74 (1H, с), 8,05 (1H, с), 8,35-8,48 (1H, м), 8,43 (1H, д); ВЭЖХ вр. уд. (мин): 9,57; МС (ES+) 554, (ES-) 552.
Пример 38:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2-азетидин-l-ил)этил)-3-метоксибензамид (I-38)
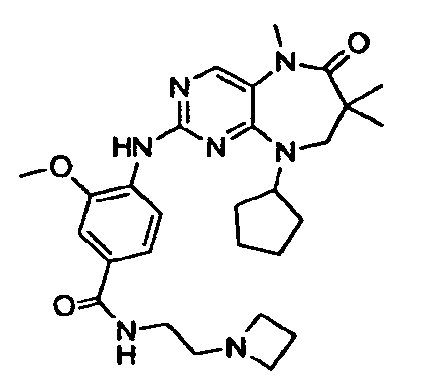
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,55-2,04 (10H, м), 2,35-2,55 (2H, м), 3,08-3,25 (6H, м), 3,20 (3H, с), 3,38 (2H, с), 3,75-3,95 (1H, м), 3,94 (3H, с), 5,15-5,25 (1H, м), 7,46 (1H, с), 7,50 (1H, с), 7,68 (1H, с), 7,80 (1H, с), 8,24-8,30 (1H, м), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 9,31; МС (ES+) 522, (ES-) 520.
Пример 39:
(R)-3-фтор-пирролидин-1-карбоксильная кислота 2-[4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо [4,5-b][1,4]диазепин-2-иламино)-3-метоксибензоиламино]-этиловый эфир(I-39)
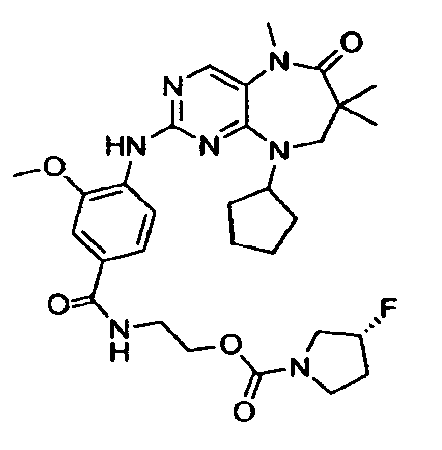
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,55-1,96 (8H, м), 2,05-2,15 (2H, м), 3,19 (3H, с), 3,88 (2H, с), 3,45-3,58 (6H, м), 3,94 (3H, с), 4,09-4,20 (2H, м), 7,46 (1H, д), 7,50 (1H, с), 7,72 (1H, с), 7,99 (1H, с), 8,37 (1H, д), 8,43-8,47 (1H, м); ВЭЖХ вр. уд. (мин): 9,49; МС (ES+) 598, (ES-) 596.
Пример 40:
4-(6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-9-фенил-5H- пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-40)
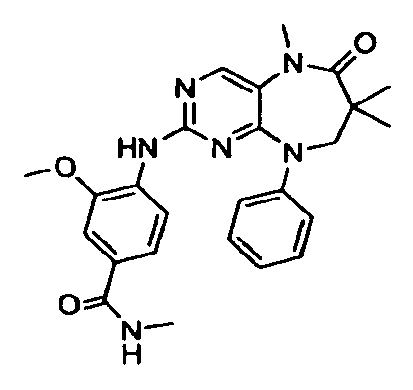
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,29 (6H, с), 2,78 (3H, д), 3,29 (3H, с), 3,89 (3H, с), 3,93 (2H, с), 6,86 (1H, дд), 7,08 (1H, д), 7,38-7,42 (3H, м), 7,52-7,57 (1H, м), 7,61 (2H, т), 8,26-8,30 (2H, м), 8,86 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,59; МС (ES+) 461, (ES-) 459.
Пример 41:
4-(9-циклопентил-5-этил-6,7,8,9-тетрaгидро-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилметилбензамид (I-41)
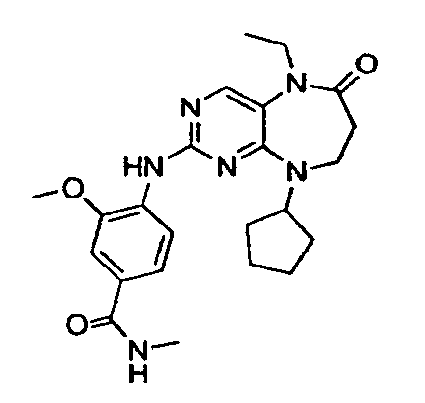
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,00 (3H, т), 1,56-1,76 (6H, м), 1,88-2,02 (2H, м), 2,50-2,56 (2H, м), 2,79 (3H, д), 3,61-3,64 (2H, м), 3,70 (2H, кв.), 3,94 (3H, с), 4,74 (1H, дт), 7,47 (1H, дд), 7,51 (1H, д), 7,86 (1H, ушир.с), 8,13 (1H, с), 8,28-8,33 (1H, м), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 8,76; МС (ES+) 439, (ES-) 437.
Пример 42:
4-(6-Циклопентил-5,6-дигидро-4H-2,3,6,7,9,10b-гексааза-бензо[e]азулен-8-иламино)-3-метокси-N-метилбензамид (I-42)
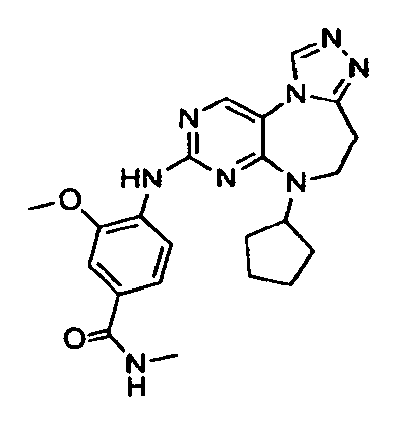
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,63-1,71 (4H, м), 1,73-1,85 (2H, м), 1,88-2,00 (2H, м), 2,85 (3H, д), 3,26-3,31 (2H, м), 3,62-3,67 (2H, м), 3,99 (3H, с), 5,26 (1H, дт), 7,53 (1H, дд), 7,57 (1H, д), 8,02 (1H, с), 8,34 (1H, д), 8,34-8,39 (1H, м), 8,45 (1H, с), 9,01 (1H, с); ВЭЖХ вр. уд. (мин): 7,88; МС (ES+) 435, (ES-) 433.
Пример 43:
2-(1H-бензо[d]имидазол-6-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-43)
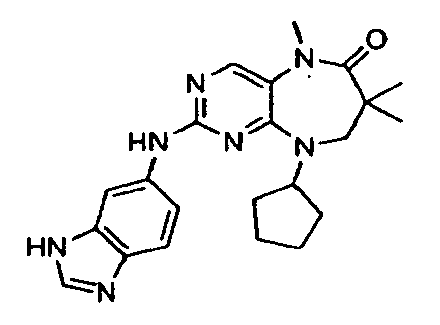
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,52-1,65 (4H, м), 1,66-1,76 (2H, м), 1,82-1,93 (2H, м), 3,20 (3H, с), 3,40 (2H, с), 5,25 (1H, дт), 7,69-7,76 (2H, м), 7,97 (1H, с), 8,26 (1H, ушир.с), 9,31 (1H, ушир.с), 9,67 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,52; МС (ES+) 406, (ES-) 404.
Пример 44:
2-(бензо[d]тиазол-6-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-44)
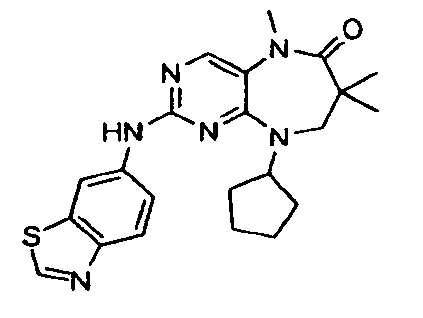
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,57-1,68 (4H, м), 1,69-1,79 (2H, м), 1,82-1,94 (2H, м), 3,20 (3H, с), 3,43 (2H, с), 5,22 (1H, дт), 7,62 (1H, дд), 7,97 (1H, с), 7,99 (1H, д), 8,65 (1H, ушир.с), 9,21 (1H, с), 9,70 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,99; МС (ES+) 423, (ES-) 421.
Пример 45:
2-(2-оксоиндолин-5-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-45)
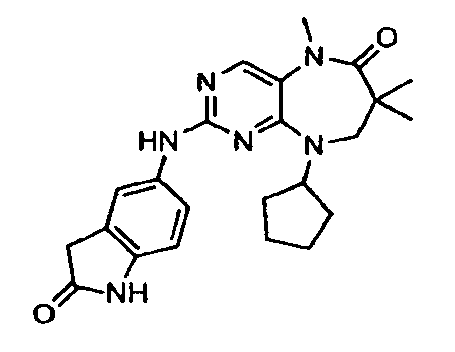
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,47-1,63 (4H, м), 1,64-1,78 (2H, м), 1,79-1,90 (2H, м), 3,17 (3H, с), 3,45 (2H, с), 3,47 (2H, с), 5,13 (1H, дт), 6,79 (1H, д), 7,29 (1H, д), 7,49 (1H, с), 7,83 (1H, с), 9,60 (1H, ушир.с), 10,33 (1H, с); ВЭЖХ вр. уд. (мин): 8,59; МС (ES+) 421, (ES-) 419.
Пример 46:
3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-метилбензамид (I-46)
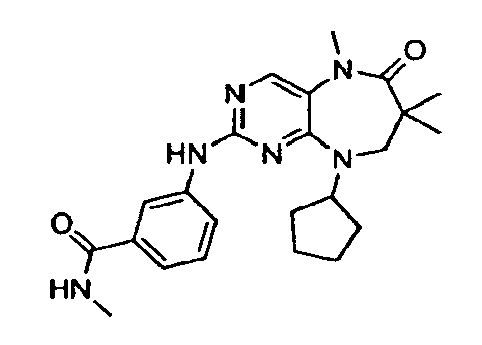
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,50-1,62 (4H, м), 1,62-1,75 (2H, м), 1,78-1,90 (2H, м), 2,77 (3H, д), 3,19 (3H, с), 3,44 (2H, с), 7,39 (1H, дд), 7,47 (1H, д), 7,59 (1H, д), 7,94 (1H, с), 8,19 (1H, дд), 8,34-8,39 (1H, м), 9,85 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 8,80; МС (ES+) 423, (ES-) 421.
Пример 47:
2-(1H-индазо-6-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-47)
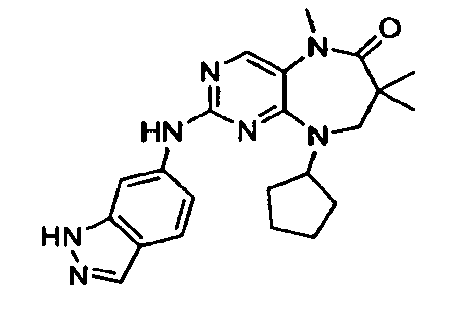
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,51-1,77 (6H, м), 1,81-1,90 (2H, м), 3,19 (3H, с), 3,46 (2H, с), 5,21 (1H, дт), 7,25 (1H, дд), 7,69 (1H, д), 7,85 (1H, с), 7,93 (1H, с), 8,01 (1H, с), 9,98 (1H, ушир.с), 12,97 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,25; MS (ES+) 406, (ES-) 404.
Пример 48:
2-(4-(lH-имидазол-1-ил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-48)
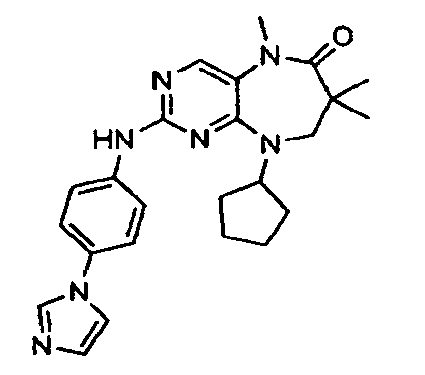
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,56-1,69 (4H, м), 1,70-1,77 (2H, м), 1,83-1,94 (2H, м), 3,19 (3H, с), 3,42 (2H, с), 5,23 (1H, дт), 7,69 (1H, с), 7,72 (1H, с), 7,87-7,93 (2H, м), 7,93 (1H, с), 8,01 (1H, с), 8,23 (1H, дд), 9,58 (1H, с), 9,79 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,75; МС (ES+) 432, (ES-) 430.
Пример 49:
2-(4-(1H-l,2,4-триазол-1-ил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-49)
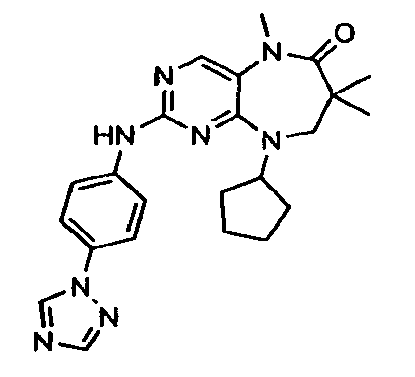
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,57-1,68 (4H, м), 1,69-1,79 (2H, м), 1,82-1,95 (2H, м), 3,19 (3H, с), 3,45 (2H, с), 5,19 (1H, дт), 7,75-7,83 (4H, м), 7,96 (1H, с), 8,22 (1H, с), 9,23 (1H, с), 9,88 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,45; МС (ES+) 433, (ES-) 431.
Пример 50:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-изопропокси-N-метилбензамид (I-50)
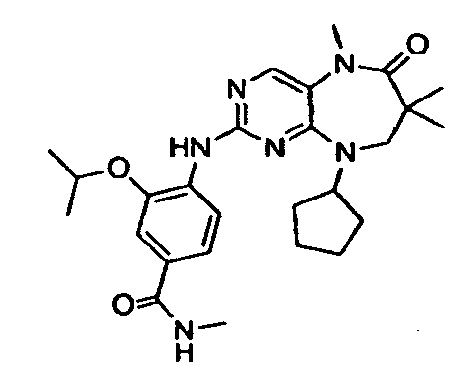
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,36 (6H, д), 1,57-1,70 (4H, м), 1,70-1,81 (2H, м), 1,85-1,94 (2H, м), 2,78 (3H,д), 3,19 (3H, с), 3,39 (2H, с), 4,68-4,78 (1H, м), 5,08-5,18 (1H, м), 7,44 (1H, д), 7,50 (1H, с), 7,62 (1H, с), 7,98 (1H, с), 8,30-8,35 (1H, м), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 9,84; МС (ES+) 481, (ES-) 479.
Пример 51:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-изопропокси-N-(1-метилпиперидин-4-ил)бензамид (I-51)
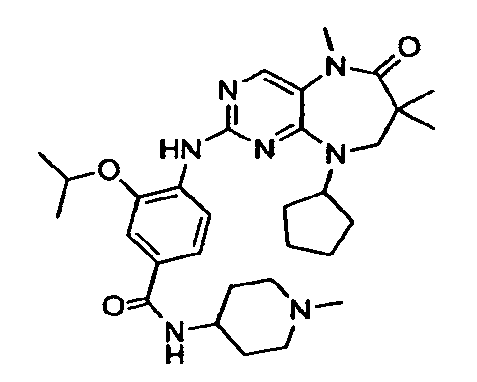
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,35 (6H, д), 1,55-2,05 (14H, м), 2,19 (3H, с), 2,78-2,87 (2H, м), 3,19 (3H, с), 3,39 (2H, с), 3,22-3,30 (1H, м), 4,73-4,82 (1H, м), 5,09-5,20 (1H, м), 7,47 (1H, д), 7,52 (1H, с), 7,34 (1H, с), 7,98 (1H, с), 8,09 (1H, д), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 10,05; МС (ES+) 564, (ES-) 562.
Пример 52:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-изопропилазетидин-3-ил)-3-метоксибензамид (I-52)
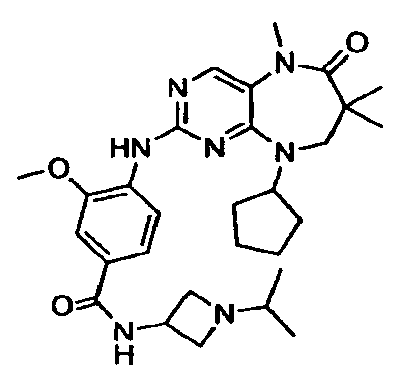
Получают по способу H, используя подходящие реагенты. ЯМР ДМСО D6 0,89 (6H, д), 1,10 (6H, с), 1,55-1,93 (8H, м), 2,32-2,42 (1H, м), 2,90-3,06 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,48-3,61 (2H, м), 3,95 (3H, с), 4,35-4,47 (1H, м), 5,17-5,26 (1H, м), 7,49 (1H, д), 7,50 (1H, с), 7,71 (1H, с), 7,99 (1H, с), 8,38 (1H, д), 8,63 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,60; МС (ES+) 536, (ES-) 534.
Пример 53:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(циклопропилметил)азетидин-3-ил)-3-метоксибензамид (I-53)
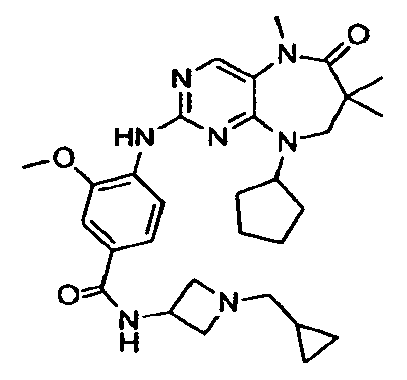
Получают по способу H, используя подходящие реагенты. ЯМР ДМСО D6 0,00-0,05 (2H, м), 0,30-0,35 (2H, м), 0,50-0,71 (1H, м), 1,00 (6H, с), 1,47-1,85 (8H, м), 2,17-2,26 (2H, м), 2,88-3,00 (2H м), 3,09 (3H, с), 3,29 (2H, с), 3,48-3,57 (2H, м), 3,85 (3H, с), 4,32-4,42 (1H, м), 5,04-5,14 (1H, м), 7,38 (1H, д), 4,41 (1H, с), 7,61 (1H, с), 7,90 (1H, с), 8,28 (1H, д), 8,53 (1H, д); ВЭЖХ вр. уд. (мин): 9,68; МС (ES+) 548, (ES-) 546.
Пример 54:
Способ J: 2-(бензиламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-54)
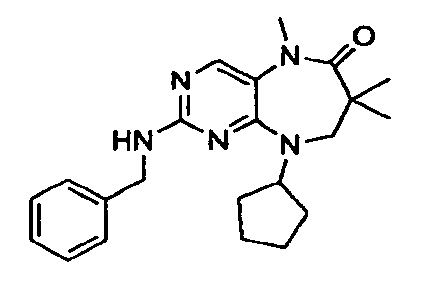
К 2-Хлор-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-ону (50 мг, 0,162 ммоль) в н-бутаноле (2 мл) добавляют бензиламин (71 мкл, 0,648 ммоль) и диизопропилэтиламин (113 мкл, 0,648 ммоль). Реакционную смесь нагревают до 140°C в микроволновой печи в течение 90 минут. Неочищенную смесь концентрируют в вакууме и очищают методом препаративной ВЭЖХ на обращенной фазе [Waters Sunfire C18, 10 мкм, 100 A колонка, градиент 10% - 95% B (растворитель A: 0,05% TFA в воде; растворитель B: CH3CN) в течение 16 минут со скоростью 25 мл/мин с получением указанного в заголовке соединения (33 мг) в виде не совсем белого порошка. ЯМР ДМСО D6 1,10 (6H, с), 1,46-1,58 (4H, м), 1,60-1,74 (4H, м), 3,13 (3H, с), 3,42 (2H, с), 4,52 (2H, д), 4,95-5,04 (1H, м), 7,24-7,30 (1H, м), 7,31-7,39 (4H, м), 7,83 (1H, с), 8,64 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 10,36; МС (ES+) 380, (ES-) 378.
Пример 55:
9-циклопентил-8,9-дигидро-5,7,7-триметил-2-(фенэтиламино)-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-55)
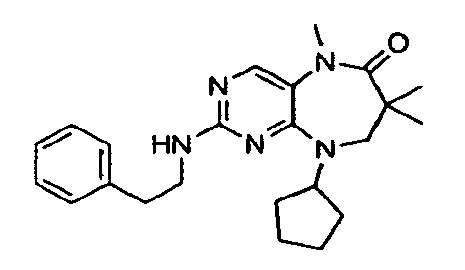
Получают по способу J, используя подходящие реагенты. ЯМР ДМСО D6 1,07 (6H, с), 1,51-1,60 (4H, м), 1,62-1,72 (2H, м), 1,77-1,89 (2H, м), 2,78-2,84 (2H, м), 3,13 (3H, с), 3,31 (2H, д), 3,36-3,45 (2H, м), 5,18-5,28 (1H, м), 7,17-7,24 (3H, м), 7,26-7,32 (2H, м), 7,78 (1H, c); ВЭЖХ вр. уд. (мин): 10,64; МС (ES+) 394, (ES-) 392.
Пример 56:
4-(6,7,8,9-тетрагидро-9-(тетрагидро-2H-пиран-4-ил)-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-56)
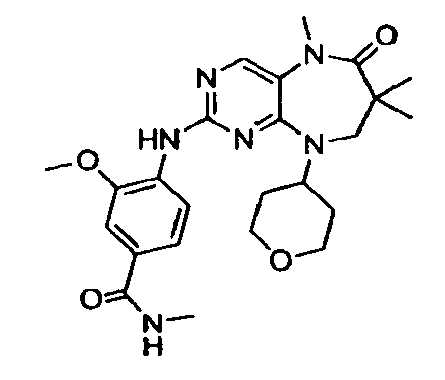
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,63 (2H, ушир.д), 1,91 (2H, дкв.), 2,82 (3H, д), 3,18 (3H, с), 3,37 (2H, т), 3,57 (2H, с), 3,94 (3H, с), 4,01 (2H, дд), 4,92 (1H, тт), 7,57 (1H, дд), 7,60 (1H, д), 8,06 (1H, д), 8,09 (1H, с), 8,51 (1H, кв.), 9,32 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 7,94; МС (ES+) 469, (ES-) 467.
Пример 57:
2-((R)-2,3-дигидро-1H-инден-1-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-57)
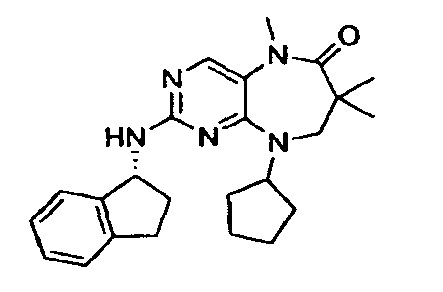
Получают по способу J, используя подходящие реагенты. ЯМР ДМСО D6 1,08 (6H, с), 1,41-1,57 (4H, м), 1,59-1,82 (4H, м), 1,91-2,04 (1H, м), 2,36-2,45 (1H, м), 2,74-2,84 (1H, м), 2,90-2,98 (1H, м), 3,15 (3H, с), 3,29 (2H, д), 5,01-5,16 (1H, м), 5,32-5,44 (1H, м), 6,94 (1H, ушир.с), 7,11-7,24 (4H, м), 7,81 (1H, с); ВЭЖХ вр. уд. (мин): 10,83; МС (ES+) 406, (ES-) 404.
Пример 58:
4-(9-(циклопропилметил)-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-58)
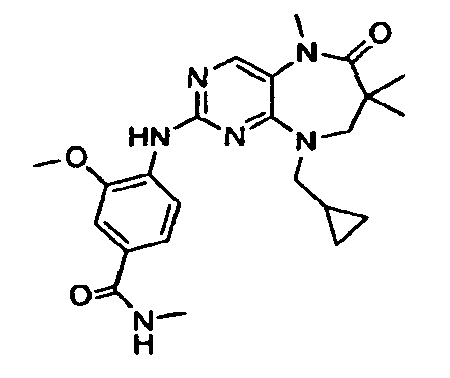
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,27-0,35 (2H, м), 0,47-0,53 (2H, м), 1,15-1,25 (7H, м), 2,80 (3H, д), 3,19 (3H, с), 3,66 (2H, д), 3,72 (2H, с), 3,94 (3H, с), 7,51 (1H, дд), 7,57 (1H, д), 8,03 (1H, с), 8,07 (1H, д), 8,46 (1H, кв.), 9,15 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,72; МС (ES+) 439, (ES-) 437.
Пример 59:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][l,4]диазепин-2-иламино)-N-(1-(циклопропилметил)пиперидин-4-ил)-3-метоксибензамид (I-59)
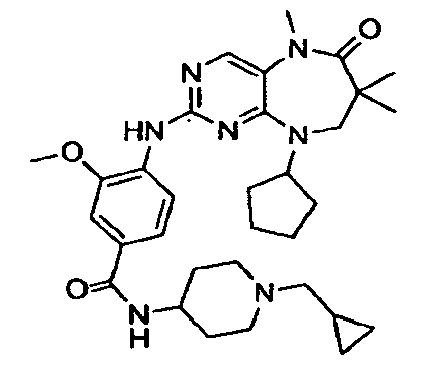
Получают по способу H, используя подходящие реагенты. ЯМР ДМСО D6 0,00-0,05 (2H, м), 0,30-0,35 (2H, м), 0,50-0,71 (1H, м), 1,00 (6H, с), 1,47-1,85 (8H, м), 2,17-2,26 (2H, м), 2,88-3,00 (2H м), 3,09 (3H, с), 3,29 (2H, с), 3,48-3,57 (2H, м), 3,85 (3H, с), 4,32-4,42 (1H, м), 5,04-5,14 (1H, м), 7,38 (1H, д), 4,41 (1H, с), 7,61 (1H, с), 7,90 (1H, с), 8,28 (1H, д), 8,53 (1H, д); ВЭЖХ вр. уд. (мин): 9,68; МС (ES+) 548, (ES-) 546.
Пример 60:
4-(9-циклопентил-5'-метил-6-оксо-5',6',8',9'-тетрагидроспиро[циклобутан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метокси-N-метилбензамид (I- 60)
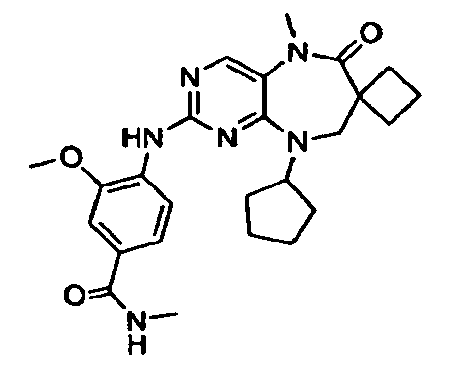
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,67-1,89 (9H, м), 2,08-2,10 (2H, м), 2,30-2,40 (3H, м), 2,85 (3H, д), 3,27 (3H, с), 3,70 (2H, с), 3,99 (3H, с), 4,88 (1H, квинт.), 7,52 (1H, д), 7,56 (1H, с), 7,79 (1H, с), 8,11 (1H, с), 8,40 (1H, д), 8,44 (1H, д); ВЭЖХ вр. уд. (мин): 9,30; МС (ES+) 465, (ES-) 463.
Пример 61:
4-((R)-S-циклопентил-6,7,8,9-тетрагидро-5,8-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-61)
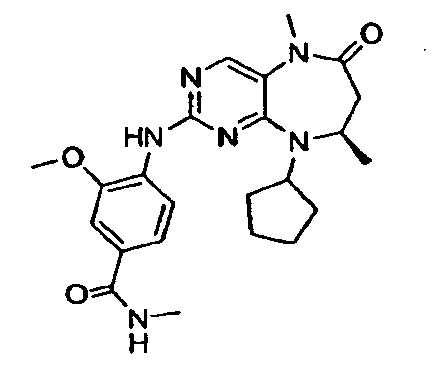
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,18 (3H, д), 1,31-1,49 (1H, м), 1,60-1,81 (5H, м), 1,90-1,96 (1H, м), 1,97-2,02 (1H, м), 2,33-2,40 (2H, м), 2,78 (3H, д), 3,19 (3H, с), 3,96 (3H, с), 4,03 (1H, т), 4,66 (1H, квинт.), 7,46 (1H, д), 7,50 (1H, с), 7,78 (1H, м), 8,10 (1H, с), 8,30-8,34 (2H, м); ВЭЖХ вр. уд. (мин): 8,70; MS (ES+) 439, (ES-) 437.
Пример 62:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][l,4]диазепин]-2'-иламино)-3-метокси-N-метилбензамид (I-62)
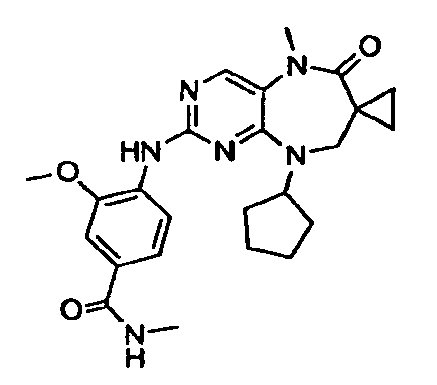
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,66-0,69 (2H, м), 0,88-0,92 (2H, м), 1,48-1,72 (6H, м), 1,85-1,91 (2H, м), 2,78 (3H, д), 3,17 (3H, с), 3,48 (2H, с), 3,94 (3H, с), 4,85 (1H, квинт.), 7,46 (1H, д), 7,49 (1H, с), 7,69 (1H, с), 7,90 (1H, с), 8,33 (1H, м), 8,40 (1H, д); ВЭЖХ вр. уд. (мин): 8,80; МС (ES+) 451, (ES-) 449.
Пример 63:
2-(4-морфолинофениламин)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-63)
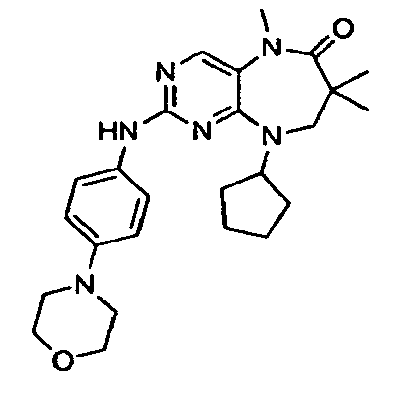
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,48-1,85 (8H, м), 3,10 (4H, т), 3,16 (3H, с), 3,48 (2H, с), 3,75 (4H, т), 5,11 (1H, дт), 6,98 (2H, д), 7,38 (2H, д), 7,84 (1H, с), 10,01 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,47; МС (ES+) 451, (ES-) 449.
Пример 64:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклобутан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид (I-64)
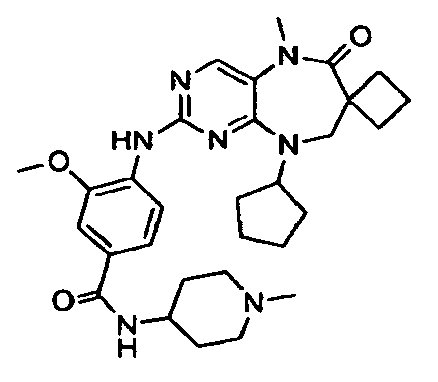
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,53-1,71 (9H, м), 1,78-1,99 (6H, м), 2,08-2,12 (2H, м), 2,20-2,33 (6H, м), 2,77-2,96 (2H, м), 3,19 (3H, с), 3,65 (2H, с), 3,75-3,84 (1H, м), 3,95 (3H, с), 4,83 (1H, квинт.), 7,48 (1H, д), 7,50 (1H, с), 7,73 (1H, с), 8,06 (1H, с), 8,13 (1H, ушир.д), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 9,50; МС (ES+) 548, (ES-) 546.
Пример 65:
4-((R)-9-циклопентил-6,7,8,9-тетрагидро-5,8-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид (I-65)
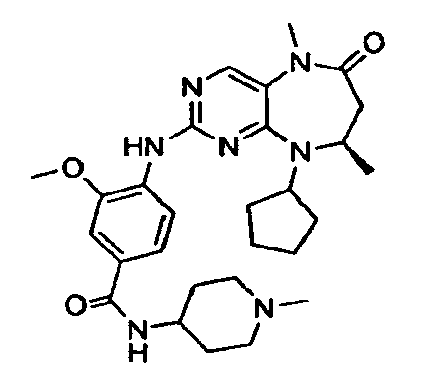
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,27 (3H, д), 1,33-1,42 (1H, м), 1,56-1,79 (9H), 1,91-2,02 (4H, м), 2,20 (3H, с), 2,41-2,54 (1H, м), 2,66-2,75 (1H, м), 2,76-2,86 (2H, м), 3,21 (3H, с), 3,71-3,79 (1H, м), 3,94 (3H, с), 4,00-4,05 (1H, м), 4,64 (1H, квинт.), 7,48 (1H, д), 7,49 (1H, с), 7,74 (1H, с), 8,11 (1H, с), 8,13 (1H, с), 8,32 (1H, д); ВЭЖХ вр. уд. (мин): 8,50; МС (ES+) 522, (ES-) 520.
Пример 66:
4-(9-((R)-1-циклопропилметил)пирролидин-3-ил)-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-66)
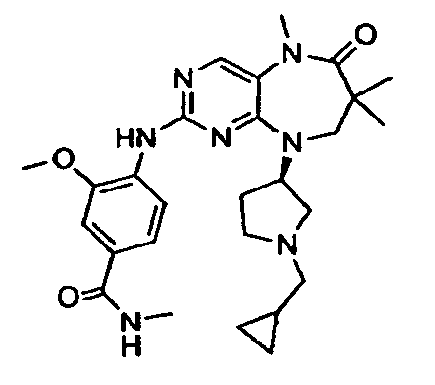
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,27-0,35 (2H, м), 0,47-0,53 (2H, м), 1,15-1,25 (7H, м), 2,80 (3H, д), 3,19 (3H, с), 3,66 (2H, д), 3,72 (2H, с), 3,94 (3H, с), 7,51 (1H, дд), 7,57 (1H, д), 8,03 (1H, с), 8,07 (1H, д), 8,46 (1H, кв.), 9,15 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 7,93; МС (ES+) 508, (ES-) 507.
Пример 67:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][l,4]диазепин-2-иламин)-N-(1-(изопропилпиперидин-4-ил)-3-метоксибензамид (I-67)
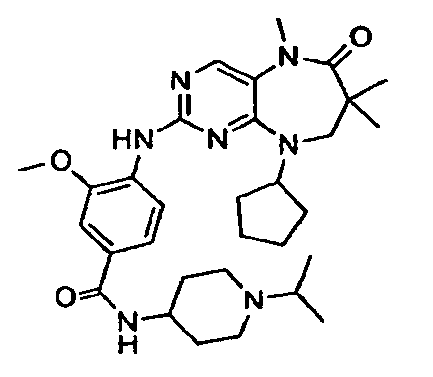
Получают по способу H, используя подходящие реагенты. ЯМР CDCl3 1,05 (6H, д), 1,13 (6H, с), 1,40-2,41 (13H, м), 2,78-2,95 (3H, м), 3,20 (3H, с), 3,30 (2H, с), 3,90 (3H, с), 3,90-4,01 (1H, м), 5,18-5,30 (1H, м), 5,96-6,01 (1H, м), 7,17 (1H, д), 7,19 (1H, с), 7,34 (1H, с), 7,55 (1H, с), 7,78 (1H, с), 8,41 (1H, д); ВЭЖХ вр. уд. (мин): 9,06; МС (ES+) 564, (ES-) 562.
Пример 68:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1,2,2,6, 6-пентаметилпиперидин-4-ил)бензамид (I-68)
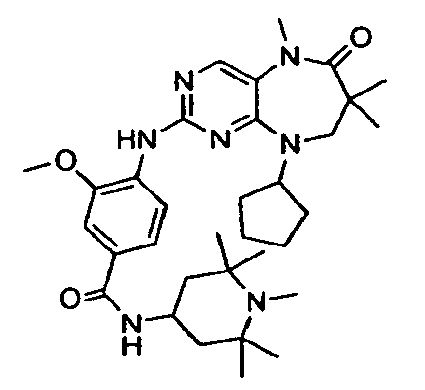
Получают по способу Е, используя подходящие реагенты. ЯМР CDCl3 1,07 (12H, с), 1,20 (6H, с), 1,40-1,95 (11H, м), 2,28 (3H, с), 3,22 (3H, с), 3,30 (2H, с), 3,90 (3H, с), 4,30-4,40 (1H, м), 5,20-5,29 (1H, м), 5,33-5,43 (1H, м), 7,16 (1H, д), 7,19 (1H, с), 7,36 (1H, с), 7,56 (1H, с), 7,78 (1H, с), 8,41 (1H, д); ВЭЖХ вр. уд. (мин): 9,07; МС (ES+) 591, (ES-) 590.
Пример 69:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1- (пропилпиперидин-4-ил)бензамид (I-69)
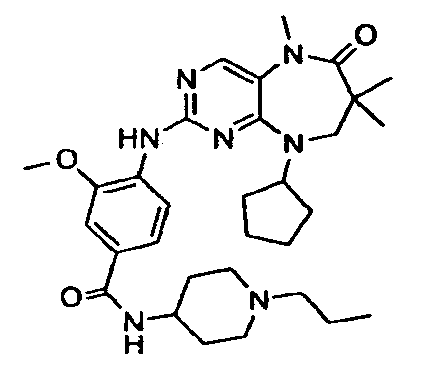
Получают по способу H, используя подходящие реагенты. ЯМР CDCl3 0,85 (3H, т), 1,13 (6H, с), 1,17-1,21 (2H, м), 1,47-2,40 (19H, м), 2,90-2,99 (2H, м), 3,22 (3H, с), 3,30 (2H, с), 3,90 (3H, с), 3,91-4,02 (1H, м), 5,18-5,28 (1H, м), 5,95-6,00 (1H, м), 7,16 (1H, д), 7,18 (1H, с), 7,34 (1H, с), 7,55 (1H, с), 7,78 (1H, с), 8,41 (1H, д); ВЭЖХ вр. уд. (мин): 9,45; МС (ES+) 564, (ES-) 562.
Пример 70:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(изобутилпиперидин-4-ил)-3-метоксибензамид (I-70)
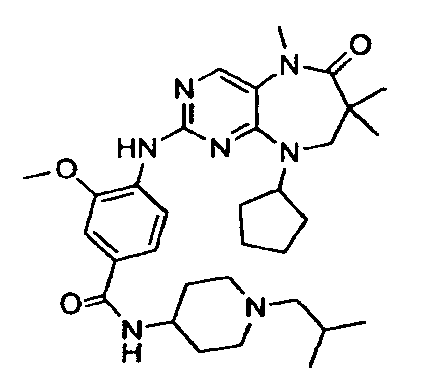
Получают по способу H, используя подходящие реагенты. ЯМР CDCl3 0,85 (6H, д), 1,13 (6H, с), 1,41-2,15 (16H, м), 2,75-2,85 (2H, м), 3,23 (3H, с), 3,30 (2H, с), 3,90 (3H, с), 3,90-3,97 (1H, м), 5,20-5,29 (1H, м), 5,91-5,97 (1H, м), 7,14 (1H, с), 7,20 (1H, с), 7,34 (1H, с), 7,55 (1H, с), 7,78 (1H, с), 8,41 (1H, д); ВЭЖХ вр. уд. (мин): 9,83; МС (ES+) 578, (ES-) 576.
Пример 71:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-трет-бутилпиперидин-4-ил)-3-метоксибензамид (I-71)
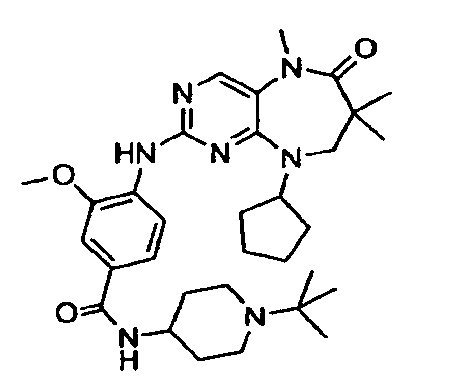
Получают по способу Е, используя подходящие реагенты. ЯМР CDCl3 1,10 (9H, с), 1,13 (6H, с), 1,40-2,09 (12H, м), 2,26-2,36 (2H, м), 2,97-3,10 (2H, м), 3,23 (3H, с), 3,30 (2H, с), 3,90 (3H, с), 3,30-3,10 (1H, м), 5,18-5,28 (1H, м), 5,95-6,01 (1H, м), 7,15 (1H, д), 7,20 (1H, с), 7,35 (1H, с), 7,55 (1H, с), 7,78 (1H, с), 8,41 (1H, д); ВЭЖХ вр. уд. (мин): 8,83; МС (ES+) 578, (ES-) 576.
Пример 72:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(этилпиперидин-4-ил)-3-метоксибензамид (I-72)
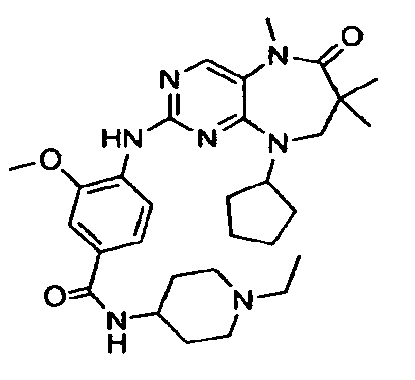
Получают по способу H, используя подходящие реагенты. ЯМР CDCl3 1,22 (3H, т), 1,26 (6H, с), 1,50-2,18 (HH, м), 2,20-2,34 (2H, м), 2,58 (2H, кв.), 3,06-3,13 (2H, м), 3,32 (3H, с), 3,39 (2H, с), 4,00 (3H, с), 4,02-4,15 (1H, м), 5,27-5,37 (1H, м), 6,00-6,07 (1H, м), 7,25 (1H, д), 7,28 (1H, с), 7,43 (1H, с), 7,65 (1H, с), 7,87 (1H, с), 8,50 (1H, с); ВЭЖХ вр. уд. (мин): 9,12; МС (ES+) 550, (ES-) 548.
Пример 73:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][l,4]диазепин-2-иламино)-N-((S)-1-изоипропилпирролидин-3-ил)-3-метоксибензамид (I-73)
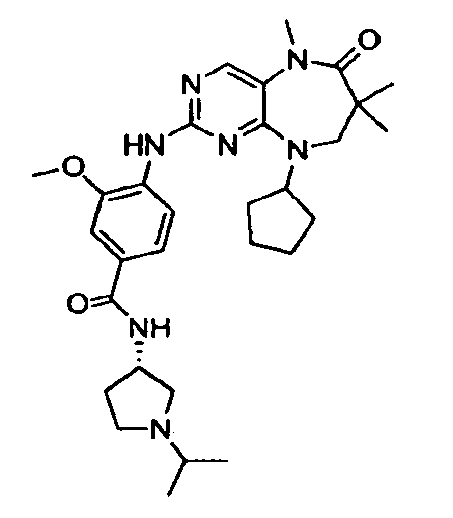
Получают по способу H, используя подходящие реагенты. ЯМР ДМСО D6 1,02-1,14 (12H, м), 1,53-2,23 (10H, м), 2,08-2,15 (1H, м), 2,45-3,00 (4H, м), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,40 (1H, м), 5,19 (1H, м), 7,47-7,53 (2H, м), 7,70 (1H, с), 7,99 (1H, с), 8,33-8,40 (2H, м); ВЭЖХ вр. уд. (мин): 9,42; МС (ES+) 551, (ES-) 549.
Пример 74:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-этокси-N-(1-метилпиперидин-4-ил)бензамид (I-74)
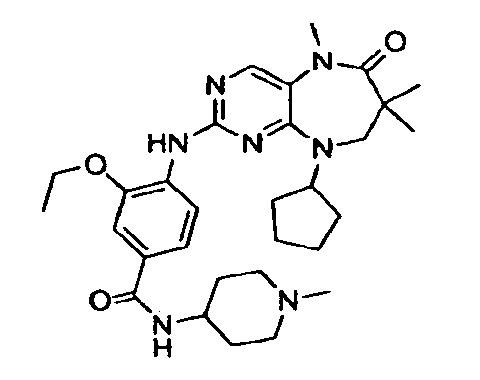
Получают по способу D, используя подходящие реагенты. ЯМР CDCl3 1,18 (6H, с), 1,43 (3H, т), 1,50 (2H, ушир.м), 1,69 (6H, ушир.м), 1,97 (4H, ушир.м), 2,22 (2H, ушир.м), 2,32 (3H, с), 2,89 (2H, ушир.м), 3,21 (3H, с), 3,31 (2H, с), 4,05 (1H, ушир.м), 4,15 (2H, кв.), 5,22 (1H, м), 6,10 (NH), 7,17 (1H, м), 7,31 (1H, с), 7,60 (NH), 7,78 (1H, с), 8,41 (1H, м); ВЭЖХ вр. уд. (мин): 9,93; МС (ES+) 550, (ES-) 548.
Пример 75:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((S)-I-(циклопропилметил)пирролидин-3-ил)-3-метоксибензамид (I-75)
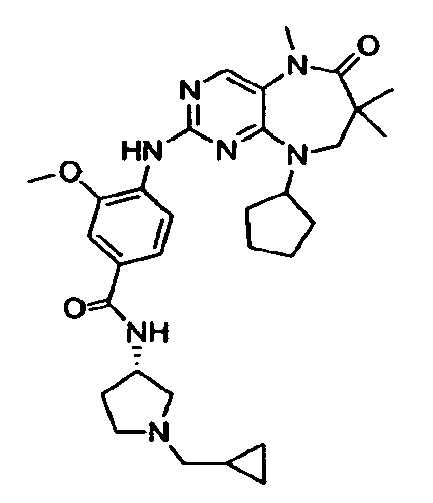
Получают по способу H, используя подходящие реагенты. ЯМР ДМСО D6 -0,01 (2H, кв.), 0,35 (2H, м), 0,76 (1H, гепт.), 1,00 (6H, с), 1,45-1,85 (9H, м), 2,07 (1H, м), 2,18 (2H, д), 2,35-2,47 (2H, м), 2,60-2,75 (2H, м), 3,09 (3H, с), 3,28 (2H, с), 3,85 (3H, с), 4,31 (1H, гекс), 5,09 (1H, квинт.), 7,40-7,47 (2H, м), 7,60 (1H, с), 7,90 (1H, с), 8,24-8,29 (2H, м); ВЭЖХ вр. уд. (мин): 9,67; МС (ES+) 562, (ES-) 561.
Пример 76:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид (I-76)
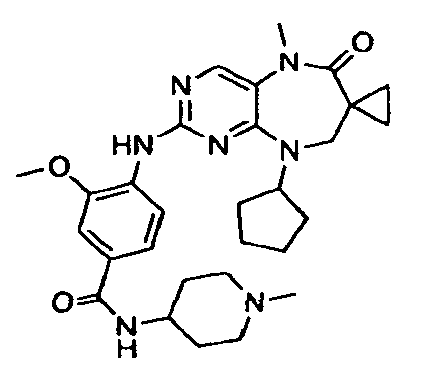
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,73-0,75 (2H, м), 0,91-0,98 (2H, м), 1,51-1,79 (8H, м), 1,84-2,00 (5H, м), 2,31-2,42 (4H, м), 2,95-3,05 (2H7 м), 3,23 (3H, с), 3,54 (2H, с), 3,81-3,94 (1H, м), 4,01 (3H, с), 4,91 (1H, квинт.), 7,54 (1H, д), 7,55 (1H, с), 7,58 (1H, с), 8,05 (1H, с), 8,20 (1H, д), 8,45 (1H, д); ВЭЖХ вр. уд. (мин): 8,90; МС (ES+) 532, (ES-) 534.
Пример 77:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(l-(2-фторэтил)пиперидин-4-ил)-3-метоксибензамид (I-77)
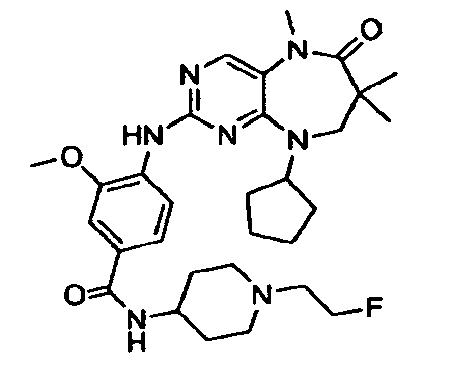
Получают по способу H, используя подходящие реагенты. ЯМР CDCl3 1,13 (6H, с), 1,40-1,80 (7H, м), 1,85-1,95 (2H, м), 1,97-2,05 {2H, м), 2,23-2,34 (2H, м), 2,66-2,78 (2H, м), 2,93-3,02 (2H, м), 3,23 (3H, с), 3,30 (2H, с), 3,91 (3H, с), 3,90-4,04 (1H, м), 1,45-1,64 (2H, м), 5,16-5,28 (1H, м), 5,85-5,95 (1H, м), 7,15 (1H, д), 7,20 (1H, с), 7,34 (1H, с), 7,56 (1H, с), 7,78 (1H, с), 8,42 (1H, д); ВЭЖХ вр. уд. (мин): 9,58; МС (ES+) 568, (ES-) 566.
Пример 78:
N-(4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)-2,2,2-трифторацетамид (I-78)
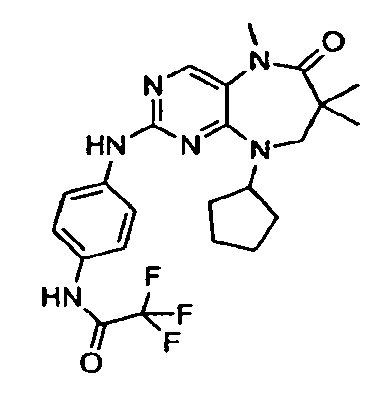
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,52-1,68 (4H, м), 1,69-1,78 (2H, м), 1,79-1,94 (2H, м), 3,17 (3H, с), 3,43 (2H, с), 5,16 (1H, дт), 7,60 (2H, д), 7,65 (2H, д), 7,92 (1H, с), 9,64 (1H, ушир.с), 11,19 (1H, с); ВЭЖХ вр. уд. (мин): 9,90; МС (ES+) 477, (ES-) 475.
Пример 79:
2-(1-ацетилиндолин-5-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-79).
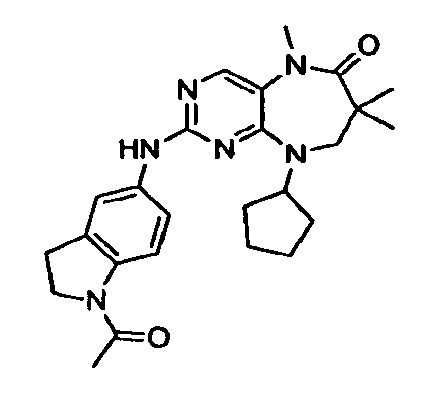
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,50-1,68 (4H, м), 1,69-1,77 (2H, м), 1,78-1,88 (2H, м), 2,14 (3H, с), 3,12 (2H, т), 3,16 (3H, с), 3,44 (2H, с), 4,10 (2H, т), 5,15 (1H, дт), 7,26 (1H, д), 7,54 (1H, с), 7,86 (1H, с), 7,97 (1H, д), 9,65 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,37; МС (ES+) 449, (ES-) 447.
Пример 80:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-метилбензамид (I-80).
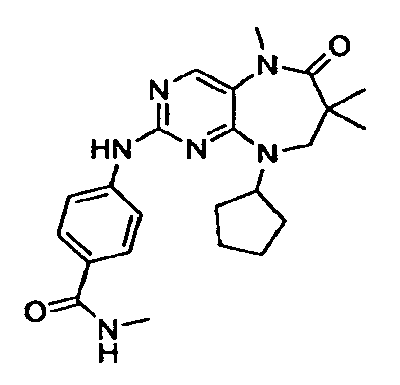
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,55-1,69 (4H, м), 1,70-1,80 (2H, м), 1,82-1,93 (2H, м), 2,78 (3H, д), 3,18 (3H, с), 3,45 (2H, с), 5,20 (1H, дт), 7,71 (2H, д), 7,79 (2H, д), 7,97 (1H, с), 8,27-8,34 (1H, м), 9,86 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,73; МС (ES+) 423, (ES-) 421.
Пример 81:
2-(1H-индазол-4-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-81).
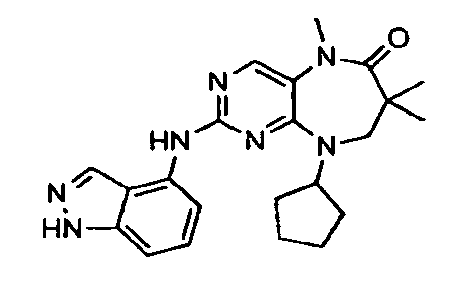
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,41-1,79 (8H, м), 3,20 (3H, с), 3,44 (2H, с), 5,10 (1H, дт), 7,22-7,34 (2H, м), 7,51-7,59 (1H, м), 7,95 (1H, с), 8,27 (1H, с), 9,91 (1H, ушир.с), 13,10 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,32; МС (ES+) 406, (ES-) 404.
Пример 82:
2-(1,6-дигидро-6-оксопиридин-3-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-82).
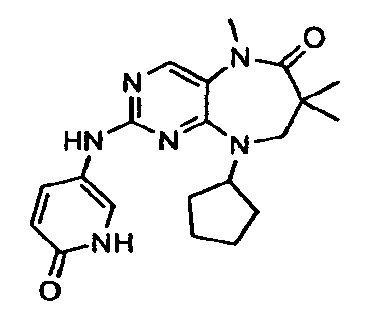
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,48-1,84 (8H, м), 3,16 (3H, с), 3,45 (2H, с), 5,00-5,09 (1H, м), 6,39 (1H, д), 7,54 (1H, д), 7,61 (1H, с), 7,81 (1H, с), 9,45 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 7,77, MS (ES+) 383, (ES-) 381.
Пример 83:
2-(1,6-дигидро-4-метил-6-оксопиридин-3-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-83)
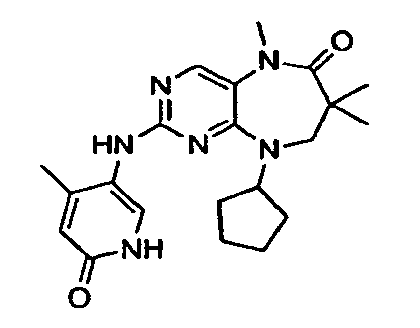
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,39-1,78 (8H, м), 2,04 (3H, с), 3,16 (3H, с), 3,48 (2H, с), 6,30 (1H, с), 7,49 (1H, с), 7,75 (1H, ушир.с), 9,39 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 7,86; MS (ES+) 397, (ES-) 395.
Пример 84:
2-(3-метокси-5-нитрофениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-84).
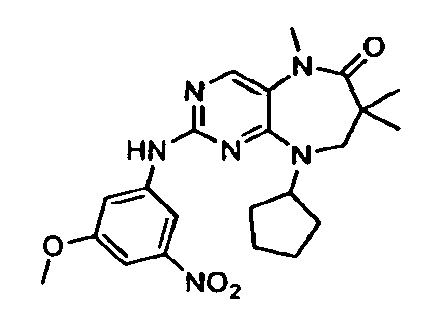
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 1,56-1,77 (6H, м), 1,83-1,96 (2H, м), 3,19 (3H, с), 3,42 (2H, с), 3,86 (3H, с), 5,29 (1H, дт), 7,33 (1H, т), 7,60 (1H, т), 8,01 (1H, с), 8,41 (1H, т), 9,88 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 10,48; МС (ES+) 441, (ES-) 439.
Пример 85:
2-(4-(4-метилпиперазин-l-ил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-85)
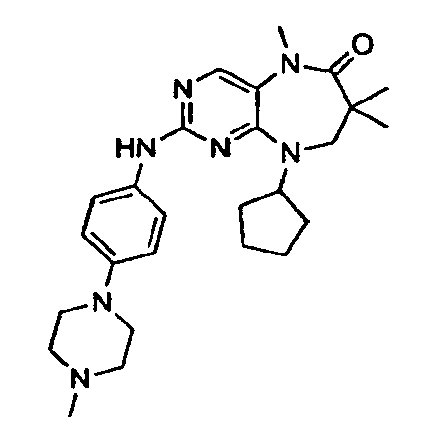
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,51-1,65 (4H, м), 1,66-1,75 (2H, м), 1,76-1,86 (2H, м), 2,88 (3H, с), 2,86-2,94 (2H, м), 3,17 (3H, с), 3,12-3,24 (2H, м), 3,45 (2H, с), 3,53 (2H, д), 3,79 (2H, д), 5,13 (1H, дт), 7,00 (2H, д), 7,46 (2H, д), 7,90 (1H, с), 9,75 (1H, ушир.с), 9,86 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 9,66; МС (ES+) 464, (ES-) 462.
Пример 86:
2-(4-морфолинметил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-86)
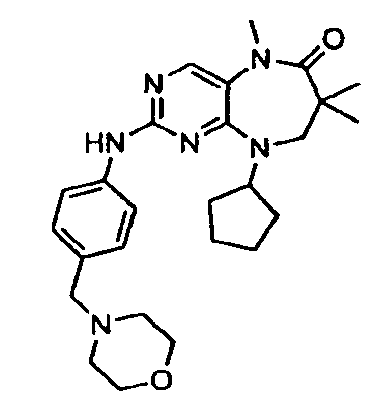
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 1,53-1,67 (4H, м), 1,69-1,78 (2H, м), 1,80-1,94 (2H, м), 3,02-3,17 (2H, м), 3,19 (3H, с), 3,26 (2H, д), 3,40 (2H, с), 3,62 (2H, т), 3,97 (2H, д), 4,28 (2H, д), 5,21 (1H, дт), 7,39 (2H, д), 7,79 (2H, д), 7,97 (1H, с), 9,62 (1H, ушир.с), 9,75 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 9,82; MS (ES+) 465, (ES-) 463.
Пример 87:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-илaмино)-N-(2-гидроксиэтил)бензамид (I-87)
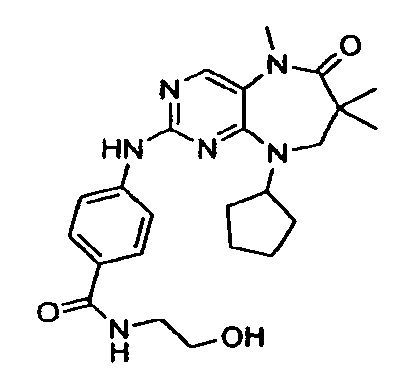
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 1,56-1,66 (4H, м), 1,68-1,81 (2H, м), 1,83-1,95 (2H, м), 3,20 (3H, с), 3,20-3,28 (2H, м), 3,41 (2H, с), 4,40 (2H, т), 5,23 (1H, дт), 7,86 (2H, д), 7,92-7,99 (4H, м), 8,01 (1H, с), 9,80 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,74; МС (ES+) 453, (ES-) 451.
Пример 88:
N-(4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)-N-метилацетамид (I-88).
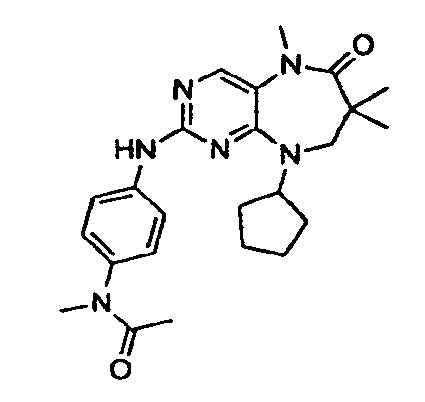
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 1,52-1,65 (4H, м), 1,66-1,73 (2H, м), 1,77 (3H, с), 1,77-1,86 (2H, м), 3,13 (3H, с), 3,18 (3H, с), 3,44 (2H, с), 5,13 (1H, дт), 7,29 (2H, д), 7,65 (2H, д), 7,93 (1H, с), 9,80 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 9,38; MS (ES+) 437, (ES-) 435.
Пример 89:
2-(1H-индазо-7-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-89)
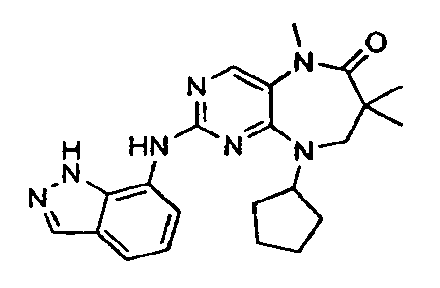
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,40-1,79 (8H, м), 3,20 (3H, с), 3,45 (2H, с), 5,09 (1H, дт), 7,25-7,34 (2H, м), 7,53 (1H, д), 7,94 (1H, с), 8,26 (1H, с), 9,95 (1H, ушир.с), 13,11 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,33; МС (ES+) 406, (ES-) 404.
Пример 90:
9-циклопентил-8,9-дигидро-5,7,7-триметил-2-(фениламино)-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-90)
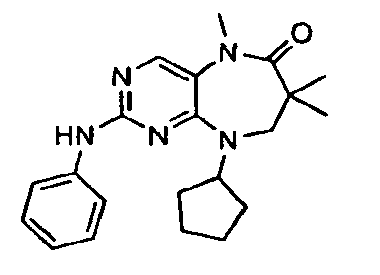
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,51-1,89 (8H, м), 3,18 (3H, с), 3,45 (2H, с), 5,16 (1H, дт), 7,07 (1H, т), 7,34 (2H, т), 7,59 (2H, д), 7,91 (1H, с), 9,77 (1H, ушир.с); ВЭЖХ вр. уд. (мин) 10,38; МС (ES+) 366, (ES-) 364.
Пример 91:
2-(2-метил-2H-индазол-7-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-91)
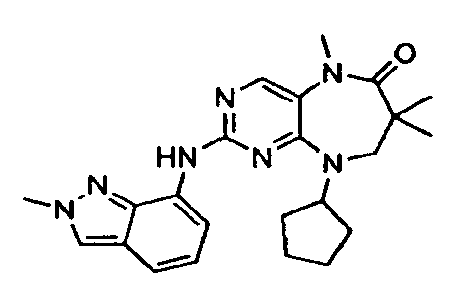
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,53-1,78 (6H, м), 1,81-1,93 (2H, м), 3,19 (3H, с), 3,53 (2H, с), 4,22 (3H, с), 5,18 (1H, дт), 7,05 (1H, т), 7,47 (1H, д), 7,80 (1H, д), 8,02 (1H, с), 8,43 (1H, с), 9,60 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 10,19; MS (ES+) 420.
Пример 92:
Способ K: 2-([1,2,4]триазоло[1,5-a]пиридин-8-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-92)
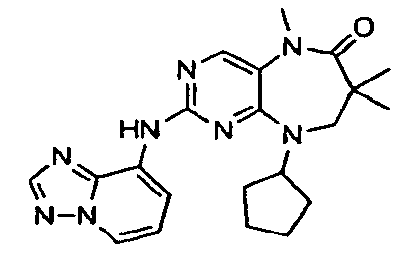
К 2-хлор-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-ону (50 мг, 0,16 ммоль) и триазолопиридинамину (22 мг, 0,16 ммоль) в диоксане (1,5 мл) добавляют ксантфос (2,8 мг, 0,005 ммоль), ацетат палладия (II) (0,7 мг, 0,003 ммоль) и карбонат цезия (106 мг, 0,32 ммоль). Реакционную смесь нагревают при 160°С в микроволновой печи в течение 40 минут. Неочищенную смесь фильтруют через слой целлита и промывают метанолом. Полученную смесь концентрируют в вакууме и очищают методом препаративной ВЭЖХ на обращенной фазе [Waters Sunfire C18, 10 мкм, 100 A колонка, градиент 10% - 95% B (растворитель A: 0,05% TFA в воде; растворитель B: CH3CN) в течение 16 минут со скоростью 25 мл/мин] с получением указанного в заголовке соединения в виде соли TFA (6,2 мг). ЯМР ДМСО D6 1,13 (6H, с), 1,53-1,66 (4H, м), 1,68-1,77 (2H, м), 1,81-1,90 (2H, м), 3,20 (3H, с), 3,46 (2H, с), 5,15 (1H, дт), 7,21 (1H, т), 8,05 (1H, с), 8,23 (1H, д), 8,53 (1H, с), 8,64 (1H, д), 9,05 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,71; МС (ES+) 407, (ES-) 405.
Пример 93:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклопропил-3-метоксибензамид (I-93)
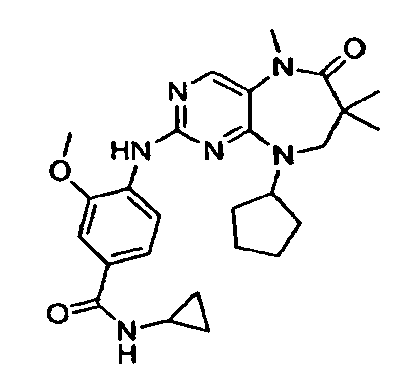
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,55-0,59 (2H, м), 0,68-0,73 (2H, м), 1,09 (6H, с), 1,54-1,68 (4H, м), 1,70-1,78 (2H, м), 1,83-1,95 (2H, м), 2,79-2,84 (1H, м), 3,19 (3H, с), 3,38 (2H, с), 4,03 (3H, с), 5,16-5,22 (1H, м), 7,43-7,47 (2H, м), 7,70 (1H, ушир.с), 7,99 (1H, с), 8,32-8,35 (2H, м); ВЭЖХ вр. уд. (мин): 9,60; MS (ES+) 479, (ES-) 477.
Пример 94:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклобутил-3-метоксибензамид (I-94)
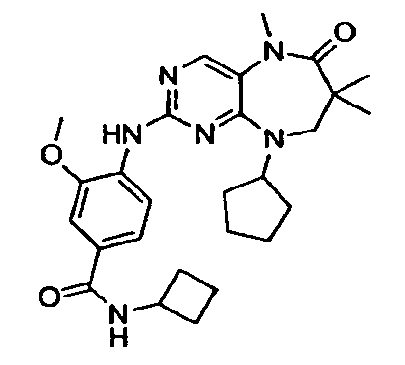
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,58-1,78 (8H, м), 1,84-1,91 (2H, м), 2,03-2,13 (2H, м), 2,18-2,23 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,37-4,46 (1H, м), 5,15-5,23 (1H, м), 7,46-7,49 (2H, м), 7,69 (1H, с), 7,99 (1H, с), 8,36 (1H, д), 8,46 (1H, д); ВЭЖХ вр. уд. (мин): 10,10; МС (ES+) 493, (ES-) 491.
Пример 95:
Трет-бутиловый эфир 4-[4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][l,4]диазепин-2-илметил)-3-метоксибензоиламино]пиперидин-l-карбоксильной кислоты (I-95)
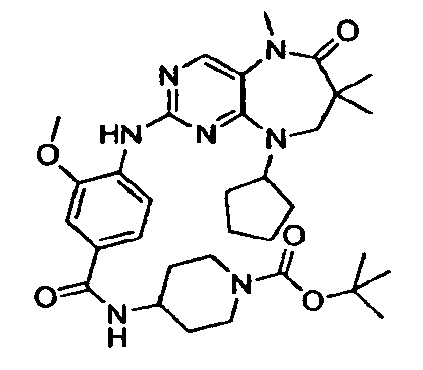
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,45 (3H, с), 1,48 (9H, с), 1,64-1,97 (10H, м), 2,90 (2H, ушир.с), 3,25 (3H, с), 3,44 (2H, с), 4,01 (3H, с), 4,02-4,10 (2H, ушир.с), 5,21-5,32 (1H, м), 7,51-7,54 (2H, м), 7,76 (1H, с), 8,06 (1H, с), 8,18 (1H, д), 8,43 (1H, с); ВЭЖХ вр. уд. (мин): 10,50; МС (ES+) 622, (ES-) 620.
Пример 96:
4-(6,7,8,9-тетрагидро-5,7,7-триметил-9-((R)-1-метилпиперидин-3-ил)-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-96)
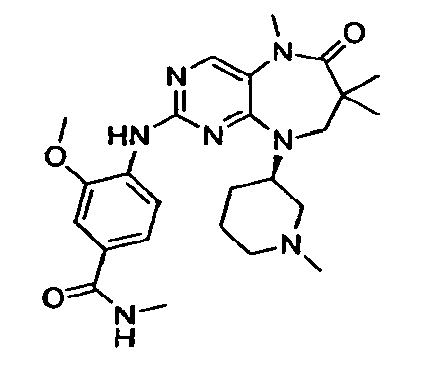
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,08 (3H, с), 1,10 (3H, с), 1,5-1,92 (5H, м), 2,00-2,10 (2H, м), 2,23 (3H, с), 2,79 (3H, д), 2,87 (1H, ушир.д), 3,18 (3H, с), 3,42 (2H, с), 3,94 (3H, с), 4,86 (1H, тт), 7,45 (1H, дд), 7,49 (1H, д), 7,66 (1H, с), 7,99 (1H, с), 8,30 (1H, кв.), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 7,64; МС (ES+) 482, (ES-) 480.
Пример 97:
4-(6,7,8,9-тетрагидро-5,7,7-триметил-9-((R)-1-метилпиперидин-4-ил)-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-97)
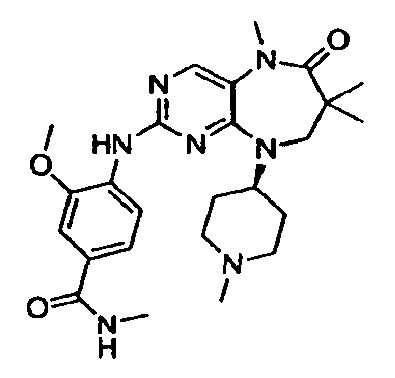
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,66 (2H, ушир.д), 1,83 (2H, дкв.), 2,00-2,15 (2H, м), 2,24 (3H, с), 2,79 (3H, д), 2,92 (2H, ушир.д), 3,18 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 4,71 (1H, тт), 7,47 (1H, дд), 7,50 (1H, д), 7,68 (1H, с), 7,98 (1H, с), 8,25-8,34 (2H, м); ВЭЖХ вр. уд. (мин): 7,28; МС (ES+) 482, (ES-) 480.
Пример 98:
2-(4-(5-гидрокси-3-метил-1H-пиразол-1-ил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-98)
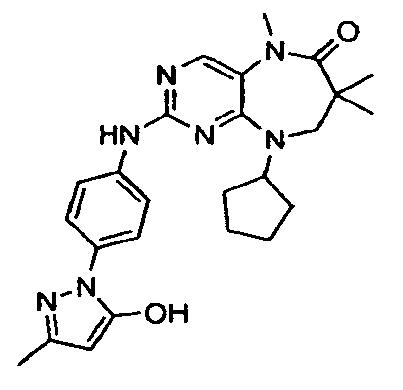
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,51-1,77 (6H, м), 1,81-1,92 (2H, м), 2,12 (3H, с), 3,19 (3H, с), 3,46 (2H, с), 5,17 (1H, дт), 5,36 (1H, с), 7,56-7,68 (4H, м), 7,90 (1H, с), 9,79 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,75; МС (ES+) 462, (ES-) 460.
Пример 99:
2-(4-(1H-пиразол-3-ил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-99)
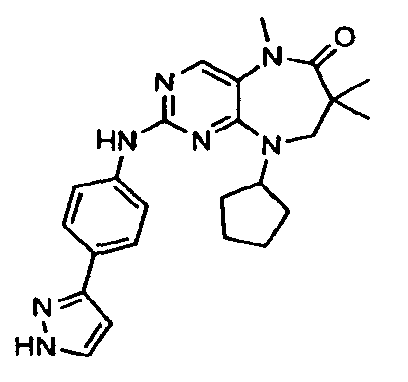
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,55-1,78 (6H, м), 1,82-1,93 (2H, м), 3,19 (3H, с), 3,48 (2H, с), 5,19 (1H, дт), 6,67 (1H, д), 7,62 (2H, д), 7,70 (1H, д), 7,78 (2H, д), 7,92 (1H, с), 9,93 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,45; МС (ES+) 432, (ES-) 430.
Пример 100:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-илтио)-N-метилбензамид (I-100)
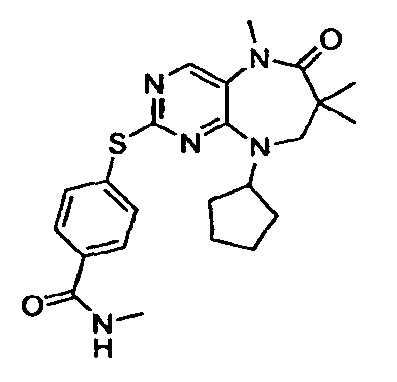
Способ L: 4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо [4,5-b][1,4]диазепин-2-илтио)-бензойная кислота
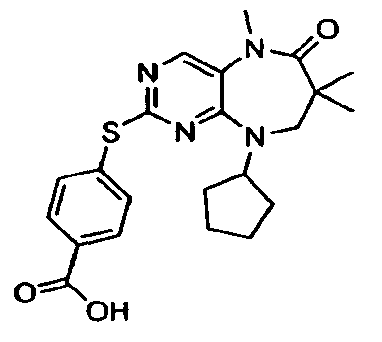
Раствор 2-хлор-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-она (100 мг, 0,324 ммоль) и 4-меркаптобензойной кислоты (50 мг, 0,324 ммоль) в ацетонитриле (5 мл) нагревают с обратным холодильникомв течение 4 часов. Затем добавляют еще порцию 4-меркаптобензойной кислоты (50 мг, 0,324 ммоль) и реакционную смесь нагревают с обратным холодильником в течение 16 часов. После охлаждения неочищенную смесь фильтруют через целит и промывают ацетонитрилом. Неочищенный продукт очищают при помощи колоночной хроматографии (0%-10% MeOH: CH2Cl2) и растирают с MeOH с получением указанного в заголовке соединения (37 мг, выход 27%) в виде твердого белого вещества. ЯМР ДМСО D6 1,03 (6H, с), 1,20-1,38 (6H, м), 1,42-1,53 (2H, м), 3,17 (3H, с), 3,27 (2H, с), 4,47 (1H, дт), 7,72 (2H, дд), 7,99 (2H, дд), 8,02 (1H, с); МС (ES+) 427, (ES-) 425.
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-илтио)-N-метилбензамид (I-100) получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,03 (6H, с), 1,22-1,44 (6H, м), 1,46-1,58 (2H, м), 2,80 (3H, д), 3,17 (3H, с), 3,28 (2H, с), 4,51 (1H, дт), 7,68 (2H, д), 7,91- (2H7 д), 8,02 (1H, с), 8,47-8,53 (1H, м); ВЭЖХ вр. уд. (мин): 8,86; МС (ES+) 440, (ES-) 438.
Пример 101:
2-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиперидин-4-ил)бензамид (I-101)
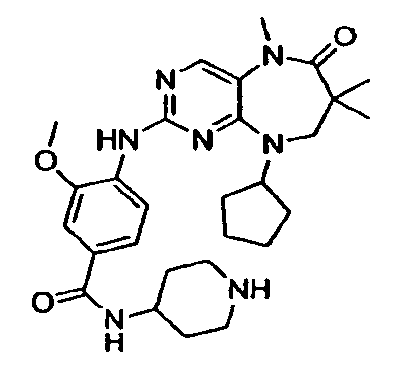
Получают по способу F, используя подходящие реагенты. ЯМР MeOD 1,21 (6H, с), 1,61-1,85 (8H, м), 2,02-2,15 (4H, м), 2,85 (2H, ушир.т), 3,23 (2H, ушир.д), 3,39 (3H, с), 3,48 (2H, с), 4,02 (3H, с), 4,03-4,10 (1H, м), 5,36 (1H, квинт.), 7,50-7,54 (2H, м), 7,94 (1H, с), 8,48 (1H, д); ВЭЖХ вр. уд. (мин): 9,00; МС (ES+) 522, (ES-) 520.
Пример 102:
2-(2-метоксифениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-102)
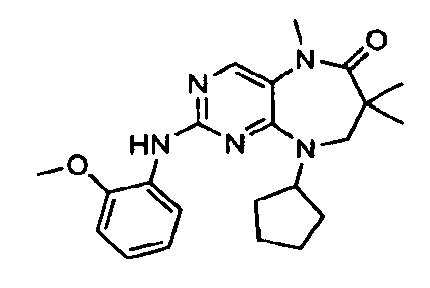
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,48-1,84 (8H, м), 3,18 (3H, с), 3,49 (2H, с), 3,87 (3H, с), 5,07 (1H, дт), 6,99 (1H, дт), 7,14 (1H, дт), 7,19 (1H, дт), 7,83 (1H, д), 7,94 (1H, с), 9,13 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 10,65; МС (ES+) 396, (ES-) 394.
Пример 103:
Метил 4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][l,4]диазепин-2-иламино)-3-метоксифенилкарбамат (I-103)
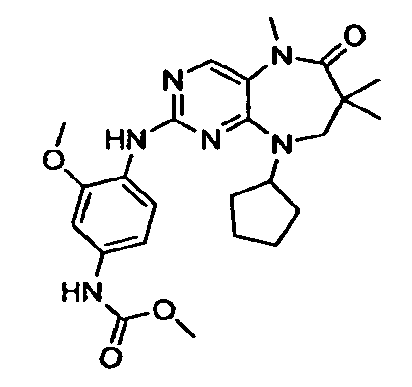
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,56 (4H, ушир.м), 1,71 (2H, ушир.м), 1,82 (2H, ушир.м), 3,17 (3H, с), 3,35 (2H, с), 3,66 (3H, с), 3,81 (3H, с), 5,11 (1H, ушир.м), 6,96 (1H, дд), 7,23 (1H, с), 7,44 (1H, с), 7,90 (1H, с), 7,98 (1H, д), 9,46 (1H ушир.с); ВЭЖХ вр. уд. (мин): 9,60; МС (ES+) 469, (ES-) 467.
Пример 104:
N-(4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксифенил)-2-метоксиацетамид (I-104)
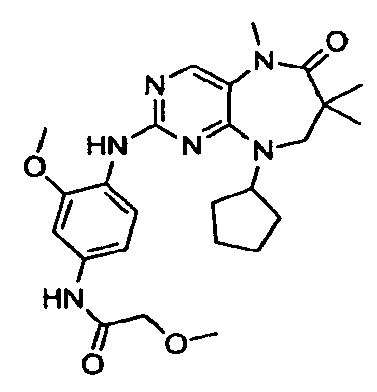
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,57 (4H, ушир.м), 1,71 (2H, ушир.м), 1,84 (2H, ушир.м), 3,18 (3H, с), 3,35 (2H, с), 3,39 (3H, с), 3,83 (3H, с), 3,98 (2H, с), 5,13 (1H, ушир.м), 7,23 (1H, дд), 7,46 (2H, с), 7,92 (1H, с), 8,06 (1H, д), 9,6O (1H, ушир.с]); ВЭЖХ вр. уд. (мин): 9,50; МС (ES+) 483, (ES-) 481.
Пример 105:
[4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2,2,2-трифторэтил)-3-метоксибензамид (I-105)
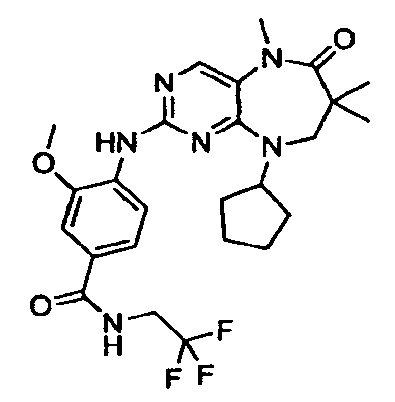
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,63 (4H, ушир.м), 1,75 (2H, ушир.м), 1,89 (2H, ушир.м), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,10 (2H, м), 5,20 (1H, м), 7,54 (2H, м), 7,73 (NH), 8,00 (1H, с), 8,43 (1H, м), 8,41 (1H, с); ВЭЖХ вр. уд. (мин): 9,94; MS (ES+) 521, (ES-) 519.
Пример 106:
9-циклопентил-5,7,7-триметил-2-[3-(4-метилпиперазин-1-карбонил)фениламино]-5,7,8,9-тетрагидропиримидо[4,5-b][1,4]диазепин-6-он (I-106)
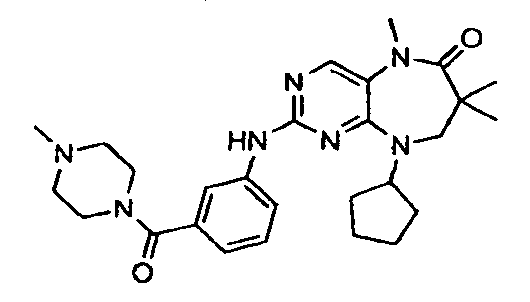
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,57 (4H, ушир.м), 1,71 (2H, ушир.м), 1,85 (2H, ушир.м), 2,82-3,34 (8H, ушир.м), 3,19 (3H, с), 3,36 (3H, с), 5,23 (1H, м), 6,97 (1H, м), 7,31 (1H, м), 7,69 (1H, м), 7,96 (2H, м), 9,33 (1H, с); ВЭЖХ вр. уд. (мин): 9,12; MS (ES+) 492, (ES-) 490.
Пример 107:
Способ M: 4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-илокси)-3-метоксибензойная кислота (I-107)
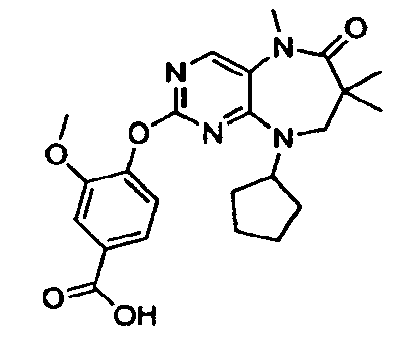
К 2-хлор-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-ону (100 мг, 0,324 ммоль) в ДМФ (5 мл) добавляют ванилиновую кислоту (55 мг, 0,324 ммоль) и карбонат калия (90 мг, 0,648 ммоль). Реакционную смесь нагревают при 80°C в течение 48 часов. После охлаждения растворитель удаляют в вакууме, остаток помещают в метанол и очищают методом препаративной ВЭЖХ на обращенной фазе [колонка Waters Sunfire C18, 10 мкM, 100 A, градиент 10% - 95% B (растворитель A: 0,05% ТФУ в воде; растворитель B: CH3CN) в течение 16 мин со скоростью 25 мл/мин] с получением указанного в заголовке соединения в виде соли ТФУ (12 мг, выход 7%). ЯМР ДМСО D6 1,06 (6H, с), 1,23-1,37 (2H, м), 1,38-1,50 (2H, м), 1,51-1,62 (4H, м), 3,18 (3H, с), 3,34 (2H, с), 3,76 (3H, с), 4,58 (1H, дт), 7,26 (1H, д), 7,56-7,62 (2H, м), 7,99 (1H, C); ВЭЖХ вр. уд. (мин): 7,18; МС (ES+) 441. (ES-) 439.
Пример 108:
2-(2,3-дигидро-2-оксо-1H-бензо[d]имидазол-6-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-108)
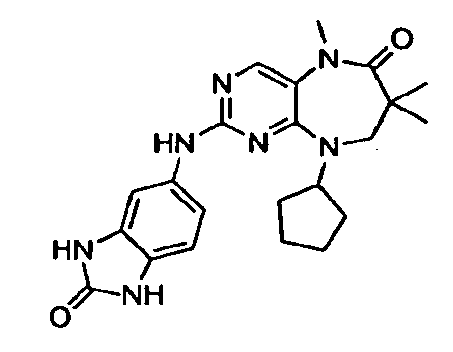
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,44-1,76 (6H, м), 1,78-1,92 (2H, м), 3,17 (3H, с), 3,46 (2H, с), 5,13 (1H, дт), 6,89 (1H, д), 7,05 (1H, д), 7,13 (1H, с), 7,81 (1H, с), 9,75 (1H, ушир.с), 10,57 (1H, с), 10,67 (1H, c); ВЭЖХ вр. уд. (мин): 8,21; MS (ES+) 422, (ES-) 420.
Пример 109:
2-(2,3-дигидро-3-оксо-1H-индазол-5-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-109)
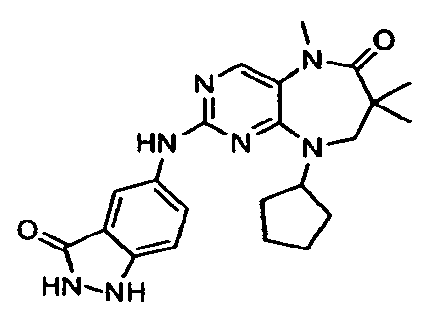
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,50-1,74 (6H, м), 1,79-1,90 (2H, м), 3,18 (3H, с), 3,46 (2H, с), 5,18 (1H, дт), 7,27 (1H, д), 7,37 (1H, дд), 7,85 (1H, с), 7,88 (1H, с), 9,76 (1H, ушир.с), 11,28 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,01; МС (ES+) 422, (ES-) 420.
Пример 110:
2-(1-метил-1H-индазол-5-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-110)
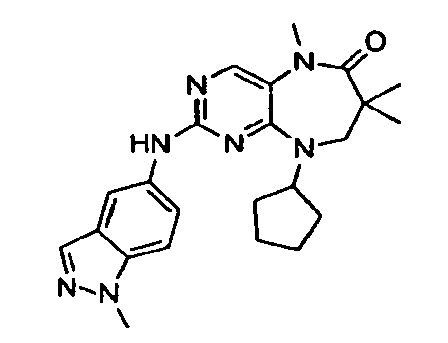
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,43-1,77 (6H, м), 1,78-1,88 (2H, м), 3,18 (3H, с), 3,48 (2H, с), 4,05 (3H, с), 5,14 (1H, дт), 7,48 (1H, дд), 7,66 (1H, д), 7,87 (1H, с), 7,96 (1H, с), 7,99 (1H, с), 10,01 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,65; MS (ES+) 420, (ES-) 418.
Пример 111:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)ацетамид (I-111)
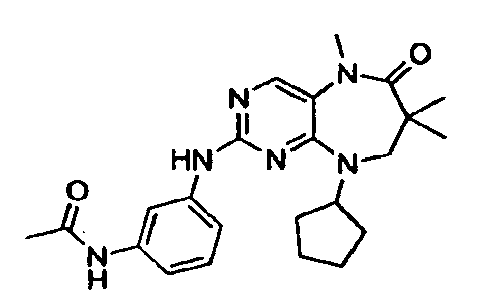
Получают по способу D, используя подходящие реагенты. ВЭЖХ вр.уд.(мин): 8,95; МС (ES+) 423, (ES-) 421.
Пример 112:
N-(4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)ацетамид (I-112)
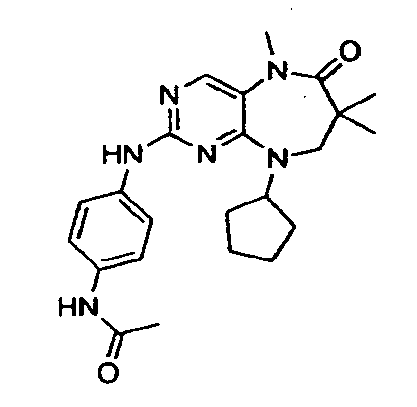
Получают по способу D, используя подходящие реагенты. ВЭЖХ вр.уд.(мин): 8,74; МС (ES+) 423, (ES-) 421.
Пример 113:
4-((S)-9-циклопентил-7-этил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метилпиперидин-4-ил)бензамид (I-113)
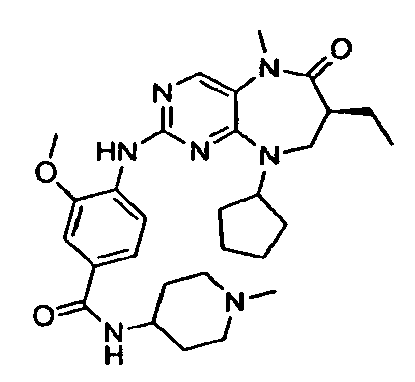
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,88 (3H, т), 1,04 (1H, д), 1,25-1,36 (1H, м), 1,52-1,85 (11H, м), 1,95-2,12 (3H, м), 2,20 (3H, с), 2,57-2,64 (1H, м), 2,78-2,83 (2H, м), 3,20 (3H, с), 3,41-3,45 (2H, м), 3,75-3,80 (1H, м), 3,95 (3H, с), 4,78 (1H, квинт.), 7,48 (1H, д), 7,49 (1H, с), 7,75 (1H, с), 8,07 (1H, д), 8,10 (1H, с), 8,39 (1H, д); ВЭЖХ вр. уд. (мин): 9,70; МС (ES+) 536, (ES-) 534.
Пример 114:
2-(1H-индазо-5-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-114)
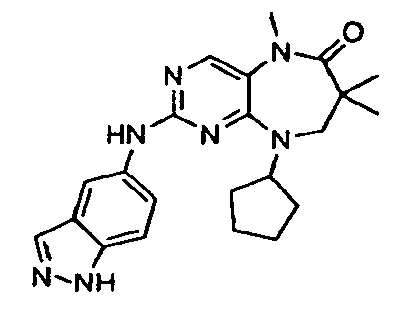
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,44-1,93 (8H, м), 3,18 (3H, с), 3,47 (2H, с), 5,14 (1H, дт), 7,43 (1H, дд), 7,55 (1H, д), 7,86 (1H, с), 7,98 (1H, с), 8,02 (1H, с), 9,92 (1H, ушир.с), 13,06 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,99; МС (ES+) 406, (ES-) 404.
Пример 115:
2-(1H-бензо[d]имидазол-4-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-115)
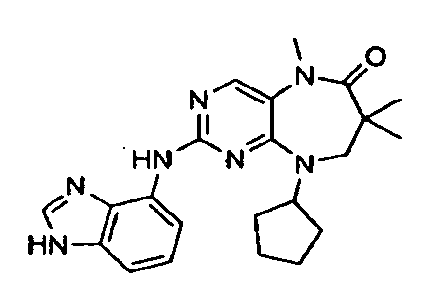
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,38-1,73 (8H, м), 3,20 (3H, с), 3,42 (2H, с), 4,96 (1H, дт), 7,42 (1H, т), 7,50 (1H, д), 7,70 (1H, д), 8,01 (1H, с), 9,09 (1H, ушир.с), 9,85 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,37; МС (ES+) 406, (ES-) 404.
Пример 116:
2-(3-аминофениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-116)
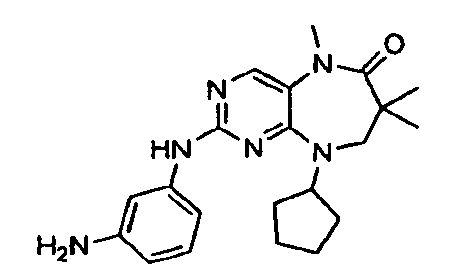
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,53-1,73 (6H, м), 1,80-1,92 (2H, м), 3,18 (3H, с), 3,43 (2H, с), 5,19 (1H, дт), 6,61 (1H, д), 7,14-7,24 (3H, м), 7,89 (1H, с), 9,67 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,16; МС (ES+) 381, (ES-) 379.
Пример 117:
2-(4-аминофениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-117)
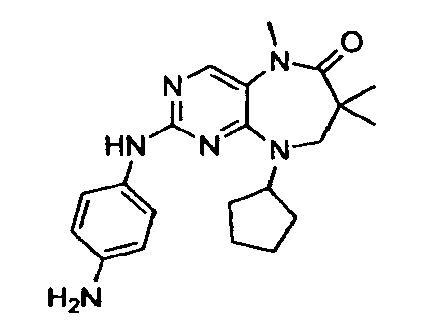
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,50-1,92 (8H, м), 3,18 (3H, с), 3,43 (2H, с), 5,16 (1H, дт), 7,01-7,10 (2H, м), 7,50-7,63 (2H, м), 7,89 (1H, с), 9,67 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 8,76; МС (ES+) 381, (ES-) 379.
Пример 118:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][l,4]диазепин-2-иламино)-3-этил-N-метилбензамид (I-118)
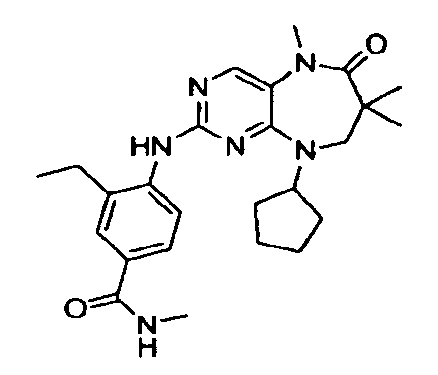
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,18 (3H, т), 1,44 (2H, ушир.м), 1,57-1,69 (6H, ушир.м), 2,51 (2H, кв.), 2,64 (3H, м), 2,79 (3H, с), 3,45 (3H, с), 4,95 (1H, м), 7,69 (2H, м), 7,78 (1H, м), 7,87 (1H, с), 8,38 (1H, c); ВЭЖХ вр. уд. (мин): 9,24; МС (ES+) 451, (ES-) 449.
Пример 119:
4-((S)-9-циклопентил-7-этил-6,7,8,9-тетрагидро-5-метил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклобутил-3-метоксибензамид (I-119)
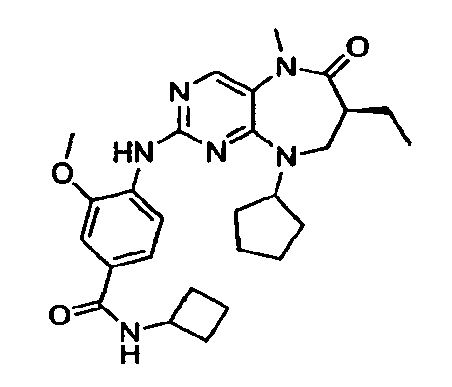
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,18 (3H, т), 1,44 (2H, ушир.м), 1,57-1,69 (6H, ушир.м), 2,51 (2H, кв.), 2,64 (3H, м), 2,79 (3H, с), 3,45 (3H, с), 4,95 (1H, м), 7,69 (2H, м), 7,78 (1H, м), 7,87 (1H, с), 8,38 (1H, с); ВЭЖХ вр. уд. (мин): 10,10; МС (ES+) 493, (ES-) 491.
Пример 120:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензойная кислота (I-120)
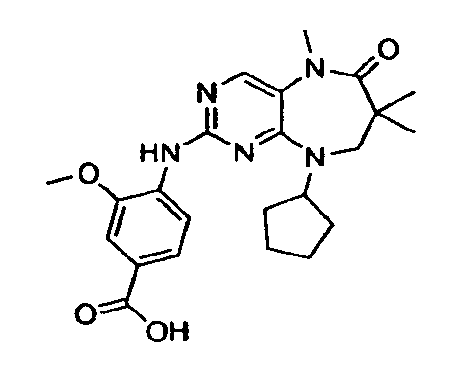
Получают по способу D, используя подходящие реагенты.
ВЭЖХ вр.уд.(мин): 7,81; МС (ES+) 440, (ES-) 438.
Пример 121:
3-(2-(пирролидин-1-ил)этокси)-4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-метилбензамид (I-121)
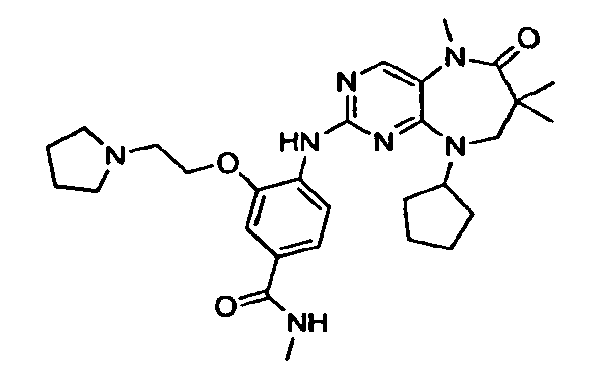
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 1,61 (4H, ушир.м), 1,74 (2H, ушир.м), 1,84 (2H, ушир.м), 1,91 (2H, ушир.м), 2,06 (2H, ушир.м), 2,79 (3H, м), 3,19 (5H, м), 3,43 (2H, с), 3,68 (4H, ушир.м), 4,42 (2H, м), 5,14 (1H, м), 7,50-7,55 (2H, м), 8,02 (1H, с), 8,24 (1H, м), 8,38 (1H, с); ВЭЖХ вр. уд. (мин): 8,87; МС (ES+) 536, (ES-) 534.
Пример 122:
4-(9-бензил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-122)
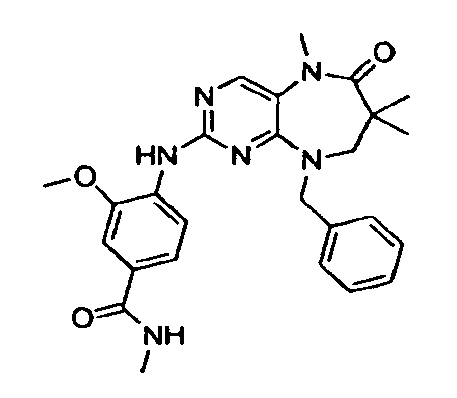
Способ N: 2-Хлор-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он
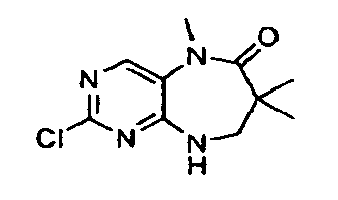
9-аллил-2-хлор-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (1,21 г, 4,34 ммоль, полученный по способу C) и дихлор(2,7-диметил-окта-2,6-диен-1,8-ил)рутений (IV) (0,26 г, 0,43 ммоль, полученный по способу, описанному в Tetrahedron Letters, 1965, 47, 4187) суспендируют в диоксане (10 мл) и воде (30 мл) в пробирке для работы под давлением. Полученную суспензию перемешивают при 100°C в течение двух ночей. Реакционную смесь оставляют охлаждаться до комнатной температуры и фильтруют через целит. Целит обильно промывают водой и DCM. Объединенные фильтраты концентрируют при пониженном давлении и распределяют между насыщенным соляным раствором и DCM. Водный слой экстрагируют дихлорметаном (5×20 мл), объединенные органические слои сушат над сульфатом натрия, фильтруют и концентрируют при пониженном давлении, получая коричневую смолу. Смолу очищают методом колоночной хроматографии (50% EtOAc в гексанах, на оксиде кремния, ~100 мл), получая белое твердое вещество, которое растирают в порошок с диэтиловым эфиром. Твердое вещество собирают фильтрацией и промывают диэтиловым эфиром (1×2 мл) и пентаном (3×2 мл), получая кремовый порошок (351 мг, выход 34%). ЯМР ДМСО D6 l,09 (6H, с), 3,22 (3H, с), 3,25 (2H, д), 8,08 (1H, с), 8,48 (1H, ушир.д); МС (ES+) 241.
Способ O: 9-бензил-2-хлор-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он
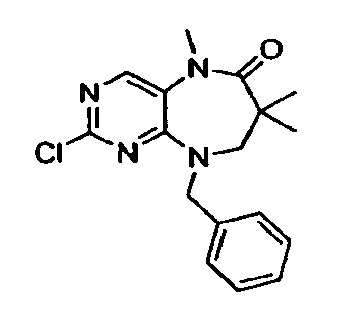
2-Хлор-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (50 мг, 0,21 ммоль) и бензилбромид (30 мл, 0,25 ммоль) в DMA (0,5 мл) обрабатывают 60% дисперсией гидрида натрия в масле (9 мг, 0,23 ммоль) при комнатной температуре. Смесь перемешивают при комнатной температуре в течение 5 часов. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией (50% EtOAc в гексанах, на оксиде кремния, ~50 мл), получая указанное в заголовке соединение в виде белого твердого вещества (63 мг, 91%). ЯМР ДМСО D6 1,00 (6H, с), 3,22 (3H, с), 3,53 (2H, с), 4,91 (2H, с), 7,28-7,39 (5H, м), 8,12 (1H, c); МС (ES+) 331.
4-(9-бензил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H- пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-122)
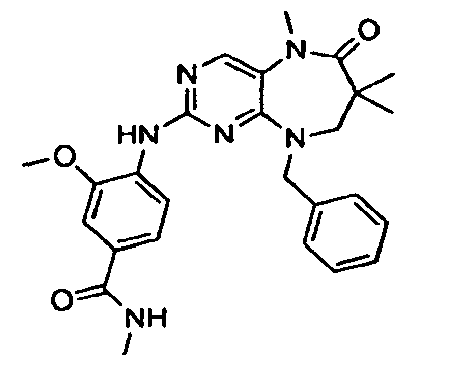
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,03 (6H, с), 2,75 (3H, д), 3,23 (3H, с), 3,47 (2H, с), 3,90 (3H, с), 4,98 (2H, ушир.с), 7,2-7,4 (6H, м), 7,45 (1H, с), 7,72 (1H, с), 8,07 (1H, с), 8,19 (1H, д), 8,27 (1H, ушир.д); ВЭЖХ вр. уд. (мин): 9,00; МС (ES+) 475, (ES-) 473.
Пример 123:
4-(9-(циклобутилметил)-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][l,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-123)
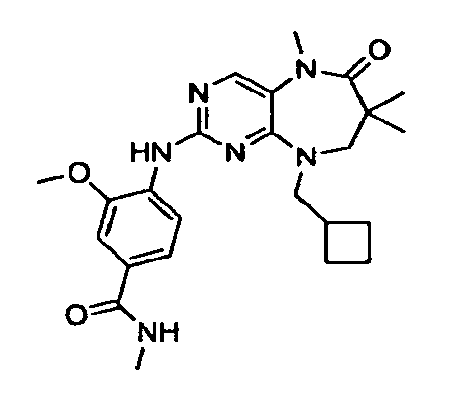
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,84 (4H, ушир.м), 2,05 (2H, ушир.м), 2,78 (4H, ушир.м), 3,18 (3H, с), 3,50 (2H, с), 3,78 (2H, д), 3,94 (3H, с), 7,47 (2H, м), 7,67 (1H, с), 7,97 (1H, с), 8,34 (2H, ушир.м); ВЭЖХ вр. уд. (мин): 9,20; МС (ES+) 453, (ES-) 451.
Пример 124:
2-(1-оксоизоиндолин-4-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-124)
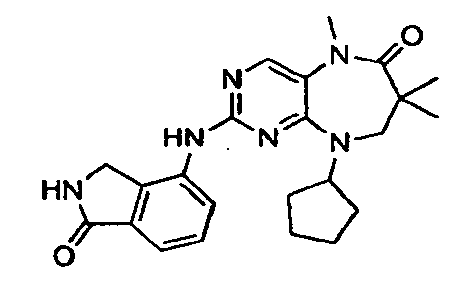
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,52 (4H, ушир.м), 1,69 (2H, ушир.м), 1,76 (2H, ушир.м), 3,18 (3H, с), 3,34 (2H, с), 4,40 (2H, с), 5,15 (1H, м), 7,31 (1H, д), 7,40 (1H, т), 7,96 (1H, с), 8,08 (1H, д), 8,52 (1H, с), 8,86 (1H, с); ВЭЖХ вр. уд. (мин): 8,90; МС (ES+) 421, (ES-) 419.
Пример 125:
2-(1-метил-2-оксоиндолин-5-илaмино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-125)
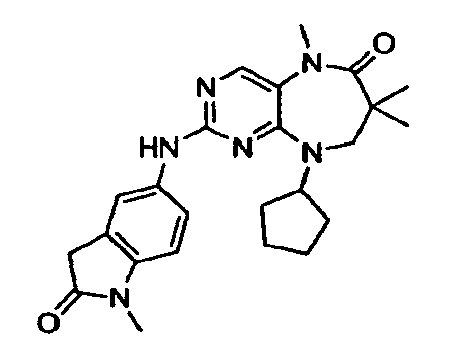
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,54 (4H, ушир.м), 1,62 (2H, ушир.м), 1,82 (2H, ушир.м), 3,12 (3H, с), 3,17 (3H, с), 3,46 (2H, с), 3,55 (2H, с), 5,13 (1H, м), 6,96 (1H, м), 7,39 (1H, м), 7,54 (1H, с), 7,86 (1H, с), 9,89 (1H, с); ВЭЖХ вр. уд. (мин): 9,24; МС (ES+) 435, (ES-) 433.
Пример 126:
6-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-метилпиридин-3-карбоксамид (I-126)
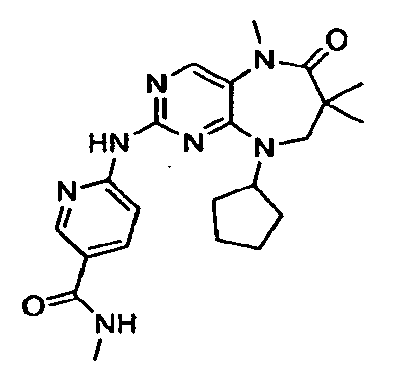
Получают по способу J, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,61 (4H, ушир.м), 1,74 (2H, ушир.м), 1,90 (2H, ушир.м), 2,79 (3H, м), 3,20 (3H, с), 3,38 (2H, с), 5,20 (1H, м), 8,02 (1H, с), 8,15 (1H, м), 8,24 (1H, м), 8,42 (1H, с), 8,70 (1H, с), 9,71 (1H, с); ВЭЖХ вр. уд. (мин): 8,63; МС (ES+) 424, (ES-) 422.
Пример 127:
2-(3-амино-1H-индазол-1-иламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-127)
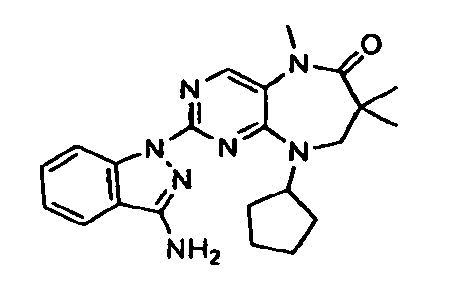
Получают по способу K, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,61-1,84 (6H, м), 1,89-1,96 (2H, м), 3,24 (3H, с), 3,43 (2H, с), 5,39 (1H, дт), 6,04 (2H, с, NH2), 7,18 (1H, т), 7,46 (1H, т), 7,85 (1H, д), 8,14 (1H, с), 8,44 (1H, д); ВЭЖХ вр. уд. (мин): 9,84; МС (ES+) 406.
Пример 128:
2-(3-нитрофениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-128)
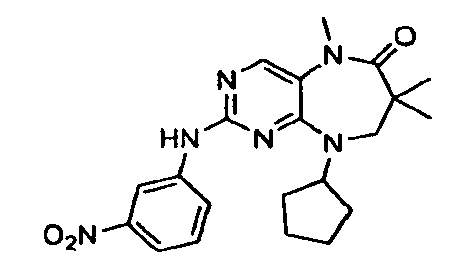
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,52-1,65 (4H, м), 1,69-1,75 (2H, м), 1,84-1,96 (2H, м), 3,20 (3H, с), 3,39 (2H, с), 5,34 (1H, квинт.), 7,52 (1H, т), 7,73 (1H, дд), 7,88 (1H, д), 8,02 (1H, с), 8,92 (1H, д), 9,74 (1H, c); ВЭЖХ вр. уд. (мин): 10,50; МС (ES+) 411, (ES-) 409.
Пример 129:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклопентил-3-метоксибензамид (I-129)
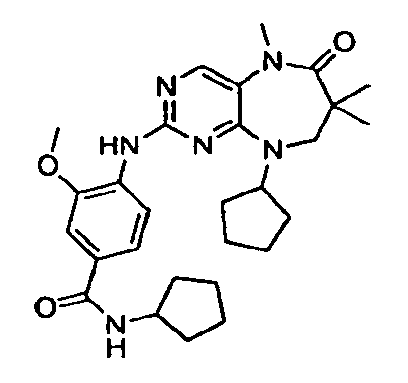
Получают по способу D, используя подходящие реагенты. ЯМР CDCl3 1,13 (6H, м), 1,36-1,78 (12H, м), 1,88-1,98 (2H, м), 2,00-2,10 (2H, м), 3,22 (3H, с), 3,31 (2H, с), 3,91 (3H, с), 4,28-4,37 (1H, м), 5,18-5,30 (1H, м), 5,93 (1H, д), 7,14 (1H, д), 7,35 (1H, с), 7,64 (1H, ушир.с), 7,77 (1H, с), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 10,33; МС (ES+) 507, (ES-) 505.
Пример 130:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-трет-бутил-3-метоксибензамид (I-130)
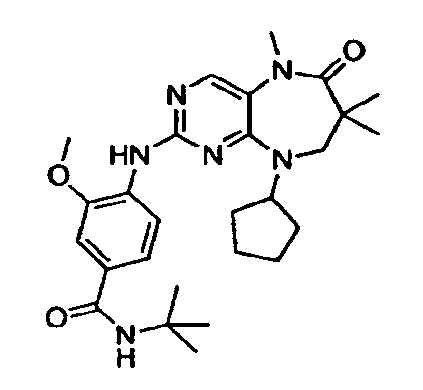
Получают по способу Е, используя подходящие реагенты. ЯМР CDCl3 1,22 (6H, с), 1,51 (9H, с), 1,50-1,87 (6H, м), 1,96-2,06 (2H, м), 3,32 (3H, с), 3,99 (2H, с), 5,26-5,38 (1H, м), 5,95 (1H, с), 7,19 (1H, д), 7,43 (1H, с), 7,22 (1H, ушир.с), 7,86 (1H, с), 8,45 (1H, д); ВЭЖХ вр. уд. (мин): 10,36; MS (ES+) 495, (ES-) 493.
Пример 131:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(циклопропилметил)-3-метоксибензамид (I-131)
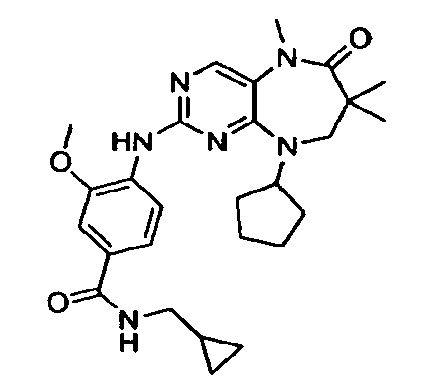
Получают по способу Е, используя подходящие реагенты. ЯМР CDCl3 0,08-0,13 (2H, м), 0,35-0,41 (2H, м), 0,75-0,84 (1H, м), 1,01 (6H, с), 1,27-1,65 (6H, м), 1,76-1,85 (2H, м), 3,08-3,18 (2H, м), 3,11 (3H, с), 3,19 (2H, с), 3,79 (3H, с), 5,08-5,18 (1H, м), 6,00 (1H, т), 7,09 (1H, д), 7,25 (1H, с), 7,57 (1H, ушир.с), 7,64 (1H, с), 8,26 (1H, д); ВЭЖХ вр. уд. (мин): 10,00; МС (ES+) 493, (ES-) 491.
Пример 132:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][l,4]диазепин-2-иламино)-N-(3,3,3-трифторпропил)-3-метоксибензамид (I-132)
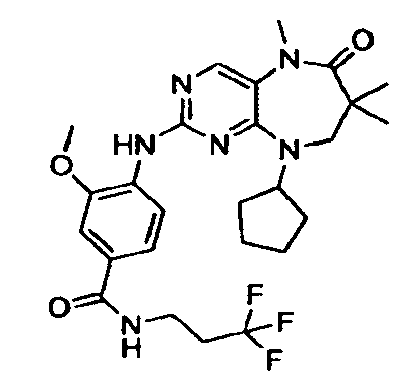
Получают по способу Е, используя подходящие реагенты. ЯМР CDCl3 1,13 (6H, с), 1,45-1,80 (6H, м), 1,88-1,97 (2H, м), 2,35-2,49 (2H, м), 3,22 (3H, с), 3,31 (2H, с), 3,64-3,70 (2H, м), 3,91 (3H, с), 5,18-5,28 (2H, м), 6,28 (1H, т), 7,17 (1H, д), 7,34 (1H, с), 7,68 (1H, ушир.с), 7,77 (1H, с), 8,41 (1H, д); ВЭЖХ вр. уд. (мин): 10,03; МС (ES+) 535, (ES-) 533.
Пример 133:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклогексид-3-метоксибензамид (I-133)
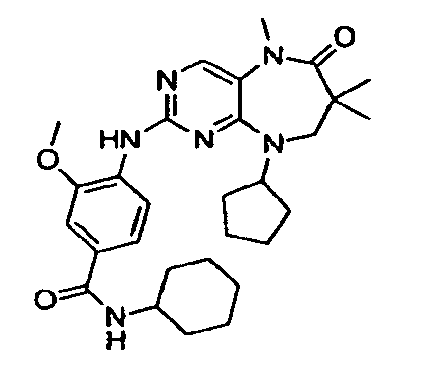
Получают по способу Е, используя подходящие реагенты. ЯМР CDCl3 1,13 (6H, с), 1,10-1,74 (14H, м), 1,88-2,05 (4H, м), 3,22 (3H, с), 3,31 (2H, c), 3,95-4,00 (1H, м), 3,91 (3H, с), 5,18-5,29 (1H, м), 5,85 (1H, д), 7,14 (1H, д), 7,35 (1H, с), 7,68 (1H, ушир.с), 7,76 (1H, с), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 10,56; МС (ES+) 521, (ES-) 519.
Пример 134:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(тетрагидро-2H-пиран-4-ил)-3-метоксибензамид (I-134)
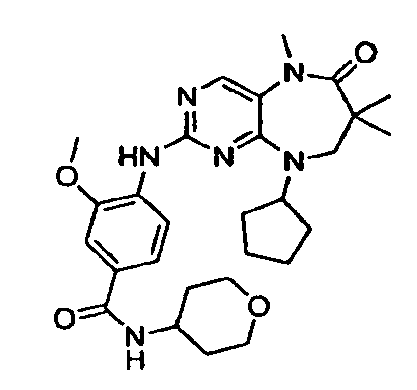
Получают по способу Е, используя подходящие реагенты. ЯМР CDCl3 1,22 (6H, с), 1,48-1,85 (12H, м), 1,97-2,08 (4H, м), 3,32 (3H, с), 3,40 (2H, с), 3,53-3,61 (2H, м), 3,97-4,07 (2H, м), 4,00 (3H, с), 5,29-5,40 (1H, м), 5,97 (1H, д), 7,24 (1H, д), 7,43 (1H, с), 7,77 (1H, ушир.с), 7,86 (1H, с), 8,48 (1H, д); ВЭЖХ вр. уд. (мин): 9,52; МС (ES+) 523, (ES-) 521.
Пример 135:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-этокси-N-(1-изопропилпиперидин-4-ил)бензамид (I-135)
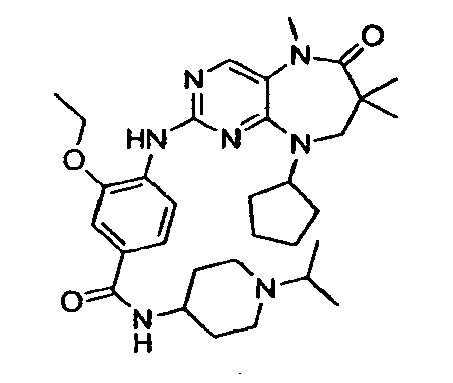
Получают по способу Е, используя подходящие реагенты. ЯМР CDCl3 1,10 (6H, д), 1,22 (6H, с), 1,52 (3H, т), 1,54-1,86 (8H, м), 1,97-2,16 (4H, м), 2,35-2,43 (2H, м), 2,77-2,89 (1H, м), 2,90-3,00 (2H, м), 3,32 (3H, с), 3,40 (2H, с), 3,98-4,07 (1H, м), 4,22 (2H, кв.), 5,25-5,36 (1H, м), 6,00 (1H, д), 7,23 (1H, д), 7,41 (1H, с), 7,66 (1H, с), 7,87 (1H, с), 8,49 (1H, д); ВЭЖХ вр. уд. (мин): 9,47; МС (ES+) 578, (ES-) 576.
Пример 136:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1,3-дигидрокси-2- метилпропан-2-ил)-3-метоксибензамид (I-136)
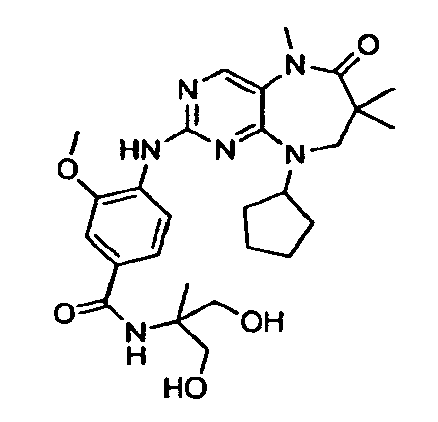
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,05 (3H, с), 1,14 (6H, с), 1,55-1,94 (8H, м), 3,13-3,26 (2H, м), 3,18 (3H, с), 3,28-3,37 (2H, м), 3,49 (2H, с), 3,96 (3H, с), 5,10-5,20 (1H, м), 7,54 (1H, д), 7,60 (1H, с), 8,01 (1H, с), 8,15 (1H, д), 8,40-8,47 (1H, м), 8,85 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,47; МС (ES+) 527, (ES-) 526.
Пример 137:
2-(3-(1H-пиразол-3-ил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][l,4]диазепин-6(7H)-он (I-137)
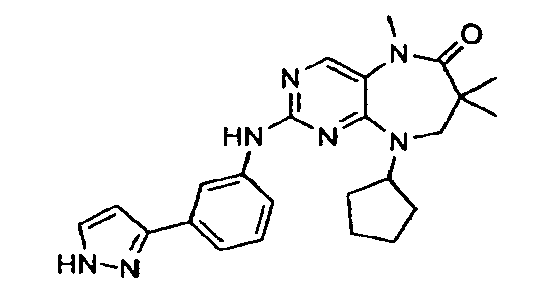
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,24-1,36 (2H, м), 1,50-1,63 (4H, м), 1,71-1,86 (2H, м), 3,19 (3H, с), 3,47 (2H, с), 5,21 (1H, дт), 6,67 (1H, д), 7,38 (2H, д), 7,48-7,56 (1H, м), 7,75 (1H, с), 7,93 (1H, д), 8,12 (1H, с), 10,01 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 9,58; МС (ES+) 432, (ES-) 430.
Пример 138:
9-Циклопентил-2-(l-метансульфонил-2,3-дигидро-1H-индол-5-иламино)-5,7,7-триметил-5,7,8,9-тетрагидро-пиримидо[4,5-b][l,4]диазепин-6-он (I-138)
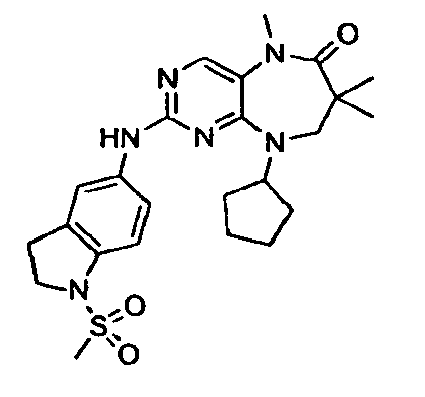
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,13 (6H, с), 1,52-1,85 (8H, м), 2,97 (3H, с), 3,11 (2H, т), 3,17 (3H, с), 3,45 (3H, с), 3,95 (2H, т), 5,14 (1H, дт), 7,20 (1H, д), 7,31 (1H, д), 7,62 (1H, с), 7,88 (1H, с), 9,75 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,42; МС (ES+) 485, (ES-) 484.
Пример 139:
5-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)индолин-2,3-дион (I-139)
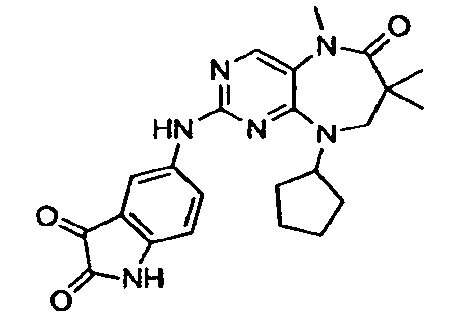
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,56-1,76 (6H, м), 1,81-1,90 (2H, м), 3,18 (3H, с), 3,42 (2H, с), 5,15 (1H, дт), 6,88 (1H, д), 7,63 (1H, д), 7,92 (1H, с), 7,99 (1H, с), 9,63 (1H, ушир.с), 10,96 (1H, с); ВЭЖХ вр. уд. (мин): 8,75; МС (ES+) 435, (ES-) 433.
Пример 140:
3-(9-Циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-5-(трифторметил)-N-метилбензамид (I-140)
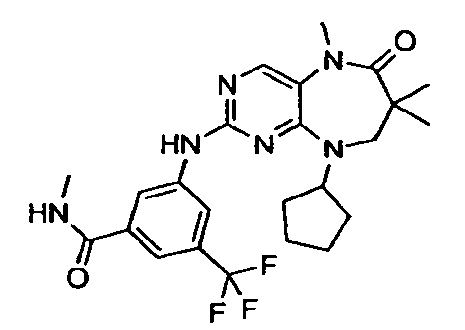
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,48-1,70 (6H, м), 1,80-1,89 (2H, м), 2,78 (3H, д), 3,19 (3H, с), 3,40 (2H, с), 5,25 (1H, дт), 7,70 (1H, с), 7,99 (1H, с), 8,23 (1H, с), 8,34 (1H, с), 8,58-8,65 (1H, м), 9,87 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,99; МС (ES+) 491, (ES-) 490.
Пример 141:
3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(тетрагидро-2H-пиран-4-ил)бензамид (I-141)
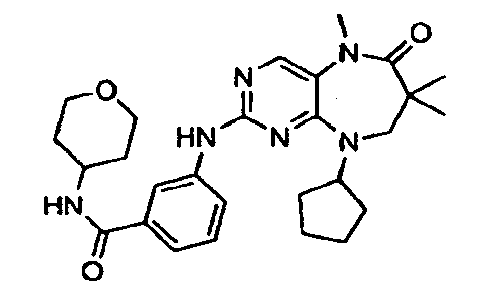
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,53-1,80 (12H, м), 3,18 (3H, с), 3,36-3,43 (5H, м), 3,90 (2H, м), 3,98 (1H, м), 5,18 (1H, м), 7,39 (1H, м), 7,48 (1H, м), 7,63 (1H, м), 7,93 (1H, с), 8,27 (1H, м), 9,75 (1H, с); ВЭЖХ вр. уд. (мин): 9,07; МС (ES+) 493, (ES-) 492.
Пример 142:
4-(9-Циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-метил-3- (трифторметокси)бензамид (I-142)
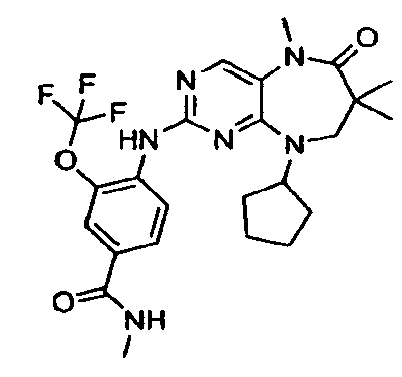
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,55 (4H, ушир.м), 1,69-1,81 (4H, ушир.м), 2,79 (3H, м), 3,18 (3H, с), 3,36 (2H, с), 5,11 (1H, м), 7,83 (2H, м), 7,98 (1H, с), 8,28 (1H, м), 8,50 (1H, с), 8,64 (1H, с); ВЭЖХ вр. уд. (мин): 9,78; МС (ES+) 507, (ES-) 505.
Пример 143:
3-[3-(9-Циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-бензоиламино]азетидин-1-карбоксильная кислота трет-бутиловый эфир (I-143)
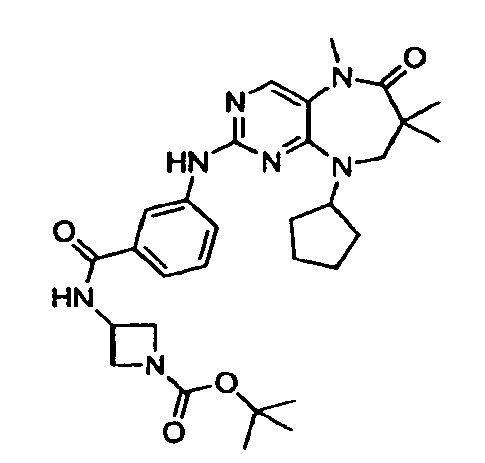
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,39 (9H, с), 1,53 (4H, м), 1,66 (2H, м), 1,83 (2H, м), 3,19 (3H, с), 3,31 (2H, с), 3,85 (2H, м), 4,10 (2H, м), 4,61 (1H, м), 5,25 (1H, м), 7,30-7,37 (2H, м), 7,68 (1H, м), 7,96 (1H, с), 8,27 (1H, с), 8,89 (1H, м), 9,29 (1H, c); ВЭЖХ вр. уд. (мин): 9,98; МС (ES+) 565, (ES-) 563.
Пример 144:
3-(9-Циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][l,4]диазепин-2-иламино)-N-(2-метоксиэтил)бензамид (I-144)
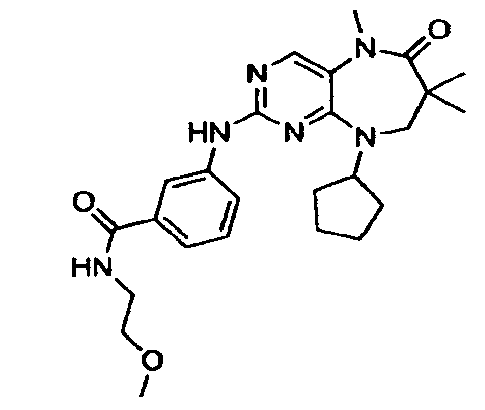
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 1,54 (4H, м), 1,67 (2H, м), 1,82 (2H, м), 3,19 (3H, с), 3,27 (2H, м), 3,85 скрытый сигнал, 4,10 (2H, м), 5,22 (1H, м), 7,35 (1H, м), 7,46 (1H, м), 7,65 (1H, м), 7,93 (1H, с), 8,20 (1H, с), 8,46 (1H, м), 9,68 (1H, с); ВЭЖХ вр. уд. (мин): 9,04; МС (ES+) 467, (ES-) 466.
Пример 145:
N-(3-(9-Циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил-3,3,3-трифторпропанамид (I-145)
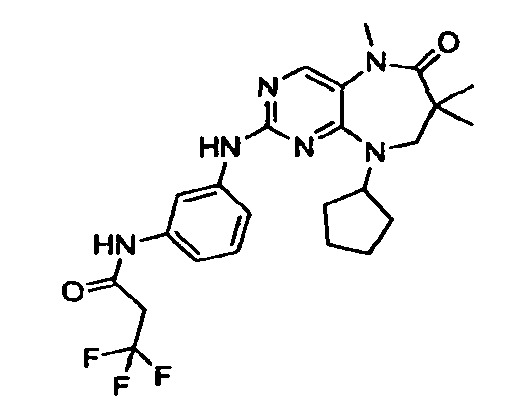
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,50-1,67 (6H, ушир.м), 1,81 (2H, ушир.м), 3,18 (3H, с), 3,44 (2H, с), 3,50 (2H, м), 5,21 (1H, м), 7,14 (1H, м), 7,28 (2H, м), 7,92 (2H, м), 9,87 (NH), 10,34 (1H, с); ВЭЖХ вр. уд. (мин): 9,63; МС (ES+) 491, (ES-) 489.
Пример 146:
N-(3-(9-Циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)-N-метилацетамид (I-146)
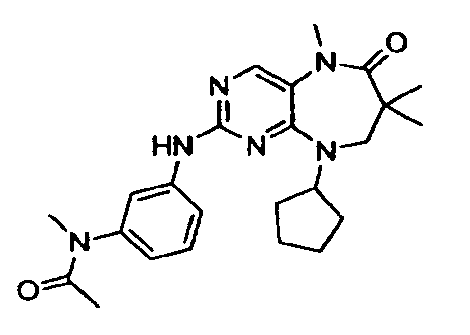
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,52-1,63 (4H, м), 1,67-1,73 (2H, м), 1,78 (3H, с), 1,81-1,88 (2H, м), 3,14 (3H, с), 3,18 (3H, с), 3,36 (2H, с), 5,23 (1H, квинт.), 6,84 (1H, д), 7,29 (1H, т), 7,49 (1H, д), 7,93 (1H, с), 7,98 (1H, с), 9,38 (1H, с); ВЭЖХ вр. уд. (мин): 9,40; МС (ES+) 437, (ES-) 435.
Пример 147:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)-2-метоксиацетамид (I-147)
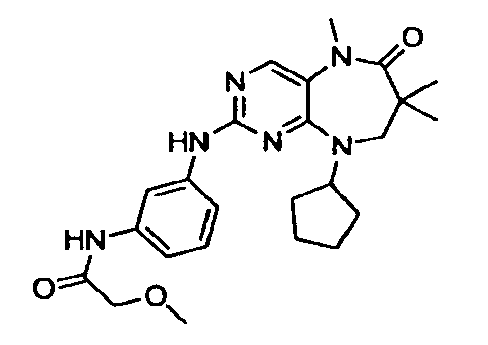
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,51-1,57 (4H, м), 1,65-1,71 (2H, м), 1,81-1,87 (2H, м), 3,18 (3H, с), 3,32 (2H, с), 3,37 (3H, с), 3,97 (2H, с), 5,26 (1H, квинт.), 7,10-7,17 (2H, м), 7,34 (1H, д), 7,94 (1H, с), 8,00 (1H, с), 9,14 (1H, с), 9,59 (1H, с); ВЭЖХ вр. уд. (мин): 9,30; МС (ES+) 453, (ES-) 451.
Пример 148:
3-(9-Циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N,N-диметилбензамид (I-148)
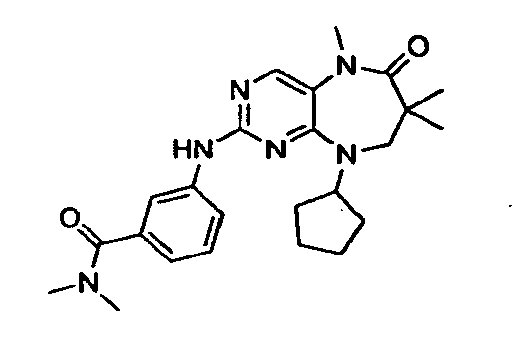
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,56 (4H, м), 1,70 (2H, м), 1,81 (2H, м), 2,91 (3H, с), 2,98 (3H, с), 3,18 (3H, с), 3,42 (2H, с), 5,19 (1H, м), 7,00 (1H, м), 7,34 (1H, м), 7,53 (1H, м), 7,86 (1H, с), 7,95 (1H, с), 9,70 (1H, с); ВЭЖХ вр. уд. (мин): 9,21; МС (ES+) 437, (ES-) 435.
Пример 149:
2-(3-(2-оксопирролидин-1-ил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-149)
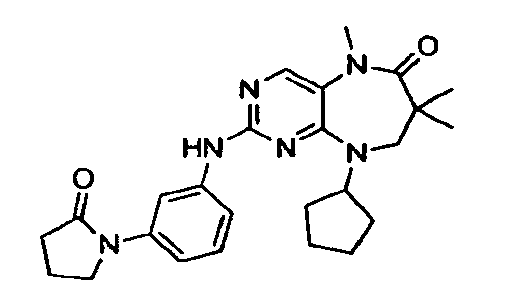
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,60 (4H, м), 1,77 (2H, м), 1,91 (2H, м), 2,12 (2H, м), 2,51 скрытый сигнал, 3,24 (3H, с), 3,37 (2H, с), 3,87 (2H, м), 5,32 (1H, м), 7,19 (1H, м), 7,27 (1H, м), 7,52 (1H, м), 8,01 (1H, с), 8,04 (1H, м), 9,22 (1H, с); ВЭЖХ вр. уд. (мин): 9,52; МС (ES+) 449, (ES-) 447.
Пример 150:
N-[3-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил]-метансульфонамид (I-150)
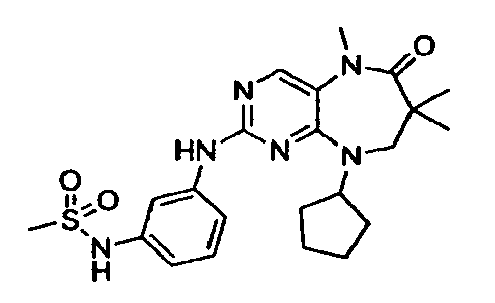
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,55-1,65 (4H, с), 1,68-1,73 (2H, м), 1,80-1,89 (2H, м), 2,94 (3H, с), 3,18 (3H, с), 3,32 (2H, с), 5,25 (1H, квинт.), 6,71 (1H, д), 7,15 (1H, т), 7,47 (1H, д), 7,59 (1H, с), 7,93 (1H, с), 9,16 (1H, с), 9,56 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,10; МС (ES+) 459, (ES-) 457.
Пример 151:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)циклобутанкарбоксамид (I-151)
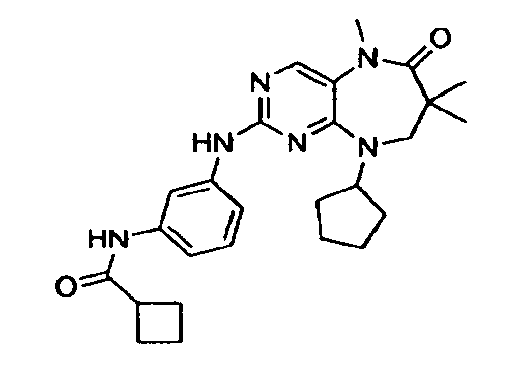
Получают по способу E, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,48-1,59 (4H, м), 1,63-1,73 (2H, м), 1,76-1,89 (3H, м), 1,90-1,98 (1H, м), 2,04-2,14 (2H, м), 2,16-2,27 (2H, м), 3,19 (3H, с), 3,18-3,26 (1H, м), 3,34 (2H, с), 5,27 (1H, квинт.), 7,03-7,12 (2H, м), 7,27 (1H, д), 7,93 (1H, с), 7,99 (1H, с), 9,08 (1H, с), 9,59 (1H, с); ВЭЖХ вр. уд. (мин): 9,80; МС (ES+) 463, (ES-) 461.
Пример 152:
9-Циклопентил-2-[3-(3-циклопропил-3-фтор-азетидин-1-карбонил)фениламино]-5,7,7-триметил-5,7,8,9-тетрагидро-пиримидо[4,5-b][1,4]диазепин-6-он (I-152)
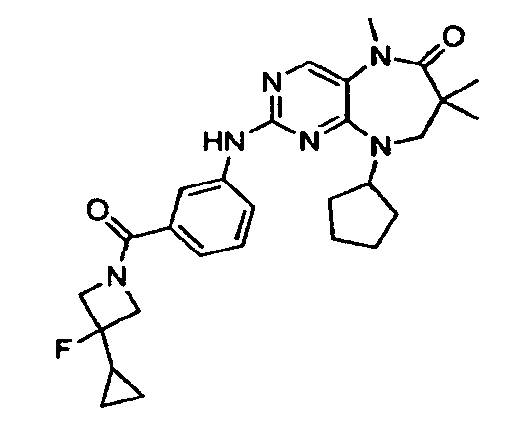
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,20 (2H, м), 0,36 (2H, м), 0,86 (6H, с), 1,16 (1H, м), 1,34 (4H, м), 1,46 (2H, м), 1,63 (2H, м), 2,95 (3H, с), 3,08 скрытый сигнал, 3,79 (2H, м), 3,96-4,08 (2H, м), 5,01 (1H, м), 6,89 (1H, м), 7,07 (1H, м), 7,73 (1H, с), 7,83 (1H, с), 9,09 (1H, c); ВЭЖХ вр. уд. (мин): 10,03; МС (ES+) 507, (ES-) 505.
Пример 153:
2-(3-(пиридин-3-ил)фениламино)-9-циклопентил-8,9-дигидро-5,7,7-триметил-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-153)
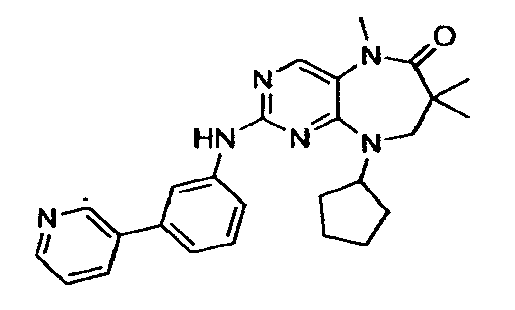
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,06 (6H, с), 1,19-1,28 (2H, м), 1,47-1,58 (4H, м), 1,70-1,83 (2H, м), 3,19 (3H, с), 3,33 (2H, с), 5,16-5,24 (1H, м), 7,20 (1H, д), 7,37 (1H, т), 7,49 (1H, дд), 7,62 (1H, д), 7,98 (1H, с), 8,00-8,02 (1H, м), 8,14-8,15 (1H, м), 8,58 (1H, дд), 8,82 (1H, д), 9,30 (1H, с); ВЭЖХ вр. уд. (мин): 10,10; МС (ES+) 443, (ES-) 441.
Пример 154:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)бензамид (I-154)
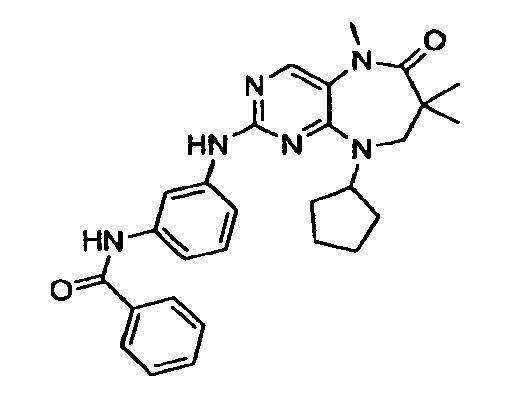
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,08 (6H, с), 1,34-1,42 (2H, м), 1,49-1,56 (4H, м), 1,78-1,86 (2H, м), 3,19 (3H, с), 3,33 (2H, с), 5,28 (1H, квинт.), 7,15-7,22 (2H, м), 7,30-7,32 (1H, м), 7,51-7,61 (3H, м), 7,94-8,00 (3H, м), 8,26 (1H, с), 9,20 (1H, с), 10,17 (1H, с); ВЭЖХ вр. уд. (мин): 9,70; МС (ES+) 485, (ES-) 483.
Пример 155:
Метил 3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-илaмино)фенил)карбамат (I-155)
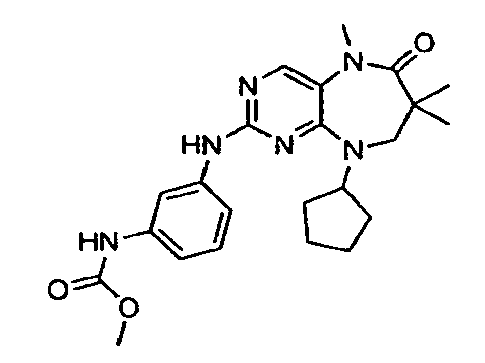
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,08 (6H, с), 1,48-1,57 (4H, м), 1,64-1,73 (2H, м), 1,79-1,88 (2H, м), 3,18 (3H, с), 3,29 (2H, с), 3,64 (3H, с), 5,26 (1H, квинт.), 6,88 (1H, д), 7,11 (1H, т), 7,26 (1H, д), 7,90 (1H, с), 7,93 (1H, с), 9,11 (1H, с), 9,50 (1H, с); ВЭЖХ вр. уд. (мин): 9,40; МС (ES+) 439, (ES-) 437.
Пример 156:
3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(азетидин-3-ил)бензамид (I-156)
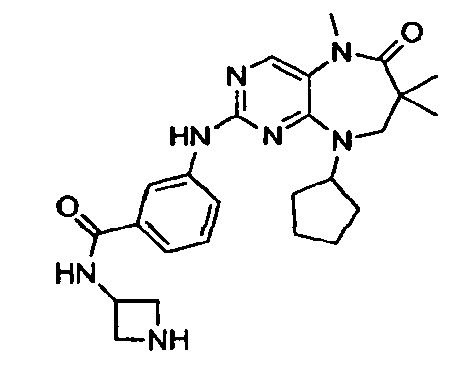
Получают по способу F, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 1,53 (4H, м), 1,67 (2H, м), 1,81 (2H, м), 3,18 (3H, с) 4,07 (4H, м), 4,81 (1H, м), 5,24 (1H, м) 7,41 (2H, м), 7,70 (1H, м), 7,97 (1H, с), 8,24 (1H, м), 8,72 (2H, ушир.c), 9,05 (1H, м), 9,72 (1H, м); ВЭЖХ вр. уд. (мин): 8,38; МС (ES+) 464, (ES-) 463.
Пример 157:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)-1-метилпиперидин-4-карбоксамид (I-157)
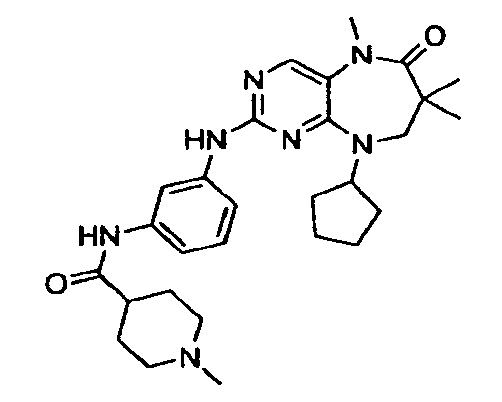
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,35 (2H, ушир.м), 1,50-1,81 (8H, ушир.м), 1,96 (2H, ушир.м), 2,51 (1H, ушир.м), 2,72 (3H, с), 2,91 (2H, м), 3,12 (3H, с), 3,43 (2H, м), 3,44 (2H, с), 5,07 (1H, м), 7,10 (2H, м), 7,31 (1H, м), 7,73 (1H, с), 7,96 (1H, с), 10,20 (1H, с); ВЭЖХ вр. уд. (мин): 8,96; МС (ES+) 506, (ES-) 504.
Пример 158:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-4-метоксифенил)ацетамид (I-158)
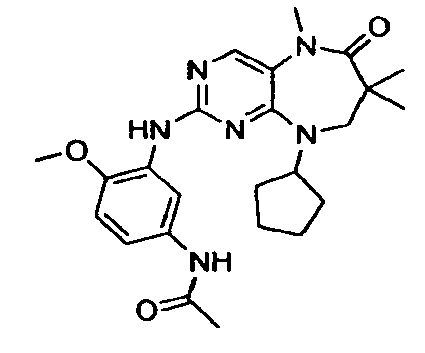
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,45-1,70 (6H, м), 1,76-1,88 (2H, м), 2,00 (3H, с), 3,17 (3H, с), 3,46 (2H, с), 3,83 (3H, с), 5,21 (1H, дт), 7,01-7,11 (2H, м), 7,93-7,96 (1H, м), 8,26-8,34 (1H, м), 9,84 (1H, с); ВЭЖХ вр. уд. (мин): 8,85; МС (ES+) 453, (ES-) 452.
Пример 159:
3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклопропилбензамид (I-159)
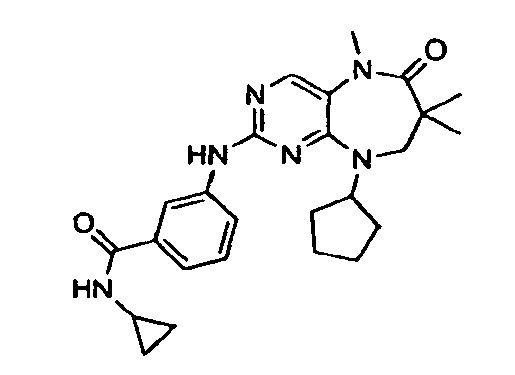
Получают по способу E, используя подходящие реагенты. ЯМР ДМСО D6 0,56 (2H, м), 0,68 (2H, м), 1,12 (6H, с), 1,55 (4H, м), 1,67 (2H, м), 1,91 (2H, м), 2,83 (1H, м), 3,18 (3H, с), 3,43 (2H, с), 5,20 (1H, м), 7,36-7,44 (2H, м), 7,60 (1H, м), 7,93 (1H, с), 8,16 (1H, с), 8,38 (1H, м), 9,70 (1H, с); ВЭЖХ вр. уд. (мин): 9,19; МС (ES+) 449, (ES-) 448.
Пример 160:
4-(9-(2,2,3,3,3-пентафторпропил)-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-160)
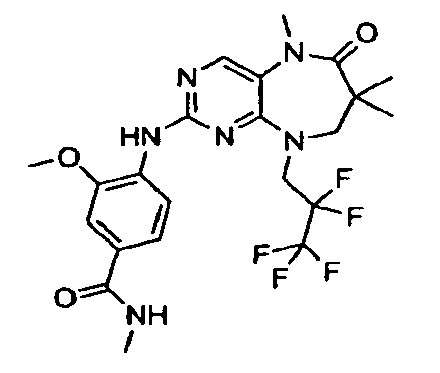
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, с), 2,79 (3H, д), 3,22 (3H, с), 3,66 (2H, с), 3,92 (3H, с), 4,83 (2H, т), 7,42 (1H, дд), 7,50 (1H, д), 7,89 (1H, с), 8,14 (1H, д), 8,15 (1H, с), 8,35 (1H, кв.); ВЭЖХ вр. уд. (мин): 9,00; МС (ES+) 517, (ES-) 515.
Пример 161:
4-(9-(3-хлорфенил)-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-161)
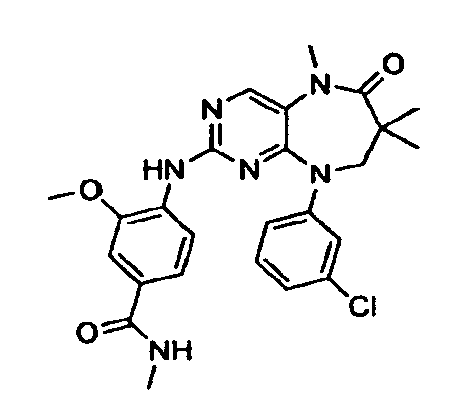
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,23 (6H, с), 2,77 (3H, д), 3,29 (3H, с), 3,82 (2H, с), 3,87 (3H, с), 6,96 (1H, дд), 7,32 (1H, д), 7,34-7,38 (2H, м), 7,49-7,54 (2H, м), 7,57 (1H, д), 7,60 (1H, с), 8,17 (1H, с), 8,23 (1H, кв.); ВЭЖХ вр. уд. (мин): 8,99; МС (ES+) 495, (ES-) 493.
Пример 162:
N-(5-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2-метилфенил)ацетамид (I-162)
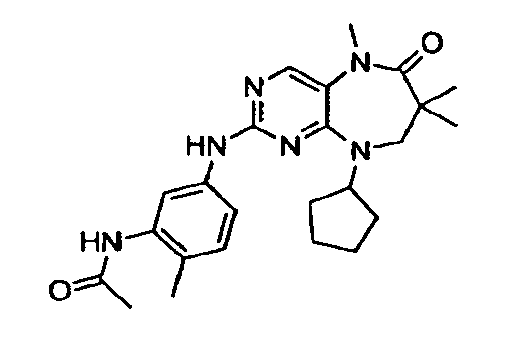
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,08 (6H, с), 1,57 (4H, ушир.м), 1,70 (2H, ушир.м), 1,84 (2H, ушир.м), 2,02 (3H, с), 2,11 (3H, с), 3,17 (3H, с), 3,34 (2H, с), 5,24 (1H, м), 7,02 (1H, м), 7,28 (1H, м), 7,83 (1H, с), 7,92 (1H, с), 9,09 (1H, с), 9,27 (1H, c); ВЭЖХ вр. уд. (мин): 8,91; МС (ES+) 437, (ES-) 435.
Пример 163:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-4-метилфенил)ацетамид (I-163)
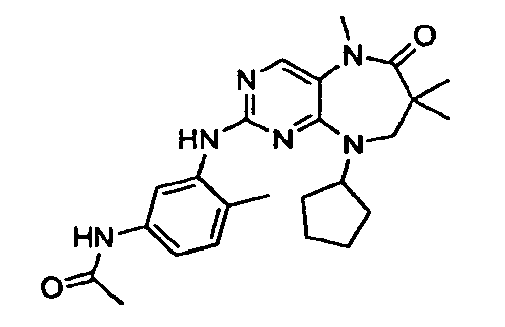
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,07 (6H, с), 1,41 (4H, ушир.м), 1,45-1,70 (4H, ушир.м), 1,99 (3H, с), 2,17 (3H, с), 3,17 (3H, с), 3,30 (2H, с), 5,07 (1H, м), 7,04-7,13 (2H, м), 7,89 (2H, м), 8,21 (1H, s), 9,77 (1H, с); ВЭЖХ вр. уд. (мин): 9,01; МС (ES+) 437, (ES-) 435.
Пример 164:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)фенил)пиперидин-1-карбоксамид (I-164)
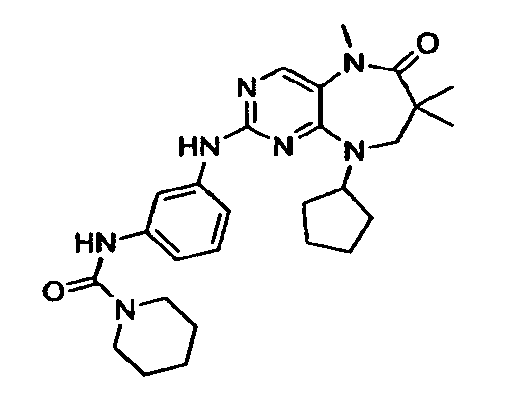
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,46-1,61 (10H, м), 1,64-1,69 (2H, м), 1,81-1,89 (2H, м), 3,18 (3H, с), 3,32 (2H, с), 3,38-3,41 (4H, м), 5,26 (1H, квинт.), 6,89 (1H, д), 7,06 (1H, т), 7,16 (1H, д), 7,88-7,90 (1H, м), 7,92 (1H, с), 8,31 (1H, с), 9,03 (1H, с); ВЭЖХ вр. уд. (мин): 9,70; МС (ES+) 492, (ES-) 490.
Пример 165:
N-(3-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-2,6-дифторфенил)ацетамид (I-165)
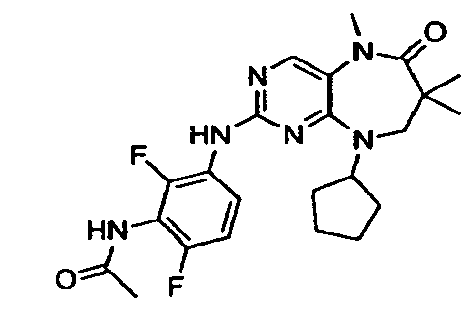
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,17 (6H, с), 1,53 (4H, ушир.м), 1,60-1,76 (4H, ушир.м), 2,13 (3H, с), 3,23 (3H, с), 3,48 (2H, с), 5,03 (1H, м), 7,23 (1H, м), 7,64 (1H, м), 7,95 (1H, с), 9,57 (1H, с), 9,83 (1H, с); ВЭЖХ вр. уд. (мин): 8,90; МС (ES+) 459, (ES-) 457.
Пример 166:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(3,3-дифторциклобутил)-3-метоксибензамид (I-166)
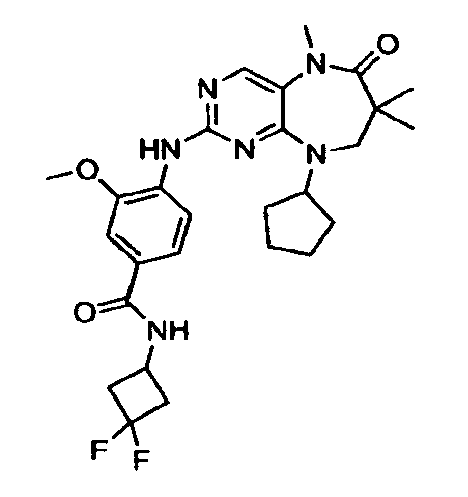
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,53-1,68 (4H, м), 1,69-1,80 (2H, м), 1,82-1,94 (2H, м), 2,69-2,86 (2H, м), 2,90-3,04 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,28 (1H, дт), 5,19 (1H, дт), 7,48 (1H, д), 7,49 (1H, с), 7,72 (1H, с), 8,00 (1H, с), 8,40 (1H, д), 8,66 (1H, д); ВЭЖХ вр. уд. (мин): 10,04; МС (ES+) 529, (ES-) 528.
Пример 167:
4-(9-циклобутил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-167)
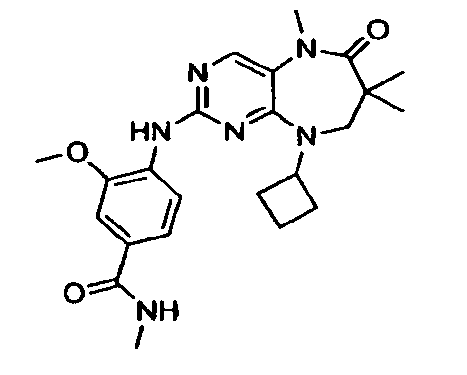
Получают по способу D, используя подходящие реагенты. ЯМР CDCl3 1,22 (6H, с), 1,76-1,85 (2H, м), 2,14 (2H, дквинт.), 2,30-2,33 (2H, м), 3,05 (3H, д), 3,32 (3H, с), 3,51 (2H, с), 4,00 (3H, с), 5,09 (1H, квинт.), 6,14 (1H, кв.), 7,30 (1H, дд), 7,47 (1H, д), 7,64 (1H, с), 7,90 (1H, с), 8,58 (1H, д); ВЭЖХ вр. уд. (мин): 8,98; МС (ES+) 439, (ES-) 437.
Пример 168:
4-(6,7,8,9-тетрагидро-5,7,7-триметил-9-неопентил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-168)
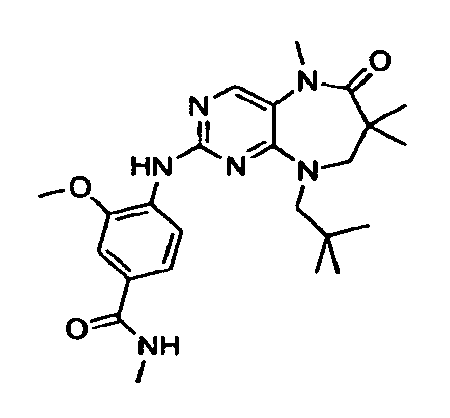
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,96 (9H, с), 1,10 (6H, с), 2,78 (3H, с), 3,21 (3H, с), 3,60 (2H, с), 3,79 (2H, с), 3,93 (3H, с), 7,49 (2H, м), 7,71 (1H, с), 8,00 (1H, с), 8,35 (2H, м); ВЭЖХ вр. уд. (мин): 9,30; МС (ES+) 455, (ES-) 453.
Пример 169:
4-(9-((2,2-дифторциклопропил)метил)-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-169)
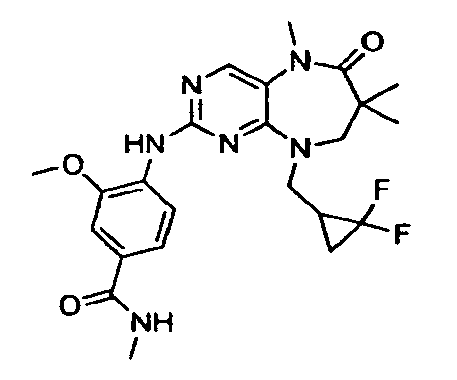
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,11 (6H, д), 1,44 (1H, ушир.м), 1,67 (1H, ушир.м), 2,17 (1H, ушир.м), 2,78 (3H, д), 3,20 (3H, с), 3,46 (2H, ушир.м), 3,63 (1H, д), 3,93 (3H, с), 4,14 (1H, ушир.м), 7,46 (2H, ушир.м), 7,76 (1H, с), 8,04 (1H, с), 8,32 (2H, ушир.д); ВЭЖХ вр. уд. (мин): 8,70; МС (ES+) 475, (ES-) 473.
Пример 170:
4-(9-(3,3-дифторциклобутил)-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-170)
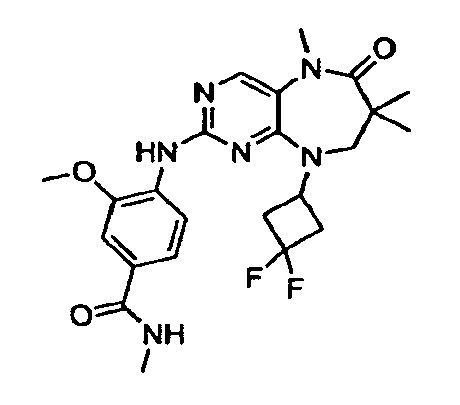
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 2,76-2,95 (4H, м), 2,78 (3H, д), 3,21 (3H, с), 3,48 (2H, с), 3,93 (3H, с), 4,58-4,64 (1H, м), 7,43-7,54 (2H, м), 7,87 (1H, с), 8,09 (1H, с), 8,30-8,38 (2H, м); ВЭЖХ вр. уд. (мин): 8,35; МС (ES+) 475, (ES-) 473.
Пример 171:
4-(9-(3,3-дифторциклобутил)-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(тетрагидро-2H-пиран-4-ил)-3-метоксибензамид (1-171)
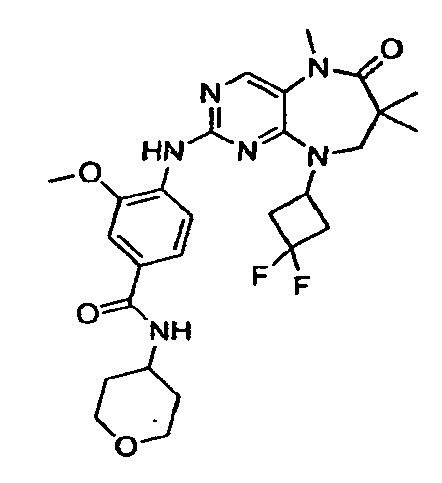
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,54-1,65 (2H, м), 1,75-1,79 (2H, м), 2,78-2,98 (4H, м), 3,21 (3H, с), 3,34-3,43 (2H, м), 3,48 (2H, с), 3,85-3,89 (1H, м), 3,90-3,93 (1H, м), 3,95 (3H, с), 3,98-4,05 (1H, м), 4,56-4,63 (1H, м), 7,48-7,51 (2H, м), 7,88 (1H, с), 8,10 (1H, с), 8,19 (1H, д), 8,33 (1H, д); ВЭЖХ вр. уд. (мин): 8,86; МС (ES+) 545, (ES-) 544.
Пример 172:
4-(9-циклопентил-6,7,8,9-тетрагидро-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((S)-тетрагидрофуран-3-ил)-3-метоксибензамид (I-172)
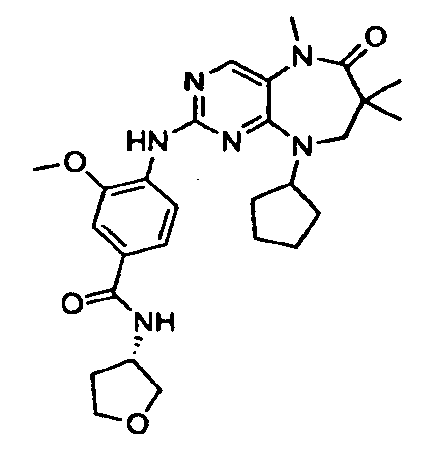
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, м), 1,55-1,68 (4H, м), 1,69-1,77 (2H, м), 1,84-1,95 (4H, м), 2,12-2,21 (1H, м), 3,19 (3H, с), 3,38 (2H, с), 3,59 (1H, дд), 3,68-3,76 (1H, м), 3,83-3,91 (2H, м), 3,95 (3H, с), 4,45-4,49 (1H, м), 5,19 (1H, дт), 7,47-7,52 (2H, м), 7,70 (1H, с), 7,99 (1H, с), 8,35-8,41 (2H, м); ВЭЖХ вр. уд. (мин): 9,37; МС (ES+) 509, (ES-) 507.
Пример 173:
4-((S)-9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклопентил-3-метоксибензамид (I-173)
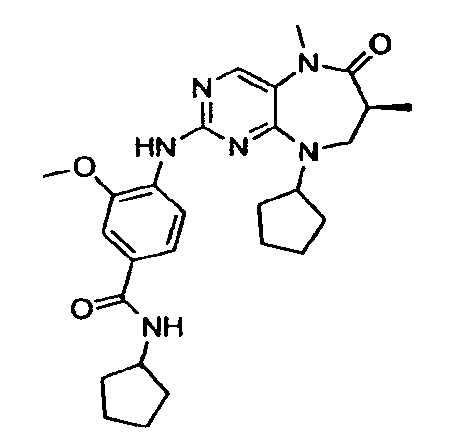
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,02 (3H, д), 1,50-1,83 (14H, м), 1,89-1,94 (2H, м), 2,08-2,11 (1H, м), 2,83-2,88 (1H, м), 3,19 (3H, с), 3,37-3,45 (1H, м), 3,95 (3H, с), 4,20-4,26 (1H, м), 4,71-4,76 (1H, м), 7,47 (1H, д), 7,49 (1H, с), 7,75 (1H, с), 8,10 (1H, с), 8,14 (1H, д), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 10,10; МС (ES+) 493, (ES-) 491.
Пример 174:
4-((S)-9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино-N-(тетрагидро-2H-пиран-4-ил)-3-метоксибензамид (I-174)
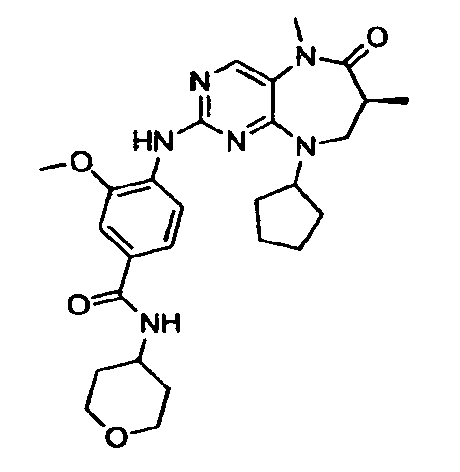
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,02 (3H, с), 1,52-1,78 (HH, м), 2,04-2,12 (1H, м), 2,84-2,90 (1H, м), 3,19 (3H, с), 3,39-3,46 (4H, м), 3,89 (2H, ушир.дд), 3,95 (3H, с), 3,96-4,06 (1H, м), 4,74 (1H, квинт.), 7,49 (1H, д), 7,50 (1H, с), 7,76 (1H, с), 8,10 (1H, с), 8,17 (1H, д), 8,40 (1H, д); ВЭЖХ вр. уд. (мин): 9,20; MS (ES+) 509, (ES-) 507.
Пример 175:
4-((S)-9-циклопентил-6,7,8,9-тетрагидро-5,7-диметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклопропил-3-метоксибензамид (I-175)
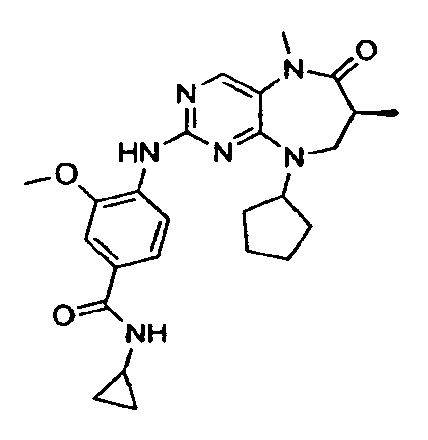
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,55-0,59 (2H, м), 0,68-0,73 (2H, м), 1,02 (3H, д), 1,47-1,85 (7H, м), 2,04-2,12 (1H, м), 2,79-2,88 (2H, м), 3,19 (3H, с), 3,36-3,46 (2H, м), 3,94 (3H, с), 4,69-4,75 (1H, м), 7,45 (1H, д), 7,47 (1H, с), 7,75 (1H, с), 8,10 (1H, с), 8,34 (1H, д), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 9,10; МС (ES+) 465, (ES-) 463.
Пример 176:
N-циклопентил-4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метоксибензамид (I-176)
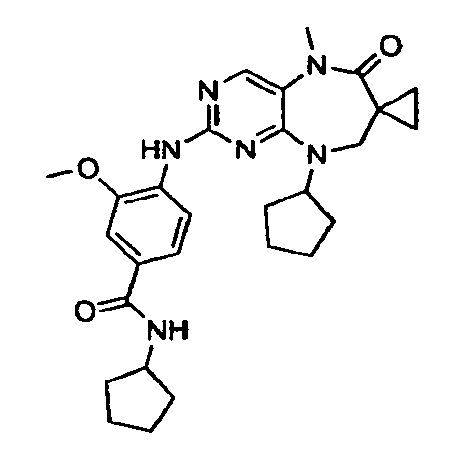
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,66-0,69 (2H, м), 0,89-0,91 (2H, м), 1,46-1,71 (12H, м), 1,85-1,95 (4H, м), 3,17 (3H, с), 3,48 (2H, с), 3,95 (3H, с), 4,23 (1H, квинт.), 4,85 (1H, квинт.), 7,47 (1H, д), 7,49 (1H, с), 7,66 (1H, с), 7,99 (1H, с), 8,13 (1H, д), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 10,00; МС (ES+) 505, (ES-) 503.
Пример 177:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метокси-N-(тетрагидро-2H-пиран-4-ил)бензамид (I-177)
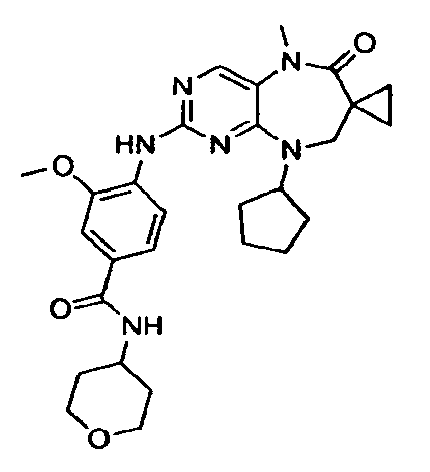
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,67 (2H, ушир.т), 0,90 (2H, ушир.т), 1,51-1,78 (HH, м), 1,75-1,85 (2H, м), 3,17 (3H, с), 3,36-3,42 (2H, м), 3,48 (2H, с), 3,89 (2H, ушир.д), 3,99 (3H, с), 3,99-4,03 (1H, м), 4,85 (1H, квинт.), 7,93 (1H, д), 7,94 (1H, с), 7,70 (1H, с), 7,99 (1H, с), 8,16 (1H, д), 8,40 (1H, д); ВЭЖХ вр. уд. (мин): 9,10; МС (ES+) 521, (ES-) 519.
Пример 178:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-циклопропил-3-метоксибензамид (I-178)
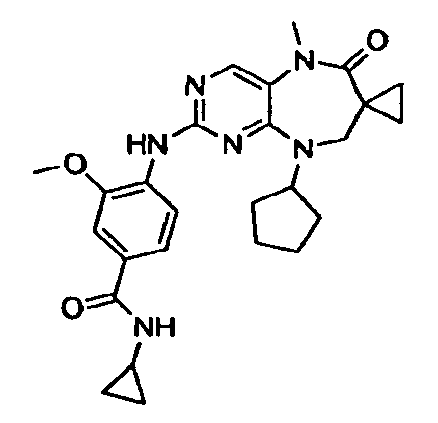
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,56-0,59 (2H, м), 0,66-0,73 (4H, м), 0,84-0,91 (2H, м), 1,50-1,76 (6H, м), 1,85-1,95 (2H, м), 2,79-2,83 (1H, м), 3,10 (3H, с), 3,49 (2H, с), 3,94 (3H, с), 4,85 (1H, квинт.), 7,45 (1H, д), 7,47 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,33 (1H, д), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 9,00; МС (ES+) 477, (ES-) 475.
Пример 179:
(S)-4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метокси-N-(тетрагидрофуран-3-ил)бензамид (I-179)
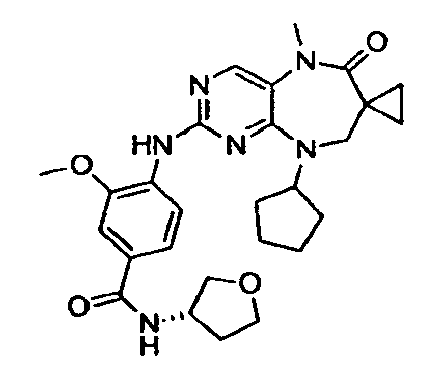
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,67 (2H, ушир.м), 0,90 (2H, ушир.м), 1,50-1,69 (6H, ушир.м), 1,88-1,91 (3H, м), 2,16 (1H, м), 3,17 (3H, с), 3,48 (2H, с), 3,60 (1H, м), 3,61 (1H, м), 3,84 (2H, м), 3,95 (3H, с), 4,46 (1H, м), 4,85 (1H, м), 7,50 (2H, м), 7,70 (1H, с), 7,99 (1H, с), 8,38 (1H, м), 8,41 (1H, с); ВЭЖХ вр. уд. (мин): 7,39; МС (ES+) 507, (ES-) 505.
Пример 180:
4-(6,7,8,9-тетрагидро-9-((S)-тетрагидрофуран-3-ил)-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-180)
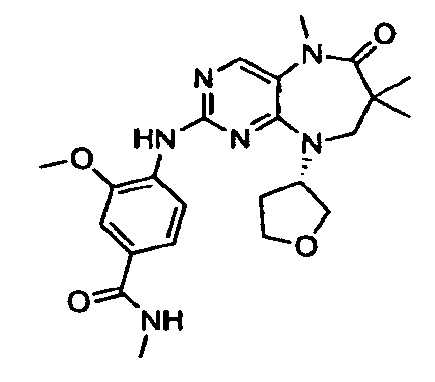
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, д), 1,92 (1H, м), 2,31 (1H, м), 2,78 (3H, д), 3,19 (3H, с), 3,47 (2H, м), 3,63 (1H, кв.), 3,80 (2H, м), 3,93 (3H, с), 3,98 (1H, м), 5,44 (1H, м), 7,48 (2H, м), 7,77 (1H, с), 8,03 (1H, с), 8,35 (2H, м); ВЭЖХ вр. уд. (мин): 7,80; МС (ES+) 455, (ES-) 453.
Пример 181:
4-(6,7,8,9-тетрагидро-9-((R)-тетрагидрофуран-3-ил)-5,7,7-триметил-6-оксо-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-181)
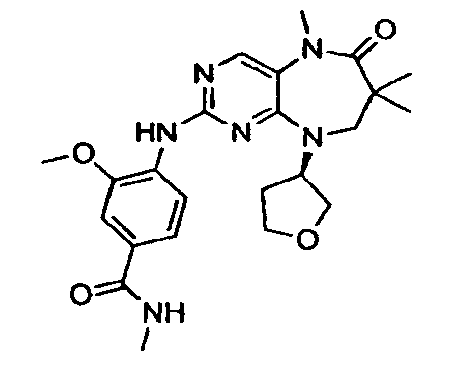
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, д), 1,92 (1H, м), 2,31 (1H, м), 2,78 (3H, д), 3,19 (3H, с), 3,47 (2H, м), 3,63 (1H, кв.), 3,80 (2H, м), 3,93 (3H, с), 3,98 (1H, м), 5,44 (1H, м), 7,48 (2H, м), 7,77 (1H, с), 8,03 (1H, с), 8,35 (2H, м); ВЭЖХ вр. уд. (мин): 7,80; МС (ES+) 455, (ES-) 453.
Пример 182:
(R)-4-(9-циклопентил-5,7-диметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(тетрагидро-2H-пиран-4-ил)бензамид (I-182)
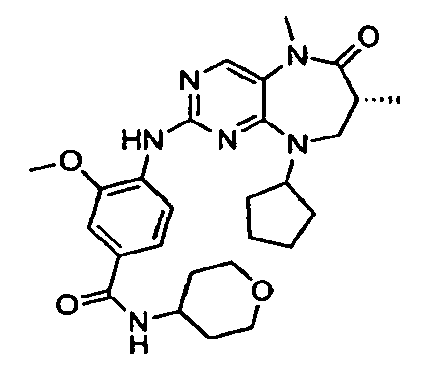
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (3H, д), 1,58-1,91 (11H, м), 2,10-2,20 (1H, м), 2,88-2,96 (1H, м), 3,25 (3H, с), 3,36-3,54 (4H, м), 3,90-3,97 (2H, м), 4,02 (3H, с), 4,03-4,12 (1H, м), 4,75-4,85 (1H, м), 7,54-7,57 (2H, м), 7,83 (1H, с), 8,17 (1H, с), 8,24 (1H, д), 8,46 (1H, д); ВЭЖХ вр. уд. (мин): 9,24.
Пример 183:
4-((R)-9-циклопентил-5,7-диметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((S)-тетрагидрофуран-3-ил)бензамид (I-183)
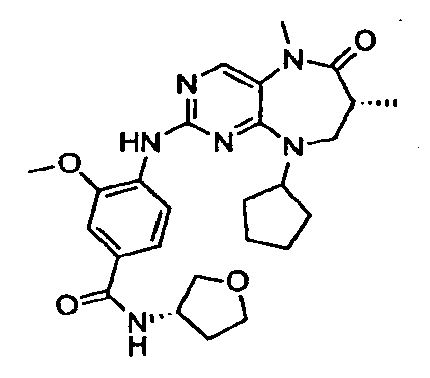
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (3H, д), 1,48-1,63 (3H, м), 1,65-1,85 (4H, м), 1,85-2,02 2,10-2,23 (1H, м), 2,30 (3H, с), 2,95-3,05 (1H, м), 3,19 (3H, с), 3,35-3,42 (1H, м), 3,54-3,65 (2H, м), 3,66-3,75 (1H, м), 3,80-3,90 (2H, м), 3,97 (3H, с), 4,42-4,52 (1H, м), 4,76-4,87 (1H, м), 7,52-7,62 (2H, м), 8,04-8,15 (2H, м), 8,52 (1H, д), 9,27 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 9,11.
Пример 184:
(R)-4-(9-циклопентил-5,7-диметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-циклопропил-3-метоксибензамид (I-184)
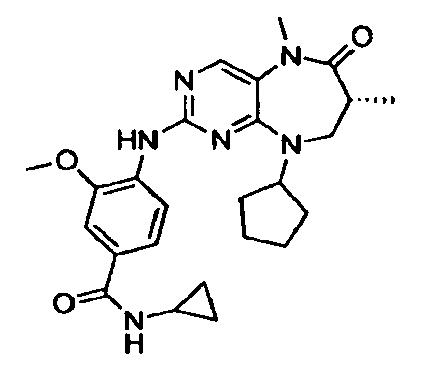
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,55-0,59 (2H, м), 0,67-0,73 (2H, м), 1,02 (3H, д), 1,52-1,83 (7H, м), 2,05-2,10 (1H, м), 2,79-2,88 (2H, м), 3,19 (3H, с), 3,59-3,45 (2H, м), 3,94 (3H, с), 4,73 (1H, квинт.), 7,45 (1H, д), 7,47 (1H, с), 7,78 (1H, с), 8,09 (1H, с), 8,33 (1H, д), 8,83 (1H, д); ВЭЖХ вр. уд. (мин): 9,40; MS (ES+) 465, (ES-) 463.
Пример 185:
(R)-N-циклопентил-4-(9-циклопентил-5,7-диметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,-b][1,4]диазепин-2-иламино)-3-метоксибензамид (I-185)
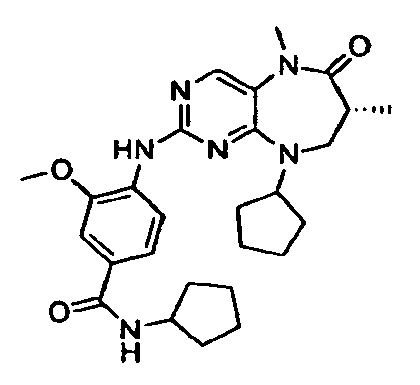
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,02 (3H, д), 1,50-1,61 (6H, м), 1,63-1,83 (8H, м), 1,86-1,96 (2H, м), 2,04-2,11 (1H, м), 2,83-2,88 (1H, м), 3,19 (3H, с), 3,36-3,46 (1H, м), 3,95 (3H, с), 4,18-4,28 (1H, м), 4,74 (1H, квинт.), 7,47 (1H, д), 7,48 (1H, с), 7,75 (1H, с), 8,10 (1H, с), 8,15 (1H, с), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 10,10; МС (ES+) 493, (ES-) 491.
Пример 186:
(R)-N-циклобутил-4-(9-циклопентил-5,7-диметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид (I-186)
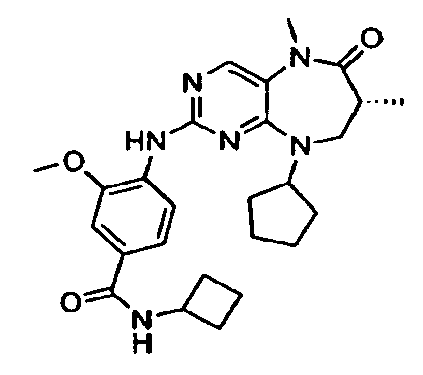
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,02 (3H, д), 1,50-1,83 (9H, м), 2,03-2,12 (3H, м), 2,19-2,23 (2H, м), 2,81-2,90 (1H, м), 3,19 (3H, с), 3,30-3,33 (1H, м), 3,43 (1H, т), 3,65 (3H, с), 4,43 (1H, кв.), 4,73 (1H, квинт.), 7,48 (1H, дд), 7,49 (1H, с), 7,76 (1H, с), 8,10 (1H, с), 8,39 (1H, д), 8,47 (1H, д); ВЭЖХ вр. уд. (мин): 9,90; МС (ES+) 479.
Пример 187:
(R)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(тетрагидрофуран-3-ил)бензамид (I-187)
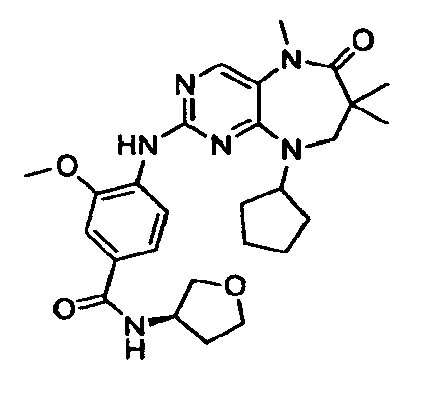
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,62 (4H, ушир.м), 1,74 (2H, ушир.м), 1,89 (3H, ушир.м), 2,16 (1H, ушир.м), 3,19 (3H, с), 3,38 (2H, с), 3,60 (1H, м), 3,71 (1H, м), 3,86 (2H, м), 3,95 (3H, с), 4,45 (1H, м), 5,20 (1H, м), 7,51 (2H, м), 7,70 (1H, с), 7,99 (1H, с), 8,39 (2H, м); ВЭЖХ вр. уд. (мин): 9,40; МС (ES+) 509.
Пример 188:
9-циклопентил-2-(2-метоксифениламино)-5-метил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-188)
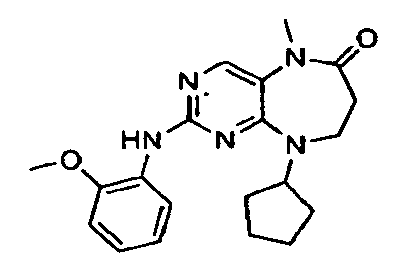
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,52-1,75 (6H, м), 1,85-1,95 (2H, м), 2,52-2,58 (2H, м), 3,16 (3H, с), 3,58-3,62 (2H, м), 3,86 (3H, с), 4,75 (1H, квинт.), 6,93 (2H, дт) 7,02 (1H, дд), 7,61 (1H, с), 8,04 (1H, с), 8,21 (1H, дд); ВЭЖХ вр. уд. (мин): 10,07; МС (ES+) 368.
Пример 189:
2-(2-метоксифениламино)-5,9-диметил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-189)
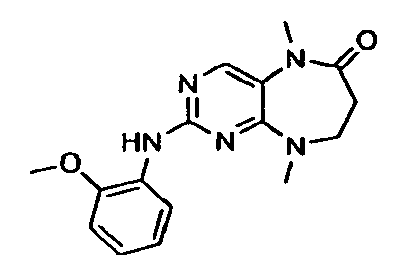
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 2,58-2,61 (2H, м), 3,03 (3H, с), 3,17 (3H, с), 3,65-3,69 (2H, м), 3,87 (3H, с), 6,90-6,97 (2H, м), 7,01-7,03 (1H, м), 7,62 (1H, с), 8,07 (1H, с), 8,30-8,33 (1H, м); ВЭЖХ вр. уд. (мин): 8,61; МС (ES+) 314.
Пример 190:
4-(9-циклопентил-7-этил-5-метил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-190)
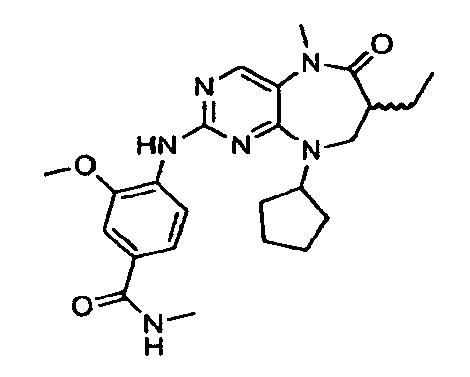
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,87 (3H, т), 1,09 (1H, т), 1,28 (1H, м), 1,69 (8H, ушир.м), 2,07 (1H, ушир.м), 2,60 (1H, м), 2,78 (3H, д), 3,19 (3H, с), 3,40 (2H, м), 3,94 (3H, с), 4,77 (1H, ушир.м), 7,48 (2H, м), 7,76 (1H, с), 8,11 (1H, с), 8,33 (1H, ушир.д), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 9,40; МС (ES+) 453.
Пример 191:
4-(9-(бицикло[2.2.1]гептан-2-ил)-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-метилбензамид (I-191)
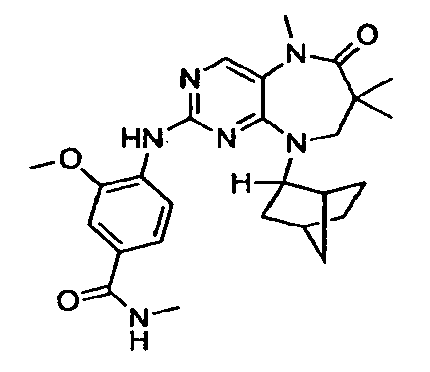
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 0,95-1,08 (2H, м), 1,06 (3H, с), 1,08 (3H, с), 1,16-1,58 (6H, м), 1,95-2,06 (1H, м), 2,18-2,23 (1H, м), 2,58-2,65 (1H, м), 2,79 (3H, д), 3,22 (3H, с), 3,30 (1H, д), 3,52 (1H, д), 3,94 (3H, с), 4,24-4,31 (1H, м), 7,44-7,51 (2H, м), 7,77 (1H, с), 8,12 (1H, с), 8,30-8,36 (1H, м), 8,39 (1H, д); ВЭЖХ вр. уд. (мин): 9,78; МС (ES+) 479.
Пример 192:
3-метокси-N-метил-4-(5,7,7-триметил-9-(морфолин-2-илметил)-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)бензамид (I-192)
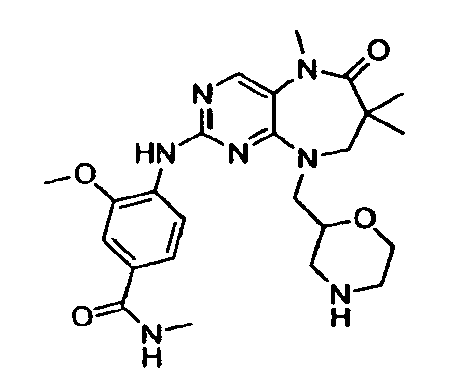
Получают по способу O, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 2,40-2,48 (1H, м), 2,60-2,69 (2H, м), 2,78 (3H, д), 2,78-2,85 (1H, м), 3,19 (3H, с), 3,34 (2H, с), 3,34-3,44 (1H, м), 3,52-3,60 (2H, м), 3,68-3,78 (2H, м), 3,85-3,95 (1H, м), 3,93 (3H, с), 7,45 (1H, д), 7,48 (1H, д), 7,69 (1H, с), 7,99 (1H, с), 8,30-8,35 (1H, м), 8,31 (1H, д); ВЭЖХ вр. уд. (мин): 6,88; МС (ES+) 484.
Пример 193:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(фуран-2-илметил)-3-метоксибензамид (I-193)
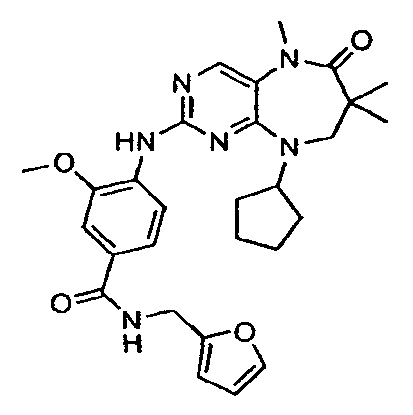
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,90; МС (ES+) 519.
Пример 194:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((тетрагидрофуран-2-ил)метил)бензамид (I-194)
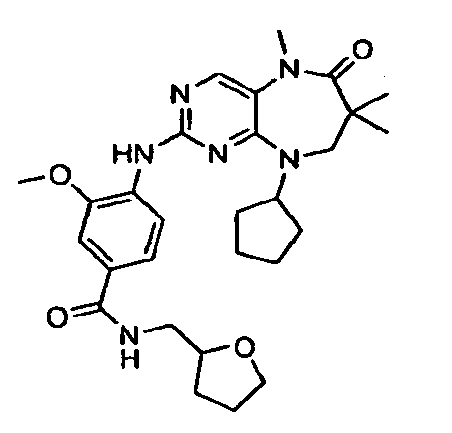
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,70; МС (ES+) 523.
Пример 195:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((тетрагидрофуран-2H-пиран-4-ил)метил)бензамид (I-195)
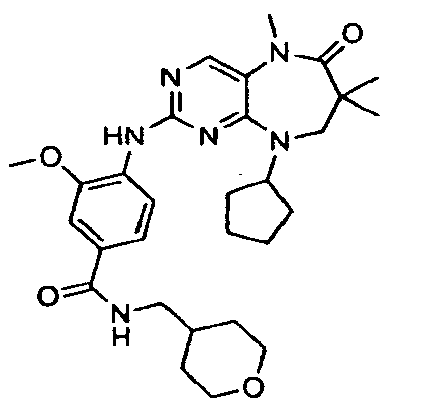
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,60; МС (ES+) 537.
Пример 196:
N-(циклогексилметил)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид (I-196)
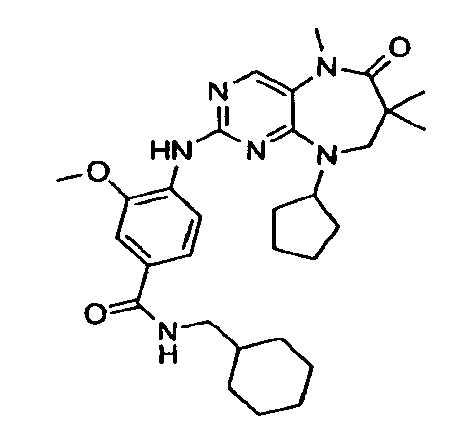
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,90-0,96 (2H, м), 1,10 (6H, с), 1,15-1,14 (3H, м), 1,54-1,73 (12H, м), 1,84-1,91 (2H, м), 3,11 (2H, т), 3,19 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 5,18 (1H, квинт.), 7,47 (1H, д), 7,50 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,32-8,37 (2H, м); ВЭЖХ вр. уд. (мин): 10,90; МС (ES+) 535.
Пример 197:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(2-метоксиэтил)бензамид (I-197)
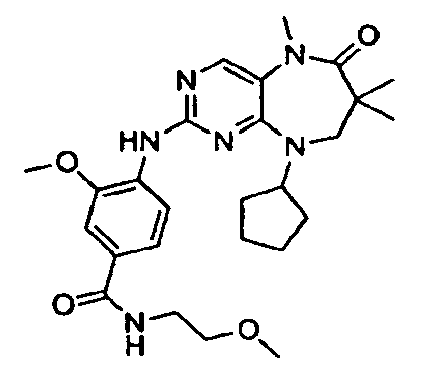
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,40; МС (ES+) 497.
Пример 198:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(3-метоксипропил)бензамид (I-198)
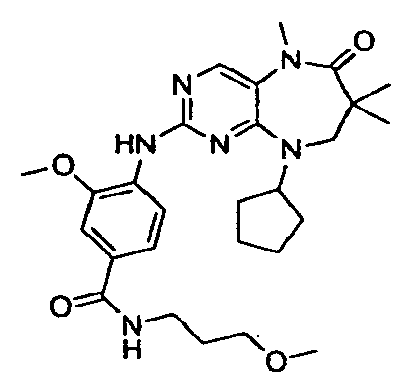
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,60; МС (ES+) 511.
Пример 199:
9-циклопентил-2-(2-метокси-4-(морфолин-4-карбонил)фениламино)-5,7,7-триметил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-199)
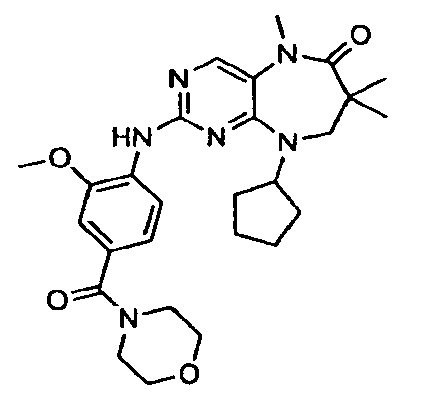
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,50; МС (ES+) 509.
Пример 200:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-фенилбензамид (I-200)
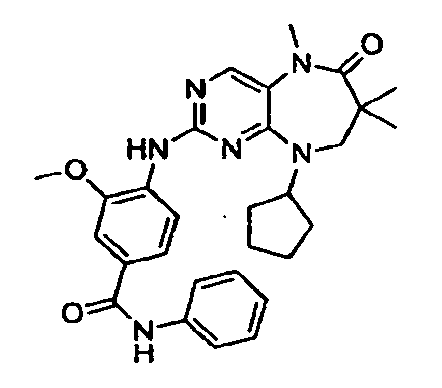
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 10,30; МС (ES+) 515.
Пример 201:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((тетрагидрофуран-2-ил)метил)бензамид (I-201)
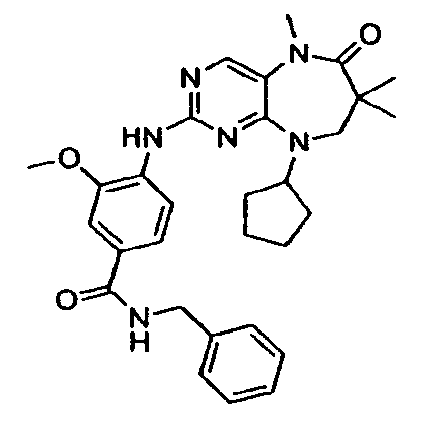
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 10,20; МС (ES+) 529.
Пример 202:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиридин-3-илметил)бензамид (I-202)
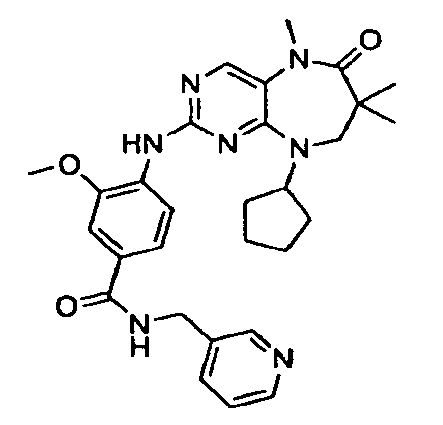
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,50; МС (ES+) 530.
Пример 203:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-фенетилбензамид (I-203)
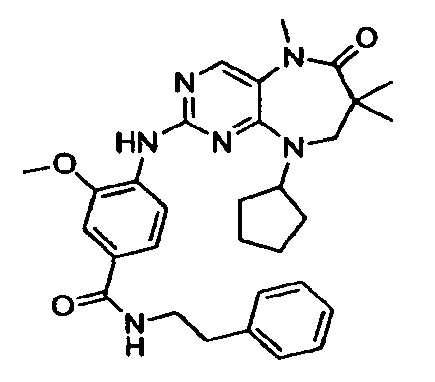
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,58-1,66 (4H, м), 1,70-1,78 (2H, м), 1,84-1,92 (2H, м), 2,85 (2H, т), 3,19 (3H, с), 3,38 (2H, с), 3,48 (2H, кв.), 3,94 (3H, с), 5,18 (1H, квинт.), 7,19-7,33 (5H, м), 7,45 (1H, д), 7,49 (1H, с), 7,70 (1H, с), 7,99 (1H, с), 8,37 (1H, д), 8,47 (1H, ушир.т); ВЭЖХ вр. уд. (мин): 10,40; МС (ES+) 543.
Пример 204:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((1R,4R)-4-гидроксоциклогексил)-3-метоксибензамид (I-204)
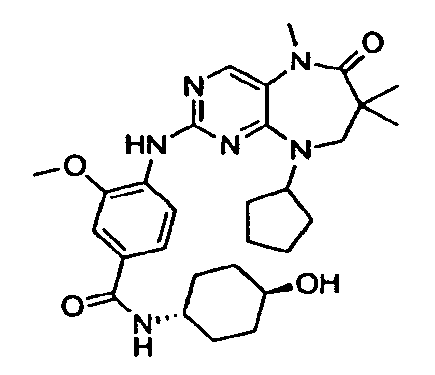
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,19-1,43 (4H, м), 1,55-1,93 (12H, м), 3,19 (3H, с), 3,34-3,45 (1H, м), 3,38 (2H, с), 3,68-3,79 (1H, м), 3,94 (3H, с), 4,57 (1H, д), 5,19 (1H, дт), 7,46 (1H, д), 7,47 (1H, с), 7,68 (1H, с), 7,99 (1H, с), 8,02 (1H, с), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 9,21; МС (ES+) 537.
Пример 205:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((1-гидроксициклогексил)метил)-3-метоксибензамид (I-205)
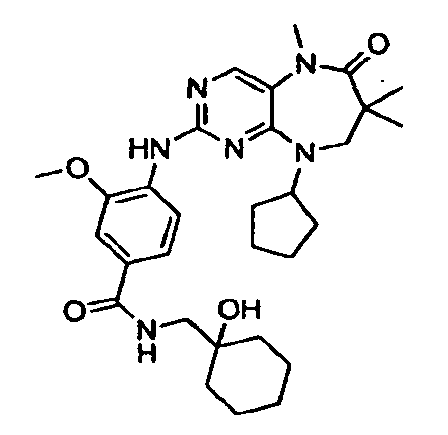
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,16-1,26 (1H, м), 1,29-1,80 (15H, м), 1,82-1,92 (2H, м), 3,19 (3H, с)7 3,28 (2H, д), 3,38 (2H, с), 3,95 (3H, с), 4,43 (1H, с), 5,19 (1H, дт), 7,51 (1H, д), 7,53 (1H, с), 7,70 (1H, с), 7,99 (1H, с), 8,16 (1H, т), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 10,06; МС (ES+) 551.
Пример 206:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пирролидин-1-ил)бензамид (I-206)
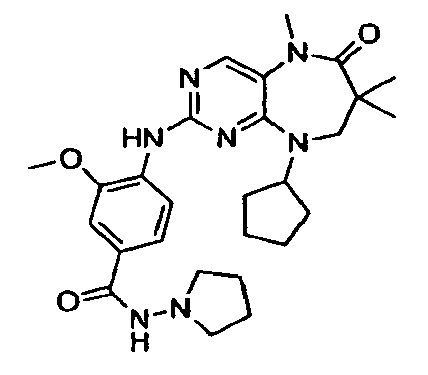
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,57-1,92 (12H, м), 2,90-2,99 (4H, м), 3,19 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 5,18 (1H, дт), 7,41 (1H, д), 7,43 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,37 (1H, д), 9,27 (1H, с); ВЭЖХ вр. уд. (мин): 9,57; МС (ES+) 508.
Пример 207:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиридин-3-ил)бензамид (I-207)
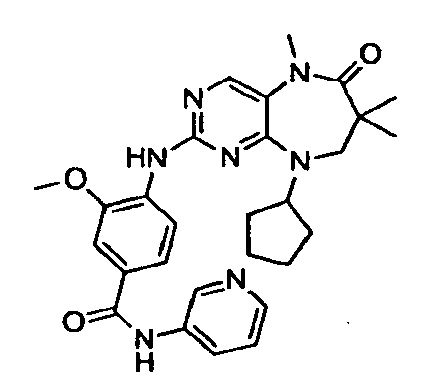
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,85; МС (ES+) 516.
Пример 208:
9-циклопентил-2-(4-(3-циклопропил-3-фторазетидин-1-карбонил)-2-метоксифениламино)-5,7,7-триметил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7)-он (I-208)
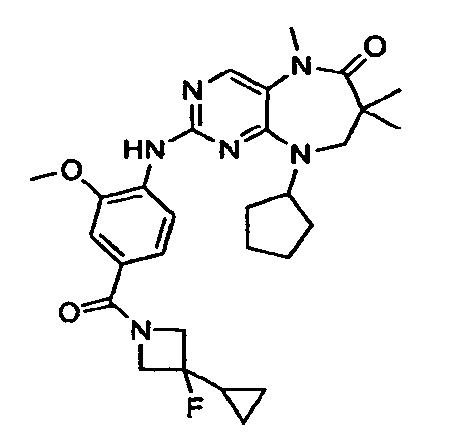
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,44 (2H, ушир.с), 0,61 (2H, д), 1,09 (6H, с), 1,35-1,45 (1H, м), 1,53-1,80 (6H, м), 1,82-1,92 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 3,96-4,13 (2H, м), 4,20-4,51 (2H, м), 5,19 (1H, дт), 7,24 (1H, с), 7,25 (1H, д), 7,73 (1H, с), 7,99 (1H, с), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 10,37; МС (ES+) 537.
Пример 209:
(R)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2,3-дигидро-1H-инден-1-ил)-3-метоксибензамид (I-209)
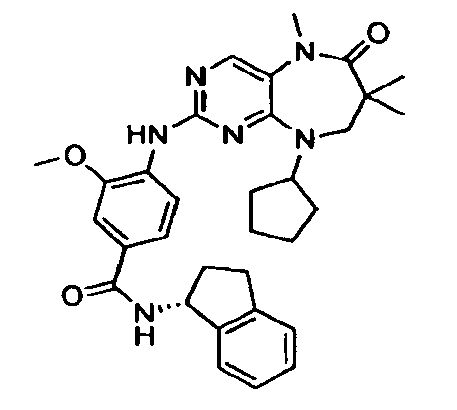
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, м), 1,55-1,79 (6H, м), 1,82-1,95 (2H, м), 1,96-2,06 (1H, м), 2,43-2,51 (1H, м), 2,82-2,93 (1H, м), 2,96-3,07 (1H, м), 3,19 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 5,19 (1H, дт), 5,61 (1H, кв.), 7,18-7,31 (4H, м), 7,55-7,60 (2H, м), 7,71 (1H, с), 8,00 (1H, с), 8,39 (1H, д), 8,67 (1H, д); ВЭЖХ вр. уд. (мин): 10,60; МС (ES+) 555.
Пример 210:
N-(бицикло[2.2.1]гептан-2-ил)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид (I-210)
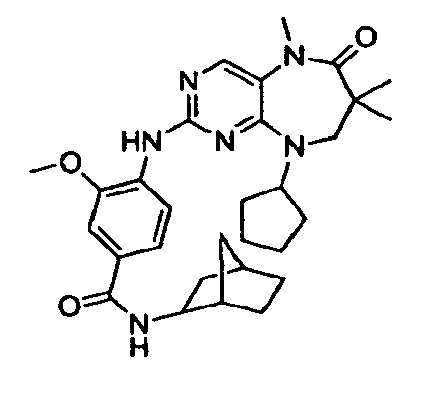
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,12-1,23 (3H, м), 1,48-1,75 (HH, м), 1,84-1,92 (2H, м), 2,18-2,28 (2H, м), 3,18 (3H, с), 3,37 (2H, с), 3,67-3,75 (1H, м), 3,94 (3H, с), 5,18 (1H, квинт.), 7,46 (1H, д), 7,47 (1H, с), 7,68 (1H, с), 7,91 (1H, д), 7,98 (1H, с), 8,34 (1H, д); ВЭЖХ вр. уд. (мин): 10,70; МС (ES+) 533.
Пример 211:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(3-гидрокси-2,2-диметилпропил)-3-метоксибензамид (I-211)
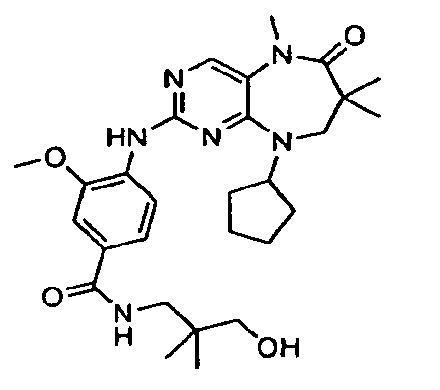
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,84 (6H, с), 1,09 (6H, с), 1,55-1,65 (4H, м), 1,70-1,77 (2H, м), 1,84-1,92 (2H, м), 3,10 (2H, д), 3,15 (2H, д), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,69 (1H, т), 5,18 (1H, квинт.), 7,48 (1H, д), 7,50 (1H, с), 7,71 (1H, с), 7,99 (1H, с), 8,33-8,39 (2H, м); ВЭЖХ вр. уд. (мин): 9,80; МС (ES+) 525.
Пример 212:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиридин-4-илметил)бензамид (I-212)
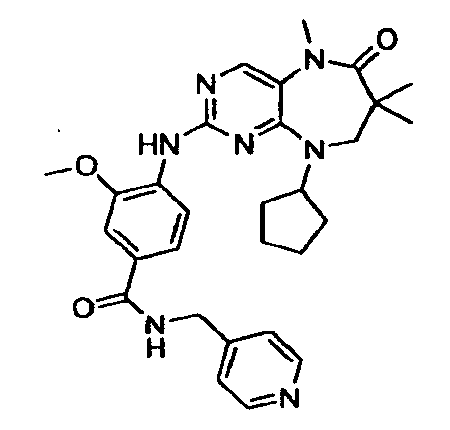
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,56-1,67 (4H, м), 1,69-1,75 (2H, м), 1,84-1,93 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,51 (2H, д), 5,19 (1H, квинт.), 7,31 (2H, д), 7,55 (1H, д), 7,56 (1H, с), 7,73 (1H, с), 8,00 (1H, с), 8,41 (1H, д), 8,51 (2H, д), 9,02 (1H, т); ВЭЖХ вр. уд. (мин): 9,40; MS (ES+) 530.
Пример 213:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(4-метоксибензил)бензамид (1-213)
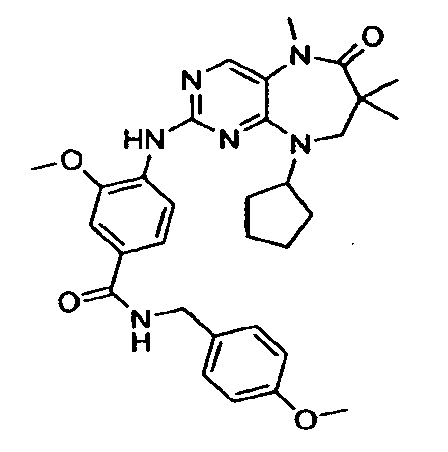
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 10,20; МС (ES+) 559.
Пример 214:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(4-(метилсульфонил)бензил)бензамид (I-214)
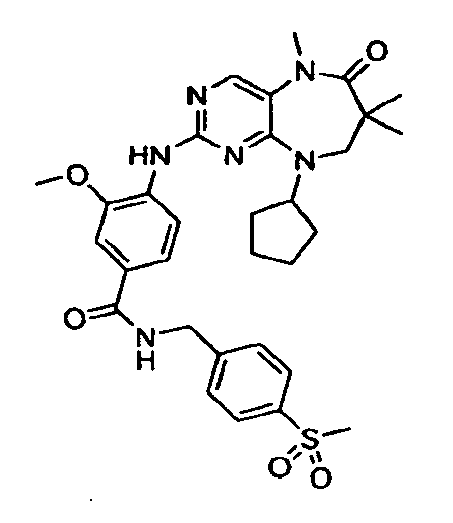
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,40; МС (ES+) 607.
Пример 215:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N,N-диметилбензамид (I-215)
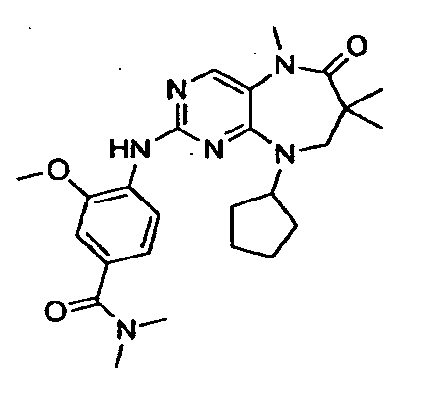
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,70; МС (ES+) 467.
Пример 216:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(((1S,2S)-2-гидроксициклогексил)метил)-3-метоксибензамид (I-216)
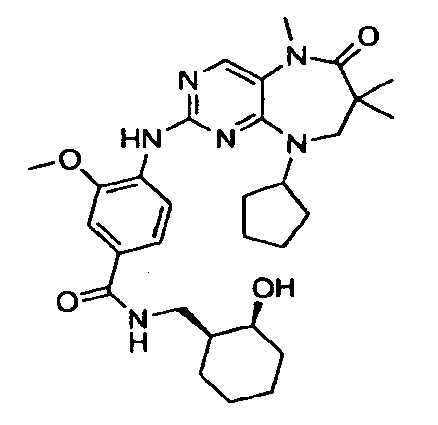
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,14-1,25 (1H, м), 1,28-1,40 (4H, м), 1,51-1,67 (10H, м), 1,84-1,92 (2H, м), 3,09-3,19 (1H, м), 3,19 (3H, с), 3,24-3,31 (1H, м), 3,38 (2H, с), 3,73 (1H, ушир.с), 3,94 (3H, с), 4,42 (1H, д), 5,18 (1H, квинт.), 7,47 (1H, д), 7,50 (1H, с), 7,70 (1H, с), 7,99 (1H, с), 8,36-8,38 (2H, м); ВЭЖХ вр. уд. (мин): 10,20; МС (ES+) 551.
Пример 217:
(S)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-метоксипропан-2-ил)бензамид (I-217)
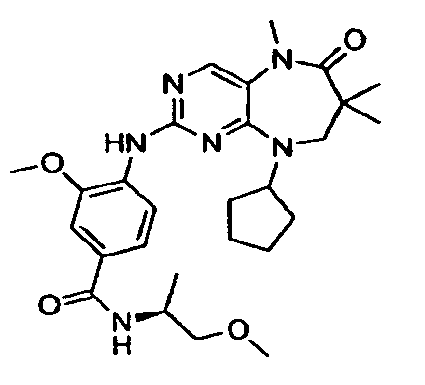
Получают по способу Е, используя подходящие реагенты. ВЭЖХ вр. уд. (мин): 9,80; МС (ES+) 511.
Пример 218:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-пропилбензамид (I-218)
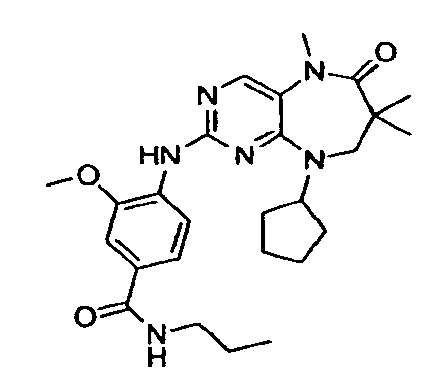
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,89 (3H, т), 1,09 (6H, с), 1,53 (2H, дт), 1,53-1,77 (6H, м), 1,82-1,92 (2H, м), 3,19 (3H, с), 3,18-3,25 (2H, м), 3,38 (2H, с), 3,94 (3H, с), 5,18 (1H, дт), 7,47 (1H, д), 7,50 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,32-8,39 (2H, м); ВЭЖХ вр. уд. (мин): 9,97; МС (ES+) 481.
Пример 219:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-этил-3-метоксибензамид (I-219)
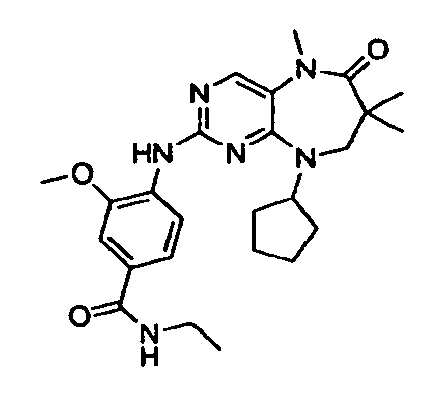
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,13 (3H, т), 1,57-1,78 (6H, м), 1,82-1,92 (2H, м), 3,18 (3H, с), 3,24-3,34 (2H, м), 3,38 (2H, с), 3,94 (3H, с), 5,18 (1H, дт), 7,47 (1H, д), 7,49 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,35-8,39 (2H, м); ВЭЖХ вр. уд. (мин): 9,65; МС (ES+) 467.
Пример 220:
9-циклопентил-2-(2-метокси-4-(3-метоксиазетидин-1-карбонил)фениламино)-5,7,7-триметил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-220)
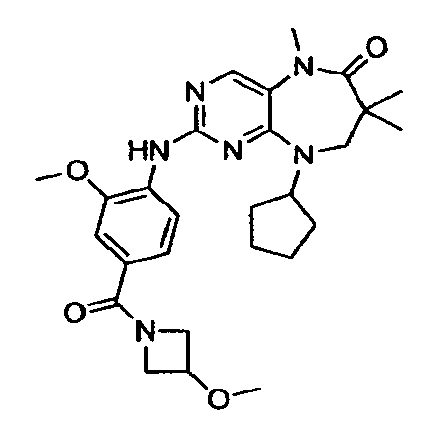
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,53-1,77 (6H, м), 1,82-1,92 (2H, м), 3,18 (3H, с), 3,22 (3H, с), 3,37 (2H, с), 3,79-3,89 (1H, м), 3,92 (3H, с), 4,13-4,27 (3H, м), 4,43-4,53 (1H, м), 5,17 (1H, дт), 7,21 (1H, д), 7,23 (1H, с), 7,71 (1H, с), 7,98 (1H, с), 8,35 (1H, д); ВЭЖХ вр. уд. (мин): 9,69; МС (ES+) 509.
Пример 221:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиридин-2-ил)бензамид (I-221)
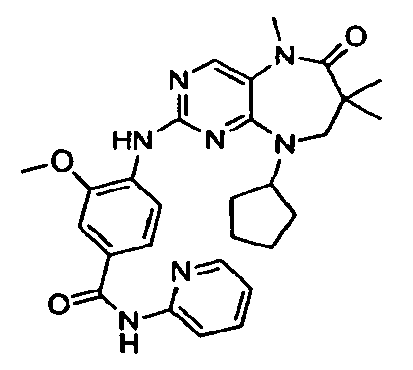
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,56-1,77 (6H, м), 1,86-1,94 (2H, м), 3,20 (3H, с), 3,42 (2H, с), 4,00 (3H, с), 5,21 (1H, квинт.), 7,16 (1H, дд), 7,72-7,77 (3H, м), 7,82-7,86 (1H, м), 8,01 (1H, с), 8,21 (1H, д), 8,38 (1H, дд), 8,46 (1H, д), 10,69 (1H, с); ВЭЖХ вр. уд. (мин): 10,30; МС (ES+) 516.
Пример 222:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиримидин-4-ил)бензамид (I-222)
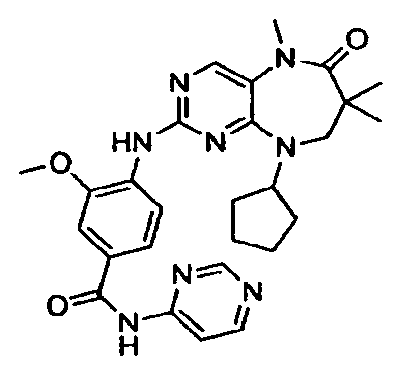
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,03 (6H, с), 1,51-1,70 (6H, м), 1,79-1,86 (2H, м), 3,13 (3H, с), 3,32 (2H, с), 3,93 (3H, с), 5,13 (1H, квинт.), 7,66-7,69 (2H, м), 7,74 (1H, с), 7,95 (1H, с), 8,16 (1H, д), 8,40-8,43 (1H, м), 8,64 (1H, д), 8,88 (1H, с), 11,07 (1H, с); ВЭЖХ вр. уд. (мин): 10,10; МС (ES+) 517.
Пример 223:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(тиазол-2-ил)бензамид (I-223)
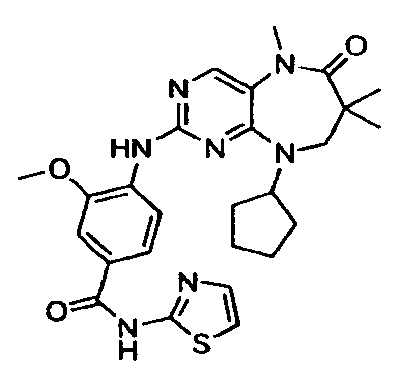
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,03 (6H, с), 1,52-1,73 (6H, м), 1,78-1,84 (2H, м), 3,13 (3H, с), 3,32 (2H, с), 3,93 (3H, с), 5,13 (1H, квинт.), 7,19 (1H, д), 7,49 (1H, д), 7,71-7,74 (3H, м), 7,95 (1H, с), 8,44 (1H, д), 12,42 (1H ушир.c); ВЭЖХ вр. уд. (мин): 10,30; МС (ES+) 522.
Пример 224:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиразин-2-ил)бензамид (I-224)
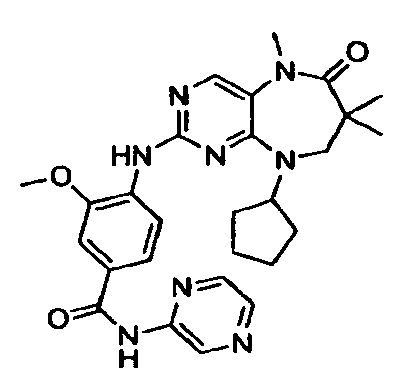
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,58-1,80 (6H, м), 1,82-1,92 (2H, м), 3,19 (3H, с), 3,50 (2H, с), 4,01 (3H, с), 5,17 (1H, дт), 7,79 (1H, д), 7,83 (1H, с), 8,05 (1H, с), 8,29 (1H, т), 8,43 (1H, д), 8,50 (1H, с), 9,46 (1H, с), 11,12 (1H, с); ВЭЖХ вр. уд. (мин): 9,99; МС (ES+) 517.
Пример 225:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((1R,2S)-2-фенилциклопропил)бензамид (I-225)
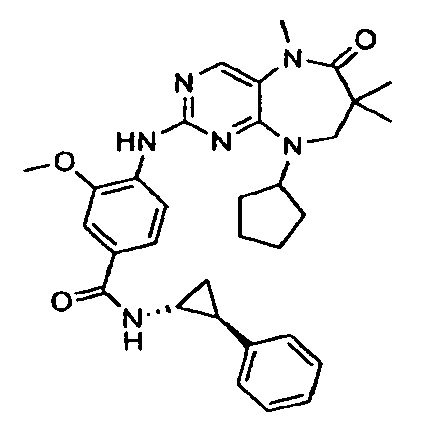
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,21-1,27 (1H, м), 1,32-1,39 (1H, м), 1,56-1,79 (6H, м), 1,82-1,92 (2H, м), 2,03-2,11 (1H, м), 2,86-3,04 (1H, м), 3,19 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 5,19 (1H, дт), 7,15-7,20 (3H, м), 7,24-7,32 (2H, м), 7,45-7,51 (2H, м), 7,70 (1H, с), 7,99 (1H, с), 8,38 (1H, д), 8,57 (1H, д); ВЭЖХ вр. уд. (мин): 10,50; МС (ES+) 555.
Пример 226:
(R)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(1-фенилэтил)бензамид (I-226)
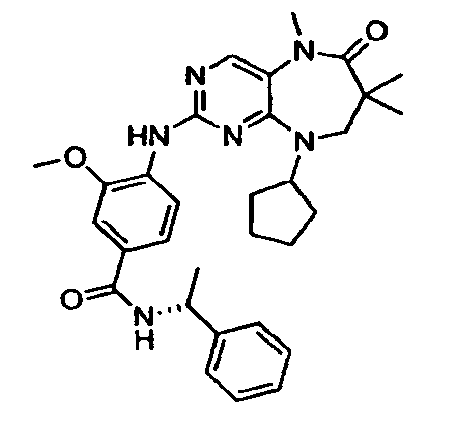
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,50 (3H, д), 1,53-1,78 (6H, м), 1,82-1,92 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 5,16-5,23 (2H, м), 7,23 (1H, т), 7,33 (2H, т), 7,39 (2H, д), 7,53 (2H, д), 7,71 (1H, с), 7,99 (1H, с), 8,38 (1H, д), 8,66 (1H, д); ВЭЖХ вр. уд. (мин): 10,39; МС (ES+) 543.
Пример 227:
N-(2-хлорпиридин-4-ил)4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид (I-227)
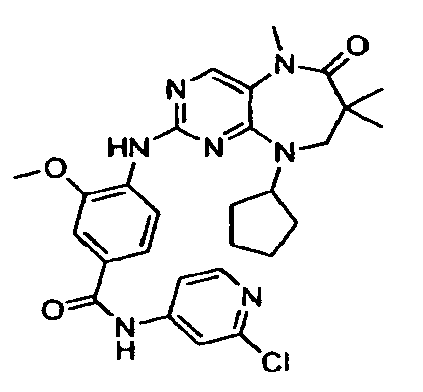
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,58-1,80 (6H, м), 1,82-1,92 (2H, м), 3,19 (3H, с), 3,51 (2H, с), 4,01 (3H, с), 5,17 (1H, дт), 7,66 (1H, с), 7,67 (1H, д), 7,77 (1H, дд), 7,95 (1H, с), 8,05 (1H, д), 8,27 (1H, т), 8,33 (1H, д), 10,69 (1H, с); ВЭЖХ вр. уд. (мин): 10,46; МС (ES+) 550.
Пример 228:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(2-метоксипиридин-3-ил)бензамид (I-228)
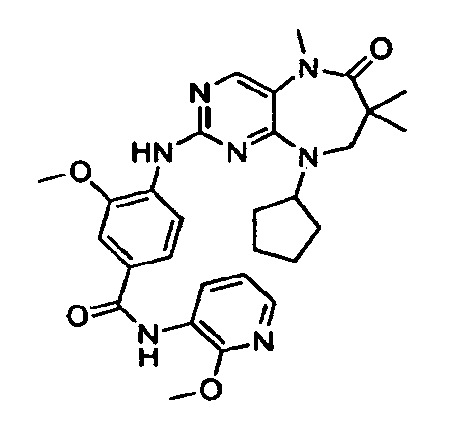
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,58-1,80 (6H, м), 1,82-1,92 (2H, м), 3,19 (3H, с), 3,50 (2H, с), 3,93 (3H, с), 3,99 (3H, с), 5,15 (1H, дт), 7,06 (1H, дд), 7,66 (1H, д), 7,69 (1H, с), 7,98-8,05 (3H, м), 8,23 (1H, т), 8,88 (1H, ушир.с), 9,64 (1H, с); ВЭЖХ вр. уд. (мин): 10,51; МС (ES+) 546.
Пример 229:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(((1S,2R)-2-гидроксициклогексил)метил)-3-метоксибензамид (I-229)
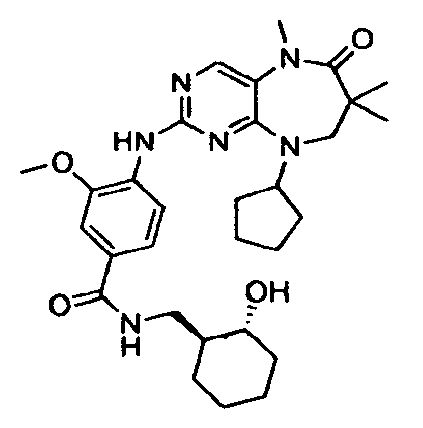
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,93-0,99 (1H, м), 1,09 (6H, с), 1,10-1,20 (2H, м), 1,36-1,46 (1H, м), 1,52-1,91 (12H, м), 3,07-3,13 (1H, м), 3,19 (3H, с), 3,35-3,45 (2H, м), 3,38 (2H, с), 3,94 (3H, с), 4,82 (1H, д), 5,18 (1H, дт), 7,48 (1H, д), 7,50 (1H, с), 7,70 (1H, с), 7,99 (1H, с), 8,32 (1H, т), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 10,17; МС (ES+) 551.
Пример 230:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(циклопентилметил)-3-метоксибензамид (I-230)
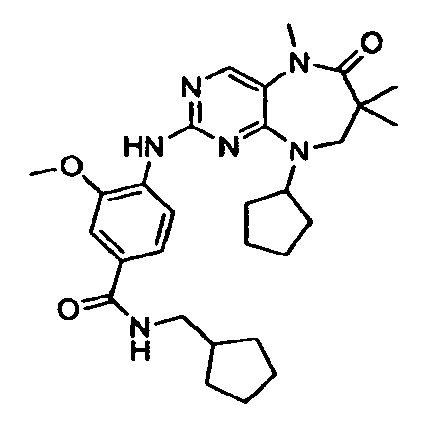
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,21-1,30 (2H, м), 1,43-1,79 (12H, м), 1,83-1,96 (2H, м), 2,11-2,19 (1H, м), 3,15-3,22 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 5,18 (1H, дт), 7,47 (1H, д), 7,50 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 10,65; МС (ES+) 521.
Пример 231:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(5-метил-1H-пиразол-3-ил)бензамид (I-231)
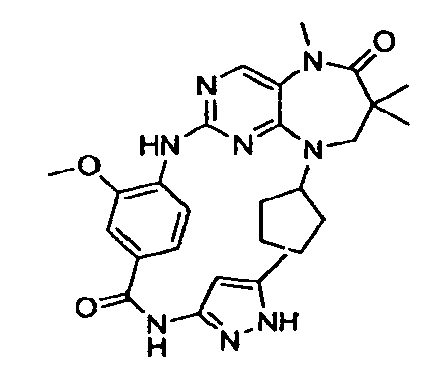
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,59-1,90 (8H, м), 2,23 (3H, с), 3,18 (3H, с), 3,50 (2H, с), 3,99 (3H, с), 5,15 (1H, дт), 6,41 (1H, ушир.с), 7,70 (1H, д), 7,76 (1H, с), 8,03 (1H, с), 8,19 (1H, д), 10,69 (1H, c); ВЭЖХ вр. уд. (мин): 9,57; МС (ES+) 519.
Пример 232:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(3-метилизотиазол-5-ил)бензамид (I-232)
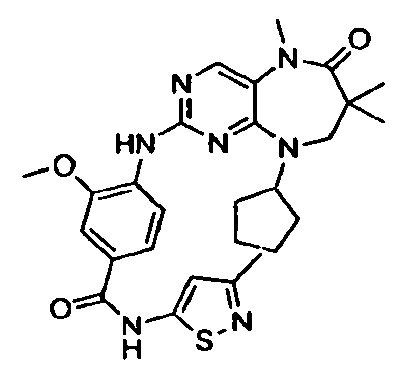
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,59-1,82 (6H, м), 1,84-1,98 (2H, м), 2,36 (3H, с), 3,19 (3H, с), 3,51 (2H, с), 4,01 (3H, с), 5,16 (1H, дт), 6,93 (1H, с), 7,74 (1H, д), 7,75 (1H, с), 8,05 (1H, с), 8,27 (1H, д), 9,01 (1H, ушир.с), 12,19 (1H, с); ВЭЖХ вр. уд. (мин): 10,15; МС (ES+) 536.
Пример 233:
N-(цианометил)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид (I-233)
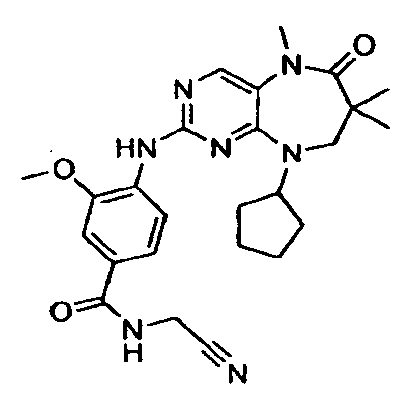
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,56-1,80 (6H, м), 1,82-1,88 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,31 (2H, д), 5,18 (1H, дт), 7,50 (1H, д), 7,52 (1H, с), 7,75 (1H, с), 8,00 (1H, с), 8,43 (1H, д), 9,07 (1H, т); ВЭЖХ вр. уд. (мин): 9,34; МС (ES+) 478.
Пример 234:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(3-трифторметил)пиридин-4-ил))бензамид (I-234)
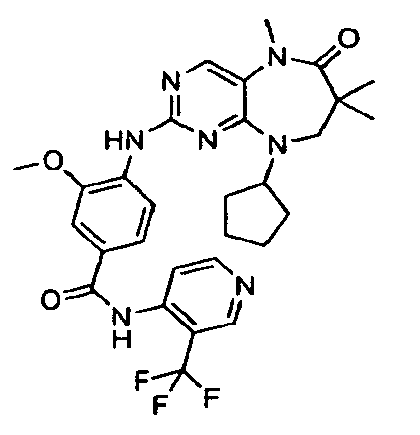
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,58-1,78 (6H, м), 1,82-1,92 (2H, м), 3,19 (3H, с), 3,52 (2H, с), 3,99 (3H, с), 5,14 (1H, квинт.), 7,64-7,69 (2H, м), 7,75-7,79 (1H, м), 8,05 (1H, д), 8,20-8,24 (1H, м), 8,89 (1H, д), 9,00 (1H, с), 9,15 (1H, ушир.с), 10,23 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 10,70; МС (ES+) 584.
Пример 235:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-((5-метилизоксазол-3-ил)метил)бензамид (I-235)
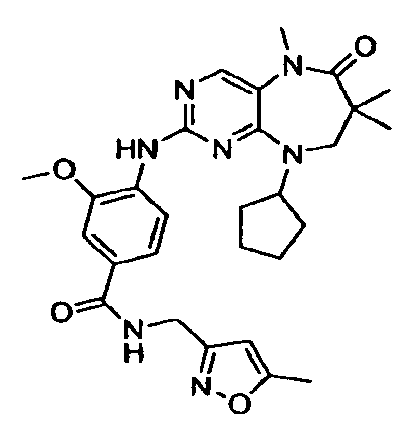
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,54-1,67 (4H, м), 1,69-1,76 (2H, м), 1,82-1,93 (2H, м), 2,37 (3H, с), 3,19 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 4,46 (2H, д), 5,18 (1H, квинт.), 6,15 (1H, с), 7,52 (1H, д), 7,53 (1H, с), 7,72 (1H, с), 7,99 (1H, с), 8,40 (1H, д), 8,96 (1H, т); ВЭЖХ вр. уд. (мин): 9,70; MS (ES+) 534.
Пример 236:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(5-метилтиазол-2-ил)бензамид (I-236)
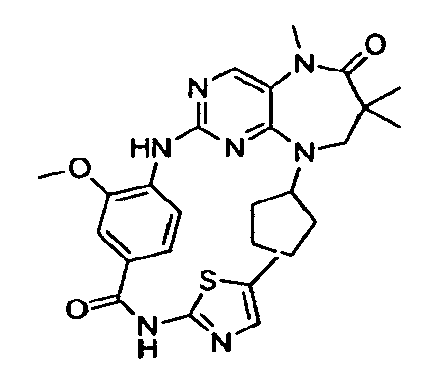
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,12 (6H, с), 1,58-1,82 (6H, с), 1,83-1,91 (2H, м), 2,38 (3H, с), 3,19 (3H, с), 3,50 (2H, с), 4,00 (3H, с), 5,16 (1H, квинт.), 7,24 (1H, с), 7,79 (1H, д), 7,85 (1H, с), 8,05 (1H, с), 8,27 (1H, д), 8,78 (1H, ушир.с), 12,44 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 10,50; МС (ES+) 536.
Пример 237:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2-(2-гидроксиэтокси)этил)-3-метоксибензамид (I-237)
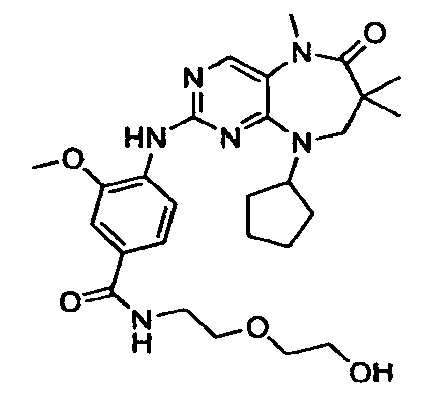
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,54-1,69 (4H, с), 1,70-1,81 (2H, м), 1,84-1,93 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,40-3,47 (4H, м), 3,49-3,55 (4H, м), 3,94 (3H, с), 4,62 (1H, т), 5,18 (1H, квинт.), 7,48 (1H, д), 7,51 (1H, с), 7,70 (1H, с), 7,99 (1H, с), 8,38 (1H, д), 8,42 (1H, т); ВЭЖХ вр. уд. (мин): 9,00; МС (ES+) 527.
Пример 238:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-изопропил-3-метоксибензамид (I-238)
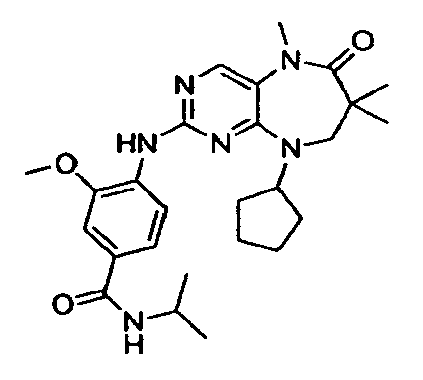
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,17 (6H, с), 1,54-1,69 (4H, м), 1,72-1,79 (2H, м), 1,82-1,93 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 4,11 (1H, дт), 5,19 (1H, квинт.), 7,48 (1H, д), 7,49 (1H, с), 7,68 (1H, с), 7,99 (1H, с), 8,08 (1H, д), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 10,10; МС (ES+) 481.
Пример 239:
(S)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-гидрокси-3-метилбутан-2-ил)-3-метоксибензамид (I-239)
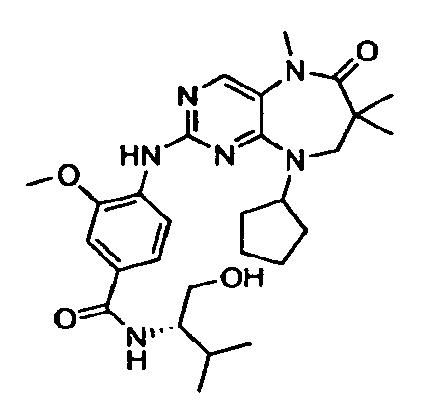
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,89 (3H, д), 0,91 (3H, д), 1,09 (6H, с), 1,58-1,77 (6H, м), 1,83-1,97 (3H, м), 3,19 (3H, с), 3,38 (2H, с), 3,53 (2H, т), 3,76-3,85 (1H, м), 3,95 (3H, с), 4,60 (1H, т), 5,19 (1H, дт), 7,51 (1H, д), 7,52 (1H, с), 7,69 (1H, с), 7,86 (1H, д), 7,99 (1H, с), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 9,75; МС (ES+) 525.
Пример 240:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-гидрокси-2-метилпропан-2-ил)-3-метоксибензамид (I-240)
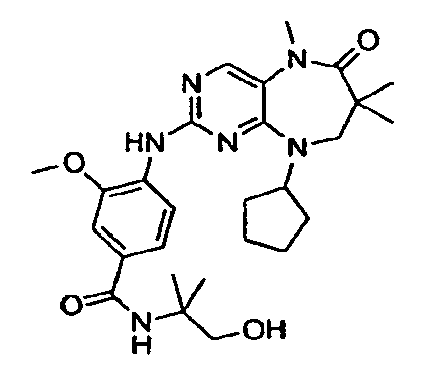
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,32 (6H, с), 1,57-1,90 (8H, м), 3,18 (3H, с), 3,38 (2H, с), 3,52 (2H, д), 3,94 (3H, с), 4,96 (1H, т), 5,19 (1H, дт), 7,40-7,44 (3H, м), 7,68 (1H, с), 7,99 (1H, с), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 9,61; МС (ES+) 511.
Пример 241:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(3-гидроксипропил)-3-метокси-N-(тиазол-2-ил)бензамид (I-241)
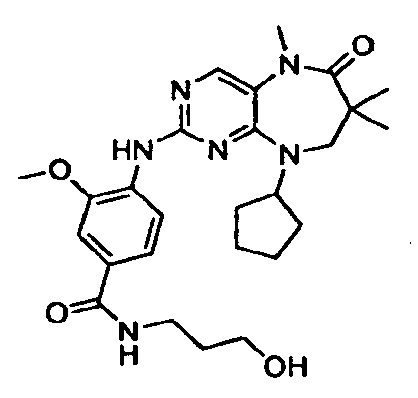
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,54-1,79 (8H, м), 1,82-1,93 (2H, м), 3,18 (3H, с), 3,28-3,36 (2H, м), 3,38 (2H, с), 3,46 (2H, дд), 3,94 (3H, с), 4,50 (1H, т), 5,18 (1H, дт), 7,47 (1H, д), 7,50 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,34-8,39 (2H, м); ВЭЖХ вр. уд. (мин): 9,02; МС (ES+) 497.
Пример 242:
(S)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2,3-дигидроксипропил)-3-метоксибензамид (I-242)
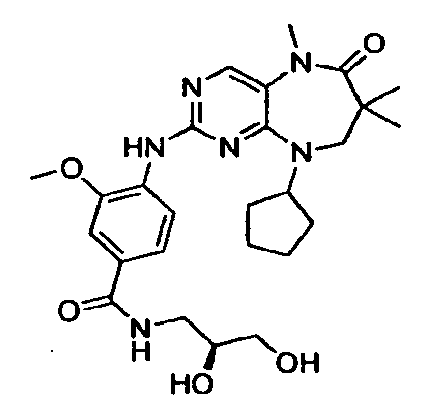
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,53-1,77 (6H, м), 1,82-1,94 (2H, м), 3,19 (3H, с), 3,18-3,24 (1H, м), 3,38 (2H, с), 3,30-3,43 (3H, м), 3,60-3,66 (1H, м), 3,94 (3H, с), 4,61 (1H, т), 4,85 (1H, д), 5,19 (1H, дт), 7,50 (1H, д), 7,53 (1H, с), 7,70 (1H, с), 7,99 (1H, с), 8,34-8,41 (2H, м); ВЭЖХ вр. уд. (мин): 8,62; МС (ES+) 513.
Пример 243:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(3-гидроксибутил)-3-метоксибензамид (I-243)
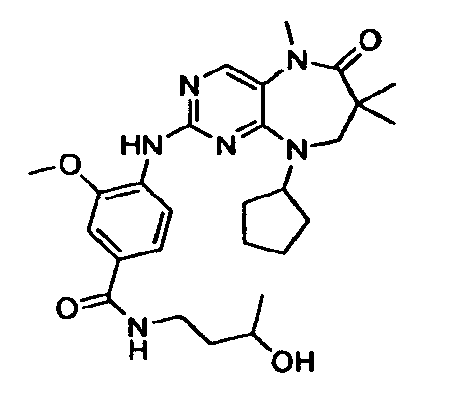
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,07-1,10 (3H, м), 1,09 (6H, с), 1,51-1,89 (10H, м), 3,18 (3H, с), 3,28-3,38 (2H, м), 3,39 (2H, с), 3,63-3,70 (1H, м), 3,93 (3H, с), 4,54 (1H, д), 5,18 (1H, дт), 7,46 (1H, д), 7,49 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,32-8,39 (2H, м); ВЭЖХ вр. уд. (мин): 9,31; МС (ES+) 511.
Пример 244:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((lR,2R)-2-гидроксициклопентил)-3-метоксибензамид (I-244)
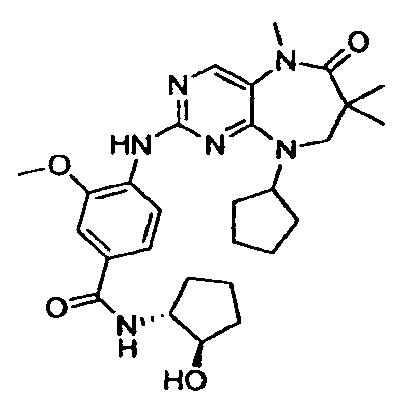
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,44-1,52 (2H, м), 1,53-1,78 (8H, м), 1,81-1,96 (3H, м), 1,97-2,04 (1H, м), 3,18 (3H, с), 3,38 (2H, с), 3,94 (3H, с), 3,94-4,03 (2H, м), 4,80 (1H, д), 5,19 (1H, дт), 7,48 (1H, д), 7,49 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,11 (1H, д), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 9,55; МС (ES+) 523.
Пример 245:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((2,2-дифторциклопропил)метил)-3-метоксибензамид (I-245)
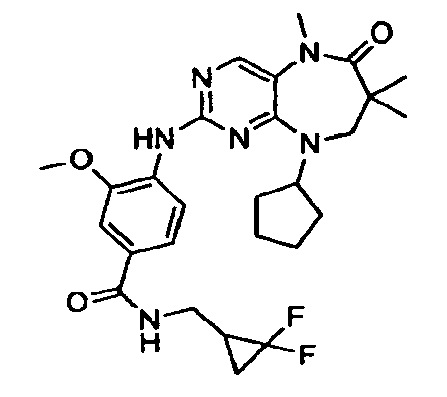
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,26-1,36 (1H, м), 1,55-1,70 (5H, м), 1,70-1,79 (2H, м), 1,82-1,94 (2H, м), 1,95-2,09 (1H, м), 3,19 (3H, с), 3,31-3,39 (2H, м), 3,39 (2H, с), 3,95 (3H, с), 5,18 (1H, дт), 7,50 (1H, д), 7,52 (1H, с), 7,76 (1H, ушир.с), 7,99 (1H, с), 8,38 (1H, д), 8,65 (1H, т); ВЭЖХ вр. уд. (мин): 10,00; МС (ES+) 529.
Пример 246:
N-(циклобутилметил)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамид (I-246)
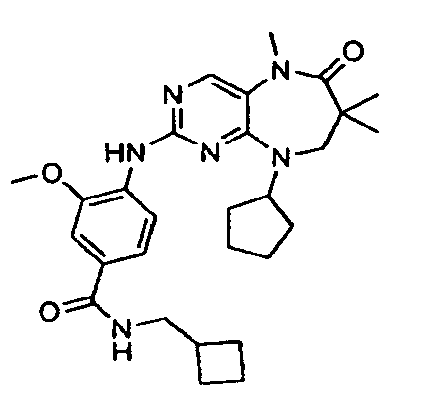
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,58-2,04 (14H, м), 2,50-2,56 (1H, м), 3,18 (3H, с), 3,30 (2H, т), 3,38 (2H, с), 3,94 (3H, с), 5,18 (1H, дт), 7,47 (1H, д), 7,49 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,32-8,38 (2H, м); ВЭЖХ вр. уд. (мин): 10,42; MS (ES+) 507.
Пример 247:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метокси-N-(пиридин-4-илметил)бензамид (I-247)
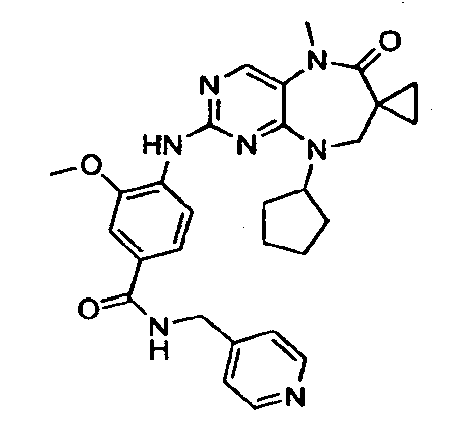
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,66-0,69 (2H, м), 0,89-0,91 (2H, м), 1,51-1,55 (2H, м), 1,60-1,64 (2H, м), 1,69 (2H, м), 1,89 (2H, м), 3,17 (3H, с), 3,44 (2H, м), 3,95 (3H, с), 4,50-4,52 (2H, м), 4,85 (1H, м), 7,30-7,31 (2H, м), 7,55-7,57 (2H, м), 7,73 (1H, с), 8,00 (1H, с), 8,44 (1H, с), 8,50-8,51 (2H, м), 9,03 (1H, м); ВЭЖХ вр. уд. (мин): 9,08; МС (ES+) 528.
Пример 248:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-(фуран-2-илметил)-3-метоксибензамид (I-248)
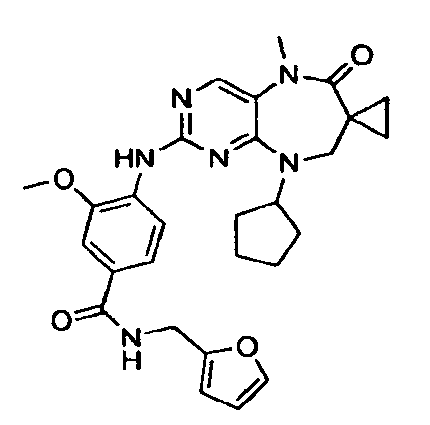
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,72 (2H, м), 0,90 (2H, м), 1,50-1,54 (2H, м), 1,60-1,64 (2H, м), 1,69 (2H, м), 1,89 (2H, м), 3,17 (3H, с), 3,48 (2H, ушир.с), 3,94 (3H, с), 4,47-4,48 (2H, м), 4,85 (1H, м), 6,27 (1H, м), 6,41 (1H, м), 7,53 (2H, м), 7,59 (1H, ушир.с), 7,70 (1H, ушир.с), 7,99 (1H, ушир.с), 8,41 (1H, д); ВЭЖХ вр. уд. (мин): 9,58; МС (ES+) 517.
Пример 249:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метокси-N-(пиридин-3-илметил)бензамид (I-249)
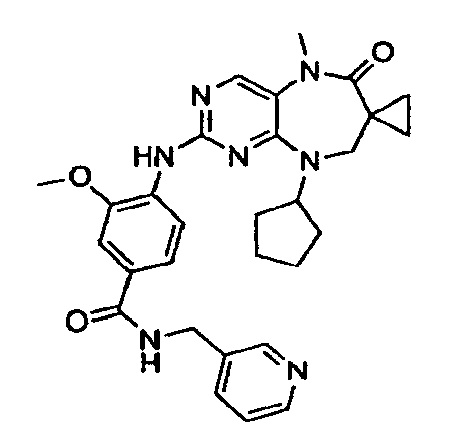
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,67-0,68 (2H, м), 0,90-0,91 (2H, м), 1,50-1,54 (2H, м), 1,59-1,64 (2H, м), 1,69 (2H, м), 1,89 (2H, м), 3,17 (3H, с), 3,45-3,48 (2H, м), 3,94 (3H, с), 4,50-4,51 (2H, м), 4,58 (1H, м), 7,37 (1H, м), 7,52-7,55 (2H, м), 7,71-7,73 (2H, м), 7,99 (1H, с), 8,42-8,47 (2H, м), 8,56 (1H, с), 9,00 (1H, м); ВЭЖХ вр. уд. (мин): 9,12; МС (ES+) 528.
Пример 250:
2-(4-(1H-имидазол-2-ил)-2-метоксифениламино)-9-циклопентил-5,7,7-триметил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-250)
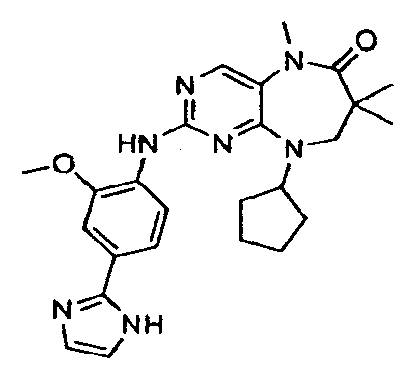
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,56-1,81 (6H, м), 1,82-1,97 (2H, м), 3,19 (3H, с), 3,30-3,40 (2H, м), 3,94 (3H, с), 5,14-5,25 (1H, м), 7,1 (2H, ушир.с), 7,49-7,54 (1H, м), 7,59-7,65 (2H, м), 7,97 (1H, с), 8,30-8,36 (1H, м), 12,40 (1H, c); ВЭЖХ вр. уд. (мин): 9,50; МС (ES+) 462.
Пример 251:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-((1R,4R)-4-гидроксициклогексил)-3-метоксибензамид (I-251)
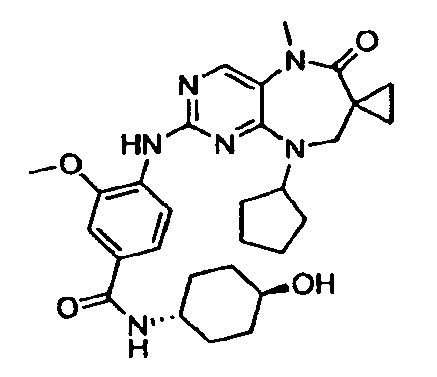
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,67 (2H, м), 0,90 (2H, м), 1,20-1,28 (2H, м), 1,34-1,43 (2H, м), 1,50-1,54 (2H, м), 1,59-1,87 (10H, м), 3,16 (3H, с), 3,47 (2H, м), 3,73 (1H, м), 3,94 (3H, с), 4,58 (1H, м), 4,86 (1H, м), 7,45-7,47 (2H, м), 7,68 (1H, м), 7,98-8,04 (2H, м), 8,38 (1H, м); ВЭЖХ вр. уд. (мин): 8,84; МС (ES+) 535.
Пример 252:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-(((1S,2S)-2-гидроксициклогексил)метил)-3-метоксибензамид (I-252)
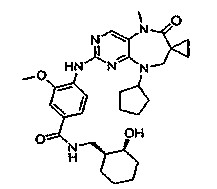
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,66-0,67 (2H, м), 0,90-0,91 (2H, м), 1,15-1,18 (2H, м), 1,23-1,35 (4H, м), 1,501-1,69 (10H, м), 1,88 (2H, м), 3,17 (3H, с), 3,48 (2H, м), 3,73 (1H, м), 3,94 (3H, с), 4,42 (1H, м), 4,84 (1H, м), 7,46-7,50 (2H, м), 7,70 (1H, ушир.с), 7,99 (1H, ушир.с), 8,36-8,41 (2H, м); ВЭЖХ вр. уд. (мин): 9,85; МС (ES+) 549.
Пример 253:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-3-метокси-N-(пирролидин-1-ил)бензамид (I-253)
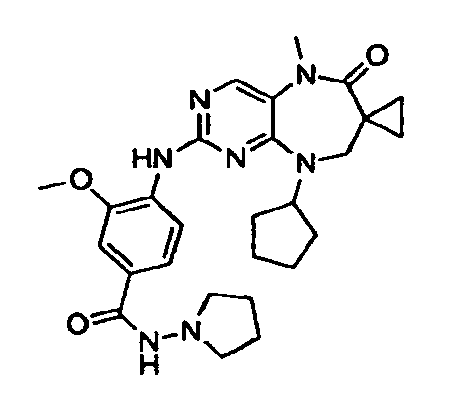
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,66-0,68 (2H, м), 0,90-0,91 (2H, м), 1,49 (2H, м), 1,50-1,54 (2H, м), 1,60-1,61 (2H, м), 1,64-1,78 (4H, м), 1,88 (2H, м), 2,95 (4H, м), 3,17 (3H, с), 3,48 (2H, м), 3,94 (3H, с), 4,84 (1H, м), 7,41 (2H, м), 7,69 (1H, с), 7,99 (1H, с), 8,40 (1H, м), 9,28 (1H, с); ВЭЖХ вр. уд. (мин): 9,20; МС (ES+) 506.
Пример 254:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(гидроксиметил)циклопентил)-3-метоксибензамид (I-254)
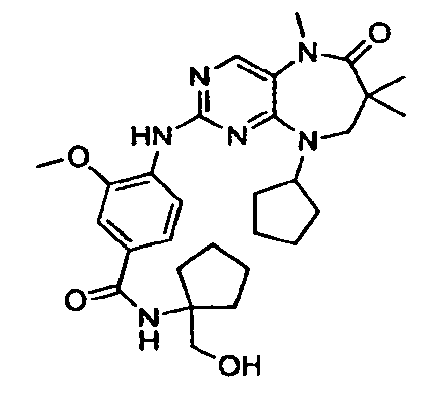
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,52-1,78 (12H, м), 1,83-1,92 (2H, м), 1,95-2,05 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,58 (2H, д), 3,94 (3H, с), 4,89 (1H, т), 5,19 (1H, квинт.), 7,44-7,46 (2H, м), 7,63 (1H, с), 7,68 (1H, с), 7,99 (1H, с), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 10,10; МС (ES+) 537.
Пример 255:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(пиридин-2-илметил)бензамид (I-255)
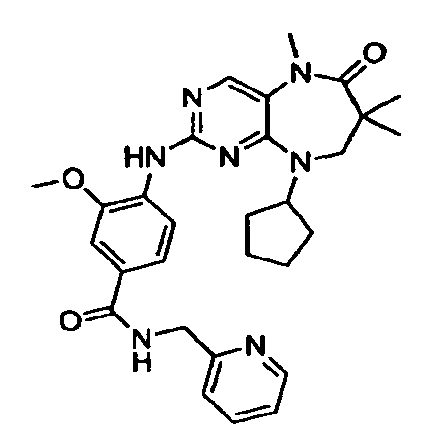
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,08 (6H, с), 1,54-1,67, (4H, м), 1,68-1,78 (2H, м), 1,85-1,93 (2H, м), 3,16 (3H, с), 3,38 (2H, с), 3,95 (3H, с), 4,57 (2H, д), 5,19 (1H, квинт.), 7,25-7,28 (1H, м), 7,32 (1H, д), 7,57 (1H, д), 7,58 (1H, с), 7,74 (1H, с), 7,76 (1H, т), 8,00 (1H, с), 8,41 (1H, д), 8,51 (1H, д), 9,04 (1H, т); ВЭЖХ вр. уд. (мин): 9,60; МС (ES+) 530.
Пример 256:
9-циклопентил-2-(4-(4,5-дигидро-1H-имидазол-2-ил)-2-метоксифениламино)-5,7,7-триметил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-256)
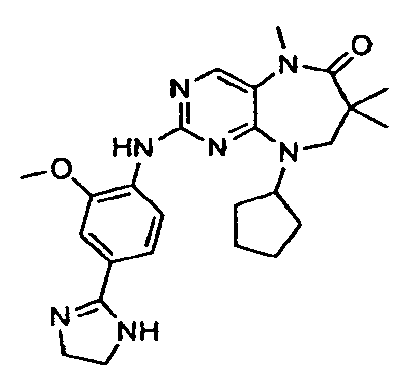
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,55-1,95 (8H, м), 3,19 (3H, с), 3,38 (2H, с), 3,65 (4H, с), 3,92 (3H, с), 5,20 (1H, квинт.), 7,42 (1H, д) 7,50 (1H, с), 7,71 (1H, с), 7,99 (1H, с), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 9,06; МС (ES+) 464.
Пример 257:
9-циклопентил-2-(4-(5,5-диметил-4,5-дигидро-1H-имидазол-2-ил)-2-метоксифениламино)-5,7,7-триметил-8,9-дигидро-5H-пиримидо[4,5-b][1,4]диазепин-6(7H)-он (I-257)
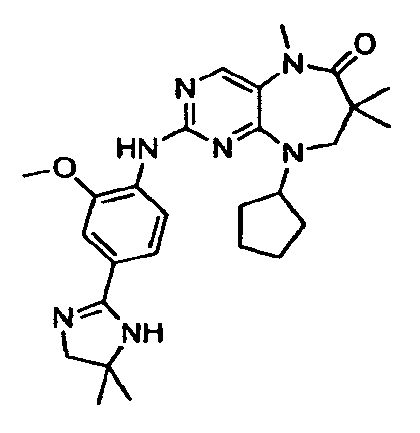
Получают по способу D, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,24 (6H, с), 1,55-1,95 (8H, м), 3,18 (3H, с), 3,32 (2H, с), 3,38 (2H, с), 3,92 (3H, с), 5,18 (1H, квинт.), 7,38 (1H, дд) 7,46 (1H, с), 7,67 (1H, с), 7,99 (1H, с), 8,36 (1H, д); ВЭЖХ вр. уд. (мин): 9,43; МС (ES+) 492.
Пример 258:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((1R,3R)-3-(гидроксициклопентил)-3-метоксибензамид (I-258)
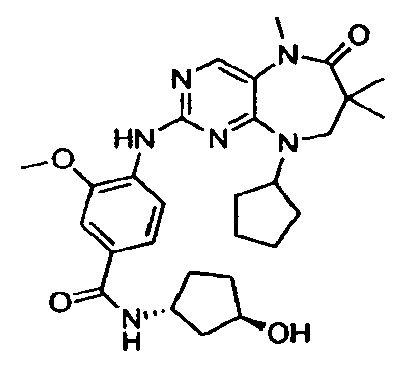
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,87 (6H, с), 1,21-1,31 (2H, м), 1,37-1,53 (7H, м), 1,60-1,74 (4H, м), 1,80-1,87 (1H, м), 2,96 (3H, с), 3,16 (2H, с), 3,72 (3H, с), 4,00 (1H, ушир.с), 4,23 (1H, дд), 4,31 (1H, д), 4,96 (1H, квинт.), 7,23 (1H, д), 7,25 (1H, с), 7,46 (1H, с), 7,77 (1H, с), 7,91 (1H, д), 8,13 (1H, д); ВЭЖХ вр. уд. (мин): 9,20; МС (ES+) 523.
Пример 259:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((1R,3R)-3-(гидроксициклопентил)метил)-3-метоксибензамид (I-259)
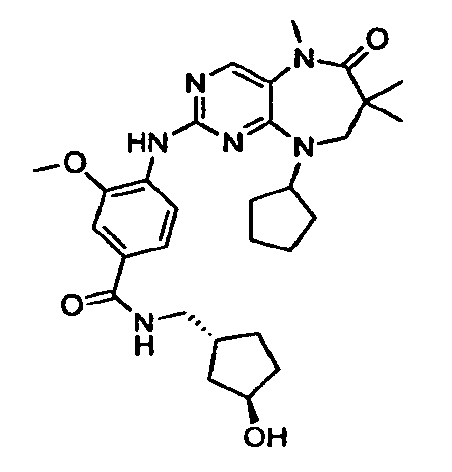
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,18-1,27 (1H, м), 1,34-1,47 (2H, м), 1,57-1,69 (5H, м), 1,72-,93 (6H, м), 2,33-2,41 (1H, м), 3,19 (3H, с), 3,34 (2H, с), 3,39 (2H, с), 3,94 (3H, с), 4,14 (1H, ушир.д), 4,38 (1H, д), 5,18 (1H, квинт.), 7,47 (1H, д), 7,50 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,35-8,37 (2H, м); ВЭЖХ вр. уд. (мин): 9,30; МС (ES+) 537.
Пример 260:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((1R,3R)-3-(гидроксиметил)циклопентил)-3-метоксибензамид (I-260)
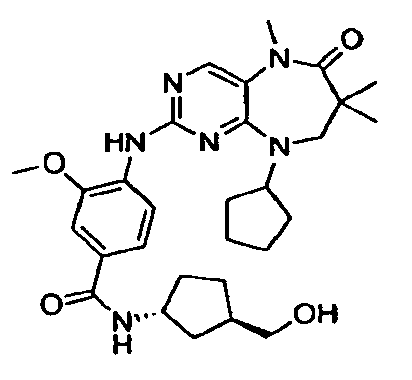
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,08 (6H, с), 1,23-1,29 (1H, м), 1,50-1,68 (6H, м), 1,70-1,76 (2H, м), 1,78-1,98 (5H, м), 2,16-2,24 (1H, м), 3,19 (3H, с), 3,30 (2H, т), 3,38 (2H, с), 3,94 (3H, с), 4,22-4,28 (1H, м), 4,55 (1H, т), 5,18 (1H, квинт.), 7,46 (1H, д), 7,47 (1H, с), 7,68 (1H, с), 7,99 (1H, с), 8,13 (1H, д), 8,35 (1H, д); ВЭЖХ вр. уд. (мин): 9,40; МС (ES+) 537.
Пример 261:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(4-метоксифенил)бензамид (I-261)
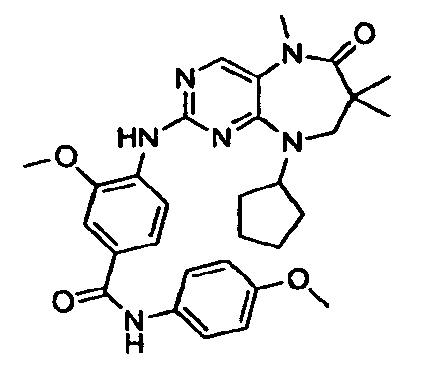
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,56-1,69 (4H, м), 1,70-1,79 (2H, м), 1,83-1,93 (2H, м), 3,19 (3H, с), 3,39 (2H, с), 3,75 (3H, с), 3,98 (3H, с), 5,21 (1H, квинт.), 6,93 (2H, д), 7,59-7,66 (4H, м), 7,76 (1H, с), 8,01 (1H, с), 8,44 (1H, д), 9,98 (1H, с); ВЭЖХ вр. уд. (мин): 10,19; МС (ES+) 545.
Пример 262:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-(3-гидроксипропил)-3-метоксибензамид (I-262)
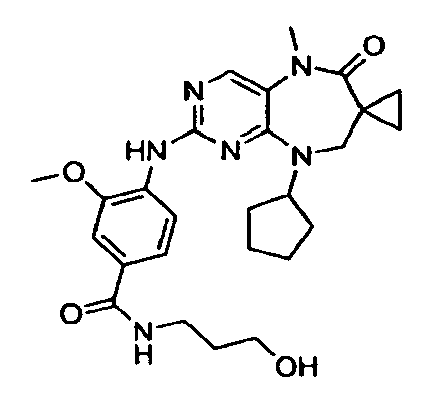
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,67 (2H, м), 0,90 (2H, м), 1,50-1,71 (6H, м), 1,89-1,91 (2H, м), 3,17 (3H, с), 3,29-3,34 (4H, м), 3,44-3,47 (4H, м), 3,94 (3H, с), 4,50 (1H, м), 4,84 (1H, м), 7,46-7,50 (2H, м), 7,69 (1H, с), 7,99 (1H, с), 8,35-8,41 (2H, м); ВЭЖХ вр. уд. (мин): 8,58; МС (ES+) 495.
Пример 263:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-изопропил-3-метоксибензамид (I-263)
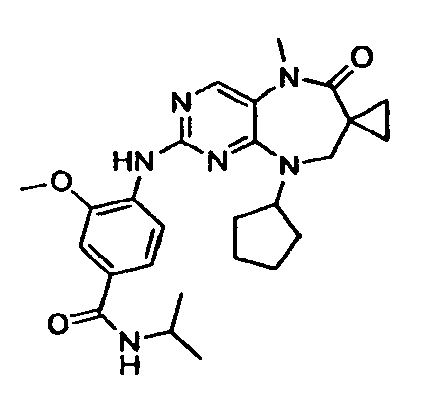
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,67 (2H, м), 0,90 (2H, м), 1,17 (3H, с), 1,18 (3H, с), 1,50-1,70 (6H, м), 1,80 (2H, м), 3,17 (3H, с), 3,48 (2H, с), 3,95 (3H, с), 4,10 (1H, м), 4,85 (1H, м), 7,49 (2H, м), 7,69 (1H, с), 7,99 (1H, с), 8,10 (1H, д), 8,40 (1H, д); ВЭЖХ вр. уд. (мин): 9,58; МС (ES+) 479.
Пример 264:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2-гидроксиэтил)-3-метоксибензамид (I-264)
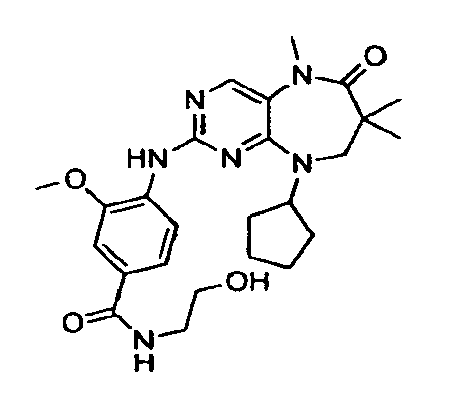
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,19 (6H, с), 1,52-1,67 (4H, м), 1,69-1,81 (2H, м), 1,82-1,94 (2H, м), 3,19 (3H, с), 3,30-3,34 (2H, ушир.м), 3,38 (2H, с), 3,48-3,53 (2H, м), 3,94 (3H, с), 4,75 (1H, т), 5,18 (1H, квинт.), 7,49 (1H, д), 7,51 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,35 (1H, с), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 8,87; МС (ES+) 483.
Пример 265:
(S)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(гидроксипропан-2-ил)-3-метоксибензамид (I-265)
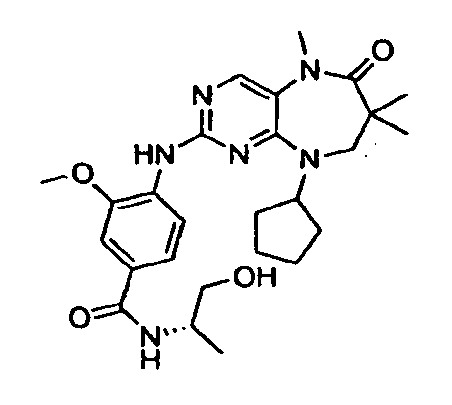
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,10 (6H, с), 1,14 (3H, д), 1,52-1,67 (4H, м), 1,69-1,81 (2H, м), 1,82-1,94 (2H, м), 3,19 (3H, с), 3,31-3,34 (1H, м), 3,38 (2H, с), 3,44-3,50 (1H, м), 3,95 (3H, с), 3,99-4,06 (1H, м), 4,74 (1H, т), 5,19 (1H, квинт.), 7,49 (1H, д), 7,50 (1H, с), 7,69 (1H, с), 7,96 (1H, с), 7,99 (1H, с), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 9,15; МС (ES+) 497.
Пример 266:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(1-(гидроксиметил)циклопентил)-3-метоксибензамид (I-266)
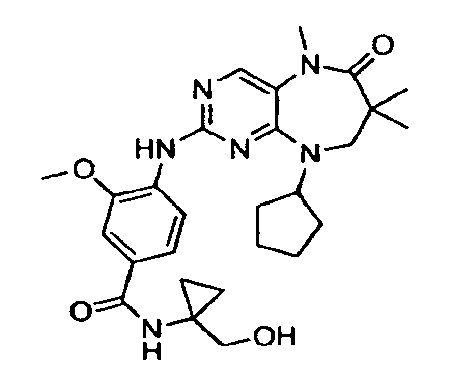
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,65-0,72 (2H, м), 0,75-0,80 (2H, м), 1,09 (6H, с), 1,57-1,94 (8H, м), 3,18 (3H, с), 3,38 (2H, с), 3,53 (2H, д), 3,93 (3H, с), 4,80 (1H, т), 5,18 (1H, дт), 7,50 (1H, д), 7,52 (1H, с), 7,68 (1H, с), 7,99 (1H, с), 8,37 (1H, д), 8,61 (1H, с); ВЭЖХ вр. уд. (мин): 9,26; МС (ES+) 510, (ES-) 508.
Пример 267:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((1S,4S)-4-фторциклогексил)-3-метоксибензамид (I-267)
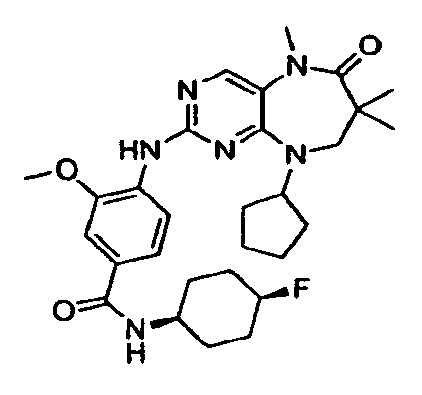
Получают по способу Е, используя подходящие реагенты. МР ДМСО D6 1,09 (6H, с), 1,55-1,79 (12H, м), 1,85-2,02 (4H, м), 3,19 (3H, с), 3,38 (2H, с), 3,85-3,94 (1H, м), 3,94 (3H, с), 4,85 (1H, д), 5,19 (1H, дт), 7,49 (1H, д), 7,50 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,13 (1H, д), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 10,17; МС (ES+) 540, (ES-) 538.
Пример 268:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-((1R, 2R)-2-гидроксициклогексил)-3-метоксибензамид (I-268)
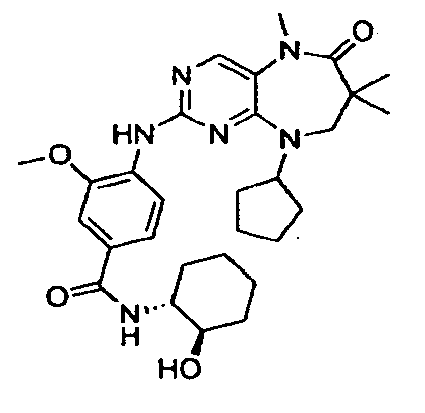
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,19-1,30 (4H, м), 1,55-1,79 (8H, м), 1,81-1,96 (4H, м), 3,19 (3H, с), 3,38 (2H, м), 3,38-3,48 (1H, м), 3,56-3,67 (1H, м), 3,95 (3H, с), 4,62 (1H, д), 5,19 (1H, дт), 7,49 (1H, д), 7,51 (1H, с), 7,69 (1H, с), 7,98 (1H, д), 7,99 (1H, с), 8,37 (1H, д); ВЭЖХ вр. уд. (мин): 9,74; МС (ES+) 538, (ES-) 536.
Пример 269:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-(3,3-дифторциклобутил)-3-метоксибензамид (I-269)
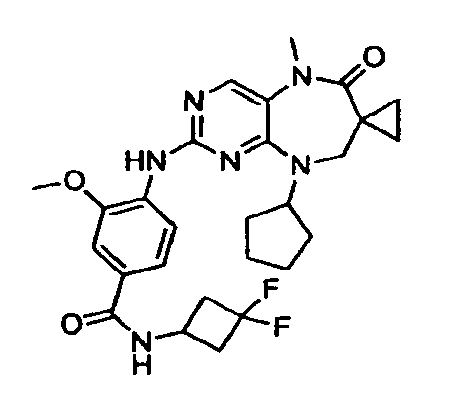
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,63-0,71 (2H, м), 0,87-0,93 (2H, м), 1,44-1,76 (6H, м), 1,84-1,94 (2H, м), 2,70-2,82 (2H, м), 2,90-3,02 (2H, м), 3,17 (3H, с), 3,48 (2H, с), 3,95 (3H, с), 4,23-4,31 (1H, м), 4,85 (1H, дт), 7,48 (1H, д), 7,49 (1H, с), 7,72 (1H, с), 7,99 (1H, с), 8,43 (1H, д), 8,66 (1H, д); ВЭЖХ вр. уд. (мин): 9,75; МС (ES+) 528, (ES-) 526.
Пример 270:
(S)-4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2-гидроксипропил)-3-метоксибензамид (I-270)
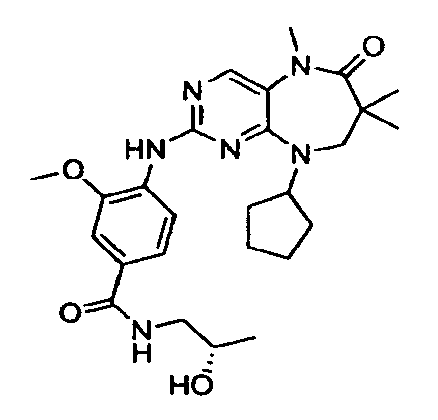
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,06 (3H, д), 1,14 (6H, с), 1,54-1,78 (6H, м), 1,82-1,94 (2H, м), 3,13-3,24 (2H, м), 3,16 (3H, с), 3,38 (2H, с), 3,73-3,82 (1H, м), 3,95 (3H, с), 4,77 (1H, д), 5,18 (1H, дт), 7,50 (1H, д), 7,52 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,30-8,40 (2H, м); ВЭЖХ вр. уд. (мин): 9,10; МС (ES+) 498, (ES-) 496.
Пример 271:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-(1-гидрокси-2-метилпропан-2-ил)-3-метоксибензамид (I-271)
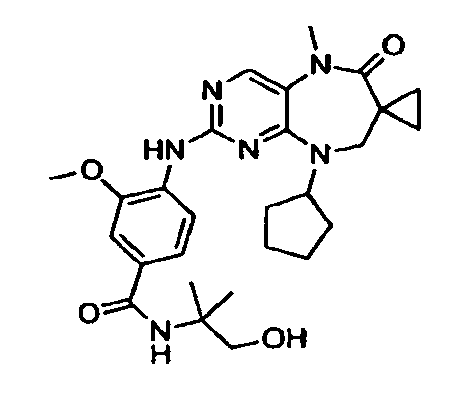
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,66-0,69 (2H, м), 0,89-0,92 (2H, м), 1,32 (6H, с), 1,48-1,69 (6H, м), 1,89 (2H, м), 3,17 (3H, с), 3,44-3,48 (2H, м), 3,51-3,52 (2H, м), 3,95 (3H, с), 4,85 (1H, м), 4,96 (1H, м), 7,42-7,43 (3H, м), 7,68 (1H, с), 7,99 (1H, с), 8,38 (1H, д); ВЭЖХ вр. уд. (мин): 9,23; МС (ES+) 510, (ES-) 508.
Пример 272:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-(1R,2R)-2-гидроксициклопентил)-3-метоксибензамид (I-272)
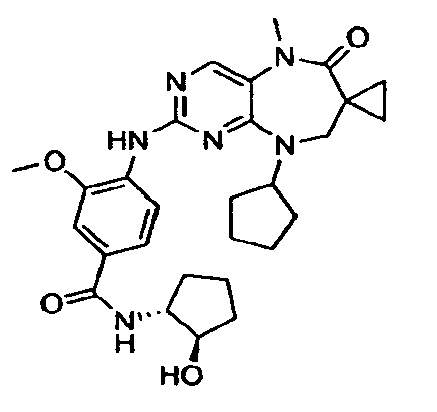
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,67 (2H, м), 0,90 (2H, м), 1,49-1,50 (2H, м), 1,55-1,68 (8H, м), 1,86-1,89 (3H, м), 2,00-2,01 (1H, м), 3,17 (3H, с), 3,48 (2H, м), 3,95 (3H, с), 3,97-4,00 (2H, м), 4,80 (1H, м), 4,85 (1H, м), 7,47-7,49 (2H, м), 7,69 (1H, с), 7,99 (1H, с), 8,11 (1H, м), 8,39 (1H, д); ВЭЖХ вр. уд. (мин): 9,16; МС (ES+) 522, (ES-) 520.
Пример 273:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метокси-N-(3,3,3-трифтор-2-гидроксипропил)бензамид (I-278)
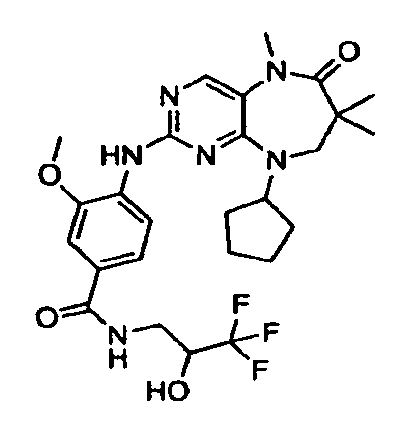
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,57-1,94 (8H, м), 3,19 (3H, с), 3,21-3,28 (1H, м), 3,38 (2H, с), 3,59-3,68 (1H, м), 3,94 (3H, с), 4,12-4,24 (1H, м), 5,18 (1H, дт), 6,54 (1H, д), 7,52 (1H, д), 7,53 (1H, с), 7,72 (1H, с), 7,99 (1H, с), 8,39 (1H, д), 8,65 (1H, т); ВЭЖХ вр. уд. (мин): 9,67; МС (ES+) 552, (ES-) 550.
Пример 274:
4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-N-(2-фторэтил)-3-метоксибензамид (I-279)
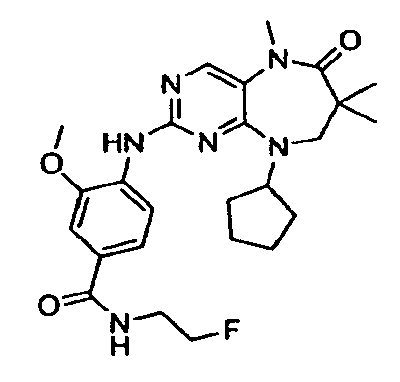
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,09 (6H, с), 1,55-1,80 (6H, м), 1,82-1,93 (2H, м), 3,19 (3H, с), 3,38 (2H, с), 3,53 (1H, кв.), 3,60 (1H, кв.), 3,94 (3H, с), 4,48 (1H, т), 4,60 (1H, т), 5,18 (1H, дт), 7,52 (1H, д), 7,53 (1H, с), 7,71 (1H, с), 7,99 (1H, с), 8,39 (1H, д), 8,61 (1H, т); ВЭЖХ вр. уд. (мин): 9,54; МС (ES+) 486, (ES-) 484.
Пример 275:
3-(4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамидо)пропилацетат (I-273)
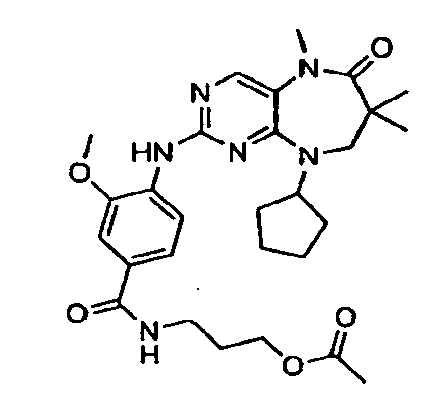
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,15 (6H, с), 1,58-1,70 (8H, м), 1,83-1,87 (2H, м), 2,01 (3H, с), 3,18 (3H, с), 3,33-3,37 (2H, м), 3,47-3,52 (2H, м), 3,94 (3H, с), 4,04-4,08 (2H, м), 5,11 (1H, м), 7,52 (1H, д), 7,59 (1H, с), 8,03 (2H, м), 8,54 (1H, м), 9,28 (1H, ушир.c); ВЭЖХ вр. уд. (мин): 9,64; МС (ES+) 540, (ES-) 538.
Пример 276:
(1r,4r)-4-(4-(9-циклопентил-5,7,7-триметил-6-оксо-6,7,8,9-тетрагидро-5H-пиримидо[4,5-b][1,4]диазепин-2-иламино)-3-метоксибензамидо)циклогексилацетат (I-280)
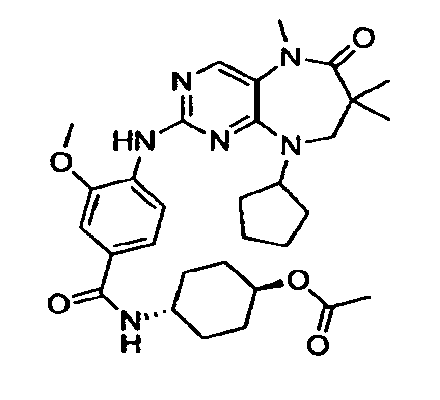
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 1,14 (6H, с), 1,44-1,96 (15H, м), 2,00 (3H, с), 3,17 (3H, с), 3,50 (3H, с), 3,82 (1H, м), 3,95 (3H, с), 4,59 (1H, м), 5,13 (1H, м), 7,50-7,55 (2H, м), 8,01 (1H, с), 8,08 (1H, д), 8,20 (1H, д), 9,00 (1H, ушир.с); ВЭЖХ вр. уд. (мин): 10,04; МС (ES+) 580, (ES-) 578.
Пример 277:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-((1s,4s)-4-фторциклогексил)-3-метоксибензамид (I-281)
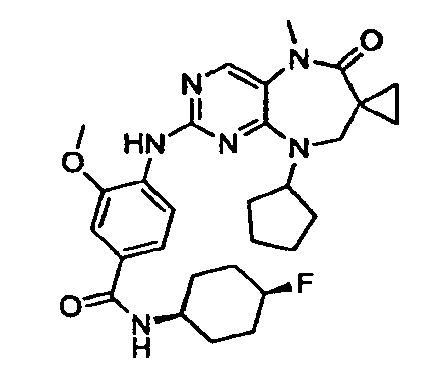
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,63-0,71 (2H, м), 0,86-0,94 (2H, м), 1,47-1,99 (16H, м), 3,17 (3H, с), 3,47 (2H, с), 3,83-3,91 (1H, м), 3,95 (3H, с), 4,78-4,89 (2H, м), 7,49 (1H, д), 7,50 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,13 (1H, д), 8,39 (1H, д); ВЭЖХ вр. уд. (мин): 9,88; МС (ES+) 538, (ES-) 536.
Пример 278:
4-(9'-циклопентил-5'-метил-6'-оксо-5',6',8',9'-тетрагидроспиро[циклопропан-1,7'-пиримидо[4,5-b][1,4]диазепин]-2'-иламино)-N-((1R,3R)-3-гидроксициклопентил)-3-метоксибензамид (I-282)
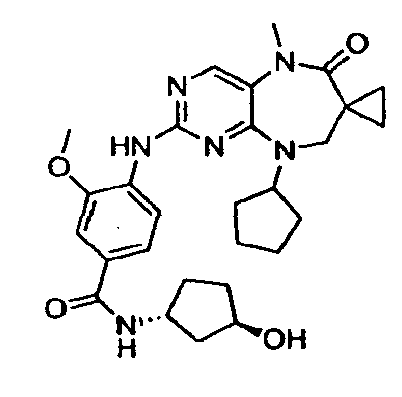
Получают по способу Е, используя подходящие реагенты. ЯМР ДМСО D6 0,63-0,69 (2H, м), 0,86-0,93 (2H, м), 1,43-1,75 (9H, м), 1,83-2,09 (5H, м), 3,17 (3H, с), 3,48 (2H, с), 3,94 (3H, с), 4,19-4,26 (1H, м), 4,46 (1H, дт), 4,53 (1H, д), 4,85 (1H, дт), 7,46 (1H, д), 7,48 (1H, с), 7,69 (1H, с), 7,99 (1H, с), 8,14 (1H, д), 8,39 (1H, д); ВЭЖХ вр. уд. (мин): 8,83; МС (ES+) 522, (ES-) 520.
Пример 279: Анализ PLK1
Активность соединений настоящего изобретения как ингибиторов человеческой киназы PLK оценивают с помощью следующих анализов.
Анализ ингибирования Plk1:
Соединения подвергают скринингу на способность ингибировать Plk1 путем анализа включения фосфата, меченного радиоактивным изотопом. Анализы проводят в смеси, содержащей 25 мМ HEPES (pH 7,5), 10 мM MgCl2 и 1 мM DTT. Конечные концентрации субстратов составляют 50 мкM для [γ-33P]АТФ (136 мКи 33P АТФ/ммоль АТФ, Amersham Pharmacia Biotech/Sigma Chemicals) и 10 мкM для пептида (белок SAM68 ∆332-443). Анализы проводят при 25°C в присутствии 15 нМ Plk1 (A20-K338). Получают исходный буферный раствор для анализа, который содержит все перечисленные выше реагенты, за исключением АТФ и представляющего интерес тестируемого соединения. 30 мкл исходного раствора помещают в 96-луночный планшет, затем добавляют 2 мкл исходного раствора в ДМСО, содержащего серийные разведения тестируемого соединения (как правило, используют 2-кратные серийные разведения, начиная с конечной концентрации 10 мкM) с двойными повторами (конечная концентрация DMSO 5%). Планшет предварительно инкубируют 10 минут при 25°C, после чего реакцию инициируют добавлением 8 мкл [γ-33P]АТФ (конечная концентрация 50 мкМ).
Реакцию останавливают через 60 минут добавлением 100 мкл 0,14 M фосфорной кислоты. 96-луночный планшет с многоситовым фосфоцеллюлозным фильтром (Millipore, № по каталогу MAPHN0B50) предварительно обрабатывают 100 мкл 0,2 M фосфорной кислоты и затем добавляют 125 мкл аналитической смеси с остановленной реакцией. Планшет промывают 4×200 мкл 0,2 M фосфорной кислоты. После сушки в лунки добавляют 100 мкл жидкой сцинтилляционной смеси Optiphase 'SuperMix' (Perkin Elmer) и считают сцинтилляции (на жидкостном сцинтилляционном счетчике 1450 Microbeta, Wallac).
Из всех экспериментальных точек вычитают средние фоновые значения и затем рассчитывают значения Ki(app) с помощью нелинейного регрессионного анализа начальной скорости с использованием программного обеспечения Prism (GraphPad Prism версия 3.0cх для Macintosh, программное обеспечение GraphPad, San Diego California, USA).
Анализ ингибирования Plk1:
Соединения подвергают скринингу на способность ингибировать Plk1 путем анализа включения фосфата, меченного радиоактивным изотопом. Анализы проводят в смеси, содержащей 25 мМ HEPES (pH 7,5), 10 мM MgCl2 и 1 мM DTT. Конечные концентрации субстратов составляют 150 мкM (350 мкM при определении значений < 1 нM) для [γ-33P]АТФ (115 мКи 33P АТФ/ммоль АТФ, Amersham Pharmacia Biotech/Sigma Chemicals) и 300 мкM (450 мкM при определении значений < 1 нM) для пептида (KKKISDELMDATFADQEAK). Анализы проводят при 25°C в присутствии 4 нМ (1 нM при определении значений < 1 нM) Plk1. Получают исходный буферный раствор для анализа, который содержит все перечисленные выше реагенты, за исключением АТФ и представляющего интерес тестируемого соединения. 30 мкл исходного раствора помещают в 96-луночный планшет, затем добавляют 2 мкл исходного раствора в ДМСО, содержащего серийные разведения тестируемого соединения (как правило, используют 2-кратные серийные разведения, начиная с конечной концентрации 10 мкM) с двойными повторами (конечная концентрация DMSO 5%). Планшет предварительно инкубируют 10 минут при 25°C, после чего реакцию инициируют добавлением 8 мкл [γ-33P]АТФ (конечная концентрация 150 мкМ (350 мкM при определении значений < 1 нM)).
Реакцию останавливают через 90 минут (240 минут при определении значений < 1 нM) добавлением 100 мкл 0,14 M фосфорной кислоты. 96-луночный планшет с многоситовым фосфоцеллюлозным фильтром (Millipore, № по каталогу MAPHN0B50) предварительно обрабатывают 100 мкл 0,2 M фосфорной кислоты и затем добавляют 125 мкл аналитической смеси с остановленной реакцией. Планшет промывают 4×200 мкл 0,2 M фосфорной кислоты. После сушки в лунки добавляют 100 мкл жидкой сцинтилляционной смеси Optiphase 'SuperMix' (Perkin Elmer) и считают сцинтилляции (на жидкостном сцинтилляционном счетчике 1450 Microbeta, Wallac).
Из всех экспериментальных точек вычитают средние фоновые значения и затем рассчитывают значения Ki(app) с помощью нелинейного регрессионного анализа начальной скорости с использованием программного обеспечения Prism (GraphPad Prism версия 3.0cх для Macintosh, программное обеспечение GraphPad, San Diego California, USA).
В целом соединения данного изобретения являются эффективными ингибиторами Plk1. Нижеследующие соединения имеют значения Ki ниже 10 нM по результатам анализа включения радиоактивной метки I-2, I-5, I-4, I-6, I-9, I-11, I-12, I-16, I-17, I-18, I-21, I-22, I-23, I-24, I-25, I-26, I-27, I-28, I-31, I-32, I-33, I-34, I-36, I-37, I-38, I-39, I-47, I-48, I-51, I-52, I-53, I-58, I-59, I-60, I-62, I-64, I-67, I-68, I-69, I-70, I-71, I-72, I-73, I-74, I-75, I-76, I-77, I-80, I-85, I-87, I-93, I-94, I-95, I-96, I-99, I-101, I-103, I-104, I-105, I-108, I-113, I-118, I-119, I-123, I-129, I-130, I-131, I-132, I-133, I-134, I-135, I-136, I-157, I-158, I-163, I-166, I-167, I-169, I-170, I-171, I-172, I-173, I-174, I-175 I-176, I-177, I-178, I-179, I-180, I-181, I-182, I-183, I-184 I-185, I-186, I-187, I-190, I-191, I-192, I-193, I-194, I-195 I-196, I-197, I-198, I-199, I-200, I-201, I-202, I-203, I-204 I-205, I-206, I-207, I-208, I-209, I-210, I-211, I-212, I-213 I-214, I-216, I-217, I-218, I-219, I-220, I-221, I-222, I-223 I-224, I-225, I-226, I-227, I-228, I-229, I-230, I-231, I-232 I-233, I-234, I-235, I-236, I-237, I-238, I-239, I-240, I-241 I-242, I-243, I-244, I-245, I-246, I-247, I-248, I-249, I-250 I-251, I-252, I-253, I-254, I-255, I-256, I-257, I-258, I-259 I-260, I-261, I-262, I-263, I-264, I-265, I-266, I-267, I-268 I-269, I-270, I-271, I-272, I-273, I-278, I-279, I-280, I-282. Нижеследующие соединения имеют значения Ki от 10 нM до 100 нМ по результатам анализа включения радиоактивной метки: I-1, I-3, I-7, I-8, I-10, I-14, I-15, I-19, I-20, I-30, I-35, I-40, I-42, I-43, I-44, I-45, I-46, I-49, I-50, I-56, I-63, I-65, I-66, I-78, I-79, I-81, I-86, I-89, I-90, I-91, I-92, I-97, I-98, I-102, I-109, I-110, I-111, I-112, I-114, I-116, I-117, I-120, I-122, I-124, I-125, I-137, I-138, I-139, I-141, I-143, I-144, I-145, I-147, I-149, I-150, I-151, I-152, I-153, I-154, I-155, I-156, I-159, I-160, I-161, I-162, I-164, I-165, I-168, I-188, I-192, I-215. Нижеследующие соединения имеют значения Ki от 100 нM до 4 мкМ по результатам анализа включения радиоактивной метки: I-29, I-41, I-54, I-55, I-57, I-61, I-82, I-83, I-84, I-88, I-100, I-106, I-115, I-121, I-127, I-128, I-140, I-146, I-148, I-189. В условиях анализа не растворимы следующие соединения: I-126 и I-142. Неактивными в пределах чувствительности анализа являются соединения: I-13 и I-107.
Анализ ингибирования Plk2:
Соединения подвергают скринингу на способность ингибировать Plk2 путем анализа включения фосфата, меченного радиоактивным изотопом. Анализы проводят в смеси, содержащей 25 мМ HEPES (pH 7,5), 10 мM MgCl2, 0,1% БСА и 2 мM DTT. Конечные концентрации субстратов составляют 200 мкM для [γ-33P]АТФ (57 мКи 33P АТФ/ммоль АТФ, Amersham Pharmacia Biotech/Sigma Chemicals) и 300 мкM для пептида (KKKISDELMDATFADQEAK). Анализы проводят при 25°C в присутствии 25 нМ Plk2. Получают исходный буферный раствор для анализа, который содержит все перечисленные выше реагенты, за исключением АТФ и представляющего интерес тестируемого соединения. 30 мкл исходного раствора помещают в 96-луночный планшет, затем добавляют 2 мкл исходного раствора в ДМСО, содержащего серийные разведения тестируемого соединения (как правило, используют 2-кратные серийные разведения, начиная с конечной концентрации 10 мкM) с двойными повторами (конечная концентрация DMSO 5%). Планшет предварительно инкубируют 10 минут при 25°C, после чего реакцию инициируют добавлением 8 мкл [γ-33P]АТФ (конечная концентрация 200 мкМ).
Реакцию останавливают через 90 минут добавлением 100 мкл 0,14 M фосфорной кислоты. 96-луночный планшет с многоситовым фосфоцеллюлозным фильтром (Millipore, № по каталогу MAPHN0B50) предварительно обрабатывают 100 мкл 0,2 M фосфорной кислоты и затем добавляют 125 мкл аналитической смеси с остановленной реакцией. Планшет промывают 4×200 мкл 0,2 M фосфорной кислоты. После сушки в лунки добавляют 100 мкл жидкой сцинтилляционной смеси Optiphase 'SuperMix' (Perkin Elmer) и считают сцинтилляции (на жидкостном сцинтилляционном счетчике 1450 Microbeta, Wallac).
Из всех экспериментальных точек вычитают средние фоновые значения и затем рассчитывают значения Ki(app) с помощью нелинейного регрессионного анализа начальной скорости с использованием программного обеспечения Prism (GraphPad Prism версия 3.0cх для Macintosh, программное обеспечение GraphPad, San Diego California, USA).
Анализ ингибирования Plk3:
Соединения подвергают скринингу на способность ингибировать Plk3 путем анализа включения фосфата, меченного радиоактивным изотопом. Анализы проводят в смеси, содержащей 25 мМ HEPES (pH 7,5), 10 мM MgCl2 и 1 мM DTT. Конечные концентрации субстратов составляют 75 мкM для [γ-33P]АТФ (60 мКи 33P АТФ/ммоль АТФ, Amersham Pharmacia Biotech/Sigma Chemicals) и 10 мкM для пептида (белок SAM68 ∆332-443). Анализы проводят при 25°C в присутствии 5 нМ Plk3 (S38-A340). Получают исходный буферный раствор для анализа, который содержит все перечисленные выше реагенты, за исключением АТФ и представляющего интерес тестируемого соединения. 30 мкл исходного раствора помещают в 96-луночный планшет, затем добавляют 2 мкл исходного раствора в ДМСО, содержащего серийные разведения тестируемого соединения (как правило, используют 2-кратные серийные разведения, начиная с конечной концентрации 10 мкM) с двойными повторами (конечная концентрация DMSO 5%). Планшет предварительно инкубируют 10 минут при 25°C, после чего реакцию инициируют добавлением 8 мкл [γ-33P]АТФ (конечная концентрация 75 мкМ).
Реакцию останавливают через 60 минут добавлением 100 мкл 0,14 M фосфорной кислоты. 96-луночный планшет с многоситовым фосфоцеллюлозным фильтром (Millipore, № по каталогу MAPHN0B50) предварительно обрабатывают 100 мкл 0,2 M фосфорной кислоты и затем добавляют 125 мкл аналитической смеси с остановленной реакцией. Планшет промывают 4×200 мкл 0,2 M фосфорной кислоты. После сушки в лунки добавляют 100 мкл жидкой сцинтилляционной смеси Optiphase 'SuperMix' (Perkin Elmer) и считают сцинтилляции (на жидкостном сцинтилляционном счетчике 1450 Microbeta, Wallac).
Из всех экспериментальных точек вычитают средние фоновые значения и затем рассчитывают значения Ki(app) с помощью нелинейного регрессионного анализа начальной скорости с использованием программного обеспечения Prism (GraphPad Prism версия 3.0cх для Macintosh, программное обеспечение GraphPad, San Diego California, USA).
Анализ ингибирования Plk4:
Соединения подвергают скринингу на способность ингибировать Plk4 путем анализа включения фосфата, меченного радиоактивным изотопом. Анализы проводят в смеси, содержащей 8 мМ MOPS (pH 7,5), 10 мM MgCl2, 0,1% БСА и 1 мM DTT. Конечные концентрации субстратов составляют 15 мкM для [γ-33P]АТФ (227 мКи 33P АТФ/ммоль АТФ, Amersham Pharmacia Biotech/Sigma Chemicals) и 300 мкM для пептида (KKKMDATFADQ). Анализы проводят при 25°C в присутствии 25 нМ Plk4. Получают исходный буферный раствор для анализа, который содержит все перечисленные выше реагенты, за исключением АТФ и представляющего интерес тестируемого соединения. 30 мкл исходного раствора помещают в 96-луночный планшет, затем добавляют 2 мкл исходного раствора в ДМСО, содержащего серийные разведения тестируемого соединения (как правило, используют 2-кратные серийные разведения, начиная с конечной концентрации 10 мкM) с двойными повторами (конечная концентрация DMSO 5%). Планшет предварительно инкубируют 10 минут при 25°C, после чего реакцию инициируют добавлением 8 мкл [γ-33P]АТФ (конечная концентрация 15 мкМ).
Реакцию останавливают через 180 минут добавлением 100 мкл 0,14 M фосфорной кислоты. 96-луночный планшет с многоситовым фосфоцеллюлозным фильтром (Millipore, № по каталогу MAPHN0B50) предварительно обрабатывают 100 мкл 0,2 M фосфорной кислоты и затем добавляют 125 мкл аналитической смеси с остановленной реакцией. Планшет промывают 4×200 мкл 0,2 M фосфорной кислоты. После сушки в лунки добавляют 100 мкл жидкой сцинтилляционной смеси Optiphase 'SuperMix' (Perkin Elmer) и считают сцинтилляции (на жидкостном сцинтилляционном счетчике 1450 Microbeta, Wallac).
Из всех экспериментальных точек вычитают средние фоновые значения и затем рассчитывают значения Ki(app) с помощью нелинейного регрессионного анализа начальной скорости с использованием программного обеспечения Prism (GraphPad Prism версия 3.0cх для Macintosh, программное обеспечение GraphPad, San Diego California, USA).
Хотя авторы описали ряд воплощений данного изобретения, очевидно, что основные приведенные ими примеры можно изменить с получением других воплощений, в которых используются или которые охватывают соединения, способы и процессы данного изобретения. Таким образом, следует понимать, что объем данного изобретения должен определяться прилагающейся формулой изобретения.

| название | год | авторы | номер документа |
|---|---|---|---|
| ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2013 |
|
RU2623221C2 |
| ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2008 |
|
RU2478100C2 |
| БИЦИКЛИЧЕСКИЕ ЛАКТАМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2716136C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2001 |
|
RU2340611C2 |
| ПРОИЗВОДНЫЕ БЕНЗОНАФТОАЗУЛЕНА, ПРИМЕНЕНИЕ ИХ В КАЧЕСТВЕ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ И ДЛЯ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКИХ КОМПОЗИЦИЙ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ИНГИБИРОВАНИЯ ПРОДУЦИРОВАНИЯ ФНО-α | 2003 |
|
RU2318827C2 |
| ТРИЦИКЛИЧЕСКИЕ ПИРРОЛО ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ | 2012 |
|
RU2591191C2 |
| ОСНОВНЫЕ НЕПЕПТИДНЫЕ АНТАГОНИСТЫ БРАДИКИНИНА И ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2003 |
|
RU2327688C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ 1,2,3,4-ТЕТРАГИДРОПИРИМИДО{1,2-a}ПИРИМИДИН-6-ОНА, ИХ ПОЛУЧЕНИЕ И ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2010 |
|
RU2561130C2 |
| БИЦИКЛИЧЕСКИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2013 |
|
RU2627269C2 |
| СОЕДИНЕНИЯ | 2012 |
|
RU2630677C2 |
Изобретение относится к соединению формулы I
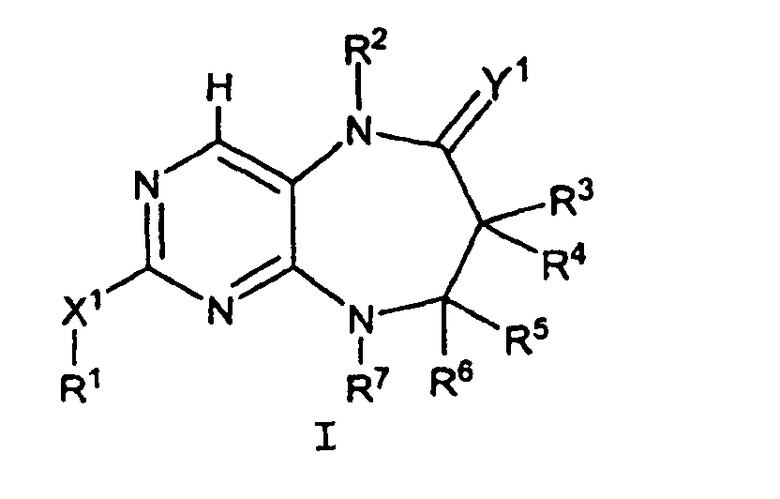
где Х1 обозначает связь, NR8 или S; Y1 обозначает О или NR9; R1 обозначает C1-10алкил, С6-10арил или 5-10-членный гетероарил, содержащий 1-3 гетероатома, независимо выбранных из N или S; где указанный R1 необязательно замещен 0-2 J1; R2 обозначает Н или С1-10алкил; каждый из R3, R4, R5 и R6 независимо обозначает Н или С1-10алкил; и R7 обозначает С1-10алкил, С3-10циклоалкил, фенил, 5-6-членный гетероциклил, содержащий 1-3 гетероатома, независимо выбранных из О и N, -(С1-6алкил)-(С3-10циклоалкил), -(C1-6алкил)-(фенил) или -(С1-6алкил)-(6-членный гетероциклил, содержащий 2 гетероатома, выбранных из О и N); где указанный R7 необязательно замещен 0-5 J7; или R3 и R4, вместе с атомом углерода, к которому они присоединены, необязательно образуют 3-4-членный насыщенный или частично ненасыщенный моноциклический фрагмент; R3 и R5 вместе с атомами углерода, к которым они присоединены, необязательно образуют 5-членный моноциклический фрагмент; R8 обозначает Н; R9 обозначает Н или незамещенный С1-6алкил; или R2 и R9 вместе с атомами, к которым они присоединены, необязательно образуют 5-членный ароматический моноциклический фрагмент, содержащий 3 атома азота; каждый J1 независимо обозначает С1-6галогеналкил, галоген, NO2, CN, Q или -Z-Q; или два J1 вместе могут необязательно образовывать =O; Z обозначает С1-6алкил, в котором 0-3 атома углерода необязательно заменены на -NR-, -O-, -С(O)- или -SO2-; причем каждый Z необязательно замещен 0-2 J2; Q обозначает Н; С1-6алкил; 3-8-членный ароматический или неароматический моноциклический фрагмент, содержащий 0-3 гетероатомов, независимо выбранных из О, N и S; или 8-10-членную ароматическую бициклическую систему; каждый Q необязательно замещен 0-2 JQ; каждый JZ независимо обозначает С1-6алкил или галоген (С1-4алкил); каждый из JQ и J7 независимо обозначает М или -Y-M; каждый Y независимо обозначает незамещенный С1-6алкил, в котором 0-3 атома углерода необязательно заменены на -O-, -С(O)- или -SO2-; каждый М независимо обозначает Н, C1-6алкил, С3-6циклоалкил, галоген (С1-6алкил), фенил, галоген, CN, ОН, OR'; или два М вместе могут необязательно образовывать =O; R обозначает Н или незамещенный С1-6алкил; R' обозначает незамещенный С1-6алкил. Изобретение также относится к способам получения указанных соединений, а также к фармацевтической композиции для ингибирования PLK на их основе. Технический результат - получены новые соединения, которые могут найти применение в медицине в качестве ингибиторов протеинкиназ. 7 н. и 27 з.п. ф-лы, 1 табл., 279 пр.
1. Соединение формулы I:
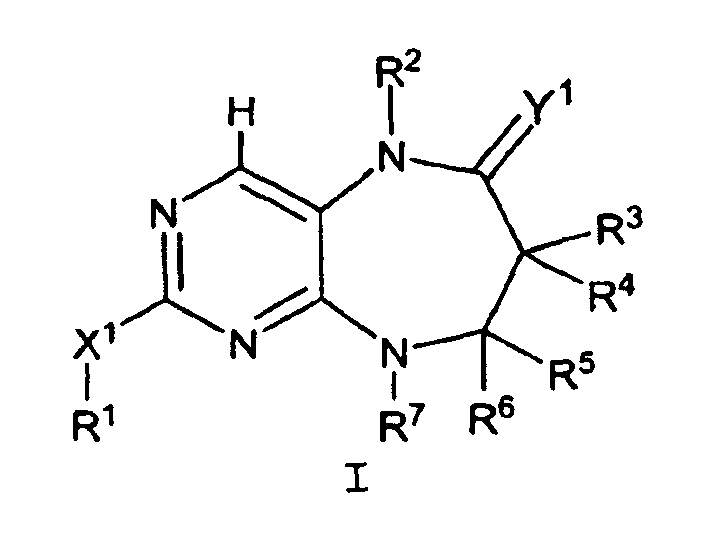
где X1 обозначает связь, NR8 или S;
Y1 обозначает О или NR9;
R1 обозначает C1-10алкил, С6-10арил или 5-10-членный гетероарил, содержащий 1-3 гетероатома, независимо выбранных из N или S; где указанный R1 необязательно замещен 0-2 J1;
R2 обозначает Н или C1-10алкил;
каждый из R3, R4, R5 и R6 независимо обозначает Н или C1-10алкил; и R7 обозначает C1-10алкил, С3-10циклоалкил, фенил, 5-6-членный гетероциклил, содержащий 1-3 гетероатома, независимо выбранных из О и N, - (C1-6алкил)-(С3-10циклоалкил), -(C1-6алкил)-(фенил) или -(C1-6алкил)-(6-членный гетероциклил, содержащий 2 гетероатома, выбранных из О и N); где указанный R7 необязательно замещен 0-5 J7; или
R3 и R4, вместе с атомом углерода, к которому они присоединены, необязательно образуют 3-4-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R3 и R5 вместе с атомами углерода, к которым они присоединены, необязательно образуют 5-членный моноциклический фрагмент;
R8 обозначает Н;
R9 обозначает Н или незамещенный C1-6алкил; или
R2 и R9 вместе с атомами, к которым они присоединены, необязательно образуют 5-членный ароматический моноциклический фрагмент, содержащий 3 атома азота;
каждый J1 независимо обозначает C1-6галогеналкил, галоген, NO2, CN, Q или -Z-Q; или два J1 вместе могут необязательно образовывать =О;
Z обозначает C1-6алкил, в котором 0-3 атома углерода необязательно заменены на -NR-, -O-, -С(О)- или -SО2-; причем каждый Z необязательно замещен 0-2 J2;
Q обозначает Н; C1-6алкил; 3-8-членный ароматический или неароматический моноциклический фрагмент, содержащий 0-3 гетероатомов, независимо выбранных из О, N и S; или 8-10-членную ароматическуюй бициклическую систему; каждый Q необязательно замещен 0-2 JQ;
каждый Jz независимо обозначает C1-6алкил или галоген(C1-4алкил);
каждый из JQ и J7 независимо обозначает М или -Y-M;
каждый Y независимо обозначает незамещенный C1-6алкил, в котором 0-3 атома углерода необязательно заменены на -O-, -С(O)-или -SО2-;
каждый М независимо обозначает Н, C1-6алкил, С3-6циклоалкил, галоген (С1-4алкил), фенил, галоген, CN, ОН, OR'; или два М вместе могут необязательно образовывать =O;
R обозначает Н или незамещенный C1-6алкил;
R' обозначает незамещенный C1-6алкил.
2. Соединение по п.1, где:
R1 обозначает С6-10арил или 5-10-членный гетероарил, содержащий 1-3 гетероатома, независимо выбранных из N или S; где указанный R1 необязательно замещен 0-2 J1;
R7 обозначает Н, С3-10циклоалкил, 5-6-членный гетероциклил, содержащий 1-3 гетероатома, независимо выбранных из О и N;
Q обозначает Н; C1-6алкил; 3-8-членный ароматический или неароматический моноциклический фрагмент, содержащий 0-3 гетероатомов, независимо выбранных из О, N и S; или 8-10-членный ароматический бициклический фрагмент; причем каждый Q необязательно замещен 0-2 J12; и
каждый М независимо обозначает Н, C1-6алкил, С3-6циклоалкил, галоген(С1-4алкил), галоген, CN, ОН или OR'.
3. Соединение по п.1 или 2, где X1 обозначает NR8.
4. Соединение по п.3, где Y1 обозначает О.
5. Соединение по п.4, где R1 обозначает С6-10арил или 5-10-членный гетероарил, содержащий 1-3 гетероатома, независимо выбранных из N или S, где R1 замещен 0-2 J1.
6. Соединение по п.5, где R2 обозначает C1-10алкил.
7. Соединение по п.6, где R2 обозначает -СН3.
8. Соединение по п.7, где R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют 3-4-членный насыщенный моноциклический фрагмент.
9. Соединение по п.1, где R7 обозначает группу, выбранную из C1-10алкила, С3-10циклоалкила, фенила и 5-6-членного гетероциклила, содержащего 1-3 гетероатома, независимо выбранных из О и N, где R7 замещен 0-5 J7.
10. Соединение по п.1, где R7 обозначает группу, выбранную из C1-10алкила, С3-8циклоалкила, фенила и 6-членного гетероциклила, содержащего 1-3 гетероатома, независимо выбранных из О и N, где R7 замещен 0-5 J7.
11. Соединение по п.1, где R7 не обозначает 3-амино-2,4-пиримидин.
12. Соединение по п.1, где R7 обозначает группу, выбранную из С3-6алкила, С3-8циклоалкила, фенила или 5-6-членного гетероциклила, где гетероциклил содержит 1 гетероатом кислорода, и где R7 замещен 0-5 J7.
13. Соединение по п.1, где R7 обозначает С4-5циклоалкил, где R7 замещен 0-5 J7.
14. Соединение по п.1, где R7 обозначает С4-5циклоалкил, замещенный 1 или 2 -F.
15. Соединение по п.1, где R7 обозначает незамещенный С4-5циклоалкил.
16. Соединение по п.1, где R7 обозначает циклопентил, замещенный 0-5 J7.
17. Соединение по п.1, где R7 обозначает циклопентил, замещенный 1 или 2 -F.
18. Соединение по п.1, где R7 обозначает незамещенный циклопентил.
19. Соединение по п.1 или 2, представленное формулой II:
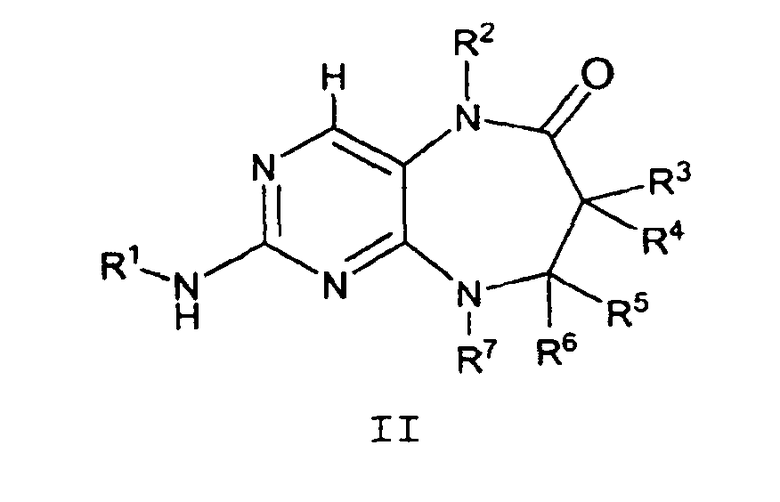
где R1 обозначает С6-10арил или 5-10-членный гетероарил, содержащий 1-3 гетероатома, независимо выбранных из N или S;
R2 обозначает Н или необязательно замещенный C1-10алкил;
каждый R3, R4, R5 и R6 независимо обозначает Н или C1-10алкил; или
R3 и R4 вместе с атомом углерода, к которому они присоединены, могут образовывать необязательно замещенный 3-4-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R3 и R5 вместе с атомами углерода, к которым они присоединены, могут образовывать 5-членный моноциклический фрагмент.
20. Соединение по п.1 или 2, представленное формулой III:
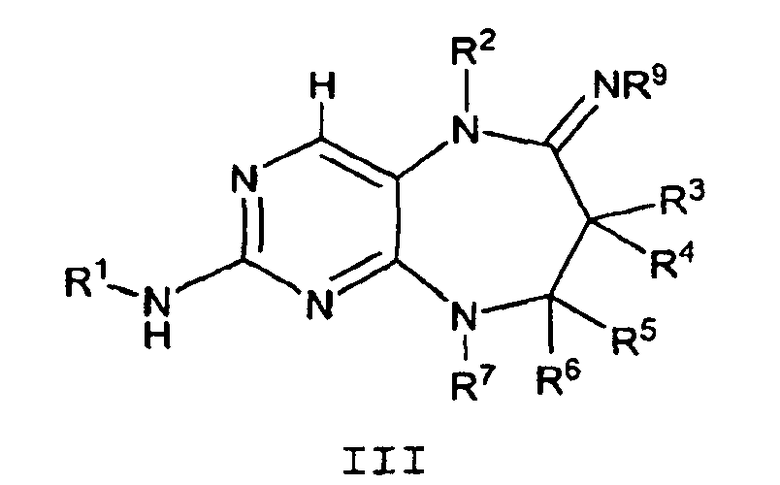
где R1 обозначает С6-10арил или 5-10-членный гетероарил, содержащий 1-3 гетероатома, независимо выбранных из N или S;
R2 обозначает Н или C1-10алкил;
каждый R3, R4, R5 и R6 независимо обозначает Н или C1-10алкил; или
R3 и R4 вместе с атомом углерода, к которому они присоединены, могут образовывать 3-4-членный насыщенный или частично ненасыщенный моноциклический фрагмент;
R3 и R5 вместе с атомами углерода, к которым они присоединены, могут образовывать 5-членный моноциклический фрагмент.
21. Соединение, выбранное из нижеследующих соединений:
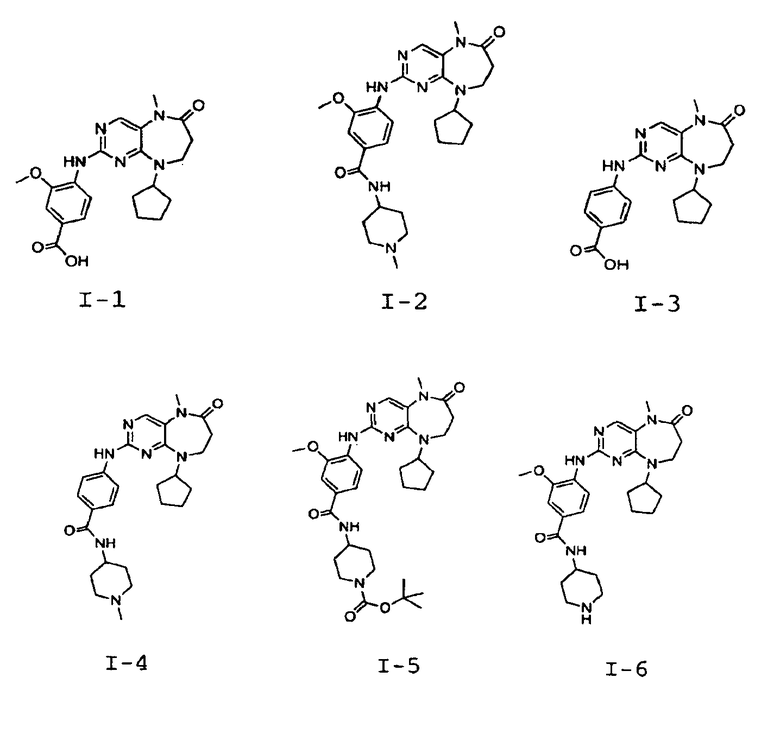
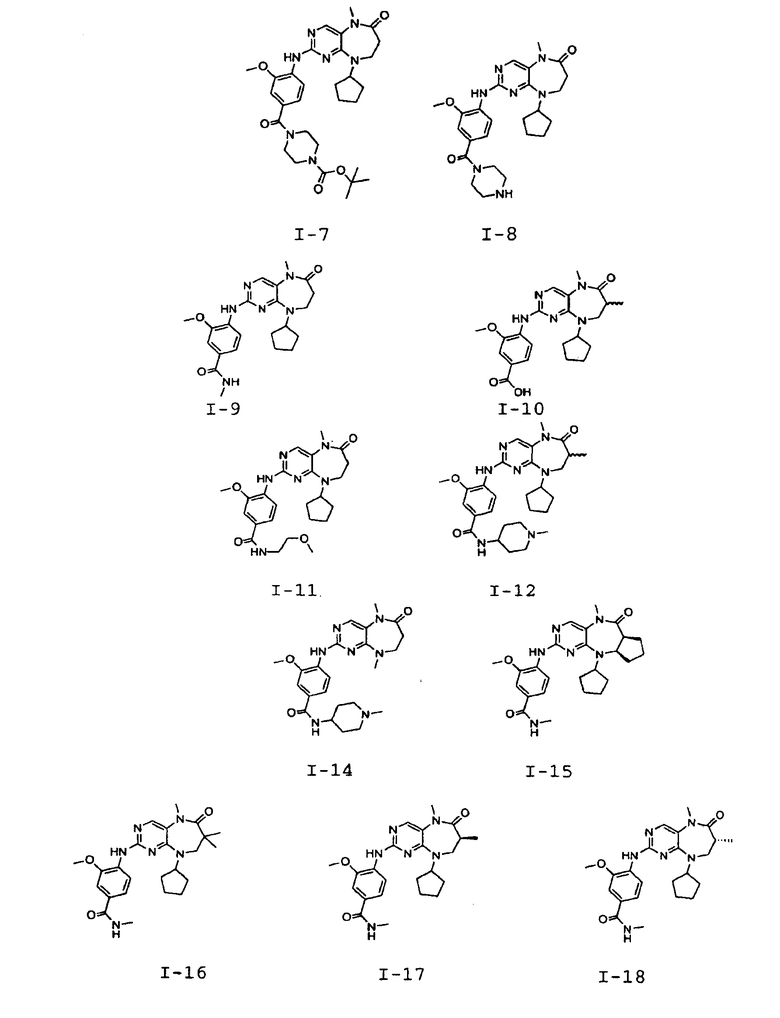
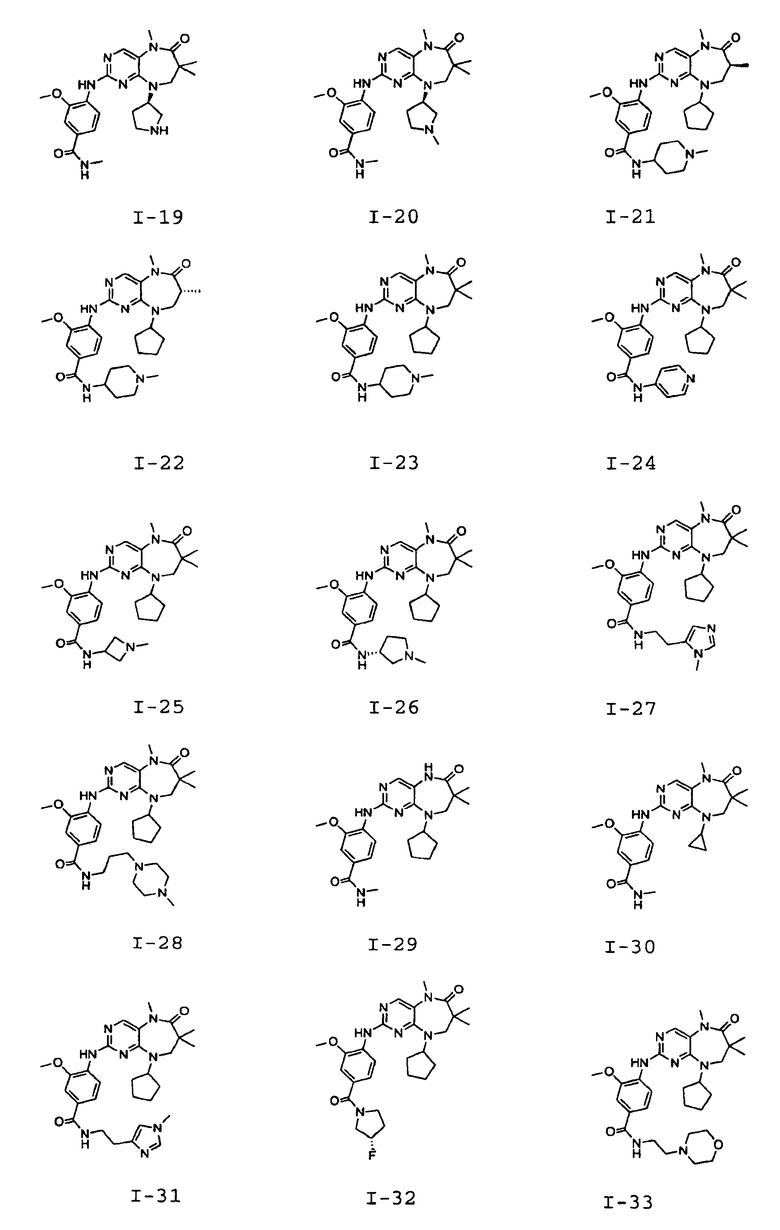
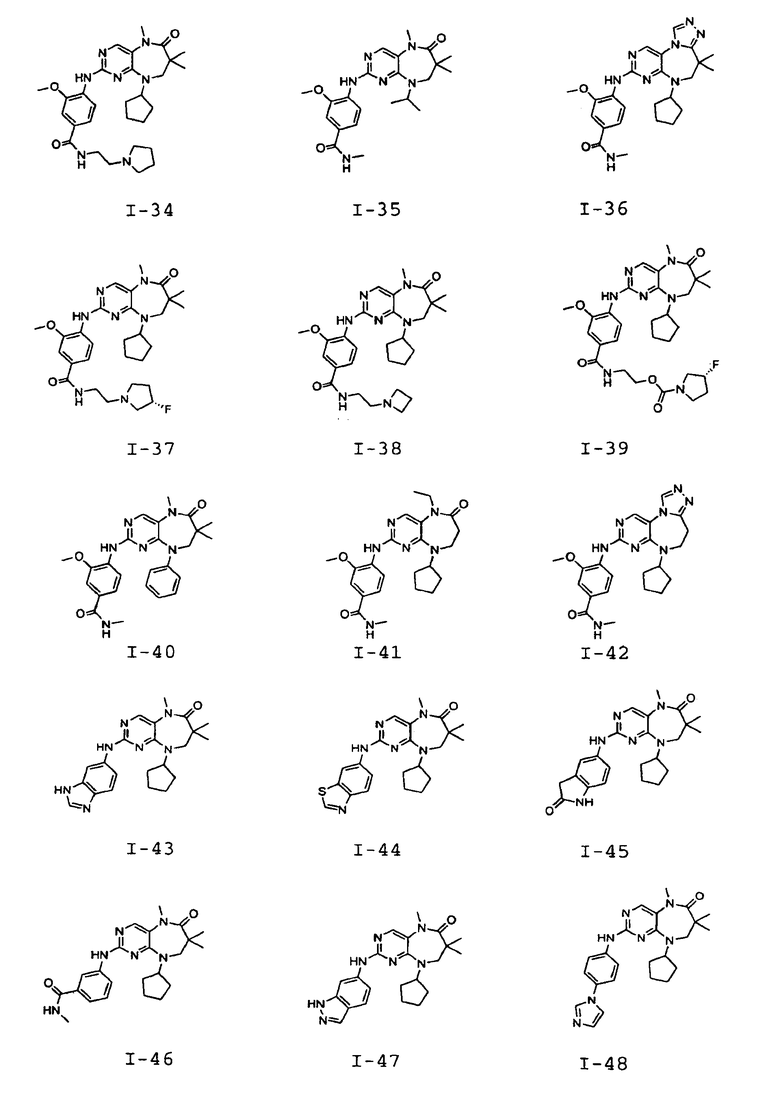
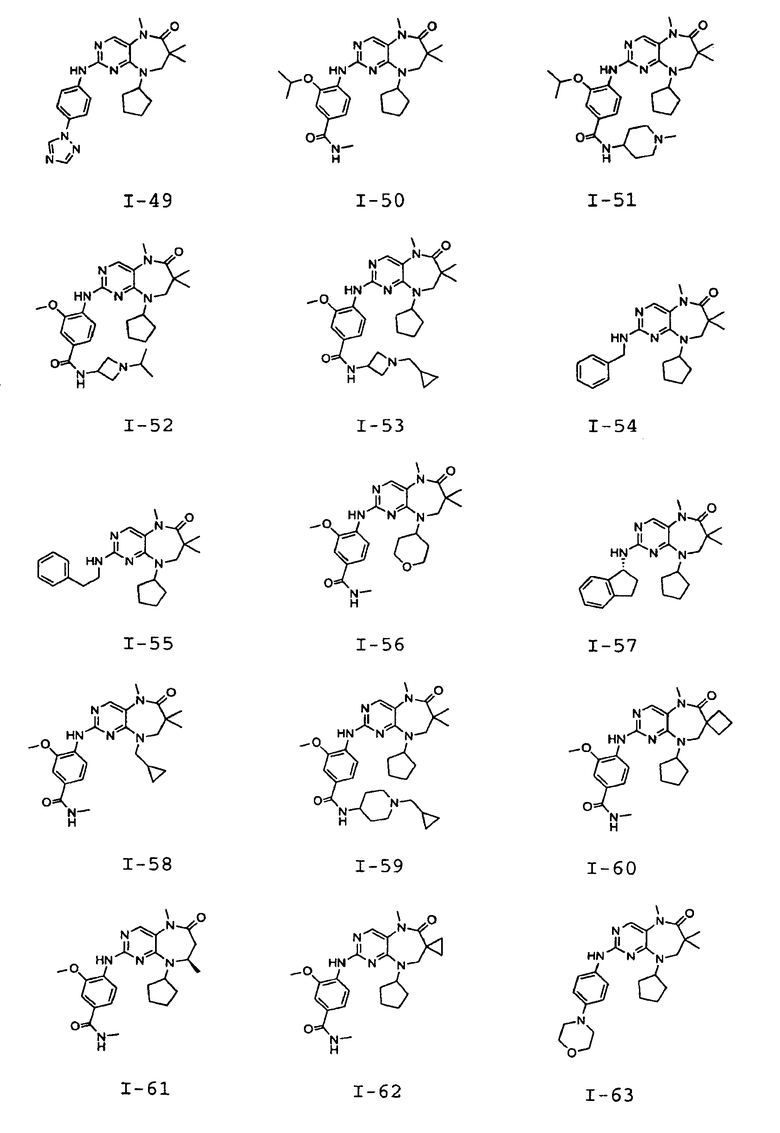
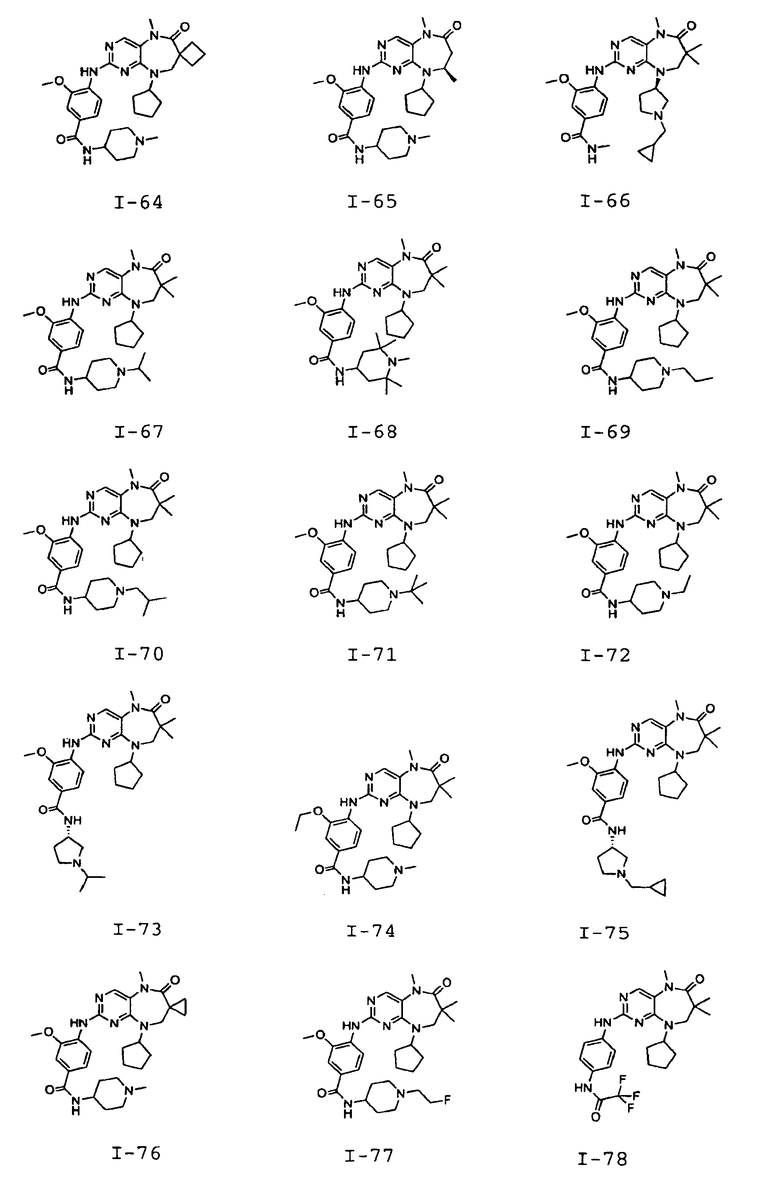
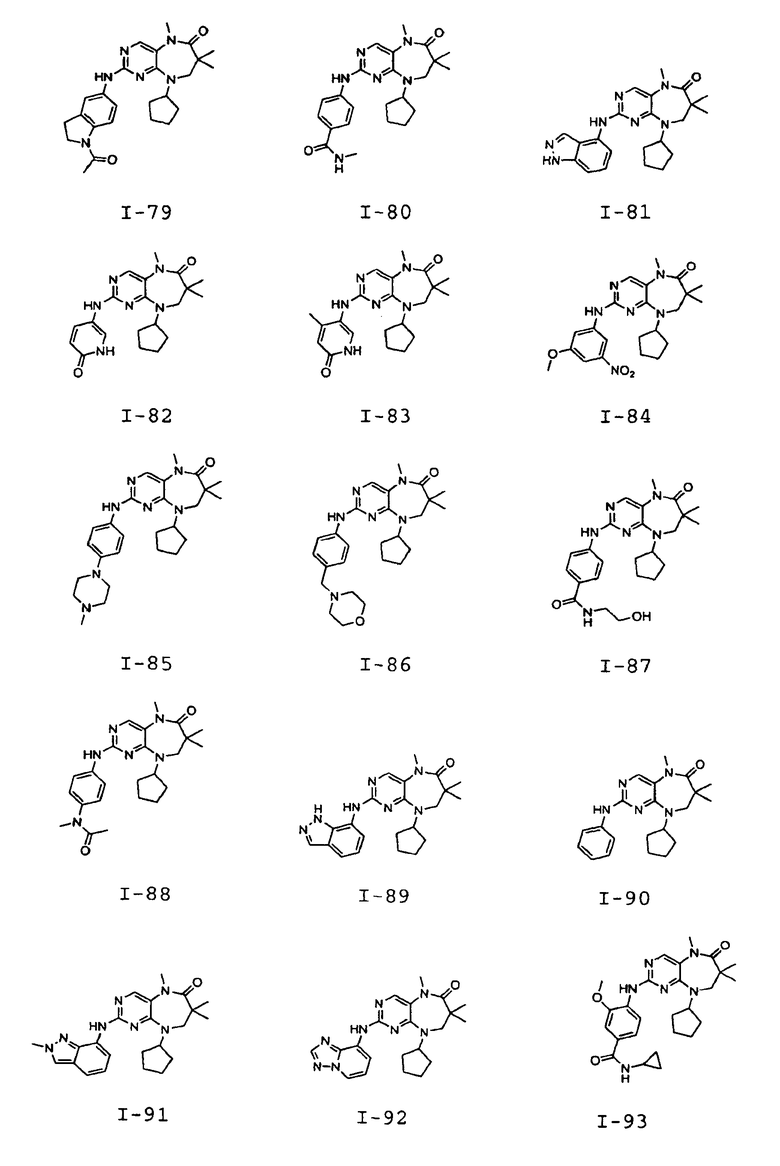
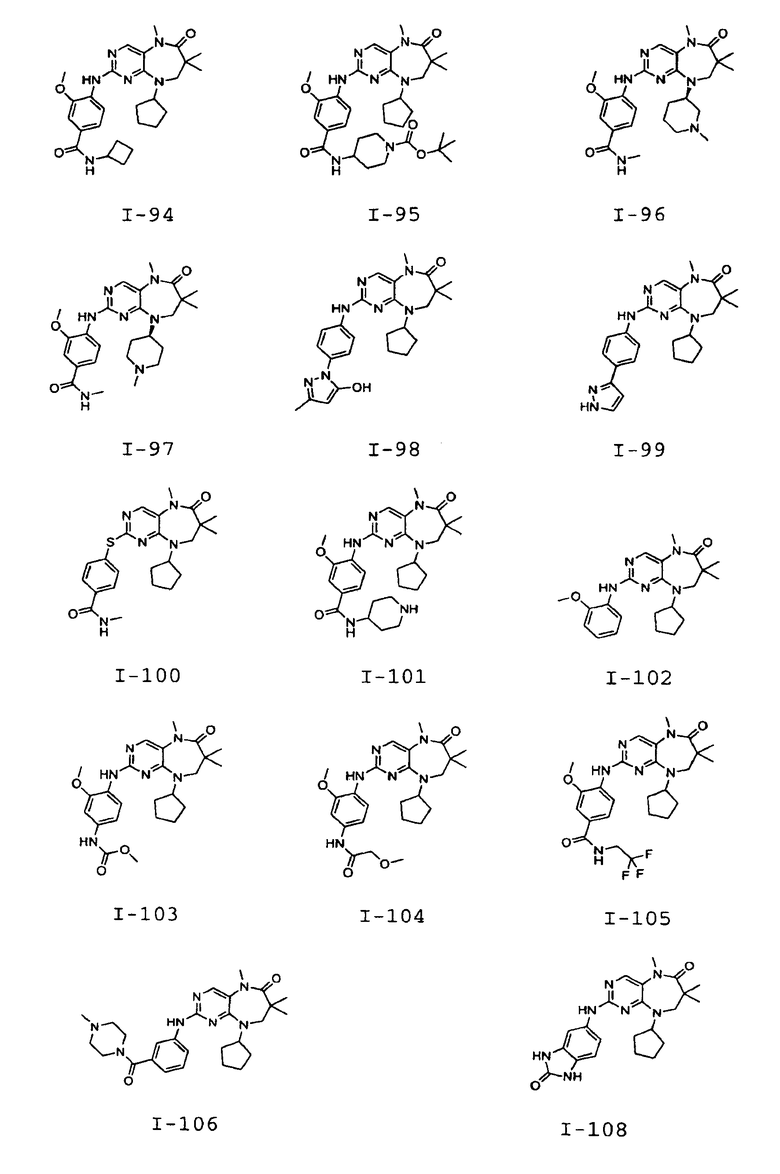
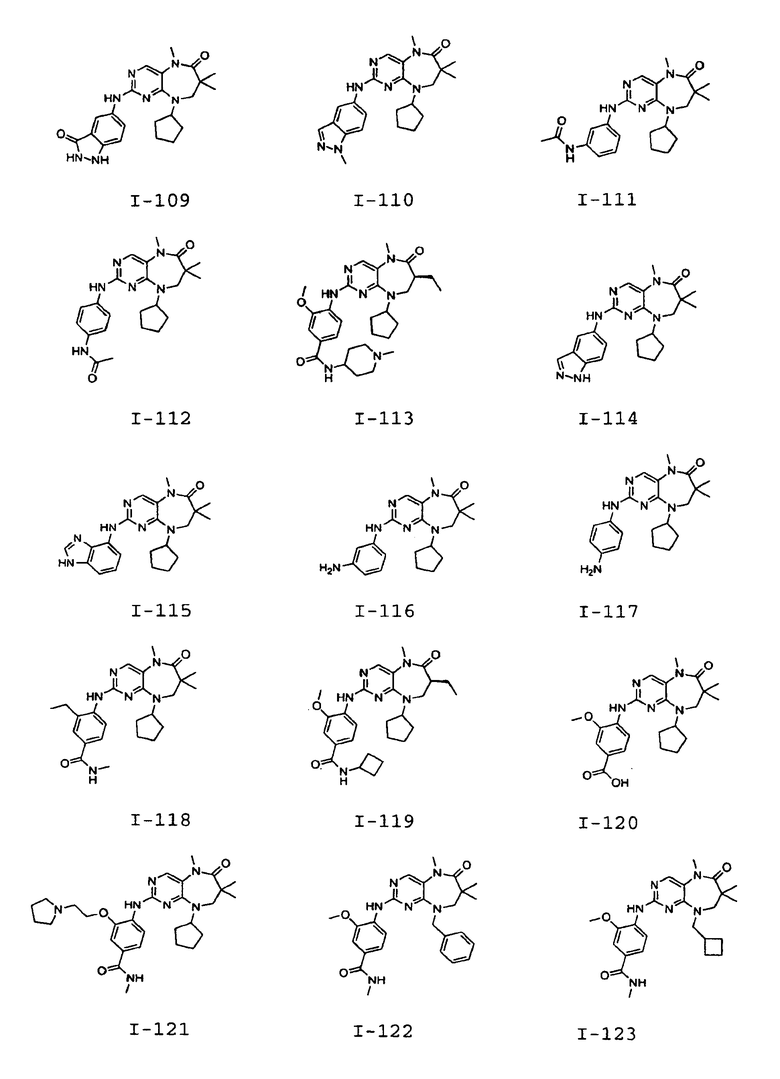
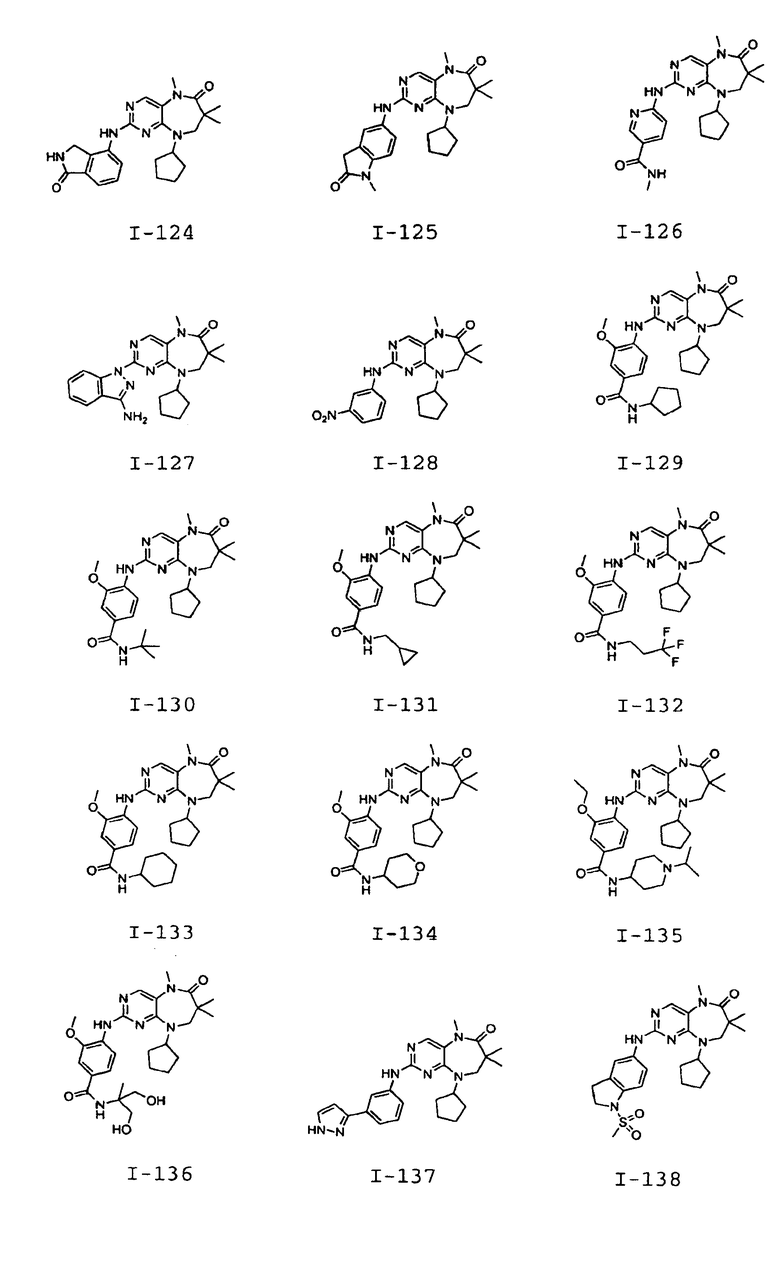
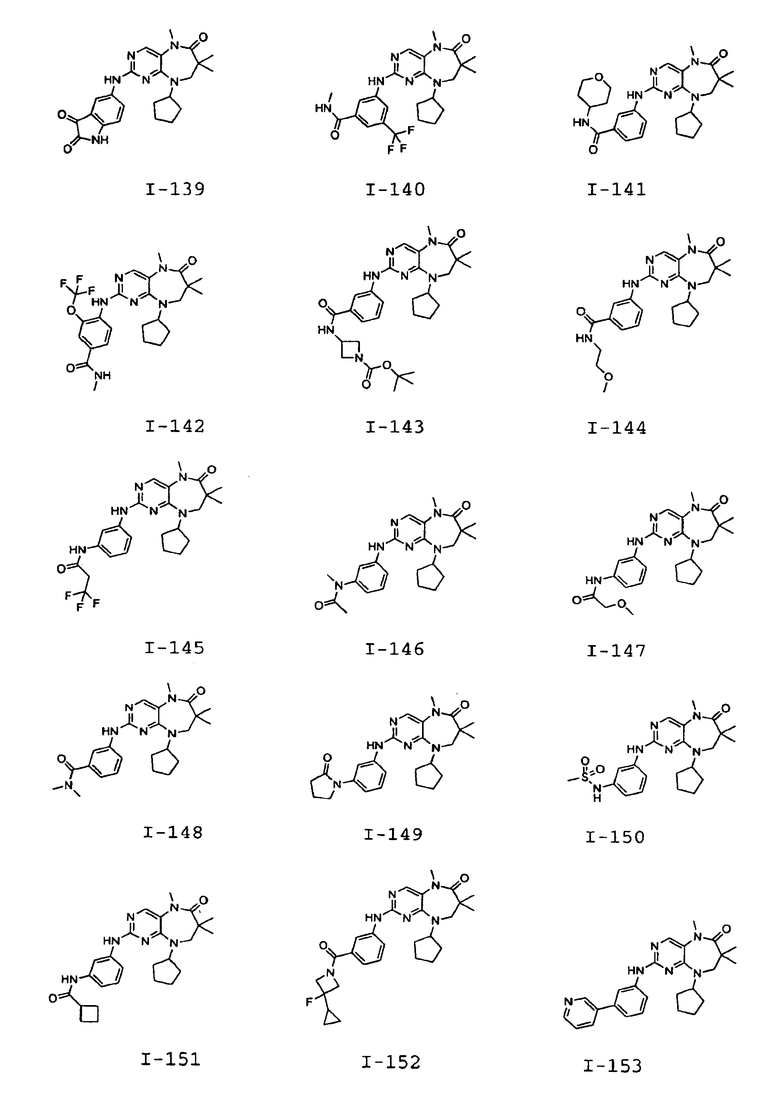
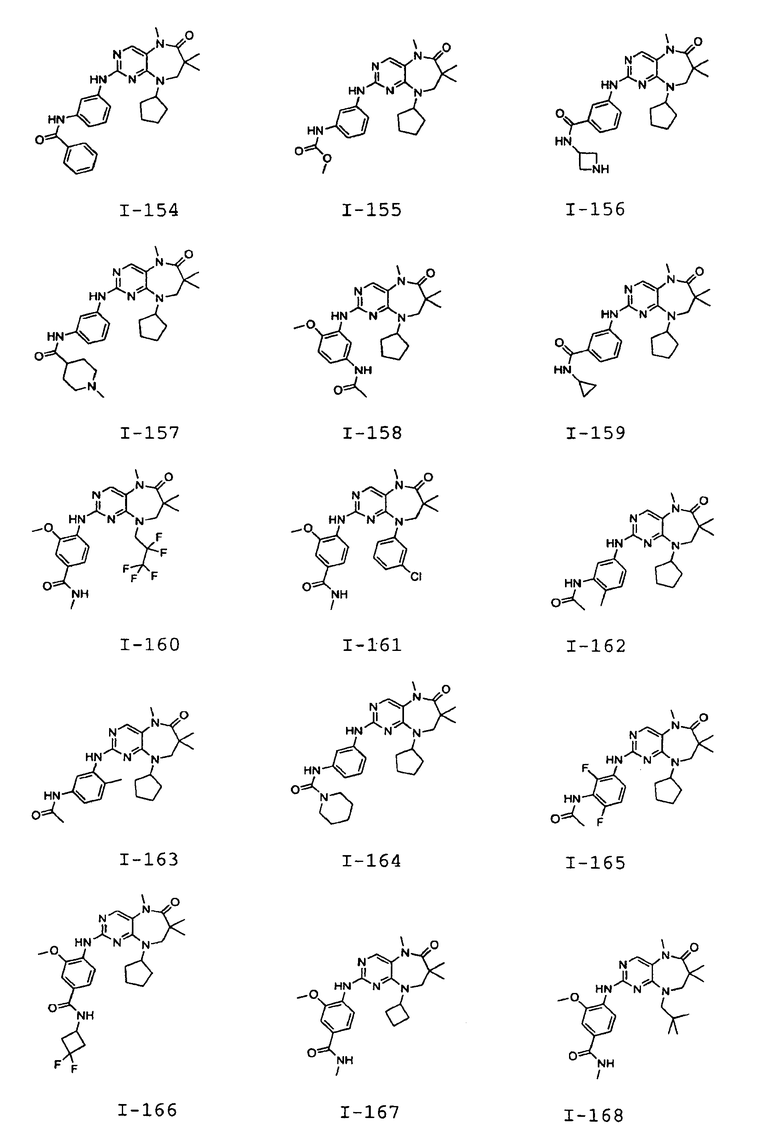
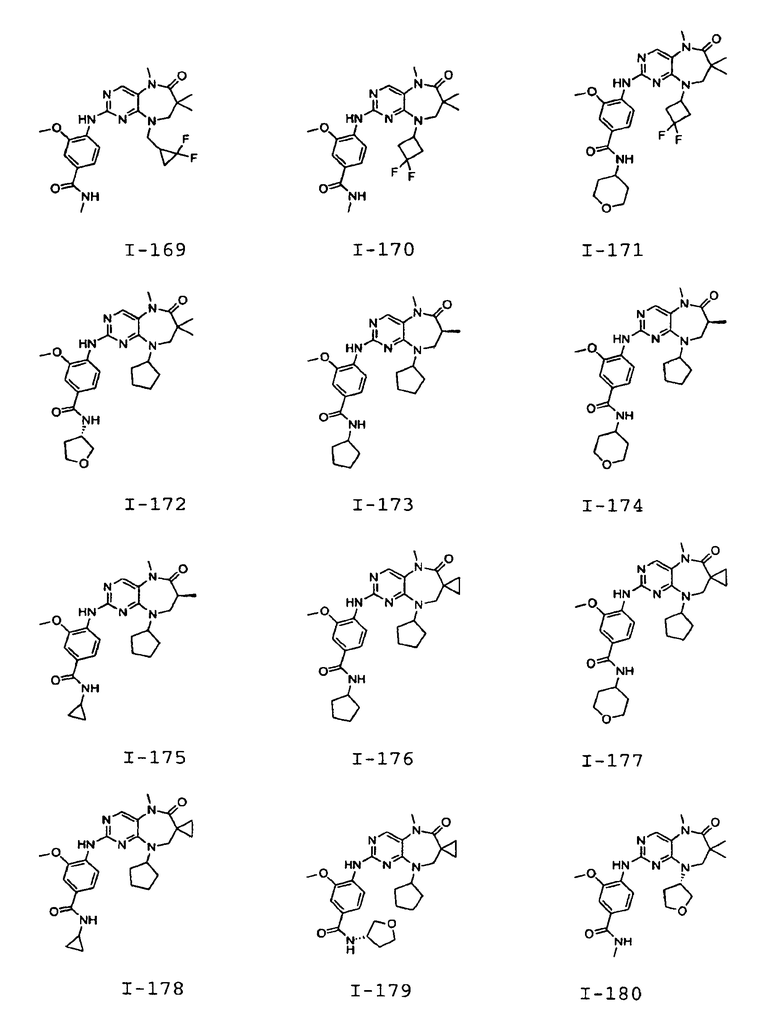
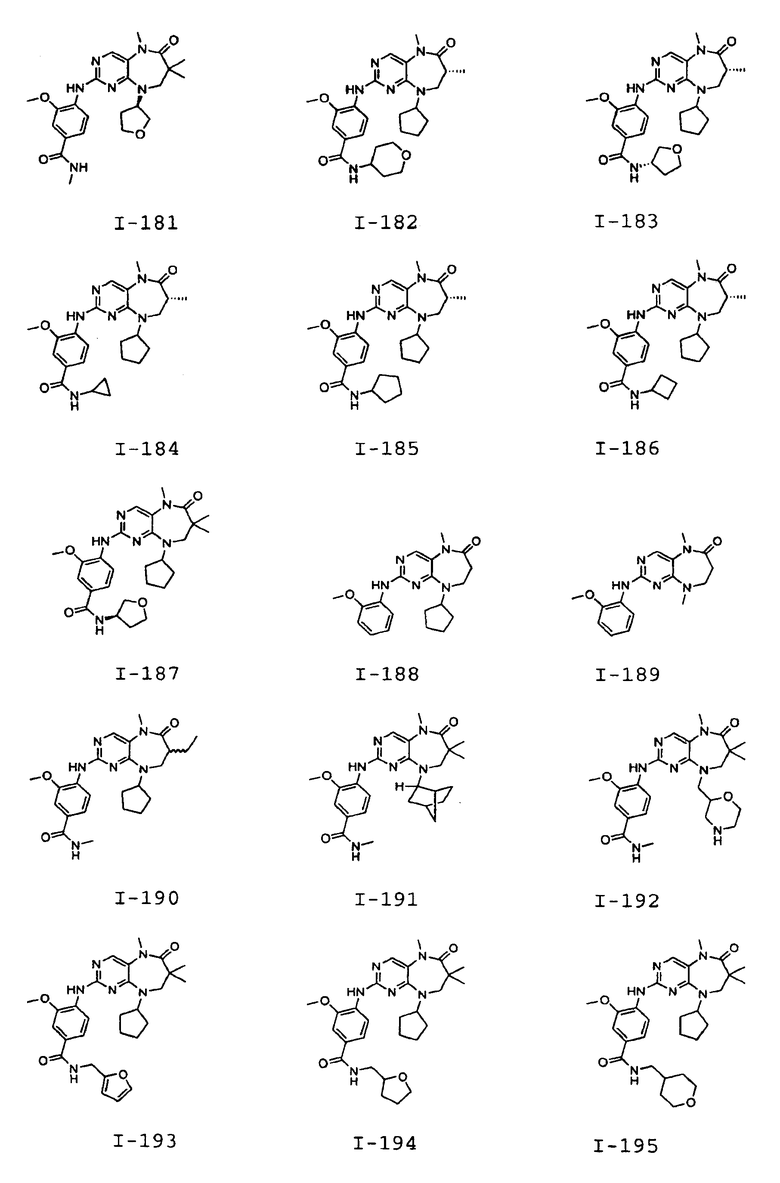
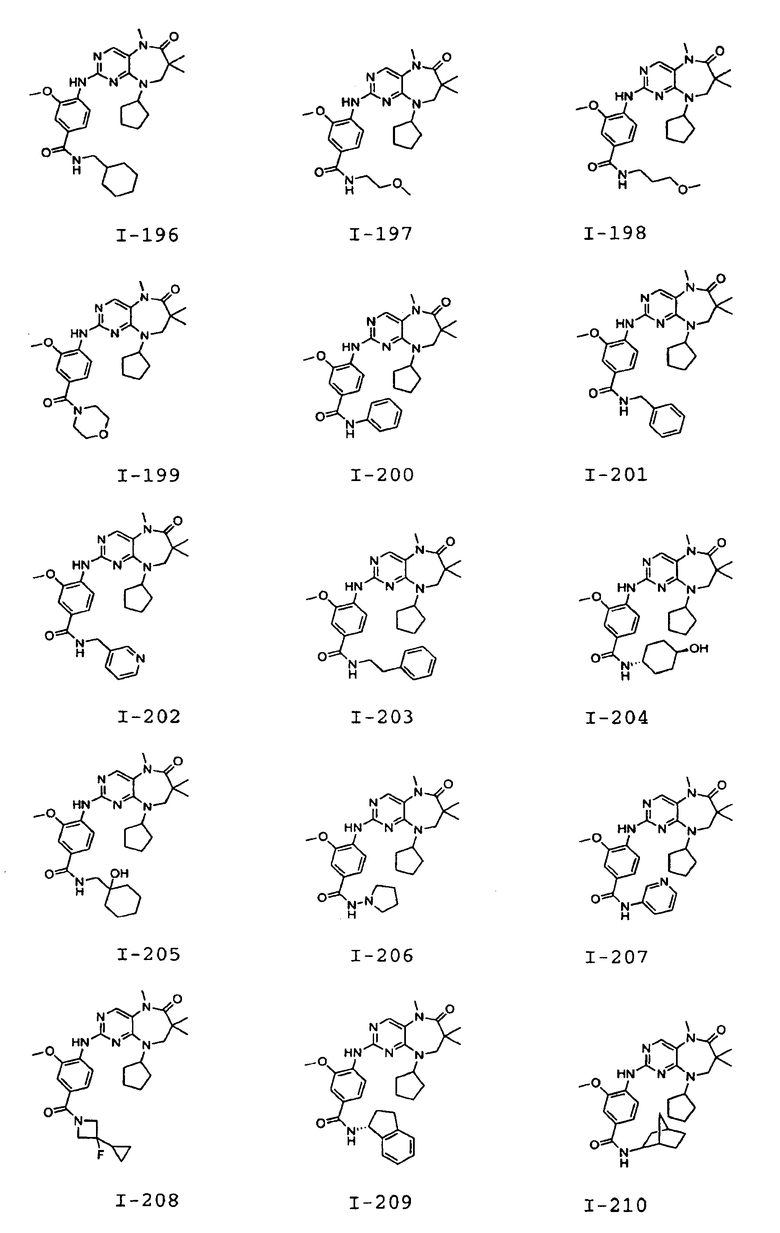
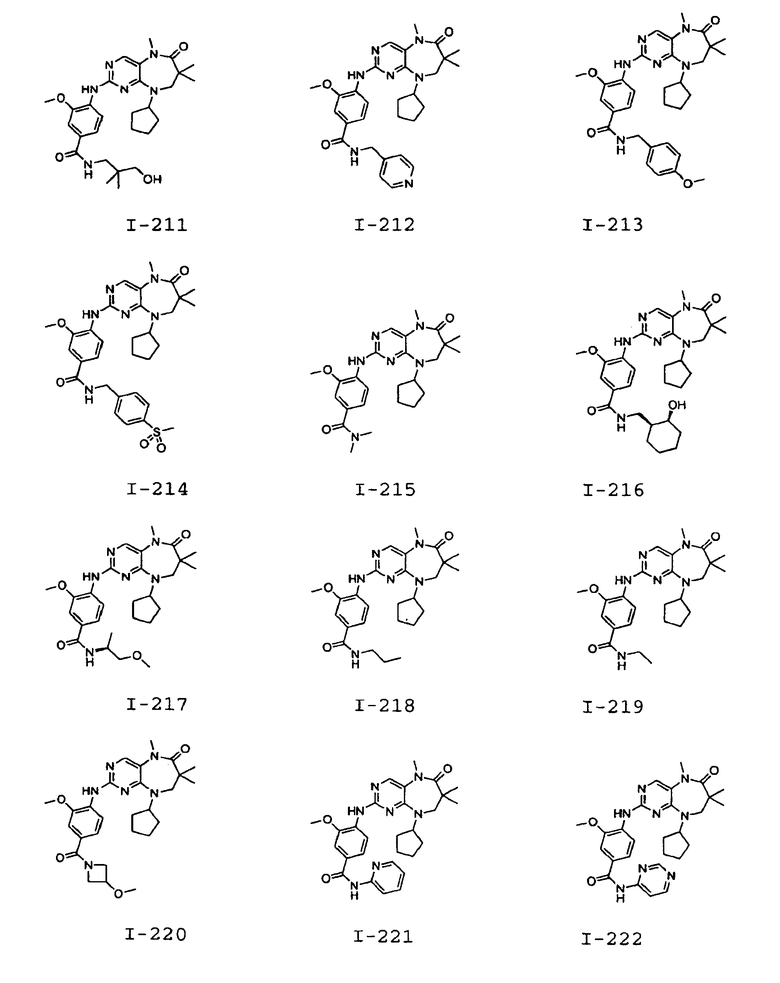
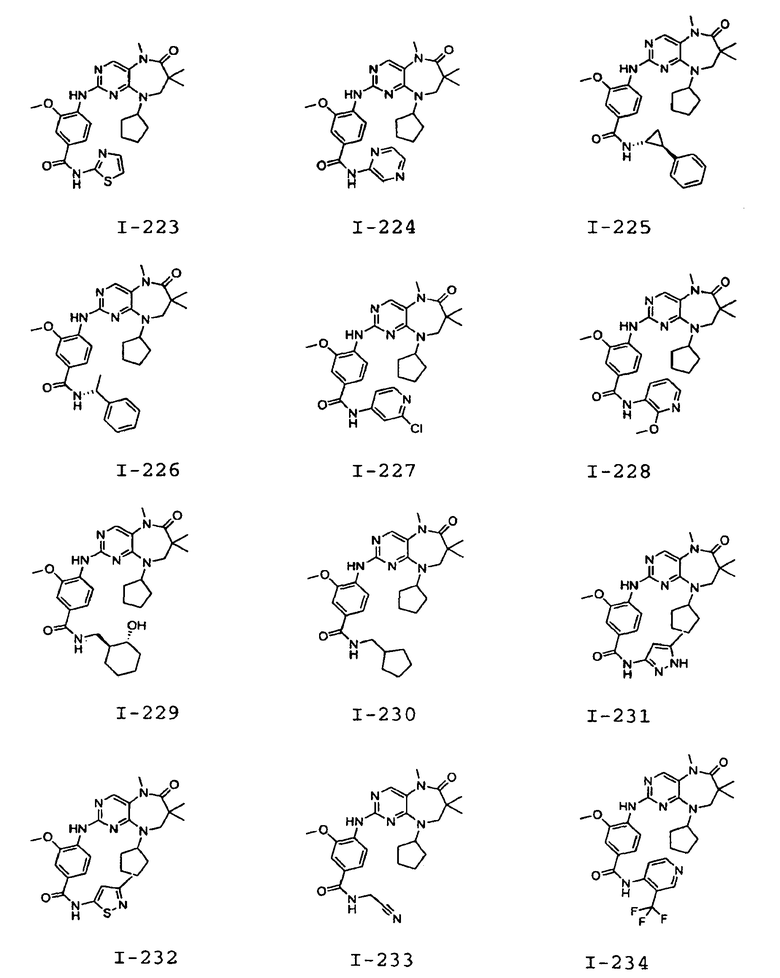
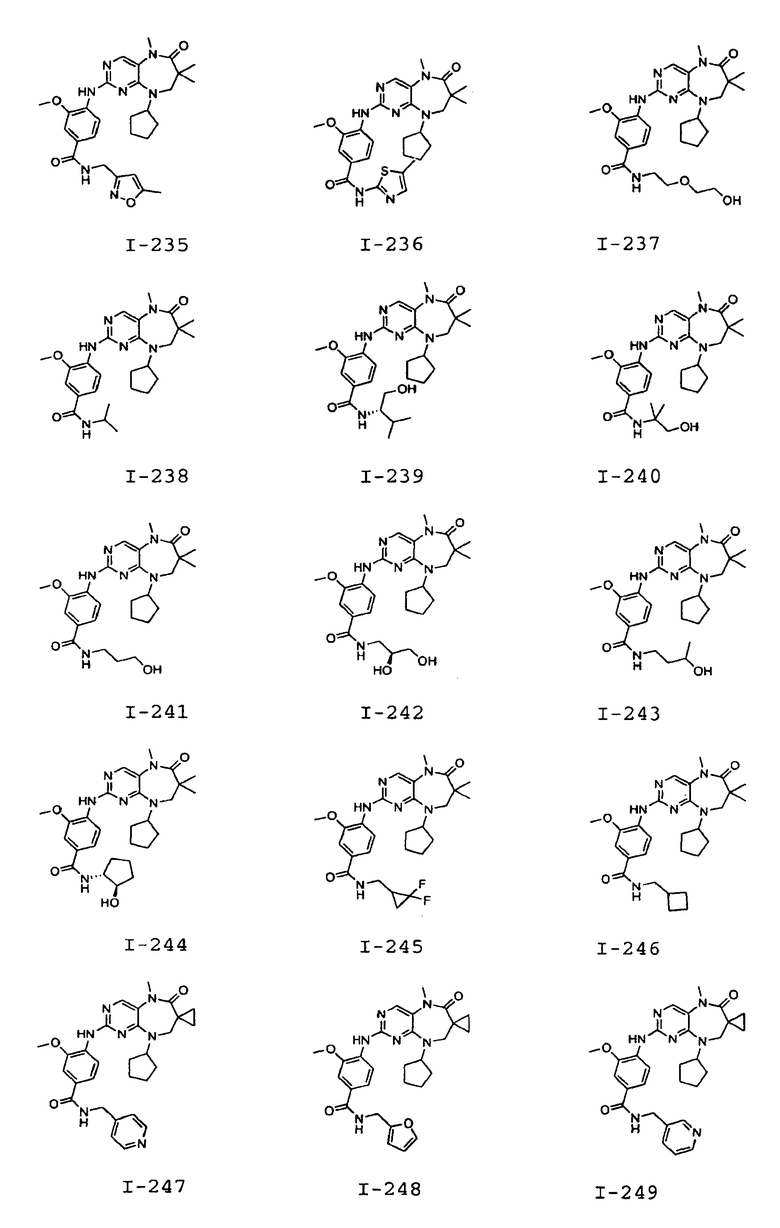
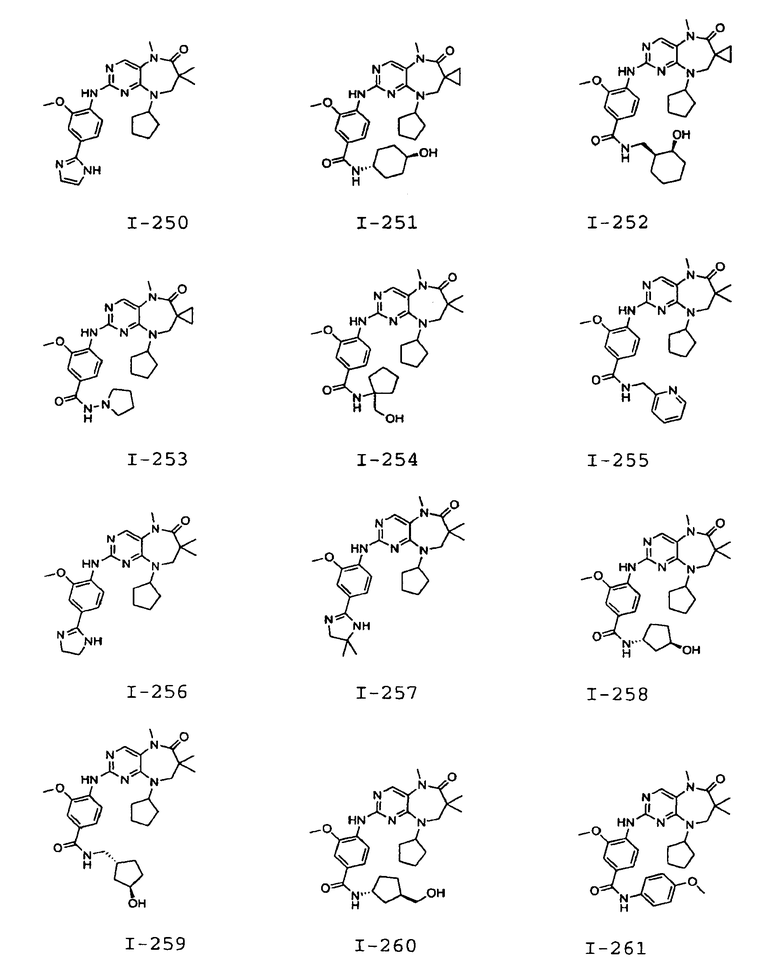
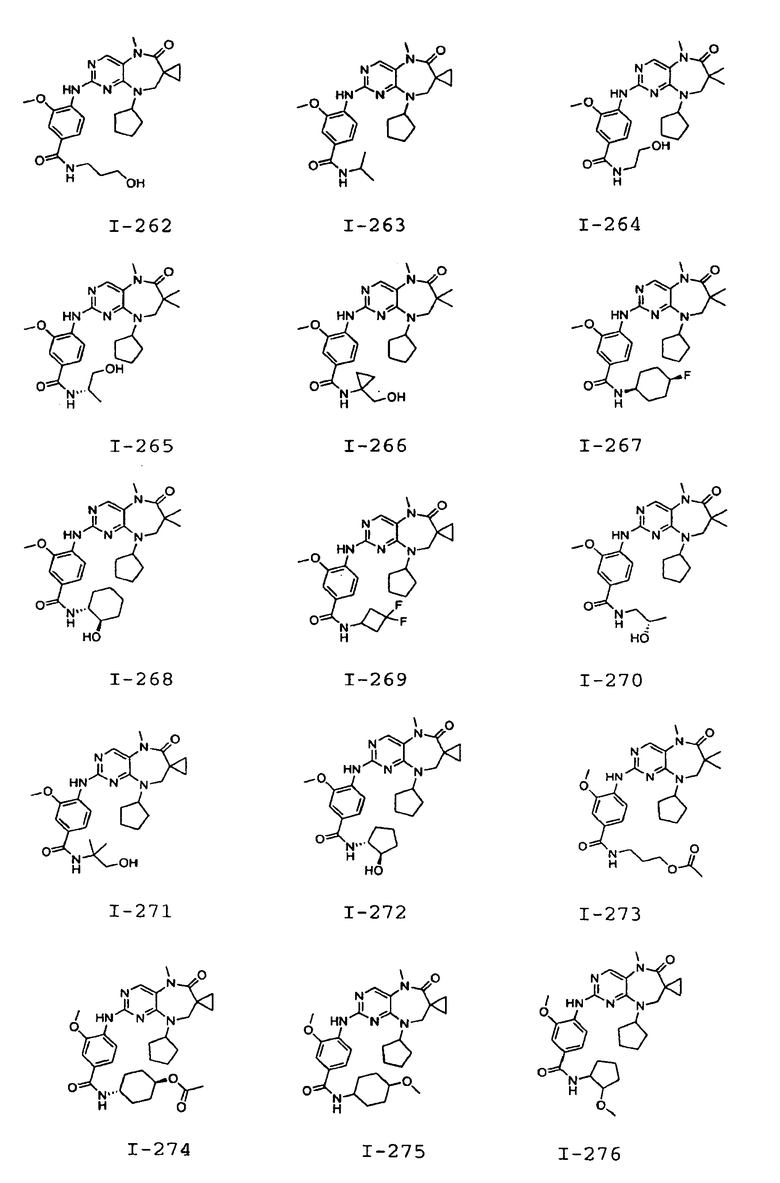
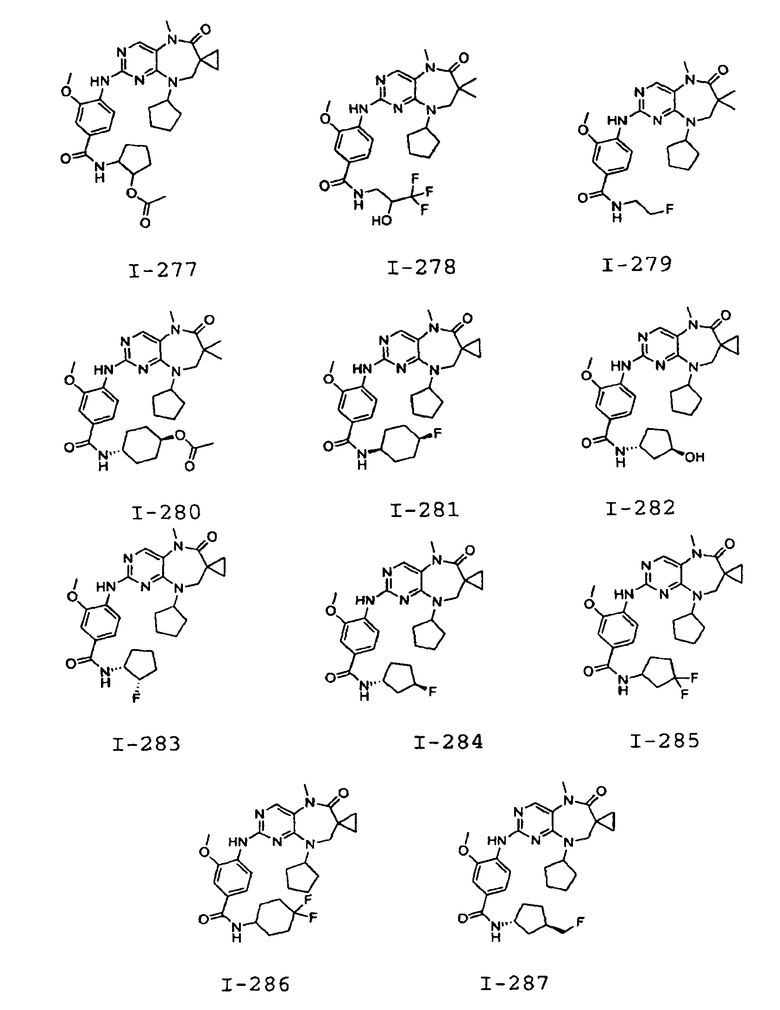
22. Композиция для ингибирования PLK, содержащая соединение по любому одному из пп.1-21 и фармацевтически приемлемые носитель, адъювант или среду.
23. Способ ингибирования активности протеинкиназы у пациента или в биологическом образце, включающий введение указанному пациенту или приведение в контакт указанного биологического образца с
а) композицией по п.22; или
b) соединения по любому одному из пп.1-21.
24. Способ по п.23, где указанная протеинкиназа представляет собой PLK.
25. Способ по п.24, где указанная протеинкиназа представляет собой PLK1.
26. Способ получения соединения формулы I:
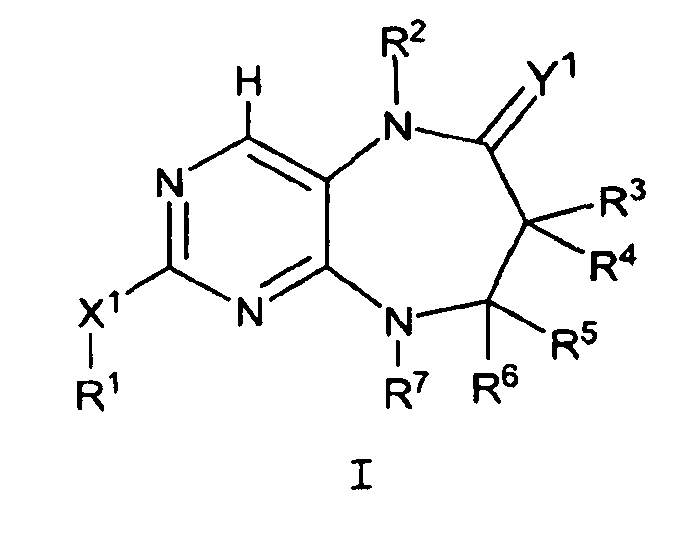
где Y1 обозначает О, а X1, R1, R2, R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21;
включающий в себя взаимодействие соединения формулы 5;
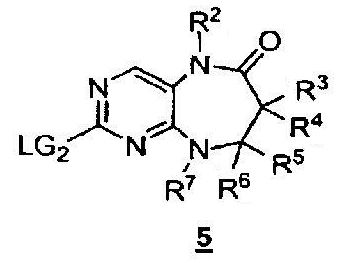
где R2, R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21, a LG2 обозначает галоген; с Х1R1 в условиях катализируемой палладием реакции присоединения с получением соединения формулы I.
27. Способ по п.26, дополнительно включающий в себя стадию взаимодействия соединения формулы 4:
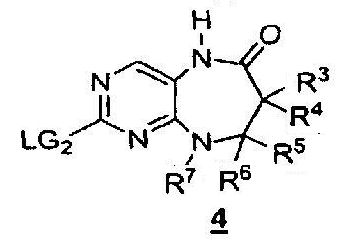
где R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21, a LG2 обозначает галоген;
с R2-LG3, где LG3 представляет собой уходящую группу, способную замещаться NH-амидом; с получением соединения формулы 5.
28. Способ по п.27, дополнительно включающий в себя циклизацию соединения формулы 3-а;
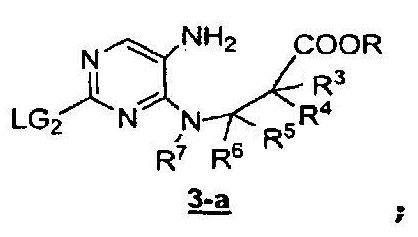
где LG2 обозначает галоген, a R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21; в условиях циклоконденсации с получением соединения формулы 4.
29. Способ по п.28, дополнительно включающий в себя стадию взаимодействия соединения формулы 3:
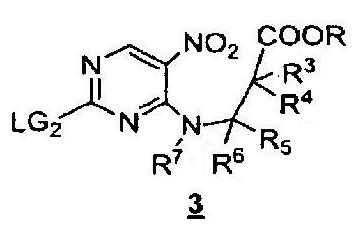
где LG2 обозначает галоген, a R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21; в условиях восстановления с получением соединения формулы 3-а.
30. Способ по п.28, дополнительно включающий в себя а) функционализацию аминогруппы соединения формулы 3-а с получением соединения формулы 3-b;
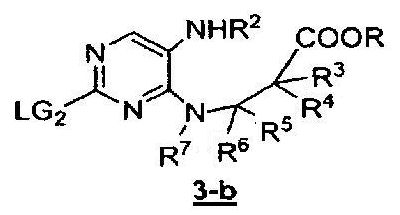
где LG2 обозначает галоген, a R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21;
b) циклизацию соединения формулы 3-b в условиях циклоконденсации с получением соединения формулы 4.
31. Способ по п.29, дополнительно включающий в себя взаимодействие соединения формулы 2:
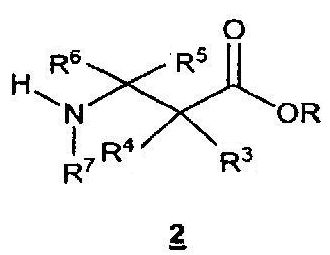
где R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21; с соединением формулы 1:
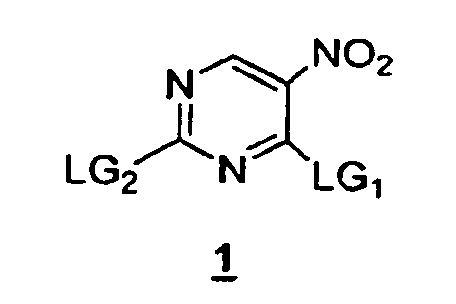
где каждый из LG1 и LG2 независимо обозначает галоген; с получением соединения формулы 3.
32. Способ получения соединение формулы I:
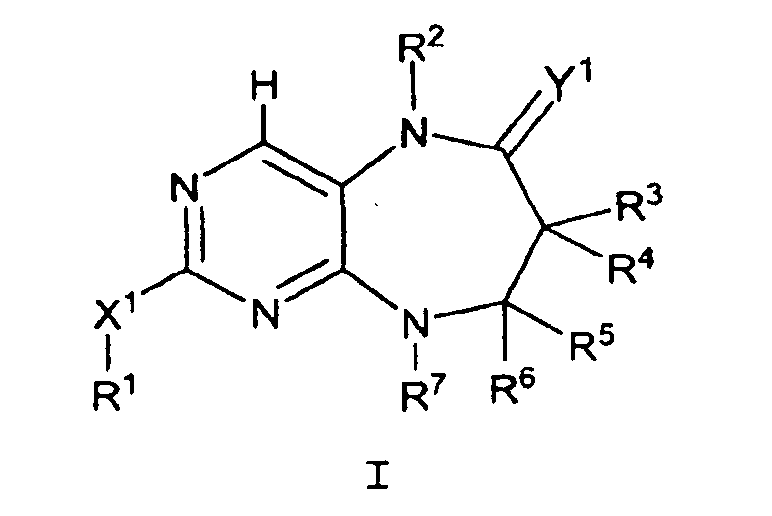
где Y1 обозначает NR9, a X1, R1, R2, R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21; включающий в себя взаимодействие соединения формулы I, где Y1 обозначает О, а X1, R1, R2, R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21; с соединением, имеющем формулу NH-R9, с получением соединения формулы I, где Y1 обозначает NR9.
33. Способ получения соединения формулы 5-а:
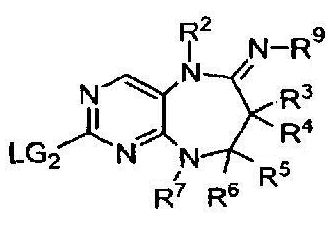
где LG2 обозначает галоген, a R2, R3, R4, R5, R6, R7 и R9 имеют определения по любому одному из пп.1-21; включающий в себя взаимодействие соединения формулы 5
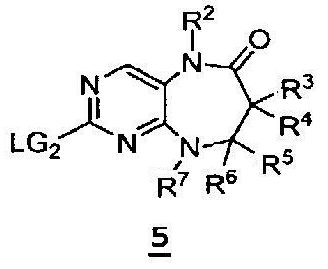
где LG2 обозначает галоген, a R2, R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21; с соединением, имеющем формулу NH-R9, с получением соединения формулы 5-а.
34. Способ по п.33, дополнительно включающий в себя замену LG2 на Х1R1 с получением соединения формулы I, где Y1 обозначает NR9, а X1, R1, R2, R3, R4, R5, R6 и R7 имеют определения по любому одному из пп.1-21.
| СТЕНД ДЛЯ ИСПЫТАНИЯ ОБРАЗЦОВ НА ПРОЧНОСТЬ | 2009 |
|
RU2418285C1 |
| RU 98117798 A, 10.10.2000. | |||
Авторы
Даты
2013-02-20—Публикация
2007-02-13—Подача