Текст описания приведен в факсимильном виде.



























































































































































































| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ, СТРУКТУРЫ И КОМПОЗИЦИИ ДЛЯ НОСОСЛЕЗНОЙ СИСТЕМЫ | 2007 |
|
RU2413480C2 |
| ИМПЛАНТАТЫ НАЗОЛАКРИМАЛЬНОЙ ДРЕНАЖНОЙ СИСТЕМЫ ДЛЯ МЕДИКАМЕНТОЗНОЙ ТЕРАПИИ | 2007 |
|
RU2414199C2 |
| ВКЛАДЫШИ В СЛЕЗНУЮ ТОЧКУ И СПОСОБЫ ДОСТАВКИ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ | 2008 |
|
RU2459646C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОВЫШЕННОГО ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ С ПОМОЩЬЮ ВНУТРИГЛАЗНОЙ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ | 2014 |
|
RU2664686C2 |
| ВНУТРИГЛАЗНЫЕ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ И СПОСОБЫ ЛЕЧЕНИЯ ГЛАЗНЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2532333C2 |
| СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА ВНУТРЬ ГЛАЗА | 2007 |
|
RU2440102C2 |
| СПОСОБ ПРОИЗВОДСТВА ОФТАЛЬМОЛОГИЧЕСКИХ ЛИНЗ, ОСНАЩЕННЫХ ПАССИВНОЙ СИСТЕМОЙ ОКРАШИВАНИЯ НА ОСНОВЕ СОБЫТИЙ | 2014 |
|
RU2642551C2 |
| ВНУТРИКАМЕРНЫЕ ИМПЛАНТАТЫ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ ТЕРАПЕВТИЧЕСКОГО АГЕНТА | 2011 |
|
RU2565445C2 |
| СНИЖЕНИЕ ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ ПРИ ПОМОЩИ ВНУТРИКАМЕРНЫХ ИМПЛАНТАТОВ БИМАТОПРОСТА | 2011 |
|
RU2586298C2 |
| УСТРОЙСТВО ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ВИДИМОЕ В РЕНТГЕНОВСКИХ ЛУЧАХ | 2005 |
|
RU2384347C2 |
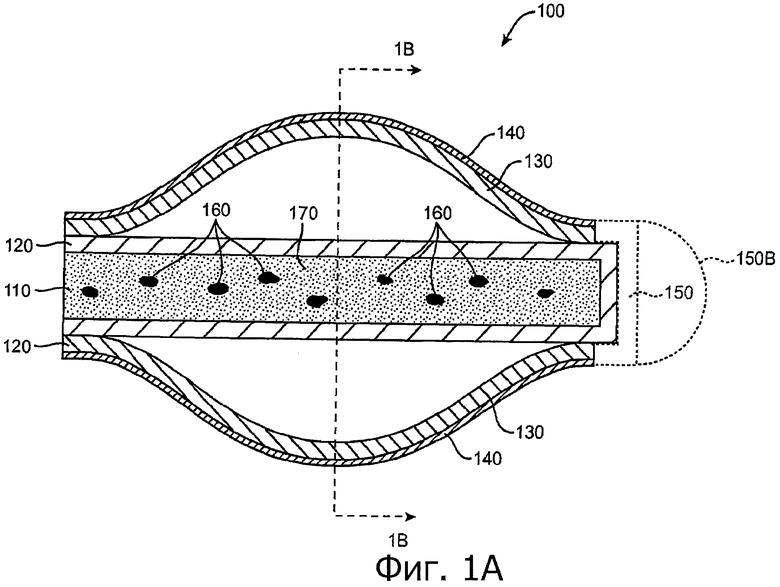
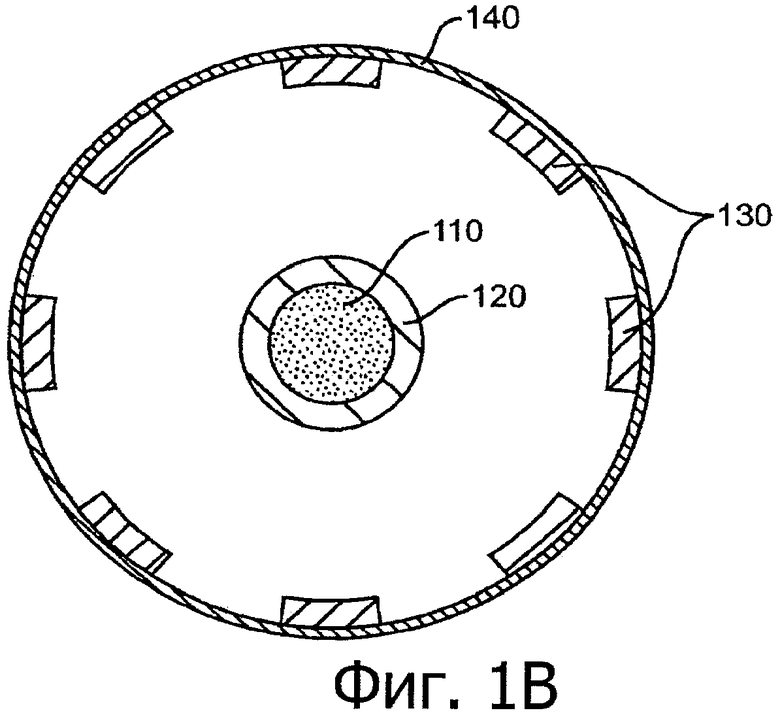
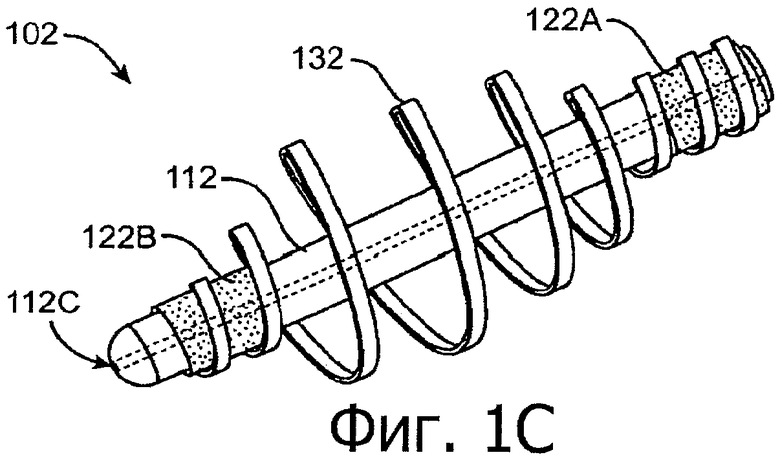
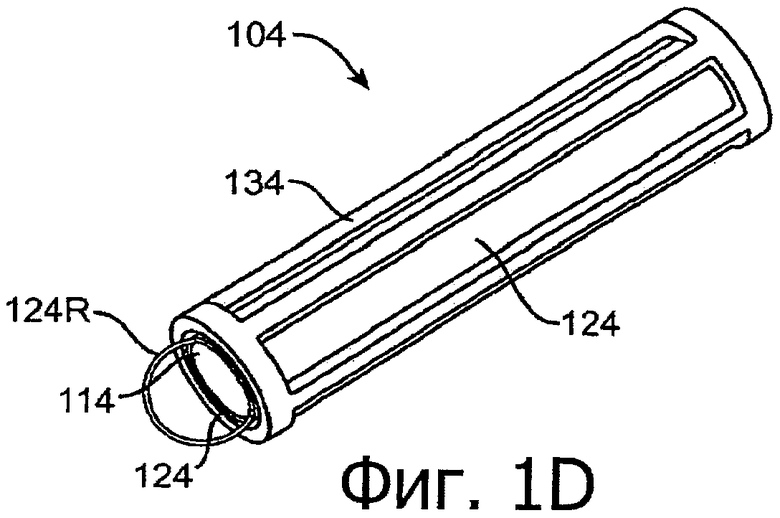
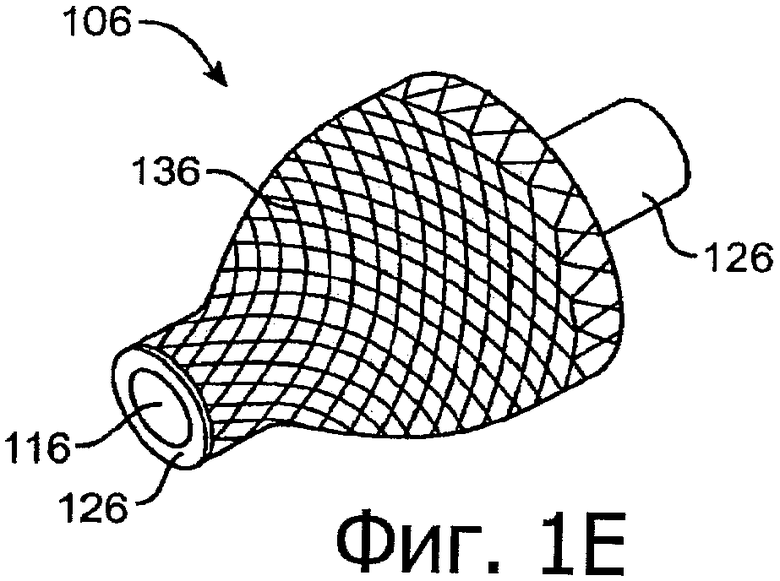
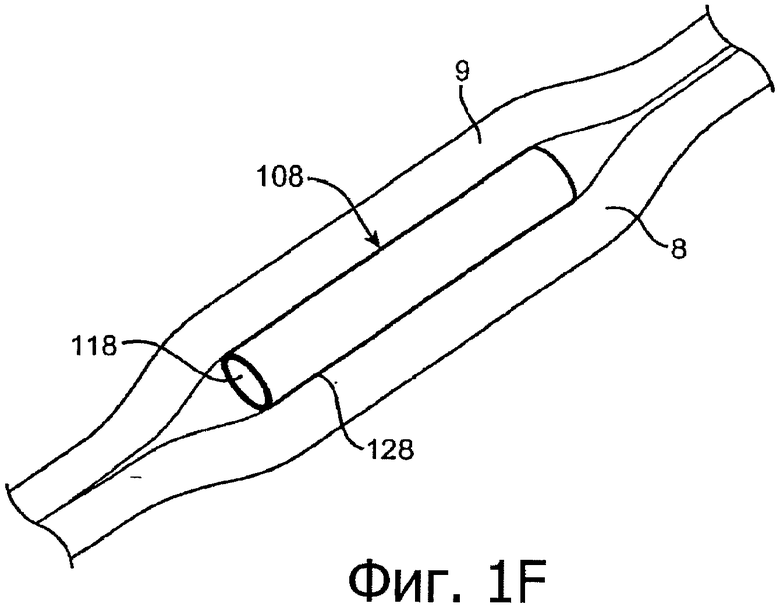
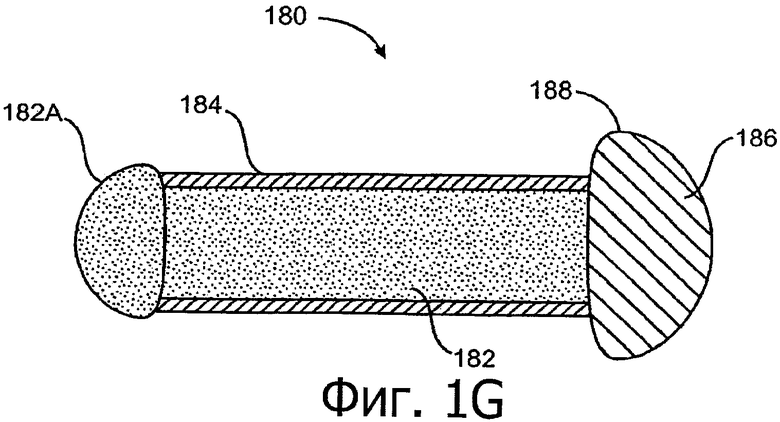
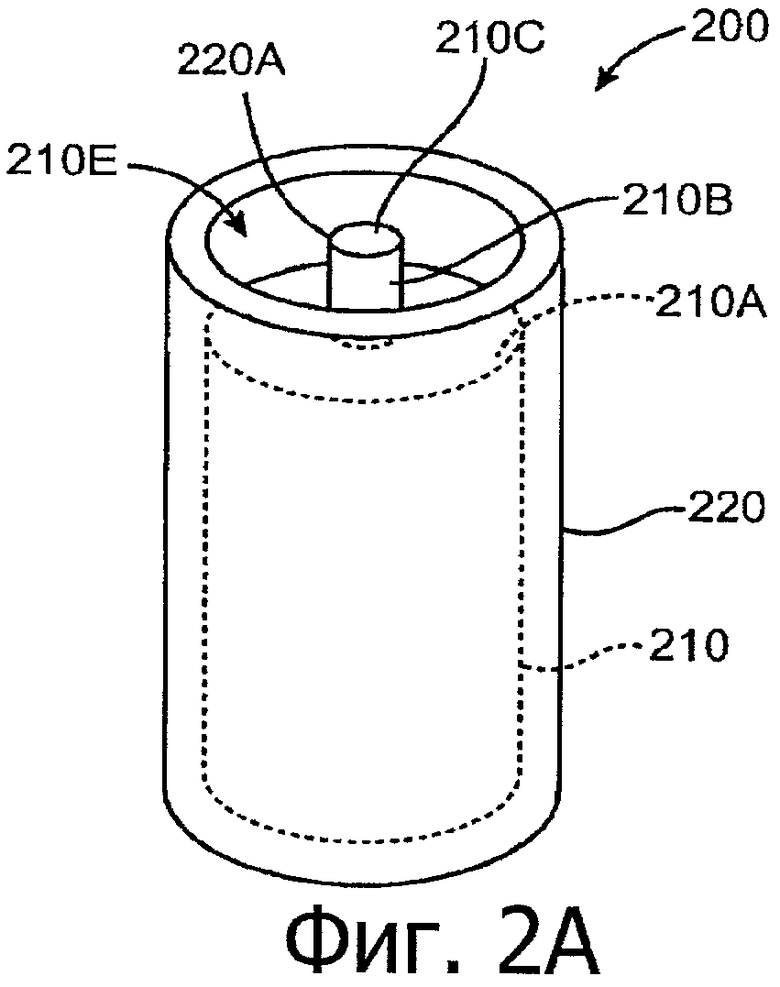
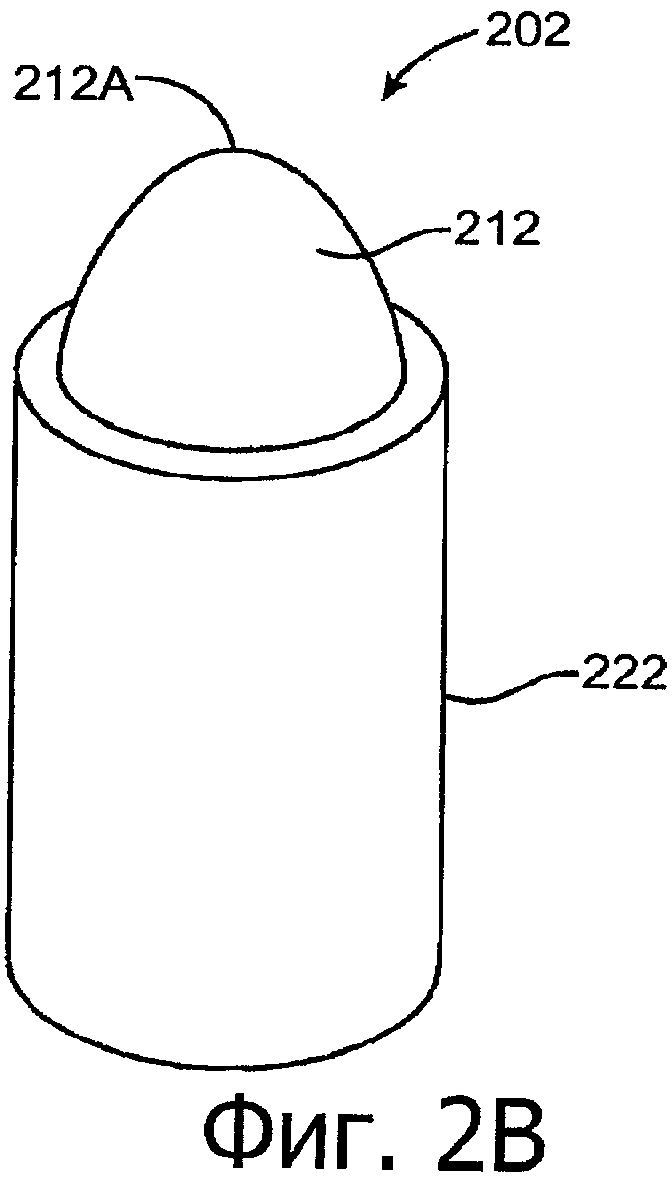
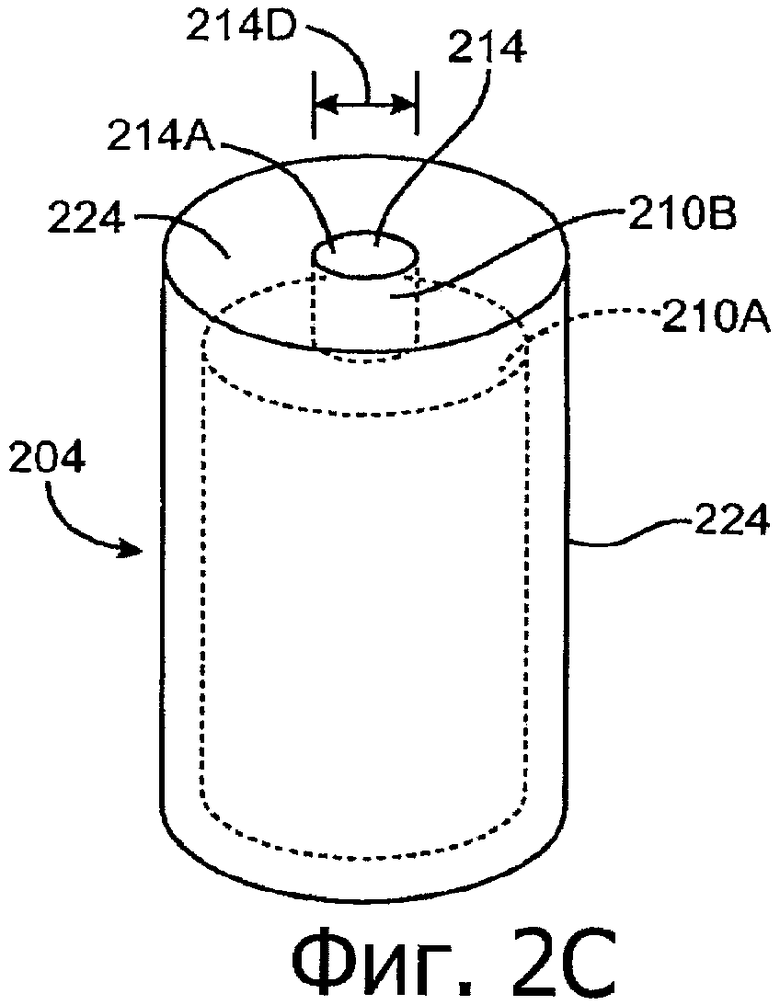
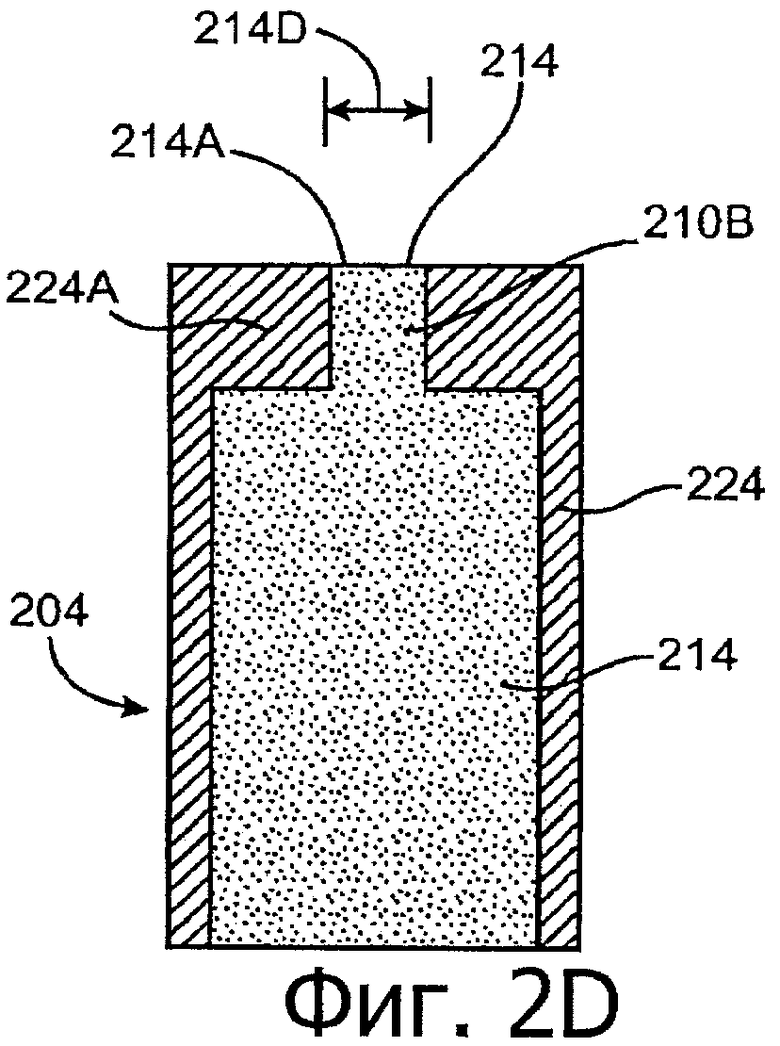
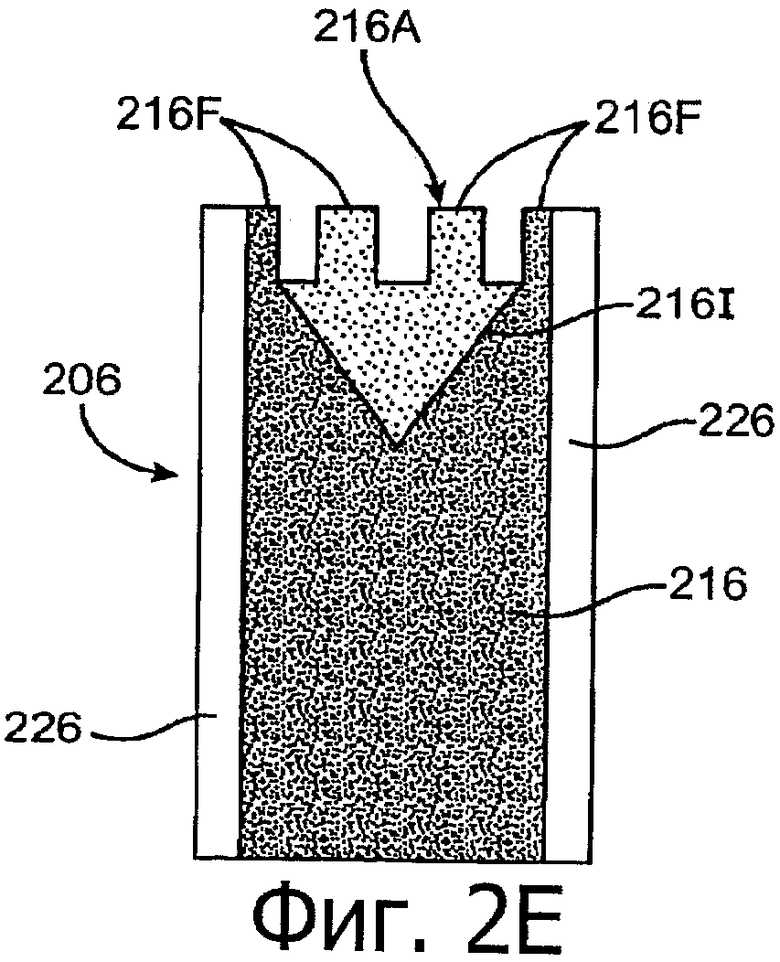
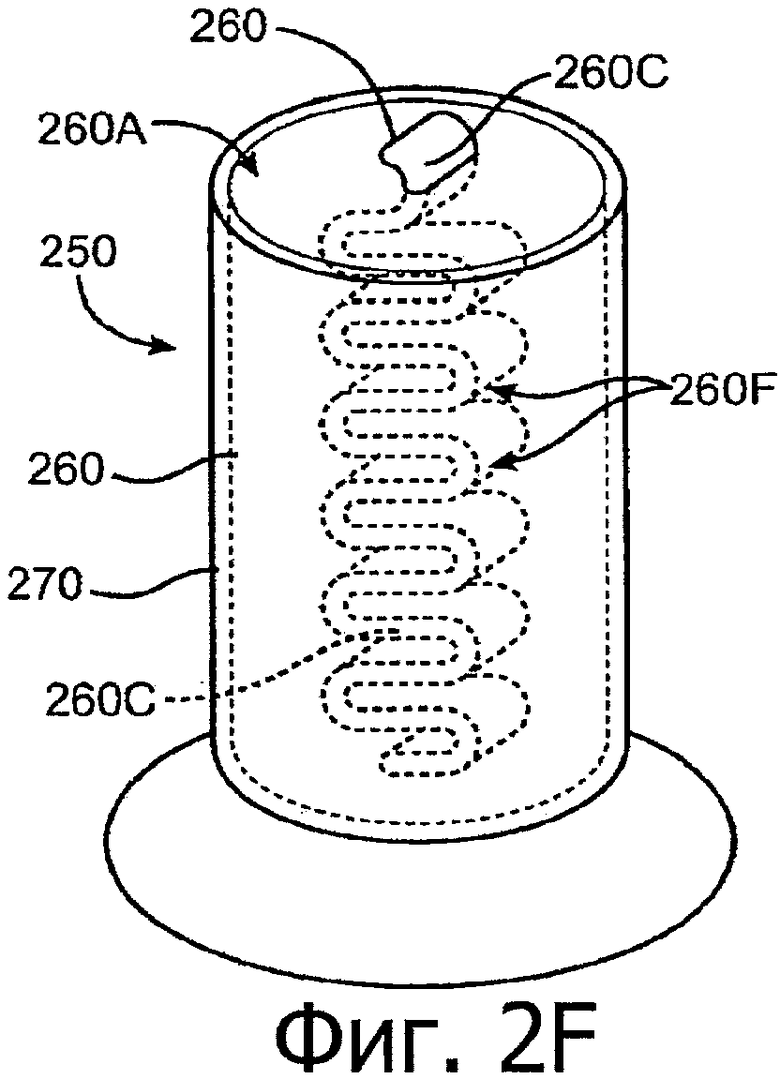
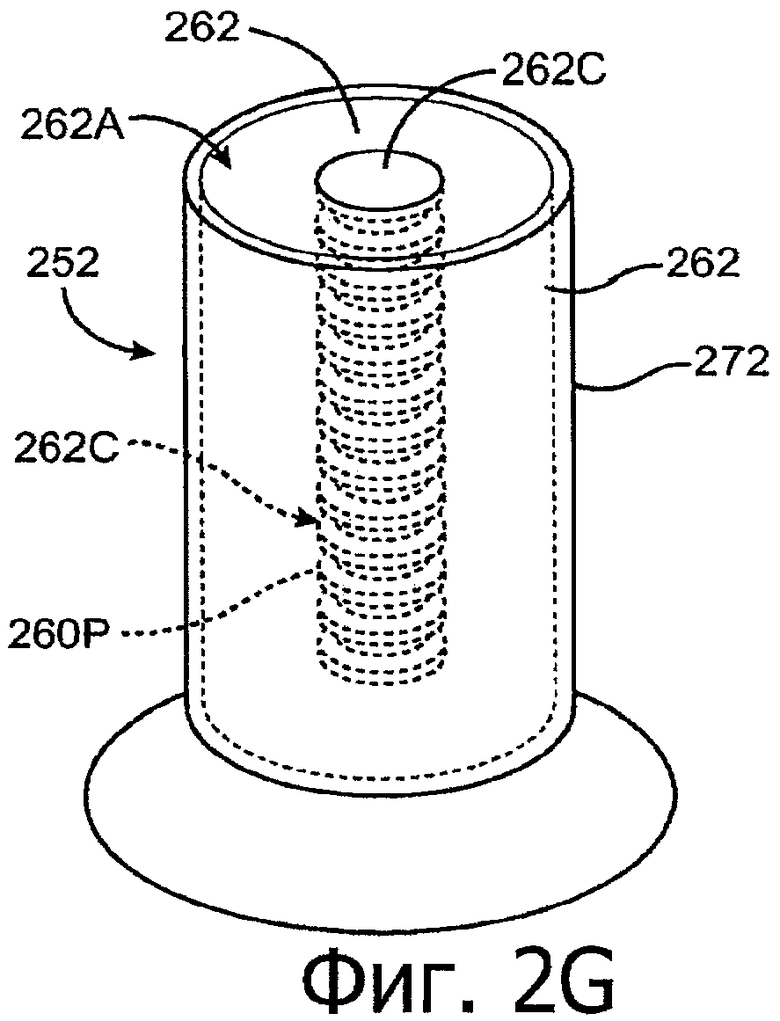
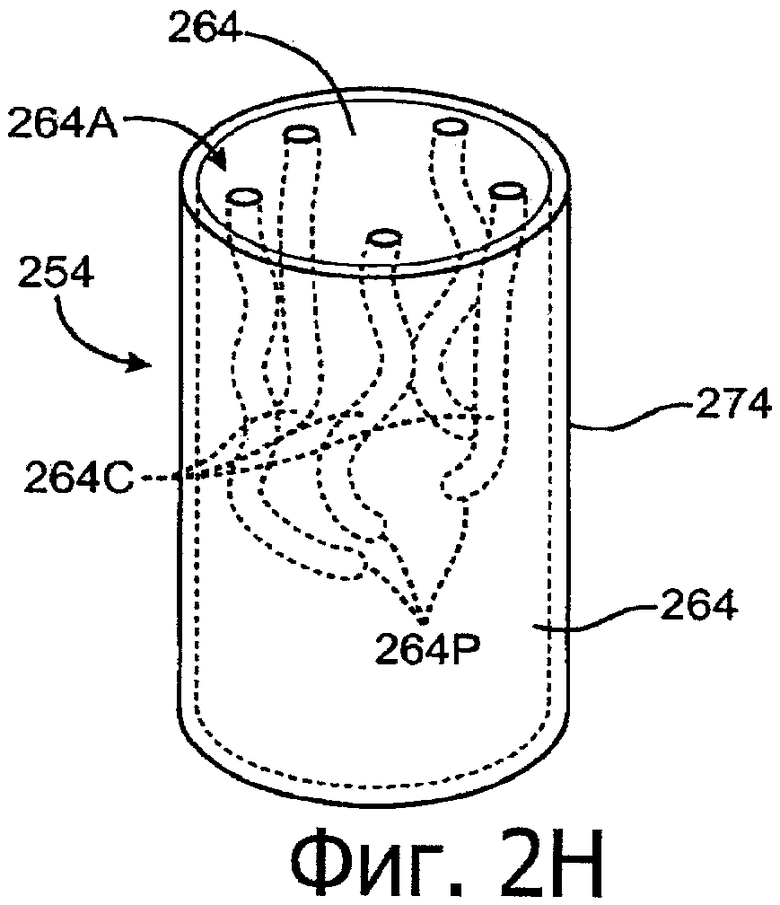
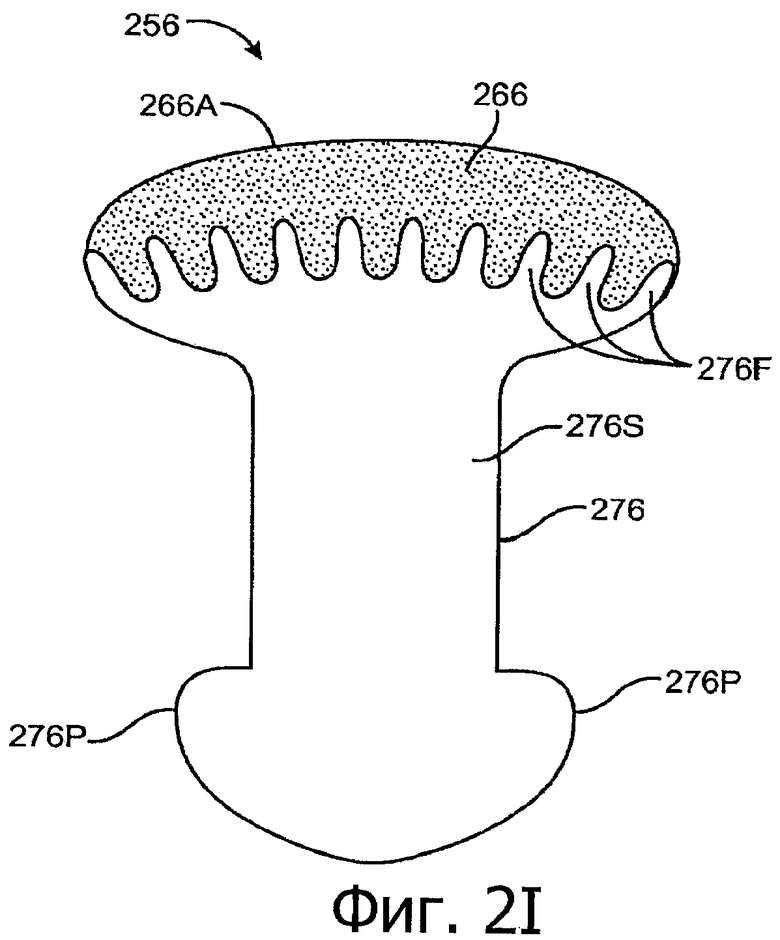
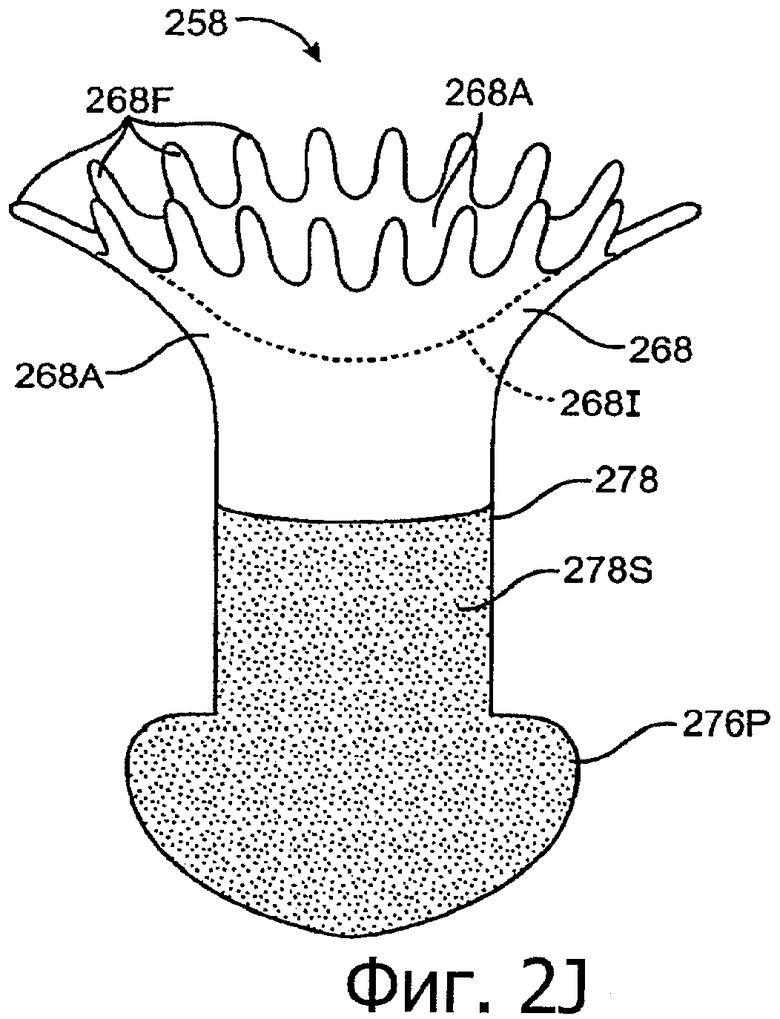
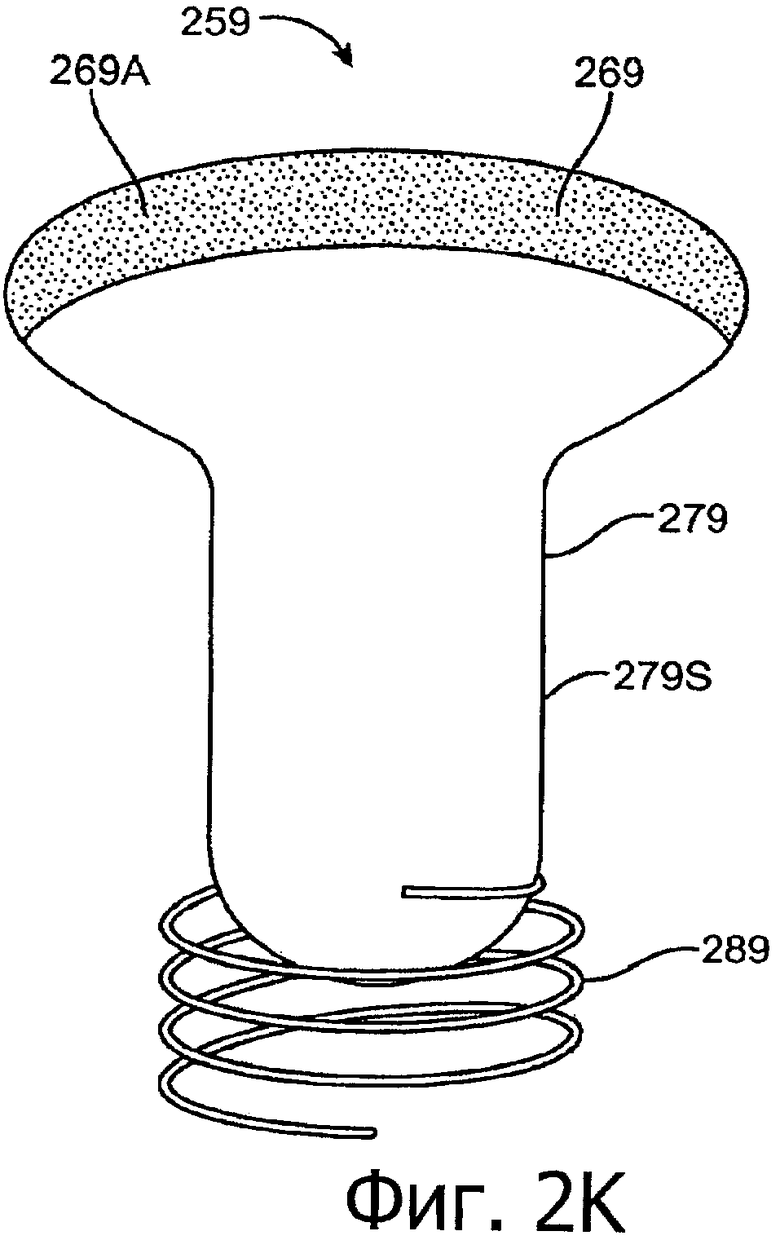
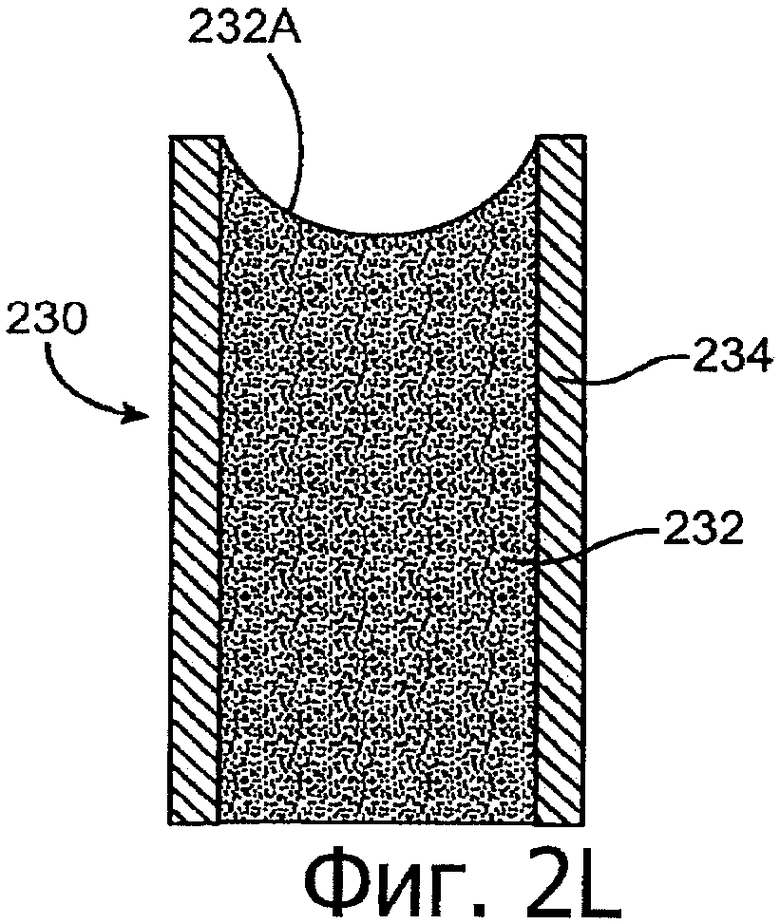
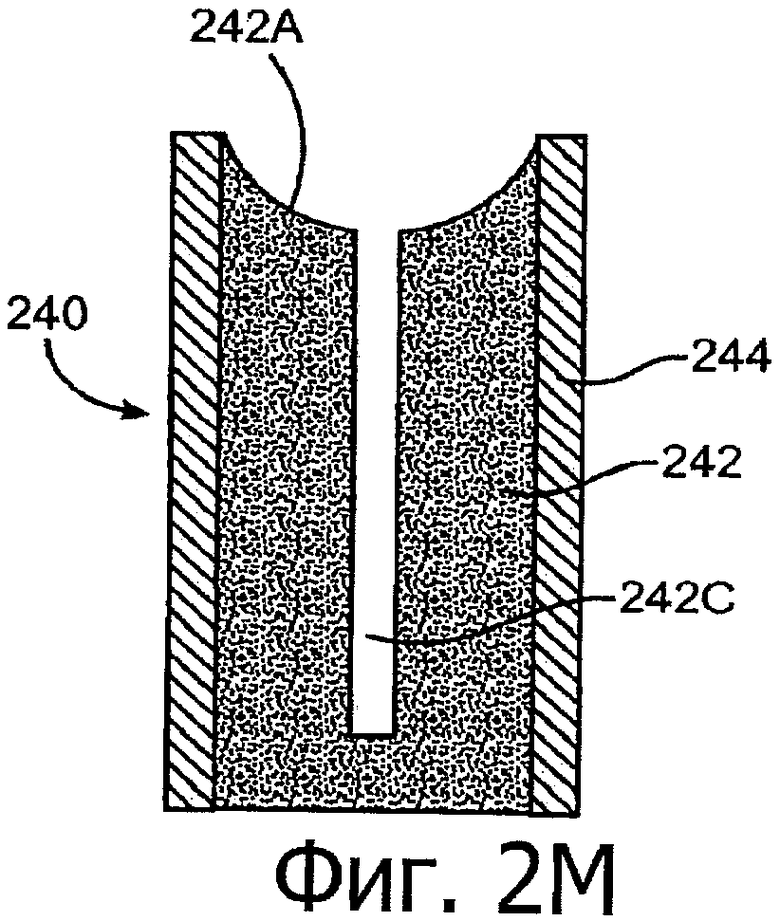
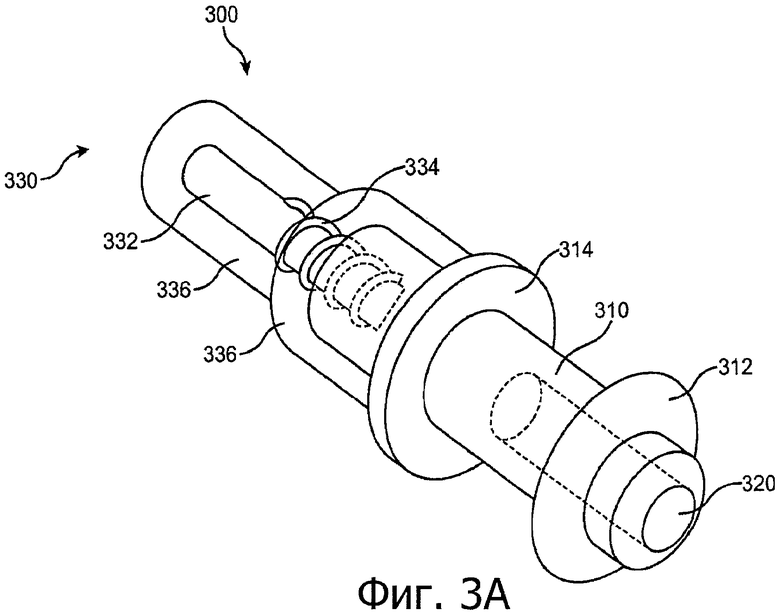
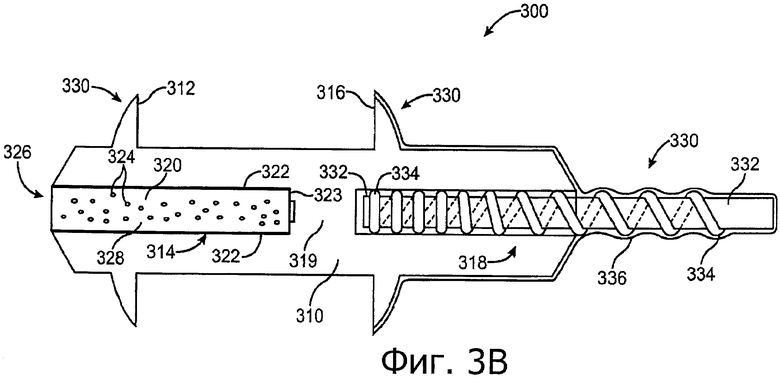
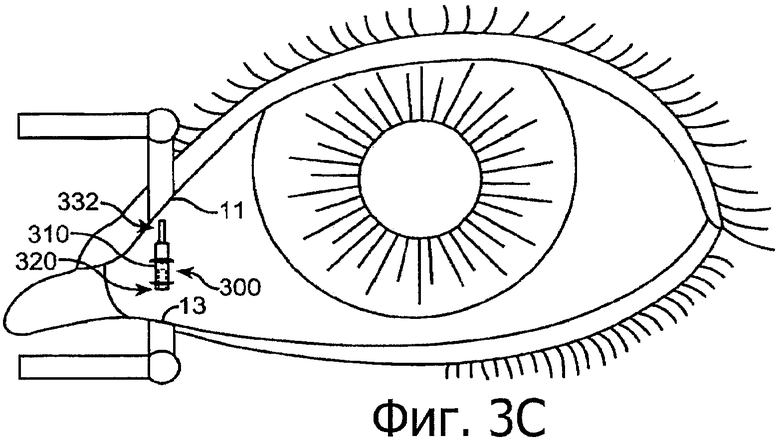
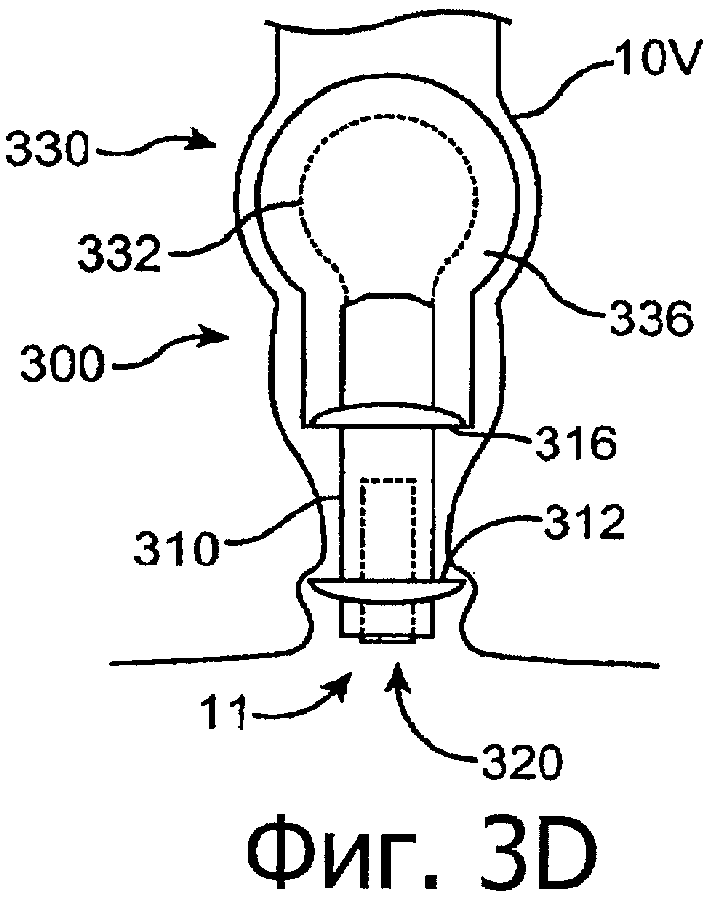
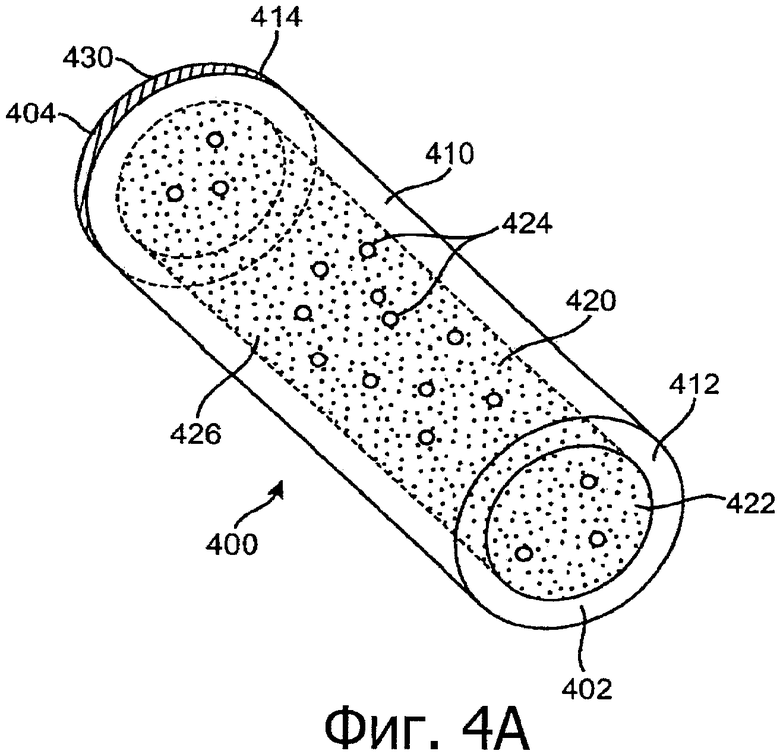
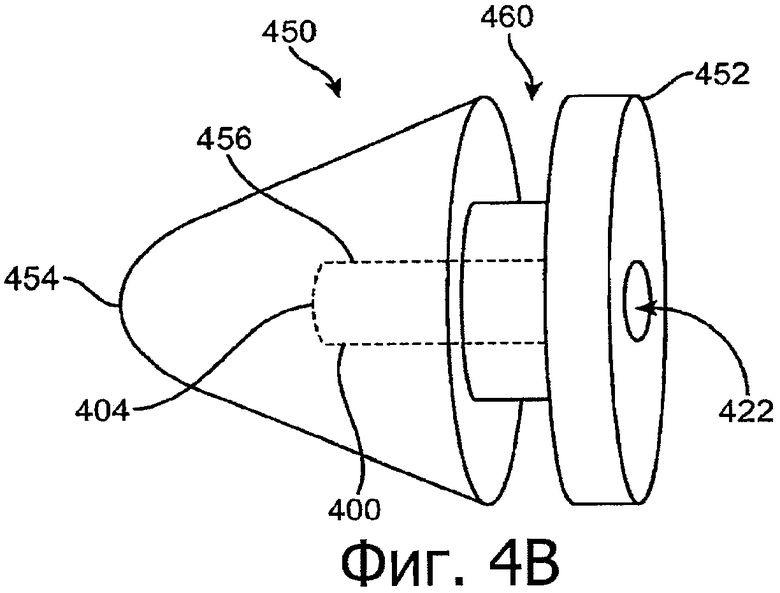
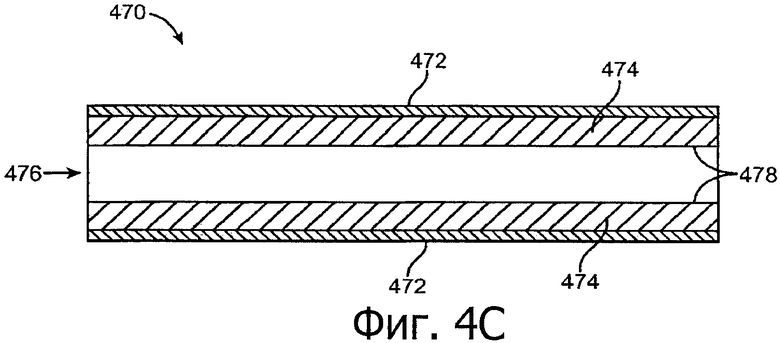
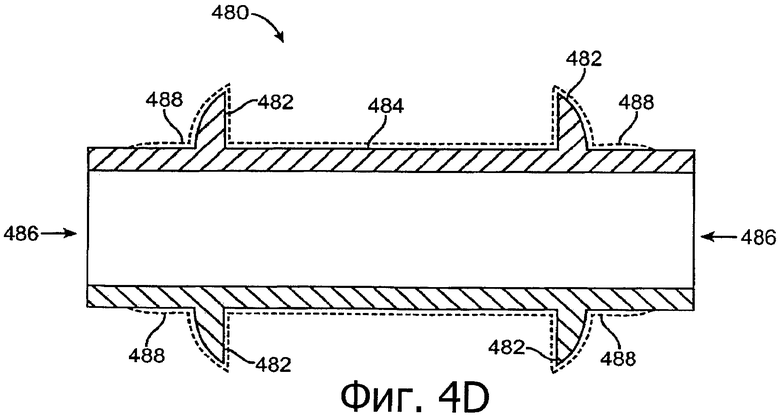
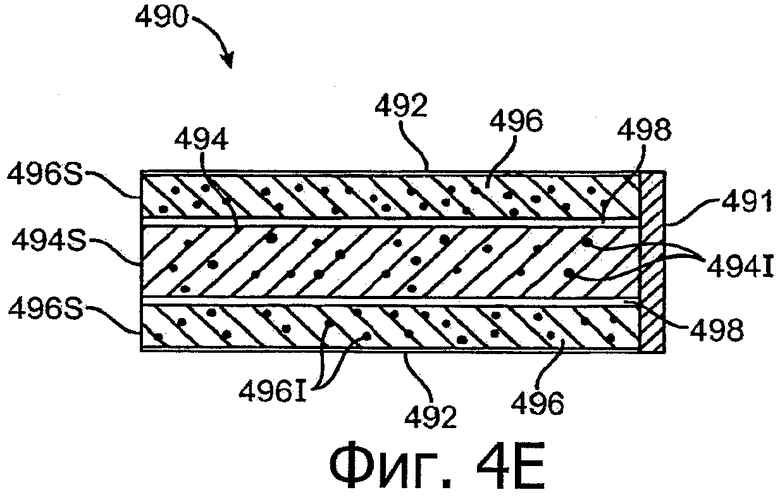
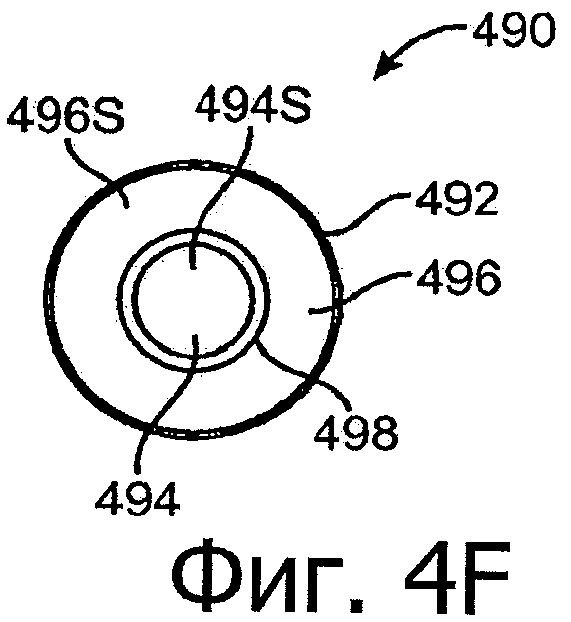
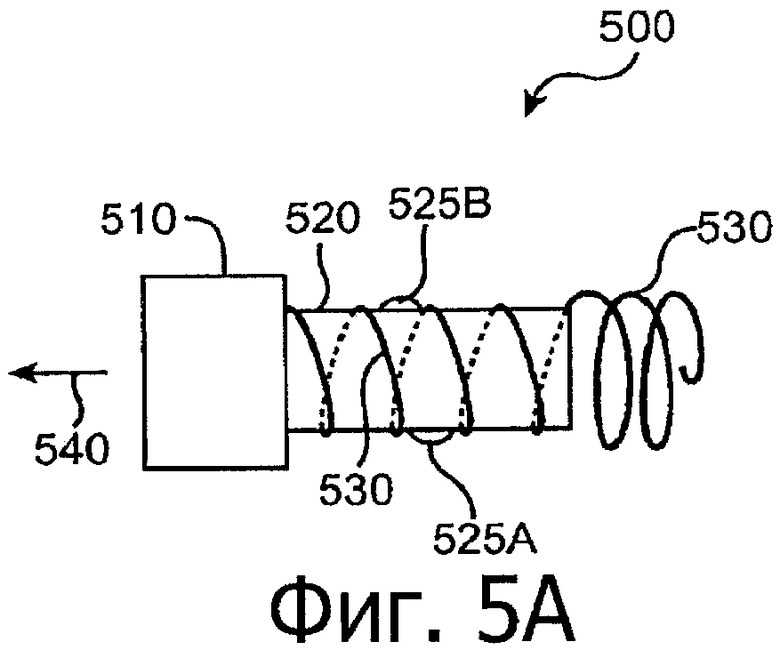
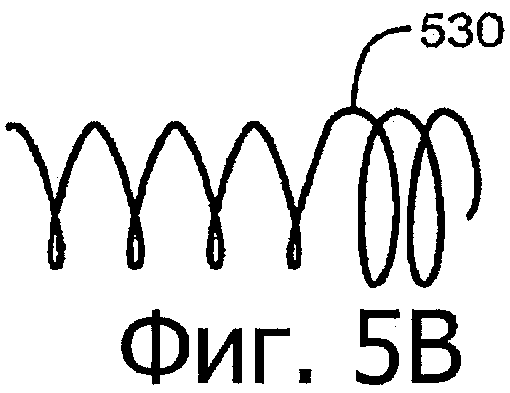
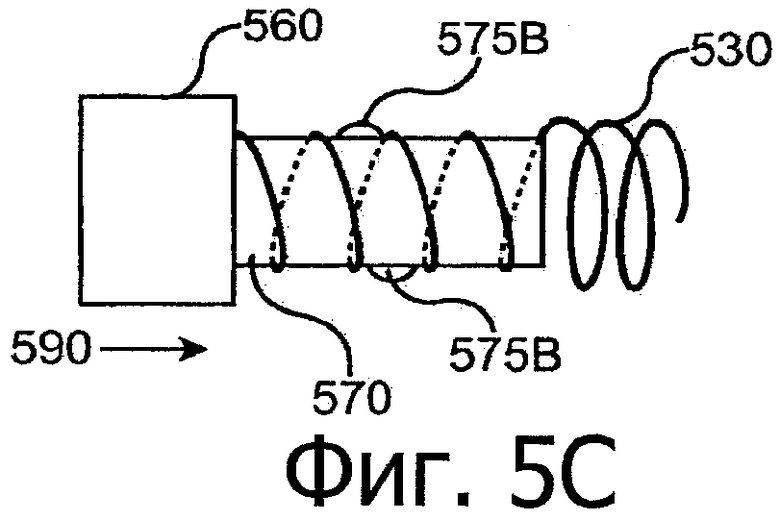
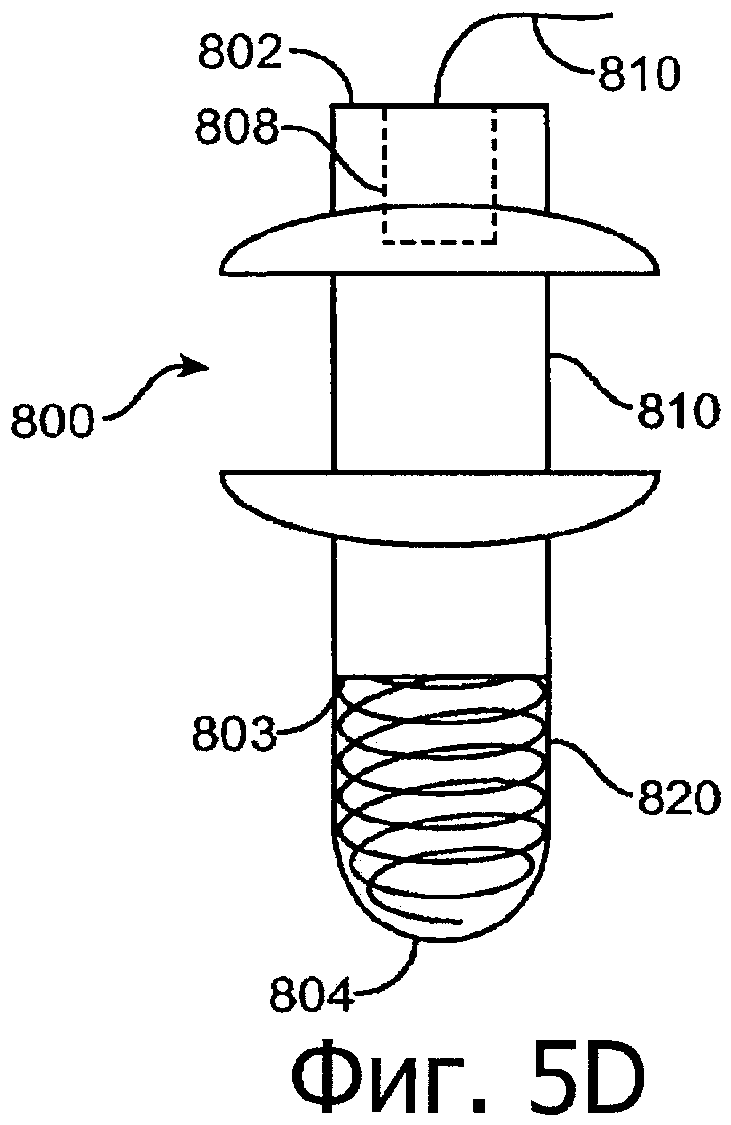
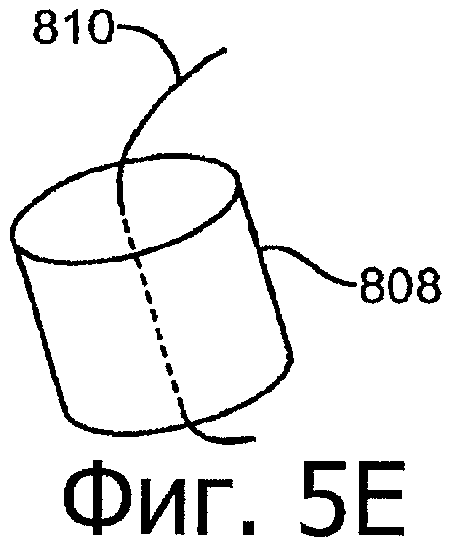
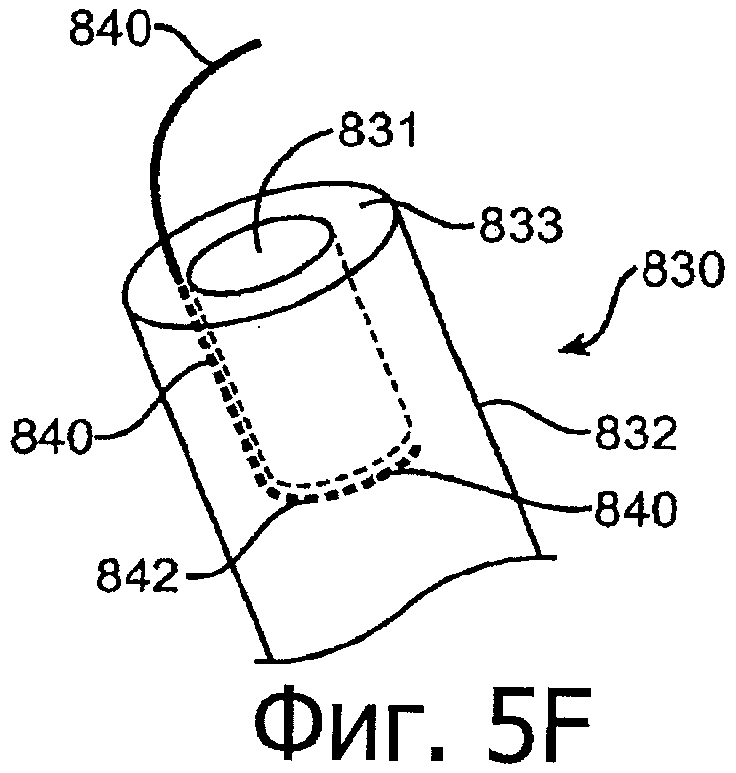
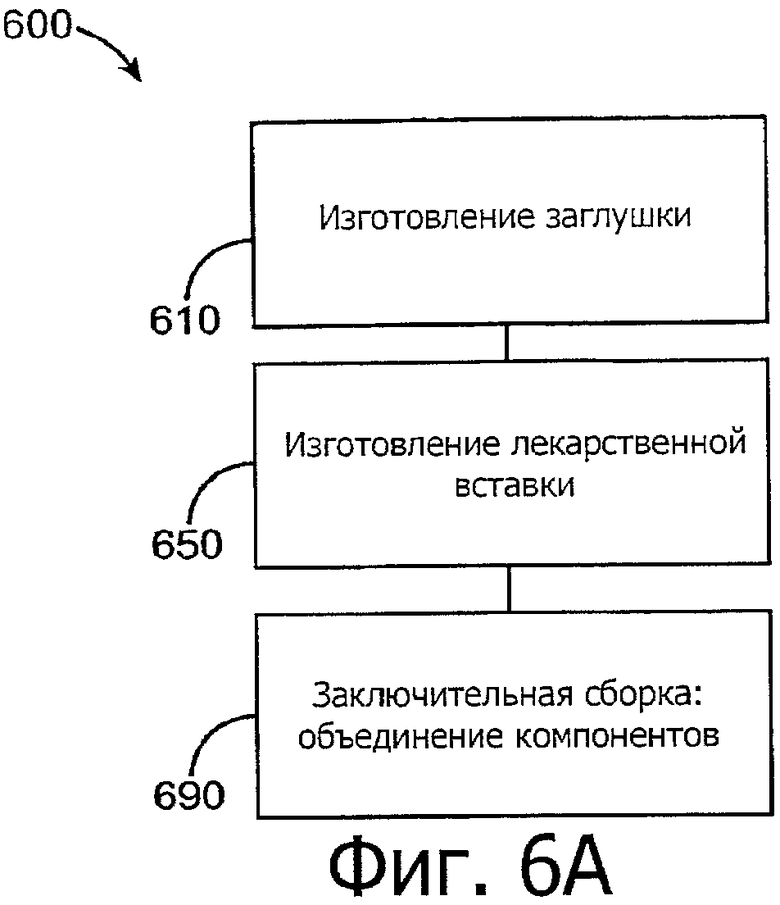
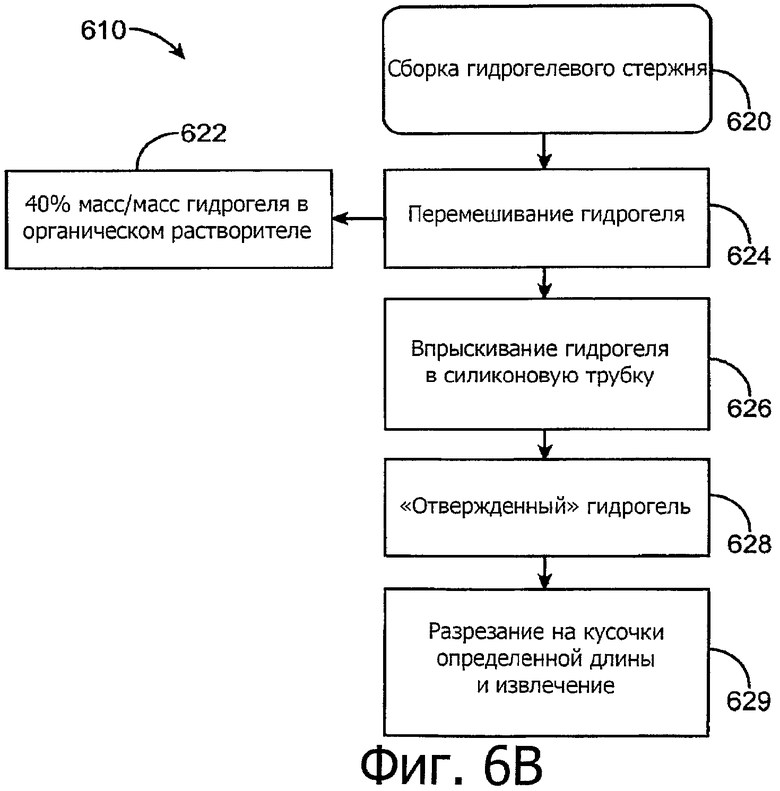
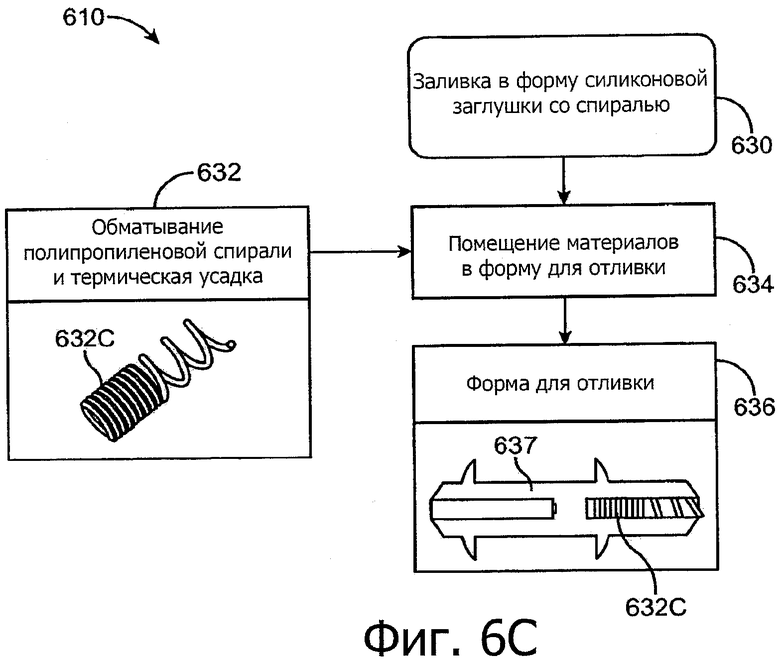
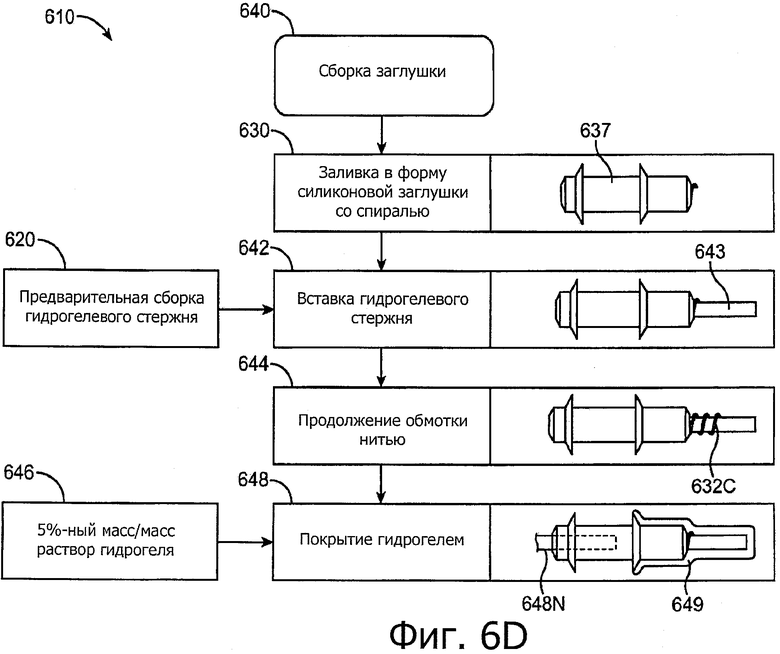

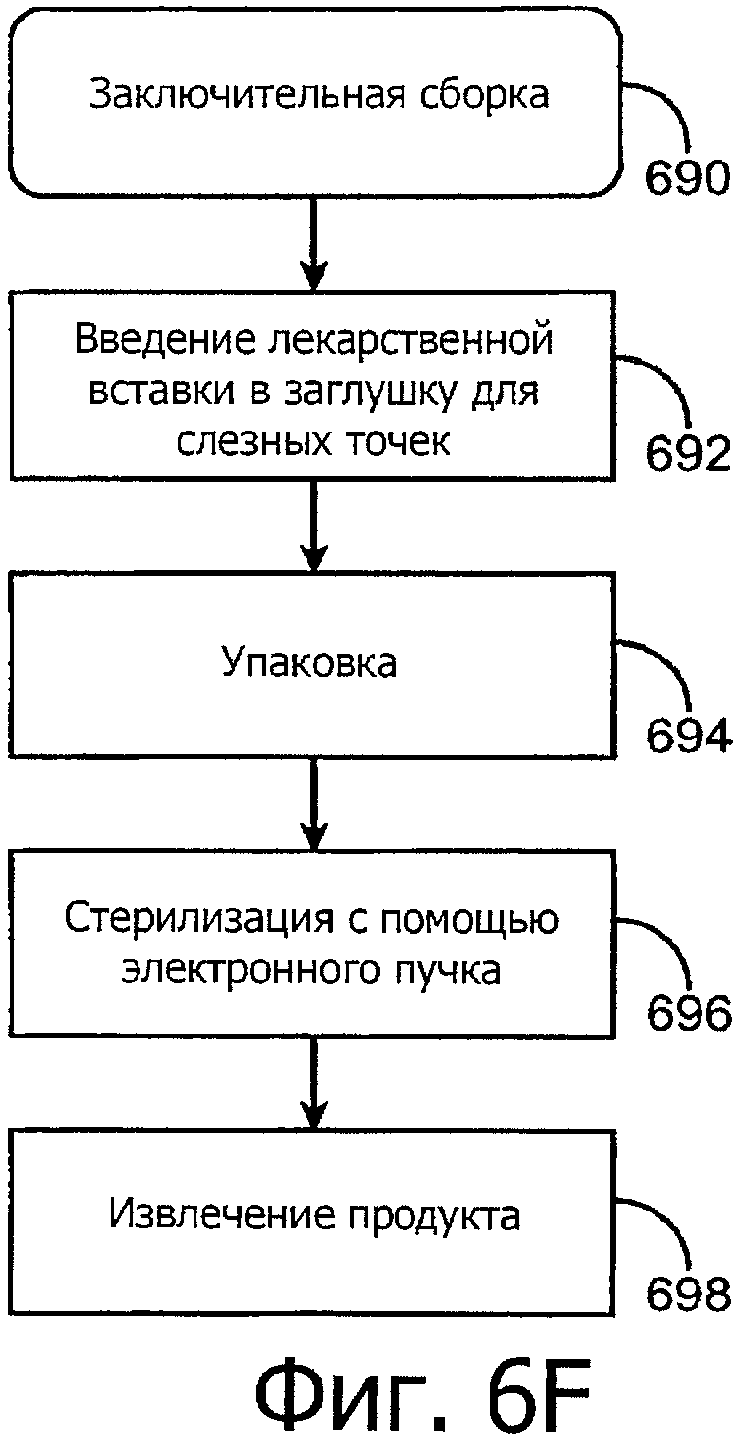
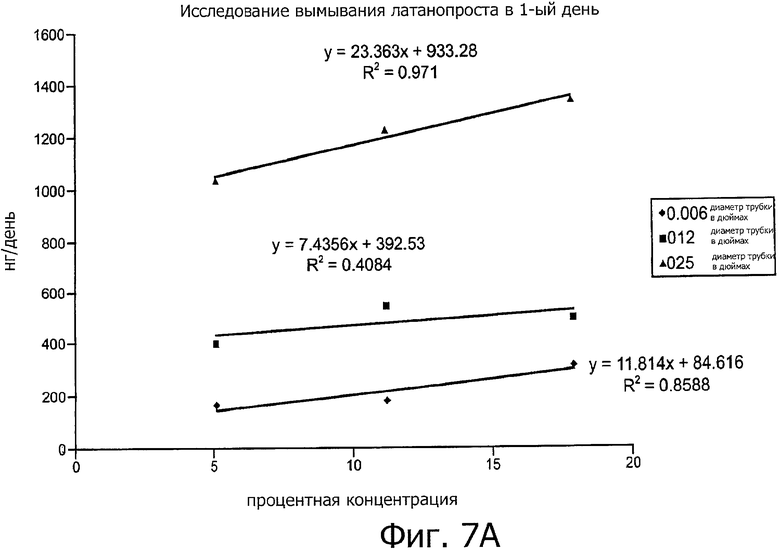
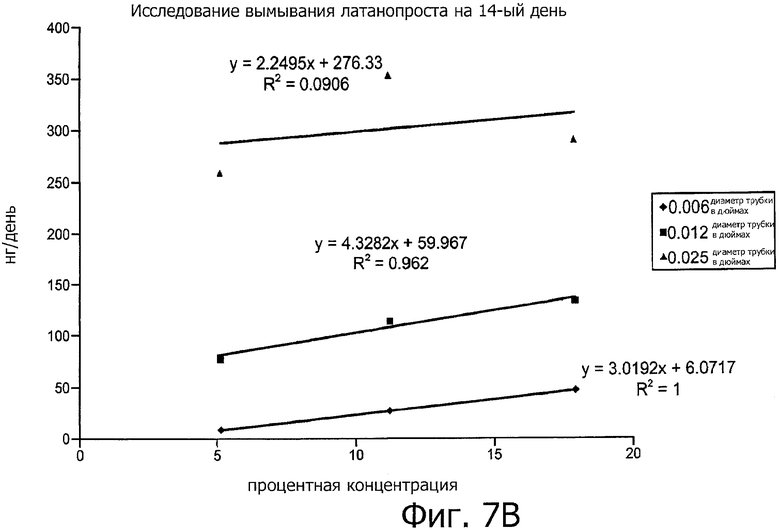
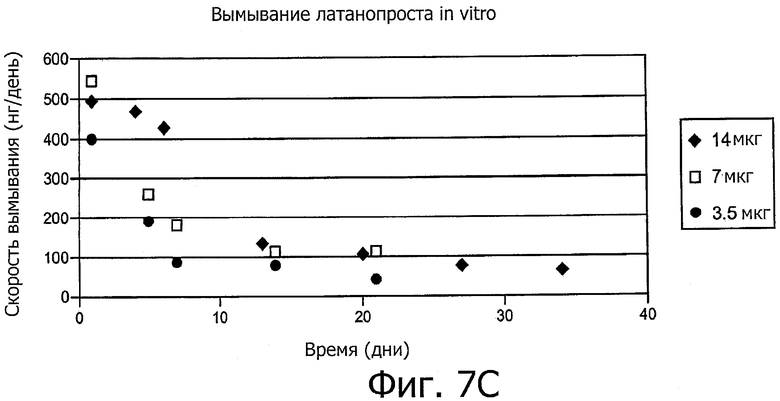
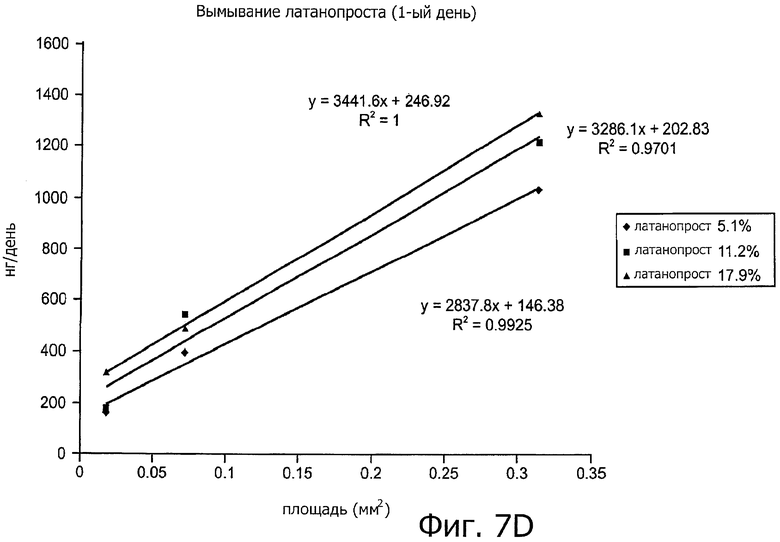
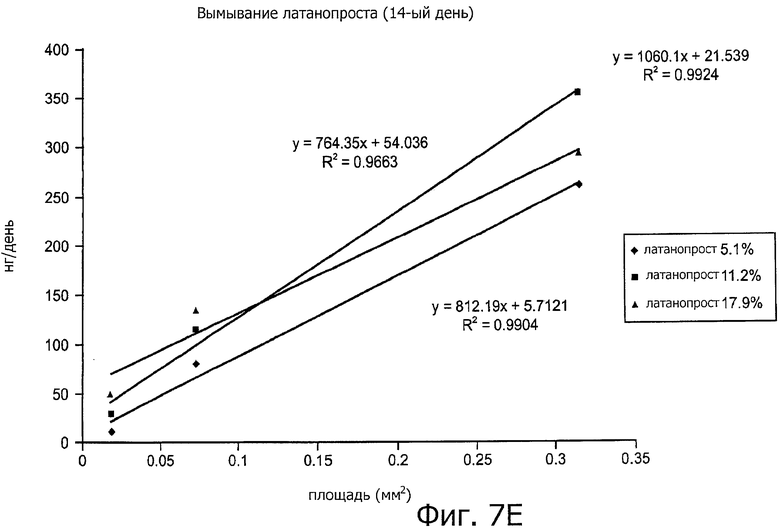
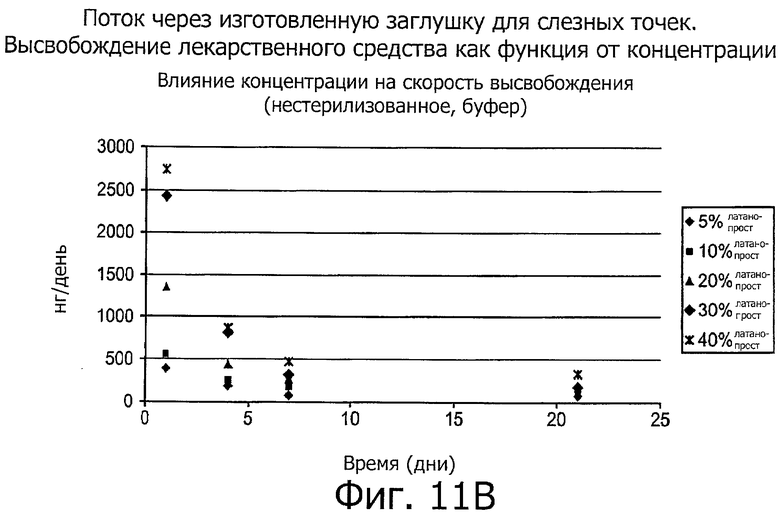
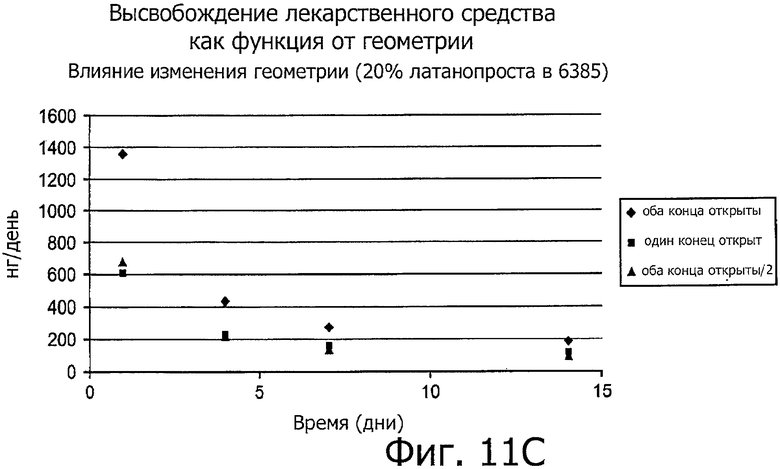
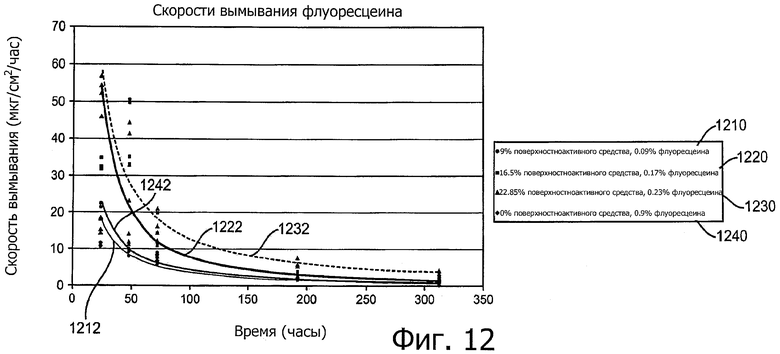
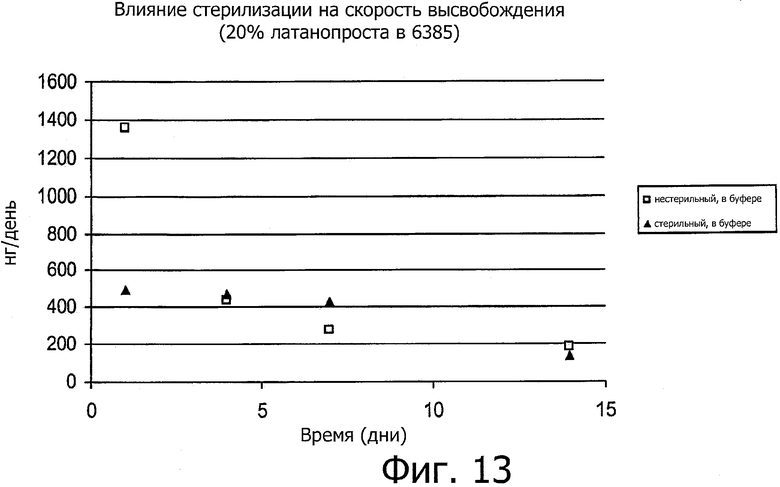
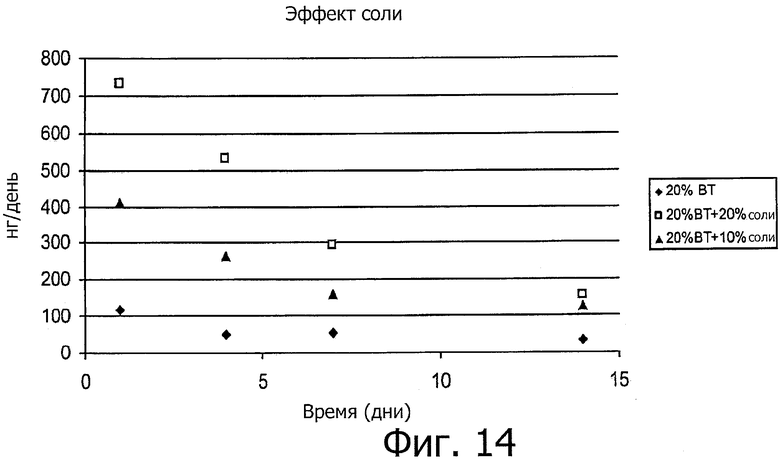




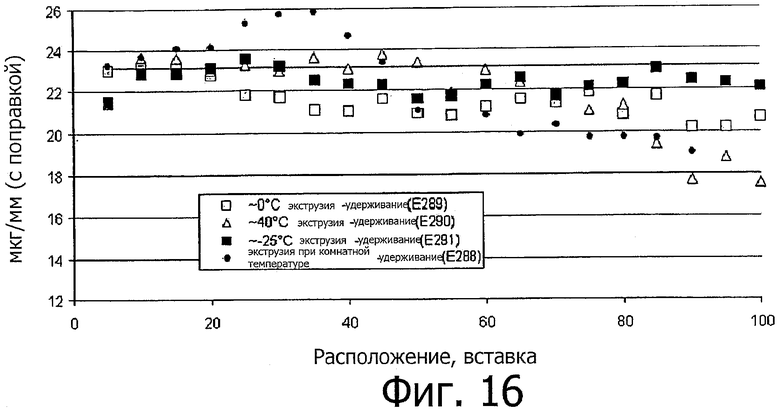
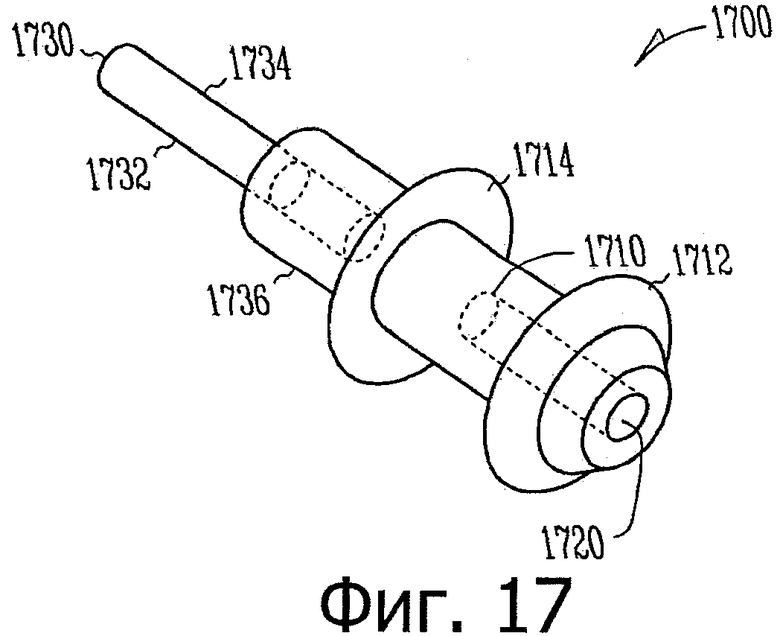
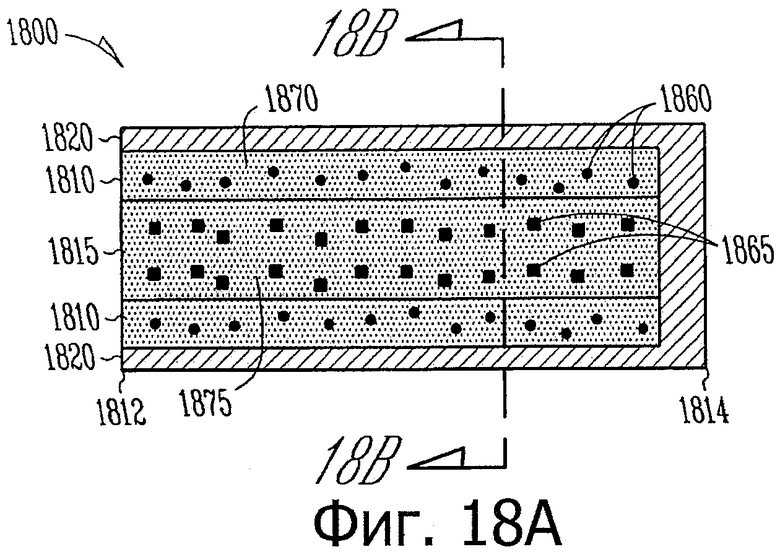
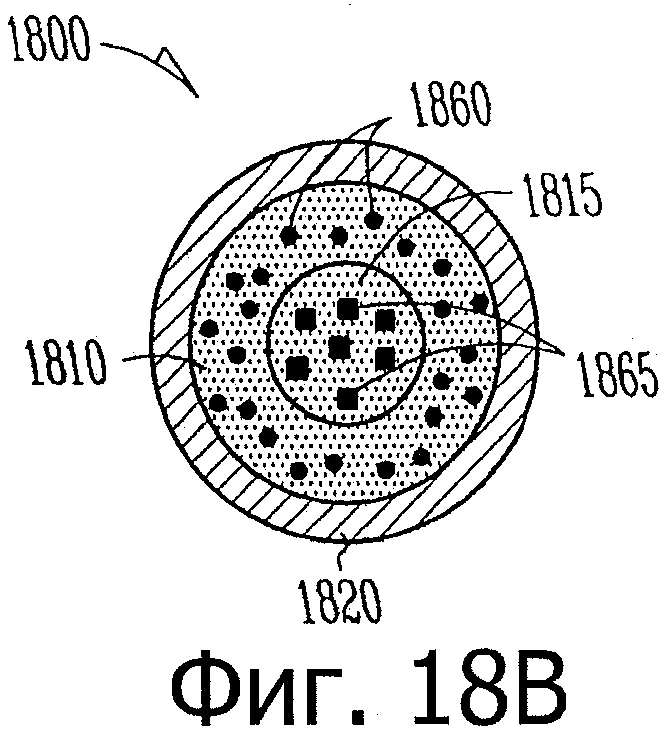
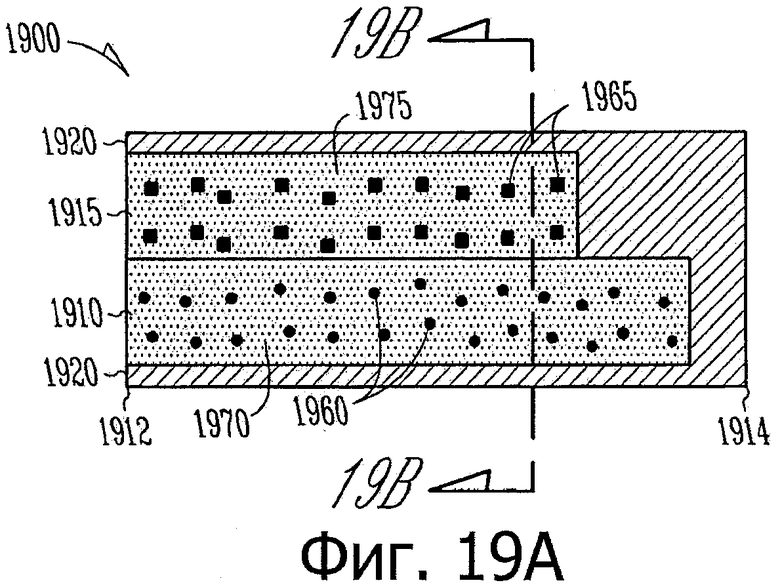
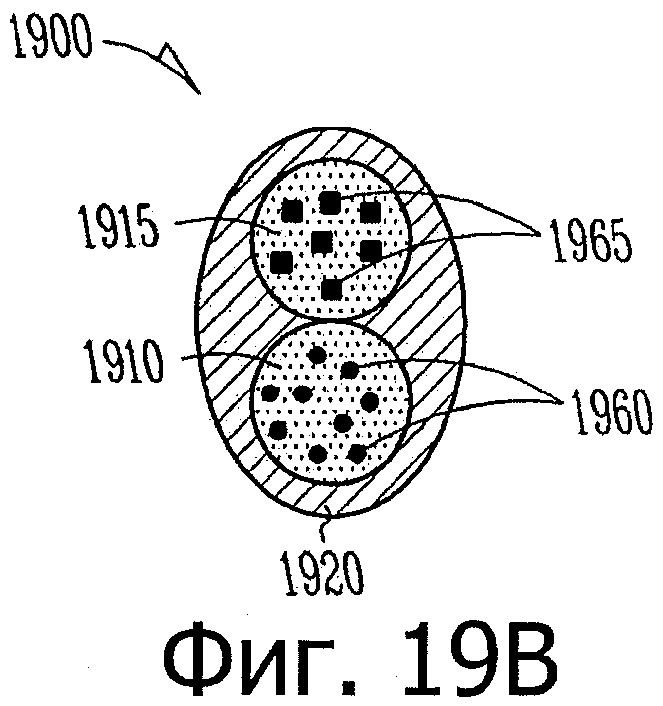
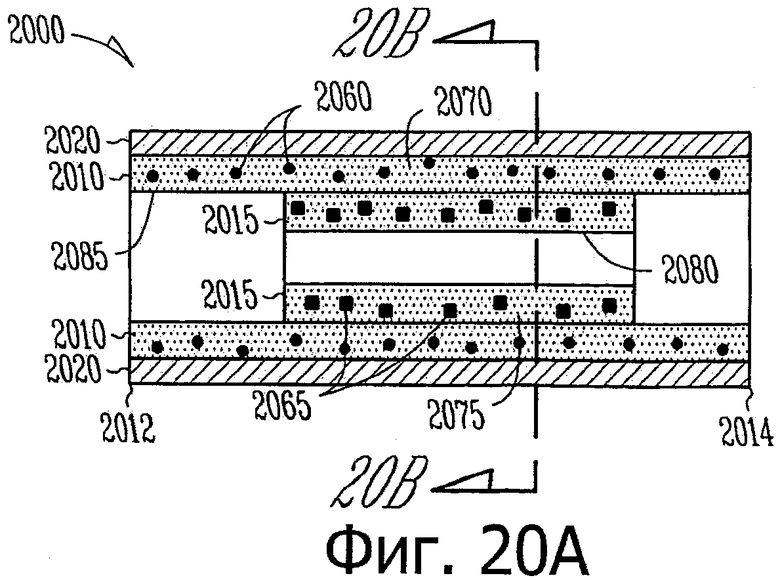
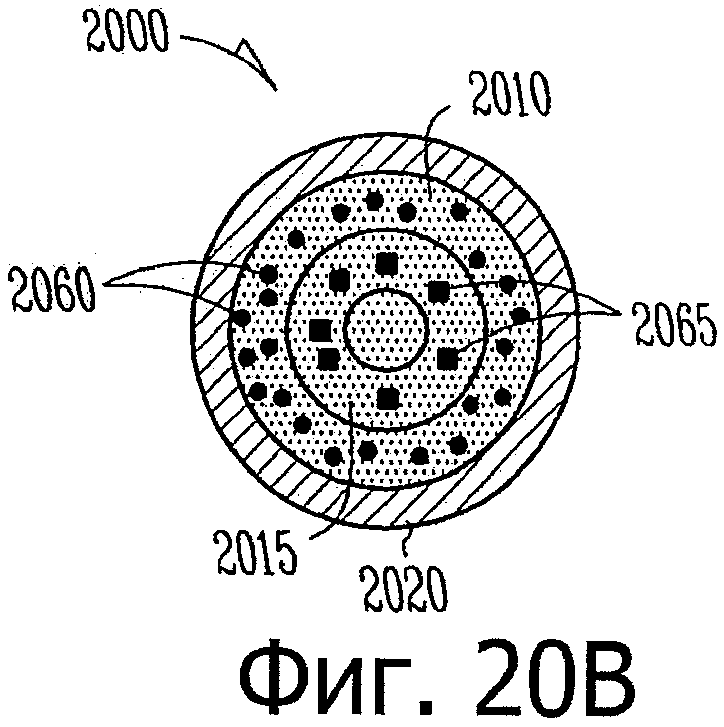
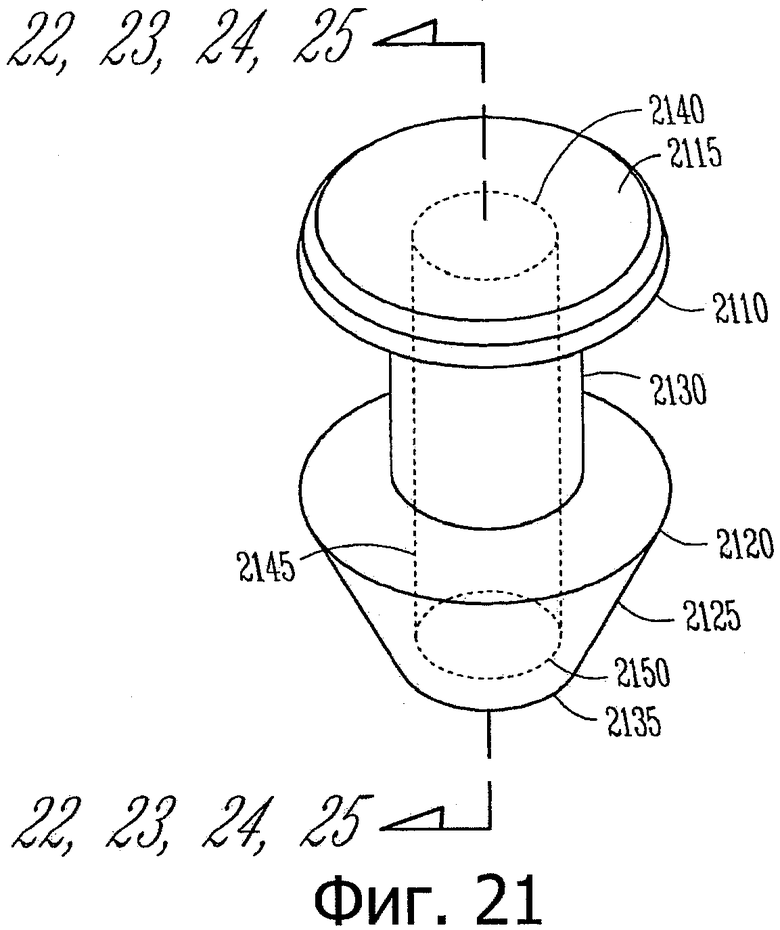
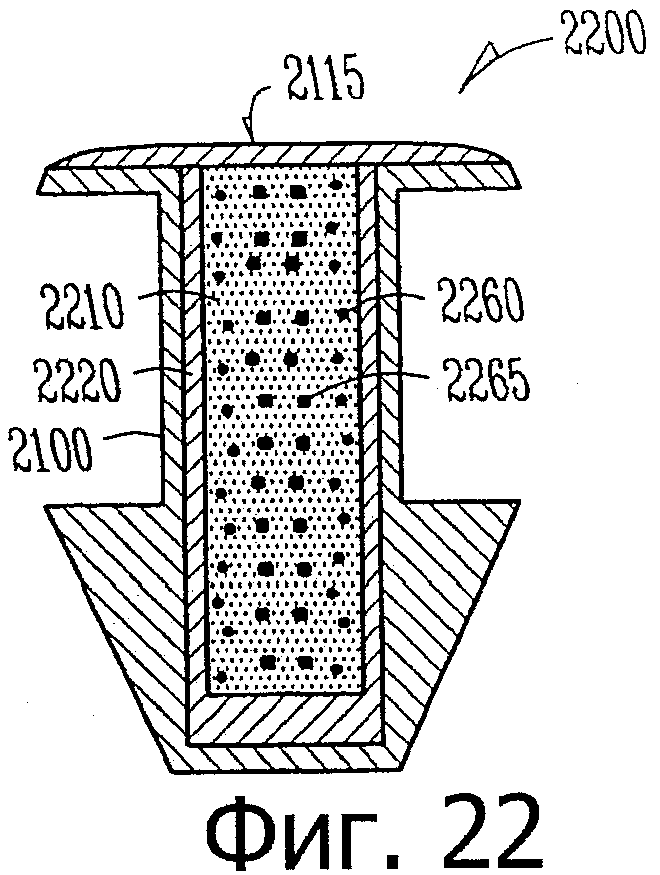
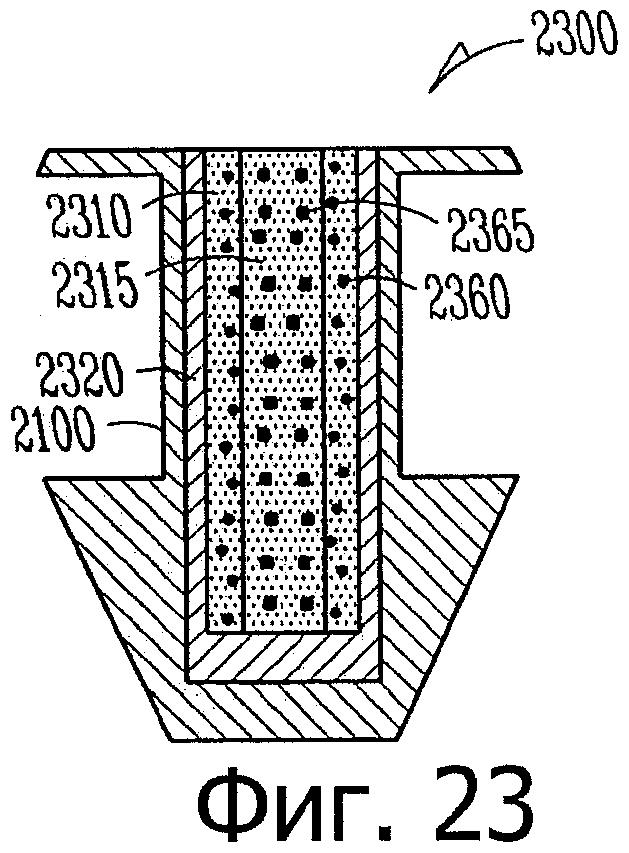
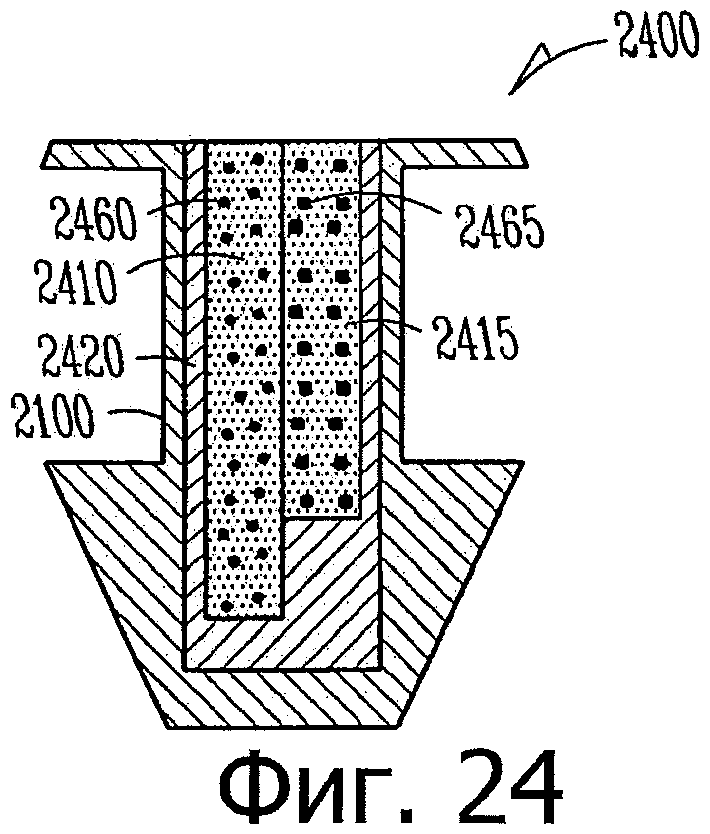
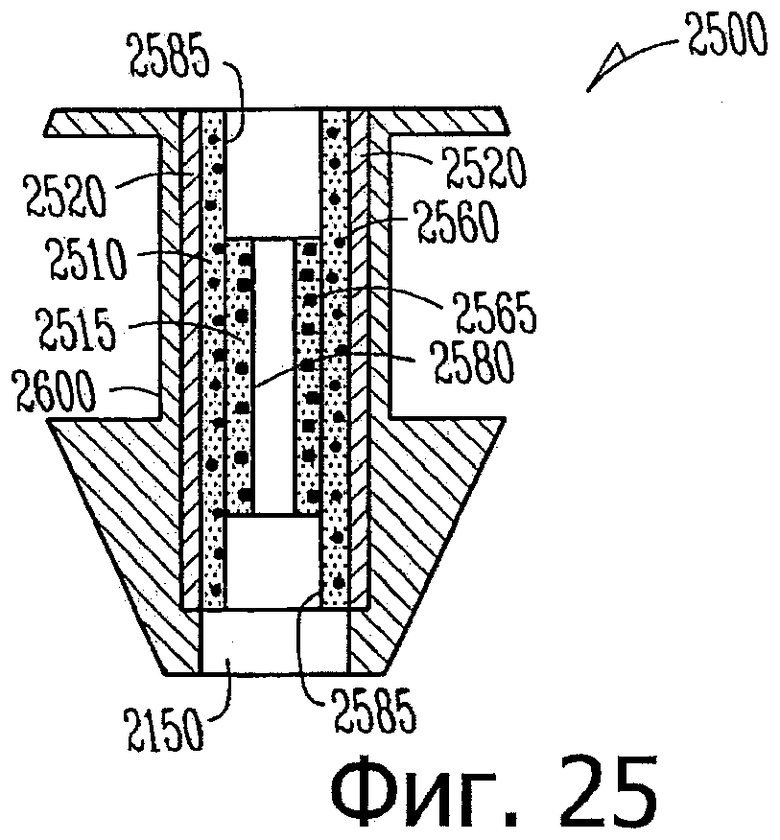
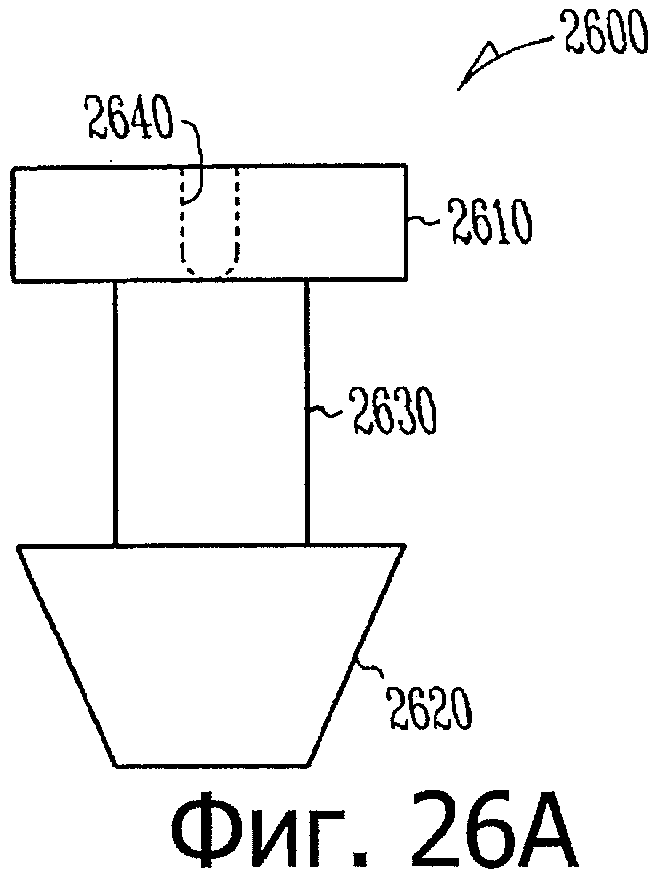
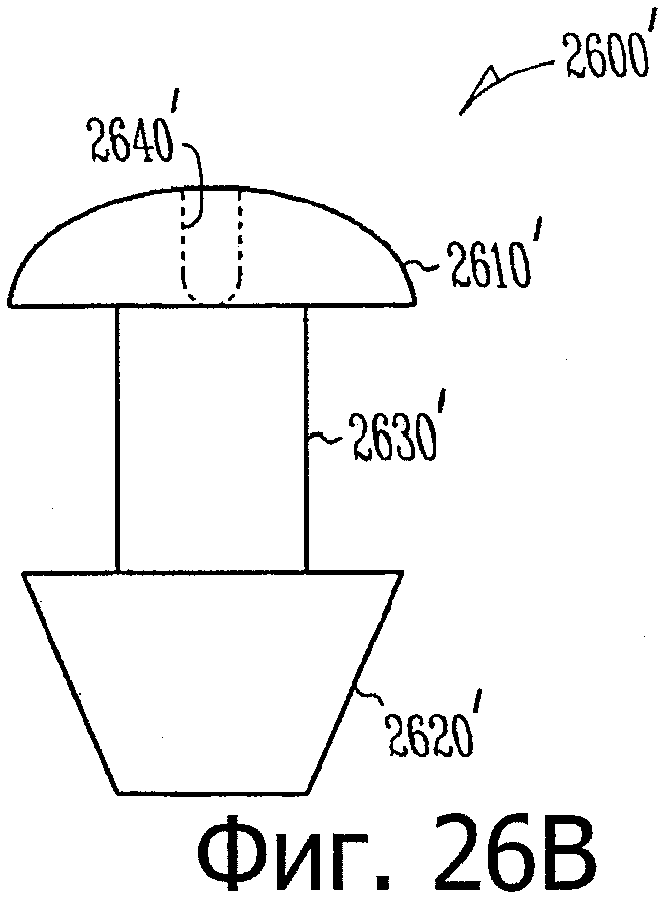
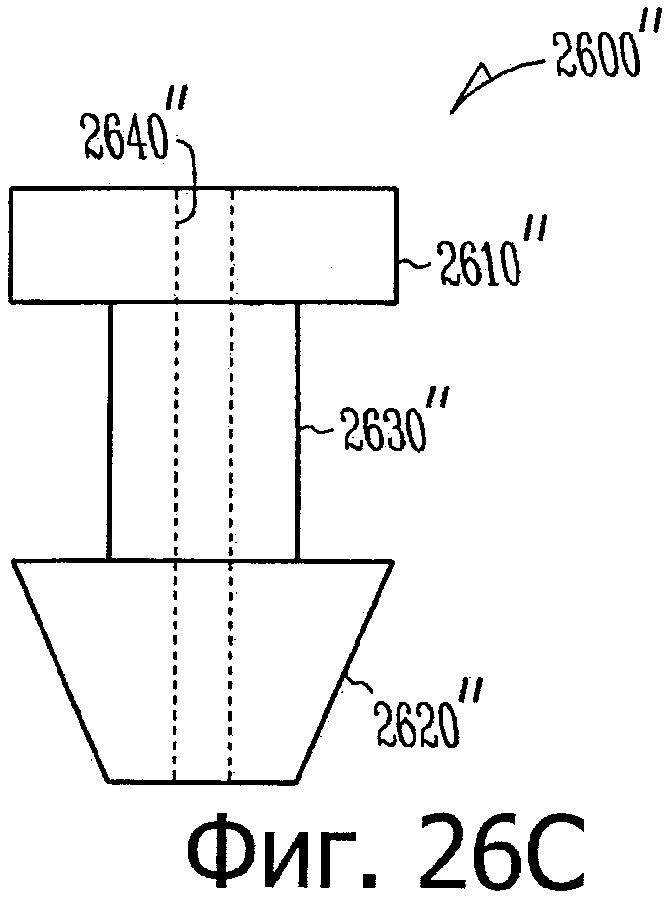
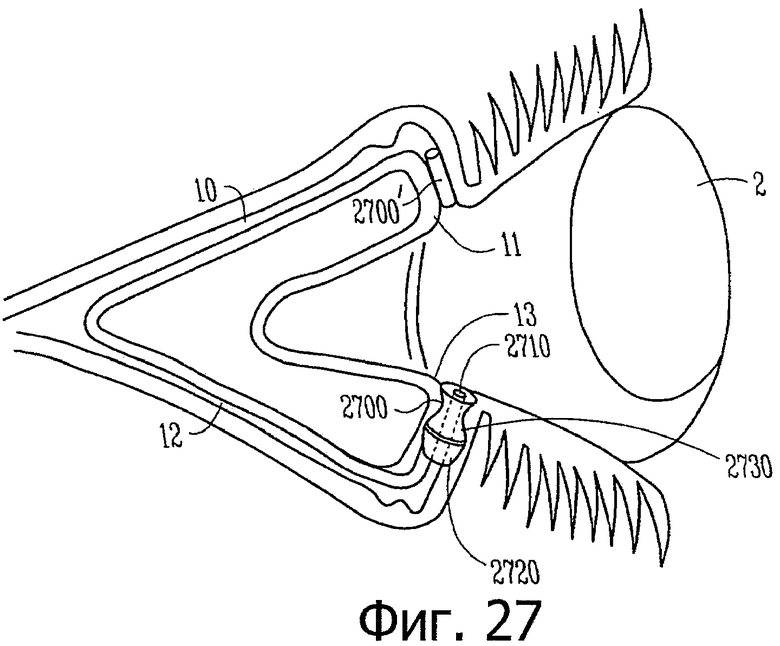
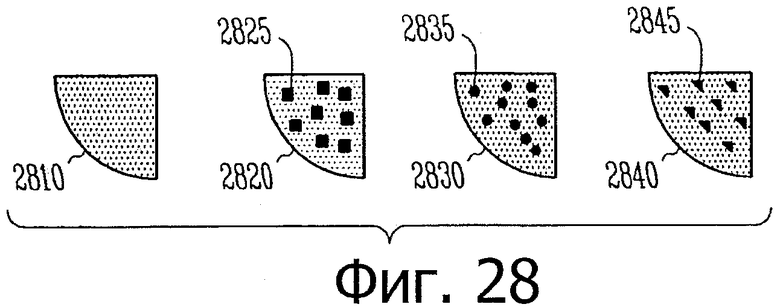
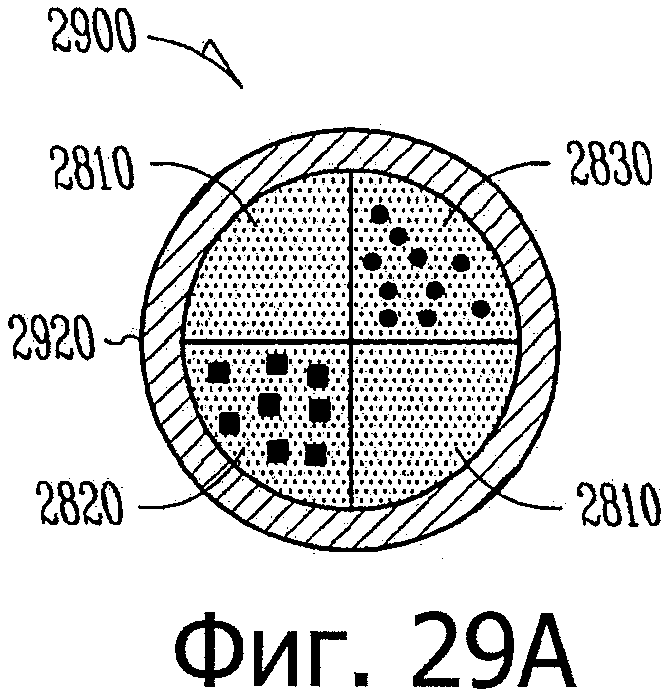
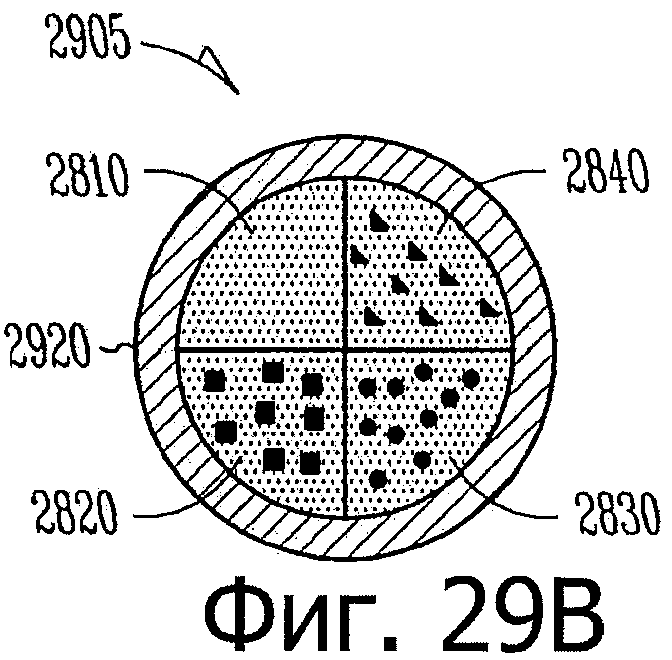
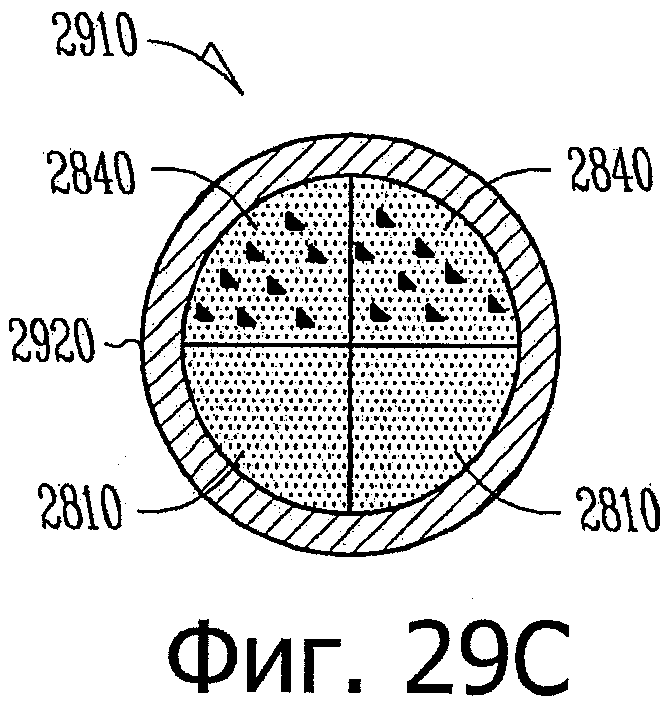
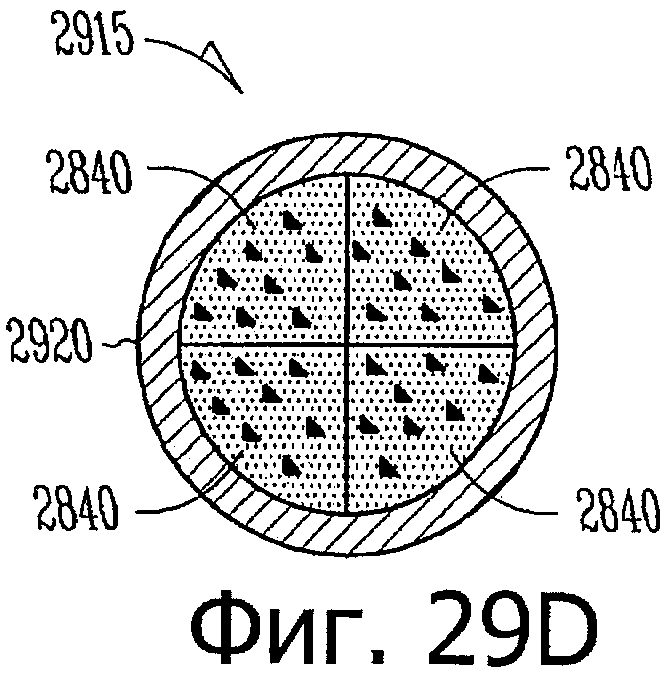
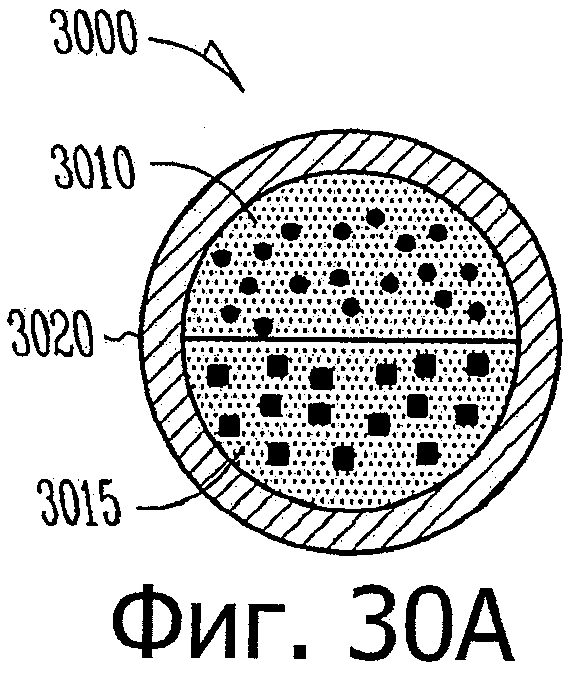
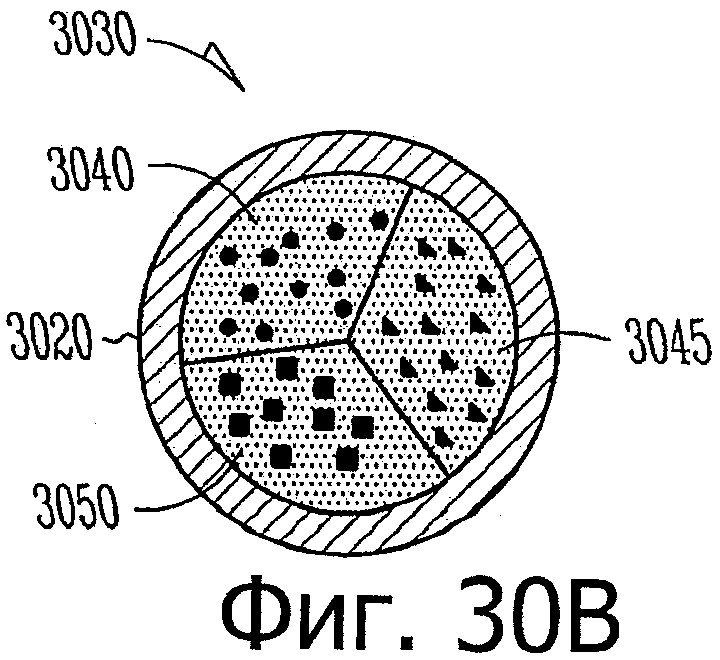
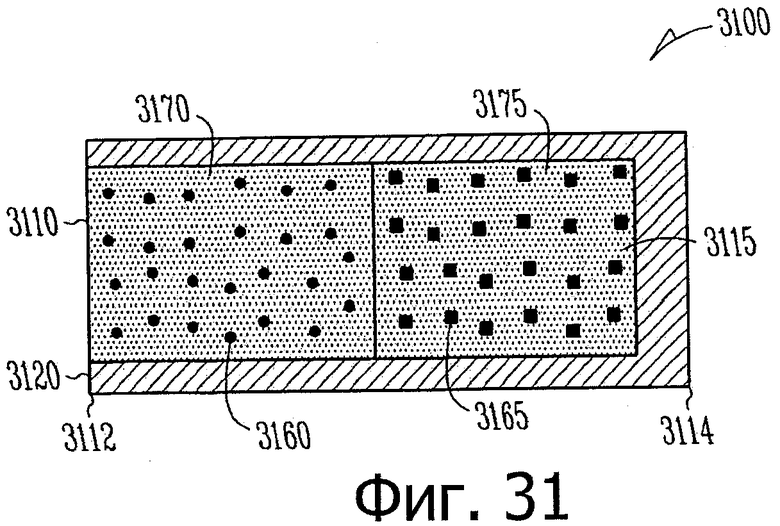
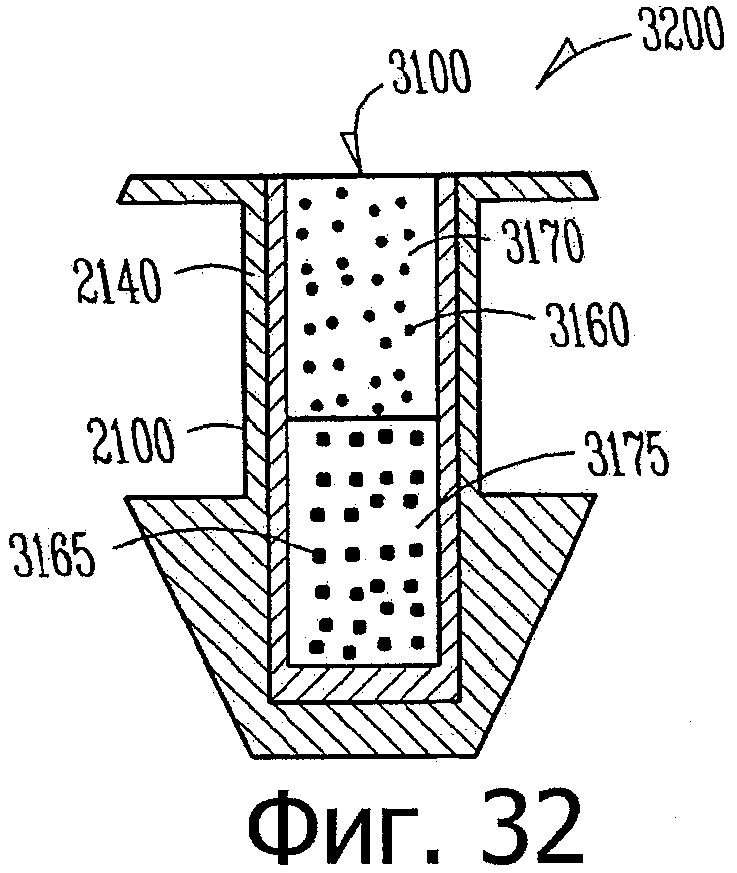
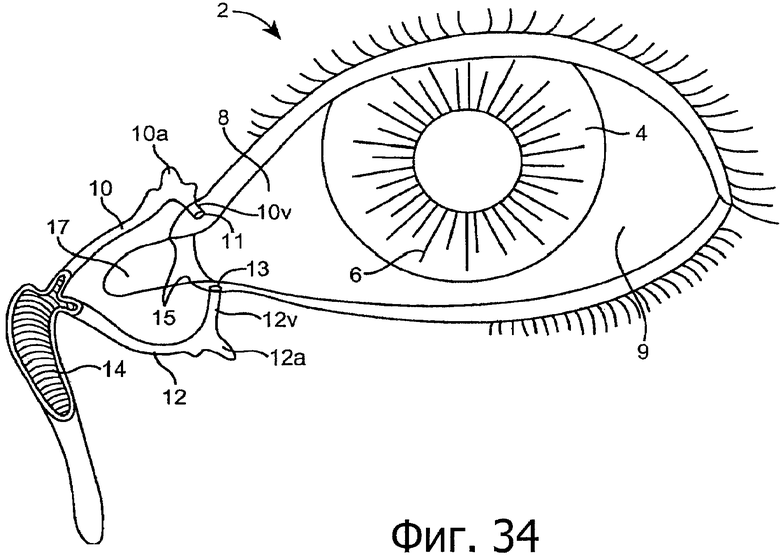
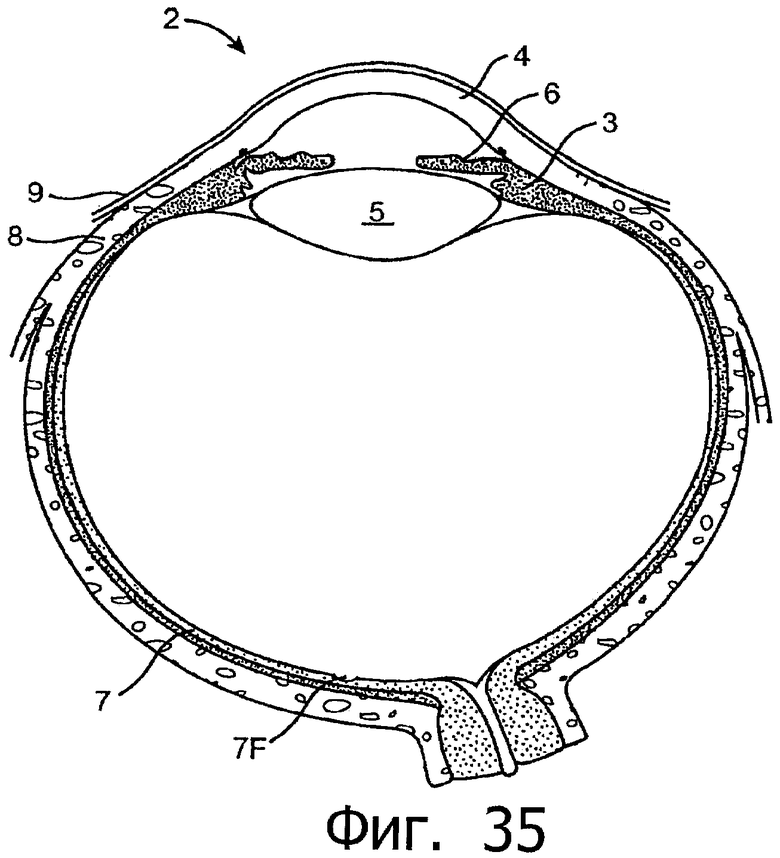
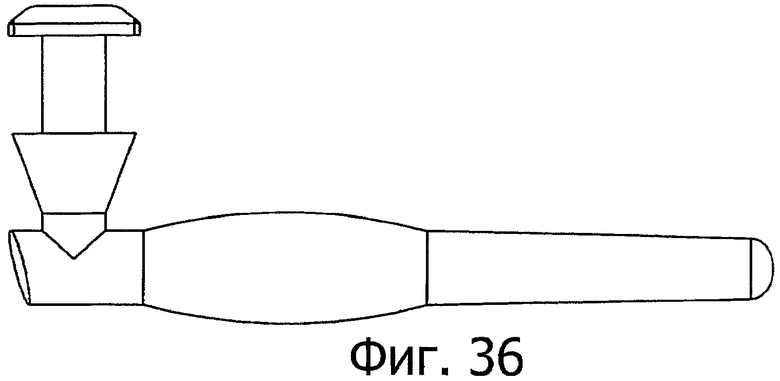
Изобретение относится к медицине. Описана твердая вставка с лекарственным ядром, которая может быть изготовлена с помощью впрыскивания жидкой смеси, включающей терапевтическое средство и исходный матрикс, в оболочку. Впрыскивание можно проводить при температурах, которые ниже температуры окружающей среды. Смесь отверждают, чтобы образовать твердое ядро, включающее лекарственное средство-матрикс. Терапевтическое средство при приблизительно комнатной температуре может быть жидкостью, которая образует дисперсию капель в материале матрикса. Поверхность твердого лекарственного ядра открыта, например, с помощью разрезания трубки, и открытая поверхность твердого лекарственного ядра высвобождает терапевтические количества терапевтического средства, если ядро имплантировано в организм пациента. В некоторых воплощениях тело вставки подавляет высвобождение терапевтического средства, например, с помощью материала, по существу непроницаемого для терапевтического средства, так что терапевтические количества высвобождаются через открытую поверхность, что, таким образом, препятствует высвобождению терапевтического средства в ткани, которые не являются мишенью действия средства. 5 н. и 106 з.п. ф-лы, 36 ил., 13 пр.
1. Способ изготовления лекарственной вставки для размещения внутри имплантата, в котором имплантат приспособлен для размещения внутри слезного канальца глаза, способ, включающий:
впрыскивание в заготовку оболочки, при температуре впрыскивания, равной менее чем примерно 25°С, смеси, включающей терапевтическое средство и силиконовый матрикс, так что заготовка оболочки в значительной степени заполняется смесью, заготовка оболочки в значительной степени непроницаемая для средства, отверждение смеси, при температуре отверждения более чем примерно 25°С, в заготовке оболочки для обеспечения отвержденной, заполненной заготовки оболочки, содержащей внутри заготовки лекарственное ядро; и разделение отвержденной заполненной заготовки оболочки для формирования множества лекарственных вставок.
2. Способ по п.1, в котором каждая из множества лекарственных вставок имеет в значительной степени одинаковую длину и в котором количество средства в первой вставке множества близко к количеству средства в любой другой вставке множества.
3. Способ по п.1, в котором: а) терапевтическое средство равномерно и гомогенно распределено по всему матриксу; или b) терапевтическое средство, по меньшей мере, частично формирует твердые или жидкие включения внутри матрикса.
4. Способ по п.1, в котором количество терапевтического средства в объемной доле отвержденной смеси отличается от количества терапевтического средства в любой другой равной объемной доле отвержденной смеси не более чем примерно на 10%.
5. Способ по п.1, в котором количество терапевтического средства в объемной доле отвержденной смеси отличается от количества терапевтического средства в любой другой равной объемной доле отвержденной смеси не более чем примерно на 5%.
6. Способ по п.1, в котором количество средства в каждой из множества вставок отличается между ними не более чем примерно на 30%.
7. Способ по п.1, в котором количество средства в каждой из множества вставок отличается между ними не более чем примерно на 20%.
8. Способ по п.1, в котором количество средства в каждой из множества вставок отличается между ними не более чем примерно на 10%.
9. Способ по п.1, в котором количество средства в каждой из множества вставок отличается между ними не более чем примерно на 5%.
10. Способ по п.1, в котором разделение отвержденной, заполненной заготовки оболочки включает нарезание отвержденной, заполненной заготовки оболочки лезвием или лазером.
11. Способ по п.1, в котором смесь дополнительно включает растворитель, в котором растворены матрикс и средство, и в котором отверждение включает, по меньшей мере, частичное удаление растворителя после впрыскивание в заготовку оболочки.
12. Способ по п.1, в котором отверждение включает помещение заготовки оболочки в камеру влажности, нагревание или обработку при пониженном давлении.
13. Способ по п.12, в котором растворитель включает углеводород, сложный эфир, галогеноуглерод, спирт, амид или их комбинацию.
14. Способ по п.1, в котором отверждение смеси включает нагревание смеси до температуры отверждения, при относительной влажности, в течение промежутка времени.
15. Способ по п.14, в котором температура отверждения включает диапазон от примерно 25°С до примерно 100°С, относительная влажность включает диапазон от примерно 40% до примерно 100%, и промежуток времени включает диапазон от примерно 1 мин до примерно 48 ч.
16. Способ по п.15, в котором температура отверждения равна, по меньшей мере, примерно 40°С, относительная влажность равна, по меньшей мере, примерно 80% или и то, и другое.
17. Способ по п.1, в котором впрыскивание включает впрыскивание под давлением, равным, по меньшей мере, примерно 40 psi.
18. Способ по п.1, в котором температура впрыскивания включает температуру, равную от примерно -50°С до примерно 25°С.
19. Способ по п.18, в котором температура впрыскивания включает температуру, равную от примерно -10°С до примерно 10°С.
20. Способ по п.1, в котором смесь впрыскивают так, что заготовка оболочки заполняется со скоростью, равной не более чем примерно 0,5 см/с.
21. Способ по п.1, в котором каждая лекарственная вставка запечатана с одного конца, обеспечивая на втором конце открытую поверхность.
22. Способ по п.21, в котором каждая лекарственная вставка запечатана с одного конца отверждаемым под действием ультрафиолетового излучения адгезивом, цианоакрилатом, эпоксидной смолой, зафиксирована термосваркой или крышечкой.
23. Способ по п.22, который дополнительно включает облучение лекарственной вставки с отверждаемым под действием ультрафиолетового излучения адгезивом ультрафиолетовым светом.
24. Способ по п.22, дополнительно включающий, после запечатывания одного конца вставки, встраивание лекарственной вставки в канал имплантата, приспособленного для приема вставки.
25. Способ по п.1, в котором вставка включает от примерно 0,1 мас.% до примерно 50 мас.% средства.
26. Способ по п.1, в котором заготовка оболочки включает, по меньшей мере, одно из следующего: полиимид, РММА, PET, нержавеющая сталь или титан.
27. Способ по п.1, в котором средство включает средство для лечения глаукомы, средство, взаимодействующее с мускариновыми рецепторами, бета-блокатор, агонист альфа-рецепторов, ингибитор карбоангидразы или простагландин или аналог простагландина; противовоспалительное средство; противоинфекционное средство; лекарственное средство для лечения синдрома сухого глаза или любую их комбинацию.
28. Способ по п.27, в котором противовоспалительное средство включает стероид, мягкий стероид или NSAID и/или любое другое соединение с обезболивающими свойствами.
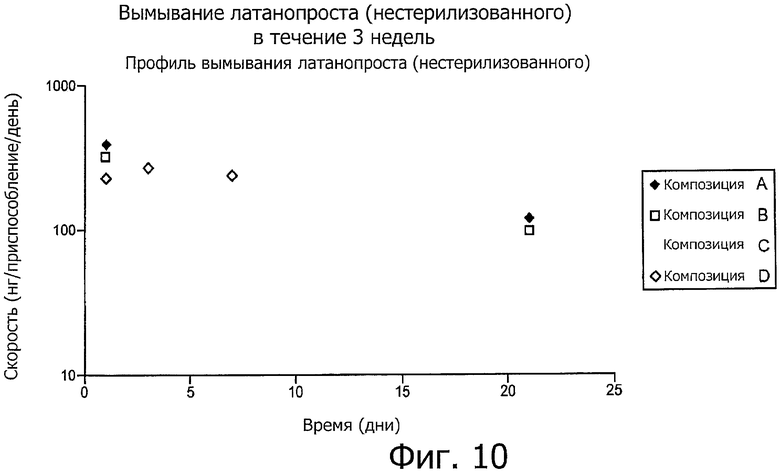
29. Способ по п.1, в котором средство включает латанопрост.
30. Способ по п.29, в котором латанопрост распределен внутри силикона в виде вкраплений.
31. Способ по п.1, в котором средство распределено в матриксе.
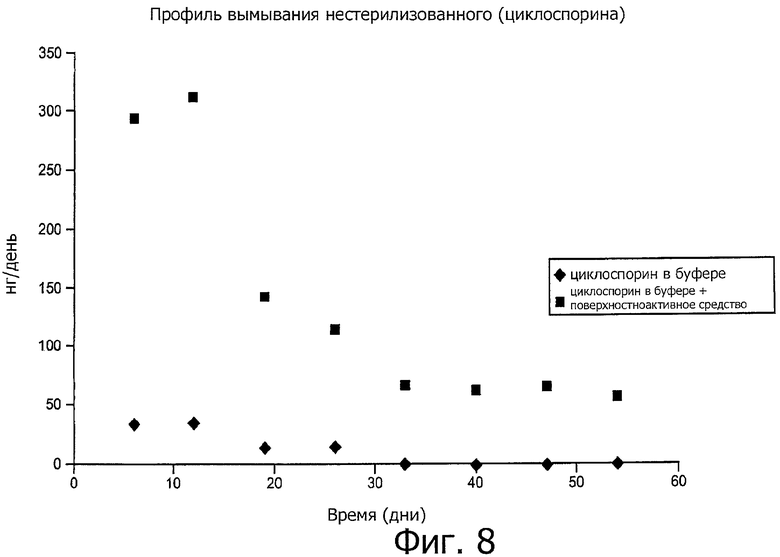
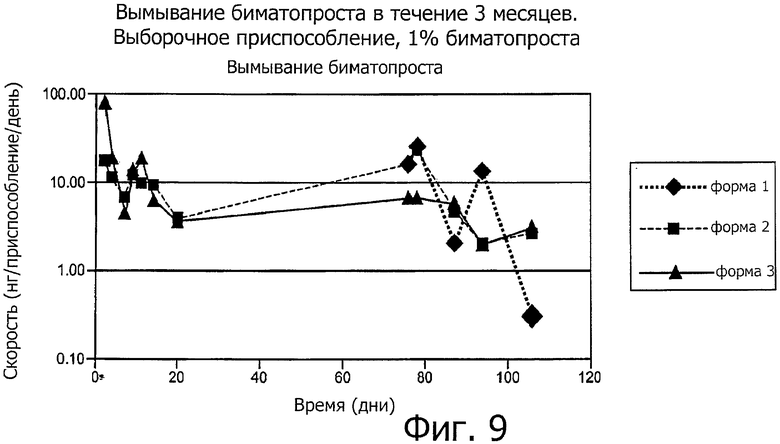
32. Способ по п.1, в котором средство представляет собой биматопрост, олопатадин или циклоспорин.
33. Способ по п.1, в котором каждая лекарственная вставка включает два или более терапевтических средств.
34. Способ по п.1, в котором температура впрыскивания включает температуру, равную менее чем примерно 20°С.
35. Способ по п.1, в котором температура впрыскивания включает температуру, равную менее чем примерно 15°С.
36. Способ по п.1, в котором температура впрыскивания включает температуру, равную менее чем примерно 10°С.
37. Способ по п.1, в котором температура впрыскивания включает температуру, равную менее чем примерно 5°С.
38. Способ изготовления имплантата, приспособленного для размещения внутри слезного канальца глаза, способ, включающий:
впрыскивание в заготовку оболочки при температуре впрыскивания, равной менее чем примерно 25°С, смеси, включающей терапевтическое средство и силиконовый матрикс, так что заготовка оболочки в значительной степени заполняется смесью, заготовка оболочки в значительной степени непроницаема для средства, отверждение смеси, при температуре отверждения более чем примерно 25°С, в заготовке оболочки, для обеспечения отвержденной, заполненной заготовки оболочки, содержащей внутри заготовки лекарственное ядро;
разделение отвержденной заполненной заготовки оболочки для формирования множества лекарственных вставок;
запечатывание каждой лекарственной вставки с одного конца лекарственной вставки; и
введение каждой лекарственной вставки в канал имплантата, приспособленного для встраивания вставки.
39. Способ по п.38, в котором каждая из множества лекарственных вставок имеет в значительной степени одинаковую длину и в котором количество средства в первой вставке множества близко к количеству средства в любой другой вставке множества.
40. Способ по п.38, в котором: а) терапевтическое средство равномерно и гомогенно распределено по всему матриксу; или b) терапевтическое средство, по меньшей мере, частично формирует твердые или жидкие включения внутри матрикса.
41. Способ по п.38, в котором количество терапевтического средства в объемной доле отвержденной смеси отличается от количества терапевтического средства в любой другой равной объемной доле отвержденной смеси не более чем примерно на 10%.
42. Способ по п.38, в котором количество терапевтического средства в объемной доле отвержденной смеси отличается от количества терапевтического средства в любой другой равной объемной доле отвержденной смеси не более чем примерно на 5%.
43. Способ по п.38, в котором количество средства в каждой из множества вставок отличается между ними не более чем примерно на 30%.
44. Способ по п.38, в котором количество средства в каждой из множества вставок отличается между ними не более чем примерно на 20%.
45. Способ по п.38, в котором количество средства в каждой из множества вставок отличается между ними не более чем примерно на 10%.
46. Способ по п.38, в котором количество средства в каждой из множества вставок отличается между ними не более чем примерно на 5%.
47. Способ по п.38, в котором разделение отвержденной, заполненной заготовки оболочки включает нарезание отвержденной, заполненной заготовки оболочки лезвием или лазером.
48. Способ по п.38, в котором смесь дополнительно включает растворитель, в котором растворены матрикс и средство, и в котором отверждение включает, по меньшей мере, частичное удаление растворителя после впрыскивание в заготовку оболочки.
49. Способ по п.38, в котором отверждение включает помещение заготовки оболочки в камеру влажности, нагревание или обработку при пониженном давлении.
50. Способ по п.49, в котором растворитель включает углеводород, сложный эфир, галогеноуглерод, спирт, амид или их комбинацию.
51. Способ по п.38, в котором отверждение смеси включает нагревание смеси до температуры отверждения, при относительной влажности, в течение промежутка времени.
52. Способ по п.51, в котором температура отверждения включает диапазон от примерно 25°С до примерно 100°С, относительная влажность включает диапазон от примерно 40% до примерно 100%, и промежуток времени включает диапазон от примерно 1 мин до примерно 48 ч.
53. Способ по п.52, в котором температура отверждения равна, по меньшей мере, примерно 40°С, относительная влажность равна, по меньшей мере, примерно 80% или и то, и другое.
54. Способ по п.38, в котором впрыскивание включает впрыскивание под давлением, равным, по меньшей мере, примерно 40 psi.
55. Способ по п.38, в котором температура впрыскивания включает температуру, равную от примерно -50°С до примерно 25°С.
56. Способ по п.55, в котором температура впрыскивания включает температуру, равную от примерно -10°С до примерно 10°С.
57. Способ по п.38, в котором смесь впрыскивают так, что заготовка оболочки заполняется со скоростью, равной не более чем примерно 0,5 см/с.
58. Способ по п.38, в котором каждая лекарственная вставка запечатана с одного конца, обеспечивая на втором конце открытую поверхность.
59. Способ по п.58, в котором каждая лекарственная вставка запечатана с одного конца отверждаемым под действием ультрафиолетового излучения адгезивом, цианоакрилатом, эпоксидной смолой, зафиксирована термосваркой или крышечкой.
60. Способ по п.59, который дополнительно включает облучение лекарственной вставки с отверждаемым под действием ультрафиолетового излучения адгезивом ультрафиолетовым светом.
61. Способ по п.59, дополнительно включающий, после запечатывания одного конца вставки, встраивание лекарственной вставки в канал имплантата, приспособленного для приема вставки.
62. Способ по п.38, в котором вставка включает от примерно 0,1 мас.% до примерно 50 мас.% средства.
63. Способ по п.38, в котором заготовка оболочки включает, по меньшей мере, одно из следующего: полиимид, РММА, PET, нержавеющая сталь или титан.
64. Способ по п.38, в котором средство включает средство для лечения глаукомы, средство, взаимодействующее с мускариновыми рецепторами, бета-блокатор, агонист альфа-рецепторов, ингибитор карбоангидразы или простагландин или аналог простагландина; противовоспалительное средство; противоинфекционное средство; лекарственное средство для лечения синдрома сухого глаза или любую их комбинацию.
65. Способ по п.64, в котором противовоспалительное средство включает стероид, мягкий стероид или NSAID и/или любое другое соединение с обезболивающими свойствами.
66. Способ по п.38, в котором средство включает латанопрост.
67. Способ по п.66, в котором латанопрост распределен внутри силикона в виде вкраплений.
68. Способ по п.38, в котором средство распределено в матриксе.
69. Способ по п.38, в котором средство представляет собой биматопрост, олопатадин или циклоспорин.
70. Способ по п.38, в котором каждая лекарственная вставка включает два или более терапевтических средств.
71. Способ по п.38, в котором температура впрыскивания включает температуру, равную менее чем примерно 20°С.
72. Способ по п.38, в котором температура впрыскивания включает температуру, равную менее чем примерно 15°С.
73. Способ по п.38, в котором температура впрыскивания включает температуру, равную менее чем примерно 10°С.
74. Способ по п.38, в котором температура впрыскивания включает температуру, равную менее чем примерно 5°С.
75. Лекарственное ядро диаметром от примерно 0,32 мм до примерно 0,64 мм и такой длины, чтобы его можно было ввести внутрь имплантата, имплантат такой формы, чтобы его можно было расположить внутри слезного канальца глаза, лекарственное ядро, включающее:
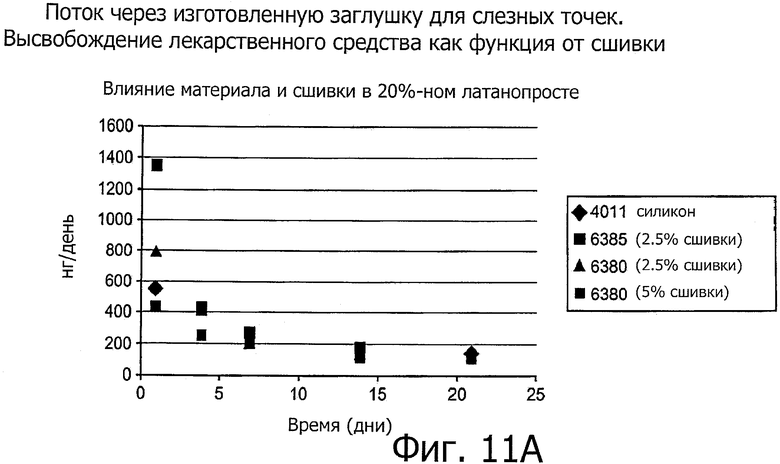
твердый силиконовый матрикс, содержащий включения монодисперсного жидкого латанопроста, существенно однородного размера, для формирования твердого лекарственного матрикса, в котором латанопрост составляет, по меньшей мере, 20 мас.% лекарственного ядра.
76. Лекарственное ядро по п.75, в котором включения жидкого латанопроста имеют средний диаметр, равный менее чем примерно 10 мкм.
77. Лекарственное ядро по п.75, в котором включения жидкого латанопроста имеют средний диаметр, равный менее чем примерно 6 мкм.
78. Лекарственное ядро по п.75, в котором размер существенно однородных включений жидкого латанопроста имеет стандартное отклонение, равное примерно 2 мкм.
79. Лекарственное ядро по п.75, в котором латанопрост составляет, по меньшей мере, 40 мас.% лекарственного ядра.
80. Лекарственное ядро по п.75, в котором латанопрост составляет примерно 50 мас.% лекарственного ядра.
81. Лекарственное ядро по п.75, в котором длина лекарственного ядра равна примерно от 0,85 мм до примерно 0,95 мм.
82. Лекарственное ядро по п.75, в котором длина лекарственного ядра равна примерно 0,95 мм.
83. Лекарственное ядро по п.75, в котором длина лекарственного ядра равна примерно 1,0 мм.
84. Лекарственное ядро по п.75, в котором имплантат представляет собой заглушку для слезного канала.
85. Лекарственная вставка такой формы, чтобы ее можно было расположить внутри имплантата, расположенного внутри слезного канальца глаза, вставка, включающая:
лекарственное ядро, включающее твердый силиконовый матрикс, содержащий включения монодисперсного жидкого латанопроста, существенно однородного размера, для формирования твердого лекарственного матрикса, в котором латанопрост составляет, по меньшей мере, 20 мас.% лекарственного ядра;
оболочку, частично покрывающую лекарственное ядро, оболочку, расположенную над частью лекарственного ядра для ингибирования высвобождения латанопроста из этой части и для того, чтобы отграничить одну или несколько открытых поверхностей.
86. Лекарственная вставка по п.85, в которой включения жидкого латанопроста имеют средний диаметр, равный менее чем примерно 10 мкм.
87. Лекарственная вставка по п.85, в которой включения жидкого латанопроста имеют средний диаметр, равный менее чем примерно 6 мкм.
88. Лекарственная вставка по п.85, в которой размер существенно однородных включений жидкого латанопроста имеет стандартное отклонение, равное примерно 2 мкм.
89. Лекарственная вставка по п.85, в которой латанопрост составляет, по меньшей мере, 40 мас.% лекарственного ядра.
90. Лекарственная вставка по п.85, в которой латанопрост составляет примерно 50 мас.% лекарственного ядра.
91. Лекарственная вставка по п.85, в которой длина лекарственного ядра равна примерно от 0,85 мм до примерно 0,95 мм.
92. Лекарственная вставка по п.85, в которой длина лекарственного ядра равна примерно 0,95 мм.
93. Лекарственная вставка по п.85, в которой длина лекарственного ядра равна примерно 1,0 мм.
94. Лекарственная вставка по п.85, в которой имплантат представляет собой заглушку для слезного канала.
95. Лекарственная вставка по п.85, в которой оболочка включает полиимид.
96. Лекарственная вставка по п.85, в которой одна или несколько открытых поверхностей представляет собой проксимальный конец лекарственной вставки.
97. Лекарственная вставка по п.85, в которой дистальный конец лекарственной вставки запечатан адгезивом, приемлемым для использования в медицине.
98. Имплантат такой формы, чтобы его можно было расположить внутри слезного канальца глаза, имплантат, включающий:
лекарственную вставку, включающую
лекарственное ядро, включающее твердый силиконовый матрикс, содержащий включения монодисперсного жидкого латанопроста, существенно однородного размера, для формирования твердого лекарственного матрикса, в котором латанопрост составляет, по меньшей мере, 20 мас.% лекарственного ядра, и
оболочку, частично покрывающую лекарственное ядро, оболочку, расположенную над частью лекарственного ядра для ингибирования высвобождения латанопроста из этой части и для того, чтобы отграничить одну или несколько открытых поверхностей;
и имплантат, включающий такой канал, приспособленный для приема лекарственной вставки, что латанопрост высвобождается, по меньшей мере, из одной или из одной из нескольких открытых поверхностей в глаз, в котором вставки расположены внутри имплантата и имплантат вставлен в слезный каналец пациента.
99. Имплантат по п.98, в котором включения жидкого латанопроста имеют средний диаметр, равный менее чем примерно 10 мкм.
100. Имплантат по п.98, в котором включения жидкого латанопроста имеют средний диаметр, равный менее чем примерно 6 мкм.
101. Имплантат по п.98, в котором размер существенно однородных включений жидкого латанопроста имеет стандартное отклонение, равное примерно 2 мкм.
102. Имплантат по п.98, в котором латанопрост составляет, по меньшей мере, 40 мас.% лекарственного ядра.
103. Имплантат по п.98, в котором латанопрост составляет примерно 50 мас.% лекарственного ядра.
104. Имплантат по п.98, в котором длина лекарственного ядра равна примерно от 0,85 мм до примерно 0,95 мм.
105. Имплантат по п.98, в котором длина лекарственного ядра равна примерно 0,95 мм.
106. Имплантат по п.98, в котором длина лекарственного ядра равна примерно 1,0 мм.
107. Имплантат по п.98, в котором имплантат представляет собой заглушку для слезного канала.
108. Имплантат по п.98, в котором оболочка включает полиимид.
109. Имплантат по п.98, в котором одна или несколько открытых поверхностей представляет собой проксимальный конец лекарственной вставки.
110. Имплантат по п.98, в котором дистальный конец лекарственной вставки запечатан адгезивом, приемлемым для использования в медицине.
111. Имплантат по п.98, в котором имплантат включает силиконовый полимер.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Дверной звонок | 1926 |
|
SU4980A1 |
Авторы
Даты
2013-04-10—Публикация
2008-09-05—Подача