УРОВЕНЬ ТЕХНИКИ
Область техники
Настоящее изобретение в целом относится к областям имплантируемых офтальмологических устройств, технологии лекарственных форм и способам доставки препаратов в глаз. Конкретнее изобретение относится к имплантируемым офтальмологическим устройствам для длительной доставки терапевтического соединения в глаз.
Описание уровня техники
Глаукома - основная причина слепоты во всем мире. Это заболевание является самой частой причиной нейропатии зрительного нерва.
Самым главным фактором риска глаукомы служит семейный анамнез. Описано несколько различных наследственных форм глаукомы. Первичная врожденная или инфантильная глаукома - наследственное заболевание, которое характеризуется аномальным развитием системы, обеспечивающей отток водянистой влаги из глаза, что ведет к повышенному внутриглазному давлению и повреждению зрительного нерва.
Открытоугольная глаукома - распространенное заболевание, которое характеризуется атрофией зрительного нерва, приводящей к сужению поля зрения и в конце концов к слепоте. Открытоугольную глаукому разделяют на две основные группы по возрасту начала и клинической картине. Ювенильная открытоугольная глаукома (ЮОУГ) обычно проявляется в позднем детстве или вскоре после вступления во взрослую жизнь. Первичная открытоугольная глаукома взрослых (ОУГВ) или глаукома с поздним началом - наиболее распространенный тип глаукомы. ОУГВ протекает мягче и прогрессирует медленнее, чем ЮОУГ, проявляясь в разном возрасте, обычно после 40 лет. ОУГВ приводит к небольшому или умеренному нарастанию внутриглазного давления; регулярно контролируемое лечение часто дает удовлетворительный результат. К сожалению, данное заболевание часто не диагностируется до тех пор, пока не возникнет необратимое повреждение зрительного нерва, потому что ОУГВ прогрессирует постепенно и безболезненно.
Глазная гипертензия - состояние, при котором внутриглазное давление повышено, но явных нарушений зрения нет; считается, что у таких пациентов высок риск потери зрения, вызванной глаукомой. Если глаукома или глазная гипертензия диагностированы рано и быстро назначено лечение препаратами, которые эффективно снижают увеличенное внутриглазное давление, потерю зрения или его прогрессирующее ухудшение обычно удается ослабить. Препараты с доказанной способностью снижать внутриглазное давление включают как средства, которые уменьшают продукцию водянистой влаги, так и средства, которые улучшают ее отток. Такие препараты в целом вводятся одним из двух возможных путей - местно (прямое введение в глаз) или перорально.
Примеры средств, используемых для лечения глаукомы, включают β-блокаторы (например, тимолол, бетаксолол, левобетаксолол, картеолол, левобунолол, пропранолол), ингибиторы карбоангидразы (например, бринзоламид и дорзоламид), α1-антагонисты (например, нипрадолол), α2-агонисты (например иопидин и бримонидин), миотические средства (например, пилокарпин и адреналин), аналоги простагландинов (например, латанопрост, травопрост, унопростон и соединения, указанные в патентах США №5889052; 5296504; 5422368; и 5151444), «гипотензивные липиды» (например, биматопрост и соединения, перечисленные в патенте США №5352708) и нейропротекторы (например, соединения из патента США №4690931, в частности элипродил и R-элипродил, которые упомянуты в заявке на патент США с регистрационным №60/203350, подходящие соединения из WO 94/13275, включая мемантин).
Одним из ограничений местного лечения является недостаточное и непостоянное поступление терапевтического средства в глаз. Например, если в глаз закапываются капли, значительная часть капель может теряться вследствие переливания через край века на щеку.
В попытке улучшить и продлить введение препаратов описаны различные глазные имплантаты, выделяющие лекарственные средства. Например, в патенте США №3949750 раскрыт вкладыш в слезную точку, сделанный из совместимого с тканями, легко стерилизуемого вещества, такого как Тефлон, HEMA, гидрофильный полимер, метилметакрилат, силикон, нержавеющая сталь или другой инертный металлический материал. Заявлено, что вкладыш в слезную точку может быть пропитан офтальмологическим препаратом, или вкладыш в слезную точку может содержать резервуар с офтальмологическим лекарственным средством.
В патенте США №5053030 раскрыт внутриканальцевый имплантат, который может использоваться в качестве носителя или средства для распределения препарата по всему организму. В патенте США №5469867 раскрыт способ обтурации канала, например, слезного канальца, путем инъекции подогретого текучего полимера в канал, после чего полимеру дают возможность охладиться и затвердеть. Полимер может комбинироваться с биологически активным веществом, которое может вымываться из твердого обтуратора, как только он сформировался в канале.
В WO 99/37260 раскрыт вкладыш в слезную точку, сделанный из нерастворимого в воде материала, абсорбирующего влагу, например, из модифицированного HEMA. Также раскрыто, что к веществу, из которого делается вкладыш в слезную точку, может быть добавлен ингибитор воспаления, такой как гепарин.
В патенте США №6196993 раскрыт вкладыш в слезную точку, содержащий антиглаукомный препарат. Препарат содержится в резервуаре внутри вкладыша. Жидкость в резервуаре сообщается с порой, через которую препарат высвобождается в глаз.
В публикации США №2003/0143280 раскрыто применение поддающихся биологическому разложению капсул полимера для лечения глазных болезней, в том числе сухого глаза и глаукомы. Капсулы производятся из любого поддающегося биологическому разложению, биологически совместимого полимера и могут содержать лекарственное средство.
В публикации США №2004/0013704 раскрыты твердые или полутвердые композиции имплантатов, лишенные полимерных ингредиентов. Эти композиции имплантатов делаются из липофильных соединений и могут имплантироваться в любой участок глаза, включая слезную точку или слезный каналец. Заявлено, что имплантат может содержать любое офтальмологическое лекарственное средство, включая антиглаукомные лекарственные средства.
В WO 2004/066980 раскрыто устройство для длительного введения ингибитора карбоангидразы (ИК) в глаз. В одном варианте осуществления у устройства есть внутреннее ядро, содержащее ИК, и внешний полимерный слой. Внешний слой может быть проницаемым, полупроницаемым или непроницаемым для лекарственного средства. Если внешний слой непроницаем для лекарственного средства, он может содержать одно отверстие и более для диффузии ИК.
В публикации США №2005/0232972 раскрыты глазные имплантаты, по меньшей мере на одну поверхность которых нанесены активные средства. В одном варианте осуществления имплантат может содержать полое ядро, заполненное препаратом. В другом варианте осуществления препарат может быть нанесен на одну полимерную ленту и более. Альтернативно, чтобы создать весь вкладыш или имплантат, может использоваться пористый или абсорбирующий материал, который может насыщаться активным средством.
В WO 2006/031658 раскрыты вкладыши в слезный канал, содержащие полимерный компонент и терапевтический компонент. Полимерный компонент может содержать один и более неподдающийся биологическому разложению полимер, один и более поддающийся биологическому разложению полимер или их комбинации. Вкладыш может содержать матрикс, состоящий из полимерного компонента и терапевтического компонента. Вкладыши могут быть покрыты по существу непроницаемым покрытием.
В публикации США №2006/0020248 раскрыто офтальмологическое устройство для введения в слезный канал, которое содержит резервуар для препарата, например, антиглаукомного, антимикробного, противовоспалительного или препарата для лечения синдрома сухого глаза.
Резервуарное устройство для доставки препарата представляет собой устройство, которое содержит емкость или камеру для хранения лекарственного средства. Резервуарные устройства для доставки препарата имеют недостатки, в частности, они сложны для производства, в них трудно достичь однородности препарата (то есть воспроизводимости от устройства к устройству, особенно это справедливо для мелких глазных устройств), прокол устройства грозит выбросом препарата. В матричных устройствах для доставки препарата лекарственное средство диспергировано по полимерному матриксу и высвобождается по мере его растворения либо диффундирует из матрикса. Матричные устройства имеют преимущество над резервуарными устройствами, поскольку их прокол не ведет к выбросу препарата. Недостаток матричных устройств состоит в том, что с их помощью трудно достичь кинетики высвобождения лекарственного средства нулевого порядка. Высвобождение лекарственного средства нулевого порядка или близкое к нулевому порядку высвобождение лекарственного средства желательно, потому что в этом случае скорость высвобождения лекарственного средства не зависит от его начальной концентрации, следовательно, лекарственное средство может высвобождаться на терапевтическом уровне длительное время. Изготовление матричных устройств также может быть сопряжено с трудностями, если лекарственное средство и полимер обрабатывают и экструдируют при повышенной температуре и/или давлении, поскольку в результате активность лекарственного средства может снизиться.
Устройства по настоящему изобретению восполняют имеющиеся пробелы в данной области техники, предлагая матричные устройства, которые достигают кинетики высвобождения лекарственного средства нулевого порядка или близкой к этому кинетики, обычно свойственной резервуарным устройствам, но без риска выброса препарата и производственных трудностей, связанных с резервуарными устройствами.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Один вариант осуществления настоящего изобретения относится к устройству для доставки лекарственного средства, содержащему: (а) корпус, содержащий матрикс из гидрофобного гибкого полимера и терапевтическое соединение; (b) покрытие, расположенное на внешней поверхности первой детали, где покрытие содержит второй неподдающийся биологическому разложению полимер, который по существу непроницаем для терапевтического соединения; и (с) по меньшей мере одну пору, проходящую от внешней поверхности покрытия к верхней части корпуса. Устройствам по настоящему изобретению может быть придана форма для имплантации в любом участке организма субъекта. В конкретных вариантах осуществления устройству придана форма для имплантации в слезную точку, слезный каналец, субконъюнктивальное пространство, переднее субтеноново пространство или в любое другое место, пригодное для высвобождения препарата в глаз субъекта. Например, для того, чтобы доставить терапевтическое соединение в глаз, из устройства по настоящему изобретению может быть сформирован вкладыш в слезную точку, слезный вкладыш или сводчатое устройство.
Гидрофобный гибкий полимер может являться, например, силиконом, полиакрилатом, полиуретаном или комбинацией двух этих полимеров и более. Силикон может быть любым неограниченным силиконом, пригодным для впрыска, прессования или литьевого прессования. Неограничивающие примеры имеющихся в продаже неограниченных силиконов, которые могут использоваться в создании устройств устройства по настоящему изобретению, включают MED-4870, MED-4830, MED-4840, MED-4850, MED-4860 или MED-4880 (NuSil Technology LLC). Неограничивающие примеры полиакрилатов включают полимеры 2-гидроксиэтилметакрилата (HEMA), метакриловой кислоты (МА), метилметакрилата (MMA). Терапевтическое соединение может быть любым терапевтическим соединением при условии, что терапевтическое соединение можно диспергировать или смешать с полимерным матриксом (например, силиконовым матриксом). Дисперсия может состоять из твердых частиц или масла. В конкретных вариантах осуществления терапевтическое соединение представляет собой соединение, которое может применяться для лечения глазного заболевания. Например, терапевтическое соединение может быть антиглаукомным препаратом, антимикробным препаратом, противовоспалительным препаратом или препаратом для лечения синдрома сухого глаза, или терапевтическим соединением, которое может применяться в лечении диабетической ретинопатии или возрастной дегенерации желтого пятна. Высокоактивные офтальмологические средства, такие как простагландины, триамцинолон, 15-HETE (Икомукрет) и римексолон, хорошо подходят для доставки с помощью устройств по настоящему изобретению. Простагландин может представлять собой природный или синтетический простагландин. Неограничивающие примеры простагландинов включают клопростенол, флупростенол, латанопрост, травопрост и унопростон.
В определенных аспектах изобретения концентрация простагландина в матриксе составляет от приблизительно 0,5 мас.% до приблизительно 15 мас.%, от приблизительно 1 мас.% до приблизительно 10 мас.%, от приблизительно 1 мас.% до приблизительно 9 мас.%, от приблизительно 1 мас.% до приблизительно 8 мас.%, от приблизительно 1 мас.% до приблизительно 7 мас.%, от приблизительно 3 мас.% до приблизительно 7 мас.%, от приблизительно 1 мас.% до приблизительно 6 мас.%, от приблизительно 1 мас.% до приблизительно 5 мас.%, от приблизительно 5 мас.% до приблизительно 10 мас.% или от приблизительно 2,5 мас.% до приблизительно 7,5 мас.%.
Покрытие, расположенное на внешней поверхности корпуса устройства, содержит второй неподдающийся биологическому разложению полимер, который по существу непроницаем для терапевтического соединения или по меньшей мере менее проницаем для терапевтического соединения, чем первый неподдающийся биологическому разложению полимер по отношению к терапевтическому соединению. В одном варианте осуществления толщина покрытия составляет от приблизительно 0,5 нанометров (нм) до приблизительно 100 микрометров (мкм), от приблизительно 100 нм до приблизительно 50 мкм, от приблизительно 1 мкм до приблизительно 20 мкм, от приблизительно 5 мкм до приблизительно 15 мкм или от приблизительно 1 мкм до приблизительно 10 мкм. В определенных аспектах изобретения покрытие является париленовым покрытием.
В покрытии вытравливается одна пора и более, чтобы сделать возможным высвобождение терапевтического соединения из матрикса. Размер и/или количество пор может регулироваться, чтобы достичь желаемой скорости высвобождения для конкретного терапевтического средства, находящегося в матриксе. В определенных вариантах осуществления изобретения пора имеет диаметр, который при измерении на уровне внешней поверхности покрытия составляет от приблизительно 1 мкм до приблизительно 100 мкм, от приблизительно 1 мкм до приблизительно 50 мкм или от приблизительно 5 мкм до приблизительно 50 мкм. В определенных вариантах осуществления количество пор составляет от 1 до приблизительно 100000; 1 до приблизительно 20000; от 1 до приблизительно 10000; от 1 до приблизительно 2000; от 1 до приблизительно 1000; от 1 до приблизительно 100; от 1 до приблизительно 50; от 1 до приблизительно 10; от 1 до приблизительно 8; от 1 до приблизительно 5; от приблизительно 5 до приблизительно 100; от приблизительно 5 до приблизительно 10; от приблизительно 10 до приблизительно 100000; от приблизительно 10 до приблизительно 10000; от приблизительно 10 до приблизительно 2000; от приблизительно 10 до приблизительно 1000; от приблизительно 10 до приблизительно 100; от приблизительно 100 до приблизительно 100000; от приблизительно 100 до приблизительно 10000; от приблизительно 100 до приблизительно 2000; или от приблизительно 100 до приблизительно 1000. В определенных аспектах изобретения поры располагаются только на поверхности устройства, которая прилегает к глазу, так что терапевтическое соединение высвобождается в глаз однонаправлено. Например, там, где устройство является вкладышем в слезную точку, пора или поры могут располагаться только на том конце вкладыша в слезную точку, который наиболее близок к передней стороне глаза и соприкасается со слезой.
В определенных аспектах устройства по настоящему изобретению терапевтически эффективная доза терапевтического соединения доставляется субъекту в течение приблизительно 20 дней, приблизительно 30 дней, приблизительно 60 дней, приблизительно 90 дней, приблизительно 120 дней, приблизительно 180 дней, приблизительно 240 дней, приблизительно 300 дней, приблизительно 1 года, приблизительно 2 лет, приблизительно 3 лет, приблизительно 4 лет, приблизительно 5 лет, приблизительно 6 лет, приблизительно 7 лет или приблизительно 8 лет или в течение любого диапазона, выводимого из этого времени. В конкретных вариантах осуществления устройства по настоящему изобретению доставляют терапевтически эффективную дозу терапевтического соединения в течение по меньшей мере 90 дней.
Определенные варианты осуществления настоящего изобретения относятся к устройству для доставки лекарственного средства, содержащему: корпус, содержащий силиконовый матрикс и простагландин, где корпус имеет: стержневидную часть, имеющую первый конец и второй конец, где стержневидной части придана форма для введения через точечное отверстие и размещения в слезной точке или слезном канальце; верхнюю часть, соединенную с первым концом стержневидной части, где верхняя часть сформирована так, чтобы находиться снаружи от слезной точки; и дистальную наконечниковую часть, соединенную со вторым концом стержневидной части; париленовое покрытие на поверхности корпуса; по меньшей мере одну пору в париленовом покрытии, где по меньшей мере одна пора проходит от внешней поверхности париленового покрытия до поверхности верхней части корпуса.
В некоторых вариантах осуществления корпус дополнительно содержит канальцевую надставку, соединенную с дистальной наконечниковой частью, где канальцевой надставке придана форма для введения через точечное отверстие и слезную точку и размещения в слезном канальце. Канальцевая надставка может удовлетворить по меньшей мере двум целям: 1) улучшить задержание вкладыша; и 2) служить дополнительным источником терапевтического соединения. В определенных вариантах осуществления изобретения канальцевая надставка достигает носослезного протока и помещается и в слезном канальце, и в носослезном протоке. В определенных аспектах изобретения канальцевая надставка имеет длину L1, и корпус - длину L2. Отношение длины L1 к L2 может составлять около 0,5:1, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1, 9:1, 10:1, 11:1, 12:1, 13:1, 14:1, 15:1, 16:1, 17:1, 18:1, 19:1, 20:1, 21:1, 22:1, 23:1, 24:1, 25:1, 26:1, 27:1, 28:1, 29:1, 30:1, 50:1 или 100:1, или любой диапазон, выводимый из них. В некоторых вариантах осуществления длина канальцевой надставки составляет от приблизительно 1 миллиметра (мм) до 30 мм, от 1,5 мм до 20 мм, от 2 мм до 15 мм, от 2 мм до 10 мм, от 2 мм до 5 мм, от 5 мм до 15 мм или от 5 мм до 10 мм. В трех предпочтительных вариантах осуществления длина канальцевой надставки составляет 8 мм, 15 мм и 30 мм соответственно. В определенных вариантах осуществления канальцевая надставка дополнительно содержит цельный штифт. Цельный штифт может быть сделан из любого биологически совместимого материала, который придает канальцевой надставке повышенную жесткость. Например, цельный штифт может быть сделан из нержавеющей стали или полимера PEEK (окси-1,4-фениленоокси-1,4-фениленкарбонил-1,4-фенилен).
В определенных вариантах осуществления корпус дополнительно содержит ленту или покрытие из биорасширяемого полимера на всех частях или стержневидной части, дистальном наконечнике и/или канальцевой надставке. Лента или покрытие из биорасширяемого полимера помогут удерживать имплантированное устройство.
Другой вариант осуществления настоящего изобретения относится к способу производства имплантируемого глазного устройства, предусматривающему: (а) экструзию силиконового матрикса и простагландина, чтобы получить корпус, сформированный для имплантации в точку, слезный каналец, субконъюнктивальное пространство или переднее субтеноново пространство; (b) нанесение париленового покрытия на внешнюю поверхность корпуса; и (с) вытравливание по меньшей мере одной поры в париленовом покрытии, причем пора проходит через париленовое покрытие, достигая верхней части корпуса. В определенных аспектах матрикс экструдируют, чтобы образовать вкладыш в слезную точку или сводчатое устройство.
Один вариант осуществления настоящего изобретения относится к способу изготовления устройства для доставки лекарственного средства, предусматривающему: (а) экструзию силиконового матрикса и простагландина, чтобы получить устройство для доставки препарата, содержащее корпус, который имеет: (i) стержневидную часть, имеющую первый конец и второй конец, где стержневидной части придана форма для введения через точечное отверстие и помещения в слезную точку или слезный каналец; (ii) верхнюю часть, соединенную с первым концом стержневидной части, где верхней части придана форма для расположения снаружи от точки; и (iii) дистальную наконечниковую часть, соединенную со вторым концом стержневидной части; (b) нанесение париленового покрытия на поверхность корпуса; и (с) вытравливание по меньшей мере одной поры в париленовом покрытии на поверхности внешней части корпуса, где по меньшей мере одна пора проходит от внешней поверхности париленового покрытия, достигая внешней поверхности верхней части корпуса.
В определенных аспектах изобретения париленовое покрытие наносят используя осаждение из паровой фазы. В конкретных вариантах осуществления пору вытравливают, используя травление кислородной плазмой или травление сфокусированным ионным пучком. В определенных вариантах осуществления париленовое покрытие наносят с толщиной, составляющей от приблизительно 0,5 нанометра (нм) до приблизительно 100 микрометров (нм), от приблизительно 100 нм до приблизительно 50 мкм или от приблизительно 1 мкм до приблизительно 10 мкм. Пора или поры могут быть вытравлены в париленовом покрытии с использованием, например, травления кислородной плазмой или сфокусированного ионного пучка (СИП). В определенных аспектах изобретения отверстие поры является по существу круглым. Количество и размер пор, вытравленных в парилене, могут регулироваться, чтобы достичь желаемой скорости высвобождения простагландина. В определенных аспектах изобретения поры вытравливаются только на поверхности устройства, которая после имплантации устройства будет соприкасаться с глазом. В определенных вариантах осуществления диаметр поры, измеренный на уровне внешней поверхности покрытия, составляет от приблизительно 1 мкм до приблизительно 100 мкм, от приблизительно 1 мкм до приблизительно 50 мкм или от приблизительно 5 мкм до приблизительно 50 мкм. В некоторых вариантах осуществления вытравливаются от 1 до приблизительно 100000; от 1 до приблизительно 10000; от 1 до приблизительно 1000; от 1 до приблизительно 100; от 1 до приблизительно 50; от 1 до приблизительно 10; от 1 до приблизительно 8; от 1 до приблизительно 5; от приблизительно 5 до приблизительно 100; от приблизительно 5 до приблизительно 10; от приблизительно 10 до приблизительно 100000; от приблизительно 10 до приблизительно 10 000; от приблизительно 10 до приблизительно 1000; или от приблизительно 10 до приблизительно 100 пор.
Один вариант осуществления настоящего изобретения относится к способу лечения заболевания глаз у субъекта, предусматривающему: (а) получение имплантируемого глазного устройства для длительного высвобождения препарата в глаз, где устройство содержит: (i) корпус, содержащий матрикс, состоящий из терапевтического средства и силикона; (ii) париленовое покрытие на внешней поверхности корпуса; и (iii) одну пору и более, проходящую от внешней поверхности париленового покрытия до верхней части корпуса; и (b) имплантацию устройства в слезную точку, слезный каналец, субконъюнктивальное пространство или переднее субтеноново пространство субъекта. Имплантируемое глазное устройство может быть, например, вкладышем в слезную точку, слезной канальцевой вставкой или сводчатым устройством.
Конкретные варианты осуществления настоящего изобретения относятся к способу лечения глаукомы или глазной гипертензии у субъекта, предусматривающему: (а) получение устройства для доставки лекарственного средства, содержащего: (i) корпус, содержащий силиконовый матрикс и простагландин, где у корпуса имеется: стержневидная часть, имеющая первый конец и второй конец, где стержневидной части придана форма для введения через точечное отверстие и помещения в слезную точку или слезный каналец; верхнюю часть, соединенную с первым концом стержневидной части, где верхней части придана форма для расположения снаружи от слезной точки; и дистальную наконечниковую часть, соединенную со вторым концом стержневидной части; (ii) париленовое покрытие на поверхности корпуса; (iii) по меньшей мере одну пору в париленовом покрытии, где по меньшей мере одна пора проходит от внешней поверхности париленового покрытия до поверхности верхней части корпуса; (b) имплантацию устройства для введения препарата в слезную точку субъекта, страдающего глаукомой или глазной гипертензией.
В некоторых вариантах осуществления сначала получают поддающиеся биологическому разложению микросферы лекарственного средства, а затем заключают их в силикон, чтобы создать матрикс. Микросферами, микрокапсулами и наносферами (вместе их называют «микросферами») принято считать сферические частицы с диаметром от приблизительно 50 нм до 1000 мкм. Они являются резервуарными устройствами, которые получают используя многочисленные известные способы, в виде ряда различных форм, включая, но не ограничиваясь этим, пористые, полые, покрытые или непокрытые формы с фармацевтически активным средством, включенным в полимерный материал или инкапсулированные посредством такого материала. Такие известные способы включают, но не ограничены этим, распылительную сушку, вращающийся диск и способы эмульсификации. Микросферы можно получить из огромного числа полимерных веществ, выбранных из, но не ограниченных этим, полимолочной кислоты, полигликолевой кислоты, полимолочных - гликолевых кислот, поликапролактонов, триглицеридов, полиэтиленгликолей, полиортоэфиров, полиангидридов, полиэфиров, полимеров целлюлозы и их комбинаций. Количество лекарственного средства, включенного или инкапсулированного в микросферу, как правило, составляет от 0,001% до приблизительно 50%. В этом варианте осуществления заранее образованные микросферы включены в корпус устройства для введения препарата так, что корпус содержит силиконовый матрикс и нагруженные лекарственным средством микросферы. Содержимое микросфер, инкорпорированных в корпус устройства для введения препарата, в целом, составляет от 1% до 50%.
Применение термина «или» в формуле изобретения используется, чтобы обозначить «и/или», если явно не указано, что этот термин относится исключительно к альтернативам, или альтернативы взаимно исключают друг друга.
В данной заявке термин «около» используется, чтобы указать, что значение включает стандартное отклонение ошибки для устройства или способа, используемого для определения показателя.
Следуя длительно существующему патентному закону, артикли «a» и «an» при использовании со словом «содержащий» в формуле или описании изобретения обозначают один и более, если это не оговорено особо.
В этом документе (включая формулу изобретения), термины «содержать» (и любая форма «содержать», например, «содержит» и «содержащий»), «иметь» (и любая форма «иметь», например, «имеет» и «имеющий») и «включать» (и любая форма «включать», например, «включает» и «включающий») являются неограничивающими глаголами-связками.
Другие объекты, особенности и преимущества настоящего изобретения будут очевидны из следующего подробного описания. Однако следует понимать, что подробное описание и конкретные примеры, обозначая конкретные варианты осуществления изобретения, даны только для иллюстрации, поскольку из настоящего подробного описания специалистам в данной области техники станут очевидны различные изменения и модификации, не выходящие за пределы сущности и объема изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Следующие чертежи являются частью настоящего описания изобретения и включены, чтобы дополнительно продемонстрировать определенные аспекты настоящего изобретения в комбинации с подробным описанием иллюстративных вариантов осуществления, представленных ниже.
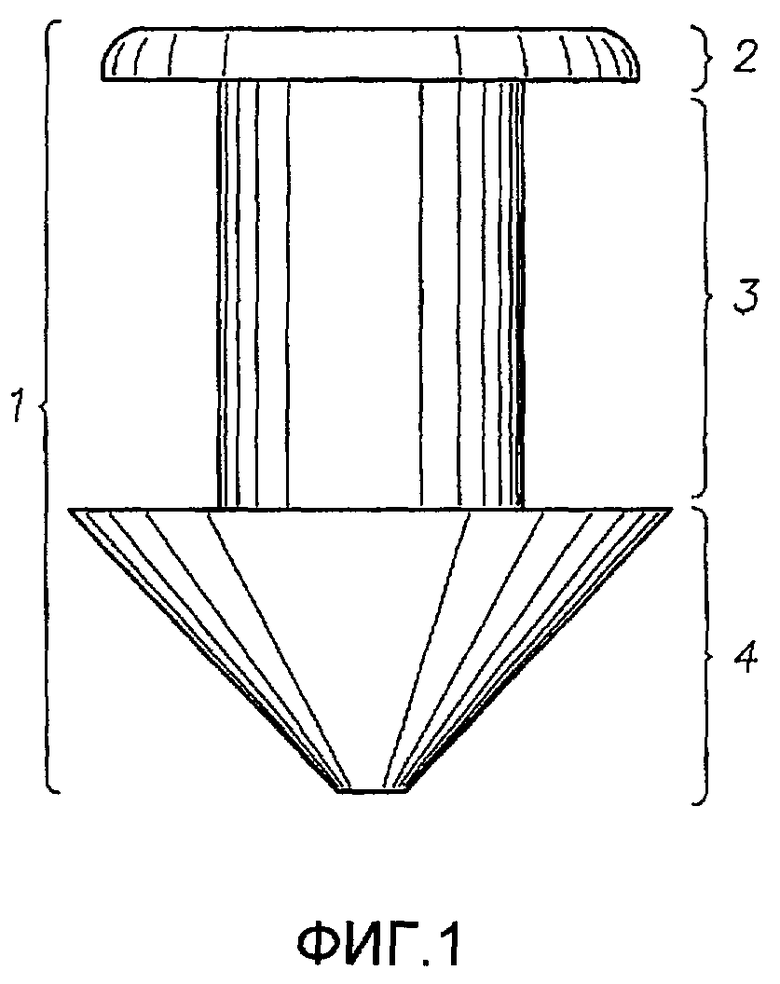
Фиг.1 - вкладыш в слезную точку, вид спереди.
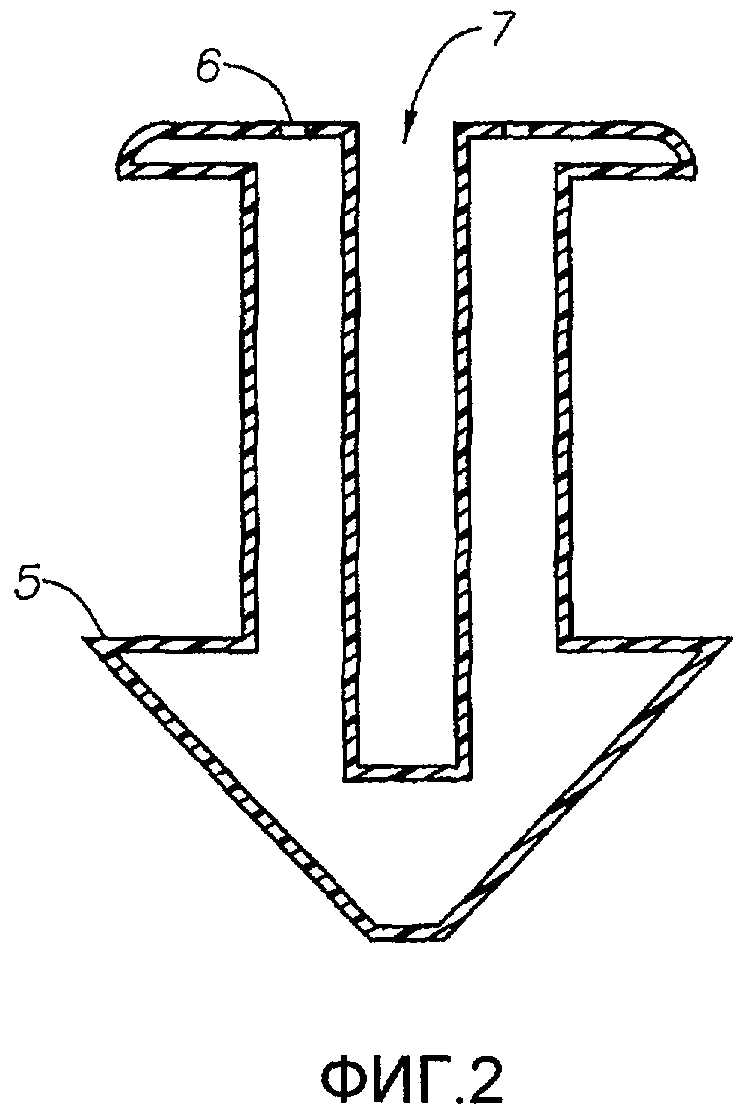
Фиг.2 - поперечный срез вкладыша в слезную точку.
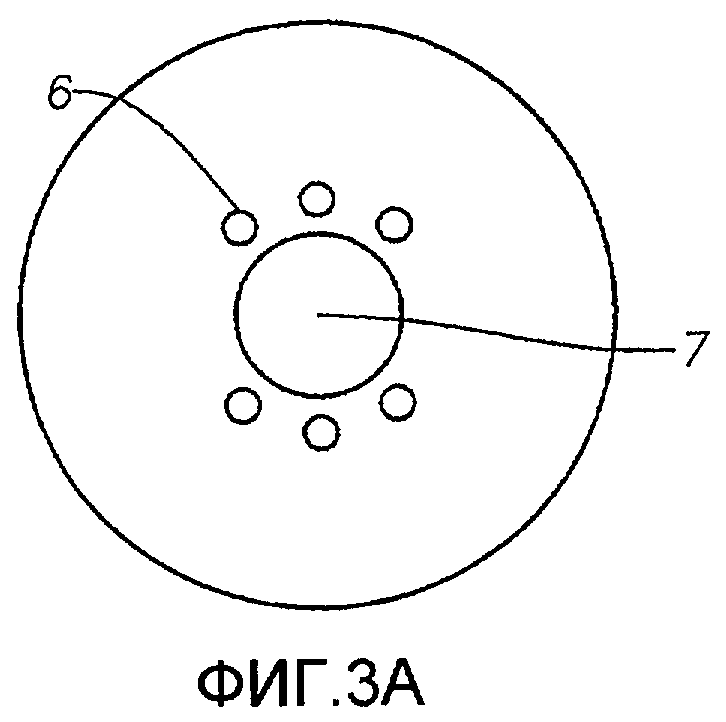
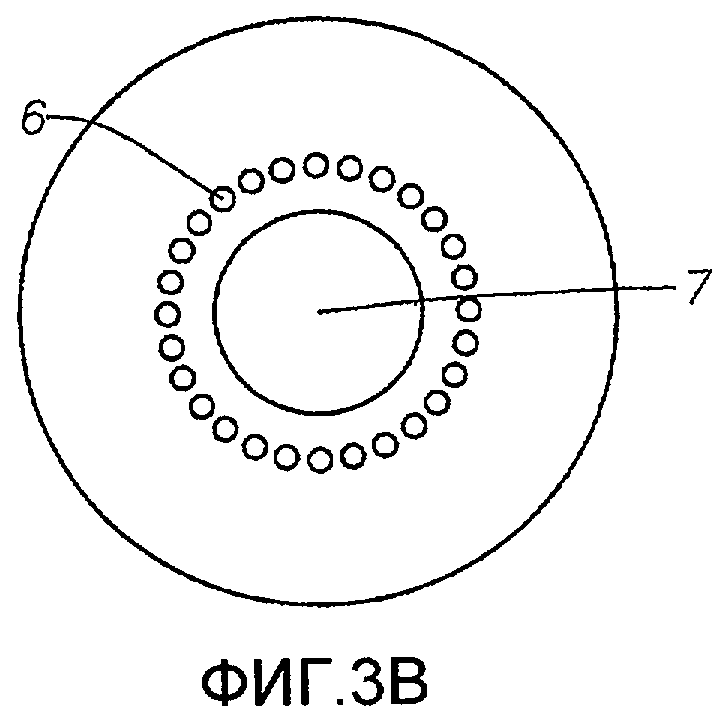
ФИГ.3A и 3B - вкладыши в слезную точку, вид сверху.
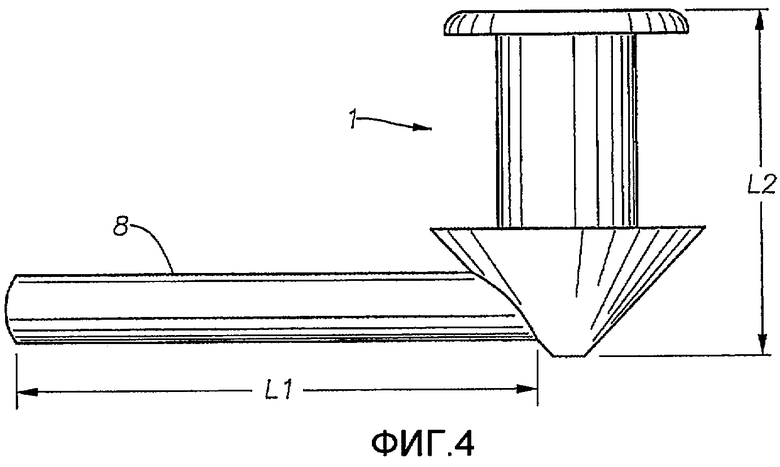
Фиг.4 - изображение вкладыша в слезную точку с канальцевой надставкой.
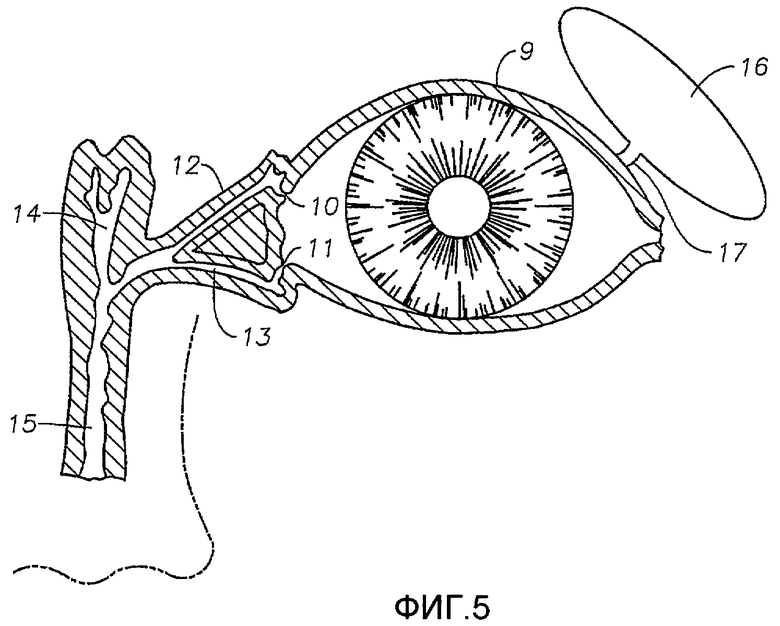
Фиг.5 - изображение системы слезного протока млекопитающего.
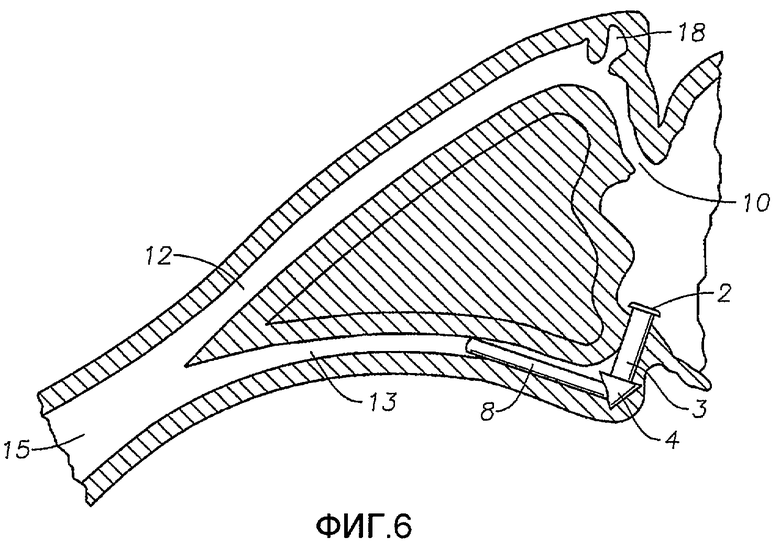
Фиг.6 - изображение одного из настоящих медицинских устройств, помещенных в систему слезного протока млекопитающего.
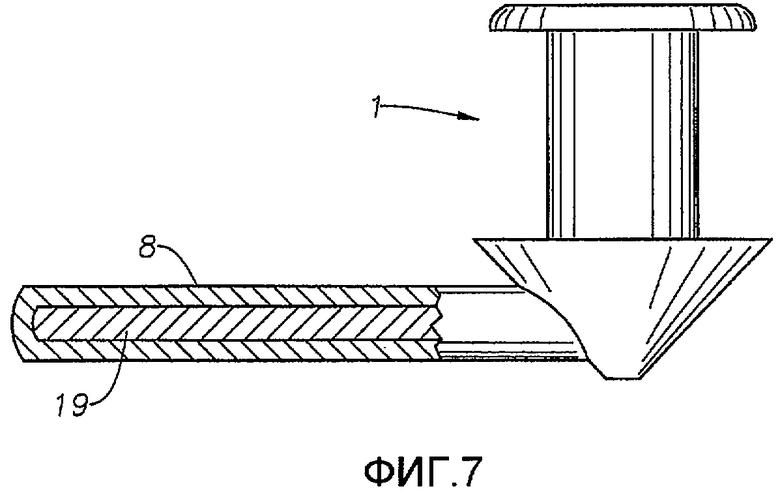
Фиг.7 - частичное поперечное сечение вкладыша в слезную точку с канальцевым надставкой.
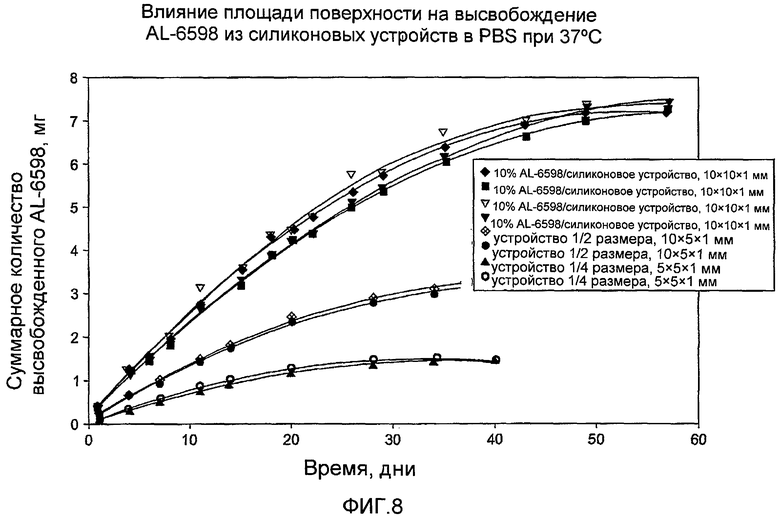
Фиг.8 показывает влияние площади поверхности на высвобождение AL-6598 из силиконовых устройств, помещенных в PBS при 37°C.
ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Силиконовый матрикс и терапевтическое соединение могут подвергаться отливке и отверждению в устройства различной формы, которые применимы в качестве системы введения препарата. Такие устройства могут отливаться в форме, приспособленной для имплантации по существу в любом участке организма субъекта. В конкретных вариантах осуществления силиконовый матрикс и простагландин отлиты в устройство для введения в глаз препарата для лечения глаукомы. В одном варианте осуществления устройство получено экструдированием, в ходе которого смесь лекарственного средства/силикона проталкивается через штамп выдавливания при нагревании, так что отвержденная форма имеет профиль штампа.
Исследования in vitro и in vivo показали, что высвобождение простагландина из монолитных силиконовых устройств определяется площадью поверхности устройства, контактирующей со средой; тем не менее, на профиль высвобождения в небольшой степени влияет и концентрация лекарственного средства. Исследования in vivo также продемонстрировали, что высвобождение простагландина из монолитных силиконовых устройств происходит в несколько раз быстрее, чем ожидалось по результатам испытаний in vitro, и что продолжительность эффективности такого устройства была бы слишком коротка для клинической практики, если только не удастся значительно снизить скорость высвобождения лекарственного средства. Чтобы получить матрикс из терапевтического соединения/силикона с профилем высвобождения лекарственного средства, который применим на практике в качестве имплантируемого офтальмологического устройства, в настоящем изобретении предлагается устройство, содержащее: первую часть, содержащую матрикс из терапевтического соединения и силикона; париленовое покрытие на внешней поверхности первой части; и одну пору и более, проходящую от внешней поверхности париленового покрытия к внешней поверхности первого участника. Наращивание диаметра и/или количества пор увеличит подтвержденную воздействию площадь поверхности матрикса и, таким образом, повысит скорость, с которой высвобождается терапевтическое соединение. Матрикс необязательно включает поддающиеся биоразложению микросферы, содержащие лекарственное средство, чтобы обеспечить дополнительный контроль скорости высвобождения лекарственного средства из матрикса.
Предпочтительно устройства по настоящему изобретению приводят к нулевому или близкому к нулевому порядку профилю высвобождения лекарственного средства. В реакции нулевого порядка скорость реакции представляет собой константу. Когда ключевой компонент реакции полностью потреблен, реакция резко останавливается. (Дифференциальный закон скорости: r=k; единицей измерения константы скорости k является моль·л-1·с-1). Этим отличаются реакции первого и второго порядка: при реакции первого порядка скорость реакции прямо пропорциональна концентрации только одного из реагентов, и поскольку реагент потребляется во время реакция, концентрация падает, а вслед за ней - и скорость реакции. (Дифференциальный закон скорости: r=k [A]; единица измерения константы скорости k-с-1). При реакции второго порядка скорость реакции прямо пропорциональна квадрату концентрации одного из реагентов (или концентрации двух реагентов первого порядка) и быстро уменьшается (быстрее линейной зависимости) по мере того, как концентрация реагента снижается (Дифференциальный закон скорости: r=k [A]2 или r=k [A][B]; единица измерения константы скорости k-моль·л-1·с-1). Близкий к нулевому порядку профиль описывает ситуацию, при котором возможен начальный короткий период, когда реакция, как представляется, следует более сложной кинетике, но затем возвращается к кинетике нулевого порядка на протяжении большей части высвобождения лекарственного средства. Обычно это относится к устройствам, у которых имеется начальный всплеск высвобождения лекарственного средства - реакция имеет начальную скорость, которая представляется меняющейся, но затем становится постоянной в течение большей части времени высвобождения.
В одном варианте осуществления настоящие устройства и системы представляют собой имплантируемое глазное устройство, сформированное в виде вкладыша для введения в слезную точку и/или слезный каналец глаза. Фиг.5 иллюстрирует систему слезного протока в глазу млекопитающего 9. Система включает нижнюю слезную точку 11, связанную с нижним слезным канальцем 13, и верхнюю слезную точку 10, связанную с верхним слезным канальцем 12. Канальцы 12 и 13 связаны со слезным мешком 14 и носослезным протоком 15. Слезная железа 16 связана с глазом 9 посредством слезного протока 17. В целом, слеза выделяется слезной железой 16 и поступает в глаз 9 посредством слезных протоков 17, и слеза отводится из глаза 9 с помощью слезной точки 10 и канальца 12, слезной точки 11 и канальца 13, и носослезного протока 15.
Ряд вкладышей для введения в слезные точки 10 и 11 и/или канальцы 12 и 13 известен в данной области техники. Вкладыши в слезные точки описаны, например, в патентах США №3949750; 5283063; 4915684; 4959048; 5723005; 6149684; 6290684; 5417651; 5423777; 5741292; 6027470; 5830171; 6016806; 6041785; 6234175; 6306114; и 6344047; каждый из которых включен посредством ссылки.
Одно из устройств для введения лекарственного средства по настоящему изобретению изображено на фиг.1-3. Устройство для доставки препарата включает: (а) корпус 1, содержащий силиконовый матрикс и простагландин, где корпус имеет внешнюю поверхность, и эта поверхность сформирована для введения через точечное отверстие и размещения в слезных точках 10 или 11 или слезных канальцах 12 или 13; (b) париленовое покрытие 5 на части внешней поверхности корпуса 1; и (с) по меньшей мере одну пору 6 в париленовом покрытии 5, где пора 6 проходит от внешней поверхности париленового покрытия 5 до верхней поверхности корпуса 1.
В одном варианте осуществления матрикс содержит силикон и нагруженные лекарственным средством микросферы, подверженные биоразложению.
Вкладыш в слезную точку типично включает корпус 1, имеющий проксимальную верхнюю часть 2, дистальную наконечниковую часть 4 и стержневидную часть 3, соединяющую проксимальную верхнюю часть 2 с дистальной наконечниковой частью 4. Поперечный размер стержневидной части 3 нередко меньше, чем проксимальной верхней части 2 и самого широкого участка дистальной наконечниковой части 4. Вкладыш в слезную точку обычно вводят, начиная с дистального наконечника, в точечное отверстие и продвигают дистально в точке 10 или 11, пока ближайшая верхняя часть 2 не достигнет точечного отверстия. Вкладыши в слезную точку можно сделать разных размеров, соответствующих анатомическим точкам и канальцам различных поперечных размеров. Проксимальная верхняя часть 2 обычно больше, чем отверстие точки, так что проксимальная верхняя часть 2 не проходит через отверстие точки и остается обнаженной в глазу 9. Поперечный размер дистальной наконечниковой части 4 типично таков, чтобы заполнить точки 10 или 11 и фиксировать вкладыш 1 на месте. Окклюзия, созданная вкладышем в слезной точке 1, мешает оттоку слезы из глаза 9 через слезную точку и соответствующий канальцевый канал. Вкладыш в слезную точку 1 может частично или полностью закрыть просвет точки 10 или 11. Вкладыши в слезную точку типично имплантируют в глаз, используя инструменты для введения (например, канюлю), поэтому вкладыши в слезную точку могут иметь осевой канал 7, легко зацепляемый инструментами для введения, для облегчения или направления имплантации.
Устройство для доставки препарата по настоящему изобретению также может быть сформировано как внутриканальцевый имплантат. Внутриканальцевые имплантаты, которые располагаются полностью внутри канала без выступания или протрузии из глаза, описаны, например, в патентах США №4660546; 5049142; и 5053030; 5163959; и 5171270, каждый из которых включен посредством ссылки.
Вкладыш в слезную точку или внутриканальцевый имплантат по настоящему изобретению также могут содержать канальцевую надставку 8, которая входит в каналец 12 или 13. Длина канальцевой надставки может быть такова, что она также достигает носослезного протока 15. Канальцевая надставка увеличивает объем матрикса и тем самым количество терапевтического соединения в устройстве. Канальцевая надставка 8 также служит, чтобы улучшить удержание имплантированного устройства. Кроме того, увеличенный размер устройства с канальцевой надставкой увеличивает вероятность того, что пациент заметит смещение устройства из точки. Одно из устройств для введения препарата, содержащее канальцевую надставку, приведено на Фиг.4. На Фиг.6 показано введение препарата, когда канальцевая надставка помещена в систему слезного протока. В определенных вариантах осуществления канальцевая надставка содержит цельный штифт 19, как показано на частичном поперечном сечении на Фиг.7.
Имплантируемые офтальмологические устройства по настоящему изобретению могут использоваться для местной доставки офтальмологических лекарств, включая, например, антиглаукомные средства, средства против глазной гипертензии, антимикробные средства, противовоспалительные средства или средства для лечения синдрома сухого глаза. В одном варианте осуществления терапевтическое соединение является простагландином. Простагландин может быть природным или синтетическим простагландином. Простагландины - это производные метаболитов арахидоновой кислоты. Арахидоновая кислота в организме превращается в простагландин G2, который впоследствии конвертируется в простагландин H2. Другие встречающиеся в природе простагландины - производные простагландина H2. В данной области техники известны различные типы простагландинов, включая A, B, C, D, E, F, G, I и J (EP 0561073 A1). Неограничивающие примеры простагландинов включают клопростенол, флупростенол, латанопрост, травопрост и унопростон.
Устройства по настоящему изобретению покрыты неподдающимся биологическому разложению полимером 5, чтобы уменьшить площадь открытой поверхности матрикса. В некоторых вариантах осуществления настоящего изобретения покрытие представляет собой парилен. Парилен гибок, гидрофобен, по существу непроницаем для простагландинов, очень устойчив к химическим веществам и может быть нанесен на поверхности осаждением из паровой фазы с высокими согласованностью и постоянством. Парилен также отвечает требованиям класса VI FDA и используется в устройствах для медицинского применения, чтобы покрывать такие имплантаты, как кардиостимуляторы и шунты. Парилен - родовое название для полимеров уникальной серии. Начальный представитель серии, названный Париленом N, является поли-пара-ксилиленом - линейным, высококристаллическим веществом. Другие представители серии включают Парилен C, Парилен D и Парилен F.
Способы нанесения париленового покрытия на силикон известны в данной области техники. Например, париленовое покрытие может быть осаждено на силиконовое устройство по настоящему изобретению из паровой фазы путем помещения устройства в камеру для вакуумного осаждения и создания в ней вакуума до приблизительно 0,1 торр. Димер парилена (ди-пара-ксилилен) испаряется приблизительно при 150°C. Затем осуществляют пиролиз мономера (пара-ксилилена) приблизительно при 680°C и 0,5 торр. После этого мономер поступает в камеру для осаждения приблизительно при комнатной температура (около 25°C), адсорбируется и полимеризируется на силиконовом устройстве. Полученное в результате покрытие конформно, покрывает все подвергнутые воздействию поверхности в одинаковой степени.
Париленовое покрытие может наноситься слоями толщиной от приблизительно 0,5 нм до нескольких миллиметров. Как только покрытие нанесено на имплантируемое глазное устройство, в покрытии можно вытравить одну пору и более, чтобы сделать возможным высвобождение терапевтического соединения из матрикса, создав отверстие в покрытии, через которое терапевтическое соединение может диффундировать. Альтернативно поры могут быть созданы во время процесса нанесения парилена путем изоляции поверхности устройства в местах, в которых поры желательны. Размер и/или количество пор могут регулироваться, чтобы достичь желаемой скорости высвобождения для конкретного терапевтического средства в матриксе. Как упоминалось выше, высвобождение терапевтического соединения из силиконового матрикса определяется площадью открытой поверхности матрикса. Таким образом, увеличение размера и/или числа пор увеличит обнаженную площадь поверхности матрикса и таким образом повысит скорость, с которой терапевтическое соединение высвобождается из матрикса. Кроме того, поры могут быть созданы на таком устройстве, что терапевтическое соединение будет высвобождаться в глаз однонаправлено. Например, если устройство - вкладыш в слезную точку, пора или поры будут расположены на верхней части вкладыша в слезную точку, которая подвергается воздействию слезы.
Поры могут быть вытравлены в покрытии устройства путем использования, например, СИП или травления кислородной плазмой (см. например, Meng and Tai, 2005; включенный посредством ссылки). Предпочтительно поры вытравливают на по существу плоской поверхности устройства, поскольку это делает процесс травления более постоянным. В СИП используется сфокусированный поток ионов галлия, уносящий атомы с поверхности протравливаемого материала. Поскольку парилен не является проводящим, сталкивающиеся ионы галлия имеют тенденцию постепенно «заряжать» слой парилена, что может в конечном счете ингибировать создание пор. Чтобы преодолеть этот эффект заряжания, поверхность парилена можно покрыть тонким слоем проводящего вещества (например, металла или углерода) или привести во временный контакт с проводящим материалом. У СИП имеется гауссов профиль. В результате боковые стенки проделанных отверстий наклонены (то есть чем глубже отверстие, тем меньше его диаметр). На основе исследования травления с помощью СИП слоя парилена толщиной 5 мкм, нанесенного на силиконовый кубик, определено, что для формирования поры, полностью пронизывающей слой парилена, требуется отношение ниже примерно 5:1 (например, через слой парилена толщиной 5 мкм проходит пора диаметром 1 мкм, измеренным на наружной поверхности париленового покрытия).
Травление кислородной плазмой представляет собой процесс сухого травления, который проходит в среде кислородной плазмы, где образуются радикалы кислорода. Типичные условия для травления кислородной плазмой включают: давление кислорода от приблизительно 10 до приблизительно 500 миллиторр и мощность RF - от приблизительно 100 до приблизительно 200 Вт. Другой способ травления пор в покрытии устройства заключается в использовании сканирующего электронного микроскопа.
Следующие примеры включены, чтобы продемонстрировать предпочтительные варианты осуществления изобретения. Специалистам в данной области техники будет ясно, что способы, раскрытые в нижеследующих примерах, представляют собой методы, которые, как обнаружил изобретатель, хорошо функционируют при практическом осуществлении изобретения и, таким образом, могут считаться составляющими предпочтительные способы его осуществления. Однако в свете настоящего раскрытия специалисты в данной области техники должны понять, что в раскрытых конкретных вариантах осуществления можно сделать множество изменений, и, тем не менее, получить подобный или схожий результат, не отступая от сущности и объема изобретения.
ПРИМЕР 1
Высвобождение простагландина из силиконового матрикса определяется площадью поверхности матрикса, подвергнутой воздействию среды
Чтобы изучить влияние площади поверхности на высвобождении простагландина из силиконового матрикса, измерили высвобождение простагландина из силиконовых кубиков трех различных размеров. Наибольший силиконовый кубик имел размер 10 мм × 10 мм × 1 мм. В настоящем исследовании также использовались устройства размером 1/2 (10 мм × 5 мм × 1 мм) и 1/4 (5 мм × 5 мм × 1 мм). Каждый силиконовый кубик содержал 10% AL-6598, который является аналогом простагландина класса DP. Силиконовые кубики поместили в физиологический раствор с фосфатным буфером (PBS) при температуре 37°C и измерили количество высвобожденного AL-6598. Как показано в Фиг.8, высвобождение AL-6598 зависело от размера силиконового кубика: более обширная площадь поверхности приводила к более быстрому высвобождению лекарственного средства.
ПРИМЕР 2
Париленовые покрытия и травление
Два силиконовых кубика (10 мм × 10 мм × 1 мм) покрыли 5 мкм парилена, используя способ осаждения из паровой фазы. Чтобы покрыть силиконовый кубик, его помещали в камеру для вакуумного осаждения и создавали вакуум глубиной примерно 0,1 торр. Димер парилена (ди-пара-ксилилен) испаряли при температуре приблизительно 150°C. Затем проводили пиролиз мономера (пара-ксилилена) при температуре около 680°C и вакууме 0,5 торр. После этого мономер поступал в камеру для осаждения примерно при комнатной температуре (около 25°C), адсорбировался и полимеризировался на силиконовом кубике.
Покрытый париленом силиконовый кубик после этого обрабатывали СИП. На одном из кубиков в слое парилена толщиной 5 мкм были сделаны поры диаметром 1 и 1,5 мкм. На создание каждой поры ушло до 30 с. Для предупреждения «эффекта заряжания» париленового слоя сталкивающимися с ним атомами галлия в процессе СИП на поверхность парилена нанесли слой металла толщиной 1000 Å. СИП имел гауссов профиль, в результате чего боковые стенки пор оказались наклонными. Чтобы определить самый мелкий размер поры, которую можно проделать в парилене, множественные поры диаметром 0,5 мкм, 1 мкм, 1,5 мкм, 3 мкм и 5 мкм были созданы в слое парилена толщиной 5 мкм, нанесенном на другой кубик. Пора диаметром 0,5 мкм не полностью прошла через слой парилена из-за наклоненных стенок, в то время как поры диаметром 1 мкм и более полностью пронизывали слой парилена. Из этого исследования можно заключить, что поры с соотношением менее 5:1 могут быть проделаны в слое парилена, используя СИП.
ПРИМЕР 3
Вкладыши в слезную точку, содержащие микросферы
Травопрост был получен в виде микросфер с полимолочной кислотой со средним диаметром 100 нм-1 мкм. Микросферы содержат 10 мас.% травопроста. 10 г нагруженных лекарственным средством микросфер добавили к 45 г силикона (часть А) в первой трубке для прессования Semco и смешивали в смесители Flack Tek при 1500 об/мин в течение 30 с. 45 г силикона (часть B) добавили к второй трубке для прессования Semco. Обе трубки для прессования поместили в блок впрыскивания пресса для силикона и впрыснули в стальную форму, чтобы получить силиконовый кубик с желаемой формой и размерами вкладыша в слезную точку. После отверждения силиконовое устройство покрыли париленом и подвергли травлению согласно процедурам, описанным в примере 2.
В свете настоящего раскрытия все композиции и способы, раскрытые и заявленные в данном документе, могут быть получены и выполнены без ненужного экспериментирования. Хотя устройства и способы по настоящему изобретению описаны, исходя из конкретных вариантов осуществления, специалистам в данной области техники будет очевидно, что в устройствах и способах, а также в стадиях или в последовательности стадий способов, описанных в данном документе, могут быть сделаны изменения, не отступая от идеи, сущности и объема изобретения. А именно, будет очевидно, что определенные агенты, близкие и химически, и физиологически, можно заменить на агенты, описанные здесь, что даст сходные результаты. Все такие подобные замены и модификации, очевидные специалистам в данной области техники, считаются находящимися в пределах сущности, объема и идеи изобретения, определенных прилагаемой формулой изобретения. Прилагаемая формула изобретения не должна интерпретироваться как включающая ограничения способов и функции, если такое ограничение явно не изложено в данном пункте, с использованием фразу(ы) «способ» и/или «стадия» соответственно.
ССЫЛКИ
Следующие ссылки в том объеме, в котором они предоставляют типовые процедурные или другие детали, дополняющие описанные в данном документе, конкретно включены в настоящий документ посредством ссылки:
патент США 3949750
патент США 4660546
патент США 4690931
патент США 4915684
патент США 4959048
патент США 5049142
патент США 5053030
патент США 5151444
патент США 5163959
патент США 5171270
патент США 5283063
патент США 5296504
патент США 5352708
патент США 5417651
патент США 5422368
патент США 5423777
патент США 5469867
патент США 5723005
патент США 5741292
патент США 5830171
патент США 5889052
патент США 6016806
патент США 6027470
патент США 6041785
патент США 6149684
патент США 6196993
патент США 6234175
патент США 6290684
патент США 6306114
патент США 6344047
патент США 60/203350
публикация патента США 2003/0143280
публикация патента США 2004/0013704
публикация патента США 2005/0232972
публикация патента США 2006/0020248
Заявка PCT WO 2004/066980
Заявка PCT WO 2006/031658
Заявка PCT WO 94/13275
Заявка PCT WO 99/37260
EP 0561073 A1
Meng and Tai, «Parylene Etching Techniques for Microfluidics and BioMEMS,» Micro Electro Mechanical Systems, 30:568-571, 2005.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИМПЛАНТАТЫ НАЗОЛАКРИМАЛЬНОЙ ДРЕНАЖНОЙ СИСТЕМЫ ДЛЯ МЕДИКАМЕНТОЗНОЙ ТЕРАПИИ | 2007 |
|
RU2414199C2 |
| ЛЕКАРСТВЕННЫЕ ЯДРА ДЛЯ ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ | 2008 |
|
RU2478366C2 |
| ПРОБКА ДЛЯ СЛЕЗНОЙ ТОЧКИ С ПОДКЛЮЧЕННОЙ К ИСТОЧНИКУ ПИТАНИЯ МАТРИЦЕЙ ИЗ УДЕРЖИВАЮЩИХ ЯЧЕЕК | 2013 |
|
RU2630601C2 |
| НЕИНВАЗИВНАЯ МЕТОДИКА ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА С ПОМОЩЬЮ ГЛАЗНОГО ВКЛАДЫША | 2017 |
|
RU2749426C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОВЫШЕННОГО ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ С ПОМОЩЬЮ ВНУТРИГЛАЗНОЙ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ | 2014 |
|
RU2664686C2 |
| СНИЖЕНИЕ ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ ПРИ ПОМОЩИ ВНУТРИКАМЕРНЫХ ИМПЛАНТАТОВ БИМАТОПРОСТА | 2011 |
|
RU2586298C2 |
| ОФТАЛЬМОЛОГИЧЕСКАЯ СИСТЕМА ДЛЯ ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА В ГЛАЗУ | 2013 |
|
RU2652063C2 |
| ОФТАЛЬМОЛОГИЧЕСКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2016 |
|
RU2734344C2 |
| ВНУТРИМАТОЧНАЯ СИСТЕМА ДЛЯ ЛЕЧЕБНОГО ИСПОЛЬЗОВАНИЯ | 2010 |
|
RU2529477C2 |
| СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА ВНУТРЬ ГЛАЗА | 2007 |
|
RU2440102C2 |
Настоящее изобретение относится к имплантируемым офтальмологическим устройствам для длительного высвобождения лекарственного средства в глаз, а также к способам изготовления и применения таких устройств. Один вариант осуществления настоящего изобретения относится к устройству, содержащему: (а) основную часть, содержащую матрикс, состоящий из простагландина и силикона; (b) париленовое покрытие на внешней поверхности основной части; и (с) одну и более пору, расположенную на конце корпуса, который является наиболее близким к передней стороне глаза, где указанная пора проходит от внешней поверхности париленового покрытия до поверхности верхней части корпуса. 3 н. и 20 з.п. ф-лы, 3 прим., 8 ил.
1. Устройство для доставки лекарственного средства, содержащее:
(a) корпус, содержащий силиконовый матрикс и офтальмологическое лекарственное средство, где корпус имеет внешнюю поверхность, и корпусу придана такая форма, чтобы его можно было ввести через точечное отверстие и поместить в слезную точку или слезный каналец;
(b) париленовое покрытие на части внешней поверхности корпуса; и
(c) по меньшей мере, одну пору в париленовом покрытии, расположенную на конце корпуса, который является наиболее близким к передней стороне глаза, где указанная, по меньшей мере, одна пора проходит от внешней поверхности париленового покрытия до поверхности верхней части корпуса.
2. Устройство по п.1, где корпус содержит:
(a) стержневидную часть, имеющую первый конец и второй конец, где стержневидной части придана форма для введения через точечное отверстие и размещения в слезной точке или слезном канальце;
(b) верхнюю часть, соединенную с первым концом стержневидной части, где верхней части придана такая форма, чтобы она могла разместиться снаружи от слезной точки; и
(c) дистальную наконечниковую часть, соединенную со вторым концом стержневидной части.
3. Устройство по п.1, где офтальмологическое лекарственное средство является простагландином, триамцинолоном, икомукретом или римексолоном.
4. Устройство по п.3, где офтальмологическое лекарственное средство является простагландином.
5. Устройство по п.4, где простагландин является клопростенолом, флупростенолом, латанопростом, травопростом или унопростоном.
6. Устройство по п.1, где концентрация простагландина в матриксе составляет от приблизительно 1 мас.% до приблизительно 10 мас.%.
7. Устройство по п.1, где концентрация простагландина в матриксе составляет от приблизительно 3 мас.% до приблизительно 7 мас.%.
8. Устройство по п.1, где толщина париленового покрытия составляет от приблизительно 1 мкм до приблизительно 20 мкм.
9. Устройство по п.1, где толщина париленового покрытия составляет от приблизительно 5 мкм до приблизительно 15 мкм.
10. Устройство по п.2, где корпус дополнительно содержит канальцевую надставку, прикрепленную к дистальной наконечниковой части корпуса, где канальцевой надставке придана форма для введения через точечное отверстие и слезную точку и размещения в слезном канальце.
11. Устройство по п.10, где длина канальцевой надставки составляет L1, и длина корпуса-L2, и где отношение длин L1 и L2 равно от приблизительно 2:1 до приблизительно 10:1.
12. Устройство по п.10, где канальцевая надставка сформирована для помещения как в слезный каналец, так и носослезный проток.
13. Способ изготовления устройства для доставки лекарственного средства, содержащий следующие стадии:
(а) экструдирование силиконового матрикса и офтальмологического лекарственного средства с образованием устройства для доставки лекарственного средства, содержащего корпус, у которого имеется:
(i) стержневидная часть, имеющая первый конец и второй конец, где стержневидной части придана форма для введения через точечное отверстие и помещения в точку или слезный каналец;
(ii) верхняя часть, соединенная с первым концом стержневидной части, где верхней части придана форма для размещения снаружи от точки; и
(iii) дистальная наконечниковая часть, соединенная со вторым концом стержневидной части;
(b) нанесение париленового покрытия на поверхность корпуса; и
(c) вытравливание, по меньшей мере, одной поры в париленовом покрытии на поверхности внешней части корпуса, расположенную на конце корпуса, который является наиболее близким к передней стороне глаза, где указанная, по меньшей мере, одна пора проходит от внешней поверхности париленового покрытия до поверхности верхней части корпуса.
14. Способ по п.13, где нанесение париленового покрытия содержит осаждение из паровой фазы.
15. Способ по п.13, где по меньшей мере одну пору вытравливают с использованием травления кислородной плазмой.
16. Способ по п.13, где париленовое покрытие наносят с толщиной от приблизительно 1 мкм до приблизительно 20 мкм.
17. Способ по п.13, где париленовое покрытие наносят с толщиной от приблизительно 5 мкм до приблизительно 15 мкм.
18. Способ по п.13, где диаметр по меньшей мере одной поры составляет от приблизительно 1 мкм до приблизительно 50 мкм.
19. Способ по п.13, где вытравливают от 1 до приблизительно 1000 пор.
20. Способ лечения глаукомы или глазной гипертензии у субъекта, содержащий:
(а) получение устройства для доставки лекарственного средства, содержащего:
(i) корпус, содержащий силиконовый матрикс и простагландин, где у корпуса имеется стержневидная часть, имеющая первый конец и второй конец, где стержневидной части придана форма для введения через точечное отверстие и помещения в слезную точку или слезный каналец; верхнюю часть, соединенную с первым концом стержневидной части, где верхняя часть сформирована так, чтобы она могла находиться снаружи от слезной точки; и дистальную наконечниковую часть, соединенную со вторым концом стержневидной части;
(ii) париленовое покрытие на поверхности корпуса;
(iii) по меньшей мере, одну пору в париленовом покрытии, расположенную на конце корпуса, который является наиболее близким к передней стороне глаза, где указанная, по меньшей мере, одна пора проходит от внешней поверхности париленового покрытия до поверхности верхней части корпуса;
(b) имплантацию устройства для введения лекарственного средства в слезную точку субъекта, больного глаукомой или глазной гипертензией.
21. Способ по п.20, где простагландин является клопростенолом, флупростенолом, латанопростом, травопростом или унопростоном.
22. Способ по п.20, где концентрация простагландина в матриксе составляет от приблизительно 1 мас.% до приблизительно 10 мас.%.
23. Способ по п.20, где концентрация простагландина в матриксе составляет от приблизительно 3 мас.% до приблизительно 7 мас.%.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Устройство для регулирования внутриглазного давления при глаукоме | 1988 |
|
SU1671295A1 |
| WO 2005121735 A2, 22.12.2005 | |||
| US 6196993 B1, 06.03.2001. | |||
Авторы
Даты
2012-08-27—Публикация
2008-01-30—Подача