Текст описания приведен в факсимильном виде.














































| название | год | авторы | номер документа |
|---|---|---|---|
| ИМПЛАНТАТЫ НАЗОЛАКРИМАЛЬНОЙ ДРЕНАЖНОЙ СИСТЕМЫ ДЛЯ МЕДИКАМЕНТОЗНОЙ ТЕРАПИИ | 2007 |
|
RU2414199C2 |
| ВНУТРИГЛАЗНЫЕ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ И СПОСОБЫ ЛЕЧЕНИЯ ГЛАЗНЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2532333C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОВЫШЕННОГО ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ С ПОМОЩЬЮ ВНУТРИГЛАЗНОЙ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ | 2014 |
|
RU2664686C2 |
| ВНУТРИКАМЕРНЫЕ ИМПЛАНТАТЫ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ ТЕРАПЕВТИЧЕСКОГО АГЕНТА | 2011 |
|
RU2565445C2 |
| ЛЕКАРСТВЕННЫЕ ЯДРА ДЛЯ ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ | 2008 |
|
RU2478366C2 |
| СНИЖЕНИЕ ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ ПРИ ПОМОЩИ ВНУТРИКАМЕРНЫХ ИМПЛАНТАТОВ БИМАТОПРОСТА | 2011 |
|
RU2586298C2 |
| ОФТАЛЬМОЛОГИЧЕСКАЯ СИСТЕМА ДЛЯ ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА В ГЛАЗУ | 2013 |
|
RU2652063C2 |
| СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА ВНУТРЬ ГЛАЗА | 2007 |
|
RU2440102C2 |
| ВКЛАДЫШИ В СЛЕЗНУЮ ТОЧКУ И СПОСОБЫ ДОСТАВКИ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ | 2008 |
|
RU2459646C2 |
| ВНУТРИГЛАЗНЫЕ ИМПЛАНТАТЫ, СОДЕРЖАЩИЕ ПРОСТАМИД, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2650614C2 |
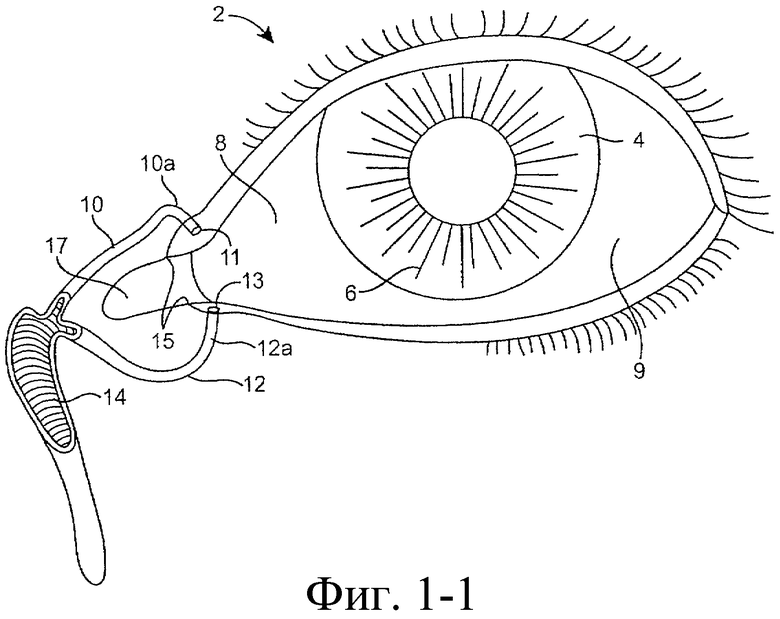
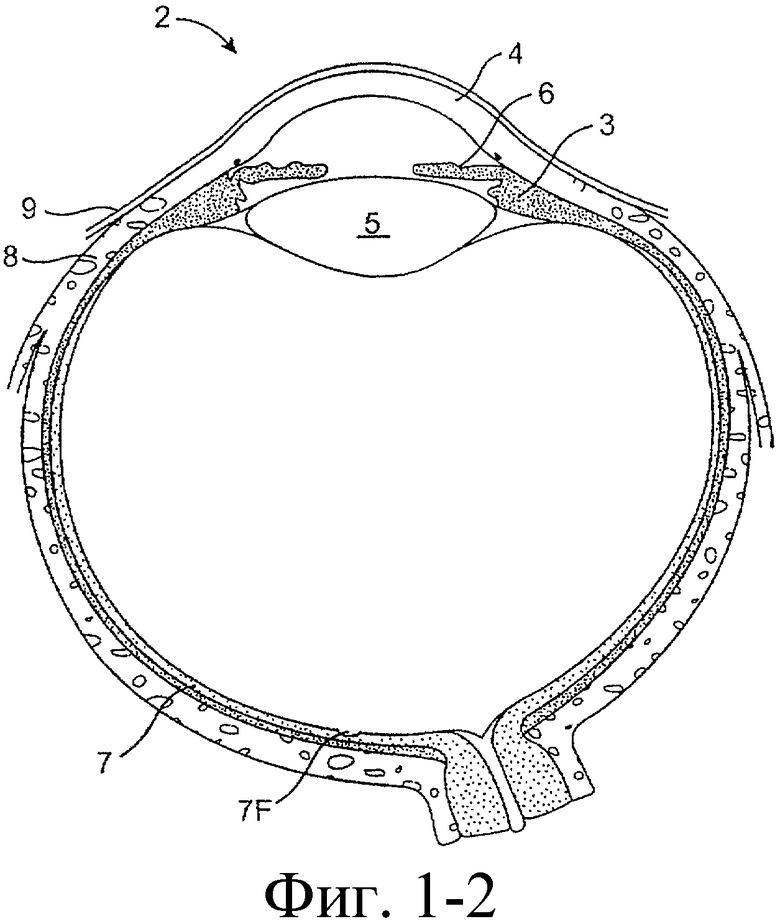
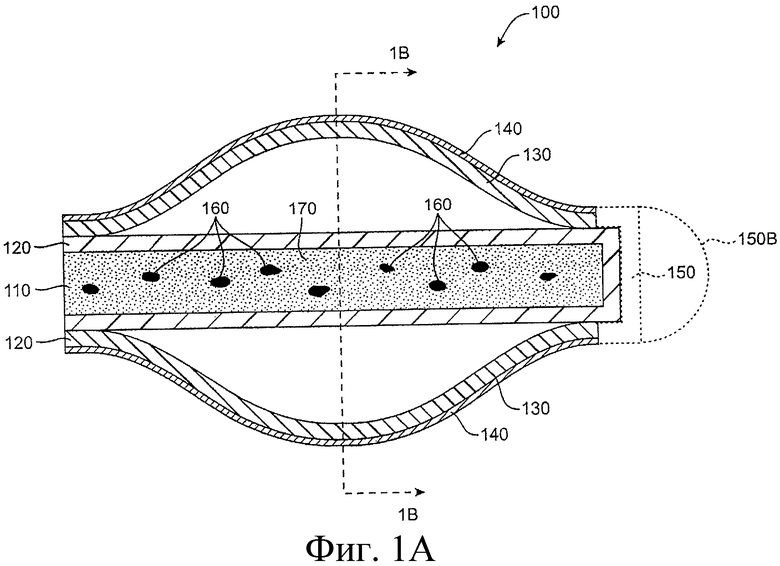
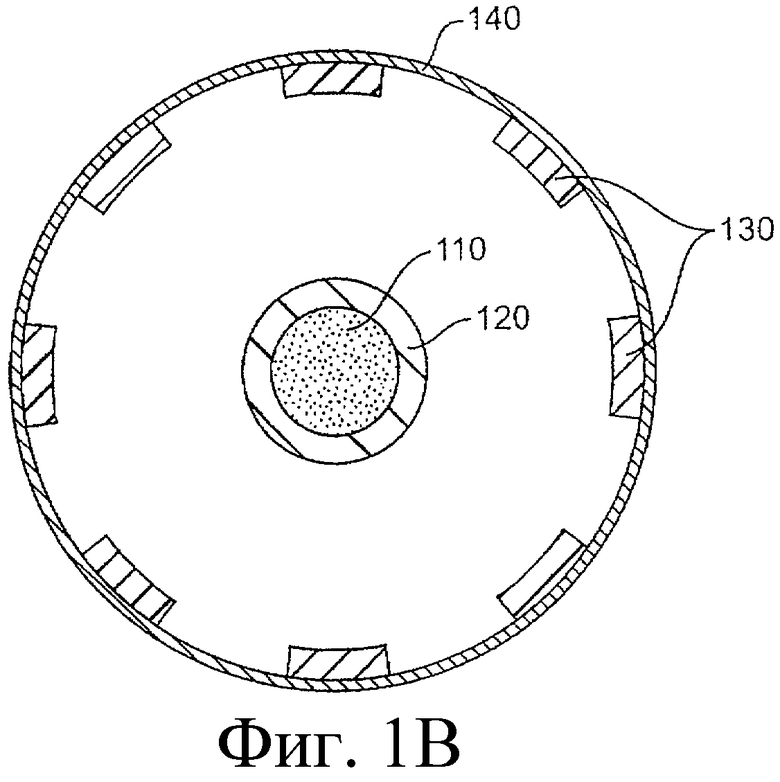
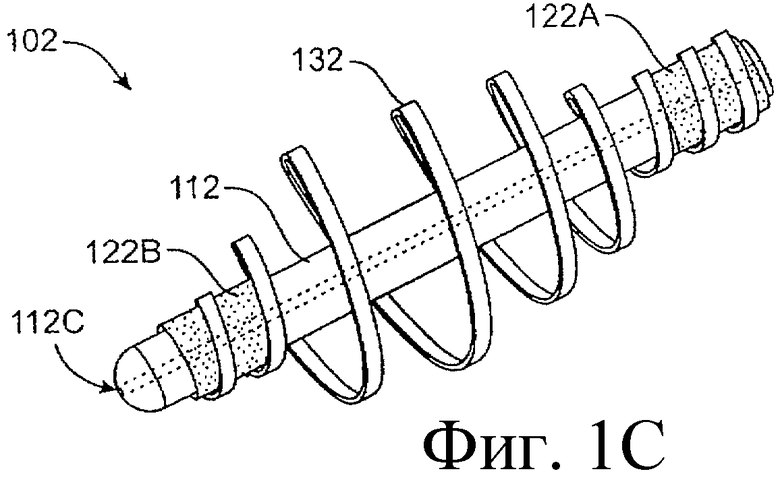
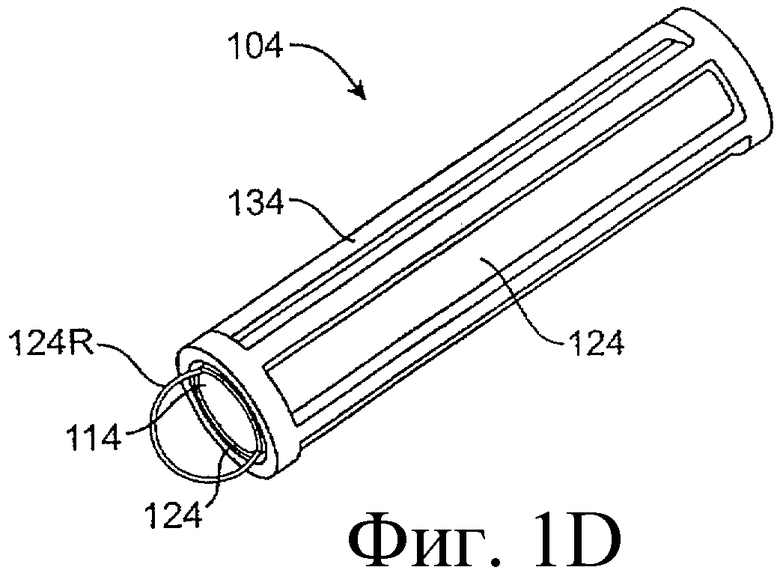
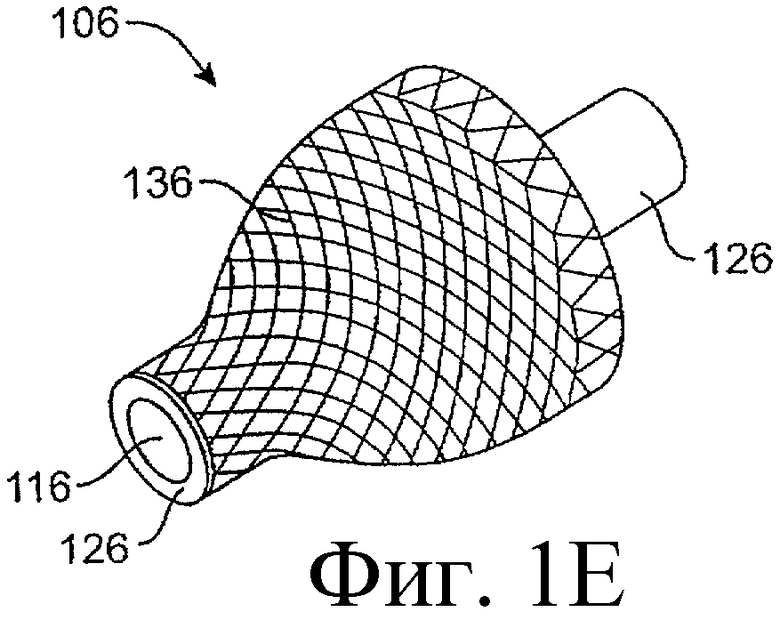
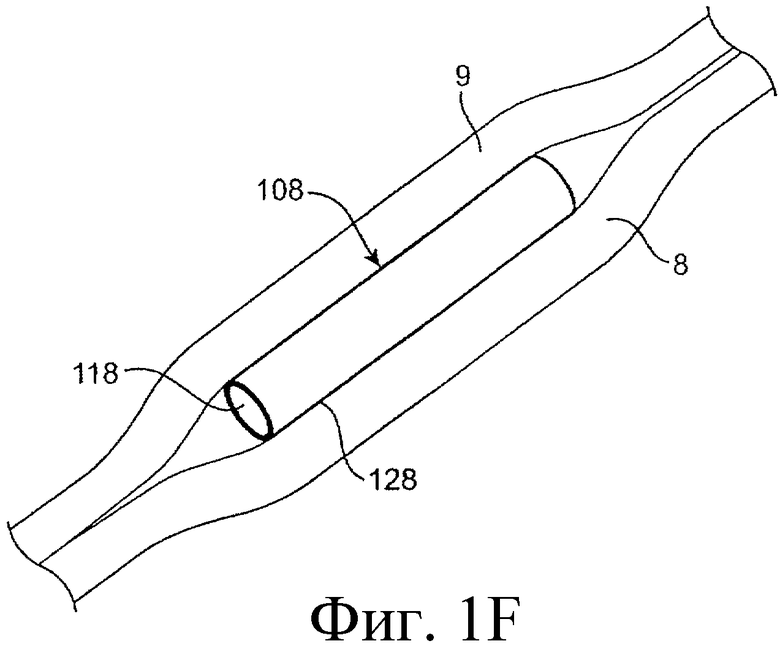
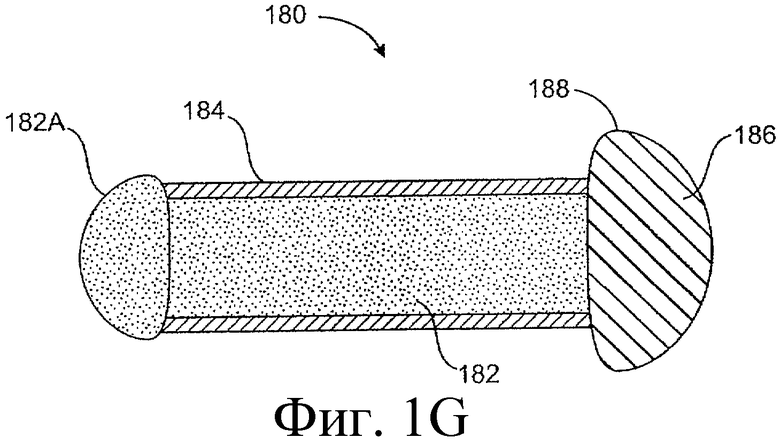
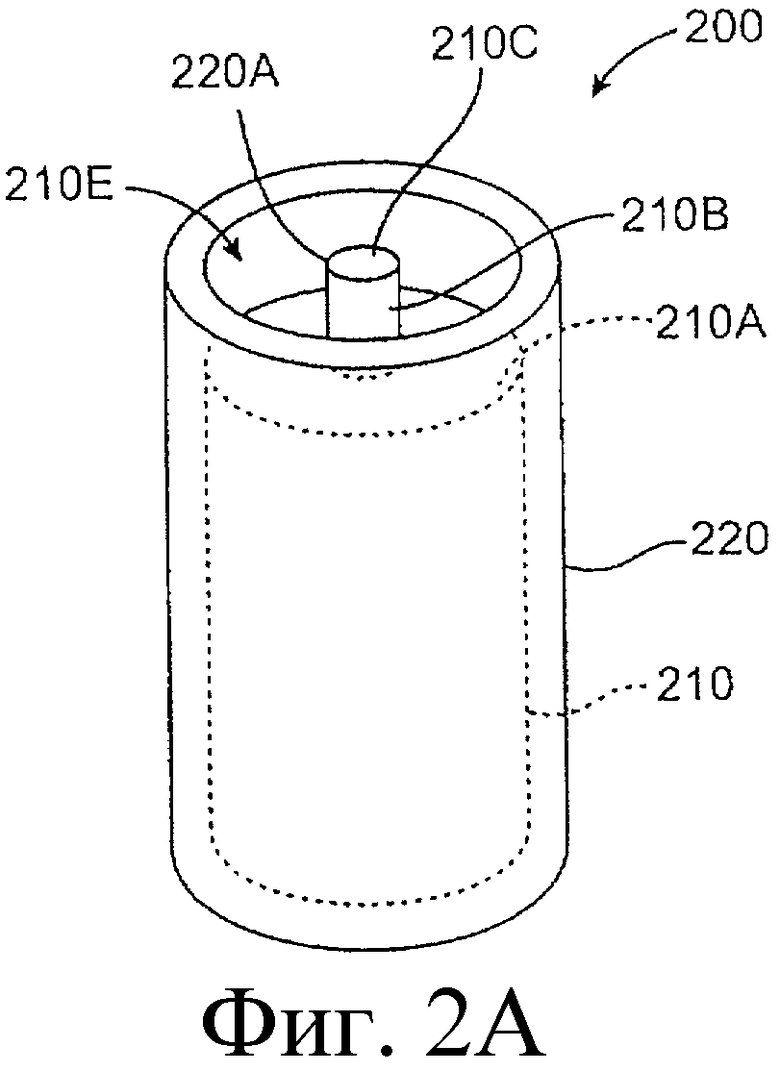
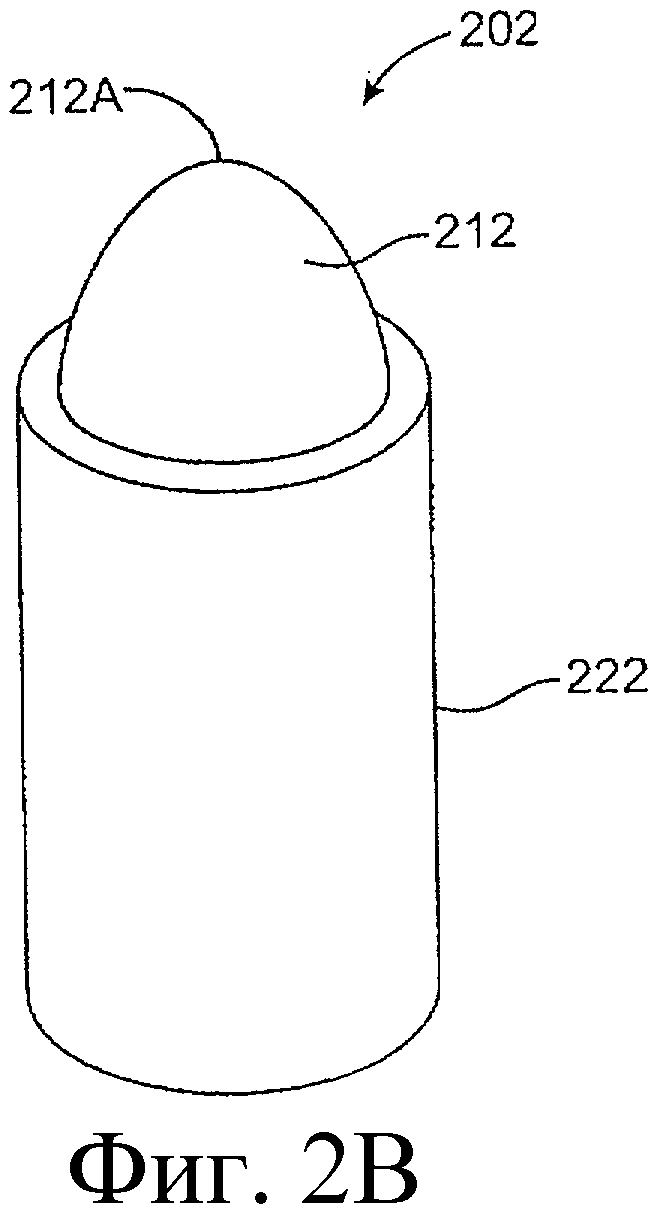
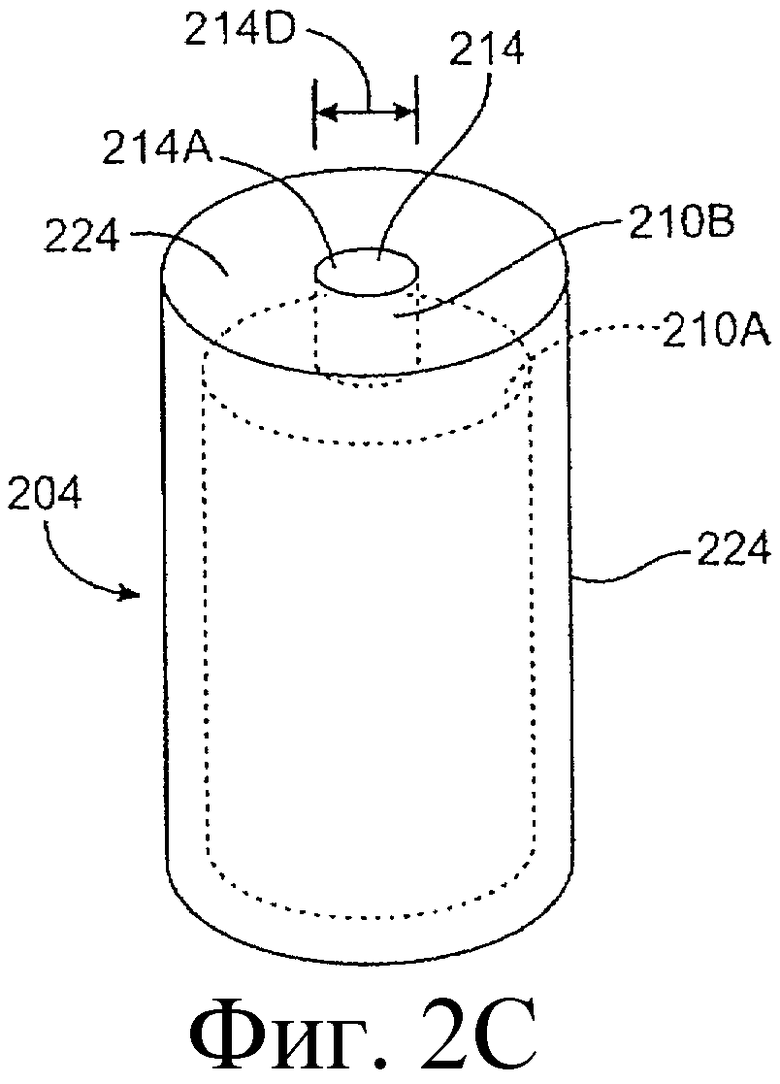
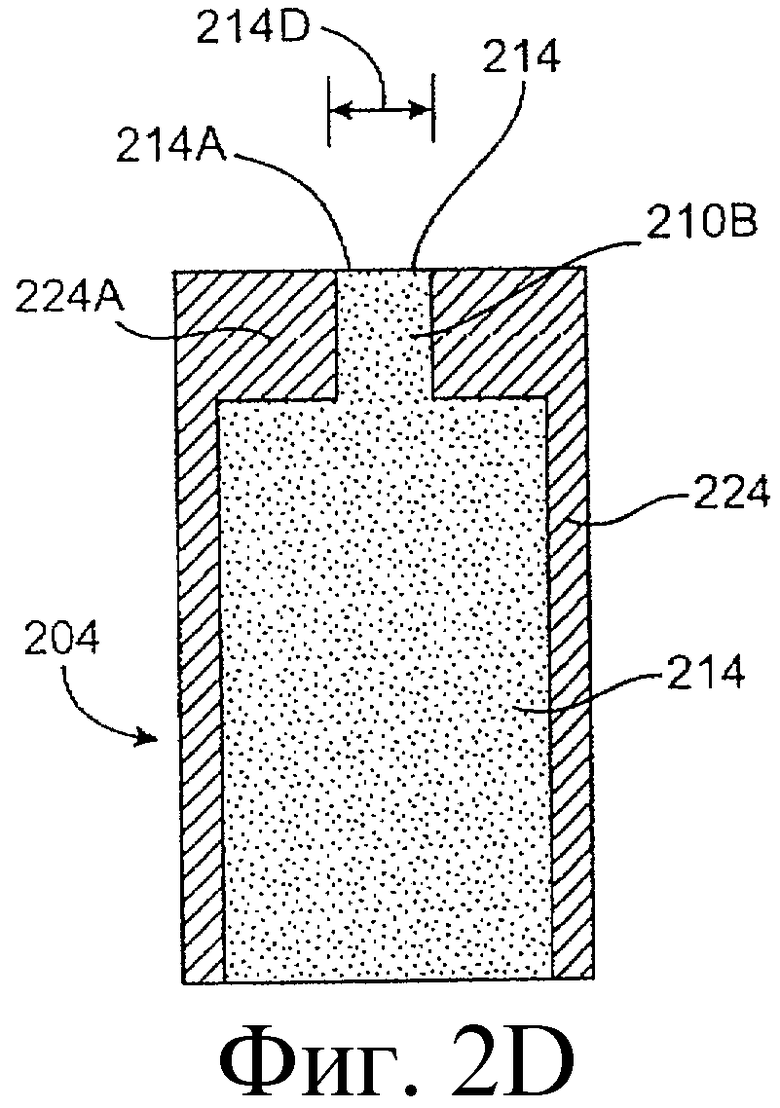
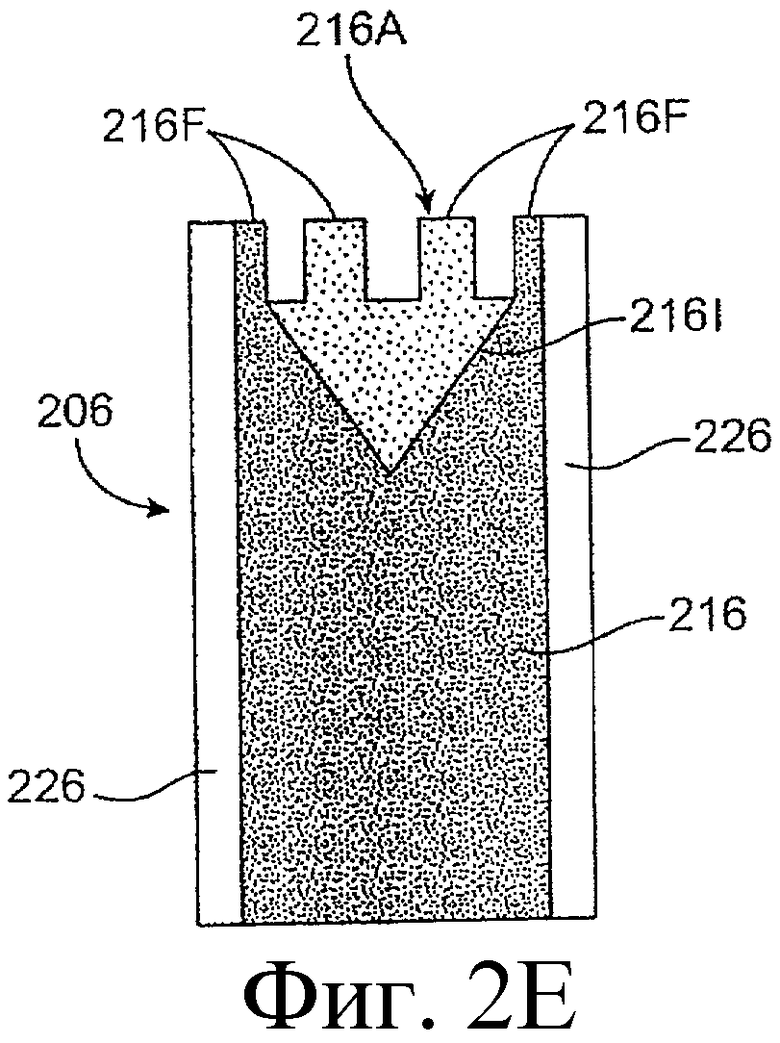
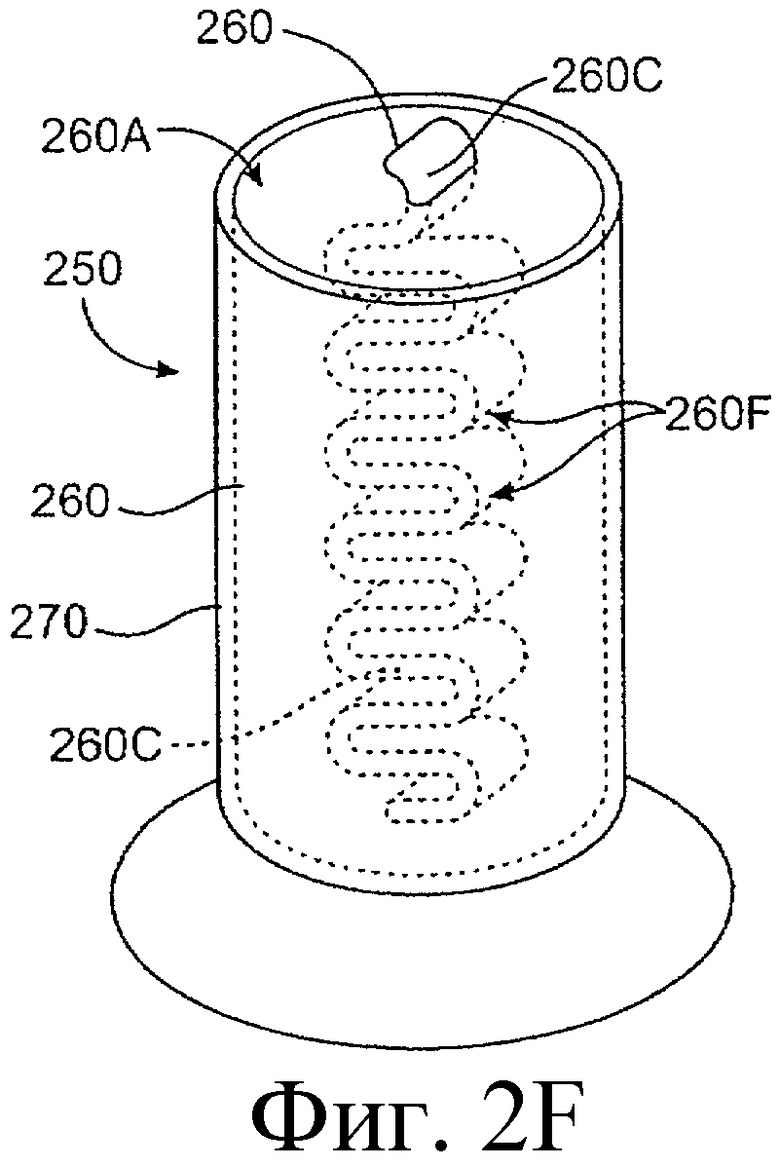
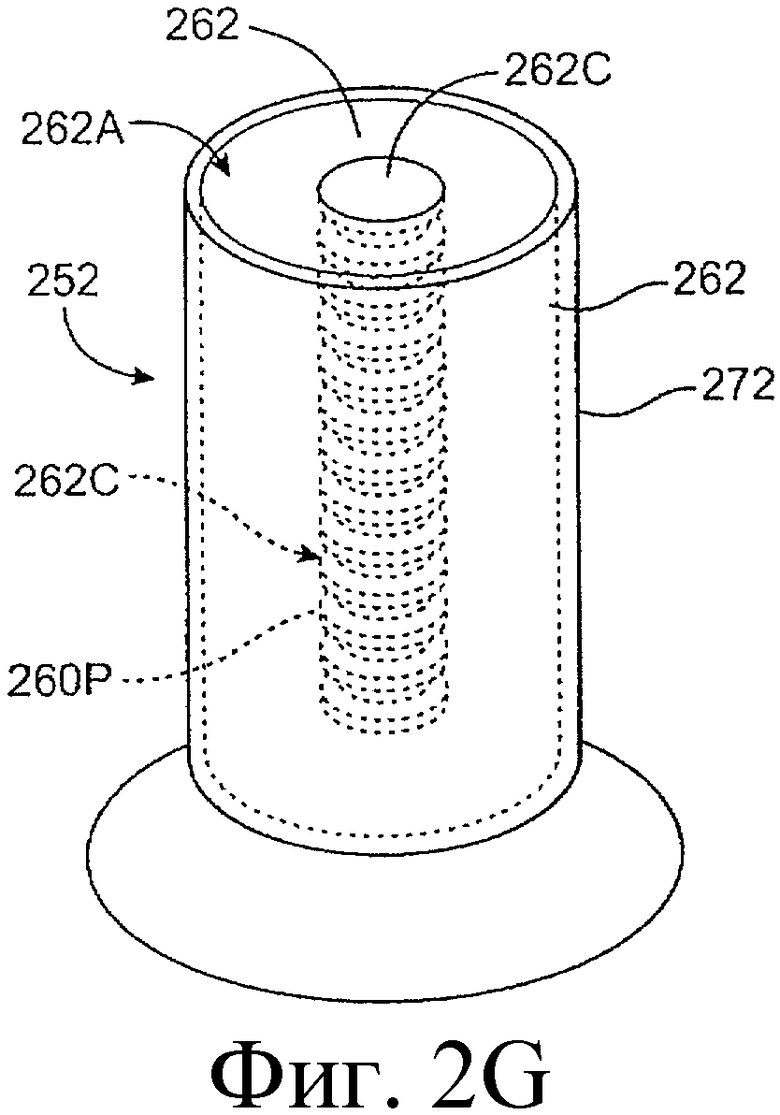
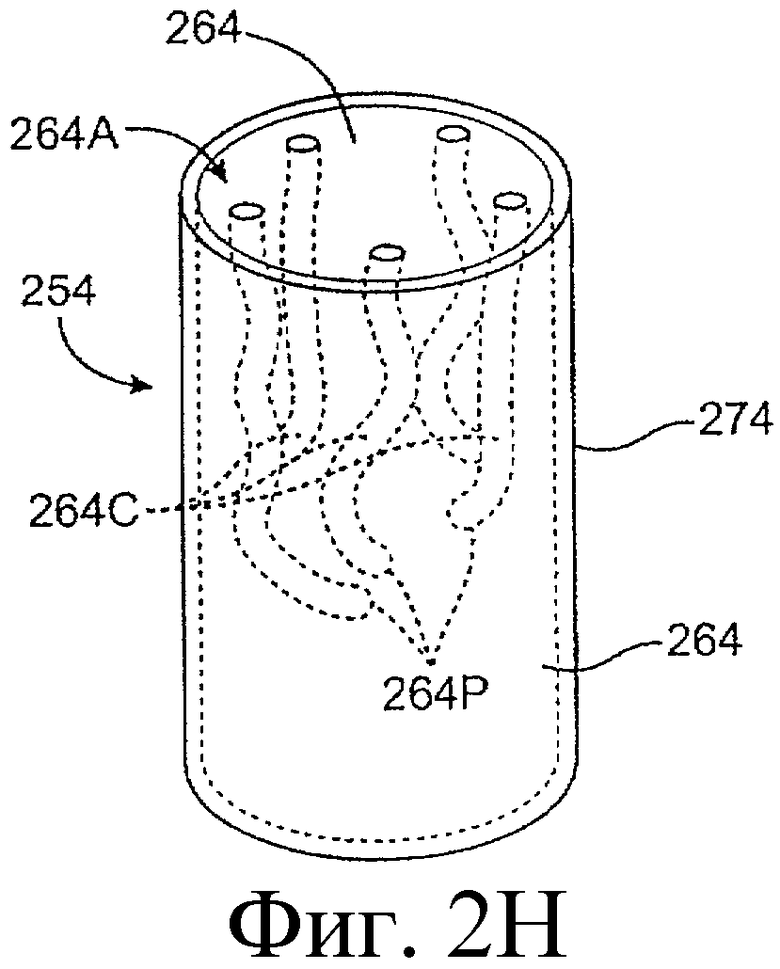
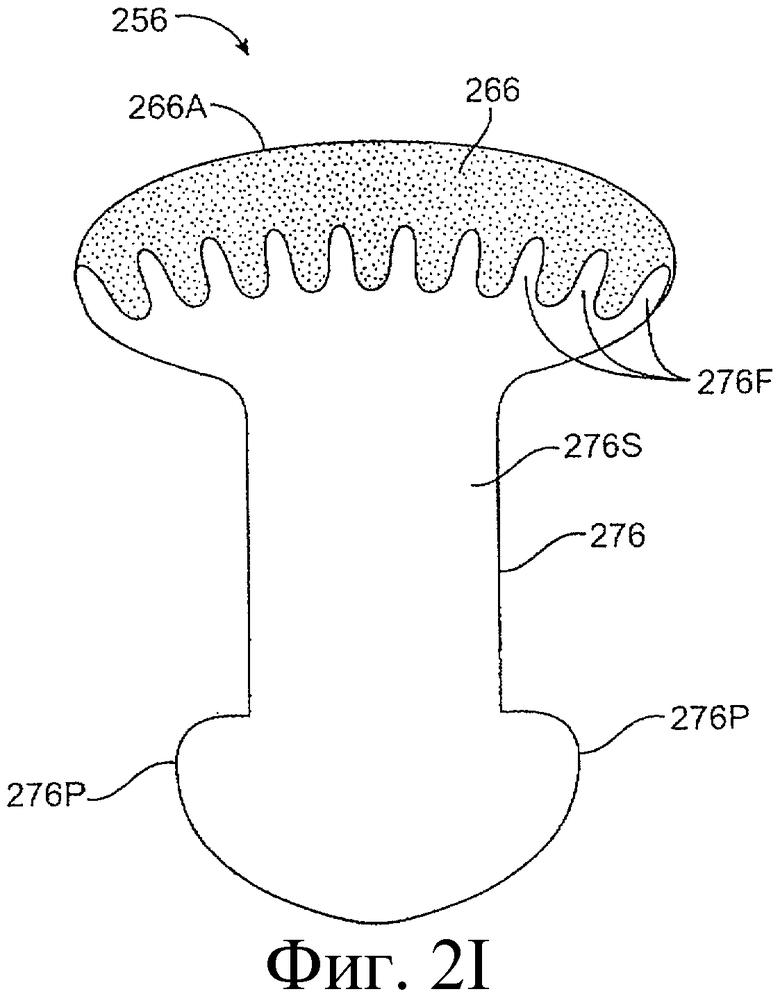
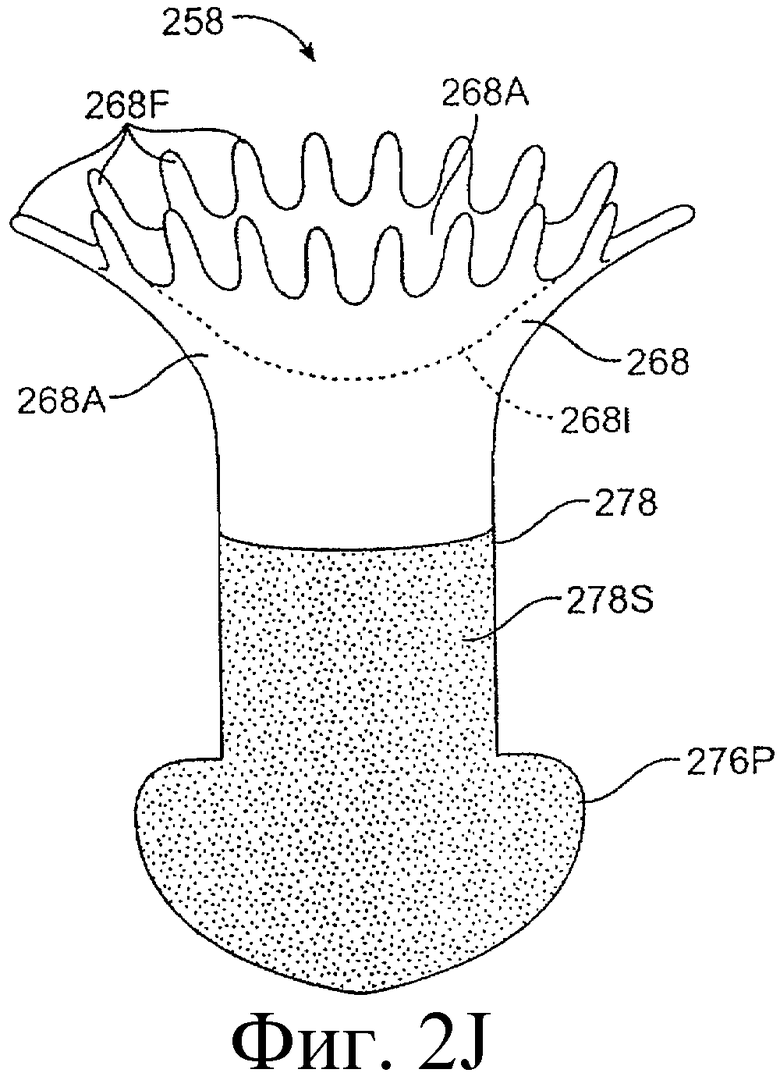
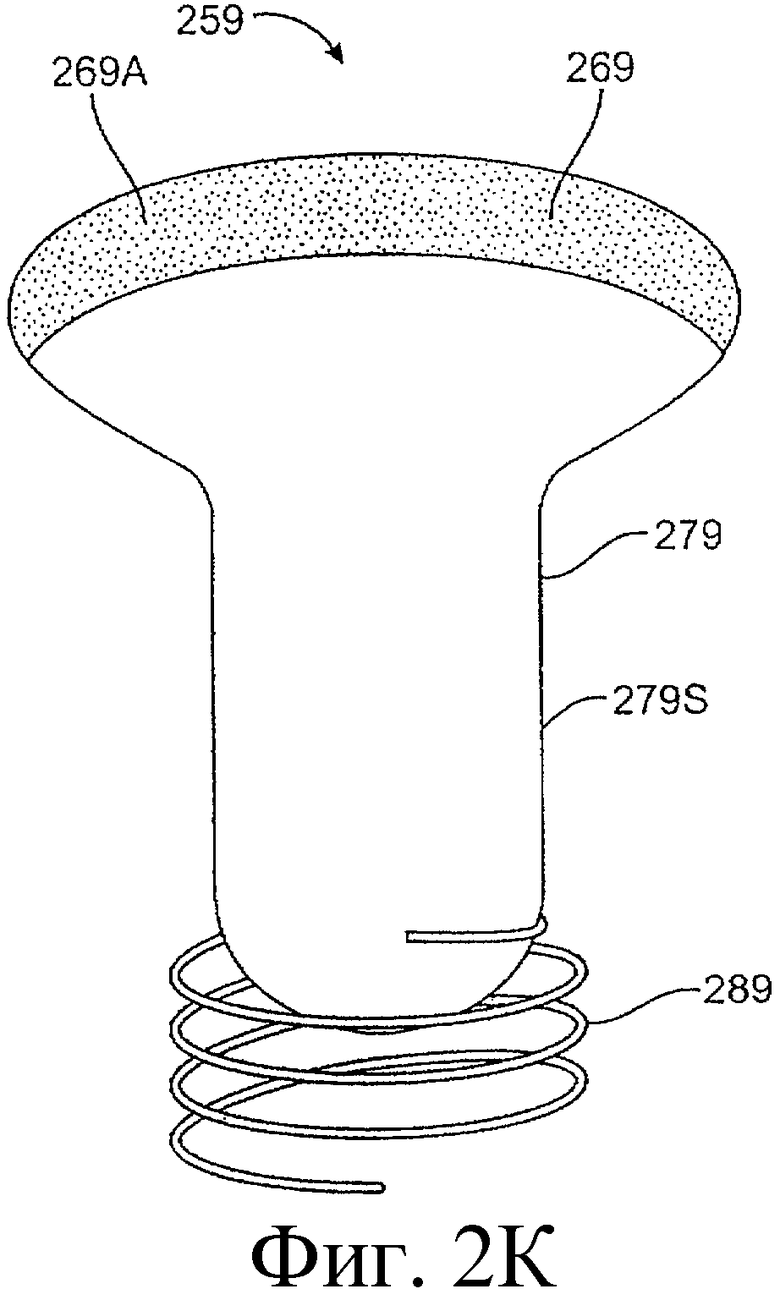
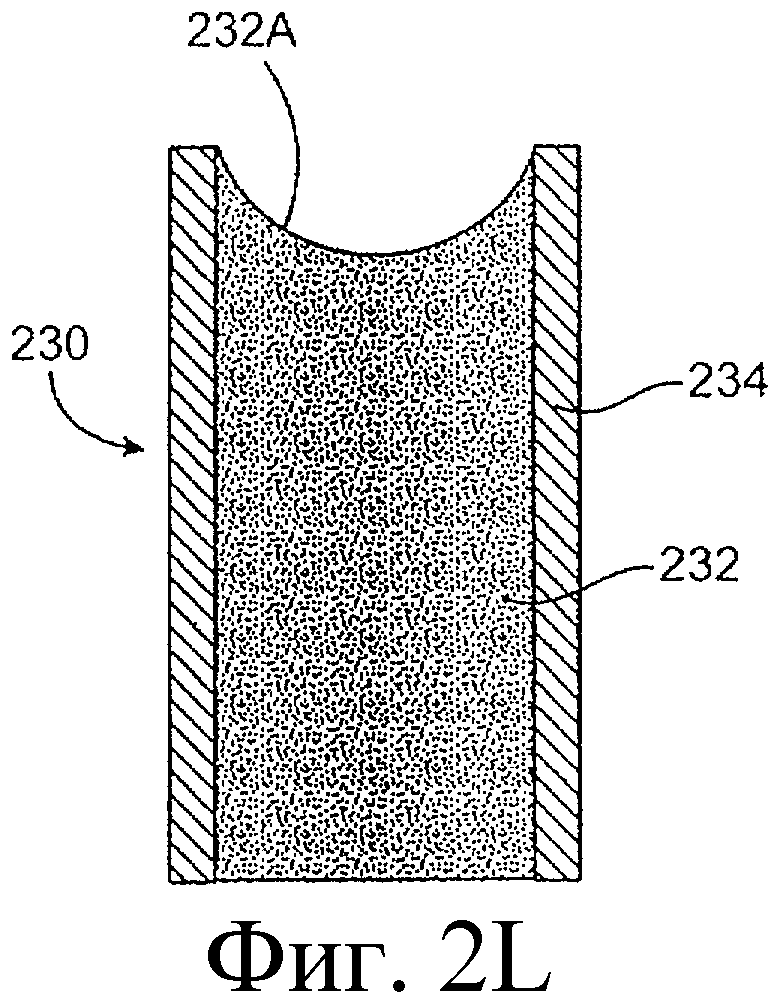
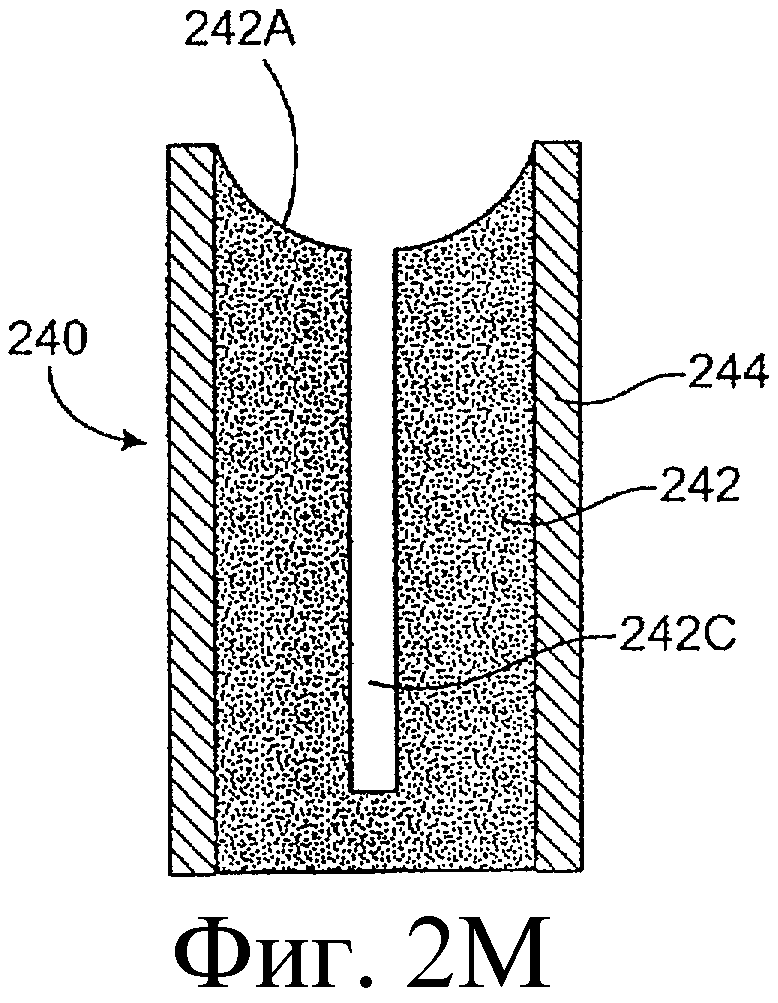
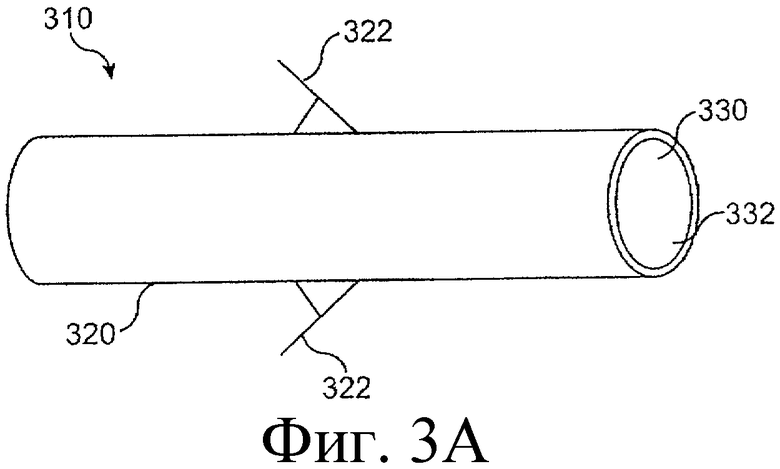
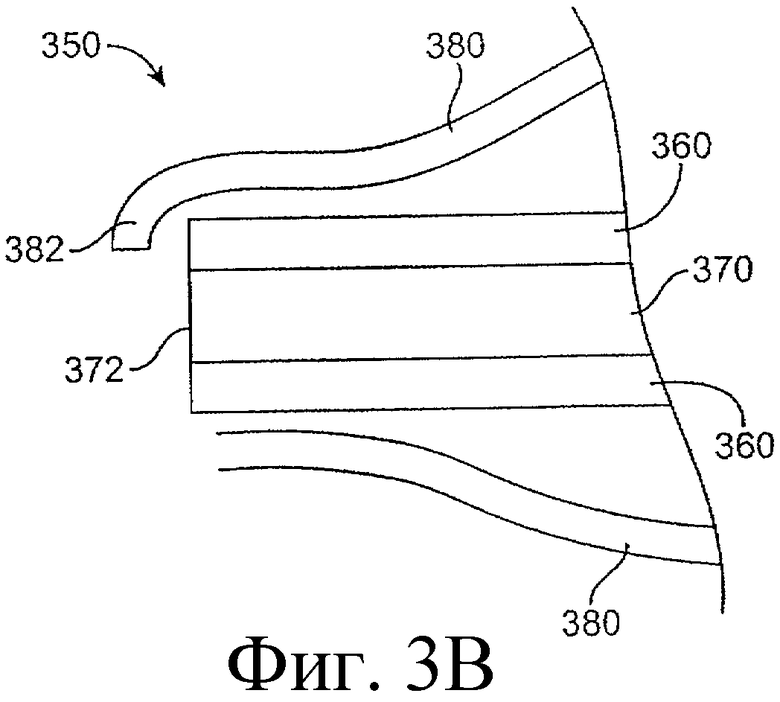
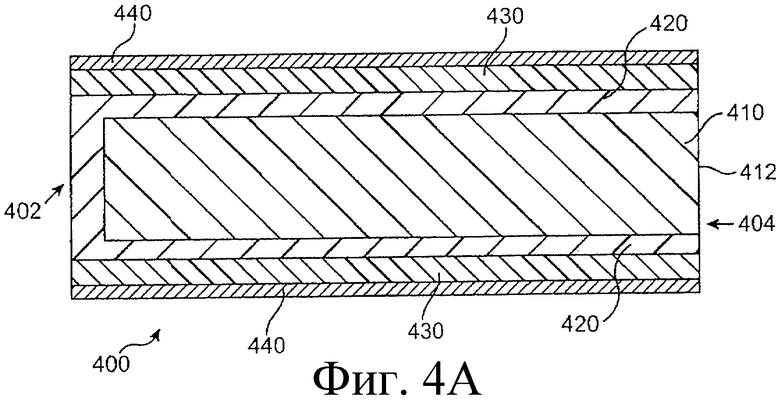
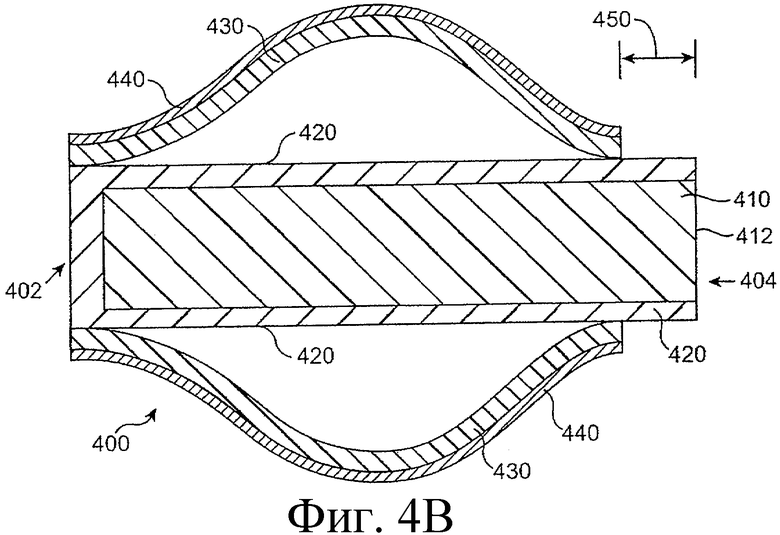
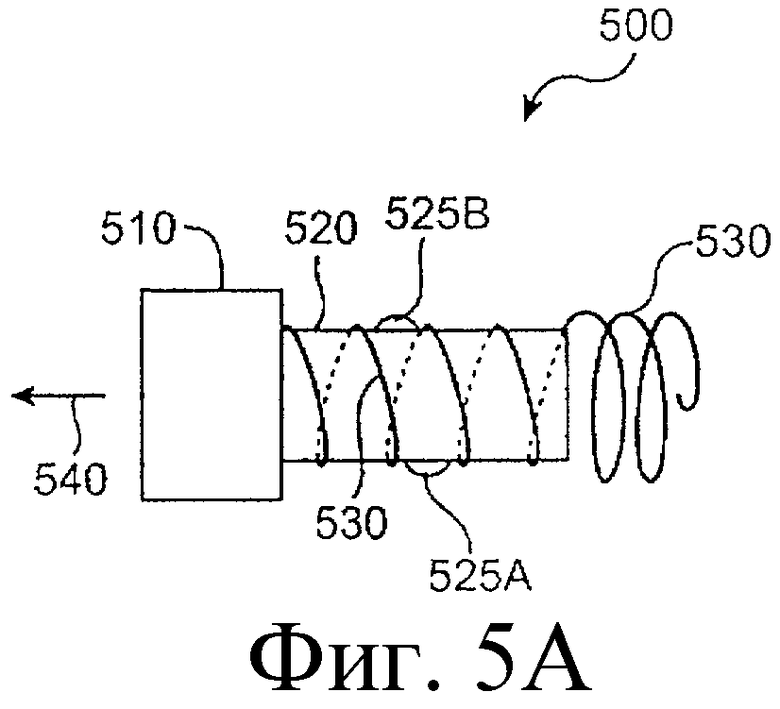
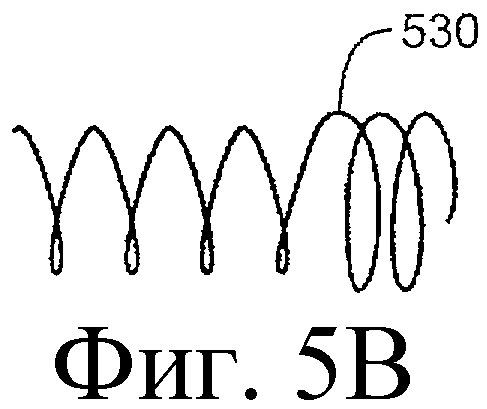
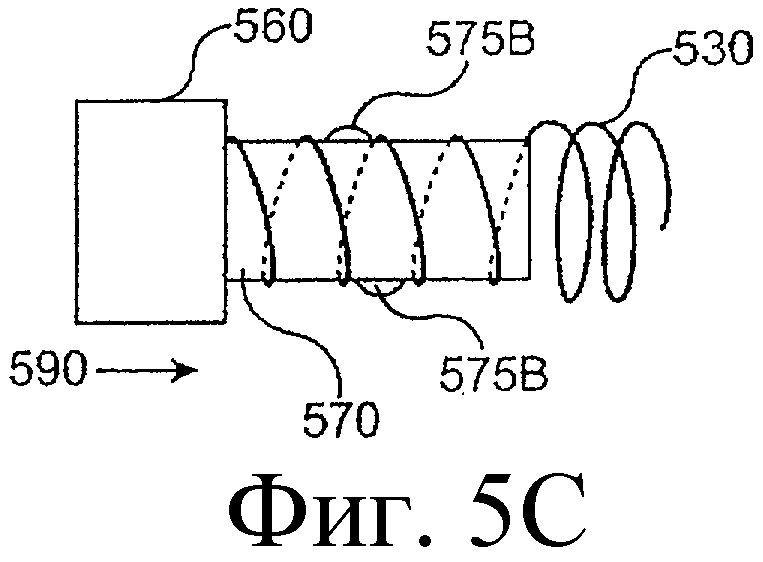
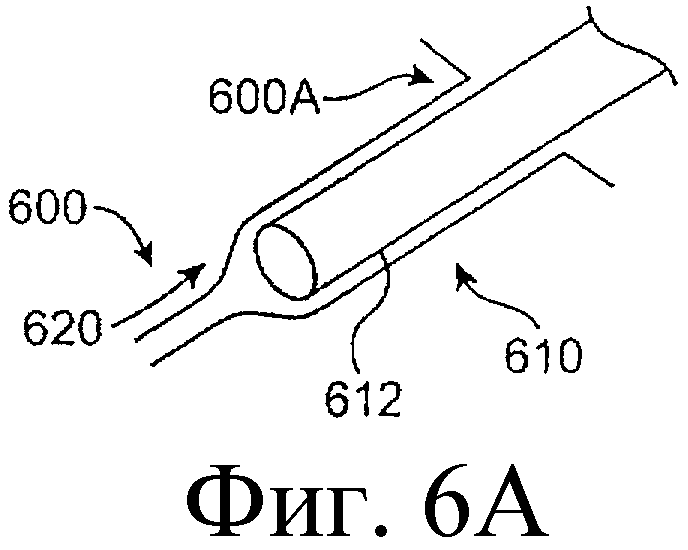
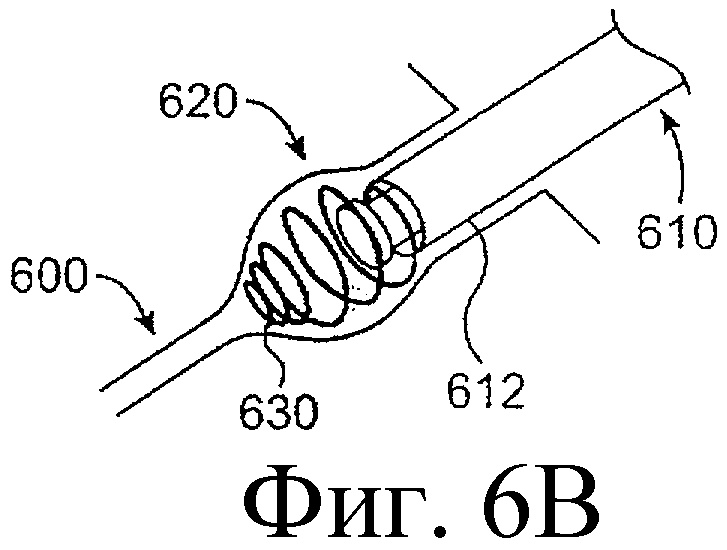
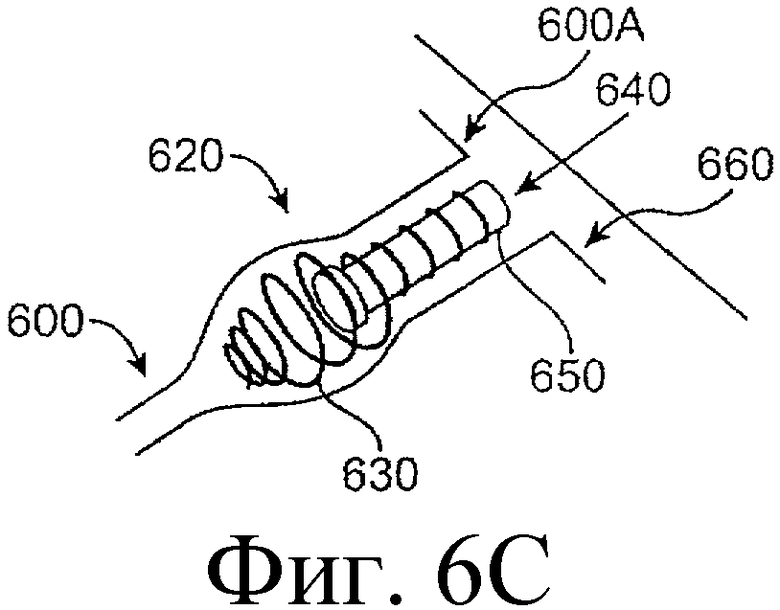
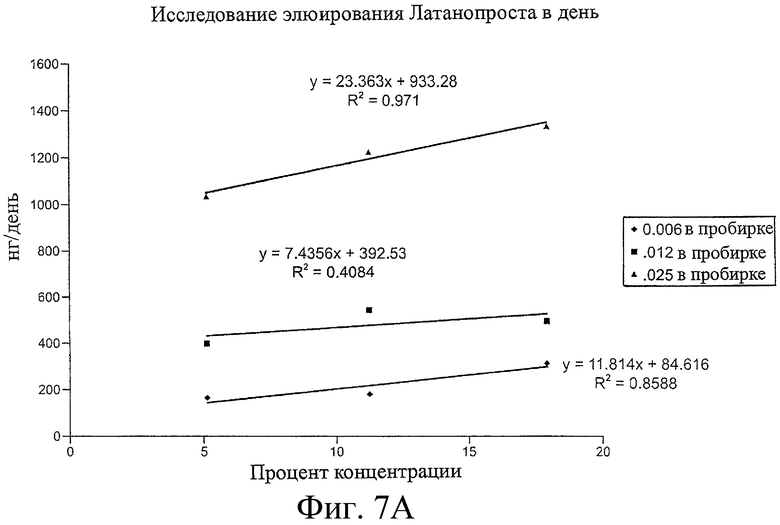
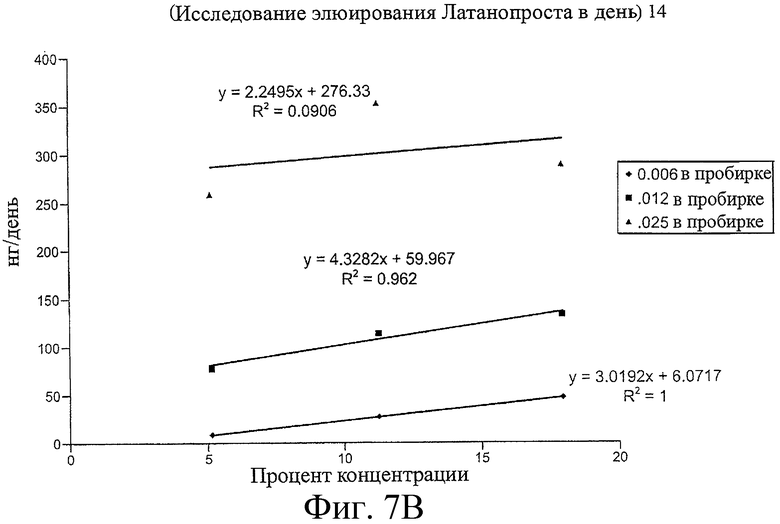
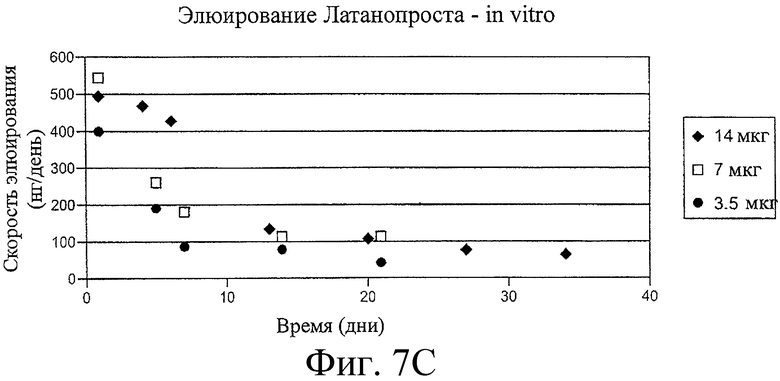
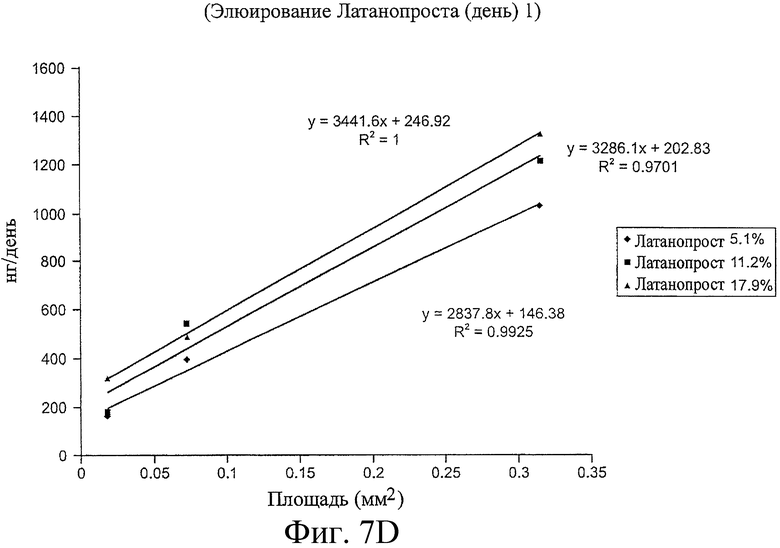
Предложенная группа изобретений предназначена для доставки лекарственных средств и включает композиции и структуры для носослезной системы. Предложена лекарственная вставка, содержащая оболочку и лекарственную сердцевину. Лекарственная вставка размещается в корпусе имплантата, предназначенного для введения в или смежно к глазу пациента. Сердцевина лекарственной вставки содержит терапевтически действующее вещество, содержащееся в матрице. Подвергание матрицы с действующим веществом действию слезной жидкости приводит к эффективному высвобождению терапевтического действующего вещества в слезную жидкость в течение продолжительного периода. В специфичных воплощениях, матрица с действующим веществом содержит небиоабсорбируемый полимер, например, силикон, в негомогенной смеси с действующим веществом. Также предложены способ изготовления лекарственной вставки и имплантат, сконфигурированный для введения в или смежно к глазу пациента, содержащий канал, адаптированный для приема лекарственной вставки или лекарственной сердцевины. Кроме того, группа изобретений включает способ доставки действующего вещества к глазу пациента, а также способ лечения глаза пациента с использованием предложенного имплантата, содержащего лекарственную вставку или лекарственную сердцевину. Заявленная группа изобретений обеспечивает возможность повышения эффективности лечения пациентов, нуждающихся в таком лечении, за счет направленной пролонгированной доставки лекарственных препаратов. 6 н. и 14 з.п. ф-лы, 2 табл., 10 ил.
1. Лекарственная вставка, адаптированная для размещения в имплантате, адаптированном для введения в или смежно к глазу пациента, для обеспечения пролонгированного высвобождения терапевтического действующего вещества в глаз или окружающие ткани или и туда и туда, содержащая лекарственную сердцевину и оболочку, частично покрывающую лекарственную сердцевину, причем лекарственная сердцевина включает терапевтическое действующее вещество, содержащееся в полимере, причем оболочка расположена поверх части лекарственной сердцевины для ингибирования высвобождения действующего вещества из указанной части так, чтобы задавать, по меньшей мере, одну экспонированную поверхность лекарственной сердцевины, адаптированной для высвобождения действующего вещества в глаз или окружающие ткани или и туда и туда, когда имплантат введен пациенту.
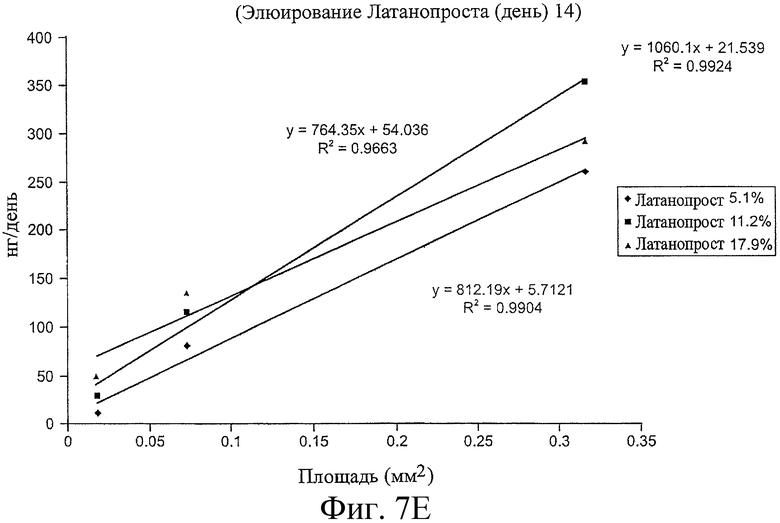
2. Лекарственная вставка по п.1, в которой терапевтическое действующее вещество выбрано из группы, состоящей из латанопроста, биматопроста, тимолола малеата и циклоспорина, или где около 3 - 135 мкг латанопроста или биматопроста присутствует в лекарственной вставке, или где около 3,5 мкг, около 7 мкг или около 14 мкг латанопроста присутствует в лекарственной вставке, или где концентрация терапевтического действующего вещества в лекарственной вставке выбрана из группы, состоящей из около 5%, около 10% и около 20%, или где лекарственная сердцевина содержит негомогенную смесь из силикона и терапевтического действующего вещества.
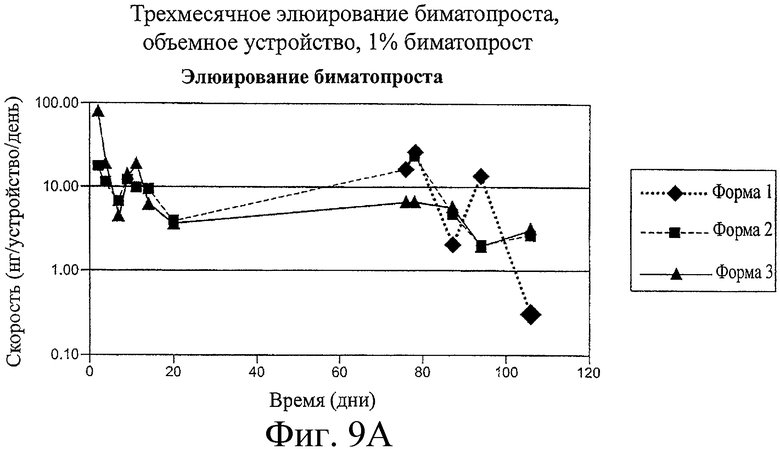
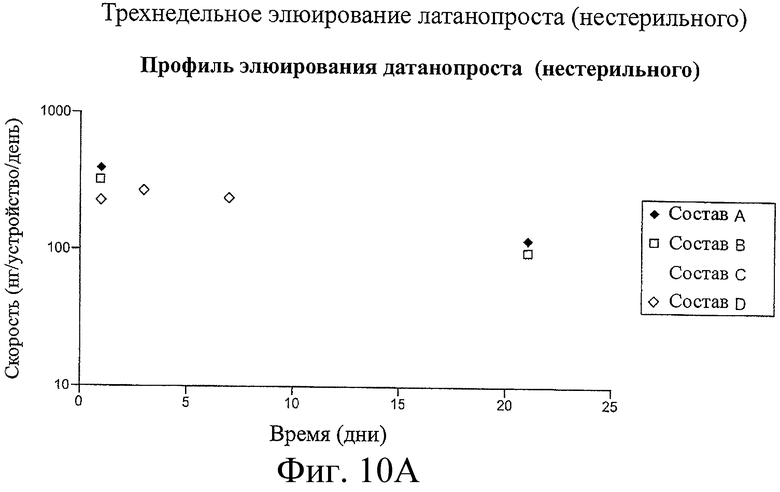
3. Лекарственная вставка по п.1, в которой лекарственная сердцевина содержит включения терапевтического действующего вещества в полимере, и где включения содержат капли и терапевтическое действующее вещество представляет латанопрост, или где включения содержат твердые частицы и терапевтическое действующее вещество представляет биматопрост, или где включения составляют по размеру от около 1 мкм до около 100 мкм.
4. Лекарственная вставка по п.1, в которой полимер включает небиодеградируемый полимер или в которой небиодеградируемый полимер выбран из группы, состоящей из силикона, акрилата, полиэтилена, полиуретана, полиэфира и Nusil 6385.
5. Лекарственная вставка по п.1, где вставка имеет диаметр, выбранный из группы, состоящей из около 0,006 дюймов, около 0,012 дюймов и около 0,025 дюймов, или где оболочка содержит, по меньшей мере, один из полиимида или полиэтилентерефталата.
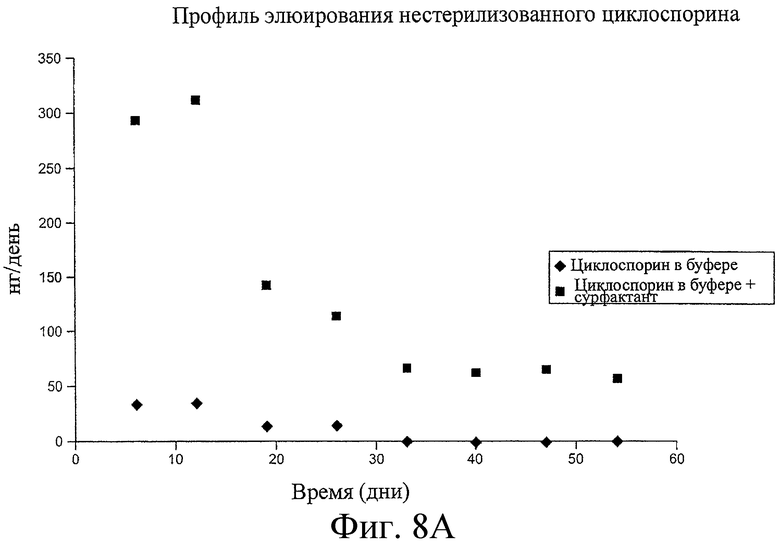
6. Лекарственная вставка по п.1, в которой лекарственная сердцевина дополнительно содержит одну или более добавок для повышения или снижения растворимости терапевтического действующего вещества для контролирования высвобождения терапевтического действующего вещества, или где одна или более добавок выбраны из группы, состоящей из сурфактантов, тинувина, солей и воды.
7. Способ изготовления лекарственной вставки для корпуса имплантата, адаптированного для введения в или смежно к глазу пациента, содержащей лекарственную сердцевину и оболочку, частично покрывающую лекарственную сердцевину, причем лекарственная сердцевина содержит терапевтическое действующее вещество, содержащееся в матрице, представляющей собой небиоабсорбируемый полимер в негомогенной смеси с терапевтическим действующим веществом, причем оболочка расположена поверх части лекарственной сердцевины для ингибирования высвобождения действующего вещества из указанной части и так, чтобы задавать, по меньшей мере, одну экспонированную поверхность лекарственной сердцевины, адаптированной для высвобождения действующего вещества в глаз или окружающие ткани, или и туда и туда, когда имплантат введен пациенту, включающий инъецирование в трубку смеси, содержащей терапевтическое действующее вещество и полимер таким образом, что трубка по существу заполнена ей, причем трубка по существу непроницаема для действующего вещества; отверждение смеси в трубке с образованием трубки, заполненной лекарственной сердцевиной; разрезание заполненной трубки с лекарственной сердцевиной с образованием из нее лекарственных вставок, причем каждая из множества лекарственных вставок имеет по существу одинаковую длину, причем каждая вставка адаптирована, чтобы помещаться в корпусе имплантата и высвобождать через экспонированную поверхность вставки терапевтические количества действующего вещества в слезную жидкость, когда лекарственная вставка содержится в имплантате, находящемся в контакте со слезной жидкостью.
8. Способ по п.7, дополнительно включающий герметизацию одного конца лекарственной вставки для обеспечения экспонированной поверхности на другом конце, или где трубка состоит, по меньшей мере, из одного полиимида или полиэтилентерефталата, или дополнительно включающий добавление катализатора в трубку перед инъецированием терапевтического действующего вещества и полимера, или где полимер содержит силикон, или где множество лекарственных вставок составляют в длину между около 0,80 мм и 0,95 мм, или где терапевтическое действующее вещество выбрано из группы, состоящей из латанопроста, биматопроста, тимолола малеата и циклоспорина.
9. Лекарственная сердцевина, содержащая терапевтическое действующее вещество, содержащееся в матрице, представляющей собой небиоабсорбируемый полимер в негомогенной смеси с терапевтическим действующим веществом, для размещения в или в качестве лекарственной вставки или имплантата, причем лекарственная вставка или имплантат адаптированы для размещения в или смежно к глазу пациента для обеспечения пролонгированного высвобождения терапевтического действующего вещества в глазе или окружающих тканях или и там и там, где терапевтическое действующее вещество растворено в матрице или образует включения в матрице.
10. Лекарственная сердцевина по п.9, расположенная в оболочке, или где матрица содержит включения жидкого масла латанопроста и полимер Nusil 6385, или где матрица содержит циклоспорин и полиуретан.
11. Имплантат, сконфигурированный для введения в или смежно к глазу пациента, причем корпус имплантата содержит канал, адаптированный для приема лекарственной вставки или лекарственной сердцевины, сконфигурированных таким образом, чтобы экспонированная поверхность вставки или лекарственной сердцевины были экспонированы в слезную жидкость, когда вставка или сердцевина располагается в имплантате, и имплантат располагается в или смежно к глазу, причем лекарственная вставка содержит лекарственную сердцевину и оболочку, частично покрывающую лекарственную сердцевину, причем лекарственная сердцевина содержит терапевтическое действующее вещество, содержащееся в матрице, представляющей собой небиоабсорбируемый полимер в негомогенной смеси с терапевтическим действующим веществом, причем оболочка расположена поверх части лекарственной сердцевины для ингибирования высвобождения действующего вещества из указанной части и таким образом, чтобы задавать, по меньшей мере, одну экспонированную поверхность лекарственной сердцевины, адаптированной для высвобождения действующего вещества в глаз или окружающие ткани или и туда и туда, когда имплантат введен пациенту.
12. Имплантат по п.11, в котором а) терапевтическое действующее вещество представляет латанопрост или биматопрост и b) от около 5 нг до около 500 нг латанопроста или биматопроста высвобождается каждый день из имплантата, или где терапевтическое действующее вещество представляет тимолола малеат и где от около 270 мкг до около 1350 мкг тимолола малеата присутствует в имплантате и где имплантат сконфигурирован для высвобождения от около 20 мкг до около 135 мкг тимолола малеата ежедневно, или где терапевтическое действующее вещество представляет циклоспорин и где имплантат сконфигурирован для высвобождения от около 50 нг до около 100 нг циклоспорина ежедневно, или где имплантат сконфигурирован для высвобождения терапевтического действующего вещества в течение, по меньшей мере, 3 месяцев.
13. Имплантат по п.11, в котором оболочка состоит, по меньшей мере, из одного полиимида или полиэтилентерефталата, или в котором матрица содержит небиодеградируемый полимер, выбранный из группы, состоящей из силикона, акрилата, полиэтилена, полиуретана и полиэфира, или в котором небиодеградируемый полимер представляет Nusil 6385, или в котором лекарственная сердцевина содержит негомогенную смесь силикона и терапевтического действующего вещества, или в котором лекарственная вставка имеет диаметр, выбранный из группы, состоящей из около 0,006 дюймов, около 0,012 дюймов и около 0,025 дюймов.
14. Имплантат по п.11, в котором корпус имплантата сконфигурирован для применения в окулярных тканях, выбранных из группы, состоящей из слезной точки, канальца, слоя конъюнктивальной ткани глаза, слоя ткани склеры, с тем, чтобы не проникать в ткань склеры.
15. Способ доставки терапевтического действующего вещества к глазу, включающий помещение имплантата в структуру глаза, где имплантат содержит корпус имплантата, содержащий канал, адаптированный для приема лекарственной вставки или лекарственной сердцевины, сконфигурированный таким образом, что экспонированная поверхность вставки или лекарственной сердцевины будет экспонирована в слезную жидкость, когда вставка или сердцевина располагается в имплантате, и имплантат располагается в или смежно к глазу, причем лекарственная вставка содержит лекарственную сердцевину и оболочку, частично покрывающую лекарственную сердцевину, причем лекарственная сердцевина содержит терапевтическое действующее вещество, содержащееся в матрице, представляющей собой небиоабсорбируемый полимер в негомогенной смеси с терапевтическим действующим веществом, причем оболочка расположена поверх части лекарственной сердцевины для ингибирования высвобождения действующего вещества из указанной части и таким образом, чтобы задавать, по меньшей мере, одну экспонированную поверхность лекарственной сердцевины, адаптированной для высвобождения действующего вещества в глаз или окружающие ткани или и туда и туда, когда имплантат введен пациенту, и где скорость высвобождения терапевтического действующего вещества из вставки в глаз зависит от экспонированной поверхности лекарственной сердцевины, тем самым доставляя терапевтическое действующее вещество в глаз в течение пролонгированного периода времени.
16. Способ по п.15, в котором пролонгированный период времени составляет, по меньшей мере, три месяца, или в котором терапевтическое действующее вещество выбрано из группы, состоящей из латанопроста, биматопроста, тимолола ацетата и циклоспорина, или в котором терапевтическое действующее вещество представляет латанопрост и биматопрост и в котором около 3 - 135 мкг латанопроста или биматопроста присутствует в имплантате и в котором около 5 - 500 нг латанопроста или биматопроста высвобождается каждый день из лекарственной сердцевины, или в котором терапевтическое действующее вещество представляет тимолола малеат, в котором около 270 - 1350 мкг тимолола малеата присутствует в имплантате, и в котором около 20 - 135 мкг тимолола малеата высвобождается каждый день из лекарственной сердцевины, или в котором терапевтическое действующее вещество представляет циклоспорин и в котором около 50 -100 нг циклоспорина высвобождается каждый день из лекарственной сердцевины, или в котором имплантат или лекарственная сердцевина сконфигурированы для применения в качестве пробки для слезной точки, или в котором лекарственная сердцевина содержит матрицу, которая содержит включения терапевтического действующего вещества, или в котором а) включения содержат капли масла терапевтического действующего вещества, и терапевтическое действующее вещество представляет собой латанопрост, или b) включения содержат твердые частицы терапевтического действующего вещества и терапевтическое действующее вещество представляет собой биматопрост, или в котором включения составляют около 1 - 100 мкм в размере, или в котором оболочка состоит, по меньшей мере, из одного полиимида или полиэтилентерефталата, или в котором матрица содержит небиодеградируемый полимер, выбранный из группы, состоящей из силикона, акрилата, полиэтилена, полиуретана и полиэфира, или в котором небиодеградируемый полимер представляет Nusil 6385, или в котором лекарственная вставка имеет диаметр, выбранный из группы, состоящей из около 0,006 дюймов, около 0,012 дюймов и около 0,025 дюймов, или в котором лекарственная сердцевина содержит негомогенную смесь силикона и терапевтического действующего вещества, или в котором лекарственная сердцевина дополнительно содержит одну или более добавок для повышения или снижения растворимости терапевтического действующего вещества для контролирования высвобождения терапевтического действующего вещества, или в котором одна или более добавок выбраны из группы, состоящей из сурфактантов, тинувина, солей и воды.
17. Способ по п.15, в котором имплантат сконфигурирован для применения в окулярных тканях, выбранных из группы, состоящей из слезной точки, канальца, слоя конъюнктивальной ткани глаза, слоя ткани склеры, чтобы не проникать в ткань склеры.
18. Способ лечения состояния глаза пациента, нуждающегося в таком лечении, включающий размещение в или смежно к глазу пациента лекарственной сердцевины, причем лекарственная сердцевина содержит терапевтическое действующее вещество, содержащееся в матрице, представляющей собой небиоабсорбируемый полимер в негомогенной смеси с терапевтическим действующим веществом, где терапевтическое действующее вещество растворено в матрице или образует включения в матрице, для обеспечения высвобождения терапевтического действующего вещества в глаз или окружающие ткани или и туда и туда в течение пролонгированного периода времени, где скорость высвобождения терапевтического действующего вещества зависит от площади экспонированной поверхности лекарственной сердцевины, где терапевтическое действующее вещество адаптировано для лечения состояния.
19. Способ по п.18, в котором пролонгированный период времени составляет, по меньшей мере, три месяца, или в котором терапевтическое действующее вещество выбрано из группы, состоящей из латанопроста, биматопроста, тимолола ацетата и циклоспорина, или в котором терапевтическое действующее вещество представляет латанопрост и биматопрост и в котором около 3 - 135 мкг латанопроста или биматопроста присутствует в лекарственной сердцевине и в котором около 5 - 500 нг латанопроста или биматопроста высвобождается каждый день из лекарственной сердцевины, или в котором терапевтическое действующее вещество представляет тимолола малеат, в котором около 270 - 1350 мкг тимолола малеата присутствует в лекарственной сердцевине, и в котором около 20 - 135 мкг тимолола малеата высвобождается каждый день из лекарственной сердцевины, или в котором терапевтическое действующее вещество представляет циклоспорин и в котором около 50 - 100 нг циклоспорина высвобождается каждый день из лекарственной сердцевины, или в котором лекарственная сердцевина сконфигурирована для применения в качестве пробки для слезной точки, или в котором лекарственная сердцевина содержит матрицу, которая содержит включения терапевтического действующего вещества, или в котором а) включения содержат капли масла терапевтического действующего вещества, и терапевтическое действующее вещество представляет собой латанопрост, или b) включения содержат твердые частицы терапевтического действующего вещества и терапевтическое действующее вещество представляет собой биматопрост, или в котором включения составляют около 1 - 100 мкм в размере, или в котором оболочка состоит, по меньшей мере, из одного полиимида или полиэтилентерефталата, или в котором матрица содержит небиодеградируемый полимер, выбранный из группы, состоящей из силикона, акрилата, полиэтилена, полиуретана и полиэфира, или в котором небиодеградируемый полимер представляет Nusil 6385, или в котором лекарственная вставка имеет диаметр, выбранный из группы, состоящей из около 0,006 дюймов, около 0,012 дюймов и около 0,025 дюймов, или в котором лекарственная сердцевина содержит негомогенную смесь силикона и терапевтического действующего вещества, или в котором лекарственная сердцевина дополнительно содержит одну или более добавок для повышения или снижения растворимости терапевтического действующего вещества для контролирования высвобождения терапевтического действующего вещества, или в котором одна или более добавок выбраны из группы, состоящей из сурфактантов, тинувина, солей и воды.
20. Способ по п.18, в котором лекарственная сердцевина сконфигурирована для применения в окулярных тканях, выбранных из группы, состоящей из слезной точки, канальца, слоя конъюнктивальной ткани глаза, слоя ткани склеры, чтобы не проникать в ткань склеры.
| WO 2004058289 А1, 15.07.2004 | |||
| ИМПЛАНТИРУЕМАЯ СИСТЕМА ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2003 |
|
RU2322233C2 |
| RU 2007115853, 10.11.2008 | |||
| WO 2006031658, 23.03.2006 | |||
| CHETONI P | |||
| et al | |||
| Silicone rubber/hydrogel composite ophthalmic inserts: preparation and preliminary in vitro/in vivo evaluation | |||
| Eur | |||
| J | |||
| Pharm | |||
| Biopharm | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
Авторы
Даты
2011-03-10—Публикация
2007-04-02—Подача