Изобретение относится к области медицины, конкретно к комбинированным противотуберкулезным препаратам, и может быть использовано для лечения туберкулеза.
Несмотря на значительные успехи, достигнутые в последние десятилетия во многих областях медицины, в том числе терапии туберкулеза, все еще достаточно высоки показатели заболеваемости туберкулезом. К основным проблемам лечения туберкулеза относятся ограниченность арсенала противотуберкулезных средств и быстрое развитие резистентности микобактерий туберкулеза к применяющимся препаратам.
В стандартной химиотерапии туберкулеза в качестве основного и наиболее эффективного противотуберкулезного препарата используется изониазид - гидразид изоникотиновой кислоты. Отличаясь высокой терапевтической активностью, изониазид обладает и сильным токсическим эффектом. Но его основным недостатком является быстрое развитие лекарственной устойчивости микобактерий туберкулеза, что существенно снижает его эффективность. Резистентность микобактерий туберкулеза к изониазиду развивается у 70% больных, а 30% пациентов переходят в разряд хронических больных.
Развитие резистентности микобактерий происходит значительно медленнее при одновременном применении нескольких препаратов. Однако при сочетанной терапии больные туберкулезом из-за сложностей и длительности подбора эффективных лекарств, а также самого курса терапии осуществляют его либо нерегулярно, либо не доводят до конца, что служит причиной возврата заболевания, быстрого появления вторичной устойчивости к лекарственным средствам. Поэтому Всемирная Организация Здравоохранения (ВОЗ) рекомендует отказ от моно- и сочетанной терапии и указывает на необходимость использования комбинированных противотуберкулезных препаратов в одной лекарственной форме.
В патенте РФ №2182483 предлагается комбинированное противотуберкулезное средство, которое содержит изониазид и пиразинамид или этамбутола гидрохлорид. Однако наличие в его составе только двух действующих компонентов не снимает полностью вышеуказанных недостатков сочетанной терапии и требует назначения дополнительно других противотуберкулезных препаратов.
С целью снижения развития лекарственной устойчивости микобактерий туберкулеза были предложены многокомпонентные противотуберкулезные препараты, содержащие три и более действующих веществ. Например, в патенте США №5104875, 1992 г., описан фармацевтический комбинированный препарат, содержащий рифампицин, тиацетазон и, необязательно, изониазид или этамбутол.
Стандартный курс комбинированной терапии туберкулеза состоит в назначении изониазида и рифампицина, к которым обычно добавляют другие противотуберкулезные препараты - пиразинамид и/или этамбутол. Известно комбинированное средство, содержащее в одной таблетке изониазид, рифампицин, пиразинамид и этамбутол (Лекарственные препараты в России: Справочник. М.: АстраФармСервис, 2003 г., с. Б-490).
В патенте РФ №2195937, 2003 г., предлагается комбинированный противотуберкулезный препарат, содержащий в качестве действующего начала комбинацию изониазида, рифампицина, пиразинамида, этамбутола и пиридоксина, а в качестве вспомогательного вещества метоцел - метиловые эфиры целлюлозы, содержащие 14-30% метоксильных групп (прототип).
Однако известным составам присущ ряд недостатков. При курсовом применении вышеописанных препаратов наблюдается выраженное токсическое действие и возникновение побочных эффектов. Кроме того, в известных комбинированных составах взаимное влияние ингредиентов приводит к существенному снижению биодоступности действующего начала, что ухудшает эффективность при лечении туберкулеза и служит причиной возврата заболевания и развитию резистентности к лекарственным средствам.
В качестве альтернативы был предложен комбинированый противотуберкулезный состав, включающий терапевтически эффективное количество действующего начала, в качестве которого содержит комбинацию ломефлоксацина, протионамида, пиразинамида, этамбутола гидрохлорида и пиридоксина гидрохлорида и фармацевтически приемлемые вспомогательные вещества (патент РФ №2247560, прототип). Однако в некоторых случаях терапии туберкулеза он недостаточно эффективен.
Таким образом, создание комбинированных противотуберкулезных препаратов сопряжено с разрешением ряда проблем - подбором эффективной комбинации лекарственных средств и их соотношений, которая способствует преодолению резистентности к лекарствам, а также сочетаемости различных лекарственных средств в процессе изготовления и хранения.
Задачей настоящего изобретения является создание высокоэффективного комбинированного противотуберкулезного состава, который обладает повышенной антимикробной активностью по отношению к микобактериям туберкулеза и минимальным токсическим побочным действием.
Поставленная задача решается тем, что предлагаемая фармацевтическая композиция с противотуберкулезным действием включает терапевтически эффективное количество действующего начала, в качестве которого содержит комбинацию левофлоксацина, протионамида, пиразинамида, этамбутола гидрохлорида, пиридоксина гидрохлорида и, по меньшей мере, одно фармацевтически приемлемое вспомогательное вещество
Предлагаемое сочетание действующих ингредиентов является новым для комбинированных противотуберкулезных препаратов, подобрано опытным путем и позволяет получить технический результат, соответствующий поставленной задаче, а именно существенное повышение антимикобактериальной активности по сравнению с прототипом.
В ходе сравнительного изучения специфической активности в отношении М. tuberculosis штамма H37Rv (МБТ) заявленного состав и прототипа на модели экссудативно-некротического туберкулеза мышей был определен средний срок жизни животных после заражения смертельной дозой МБТ в различных экспериментальных группах животных; изучена микробиологическим методом in vivo бактерицидная и бактериостатическая активность; оценен морфологическими методами характер репаративных процессов в паренхиматозных органах в процессе лечения экспериментального туберкулеза мышей исследуемых групп.
Определение специфической противотуберкулезной активности препаратов в системе in vivo проводили на самцах инбредных мышей линии BALB/c, полученных из вивария ЦНИИТ РАМН. Вес мышей - 22-23 грамма. Мышей заражали внутривенным введением М. tuberculosis штамма H37Rv из коллекции института Пастера (Франция) в латеральную хвостовую вену в дозе 5×106 КОЕ/мышь.
Испытуемые препараты вводили внутрижелудочно ежедневно (кроме выходных) в течение 4-х недель через 18 дней после инфицирования. Согласно программе исследования через 4 недели после начала лечения экспериментальных животных выводили из эксперимента методом цервикальной дислокации для определения количества колониеобразующих единиц (КОЕ) М. tuberculosis (МБТ) в легких мышей и гистологического исследования тканей легкого, печени и селезенки.
Для определения количества микобактерий (КОЕ МБТ) в легких зараженных мышей легкие гомогенизировали в 2 мл физиологического раствора, готовили серию 10-кратных разведении исходной суспензии в физиологическом растворе и 50 мкл каждого разведения помещали на чашку Петри, покрытую агаром Дюбо. Чашки Петри с нанесенными суспензиями клеток легкого инкубировали в течение 21 дня при 37°С, после чего подсчитывали число колоний на чашке и определяли количество КОЕ микобактерий в легких по формуле: 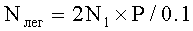 , где N - количество колоний в легких. Для гистологического изучения кусочки легкого, селезенки и печени фиксировали 10% забуференным формалином, заключали в парафин, готовили гистологические срезы, которые окрашивали гематоксилином и эозином.
, где N - количество колоний в легких. Для гистологического изучения кусочки легкого, селезенки и печени фиксировали 10% забуференным формалином, заключали в парафин, готовили гистологические срезы, которые окрашивали гематоксилином и эозином.
Основными показателями резистентности животного к туберкулезу являются срок выживаемости после инфицирования, количество КОЕ МБТ в органах инфицированных животных, тропных к туберкулезу, и степень патологических изменений внутренних органов.
У мышей контрольной группы, не получавших никаких препаратов, выживаемость после смертельной дозы заражения составила 25,5±0,26 дней. Мыши, получавшие исследуемые препараты, на момент окончания лечения и забоя (46 дней после инфицирования) были живы. Результаты микробиологического исследования in vivo представлены в таблице 1.
Согласно полученным данным показатели КОЕ МБТ в группе животных, получавших новый состав, были приблизительно на порядок ниже, чем в экспериментальной группе, получавшей прототип, т.е. изменение состава комбинированного препарата - прототипа (замена ломефлоксацина на левофлоксацин) неожиданно увеличило бактериостатическую активность препарата почти в 10 раз.
В результате гистологического исследования сравнительной терапевтической эффективности препаратов были получены следующие данные. При внутривенном введении МБТ у мышей развивается экссудативно-некротический воспалительный процесс, поражающий различные паренхиматозные органы. Контрольные животные погибли от генерализованного туберкулеза через 25 дней. К моменту гибели в легких, печени и селезенке наблюдается полнокровие, сладж эритроцитов, в кровеносных сосудах крупного и среднего калибра выявляются юные и зрелые формы ПЯЛ. Вокруг сосудов формируются клеточные инфильтраты, состоящие из моно- и полинуклеаров; количество последних варьирует в разных органах.
Особенно крупные пневмонические фокусы формируются в легких, где наряду с макрофагами и лимфоцитами определяются крупные скопления ПЯЛ. Среди альвеолярных макрофагов преобладают липофаги, которые на гистологических срезах имеют пенистую цитоплазму из-за многочисленных гранул нейтрального липида. Именно в этих клетках определяются скопления МБТ. При разрушении липофагов МБТ попадают во внутриальвеолярное пространство, где вокруг них концентрируются ПЯЛ. Поэтому наличие пенистых клеток (ПК), особенно разрушенных их форм, отражает активность специфического воспаления у мышей, которая максимально выражена у животных контрольной группы. В терминальном периоде процесса клеточные инфильтраты занимают до 70% гистологического среза; в их составе определяются крупные скопления ПК, здесь же концентрируются ПЯЛ, формирующие зоны некроза. Пограничные с очагами альвеолы частично или полностью заполнены отечной жидкостью, содержат фибрин и фрагменты разрушенных клеточных элементов. В участках паренхимы, сохраняющей воздух, межальвеолярные перегородки утолщены за счет интерстициального отека и инфильтрации моно- и полинуклеарами. Эти же клетки определяются в расширенных петлях капиллярной сети. В печени мышей контрольной группы помимо экссудативной реакции, формирования периваскулярных инфильтратов обращает внимание развитие дистрофических изменений гепатоцитов, особенно выраженных в терминальный период воспаления. Клетки печеночных балок имеют просветленную вакуолизированную цитоплазму, часто с признаками деструкции. В зонах некроза определяются ПЯЛ. Селезенка контрольных мышей обеднена лимфоцитами, наблюдается пролиферация стромальных элементов, формирование диффузных мононуклеарных инфильтратов, в составе которых определяются ПЯЛ.
У опытных мышей терапевтических групп, получавших прототип и заявленную композицию, картина туберкулезного воспаления в легких, печени и селезенке так же, как и в контроле, носит прогрессирующий характер. Наиболее характерные изменения наблюдаются в легких, где развивается экссудативно-некротический воспалительный процесс, поражающий 55-70% паренхимы. В обеих терапевтических группах повсеместно определяются крупные, сливающиеся между собой пневмонические фокусы, содержащие значительное количество ПЯЛ, в том числе в стадии деструкции. Основу пневмонических фокусов составляют пенистые макрофаги, в цитоплазме которых концентрируются МБТ (В.В.Ерохин и др., 1997). Многие макрофаги имеют разрушенную цитоплазму. Вокруг таких клеток располагаются ПЯЛ, что отражает высокую активность специфического воспаления в обеих терапевтических группах. Вместе с тем, у животных, получавших состав по изобретению, обращает внимание низкая частота выявления микронекрозов, чем в группе животных, получающих прототип или контрольной группе. В составе пневмонических фокусов ПЯЛ чаще всего располагаются диффузно, не формируют крупных скоплений, как в 3-й группе (прототип) и особенно у контрольных животных. Это свидетельствует о более выраженной терапевтической активности заявленного препарата по сравнению с препаратом сравнения.
Полученные результаты гистологического исследования свидетельствуют о том, что заявленная композиция оказывает более выраженное положительное влияние на динамику туберкулезного воспаления у экспериментальных животных по сравнению с прототипом. Таким образом, в результате исследований установлено увеличение среднего срока жизни мышей, получавших терапию препаратами в исследуемых дозах по сравнению с животными контрольной группы, при этом установлено микробиологически, что бактериостатическое действие заявленной композиции in vivo в отношении M.tuberculosis H37Rv на острой модели экссудативно-некротического туберкулеза почти на порядок превышало бактериостатический эффект препарата-прототипа; показана гистологически более выраженная терапевтическая активность новой композиции по сравнению с прототипом в связи с более низкой частотой выявления микронекрозов легочной ткани и ПЯЛ. На основании полученных данных можно сделать заключение, что композиция согласно изобретению обладает более выраженным терапевтическим действием в отношении М.tuberculosis, чем применяемый в настоящее время прототип.
Входящий в состав композиции пиридоксина гидрохлорид предупреждает или уменьшает токсические воздействия на организм, наблюдающиеся при применении противотуберкулезных препаратов. Изучение токсического действия нового препарата показало, что через две недели внутрижелудочного введения крысам в дозе 500 мг/кг (по действующему началу) гематологические (эритроциты, гемоглобин, лейкоциты, ретикулоциты, тромбоциты) и биохимические (общие липиды и глюкоза) параметры крови как показатели токсичности не отличаются от контроля. Не отмечено структурных нарушений в органах и тканях, не обнаружено также раздражающего действия новой композиции на слизистую оболочку желудочно-кишечного тракта.
Таким образом, на основании полученных результатов биологических исследований можно сделать вывод о высокой терапевтической эффективности нового препарата и возможности его применения как противотуберкулезного средства.
Предпочтительно предлагаемая композиция содержит ингредиенты действующего начала в следующем соотношении, мас.ч.:
Левофлоксацин - 1,0,
Протионамид - 0,4-1,2,
Пиразинамид - 1,35-2,75,
Этамбутола гидрохлорид - 1,4-3,3,
Пиридоксина гидрохлорид - 0,01-1,0.
Предлагаемое лекарственное средство предпочтительно выполняют в виде различных твердых лекарственных форм - таблеток, капсул, гранул, порошков. В качестве вспомогательных веществ могут быть использованы вещества, обычно применяемые в фармацевтической промышленности для производства твердых лекарственных форм, например крахмал, сахарид, целлюлоза и ее производные, желатин, поливинилпирролидон, полиэтиленоксид, фосфат кальция, лубрикант, смачивающий агент, как натрийлаурилсульфат, сложные эфиры полиоксиэтиленсорбитана и жирных кислот (твины), сложные эфиры сорбитана и жирных кислот (спаны), предпочтительно крахмал, в том числе модифицированный, лактоза, микрокристаллическая целлюлоза, натрийкроскарбоксиметилцеллюлоза, поливинилпирролидон, лубрикант. Примерами последнего являются стеариновая кислота и/или ее соли - стеарат кальция, стеарат магния, стеарат цинка, тальк, коллоидная двуокись кремния, аэросил, полиэтиленгликоль, гидрогенизованное растительное масло, жидкий парафин. Новая композиция может также содержать ароматизаторы, красители и/или вкусовые добавки. Предпочтительно препарат изготавливают в форме таблетки, которая может иметь оболочку. Наличие последней улучшает внешний вид и органолептические свойства лекарственной формы, защищает ее от механических повреждений. Предпочтительно оболочка выполняется на основе производного целлюлозы, например оксипропилметилцеллюлозы, или готовой смеси марки "Opadry".
Предпочтительное количество ингредиентов действующего начала в единичной дозе составляет: для левофлоксацина от 180 мг до 220 мг, более предпочтительно 200 мг, для протионамида от 135 мг до 165 мг, более предпочтительно 150 мг, для пиразинамида от 333 мг до 440 мг, более предпочтительно 370 мг, для этамбутола гидрохлорида от 292 мг до 400 мг, более предпочтительно 325 мг, и для пиридоксина гидрохлорида от 5 до 15 мг, более предпочтительно 10 мг.
В рамках настоящего изобретения термин левофлоксацин подразумевает также гидраты и соли левофлоксацина, например гидрохлорид левофлоксацина. Предпочтительно левофлоксацин применяется в виде гемигидрата. Данное разъяснение относится также к другим активным ингредиентам действующего начала - протионамиду, пиразинамиду, этамбутолу и пиридоксину.
В предпочтительном варианте композиция содержит в качестве левофлоксацина гемигидрат левофлоксацина.
Предпочтительно композиция содержит в качестве вспомогательных ингредиентов многофункциональный наполнитель, который одновременно является наполнителем, сухим связующим и дезинтегрантом, связующий агент, пластификатор, придающий таблетной массе пластичность и повышающий прочность получаемых таблеток-ядер (от 190 Н до 240 Н) глидант, улучшающий текучесть таблетной массы (от 3,0 г/с до 6 г/с), супердезинтегрант, обеспечивающий более быструю распадаемость таблеток-ядер, и лубрикант, предотвращающий при таблетировании налипание массы на пуансоны, затирание матриц и обеспечивающий выталкивание таблеток-ядер из них.
Предпочтительное соотношение ингредиентов заявляемой композиции составляет, г:
Левофлоксацина гемигидрат
(в пересчете на 100%-ный левофлоксацин) - 0,2000
Протионамид - 0,1500
Пиразинамид - 0,3700
Этамбутола гидрохлорид - 0,3250
Пиридоксина гидрохлорид - 0,0100
Многофункциональный наполнитель - 0,0090÷0,1600
Повидон - 0,0010÷0,0210
Макрогол - 0,0005÷0,0084
Супердезинтегрант - 0,0130÷0,2400
Глидант (скользящее вещество) - 0,0048÷0,0950
Лубрикант (смазывающее вещество) - 0,0050÷0,1000
Оболочка
Пленкообразователь - 0,0065÷0,1200
Пластификатор - 0,0018÷0,0330
Пигмент - 0,0008÷0,0150
Краситель - 0,0001÷0,0020
В качестве многофункционального наполнителя предпочтительно использовать крахмал прежелатинизированный, в качестве связующего агента - повидон, в качестве пластификатора - макрогол, в качестве супердезинтегранта - натрия кроскармеллозу, в качестве глидантов - кремния диоксид коллоидный и тальк, в качестве лубриканта - натрия стеарилфумарат, стеариновую кислоту и соли стеариновой кислоты, предпочтительно стеарат кальция и/или магния.
В качестве пленкообразователя предпочтительно использовать гипромеллозу, в качестве пластификатора - макрогол 6000 и глицерол, в качестве глиданта - тальк, в качестве пигмента - титана диоксид, в качестве красителя - железа оксид желтый.
В другом аспекте изобретения предлагается применение комбинации левофлоксацина, протионамида, пиразинамида, этамбутола гидрохлорида, пиридоксина гидрохлорида для изготовления фармацевтической композиции с противотуберкулезным действием.
В предпочтительном варианте получение заявляемой лекарственной формы может быть осуществлено методом влажной грануляции с последующим добавлением к сухим гранулам лубриканта, формованием окончательной смеси ингредиентов с образованием лекарственной формы заданной конфигурации и размера и, при необходимости, нанесением оболочки.
Изобретение иллюстрируется следующими примерами (см. Таблицу 2), которые являются лишь поясняющими, но не ограничивающими.
Пример 1. Левофлоксацин - 200 мг (1 м.ч.), протионамид 150 мг (0,75 м.ч.), пиразинамид - 370 мг (1,85 м.ч.), этамбутола гидрохлорид 325 мг (1,625 м.ч.), пиридоксина гидрохлорид 10 мг (0,05 м.ч.), вспомогательные вещества - 200 мг, в том числе прежелатинизированный крахмал - 52,9 мг, повидон - 10,0 мг, кремния диоксид коллоидный - 6,3 мг, натрийкроскармеллоза - 80,6 мг, тальк - 18,9 мг, лубрикант - 31,5 мг. Средняя масса таблетки 1260,0 мг (количество ингредиентов в мг указано на 1 таблетку).
Предварительно просеянные порошки субстанций левофлоксацина (в виде гемигидрата), протионамида, пиразинамида, этамбутола гидрохлорида и порошка крахмала прежелатинизированного перемешивают до однородного состояния, гранулируют водным раствором повидона с макроголом, сушат и размалывают полученный гранулят.
В связи с низким содержанием пиридоксина гидрохлорида в составе таблетной массы для достижения равномерного распределения его в таблетках предварительно готовят смесь пиридоксина гидрохлорида и кремния диоксида коллоидного. Для этого просеянный порошок пиридоксина гидрохлорида смешивают с просеянным порошком кремния диоксида коллоидного и полученную смесь вручную просеивают через сито.
К размолотому грануляту прибавляют предварительно приготовленную смесь пиридоксина гидрохлорида с кремния диоксидом коллоидным, натрия кроскармеллозу, тальк, лубрикант (натрия стеарилфумарат, кислоту стеариновую и соль стеариновой кислоты) и готовую массу таблетируют. Получают таблетки-ядра со средней массой 1,2600 г и прочностью 200÷250 Н.
На полученные таблетки-ядра наносят пленкообразующий состав на основе пленкообразователя гипромеллозы. К раствору пленкообразователя добавляют гомогенизированную суспензию, состоящую из талька, титана диоксида, железа оксида желтого, глицерина и раствора макрогола 6000. Нанесение оболочки проводят до получения пленки удовлетворительной толщины. Полученные таблетки, покрытые пленочной оболочкой, удовлетворяют нормативным требованиям на фармацевтическое средство. Растворение, % высвобождения левофлоксацина и протионамида в среду растворения - 0,001Н раствор кислоты хлористоводородной - через 45 минут (ВЭЖХ) - 99 и 95 соответственно, содержание активных веществ в одной таблетке (ВЭЖХ) - 200 мг (левофлоксацин), 150 мг (протионамид), 370 мг (пиразинамид), 325 мг (этамбутола гидрохлорид) и 10 мг (пиридоксина гидрохлорид). Полученные таблетки имеют срок годности более 2 лет.
Пример 2. Левофлоксацин - 200 мг (1 м.ч.), протионамид - 80 мг (0,4 м.ч.), пиразинамид - 270 мг (1,35 м.ч.), этамбутола гидрохлорид - 280 мг (1,4 м.ч.), пиридоксина гидрохлорид - 20 мг (0,1 м.ч.), вспомогательные вещества (крахмал - 36,0 мг, лактоза 55,0 мг, микрокристаллическая целлюлоза - 50,0 мг, поливинилпирролидон - 15,0 мг, полиэтиленгликоль - 5 мг, тальк - 11,0 мг, стеарат кальция - 8,0 мг). Средняя масса таблетки 1030,0 мг (количество ингредиентов в мг указано на 1 таблетку).
Смесь левофлоксацин, протионамида, пиразинамида и этамбутола гидрохлорида с микрокристаллической целлюлозой, лактозой и частью крахмала (70%) гранулируют, используя раствор поливинилпирролидона в водном спирте, в который добавляют полиэтиленгликоль, и сушат. Сухие гранулы размалывают, смешивают с пиридоксина гидрохлоридом, остатком крахмала, тальком и стеаратом кальция и таблетируют.
Пример 3. Левофлоксацин - 100 г (1 м.ч.), протионамид - 120 г (1,2 м.ч.), пиразинамид 275 г (2,75 м.ч.), этамбутола гидрохлорид - 330 г (3,3 м.ч.), пиридоксина гидрохлорид 100 г (1,0 м.ч.), вспомогательные вещества - кукурузный крахмал - 25,0 г, микрокристаллическая целлюлоза - 72,5 г, двуокись кремния - 2,5 г. Микрокристаллическую целлюлозу и двуокись кремния смешивают для получения предварительной смеси. Эту смесь, в свою очередь, смешивают с левофлоксацином, протионамидом, пиразинамидом, этамбутола гидрохлоридом, пиридоксина гидрохлоридом и крахмалом. Полученной смесью заполняют твердые желатиновые капсулы подходящего размера, используя обычные машины для заполнения капсул.
Пример 4. Левофлоксацин - 60,0 г (1 м.ч.), протионамид - 45,0 г (0,75 м.ч.), пиразинамид 111 г (1,85 м.ч.), этамбутола гидрохлорид 97,5 г (1,625 м.ч.), пиридоксина гидрохлорид 0,6 г (0,01 м.ч.), вспомогательные вещества поливинилпирролидон - 9,7 г, корригент вкуса (натрийсахаринат) - 10,2 г, ароматизатор - 10,3 г, манитол - 332,8 г, натрийлаурилсульфат - 17,5 г. Увлажняют раствором поливинилпирролидона смесь остальных ингредиентов, гранулируют на установке для получения гранулята и сушат. Получают гранулы для приготовления водно-диспергируемой суспензии орального применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННЫЙ СОСТАВ С ПРОТИВОТУБЕРКУЛЁЗНЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2247560C1 |
| КОМБИНИРОВАННЫЙ ПРОТИВОТУБЕРКУЛЕЗНЫЙ ПРЕПАРАТ | 2009 |
|
RU2430724C2 |
| КОМБИНИРОВАННАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ КОМПОЗИЦИЯ | 2009 |
|
RU2413517C1 |
| ПРОТИВОТУБЕРКУЛЁЗНОЕ СРЕДСТВО | 2003 |
|
RU2247559C1 |
| КОМБИНИРОВАННАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2468802C2 |
| КОМБИНИРОВАННЫЙ ПРОТИВОТУБЕРКУЛЕЗНЫЙ ПРЕПАРАТ | 2007 |
|
RU2354378C1 |
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА С МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ | 2013 |
|
RU2554753C2 |
| КОМБИНИРОВАННОЕ ПРОТИВОТУБЕРКУЛЕЗНОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2431487C2 |
| КОМБИНИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ПРОТИВОТУБЕРКУЛЁЗНЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2247561C1 |
| КОМБИНИРОВАННОЕ ПРОТИВОТУБЕРКУЛЕЗНОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2182483C1 |
Изобретение относится к области медицины и касается комбинированной фармацевтической композиции, обладающей противотуберкулезным действием. Состав выполняют в виде твердой лекарственной формы, которая содержит в качестве действующего начала комбинацию левофлоксацина, протионамида, пиразинамида, этамбутола гидрохлорида и пиридоксина гидрохлорида и фармацевтически приемлемые вспомогательные вещества. Состав характеризуется высокой терапевтической эффективностью. 2 н. и 8 з.п. ф-лы, 2 табл., 4 пр.
1. Фармацевтическая композиция с противотуберкулезным действием, включающая терапевтически эффективное количество действующего начала, в качестве которого содержит комбинацию левофлоксацина, протионамида, пиразинамида, этамбутола гидрохлорида и пиридоксина гидрохлорида, и, по меньшей мере, одно фармацевтически приемлемое вспомогательное вещество.
2. Фармацевтическая композиция по п.1, характеризующаяся тем, что включает ингредиенты действующего начала при следующем соотношении, мас.ч.:
3. Фармацевтическая композиция по п.1, характеризующаяся тем, что она выполнена в виде твердой лекарственной формы.
4. Фармацевтическая композиция по п.3, характеризующаяся тем, что она выполнена в форме таблетки.
5. Фармацевтическая композиция по п.4, характеризующаяся тем, что она содержит в качестве вспомогательных веществ прежелатинизированный крахмал, повидон, макрогол, кремния диоксид коллоидный, натрия кроскармеллозу, тальк, натрия стеарилфумарат, кислоту стеариновую и соль стеариновой кислоты.
6. Фармацевтическая композиция по п.4, характеризующаяся тем, что она имеет оболочку.
7. Фармацевтическая композиция по любому из пп.3-6, характеризующаяся тем, что содержит ингредиенты действующего начала в единичной дозе в следующем количестве, мг:
левофлоксацин - 200 мг, протионамид - 150 мг, пиразинамид - 370 мг этамбутола гидрохлорид - 325 мг и пиридоксина гидрохлорида - 10 мг.
8. Фармацевтическая композиция по п.7, характеризующаяся тем, что включает левофлоксацин в виде гемигидрата.
9. Применение комбинации левофлоксацина, протионамида, пиразинамида, этамбутола гидрохлорида и пиридоксина гидрохлорида для изготовления композиции с противотуберкулезным действием.
10. Применение по п.9, по которому левофлоксацин используется в виде гемигидрата.
| КОМБИНИРОВАННЫЙ СОСТАВ С ПРОТИВОТУБЕРКУЛЁЗНЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2247560C1 |
| КОМБИНИРОВАННЫЙ ПРОТИВОТУБЕРКУЛЕЗНЫЙ ПРЕПАРАТ | 2007 |
|
RU2354378C1 |
| RU 2009134910 A, 20.03.2011. | |||
Авторы
Даты
2013-04-10—Публикация
2011-07-12—Подача