Изобретение относится к медицине, в частности к материалам для возмещения дефектов костей (остеомиелитических секвестров, костных кист, очагов остеонекроза) посредством осуществления остеоиндукции и остеокондукции в полостях, заполненных предлагаемым биоматериалом.
Известен имплантат для пластики костных полостей на основе крупноячеистой коллагеновой матрицы из декальцинированной губчатой кости, причем на нем осуществляют иммобилизацию антибактериальных препаратов, культур бластных клеток и стимуляторов биогенеза (RU №2335258, 27.05.2008).
Известен биоимплантат для возмещения дефектов минерализованных тканей, который содержит минеральную составляющую, выделенную из костной ткани диафизов сельскохозяйственных животных путем воздействия 0,5 н. раствором соляной кислоты и насыщенного раствора щелочи, дополнительно содержит коллаген, белки плазмы крови пациентов с активным остеогенезом, взятой в период дистракции, физиологический раствор (RU №2311167 С2, 20.06.2006).
Недостатками известных имплантатов являются: сложность изготовления, низкая остеоиндуктивная и остеопластическая эффективность, отсутствие остеокондуктивной активности, они ограниченно биосовместимы, окружаются фиброзной капсулой. При получении известных имплантатов используют деминерализующие вещества, нарушающие естественную микроархитектонику и химический состав костной ткани, что отрицательно сказывается на остеинтеграционных свойствах имплантатов и клинических результатах.
Задачей изобретения является создание биоматериала с высокими остеоиндуктивными, остеокондуктивными и остеоинтеграционными свойствами, имеющего высокопористую структуру, близкую к естественной структуре минерального матрикса костной ткани, а также упрощение процедуры изготовления.
Указанный технический результат достигается тем, что способ получения биоматериала для возмещения дефектов костей включает механическую очистку костей от параоссальных мягких тканей, органические компоненты кости удаляют с помощью 6% раствора гипохлорита натрия в течение 6-8 суток, измельчают в фарфоровой ступке до размеров гранул диаметром 50-100 мкм, промывают в дистиллированной воде и 96% этаноле и высушивают при комнатной температуре в течение суток. Полученный биоматериал характеризуется шероховатостью и наноструктурированностью и имеет упорядоченную высокопористую структуру с размером пор 50-150 мкм, близкую к естественной структуре минерального матрикса костной ткани.
Настоящее изобретение поясняют описанием, примером использования и иллюстрациями, на которых изображено:
Фиг.1 - упорядоченная высокопористая трехмерная организация биоматериала, близкая к естественной структуре минерализованного матрикса костной ткани. Сканирующая электронная микроскопия;
Фиг.2 - прикрепление к поверхности биоматериала остеогенных клеток и кровеносного сосуда свидетельствует об остеоинтеграционной эффективности биоматериала. Сканирующая электронная микроскопия;
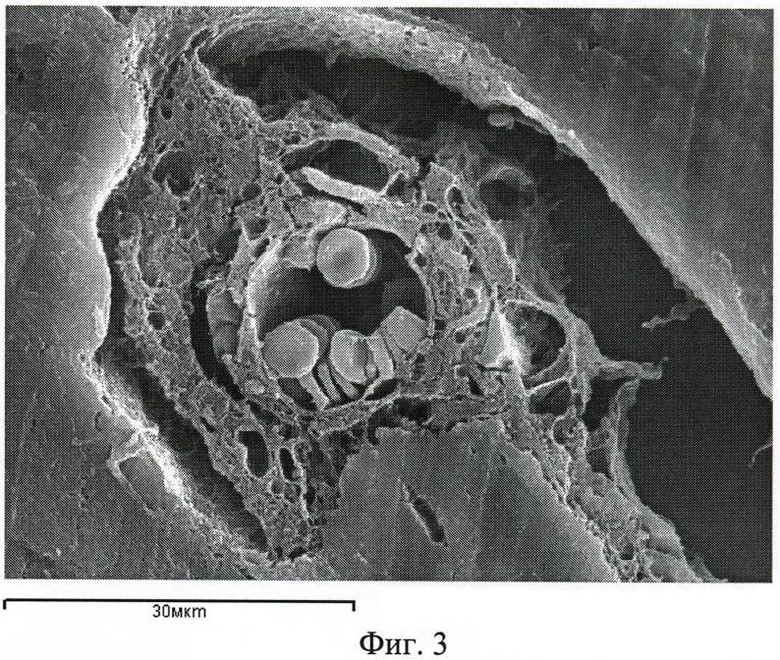
Фиг.3 - врастание кровеносных сосудов и периваскулярных остеогенных клеток в трехмерную высокопористую структуру биоматериала свидетельствует о высоких остеоиндуктивных и остеокондуктивных свойствах биоминерала. Сканирующая электронная микроскопия;
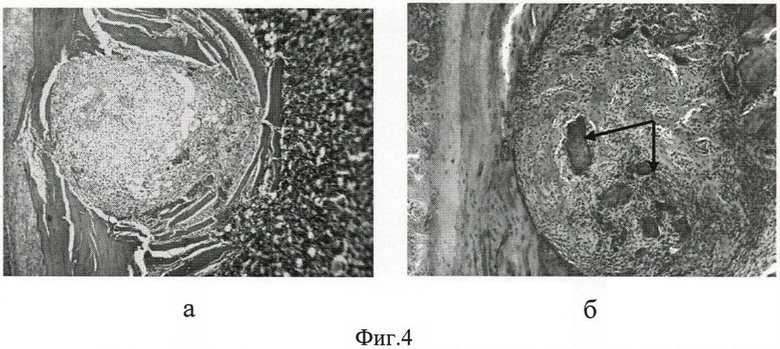
Фиг.4 - эффективность биоматериала, как стимулятора регенерации костной ткани при возмещении дырчатого дефекта большеберцовой кости экспериментальных животных (крыс): а - регенерат животного контрольной группы, б - регенерат животного опытной группы. Срок эксперимента 7 суток. Стрелками обозначены гранулы биоматериала, окруженные новообразованной костной тканью в необычно ранние сроки. Световая микроскопия парафинового среза. Окраска гематоксилином и эозином. Объектив 10, окуляр 10;
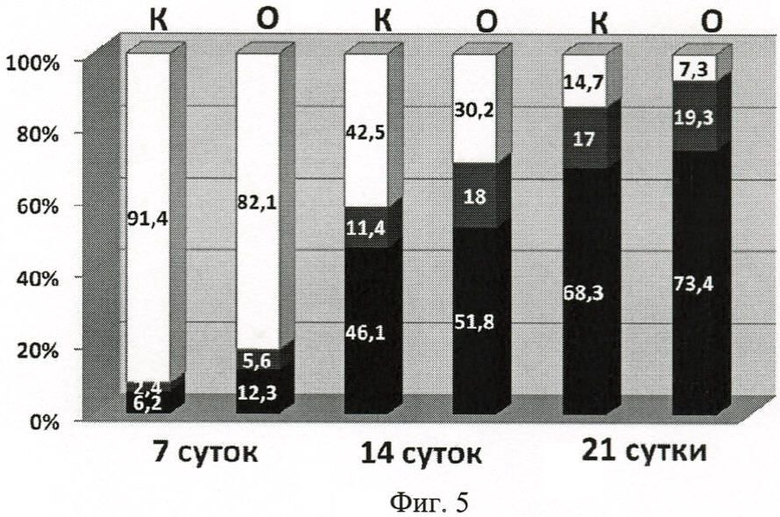
Фиг.5 - доля различных тканевых компонентов в составе регенерата, формирующегося после перфорационной травмы большеберцовой кости крыс, в контроле (K) и опыте (О) через 7, 14 и 21 сутки после операции. Белый цвет - неминерализованные компоненты; темно-серый - остеоид костной ткани; черный - минерализованный матрикс костной ткани. Результаты рентгеновского эдектронно-зондового микроанализа.
Способ получения биоматериала осуществляют следующим образом.
Кости сельскохозяйственных животных очищают механическим способом от параоссальных мягких тканей. Органические компоненты кости (клетки, сосуды, костный мозг) удаляют с помощью 6% раствора гипохлорита натрия в течение 6-8 суток. Очищенную кость либо костные блоки измельчают в фарфоровой ступке до размеров частиц 50-100 мкм по трем измерениям (ширина, длина и высота). Полученный порошок, состоящий из гранул диаметром 50-100 мкм, промывают в дистиллированной воде и 96% этаноле и высушивают при комнатной температуре в течение суток.
Полученный биоматериал имеет упорядоченную высокопористую структуру с размером пор 50-150 мкм, близкую к естественной структуре минерального матрикса костной ткани (фиг.1).
Пример использования биоматериала.
В эксперименте на 60 взрослых крысах линии Wistar под общей анестезией в проксимальной трети диафиза большеберцовых костей в контрольной и опытной группах моделировали несквозные дырчатые дефекты диаметром 2 мм и глубиной 2,5-3 мм. В опытной группе животным непосредственно после операции в область сформированного дефекта вводили стерильный порошок биоматериала. Операционную рану послойно ушивали узловыми швами.
Сканирующая электронная микроскопия показала, что биоматериал имеет высокопористую структуру, содержит взаимосвязанные поры размером 50-150 мкм и сохраняет естественную архитектонику минерализованного матрикса костной ткани (фиг.1). Микрорельеф поверхности биоматериала характеризуется шероховатостью и наноструктурированностью, что обеспечивают оптимальные отношения между уровнем адгезии, темпами пролиферации и степенью дифференциации остеогенных клеток (фиг.2). Кровеносные сосуды и остеогенные клетки вросли в биоматериал, что свидетельствует о его высоких остеокондуктивных и остеоиндуктивных свойствах (фиг.3). После введения биоматериала активизировалось репаративное костеобразование и сократились сроки возмещения дефекта кости, о чем свидетельствует проведенное гистологическое исследование (фиг.4). Так в опытной группе животных через 7 суток после операции объем костной ткани в регенерате возрос более чем в 2 раза - с 8,6±0,41% в контроле до 17,9±0,63% в опыте (Р<0,001) (фиг.5).
Использование предлагаемого способа в отделе экспериментальной травматологии и ортопедии ФГБУ «РНЦ «ВТО» им. акад. Г.А.Илизарова» позволило получить биоматериал без воздействия деминерализующих веществ, который имеет высокопористую структуру, близкую к естественной структуре минерального матрикса костной ткани. Предложенный способ упростил процедуру изготовления биоматериала, а его применение позволило сократить сроки возмещения дефектов костей.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ ВЫСОКООЧИЩЕННОГО МИНЕРАЛЬНОГО МАТРИКСА В ВИДЕ СЕГМЕНТОВ И ГРАНУЛ С ОСТЕОИНДУКТИВНЫМИ СВОЙСТВАМИ ДЛЯ ЗАМЕЩЕНИЯ КОСТНЫХ ДЕФЕКТОВ | 2018 |
|
RU2693606C1 |
| Скаффолд для замещения костных дефектов | 2020 |
|
RU2768571C1 |
| БИОТРАНСПЛАНТАТ НА ОСНОВЕ ПЕНОКЕРАМИЧЕСКИХ НОСИТЕЛЕЙ СИСТЕМЫ ОКСИД ЦИРКОНИЯ - ОКСИД АЛЮМИНИЯ И МУЛЬТИПОТЕНТНЫХ СТРОМАЛЬНЫХ КЛЕТОК КОСТНОГО МОЗГА ЧЕЛОВЕКА ДЛЯ ВОССТАНОВЛЕНИЯ ПРОТЯЖЕННЫХ ДЕФЕКТОВ КОСТНОЙ ТКАНИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2386453C1 |
| КОМПОЗИЦИЯ - ОСТЕОИНДУКТОР И ОСТЕОКОНДУКТОР, ПРИ ЛЕЧЕНИИ КОСТНОЙ ПАТОЛОГИИ В СТОМАТОЛОГИИ И ЧЕЛЮСТНО-ЛИЦЕВОЙ ХИРУРГИИ, И СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ - ОСТЕОИНДУКТОРА И ОСТЕОКОНДУКТОРА, ПРИ ЛЕЧЕНИИ КОСТНОЙ ПАТОЛОГИИ В СТОМАТОЛОГИИ И ЧЕЛЮСТНО-ЛИЦЕВОЙ ХИРУРГИИ | 2008 |
|
RU2383564C1 |
| ТРЕХМЕРНЫЕ МАТРИЦЫ ИЗ СТРУКТУРИРОВАННОГО ПОРИСТОГО МОНЕТИТА ДЛЯ ТКАНЕВОЙ ИНЖЕНЕРИИ И РЕГЕНЕРАЦИИ КОСТИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2009 |
|
RU2491960C9 |
| МЕДИЦИНСКИЙ КЛЕЙ-БИОИМПЛАНТАТ НОВОГО ПОКОЛЕНИЯ НА ОСНОВЕ БИОПОЛИМЕРНЫХ НАНОКОМПОЗИТОВ В ВИДЕ ПОЛУСИНТЕТИЧЕСКОЙ ПОЛИМЕРНОЙ МАТРИЦЫ С ПРИМЕНЕНИЕМ ЛАЗЕРНЫХ ТЕХНОЛОГИЙ | 2011 |
|
RU2477996C1 |
| МНОГОМЕРНЫЙ БИОМАТЕРИАЛ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2010 |
|
RU2542430C2 |
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2783642C1 |
| Устройство, комплект и способ для введения трансплантата в костный регенерат | 2020 |
|
RU2741206C1 |
| Способ трансплантации биокомпозитных сфероидов для обеспечения возможности восстановления целостности кости при дефектах, размеры которых превышают критические | 2020 |
|
RU2744756C1 |


Настоящее изобретение относится к медицине и описывает способ получения биоматериала для возмещения дефектов костей, включающий механическую очистку костей от параоссальных мягких тканей, где органические компоненты кости удаляют с помощью 6% раствора гипохлорита натрия в течение 6-8 суток, измельчают в фарфоровой ступке до размеров гранул диаметром 50-100 мкм, промывают в дистиллированной воде и 96% этаноле и высушивают при комнатной температуре в течение суток. Полученный биоматериал характеризуется шероховатостью, наноструктурированностью и имеет упорядоченную высокопористую структуру с размером пор 50-150 мкм, близкую к естественной структуре минерального матрикса костной ткани. 2 н.п. ф-лы, 1 пр., 5 ил.
1. Способ получения биоматериала для возмещения дефектов костей, включающий механическую очистку костей от параоссальных мягких тканей, отличающийся тем, что органические компоненты кости удаляют с помощью 6%-ного раствора гипохлорита натрия в течение 6-8 суток, измельчают в фарфоровой ступке до размеров гранул диаметром 50-100 мкм, промывают в дистиллированной воде и 96% этаноле и высушивают при комнатной температуре в течение суток.
2. Биоматериал для возмещения дефектов костей, полученный способом по п.1, состоящий из минерального порошка, выделенного из костной ткани сельскохозяйственных животных, отличающийся тем, что полученный биоматериал характеризуется шероховатостью, наноструктурированностью и имеет упорядоченную высокопористую структуру с размером пор 50-150 мкм, близкую к естественной структуре минерального матрикса костной ткани.
| WO 2008032928 А1, 20.03.2008 | |||
| US 5417975 А, 23.05.1995 | |||
| US 4919931 А, 24.04.1990 | |||
| БИОИМПЛАНТАТ ДЛЯ ВОЗМЕЩЕНИЯ ДЕФЕКТОВ МИНЕРАЛИЗОВАННЫХ ТКАНЕЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2311167C2 |
Авторы
Даты
2013-04-10—Публикация
2011-11-23—Подача