Предлагаемое изобретение относится к органической химии, в частности к способу получения N,S-циклосодержащего производного хитозана (I), имеющего структурную формулу:

где n=50-70%, m=30-50%.
В настоящее время хитозан и его производные рассматриваются как почвенные структурообразователи: компания Экогель выпускает запатентованный хитозансодержащий препарат «Антистресс», предназначенный для ускорения приживляемости, а также акклиматизации импортных или пересаженных растений (http://www.ecogel.ru).
Подобные N,S-циклосодержащие биополимеры, имеющие глюкопиранозные и 1-окса-6-тиа-4,8-диазциклоундекановые гетероциклы, представляют интерес как высокоэффективные сорбенты тяжелых металлов для очистки сточных вод, экстрагенты для разделения редких, благородных и драгоценных металлов, а также селективные комплексообразователи биологических молекул (T.Becker, М.Schlaak, Н.Strasdeit // Reactive and Functional Polymers, 2000, 44, p.289-298. Z. Cao, H. Ge, S. Lai // European Polymer Journal, 2001, 37, p.2141-2143).
Известно, что хитозан, а также его производные являются перспективными полисахаридными материалами для создания ионообменных мембран, применяемых при ультрафильтрации и диализе, а их комплексообразующая способность может использоваться для селективного извлечения ряда металлов из морской воды (Э.В.Прут, А.Н.Зеленецкий // Успехи химии, 2001, т.70, №1, с.72-87). Хитозан и его фосфорсодержащие производные, в частности фосфат хитозана, могут использоваться в качестве биосовместимых материалов (Wang X., Ma J., Wang Y., He B. // Biomaterials, 2001, v.22, no.16, p.2247), сорбентов для извлечения урана (Sakaguchi Т., Hirokoshi Т., Nakajima А. // Agric. Biol. Chem., 1981, v.45, no.10, p.2191), хиральных матриц для создания металлокомплексных катализаторов (Guibal Е. // Prog. Polym. Sci., 2005, v.30, no.1, p.71).
Согласно литературным данным химическая модификация хитозана может осуществляться по всем функциональным группам. Так, известен способ получения N,О-карбоксиметил-N,О-сульфопроизводного хитозана (Zhao Xia, LV Zhihua, XU Jiamin, YU Guangli // Journal of Ocean University of Qingdao, 2003, v.2, no.1, p.69-74), обладающего ингибирующим действием по отношению к тромбоцитам крови:

Существуют примеры модификации хитозана исключительно по первичной аминогруппе полисахарида. Известен способ получения N-алкилпроизводных хитозана, который основан на взаимодействии хитозана с алифатическими альдегидами путем введения алкильных заместителей по аминогруппе исходного полимера через основания Шиффа (Keisuke Kurita, Satoko Mori, Yasuhiro Nishiyama, Manabu Harata // Polymer Bulletin, 2002, 48, p.159-166). Было показано, что с увеличением алкильного радикала возрастает антибактериальная активность производных хитозана (Chun Но Kim, Jang Won Choi, Heung Jae Chun, Kyu Suk Choi // Polymer Bulletin, 1997, v.38, no.4, p.387-393).

Наиболее близким прототипом является способ, основанный на взаимодействии хитозана с формальдегидом и тиолом с получением серосодержащего производного, имеющего привитые линейные N-алкилтиометильные группы (Tanja Becker, Michael Schlaak, Henry Strasdeit // Reactive and Functional Polymers, 2000, 44, p.289-298), который селективно сорбирует кадмий в присутствии солей никеля и цинка.

Таким образом, в литературе отсутствуют данные о модификации хитозана по аминогруппе с получением N,S-содержащих циклических производных хитозана.
Перед авторами стояла задача получения циклического N,S-содержащего производного хитозана взаимодействием тиометилирующего реагента «CH2O-H2S» (A Wohl. Berichte, 1886, 19, 2344) с первичными аминогруппами исходного биополимера. Сведения о получении указанного выше циклического производного подобным методом в литературе отсутствуют.
Поставленная цель достигается взаимодействием насыщенного сероводородом водного 37%-ного раствора формальдегида с солянокислым раствором хитозана, взятыми в мольном соотношении исходных реагентов хитозан:формальдегид:сероводород, равном 1:2:1, при температуре 0-60°С и перемешивании в течение 24 часов. Реакционную смесь нейтрализуют слабым раствором NaOH, модифицированный полимер осаждают 70%-ным этанолом и центрифугируют. При этом получают N,S-циклосодержащее производное хитозана (I), в макроцепи которого наряду с 2-амино-D-пиранозными фрагментами имеются 1-окса-6-тиа-4,8-диазациклоундекановые фрагменты. Реакция протекает по схеме:

где n=50-70%, m=30-50%.
Изучено влияние модифицированного хитозана (I) и его солей на основе щавелевой (С2Н2О4) и аскорбиновой (С6Н8О6) кислот на силу роста проростков и развитие корневой гнили на растениях пшеницы. Объекты исследований были обработаны водными растворами образца (I) и его солями с концентрацией 1%, 0,1% и 0,01%. Результаты исследований представлены в таблице 1. Величина показателей характеризует отношение длины листа к длине корня.
Показано, что продукт (I) в концентрации 0,01% влияет на силу роста проростков пшеницы, а на подавление корневой гнили влияет как сам, так и его соли в концентрациях от 1,0% до 0,01%. Аддукт с аскорбиновой кислотой в концентрации 0,1% подавляет развитие корневой гнили полностью. В результате проведенных исследований выявлено, что продукт тиометилирования хитозана проявляет хорошую фунгицидную активность, при этом он экологически абсолютно безопасен и коммерчески доступен.
Существенные отличия предлагаемого способа
В предлагаемом способе осуществляется взаимодействие насыщенного сероводородом формальдегида - диэлектрофильного реагента, способного одновременно взаимодействовать с двумя аминогруппами хитозана - (1-4)-2-амино-2-дезокси-D-гликополисахаридом. В результате данный способ позволяет получить циклическое N,S-содержащее производное хитозана (I) с 1-окса-6-тиа-4,8-диазациклоундекановыми фрагментами в макроцепи, сведения о котором в литературе отсутствуют.
В отличие от прототипа (Tanja Becker, Michael Schlaak, Henry Strasdeit // Reactive and Functional Polymers, 2000, 44, p.289-298) реакция проходит с образованием S,N-гетероциклов на хитозановой матрице.
Преимущества предлагаемого способа
Способ позволяет получить N,S-циклосодержащее производное хитозана (I), образующее устойчивый гидрогель, синтез которого в литературе не описан, и отличается простотой проведения эксперимента.
Способ поясняется примером
Пример 1. В трехгорлую колбу, снабженную мешалкой, обратным холодильником и барботером, термостатированную при заданной температуре, загружали 3,3 мл 37%-ного (10 ммоль) формалина, 30 мин барботировали сероводород (получен из расчетного количества Na2S и HCl) с образованием смеси CH2O и H2S в соотношении 2:1. Затем к реакционной массе прибавляли по каплям 0,8 г (5 ммоль) хитозана, растворенного в 100 мл 2%-ной HCl. Смесь перемешивали при 0°С в течение 24 часов. Реакционную массу нейтрализовали раствором NaOH до pH=7, модифицированный хитозан осаждали 70%-ным этанолом в соотношении по объему 1:3, добавляя по каплям концентрированный раствор NaCI. Осажденный полимер центрифугировали и трехкратно промывали 70%-ным спиртом, сушили на воздухе. В результате получили 1,04 г N,S-циклосодержащего производного хитозана (I) с 30%-ной функционализацией.
Пример 2. В трехгорлую колбу, снабженную мешалкой, обратным холодильником и барботером, термостатированную при заданной температуре, загружали рассчитанное количество 37%-ного формалина, 30 мин барботировали сероводород (получен из расчетного количества Na2S и HCl) с образованием смеси CH2O и H2S в соотношении 2:1. Затем к реакционной массе прибавляли по каплям расчетное количество моль хитозана (0,8 г), растворенного в 100 мл 2%-ной HCl. Смесь перемешивали при температуре 20°С в течение 24 часов. Реакционную массу нейтрализовали раствором NaOH до рН 7, модифицированный хитозан осаждали 70%-ным этанолом в соотношении по объему 1:3, добавляя по каплям концентрированный раствор NaCI. Осажденный полимер центрифугировали и трехкратно промывали 70%-ным спиртом, сушили на воздухе. В результате получили 1,20 г N,S-циклосодержащего производного хитозана (I) с 35%-ной функционализацией.
Пример 3. В трехгорлую колбу, снабженную мешалкой, обратным холодильником и барботером, термостатированную при заданной температуре, загружали рассчитанное количество 37%-ного формалина, 30 мин барботировали сероводород (получен из расчетного количества Na2S и HCl) с образованием смеси CH2O и H2S в соотношении 2:1. Затем к реакционной массе прибавляли по каплям расчетное количество моль хитозана (0,8 г), растворенного в 100 мл 2%-ной HCl. Смесь перемешивали при 60°С в течение 24 часов. Реакционную массу нейтрализовали раствором NaOH до рН 7, модифицированный хитозан осаждали 70%-ным этанолом в соотношении по объему 1:3, добавляя по каплям концентрированный раствор NaCI. Осажденный полимер центрифугировали и трехкратно промывали 70%-ным спиртом. В результате получили 1,04 г N,S-циклосодержащего производного хитозана (I) с 50%-ной функционализацией.
Спектральные характеристики1 (1ИК-спектры получили на спектрофотометре «Specord 75IR» в суспензии в вазелиновом масле. Одномерные спектры ЯМР1H, 13C и двумерные спектры (HSQC, COSY) соединения I зарегистрированы на спектрометре “Bruker Avance 400”, внутренний стандарт - ТМС, растворитель DMSO-d6.)
N,S-циклосодержащего производного хитозана (I):
Соединение I
ИК-спектр, v, см-1: 750, 1050, 1170, 1620, 2900, 3200.
Спектр ЯМР 1Н, D2O, м.д., δ: 1.83 с (3Н, NHAc), 2.88 уш.с (1Н, Н-2); 3.45 уш.с (1Н, Н-5); 3.69 уш.с (5Н, Н-4, Н-6, Н-7); 3.82 уш.с (1H, Н-3), 4.95 уш.с (1H, Н-1), 5.45 уш.с (1Н, NH), 8.54 уш.с (2Н, NH2).
Спектр ЯМР 13С, м.д., δ: 55.9 д, (С-2); 57.8 т (С-7); 57.9 т (С-6); 71.8 д (С-3), 75.9 д (С-5), 77.7 д (С-4), 97.5 д (С-1).

где n=50-70%, m=30-50%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СЕРОСОДЕРЖАЩИХ ПРОИЗВОДНЫХ ПОЛИАКРИЛАМИДА | 2011 |
|
RU2465287C1 |
| СПОСОБ ПОЛУЧЕНИЯ НЕРАСТВОРИМОГО В ВОДЕ СЕРОСОДЕРЖАЩЕГО БИОПОЛИМЕРА НА ОСНОВЕ ХИТОЗАНА | 2012 |
|
RU2520493C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 2-, 3- И 4-(1,3,5-ДИТИАЗИНАН-5-ИЛ) ТИОФЕНОЛОВ | 2009 |
|
RU2425039C2 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 6,7-ДИГИДРО-1,3,5,7-БЕНЗОТРИТИАЗОНИНА | 2008 |
|
RU2440348C2 |
| СПОСОБ ПОЭТАПНОГО ПОЛУЧЕНИЯ 1,7,13,19,25,31,37,43-ОКТАТИА-3,5,9,11,15, 17,21,23,27,29,33,35,39,41,45,47-ГЕКСАДЕКААЗАЦИКЛООКТАТЕТРАКОНТАН-4,10,16,22,28,34,40,46-ОКТАТИОНА И 5,6-ДИГИДРО-2Н-ТИАДИАЗИН ГИДРОЙОДИДА | 2010 |
|
RU2490264C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,7-ДИТИА-1,5-ДИАЗАБИЦИКЛО[3.3.1]НОНАНА, ОБЛАДАЮЩЕГО ФУНГИЦИДНЫМИ СВОЙСТВАМИ | 2011 |
|
RU2489438C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-(1,3,5-ДИТИАЗИНАН-5-ИЛ)-ТИОМОЧЕВИНЫ | 2009 |
|
RU2414460C1 |
| ВЫСВОБОЖДАЮЩИЕ СЕРОВОДОРОД ПОЛИМЕРНЫЕ СОЕДИНЕНИЯ | 2017 |
|
RU2768716C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3,5-ТИАДИАЗИНАН-4-(ТИ)ОНОВ | 2010 |
|
RU2447067C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3,3'-(3,6-ДИОКСАОКТАН-1,8-ДИИЛ)БИС-1,5,3-ДИТИАЗЕПИНАНА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2547267C2 |
Настоящее изобретение относится к способу получения N,S-циклосодержащего производного хитозана. Описан способ получения N,S-циклосодержащего полимера (I) на основе хитозана, содержащего в макроцепи 1-окса-6-тиа-4,8-диазоциклоундекановые фрагменты:

взаимодействием хитозана с формальдегидом и S-содержащим соединением, отличающийся тем, что в качестве S-содержащего соединения используют сероводород, раствор формальдегида предварительно насыщают H2S и реакцию проводят при мольном соотношении хитозан - формальдегид - сероводород, равном 1:2:1, при температуре 0÷60°С в солянокислой среде в течение 24 часов. Технический результат - получение модифицированного хитозана, проявляющего свойства высокоэффективного сорбента тяжелых металлов для очистки сточных вод, экстрагента для разделения редких, благородных и драгоценных металлов, комплексообразователя биологических молекул. 1 табл., 3 пр.
Способ получения N,S-циклосодержащего полимера (I) на основе хитозана, содержащего в макроцепи 1-окса-6-тиа-4,8-диазоциклоундекановые фрагменты
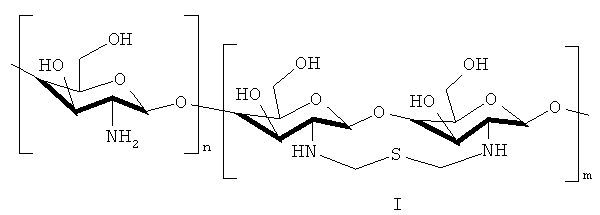
взаимодействием хитозана с формальдегидом и S-содержащим соединением, отличающийся тем, что в качестве S-содержащего соединения используют сероводород, раствор формальдегида предварительно насыщают H2S и реакцию проводят при мольном соотношении хитозан - формальдегид - сероводород, равном 1:2:1, при температуре 0÷60°С в солянокислой среде в течение 24 ч.
Авторы
Даты
2013-04-10—Публикация
2010-06-02—Подача