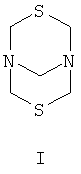
Предлагаемое изобретение относится к органической химии, в частности к усовершенствованному способу получения 3,7-дитиа-1,5-диазабицикло[3.3.1]нонана общей формулы (I), обладающего фунгицидными свойствами:

Подобные N,S-содержащие гетероциклы могут найти применение в качестве биологически активных веществ по отношению к различным патогенным микроорганизмам, в частности к плесневым грибам [Ахметова В.Р., Мурзакова Н.Н., Хабибуллина Г.Р., Галимзянова Н.Ф. ЖПХ. 2011, 2, 229; Ахметова В.Р., Ниатшина З.Т., Буракаева А.Д., Галимзянова Н.Ф., Кунакова Р.В. ЖПХ. 2011, 3, 424].
Известен способ получения 3,7-дитиа-1,5-диазабицикло[3.3.1]нонана (I) исходя из гидросульфида аммония и формальдегида [C.G.LeFevre, R.J.W.LeFevre, J. Chem. Soc, 1932, 1142]. Структура (I) доказана методом ЯМР 1H и PCA [Глейтер Р., Зефиров Н.С., Палюлин В.А., Потехин К.А., Куркутова Е.И., Стручков Ю.Т., Антипин М.Ю. ЖОрХ. 1978, 14, 1630].
Недостатком способа является труднодоступность исходного реагента аммонийгидросульфида.

Наиболее близким аналогом является способ получения (I) исходя из аммонийгидроксида, формальдегида и сероводорода [Ахметова В.Р., Надыргулова Г.Р., Тюмкина Т.В., Старикова З.А., Антипин М.Ю., Кунакова Р.В., Джемелев У.М. Циклотиометилирование аминоспиртов с помощью СН2О и H2S. ЖОрХ. 2007, 6, 919].
Известная реакция проходит неселективно и выход 3,7-дитиа-1,5-диазабицикло[3.3.1]нонана (I) составляет 39%.

Предлагаемый новый способ селективного получения 3,7-дитиа-1,5-диазабицикло[3.3.1]нонана (I) с высоким выходом на основе доступных реагентов.
Сущность способа заключается во взаимодействии при температуре -5÷5°C в течение 4-8 ч, аммония хлористого с водным раствором тиометилирующей смеси, предварительно полученной барботажем сероводорода через 37%-ный раствор формальдегида, взятых в мольном соотношении NH4Cl:CH2O:H2S=10:(25-35):(25-35). После нейтрализации раствора (NaOH) до pH~7 получают кристаллический 3,7-дитиа-1,5-диазабицикло[3.3.1]нонан, общей формулы (I) с выходом 81-99%.
Реакция протекает по схеме

Существенные отличия предлагаемого способа
В предлагаемом способе в качестве исходного реагента применяется аммоний хлористый, реакция идет при температуре -5÷5°C. Данный способ позволяет селективно (100%) и с высоким выходом до 99% получать 3,7-дитиа-1,5-диазабицикло[3.3.1]нонан (I).
В известном способе [Ахметова В.Р., Надыргулова Г.Р., Тюмкина Т.В., Старикова З.А., Антипин М.Ю., Кунакова Р.В., Джемелев У.М. Циклотиометилирование аминоспиртов с помощью CH2O и H2S. ЖОрХ. 2007, 6, 919] в качестве исходного реагента применяется аммонийгидроксид, реакция проводится при температуре 70°C, образуется бицикл (I) с выходом 39%.
Преимущества предлагаемого способа
Способ позволяет селективно (~100%) и с высоким выходом (до 99%) получать 3,7-дитиа-1,5-диазабицикло[3.3.1]нонан (I).
Способ поясняется следующими примерами.
Пример
В трехгорлую колбу, снабженную мешалкой, обратным холодильником и барботером, термостатированную при заданной температуре, загружают 30 ммоль 37%-ного формалина, барботируют ~0.5 ч 30 ммоль сероводорода (H2S получают из Na2S и HCl), затем к реакционной массе добавляют 10 ммоль аммоний хлористый в 10 мл воды, перемешивают при температуре 0°C в течение 6 ч, нейтрализуют раствором NaOH до рН~7. Образовавшийся осадок фильтруют и сушат, получают индивидуальный 3,7-дитиа-1,5-диазабицикло[3.3.1]нонан (I) с выходом 92%.
Спектральные характеристики1 (1 ИК-спектр получили на спектрофотометре «Specord 75IR» в суспензии в вазелиновом масле. Элементный анализ образца (С, N, H, S) определили на анлизаторе фирмы Karlo Erba, модель 1106. Температуру плавления определили на приборе PIIMK 80/2617. Криоскопическое определение (Мкр) проводили по методу Раста. Спектры ЯМР 1H и 13C зарегистрированы на спектрометре «Jeol FX 90Q» (89.55 и 22.50 МГц) и Broker Avance-400, внутренний стандарт Me4Si, растворитель ДМСО-d6)) 3,7-дитиа-1,5-диазабицикло[3.3.1]ионана (I):
соединение (I), белое порошкообразное вещество. Тпл. 65-67°C.
ИК-спектр, ν/см-1: 491, 598, 678, 702, 820, 963, 1022, 1263, 1318, 1672.
Найдено(%): C 37.2; H 6.2; N 17.3; S 39.5.
Масс-спектр, m/z (Iотн, %): 162(20) [M]+, 129(7) [М-SH]+, 120(9) [М-CH2NCH2], 97(11) [М-NCH2NCCl]+, 89(6) [М-SCH2NCH]+, 73(5) [SCH2NCH]+, 57(15) [CSCH]+, 46(8) [CH2S]+, 42(100) [CH2NCH]+.
Спектр ЯМР 13C (CDCl3, δ, м.д.): 55.04 (c, C (2, 4, 6, 8)), 70.02 (c, C (9)).
Спектр ЯМР 1H и параметры ренгентоструктурного анализа совпадают с описанным в литературе [Глейтер Р., Зефиров Н.С., Палюлин В.А., Потехин К.А., Куркутова Е.И., Стручков Ю.Т., Антипин М.Ю. ЖОрХ. 1978, 14, 1630].
Другие примеры, потверждающие способ, приведены в таблице 1
Все опыты проводили при атмосферном давлении с последующей нейтрализацией реакционной массы с помощью водного раствора NaOH до рН~7.
Оценку фунгицидной активности проводили методом диффузии в агар. Поверхность питательных сред КГА (картофельно-глюкозный агар), среда Чапека, разлитых по 20-25 мл в стандартные чашки Петри d 90 мм, засевали суспензией спор тест-культур грибов. Затем в среде сверлом диаметром 10 мм вырезали 3 лунки, в которые помещали по 100 мкл испытываемых растворов. Фунгицидную активность оценивали по диаметру зоны подавления роста микромицетов, а также наблюдая за развитием тест-культур с использованием светового микроскопа «Amplival» (Carl Zeiss, JENA). Контролем служило развитие грибов на питательной среде. Время инкубации 7 суток при 28°C.
В качестве тест-культур были использованы Bipolaris sorokiniana, Fusarium oxysporum, Aspergillus niger, Bipolaris sorokiniana и Fusarium oxysporum, которые вызывают различные заболевания сельскохозяйственных растений, в том числе и корневые гнили зерновых культур. Aspergillus niger является распространенным контаминантом различных материалов, способен вызывать аллергические реакции и микозы у людей с ослабленной иммунной системой, кроме того, Aspergillus niger используется при лабораторных испытаниях материалов и изделий на грибостойкость.
Нами изучена фунгицидная активность 3,7-дитиа-1,5-диазабицикло[3.3.1]нонана (I) в растворе ДМФА. Предварительно установили, что ДМФА не оказывает влияния на развитие грибов. Результаты фунгицидной активности приведены в таблице 2.
Соединение - 3,7-дитиа-1,5-диазабицикло[3.3.1]нонан (I) проявляет фунгицидные действия по отношению к микроскопическим грибам: максимальный ингибирующий эффект по отношению Bipolaris sorokiniana проявляется начиная с концентрации 0.015, Fusarium oxysporum - 0.02, по отношению к Aspergillus niger - 0.01.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-КООРДИНИРОВАННЫЙ МЕТИЛИОДИДОМ 3,7-ДИТИА-1,5-ДИАЗАБИЦИКЛО[3.3.0]ОКТАН - ВОДОРАСТВОРИМОЕ СРЕДСТВО С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2442329C1 |
| 3,7-ДИТИА-1,5-ДИАЗАБИЦИКЛО[3.3.0]ОКТАН - СРЕДСТВО С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2448971C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,3'-БИ-1,5,3-ДИТИАЗЕПИНАНА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2448107C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,3'-(3,6-ДИОКСАОКТАН-1,8-ДИИЛ)БИС-1,5,3-ДИТИАЗЕПИНАНА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2547267C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,6-БИС-(1,5,3-ДИТИАЗЕПАН-3-ИЛ)-2,5-ДИСУЛЬФАНИЛГЕКСАНА, ОБЛАДАЮЩЕГО ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2547266C2 |
| СПОСОБ ПОЛУЧЕНИЯ 5-МЕТОКСИКАРБОНИЛ-1,3-ДИТИАНА, ОБЛАДАЮЩЕГО ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2536205C2 |
| 2-ФЕНИЛТИОМЕТИЛ ЗАМЕЩЕННЫЕ 1,3-ДИКЕТОНЫ И ДИМЕТИЛМАЛОНАТ - СРЕДСТВА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2616603C2 |
| СРЕДСТВО ДЛЯ БОРЬБЫ С ГРИБКОВЫМИ ЗАБОЛЕВАНИЯМИ СЕЛЬСКОХОЗЯЙСТВЕННЫХ КУЛЬТУР | 2011 |
|
RU2483539C1 |
| СПОСОБ ПОЛУЧЕНИЯ N, N'-БИС-(2-ГИДРОКСИЭТИЛ)ТЕТРАТИАДИАЗАЦИКЛОАЛКАНОВ, ПРОЯВЛЯЮЩИХ ФУНГИЦИДНУЮ АКТИВНОСТЬ | 2013 |
|
RU2541793C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-[(ФЕНИЛСУЛЬФАНИЛ)МЕТИЛ]ПЕНТАН-2,4-ДИОНА, ПРОЯВЛЯЮЩЕГО ФУНГИЦИДНУЮ АКТИВНОСТЬ | 2015 |
|
RU2615155C2 |
Изобретение относится к способу получения 3,7-дитиа-1,5-диазабицикло[3.3.1]нонана общей формулы (I). Сущность способа заключается во взаимодействии тиометилирующей смеси, предварительно полученной барботажем сероводорода через 37%-ный водный раствор формальдегида, с водным раствором аммония хлористого в мольном соотношении NH4Cl : CH2O : H2S = 10 : (25-35) : (25-35), при температуре -5÷5°C в течение 4-8 ч. Технический результат: разработан селективный (100%) способ получения 3,7-дитиа-1,5-диазабицикло[3.3.1]нонана, который может найти применение в качестве фунгицидного агента по отношению к плесневым грибам. 2 табл., 1 пр.
Способ получения 3,7-дитиа-1,5-диазабицикло[3.3.1]нонана общей формулы (I), обладающего фунгицидныси свойствами в отношении Bipolaris sorokiniana, начиная с концентрации 0.015, Fusarium oxysporum - 0.02, Aspergillus niger - 0.01,

отличающийся тем, что тиометилирующую смесь, предварительно полученную барботажем сероводорода через 37%-ный раствор формальдегида, подвергают взаимодействию с водным раствором аммония хлористого в мольном соотношении NH4Cl : CH2O : H2S = 10 :(25-35):(25-35), при температуре -5÷5°C в течение 4-8 ч.
| СПОСОБ СТЕРЕОСЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 2,4-ЦИС-8-АНТИ-ТРИАЛКИЛ-3-ТИА-1,5-ДИАЗАБИЦИКЛО[3.2.1]ОКТАНОВ | 2008 |
|
RU2378276C1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСИ 3-ТИА-1,5-ДИАЗАБИЦИКЛО[4.3.1]ДЕКАНА И 5-[4-(1,3,5-ДИТИАЗИНАН-5-ИЛ)БУТИЛ]1,3,5-ДИТИАЗИНАНА | 2006 |
|
RU2323933C1 |
| DE 4111656 A, 15.10.1992. | |||
Авторы
Даты
2013-08-10—Публикация
2011-11-08—Подача