Перекрестная ссылка
Данная заявка заявляет приоритет по заявке США с регистрационным номером 60/981,981, поданной 23 октября 2007, и заявке США с регистрационным номером 60/984,838, поданной 2 ноября 2007 года, которая включена в данный документ путем ссылки в полном объеме.
Описание изобретения
В данном документе предложены соединения формулы:
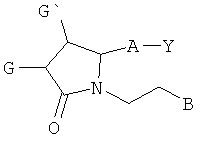
где Y содержит от 0 до 14 атомов углерода и представляет собой:
функциональную группу органической кислоты, либо ее амид или сложный эфир; гидроксиметил или его простой эфир; либо функциональную группу тетразолил; А представляет собой -(СН2)6-, цис-СН2СН=СН-(СН2)3-, или -СН2С=С-(СН2)3-, где 1 или 2 атома углерода могут быть замещены атомами S или О; либо А является
-(СН2)m-Ar-(СН2)о-, где Ar представляет собой интерарилен, сумма m и о равна 1, 2, 3 или 4, и где 1 группа -СН2- может быть замещена S или О, и где 1 группа -СН2-СН2- может быть замещена -СН=СН- или -С=С-;
G и G` независимо друг от друга представляют собой -Н, -ОН, -O-алкил, содержащий от 1 до 6 атомов углерода, галоген, C1-6алкил, -CF3, -CN, либо =O;
и
В является арилом.
Такие соединения могут использоваться для понижения внутриглазного давления. Как было показано, понижение внутриглазного давления замедляет развитие или препятствует возникновению первичной открытоугольной глаукомы. Следовательно, такие соединения также могут использоваться для лечения глаукомы. Различные типы подходящих лекарственных форм и лекарственных препаратов, хорошо известных из уровня техники, можно использовать для доставки соединений, описываемых в настоящем документе. Например, соединение можно растворить или суспендировать в водном растворе или эмульсии с получением соответствующего уровня рН и вводить местно в глаз млекопитающего.
В настоящем описании термин «лечить», «лечение», или «воздействие» относится к использованию соединения, композиции, терапевтически активного компонента, либо лекарства для диагностики, терапии, облегчения, лечения, либо предотвращения заболевания или другого нежелательного состояния.
«Стабильный» означает, что соединение остается достаточно стабильным при хранении в сосуде при комнатной температуре в условиях нормального давления в течение не менее 12 часов, либо является достаточно стабильным, чтобы удовлетворять любым целям, описанным в настоящем документе.
Если не указано иное, ссылку на соединение следует понимать широко с включением фармацевтически приемлемых солей, пролекарств, таутомеров, альтернативных твердых форм, нековалентных комплексов, а также их комбинаций, химического объекта с изображенной структурой или химического наименования.
Фармацевтически приемлемая соль представляет собой соль исходного соединения, которая подходит для введения животному или человеку. Фармацевтически приемлемая соль также относится к любой соли, образующейся in vivo в результате введения кислоты, другой соли или пролекарства, которое преобразуется в кислоту или соль. Соль включает одну или несколько ионных форм соединения, таких как конъюгированная кислота или основание, связанные с одним или несколькими соответствующими противоионами. Соли могут быть образованы или включать одну или несколько депротонированных кислотных групп (например, карбоновых кислот), одну или несколько протонированных основных групп (например, амины), или оба типа одновременно (например, цвиттер-ионы).
Пролекарство представляет собой соединение, переходящее в терапевтически активное соединение после введения. Например, переход может произойти в результате гидролиза сложноэфирной группы или другой биологически неустойчивой группы. Получение пролекарств хорошо известно в уровне техники. Например, в главе "Prodrugs and Drug Delivery Systems" ("Пролекарства и системы доставки лекарств") из книги Ричарда Б. Силвермана «Organic Chemistry of Drug Design and Drug Action» (Органическая химия производства и действия лекарств), 2nd Ed., Elsevier Academic Press: Amsterdam, 2004, pp.496-557, представлена более полная информация по этой теме. Например, рассматриваются алкиловые эфиры, такие как метиловый, этиловый, изопропиловый, и подобные. Также рассматриваются Пролекарства, содержащие полярные группы, такие как гидроксил или морфолин.
Примеры таких пролекарств включают соединения, содержащие функциональные группы -CO2(СН2)2OH,
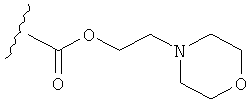
и подобные.
Таутомеры являются изомерами, находящимися в состоянии динамического равновесия одного с другим. Например, таутомеры могут быть связаны путем переноса протона, атома водорода, или гидрид-иона.
За исключением случаев, когда стереохимия обозначена ясно и однозначно, понимается, что структура включает все возможные стереоизомеры, как в чистом виде, так и любые их возможные смеси.
Альтернативные твердые формы представляют собой различные твердые формы, отличные от тех, что образуются в результате выполнения техник, описанных в данном документе. Например, альтернативными твердыми формами могут быть полиморфы, различные виды аморфных твердых форм, стекловидные формы и тому подобные.
Нековалентные комплексы представляют собой комплексы, которые могут образовываться между соединением и одним или несколькими дополнительными химическими фрагментами без ковалентного взаимодействия между соединением и дополнительными химическими фрагментами. Они могут либо характеризоваться, либо нет, особенным соотношением между соединением и дополнительными химическими фрагментами. Примеры могут включать сольваты, гидраты, комплексы с переносом заряда и тому подобные.
Y представляет собой функциональную группу органической кислоты, либо ее амид или сложный эфир; либо Y представляет собой гидроксиметил или его простой эфир, либо Y представляет собой функциональную группу тетразолила. В контексте настоящего изобретения, Y содержит от 0 до 14 атомов углерода, от 0 до 5 атомов кислорода, от 0 до 2 атомов азота, от 0 до 2 атомов серы и от 0 до 1 атома фосфора и любое необходимое количество атомов водорода.
Функциональная группа органической кислоты представляет собой кислотную функциональную группу органической молекулы. Не ограничивая объем настоящего изобретения, функциональные группы органической кислоты могут содержать оксид углерода, серу или фосфор. Так, не ограничивая объем настоящего изобретения, в некоторых соединениях Y представляет собой функциональную группу карбоновой кислоты, сульфоновой или фосфоновой кислоты.
Эфиры и амиды органических функциональных групп представляют собой карбонильные группы, напрямую соединенные с атомом азота или кислорода. Так, ниже изображены эфиры амидов карбоновых кислот, сульфоновой кислоты, а также функциональные группы фосфоновой кислоты.
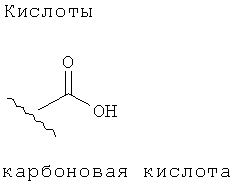
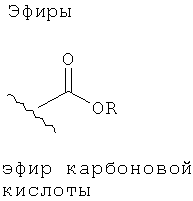
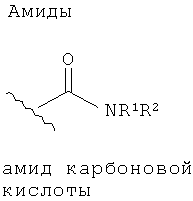
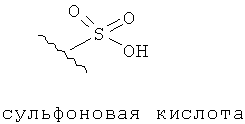
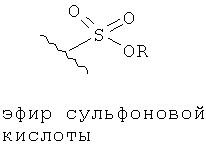
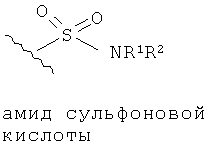
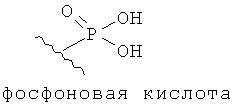
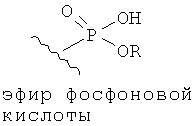
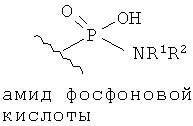
Амид также может содержать функциональную группу -SO2-. Например, амид -CONHSO2R3, где R3 представляет собой углеводородный остаток, содержащий от 1 до 14 атомов углерода. R, R1, R2 и R3 являются углеводородными остатками, для которых также распространяется условие, что Y должен содержать не более 14 атомов углерода.
Углеводородный остаток представляет собой фрагмент, состоящий из углерода и водорода, включая, но не ограничиваясь ими:
а. Алкил, представляющий собой углеводородный остаток, не содержащий двойных или тройных связей, такой как:
- линейный алкил, например метил, этил, н-пропил, н-бутил, н-пентил, н-гексил и тому подобные,
- разветвленный алкил, такой как изопропил, трет-бутил и другие разветвленные изомеры бутила, разветвленные изомеры пентила и тому подобные,
- циклоалкил, например циклопропил, циклобутил, циклопентил, циклогексил и тому подобные,
- комбинации линейных, разветвленных и/или циклических алкилов;
б. Алкенил, представляющий собой углеводородный остаток, содержащий одну или несколько двойных связей, включая линейные, разветвленные или циклические алкенилы;
в. Алкинил, представляющий собой углеводородный остаток, содержащий одну или несколько тройных связей, включая линейные, разветвленные и циклические алкинилы;
г. Комбинации алкилов, алкенилов и/или алкинилов.
С1-6 углеводородный остаток представляет собой углеводородный остаток, содержащий 1, 2, 3, 4, 5 или 6 атомов углерода.
C1-6 алкил представляет собой алкил, содержащий 1, 2, 3, 4, 5 или 6 атомов углерода, такой как метил, этил, изомеры пропила, изомеры бутила, изомеры пентила и изомеры гексила и тому подобные.
Гидроксиалкил представляет собой алкил-ОН, такой как гидроксиметил, гидроксиэтил и тому подобные. C1-6 гидроксиалкил представляет собой гидроксиалкил, содержащий 1, 2, 3, 4, 5 или 6 атомов углерода.
Простым эфиром гидроксиметила является -CH2OR.
Функциональная группа незамещенного тетразолила имеет две таутомерные формы, которые могут быстро переходить из одной формы в другую в водной или биологической среде, и которые тем самым являются эквивалентными друг другу.
Данные таутомеры показаны ниже.
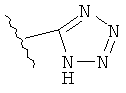
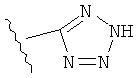
Более того, если R2 представляет собой C1-C6 алкил, фенил или бифенил, также возможны другие изомерные формы тетразольной функциональной группы, подобные изображенным ниже, незамещенные и замещенные углеводородным остатком тетразолилы вплоть до С14 также понимаются включенными в понятие «тетразолил».
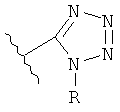
В одном из воплощений Y представляет собой -CO2R4, -CONR5R6,
-CON(CH2CH2OH)2, -CONH(СН2СН2ОН), -СН2ОН, -Р(O)(ОН)2, -CONHSO2R4,
-SO2NR5R6,
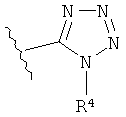 или
или 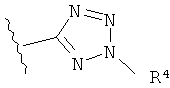
где R4, R5, и R6 независимо друг от друга представляют собой Н, C1-С6 алкил, С1-C6 гидроксиалкил, незамещенный фенил или незамещенный бифенил, при условии, что Y должен содержать не более 14 атомов углерода.
А представляет собой -(СН2)6-, цис-СН2СН=СН-(СН2)3-, либо -СН2С≡С-(СН2)3-, где 1 или 2 атома углерода могут быть замещены S или О; либо А представляет собой -(CH2)m-Ar-(CH2)о-, где Ar представляет собой интерарилен, сумма m и о равна 1, 2, 3 или 4, где одна группа -СН2- может быть замещена атомами S или О, и 1 группа -СН2-СН2- может быть замещена -СН=СН- или -С=С-.
Так, А может представлять собой -(СН2)6-, цис-СН2СН=СН-(СН2)3-, либо
-СН2С≡С-(СН2)3-.
В качестве альтернативы, А может представлять собой группу, относящуюся к одной из этих трех функциональных групп, где любой атом углерода замещен S или О. Например, А может представлять собой функциональную группу, где S замещает один или два атома углерода так, как в случаях, приведенных ниже, или подобным образом.
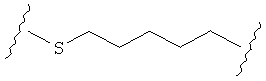
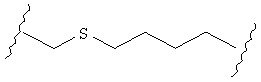
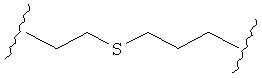
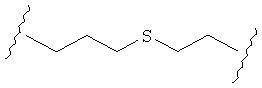
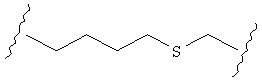
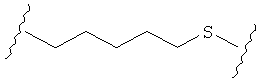
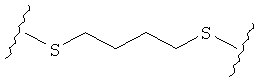
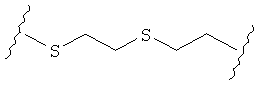
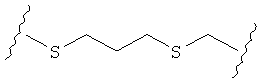
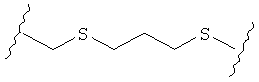
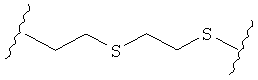
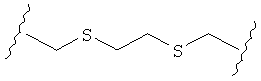
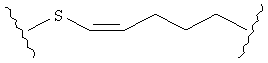
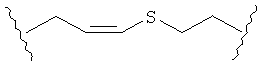
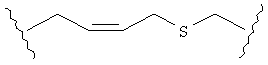
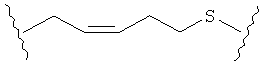
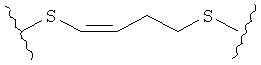
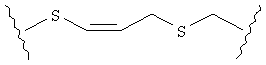
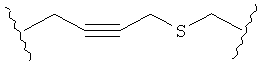
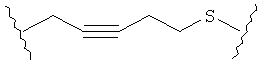
В другом случае А может представлять собой функциональную группу, где О замещает один или два атома углерода так, как в случаях, приведенных ниже, или подобным образом.
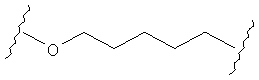
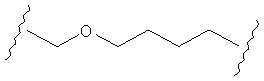
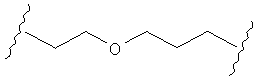
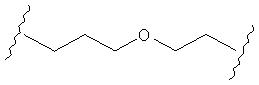
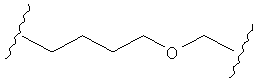
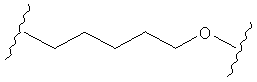
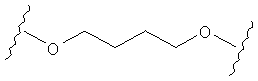
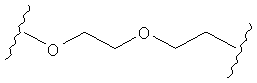
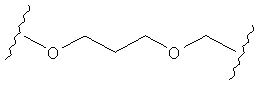
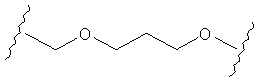
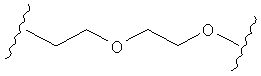
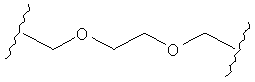
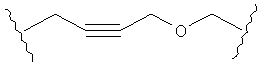
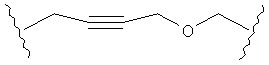
С другой стороны, А может содержать атом О, замещающий один атом углерода и атом S, замещающий другой атом углерода так, как в случаях, приведенных ниже, или подобным образом.
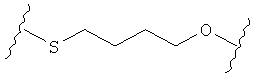
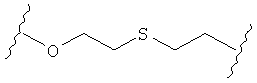
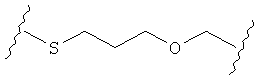
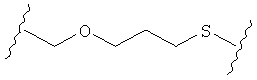
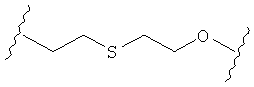
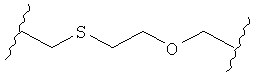
Иначе, в некоторых воплощениях А представляет собой -(CH2)m-Ar-(CH2)o-, где Ar является интерариленом или сумма m и о равна 1, 2, 3 или 4, и где 1 группа -СН2- может быть замещена S или О, и 1 группа -CH2-CH2- может быть замещена -СН=СН- или -С≡С-. Другими словами, в одном воплощении А содержит:
1) а) 1, 2, 3 или 4 функциональные группы -СН2-, или
б) 0, 1 или 2 функциональные группы -СН2- и -СН=СН- или -С≡С-; и
2) Ar;
например, -СН2-Ar, -(СН2)2-Ar-, -СН=СН-Ar, -C≡C-Ar-, -СН2-Ar-СН2-, -CH2Ar-(СН2)2-, -CH2Ar-СН=СН-, -CH2Ar-С≡С-, -(СН2)2-Ar-(СН2)2-, и тому подобные;
в другом воплощении А содержит:
1) а) О; и 0, 1, 2 или 3 функциональные группы -СН2-; или
б) О; и 0 или 1 функциональную группу -СН2- и -СН=СН- или -С≡С-; и
2) Ar;
например, -O-Ar-, -Ar-СН2-O-, -O-Ar-(СН2)2-, -OAr-СН=СН-, -O-Ar-С≡С-,
-O-СН2-Ar-, -O-СН2-Ar-(СН2)2, -O-CH2Ar-СН=СН-, -O-CH2Ar-С≡С- и тому подобные, либо
в другом воплощении А содержит:
1) а) S; и 0, 1, 2 или 3 функциональные группы -СН2-; либо
б) S; и 0 или 1 функциональную группу -СН2- и -СН=СН- либо -С≡С-, и
2) Ar;
например, -S-Ar-, -Ar-CH2-S-, -S-Ar-(CH2)2-, -SAr-CH=CH-, -S-Ar-C≡C-, -S-CH2-Ar-, -S-CH2-Ar-(CH2)2, -S-CH2Ar-CH=CH-, -S-CH2Ar-C≡C- и тому подобные.
В другом воплощении сумма m и о равна 2, 3 или 4, причем одна группа -СН2 может быть замещена атомами S или О, и 1 группа -CH2-CH2- может быть замещена
-СН=СН- или -С≡С-.
В другом воплощении сумма m и о равна 3, причем одна группа -СН2 может быть замещена S или О, и 1 группа -СН2-СН2- может быть замещена -СН=СН- или -С≡С-.
В другом воплощении сумма m и о равна 2, причем одна группа -CH2- может быть замещена S или О, или 1 группа -СН2-СН2- может быть замещена -СН=СН- или -С≡С-.
В другом воплощении сумма m и о равна 4, причем одна группа -СН2- может быть замещена S или О, и 1 группа -СН2-СН2- может быть замещена -СН=СН или -С≡С-.
Интерарилен относится к арильному кольцу или кольцевой системе, включая гетероарильное кольцо или кольцевую систему, соединяющим две разные части молекулы, то есть две части объединены в кольцо в двух совершенно разных кольцевых положениях. Интерарилен может быть замещенным или незамещенным.
Незамещенный интерарилен не содержит заместителей, отличных от двух частей молекулы, которые он соединяет. Замещенный интерарилен имеет дополнительные заместители помимо двух частей молекулы, которые он соединяет.
В одном воплощении Ar представляет собой замещенный или незамещенный интерфенилен, интертиенилен, интерфурилен, интерпиридинилен, интероксазолилен и интертиазолилен. Заместители Ar должны быть стабильными, и каждый должен содержать от 0 до 4 атомов углерода, от 0 до 3 атомов кислорода, от 0 до 2 атомов серы, от 0 до 2 атомов азота, от 0 до 3 атомов фтора, от 0 до 1 атома хлора, от 0 до 1 атома брома, от 0 до 1 атома йода и от 0 до 10 атомов водорода. Если заместитель является кислотным или основным, число атомов, указанное выше, относится к нейтральной форме заместителя. Например, нейтральная форма включает -СО2Н, но не -CO2 -Na+ либо -NH3, а не NH4 +Cl.
В ином воплощении А представляет собой -СН2-Ar-ОСН2-. В другом воплощении А представляет собой -CH2-Ph-OCH2-. В другом воплощении, Ph(фенил) присоединен в положениях 1 и 3, известный под названием м-интерфенилен, так, что А имеет структуру, показанную ниже.
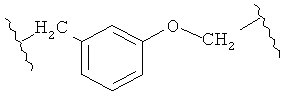
В другом воплощении А представляет собой -(СН2)6-, цис-СН2-СН=СН-(СН2)3-, либо -СН2С≡С-(СН2)3-, где 1 или 2 атома углерода могут быть замещены S или О, либо А представляет собой -(СН2)2-Ph, где одна группа -СН2- может быть замещена атомом S или О.
В другом воплощении А является -(CH2)6-, цис-СН2СН=СН-(СН2)3-, или -СН2С≡С-(СН2)3-, где 1 или 2 атома углерода могут быть замещены S или О; либо А представляет собой -(СН2)2-Ph-.
В другом воплощении Ar является тиенилом.
В других воплощениях А имеет одну из приведенных ниже структур.
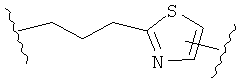
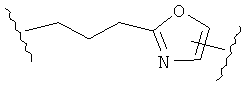
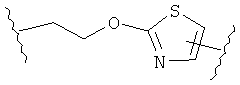
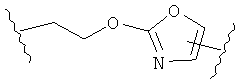
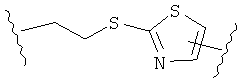
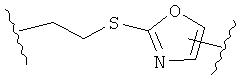
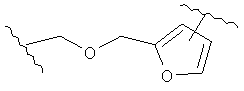
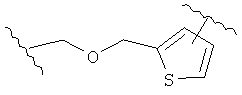
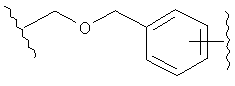
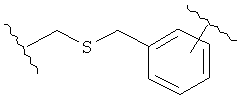
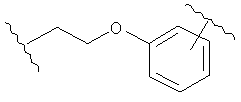
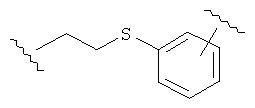
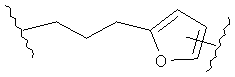
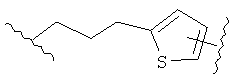
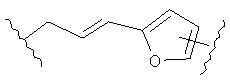
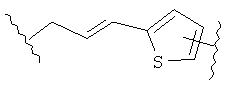
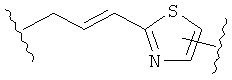
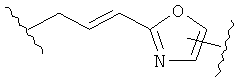
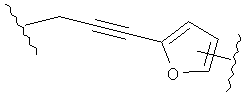
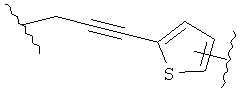
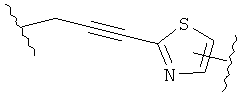
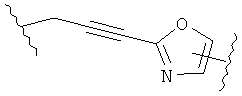
В другом воплощении А представляет собой -CH2OCH2Ar-.
В другом воплощении А представляет собой -CH2SCH2Ar-.
В другом воплощении А представляет собой -(СН2)3Ar-.
В другом воплощении А представляет собой -CH2O(СН2)4-.
В другом воплощении А представляет собой -CH2S(CH2)4-.
В другом воплощении А представляет собой -(СН2)6-.
В другом воплощении А представляет собой цис-СН2СН=СН-(СН2)3-.
В другом воплощении А представляет собой -СН2С≡С-(СН2)3-.
В другом воплощении А представляет собой -S(СН2)3S(СН2)2-.
В другом воплощении А представляет собой -(СН2)4OCH2-.
В другом воплощении А представляет собой цис-СН2-СН=СН-CH2OCH2-.
В другом воплощении А представляет собой -СН2СН≡СН-CH2OCH2-.
В другом воплощении А представляет собой -(CH2)2S(CH2)3-.
В другом воплощении А представляет собой -СН2-Ph-ОСН2-, где Ph представляет собой интерфенилен.
В другом воплощении А представляет собой -CH2-мPh-OCH2-, где мРh представляет собой м-интерфенилен.
В другом воплощении А представляет собой -СН2-O-(СН2)4-.
В другом воплощении А представляет собой -СН2-O-СН2-Ar-, где Ar представляет собой 2,5-интертиенилен.
В другом воплощении А представляет собой -СН2-O-СН2-Ar-, где Ar представляет собой 2,5-интерфурилен.
В другом воплощении А представляет собой (3-метилфенокси)метил.
В другом воплощении А представляет собой (4-бут-2-инилокси)метил.
В другом воплощении А представляет собой 2-(2-этилтио)тиазол-4-ил.
В другом воплощении А представляет собой 2-(3-пропил)тиазол-5-ил.
В другом воплощении А представляет собой 3-(метоксиметил)фенил.
В другом воплощении А представляет собой 3-(3-пропилфенил).
В другом воплощении А представляет собой 3-метилфенетил.
В другом воплощении А представляет собой 4-(2-этил)фенил.
В другом воплощении А представляет собой 4-фенетил.
В другом воплощении А представляет собой 4-метоксибутил.
В другом воплощении А представляет собой 5-(метоксиметил)фуран-2-ил.
В другом воплощении А представляет собой 5-(метоксиметил)тиофен-2-ил.
В другом воплощении А представляет собой 5-(3-пропил)фуран-2-ил.
В другом воплощении А представляет собой 5-(3-пропил)тиофен-2-ил.
В другом воплощении А представляет собой 6-гексил.
В другом воплощении А представляет собой (Z)-6-гекс-4-енил.
G представляет собой -Н, -ОН, -O-алкил, содержащий от 1 до 6 атомов углерода, галоген, C1-6 алкил, -CF3, -CN или =O.
В одном воплощении, G представляет собой -Н.
В другом воплощении, G представляет собой -ОН.
В другом воплощении, G представляет собой O-алкил, содержащий от 1 до 6 атомов углерода. Другими словами, G представляет собой -ОМе, -OEt, -OiPr и тому подобные, вплоть до 6 атомов углерода.
В другом воплощении G представляет собой галоген.
В другом воплощении G представляет собой С1-6алкил.
В другом воплощении G представляет собой -CF3.
В другом воплощении G представляет собой -CN.
В другом воплощении G представляет собой =O.
G` представляет собой -Н, -ОН, -O-алкил, содержащий от 1 до 6 атомов углерода, галоген, C1-6алкил, -CF3, -CN или =O.
В одном воплощении G` представляет собой Н.
В другом воплощении G` представляет собой -ОН.
В другом воплощении G` представляет собой -O-алкил, содержащий от 1 до 6 атомов углерода. Другими словами, G` представляет собой -ОМе, -OEt, -OiPr и тому подобные, вплоть до 6 атомов углерода.
В другом воплощении G` является галогеном.
В другом воплощении G` является С1-6 алкилом.
В другом воплощении G` является -CF3.
В другом воплощении G` является -CN.
В другом воплощении G` является =O.
G и G` являются независимыми, это означает, что природа одного не влияет на природу другого. Так, они могут быть одинаковыми, например G и G` могут представлять собой -Н. Либо они могут быть разными, например G может быть -Н, а G` может представлять собой =O.
В представляет собой арил.
Арил представляет собой ароматическое кольцо или кольцевую систему, такую как фенил, нафтил, бифенил и тому подобные. Арил также включает гетероарил, который представляет собой ароматическое кольцо или кольцевую систему, содержащую один или несколько гетероатомов О, N или S. Арил может быть замещенным или незамещенным, и если не оговорено иное, «арил» или «гетероарил» следует понимать как «замещенный или незамещенный арил» или «замещенный или незамещенный гетероарил». Аналогично, если не указано иное, любое конкретное арильное кольцо, такое как «фенил», «пиридинил», «тиенил», «фурил» и тому подобные, следует понимать как «замещенный или незамещенный фенил», «замещенный или незамещенный пиридинил», «замещенный или незамещенный тиенил», «замещенный или незамещенный фурил» и тому подобные. Заместители арила для В должны быть стабильными, и могут содержать от 0 до 12 атомов углерода, от 0 до 4 атомов кислорода, от 0 до 2 атомов серы, от 0 до 3 атомов азота, от 0 до 3 атомов фтора, от 0 до 2 атомов хлора, от 0 до 2 атомов брома, от 0 до 1 атома йода. Если заместитель является кислотным или основным, число атомов, указанное выше, относится к нейтральной форме заместителя. Например, нейтральные формы включают -CO2H, но не 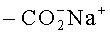
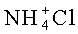
В одном воплощении В представляет собой фенил.
В другом воплощении В представляет собой пиридинил.
В другом воплощении В представляет собой тиенил.
В другом воплощении В представляет собой фурил.
Примеры заместителей могут включать следующие, с учетом ограничений, определенных в данном документе для конкретной функциональной группы или заместителя:
А. углеводородный остаток, включая, но не ограничиваясь ими:
а. Алкил, такой как:
- линейный алкил, например метил, этил, н-пропил, н-бутил, н-пентил, н-гексил, и тому подобные.
- разветвленный алкил, например изо-пропил, трет-бутил и другие разветвленные изомеры бутила, разветвленные изомеры пентила, и тому подобные.
- циклоалкил, например циклопропил, циклобутил, циклопентил, циклопентил и тому подобные.
- комбинации линеных, разветвленных и/или циклических алкилов;
б. Алкенил, представляющий собой углеводородный остаток, содержащий 1 или несколько двойных связей, включая линейные, разветвленные или циклические алкенилы;
в. Алкинил, представляющий собой углеводородный остаток, содержащий 1 или несколько тройных связей, включая линейные, разветвленные или циклические алкинилы;
г. Комбинации алкилов, алкенилов и/или алкинилов.
Б. алкил-CN, такой как -СН2-CN, -(CH2)2-CN, -(СН2)3-CN и тому подобные.
В. Гидрокси, -ОН.
Г. Гидроксиалкил, то есть алкил-ОН, такой как гидроксиметил, гидроксиэтил и тому подобные.
Д. Эфирные заместители, включая -O-алкил, алкил-O-алкил и тому подобные.
Е. Тиоэфирные заместители, включая -S-алкил, алкил-S-алкил и тому подобные.
Ж. Аминные заместители, включая -NH2, -NH-алкил, -N-алкил1алкил2 (то есть алкил1 и алкил2 могут быть одинаковыми или разными, и оба присоединены к N), алкил-NH2, алкил-NH-алкил, алкил-N-алкил1алкил2 и тому подобные.
З. Аминоалкил, означающий алкил-амин, такой как аминометил(-СН2-амин),
-аминоэтил и тому подобные.
И. Другие заместители, включая -CO2-алкил, -CO2-фенил и тому подобные.
К. Другие карбонильные заместители, включая альдегиды, кетоны, такие как ацил, включая ацетил, пропионил и бензоил.
Л. Фторуглеводороды или гидрофторуглеводороды, такие как -CF3, -CH2CF3 и тому подобные, и
М. другие заместители, содержащие азот, такие как -CN, -NO2.
Н. Другие заместители, содержащие серу, такие как сульфиды, сульфонил или сульфоксид.
О. Арил.
П. Комбинации указанных выше заместителей также возможны, учитывая указанные ограничения.
Р. В другом случае, заместителями могут являться -F, -Cl, -Br или -J.
В одном воплощении Y представляет собой CO2R4.
В другом воплощении G представляет собой водород.
Другое воплощение представляет собой соединение формулы:
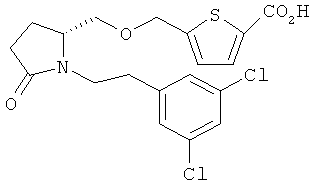
Другое воплощение представляет собой соединение формулы:
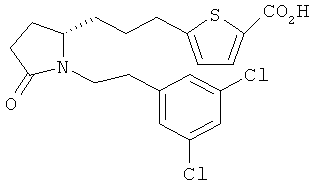
Другое воплощение представляет собой соединение формулы:
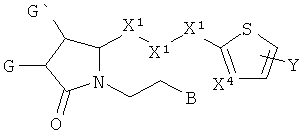
причем каждый X1 независимо представляет собой -CH2-, -O-, или -S-; и
X4 представляет собой -СН- или -N-.
Так, поскольку каждый X1 является независимым, Х1-Х1-Х1 может представлять собой -(СН2)3-, -O(СН2)2-, -S(CH2)2-, -(CH2)2O-, -(CH2)2S-, -CH2OCH2-, -CH2SCH2- и тому подобные.
В одном воплощении X4 представляет собой -СН-.
В другом воплощении X4 представляет собой -N-.
Другое воплощение представляет собой соединение формулы:
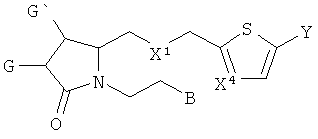
Другое воплощение представляет собой соединение формулы:
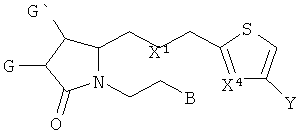
В другом воплощении G представляет собой водород.
В другом воплощении G` представляет собой -Н, -ОН, -ОСН3, F, Cl, -СН3, -CF3, -CN либо =O.
В другом воплощении G` представляет собой -Н.
В другом воплощении G представляет собой -Н, -ОН, -ОСН3, F, Cl, -СН3, -CF3, -CN либо =O.
В другом воплощении В представляет собой фенил или пиридинил.
В другом воплощении В представляет собой фенил.
В другом воплощении В представляет собой фенил с 1-3 заместителями, независимо выбранными из: -F, -Cl, -Br, -J, -ОН, -NH2, -NO2, -ОСН3, -С1-4алкила, -CF3, -CN, -СНО, -CO2H и -CH2OH.
В другом воплощении В представляет собой дихлорфенил.
Другим воплощением является применение соединений, описанных в настоящем изобретении, в производстве лекарственных препаратов для лечения глаукомы или глазной гипертензии у млекопитающего.
Другим воплощением является способ лечения глаукомы или глазной гипертензии, включающий введение соединения, описанного в настоящем документе, млекопитающему в случае необходимости такого лечения.
Жидкая композиция, включающая соединение, описанное в настоящем документе, и фармацевтически приемлемый эксципиент.
Структуры, изображенные ниже, иллюстрируют гипотетические примеры используемых соединений.
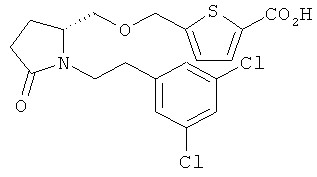
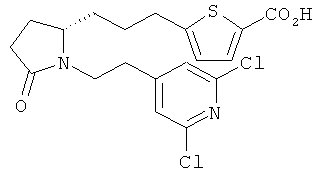
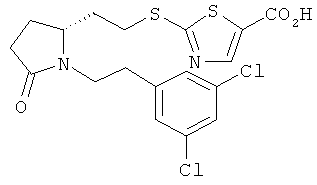
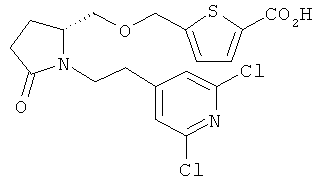
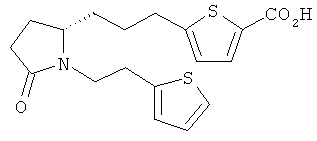
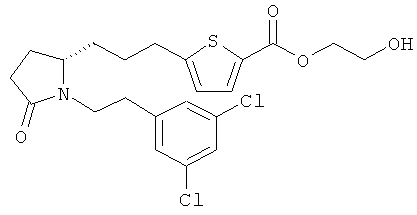
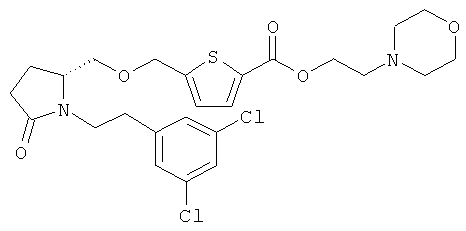
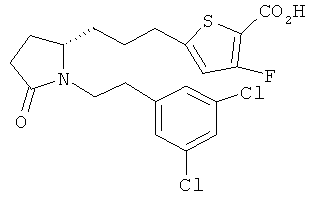
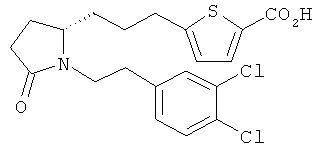
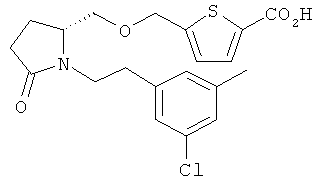
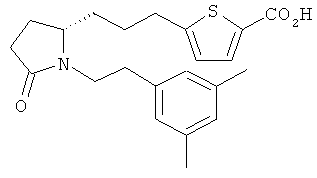
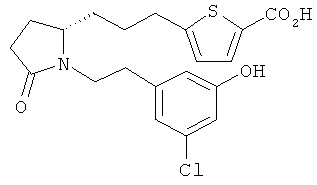
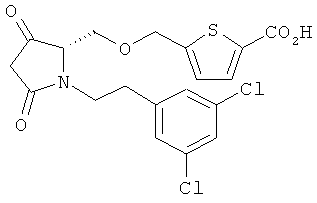
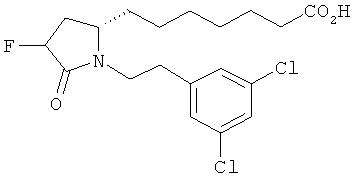
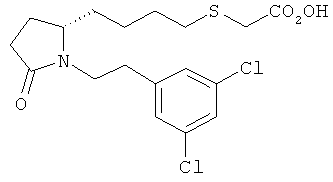
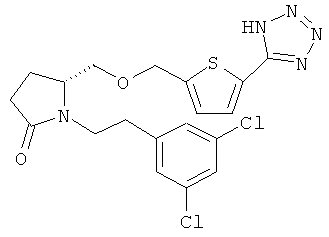
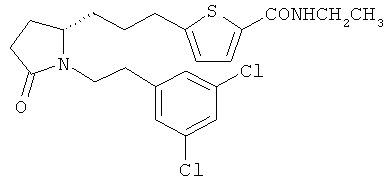
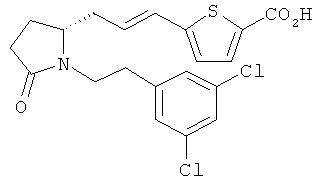
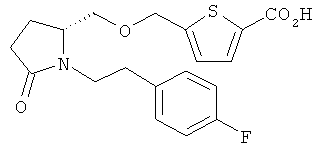
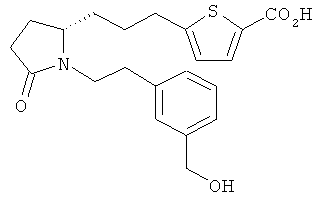
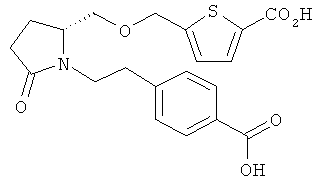
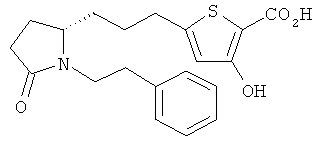
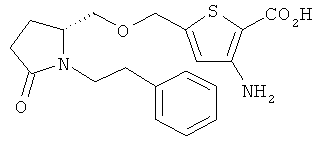
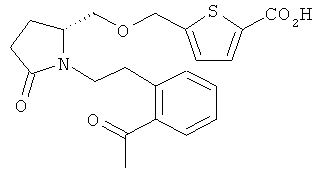
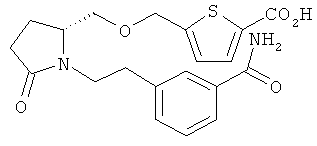
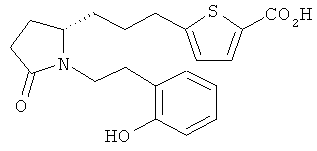
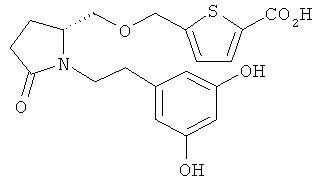
Способы получения
Соединения, описанные в настоящем изобретении, можно получить способами, известными из уровня техники. Например, схемы А-В иллюстрируют примерный общий способ, который можно применить.
Схема А
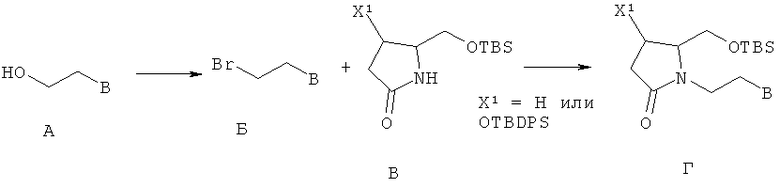
ω-Цепь (-СН2СН2-В) можно присоединить к ядру пирролидин-2-она, используя способ, подобный показанному на схеме А. Присоединение Б и В с получением соединения Г можно выполнять несколькими способами, известными из уровня техники. Например, взаимодействие можно катализировать, используя основание, такое как гидрид натрия. Для соединения Б можно использовать другие уходящие группы, отличные от -Br.
Схема Б
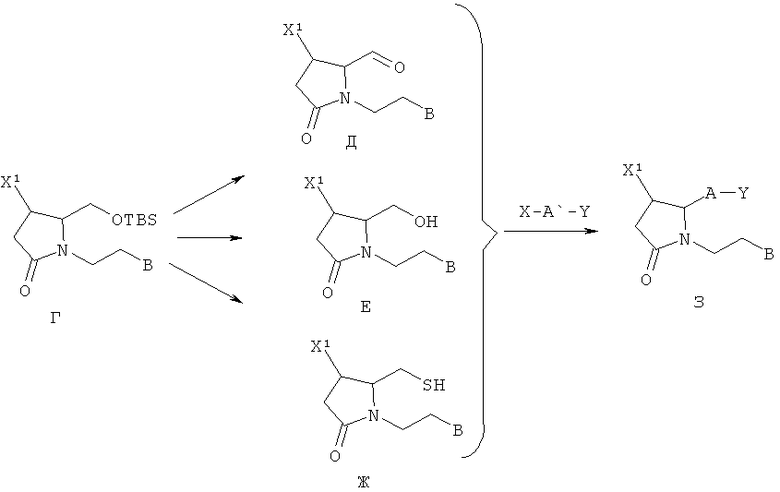
Защищенный спирт соединения Г позволяет получать широкий диапазон α-цепей. Например, его можно окислить до альдегида (Д) и связать с X-A`-Y путем сочетания Виттига, где Х представляет собой фрагмент фосфония. Также его можно подвергнуть гидрогенизации с получением насыщенной связи С-С, либо оставить ненасыщенную связь. Можно также снять защиту с соединения Г, получив соединение (Е), либо перевести в SH (Ж) и связать с X-A`-Y путем нуклеофильного замещения, где Х представляет собой уходящую группу.
Схема В
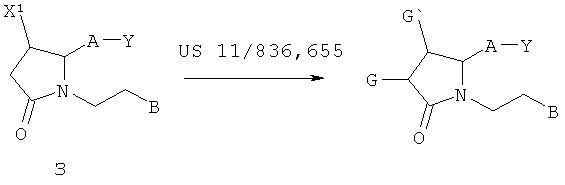
Заместители в ядро пирролидин-2-она можно ввести, применяя способы, описанные в Патентной заявке США №11/836655, поданной 9 Августа 2007 года на соединение 3.
Схема 1
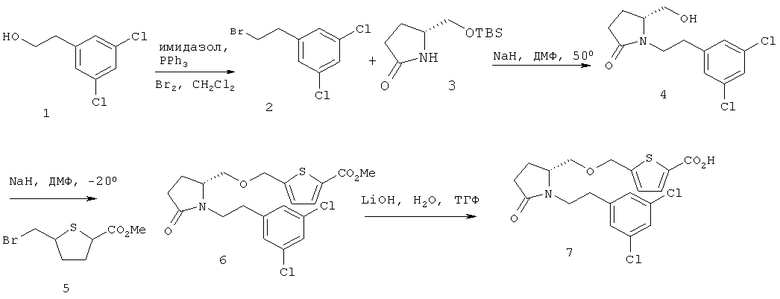
Пример 1
(R)-5-(((1-(3,5-дихлорфенэтил)-5-оксопирролидин-2-ил)метокси)тиофен-2-карбоновая кислота (7)
Стадия 1. Получение бромида 2
Бром (0,80 мл, 15,5 ммоль) добавляли к раствору трифенилфосфина (4,12 г, 15,7 ммоль) и имидазола (1,07 г, 15,7 ммоль) в CH2Cl2 (52 мл) при 0°С, далее смесь оставляли нагреваться при комнатной температуре. Через канюлю добавляли раствор 2-(3,5-дихлорфенил)этанола (1, 2,5 г, 13,1 ммоль) в CH2Cl2 (13 мл). Через 30 мин при комнатной температуре смесь фильтровали через целит, промывали избытком CH2Cl2. Фильтрат концентрировали в вакууме. Неочищенный остаток очищали хроматографией на 120 г силикагеля (гексан → 20% EtOAc (этилацетат)/гексан, градиент) с получением 3,13 г (94%) бромида 2.
Стадия 2. Алкилирование 3 соединением 2 с получением 4
Гидрид натрия (80 мг 60% дисперсии в масле, 2,0 ммоль) добавляли к раствору 3 (115 мг, 0,50 ммоль) в ДМФ (4 мл). По истечении 45 мин при комнатной температуре через канюлю добавляли раствор бромида 2 (255 мг, 1,0 ммоль) в ДМФ (1 мл). Смесь нагревали при 50°С в течение 18 часов, далее охлаждали до комнатной температуры и охлаждали насыщенным водным раствором NH4Cl (20 мл). Смесь экстрагировали EtOAc (125 мл). Органическую фазу промывали водой (2×50 мл) и рассолом (50 мл), затем сушили (Na2SO4), фильтровали и концентрировали в вакууме. Неочищенный остаток очищали хроматографией на 12 г силикагеля (гексан → EtOAc/гексан, градиент) с получением 39 мг (27%) спирта 4.
Стадия 3. Алкилирование 4 соединением 5 с получением 6
Гидрид натрия (21 мг 60% дисперсии в масле, 0,53 ммоль) добавляли к раствору 4 (100 мг, 0,35 ммоль) в ДМФ (0,43 мл) при 0°С, и смесь оставляли нагреваться при комнатной температуре. По истечении 30 мин при комнатной температуре смесь охлаждали до
-40°С, и через канюлю прибавляли раствор бромида 5 (см. предварительную патентную заявку США 60/804680, поданную 14 июня 2006 года, 70 мг, 0,30 ммоль) в ДМФ (0,43 мл). По истечении 10 мин при -40°С реакционную смесь разделяли на водную (10 мл) и CH2Cl2 (20 мл). Фазы разделяли, и водную фазу дополнительно экстрагировали CH2Cl2 (2×10 мл). Объединенную органическую фазу сушили (MgSO4), фильтровали и концентрировали в вакууме. Неочищенный остаток очищали хроматографией на силикагеле (гексан → EtOAc, градиент) с получением 84 мг (64%) соединения 6.
Стадия 4. Омыление 6 с получением соединения 7
Водный раствор гидроксида лития 1,0 Н (0,36 мл, 0,36 ммоль) добавляли к раствору эфира 6 (40 мг, 0,090 ммоль) в ТГФ (0,9 мл). Раствор нагревали до 40°С в течение 18 часов, далее охлаждали до комнатной температуры. Смесь охлаждали 10% водным раствором HCl (10 мл) и экстрагировали EtOAc (2×20 мл). Объединенную органическую фазу промывали рассолом (10 мл), сушили (MgSO4), фильтровали и концентрировали в вакууме. Неочищенный остаток очищали хроматографией на 4 г силикагеля (CH2Cl2 → 10% МеОН/CH2Cl2, градиент) с получением 11 мг (28%) соединения, указанного в заголовке.
Схема 2
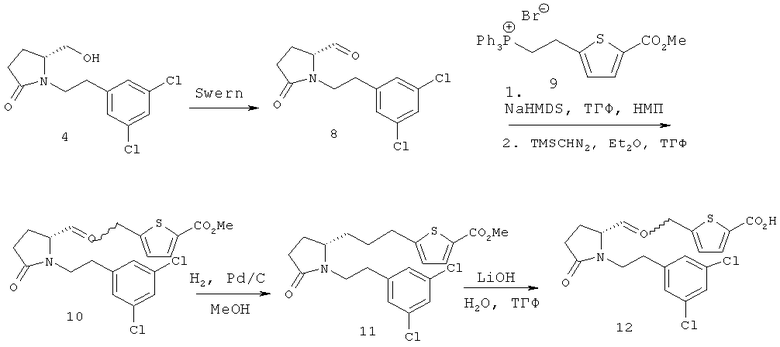
Пример 2
(S)-5-(3-(1-(3,5-дихлорфенэтил)-5-оксопирролидин-2-ил)пропил)тиофен-2-карбоновая кислота (12)
Стадия 1. Окисление 4 с получением 8
ДМСО (65 мкл, 0,92 ммоль) добавляли к раствору оксалилхлорида (220 мкл 2,0 М раствора в CH2Cl2, 0,44 ммоль) и CH2Cl2 (3,1 мл) при -78°С. По истечении 15 мин через канюлю добавляли раствор спирта 4 (100 мг, 0,35 ммоль) в CH2Cl2 (1,0 мл). По истечении 15 минут добавляли триэтиламин (412 мкл, 2,96 ммоль), и реакционную смесь оставляли нагреваться при комнатной температуре. Через 1 час при комнатной температуре смесь разделяли на CH2Cl2 (25 мл) и насыщенный водный раствор NaHCO3 (25 мл). Фазы разделяли, и водную фазу экстрагировали CH2Cl2 (2×30 мл). Объединенную органическую фазу сушили (Na2SO4), фильтровали и концентрировали в вакууме с получением 100 мг (количественно) неочищенного альдегида 8, который далее использовали без дополнительной очистки.
Стадия 2. Реакция Виттига соединения 8 с 9 и последующая эстерификация с получением 10.
Раствор бис(триметилсилил)амида натрия (0,7 мл 1,0 М раствора в ТГФ, 0,70 ммоль) добавляли к раствору соли фосфония 9 (см. предварительную патентную заявку США №60/894267, 173 мг, 0,35 ммоль) в 1-метил-2-пирролидиноне (НМП, 0,5 мл) при 0°С. После интенсивного перемешивания в течение 30 мин при 0°С смесь охлаждали до -20°С и с помощью спринцовки добавляли раствор альдегида 8 (50 мг, 0,17 ммоль) в ТГФ (0,4 мл). По истечении 30 мин при -20°С смесь оставляли нагреваться до 0°С. По истечении 1 ч при 0°С реакционную смесь охлаждали насыщенным водным раствором NH4Cl (10 мл) и разбавляли CH2Cl2 (25 мл). Полученную эмульсию фильтровали через цеолит, промывали CH2Cl2. Фазы разделяли, и водную фазу экстрагировали CH2Cl2 (3×75 мл). Объединенную органическую фазу сушили (Na2SO4), фильтровали и концентрировали в вакууме. Неочищенный остаток растворяли в ТГФ (0,87 мл), и к раствору добавляли по каплям раствор (триметилсилил)диазометана (0,43 мл 2,0 М раствора в Et2O, 0,86 ммоль). По истечении 30 мин при комнатной температуре реакционную смесь концентрировали в вакууме.
Очищение неочищенного остатка хроматографическим способом на 12 г силикагеля (CH2Cl2 → 15% МеОН/CH2Cl2, градиент) приводило к недостаточному разделению продукта и примесей. Фракции, содержащие желаемый продукт, концентрировали в вакууме и очищали хроматографией на 12 г силикагеля (50% EtOAc/гексан → EtOAc, градиент) с получением 14 мг (18%) эфира соединения 10 в виде смеси олефиновых изомеров.
Стадия 3. Гидрирование 10 с получением 11.
Палладий на углероде (10 масс.%, 6,8 мг) добавляли к раствору алкена 10 (14 мг, 0,032 ммоль) в МеОН (0,7 мл). После вакуумирования и заполнения водородом (5×), смесь перемешивали в атмосфере водорода. По истечении 18 ч реакционную смесь фильтровали через целит, промывали избытком МеОН. Фильтрат концентрировали в вакууме. Очищение неочищенного остатка на 4 г силикагеля (35% EtOAc/гексан → 80% EtOAc/гексан, градиент) приводило к получению 3 мг (21%) соединения 11.
Стадия 4. Омыление 11 с получением соединения 12
Водный раствор гидроксида лития 1,0 Н (0,05 мл, 0, 05 ммоль) добавляли к раствору эфира 11 (2 мг, 0,0045 ммоль) в ТГФ (0,1 мл). После 18 часов при 30°С смесь охлаждали, и летучие компоненты удаляли потоком азота. Остаток разбавляли водой (0,2 мл) и подкисляли 1 Н водным раствором HCl (0,5 мл). Смесь экстрагировали EtOAc (3×2 мл). Объединенные экстракты промывали рассолом (1 мл), сушили (Na2SO4), фильтровали и концентрировали в вакууме. Неочищенный остаток очищали хроматографией на 4 г силикагеля (CH2Cl2 → 20% MeOH/CH2Cl2, градиент) с получением 1,3 мг (67%) соединения, указанного в заголовке.
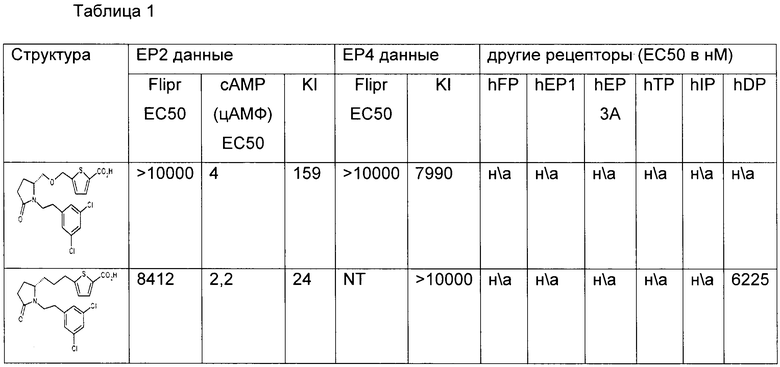
Испытания in vitro
В патентной заявке США №11/553,143, поданной 26 октября 2006 года, которая включена здесь путем ссылки, описаны способы получения данных in vitro, представленных в таблице, приведенной ниже.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ ГАММА-ЛАКТАМЫ В КАЧЕСТВЕ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ | 2006 |
|
RU2412933C2 |
| ТЕРАПЕВТИЧЕСКИЕ СОЕДИНЕНИЯ | 2009 |
|
RU2500674C2 |
| Агонисты V1а-рецепторов | 2013 |
|
RU2634617C2 |
| АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ КАК ПРОТИВОВОСПАЛИТЕЛЬНЫЕ, ИММУНОМОДУЛИРУЮЩИЕ И АНТИПРОЛИФЕРАТИВНЫЕ СРЕДСТВА | 2003 |
|
RU2386625C2 |
| ИНГИБИТОРЫ ГИРАЗЫ БАКТЕРИЙ И ИХ ПРИМЕНЕНИЯ | 2001 |
|
RU2262932C2 |
| ТРИЦИКЛИЧЕСКИЕ АНТАГОНИСТЫ ТРОМБИНОВОГО РЕЦЕПТОРА | 2003 |
|
RU2329264C9 |
| Промежуточные соединения и способы синтеза производных калихеамицина | 2014 |
|
RU2640197C1 |
| АДРЕНЕРГИЧЕСКИЕ СОЕДИНЕНИЯ | 2008 |
|
RU2491284C2 |
| СОЧЕТАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ ПЕНТАФТОРБЕНЗОЛСУЛЬФОНАМИДОВ | 2000 |
|
RU2268054C2 |
| АМИНО-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 3-ГЕТЕРОАРОИЛАМИНОПРОПИОНОВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2012 |
|
RU2605600C2 |
Изобретение относится к соединению формулы:

где Y представляет собой -СО2Н; А представляет собой -(СН2)m-Ar-(СН2)o-, где Ar представляет собой тиофенил, сумма m и о равна 3, и где 1 группа -СН2- может быть замещена О; G и G' представляют собой -Н; и В представляет собой фенил, содержащий от 1 до 2 заместителей, независимо выбранных из -F, -О и -Br. Изобретение также относится к композиции на основе указанных соединений. Технический результат - получены новые соединения и композиция на их основе, которые могут найти применение в медицине для лечения глаукомы или глазной гипертензии. 4 н. и 6 з.п. ф-лы, 1 табл., 2 пр.
1. Соединение формулы:
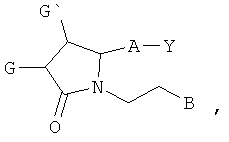
где Y представляет собой -СО2Н;
А представляет собой -(СН2)m-Ar-(СН2)о-, где Ar представляет собой тиофенил, сумма m и о равна 3, и где 1 группа -СН2- может быть замещена О;
G и G' представляют собой -Н; и
В представляет собой фенил, содержащий от 1 до 2 заместителей, независимо выбранных из -F, -Cl и -Br.
2. Соединение по п.1 формулы:
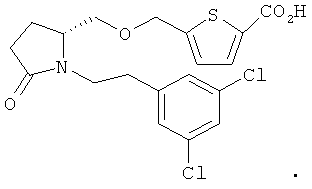
3. Соединение по п.1 формулы:
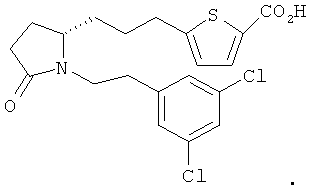
4. Соединение по п.1 формулы
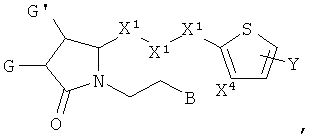
где каждый X1 представляет собой -СН2- или 1 группа -СН2- может быть замещена О; и где X4 представляет собой -СН-.
5. Соединение по п.4 формулы:
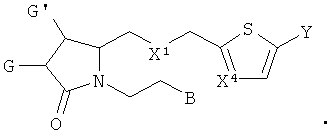
6. Соединение по п.4 формулы
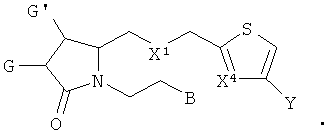
7. Соединение по п.1, где В представляет собой дихлорфенил.
8. Применение соединения по п.1 в производстве лекарственных препаратов для лечения глаукомы или глазной гипертензии у млекопитающего.
9. Способ лечения глаукомы или глазной гипертензии, включающий введение соединения по п.1 млекопитающему в случае необходимости такого лечения.
10. Жидкая композиция для лечения глаукомы или глазной гипертензии у млекопитающего, содержащая соединение по п.1 и фармацевтически приемлемый эксципиент.
| WO 2005108360 А1, 17.11.2005 | |||
| АНАЛОГИ ПРОСТАГЛАНДИНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СЕЛЕКТИВНОЙ АГОНИСТИЧЕСКОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ РЕЦЕПТОРА EP | 2002 |
|
RU2288913C2 |
| ПРОИЗВОДНОЕ 8-АЗАПРОСТАГЛАНДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, АГЕНТ ДЛЯ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ | 2003 |
|
RU2306309C2 |
Авторы
Даты
2013-05-10—Публикация
2008-10-16—Подача