Область техники, к которой относится изобретение
Настоящее изобретение относится к HLA-A*1101-ограниченному пептиду WT1, в частности пептиду, содержащему аминокислотную последовательность, состоящую из 9 последовательных аминокислот из белка WT1, где пептид обладает способностью связываться с молекулой HLA-A*1101, а также индуцировать CTL. Настоящее изобретение также относится к пептидному димеру, обладающему способностью связываться с молекулой HLA-A*1101 и индуцировать CTL, в котором два пептидных мономера, каждый содержащий аминокислотную последовательность, состоящую из 9 последовательных аминокислот белка WT1, и содержащий по крайней мере один остаток цистеина, связаны между собой дисульфидной связью. Кроме того, настоящее изобретение относится к полинуклеотиду, кодирующему этот пептид, к фармацевтической композиции для лечения и/или профилактики рака, содержащей этот пептид, и тому подобное.
Уровень техники
Ген WT1 (ген опухоли Вильямса 1) был идентифицирован как ген, ответственный за опухоль Вильямса, которая представляет собой рак почек у детей (непатентные документы 1 и 2). WT1 является транскрипционным фактором, со структурой «цинкового пальца». Первоначально ген WT1 считался геном-супрессором рака. Однако последующие исследования (непатентные документы 3, 4, 5 и 6) показали, что ген WT1 скорее функционирует как онкоген в гематопоэтических опухолях и солидных раках.
Ген WT1 экспрессируется на высоком уровне во многих типах злокачественных опухолей. Кроме того, было изучено, свободен ли от мутаций продукт гена WT1, который является аутогенным белком, обладает иммуногенностью в живом организме. Результаты показали, что этот белок является продуктом гена WT1, который экспрессируется на высоком уровне в клетках опухоли, фрагментируется в результате внутриклеточного процессинга, конечные пептиды образуют комплексы с молекулами MHC класса I, и эти комплексы находятся на поверхностях клеток, и что CTL, распознающие такие комплексы, могут быть индуцированы с помощью пептидной вакцинации (непатентные документы 7, 8 и 9). Было также показано, что у мыши, иммунизированной пептидом WT1 или кДНК WT1, трансплантированные клетки опухоли, экспрессирующие ген WT1, с высокой вероятностью отторгаются (непатентные документы 7 и 10), в то время как нормальные ткани, физиологически экспрессирующие ген WT1, не повреждаются индуцированными CTL (непатентный документ 7). Было показано в экспериментах in vitro с использованием клеток человека, что, если пептид Db126 или пептид WH187 (аминокислоты 187-195 из SEQ ID NO:1, SLGEQQYSV), обладающий высокой способностью связываться с молекулой HLA-A*0201, которая является одной из молекул MHC класса I человека, используются для стимуляции мононуклеарных клеток периферической крови человека, имеющих HLA-A*0201, индуцируются WT1-специфичные CTL, эти индуцированные CTL имеют цитоксическую активность, специфичную для клеток опухоли, экспрессирующих эндогенно ген WT1 на высоком уровне, а цитоксическая активность таких CTL является HLA-A2-ограниченной (непатентный документ 11). Было показано в экспериментах in vitro на клетках человека с использованием пептида WT1, который соответствует HLA-A*2402 (было обнаружено, что среди HLA-A аллелей он наиболее часто встречается у японцев) (WT1235; аминокислоты 235-243 из SEQ ID NO:1, CMTWNQMNL), что индуцируются WT1-специфические CTL (TAK-1) (непатентный документ 12), и индуцированные CTL не супрессируют способность к образованию колоний нормальных гематопоэтических стволовых, которые частично физиологически экспрессируют ген WT1 (непатентные документы 12 и 13). Эти данные убедительно указывают на то, что не только у мышей, но и у человека, могут быть индуцированы WT1-специфичные CTL; такие CTL обладают цитоксической активностью против опухолевых клеток, экспрессирующих ген WT1 на высоком уровне, но не имеют цитоксической активности против нормальных клеток, экспрессирующих физиологически ген WT1 (непатентные документы 7, 10, 11, 12 и 13).
Продуктом гена WT1 является ядерный белок, который расщепляется протеасомами в цитоплазме на пептиды. Фрагментированные пептиды транспортируются в просвет эндоплазматического ретикулума с помощью молекул TAP (транспортер, связанный с процессингом антигена), образуют комплексы с молекулами MHC класса I и располагаются на поверхности клеток. WT1-специфичные CTL индуцируются в результате распознавания комплексов WT1 пептид - молекула MHC класса I клетками-предшественниками CTL посредством TCR, оказывая таким образом цитоксический эффект на клетки опухоли, презентирующие продукт гена WT1 с помощью молекул MHC класса I (непатентные документы 7, 8 и 9). Кроме того, требуется по крайней мере чтобы пептид WT1, используемый в иммунотерапии рака, направленной на продукт гена WT1, находился в форме, которая связывается с молекулой MHC класса I в живом организме. Однако молекулы MHC класса I различные, и аминокислотные последовательности пептидов WT1, связанных с соответствующими молекулами MHC класса I, отличаются друг от друга. Поэтому, требуется получить пептид, соответствующий каждому подтипу MHC класса I. Однако к настоящему времени известны только HLA-A*2402, HLA-A*0201-, HLA-A*2601- и HLA-A*3303-ограниченные пептиды как HLA-ограниченные пептиды WT1. (Патентный документ 1, непатентный документ 11, патентный документ 2 и патентный документ 3, соответственно). Таким образом, существует необходимость найти HLA-A*1101-ограниченный пептид WT1.
Патентный документ 1: WO 2003/106682.
Патентный документ 2: WO 2005/095598.
Патентный документ 3: Японская Патентная Заявка №2006-45287.
Непатентный документ 1: Daniel A. Haber et al., Cell. 1990 Jun 29; 61(7):1257-69.
Непатентный документ 2: Call KM et al., Cell. 1990 Feb 9; 60(3):509-20.
Непатентный документ 3: Menke AL et al., Int Rev Cytol. 1998; 181:151-212. Review.
Непатентный документ 4: Yamagami T et al., Blood. 1996 Apr 1; 87(7):2878-84.
Непатентный документ 5: Inoue K et al., Blood. 1998 Apr 15; 91(8):2969-76.
Непатентный документ 6: Tsuboi A et al., Leuk Res. 1999 May; 23(5):499-505.
Непатентный документ 7: Oka Y et al., J Immunol. 2000 Feb 15; 164(4):1873-80.
Непатентный документ 8: Melief CJ et al., Immunol Rev. 1995 Jun; 145:167-77.
Непатентный документ 9: Ritz J, J Clin Oncol. 1994 Feb; 12(2):237-8.
Непатентный документ 10: Tsuboi A et al., J Clin Immunol. 2000 May; 20(3):195-202.
Непатентный документ 11: Oka Y et al., Immunogenetics. 2000 Feb; 51(2):99-107.
Непатентный документ 12: Ohminami H et al., Blood. 2000 Jan 1; 95(1):286-93.
Непатентный документ 13: Gao L et al., Blood. 2000 Apr 1; 95(7):2198-203.
Сущность изобретения
Задачи, решаемые изобретением
Задачи, решаемые настоящим изобретением, состоят в получении пептида, который является HLA-A*1101 - ограниченным и содержит аминокислотную последовательность из белка WT1, и полинуклеотида, его кодирующего, а также фармацевтической композиции для лечения и профилактики рака, их содержащей, и тому подобное.
Способы решения задач
В результате интенсивных исследований с учетом ситуации, описанной выше, автор изобретения обнаружил, что среди пептидов, каждый из которых содержит аминокислотную последовательность, включающую 9 последовательных аминокислот белка WT1, пептиды, каждый обладающий способностью связываться с молекулой HLA-A*1101, могут интенсивно индуцировать WT1-специфичную CTL. Таким образом, было выполнено настоящее изобретение.
Настоящее изобретение представляет:
(1) пептид, содержащий аминокислотную последовательность, состоящую из 9 последовательных аминокислот белка WT1, где пептид обладает способностью связываться с молекулой HLA-A*1101 и индуцировать CTL;
(2) пептид согласно (1), где аминокислота в положении 9 аминокислотной последовательности представляет собой Lys или Arg;
(3) пептид согласно (1), где аминокислотная последовательность выбрана из группы, состоящей из:
Ala Ala Gly Ser Ser Ser Ser Val Lys (SEQ ID NO:2),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3),
Arg Ser Ala Ser Glu Thr Ser Glu Lys (SEQ ID NO:4),
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5),
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Lys Thr Cys Gln Arg Lys Phe Ser Arg (SEQ ID NO:8),
Ser Cys Arg Trp Pro Ser Cys Gln Lys (SEQ ID NO:9),
Asn Met His Gln Arg Asn Met Thr Lys (SEQ ID NO:10);
(4) пептид согласно (3), где аминокислотная последовательность представляет собой Ala Ala Gly Ser Ser Ser Ser Val Lys (SEQ ID NO:2);
(5) пептидный димер, обладающий способностью связываться с молекулой HLA-A*1101 и индуцировать CTL, в котором два пептидных мономера, каждый содержащий аминокислотную последовательность, состоящую из 9 последовательных аминокислот из белка WT1 и включающую по крайней мере один остаток цистеина, связаны друг с другом посредством дисульфидной связи;
(6) пептидный димер согласно (5), где аминокислотная последовательность пептидного мономера выбрана из группы, состоящей из:
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Lys Thr Cys Gln Arg Lys Phe Ser Arg (SEQ ID NO:8),
Ser Cys Arg Trp Pro Ser Cys Gln Lys (SEQ ID NO:9);
(7) фармацевтическая композиция для лечения и профилактики рака, содержащая пептид согласно (1) и/или пептидный димер согласно (5);
(8) способ лечения или профилактики рака, включающий введение эффективного количества пептида согласно (1) и/или пептидного димера согласно (5) HLA-A*1101-позитивному индивиду;
(9) полинуклеотид, кодирующий пептид согласно (1);
(10) вектор экспрессии, содержащий полинуклеотид согласно (9);
(11) фармацевтическая композиция для лечения и профилактики рака, содержащая полинуклеотид согласно (9) или вектор согласно (10);
(12) способ лечения или профилактики рака, включающий введение эффективного количества полинуклеотида согласно (9) или вектора согласно (10) HLA-A*1101-позитивному индивиду;
(13) WT1-специфичный CTL, который индуцирован с помощью пептида согласно (1) и/или пептидного димера согласно (5);
(14) способ индукции WT1-специфичного CTL, включающий культивирование мононуклеарной клетки периферической крови в присутствии пептида согласно (1) и/или пептидного димера согласно (5) для индуцирования WT1-специфичного CTL из мононуклеарной клетки периферической крови;
(15) набор для индукции WT1-специфичного CTL, содержащий пептид согласно (1) и/или пептидный димер согласно (5) в качестве существенного компонента;
(16) антиген-презентирующая клетка, презентирующая пептид WT1, который индуцирован с помощью пептида согласно (1) и/или пептидного димера согласно (5);
(17) способ индукции антиген-презентирующей клетки, презентирующий пептид WT1, включающий культивирование незрелой антиген-презентирующей клетки в присутствии пептида согласно (1) и/или пептидного димера согласно (5) для индуцирования антиген-презентирующей клетки, презентирующей пептид WT1, из незрелой антиген-презентирующей клетки;
(18) набор для индуции антиген-презентирующей клетки, презентирующий пептид WT1, включающий пептид согласно (1) и/или пептидный димер согласно (5) как существенный компонент; и
(19) способ диагностики рака, включающий использование CTL согласно (13) или антиген-презентирующей клетки согласно (16).
Осуществление изобретения
Настоящее изобретение относится к пептиду, который является HLA-A*1101-ограниченным и содержит аминокислотную последовательность, состоящую из 9 последовательных аминокислот белка WT1, и кодирующий его полинуклеотид, а также фармацевтическую композицию для лечения и/или профилактики рака, содержащую пептид и тому подобное. Следовательно, возможно индуцировать in vivo и in vitro WT1-специфичные CTL у индивидов, имеющих HLA-A*1101. Поскольку доля позитивных HLA-A*1101 среди японцев высока (около 17,9%), то WT1-специфичные CTL можно индуцировать у большого числа индивидов.
Краткое описание чертежей
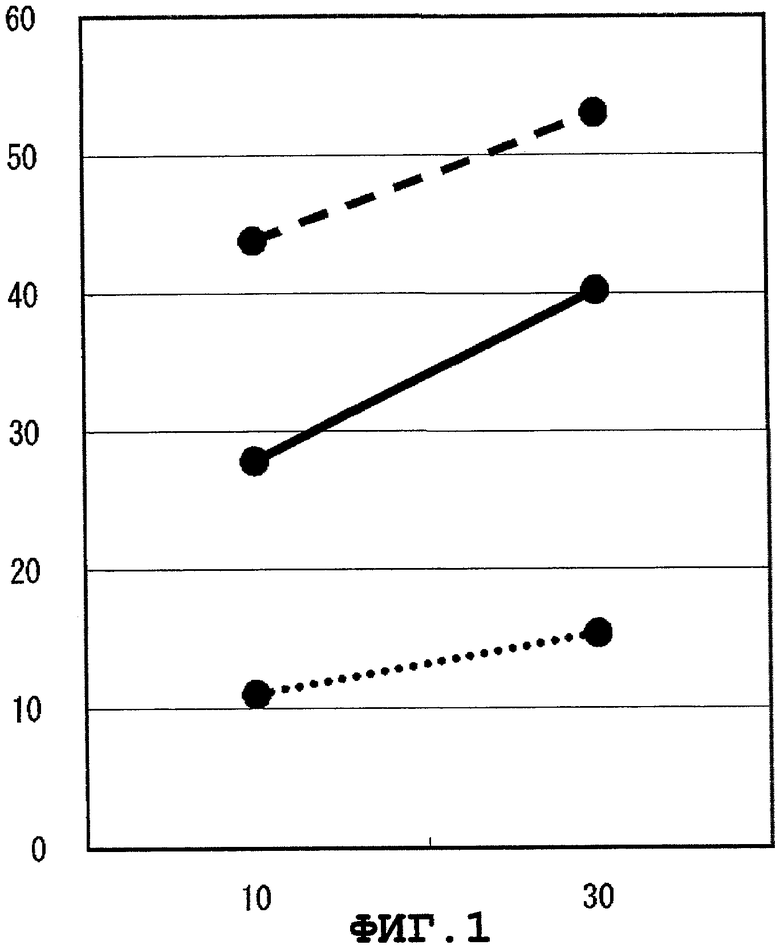
Фиг.1 представляет цитоксическую активность CTL, индуцированного WT1251.
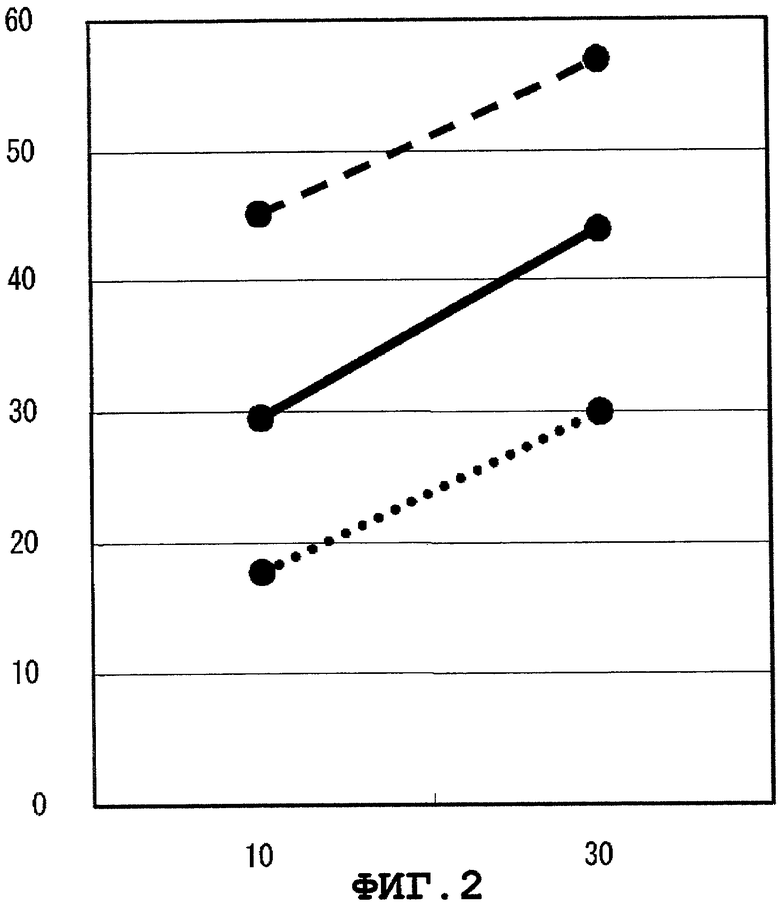
Фиг.2 представляет цитоксическую активность CTL, индуцированного WT1279.
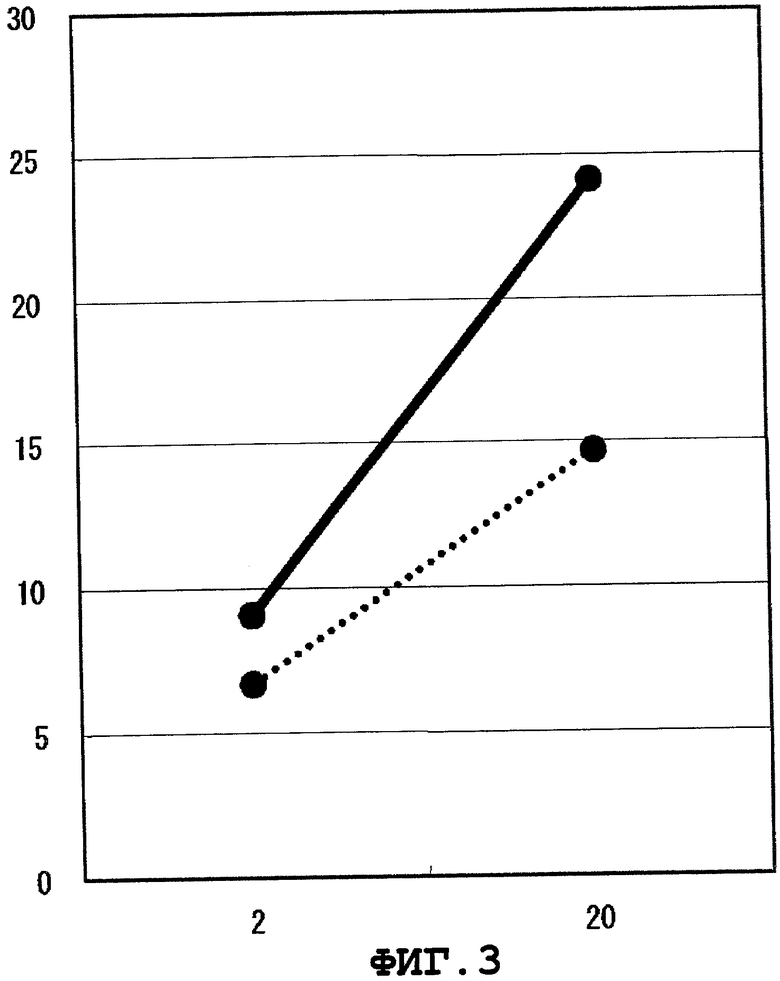
Фиг.3 представляет цитоксическую активность CTL, индуцированного WT1312.
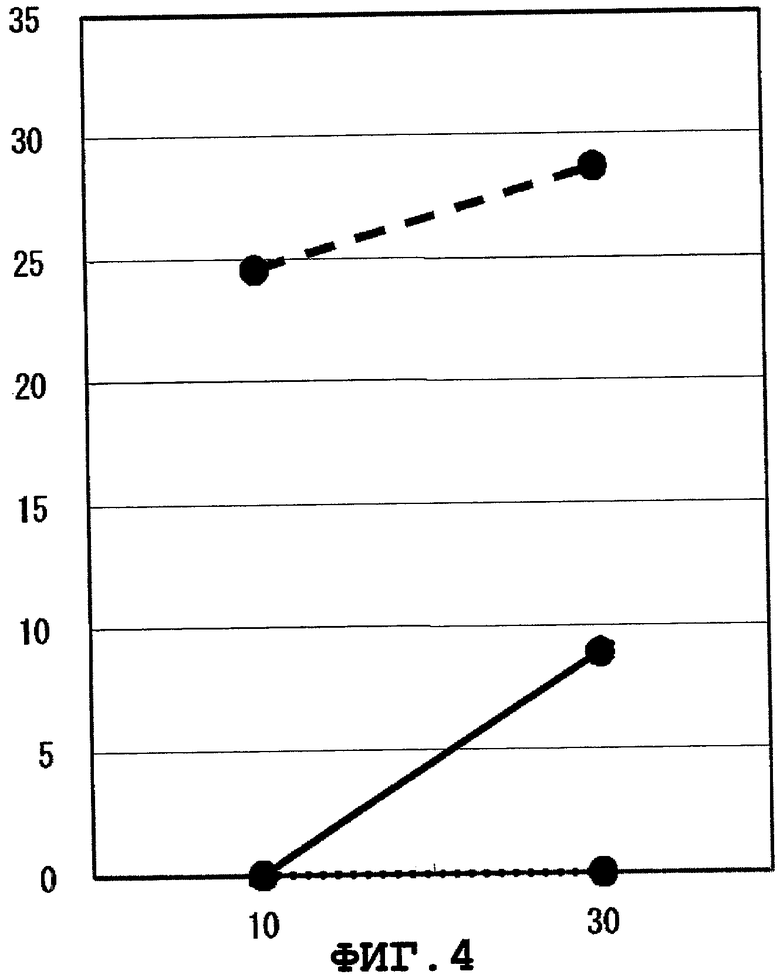
Фиг.4 представляет цитоксическую активность CTL, индуцированного WT1313.
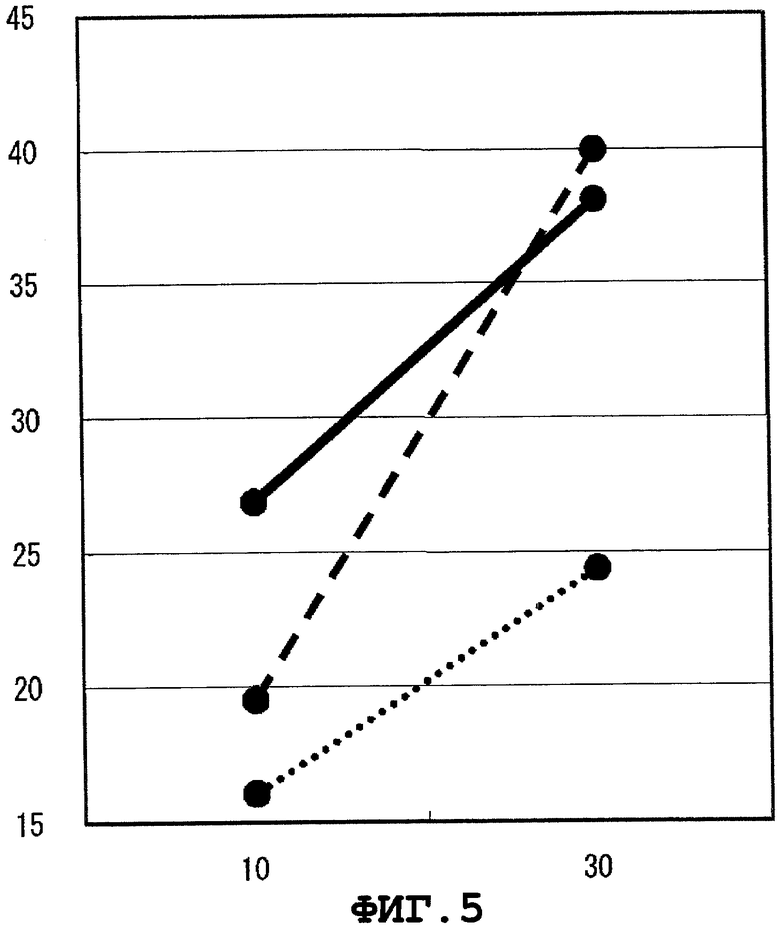
Фиг.5 представляет цитоксическую активность CTL, индуцированного WT1338.
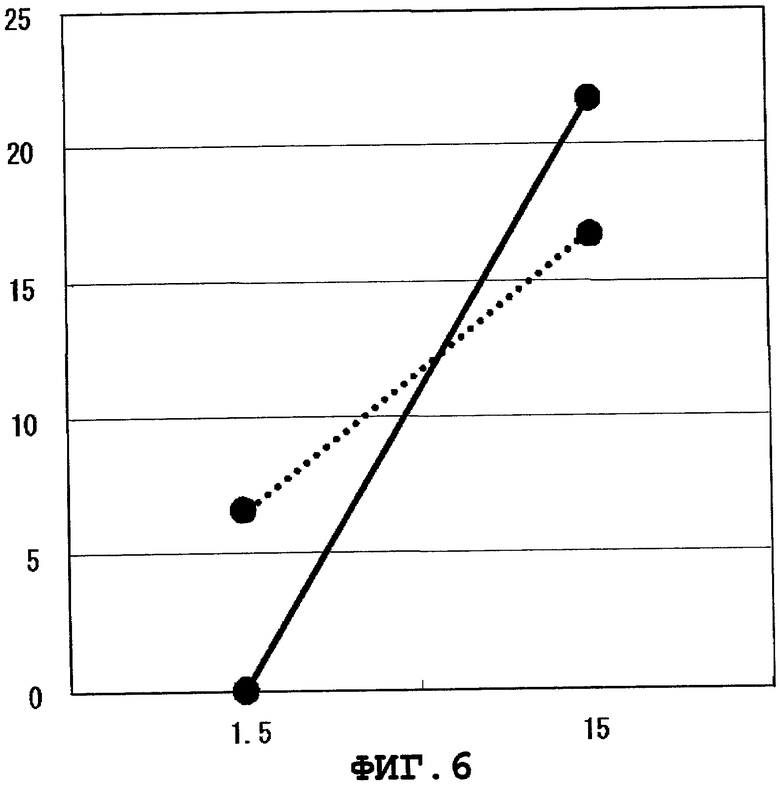
Фиг.6 представляет цитоксическую активность CTL, индуцированного WT1378.
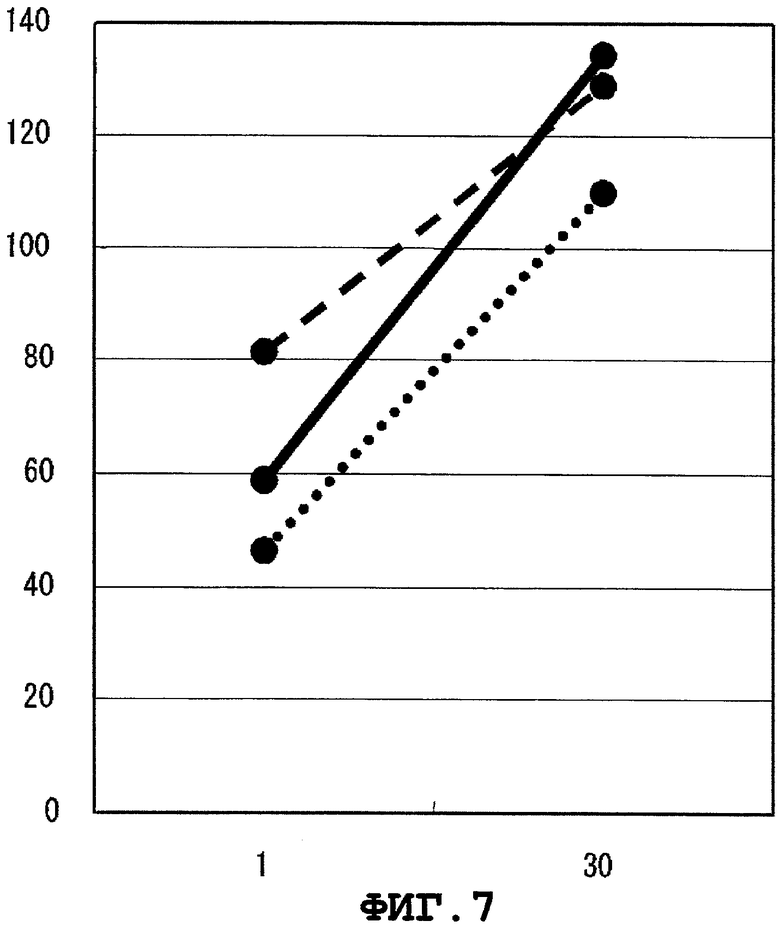
Фиг.7 представляет цитоксическую активность CTL, индуцированного WT1386.
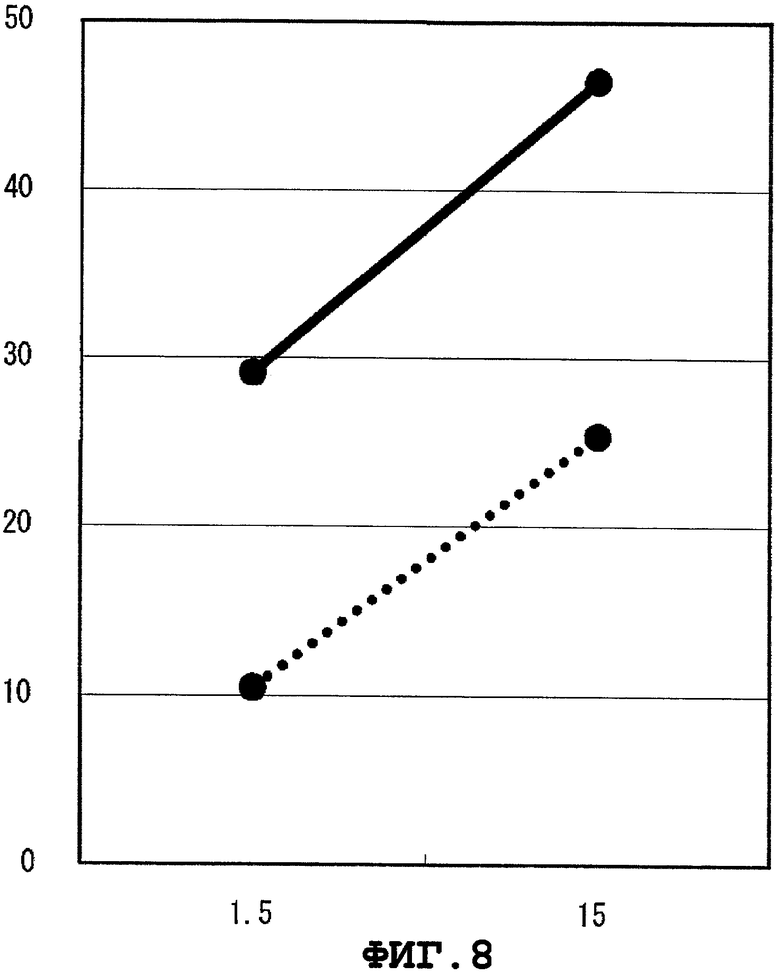
Фиг.8 представляет цитоксическую активность CTL, индуцированного WT1415.
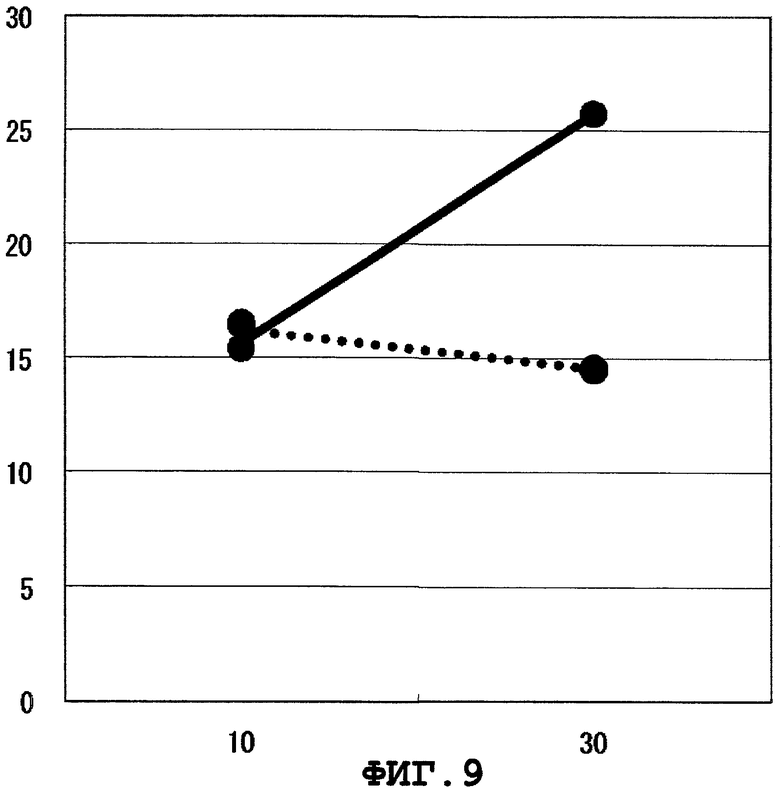
Фиг.9 представляет цитоксическую активность CTL, индуцированного WT1436.
Фиг.10 представляет цитоксическую активность CTL, индуцированного WT1378 пептидом (a, b и c представляют цитоксическую активность, наблюдаемую при использовании PBMCs от HLA-A*1101-позитивных здоровых доноров 1, 2 и 3, соответственно).
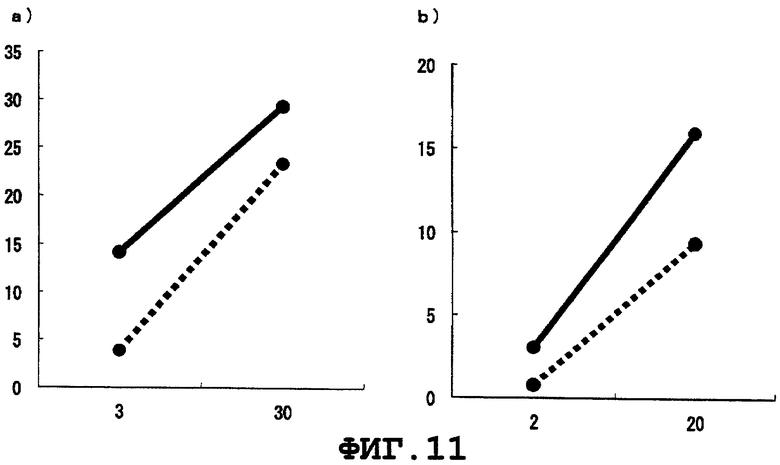
Фиг.11 представляет цитоксическую активность CTL, индуцированного WT1378 пептидным димером (a и b представляют цитоксическую активность, наблюдаемую при использовании PBMCs от HLA-A*1101-позитивных здоровых доноров 1 и 2, соответственно).
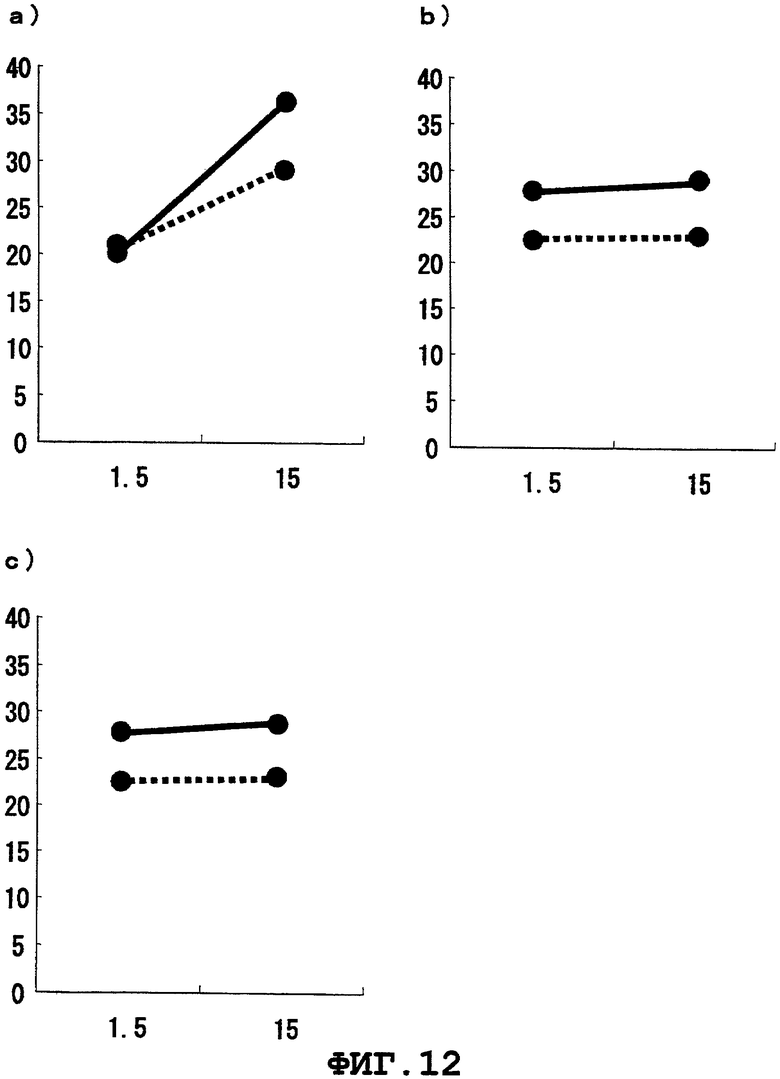
Фиг.12 представляет цитоксическую активность CTL, индуцированного модифицированным WT1378 пептидом (G → I) (a, b и c представляют цитоксическую активность, наблюдаемую при использовании PBMCs от HLA-A*1101-позитивных здоровых доноров 1, 2 и 3, соответственно).
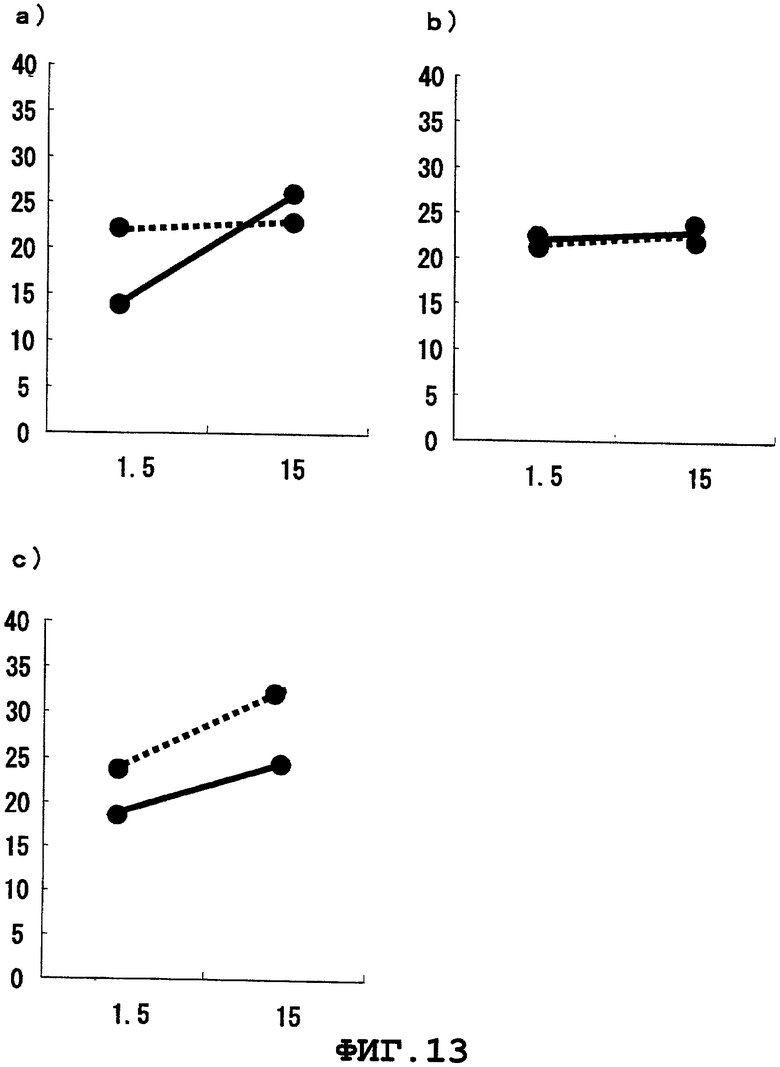
Фиг.13 представляет цитоксическую активность CTL, индуцированного модифицированным WT1378 пептидом (G → V) (a, b и c представляют цитоксическую активность, наблюдаемую при использовании PBMCs от HLA-A*1101-позитивных здоровых доноров 1, 2 и 3, соответственно).
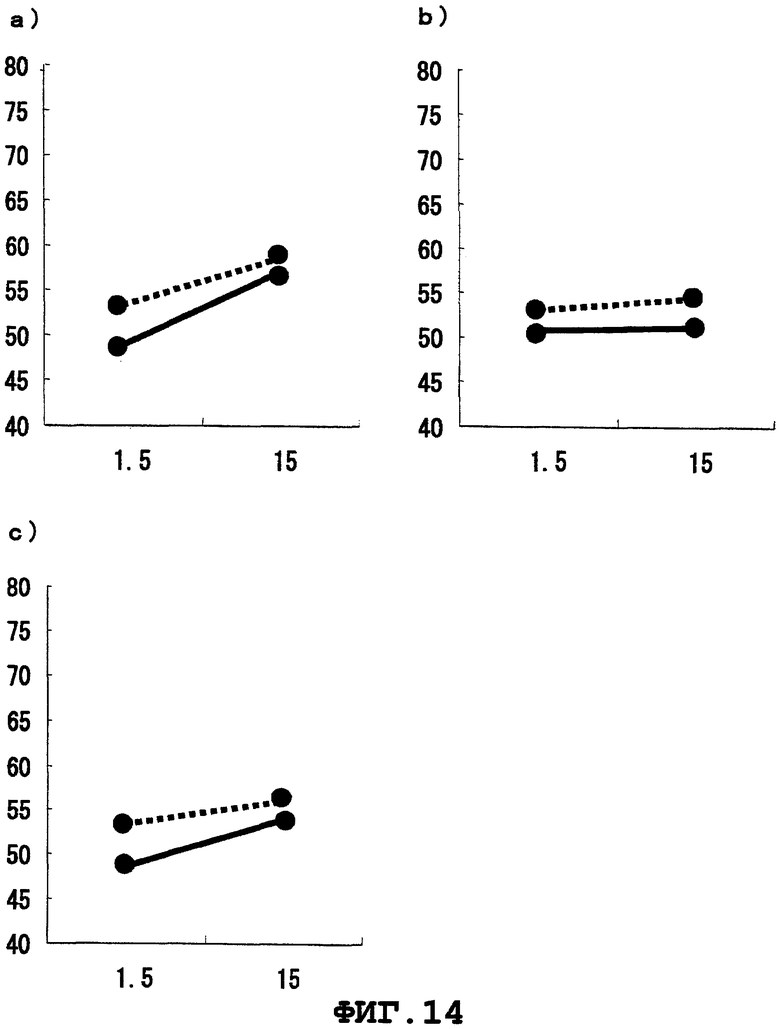
Фиг.14 представляет цитоксическую активность CTL, индуцированного WT1379 пептидом (a, b и c представляют цитоксическую активность, наблюдаемую при использовании PBMCs от HLA-A*1101-позитивных здоровых доноров 1, 2 и 3, соответственно).
Наилучший вариант осуществления изобретения
В одном из аспектов настоящее изобретение относится к пептиду, содержащему аминокислотную последовательность, состоящую из 9 последовательных аминокислот из белка WT1, где пептид обладает способностью связываться с молекулой HLA-A*1101 и индуцировать CTL (в описании также обозначен как "пептид WT1"). Аминокислотная последовательность белка WT1 человека представлена как SEQ ID NO:1. Пептид по настоящему изобретению содержит аминокислотную последовательность, состоящую из 9 последовательных аминокислот аминокислотной последовательности SEQ ID NO:1. Если пептид по настоящему изобретению содержит аминокислотную последовательность, включающую цистеин(ы), такую как аминокислотная последовательность SEQ ID NO:3, 7, 8 или 9, как описано ниже, то стабильность может быть увеличена путем замещения цистеина(нов) в аминокислотной последовательности другим веществом, такой как другая аминокислота (например, серин, аланин и α-аминобутировая кислота) или путем модифицирования SH-группы цистеина(нов) защитной группой, известной в данной области техники (например, карбоксиметильной группой или пиридилэтильной группой). Пептид по настоящему изобретению является пептидом ракового антигена, который может индуцировать CTL вследствие презентации (с помощью антиген-презентирующей клетки) пептида, формируемого в результате процессинга пептида по настоящему изобретению в клетке.
Как описано выше, объектом настоящего изобретение является получение HLA-A*1101-ограниченного пептида. Таким образом, пептид по настоящему изобретению обладает способностью связываться с молекулой HLA-A*1101. Способность к связыванию может определяться способом, известным в данной области. Примеры таких способов включают способ, основанный на использовании компьютера, такой как Rankpep, BIMAS или SYFPEITHI, и исследование конкурентного связывания с известным пептидом, обладающим способностью связываться с молекулой HLA-A*1101. Например, чтобы оценить обладает ли пептид по настоящему изобретению способностью к связыванию, установленная способность к связыванию может сравниваться с таковой у известного HLA-A*1101-ограниченного пептида. Примеры пептидов, обладающих способностью к связыванию в соответствии с настоящим изобретением, включают пептид, у которого показатель афинности к HLA-A*1101 молекуле, как определено способом, описанным в примере 1, составляет 4 или более, предпочтительнее 5 или более, более предпочтительнее, 6 или более.
Пептид по настоящему изобретению дополнительно обладает способностью индуцировать CTL. Ген WT1 экспрессируется в своей нативной форме на высоком уровне, например, в гематопоэтических опухолях, таких как лейкоз, миелодиспластический синдром, множественная миелома или злокачественная лимфома, и солидных раках, таких как рак желудка, рак толстой кишки, рак легкого, рак молочной железы, герминогенный рак, рак печени, рак кожи, рак мочевого пузыря, рак простаты, рак матки, рак шейки матки или рак яичников. Следовательно, пептид по настоящему изобретению может индуцировать CTL с высокой скоростью у индивида, страдающего таким заболеванием. Способность индуцировать CTL относится к способности индуцировать CTL in vivo или in vitro. Такую способность можно определить, используя общий способ, такой как способ, в котором цитоксическая активность CTL определяется с использованием теста с высвобождением хрома.
Пептид по настоящему изобретению может иметь Lys или Arg в положении 9 аминокислотной последовательности. Считается, что при наличии такой аминокислоты, способность пептида связываться с молекулой HLA-A*1101 становится выше.
Аминокислотная последовательность, состоящая из 9 аминокислот, включенных в пептид по настоящему изобретению, предпочтительно представляет собой Ala Ala Gly Ser Ser Ser Ser Val Lys (SEQ ID NO:2), Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3), Arg Ser Ala Ser Glu Thr Ser Glu Lys (SEQ ID NO:4), Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5), Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6), Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7), Lys Thr Cys Gln Arg Lys Phe Ser Arg (SEQ ID NO:8), Ser Cys Arg Trp Pro Ser Cys Gln Lys (SEQ ID NO:9) или Asn Met His Gln Arg Asn Met Thr Lys (SEQ ID NO:10). Наиболее предпочтительной последовательностью является последовательность Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7). Кроме того, последовательность может иметь замещение одной или нескольких, предпочтительно, от одной до пяти, аминокислот на другие аминокислоты в девяти аминокислотах любой из SEQ ID NO:2-10. Любая из этих девяти аминокислот или другие замещенные аминокислоты могут быть соответствующим образом модифицированы. В любом случае, пептид по настоящему изобретению сохраняет способность связываться с молекулой HLA-A*1101.
Как описано выше, пептидом по настоящему изобретению может быть любой пептид при условии, что он содержит аминокислотную последовательность, которая получена из белка WT1 и состоит из 9 последовательных аминокислот. Таким образом, пептидом по настоящему изобретению может быть, например, пептид, состоящий только из аминокислотной последовательности любой SEQ ID NO:2-10, или белок WT1 или его часть, включающая аминокислотную последовательность любой SEQ ID NO:2-10. Количество аминокислот, включенных в пептид по настоящему изобретению, конкретно не ограничено, и это количество составляет, например, 9-500, 9-300, 9-200, 9-100, 9-50, 9-30 и 9-12 аминокислот. Разные вещества можно присоединить к N-концу и/или к C-концу аминокислотной последовательности, состоящей из 9 последовательных аминокислот в пептиде по настоящему изобретению. Например, можно присоединить аминокислоту, пептид или его аналог. Если такое вещество присоединено к пептиду по настоящему изобретению, это вещество может подвергаться обработке, например, ферментом в живом организме или посредством процесса, такого как внутриклеточный процессинг, и, в конечном счете, аминокислотная последовательность, состоящая из 9 последовательных аминокислот, может продуцироваться и презентироваться как комплекс с молекулой HLA-A*1101 на поверхности клетки, тем самым приводя к эффекту индуцирования CTL. Таким веществом может быть вещество, которое модулирует растворимость пептида по настоящему изобретению или увеличивает его стабильность (устойчивость к протеазам, и т.д.). Альтернативно, это может быть вещество, которое специфически доставляет пептид по настоящему изобретению, например, к данной ткани или органу, или она может обладать способностью увеличивать эффективность поглощения с помощью антиген-презентирующей клетки или тому подобное. Таким может быть вещество, которое увеличивает способность индуцировать CTL, такое как пептид-помощник или тому подобное.
Пептид по настоящему изобретению может быть синтезирован способами, в основном используемыми в данной области или их вариантами. Такие способы описаны, например, в Peptide Synthesis, Interscience, New York, 1966; The Proteins, Vol 2, Academic Press Inc., New York, 1976; Peptide-Gosei, Maruzen Co., Ltd., 1975; Peptide-Gosei No Kiso To Jikken, Maruzen Co., Ltd., 1985; и Iyakuhin No Kaihatsu (Zoku), Vol. 14, Peptide-Gosei, Hirokawa - Book store, 1991.
Пептид по настоящему изобретению может быть также получен с помощью методов генной инженерии, основанных на информации о нуклеотидной последовательности, которая кодирует пептид по настоящему изобретению. Такие методы генной инженерии хорошо известны специалистам в данной области.
В дополнительном аспекте настоящее изобретение относится к пептидному димеру, обладающему способностью связываться с молекулой HLA-A*1101 и индуцировать CTL, в котором два пептидных мономера, каждый включающий аминокислотную последовательность, состоящую из 9 последовательных аминокислот из белка WT1, и включающий по крайней мере один остаток цистеина, связаны друг с другом посредством дисульфидной связи (в настоящем описании обозначен как "пептидный димер WT1"). Стабильность пептидного димера по настоящему изобретению увеличивается по сравнению с таковой у пептидного мономера вследствие образования димера. Пептидным димером по настоящему изобретению является пептидный димер опухолевого антигена, который может индуцировать CTL благодаря презентации (с помощью антиген-презентирующей клетки) пептида, формирующегося в результате процессинга пептида по настоящему изобретению в клетке.
Пептидный димер по настоящему изобретению образуется путем связывания двух пептидных мономеров посредством дисульфидной связи между остатками цистеина, представленными в мономерах. Таким образом, каждый из пептидных мономеров, включенный в пептидный димер WT1 настоящего изобретения, представляет собой пептид WT1, как описано выше, и включает по крайней мере один остаток цистеина. Пептидный димер WT1 по настоящему изобретению может быть гомодимером или гетеродимером.
В пептидном димере WT1 по настоящему изобретению аминокислотная последовательность, входящая в состав пептидного мономера, предпочтительно представляет собой Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3), Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7), Lys Thr Cys Gln Arg Lys Phe Ser Arg (SEQ ID NO:8) или Ser Cys Arg Trp Pro Ser Cys Gln Lys (SEQ ID NO:9). Наиболее предпочтительно, последовательность представляет собой последовательность Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7).
Пептидный димер WT1 настоящего изобретения можно получить способами, известными в данной области. Например, если пептидные мономеры включают одну пару остатков цистеина, то пептидный димер WT1 по настоящему изобретению может быть получен, например, путем удаления всех защитных групп, включая группы на цистеиновых боковых цепях, и затем, подвергая полученный мономерный раствор окислению воздухом в щелочной среде, либо добавлением оксиданта в щелочной или кислой среде до образования дисульфидной связи. Примеры оксидантов включают йод, диметилсульфоксид (DMSO) и гексацианожелезокислый калий.
Если каждый из пептидных мономеров включает два или более остатка цистеина, то пептидный димер WT1 по настоящему изобретению можно также получить способом, описанным выше. В этом случае, изомеры получают за счет разных типов дисульфидных связей. Альтернативно, пептидный димер WT1 по настоящему изобретению можно получить путем выбора комбинации защитных групп для цистеиновых боковых цепей. Примеры комбинаций защитных групп включают комбинации MeBzl (метилбензиловую) группы и Acm (ацетамидметиловую) группу, Trt (тритильную) группу и Acm группу, Npys (3-нитро-2-пиридилтио) группу и Acm группу, и S-Bu-t (S-трет-бутиловую) группу и Acm группу. Например, в случае комбинации MeBzl группы и Acm группы, пептидный димер WT1 можно получить путем удаления защитных групп, отличных от MeBzl группы и защитной группы на цистеиновой боковой цепи, подвергая полученный мономерный раствор окислению воздухом до образования дисульфидной связи между защищенными цистеиновыми остатками, и затем депротекцией и окислением, с применением йода до образования дисульфидной связи между остатками цистеина, предварительно защищенными Acm.
В другом аспекте, настоящее изобретение относится к фармацевтической композиции для лечения и профилактики рака, включающей HLA-A*1101-ограниченный пептид WT1 и/или пептидный димер WT1. Ген WT1 экспрессируется на высоком уровне при разных видах рака и опухолей, включая гематопоэтические опухоли, такие как лейкоз, миелодиспластический синдром, множественная миелома или злокачественная лимфома и солидные раки, такие как рак желудка, рак толстой кишки, рак легкого, рак молочной железы, герминогенный рак, рак печени, рак кожи, рак мочевого пузыря, рак простаты, рак матки, рак шейки матки или рак яичников. Следовательно, фармацевтическая композиция по настоящему изобретению может использоваться для лечения или профилактики рака. Если фармацевтическая композиция по настоящему изобретению вводится HLA-A*1101-позитивному индивиду, то индуцируются WT1-специфичные CTL с помощью HLA-A*1101-ограниченного пептида WT1 или пептидного димера, включенных в фармацевтическую композицию, и при помощи таких CTL раковые клетки у индивида повреждаются.
Фармацевтическая композиция по настоящему изобретению может включать, кроме HLA-A*1101-ограниченного пептида WT1 и/или пептидного димера WT1 в качестве активных ингредиентов, например, носитель, эксципиент или тому подобное. HLA-A*1101-ограниченный пептид WT1 или пептидный димер WT1, включенный в фармацевтическую композицию по настоящему изобретению, индуцирует WT1-специфичный CTL. Таким образом, фармацевтическая композиция по настоящему изобретению может содержать соответствующий адьювант или может использоваться вместе с соответствующим адьювантом для усиления эффективности индукции. Примеры предпочтительных адьювантов включают, но ими не ограничиваются, полный или неполный адьювант Фрейнда и гидроокись алюминия.
Способ использования фармацевтической композиции по настоящему изобретению может быть соответствующим образом выбран, в зависимости от условий, таких как тип заболевания, состояние индивида или участок-мишень. Примеры таких способов включают, но ими не ограничиваются, внутрикожное введение, подкожное введение, внутривенное введение, назальное применение и пероральное введение. Количество пептида или димера пептидного, включенного в фармацевтическую композицию по настоящему изобретению, а также лекарственная форма, количество введений и тому подобное фармацевтической композиции по изобретению можно соответствующим образом выбрать, в зависимости от условий, таких как тип заболевания, состояние индивида или участок-мишень. Единичная доза пептида составляет обычно 0,0001 мг-1000 мг, предпочтительно, 0,001 мг-1000 мг.
В другом аспекте настоящее изобретение относится к способу лечения и профилактики рака, включающему введение эффективного количества пептида WT1 и/или пептидного димера WT1 HLA-A*1101-позитивному индивиду. Рак, на который направлено лечение или профилактика, может быть любым, и примеры рака включают гематопоэтические опухоли, такие как лейкоз, миелодиспластический синдром, множественная миелома или злокачественная лимфома и солидных раков, такие как рак желудка, рак толстой кишки, рак легкого, рак молочной железы, герминогенный рак, рак печени, рак кожи, рак мочевого пузыря, рак простаты, рак матки, рак шейки матки или рак яичников.
В дополнительном аспекте, настоящее изобретение относится к способу определения наличия или количества WT1-специфичного CTL у HLA-A*1101-позитивного индивида, включающий:
(a) взаимодействие комплекса пептида WT1 и молекулы HLA-A*1101 с образцом индивида; и
(b) определение наличия и/или количества CTL, распознающего комплекс, содержащийся в образце. Образец индивида может быть любым при условии, что существует вероятность, что он содержит лимфоцит. Примеры образцов включают жидкость организма, такую как кровь или лимфу, и ткань. Комплекс пептида WT1 и молекулы HLA-A*1101 может быть получен, например, в виде тетрамера или пентамера с применением способа, известного специалисту в данной области, такого как биотин-стрептавидин способ. Наличие и количество CTL, распознающего такой комплекс, может быть измерено способом, известным специалисту в данной области. В этом аспекте настоящего изобретения комплекс может быть помечен. В качестве метки может использоваться известная метка, такая как флуоресцентная метка или радиоактивная метка. Мечение делает определение наличия и количества CTL легким и быстрым.
Таким образом, настоящее изобретение также относится к композиции для определения наличия и количества WT1-специфичного CTL у HLA-A*1101-позитивного индивида, включающей HLA-A*1101-ограниченный пептид WT1.
Кроме того, настоящее изобретение относится к набору для определения наличия или количества WT1-специфичного CTL у HLA-A*1101-позитивного индивида, содержащему HLA-A*1101- ограниченный пептид WT1.
В дополнительном аспекте настоящее изобретение относится к способу получения WT1-специфичного CTL с использованием комплекса пептида WT1 и молекулы HLA-A*1101, включающему:
(a) взаимодействие комплекса и образца; и
(b) получение CTL, распознающего комплекс, содержащийся в образце. Комплекс пептида WT1 и молекулы HLA-A*1101 описан выше. Образец может быть любым при условии, что существует вероятность, что он содержит лимфоцит. Примеры образцов включают образец, полученный у индивида, такой как кровь, и культуру клеток. CTL, распознающий комплекс, может быть получен с использованием способа, известного специалисту в данной области, такого как FACS или MACS. Настоящее изобретение позволяет культивировать полученный WT1-специфичный CTL и использовать его для лечения или профилактики разных типов рака.
Таким образом, настоящее изобретение также относится к WT1-специфичному CTL, получаемому способом получения WT1-специфичного CTL, с использованием комплекса пептида WT1 и молекулы HLA-A*1101.
В другом аспекте настоящее изобретение относится к полинуклеотиду, кодирующему HLA-A*1101-ограниченный пептид WT1. Полинуклеотидом по настоящему изобретению может быть ДНК или РНК. Последовательность нуклеотидов настоящего изобретения может быть определена на основе аминокислотной последовательности HLA-A*1101-ограниченного пептида WT1. Этот полинуклеотид может быть получен известным способом синтеза ДНК или РНК (например, химическим синтетическим методом), методом ПЦР или тому подобное.
В другом аспекте настоящее изобретение относится к вектору экспрессии, содержащему этот полинуклеотид. Тип вектора экспрессии, включенную последовательность, отличную от последовательности полинуклеотида, и тому подобное можно соответствующим образом выбрать, в зависимости от типа хозяина, в котором продуцируется вектор экспрессии по настоящему изобретению, цели применения или тому подобное. Возможно лечение и профилактика гематопоэтических опухолей или солидных раков с помощью введения вектора экспрессии настоящего изобретения HLA-A*1101-позитивному индивиду для продуцирования HLA-A*1101-ограниченного пептида WT1 в живом организме и индукции WT1-специфичного CTL, и повреждения клеток гематопоэтической опухоли или клеток солидного рака у индивида.
В дополнительном аспекте настоящее изобретение относится к фармацевтической композиции для лечения и профилактики рака, содержащей полинуклеотид или вектор экспрессии. Эта композиция, способ использования и тому подобное фармацевтической композиции настоящего изобретения в этом аспекте описаны выше.
В другом аспекте, настоящее изобретение относится к способу лечения и профилактики рака, включающему введение эффективного количества полинуклеотида или вектора экспрессии HLA-A*1101-позитивному индивиду. Примеры типов рака для лечения и профилактики включают гематопоэтические опухоли, такие как лейкоз, миелодиспластический синдром, множественная миелома или злокачественная лимфома, и солидных раков, таких как рак желудка, рак толстой кишки, рак легкого, рак молочной железы, герминогенный рак, рак печени, рак кожи, рак мочевого пузыря, рак простаты, рак матки, рак шейки матки или рак яичников.
В другом аспекте настоящее изобретение относится к клетке, содержащей вектор экспрессии. Клетка по настоящему изобретению может быть получена, например, путем трансформирования клетки-хозяина, такой как E. coli, дрожжей, клетки насекомого или клетки животного, вектором экспрессии. Способ введения вектора экспрессии в клетку-хозяина можно соответствующим образом выбрать из нескольких способов. Пептид по настоящему изобретению может быть получен путем культивирования трансформированной клетки и выделения и очищения получаемого пептида WT1.
В дополнительном аспекте настоящее изобретение относится к WT1-специфичному CTL, который индуцируется с помощью HLA-A*1101-ограниченного пептида WT1 и/или пептидного димера WT1. CTL по настоящему изобретению распознает комплекс пептида WT1 и молекулы HLA-A*1101. Таким образом, CTL по настоящему изобретению может использоваться для специфического повреждения клеток опухоли, позитивной по HLA-A*1101, и экспрессии WT1 на высоком уровне.
В другом аспекте настоящее изобретение относится к способу лечения и профилактики рака, включающему введение WT1-специфичного CTL HLA-A*1101-позитивному индивиду. Этот способ применения WT1-специфичного CTL можно соответствующим образом выбрать, в зависимости от условий, таких как тип заболевания, состояние индивида или участок-мишень. Примеры таких способов включают, но ими не ограничиваются, внутривенное введение, внутрикожное введение, подкожное введение, внутримышечное введение, назальное применение и пероральное введение.
В другом аспекте настоящее изобретение относится к способу индукции WT1-специфичного CTL, включающему культивирование мононуклеарной клетки периферической крови в присутствии HLA-А*1101-ограниченного пептида WT1 и/или пептидного димера WT1 для индукции WT1-специфичного CTL из мононуклеарной клетки периферической крови. Индивид, у которого получают мононуклеарную клетку периферической крови, может быть любым, при условии, что он позитивен по HLA-A*1101. С помощью культивирования мононуклеарных клеток периферической крови в присутствии НLА-А*1101-ограниченного пептида WT1 и/или пептидного димера WT1, индуцируются WT1-специфичные CTL из клеток-предшественников CTL, содержащихся в мононуклеарных клетках периферической крови. Возможно лечение и профилактика гематопоэтических опухолей или солидных раков у HLA-A*1101-позитивных индивидов с помощью введения индивиду WT1-специфичного CTL, полученного в соответствии с настоящим изобретением.
В другом аспекте настоящее изобретение относится к набору для индукции WT1-специфичного CTL, содержащему HLA-A*1101-ограниченный пептид WT1 и/или пептидный димер WT1 в качестве основного компонента. Предпочтительно, этот набор используется в способе индукции WT1-специфичного CTL. Набор по настоящему изобретению может включать кроме HLA-A*1101-ограниченного пептида WT1 и/или пептидного димера WT1, например, средство для получения мононуклеарной клетки периферической крови, адьювант, реакционный сосуд или тому подобное. Как правило, к набору прилагается инструкция по применению. Используя набор по настоящему изобретению, можно эффективно индуцировать WT1-специфичные CTL.
В дополнительном аспекте настоящее изобретение относится к антиген-презентирующей клетке (такой как дендритная клетка), презентирующей пептид WT1 посредством молекулы HLA-A*1101, которая индуцируется с помощью HLA-A*1101-ограниченного пептида WT1 и/или пептидного димера WT1. При применении антиген-презентирующей клетки настоящего изобретения эффективно индуцируются WT1-специфичные CTL.
В другом аспекте настоящее изобретение относится к способу лечения и профилактики рака, включающему введение антиген-презентирующей клетки, презентирующей пептид WT1 посредством молекулы HLA-A*1101, HLA-A*1101-позитивному индивиду. Способ использования антиген-презентирующей клетки можно соответствующим образом выбрать в зависимости от условий, таких как тип заболевания, состояние индивида или участок-мишень. Примеры таких способов включают, но не ограничиваются таковыми, внутривенное введение, внутрикожное введение, подкожное введение, внутримышечное введение, назальное применение и оральное введение.
В другом аспекте настоящее изобретение относится к способу интродукции антиген-презентирующей клетки, презентирующей пептид WT1 посредством молекулы HLA-A*1101, включающему культивирование незрелой антиген-презентирующей клетки в присутствии HLA-A*1101-ограниченного пептида WT1 и/или пептидного димера WT1 для индукции антиген-презентирующей клетки, презентирующей пептид WT1 посредством молекулы HLA-A*1101 из незрелой антиген-презентирующей клетки. Незрелой антиген-презентирующей клеткой именуется клетка, такая как незрелая дендритная клетка, которая может преобразоваться в антиген-презентирующую клетку. Индивид, от которого получена незрелая антиген-презентирующая клетка, может быть любым, при условии, что он является позитивным по HLA-A*1101. Поскольку незрелые антиген-презентирующие клетки содержатся, например, в мононуклеарных клетках периферической крови, такие клетки могут культивироваться в присутствии пептида WT1 и/или пептидного димера WT1.
В другом аспекте настоящее изобретение относится к набору для индукции антиген-презентирующей клетки, презентирующей пептид WT1 посредством молекулы HLA-A*1101, включающему HLA-A*1101-ограниченный WT1 пептид WT1 и/или пептидный димер WT1 как существенный компонент. Предпочтительно, чтобы набор применялся в способе индукции антиген-презентирующей клетки. Другой компонент, который должен включаться в набор настоящего изобретения и тому подобное, описаны выше. Набор настоящего изобретения может применяться для эффективной индукции антиген-презентирующей клетки, презентирующей пептид WT1 посредством молекулы HLA-A*1101.
В другом аспекте настоящее изобретение относится к антителу против HLA-A*1101-ограниченного пептида WT1 или полинуклеотида, кодирующего этот пептид. Антитело настоящего изобретения может быть поликлональным или моноклональным антителом.
В дополнительном аспекте настоящее изобретение относится к способу диагностики рака, включающему применение WT1-специфичного CTL, антиген-презентирующей клетки, презентирующей пептид WT1 посредством молекулы HLA-A*1101, или антитела против HLA-A-ограниченного пептида WT1 или полинуклеотида, кодирующего этот пептид. Предпочтительно, чтобы WT1-специфичный CTL применялся в способе диагностики настоящего изобретения. Например, возможно, диагностика рака с помощью инкубации CTL, антиген-презентирующей клетки или антитела с образцом от HLA-A*1101-позитивного индивида, или введения этого HLA-A*1101-позитивному индивиду и определения, например, положения, сайта или количества такового. CTL, антиген-презентирующая клетка или антитело могут быть помечены. Присоединяя метку, можно эффективно использовать на практике способ для диагностики настоящего изобретения.
Примеры
Следующие примеры более детально иллюстрируют настоящее изобретение, но они не должны быть истолкованы как ограничивающие диапазон его применения.
Пример 1: Выбор пептида WT1
RANKPEP
(http://bio.dfci.harvard.edu/Tools/rankpep.html) применялась для выбора WT1251, WT1279, WT1312, WT1313, WT1338, WT1378, WT1386, WT1415 и WT1436, обладающих высокой способностью связываться с молекулой HLA-A*1101, полученной из пептидов из белка WT1 (SEQ ID NO:1). Аминокислотные последовательности, число аминокислот в SEQ ID NO:1 и показатели афинности к молекуле HLA-A*1101 у этих пептидов представлены в Таблице 1.
(SEQ ID NO:2)
(SEQ ID NO:3)
(SEQ ID NO:4)
(SEQ ID NoO:5)
(SEQ ID NO:6)
(SEQ ID NO:7)
(SEQ ID NO:8)
(SEQ ID NO:9)
(SEQ ID NO:10)
Получение B-LCL клетки
Мононуклеарные клетки периферической крови (PBMCs) выделялись с помощью метода центрифугирования в градиенте плотности на основе фиколла (Ficoll-Hypaque) из периферической крови, забранной у HLA-A*1101-позитивного здорового донора. PBMCs высевались в 24-луночный планшет для клеточных культур с плотностью приблизительно 1×107 в среде RPMI 1640, содержащей 10% ФТС (FCS), с добавлением культурального супернатанта клеток B95-8 (клетки, продуцирующие EB вирус). Они культивировались при 37°C с 5% CO2 приблизительно 1 месяц. Были получены B-LCL клетки, трансформированные вирусом EB, которые являлись B-клеточными опухолевыми клетками. Было подтверждено, что полученные B-LCL клетки не экспрессировали ген WT1. B-LCL клетки пульсировали при помощи инкубирования их с 20 мкг/мл WT1251, WT1279, WT1312, WT1313, WT1338, WT1378, WT1386, WT1415 или WT1436 в течение 2 часов, и облучали при 80 Гр радиации. Полученные в результате B-LCL клетки (далее именуемые как B-LCL клетки, пульсированные пептидом WT1) использовали как антигенпрезентирующие клетки для последующих экспериментов.
Индукция WT1-специфичного CTL
3×106 аутологических PBMCs культивировали в 24-луночном планшете для клеточных культур в полной среде (45% RPMI, 45% AMI-V среда и 10% сыворотка AB человека), содержащей 20 мкг/мл WT1251, WT1279, WT1312, WT1313, WT1338, WT1378, WT1386, WT1415 или WT1436 при 37°C с 5% CO2 в течение 1 недели для получения отвечающих клеток. 2×106 полученных отвечающих клеток культивировали вместе с 1×106 B-LCL клетками, пульсированными тем же пептидом WT1 в полной среде в течение 1 недели (первая стимуляция). PBMCs кокультивировали с B-LCL клетками, пульсированными пептидом WT1, еще три раза (со второй по четвертую стимуляции) при условиях, при которых добавляли 20 IU/мл (конечная концентрация) IL2 следующим образом: вторая стимуляция: два раза через день через 3 дня после инициирования стимуляции; третья и четвертая стимуляции: три раза с интервалом в один день через день после инициирования стимуляции. Полученные клетки концентрировали, используя набор Negative Selection Columns Gravity Feed (StemSp), так что соотношение CD8-позитивных T-клеток становилось равным приблизительно 80%, и кокультивировали с B-LCL клетками, пульсированными пептидом WT1 (пятая стимуляция). Для измерения цитоксической активности применялись CD8-позитивные T-клетки (CTLs), полученные через 5 дней после финальной стимуляции.
Цитоксическая активность CTL
Цитоксическая активность CTLs измерялась с использованием теста с высвобождением 51Cr. CTL клетки (далее именуемые эффекторные клетки) смешивали в соотношении (E/T отношение) от 1:1 до 30:1 в 200 мкл среды с клетками-мишенями, в которые инкорпорировался 51Cr, и культивировали в 96-луночном планшете для клеточных культур при 37°C с 5% CO2 в течение 4 часов. B-LCL клетки, пульсированные тем же пептидом WT1, который применялся для индукции CTLs (BLCL-Ps), и B-LCL клетки без пульсирования пептидом WT1 (BLCL-NPs) использовались как клетки-мишени. После культивирования, с помощью центрифугирования собирали супернатанты. Количеств 51Cr, высвобожденного в супернатанты, измеряли с применением жидкостных сцинтиляционных счетчиков. Цитоксическая активность (%) определялась по следующей формуле:
(Высвобождение 51Cr в супернатант образца - Спонтанное высвобождение 51Cr)/(Максимальное высвобождение 51Cr - Спонтанное высвобождение 51Cr)×100,
где Спонтанное высвобождение 51Cr есть высвобождение 51Cr, наблюдаемое, когда клетки-мишени, в которые инкорпорировался 51Cr, культивировали отдельно при тех же условиях, а Максимальное высвобождение 51Cr есть высвобождение 51Cr, наблюдаемое, когда клетки-мишени, в которые инкорпорировался 51Cr, были полностью лизированы с применением 1% Тритона X-100.
Результаты показаны на Фиг.1-9. На этих фигурах, вертикальной оси представляют специфический лизис (%), а горизонтальные оси представляют E/T отношения. BLCL-P изображены сплошными линиями, а BLCL-NP представлены линиями, состоящими из точек. Было подтверждено, что CTL, индуцированные WT1251, WT1279, WT1312, WT1313, WT1338, WT1378, WT1386, WT1415 или WT1436, специфично повреждают BLCL-P, презентирующие пептид WT1 как комплекс с молекулой HLA-A*1101, при сравнении с BLCL-NP. CTL, индуцированные WT1251, WT1279, WT1313, WT1338 или WT1386, применяли для дополнительных экспериментов ниже.
Цитоксическая активность CTL против клетки, эндогенно-экспрессирующей WT1
Цитоксическая активность CTL, индуцированных WT1251, WT1279, WT1313, WT1338 или WT1386, против B-LCL, экспрессирующих WT1, определялась способом, описанным выше. Клетка, экспрессирующая WT1, относится к B-LCL, в которую внесен ген WT1 человека и которая экспрессирует белок WT1 в клетке, и представляет пептид, состоящий приблизительно из 9 аминокислот, полученных в результате процессинга молекулы HLA-A*1101. Результаты показаны на Фиг.1, 2, 4, 5 и 7. На Фигурах, B-LCLs, экспрессирующие WT1, изображены пунктирными линиями. Было подтверждено, что CTL, индуцированные WT1251, WT1279, WT1313, WT1338 или WT1386, обладают цитоксической активностью против клеток, эндогенно-экспрессирующих ген WT1.
Приготовление пептидного димера WT1
Смесь из 227,5 мг WT1378 пептидного мономера, 227,5 мг N-метилглукамин (NMG) и 23 мл воды окисляли воздухом с помощью перемешивания при комнатной температуре приблизительно в течение 2 дней. К полученной смеси добавляли водный раствор 2 г натрия ацетата в 5 мл воды и смесь перемешивали при комнатной температуре приблизительно в течение 20 минут. К полученному раствору добавляли 200 мл воды и около 200 мл ацетонитрила и смесь фильтровали через воронку Кирияма (фильтровальная бумага №5C) и промывали водой (около 50 мл×3). К остатку добавляли около 200 мл воды и остаток лиофилизировали для получения 158 мг неочищенного WT1378 пептидного димера.
Очищение неочищенного пептидного димера WT1
158 мг неочищенного WT1378 пептидного димера растворяли в 9 мл DMSO и инжектировали в ODS C18 колонку (5 cm Φ × 50 cm L, YMC Co., LTD.), соединенную с ВЭЖХ (HPLC) (Shimadzu, LC8AD тип), и калибровали раствором 1 (H2O/1% AcOH) с применением ВЭЖХ (HPLC) насоса. Колонку оставляли приблизительно на 30 минут и элюировали в градиенте концентрации раствора 2 от 0% до 40% (CH3CN/1% AcOH) свыше 360 минут. Фракции, содержащие пептидный димер WT1, собирали с помощью автоматического коллектора фракций, при УФ мониторинге абсорбции при 220 нм. Собранные фракции объединяли, инжектировали в ODS C18 колонку (4,6 mm Φ × 25 cm L, YMC Co., LTD.), соединенную с ВЭЖХ (Hitachi, L-4000 тип), калибровали с помощью 17% раствора 2 и элюировали в градиенте концентрации раствора 2 от 0% до 47% свыше 30 минут для получения 46,6 мг очищенного WT1378 пептидного димера при времени удерживания 20,51 минуты.
FAB.MS 2365,0 (теоретическое значение (theoretical value): 2342,70) Na+ F=0,25%
Индукция CTL с помощью пептидного димера WT1
Способность полученного в результате WT1378 пептидного димера, WT1378 пептида, модифицированного WT1378 пептида (G → I) (SEQ ID NO:11) и модифицированного WT1378 пептида (G → V) (SEQ ID NO:12), а также WT1379 пептида (SEQ ID NO:13, как раскрывается в WO 2002/28414), индуцировать CTL, были изучены с применением PBMCs от HLA-A*1101-позитивных здоровых доноров 1-3 в соответствии со способом, описанным выше. Результаты показаны на Фиг.10-14. На этих фигурах вертикальные оси представляют специфический лизис (%), а горизонтальные оси представляют E/T отношение. BLCL-Ps изображены сплошными линиями, а BLCL-NPs представлены линиями, состоящими из точек. Было подтверждено, что WT1378 пептидный димер обладает способностью индуцировать CTL. Кроме того, было обнаружено, что способность каждого WT1379 пептида, аминокислотная последовательность которого отличается от таковой у WT1378 пептида на одну аминокислоту в одной аминокислотной последовательности белка WT1, индуцировать CTL намного ниже, чем таковая у WT1378 пептида, и, таким образом, пептид WT1 настоящего изобретения обладает отличным и неожиданным эффектом по сравнению с известным пептидом.
Промышленная применимость
Настоящее изобретение относится к HLA-A*1101-ограниченному пептиду WT1, полинуклеотиду, кодирующему этот пептид, фармацевтической композиции, содержащей этот пептид, и тому подобное. Следовательно, настоящее изобретение может использоваться в медицине и тому подобному, например, в области разработки и получения фармацевтической композиции для профилактики или лечения различных гематопоэтических опухолей и солидных раков, которые экспрессируют ген WT1 на высоком уровне.
Свободный текст перечня последовательностей
SEQ ID NO:11: Модифицированный пептид WT1
SEQ ID NO:12: Модифицированный пептид WT1.






Изобретение относится к области иммунологии. Представлен пептид, полученный из белка WT1, который способен связываться с молекулой HLA-А*1101 и индуцировать CTL, имеющий последовательность SEQ ID NO:6 или SEQ ID NO:7, представленные в описании. Кроме того, описан пептидный димер, применяемый для тех же целей и состоящий из двух пептидных мономеров, выбранных из группы пептидов, состоящей из SEQ ID NO:7, SEQ ID NO:3, SEQ ID NO:8 и SEQ ID NO:9, имеющихся в описании. Представлена нуклеиновая кислота, кодирующая указанный пептид и экспрессионный вектор, содержащий указанную нуклеиновую кислоту. Описана фармацевтическая композиция для лечения или профилактики рака у индивида, позитивного по HLA-A*1101, содержащая указанные пептид, нуклеиновую кислоту или вектор. Описаны WT1-специфичный CTL, индуцируемый указанным пептидом или димером, и антиген-презентирующая клетка, презентирующая указанный пептид. Имеются сведения о способе и наборе для индукции WT1-специфичного CTL и для индукции антиген-презентирующей клетки. Представлен способ in vitro диагностики рака у индивида, позитивного по HLA-A*1101, включающий инкубирование указанных CTL или антиген-презентирующей клетки с образцом, полученным у индивида, позитивного по HLA-A*1101, и определение количества указанной CTL или антиген-презентирующей клетки. Изобретение позволяет расширить ассортимент связывающихся с HLA-A*1101 пептидов, полученных из антигена WT1. 14 н.п. ф-лы, 1 табл., 14 ил., 1пр.
1. Пептид, состоящий из аминокислотной последовательности, которая выбрана из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6) или
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
где пептид способен связываться с молекулой HLA-A*1101 и способен индуцировать CTL.
2. Пептидный димер, состоящий из пептидных мономеров (1) и (2), которые связаны между собой дисульфидной связью:
(1) пептидный мономер, состоящий из аминокислотной последовательности:
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
(2) пептидный мономер, состоящий из аминокислотной последовательности, выбранной из:
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3),
Lys Thr Cys Gln Arg Lys Phe Ser Arg (SEQ ID NO:8) или
Ser Cys Arg Trp Pro Ser Cys Gln Lys (SEQ ID NO:9),
где пептидный димер способен связываться с молекулой HLA-A*1101 и способен индуцировать CTL.
3. Фармацевтическая композиция для лечения или профилактики рака у индивида, позитивного по HLA-A*1101, содержащая пептид, состоящий из аминокислотной последовательности, которая выбрана из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) или
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5), и/или пептидный димер по п.2.
4. Применение пептида, состоящего из аминокислотной последовательности, которая выбрана из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) и
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5),
и/или пептидного димера по п.2 для получения лекарственного средства для лечения или профилактики рака у индивида, позитивного по HLA-А*1101.
5. Полинуклеотид, кодирующий пептид, состоящий из аминокислотной последовательности, которая выбрана из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6), и
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
где пептид способен связываться с молекулой HLA-A*1101 и способен индуцировать CTL.
6. Вектор экспрессии, содержащий полинуклеотид по п.5.
7. Фармацевтическая композиция для лечения или профилактики рака у индивида, позитивного по HLA-A*1101, содержащая полинуклеотид, кодирующий пептид, состоящий из аминокислотной последовательности, выбранной из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) или
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5),
или вектор, содержащий указанный полинуклеотид.
8. Применение полинуклеотида, кодирующего пептид, который состоит из аминокислотной последовательности, которая выбрана из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) или
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5),
или вектора, содержащего указанный полинуклеотид, для получения лекарственного средства для лечения или профилактики рака у индивида, позитивного по HLA-A*1101.
9. WT1-специфичный CTL, который индуцируется in vitro с помощью пептида, состоящего из аминокислотной последовательности, выбранной из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) или
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5).
10. Способ in vitro индукции WT1-специфичного CTL, включающий культивирование мононуклеарной клетки периферической крови, полученной от индивида, позитивного по HLA-A*1101, в присутствии пептида, состоящего из аминокислотной последовательности, выбранной из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) и
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5),
для индукции WT1-специфичного CTL из мононуклеарной клетки периферической крови.
11. Антиген-презентирующая клетка, презентирующая пептид WT1 посредством молекулы HLA-A*1101, которая индуцируется in vitro посредством пептида, состоящего из аминокислотной последовательности, выбранной из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) и
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5).
12. Способ индукции антиген-презентирующей клетки, презентирующей пептид WT1, предусматривающий культивирование незрелой антиген-презентирующей клетки, полученной у индивида, позитивного по HLA-А*1101, в присутствии пептида, состоящего из аминокислотной последовательности, выбранной из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) и
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5),
для индукции антиген-презентирующей клетки, презентирующей пептид WT1, из незрелой антиген-презентирующей клетки.
13. Набор для индукции WT1-специфичного CTL и для индукции антиген-презентирующей клетки, презентирующей пептид WT1, содержащий в качестве основного компонента пептид, состоящий из аминокислотной последовательности, выбранной из:
Ser His Leu Gln Met His Ser Arg Lys (SEQ ID NO:6),
Thr Gly Val Lys Pro Phe Gln Cys Lys (SEQ ID NO:7),
Pro Ile Leu Cys Gly Ala Gln Tyr Arg (SEQ ID NO:3) и
Ser Ala Ser Glu Thr Ser Glu Lys Arg (SEQ ID NO:5),
и/или пептидный димер по п.2, и инструкцию по применению.
14. Способ in vitro диагностики рака у индивида, позитивного по HLA-А*1101, отличающийся тем, что предусматривает инкубирование CTL по п.9 или антиген-презентирующей клетки по п.11 с образцом, полученным у индивида, позитивного по HLA-A*1101, и определение количества указанной CTL или антиген-презентирующей клетки.
| US 7144581 В2, 05.12.2006 | |||
| 0 |
|
SU162920A1 | |
| WO 03105855 A1, 24.12.2003 | |||
| Бронированной фюзеляж для летательных аппаратов | 1926 |
|
SU5140A1 |
| КОМПОЗИЦИИ И СПОСОБЫ WT1-СПЕЦИФИЧНОЙ ИММУНОТЕРАПИИ | 1999 |
|
RU2237674C2 |
Авторы
Даты
2013-05-10—Публикация
2007-12-14—Подача