[Область техники]
Настоящее изобретение относится к области биологической науки, более конкретно, к области терапии злокачественных опухолей. В частности, настоящее изобретение относится к новым пептидам, которые эффективны в качестве противоопухолевых вакцин, к способам для лечения и/или профилактики опухолей с использованием пептида/пептидов, и фармацевтическим композициям, содержащим пептид(-ы).
[Предшествующий уровень техники]
Было известно, что CD8-положительные цитотоксические T-лимфоциты (ЦТЛ) распознают эпитопные пептиды, полученные из опухолеассоциированных антигенов (TAA) и презентированные на молекуле главного комплекса гистосовместимости (MHC) класса I, которая экспрессируется на клеточной поверхности, а затем убивают опухолевые клетки. С момента открытия семейства антигенов меланомы (MAGE) с использованием иммунологических подходов было обнаружено много других TAA (NPL1: Boon T, Int J Cancer 1993, 54(2): 177-80; NPL2: Boon T & van der Bruggen P, J Exp Med 1996, 183(3): 725-9). Некоторые из этих TAA в настоящее время проходят клиническую разработку в качестве мишеней для иммунотерапии.
В некоторых из этих TAA были выявлены эпитопные пептиды, которые могут распознаваться ЦТЛ, и планируется их применение в иммунотерапии для различных типов злокачественных опухолей (NPL3: Harris CC, J Natl Cancer Inst 1996, 88(20): 1442-55; NPL4: Butterfield LH et al., Cancer Res 1999, 59(13): 3134-42; NPL5: Vissers JL et al., Cancer Res 1999, 59(21): 5554-9; NPL6: van der Burg SH et al., J Immunol 1996, 156(9) 3308-14; NPL7: Tanaka F et al., Cancer Res 1997, 57(20): 4465-8; NPL8: Fujie T et al., Int J Cancer 1999, 80(2): 169-72; NPL9: Kikuchi M et al., Int J Cancer 1999, 81(3): 459-66; NPL10: Oiso M et al., Int J Cancer 1999, 81(3): 387-94). До настоящего времени, было зарегистрировано несколько клинических испытаний с использованием этих эпитопных пептидов, полученных из TAA. Однако, к сожалению, многие из этих клинических испытаний показали низкую частоту объективных ответов (NPL11: Belli F et al., J Clin Oncol 2002, 20(20): 4169-80; NPL12: Coulie PG et al., Immunol Rev 2002, 188: 33-42; NPL13: Rosenberg SA et al., Nat Med 2004, 10(9): 909-15). Таким образом, все еще существует потребность в выявлении новых эпитопных пептидов для ЦТЛ, которые можно использовать в иммунотерапии злокачественных опухолей.
FOXM1 (номер доступа GenBank: NM_202003; Forkhead box M1) был идентифицирован и описан как ген, чья экспрессия повышена в тканях внутрипеченочной холангиокарциономы, немелкоклеточного рака легких и рака пищевода, как следует из анализа полногеномного профиля экспрессии генов с использованием кДНК, нацеленного на 27648 генов (NPL14: Obama K et al., Hepatology 2005, 41(6): 1339-48; NPL15: Yokomine K et al., Int J Cancer 2010, 126(9): 2153-63; PTL1: WO2005/090603). С другой стороны, уровень экспрессии FOXM1 в нормальной ткани очень низок по сравнению с этими опухолевыми тканями. Кроме того, при ингибировании экспрессии FOXM1 была подавлена пролиферация клеток медуллобластомы (NPL16: Priller M et al., Clin Cancer Res 2011, 17(21): 6791-801); предполагают, что FOXM1 является геном, участвующим в регуляции пролиферации раковых клеток. Более конкретно, FOXM1 представляет собой TAA для повторной пролиферации многих раков, и, таким образом, эпитопные пептиды, полученные из FOXM1, рассматриваются для применения в иммунотерапии, направленной на пациентов со злокачественными опухолями.
Недавно были идентифицированы эпитопные пептиды для ЦТЛ, полученные из FOXM1 и рестриктированные по HLA-A02 (PTL2: WO2009/025196) и HLA-A24 (PTL3: WO2010/095428). Можно ожидать терапевтического эффекта от этих пептидов у пациентов со злокачественными опухолями, имеющих тип HLA-A02 или HLA-A24, но не у других раковых пациентов.
[Список цитирования]
[Патентная литература]
[PTL 1] WO2005/090603
[PTL 2] WO2009/025196
[PTL 3] WO2010/095428
[Непатентная литература]
[NPL 1] Boon T, Int J Cancer 1993, 54(2): 177-80
[NPL 2] Boon T & van der Bruggen P, J Exp Med 1996, 183(3): 725-9
[NPL 3] Harris CC, J Natl Cancer Inst 1996, 88(20): 1442-55
[NPL 4] Butterfield LH et al., Cancer Res 1999, 59(13): 3134-42
[NPL 5] Vissers JL et al., Cancer Res 1999, 59(21): 5554-9
[NPL 6] van der Burg SH et al., J Immunol 1996, 156(9): 3308-14
[NPL 7] Tanaka F et al., Cancer Res 1997, 57(20): 4465-8
[NPL 8] Fujie T et al., Int J Cancer 1999, 80(2): 169-72
[NPL 9] Kikuchi M et al., Int J Cancer 1999, 81(3): 459-66
[NPL 10] Oiso M et al., Int J Cancer 1999, 81(3): 387-94
[NPL 11] Belli F et al., J Clin Oncol 2002, 20(20): 4169-80
[NPL 12] Coulie PG et al., Immunol Rev 2002, 188: 33-42
[NPL 13] Rosenberg SA et al., Nat Med 2004, 10(9): 909-15
[NPL 14] Obama K et al., Hepatology 2005, 41(6): 1339-48
[NPL 15] Yokomine K et al., Int J Cancer 2010, 126(9): 2153-63
[NPL 16] Priller M et al., Clin Cancer Res 2011, 17(21): 6791-801
Сущность изобретения
Настоящее изобретение относится к пептидам, которые могут индуцировать ЦТЛ, которые специфически реагируют на клетки, экспрессирующие FOXM1. Когда эти пептиды образуют комплекс с человеческим лейкоцитарным антигеном (HLA) и презентируются CD8-положительным T-клеткам при помощи антигенпрезентирующих клеток (APC), которые презентируют на своей поверхности этот комплекс, индуцируются ЦТЛ, которые демонстрируют пептид-специфическую цитотоксическую активность. Пептиды, полученные из FOXM1, которые были идентифицированы к настоящему времени, как имеющие способность индуцировать ЦТЛ (индуцибельность ЦТЛ), являются или HLA-A02-рестриктированными или HLA-A24-рестриктированными пептидами, и не могут индуцировать ЦТЛ против клеток, которые не экспрессируют эти HLA. Таким образом, известные пептиды не подходят для проведения иммунотерапии у индивидуумов, у которых нет этих HLA. HLA-A33 представляет собой аллель, который часто встречается у азиатов, и HLA-A01 представляет собой аллель HLA, который часто встречается у европеоидов (Cao et al., Hum Immunol 2001; 62(9): 1009-30). Желательно вводить HLA-A33-рестриктированные пептиды HLA-A33-положительным индивидуумам, и HLA-A01-рестриктированные пептиды HLA-A01-положительным индивидуумам. Таким образом, настоящее изобретение относится к пептидам, полученным из FOXM1 и способным индуцировать ЦТЛ, и которые являются рестриктированными по HLA-A33 или HLA-A01. На основании результатов, описываемых в настоящем документе, было доказано, что пептиды по настоящему изобретению являются эпитопными пептидами, которые могут индуцировать мощный и специфический иммунный ответ против клеток, экспрессирующих FOXM1 и HLA-A33 или HLA-A01.
Таким образом, одной из задач по настоящему изобретению является создание пептидов, полученных из FOXM1, которые могут индуцировать ЦТЛ ограничительно по HLA-A33 или HLA-A01. Эти пептиды можно использовать для индуцирования ЦТЛ in vitro, ex vivo или in vivo, или можно использовать для введения индивидуумам с целью индуцирования иммунного ответа против FOXM1-экспрессирующих злокачественных клеток. Предпочтительными пептидами являются пептиды, содержащие аминокислотную последовательность, выбранную из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61; более предпочтительными пептидами являются нонапептиды или декапептиды; и еще более предпочтительными пептидами являются пептиды, состоящие из аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61.
Пептиды по настоящему изобретению включают пептиды, в которых одна, две или более аминокислот замещены, удалены, вставлены и/или добавлены, при условии, что полученные модифицированные пептиды сохраняют способность исходного пептида индуцировать ЦТЛ.
Настоящее изобретение дополнительно относится к изолированным полинуклеотидам, кодирующим любой один из пептидов по настоящему изобретению. Аналогично пептидам по настоящему изобретению, эти полинуклеотиды можно использовать для индуцирования АПК со способностью индуцировать ЦТЛ, и можно вводить индивидуумам для индуцирования иммунного ответа против FOXM1-экспрессирующих злокачественных клеток.
Настоящее изобретение также относится к композициям, содержащим один или несколько типов пептидов по настоящему изобретению, один или несколько типов полинуклеотидов, кодирующих один или несколько типов пептидов по настоящему изобретению, АПК по настоящему изобретению, экзосомы, презентирующие пептиды по настоящему изобретению, и/или ЦТЛ по настоящему изобретению. Композиции по настоящему изобретению предпочтительно являются фармацевтическими композициями. Фармацевтические композиции по настоящему изобретению можно использовать для лечения и/или профилактики злокачественной опухоли, а также для профилактики послеоперационных рецидивов злокачественной опухоли. Их также можно использовать для индуцирования иммунного ответа против злокачественной опухоли. При введении индивидууму, пептид по настоящему изобретению презентируется на поверхности АПК, и в результате индуцируются ЦТЛ, нацеленные на пептид. Таким образом, другой задачей по настоящему изобретению является создание композиций для индуцирования ЦТЛ, где композиции содержат один или несколько типов пептидов по настоящему изобретению, один или несколько типов полинуклеотидов, кодирующих один или несколько типов пептидов по настоящему изобретению, АПК по настоящему изобретению и/или экзосомы, презентирующие пептиды по настоящему изобретению.
Следующей задачей по настоящему изобретению является создание способов индуцирования АПК, имеющих способность индуцировать ЦТЛ, где способы включают этап контакта одного или нескольких типов пептидов по настоящему изобретению с АПК, или этап введения полинуклеотида, кодирующего любой один пептид по настоящему изобретению, в АПК.
Настоящее изобретение дополнительно относится к способу индуцирования ЦТЛ, включающему этап совместного культивирования CD8-положительной T-клетки с АПК, которая презентирует на поверхности комплекс антигена HLA и пептида по настоящему изобретению, этап совместного культивирования CD8-положительной T-клетки с экзосомой, которая презентирует на поверхности комплекс антигена HLA и пептида по настоящему изобретению, или этап введения в CD8-положительную T-клетку вектора, содержащего полинуклеотид, кодирующий каждую субъединицу T-клеточного рецептора (TCR), способного связываться с пептидом по настоящему изобретению, который презентируется посредством антигена HLA на клеточной поверхности. Предпочтительным антигеном HLA в настоящем изобретении является HLA-A33 или HLA-A01.
Следующей задачей по настоящему изобретению является получение изолированных АПК, которые презентируют на поверхности комплекс антигена HLA и пептида по настоящему изобретению. Настоящее изобретение дополнительно относится к изолированным ЦТЛ, нацеленным на пептид по настоящему изобретению. Эти АПК и ЦТЛ можно использовать в иммунотерапии для FOXM1-экспрессирующих злокачественных опухолей. В настоящем изобретении, злокачественная опухоль, которую лечат иммунотерапией, является, например, злокачественной опухолью у пациентом, гомозиготных или гетерозиготных по HLA-A33 или HLA-A01. Следовательно, АПК или ЦТЛ также представляют собой клетки с гетерозиготой или гомозиготой по HLA-A33 или HLA-A01. Таким образом, настоящее изобретение относится к иммунотерапии для злокачественных опухолей, экспрессирующих FOXM1 и, по меньшей мере, один антиген HLA, выбранный из HLA-A33 и HLA-A01.
Другой задачей по настоящему изобретению является создание способов индуцирования иммунного ответа против злокачественной опухоли у индивидуума, где способы включают этап введения индивидууму композиции, содержащей пептид (-ы) по настоящему изобретению или полинуклеотид (-ы), кодирующие пептид(-ы), АПК по настоящему изобретению, экзосомы/экзосом, презентирующих пептид(-ы) по настоящему изобретению, и/или ЦТЛ по настоящему изобретению. Другой задачей по настоящему изобретению является создание способов для лечения и/или профилактики злокачественной опухоли, а также для профилактики послеоперационных рецидивов злокачественной опухоли у индивидуума, где способы включают этап введения индивидууму пептида/пептидов по настоящему изобретению, полинуклеотида/полинуклеотидов, кодирующих пептид(-ы), АПК по настоящему изобретению, экзосомы/экзосом, презентирующих пептид(-ы) по настоящему изобретению, и/или ЦТЛ по настоящему изобретению.
В дополнение к вышеизложенному, другие задачи и признаки настоящего изобретения станут более очевидными после прочтения последующего подробного описания в сочетании с сопутствующими фигурами и примерами. Однако следует понимать, что как указанная выше сущность по настоящему изобретению, так и последующее подробное описание являются примерами вариантов осуществления, и не ограничивают настоящее изобретение или другие альтернативные варианты осуществления настоящего изобретения. В частности, хотя настоящее изобретение описано в настоящем документе со ссылкой на ряд конкретных вариантов осуществления, следует понимать, что описание является иллюстративным по отношению к настоящему изобретению и не ограничивает настоящее изобретение. Специалисту в данной области могут прийти на ум различные модификации и применения, в пределах сущности и объема по настоящему изобретению, описанных в прилагаемой формуле изобретения. Кроме того, другие цели, особенности, выгоды и преимущества настоящего изобретения будут очевидны из сущности и определенных вариантов осуществления, описанных ниже, и будут легко понятны специалистам в данной области. Такие цели, особенности, выгоды и преимущества будут понятны из вышеизложенного в сочетании с сопутствующими примерами, данными, фигурами и всеми разумными выводами, вытекающими из них, по отдельности или с учетом ссылок, включенных в настоящий документ.
Краткое описание чертежей
Фиг. 1-1 состоит из фотографий от (a) до (v), показывающих результаты анализа способом иммуноферментных пятен (ELISPOT) с интерфероном (IFN)-гамма, который проводили с использованием клеток, индуцированных при помощи пептидов, полученных из FOXM1. На фигуре, «+» показывает выработку IFN-гамма против клеток-мишеней, активированных интересующим пептидом; и «-» показывает выработку IFN-гамма против клеток-мишеней, которые не были активированы ни одним из пептидов (отрицательные контроли). При сравнении с отрицательными контролями можно видеть, что пептид-специфическую выработку IFN-гамма наблюдали в
Лунке #6 с FOXM1-A33-9-180 (SEQ ID NO: 1) (a),
Лунке #3 с FOXM1-A33-9-308 (SEQ ID NO: 2) (b),
Лунке #4 с FOXM1-A33-9-693 (SEQ ID NO: 3) (c),
Лунке #3 с FOXM1-A33-9-516 (SEQ ID NO: 6) (d),
Лунке #5 с FOXM1-A33-9-146 (SEQ ID NO: 7) (e),
Лунке #6 с FOXM1-A33-9-289 (SEQ ID NO: 11) (f),
Лунке #6 с FOXM1-A33-9-228 (SEQ ID NO: 12) (g),
Лунке #4 с FOXM1-A33-9-502 (SEQ ID NO: 17) (h),
Лунке #2 с FOXM1-A33-9-321 (SEQ ID NO: 18) (i),
Лунке #6 с FOXM1-A33-9-341 (SEQ ID NO: 20) (j),
Лунке #8 с FOXM1-A33-10-514 (SEQ ID NO: 22) (k),
Лунке #6 с FOXM1-A33-10-179 (SEQ ID NO: 24) (l),
Лунке #5 с FOXM1-A33-10-501 (SEQ ID NO: 26) (m),
Лунке #5 с FOXM1-A33-10-124 (SEQ ID NO: 32) (n),
Лунке #3 с FOXM1-A33-10-595 (SEQ ID NO: 33) (o),
Лунке #5 с FOXM1-A33-10-546 (SEQ ID NO: 36) (p),
Лунке #6 с FOXM1-A33-10-391 (SEQ ID NO: 39) (q),
Лунке #3 с FOXM1-A33-10-607 (SEQ ID NO: 41) (r),
Лунке #2 с FOXM1-A33-10-265 (SEQ ID NO: 42) (s),
Лунке #6 с FOXM1-A33-10-4 (SEQ ID NO: 45) (t) и
Лунке #5 с FOXM1-A33-10-388 (SEQ ID NO: 46) (u). Клетки, которые продемонстрировали реакцию и выделены квадратом на фотографиях, размножали для получения линии ЦТЛ. При этом, FOXM1-A33-10-288 (SEQ ID NO: 25) (v) показан как пример типичных отрицательных данных, при котором не наблюдали пептид-специфической выработки IFN-гамма.
Фиг. 1-2 показывает продолжение Фиг. 1-1.
Фиг. 2 состоит из линейных графиков от (a) до (d), показывающих результаты измерений твердофазного иммуноферментного анализа (ELISA) для IFN-гамма, произведенного линией ЦТЛ, которая была стимулирована FOXM1-A33-9-308 (SEQ ID NO: 2) (a), FOXM1-A33-9-146 (SEQ ID NO: 7) (b), FOXM1-A33-10-391 (SEQ ID NO: 39) (c) или FOXM1-A33-10-265 (SEQ ID NO: 42) (d). Эти результаты показывают, что линии ЦТЛ, которые вырабатывают IFN-гамма пептид-специфическим образом, были получены после индуцирования каждым из пептидов. На фигуре, «+» показывает выработку IFN-гамма линией ЦТЛ против клеток-мишеней, активированных интересующим пептидом; и «-» показывает выработку IFN-гамма линией ЦТЛ против клеток-мишеней, которые не были активированы ни одним из пептидов. Соотношение R/S указывает на соотношение числа клеток линий ЦТЛ (клетки-респондеры) и числа клеток-мишеней, которые их стимулируют (клетки-стимуляторы).
Фиг. 3 состоит из линейных графиков от (a) до (b), показывающих выработку IFN-гамма в клоне ЦТЛ, полученном способом серийных разведений после индуцирования FOXM1-A33-9-308 (SEQ ID NO: 2) (a) или FOXM1-A33-9-146 (SEQ ID NO: 7) (b). Эти результаты показывают пептид-специфическую выработку IFN-гамма клонами ЦТЛ. На фигуре, «+» показывает выработку IFN-гамма клонами ЦТЛ против клеток-мишеней, активированных интересующим пептидом; и «-» показывает выработку IFN-гамма клонами ЦТЛ против клеток-мишеней, которые не были активированы ни одним из пептидов. Соотношение R/S указывает на соотношение числа клеток клона ЦТЛ (клетки-респондеры) и числа клеток-мишеней, которые их стимулируют (клетки-стимуляторы).
Фиг. 4 представляет собой линейный график, показывающий выработку IFN-гамма клонами ЦТЛ против клеток-мишеней, экспрессирующих и FOXM1, и HLA-A*33:03. Клетки-мишени, в которые был вставлен или HLA-A*33:03, или полноразмерный ген FOXM1, использовали в качестве отрицательного контроля. Клон CTL, полученный при индуцировании с использованием FOXM1-A33-9-308 (SEQ ID NO: 2), показал выработку IFN-гамма против клеток COS7, в которые были вставлены гены и FOXM1, и HLA-A*33:03 (черный ромб). С другой стороны, не было выявлено значительной выработки IFN-гамма против клеток COS7, в которые был вставлен один из HLA-A*33:03 (треугольник) и FOXM1 (белый круг).
Фиг. 5-1 состоит из фотографий от (a) до (n), показывающих результаты анализа способом иммуноферментных пятен (ELISPOT) с интерфероном (IFN)-гамма, который проводили с использованием клеток, индуцированных пептидами, полученными из FOXM1. На фигуре, «+» показывает выработку IFN-гамма против клеток-мишеней, активированных интересующим пептидом; и «-» показывает выработку IFN-гамма против клеток-мишеней, которые не были активированы ни одним из пептидов (негативные контроли). При сравнении с негативными контролями можно видеть, что пептид-специфическую выработку IFN-гамма наблюдали в
Лунке #3 с FOXM1-A01-9-233 (SEQ ID NO: 48) (a),
Лунке #3 с FOXM1-A01-9-539 (SEQ ID NO: 49) (b),
Лунке #3 с FOXM1-A01-9-631 (SEQ ID NO: 50) (c),
Лунке #2 с FOXM1-A01-9-231 (SEQ ID NO: 52) (d),
Лунке #2 с FOXM1-A01-9-663 (SEQ ID NO: 53) (e),
Лунке #5 с FOXM1-A01-9-494 (SEQ ID NO: 55) (f),
Лунке #2 с FOXM1-A01-9-341 (SEQ ID NO: 20) (g),
Лунке #1 с FOXM1-A01-10-566 (SEQ ID NO: 56) (h),
Лунке #2 с FOXM1-A01-10-263 (SEQ ID NO: 57) (i),
Лунке #4 с FOXM1-A01-10-308 (SEQ ID NO: 58) (j),
Лунке #6 с FOXM1-A01-10-232 (SEQ ID NO: 59) (k),
Лунке #6 с FOXM1-A01-10-663 (SEQ ID NO: 60) (l) и
Лунке #6 с FOXM1-A01-10-341 (SEQ ID NO: 61) (m). Клетки, которые продемонстрировали реакцию и выделены квадратом на фотографиях, размножали для получения линии ЦТЛ. При этом, FOXM1-A01-10-265 (SEQ ID NO: 42) (n) показан как пример типичных отрицательных данных, при котором не наблюдали пептид-специфической выработки IFN-гамма.
Фиг. 5-2 показывает продолжение Фиг. 5-1.
Фиг. 6 представляет собой линейный график, показывающий результат измерения путем ELISA IFN-гамма, выработанного линией ЦТЛ, которая была стимулирована FOXM1-A01-10-566 (SEQ ID NO: 56). Результат показывает, что линия ЦТЛ, которая вырабатывает IFN-гамма пептид-специфическим образом, была получена после индуцирования пептидом. На фигуре, «+» показывает выработку IFN-гамма линией ЦТЛ против клеток-мишеней, активированных интересующим пептидом; и «-» показывает выработку IFN-гамма линией ЦТЛ против клеток-мишеней, которые не были активированы ни одним из пептидов. Соотношение R/S указывает на соотношение числа клеток линии ЦТЛ (клетки-респондеры) и числа клеток-мишеней, которые их стимулируют (клетки-стимуляторы).
Фиг. 7 состоит из серий линейных графиков от (a) до (b) показывающих выработку IFN-гамма в клоне ЦТЛ, полученном способом серийных разведений после индуцирования FOXM1-A01-9-233 (SEQ ID NO: 48) или FOXM1-A01-10-566 (SEQ ID NO: 56). Эти результаты показывают пептид-специфическую выработку IFN-гамма клонами ЦТЛ.. На фигуре, «+» показывает выработку IFN-гамма клонами ЦТЛ против клеток-мишеней, активированных интересующим пептидом; и «-» показывает выработку IFN-гамма клонами ЦТЛ против клеток-мишеней, которые не были активированы ни одним из пептидов. Соотношение R/S указывает на соотношение числа клеток клона ЦТЛ (клетки-респондеры) и числа клеток-мишеней, которые их стимулируют (клетки-стимуляторы).
Фиг. 8 представляет собой линейный график, показывающий выработку IFN-гамма клонами ЦТЛ против клеток-мишеней, экспрессирующих и FOXM1, и HLA-A*01:01. Клетки-мишени, в которые был вставлен или HLA-A*01:01, или полноразмерный ген FOXM1, использовали в качестве отрицательного контроля. Клон CTL, полученный при индуцировании с использованием FOXM1-A01-10-566 (SEQ ID NO: 56), показал выработку IFN-гамма против клеток COS7, в которые были вставлены гены и FOXM1, и HLA-A*01:01 (черный ромб). С другой стороны, не было выявлено значительной выработки IFN-гамма против клеток COS7, в которые был вставлен один из HLA-A*01:01 (треугольник) и FOXM1 (белый круг).
[Способ осуществления изобретения]
Описание вариантов осуществления
Хотя в практическом осуществлении или тестировании вариантов осуществления настоящего изобретения можно использовать любые способы и материалы, аналогичные или эквивалентные тем, что описаны в настоящем документе, предпочтительные способы, устройства и материалы описаны в настоящем документе. Однако перед тем как будут описаны материалы и способы по настоящему изобретению, следует понимать, что настоящее изобретение не ограничено конкретными размерами, формами, измерениями, материалами, способами, протоколами, и т.д., описываемыми в настоящем документе, поскольку они могут варьировать в соответствии с рутинной экспериментальной деятельностью и оптимизацией. Также следует понимать, что терминология, применяемая в описании, предназначена только для описания конкретных версий или вариантов осуществления, и не предназначена для ограничения объема по настоящему изобретению, который ограничен только прилагаемой формулой изобретения.
I. Определения
Определители единственного числа, используемые в настоящем документе, означают «по меньшей мере, один», если конкретно не указано иное.
Термины «изолированный» и «очищенный», применяемые по отношению к веществу (например, пептиду, антителу, полинуклеотиду или т.п.), указывают на то, что вещество по существу не содержит, по меньшей мере, ни одно вещество, которое также может входить в натуральный источник. Таким образом, изолированный или очищенный пептид относится к пептиду, который по существу не содержит другой клеточный материал, например, углевод, липид и другие загрязняющие белки из источника клеток или ткани, из которого получают пептид. Если пептид синтезируют химическим путем, изолированный или очищенный пептид относится к пептиду, который по существу не содержит вещество-предшественник или другое химическое вещество. Фраза «по существу не содержит клеточный материал» включает получение пептида, при котором пептид отделяют от клеточных компонентов из клеток, из которых пептид выделен или где он был рекомбинантно произведен. Таким образом, пептид, который по существу не содержит клеточный материал, включает пептидные препараты, которые содержат менее чем приблизительно 30%, 20%, 10%, или 5%, 3%, 2% или 1% (на основании сухой массы) других клеточных материалов.
Если пептид производят рекомбинантным способом, изолированный или очищенный пептид, который по существу не содержит среду для культивирования, и пептид, который по существу не содержит среду для культивирования, включает пептидные препараты, которые содержат среду для культивирования, менее чем приблизительно 20%, 10% или 5%, 3%, 2% или 1% (на основании сухой массы) от объема пептидного препарата.
Альтернативно, если пептид синтезируют химическим путем, изолированный или очищенный пептид по существу не содержит вещество-предшественник или другое химическое вещество, и пептид, который по существу не содержит вещество-предшественник или другое химическое вещество, включает пептидные препараты, которые содержат вещество-предшественник или другие химические вещества, менее чем приблизительно 30%, 20%, 10%, 5%, 3%, 2% или 1% (на основании сухой массы) от объема пептидного препарата. То, что конкретный пептидный препарат является изолированным или очищенным можно подтверждать, например, при появлении одиночной полосы при электрофорезе с додецилсульфатом натрия (SDS) в полиакриламидном геле и окраске Кумасси бриллиантовым голубым или на подобном геле. В предпочтительном варианте осуществления пептиды и полинуклеотиды по настоящему изобретению являются изолированными или очищенными.
Термины «полипептид», «пептид» и «белок» в настоящем документе используются взаимозаменяемо, и относятся к полимерам из аминокислотных остатков. Эти термины также применяют к неприродным аминокислотным полимерам, содержащим один или несколько неприродных аминокислотных остатков, в дополнение к природным аминокислотным полимерам. Неприродные аминокислоты включают аналоги аминокислот, миметики аминокислот, и т.п.
Термин «аминокислота», применяемый в настоящем документе, относится к природным аминокислотам, а также аналогам аминокислот и миметикам аминокислот, которые функционируют аналогично природным аминокислотам. Природными аминокислотами являются аминокислоты, которые кодируются генетическим кодом, а также аминокислоты, модифицированные после трансляции в клетках (например, гидроксипролин, гамма-карбоксиглутаминат, и O-фосфосерин, и т.д.). Фраза «аналог аминокислоты» относится к соединениям, которые имеют такую же основную химическую структуру (альфа углерод, связанный с водородом, карбоксигруппу, аминогруппу, и группу R), как и природная аминокислота, но имеют модифицированную R-группу или модифицированные остовы (например, гомосерин, норлейцин, метионин сульфоксид, метионин метил сульфоний, и т.п.). Фраза «миметик аминокислоты» относится к соединениям, которые имеют различные структуры с основными аминокислотами, но аналогичные функции с аминокислотами. Аминокислоты могут быть или L-аминокислотами или D-аминокислотами, и пептиды по настоящему изобретению предпочтительно являются L-аминокислотными полимерами.
Термины «полинуклеотид», «олигонуклеотид» и «нуклеиновая кислота» используются взаимозаменяемо в настоящем документе, и относятся к полимеру из нуклеотидов.
Термин «композиция», применяемый в настоящем описании, предназначен для включения продуктов, которые содержат конкретно оговоренные ингредиенты в конкретно оговоренных количествах, и любых продуктов, полученных прямо или косвенно из комбинации конкретно оговоренных ингредиентов в конкретно оговоренных количествах. Если композиция представляет собой фармацевтическую композицию, термин «композиция» предназначен для включения продуктов, содержащих активный ингредиент/ингредиенты и инертный ингредиент/ингредиенты, а также любых продуктов, полученных прямо или косвенно из комбинации, комплексообразования или агрегации любых двух или более ингредиентов, из диссоциации одного или нескольких ингредиентов, или из реакций другого типа или взаимодействий одного или нескольких ингредиентов. Таким образом, фармацевтические композиции по настоящему изобретению включают в себя любые композиции, полученные путем смешивания соединений или клеток по настоящему изобретению с фармацевтически или физиологически приемлемым носителем. Не являясь ограничивающими, термины «фармацевтически приемлемый носитель» или «физиологически приемлемый носитель», применяемые в настоящем описании, включают жидкие или твердые наполнители, разбавители, эксципиенты, растворители, и инкапсулирующие материалы; и означают фармацевтически или физиологически приемлемые материалы, композиции, вещества или среды.
Если не указано иначе, термин «злокачественная опухоль» относится к злокачественной опухоли, которая гиперэкспрессирует ген FOXM1; и примеры таких опухолей включают острый миелоидный лейкоз, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, хронический миелолейкоз (ХМЛ), рак толстого кишечника, рак пищевода, рак желудка, диффузный рак желудка, немелкоклеточный рак легких (NSCLC), лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак почки, мелкоклеточный рак легких (SCLC), опухоль мягких тканей, рак яичка и т.п., не ограничиваясь вышеизложенными. В иллюстративном варианте осуществления «злокачественная опухоль» представляет собой злокачественную опухоль, которая экспрессирует FOXM1 и HLA-A33 и/или HLA-A01.
Если не указано иначе, термины «цитотоксический T-лимфоцит» и «цитотоксическая T-клетка» и «ЦТЛ» используют взаимозаменяемо в настоящем документе. Если конкретно не указано иное, они относятся к подгруппе T-лимфоцитов, которая может распознавать «чужие» клетки (например, опухолевые/злокачественные клетки, вирус-инфицированные клетки) и индуцировать гибель таких клеток.
Если не указано иначе, термин «HLA-A33» относится к типу HLA-A33, который включает подтипы, такие как HLA-A*33:03, HLA-A*33:01 и HLA-A*33:04.
Если не указано иначе, термин «HLA-A01» относится к типу HLA-A01, который включает подтипы, такие как HLA-A*01:01, HLA-A*01:03 и HLA-A*01:04.
В отношении индивидуума или пациента, фраза «антиген HLA индивидуума (или пациента) представляет собой HLA-A33», применяемая в настоящем документе, указывает, что индивидуум или пациент имеет ген антигена HLA-A33 в гомозиготном или гетерозиготном состоянии как молекулу MHC (Главного комплекса гистосовместимости) класса I, и что антиген HLA-A33 экспрессируется в клетках индивидуума или пациента в виде антигена HLA. Аналогично, фраза «антиген HLA индивидуума (или пациента) представляет собой HLA-A01», применяемая в настоящем документе, указывает, что индивидуум или пациент имеет ген HLA-A01 в гомозиготном или гетерозиготном состоянии как молекулу MHC (Главного комплекса гистосовместимости) класса I, и что антиген HLA-A01 экспрессируется в клетках индивидуума или пациента в виде антигена HLA.
При условии, что способы и композиции по настоящему изобретению пригодны в отношении «лечения» злокачественной опухоли, лечение считается «эффективным», если оно достигает клинических преимуществ, например, уменьшение размера, распространения или метастатических свойств злокачественной опухоли, замедление прогрессирования злокачественной опухоли, ослабление клинических симптомов злокачественной опухоли, продление периода выживания, подавление послеоперационных рецидивов у индивидуума. Если лечение применяется профилактически, «эффективность» означает, что лечение замедляет или предотвращает образование злокачественной опухоли, или предупреждает или ослабляет клинические симптомы злокачественной опухоли. Эффективность определяют по отношению к любым общеизвестным способам для диагностики или лечения конкретного типа опухоли.
При условии, что способы и композиции по настоящему изобретению пригодны в отношении «предупреждения (профилактики)» злокачественной опухоли, термин «предупреждение (профилактика)» в настоящем документе включает любую работу, которая облегчает бремя смертности или заболеваемости, ассоциированных со злокачественными опухолями. Предупреждение (профилактику) можно проводить на «первичном, вторичном и третичном профилактических уровнях». В то время как первичное предупреждение (профилактика) помогает избежать развития заболевания, вторичное и третичное предупреждение (профилактика) включает в себя предупреждение (профилактику) прогрессирования заболевания и появления симптомов, а также деятельность, предназначенную для снижения неблагоприятных воздействий существующего заболевания путем восстановления функций и уменьшения осложнений, ассоциированных с заболеванием. С другой стороны, предупреждение (профилактика) может включать в себя ослабление тяжести конкретного нарушения, например, обширную профилактическую терапию, предназначенную для уменьшения роста опухоли и метастазирования.
В контексте настоящего изобретения, лечение и/или предупреждение (профилактика) злокачественной опухоли и/или предупреждение (профилактика) ее послеоперационного рецидива включают в себя любое из событий, таких как ингибирование пролиферации злокачественных клеток, инволюцию или регрессию опухоли, инициацию ремиссии и подавление развития злокачественной опухоли, регрессию опухоли, а также уменьшение или ингибирование метастазирования, подавление послеоперационных рецидивов злокачественной опухоли, и продление периода выживания. Эффективное лечение и/или предупреждение (профилактика) злокачественной опухоли снижает смертность, улучшает прогноз индивидуума со злокачественной опухолью, снижает уровень опухолевых маркеров в крови, и облегчает выявляемые симптомы, ассоциированные со злокачественной опухолью. Например, облегчение или улучшение симптомов составляет эффективное лечение и/или предупреждение (профилактику), и включает состояние, при котором симптомы стабильны или улучшены на 10%, 20%, 30% или больше.
В контексте настоящего изобретения, термин «антитело» относится к иммуноглобулинам и их фрагментам, которые специфически реакционноспособны по отношению к обозначенному белку или его пептиду. Антитело может включать антитела человека, приматизированные антитела, химерные антитела, биспецифические антитела, гуманизированные антитела, антитела, слитые с другими белками или радиоактивными метками, и фрагменты антител. Кроме того, «антитело» в настоящем документе используется в самом широком смысле и конкретно включает интактные моноклональные антитела, поликлональные антитела, полиспецифические антитела (например, биспецифические антитела), образованные из двух или более интактных антител, и фрагменты антител при условии, что они проявляют желательную биологическую активность. «Антитело» может быть антителами всех классов (например, IgA, IgD, IgE, IgG и IgM).
Если не указано иначе, все технические термины и научные термины, применяемые в настоящем документе, имеют то же самое значение, в каком их обычно понимает специалист в области, к которой относится настоящее изобретение.
II. Пептиды
HLA-A33 представляет собой аллель, который часто встречается у азиатов, и HLA-A01 представляет собой аллель, который часто встречается у европеоидов (Cao et al., Hum Immunol 2001; 62(9): 1009-30). Таким образом, предлагается эффективный способ лечения FOXM1-экспрессирующих злокачественных опухолей для большой популяции азиатов или европеоидов путем создания пептидов, полученных из FOXM1, которые способны к индуцированию ЦТЛ и рестриктированы по HLA-A33 или HLA-A01. Таким образом, настоящее изобретение относится к пептидам, полученным из FOXM1, которые способны индуцировать ЦТЛ ограничительно по HLA-A33 или HLA-A01.
Пептиды по настоящему изобретению представляют собой пептиды, полученные из FOXM1, которые способны индуцировать ЦТЛ ограничительно по HLA-A33 или HLA-A01. Пептиды, способные индуцировать ЦТЛ ограничительно по HLA-A33, включают пептиды с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46. Пептиды, способные индуцировать ЦТЛ ограничительно по HLA-A01, включают пептиды с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61.
ЦТЛ с цитотоксической активностью, специфичные по отношению к этим пептидам, можно создавать при стимуляции Т-клеток in vitro дендритными клетками (DC), активированными этими пептидами. Полученные ЦТЛ демонстрируют специфическую цитотоксическую активность против клеток-мишеней, активированных каждым из пептидов.
Ген FOXM1 сверхэкспрессирован в злокачественных клетках, таких как злокачественные клетки, например, при остром миелоидном лейкозе, раке мочевого пузыря, раке молочной железы, раке шейки матки, холангиоцеллюлярном раке, хроническом миелолейкозе (ХМЛ), раке толстого кишечника, раке пищевода, раке желудка, диффузном раке желудка, немелкоклеточном раке легких (NSCLC), лимфоме, остеосаркоме, раке яичников, раке поджелудочной железы, раке предстательной железы, раке почки, мелкоклеточном раке легких (SCLC), опухоли мягких тканей, раке яичка и т.п., но не экспрессируется в большинстве здоровых органов. Следовательно, он представляет собой превосходную мишень для иммунотерапии. Таким образом, пептиды по настоящему изобретению могут быть подходящим образом использованы для иммунотерапии злокачественной опухоли. Предпочтительным пептидом является нонапептид (пептид, состоящий из 9 аминокислотных остатков) или декапептид (пептид, состоящий из 10 аминокислотных остатков), и более предпочтительным является пептид, состоящий из аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61. Например, пептид с аминокислотной последовательностью из SEQ ID NO: 2 подходит для индуцирования ЦТЛ, демонстрирующих цитотоксическую активность против клеток, экспрессирующих HLA-A33 и FOXM1, и может быть подходящим образом использован для иммунотерапии злокачественной опухоли у HLA-A33-положительных пациентов. В более предпочтительном варианте осуществления пептид по настоящему изобретению представляет собой пептид, состоящий из аминокислотной последовательности SEQ ID NO: 2. Дополнительно, например, пептид с аминокислотной последовательностью SEQ ID NO: 56 подходит для индуцирования ЦТЛ, демонстрирующих цитотоксическую активность против клеток, экспрессирующих HLA-A01 и FOXM1, и может быть подходящим образом использован для иммунотерапии злокачественной опухоли у HLA-A01- положительных пациентов. В более предпочтительном варианте осуществления пептид по настоящему изобретению представляет собой пептид, состоящий из аминокислотной последовательности SEQ ID NO: 56.
Для пептидов по настоящему изобретению, дополнительный аминокислотный остаток/остатки могут быть присоединены к аминокислотной последовательности пептида по настоящему изобретению, при условии, что полученные пептиды сохраняют способность исходного пептида индуцировать ЦТЛ. Дополнительный аминокислотный остаток/остатки могут состоять из любых типов аминокислот, при условии, что они не снижают способность исходного пептида индуцировать ЦТЛ. Таким образом, пептиды по настоящему изобретению включают пептиды, способные индуцировать ЦТЛ, состоящие из аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61. Такие пептиды состоят, например, менее чем из приблизительно 40 аминокислот, во многих случаях менее чем из приблизительно 20 аминокислот, и, как правило, менее чем из приблизительно 15 аминокислот. Таким образом, если исходный пептид представляет собой нонапептид, пептид по настоящему изобретению относится к пептидам, которые имеют 10 аминокислот в длину или 11-40 аминокислот в длину, которые получены добавлением дополнительной аминокислоты/аминокислот к пептиду. Более того, если исходный пептид представляет собой декапептид, пептид по настоящему изобретению относится к пептидам, которые имеют 11-40 аминокислот в длину. Такой пептид может быть, например, пептидом, который имеет 11-20 аминокислот в длину, или пептидом, который имеет 11-15 аминокислот в длину. Предпочтительным примером дополнительного аминокислотного остатка/остатков является аминокислотный остаток/остатки, примыкающие к аминокислотной последовательности пептида по настоящему изобретению в полноразмерной аминокислотной последовательности FOXM1 (например,, SEQ ID NO: 67, 69, 71, 73 или 75). Таким образом, пептиды по настоящему изобретению включают пептиды, содержащие аминокислотную последовательность, выбранную из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 and 61, и где пептиды представляют собой пептидные фрагменты FOXM1 и имеют способность индуцировать ЦТЛ.
Как правило, модификации одной, двух или более аминокислот в определенном пептиде не влияют на функции пептида, или в некоторых случаях даже усиливают желаемые функции исходного пептида. Фактически, известно, что модифицированные пептиды (т.е., пептиды, состоящие из аминокислотной последовательности, в которой один, два или несколько аминокислотных остатков являются модифицированными (т.е., замещены, удалены, вставлены, и/или добавлены) по сравнению с исходной референсной последовательностью) сохраняют биологическую активность исходного пептида (Mark et al., Proc Natl Acad Sci USA 1984, 81: 5662-6; Zoller and Smith, Nucleic Acids Res 1982, 10: 6487-500; Dalbadie-McFarland et al., Proc Natl Acad Sci USA 1982, 79: 6409-13). Таким образом, в одном из вариантов осуществления пептиды по настоящему изобретению могут быть пептидами, содержащими аминокислотную последовательность, в которой одна, две или несколько аминокислот замещены, удалены, вставлены, и/или добавлены к аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61, и имеющими способность индуцировать ЦТЛ.
Специалисту в данной области ясно, что отдельные замены в аминокислотной последовательности, которые изменяют единичную аминокислоту или небольшое процентное содержание аминокислот, как правило, приводят к сохранению свойств исходной боковой цепи/цепей аминокислоты. Таким образом, на них часто ссылаются как на «консервативные замены» или «консервативные модификации»; и модификация белка «консервативной заменой» или «консервативной модификацией» может приводить к модифицированному белку, который имеет функции, аналогичные функциям исходного белка. Таблицы консервативных замен, представляющие функционально сходные аминокислоты, хорошо известны в данной области. Примеры характеристик боковых цепей аминокислот, которые функционально похожи, включают, например, гидрофобные аминокислоты (A, I, L, M, F, P, W, Y, V), гидрофильные аминокислоты (R, D, N, C, E, Q, G, H, K, S, T), и боковые цепи со следующими общими функциональными группами или характеристиками: алифатические боковые цепи (G, A, V, L, I, P); боковые цепи, содержащие гидроксильную группу (S, T, Y); боковые цепи, содержащие атом серы (C, M); боковые цепи, содержащие карбоновую кислоту и амид (D, N, E, Q); боковые цепи, содержащие основание (R, K, H); и ароматические боковые цепи (H, F, Y, W). Кроме того, следующие восемь групп содержат аминокислоты, которые принимаются в данной области в качестве консервативных замен друг для друга:
1) Аланин (A), Глицин (G);
2) Аспарагиновая кислота (D), Глутаминовая кислота (E);
3) Аспарагин (N), Глутамин (Q);
4) Аргинин (R), Лизин (K);
5) изолейцин (I), Лейцин (L), Метионин (M), Валин (V);
6) Фенилаланин (F), Тирозин (Y), Триптофан (W);
7) Серин (S), Треонин (T); и
8) Цистеин (C), Метионин (M) (см., например, Creighton, Proteins 1984).
Такие консервативно модифицированные пептиды также включены в пептиды по настоящему изобретению. Однако пептиды по настоящему изобретению не ограничены ими и могут включать неконсервативные модификации, при условии, что модифицированный пептид сохраняет способность исходного пептида индуцировать ЦТЛ. Кроме того, модифицированные пептиды не исключают пептиды, способные индуцировать ЦТЛ, которые получены из полиморфных вариантов, межвидовых гомологов, и аллелей FOXM1.
При условии, что пептид сохраняет способность исходного пептида индуцировать ЦТЛ, можно модифицировать (т.е., замещать, удалять, вставлять и/или добавлять) небольшое число (например, 1, 2 или несколько) или небольшое процентное содержание аминокислот. В настоящем документе, термин «несколько» означает 5 или менее аминокислот, например, 4 или 3, или менее. Процентное содержание аминокислот, которые будут модифицированы, предпочтительно составляет 20% или менее, более предпочтительно, 15% или менее, даже более предпочтительно, 10% или менее, или от 1 до 5%.
При использовании для иммунотерапии, пептиды по настоящему изобретению должны презентироваться на поверхности клетки или экзосомы, предпочтительно в виде комплекса с антигеном HLA. Таким образом, предпочтительно, что пептиды по настоящему изобретению обладают высокой аффинностью связывания с антигеном HLA. С этой целью, пептиды можно модифицировать при помощи замены, делеции, вставки, и/или добавления аминокислотных остатков для получения модифицированного пептида с улучшенной аффинностью связывания. Поскольку закономерность последовательностей пептидов, показанная путем связывания с антигенами HLA, уже известна (Falk, et al., Immunogenetics 1994 40 232-41; Chujoh, et al., Tissue Antigens 1998: 52: 501-9; Takiguchi, et al., Tissue Antigens 2000: 55: 296-302.), модификации на основании такой закономерности можно вводить в пептиды по настоящему изобретению.
Например, в пептидах с аффинностью связывания для HLA класса I, вторая аминокислота с N-конца и C-концевая аминокислота, как правило, представляют собой якорные остатки, участвующие в связывании с HLA класса I (Rammensee HG, et al., Immunogenetics. 1995; 41(4): 178-228). Например, в HLA-A33, фенилаланин, тирозин, аланин, изолейцин, лейцин и валин в качестве второй аминокислоты с N-конца, и лизин и аргинин в качестве C-концевой аминокислоты известны как якорные остатки с высокой аффинностью связывания для HLA-A33 (Falk, et al., Immunogenetics 1994, 40: 232-41; Takiguchi, et al., Tissue Antigens 2000, 55: 296-302).
Дополнительно, в HLA-A33, также известно, что первый аминокислотный остаток с N-конца функционирует как якорный остаток, и известно, что аспарагиновая кислота и глутаминовая кислота являются предпочтительными в качестве первой аминокислоты с N-конца (Falk, et al., Immunogenetics 1994, 40: 232-41; Takiguchi, et al., Tissue Antigens 2000: 55: 296-302). Таким образом, для того чтобы сохранить или усилить аффинность связывания с HLA-A33, существует вероятность того, что желательно заменить первую аминокислоту с N-конца аспарагиновой кислотой или глутаминовой кислотой, вторую аминокислоту с N-конца - фенилаланином, тирозином, аланином, изолейцином, лейцином или валином, и/или С-концевую аминокислоту - аргинином или лизином.
Следовательно, пептиды по настоящему изобретению включают в себя пептиды со способностью индуцировать ЦТЛ, содержашие аминокислотную последовательность, в которой в аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, первая аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой, вторая аминокислота с N-конца замещена фенилаланином, тирозином, аланином, изолейцином, лейцином или валином, и/или С-концевая аминокислота замещена аргинином или лизином.
В предпочтительном варианте осуществления, пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который состоит из аминокислотной последовательности, в которой в аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, первая аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой, вторая аминокислота с N-конца замещена фенилаланином, тирозином, аланином, изолейцином, лейцином или валином, и/или С-концевая аминокислота замещена аргинином или лизином.
То есть, пептиды по настоящему изобретению включают в себя пептид со способностью индуцировать ЦТЛ, который содержит аминокислотную последовательность с одной или несколькими заменами, которые выбраны из нижеизложенных от (a) до (c), в аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46:
(a) первая аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой;
(b) вторая аминокислота с N-конца замещена фенилаланином, тирозином, аланином, изолейцином, лейцином или валином; и
(c) С-концевая аминокислота замещена аргинином или лизином.
В предпочтительном варианте осуществления пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который состоит из аминокислотной последовательности с одной или несколькими заменами, которые выбраны из вышеизложенных от (a) до (c) в аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46. В настоящем изобретении, предпочтительное число замен составляет 1, 2 или 3 замены, выбранные из вышеизложенных от (a) до (c).
Кроме того, пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который содержит аминокислотную последовательность, в которой в аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, вторая аминокислота с N-конца замещена фенилаланином, тирозином, аланином, изолейцином, лейцином или валином, и/или С-концевая аминокислота замещена аргинином или лизином. Предпочтительно, пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который состоит из аминокислотной последовательности, в которой, в аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, вторая аминокислота с N-конца замещена фенилаланином, тирозином, аланином, изолейцином, лейцином или валином, и/или С-концевая аминокислота замещена аргинином или лизином. То есть, пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который содержит аминокислотную последовательность, в которой одна или несколько замен выбраны из нижеизложенных (a) и (b) в аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 and 46:
(a) вторая аминокислота с N-конца замещена фенилаланином, тирозином, аланином, изолейцином, лейцином или валином; и
(b) С-концевая аминокислота замещена аргинином или лизином.
В предпочтительном варианте осуществления пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который состоит из аминокислотной последовательности с одной или несколькими заменами, выбранными из вышеизложенных от (a) до (b) в аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46. В более предпочтительном варианте осуществления вторая аминокислота с N-конца замещена фенилаланином или тирозином.
Для HLA-A01, аспарагиновая кислота и глутаминовая кислота в качестве третьей аминокислоты с N-конца, и тирозин в качестве C-концевой аминокислоты известны как якорные остатки с высокой аффинностью связывания для HLA-A01. Дополнительно, известно, что существуют вспомогательные якорные остатки в положении 2 с N-конца для HLA-A01, и что треонин и серин являются предпочтительными в качестве второй аминокислоты с N-конца (Kubo, R.T Journal of Immunology 1994, 152: 3913; Gambacorti-Passerini, C. Clinical Cancer Research 1997, 3: 675-83; Falk, K. Immunogenetics 1994, 40: 238-41).
Таким образом, для сохранения или повышения аффинности связывания с HLA-A01, существует вероятность того, что желательно заменить третью аминокислоту с N-конца аспарагиновой кислотой или глутаминовой кислотой, и/или C-концевую аминокислоту тирозином. Дополнительно, существует вероятность того, что также желательно заменить вторую аминокислоту с N-конца треонином или серином. Таким образом, пептиды со способностью индуцировать ЦТЛ, содержащие аминокислотную последовательность, в которой, в аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61, вторая аминокислота с N-конца замещена треонином или серином, третья аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой, и/или C-концевая аминокислота замещена тирозином, охватываются пептидами по настоящему изобретению.
В предпочтительном варианте осуществления пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который состоит из аминокислотной последовательности, в которой, в аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61, вторая аминокислота с N-конца замещена треонином или серином, третья аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой, и/или C-концевая аминокислота замещена тирозином
То есть, пептиды по настоящему изобретению включают в себя пептид со способностью индуцировать ЦТЛ, который содержит аминокислотную последовательность с одной или несколькими заменами, выбранными из нижеизложенных от (a) до (c), в аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61:
(a) вторая аминокислота с N-конца замещена треонином или серином;
(b) третья аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой; и
(c) C-концевая аминокислота замещена тирозином.
В предпочтительном варианте осуществления пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который состоит из аминокислотной последовательности с одной или несколькими заменами, выбранными из вышеизложенных от (a) до (c), в аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61. В настоящем изобретении, предпочтительное число замен составляет 1, 2 или 3 замены, выбранные из числа вышеизложенных от (a) до (c).
Кроме того, пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который содержит аминокислотную последовательность, в которой, в аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61, третья аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой, и/или C-концевая аминокислота замещена тирозином. Предпочтительно, пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который содержит аминокислотную последовательность, в которой, в аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61, третья аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой, и/или C-концевая аминокислота замещена тирозином. То есть, пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который содержит аминокислотную последовательность с одной или несколькими заменами, которые выбраны из нижеизложенных от (a) до (b) в аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61:
(a) третья аминокислота с N-конца замещена аспарагиновой кислотой или глутаминовой кислотой; и
(b) C-концевая аминокислота замещена тирозином.
В предпочтительном варианте осуществления пептид по настоящему изобретению может быть пептидом со способностью индуцировать ЦТЛ, который состоит из аминокислотной последовательности с одной или несколькими заменами, которые выбраны из вышеуказанных от (a) до (b), в аминокислотной последовательности, выбранной из числа SEQ ID NOs: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61.
Замену/замены можно вводить в аминокислоту/аминокислоты пептидов не только в якорном участке/участках, но также в положении/положениях потенциальных участков распознавания T-клеточного рецептора (TCR) пептидов. Несколько исследовательских работ продемонстрировали, что пептид, который имеет замены аминокислот, такие как CAP1, p53(264-272), Her-2/neu(369-377) или gp100(209-217), может иметь равную или лучшую активность по сравнению с исходным пептидом (Zaremba et al. Cancer Res., 1997, 57, 4570-7; T. K. Hoffmann et al. J Immunol., 2002, 168(3): 1338-47; S. O. Dionne et al. Cancer Immunol immunother., 2003, 52: 199-206; and S. O. Dionne et al. Cancer Immunology, Immunotherapy, 2004, 53, 307-14).
Настоящее изобретение также предполагает, что одну, две или несколько аминокислот можно добавлять с N-конца и/или C-конца пептидов по настоящему изобретению (например, пептидов, состоящих из аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61). Более конкретно, настоящее изобретение относится к пептидам, состоящим из аминокислотных последовательностей, в которых одна, две или несколько аминокислот добавлены или к одному, или к обоим из N-конца и C-конца аминокислотных последовательностей, на которые ссылается каждая из SEQ ID NO. Такие модифицированные пептиды, которые сохраняют способность индуцировать ЦТЛ, также включены в настоящее изобретение. Например, если пептид, в котором одна, две или несколько аминокислот добавлены с N-конца и/или C-конца пептида, состоящего из аминокислотной последовательности SEQ ID NO: 2 или 56, контактирует с АПК, он захватывается в АПК и процессируется до пептида, состоящего из аминокислотной последовательности SEQ ID NO: 2 или 56. Он может затем индуцировать ЦТЛ путем презентирования на клеточной поверхности АПК с помощью пути презентации антигена. Более конкретно, пептиды по настоящему изобретению могут быть пептидами, в которых одну, две или несколько аминокислот добавляют к любому из N-конца и C-конца, или к обоим.
Дополнительно, в другом варианте осуществления настоящего изобретения, предлагаются пептиды, состоящие из аминокислотных последовательностей, содержащих одну, две или несколько замен аминокислот в аминокислотных последовательностях, на которые ссылается каждая из SEQ ID NO, и в которых одна, две или несколько аминокислоты добавлены или к одному, или к обоим из N-конца и C-конца этих замещенных аминокислотных последовательностей.
Если пептиды по настоящему изобретению содержат замену аминокислоты/аминокислот, желаемые положения для замены могут быть, например, одним, двумя или тремя положениями, выбранными из первого положения с N-конца, второго положения с N-конца и C-конца в аминокислотных последовательностях, на которые ссылаются SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, или одним, двумя или тремя положениями, выбранными из второго положения с N-конца, третьего положения с N-конца и C-конца в аминокислотных последовательностях, на которые ссылаются SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61, содержащиеся в пептидах по настоящему изобретению.
Однако если аминокислотная последовательность пептида идентична части аминокислотной последовательности эндогенного или экзогенного белка с отличающейся функцией, могут быть индуцированы побочные эффекты, такие как аутоиммунные нарушения и/или аллергические симптомы против конкретных веществ. Таким образом, предпочтительно проводить поиски с использованием доступных баз данных, для того чтобы избежать ситуаций, в которых аминокислотная последовательность пептида соответствует аминокислотной последовательности другого белка. Если из поисков гомологии становится ясно, что не существует пептида всего лишь с одной или двумя различающимися аминокислотами по сравнению с указанным пептидом, указанный пептид можно модифицировать для того чтобы повысить его аффинность связывания с антигенами HLA, и/или увеличить его способность индуцировать ЦТЛ без опасности таких побочных эффектов.
Пептиды, в которых модифицированы одна, две или несколько аминокислот из пептида по настоящему изобретению, теоретически спрогнозированы для сохранения способности исходного пептида индуцировать ЦТЛ; однако предпочтительно проверить способность модифицированных пептидов индуцировать ЦТЛ. В настоящем документе, «пептид со способностью индуцировать ЦТЛ (индуцибельность ЦТЛ)» относится к пептиду, который индуцирует ЦТЛ при помощи АПК, стимулированных пептидом. «Индуцирование ЦТЛ» включает индуцирование дифференцировки в ЦТЛ, индуцирование активации ЦТЛ, индуцирование пролиферации ЦТЛ, индуцирование цитотоксической активности ЦТЛ, индуцирование опосредованного ЦТЛ разрушения клеток-мишеней, и индуцирование повышенной выработки IFN-гамма ЦТЛ.
Способность индуцировать ЦТЛ можно подтверждать путем стимулирования АПК, которые экспрессируют интересующий антиген HLA (например, B-лимфоциты, макрофаги или дендритные клетки), с пептидом, и смешивания с CD8-положительными Т-клетками; и затем с помощью измерения IFN-гамма, высвобожденного ЦТЛ против клеток-мишеней. В качестве АПК можно предпочтительно использовать дендритные клетки, полученные из мононуклеарных клеток периферической крови человека. В качестве реакционной системы можно использовать трансгенных животных, созданных для экспрессии антигена HLA. Альтернативно, клетки-мишени могут быть радиоактивно-меченными с помощью 51Cr и так далее, и цитотоксическая активность пептид-индуцированных ЦТЛ может быть рассчитана на основании радиоактивности, испускаемой клетками-мишенями. Альтернативно, способность индуцировать ЦТЛ можно оценивать путем измерения IFN-гамма, выработанного и высвобожденного ЦТЛ в присутствии пептид-стимулированных АПК, и путем визуализации области ингибирования на среде с использованием моноклональных антител к IFN-гамма.
В дополнение к вышеизложенным модификациям, пептиды по настоящему изобретению могут быть связаны с другими пептидами при условии, что полученный связанный пептид сохраняет способность индуцировать ЦТЛ. Пример подходящего пептида для связывания с пептидами по настоящему изобретению включает пептид, индуцирующему ЦТЛ и полученному из других TAA. Дополнительно, пептиды по настоящему изобретению могут также быть связаны друг с другом. Подходящие линкеры для применения для связывания пептидов известны в данной области, и, например, можно использовать линкеры, такие как AAY (P. M. Daftarian et al., J Trans Med 2007, 5:26), AAA, NKRK (SEQ ID NO: 62) (R. P. M. Sutmuller et al., J Immunol. 2000, 165: 7308-15), или K (S. Ota et al., Can Res. 62, 1471-6, K. S. Kawamura et al., J Immunol. 2002, 168: 5709-15). Пептиды можно связывать в различных расположениях (например, мелкими цепочками, повторами, и т.д.), и можно также связывать три или более пептидов.
Пептиды по настоящему изобретению могут также быть связааны с другими веществами при условии, что полученный связанный пептид сохраняет способность индуцировать ЦТЛ. Примеры подходящего вещества для связывания с пептидом по настоящему изобретению включают, например, пептид, липид, сахар или цепь сахаров, ацетильную группу, и природный или синтетический полимер. Пептиды по настоящему изобретению можно модифицировать путем гликозилирования, окисления боковых цепей, фосфорилирования или т.п., при условии, что их способность индуцировать ЦТЛ не будет нарушена. Можно также проводить такие типы модификаций для придания дополнительных функций (например, нацеливающей функции и функции доставки) или для стабилизации пептида.
Например, для повышения стабильности пептида in vivo в данной области известно введение D-аминокислот, миметиков аминокислот или неприродных аминокислот, и эта концепция также может быть применима к пептидам по настоящему изобретению. Стабильность пептидов можно оценивать несколькими способами. Например, стабильность можно тестировать с использованием пептидазы, а также различных биологических сред, таких как плазма и сыворотка человека (см., например, Verhoef et al., Eur J Drug Metab Pharmacokin 1986, 11: 291-302).
Дополнительно, как указано выше, среди модифицированных пептидов, в которых один, два, или несколько аминокислотных остатков были замещены, удалены, вставлены и/или добавлены, можно проводить скрининг или отбор по тем пептидам, которые имеют такую же или более высокую активность, как и исходные пептиды. Таким образом, настоящее изобретение также относится к способам скрининга или отбора модифицированных пептидов, которые имеют такую же или более высокую активность, как и исходный пептид. Конкретно, настоящее изобретение относится к способу скрининга на пептид со способностью индуцировать ЦТЛ, где способ включает этапы:
(a) создания кандидатных последовательностей, состоящих из аминокислотной последовательности, в которой один, два, или несколько аминокислотных остатков замещены, удалены, вставлены и/или добавлены по сравнению с исходной аминокислотной последовательностью, состоящей из аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61;
(b) отбора в кандидатных последовательностях, полученных в (a), кандидатной последовательности, которая не имеет значительной гомологии (идентичности последовательности) с любым известным продуктом гена человека, за исключением FOXM1;
(c) контакта пептида, состоящего из кандидатной последовательности, выбранной в (b), с АПК;
(d) контакта АПК из (c) с CD8-положительными T-клетками; и
(e) отбора пептида, который имеет равную или более высокую способность индуцировать ЦТЛ, чем пептид, состоящий из исходной аминокислотной последовательности.
В настоящем документе, пептид по настоящему изобретению также описан как «пептид(-ы) FOXM1».
III. Получение пептидов по настоящему изобретению
Для получения пептидов по настоящему изобретению можно использовать хорошо известные способы. Например, для получения пептидов по настоящему изобретению можно использовать технологию рекомбинантных ДНК или химический синтез. Пептиды по настоящему изобретению можно синтезировать по отдельности, или в виде более длинных полипептидов, включающих два или более пептида. Пептиды по настоящему изобретению можно выделять из клеток-хозяев или продуктов реакции синтеза, после того как они были произведены в клетках-хозяевах при помощи технологии рекомбинантных ДНК или после того как они были синтезированы химическим путем. То есть, пептиды по настоящему изобретению можно очищать или изолировать таким образом, что они по существу не содержат других белков и их фрагментов из клетки-хозяина, или любых других химических веществ.
Пептиды по настоящему изобретению могут содержать модификации, такие как гликозилирование, окисление боковых цепей, фосфорилирование при условии, что такие модификации не разрушают биологическую активность исходного пептида. Другие иллюстративные модификации включают введение D-аминокислот или других миметиков аминокислот, которые можно использовать, например, для увеличения времени полувыведения пептидов из сыворотки.
Пептид по настоящему изобретению можно получать путем химического синтеза на основании выбранной аминокислотной последовательности. Примеры общепринятых способов пептидного синтеза, которые можно адаптировать для синтеза, включают способы, описанные в документах ниже:
(i) Peptide Synthesis, Interscience, New York, 1966;
(ii) The Proteins, Vol. 2, Academic Press, New York, 1976;
(iii) ʺPeptide Synthesisʺ (in Japanese), Maruzen Co., 1975;
(iv) ʺBasics and Experiment of Peptide Synthesisʺ (in Japanese), Maruzen Co., 1985;
(v) ʺDevelopment of Pharmaceuticalsʺ (in Japanese), Continued Vol. 14 (peptide synthesis), Hirokawa, 1991;
(vi) WO99/67288; и
(vii) Barany G. & Merrifield R.B., Peptides Vol. 2, Solid Phase Peptide Synthesis, Academic Press, New York, 1980, 100-118.
Альтернативно, пептиды по настоящему изобретению можно получать, адаптируя любые известные способы генетической инженерии для выработки пептидов (например, Morrison J, J Bacteriology 1977, 132: 349-51; Clark-Curtiss & Curtiss, Methods in Enzymology (Wu et al.) 1983, 101: 347-62). Например, сначала получают подходящий вектор, несущий полинуклеотид, который кодирует пептид по настоящему изобретению, в экспресирующейся форме (например, после регуляторной последовательности, соответствующей промоторной последовательности), и транформируют подходящую клетку-хозяина. Клетку-хозяина затем культивируют для получения пептида по настоящему изобретению. Пептид по настоящему изобретению также можно получать in vitro с использованием системы для трансляции in vitro.
IV. Полинуклеотиды
Настоящее изобретение также относится к полинуклеотиду, который кодирует любой из пептидов по настоящему изобретению. Он включает полинуклеотиды, полученные из природного гена FOXM1 (например, номер доступа GenBank NM_202003 (SEQ ID NO: 52), NM_001243088 (SEQ ID NO: 54), NM_001243089 (SEQ ID NO: 56), NM_021953 (SEQ ID NO: 58) или NM202002 (SEQ ID NO: 60)) а также полинуклеотиды с консервативно модифицированной нуклеотидной последовательностью. В настоящем документе, фраза «консервативно модифицированная нуклеотидная последовательность» относится к последовательностям, которые кодируют идентичные или по существу идентичные аминокислотные последовательности. Из-за вырожденности генетического кода, большое количество функционально идентичных нуклеиновых кислот кодирует любой указанный белок. Например, все кодоны GCA, GCC, GCG, и GCU кодируют аминокислоту аланин. Таким образом, в каждом положении, где кодоном определен аланин, кодон можно изменять на любой из соответствующих вышеописанных кодонов без изменения кодируемого полипептида. Такие вариации нуклеиновых кислот представляют собой «молчащие вариации», которые являются одним из видов консервативно модифицированных вариаций. Каждая последовательность нуклеиновой кислоты в настоящем документе, которая кодирует пептид, также описывает любую возможную молчащую вариацию нуклеиновой кислоты. Специалисту в данной области будет понятно, что каждый кодон в нуклеиновой кислоте (за исключением AUG, который, как правило, является единственным кодоном для метионина, и TGG, который, как правило, является единственным кодоном для триптофана) можно модифицировать для получения функционально идентичной молекулы. Таким образом, каждая молчащая вариация нуклеиновой кислоты, кодирующей пептид, неявно описана в каждой раскрытой последовательности.
Полинуклеотид по настоящему изобретению может состоять из ДНК, РНК, и их производных. ДНК соответствующим образом состоит из оснований, таких как A, T, C, и G, и T заменена на U в РНК.
Полинуклеотид по настоящему изобретению может кодировать несколько пептидов по настоящему изобретению с наличием или отсутствием между ними промежуточных аминокислотных последовательностей. Например, промежуточная аминокислотная последовательность может обеспечивать участок расщепления (например, последовательность распознавания фермента) полинуклеотида или транслированных пептидов. Кроме того, полинуклеотид может включать любые дополнительные последовательности в кодирующую последовательность, которая кодирует пептид по настоящему изобретению. Например, полинуклеотид может быть рекомбинантным полинуклеотидом, который включает регуляторные последовательности, необходимые для экспрессии пептида или может быть экспрессирующим вектором (например, плазмидой) с маркерными генами и т.п. Как правило, такие рекомбинантные полинуклеотиды можно получать путем манипуляций с полинуклеотидами путем общепринятых рекомбинантных способов при помощи, например, полимераз и эндонуклеаз.
Для получения полинуклеотидов по настоящему изобретению можно использовать и рекомбинантные способы, и способы химического синтеза. Например, полинуклеотид можно получать путем вставки в соответствующий вектор, который можно экпрессировать после трансфекции в компетентных клетках. Альтернативно, полинуклеотид можно амплифицировать при помощи способов ПЦР или экспрессии в подходящих хозяевах (см., например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, New York, 1989). Альтернативно, полинуклеотид можно синтезировать с ипользованием твердофазных способов, как описано в Beaucage SL & Iyer RP, Tetrahedron 1992, 48: 2223-311; Matthes et al., EMBO J 1984, 3: 801-5. Продукты связывания из нескольких пептидов, которые можно получать таким образом, можно очищать по мере необходимости и вводить в таком связанном состоянии. В этом случае, из связанных пептидов путем процессинга можно получать антигенпрезентирующие пептиды и выявлять ЦТЛ-индуцирующую активность каждого из пептидов. Таким образом, присвязывании пептидов предпочтительно комбинировать пептиды с одинаковым ограничением по HLA. Альтернативно, пептиды можно вводить в виде смеси отдельных пептидов, расщепляя связанную часть.
V. Экзосомы
Настоящее изобретение дополнительно относится к внутриклеточным пузырькам, обозначаемым как экзосомы, которые презентируют на своей поверхности комплексы, образованные между пептидами по настоящему изобретению и антигенами HLA. Экзосомы можно получать, например, при помощи способов, подробно описанных в JPH11-510507 и WO99/03499, и можно получать с использованием АПК, полученных от пациентов, которые являются объектами для лечения и/или предупреждения заболевания (профилактики). Экзосомы по настоящему изобретению можно прививать как вакцины, аналогичным образом, как и пептиды по настоящему изобретению.
Тип антигенов HLA, включенных в описанные выше комплексы, должен совпадать с типом у индивидуума, которому необходимо лечение и/или предупреждение заболевания (профилактика). Например, HLA-A33 (например, HLA-A*33:03) представляют собой аллели широко и повсеместно наблюдаемые в азиатских популяциях, и этот тип антигенов HLA считается подходящим для лечения азиатских пациентов. Дополнительно, HLA-A01 (например, HLA-A*01:01) представляет собой аллель HLA, часто наблюдаемый у европеоидов, и этот тип антигенов HLA считается подходящим для лечения европеоидных пациентов. Как правило, в клинической практике, за счет предварительного исследования типа антигена HLA у пациента, нуждающегося в лечении, возможно выбрать подходящий пептид, который имеет высокий уровень аффинности связывания с конкретным антигеном HLA, или который имеет способность индуцировать ЦТЛ за счет презентации антигена, опосредованной конкретным антигеном HLA.
Экзосомы по настоящему изобретению презентируют на своей поверхности комплекс пептида по настоящему изобретению и HLA-A33 или HLA-A01. Если HLA, который образует комплекс с пептидом по настоящему изобретению, представляет собой HLA-A33, пептид по настоящему изобретению предпочтительно является пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46 или его модифицированным пептидом, и, более предпочтительно, пептидом, состоящим из аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46 или его модифицированным пептидом. Дополнительно, если HLA, который образует комплекс с пептидом по настоящему изобретению, представляет собой HLA-A01, пептид по настоящему изобретению предпочтительно является пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61 или его модифицированным пептидом, и, более предпочтительно, пептидом, состоящим из аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61 или его модифицированным пептидом.
VI. Антигенпрезентирующие клетки (АПК)
Настоящее изобретение дополнительно относится к АПК, которые презентируют на своей поверхности комплексы, образованные между антигенами HLA и пептидами по настоящему изобретению. Альтернативно, настоящее изобретение относится к АПК, имеющим на своей клеточной поверхности комплексы, образованные между антигенами HLA и пептидами по настоящему изобретению. АПК по настоящему изобретению могут быть изолированными АПК. При применении в отношении клетки (АПК, ЦТЛ, и т.д.), термин «изолированный» означает, что клетки отделены от другого типа клеток. АПК по настоящему изобретению могут быть АПК, индуцированными из АПК, полученных от пациента, которого собираются подвергать лечению и/или предупреждению (профилактике), и их можно вводить в виде вакцины сами по себе или в комбинации с другими лекарственными средствами, включая пептид(-ы), экзосому/экзосомы или ЦТЛ по настоящему изобретению.
АПК по настоящему изобретению не ограничиваются конкретным типом клеток, и могут быть клетками, о которых известно, что они презентируют белковые антигены на своей клеточной поверхности таким образом, что они распознаются лимфоцитами, например, дендритные клетки (DC), клетки Лангерганса, макрофаги, B-клетки, и активированные T-клетки. Поскольку DC является типичной АПК, которая имеет самую сильную способность индуцировать ЦТЛ среди АПК, DC могут быть предпочтительно использованы в качестве АПК по настоящему изобретению. В настоящем изобретении, предпочтительная DC является изолированной DC, полученной от человека. Дополнительно, АПК по настоящему изобретению могут также представлять собой смеси нескольких типов клеток с антиген-презентирующей функцией и могут быть смесями АПК, каждая из которых презентирует различные типы пептидов по настоящему изобретению.
Например, АПК по настоящему изобретению можно получать, выделяя DC из мононуклеарных клеток периферической крови, а затем стимулируя их in vitro, ex vivo или in vivo пептидами по настоящему изобретению. Когда пептид по настоящему изобретению вводят индивидууму, АПК, презентирующие пептид по настоящему изобретению, индуцируются в организме индивидуума. Таким образом, после того как пептиды по настоящему изобретению вводят индивидууму, можно получать АПК по настоящему изобретению путем забора АПК от индивидуума. Альтернативно, АПК по настоящему изобретению можно получать путем контакта АПК, собранных у индивидуума, с пептидом по настоящему изобретению.
Для того чтобы индуцировать иммунный ответ против FOXM1-экспрессирующих злокачественных клеток у индивидуума, АПК по настоящему изобретению можно вводить индивидууму сами по себе или в комбинации с другими лекарственными средствами, включая пептид(-ы), экзосому/экзосомы или ЦТЛ по настоящему изобретению. Например, введение ex vivo может включать следующие этапы:
(a) забор АПК у первого индивидуума;
(b) контакт АПК из этапа (a) с пептидом; и
(c) введение АПК из этапа (b) второму индивидууму.
Первый индивидуум и второй индивидуум могут быть одним и тем же индивидуумом, или могут быть разными индивидуумами. Когда первый индивидуум и второй индивидуум являются разными индивидуумами, предпочтительно, что HLA первого индивидуума и второго индивидуума представляют собой HLA одного типа. АПК, полученные на вышеописанном этапе (b), могут быть вакциной для лечения злокачественной опухоли и/или предупреждения заболевания (профилактики).
АПК по настоящему изобретению, полученные вышеописанным способом, имеют способность индуцировать ЦТЛ. Термин «способность индуцировать ЦТЛ (индуцибельность ЦТЛ)», применяемый в отношении АПК, относится к способности АПК индуцировать ЦТЛ при контакте с CD8-положительной T-клеткой/клетками. Дополнительно, «способность индуцировать ЦТЛ (индуцибельность ЦТЛ)» включает способность АПК индуцировать активацию ЦТЛ, способность АПК индуцировать пролиферацию ЦТЛ, способность АПК способствовать опосредованному ЦТЛ разрушению клеток-мишеней, и способность АПК повышать опосредованную ЦТЛ выработку IFN-гамма. ЦТЛ, индуцированная АПК по настоящему изобретению, представляет собой ЦТЛ, специфичную к FOXM1, и демонстрирует специфическую цитотоксическую активность против FOXM1-экспрессирующих клеток.
В дополнение к вышеописанным способам, АПК по настоящему изобретению можно получать путем введения полинуклеотида, кодирующего пептид по настоящему изобретению, в АПК in vitro. Вводимый полинуклеотид может быть в форме ДНК или РНК. Способ введения конкретно не ограничен, и его примеры включают различные способы, применяемые обычно в данной области, такие как липофекция, электропорация и способ с фосфатом кальция. Более конкретно, можно использовать способы, описанные в Cancer Res 1996, 56: 5672-7; J Immunol 1998, 161: 5607-13; J Exp Med 1996, 184: 465-72 и JP2000-509281. За счет введения полинуклеотида, кодирующего пептид по настоящему изобретению, в АПК, полинуклеотид транскрибируется и транслируется в клетке, а затем произведенный пептид процессируется MHC класса I и проходит через путь презентации пептида по настоящему изобретению на клеточной поверхности АПК.
В предпочтительном варианте осуществления АПК по настоящему изобретению презентирует на своей клеточной поверхности комплекс, образованный между пептидом по настоящему изобретению и HLA-A33 (более предпочтительно HLA-A*33:03) или HLA-A01 (более предпочтительно HLA-A*01:01). Если HLA, который образует комплекс с пептидом по настоящему изобретению, представляет собой HLA-A33, пептид по настоящему изобретению предпочтительно является пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 или 46 или его модифицированным пептидом, и, более предпочтительно, пептидом, состоящим из аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46. Если HLA, который образует комплекс с пептидом по настоящему изобретению, представляет собой HLA-A01, пептид по настоящему изобретению предпочтительно является пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61 или его модифицированным пептидом, и, более предпочтительно, пептидом, состоящим из аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 and 61.
АПК по настоящему изобретению предпочтительно представляет собой АПК, индуцированную способом, включающим этап, описанный (a) или (b) ниже:
(a) контакт АПК, экспрессирующей, по меньшей мере, один HLA, выбранный из HLA-A33 (более предпочтительно HLA-A*33:03) или HLA-A01 (более предпочтительно HLA-A*01:01) с пептидом по настоящему изобретению; или
(b) введение полинуклеотида, кодирующего пептид по настоящему изобретению, в АПК, экспрессирующую, по меньшей мере, один HLA, выбранный из HLA-A33 (более предпочтительно HLA-A*33:03) или HLA-A01 (более предпочтительно HLA-A*01:01).
Пептид по настоящему изобретению, который контактирует с HLA-A33-экспрессирующей/экспрессирующими АПК, предпочтительно представляет собой пептид, имеющий аминокислотную последовательность, выбранную из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46 или его модифицированный пептид, и более предпочтительно пептид, состоящий из аминокислотной последовательности, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46.
Пептид по настоящему изобретению, который контактирует с HLA-A01-экспрессирующей/экспрессирующими АПК, предпочтительно представляет собой пептид имеющий аминокислотную последовательность, выбранную из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61 или его модифицированный пептид, и более предпочтительно пептид, состоящий из аминокислотной последовательности, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61.
Настоящее изобретение относится к применению пептида по настоящему изобретению для получения фармацевтической композиции, которая индуцирует АПК со способностью индуцировать ЦТЛ. Кроме того, настоящее изобретение относится к способу или процессу производства фармацевтической композиции, которая индуцирует АПК со способностью индуцировать ЦТЛ. Дополнительно, настоящее изобретение относится к пептиду по настоящему изобретению для индуцирования АПК со способностью индуцировать ЦТЛ.
VII. Цитотоксические T-лимфоциты (ЦТЛ)
ЦТЛ, индуцированные пептидом по настоящему изобретению можно использовать в качестве вакцины аналогичным образом, как и пептид по настоящему изобретению, для усиления in vivo иммунного ответа, нацеленного на FOXM1-экспрессирующую раковую клетку. Таким образом, настоящее изобретение относится к ЦТЛ, которые индуцируются или активируются пептидом по настоящему изобретению. ЦТЛ по настоящему изобретению представляют собой ЦТЛ, которые нацелены на пептид по настоящему изобретению, и способны к связыванию с комплексом пептида по настоящему изобретению и антигена HLA. Связывание ЦТЛ с комплексом опосредуется через T-клеточный рецептор (TCR), присутствующий на клеточной поверхности ЦТЛ. ЦТЛ по настоящему изобретению могут быть изолированными ЦТЛ. Предпочтительные ЦТЛ представляют собой изолированные ЦТЛ человеческого происхождения. ЦТЛ по настоящему изобретению могут также представлять собой смеси ЦТЛ, каждая из которых нацелена на различные типы пептидов по настоящему изобретению.
ЦТЛ по настоящему изобретению можно получать путем (1) введения пептидов по настоящему изобретению индивидууму, (2) стимулирования АПК и CD8-положительных T-клеток, или мононуклеарных клеток периферической крови (PBMC),полученных от индивидуума, пептидом по настоящему изобретению in vitro, (3) контакта CD8-положительных T-клеток или PBMC с АПК или экзосомами, которые презентируют на своей поверхности комплекс антигена HLA и пептида по настоящему изобретению, in vitro, или (4) введения в CD8-положительные T-клетки вектора, содержащего полинуклеотид, кодирующий каждую субъединицу T-клеточного рецептора (TCR), способного связываться с пептидом по настоящему изобретению, презентированным на клеточной поверхности посредством антигена HLA. Экзосомы и АПК, применяемые в способе (2) или (3) выше, можно получать путем способов, описанных в разделах «V. Экзосомы» и «VI. Антигенпрезентирующие клетки (АПК)», соответственно, а подробности способа (4) выше будут описаны в разделе «VIII. T-клеточный рецептор (TCR)».
ЦТЛ по настоящему изобретению можно вводить сами по себе пациентам, которые подвергаются лечению и/или предупреждению (профилактике), или в комбинации с другими лекарственными средствами, включая пептид(-ы), АПК или экзосому/экзосомы по настоящему изобретению с целью регулирования воздействий. Дополнительно, ЦТЛ по настоящему изобретению могут быть ЦТЛ, индуцированными из CD8-положительных T-клеток, полученных от пациентов, которым предполагается вводить ЦТЛ. ЦТЛ по настоящему изобретению действуют специфически на клетки-мишени, которые презентируют пептиды по настоящему изобретению, например, те же самые пептиды, которые использовали для индуцирования ЦТЛ по настоящему изобретению. Клетки-мишени могут быть клетками, которые эндогенно экспрессируют FOXM1, такими как злокачественные клетки, или клетки, трансфецированные геном FOXM1. Клетки, которые презентируют пептид по настоящему изобретению на своей клеточной поверхности из-за стимулирования пептидом, могут становиться мишенью для атаки ЦТЛ по настоящему изобретению. Клетки, являющиеся мишенями для ЦТЛ по настоящему изобретению, предпочтительно являются клетками, которые положительны, по меньшей мере, по одному из HLA-A33 (более предпочтительно HLA-A*33:03) и HLA-A01 (более предпочтительно HLA-A*01:01).
В предпочтительном варианте осуществления ЦТЛ по настоящему изобретению специфически нацелены на клетки, которые экспрессируют и FOXM1, и, по меньшей мере, один HLA, выбранный из HLA-A33 (более предпочтительно HLA-A*33:03) и HLA-A01 (более предпочтительно HLA-A*01:01). В настоящем изобретении, клетки, являющиеся мишенями для ЦТЛ, могут быть клетками, которые имеют любые из аллелей HLA-A33 и HLA-A01 в гомозиготном или гетерозиготном состоянии.
В настоящем документе, то, что ЦТЛ «нацелен на» клетки, относится к распознаванию ЦТЛ клеток, которые презентируют на своей клеточной поверхности комплекс HLA и пептида по настоящему изобретению, и демонстрации цитотоксической активности против клеток. Дополнительно, «специфически нацелен на» относится к тому, что ЦТЛ демонстрирует цитотоксическую активность против таких клеток, но не демонстрирует повреждающей активности по отношению к другим клеткам. Выражение «распознавать клетки», применяемое в отношении ЦТЛ, относится к связыванию с комплексом HLA и пептида по настоящему изобретению, презентированным на клеточной поверхности, через TCR, и к демонстрации цитотоксической активности против клеток. Таким образом, ЦТЛ по настоящему изобретению предпочтительно является ЦТЛ, который может связываться через TCR с комплексом, образованным между пептидом по настоящему изобретению и HLA-A33 (более предпочтительно HLA-A*33:03) и HLA-A01 (более предпочтительно HLA-A*01:01), презентированным на клеточной поверхности.
Кроме того, ЦТЛ по настоящему изобретению предпочтительно являются ЦТЛ, индуцированными способом, включающим этап, описанный в (a) или (b) ниже:
(a) контакт in vitro CD8-положительных T-клеток с АПК или экзосомами, которые презентируют на своей поверхности комплекс пептида по настоящему изобретению и HLA-A33 (более предпочтительно HLA-A*33:03) и HLA-A01 (более предпочтительно HLA-A*01:01); или
(b) введение в CD8-положительные T-клетки полинуклеотида, кодирующего каждую субъединицу TCR, способного связываться с пептидом по настоящему изобретению, презентированным на клеточной поверхности посредством HLA-A33 (более предпочтительно HLA-A*33:03) и HLA-A01 (более предпочтительно HLA-A*01:01). ЦТЛ, индуцированные таким способом, представляют собой клетки с TCR, которые специфически распознают комплекс пептида и антигена HLA, использованный для индукции. Таким образом, они представляют собой клетки со структурным отличием от других ЦТЛ, которые имеют отличающуюся специфичность реакции из-за различий в структуре TCR.
VIII. T-клеточные рецепторы (TCR)
Настоящее изобретение также относится к композициям, содержащим полинуклеотид, кодирующий каждую субъединицу TCR, способного связываться с пептидом по настоящему изобретению, который презентирован на клеточной поверхности при помощи антигена HLA, и к способам применения таких композиций. Полинуклеотид наделяет CD8-положительные T-клетки специфичностью против FOXM1-экспрессирующих злокачественных клеток за счет экспрессии TCR на поверхности CD8-положительных T-клеток, способного связываться с пептидом по настоящему изобретению, который презентирован на поверхности клетки-мишени при помощи антигена HLA. Полинуклеотиды, кодирующие альфа цепь/цепи и бета цепь/цепи, можно идентифицировать как субъединицу TCR ЦТЛ, индуцированных пептидом по настоящему изобретению, с применением способов, известных в данной области (WO2007/032255 и Morgan et al., J Immunol, 171, 3288 (2003)). Например, для анализа TCR предпочтительными являются способы ПЦР. Не ограничиваясь нижеописанными, праймеры для ПЦР для анализа могут быть, например, набором/наборами праймеров для амплификации путем комбинирования 5'-концевого праймера и 3'-концевого праймера/праймеров ниже:
5'-концевой праймер:
5'-R праймер (5'-gtctaccaggcattcgcttcat-3') (SEQ ID NO: 62)
3'-концевой праймер:
Специфичный к области С альфа-цепи TCR
3-TRa-C праймер (5'-tcagctggaccacagccgcagcgt-3') (SEQ ID NO: 63)
Специфичный к области С1 бета-цепи TCR
3-TRb-C1 праймер (5'-tcagaaatcctttctcttgac-3') (SEQ ID NO: 64) или
Специфичный к области С2 бета-цепи TCR
3-TR-бета-C2 праймер (5'-ctagcctctggaatcctttctctt-3') (SEQ ID NO: 65)
TCR, образованные за счет введения идентифицированных полинуклеотидов в CD8-положительные T-клетки, могут связываться с высокой аффинностью связывания с клетками-мишенями, которые презентируют пептид по настоящему изобретению, и опосредовать эффективный лизис клеток-мишеней, презентирующих пептид по настоящему изобретению, in vivo и in vitro.
Полинуклеотид, кодирующий каждую субъединицу TCR, можно вставлять в подходящий вектор, например, ретровирусный вектор. Эти векторы хорошо известны в данной области. Полинуклеотид или вектор, содержащий его в экспрессируемой форме, можно вводить в CD8-положительную T-клетку, например, CD8-положительную T-клетку, полученную от пациента. Настоящее изобретение относится к готовым композициям, которые позволяют легко и быстро получить модифицированные T-клетки, имеющие превосходные свойства лизиса злокачественных клеток, за счет быстрой модификации собственных Т-клеток пациента (или T-клеток, полученных от другого индивидуума).
В настоящем документе, специфический TCR представляет собой TCR, который может придавать специфическую цитотоксическую активность против клеток-мишеней за счет специфического распознавания комплекса пептида по настоящему изобретению и антигена HLA, презентированного на поверхности клеток-мишеней, при этом TCR присутствует на поверхности CD8-положительной T-клетки. Специфическое распознавание вышеописанного комплекса можно подтверждать любым известным способом, и предпочтительные примеры способов включают анализ окрашивания мультимеров HLA с использованием молекул HLA и пептидов по настоящему изобретению, и способы анализа иммуноферментных пятен (ELISPOT). Специфическое, опосредованное TCR, распознавание клетки-мишени Т-клеткой, в которую был введен вышеописанный полинуклеотид, и передачу сигнала в клетке можно подтверждать, проводя анализ ELISPOT. Когда вышеописанный TCR присутствует на поверхности CD8-положительной T-клетки, может ли он наделять CD8-положительную T-клетку специфической цитотоксической активностью против клетки-мишени можно также подтверждать известными способами. Предпочтительные способы включают, например, измерение цитотоксической активности против клеток-мишеней при помощи анализа высвобождения хрома или т.п.
Настоящее изобретение в отношении HLA-A33 относится к ЦТЛ, полученным путем трансформации CD8-положительных T-клеток полинуклеотидом, кодирующим каждую субъединицу TCR, которая связывается, например, с комплексом, образованным пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, и антигеном HLA-A33.
Настоящее изобретение в отношении HLA-A01 относится к ЦТЛ, полученным путем трансформации CD8-положительных T-клеток полинуклеотидом, кодирующим каждую субъединицу TCR, которая связывается, например, с комплексом, образованным пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NOs: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61, и антигеном HLA-A01.
Трансформированные ЦТЛ способны к хоумингу (перемещению лимфоцитов из крови в лимфатические ткани) in vivo и могут быть выращены при помощи хорошо известного способа культивирования in vitro (например, Kawakami et al., J Immunol., 1989, 142: 3252-61). ЦТЛ по настоящему изобретению можно использовать для получения иммуногенной композиции, подходящей для лечения заболевания или предупреждения заболевания (профилактики) у пациента, нуждающегося в лечении или предупреждении заболевания (профилактике) (содержание включено в настоящий документ в виде ссылки WO2006/031221).
IX. Фармацевтические композиции
Настоящее изобретение дополнительно относится к композициям или фармацевтическим композициям, содержащим, по меньшей мере, один активный ингредиент, выбранный из нижеизложенных:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК по настоящему изобретению;
(d) экзосома по настоящему изобретению; и
(e) ЦТЛ по настоящему изобретению.
Фармацевтические композиции по настоящему изобретению могут содержать по мере необходимости носитель/носители, эксципиент (-ы) или т.п., широко используемые в фармацевтических препаратах без конкретных ограничений, в дополнение к вышеописанному активному ингредиенту/ингредиентам. Примеры носителя, который можно использовать в фармацевтической композиции по настоящему изобретению, относятся к стерилизованной воде, физиологическому раствору, фосфатному буферу, культуральной жидкости и т.п. Таким образом, настоящее изобретение также относится к фармацевтическим композициям, содержащим, по меньшей мере, один активный ингредиент, выбранный из нижеизложенных от (a) до (e), и фармацевтически приемлемый носитель:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК по настоящему изобретению;
(d) экзосома по настоящему изобретению; и
(e) ЦТЛ по настоящему изобретению.
Дополнительно, фармацевтические композиции по настоящему изобретению могут содержать, по мере необходимости, стабилизаторы, суспензии, консерванты, поверхностно-активные вещества, солюбилизаторы, регуляторы pH, ингибиторы агрегации и т.п.
Экспрессия FOXM1 значительно повышена в злокачественных клетках по сравнению с нормальными тканями. Таким образом, пептид по настоящему изобретению или полинуклеотид, кодирующий пептид, можно использовать для лечения и/или профилактики злокачественной опухоли, и/или профилактики ее послеоперационного рецидива. Таким образом, настоящее изобретение относится к фармацевтическим композициям для лечения и/или профилактики злокачественной опухоли, и/или профилактики ее послеоперационного рецидива, содержащим один или несколько типов пептидов или полинуклеотидов по настоящему изобретению в качестве активного ингредиента. Альтернативно, пептиды по настоящему изобретению можно производить для презентирования на поверхности экзосом или АПК для применения в качестве фармацевтических композиций. Кроме того, ЦТЛ по настоящему изобретению, нацеленный на любой один из пептидов по настоящему изобретению, также можно использовать в качестве активного ингредиента фармацевтических композиций по настоящему изобретению. Фармацевтические композиции по настоящему изобретению могут содержать терапевтически эффективное количество или фармацевтически эффективное количество вышеописанного активного ингредиента.
Фармацевтические композиции по настоящему изобретению также можно использовать в качестве вакцины. В контексте настоящего изобретения, термин «вакцина» (также называемая «иммуногенная композиция») относится к композициям, которые имеют функцию индуцирования иммунного ответа, приводящего к противоопухолевому действию при введении животному. Таким образом, фармацевтическую композицию по настоящему изобретению можно использовать для индуцирования иммунного ответа, приводящего к противоопухолевому действию у индивидуума. Иммунный ответ, индуцируемый пептидом, полинуклеотидом, АПК, ЦТЛ и фармацевтической композицией по настоящему изобретению, конкретно не ограничен при условии, что он является иммунным ответом, который приводит к противоопухолевому действию, и примеры включают индуцирование ЦТЛ, специфичных к злокачественным клеткам, и индуцирование специфической цитотоксической активности против злокачественных клеток.
Фармацевтические композиции по настоящему изобретению можно использовать для лечения и/или профилактики злокачественной опухоли, и/или профилактики ее послеоперационного рецидива у человеческих индивидуумов или пациентов. Фармацевтические композиции по настоящему изобретению можно использовать предпочтительно индивидууму, положительному, по меньшей мере, по одному HLA, выбранному из HLA-A33 и HLA-A01. Дополнительно, фармацевтические композиции по настоящему изобретению можно использовать предпочтительно для лечения и/или профилактики злокачественных опухолей, экспрессирующих FOXM1 и, по меньшей мере, один HLA, выбранный из HLA-A33 и HLA-A01, и/или для профилактики их послеоперационного рецидива.
В другом варианте осуществления настоящее изобретение относится к применению активного ингредиента, выбранного из нижеуказанных, в производстве фармацевтической композиции для лечения или профилактики злокачественной опухоли:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
Альтернативно, настоящее изобретение дополнительно относится к активному ингредиенту, выбранному из нижеуказанных, для применения в лечении или профилактике злокачественной опухоли:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
Альтернативно, настоящее изобретение дополнительно относится к способу или процессу для производства фармацевтической композиции для лечения или профилактики злокачественной опухоли, где способ или процесс включает этап формулирования, по меньшей мере, одного активного ингредиента, выбранного из нижеуказанных, с фармацевтически или физиологически приемлемым носителем:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
В другом варианте осуществления настоящее изобретение дополнительно относится к способу или процессу для производства фармацевтической композиции для лечения или профилактики злокачественной опухоли, где способ или процесс включает этап смешивания активного ингредиента, выбранного из нижеуказанных, с фармацевтически или физиологически приемлемым носителем:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
В другом варианте осуществления настоящее изобретение дополнительно относится к способу лечения или профилактики злокачественной опухоли, который включает этап введения индивидууму, по меньшей мере, одного активного ингредиента, выбранного из нижеуказанных:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
В настоящем изобретении, пептид с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46 идентифицирован как эпитопный пептид, рестриктированный по HLA-A33, который может индуцировать мощный и специфический иммунный ответ. Таким образом, фармацевтические композиции по настоящему изобретению, содержащие, по меньшей мере, один из пептидов с аминокислотной последовательностью, выбранной из SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46 являются подходящими, в частности для введения индивидууму с HLA-A33 (например, HLA-A*33:03) в качестве антигена HLA. То же самое относится и к фармацевтическим композициям, содержащим полинуклеотид, кодирующий любые из этих пептидов (т.е., полинуклеотиды по настоящему изобретению), АПК или экзосому, которые презентируют эти пептиды (т.е., АПК или экзосомы по настоящему изобретению), или ЦТЛ, нацеленный на эти пептиды (т.е., ЦТЛ по настоящему изобретению). То есть, фармацевтические композиции, содержащие активный ингредиент в сочетании с пептидом с аминокислотной последовательностью, выбранной из SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46 являются подходящими для введения индивидуумам с HLA-A33 (т.е., HLA-A33-положительным индивидуумам). В более предпочтительном варианте осуществления фармацевтическая композиция по настоящему изобретению представляет собой фармацевтическую композицию, которая содержит пептид с аминокислотной последовательностью из SEQ ID NO: 2.
Аналогично, в настоящем изобретении, пептиды с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61 идентифицированы как эпитопные пептиды, рестриктированные по HLA-A01, которые могут индуцировать мощный и специфический иммунный ответ. Таким образом, фармацевтические композиции по настоящему изобретению, содержащие, по меньшей мере, один из пептидов с аминокислотной последовательностью, выбранной из числа SEQ ID NOs: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61 являются подходящими, в частности для введения индивидууму с HLA-A01 (например, HLA-A*01:01) в качестве антигена HLA. То же самое относится и к фармацевтическим композициям, содержащим полинуклеотид, кодирующий любые из этих пептидов (т.е., полинуклеотиды по настоящему изобретению), АПК или экзосому, которые презентируют эти пептиды (т.е., АПК или экзосомы по настоящему изобретению), или a ЦТЛ, нацеленный на эти пептиды (т.е., ЦТЛ по настоящему изобретению). То есть, фармацевтические композиции, содержащие активный ингредиент в сочетании с пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61 являются подходящими для введения индивидуумам с HLA-A01 (т.е., HLA-A01-положительным индивидуумам). В более предпочтительном варианте осуществления фармацевтическая композиция по настоящему изобретению представляет собой фармацевтическую композицию, которая содержит пептид с аминокислотной последовательностью из SEQ ID NO: 56.
Злокачественные опухоли для лечения и/или профилактики при помощи фармацевтических композиций по настоящему изобретению конкретно не ограничены при условии, что они являются злокачественными опухолями, экспрессирующими FOXM1, и включают различные злокачественные опухоли, например, острый миелоидный лейкоз, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, хронический миелолейкоз (ХМЛ), рак толстого кишечника, рак пищевода, рак желудка, диффузный рак желудка, немелкоклеточный рак легких (NSCLC), лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак почки, мелкоклеточный рак легких (SCLC), опухоль мягких тканей, рак яичка и т.п. Помимо этого, фармацевстические композиции по настоящему изобретению могут быть предпочтительно использованы для индивидуумов, которые имеют аллель HLA в гомозиготном или гетерозиготном состоянии, выбранный из числа HLA-A33 и HLA-A01.
В дополнение к активным ингредиентам, описанным выше, фармацевтические композиции по настоящему изобретению могут содержать другие пептиды, которые имеют способность индуцировать ЦТЛ против злокачественных клеток (например, другие пептиды, полученные из TAA и индуцирующие ЦТЛ), другие полинуклеотиды, кодирующие другие пептиды, другие клетки, которые презентируют другие пептиды, или т.п.
Фармацевтические композиции по настоящему изобретению могут также необязательно содержать другие терапевтические вещества в качестве активного ингредиента, при условии, что они не ингибируют противоопухолевые воздействия вышеписанных активных ингредиентов, таких как пептиды по настоящему изобретению. Например, фармацевтические композиции по настоящему изобретению необязательно могут содержать противовоспалительные композиции, анальгетики, химиотерапевтические препараты и т.п. В дополнение к включению других терапевтических веществ в фармацевтическую композицию по настоящему изобретению, можно также вводить фармацевтическую композицию по настоящему изобретению последовательно или одновременно с одной или несколькими другими фармацевтическими композициями. Доза фармацевтической композиции по настоящему изобретению и других фармацевтических композиций зависит, например, от типа применяемой фармацевтической композиции и заболевания, которое лечат, а также от режима и путей введения.
Следует понимать, что с учетом типа состава, фармацевтическая композиция по настоящему изобретению может включать другие компоненты, общепринятые в данной области, в дополнение к ингредиентам, конкретно упомянутым в настоящем документе.
Настоящее изобретение также относится к промышленным изделиям или наборам, которые содержат фармацевтическую композицию по настоящему изобретению. Промышленные изделия или наборы по настоящему изобретению могут включать контейнер, который содержит фармацевтическую композицию по настоящему изобретению. Пример подходящего контейнера включает бутылку, флакон или пробирку, но не ограничивается ими. Контейнер может быть сделан из различных материалов, таких как стекло или пластик. К контейнеру может быть присоединена этикетка, и на этикетке может быть описано заболевание или состояние болезни, для которого должна быть использована фармацевтическая композиция по настоящему изобретению. Этикетка может также содержать указания для введения и т.п.
Промышленные изделия или наборы по настоящему изобретению могут дополнительно включать второй контейнер, который содержит фармацевтически приемлемые разбавители, необязательно, в дополнение к контейнеру, который содержит фармацевтическую композицию по настоящему изобретению. Промышленные изделия или наборы по настоящему изобретению могут дополнительно содержать другие материалы, необходимые с коммерческой точки зрения и с точки зрения пользователя, такие как другие буферы, разбавители, фильтры, иглы для инъекций, шприцы и вкладыши в упаковку с инструкциями по применению.
По мере необходимости, фармацевтическую композицию по настоящему изобретению можно предоставлять в упаковке или в дозаторном устройстве, которые могут содержать одну или несколько единиц лекарственных форм, содержащих активные ингредиенты. Упаковка может включать, например, металлическую пленку или полимерную пленку, такую как блистерная упаковка. Инструкции для введения могут быть прикреплены к упаковке или к дозаторному устройству.
(1) Фармацевтические композиции, содержащие пептид(-ы) в качестве активного ингредиента
Фармацевтическую композицию, содержащую пептид по настоящему изобретению можно формулировать путем общепринятых способов рецептуры по мере необходимости. Фармацевтические композиции по настоящему изобретению могут включать по мере необходимости в дополнение к пептиду по настоящему изобретению, носители, эксципиенты и т.п., широко используемые в фармацевтических препаратах без конкретных ограничений. Примеры носителей, которые можно использовать в фармацевтических композициях по настоящему изобретению включают стерилизованную воду (например, воду для инъекций), физиологический раствор, фосфатный буфер, фосфатно-солевой буфер, физиологический раствор, забуференный Трисом, 0,3% глицин, культуральную жижкость, и т.п. Дополнительно, фармацевтические композиции по настоящему изобретению могут содержать по мере необходимости стабилизаторы, суспензии, консерванты, поверхностно-активные вещества, солюбилизаторы, регуляторы pH, ингибиторы агрегации, и т.п. Фармацевтические композиции по настоящему изобретению могут индуцировать специфический иммунитет против FOXM1-экспрессирующих злокачественных клеток, и, таким образом, их можно применять с целью лечения злокачественных опухолей или предупреждения (профилактики) злокачественных опухолей.
Например, фармацевтические композиции по настоящему изобретению можно получать путем растворения в фармацевтически или физиологически приемлемых водорастворимых носителях, таких как стерилизованная вода (например, вода для инъекций), физиологический раствор, фосфатный буфер, фосфатно-солевой буфер, физиологический раствор, забуференный Трисом, и добавления, по мере необходимости, стабилизаторов, суспензий, консервантов, поверхностно-активных веществ, солюбилизаторов, регуляторов pH, ингибиторов агрегации, и т.п., а затем стерилизации раствора пептида. Способ стерилизации раствора пептида конкретно не ограничен, и предпочтительно проводится путем стерилизации фильтрацией. Стерилизацию фильтрацией можно проводить при помощи, например, фильтра для стерилизации фильтрацией 0,22 мкм или менее по диаметру пор. Раствор пептида, стерилизованный фильтрацией, можно вводить индивидууму, например, в виде инъекции, не ограничиваясь ею.
Фармацевтические композиции по настоящему изобретению можно получать в виде лиофилизированного состава путем лиофильного высушивания вышеописанного раствора пептида. Лиофилизированный состав можно получать путем заполнения раствором пептида, приготовленным, как описано выше, подходящего контейнера, такого как ампула, флакон или пластиковый контейнер, с последующей лиофильной сушкой и инкапсуляцией в контейнер с промытой стерилизованной резиновой пробкой или т.п. после восстановления давления. Лиофилизированный состав можно вводить индивидууму после повторного растворения в фармацевтически или физиологически приемлемых водорастворимых носителях, таких как стерилизованная вода (например, вода для инъекций), физиологический раствор, фосфатный буфер, фосфатно-солевой буфер, физиологический раствор, забуференный Трисом, и т.п., перед введением. Предпочтительные примеры фармацевтических композиций по настоящему изобретению включают инъекции такого стерилизованного фильтрацией раствора пептида, и лиофилизированные составы, которые получают из лиофилизированного раствора пептида. Настоящее изобретение дополнительно включает наборы, содержащие такой лиофилизированный состав и раствор для повторного растворения. Настоящее изобретение также включает наборы, содержащие контейнер, который содержит лиофилизированный состав, который представляет собой фармацевтическую композицию по настоящему изобретению, и контейнер, который содержит раствор для его повторного растворения.
Фармацевтические композиции по настоящему изобретению могут включать комбинацию двух или более типов пептидов по настоящему изобретению. Комбинация пептидов может быть в форме коктейля из смешанных пептидов, или они могут быть конъюгированы друг с другом стандартными способами. Например, пептиды могут быть химически связаны или могут экспрессироваться в виде последовательностей одиночного слитого полипептида. За счет введения пептида по настоящему изобретению, пептид с высокой плотностью презентируется на АПК при помощи антигена HLA, а затем ЦТЛ, которые специфически реагируют с комплексом, образованным между презентируемым пептидом и антигеном HLA, индуцируются. Альтернативно, АПК (например, DC) забирают у индивидуума, и затем стимулируют пептидами по настоящему изобретению для получения АПК, которые презентируют любой из пептидов по настоящему изобретению на своей клеточной поверхности. Эти АПК повторно вводят индивидууму для индуцирования ЦТЛ у индивидуума, и в результате, повышается их агрессивность по отношению к FOXM1-экспрессирующим злокачественным клеткам.
Фармацевтические композиции по настоящему изобретению могут также содержать адъювант, известный эффективным формированием клеточного иммунитета. Адъювант относится к соединению, которое усиливает иммунный ответ против антигена и которое имеет иммунологическую активность при введении вместе (или последовательно) с антигеном. Можно использовать известные адъюванты, описанные в литературе, например, Clin Microbiol Rev 1994, 7: 277-89. Примеры подходящего адъюванта включают соли алюминия (фосфат алюминия, гидроксид алюминия, алюминий оксигидроксид и т.п.), квасцы, холерный токсин, токсин сальмонеллы, неполный адъювант Фрейнда (IFA), полный адъювант Фрейнда (CFA), ISCOMatrix, GM-CSF и другие иммуностимулирующие цитокины, олигодезоксинуклеотид, содержащий мотив CpG (CpG7909 и т.п.), эмульсии «масло-в-воде», сапонин или его производные (QS21 и т.п.), липополисахарид, такой как липид A или его производные (MPL, RC529, GLA, E6020 и т.п.), липопептиды, лактоферрин, флагеллин, двухцепочечную РНК или ее производные (poly I:C и т.п.), бактериальную ДНК, имидазохинолины (имиквимод, R848 и т.п.), лиганд лектина С-типа (трегалоза-6,6'-дибегенат (TDB) и т.п.), лиганд CD1d (альфа-галактозилцерамид и т.п.), скваленовые эмульсии (MF59, AS03, AF03 и т.п.), PLGA, и т.п., не ограничиваясь указанными.
Адъювант может находиться в другом контейнере отдельно от фармацевтической композиции, содержащей пептид по настоящему изобретению, в наборах, содержащих фармацевтическую композицию по настоящему изобретению. В этом случае, адъювант и фармацевтическую композицию можно вводить индивидууму последовательно, или смешивать друг с другом непосредственно перед введением индивидууму. Такие наборы, содержащие фармацевтическую композицию, включающую пептид по настоящему изобретению и адъювант, также предусмотрены настоящим изобретением. Когда фармацевтическая композиция по настоящему изобретению представляет собой лиофилизированный состав, набор может дополнительно содержать раствор для повторного растворения. Дополнительно, настоящее изобретение относится к наборам, содержащим контейнер, который содержит фармацевтическую композицию по настоящему изобретению и контейнер, который содержит адъювант. Набор может дополнительно содержать по мере необходимости контейнер, который содержит раствор для повторного растворения.
Когда в качестве адъюванта используют масляный адъювант, фармацевтическую композицию по настоящему изобретению можно получать в виде эмульсии. Эмульсии можно получать, например, путем смешивания и перемешивания раствора пептида, приготовленного, как описано выше, и масляного адъюванта. Раствор пептида может быть раствором, который был восстановлен после лиофилизации. Эмульсия может быть или типа «вода в масле», или типа «масло в воде», и эмульсия типа «вода в масле» является предпочтительной для получения высокоэффективного усиленного иммунного ответа. В качестве масляного адъюванта может быть предпочтительно использован IFA, без ограничений упомянутым. Получение эмульсии можно проводить непосредственно перед введением индивидууму, и в этом случае, фармацевтическая композиция по настоящему изобретению может быть предоставлена в виде набора, содержащего раствор пептида по настоящему изобретению и масляный адъювант. Когда фармацевтическая композиция по настоящему изобретению представляет собой лиофилизированный состав, набор может дополнительно содержать раствор для повторного растворения.
Дополнительно, фармацевтическая композиция по настоящему изобретению может быть составом с липосомами, в которые инкапсулирован пептид по настоящему изобретению, гранулярным составом, в котором пептид связан с гранулами несколько микрометров в диаметре, или составом, в котором липид связан с пептидом.
В другом варианте осуществления настоящего изобретения пептид по настоящему изобретению также можно вводить в форме фармацевтически приемлемой соли. Предпочтительные примеры солей включают соли со щелочными металлами (литием, калием, натрием и т.п.), соли со щелочноземельными металлами (кальцием, магнием и т.п.), соли с другими металлами (медью, железом, цинком, марганцем и т.п.), соли с органическими основаниями, соли с аминами, соли с органическими кислотами (уксусной кислотой, муравьиной кислотой, пропионовой кислотой, фумаровой кислотой, малеиновой кислотой, янтарной кислотой, винной кислотой, лимонной кислотой, яблочной кислотой, щавелевой кислотой, бензойной кислотой, метансульфоновой кислотой и т.п.), и соли с неорганическими кислотами (соляной кислотой, фосфорной кислотой, бромистоводородной кислотой, серной кислотой, азотной кислотой и т.п.). Фраза «фармацевтически приемлемая соль», применяемая в настоящем документе, относится к соли, которая сохраняет фармакологическую и фармацевтическую эффективность и свойства соединений. Таким образом, фармацевтические композиции, содержащие фармацевтически приемлемую соль пептида по настоящему изобретению, также охватываются настоящим изобретением. Дополнительно, «пептид по настоящему изобретению» также включает, в дополнение к свободному пептиду, его фармацевтически приемлемые соли.
В некоторых вариантах осуществления фармацевтические композиции по настоящему изобретению могут дополнительно включать компонент, который примирует ЦТЛ. Липиды были идентифицированы как вещества, способные примировать ЦТЛ in vivo против вирусных антигенов. Например, остатки пальмитиновой кислоты можно присоединять к эпсилон- и альфа-аминогруппам остатка лизина, а затем связывать с пептидом по настоящему изобретению. Липидированный пептид затем можно вводить или напрямую в мицеллу или частицу, включенную в липосому, или эмульгировать в адъюванте. В качестве другого примера липида, примирующего ответы ЦТЛ, можно использовать липопротеины E. coli, такие как трипальмитоил-S-глицерилцистенил-серил-серин (P3CSS), для примирования ЦТЛ при ковалентном присоединении к соответствующему пептиду (см., например, Deres et al., Nature 1989, 342: 561-4).
Примеры подходящих способов для введения пептидов или фармацевтических композиций по настоящему изобретению включают пероральные, эпидермальные, подкожные, внутримышечные, внутрикостные, внутрибрюшинные, и внутривенные инъекции, а также системное введение или местное введение в непосредственной близости от участков-мишеней, но не ограничиваются перечисленными. Предпочтительный способ введения включает подкожную инъекцию в непосредственной близости от лимфоузлов, таких как подмышечный или паховый. Более конкретно, например, подкожное введение является предпочтительным, если фармацевтическая композиция по настоящему изобретению в качестве активного ингредиента содержит пептид или экзосому. Альтернативно, композиции с APC или ЦТЛ в качестве активного ингредиента можно вводить путем внутривенной инъекции или т.п. Введение можно проводить путем одиночного введения или разделенным на несколько введений. Пептиды по настоящему изобретению можно вводить индивидууму в терапевтически или фармацевтически эффективном количестве для лечения злокачественной опухоли или в терапевтически или фармацевтически эффективном количестве для индуцирования иммунитета (более конкретно, ЦТЛ) против FOXM1-экспрессирующих злокачественных клеток. Доза пептидов по настоящему изобретению может быть соответствующим образом скорректирована в соответствии с заболеванием, подлежащим лечению, возрастом и массой пациента, способом введения и т.п. Для каждого из пептидов по настоящему изобретению, доза составляет, как правило, 0,001 мг - 1000 мг, например, 0,01 мг - 100 мг, например, 0,1 мг - 30 мг, например, 0,1 мг - 10 мг, например, 0,5 мг - 5 мг. Интервал между дозами может составлять от одного раза каждые несколько суток до нескольких месяцев, и например, дозировку можно производить с интервалом раз в неделю. Специалист в данной области может соответствующим образом выбрать подходящую дозу (дозирование).
В предпочтительном варианте осуществления фармацевтические композиции по настоящему изобретению содержат терапевтически эффективное количество пептида по настоящему изобретению и фармацевтически или физиологически приемлемый носитель. В другом варианте осуществления фармацевтические композиции по настоящему изобретению содержат терапевтически эффективное количество пептида по настоящему изобретению, фармацевтически или физиологически приемлемый носитель и адъювант. Фармацевтические композиции по настоящему изобретению могут содержать 0,001 мг - 1000 мг, предпочтительно 0,01 мг - 100 мг, более предпочтительно 0,1 мг - 30 мг, даже более предпочтительно 0,1 мг - 10 мг, например, 0,5 мг - 5 мг пептида по настоящему изобретению. Когда фармацевтическая композиция по настоящему изобретению представляет собой инъекцию, она может содержать пептид по настоящему изобретению в концентрации 0,001 мг/мл - 1000 мг/мл, предпочтительно 0,01 мг/мл - 100 мг/мл, более предпочтительно 0,1 мг/мл - 30 мг/мл, даже более предпочтительно 0,1 мг/мл - 10 мг/мл, например, 0,5 мг/мл - 5 мг/мл. В этом случае, например, можно вводить индивидууму путем инъекции от 0,1 до 5 мл, предпочтительно, от 0,5 мл до 2 мл фармацевтической композиции по настоящему изобретению.
Дополнительно, настоящее изобретение относится к способам лечения и/или профилактики злокачественной опухоли и/или профилактики ее послеоперационного рецидива, которые включают введение индивидууму терапевтически эффективного количества пептида по настоящему изобретению или фармацевтической композиции по настоящему изобретению. Как описано выше, пептиды по настоящему изобретению можно вводить индивидууму в однократной дозе, как правило, 0,001 мг - 1000 мг, например, 0,01 мг - 100 мг, например, 0,1 мг - 30 мг, например, 0,1 мг - 10 мг, или например, 0,5 мг - 5 мг. В предпочтительном варианте осуществления пептиды по настоящему изобретению вводят индивидууму вместе с адъювантом. Дополнительно, интервал между дозами может составлять от одного раза каждые несколько суток до нескольких месяцев, предпочтительно от одного раза каждые несколько суток до раза в месяц, например, от одного раза в неделю или одного раза в две недели.
(2) Фармацевтические композиции, содержащие полинуклеотиды в качестве активного ингредиента
Фармацевтические композиции по настоящему изобретению могут также содержать полинуклеотиды, кодирующие пептиды по настоящему изобретению, в экспрессируемой форме. В настоящем документе, фраза «в экспрессируемой форме» означает, что полинуклеотид, при введении в клетку, будет экспрессироваться как пептид по настоящему изобретению. В примере варианта осуществления, последовательность полинуклеотида по настоящему изобретению относится к регуляторным элементам, необходимым для экспрессии пептида по настоящему изобретению. Полинуклеотид(-ы) по настоящему изобретению могут быть дополнены последовательностью, необходимой для достижения стабильной вставки в геном клеток-мишеней (см., например, Thomas KR & Capecchi MR, Cell 1987, 51: 503-12 для описания кассетных векторов для гомологичной рекомбинации). См., например, Wolff et al., Science 1990, 247: 1465-8; патенты США №№ 5580859, 5589466, 5804566, 5739118, 5736524, 5679647; и WO98/04720. Примеры технологий доставки на основе ДНК включают «голую ДНК», облегченную доставку (бупивакаин, полимеры, опосредованную пептидами), комплексы катионных липидов, и доставку, опосредованную частицами («генная пушка») или давлением (см., например, патент США № 5922687).
Пептиды по настоящему изобретению можно также экспрессировать при помощи вирусных или бактериальных векторов. Примеры экспрессирующих векторов включают аттенуированные вирусы-хозяева, такие как вирус осповакцины или вирус оспы кур. Например, можно использовать вирус осповакцины в качестве вектора для экспрессии пептида по настоящему изобретению. После введения в хозяина, рекомбинантный вирус осповакцины экспрессирует иммуногенный пептид, и, таким образом, вызывает иммунный ответ. Векторы на основе вируса осповакцины и способы, подходящие для протоколов иммунизации, описаны, например, в патенте США № 4722848. Другим вектором является БЦЖ (бацилла Кальмета-Герена). Векторы на основе БЦЖ описаны у Stover et al., Nature 1991, 351: 456-60. Будет очевиден широкий спектр других векторов, подходящих для терапевтического введения или иммунизации, например, аденовирусные и аденоассоциированные вирусные векторы, ретровирусные векторы, векторы на основе Salmonella typhi, векторы на основе обезвреженного токсина сибирской язвы и т.п. См., например, Shata et al., Mol Med Today 2000, 6: 66-71; Shedlock et al., J Leukoc Biol 2000, 68: 793-806; Hipp et al., In Vivo 2000, 14: 571-85.
Доставка полинуклеотида по настоящему изобретению пациенту может быть или прямой, при этом пациент может напрямую получать вектор, несущий полинуклеотид по настоящему изобретению, или опосредованной, при этом, сначала клетки трансформируются вектором, несущим полинуклеотид по настоящему изобретению in vitro, затем клетки пересаживают пациенту. Эти два подхода известны, соответственно, как генная терапия in vivo и ex vivo.
Для общих обзоров способов генотерапии, см. Goldspiel et al., Clinical Pharmacy 1993, 12: 488-505; Wu и Wu, Biotherapy 1991, 3: 87-95; Tolstoshev, Ann Rev Pharmacol Toxicol 1993, 33: 573-96; Mulligan, Science 1993, 260: 926-32; Morgan & Anderson, Ann Rev Biochem 1993, 62: 191-217; Trends in Biotechnology 1993, 11(5): 155-215. Способы, общеизвестные в области технологии рекомбинантных ДНК, которые также можно использовать для настоящего изобретения, описаны в Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, NY, 1993; и Krieger, Gene Transfer и Expression, A Laboratory Manual, Stockton Press, NY, 1990.
Аналогично введению пептидов, введение полинуклеотидов можно проводить путем пероральной, интрадермальной, подкожной, внутривенной, внутримышечной, внутрикостной и/или внутрибрюшинной инъекции, и т.п. Введение полинуклеотидов может быть системным введением или местным введением в непосредственной близости от участков-мишеней. Введение можно проводить путем одиночного введения или разделенным на несколько введений. Полинуклеотиды по настоящему изобретению можно вводить индивидууму в терапевтически или фармацевтически эффективном количестве для лечения злокачественной опухоли или в терапевтически или фармацевтически эффективном количестве для индуцирования иммунитета (более конкретно, ЦТЛ) против FOXM1-экспрессирующих злокачественных клеток. Доза полинуклеотида в подходящем носителе или доза полинуклеотида в клетках, трансформированных полинуклеотидом, кодирующим пептид по настоящему изобретению, может быть соответствующим образом скорректирована в соответствии с заболеванием, подлежащим лечению, возрастом и массой пациента, способом введения и т.п., и она может составлять, как правило, 0,001 мг - 1000 мг, например, 0,01 мг - 100 мг, например, 0,1 мг - 30 мг, например, 0,1 мг - 10 мг, или например, 0,5 мг - 5 мг. Интервал между дозами может составлять от одного раза каждые несколько суток до нескольких месяцев, и например, дозировку можно производить с интервалом раз в неделю. Специалист в данной области может соответствующим образом выбрать подходящую дозу (дозирование).
X. Способы применения пептидов, экзосом, АПК и ЦТЛ
Пептиды и полинуклеотиды по настоящему изобретению можно использовать для индуцирования АПК и ЦТЛ. ЦТЛ можно также индуцировать при помощи экзосом и АПК по настоящему изобретению. Пептиды, полинуклеотиды, экзосомы и АПК по настоящему изобретению можно использовать в комбинации с любым другим соединением/соединениями при условии, что не будет ингибирована их способность индуцировать ЦТЛ. Таким образом, ЦТЛ по настоящему изобретению можно индуцировать при помощи фармацевтической композиции, содержащей любой из пептидов, полинуклеотиды, АПК и экзосомы по настоящему изобретению. Дополнительно, АПК по настоящему изобретению можно индуцировать при помощи фармацевтической композиции, содержащей пептид или полинуклеотид по настоящему изобретению.
(1) Способы индуцирования АПК
Настоящее изобретение относится к способам индуцирования АПК со способностью индуцировать ЦТЛ, при помощи пептида/пептидов или полинуклеотида/полинуклеотидов по настоящему изобретению.
Способы по настоящему изобретению включают этап контакта АПК с пептидом по настоящему изобретению in vitro, ex vivo, или in vivo. Например, способ контакта АПК с пептидом ex vivo может включать нижеизложенные этапы:
(a) забор АПК у индивидуума; и
(b) контакт АПК из этапа (a) с пептидом по настоящему изобретению.
Вышеописанные АПК не ограничиваются конкретным типом клеток, и можно использовать DC, клетки Лангерганса, макрофаги, B-клетки, и активированные T-клетки, о которых известно, что они презентируют белковые антигены на своей клеточной поверхности, таким образом, что они распознаются лимфоцитами. Среди АПК, DC имеют наиболее мощную способность индуцировать ЦТЛ, и, таким образом, предпочтительно использовать DC. Любые пептиды по настоящему изобретению можно использовать сами по себе или в комбинации с другими пептидами по настоящему изобретению. Дополнительно, пептиды по настоящему изобретению можно использовать в комбинации с другими пептидами, индуцирующими ЦТЛ (например, другими пептидами, полученными из TAA и индуцирующими ЦТЛ).
Помимо этого, когда пептид по настоящему изобретению вводят индивидууму, АПК контактируют с пептидом in vivo, и в результате АПК, имеющие высокую способность индуцировать ЦТЛ, индуцируются в организме индивидуума. Таким образом, способы по настоящему изобретению могут включать этап введения пептида по настоящему изобретению индивидууму. Аналогично, когда полинуклеотид по настоящему изобретению вводят индивидууму в экспрессируемой форме, пептид по настоящему изобретению экспрессируется in vivo, экспрессировавшийся пептид контактирует с АПК in vivo, и в результате АПК, имеющие высокую способность индуцировать ЦТЛ, индуцируются в организме индивидуума. Таким образом, настоящее изобретение может также включать этап введения полинуклеотида по настоящему изобретению индивидууму.
Для того чтобы индуцировать АПК со способностью индуцировать ЦТЛ, настоящее изобретение может включать этап введения полинуклеотида по настоящему изобретению в АПК. Например, способ может включать нижеизложенные этапы:
(a) забор АПК у индивидуума; и
(b) введение полинуклеотида, кодирующего пептид по настоящему изобретению, в АПК из этапа (a).
Этап (b) можно проводить, как описано выше в разделе «VI. Антигенпрезентирующие клетки (АПК)».
Таким образом, в одном из вариантов осуществления настоящее изобретение относится к способу индуцирования АПК со способностью индуцировать ЦТЛ, включающему нижеизложенные этапы (a) или (b):
(a) контакт АПК с пептидом по настоящему изобретению; или
(b) введение полинуклеотида, кодирующего пептид по настоящему изобретению, в АПК.
Кроме того, настоящее изобретение относится к способу получения АПК со способностью индуцировать ЦТЛ, включающему нижеизложенные этапы (a) или (b):
(a) контакт АПК с пептидом по настоящему изобретению; или
(b) введение полинуклеотида, кодирующего пептид по настоящему изобретению, в АПК.
Вышеописанные способы можно проводить in vitro, ex vivo, или in vivo, и предпочтительно проводить их in vitro или ex vivo. АПК, применяемые в вышеописанных способах, можно получать от индивидуума, которому планируется вводить индуцированные АПК, или их можно получать от другого индивидуума. Когда используют АПК, полученные от индивидуума (донора), отличного от индивидуума, для которого запланировано введение, индивидуум для введения и донор должны иметь идентичный тип HLA.
В способах по настоящему изобретению, когда пептид с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, или его модифицированный пептид используют в качестве пептида по настоящему изобретению, HLA предпочтительно представляет собой HLA-A33 (более предпочтительно HLA-A*33:03) как у индивидуума для введения, так и у донора. Альтернативно, АПК, применяемые в вышеописанных способах, предпочтительно представляют собой АПК, которые экспрессируют HLA-A33 (более предпочтительно HLA-A*33:03).
Аналогично, когда пептид с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 или 61, или его модифицированный пептид используют в качестве пептида по настоящему изобретению, HLA предпочтительно представляет собой HLA-A01 (более предпочтительно HLA-A*01:01), как у индивидуума для введения, так и у донора. Альтернативно, АПК, применяемые в вышеописанных способах, предпочтительно представляют собой АПК, которые экспрессируют HLA-A01 (более предпочтительно HLA-A*01:01). АПК можно получать с применением известных способов из PBMC, после того как PBMC выделены из крови, полученной от донора, путем способа центрифугирования с удельной плотностью или т.п.
В другом варианте осуществления настоящее изобретение также относится к фармацевтическим композициям, которые содержат пептид по настоящему изобретению или полинуклеотид, кодирующий пептид, для индуцирования АПК со способностью индуцировать ЦТЛ.
Альтернативно, настоящее изобретение дополнительно относится к применению пептида по настоящему изобретению или полинуклеотида, кодирующего пептид, в производстве фармацевтической композиции для индуцирования АПК со способностью индуцировать ЦТЛ.
Альтернативно, настоящее изобретение дополнительно относится к пептидам по настоящему изобретению или полинуклеотидам, кодирующим пептиды, для применения для индуцирования АПК со способностью индуцировать ЦТЛ.
Альтернативно, настоящее изобретение дополнительно относится к способам или процессам производства фармацевтической композиции для индуцирования АПК, где способ или процесс включают этап формулирования пептида по настоящему изобретению или полинуклеотида, кодирующего пептид, с фармацевтически или физиологически приемлемым носителем.
В другом варианте осуществления настоящее изобретение дополнительно относится к способам или процессам производства фармацевтической композиции для индуцирования АПК со способностью индуцировать ЦТЛ, где способ или процесс включают этап смешивания пептида по настоящему изобретению или полинуклеотида, кодирующего пептид, с фармацевтически или физиологически приемлемым носителем.
АПК, индуцированные способами по настоящему изобретению, могут индуцировать ЦТЛ, специфичные к FOXM1 (т.е., ЦТЛ по настоящему изобретению).
(2) Способы индуцирования ЦТЛ
Настоящее изобретение также относится к способам индуцирования ЦТЛ с использованием пептидов, полинуклеотидов, экзосом или АПК по настоящему изобретению. Настоящее изобретение дополнительно относится к способам индуцирования ЦТЛ с использованием одного или нескольких полинуклеотидов, кодирующих полипептид(-ы), которые могут формировать T-клеточный рецептор (TCR) (т.е., субъединицу TCR), способный распознавать комплекс пептида по настоящему изобретению и антигена HLA. Предпочтительно, способы индуцирования ЦТЛ включают, по меньшей мере, один этап, выбранный из нижеизложенных:
(a) контакт CD8-положительных T-клеток с антигенпрезентирующими клетками, которые презентируют на своей поверхности комплекс антигена HLA и пептида по настоящему изобретению;
(b) контакт CD8-положительных T-клеток с экзосомами, которые презентируют на своей поверхности комплекс антигена HLA и пептида по настоящему изобретению; и
(c) введение в CD8-положительные T-клетки одного или нескольких полинуклеотидов, кодирующих полипептид(-ы), которые могут формировать TCR, способный распознавать комплекс пептида по настоящему изобретению и антигена HLA.
Когда пептид(-ы), полинуклеотид(-ы), экзосому/экзосомы или АПК по настоящему изобретению вводят индивидууму, ЦТЛ индуцируются в организме индивидуума, и сила иммунного ответа, нацеленного на FOXM1-экспрессирующие злокачественные клетки, возрастает. Таким образом, способы по настоящему изобретению могут включать этап введения индивидууму пептида/пептидов, полинуклеотида/полинуклеотидов, АПК или экзосомы/экзосом по настоящему изобретению.
Альтернативно, ЦТЛ можно индуцировать при использовании их in vitro или ex vivo. Например, способы по настоящему изобретению могут включать следующие этапы:
(a) забор АПК у индивидуума;
(b) контакт АПК из этапа (а) с пептидом по настоящему изобретению; и
(c) совместное культивирование АПК из этапа (b) с CD8-положительными T-клетками.
Индуцированные ЦТЛ впоследствии можно возвращать индивидууму.
АПК для совместного культивирования с CD8-положительными T-клетками из этапа (c) выше также можно получать путем введения в АПК полинуклеотида, кодирующего пептид по настоящему изобретению, как описано выше в разделе «VI. Антигенпрезентирующие клетки (АПК)». Однако АПК для применения в способах по настоящему изобретению не ограничиваются вышеуказанными, и можно использовать любые АПК, которые презентируют на своей поверхности комплекс антигена HLA и пептида по настоящему изобретению.
В способах по настоящему изобретению, вместо таких АПК, также можно использовать экзосомы, которые презентируют на своей поверхности комплекс антигена HLA и пептида по настоящему изобретению. То есть, способы по настоящему изобретению могут включать этап совместного культивирования с экзосомами, которые презентируют на своей поверхности комплекс антигена HLA и пептида по настоящему изобретению. Такие экзосомы можно получать способами, описанными выше в разделе «V. Экзосомы».
Дополнительно, ЦТЛ также можно индуцировать путем введения в CD8-положительную T-клетку вектора, содержащего полинуклеотид, кодирующий каждую субъединицу TCR, способного связываться с пептидом по настоящему изобретению, презентированным при помощи антигена HLA на клеточной поверхности. Такую трансформацию можно проводить, как описано выше в разделе «VIII. T-клеточные рецепторы (TCR)».
Таким образом, в одном из вариантов осуществления настоящее изобретение относится к способам индуцирования ЦТЛ, включающим этап, выбранный из нижеизложенных:
(a) совместное культивирование CD8-положительных T-клеток с АПК, которые презентируют на своей поверхности комплекс антигена HLA и пептида по настоящему изобретению;
(b) совместное культивирование CD8-положительных T-клеток с экзосомами, которые презентируют на своей поверхности комплекс антигена HLA и пептида по настоящему изобретению; и
(c) введение в CD8-положительные T-клетки вектора, содержащего полинуклеотид, кодирующий каждую субъединицу TCR, способного связываться с пептидом по настоящему изобретению, презентированным при помощи антигена HLA на клеточной поверхности.
Вышеописанные способы можно проводить in vitro, ex vivo, или in vivo, и предпочтительно проводить их in vitro или ex vivo. АПК, или экзосомы, и CD8-положительные T-клетки, применяемые в вышеописанных способах, можно получать от индивидуума, которому планируется вводить индуцированные АПК, или их можно получать от другого индивидуума. Когда используют АПК, или экзосомы, и CD8-положительные T-клетки, полученные от индивидуума (донора), отличного от индивидуума, для которого запланировано введение, индивидуум для введения и донор должны иметь идентичный тип HLA.
Например, когда пептид с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, или его модифицированный пептид используют в качестве пептидов по настоящему изобретению, HLA и у индивидуума, которому проводят введение, и у донора предпочтительно представляет собой HLA-A33 (более предпочтительно HLA-A*33:03). Альтернативно, АПК или экзосомы, используемые в вышеописанных способах, предпочтительно являются АПК или экзосомами, которые презентируют на своей поверхности комплекс HLA-A33 (более предпочтительно HLA-A*33:03) и пептида по настоящему изобретению (пептида с аминокислотной последовательностью, выбранной из SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, или его модифицированного пептида). В этом случае, индуцированные ЦТЛ показывают специфическую цитотоксическую активность против клеток, которые презентируют комплекс HLA-A33 и пептид по настоящему изобретению (например, FOXM1-экспрессирующие HLA-A33-положительные клетки).
Альтернативно, например, когда пептид с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61, или его модифицированный пептид используют в качестве пептидов по настоящему изобретению, HLA и у индивидуума, которому проводят введение, и у донора предпочтительно представляет собой HLA-A01 (более предпочтительно HLA-A*01:01). Альтернативно, АПК или экзосомы, используемые в вышеописанных способах, предпочтительно являются АПК или экзосомами, которые презентируют на своей поверхности комплекс HLA-A01 (более предпочтительно HLA-A*01:01) и пептида по настоящему изобретению (пептида с аминокислотной последовательностью, выбранной из SEQ ID NO: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61 или его модифицированного пептида). В этом случае, индуцированные ЦТЛ показывают специфическую цитотоксическую активность против клеток, которые презентируют комплекс HLA-A01 и пептид по настоящему изобретению (например, FOXM1-экспрессирующие HLA-A01-положительные клетки).
В другом варианте осуществления настоящее изобретение также относится к композициям или фармацевтическим композициям для индуцирования ЦТЛ, содержащим по меньшей мере один активный ингредиент, выбранный из нижеизложенных:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности.
В другом варианте осуществления настоящее изобретение также относится к применению активного ингредиента, выбранного из нижеизложенных, в производстве композиций или фармацевтических композиций для индуцирования ЦТЛ:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности.
Альтернативно, настоящее изобретение дополнительно относится к активному ингредиенту, выбранному из нижеизложенных, для применения в индуцировании ЦТЛ:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности.
Альтернативно, настоящее изобретение дополнительно относится к способу или процессу для производства композиции или фармацевтической композиции для индуцирования ЦТЛ, где способ или процесс включает этап формулирования активного ингредиента, выбранного из нижеизложенных, с фармацевтически или физиологически приемлемым носителем:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности.
В другом варианте осуществления настоящее изобретение дополнительно относится к способу или процессу для производства композиции или фармацевтической композиции для индуцирования ЦТЛ, где способ или процесс включает этап смешивания активного ингредиента, выбранного из нижеизложенных, с фармацевтически или физиологически приемлемым носителем:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности.
XI. Способы индуцирования иммунного ответа
Настоящее изобретение дополнительно относится к способам индуцирования иммунного ответа против FOXM1-экспрессирующих злокачественных опухолей. Подходящие злокачественные опухоли включают острый миелоидный лейкоз, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, хронический миелолейкоз (ХМЛ), рак толстого кишечника, рак пищевода, рак желудка, диффузный рак желудка, немелкоклеточный рак легких (NSCLC), лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак почки, мелкоклеточный рак легких (SCLC), опухоль мягких тканей, рак яичка и т.п., но не ограничиваются указанными. Предпочтительно, чтобы злокачественная опухоль экспрессировала, по меньшей мере, один HLA, выбранный из HLA-A33 и HLA-A01.
Настоящее изобретение дополнительно относится к способам индуцирования иммунного ответа против FOXM1-экспрессирующих злокачественных клеток. Признано, что FOXM1 сверхэкспрессирован в различных типах злокачественных опухолей, описанных выше. Таким образом, когда индуцируется иммунный ответ против FOXM1-экспрессирующих злокачественных клеток, в результате ингибируется пролиферация злокачественных клеток. Таким образом, настоящее изобретение дополнительно относится к способам ингибирования пролиферации FOXM1-экспрессирующих злокачественных клеток. Способы по настоящему изобретению подходят, в частности, для ингибирования пролиферации злокачественных клеток, экспрессирующих FOXM1 и, по меньшей мере, один HLA, выбранный из HLA-A33 и HLA-A01.
Способы по настоящему изобретению могут включать этап введения композиции, содержащей любой из пептидов по настоящему изобретению или полинуклеотида/полинуклеотидов, кодирующих пептид(-ы). Способы по настоящему изобретению также включают введение АПК или экзосом, презентирующих любой из пептидов по настоящему изобретению. За деталями можно обращаться в раздел «IX. Фармацевтические композиции», в частности, к частям, описывающим применение фармацевтических композиций по настоящему изобретению в качестве вакцин. Кроме того, экзосомы и АПК, которые можно использовать в способах по настоящему изобретению для индуцирования иммунного ответа, описаны подробно в «V. Экзосомы», «VI. Антигенпрезентирующие клетки (АПК)» и в пунктах (1) и (2) из «X. Способы применения пептидов, экзосом, АПК и ЦТЛ», описанных выше.
В другом варианте осуществления настоящее изобретение относится к фармацевтическим композициям или вакцинам для индуцирования иммунного ответа против FOXM1-экспрессирующих злокачественных опухолей, где фармацевтическая композиция или вакцина содержит активный ингредиент, выбранный из нижеизложенных:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
Альтернативно, настоящее изобретение также относится к фармацевтическим композициям или вакцинам для индуцирования иммунного ответа против FOXM1-экспрессирующих злокачественных клеток, где фармацевтическая композиция или вакцина содержит активный ингредиент, выбранный из нижеизложенных:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
Альтернативно, настоящее изобретение дополнительно относится к фармацевтическим композициям или вакцинам для ингибирования пролиферации FOXM1-экспрессирующих злокачественных клеток, где фармацевтическая композиция или вакцина содержит активный ингредиент, выбранный из нижеизложенных:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
В другом варианте осуществления настоящее изобретение относится к применению активного ингредиента, выбранного из нижеизложенных, в производстве фармацевтических композиций или вакцин для индуцирования иммунного ответа против FOXM1-экспрессирующих злокачественных опухолей:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
Альтернативно, настоящее изобретение относится к применению активного ингредиента, выбранного из нижеизложенных, в производстве фармацевтических композиций или вакцин для индуцирования иммунного ответа против FOXM1-экспрессирующих злокачественных клеток:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
Альтернативно, настоящее изобретение относится к применению активного ингредиента, выбранного из нижеизложенных, в производстве фармацевтических композиций или вакцин для ингибирования пролиферации FOXM1-экспрессирующих злокачественных клеток:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
Настоящее изобретение дополнительно относится к способам или процессам для производства фармацевтических композиций, которые индуцируют иммунный ответ против FOXM1-экспрессирующих злокачественных опухолей, при этом способ может включать этап смешивания или формулирования пептида или полинуклеотида по настоящему изобретению с фармацевтически приемлемым носителем.
Альтернативно, настоящее изобретение относится к способам для ингибирования пролиферации FOXM1-экспрессирующих злокачественных клеток или к способам индуцирования иммунного ответа против злокачественных опухолей, которые включают этап введения индивидууму вакцин или фармацевтических композиций, содержащих активный ингредиент, выбранный из нижеизложенных:
(a) пептид по настоящему изобретению;
(b) полинуклеотид, кодирующий пептид по настоящему изобретению в экспрессируемой форме;
(c) АПК, которая презентирует пептид по настоящему изобретению на своей поверхности;
(d) экзосома, которая презентирует пептид по настоящему изобретению на своей поверхности; и
(e) ЦТЛ по настоящему изобретению.
В контексте настоящего изобретения,, FOXM1-экспрессирующие злокачественные опухоли можно лечить путем введения пептида, полинуклеотида, АПК, экзосомы и/или ЦТЛ по настоящему изобретению. Альтернативно, иммунный ответ против FOXM1-экспрессирующих злокачественных опухолей можно индуцировать путем введения пептида, полинуклеотида, АПК, экзосомы и/или ЦТЛ по настоящему изобретению. Примеры таких злокачественных опухолей включают острый миелоидный лейкоз, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, хронический миелолейкоз (ХМЛ), рак толстого кишечника, рак пищевода, рак желудка, диффузный рак желудка, немелкоклеточный рак легких (NSCLC), лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак почки, мелкоклеточный рак легких (SCLC), опухоль мягких тканей, рак яичка и т.п., но не ограничиваются указанными. Дополнительно, иммунный ответ против FOXM1-экспрессирующих злокачественных клеток можно индуцировать путем введения пептида, полинуклеотида, АПК, экзосомы и/или ЦТЛ по настоящему изобретению. Таким образом, перед введением вакцины или фармацевтической композиции, содержащей вышеописанный активный ингредиент, предпочтительно подтвердить, увеличен ли уровень экспрессии FOXM1 в больном участке у индивидуума, подлежащего лечению, или нет.
Таким образом, в одном из вариантов осуществления настоящее изобретение относится к лечению FOXM1-экспрессирующей злокачественной опухоли у пациента, нуждающегося в лечении злокачественных опухолей, где способ включает нижеизложенные этапы:
(i) измерение уровня экспрессии FOXM1 в биологическом образце, полученном из больного участка индивидуума со злокачественной опухолью;
(ii) выявление индивидуума с FOXM1-экспрессирующей злокачественной опухолью на основании уровня экспрессии FOXM1, измеренного в (i); и
(iii) введение индивидууму с опухолью со сверхэкспрессией FOXM1 по сравнению со здоровым контролем, по меньшей мере, одного ингредиента, выбранного из группы, состоящей из вышеописанных от (a) до (e).
Альтернативно, настоящее изобретение дополнительно относится к вакцинам и фармацевтическим композициям, содержащим, по меньшей мере, один активный ингредиент, выбранный из группы, состоящей из вышеописанных от (a) до (e), для введения индивидууму с FOXM1-экспрессирующей злокачественной опухолью. Настоящее изобретение дополнительно относится к способу выявления или отбора индивидуума, подлежащего лечению, по меньшей мере, одним активным ингредиентом, выбранным из группы, состоящей из вышеописанных от (a) до (e), где способ включает нижеизложенные этапы:
(i) измерение уровня экспрессии FOXM1 в биологическом образце, полученном из больного участка индивидуума со злокачественной опухолью;
(ii) выявление индивидуума с FOXM1-экспрессирующей злокачественной опухолью на основании уровня экспрессии FOXM1, измеренного в (i); и
(iii) идентификация или отбор индивидуума, выявленного в (ii) как индивидуума, которого можно лечить, по меньшей мере, одним активным ингредиентом, выбранным из группы, состоящей из вышеописанных от (a) до (e).
Биологические образцы, собранные у индивидуума для измерения уровня экспрессии FOXM1 в вышеописанных способах конкретно не ограничены, и например, можно предпочтительно использовать образцы ткани, полученные путем биопсии и т.п и содержащие злокачественные клетки. Уровень экспрессии FOXM1 в биологическом образце можно измерять известными способами, и например, можно использовать способы, которые детектируют продукты транскрипции гена FOXM1 при помощи зондов, или способы ПЦР (например, способ микропанелей с кДНК, способ Нозерн-блоттинга, способ ОТ-ПЦР или т.п.), способы, которые детектируют продукты трансляции гена FOXM1 при помощи антител или т.п. (например, способ Вестерн-блоттинга, способ иммуноокрашивания или т.п.), и т.п. Дополнительно, биологические образцы могут быть образцами крови, и в этом случае, измеряют уровень антител против FOXM1 в крови, и можно оценивать уровень экспрессии FOXM1 в месте заболевания на основании уровня в крови. Уровень антитела против FOXM1 или его фрагментов в крови можно измерять с применением известных способов, и, например, можно использовать иммуноферментный анализ (EIA), твердофазный иммуноферментный анализ (ELISA), радиоиммунологический анализ (РИА) и т.п., с использованием белка FOXM1 или пептида по настоящему изобретению в качестве антигена.
Как правило, в тканях и клетках, которые не экспрессируют FOXM1, практически не выявляются продукты транскрипции и трансляции FOXM1. Таким образом, когда продукт транскрипции или трансляции FOXM1 детектируется в полученных от индивидуума злокачественных клетках или образце ткани, содержащем злокачественные клетки, можно определить, что злокачественная опухоль индивидуума экспрессирует FOXM1. В образцах крови индивидуума, у которого нет FOXM1-экспрессирующей злокачественной опухоли, практически не выявляются антитела против FOXM1 или их фрагменты. Таким образом, когда антитела против FOXM1 или их фрагменты детектируются в образце крови, полученном от индивидуума, можно определить, что злокачественная опухоль индивидуума экспрессирует FOXM1. Экспрессирует ли злокачественная опухоль индивидуума FOXM1 или нет, также можно определить при сравнении результатов измерений в биологическом материале того же типа, полученном из неопухолевого участка индивидуума или в биологическом материале того же типа, полученном от индивидуума без злокачественной опухоли (образец здорового контроля). То есть, при сравнении с уровнем мишени измерения в образце здорового контроля (уровень у здорового контроля), если уровень в биологическом образце исследуемого индивидуума повышен, злокачественную опухоль индивидуума оценивают как экспрессирующую FOXM1. Например, когда количество выявленной мишени измерения повышено, по меньшей мере, на 10% или более по сравнению уровнем у здорового контроля, злокачественную опухоль индивидуума можно оценивать как экспрессирующую FOXM1. Желательно, чтобы количество выявленной мишени измерения было повышено предпочтительно на 25% или более, и более предпочтительно, на 50% или более, чем уровень у здорового контроля. Дополнительно, количество выявленного продукта транскрипции или трансляции FOXM1 можно оценивать при нормализации его против выявленного количества известного гена «домашнего хозяйства», такого как бета-актин, глицеральдегид-3-фосфат дегидрогеназа, или рибосомальный белок P1.
В предпочтительном варианте осуществления, предпочтительно подтверждать тип HLA у индивидуума перед введением, по меньшей мере, одного активного ингредиента, выбранного из группы, состоящей из вышеизложенных от (a) to (e). Например, для индивидуумов, которым вводят активный ингредиент, связанный с пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46, предпочтительно выбирать HLA-A33-положительных индивидуумов. Для индивидуумов, которым вводят активный ингредиент, связанный с пептидом с аминокислотной последовательностью, выбранной из числа SEQ ID NO:48, 49, 50, 52, 53 55, 20, 56, 57, 58, 59, 60 и 61, предпочтительно выбирать HLA-A01-положительных индивидуумов.
Настоящее изобретение дополнительно относится к комплексам пептида по настоящему изобретению и HLA. Вышеописанные комплексы по настоящему изобретению могут быть мономерами или мультимерами. Когда комплекс по настоящему изобретению является мультимером, число полимеров конкретно не ограничено, и он может быть мультимером с любым числом полимеров. Примеры включают тетрамер, пентамер, гексамер и т.п., но не ограничиваются перечисленными. Мультимеры по настоящему изобретению также включают декстрамеры (WO2002/072631) и стрептамеры (Knabel M et al., Nat Med. 2002 Jun; 8(6): 631-7.). Комплексы пептида по настоящему изобретению и HLA можно получать в соответствии с известными способами (например, Altman JD et al., Science.1996, 274(5284): 94-6; WO2002/072631; WO2009/003492; Knabel M et al., Nat Med. 2002 Jun; 8(6): 631-7, и т.д.). Комплексы по настоящему изобретению, например, можно использовать в количественной оценке ЦТЛ, специфичных к пептиду по настоящему изобретению. Например, образец крови получают у индивидуума, которому вводили фармацевтическую композицию по настоящему изобретению, и после отделения PBMC получают CD4-негативные клетки и приводят их в контакт с комплексом по настоящему изобретению, который конъюгирован с флуоресцентным красителем. Затем, можно измерять процентное содержание ЦТЛ, специфичных к пептиду по настоящему изобретению, путем анализа проточной цитометрией. Например, воздействия фармацевтической композиции по настоящему изобретению на индуцирование иммунного ответа можно контролировать, измеряя специфические ЦТЛ против пептида по настоящему изобретению до, во время и/или после введения фармацевтической композиции по настоящему изобретению.
XII. Антитела
Настоящее изобретение дополнительно относится к антителам, которые связываются с пептидом по настоящему изобретению. Предпочтительные антитела специфически связываются с пептидом по настоящему изобретению, но не связываются (или слабо связываются) с пептидом, который не является пептидом по настоящему изобретению. В другом варианте осуществления такое антитело может включать антитело, которое распознает пептид относительно молекул HLA, т.е., антитело, которое связывается с комплексом пептид-MHC. Специфичность связывания антитела можно подтверждать анализом ингибирования. То есть, если связывание между анализируемым антителом и полноразмерным полипептидом FOXM1 ингибируется в присутствии пептида по настоящему изобретению, такое антитело демонстрирует специфическое связывание с пептидом по настоящему изобретению. Антитела против пептидов по настоящему изобретению можно использовать в анализах для диагностики и прогнозирования заболевания, а также отбора индивидуума для введения фармацевтических композиций по настоящему изобретению и мониторинга фармацевтических композиций по настоящему изобретению.
Настоящее изобретение также относится к различным иммунологическим анализам для детекции и/или количественного определения пептидов по настоящему изобретению или их фрагментов. Такие иммунологические анализы включают радиоиммунологический анализ, имунохроматографию, твердофазный иммуноферментный анализ (ELISA), иммуноферментный флуоресцентный анализ (ELIFA) и т.п., не ограничиваясь перечисленными, и их проводят в рамках различных форматов иммунологических анализов, хорошо известных в данной области.
Антитела по настоящему изобретению можно использовать в способах иммунологической визуализации, которые могут выявлять FOXM1-экспрессирующие заболевания, и их примеры включают радиоактивную сцинтиграфию с использованием меченого антитела по настоящему изобретению, не ограничиваясь указанным. Такие способы анализа используют в клинике для детекции, мониторинга, и прогнозирования FOXM1-экспрессирующих злокачественных опухолей; и примеры таких злокачественных опухолей включают острый миелоидный лейкоз, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, хронический миелолейкоз (ХМЛ), рак толстого кишечника, рак пищевода, рак желудка, диффузный рак желудка, немелкоклеточный рак легких (NSCLC), лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак почки, мелкоклеточный рак легких (SCLC), опухоль мягких тканей, рак яичка и т.п., но не ограничиваются указанными.
Антитела по настоящему изобретению можно использовать в любой произвольной форме, такой как моноклональные антитела или поликлональные антитела, и они могут дополнительно включать антитела, полученные при иммунизации животного, такого как кролик, пептидом по настоящему изобретению, все классы поликлональных антител и моноклональных антител, антитела человека, а также химерные антитела и гуманизированные антитела, полученные путем генетической рекомбинации.
Пептид по настоящему изобретению или его фрагмент, применяемый в качестве антигена для получения антител, можно получать путем химического синтеза или способов генетической инженерии, на основании аминокислотных последовательностей, описываемых в настоящем документе.
Пептид, применяемый в качестве иммунизирующего антигена, может быть пептидом по настоящему изобретению или фрагментом пептида по настоящему изобретению. Дополнительно, пептид может быть связан или конъюгирован с носителем для повышения иммуногенности. Гемоцианин морского блюдца (KLH) является хорошо известным носителем. Способы для связывания KLH с пептидом также хорошо известны в данной области.
Любое млекопитающее можно иммунизировать вышеописанным антигеном, и предпочтительно рассматривать совместимость сродительской клеткой, применяемой в слиянии клеток, при получении моноклонального антитела. Как правило, можно использовать животных отряда Грызуны (Rodentia), Зайцеобразные (Lagomorpha) или Приматы (Primate). Животные отряда Грызунов включают, например, мышей, крыс и хомяков. Животные отряда Зайцеобразных включают, например, кроликов. Животные отряда Приматов включают, например, обезьян катарринов (обезьян старого света), таких как яванский макак (Macaca fascicularis), макаки-резусы, гамадрилы, и шимпанзе.
Способы иммунизации животных антигеном известны в данной области. Интраперитонеальная и подкожная инъекции антигена являются стандартными способами для иммунизации млекопитающих. Более конкретно, антиген разбавляют и суспендируют в соответствующем количестве фосфатно-солевого буфера (PBS), физиологического раствора, или т.п. По мере необходимости, раствор суспензии антигена можно вводить млекопитающим после смешивания с соответствующим количеством стандартного адъюванта, такого как полный адъювант Фрейнда, и эмульсификации. Затем предпочтительно вводить антиген, смешанный с соответствующим количеством неполного адъюванта Фрейнда несколько раз в интервале от 4 до 21 суток. Для иимунизации можно использовать подходящий носитель. После вышеуказанной иммунизации, сыворотку можно тестировать стандартным способом на увеличение количества желаемого антитела.
Поликлональные антитела против пептида по настоящему изобретению можно получать, забирая кровь у млекопитающих, у которых было подтверждено увеличение уровня желаемого антитела в сыворотке после иммунизации, и отделяя сыворотку от крови любым общепринятым способом. Поликлональное антитело может быть сывороткой, содержащей поликлональное антитело, или из сывороткии можно выделять фракцию, содержащую поликлональное антитело. Иммуноглобулин G или M можно получать из фракций, которые распознают только пептид по настоящему изобретению, например, с использованием аффинной колонки, конъюгированной с пептидом по настоящему изобретению, а затем дополнительной очистки фракций с использованием колонки с белком A или белком G.
Для того чтобы приготовить моноклональные антитела, после подтверждения увеличения уровня желаемого антитела в сыворотке после иммунизации, у млекопитающих забирают иммунные клетки и проводят клеточное слияние. Иммунные клетки, используемые для слияния клеток, предпочтительно можно получать из селезенки. Для других родительских клеток, которые сливают с вышеуказанными иммунными клетками, можно использовать, например, миеломную клетку млекопитающих, и более предпочтительно, миеломную клетку, которая приобрела свойство селекции по лекарственному средству клеток для слияния.
Вышеуказанные иммунные клетки можно сливать с миеломными клетками следующими известными способами, например, способом из Milstein et al. (Galfre и Milstein, Methods Enzymol, 1981, 73: 3-46).
Гибридомы, полученные путем слияния клеток, можно отбирать, культивируя их в стандартной селективной среде, такой как среда HAT (среда, содержащая гипоксантин, аминоптерин и тимидин). Культивирование клеток обычно продолжают в среде HAT в течение достаточного периода времени (например, от нескольких суток до нескольких недель), чтобы погибли все остальные клетки (не слитые клетки), кроме желаемых гибридом. Затем, гибридомные клетки, вырабатывающие желаемое антитело можно отбирать и клонировать, проводя стандартные лимитирующие разведения.
В дополнение к вышеописанным способам иммунизации не являющегося человеком животного при помощи антигена для получения гибридомы, можно иммунизировать лимфоциты человека, такие как лимфоциты, инфицированные вирусом Эпштейна-Барр, in vitro пептидом, клетками, экспрессирующими пептид, или их лизатами. Затем иммунизированные лимфоциты можно сливать с иммортализованными миеломными клетками, полученными от человека, такими как U266, для получения гибридом, производящих желаемое антитело человека, способное связываться с пептидом (JPS63-17688).
Затем, полученную гибридому пересаживают в брюшную полость мыши, и забирают асцитную жидкость. Полученное моноклональное антитело можно очищать, например, путем осаждения сульфатом аммония, на колонках с белком A или белком G, ионообменной хроматографией с DEAE, или на аффинной колонке, конъюгированной с пептидом по настоящему изобретению.
Альтернативно, антителопродуцирующие иммунные клетки, такие как иммунизированные лимфоциты, можно иммортализовать при помощи гена злокачественной опухоли ген и использовать для получения моноклональных антител.
Моноклональные антитела, полученные таким образом, также можно получать путем рекомбинации с использованием способов генетической инженерии (см., например, Borrebaeck и Larrick, Therapeutic Monoclonal Antibodies, опубликованную в Великобритании у MacMillan Publishers LTD (1990)). Например, ДНК, кодирующую антитело, можно клонировать в иммунные клетки, такие как клетки антителопродуцирующей гибридомы или иммунизированные лимфоциты, и вставить в подходящий вектор, а затем ввести в клетки-хозяева для получения рекомбинантного антитела. Настоящее изобретение также относится к рекомбинантным антителам, полученным, как описано выше.
Дополнительно, антитела по настоящему изобретению могут быть фрагментами антител или модифицированными антителами, при условии, что они связываются с пептидами по настоящему изобретению. Например, желательно, чтобы фрагмент антитела содержал антигенсвязывающий участок/участки антител. Конкретно, фрагменты антител могут быть Fab, F(ab')2, Fv, или одноцепочечным Fv(scFv), в котором фрагменты Fv, полученные из тяжелой и легкой цепей связаны подходящим линкером (Huston et al., Proc Natl Acad Sci USA, 1988, 85: 5879-83). Более конкретно, фрагменты антител можно получать при обработке антитела ферментом, таким как папаин или пепсин. Альтернативно, можно сконструировать ген, кодирующий фрагмент антитела, вставить в экспрессирующий вектор, и экспрессировать в подходящей клетке-хозяине (см., например, Co et al., J Immunol, 1994, 152: 2968-76; Better и Horwitz, Methods Enzymol, 1989, 178: 476-96; Pluckthun и Skerra, Methods Enzymol, 1989, 178: 497-515; Lamoyi, Methods Enzymol, 1986, 121: 652-63; Rousseaux et al., Methods Enzymol, 1986, 121: 663-9; Bird и Walker, Trends Biotechnol, 1991, 9: 132-7).
Антитела можно модифицировать путем конъюгации с различными молекулами, такими как полиэтиленгликоль (ПЭГ). Настоящее изобретение относится к таким модифицированным антителам. Модифицированные антитела можно получать путем химической модификации антител. Эти способы модификации являются общепринятыми в данной области.
Альтернативно, антитела по настоящему изобретению можно получать в виде химерных антител из вариабельной области антитела, не принадлежащего человеку, и константной области антитела человека, или в виде гуманизированных антител, которые содержат определяющую комплементарность область (CDR) из антитела, не принадлежащего человеку, и каркасную область, и константную область (FR) из антитела человека. Такие антитела можно получать в соответствии с известными способами. Гуманизацию можно проводить, замещая последовательность/последовательности антитела человека соответствующей последовательностью/последовательностями CDR из антитела, не принадлежащего человеку (см., например, Verhoeyen et al., Science, 1988, 239: 1534-6). Таким образом, такие гуманизированные антитела представляют собой химерные антитела, в которых по существу менее чем интактный вариабельный домен человека замещен соответствующей последовательностью от видов, не являющихся человеком.
Также можно использовать интактные антитела человека, содержащие вариабельную область человека в дополнение к каркасу и константным областям человека. Такие антитела можно получать при помощи различных способов, известных в данной области. Например, способы in vitro включают использование рекомбинантных библиотек из фрагментов антител человека, презентированных на бактериофагах (например, Hoogenboom & Winter, J. Mol. Biol., 1991, 227: 381). Аналогично, антитела человека можно также получать, вводя локусы гена иммуноглобулина человека трансгенным животным, например, мышам, у которых гены эндогенных иммуноглобулинов были частично или полностью инактивированы. Этот подход описан, например, в патентах США №№ 6150584, 5545807, 5545806, 5569825, 5625126, 5633425 и 5661016.
Антитела, полученные, как описано выше, можно очищать для гомогенности. Например, выделение и очистку антител можно проводить в соответствии со способами выделения и способами очистки, применяемыми для распространенных белков. Например, антитело можно отделять и изолировать при помощи соответствующим образом выбранного и скомбинированного применения хроматографии на колонках, такой как аффинная хроматография, фильтрации, ультрафильтрации, высаливания, диализа, SDS-электрофореза в полиакриламидном геле и электрофореза с изоэлектрофокусированием (Antibodies: A Laboratory Manual. Ed Harlow и David Lane, Cold Spring Harbor Laboratory (1988)), но не ограничиваясь перечисленными. Колонку с белком A и колонку с белком G можно использовать в качестве аффинной колонки. Примеры колонок с белком A, которые можно использовать, включают, например, Hyper D, POROS и Sepharose F.F. (Pharmacia).
Кроме аффинной хроматографии, примеры хроматографии включают, например, ионообменную хроматографию, гидрофобную хроматографию, гель-фильтрацию, хроматографию с обратной фазой, адсорбционную хроматографию и т.п. (Strategies for Protein Purification and Characterization: A Laboratory Course Manual. Ed Daniel R. Marshak et al., Cold Spring Harbor Laboratory Press (1996)). Хроматографию можно проводить путем хроматографии в жидкой фазе, такой как ВЭЖХ и FPLC.
Активность связывания антигена для антитела по настоящему изобретению можно измерять, например, при помощи измерения оптической плотности, твердофазного иммуноферментного анализа (ELISA), иммуноферментного анализа (EIA), радиоиммунологического анализа (РИА), и/или иммунофлуоресценции (IF). В случае ELISA, антитело по настоящему изобретению иммобилизуют на планшете, пептид по настоящему изобретению наносят на планшет, а затем наносят образец, содержащий желаемое антитело, такой как культуральный супернатант антителопродуцирующих клеток или очищенные антитела. Затем наносят вторичное антитело, которое распознает первичное антитело и помечено ферментом, таким как щелочная фосфатаза, и инкубируют планшет. Затем после отмывания на планшет наносят субстрат для фермента, такой как п-нитрофенилфосфат, и оценивают активность связывания антигена для образца по измерению оптической плотности. Для оценки активности связывания антитела, в качестве антигена можно использовать пептидные фрагменты, такие как C-концевые или N-концевые фрагменты. Для оценки активности антитела по настоящему изобретению можно использовать BIAcore (Pharmacia).
Возможно выявлять или измерять пептид по настоящему изобретению при помощи вышеописанных способов, добавляя антитело по настоящему изобретению к образцу, предположительно содержащему пептид по настоящему изобретению, и выявляя или измеряя иммунный комплекс, образовавшийся между антителом и пептидом.
Например, антитело по настоящему изобретению можно использовать для выявления пептида по настоящему изобретению, присутствующего в образце крови (например, образце сыворотки) индивидуума. Альтернативно, антитело по настоящему изобретению, присутствующее в образце крови (например, образце сыворотки) индивидуума, также можно выявлять при помощи пептида по настоящему изобретению. Результат измерения пептида по настоящему изобретению или антитела по настоящему изобретению в образце крови индивидуума можно использовать для отбора индивидуума для введения фармацевтических композиций по настоящему изобретению или мониторинга эффективности фармацевтических композиций по настоящему изобретению. Кроме того, опубликовано, что пациенты, у которых есть антитело против пептида, вводимого в качестве вакцины, могут иметь высокую восприимчивость к вакцине. Таким образом, пептид по настоящему изобретению можно использовать в качестве антигена для иммунологического анализа с использованием антитела к пептиду как индикатора для отбора из числа раковых пациентов пациента с ожидаемой высокой восприимчивостью к вакцине, содержащей пептид.
XIII. Векторы и клетки-хозяева
Настоящее изобретение относится к векторам, содержащим полинуклеотид, кодирующий пептид по настоящему изобретению, и клетки-хозяева, в которые введены векторы. Вектор по настоящему изобретению можно использовать для хранения полинуклеотида по настоящему изобретению в клетке-хозяине, для экспрессии пептида по настоящему изобретению в клетке-хозяине, или для введения полинуклеотида по настоящему изобретению для генотерапии.
Когда E. coli является клеткой-хозяином и вектор амплифицируют в большом количестве в E. coli (например, JM109, DH5-альфа, HB101 или XL1-Blue), вектор должен иметь «точку начала репликации» для амплификации в E. coli и маркерный ген для селекции трансформированных E. coli (например, ген резистентности к лекарственному средству, отбирающий по лекарственному средству, такому как ампициллин, тетрациклин, канамицин, хлорамфеникол). Например, можно использовать векторы серии M13, векторы серии pUC, pBR322, pBluescript, pCR-Script и т.п. Кроме того, для клонирования можно использовать pGEM-T, pDIRECT и pT7, а также вышеуказанные векторы. Когда вектор используют для продукции пептида по настоящему изобретению, можно использовать экспрессирующий вектор. Например, экспрессирующий вектор для экспрессии в E. coli должен иметь вышеуказанные характеристики для амплификации в E. coli. Когда E. coli, такие как JM109, DH5-альфа, HB101 или XL1-Blue используют в качестве клетки-хозяина, вектор должен иметь промотор, например, промотор lacZ (Ward et al., Nature, 1989, 341: 544-6; FASEB J, 1989, 6: 2422-7), промотор araB (Better et al., Science, 1988, 240: 1041-3), промотор T7 или т.п., который может эффективно экспрессировать желаемый ген в E. coli. В этом отношении вместо вышеуказанных векторов можно использовать, например, pGEX-5X-1 (Pharmacia), "QIAexpress system" (Qiagen), pEGFP и pET (в этом случае, хозяином предпочтительно являются BL21, которые экспрессируют РНК-полимеразу T7). Дополнительно, вектор может содержать сигнальную последовательность для секреции пептида. Иллюстративной сигнальной последовательностью, которая направляет пептид для секреции в периплазматическое пространство E. Coli, является сигнальная последовательность pelB (Lei et al., J Bacteriol, 1987, 169: 4379). Способы для введения векторов в целевые клетки-хозяева включают, например, способ с хлоридом кальция и способ электропорации.
В дополнение к E. coli, для получения полипептида по настоящему изобретению можно использовать, например, экспрессирующие векторы, полученные от млекопитающих (например, pcDNA3 (Invitrogen) и pEGF-BOS (Nucleic Acids Res, 1990, 18(17): 5322), pEF, pCDM8), экспрессирующие векторы, полученные из клеток насекомых (например, "экспрессирующая бакуловирусная система Bac-to-BAC" (GIBCO BRL), pBacPAK8), экспрессирующие векторы, полученные из растений (например, pMH1, pMH2), экспрессирующие векторы, полученные из вирусов животных (например, pHSV, pMV, pAdexLcw), экспрессирующие векторы, полученные из ретровирусов (например, pZIpneo), экспрессирующие векторы, полученные из дрожжей (например, "Pichia Expression Kit" (Invitrogen), pNV11, SP-Q01) и экспрессирующие векторы, полученные из Bacillus subtilis (например, pPL608, pKTH50).
Для того чтобы экспрессировать вектор в клетках животных, таких как клетки CHO, COS или NIH3T3, вектор должен нести промотор, необходимый для экспрессии в таких клетках, например, промотор SV40 (Mulligan et al., Nature, 1979, 277: 108)), промотор MMLV-LTR, промотор EF1-альфа (Mizushima et al., Nucleic Acids Res, 1990, 18: 5322), промотор CMV и т.п., и предпочтительно маркерный ген для селекции трансформантов (например, ген резистентности к лекарственному средству, отбирающий по лекарственному средству (например, неомицину, G418)). Примеры известных векторов с этими характеристиками включают, например, pMAM, pDR2, pBK-RSV, pBK-CMV, pOPRSV и pOP13.
Варианты осуществления настоящего изобретения проиллюстрированы ниже на основании вышеизложенного объяснения, однако настоящее изобретение не ограничено этими вариантами осуществления.
[1] Пептид менее чем из 15 аминокислот со способностью индуцировать цитотоксическую T-клетку (ЦТЛ), который содержит аминокислотную последовательность, выбранную из группы, состоящей из:
(a) аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61; и
(b) аминокислотной последовательности, в которой одна, две или несколько аминокислот замещены, удалены, вставлены и/или добавлены к аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61.
[2] Пептид из [1], который выбран из группы, состоящей из нижеизложенных от (i) до (ii):
(i) пептид, содержащий аминокислотную последовательность, включающую одну или несколько замен, выбранных из группы, состоящей из нижеизложенных от (a) до (c), в аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOs: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45 и 46:
(a) первая аминокислота с N-конца замещена аминокислотой, выбранной из группы, состоящей из аспарагиновой кислоты и глутаминовой кислоты;
(b) вторая аминокислота с N-конца замещена аминокислотой, выбранной из группы, состоящей из фенилаланина, тирозина, аланина, изолейцина, лейцина и валина; и
(c) С-концевая аминокислота замещена аминокислотой, выбранной из группы, состоящей из аргинина и лизина; и
(ii) пептид, содержащий аминокислотную последовательность, в которой одна или несколько замен, выбранных из группы, состоящей из нижеизложенных от (a) до (c), введены в аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 48, 49, 50, 52, 53, 55, 20, 56, 57, 58, 59, 60 и 61:
(a) вторая аминокислота с N-конца замещена аминокислотой, выбранной из группы, состоящей из треонина и серина;
(b) третья аминокислота с N-конца замещена аминокислотой, выбранной из группы, состоящей из аспарагиновой кислоты и глутаминовой кислоты; и
(c) С-концевая аминокислота замещена тирозином.
[3] Пептид из [1], который состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61.
[4] Полинуклеотид, который кодирует пептид по любому из пп. с [1] до [3].
[5] Композиция, содержащая фармацевтически приемлемый носитель и, по меньшей мере, один ингредиент, выбранный из группы, состоящей из нижеизложенных от (a) до (e):
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA; и
(e) ЦТЛ, который нацелен на пептид по любому из пп. с [1] до [3].
[6] Композиция по п. [5], которая является композицией для индуцирования ЦТЛ, где ингредиент представляет собой, по меньшей мере, один ингредиент, выбранный из группы, состоящей из из нижеизложенных от (a) до (d):
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA.
[7] Композиция по п. [5], которая является фармацевтической композицией.
[8] Композиция по п. [7], которая является фармацевтической композицией для одного или нескольких применений, выбранных из группы, состоящей из (i) лечения злокачественных опухолей, (ii) предупреждения (профилактики) злокачественной опухоли и (iii) предупреждения (профилактики) послеоперационного рецидива злокачественной опухоли.
[9] Композиция по п. [7], которая предназначена для индуцирования иммунного ответа против злокачественной опухоли.
[10] Композиция по п. [8] или [9], где злокачественная опухоль выбрана из группы, включающей острый миелоидный лейкоз, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, хронический миелолейкоз (ХМЛ), рак толстого кишечника, рак пищевода, рак желудка, диффузный рак желудка, немелкоклеточный рак легких (NSCLC), лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак почки, мелкоклеточный рак легких (SCLC), опухоль мягких тканей и рак яичка.
[11] Композиция по любому из пп. с [5] до [10], которую формулируют для введения индивидууму, положительному, по меньшей мере, по одному HLA, выбранному из группы, состоящей из HLA-A33 и HLA-A01.
[12] Способ индуцирования АПК со способностью индуцировать ЦТЛ, который включает этап, выбранный из группы, состоящей из нижеизложенных:
(a) контакт АПК с пептидом по любому из пп. с [1] до [3] in vitro, ex vivo или in vivo; и
(b) введение полинуклеотида, кодирующего пептид по любому из пп. с [1] до [3], в АПК.
[13] Способ индуцирования ЦТЛ, который включает этап, выбранный из группы, состоящей из нижеизложенных от (a) до (c):
(a) совместное культивирование CD8-положительной T-клетки/клеток с АПК, которые презентируют на своей поверхности комплекс из антигена HLA и пептида по любому из пп. с [1] до [3];
(b) совместное культивирование CD8-положительной T-клетки/клеток с экзосомой/экзосомами, которые презентируют на своей поверхности комплекс из антигена HLA и пептида по любому из пп. с [1] до [3]; и
(c) введение в CD8-положительную T-клетку/клетки полинуклеотида, кодирующего каждую субъединицу T-клеточного рецептора (TCR), способного связываться с пептидом по любому из пп. с [1] до [3], презентированным при помощи антигена HLA на клеточной поверхности.
[14] АПК, которая презентирует на своей поверхности комплекс из антигена HLA и пептида по любому из пп. с [1] до [3].
[15] АПК по п. [14], которая индуцирована при помощи способа из п. [12].
[16] ЦТЛ, которая нацелена на пептид по любому из пп. с [1] до [3].
[17] ЦТЛ из п. [16], которая индуцирована при помощи способа из п. [13].
[18] Способ индуцирования иммунного ответа против злокачественной опухоли, который включает введение индивидууму, по меньшей мере, одного ингредиента, выбранного из группы, состоящей из нижеизложенных с (a) по (e):
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA; и
(e) ЦТЛ, который нацелен на пептид по любому из пп. с [1] до [3].
[19] Способ лечения и/или профилактики злокачественной опухоли, и/или профилактики ее послеоперационного рецидива, который включает введение индивидууму, по меньшей мере, одного ингредиента, выбранного из группы, состоящей из нижеизложенных пп. с (a) по (e):
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA; и
(e) ЦТЛ, который нацелен на пептид по любому из пп. с [1] до [3].
[20] Антитело, которое связывается с пептидом по любому из пп. с [1] до [3].
[21] Способ скрининга на пептид со способностью индуцировать ЦТЛ, который включает этапы:
(a) создания кандидатных последовательностей, состоящих из аминокислотной последовательности, в которой один, два, или несколько аминокислотных остатков замещены, удалены, вставлены и/или добавлены по сравнению с исходной аминокислотной последовательностью, состоящей из аминокислотной последовательности, выбранной из SEQ ID NO: 1, 2, 3, 6, 7, 11, 12, 17, 18, 20, 22, 24, 26, 32, 33, 36, 39, 41, 42, 45, 46, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61;
(b) отбора в кандидатных последовательностях, полученных в (a), кандидатной последовательности, которая не имеет значительной гомологии (идентичности последовательности) с любым известным продуктом гена человека, за исключением FOXM1;
(c) контакта пептида, состоящего из кандидатной последовательности, выбранной в (b), с АПК;
(d) контакта АПК из (c) с CD8-положительной T-клеткой/клетками; и
(e) отбора пептида, который имеет равную или более высокую способность индуцировать ЦТЛ, по сравнению с пептидом, состоящим из исходной аминокислотной последовательности.
[22] Применение, по меньшей мере, одного активного ингредиента выбранного из группы, состоящей из нижеизложенных пп. с (a) по (e), в производстве композиции для индуцирования иммунного ответа против злокачественной опухоли:
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA; и
(e) ЦТЛ, который нацелен на пептид по любому из пп. с [1] до [3].
[23] Применение, по меньшей мере, одного ингредиента выбранного из группы, состоящей из нижеизложенных пп. с (a) по (e), в производстве фармацевтической композиции для лечения и/или профилактики злокачественной опухоли, и/или профилактики ее послеоперационного рецидива:
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA; и
(e) ЦТЛ, который нацелен на пептид по любому из пп. с [1] до [3].
[24] Применение, по меньшей мере, одного ингредиента выбранного из группы, состоящей из нижеизложенных пп. с (a) по (e), для индуцирования иммунного ответа против злокачественной опухоли:
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA; и
(e) ЦТЛ, который нацелен на пептид по любому из пп. с [1] до [3].
[25] Применение, по меньшей мере, одного ингредиента выбранного из группы, состоящей из нижеизложенных пп. с (a) по (e), для лечения и/или профилактики злокачественной опухоли, и/или профилактики ее послеоперационного рецидива:
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA; и
(e) ЦТЛ, который нацелен на пептид по любому из пп. с [1] до [3].
[26] Способ индуцирования цитотоксической активности против FOXM1-экспрессирующей клетки/клеток, который включает этап введения индивидууму, по меньшей мере, одного ингредиента, выбранного из группы, состоящей из нижеизложенных пп. с (a) по (e):
(a) один или несколько типов пептидов по любому из пп. с [1] до [3];
(b) один или несколько типов полинуклеотидов, кодирующих пептид(-ы) по любому из пп. с [1] до [3] в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. с [1] до [3] и антигена HLA; и
(e) ЦТЛ, который нацелен на пептид по любому из пп. с [1] до [3].
[27] Лиофилизированный состав, содержащий один или несколько типов пептидов по любому из пп. с [1] до [3].
[28] Фармацевтическая композиция, которую получают способом, включающим растворение одного или нескольких типов пептидов по любому из пп. с [1] до [3] в водорастворимом носителе, и проведение стерилизации фильтрованием.
[29] Водный раствор, стерилизованный фильтрованием, который представляет собой водный раствор, содержащий один или несколько типов пептидов по любому из пп. с [1] до [3] и водорастворимый носитель.
[30] Эмульсия, содержащая один или несколько типов пептидов по любому из пп. с [1] до [3], водорастворимый носитель и масляный адъювант.
[31] Набор, включающий контейнер, который содержит композицию по любому из пп. с [5] по [11], и контейнер, который содержит адъювант.
[32] Набор, включающий контейнер, в котором находится лиофилизированный состав, содержащий пептид по любому из пп. с [1] до [3], контейнер, в котором находится адъювант, и контейнер, в котором находится раствор для повторного растворения лиофилизированного состава.
Настоящее изобретение поясняется в настоящем документе подробно со ссылкой на его конкретные варианты осуществления. Однако следует понимать, что вышеизложенное объяснение по факту является иллюстративным и пояснительным, и предназначено для объяснения настоящего изобретения и его предпочтительных вариантов осуществления. Путем общепринятого экспериментирования, специалист в данной области легко поймет, что можно производить различные изменения и модификации в пределах сущности и объема настоящего изобретения. Таким образом, настоящее изобретение не ограничивается вышеизложенным разъяснением, а определяется прилагаемой формулой изобретения и ее эквивалентами.
Здесь и далее, настоящее изобретение более подробно описано со ссылкой на примеры. Однако, хотя последующие материалы, способ и примеры могут помочь специалисту в производстве и использовании определенных вариантов настоящего изобретения, они существуют только для иллюстрации аспектов настоящего изобретения, и, таким образом, никоим образом не ограничивают объем настоящего изобретения. Специалист в данной области может использовать способы и материалы, аналогичные или эквивалентные тем, что описаны в настоящем документе, в практическом осуществлении или испытаниях по настоящему изобретению.
Все документы по известному уровню техники, процитированные в настоящем документе, включены посредством ссылки в настоящее описание.
Примеры
[Пример 1]
Материалы и способы
Линии клеток
Клетки C1R, HLA-A- и HLA-B-негативную В-лимфобластную линию клеток человека, и клетки COS7, линию клеток почки африканской зеленой мартышки, приобретали у ATCC.
Создание клеток-мишеней со стабильной экспрессией HLA-A*33:03
Клетки C1R (C1R-A33), которые стабильно экспрессируют HLA-A*33:03, использовали в качестве клеток-стимуляторов ЦТЛ. Амплифицировали путем ПЦР кДНК, кодирующую ген HLA-A*33:03, и клонировали в экспрессирующий вектор. Клетки C1R, в которые был введен экспрессирующий вектор с геном HLA-A*33:03, культивировали с отбором по чувствительности к лекарственному препарату в течение двух недель в среде, содержащей G418 (Invitrogen). Суспензию G418-устойчивых клеток C1R разводили, высевали в 96-луночный планшет и дополнительно селективно культивировали в течение 30 суток в среде для культивирования с G418. Экспрессию HLA-A*33:03 в клетках C1R подтверждали анализом проточной цитометрии.
Селекция пептидов, полученных из FOXM1
Девяти- и десятимерные пептиды, полученные из FOXM1, которые, как ожидают, будут связываться с молекулой HLA-A*33:03, определяли при помощи сервера для предсказания связывания «NetMHC pan2.8» (www.cbs.dtu.dk/services/NetMHCpan-2.8/) (Buus et al., Tissue Antigens. 2003, 62(5): 378-84; Nielsen et al., Protein Sci. 2003, 12(5): 1007-17; Bioinformatics. 2004, 20(9): 1388-97).
Пептидный синтез
Пептиды синтезировали в American Пептид Company (Sunnyvale, CA) в соответствии со стандартным способом синтеза на твердой фазе, и очищали при помощи обратно-фазовой высокоэффективной жидкостной хроматографии (ВЭЖХ). Качество пептидов (чистота от 90% или выше) было гарантировано путем ВЭЖХ и масс-спектрометрии. Пептиды растворяли в диметилсульфоксиде (конечная концентрация: 20 мг/мл) и хранили при -80°C.
Индукция ЦТЛ in vitro
Дендритные клетки (DC) моноцитарного происхождения использовали в качестве антигенпрезентирующей клетки для того чтобы индуцировать специфический ответ цитотоксического T-лимфоцита (ЦТЛ) против пептидов, презентированных на лейкоцитарных антигенах человека (HLA). Как уже описано в литературе, DC получали in vitro (Nakahara S et al., Cancer Res 2003, 63(14): 4112-8). Конкретно, мононуклеарные клетки периферической крови (PBMC), выделенные у здоровых добровольцев (HLA-A*33:03-положительных) при помощи раствора Фиколл-Пак плюс (Pharmacia) высевали на пластиковые чашки для тканевой культуры (Corning), чтобы позволить PBMC прикрепиться к чашкам. Их культивировали в присутствии 1000 МЕ/мл гранулоцитарно-макрофагального колониестимулирующего фактора (R&D System) и 1000 МЕ/мл интерлейкина(IL)-4 (R&D System) в течение семи суток. В качестве среды использовали среду AIM-V (Invitrogen), содержащую 2% инактивированной сыворотки АВ-типа (AВS). DC, которые были активированы цитокинами для того чтобы отличить их от моноцитов, были активированы 20 мкг/мл каждого из синтезированных пептидов (37 градусов C, три часа). Активацию пептидами проводили в среде AIM-V, содержащей 3 мкг/мл бета 2-микроглобулина. Эти активированные пептидами DC были инактивированы рентгеновским облучением (20 Гр), смешаны в соотношении 1:20 с аутологичными CD8+ T-клетками, полученными путем положительной селекции при помощи CD8 Positive Isolation Kit (Invitrogen) (1,5×104 DC и 3×105 CD8+-положительных T-клеток) и их культивировали в 48-луночном планшете (Corning). Каждая лунка содержала 0,5 мл среды 5% ABS/AIM-V, и в каждую лунку был добавлен IL-7 (R&D System) (конечная концентрация: 10 нг/мл). Через два дня после начала культивирования добавляли IL-2 (конечная концентрация 20 МЕ/мл). На сутки 7 и сутки 14 культивирования, CD8+-положительные T-клетки дополнительно стимулировали DC, активированными пептидами. DC готовили ко времени использования тем же способом, что и вышеописанный. После суток 21 (после трех стимуляций DC) подтверждали выработку IFN-гамма против активированных пептидами C1R-A33 с использованием метода иммуноферментных пятен(ELISPOT) для человеческого интерферона(IFN)-гамма (Tanaka H et al., Br J Cancer 2001, 84(1): 94-9; Umano Y et al., Br J Cancer 2001, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004, 10(24): 8577-86; Suda T et al., Cancer Sci 2006, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005, 96(8): 498-506).
Способ наращивания ЦТЛ
ЦТЛ наращивали при помощи способов, аналогичных, описанным у Riddell et al. (Walter EA et al., N Engl J Med 1995, 333(16): 1038-44; Riddell SR et al., Nat Med 1996, 2(2): 216-23). ЦТЛ культивировали в 25 мл среды 5% ABS/AIM-V вместе с двумя типами В-лимфобластных клеточных линий человека, обработанных митомицином C (5×106 клеток/25мл среды каждая) и антитела к CD3 (конечная концентрация: 40 нг/мл). Через сутки после начала культивирования к культуре добавляли IL-2 (конечная концентрация: 120 МЕ/мл). На сутки 5, 8 и 11 среду меняли на среду 5% ABS/AIM-V, содержащую IL-2 (конечная концентрация: 30 МЕ/мл) (Tanaka H et al., Br J Cancer 2001, 84(1): 94-9; Umano Y et al., Br J Cancer 2001, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004, 10(24): 8577-86; Suda T et al., Cancer Sci 2006, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005, 96(8): 498-506)
Создание клонов ЦТЛ
После индукции ЦТЛ in vitro, ЦТЛ высаживали на 96-луночные круглодонные планшеты для микротитрования (Nalge Nunc International) в концентрации 1 клетка/на лунку или 10 клеток/на лунку. ЦТЛ культивировали с двумя типами В-лимфобластных клеточных линий человека, обработанных митомицином C (1×104 клеток/лунку каждая) в общем объеме 150 мкл/лунку среды 5% ABS/AIM-V с антителом к CD3 (конечная концентрация: 30 нг/мл) и IL-2 (конечная концентрация: 125 МЕ/мл). Через десять суток к среде добавляли 500 МЕ/мл IL-2 в 50 мкл среды 5% ABS/AIM-V. На сутки 14 или позже, ЦТЛ, которые продемонстрировали пептид-специфическую выработку IFN-гамма в анализе ELISPOT, наращивали с использованием способа, аналогичного описанному выше (Uchida N et al., Clin Cancer Res 2004, 10(24): 8577-86; Suda T et al., Cancer Sci 2006, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005, 96(8): 498-506).
Подтверждение выработки IFN-гамма
Для подтверждения пептид-специфической выработки IFN-гамма ЦТЛ, индуцированных пептидом, проводили анализы ELISPOT и ELISA для IFN-гамма. Активированные пептидами C1R-А01 (1×104 клеток/лунку) готовили в качестве клеток-мишеней. Анализы ELISPOT и ELISA для IFN-гамма проводили в соответствии с руководством производителя к набору для анализа.
Получение клеток-мишеней, принудительно экспрессирующих FOXM1 и HLA-A*33:03
кДНК, кодирующую ген FOXM1 или HLA-A*33:03, амплифицировали при помощи ПЦР. Амплифицированный продукт клонировали в экспрессирующий вектор. Вектор, экспрессирующий FOXM1 и вектор, экспрессирующий HLA-A*33:03, вместе или по отдельности были трансфецированы в клетки COS7, которые представляют собой линию клеток, отрицательную по HLA, с использованием липофектамина 2000 (Invitrogen). Через день после трансфекции, клетки COS7 отделяли и собирали с использованием версена (Invitrogen) и использовали в качестве клеток-мишеней для подтверждения выработки IFN-гамма (5×104 клетки/лунку).
Результаты
Предсказание пептидов, полученных из FOXM1 и связывающихся с HLA-A*33:03
Таблицы 1a и 1b показывают девятимерные и десятимерные пептиды, полученные из FOXM1, которые были теоретически рассчитаны как связывающиеся с HLA-A*33:03 при помощи «NetMHC pan2.8», в порядке уменьшения аффинности связывания. Всего в качестве эпитопных кандидатных пептидов были использованы 47 пептидов, которые потенциально обладают свойством связываться с HLA-A*33:03.

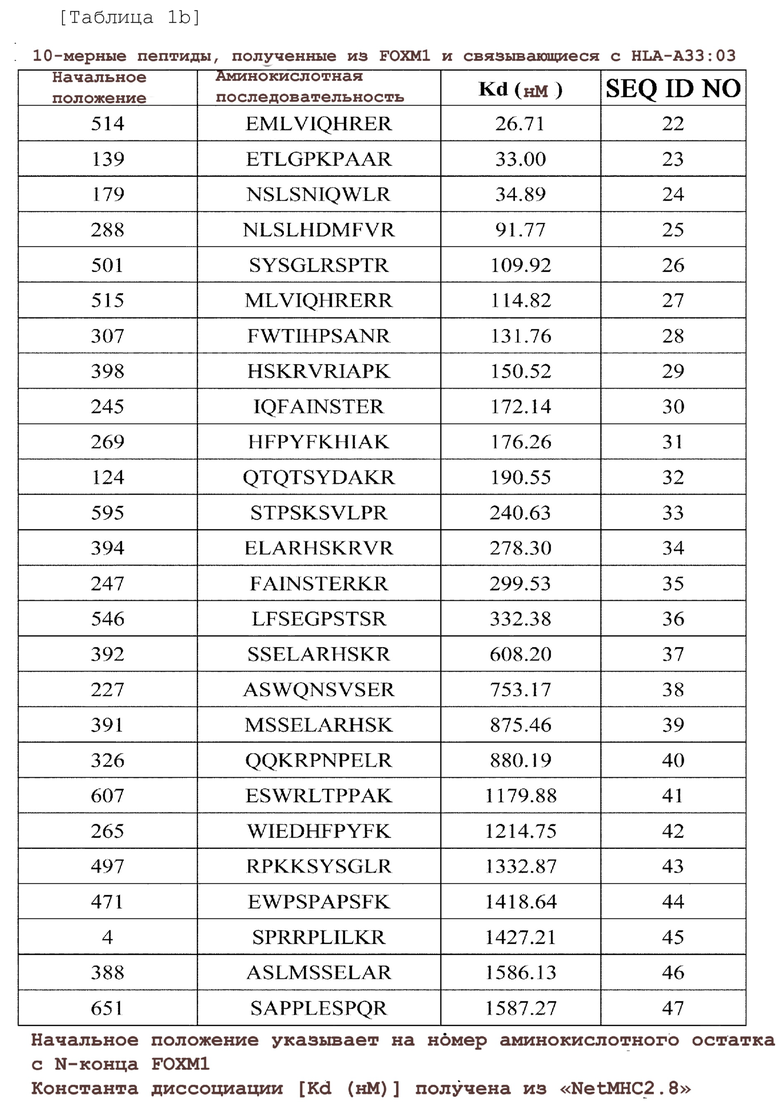
Индуцирование ЦТЛ теоретически рассчитанными пептидами, полученными из FOXM1 и рестриктированными по HLA-A*33:03
ЦТЛ, специфические к пептидам, полученным из FOXM1, индуцировали в соответствии с протоколом, описанным в «Материалах и способах». Пептид-специфическую выработку IFN-гамма подтверждали путем анализа ELISPOT (фиг. 1). Пептид-специфическую выработку IFN-гамма наблюдали в Лунке #6 c FOXM1-A33-9-180 (SEQ ID NO: 1) (a),
Лунке #3 c FOXM1-A33-9-308 (SEQ ID NO: 2) (b),
Лунке #4 c FOXM1-A33-9-693 (SEQ ID NO: 3) (c),
Лунке #3 c FOXM1-A33-9-516 (SEQ ID NO: 6) (d),
Лунке #5 c FOXM1-A33-9-146 (SEQ ID NO: 7) (e),
Лунке #6 c FOXM1-A33-9-289 (SEQ ID NO: 11) (f),
Лунке #6 c FOXM1-A33-9-228 (SEQ ID NO: 12) (g),
Лунке #4 c FOXM1-A33-9-502 (SEQ ID NO: 17) (h),
Лунке #2 c FOXM1-A33-9-321 (SEQ ID NO: 18) (i),
Лунке #6 c FOXM1-A33-9-341 (SEQ ID NO: 20) (j),
Лунке #8 c FOXM1-A33-10-514 (SEQ ID NO: 22) (k),
Лунке #6 c FOXM1-A33-10-179 (SEQ ID NO: 24) (l),
Лунке #5 c FOXM1-A33-10-501 (SEQ ID NO: 26) (m),
Лунке #5 c FOXM1-A33-10-124 (SEQ ID NO: 32) (n),
Лунке #3 c FOXM1-A33-10-595 (SEQ ID NO: 33) (o),
Лунке #5 c FOXM1-A33-10-546 (SEQ ID NO: 36) (p),
Лунке #6 c FOXM1-A33-10-391 (SEQ ID NO: 39) (q),
Лунке #3 c FOXM1-A33-10-607 (SEQ ID NO: 41) (r),
Лунке #2 c FOXM1-A33-10-265 (SEQ ID NO: 42) (s),
Лунке #6 c FOXM1-A33-10-4 (SEQ ID NO: 45) (t) b
Лунке #5 c FOXM1-A33-10-388 (SEQ ID NO: 46) (u). Кроме этого, не наблюдали специфической выработки IFN-гамма против других пептидов, показанных в таблицах 1a и 1b. Например, не наблюдали специфической выработки IFN-гамма против FOXM1-A33-10-288 (SEQ ID NO: 25) (v). В результате, хотя все пептиды имели потенциал связывания с HLA-A*33:03, отобрали 21 пептид в качестве пептидов со способностью индуцировать ЦТЛ.
Получение линий и клонов ЦТЛ, специфичных к пептидам, полученным из FOXM1 и рестриктированным по HLA-A*33:03
Линии ЦТЛ получали, наращивая клетки в лунке #3 с FOXM1-A33-9-308 (SEQ ID NO: 2) (a), лунке #5 с FOXM1-A33-9-146 (SEQ ID NO: 7) (b), лунке #6 с FOXM1-A33-10-391 (SEQ ID NO: 39) (c) и лунке #2 с FOXM1-A33-10-265 (SEQ ID NO: 42) (d) из анализа ELISPOT для IFN-гамма. В результате измерения IFN-гамма путем ELISA, наблюдали выработку IFN-гамма ЦТЛ против клеток-мишеней (C1R-A33), активированных при помощи лунки #3 с FOXM1-A33-9-308 (SEQ ID NO: 2) (a), лунки #5 с FOXM1-A33-9-146 (SEQ ID NO: 7) (b), лунки #6 с FOXM1-A33-10-391 (SEQ ID NO: 39) (c), или FOXM1-A33-10-265 (SEQ ID NO: 42) (Фиг. 2). Дополнительно, клоны ЦТЛ получали способом серийных разведений, как описано в разделе «Материалы и способы» выше. В результате измерения IFN-гамма путем ELISA, клоны ЦТЛ, стимулированные FOXM1-A33-9-308 (SEQ ID NO: 2) (a) или FOXM1-A33-9-146 (SEQ ID NO: 7) (b) показали пептид-специфическую выработку IFN-гамма (Фиг. 3).
Выработка IFN-гамма против клеток-мишеней, экспрессирующих FOXM1 и HLA-A*33:03
Исследовали выработку IFN-гамма клоном ЦТЛ, специфическим по FOXM1-A33-9-308 (SEQ ID NO: 2), против клеток-мишеней, экспрессирующих FOXM1 и HLA-A*33:03. Клетки COS7, трансфецированные и FOXM1, и HLA-A*33:03, получали в качестве клеток-мишеней. Клетки COS7, транфецированные или FOXM1, или HLA-A*33:03, получали в качестве отрицательного клеточного контроля. Клон ЦТЛ, специфический по FOXM1-A33-9-308 (SEQ ID NO: 2), показал выработку IFN-гамма против клеток COS7, экспрессирующих и FOXM1, и HLA-A*33:03 (фиг. 4). С другой стороны, не было выявлено значительной выработки IFN-гамма против отрицательных клеточных контролей. Это ясно доказывает, что FOXM1-A33-9-308 (SEQ ID NO: 2) представляет собой пептид, полученный в результате антигенного процессинга, и он презентируется на клетках-мишенях при помощи молекулы HLA-A*33:03 и распознается ЦТЛ. Этот результат подтверждает, что FOXM1-A33-9-308 (SEQ ID NO: 2) может быть полезен в качестве противораковой вакцины для пациентов с повышенной экспрессией FOXM1 в злокачественных клетках.
Анализ гомологии антигенных пептидов
Было подтверждено, что FOXM1-A33-9-180 (SEQ ID NO: 1), FOXM1-A33-9-308 (SEQ ID NO: 2), FOXM1-A33-9-693 (SEQ ID NO: 3), FOXM1-A33-9-516 (SEQ ID NO: 6), FOXM1-A33-9-146 (SEQ ID NO: 7), FOXM1-A33-9-289 (SEQ ID NO: 11), FOXM1-A33-9-228 (SEQ ID NO: 12), FOXM1-A33-9-502 (SEQ ID NO: 17), FOXM1-A33-9-321 (SEQ ID NO: 18), FOXM1-A33-9-341 (SEQ ID NO: 20), FOXM1-A33-10-514 (SEQ ID NO: 22), FOXM1-A33-10-179 (SEQ ID NO: 24), FOXM1-A33-10-501 (SEQ ID NO: 26), FOXM1-A33-10-124 (SEQ ID NO: 32), FOXM1-A33-10-595 (SEQ ID NO: 33), FOXM1-A33-10-546 (SEQ ID NO: 36), FOXM1-A33-10-391 (SEQ ID NO: 39), FOXM1-A33-10-607 (SEQ ID NO: 41), FOXM1-A33-10-265 (SEQ ID NO: 42), FOXM1-A33-10-4 (SEQ ID NO: 45) и FOXM1-A33-10-388 (SEQ ID NO: 46) могут индуцировать CTL, показывающие пептид-специфическую выработку IFN-гамма. Таким образом, для того чтобы подтвердить, что последовательности FOXM1-A33-9-180 (SEQ ID NO: 1), FOXM1-A33-9-308 (SEQ ID NO: 2), FOXM1-A33-9-693 (SEQ ID NO: 3), FOXM1-A33-9-516 (SEQ ID NO: 6), FOXM1-A33-9-146 (SEQ ID NO: 7), FOXM1-A33-9-289 (SEQ ID NO: 11), FOXM1-A33-9-228 (SEQ ID NO: 12), FOXM1-A33-9-502 (SEQ ID NO: 17), FOXM1-A33-9-321 (SEQ ID NO: 18), FOXM1-A33-9-341 (SEQ ID NO: 20), FOXM1-A33-10-514 (SEQ ID NO: 22), FOXM1-A33-10-179 (SEQ ID NO: 24), FOXM1-A33-10-501 (SEQ ID NO: 26), FOXM1-A33-10-124 (SEQ ID NO: 32), FOXM1-A33-10-595 (SEQ ID NO: 33), FOXM1-A33-10-546 (SEQ ID NO: 36), FOXM1-A33-10-391 (SEQ ID NO: 39), FOXM1-A33-10-607 (SEQ ID NO: 41), FOXM1-A33-10-265 (SEQ ID NO: 42), FOXM1-A33-10-4 (SEQ ID NO: 45) и FOXM1-A33-10-388 (SEQ ID NO: 46) получены только из FOXM1, проводили анализ гомологии пептидных последовательностей с использованием алгоритма BLAST (blast.ncbi.nlm.nih.gov/Blast.cgi). В результате, последовательности FOXM1-A33-9-180 (SEQ ID NO: 1), FOXM1-A33-9-308 (SEQ ID NO: 2), FOXM1-A33-9-693 (SEQ ID NO: 3), FOXM1-A33-9-516 (SEQ ID NO: 6), FOXM1-A33-9-146 (SEQ ID NO: 7), FOXM1-A33-9-289 (SEQ ID NO: 11), FOXM1-A33-9-228 (SEQ ID NO: 12), FOXM1-A33-9-502 (SEQ ID NO: 17), FOXM1-A33-9-321 (SEQ ID NO: 18), FOXM1-A33-9-341 (SEQ ID NO: 20), FOXM1-A33-10-514 (SEQ ID NO: 22), FOXM1-A33-10-179 (SEQ ID NO: 24), FOXM1-A33-10-501 (SEQ ID NO: 26), FOXM1-A33-10-124 (SEQ ID NO: 32), FOXM1-A33-10-595 (SEQ ID NO: 33), FOXM1-A33-10-546 (SEQ ID NO: 36), FOXM1-A33-10-391 (SEQ ID NO: 39), FOXM1-A33-10-607 (SEQ ID NO: 41), FOXM1-A33-10-265 (SEQ ID NO: 42), FOXM1-A33-10-4 (SEQ ID NO: 45) и FOXM1-A33-10-388 (SEQ ID NO: 46) обнаружены только в FOXM1. Таким образом, как известно авторам настоящего изобретения, эти пептиды специфичны для FOXM1, так что практически не существует возможности того, что эти пептиды могли бы вызвать непреднамеренную иммунную реакцию против молекул, иных чем FOXM1 и уже известных тем, что они сенсибилизируют иммунную систему человека. Подводя итоги, были идентифицированы новые эпитопные пептиды, полученные из FOXM1 и рестриктированные по HLA-A*33:03. Было продемонстрировано, что эпитопные пептиды, полученные из FOXM1, применимы для иммунотерапии злокачественных опухолей.
[Пример 2]
Материалы и способы
Линии клеток
Клетки C1R, HLA-A- и HLA-B-негативную В-лимфобластную линию клеток человека, и клетки COS7, линию клеток почки африканской зеленой мартышки, приобретали у ATCC.
Создание клеток-мишеней со стабильной экспрессией HLA-A*01:01
Клетки C1R (C1R-A01), которые стабильно экспрессируют HLA-A*01:01, использовали в качестве клеток-стимуляторов ЦТЛ. Амплифицировали путем ПЦР кДНК, кодирующую ген HLA-A*01:01, и клонировали в экспрессирующий вектор. Клетки C1R, в которые был введен экспрессирующий вектор с геном HLA-A*01:01, культивировали с отбором по чувствительности к лекарственному препарату в течение двух недель в среде, содержащей G418 (Invitrogen). Суспензию G418-устойчивых клеток C1R разводили, высевали в 96-луночный планшет и дополнительно селективно культивировали в течение 30 суток в среде для культивирования с G418. Экспрессию HLA-A*01:01 в клетках C1R подтверждали анализом проточной цитометрии.
Селекция пептидов, полученных из FOXM1
Девяти- и десятимерные пептиды, полученные из FOXM1, которые, как ожидают, будут связываться с молекулой HLA-A*01:01, определяли при помощи сервера для предсказания связывания «NetMHC 3.4» (www.cbs.dtu.dk/services/NetMHC-3.4/) (Buus S et al., Tissue Antigens. 2003, 62(5): 378-84; Nielsen M et al., Protein Sci. 2003, 12(5): 1007-17; Nielsen M et al., Bioinformatics. 2004, 20(9): 1388-97).
Пептидный синтез
Пептиды синтезировали в American Пептид Company (Sunnyvale, CA) в соответствии со стандартным способом синтеза на твердой фазе, и очищали при помощи обратно-фазовой высокоэффективной жидкостной хроматографии (ВЭЖХ). Качество пептидов (чистота от 90% или выше) было гарантировано путем ВЭЖХ и масс-спектрометрии. Пептиды растворяли в диметилсульфоксиде (конечная концентрация: 20 мг/мл) и хранили при -80°C.
Индукция ЦТЛ in vitro
Дендритные клетки (DC) моноцитарного происхождения использовали в качестве антигенпрезентирующей клетки для того чтобы индуцировать специфический ответ цитотоксического T-лимфоцита (ЦТЛ) против пептидов, презентированных на лейкоцитарных антигенах человека (HLA). Как уже описано в литературе, DC получали in vitro (Nakahara S et al., Cancer Res 2003, 63(14): 4112-8). Конкретно, мононуклеарные клетки периферической крови (PBMC), выделенные у здоровых добровольцев (HLA-A*01:01-положительных) при помощи раствора Фиколл-Пак плюс (Pharmacia) высевали на пластиковые чашки для тканевой культуры (Corning), чтобы позволить PBMC прикрепиться к чашкам. Их культивировали в присутствии 1000 МЕ/мл гранулоцитарно-макрофагального колониестимулирующего фактора (R&D System) и 1000 МЕ/мл интерлейкина(IL)-4 (R&D System) в течение семи суток. В качестве среды использовали среду AIM-V (Invitrogen), содержащую 2% инактивированной сыворотки АВ-типа (AВS). DC, которые были активированы цитокинами для того чтобы отличить их от моноцитов, были активированы 20 мкг/мл каждого из синтезированных пептидов (37 градусов C, три часа). Активацию пептидами проводили в среде AIM-V, содержащей 3 мкг/мл бета 2-микроглобулина. Эти активированные пептидами DC были инактивированы рентгеновским облучением (20 Гр), смешаны в соотношении 1:20 с аутологичными CD8+ T-клетками, полученными путем положительной селекции при помощи CD8 Positive Isolation Kit (Invitrogen) (1,5×104 DC и 3×105 CD8+-положительных T-клеток)и культивировали в 48-луночном планшете (Corning). Каждая лунка содержала 0,5 мл среды 5% ABS/AIM-V, и в каждую лунку был добавлен IL-7 (R&D System) (конечная концентрация: 10 нг/мл). Через два дня после начала культивирования добавляли IL-2 (конечная концентрация 20 МЕ/мл). На сутки 7 и сутки 14 культивирования, CD8+-положительные T-клетки дополнительно стимулировали DC, активированными пептидами. DC готовили ко времени использования тем же способом, что и вышеописанный. После суток 21 (после трех стимуляций DC) подтверждали выработку IFN-гамма против активированных пептидами C1R-A01 с использованием метода иммуноферментных пятен (ELISPOT) (Tanaka H et al., Br J Cancer 2001, 84(1): 94-9; Umano Y et al., Br J Cancer 2001, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004, 10(24): 8577-86; Suda T et al., Cancer Sci 2006, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005, 96(8): 498-506).
Способ наращивания ЦТЛ
ЦТЛ наращивали при помощи способов, аналогичных, описанным у Riddell et al. (Walter EA et al., N Engl J Med 1995, 333(16): 1038-44; Riddell SR et al., Nat Med 1996, 2(2): 216-23). ЦТЛ культивировали в 25 мл среды 5% ABS/AIM-V вместе с двумя типами В-лимфобластных клеточных линий человека, обработанных митомицином C (5×106 клеток/25мл среды каждая) и антитела к CD3 (конечная концентрация: 40 нг/мл). Через сутки после начала культивирования к культуре добавляли IL-2 (конечная концентрация: 120 МЕ/мл). На сутки 5, 8 и 11 среду меняли на среду 5% ABS/AIM-V, содержащую IL-2 (конечная концентрация: 30 МЕ/мл) (Tanaka H et al., Br J Cancer 2001, 84(1): 94-9; Umano Y et al., Br J Cancer 2001, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004, 10(24): 8577-86; Suda T et al., Cancer Sci 2006, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005, 96(8): 498-506)
Создание клонов ЦТЛ
После индукции ЦТЛ in vitro, ЦТЛ высаживали на 96-луночные круглодонные планшеты для микротитрования (Nalge Nunc International) в концентрации 1 клетка/на лунку или 10 клеток/на лунку. ЦТЛ культивировали с двумя типами В-лимфобластных клеточных линий человека, обработанных митомицином C (1×104 клеток/лунку каждая) в общем объеме 150 мкл/лунку среды 5% ABS/AIM-V с антителом к CD3 (конечная концентрация: 30 нг/мл) и IL-2 (конечная концентрация: 125 МЕ/мл). Через десять суток к среде добавляли 500 МЕ/мл IL-2 в 50 мкл среды 5% ABS/AIM-V. На сутки 14 или позже, ЦТЛ, которые продемонстрировали пептид-специфическую выработку IFN-гамма в анализе ELISPOT, наращивали с использованием способа, аналогичного описанному выше (Uchida N et al., Clin Cancer Res 2004, 10(24): 8577-86; Suda T et al., Cancer Sci 2006, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005, 96(8): 498-506).
Подтверждение выработки IFN-гамма
Для подтверждения пептид-специфической выработки IFN-гамма ЦТЛ, индуцированных пептидом, проводили анализы ELISPOT и ELISA для IFN-гамма. Активированные пептидами C1R-A01 (1×104 клеток/лунку) готовили в качестве клеток-мишеней. Анализы ELISPOT и ELISA для IFN-гамма проводили в соответствии с руководством производителя к набору для анализа.
Получение клеток-мишеней, принудительно экспрессирующих FOXM1 и HLA-A*01:01
кДНК, кодирующую ген FOXM1 или HLA-A*01:01, амплифицировали при помощи ПЦР. Амплифицированный продукт клонировали в экспрессирующий вектор. Вектор, экспрессирующий FOXM1 и вектор, экспрессирующий HLA-A*01:01, вместе или по отдельности были трансфецированы в клетки COS7, которые представляют собой линию клеток, отрицательную по HLA, с использованием липофектамина 2000 (Invitrogen). Через день после трансфекции, клетки COS7 отделяли и собирали с использованием версена (Invitrogen) и использовали в качестве клеток-мишеней для подтверждения выработки IFN-гамма (5×104 клетки/лунку).
Результаты
Отбор пептидов, полученных из FOXM1 и связывающихся с HLA-A*33:03
Таблицы 2a и 2b показывают девятимерные и десятимерные пептиды, полученные из FOXM1, которые были теоретически рассчитаны как связывающиеся с HLA-A*01:01 при помощи «NetMHC 3.4», в порядке уменьшения аффинности связывания. Всего в качестве эпитопных кандидатных пептидов были использованы 16 пептидов, которые потенциально обладают свойством связываться с HLA-A*01:01.
[Таблица 2a]
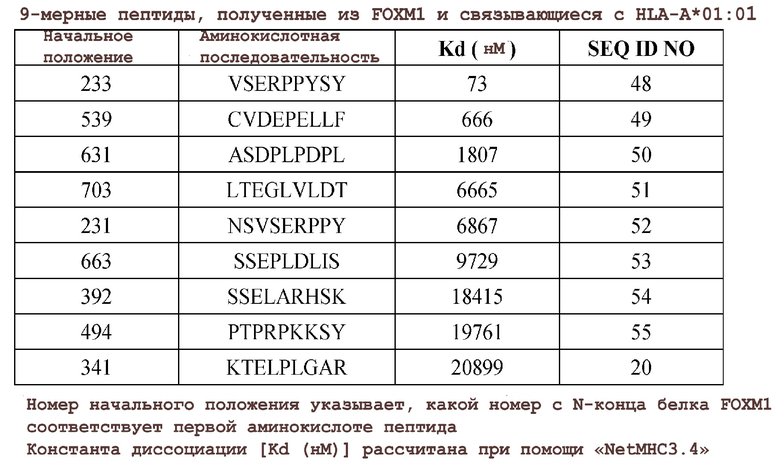
[Таблица 2b]

Индуцирование ЦТЛ теоретически рассчитанными пептидами, полученными из FOXM1 и рестриктированными по HLA-A*01:01
ЦТЛ, специфические к пептидам, полученным из FOXM1, индуцировали в соответствии с протоколом, описанным в «Материалах и способах». Пептид-специфическую выработку IFN-гамма подтверждали путем анализа ELISPOT (фиг. 5). Пептид-специфическую выработку IFN-гамма наблюдали в
Лунке #3 c FOXM1-A01-9-233 (SEQ ID NO: 48) (a),
Лунке #3 c FOXM1-A01-9-539 (SEQ ID NO: 49) (b),
Лунке #3 c FOXM1-A01-9-631 (SEQ ID NO: 50) (c),
Лунке #2 c FOXM1-A01-9-231 (SEQ ID NO: 52) (d),
Лунке #2 c FOXM1-A01-9-663 (SEQ ID NO: 53) (e),
Лунке #5 c FOXM1-A01-9-494 (SEQ ID NO: 55) (f),
Лунке #2 c FOXM1-A01-9-341 (SEQ ID NO: 20) (g),
Лунке #1 c FOXM1-A01-10-566 (SEQ ID NO: 56) (h),
Лунке #2 c FOXM1-A01-10-263 (SEQ ID NO: 57) (i),
Лунке #4 c FOXM1-A01-10-308 (SEQ ID NO: 58) (j),
Лунке #6 c FOXM1-A01-10-232 (SEQ ID NO: 59) (k),
Лунке #6 c FOXM1-A01-10-663 (SEQ ID NO: 60) (l) и
Лунке #6 c FOXM1-A01-10-341 (SEQ ID NO: 61) (m). Кроме этого, не наблюдали специфической выработки IFN-гамма против других пептидов, показанных в таблицах 2a и 2b. Например, не наблюдали специфической выработки IFN-гамма против FOXM1-A01-10-265 (SEQ ID NO: 42) (n). В результате, хотя все пептиды имели потенциал связывания с HLA-A*01:01, отобрали 13 пептидов в качестве пептидов со способностью индуцировать ЦТЛ.
Получение линий и клонов ЦТЛ, специфичных к пептидам, полученным из FOXM1 и рестриктированным по HLA-A*01:01
Линии ЦТЛ получали, наращивая клетки в лунке #1, которая показала специфическую выработку IFN-гамма против FOXM1-A01-10-566 (SEQ ID NO: 56) в анализе ELISPOT для IFN-гамма. В результате измерения IFN-гамма путем ELISA, наблюдали выработку IFN-гамма линиями ЦТЛ против клеток-мишеней (C1R-A01), активированных FOXM1-A01-10-566 (SEQ ID NO: 56) (Фиг. 6). Дополнительно, клоны ЦТЛ получали способом серийных разведений. В результате измерения IFN-гамма путем ELISA, клоны ЦТЛ, стимулированные FOXM1-A01-9-233 (SEQ ID NO: 48) (a) или FOXM1-A01-10-566 (SEQ ID NO: 56) (b) показали пептид-специфическую выработку IFN-гамма (Фиг. 7).
Выработка IFN-гамма против клеток-мишеней, экспрессирующих FOXM1 и HLA-A*01:01
Исследовали выработку IFN-гамма клоном ЦТЛ, специфическим по FOXM1-A01-10-566 (SEQ ID NO: 56), против клеток-мишеней, экспрессирующих FOXM1 и HLA-A*01:01. Клетки COS7, трансфецированные и FOXM1, и HLA-A*01:01, получали в качестве клеток-мишеней. Клетки COS7, транфецированные или FOXM1, или HLA-A*01:01, получали в качестве отрицательного клеточного контроля. Клон ЦТЛ, специфический по FOXM1-A01-10-566 (SEQ ID NO: 56), показал выработку IFN-гамма против клеток COS7, экспрессирующих и FOXM1, и HLA-A*01:01 (фиг. 4). С другой стороны, не было выявлено значительной выработки IFN-гамма против отрицательных клеточных контролей. Это ясно доказывает, что FOXM1-A01-10-566 (SEQ ID NO: 56) представляет собой пептид, полученный в результате антигенного процессинга, и он презентируется на клетках-мишенях при помощи молекулы HLA-A*01:01 и распознается ЦТЛ. Этот результат подтверждает, что FOXM1-A01-10-566 (SEQ ID NO: 56) может быть полезен в качестве противораковой вакцины для пациентов с повышенной экспрессией FOXM1 в злокачественных клетках.
Анализ гомологии антигенных пептидов
Было подтверждено, что FOXM1-A01-9-233 (SEQ ID NO: 48), FOXM1-A01-9-539 (SEQ ID NO: 49), FOXM1-A01-9-631 (SEQ ID NO: 50), FOXM1-A01-9-231 (SEQ ID NO: 52), FOXM1-A01-9-663 (SEQ ID NO: 53), FOXM1-A01-9-494 (SEQ ID NO: 55), FOXM1-A01-9-341 (SEQ ID NO: 20), FOXM1-A01-10-566 (SEQ ID NO: 56), FOXM1-A01-10-263 (SEQ ID NO: 57), FOXM1-A01-10-308 (SEQ ID NO: 58), FOXM1-A01-10-232 (SEQ ID NO: 59), FOXM1-A01-10-663 (SEQ ID NO: 60) и FOXM1-A01-10-341 (SEQ ID NO: 61) могут индуцировать CTL, показывающие пептид-специфическую выработку IFN-гамма. Таким образом, для того чтобы подтвердить, что последовательности FOXM1-A01-9-233 (SEQ ID NO: 48), FOXM1-A01-9-539 (SEQ ID NO: 49), FOXM1-A01-9-631 (SEQ ID NO: 50), FOXM1-A01-9-231 (SEQ ID NO: 52), FOXM1-A01-9-663 (SEQ ID NO: 53), FOXM1-A01-9-494 (SEQ ID NO: 55), FOXM1-A01-9-341 (SEQ ID NO: 20), FOXM1-A01-10-566 (SEQ ID NO: 56), FOXM1-A01-10-263 (SEQ ID NO: 57), FOXM1-A01-10-308 (SEQ ID NO: 58), FOXM1-A01-10-232 (SEQ ID NO: 59), FOXM1-A01-10-663 (SEQ ID NO: 60) и FOXM1-A01-10-341 (SEQ ID NO: 61) получены только из FOXM1, проводили анализ гомологии пептидных последовательностей с использованием алгоритма BLAST (blast.ncbi.nlm.nih.gov/Blast.cgi). В результате, последовательности FOXM1-A01-9-233 (SEQ ID NO: 48), FOXM1-A01-9-539 (SEQ ID NO: 49), FOXM1-A01-9-631 (SEQ ID NO: 50), FOXM1-A01-9-231 (SEQ ID NO: 52), FOXM1-A01-9-663 (SEQ ID NO: 53), FOXM1-A01-9-494 (SEQ ID NO: 55), FOXM1-A01-9-341 (SEQ ID NO: 20), FOXM1-A01-10-566 (SEQ ID NO: 56), FOXM1-A01-10-263 (SEQ ID NO: 57), FOXM1-A01-10-308 (SEQ ID NO: 58), FOXM1-A01-10-232 (SEQ ID NO: 59), FOXM1-A01-10-663 (SEQ ID NO: 60) и FOXM1-A01-10-341 (SEQ ID NO: 61 обнаружены только в FOXM1. Таким образом, как известно авторам настоящего изобретения, эти пептиды специфичны для FOXM1, так что практически не существует возможности того, что эти пептиды могли бы вызвать непреднамеренную иммунную реакцию против молекул, иных чем FOXM1 и уже известных тем, что они сенсибилизируют иммунную систему человека. Подводя итоги, были идентифицированы новые эпитопные пептиды, полученные из FOXM1 и рестриктированные по HLA-A*01:01. Было продемонстрировано, что эпитопные пептиды, полученные из FOXM1, применимы для иммунотерапии злокачественных опухолей.
[Пример 3]
Получение составов эмульсий
Пептид растворяли в растворителе для инъекций или стерильном физиологическом растворе до получения концентрации от 1,0 мг/мл до 10,0 мг/мл, и набирали в шприц. Его соединяли через коннектор со шприцем, наполненным неполным адъювантом Фрейнда (IFA), в количестве, эквивалентном количеству растворителя для инъекций или стерильного физиологического раствора, и перемешивали, поочередно нажимая на поршни двух соединенных шприцев. После нескольких минут перемешивания, готовность эмульсии оценивали путем капельной пробы. Капельную пробу можно проводить, капая одну каплю смешанного образца на воду. Эмульсию оценивают как готовую, когда образец, капнутый на воду, не сразу диффундирует в воде; и эмульсию оценивают, как не готовую, когда образец, капнутый на воду, сразу растворяется в воде. Когда эмульсию оценивают как не готовую, дополнительно проводят перемешивание до готовности эмульсии. Готовую эмульсию можно вводить пациенту со злокачественной опухолью путем подкожной инъекции. Пациента со злокачественной опухолью, подходящего для введения, можно выбирать из пациентов, страдающих от острого миелоидного лейкоза, рака мочевого пузыря, рака молочной железы, рака шейки матки, холангиоцеллюлярного рака, хронического миелолейкоза (ХМЛ), рака толстого кишечника, рака пищевода, рака желудка, диффузный рака желудка, немелкоклеточного рака легких (NSCLC), лимфомы, остеосаркомы, рака яичников, рака поджелудочной железы, рака предстательной железы, рак почки, мелкоклеточного рака легких (SCLC), опухоли мягких тканей, рака яичка или т.п.
Получение лиофилизированных составов
Пептид растворяли в растворителе для инъекций растворе до получения концентрации от 1,0 мг/мл до 10,0 мг/мл, и стерилизовали фильтрованием. Раствором заполняли стерилизованный флакон, и наполовину закрывали стерилизованной резиновой пробкой. После лиофилизации флакона, его полностью закрывали и запаивали алюминиевой крышкой для получения лиофилизированного состава. При использовании, растворитель для инъекций или стерильный физиологический раствор инъецировали во флакон для повторного растворения лиофилизированного порошка. Повторно растворенный раствор во флаконе собирали в шприц, и шприц соединяли через коннектор со шприцем, наполненным IFA, в количестве, эквивалентном собранному повторно растворенному раствору. Повторно растворенный раствор и IFA смешивали, поочередно нажимая на поршни двух соединенных шприцев. После нескольких минут перемешивания, готовность эмульсии оценивали путем капельной пробы. Готовую эмульсию можно вводить пациенту со злокачественной опухолью путем подкожной инъекции. Пациента со злокачественной опухолью, подходящего для введения, можно выбирать из пациентов, страдающих от острого миелоидного лейкоза, рака мочевого пузыря, рака молочной железы, рака шейки матки, холангиоцеллюлярного рака, хронического миелолейкоза (ХМЛ), рака толстого кишечника, рака пищевода, рака желудка, диффузный рака желудка, немелкоклеточного рака легких (NSCLC), лимфомы, остеосаркомы, рака яичников, рака поджелудочной железы, рака предстательной железы, рак почки, мелкоклеточного рака легких (SCLC), опухоли мягких тканей, рака яичка или т.п.
Промышленная применимость
Настоящее изобретение относится к новым эпитопным пептидам, полученным из FOXM1 и рестриктированным по HLA-A33 и HLA-A01, которые могут индуцировать мощный и специфический противоопухолевый иммунный ответ, и, таким образом, иметь применимость для широкого спектра типов злокачественных опухолей. Пептиды, композиции, АПК, и ЦТЛ по настоящему изобретению можно использовать в качестве пептидной вакцины для злокачественной опухоли, экспрессирующей FOXM1, например, острого миелоидного лейкоза, рака мочевого пузыря, рака молочной железы, рака шейки матки, холангиоцеллюлярного рака, хронического миелолейкоза (ХМЛ), рака толстого кишечника, рака пищевода, рака желудка, диффузный рака желудка, немелкоклеточного рака легких (NSCLC), лимфомы, остеосаркомы, рака яичников, рака поджелудочной железы, рака предстательной железы, рак почки, мелкоклеточного рака легких (SCLC), опухоли мягких тканей и рака яичка.
Хотя настоящее изобретение в настоящем документе описано подробно и относительно его конкретных вариантов осуществления, следует понимать, что вышеуказанное описание является по своему характеру иллюстративным и пояснительным и предназначено для иллюстрации настоящего изобретения и его предпочтительных вариантов осуществления. Путем рутинных экспериментов, специалист в данной области легко поймет, что в изобретении можно производить различные изменения и модификации в пределах существа и объема настоящего изобретения, пределы которых определены прилагаемой формулой изобретения.
--->
СПИСКИ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ONCOTHERAPY SCIENCE,INC.
<120> ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ FOXM1, И ВКЛЮЧАЮЩАЯ ЕГО ВАКЦИНА
<130> ONC-A1604P
<150> JP 2015-200221
<151> 2015-10-08
<160> 76
<170> PatentIn version 3.5
<210> 1
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 1
Ser Leu Ser Asn Ile Gln Trp Leu Arg
1 5
<210> 2
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 2
Trp Thr Ile His Pro Ser Ala Asn Arg
1 5
<210> 3
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 3
Gln Val Ser Gly Leu Ala Ala Asn Arg
1 5
<210> 4
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 4
Met Ser Ser Asp Gly Leu Gly Ser Arg
1 5
<210> 5
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 5
Met Leu Val Ile Gln His Arg Glu Arg
1 5
<210> 6
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 6
Leu Val Ile Gln His Arg Glu Arg Arg
1 5
<210> 7
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 7
Ala Ala Arg Asp Val Asn Leu Pro Arg
1 5
<210> 8
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 8
Thr Leu Gly Pro Lys Pro Ala Ala Arg
1 5
<210> 9
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 9
Ser Leu Met Ser Ser Glu Leu Ala Arg
1 5
<210> 10
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 10
Gln Phe Ala Ile Asn Ser Thr Glu Arg
1 5
<210> 11
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 11
Leu Ser Leu His Asp Met Phe Val Arg
1 5
<210> 12
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 12
Ser Trp Gln Asn Ser Val Ser Glu Arg
1 5
<210> 13
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 13
Thr Gln Thr Ser Tyr Asp Ala Lys Arg
1 5
<210> 14
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 14
Asp Ser Ser Gln Ser Pro Thr Pro Arg
1 5
<210> 15
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 15
Phe Pro Tyr Phe Lys His Ile Ala Lys
1 5
<210> 16
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 16
Gln Val Lys Val Glu Glu Pro Ser Arg
1 5
<210> 17
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 17
Tyr Ser Gly Leu Arg Ser Pro Thr Arg
1 5
<210> 18
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 18
Asp Gln Val Phe Lys Gln Gln Lys Arg
1 5
<210> 19
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 19
Ser Glu Leu Ala Arg His Ser Lys Arg
1 5
<210> 20
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 20
Lys Thr Glu Leu Pro Leu Gly Ala Arg
1 5
<210> 21
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 21
Phe Ser Glu Gly Pro Ser Thr Ser Arg
1 5
<210> 22
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 22
Glu Met Leu Val Ile Gln His Arg Glu Arg
1 5 10
<210> 23
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 23
Glu Thr Leu Gly Pro Lys Pro Ala Ala Arg
1 5 10
<210> 24
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 24
Asn Ser Leu Ser Asn Ile Gln Trp Leu Arg
1 5 10
<210> 25
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 25
Asn Leu Ser Leu His Asp Met Phe Val Arg
1 5 10
<210> 26
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 26
Ser Tyr Ser Gly Leu Arg Ser Pro Thr Arg
1 5 10
<210> 27
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 27
Met Leu Val Ile Gln His Arg Glu Arg Arg
1 5 10
<210> 28
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 28
Phe Trp Thr Ile His Pro Ser Ala Asn Arg
1 5 10
<210> 29
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 29
His Ser Lys Arg Val Arg Ile Ala Pro Lys
1 5 10
<210> 30
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 30
Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg
1 5 10
<210> 31
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 31
His Phe Pro Tyr Phe Lys His Ile Ala Lys
1 5 10
<210> 32
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 32
Gln Thr Gln Thr Ser Tyr Asp Ala Lys Arg
1 5 10
<210> 33
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 33
Ser Thr Pro Ser Lys Ser Val Leu Pro Arg
1 5 10
<210> 34
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 34
Glu Leu Ala Arg His Ser Lys Arg Val Arg
1 5 10
<210> 35
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 35
Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg
1 5 10
<210> 36
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 36
Leu Phe Ser Glu Gly Pro Ser Thr Ser Arg
1 5 10
<210> 37
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 37
Ser Ser Glu Leu Ala Arg His Ser Lys Arg
1 5 10
<210> 38
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 38
Ala Ser Trp Gln Asn Ser Val Ser Glu Arg
1 5 10
<210> 39
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 39
Met Ser Ser Glu Leu Ala Arg His Ser Lys
1 5 10
<210> 40
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 40
Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg
1 5 10
<210> 41
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 41
Glu Ser Trp Arg Leu Thr Pro Pro Ala Lys
1 5 10
<210> 42
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 42
Trp Ile Glu Asp His Phe Pro Tyr Phe Lys
1 5 10
<210> 43
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 43
Arg Pro Lys Lys Ser Tyr Ser Gly Leu Arg
1 5 10
<210> 44
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 44
Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys
1 5 10
<210> 45
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 45
Ser Pro Arg Arg Pro Leu Ile Leu Lys Arg
1 5 10
<210> 46
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 46
Ala Ser Leu Met Ser Ser Glu Leu Ala Arg
1 5 10
<210> 47
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 47
Ser Ala Pro Pro Leu Glu Ser Pro Gln Arg
1 5 10
<210> 48
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 48
Val Ser Glu Arg Pro Pro Tyr Ser Tyr
1 5
<210> 49
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 49
Cys Val Asp Glu Pro Glu Leu Leu Phe
1 5
<210> 50
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 50
Ala Ser Asp Pro Leu Pro Asp Pro Leu
1 5
<210> 51
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 51
Leu Thr Glu Gly Leu Val Leu Asp Thr
1 5
<210> 52
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 52
Asn Ser Val Ser Glu Arg Pro Pro Tyr
1 5
<210> 53
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 53
Ser Ser Glu Pro Leu Asp Leu Ile Ser
1 5
<210> 54
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 54
Ser Ser Glu Leu Ala Arg His Ser Lys
1 5
<210> 55
<211> 9
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 55
Pro Thr Pro Arg Pro Lys Lys Ser Tyr
1 5
<210> 56
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 56
Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr
1 5 10
<210> 57
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 57
Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr
1 5 10
<210> 58
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 58
Trp Thr Ile His Pro Ser Ala Asn Arg Tyr
1 5 10
<210> 59
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 59
Ser Val Ser Glu Arg Pro Pro Tyr Ser Tyr
1 5 10
<210> 60
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 60
Ser Ser Glu Pro Leu Asp Leu Ile Ser Val
1 5 10
<210> 61
<211> 10
<212> белок
<213> искусственная последовательность
<220>
<223> пептид, полученный из FOXM1
<400> 61
Lys Thr Glu Leu Pro Leu Gly Ala Arg Arg
1 5 10
<210> 62
<211> 22
<212> ДНК
<213> искусственная последовательность
<220>
<223> ПЦР-праймер для анализа TCR
<400> 62
gtctaccagg cattcgcttc at 22
<210> 63
<211> 24
<212> ДНК
<213> искусственная последовательность
<220>
<223> ПЦР-праймер для анализа TCR
<400> 63
tcagctggac cacagccgca gcgt 24
<210> 64
<211> 21
<212> ДНК
<213> искусственная последовательность
<220>
<223> ПЦР-праймер для анализа TCR
<400> 64
tcagaaatcc tttctcttga c 21
<210> 65
<211> 24
<212> ДНК
<213> искусственная последовательность
<220>
<223> ПЦР-праймер для анализа TCR
<400> 65
ctagcctctg gaatcctttc tctt 24
<210> 66
<211> 3506
<212> ДНК
<213> Homo sapiens
<220>
<221> кодирующая последовательность
<222> (284)..(2530)
<400> 66
tttcaaacag cggaacaaac tgaaagctcc ggtgccagac cccacccccg gccccggccc 60
gggaccccct cccctcccgg gatcccccgg ggttcccacc ccgcccgcac cgccggggac 120
ccggccggtc cggcgcgagc ccccgtccgg ggccctggct cggcccccag gttggaggag 180
cccggagccc gccttcggag ctacggccta acggcggcgg cgactgcagt ctggagggtc 240
cacacttgtg attctcaatg gagagtgaaa acgcagattc ata atg aaa act agc 295
Met Lys Thr Ser
1
ccc cgt cgg cca ctg att ctc aaa aga cgg agg ctg ccc ctt cct gtt 343
Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu Pro Leu Pro Val
5 10 15 20
caa aat gcc cca agt gaa aca tca gag gag gaa cct aag aga tcc cct 391
Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro Lys Arg Ser Pro
25 30 35
gcc caa cag gag tct aat caa gca gag gcc tcc aag gaa gtg gca gag 439
Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys Glu Val Ala Glu
40 45 50
tcc aac tct tgc aag ttt cca gct ggg atc aag att att aac cac ccc 487
Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile Ile Asn His Pro
55 60 65
acc atg ccc aac acg caa gta gtg gcc atc ccc aac aat gct aat att 535
Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn Asn Ala Asn Ile
70 75 80
cac agc atc atc aca gca ctg act gcc aag gga aaa gag agt ggc agt 583
His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys Glu Ser Gly Ser
85 90 95 100
agt ggg ccc aac aaa ttc atc ctc atc agc tgt ggg gga gcc cca act 631
Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly Gly Ala Pro Thr
105 110 115
cag cct cca gga ctc cgg cct caa acc caa acc agc tat gat gcc aaa 679
Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser Tyr Asp Ala Lys
120 125 130
agg aca gaa gtg acc ctg gag acc ttg gga cca aaa cct gca gct agg 727
Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys Pro Ala Ala Arg
135 140 145
gat gtg aat ctt cct aga cca cct gga gcc ctt tgc gag cag aaa cgg 775
Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys Glu Gln Lys Arg
150 155 160
gag acc tgt gca gat ggt gag gca gca ggc tgc act atc aac aat agc 823
Glu Thr Cys Ala Asp Gly Glu Ala Ala Gly Cys Thr Ile Asn Asn Ser
165 170 175 180
cta tcc aac atc cag tgg ctt cga aag atg agt tct gat gga ctg ggc 871
Leu Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser Asp Gly Leu Gly
185 190 195
tcc cgc agc atc aag caa gag atg gag gaa aag gag aat tgt cac ctg 919
Ser Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu Asn Cys His Leu
200 205 210
gag cag cga cag gtt aag gtt gag gag cct tcg aga cca tca gcg tcc 967
Glu Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg Pro Ser Ala Ser
215 220 225
tgg cag aac tct gtg tct gag cgg cca ccc tac tct tac atg gcc atg 1015
Trp Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser Tyr Met Ala Met
230 235 240
ata caa ttc gcc atc aac agc act gag agg aag cgc atg act ttg aaa 1063
Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg Met Thr Leu Lys
245 250 255 260
gac atc tat acg tgg att gag gac cac ttt ccc tac ttt aag cac att 1111
Asp Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr Phe Lys His Ile
265 270 275
gcc aag cca ggc tgg aag aac tcc atc cgc cac aac ctt tcc ctg cac 1159
Ala Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn Leu Ser Leu His
280 285 290
gac atg ttt gtc cgg gag acg tct gcc aat ggc aag gtc tcc ttc tgg 1207
Asp Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys Val Ser Phe Trp
295 300 305
acc att cac ccc agt gcc aac cgc tac ttg aca ttg gac cag gtg ttt 1255
Thr Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu Asp Gln Val Phe
310 315 320
aag cag cag aaa cga ccg aat cca gag ctc cgc cgg aac atg acc atc 1303
Lys Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg Asn Met Thr Ile
325 330 335 340
aaa acc gaa ctc ccc ctg ggc gca cgg cgg aag atg aag cca ctg cta 1351
Lys Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met Lys Pro Leu Leu
345 350 355
cca cgg gtc agc tca tac ctg gta cct atc cag ttc ccg gtg aac cag 1399
Pro Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe Pro Val Asn Gln
360 365 370
tca ctg gtg ttg cag ccc tcg gtg aag gtg cca ttg ccc ctg gcg gct 1447
Ser Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu Pro Leu Ala Ala
375 380 385
tcc ctc atg agc tca gag ctt gcc cgc cat agc aag cga gtc cgc att 1495
Ser Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys Arg Val Arg Ile
390 395 400
gcc ccc aag gtg ctg cta gct gag gag ggg ata gct cct ctt tct tct 1543
Ala Pro Lys Val Leu Leu Ala Glu Glu Gly Ile Ala Pro Leu Ser Ser
405 410 415 420
gca gga cca ggg aaa gag gag aaa ctc ctg ttt gga gaa ggg ttt tct 1591
Ala Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe Gly Glu Gly Phe Ser
425 430 435
cct ttg ctt cca gtt cag act atc aag gag gaa gaa atc cag cct ggg 1639
Pro Leu Leu Pro Val Gln Thr Ile Lys Glu Glu Glu Ile Gln Pro Gly
440 445 450
gag gaa atg cca cac tta gcg aga ccc atc aaa gtg gag agc cct ccc 1687
Glu Glu Met Pro His Leu Ala Arg Pro Ile Lys Val Glu Ser Pro Pro
455 460 465
ttg gaa gag tgg ccc tcc ccg gcc cca tct ttc aaa gag gaa tca tct 1735
Leu Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys Glu Glu Ser Ser
470 475 480
cac tcc tgg gag gat tcg tcc caa tct ccc acc cca aga ccc aag aag 1783
His Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr Pro Arg Pro Lys Lys
485 490 495 500
tcc tac agt ggg ctt agg tcc cca acc cgg tgt gtc tcg gaa atg ctt 1831
Ser Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys Val Ser Glu Met Leu
505 510 515
gtg att caa cac agg gag agg agg gag agg agc cgg tct cgg agg aaa 1879
Val Ile Gln His Arg Glu Arg Arg Glu Arg Ser Arg Ser Arg Arg Lys
520 525 530
cag cat cta ctg cct ccc tgt gtg gat gag ccg gag ctg ctc ttc tca 1927
Gln His Leu Leu Pro Pro Cys Val Asp Glu Pro Glu Leu Leu Phe Ser
535 540 545
gag ggg ccc agt act tcc cgc tgg gcc gca gag ctc ccg ttc cca gca 1975
Glu Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu Leu Pro Phe Pro Ala
550 555 560
gac tcc tct gac cct gcc tcc cag ctc agc tac tcc cag gaa gtg gga 2023
Asp Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr Ser Gln Glu Val Gly
565 570 575 580
gga cct ttt aag aca ccc att aag gaa acg ctg ccc atc tcc tcc acc 2071
Gly Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu Pro Ile Ser Ser Thr
585 590 595
ccg agc aaa tct gtc ctc ccc aga acc cct gaa tcc tgg agg ctc acg 2119
Pro Ser Lys Ser Val Leu Pro Arg Thr Pro Glu Ser Trp Arg Leu Thr
600 605 610
ccc cca gcc aaa gta ggg gga ctg gat ttc agc cca gta caa acc tcc 2167
Pro Pro Ala Lys Val Gly Gly Leu Asp Phe Ser Pro Val Gln Thr Ser
615 620 625
cag ggt gcc tct gac ccc ttg cct gac ccc ctg ggg ctg atg gat ctc 2215
Gln Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu Gly Leu Met Asp Leu
630 635 640
agc acc act ccc ttg caa agt gct ccc ccc ctt gaa tca ccg caa agg 2263
Ser Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu Glu Ser Pro Gln Arg
645 650 655 660
ctc ctc agt tca gaa ccc tta gac ctc atc tcc gtc ccc ttt ggc aac 2311
Leu Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser Val Pro Phe Gly Asn
665 670 675
tct tct ccc tca gat ata gac gtc ccc aag cca ggc tcc ccg gag cca 2359
Ser Ser Pro Ser Asp Ile Asp Val Pro Lys Pro Gly Ser Pro Glu Pro
680 685 690
cag gtt tct ggc ctt gca gcc aat cgt tct ctg aca gaa ggc ctg gtc 2407
Gln Val Ser Gly Leu Ala Ala Asn Arg Ser Leu Thr Glu Gly Leu Val
695 700 705
ctg gac aca atg aat gac agc ctc agc aag atc ctg ctg gac atc agc 2455
Leu Asp Thr Met Asn Asp Ser Leu Ser Lys Ile Leu Leu Asp Ile Ser
710 715 720
ttt cct ggc ctg gac gag gac cca ctg ggc cct gac aac atc aac tgg 2503
Phe Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro Asp Asn Ile Asn Trp
725 730 735 740
tcc cag ttt att cct gag cta cag tag agccctgccc ttgcccctgt 2550
Ser Gln Phe Ile Pro Glu Leu Gln
745
gctcaagctg tccaccatcc cgggcactcc aaggctcagt gcaccccaag cctctgagtg 2610
aggacagcag gcagggactg ttctgctcct catagctccc tgctgcctga ttatgcaaaa 2670
gtagcagtca caccctagcc actgctggga ccttgtgttc cccaagagta tctgattcct 2730
ctgctgtccc tgccaggagc tgaagggtgg gaacaacaaa ggcaatggtg aaaagagatt 2790
aggaaccccc cagcctgttt ccattctctg cccagcagtc tcttaccttc cctgatcttt 2850
gcagggtggt ccgtgtaaat agtataaatt ctccaaatta tcctctaatt ataaatgtaa 2910
gcttatttcc ttagatcatt atccagagac tgccagaagg tgggtaggat gacctggggt 2970
ttcaattgac ttctgttcct tgcttttagt tttgatagaa gggaagacct gcagtgcacg 3030
gtttcttcca ggctgaggta cctggatctt gggttcttca ctgcagggac ccagacaagt 3090
ggatctgctt gccagagtcc tttttgcccc tccctgccac ctccccgtgt ttccaagtca 3150
gctttcctgc aagaagaaat cctggttaaa aaagtctttt gtattgggtc aggagttgaa 3210
tttggggtgg gaggatggat gcaactgaag cagagtgtgg gtgcccagat gtgcgctatt 3270
agatgtttct ctgataatgt ccccaatcat accagggaga ctggcattga cgagaactca 3330
ggtggaggct tgagaaggcc gaaagggccc ctgacctgcc tggcttcctt agcttgcccc 3390
tcagctttgc aaagagccac cctaggcccc agctgaccgc atgggtgtga gccagcttga 3450
gaacactaac tactcaataa aagcgaaggt ggacatgaaa aaaaaaaaaa aaaaaa 3506
<210> 67
<211> 748
<212> белок
<213> Homo sapiens
<400> 67
Met Lys Thr Ser Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu
1 5 10 15
Pro Leu Pro Val Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro
20 25 30
Lys Arg Ser Pro Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys
35 40 45
Glu Val Ala Glu Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile
50 55 60
Ile Asn His Pro Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn
65 70 75 80
Asn Ala Asn Ile His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys
85 90 95
Glu Ser Gly Ser Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly
100 105 110
Gly Ala Pro Thr Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser
115 120 125
Tyr Asp Ala Lys Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys
130 135 140
Pro Ala Ala Arg Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys
145 150 155 160
Glu Gln Lys Arg Glu Thr Cys Ala Asp Gly Glu Ala Ala Gly Cys Thr
165 170 175
Ile Asn Asn Ser Leu Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser
180 185 190
Asp Gly Leu Gly Ser Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu
195 200 205
Asn Cys His Leu Glu Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg
210 215 220
Pro Ser Ala Ser Trp Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser
225 230 235 240
Tyr Met Ala Met Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg
245 250 255
Met Thr Leu Lys Asp Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr
260 265 270
Phe Lys His Ile Ala Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn
275 280 285
Leu Ser Leu His Asp Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys
290 295 300
Val Ser Phe Trp Thr Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu
305 310 315 320
Asp Gln Val Phe Lys Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg
325 330 335
Asn Met Thr Ile Lys Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met
340 345 350
Lys Pro Leu Leu Pro Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe
355 360 365
Pro Val Asn Gln Ser Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu
370 375 380
Pro Leu Ala Ala Ser Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys
385 390 395 400
Arg Val Arg Ile Ala Pro Lys Val Leu Leu Ala Glu Glu Gly Ile Ala
405 410 415
Pro Leu Ser Ser Ala Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe Gly
420 425 430
Glu Gly Phe Ser Pro Leu Leu Pro Val Gln Thr Ile Lys Glu Glu Glu
435 440 445
Ile Gln Pro Gly Glu Glu Met Pro His Leu Ala Arg Pro Ile Lys Val
450 455 460
Glu Ser Pro Pro Leu Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys
465 470 475 480
Glu Glu Ser Ser His Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr Pro
485 490 495
Arg Pro Lys Lys Ser Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys Val
500 505 510
Ser Glu Met Leu Val Ile Gln His Arg Glu Arg Arg Glu Arg Ser Arg
515 520 525
Ser Arg Arg Lys Gln His Leu Leu Pro Pro Cys Val Asp Glu Pro Glu
530 535 540
Leu Leu Phe Ser Glu Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu Leu
545 550 555 560
Pro Phe Pro Ala Asp Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr Ser
565 570 575
Gln Glu Val Gly Gly Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu Pro
580 585 590
Ile Ser Ser Thr Pro Ser Lys Ser Val Leu Pro Arg Thr Pro Glu Ser
595 600 605
Trp Arg Leu Thr Pro Pro Ala Lys Val Gly Gly Leu Asp Phe Ser Pro
610 615 620
Val Gln Thr Ser Gln Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu Gly
625 630 635 640
Leu Met Asp Leu Ser Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu Glu
645 650 655
Ser Pro Gln Arg Leu Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser Val
660 665 670
Pro Phe Gly Asn Ser Ser Pro Ser Asp Ile Asp Val Pro Lys Pro Gly
675 680 685
Ser Pro Glu Pro Gln Val Ser Gly Leu Ala Ala Asn Arg Ser Leu Thr
690 695 700
Glu Gly Leu Val Leu Asp Thr Met Asn Asp Ser Leu Ser Lys Ile Leu
705 710 715 720
Leu Asp Ile Ser Phe Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro Asp
725 730 735
Asn Ile Asn Trp Ser Gln Phe Ile Pro Glu Leu Gln
740 745
<210> 68
<211> 3506
<212> ДНК
<213> Homo sapiens
<220>
<221> кодирующая последовательность
<222> (284)..(2530)
<400> 68
tttcaaacag cggaacaaac tgaaagctcc ggtgccagac cccacccccg gccccggccc 60
gggaccccct cccctcccgg gatcccccgg ggttcccacc ccgcccgcac cgccggggac 120
ccggccggtc cggcgcgagc ccccgtccgg ggccctggct cggcccccag gttggaggag 180
cccggagccc gccttcggag ctacggccta acggcggcgg cgactgcagt ctggagggtc 240
cacacttgtg attctcaatg gagagtgaaa acgcagattc ata atg aaa act agc 295
Met Lys Thr Ser
1
ccc cgt cgg cca ctg att ctc aaa aga cgg agg ctg ccc ctt cct gtt 343
Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu Pro Leu Pro Val
5 10 15 20
caa aat gcc cca agt gaa aca tca gag gag gaa cct aag aga tcc cct 391
Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro Lys Arg Ser Pro
25 30 35
gcc caa cag gag tct aat caa gca gag gcc tcc aag gaa gtg gca gag 439
Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys Glu Val Ala Glu
40 45 50
tcc aac tct tgc aag ttt cca gct ggg atc aag att att aac cac ccc 487
Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile Ile Asn His Pro
55 60 65
acc atg ccc aac acg caa gta gtg gcc atc ccc aac aat gct aat att 535
Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn Asn Ala Asn Ile
70 75 80
cac agc atc atc aca gca ctg act gcc aag gga aaa gag agt ggc agt 583
His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys Glu Ser Gly Ser
85 90 95 100
agt ggg ccc aac aaa ttc atc ctc atc agc tgt ggg gga gcc cca act 631
Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly Gly Ala Pro Thr
105 110 115
cag cct cca gga ctc cgg cct caa acc caa acc agc tat gat gcc aaa 679
Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser Tyr Asp Ala Lys
120 125 130
agg aca gaa gtg acc ctg gag acc ttg gga cca aaa cct gca gct agg 727
Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys Pro Ala Ala Arg
135 140 145
gat gtg aat ctt cct aga cca cct gga gcc ctt tgc gag cag aaa cgg 775
Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys Glu Gln Lys Arg
150 155 160
gag acc tgt gat ggt gag gca gca ggc tgc act atc aac aat agc cta 823
Glu Thr Cys Asp Gly Glu Ala Ala Gly Cys Thr Ile Asn Asn Ser Leu
165 170 175 180
tcc aac atc cag tgg ctt cga aag atg agt tct gat gga ctg ggc tcc 871
Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser Asp Gly Leu Gly Ser
185 190 195
cgc agc atc aag caa gag atg gag gaa aag gag aat tgt cac ctg gag 919
Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu Asn Cys His Leu Glu
200 205 210
cag cga cag gtt aag gtt gag gag cct tcg aga cca tca gcg tcc tgg 967
Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg Pro Ser Ala Ser Trp
215 220 225
cag aac tct gtg tct gag cgg cca ccc tac tct tac atg gcc atg ata 1015
Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser Tyr Met Ala Met Ile
230 235 240
caa ttc gcc atc aac agc act gag agg aag cgc atg act ttg aaa gac 1063
Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg Met Thr Leu Lys Asp
245 250 255 260
atc tat acg tgg att gag gac cac ttt ccc tac ttt aag cac att gcc 1111
Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr Phe Lys His Ile Ala
265 270 275
aag cca ggc tgg aag aac tcc atc cgc cac aac ctt tcc ctg cac gac 1159
Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn Leu Ser Leu His Asp
280 285 290
atg ttt gtc cgg gag acg tct gcc aat ggc aag gtc tcc ttc tgg acc 1207
Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys Val Ser Phe Trp Thr
295 300 305
att cac ccc agt gcc aac cgc tac ttg aca ttg gac cag gtg ttt aag 1255
Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu Asp Gln Val Phe Lys
310 315 320
cag cag cag aaa cga ccg aat cca gag ctc cgc cgg aac atg acc atc 1303
Gln Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg Asn Met Thr Ile
325 330 335 340
aaa acc gaa ctc ccc ctg ggc gca cgg cgg aag atg aag cca ctg cta 1351
Lys Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met Lys Pro Leu Leu
345 350 355
cca cgg gtc agc tca tac ctg gta cct atc cag ttc ccg gtg aac cag 1399
Pro Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe Pro Val Asn Gln
360 365 370
tca ctg gtg ttg cag ccc tcg gtg aag gtg cca ttg ccc ctg gcg gct 1447
Ser Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu Pro Leu Ala Ala
375 380 385
tcc ctc atg agc tca gag ctt gcc cgc cat agc aag cga gtc cgc att 1495
Ser Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys Arg Val Arg Ile
390 395 400
gcc ccc aag gtg ctg cta gct gag gag ggg ata gct cct ctt tct tct 1543
Ala Pro Lys Val Leu Leu Ala Glu Glu Gly Ile Ala Pro Leu Ser Ser
405 410 415 420
gca gga cca ggg aaa gag gag aaa ctc ctg ttt gga gaa ggg ttt tct 1591
Ala Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe Gly Glu Gly Phe Ser
425 430 435
cct ttg ctt cca gtt cag act atc aag gag gaa gaa atc cag cct ggg 1639
Pro Leu Leu Pro Val Gln Thr Ile Lys Glu Glu Glu Ile Gln Pro Gly
440 445 450
gag gaa atg cca cac tta gcg aga ccc atc aaa gtg gag agc cct ccc 1687
Glu Glu Met Pro His Leu Ala Arg Pro Ile Lys Val Glu Ser Pro Pro
455 460 465
ttg gaa gag tgg ccc tcc ccg gcc cca tct ttc aaa gag gaa tca tct 1735
Leu Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys Glu Glu Ser Ser
470 475 480
cac tcc tgg gag gat tcg tcc caa tct ccc acc cca aga ccc aag aag 1783
His Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr Pro Arg Pro Lys Lys
485 490 495 500
tcc tac agt ggg ctt agg tcc cca acc cgg tgt gtc tcg gaa atg ctt 1831
Ser Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys Val Ser Glu Met Leu
505 510 515
gtg att caa cac agg gag agg agg gag agg agc cgg tct cgg agg aaa 1879
Val Ile Gln His Arg Glu Arg Arg Glu Arg Ser Arg Ser Arg Arg Lys
520 525 530
cag cat cta ctg cct ccc tgt gtg gat gag ccg gag ctg ctc ttc tca 1927
Gln His Leu Leu Pro Pro Cys Val Asp Glu Pro Glu Leu Leu Phe Ser
535 540 545
gag ggg ccc agt act tcc cgc tgg gcc gca gag ctc ccg ttc cca gca 1975
Glu Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu Leu Pro Phe Pro Ala
550 555 560
gac tcc tct gac cct gcc tcc cag ctc agc tac tcc cag gaa gtg gga 2023
Asp Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr Ser Gln Glu Val Gly
565 570 575 580
gga cct ttt aag aca ccc att aag gaa acg ctg ccc atc tcc tcc acc 2071
Gly Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu Pro Ile Ser Ser Thr
585 590 595
ccg agc aaa tct gtc ctc ccc aga acc cct gaa tcc tgg agg ctc acg 2119
Pro Ser Lys Ser Val Leu Pro Arg Thr Pro Glu Ser Trp Arg Leu Thr
600 605 610
ccc cca gcc aaa gta ggg gga ctg gat ttc agc cca gta caa acc tcc 2167
Pro Pro Ala Lys Val Gly Gly Leu Asp Phe Ser Pro Val Gln Thr Ser
615 620 625
cag ggt gcc tct gac ccc ttg cct gac ccc ctg ggg ctg atg gat ctc 2215
Gln Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu Gly Leu Met Asp Leu
630 635 640
agc acc act ccc ttg caa agt gct ccc ccc ctt gaa tca ccg caa agg 2263
Ser Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu Glu Ser Pro Gln Arg
645 650 655 660
ctc ctc agt tca gaa ccc tta gac ctc atc tcc gtc ccc ttt ggc aac 2311
Leu Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser Val Pro Phe Gly Asn
665 670 675
tct tct ccc tca gat ata gac gtc ccc aag cca ggc tcc ccg gag cca 2359
Ser Ser Pro Ser Asp Ile Asp Val Pro Lys Pro Gly Ser Pro Glu Pro
680 685 690
cag gtt tct ggc ctt gca gcc aat cgt tct ctg aca gaa ggc ctg gtc 2407
Gln Val Ser Gly Leu Ala Ala Asn Arg Ser Leu Thr Glu Gly Leu Val
695 700 705
ctg gac aca atg aat gac agc ctc agc aag atc ctg ctg gac atc agc 2455
Leu Asp Thr Met Asn Asp Ser Leu Ser Lys Ile Leu Leu Asp Ile Ser
710 715 720
ttt cct ggc ctg gac gag gac cca ctg ggc cct gac aac atc aac tgg 2503
Phe Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro Asp Asn Ile Asn Trp
725 730 735 740
tcc cag ttt att cct gag cta cag tag agccctgccc ttgcccctgt 2550
Ser Gln Phe Ile Pro Glu Leu Gln
745
gctcaagctg tccaccatcc cgggcactcc aaggctcagt gcaccccaag cctctgagtg 2610
aggacagcag gcagggactg ttctgctcct catagctccc tgctgcctga ttatgcaaaa 2670
gtagcagtca caccctagcc actgctggga ccttgtgttc cccaagagta tctgattcct 2730
ctgctgtccc tgccaggagc tgaagggtgg gaacaacaaa ggcaatggtg aaaagagatt 2790
aggaaccccc cagcctgttt ccattctctg cccagcagtc tcttaccttc cctgatcttt 2850
gcagggtggt ccgtgtaaat agtataaatt ctccaaatta tcctctaatt ataaatgtaa 2910
gcttatttcc ttagatcatt atccagagac tgccagaagg tgggtaggat gacctggggt 2970
ttcaattgac ttctgttcct tgcttttagt tttgatagaa gggaagacct gcagtgcacg 3030
gtttcttcca ggctgaggta cctggatctt gggttcttca ctgcagggac ccagacaagt 3090
ggatctgctt gccagagtcc tttttgcccc tccctgccac ctccccgtgt ttccaagtca 3150
gctttcctgc aagaagaaat cctggttaaa aaagtctttt gtattgggtc aggagttgaa 3210
tttggggtgg gaggatggat gcaactgaag cagagtgtgg gtgcccagat gtgcgctatt 3270
agatgtttct ctgataatgt ccccaatcat accagggaga ctggcattga cgagaactca 3330
ggtggaggct tgagaaggcc gaaagggccc ctgacctgcc tggcttcctt agcttgcccc 3390
tcagctttgc aaagagccac cctaggcccc agctgaccgc atgggtgtga gccagcttga 3450
gaacactaac tactcaataa aagcgaaggt ggacatgaaa aaaaaaaaaa aaaaaa 3506
<210> 69
<211> 748
<212> белок
<213> Homo sapiens
<400> 69
Met Lys Thr Ser Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu
1 5 10 15
Pro Leu Pro Val Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro
20 25 30
Lys Arg Ser Pro Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys
35 40 45
Glu Val Ala Glu Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile
50 55 60
Ile Asn His Pro Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn
65 70 75 80
Asn Ala Asn Ile His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys
85 90 95
Glu Ser Gly Ser Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly
100 105 110
Gly Ala Pro Thr Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser
115 120 125
Tyr Asp Ala Lys Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys
130 135 140
Pro Ala Ala Arg Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys
145 150 155 160
Glu Gln Lys Arg Glu Thr Cys Asp Gly Glu Ala Ala Gly Cys Thr Ile
165 170 175
Asn Asn Ser Leu Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser Asp
180 185 190
Gly Leu Gly Ser Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu Asn
195 200 205
Cys His Leu Glu Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg Pro
210 215 220
Ser Ala Ser Trp Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser Tyr
225 230 235 240
Met Ala Met Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg Met
245 250 255
Thr Leu Lys Asp Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr Phe
260 265 270
Lys His Ile Ala Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn Leu
275 280 285
Ser Leu His Asp Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys Val
290 295 300
Ser Phe Trp Thr Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu Asp
305 310 315 320
Gln Val Phe Lys Gln Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg
325 330 335
Asn Met Thr Ile Lys Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met
340 345 350
Lys Pro Leu Leu Pro Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe
355 360 365
Pro Val Asn Gln Ser Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu
370 375 380
Pro Leu Ala Ala Ser Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys
385 390 395 400
Arg Val Arg Ile Ala Pro Lys Val Leu Leu Ala Glu Glu Gly Ile Ala
405 410 415
Pro Leu Ser Ser Ala Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe Gly
420 425 430
Glu Gly Phe Ser Pro Leu Leu Pro Val Gln Thr Ile Lys Glu Glu Glu
435 440 445
Ile Gln Pro Gly Glu Glu Met Pro His Leu Ala Arg Pro Ile Lys Val
450 455 460
Glu Ser Pro Pro Leu Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys
465 470 475 480
Glu Glu Ser Ser His Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr Pro
485 490 495
Arg Pro Lys Lys Ser Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys Val
500 505 510
Ser Glu Met Leu Val Ile Gln His Arg Glu Arg Arg Glu Arg Ser Arg
515 520 525
Ser Arg Arg Lys Gln His Leu Leu Pro Pro Cys Val Asp Glu Pro Glu
530 535 540
Leu Leu Phe Ser Glu Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu Leu
545 550 555 560
Pro Phe Pro Ala Asp Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr Ser
565 570 575
Gln Glu Val Gly Gly Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu Pro
580 585 590
Ile Ser Ser Thr Pro Ser Lys Ser Val Leu Pro Arg Thr Pro Glu Ser
595 600 605
Trp Arg Leu Thr Pro Pro Ala Lys Val Gly Gly Leu Asp Phe Ser Pro
610 615 620
Val Gln Thr Ser Gln Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu Gly
625 630 635 640
Leu Met Asp Leu Ser Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu Glu
645 650 655
Ser Pro Gln Arg Leu Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser Val
660 665 670
Pro Phe Gly Asn Ser Ser Pro Ser Asp Ile Asp Val Pro Lys Pro Gly
675 680 685
Ser Pro Glu Pro Gln Val Ser Gly Leu Ala Ala Asn Arg Ser Leu Thr
690 695 700
Glu Gly Leu Val Leu Asp Thr Met Asn Asp Ser Leu Ser Lys Ile Leu
705 710 715 720
Leu Asp Ile Ser Phe Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro Asp
725 730 735
Asn Ile Asn Trp Ser Gln Phe Ile Pro Glu Leu Gln
740 745
<210> 70
<211> 3503
<212> ДНК
<213> Homo sapiens
<220>
<221> кодирующая последовательность
<222> (284)..(2527)
<400> 70
tttcaaacag cggaacaaac tgaaagctcc ggtgccagac cccacccccg gccccggccc 60
gggaccccct cccctcccgg gatcccccgg ggttcccacc ccgcccgcac cgccggggac 120
ccggccggtc cggcgcgagc ccccgtccgg ggccctggct cggcccccag gttggaggag 180
cccggagccc gccttcggag ctacggccta acggcggcgg cgactgcagt ctggagggtc 240
cacacttgtg attctcaatg gagagtgaaa acgcagattc ata atg aaa act agc 295
Met Lys Thr Ser
1
ccc cgt cgg cca ctg att ctc aaa aga cgg agg ctg ccc ctt cct gtt 343
Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu Pro Leu Pro Val
5 10 15 20
caa aat gcc cca agt gaa aca tca gag gag gaa cct aag aga tcc cct 391
Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro Lys Arg Ser Pro
25 30 35
gcc caa cag gag tct aat caa gca gag gcc tcc aag gaa gtg gca gag 439
Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys Glu Val Ala Glu
40 45 50
tcc aac tct tgc aag ttt cca gct ggg atc aag att att aac cac ccc 487
Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile Ile Asn His Pro
55 60 65
acc atg ccc aac acg caa gta gtg gcc atc ccc aac aat gct aat att 535
Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn Asn Ala Asn Ile
70 75 80
cac agc atc atc aca gca ctg act gcc aag gga aaa gag agt ggc agt 583
His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys Glu Ser Gly Ser
85 90 95 100
agt ggg ccc aac aaa ttc atc ctc atc agc tgt ggg gga gcc cca act 631
Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly Gly Ala Pro Thr
105 110 115
cag cct cca gga ctc cgg cct caa acc caa acc agc tat gat gcc aaa 679
Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser Tyr Asp Ala Lys
120 125 130
agg aca gaa gtg acc ctg gag acc ttg gga cca aaa cct gca gct agg 727
Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys Pro Ala Ala Arg
135 140 145
gat gtg aat ctt cct aga cca cct gga gcc ctt tgc gag cag aaa cgg 775
Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys Glu Gln Lys Arg
150 155 160
gag acc tgt gat ggt gag gca gca ggc tgc act atc aac aat agc cta 823
Glu Thr Cys Asp Gly Glu Ala Ala Gly Cys Thr Ile Asn Asn Ser Leu
165 170 175 180
tcc aac atc cag tgg ctt cga aag atg agt tct gat gga ctg ggc tcc 871
Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser Asp Gly Leu Gly Ser
185 190 195
cgc agc atc aag caa gag atg gag gaa aag gag aat tgt cac ctg gag 919
Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu Asn Cys His Leu Glu
200 205 210
cag cga cag gtt aag gtt gag gag cct tcg aga cca tca gcg tcc tgg 967
Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg Pro Ser Ala Ser Trp
215 220 225
cag aac tct gtg tct gag cgg cca ccc tac tct tac atg gcc atg ata 1015
Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser Tyr Met Ala Met Ile
230 235 240
caa ttc gcc atc aac agc act gag agg aag cgc atg act ttg aaa gac 1063
Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg Met Thr Leu Lys Asp
245 250 255 260
atc tat acg tgg att gag gac cac ttt ccc tac ttt aag cac att gcc 1111
Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr Phe Lys His Ile Ala
265 270 275
aag cca ggc tgg aag aac tcc atc cgc cac aac ctt tcc ctg cac gac 1159
Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn Leu Ser Leu His Asp
280 285 290
atg ttt gtc cgg gag acg tct gcc aat ggc aag gtc tcc ttc tgg acc 1207
Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys Val Ser Phe Trp Thr
295 300 305
att cac ccc agt gcc aac cgc tac ttg aca ttg gac cag gtg ttt aag 1255
Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu Asp Gln Val Phe Lys
310 315 320
cag cag aaa cga ccg aat cca gag ctc cgc cgg aac atg acc atc aaa 1303
Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg Asn Met Thr Ile Lys
325 330 335 340
acc gaa ctc ccc ctg ggc gca cgg cgg aag atg aag cca ctg cta cca 1351
Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met Lys Pro Leu Leu Pro
345 350 355
cgg gtc agc tca tac ctg gta cct atc cag ttc ccg gtg aac cag tca 1399
Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe Pro Val Asn Gln Ser
360 365 370
ctg gtg ttg cag ccc tcg gtg aag gtg cca ttg ccc ctg gcg gct tcc 1447
Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu Pro Leu Ala Ala Ser
375 380 385
ctc atg agc tca gag ctt gcc cgc cat agc aag cga gtc cgc att gcc 1495
Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys Arg Val Arg Ile Ala
390 395 400
ccc aag gtg ctg cta gct gag gag ggg ata gct cct ctt tct tct gca 1543
Pro Lys Val Leu Leu Ala Glu Glu Gly Ile Ala Pro Leu Ser Ser Ala
405 410 415 420
gga cca ggg aaa gag gag aaa ctc ctg ttt gga gaa ggg ttt tct cct 1591
Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe Gly Glu Gly Phe Ser Pro
425 430 435
ttg ctt cca gtt cag act atc aag gag gaa gaa atc cag cct ggg gag 1639
Leu Leu Pro Val Gln Thr Ile Lys Glu Glu Glu Ile Gln Pro Gly Glu
440 445 450
gaa atg cca cac tta gcg aga ccc atc aaa gtg gag agc cct ccc ttg 1687
Glu Met Pro His Leu Ala Arg Pro Ile Lys Val Glu Ser Pro Pro Leu
455 460 465
gaa gag tgg ccc tcc ccg gcc cca tct ttc aaa gag gaa tca tct cac 1735
Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys Glu Glu Ser Ser His
470 475 480
tcc tgg gag gat tcg tcc caa tct ccc acc cca aga ccc aag aag tcc 1783
Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr Pro Arg Pro Lys Lys Ser
485 490 495 500
tac agt ggg ctt agg tcc cca acc cgg tgt gtc tcg gaa atg ctt gtg 1831
Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys Val Ser Glu Met Leu Val
505 510 515
att caa cac agg gag agg agg gag agg agc cgg tct cgg agg aaa cag 1879
Ile Gln His Arg Glu Arg Arg Glu Arg Ser Arg Ser Arg Arg Lys Gln
520 525 530
cat cta ctg cct ccc tgt gtg gat gag ccg gag ctg ctc ttc tca gag 1927
His Leu Leu Pro Pro Cys Val Asp Glu Pro Glu Leu Leu Phe Ser Glu
535 540 545
ggg ccc agt act tcc cgc tgg gcc gca gag ctc ccg ttc cca gca gac 1975
Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu Leu Pro Phe Pro Ala Asp
550 555 560
tcc tct gac cct gcc tcc cag ctc agc tac tcc cag gaa gtg gga gga 2023
Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr Ser Gln Glu Val Gly Gly
565 570 575 580
cct ttt aag aca ccc att aag gaa acg ctg ccc atc tcc tcc acc ccg 2071
Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu Pro Ile Ser Ser Thr Pro
585 590 595
agc aaa tct gtc ctc ccc aga acc cct gaa tcc tgg agg ctc acg ccc 2119
Ser Lys Ser Val Leu Pro Arg Thr Pro Glu Ser Trp Arg Leu Thr Pro
600 605 610
cca gcc aaa gta ggg gga ctg gat ttc agc cca gta caa acc tcc cag 2167
Pro Ala Lys Val Gly Gly Leu Asp Phe Ser Pro Val Gln Thr Ser Gln
615 620 625
ggt gcc tct gac ccc ttg cct gac ccc ctg ggg ctg atg gat ctc agc 2215
Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu Gly Leu Met Asp Leu Ser
630 635 640
acc act ccc ttg caa agt gct ccc ccc ctt gaa tca ccg caa agg ctc 2263
Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu Glu Ser Pro Gln Arg Leu
645 650 655 660
ctc agt tca gaa ccc tta gac ctc atc tcc gtc ccc ttt ggc aac tct 2311
Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser Val Pro Phe Gly Asn Ser
665 670 675
tct ccc tca gat ata gac gtc ccc aag cca ggc tcc ccg gag cca cag 2359
Ser Pro Ser Asp Ile Asp Val Pro Lys Pro Gly Ser Pro Glu Pro Gln
680 685 690
gtt tct ggc ctt gca gcc aat cgt tct ctg aca gaa ggc ctg gtc ctg 2407
Val Ser Gly Leu Ala Ala Asn Arg Ser Leu Thr Glu Gly Leu Val Leu
695 700 705
gac aca atg aat gac agc ctc agc aag atc ctg ctg gac atc agc ttt 2455
Asp Thr Met Asn Asp Ser Leu Ser Lys Ile Leu Leu Asp Ile Ser Phe
710 715 720
cct ggc ctg gac gag gac cca ctg ggc cct gac aac atc aac tgg tcc 2503
Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro Asp Asn Ile Asn Trp Ser
725 730 735 740
cag ttt att cct gag cta cag tag agccctgccc ttgcccctgt gctcaagctg 2557
Gln Phe Ile Pro Glu Leu Gln
745
tccaccatcc cgggcactcc aaggctcagt gcaccccaag cctctgagtg aggacagcag 2617
gcagggactg ttctgctcct catagctccc tgctgcctga ttatgcaaaa gtagcagtca 2677
caccctagcc actgctggga ccttgtgttc cccaagagta tctgattcct ctgctgtccc 2737
tgccaggagc tgaagggtgg gaacaacaaa ggcaatggtg aaaagagatt aggaaccccc 2797
cagcctgttt ccattctctg cccagcagtc tcttaccttc cctgatcttt gcagggtggt 2857
ccgtgtaaat agtataaatt ctccaaatta tcctctaatt ataaatgtaa gcttatttcc 2917
ttagatcatt atccagagac tgccagaagg tgggtaggat gacctggggt ttcaattgac 2977
ttctgttcct tgcttttagt tttgatagaa gggaagacct gcagtgcacg gtttcttcca 3037
ggctgaggta cctggatctt gggttcttca ctgcagggac ccagacaagt ggatctgctt 3097
gccagagtcc tttttgcccc tccctgccac ctccccgtgt ttccaagtca gctttcctgc 3157
aagaagaaat cctggttaaa aaagtctttt gtattgggtc aggagttgaa tttggggtgg 3217
gaggatggat gcaactgaag cagagtgtgg gtgcccagat gtgcgctatt agatgtttct 3277
ctgataatgt ccccaatcat accagggaga ctggcattga cgagaactca ggtggaggct 3337
tgagaaggcc gaaagggccc ctgacctgcc tggcttcctt agcttgcccc tcagctttgc 3397
aaagagccac cctaggcccc agctgaccgc atgggtgtga gccagcttga gaacactaac 3457
tactcaataa aagcgaaggt ggacatgaaa aaaaaaaaaa aaaaaa 3503
<210> 71
<211> 747
<212> белок
<213> Homo sapiens
<400> 71
Met Lys Thr Ser Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu
1 5 10 15
Pro Leu Pro Val Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro
20 25 30
Lys Arg Ser Pro Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys
35 40 45
Glu Val Ala Glu Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile
50 55 60
Ile Asn His Pro Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn
65 70 75 80
Asn Ala Asn Ile His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys
85 90 95
Glu Ser Gly Ser Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly
100 105 110
Gly Ala Pro Thr Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser
115 120 125
Tyr Asp Ala Lys Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys
130 135 140
Pro Ala Ala Arg Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys
145 150 155 160
Glu Gln Lys Arg Glu Thr Cys Asp Gly Glu Ala Ala Gly Cys Thr Ile
165 170 175
Asn Asn Ser Leu Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser Asp
180 185 190
Gly Leu Gly Ser Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu Asn
195 200 205
Cys His Leu Glu Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg Pro
210 215 220
Ser Ala Ser Trp Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser Tyr
225 230 235 240
Met Ala Met Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg Met
245 250 255
Thr Leu Lys Asp Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr Phe
260 265 270
Lys His Ile Ala Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn Leu
275 280 285
Ser Leu His Asp Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys Val
290 295 300
Ser Phe Trp Thr Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu Asp
305 310 315 320
Gln Val Phe Lys Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg Asn
325 330 335
Met Thr Ile Lys Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met Lys
340 345 350
Pro Leu Leu Pro Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe Pro
355 360 365
Val Asn Gln Ser Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu Pro
370 375 380
Leu Ala Ala Ser Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys Arg
385 390 395 400
Val Arg Ile Ala Pro Lys Val Leu Leu Ala Glu Glu Gly Ile Ala Pro
405 410 415
Leu Ser Ser Ala Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe Gly Glu
420 425 430
Gly Phe Ser Pro Leu Leu Pro Val Gln Thr Ile Lys Glu Glu Glu Ile
435 440 445
Gln Pro Gly Glu Glu Met Pro His Leu Ala Arg Pro Ile Lys Val Glu
450 455 460
Ser Pro Pro Leu Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys Glu
465 470 475 480
Glu Ser Ser His Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr Pro Arg
485 490 495
Pro Lys Lys Ser Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys Val Ser
500 505 510
Glu Met Leu Val Ile Gln His Arg Glu Arg Arg Glu Arg Ser Arg Ser
515 520 525
Arg Arg Lys Gln His Leu Leu Pro Pro Cys Val Asp Glu Pro Glu Leu
530 535 540
Leu Phe Ser Glu Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu Leu Pro
545 550 555 560
Phe Pro Ala Asp Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr Ser Gln
565 570 575
Glu Val Gly Gly Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu Pro Ile
580 585 590
Ser Ser Thr Pro Ser Lys Ser Val Leu Pro Arg Thr Pro Glu Ser Trp
595 600 605
Arg Leu Thr Pro Pro Ala Lys Val Gly Gly Leu Asp Phe Ser Pro Val
610 615 620
Gln Thr Ser Gln Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu Gly Leu
625 630 635 640
Met Asp Leu Ser Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu Glu Ser
645 650 655
Pro Gln Arg Leu Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser Val Pro
660 665 670
Phe Gly Asn Ser Ser Pro Ser Asp Ile Asp Val Pro Lys Pro Gly Ser
675 680 685
Pro Glu Pro Gln Val Ser Gly Leu Ala Ala Asn Arg Ser Leu Thr Glu
690 695 700
Gly Leu Val Leu Asp Thr Met Asn Asp Ser Leu Ser Lys Ile Leu Leu
705 710 715 720
Asp Ile Ser Phe Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro Asp Asn
725 730 735
Ile Asn Trp Ser Gln Phe Ile Pro Glu Leu Gln
740 745
<210> 72
<211> 3551
<212> ДНК
<213> Homo sapiens
<220>
<221> кодирующая последовательность
<222> (284)..(2575)
<400> 72
tttcaaacag cggaacaaac tgaaagctcc ggtgccagac cccacccccg gccccggccc 60
gggaccccct cccctcccgg gatcccccgg ggttcccacc ccgcccgcac cgccggggac 120
ccggccggtc cggcgcgagc ccccgtccgg ggccctggct cggcccccag gttggaggag 180
cccggagccc gccttcggag ctacggccta acggcggcgg cgactgcagt ctggagggtc 240
cacacttgtg attctcaatg gagagtgaaa acgcagattc ata atg aaa act agc 295
Met Lys Thr Ser
1
ccc cgt cgg cca ctg att ctc aaa aga cgg agg ctg ccc ctt cct gtt 343
Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu Pro Leu Pro Val
5 10 15 20
caa aat gcc cca agt gaa aca tca gag gag gaa cct aag aga tcc cct 391
Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro Lys Arg Ser Pro
25 30 35
gcc caa cag gag tct aat caa gca gag gcc tcc aag gaa gtg gca gag 439
Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys Glu Val Ala Glu
40 45 50
tcc aac tct tgc aag ttt cca gct ggg atc aag att att aac cac ccc 487
Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile Ile Asn His Pro
55 60 65
acc atg ccc aac acg caa gta gtg gcc atc ccc aac aat gct aat att 535
Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn Asn Ala Asn Ile
70 75 80
cac agc atc atc aca gca ctg act gcc aag gga aaa gag agt ggc agt 583
His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys Glu Ser Gly Ser
85 90 95 100
agt ggg ccc aac aaa ttc atc ctc atc agc tgt ggg gga gcc cca act 631
Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly Gly Ala Pro Thr
105 110 115
cag cct cca gga ctc cgg cct caa acc caa acc agc tat gat gcc aaa 679
Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser Tyr Asp Ala Lys
120 125 130
agg aca gaa gtg acc ctg gag acc ttg gga cca aaa cct gca gct agg 727
Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys Pro Ala Ala Arg
135 140 145
gat gtg aat ctt cct aga cca cct gga gcc ctt tgc gag cag aaa cgg 775
Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys Glu Gln Lys Arg
150 155 160
gag acc tgt gca gat ggt gag gca gca ggc tgc act atc aac aat agc 823
Glu Thr Cys Ala Asp Gly Glu Ala Ala Gly Cys Thr Ile Asn Asn Ser
165 170 175 180
cta tcc aac atc cag tgg ctt cga aag atg agt tct gat gga ctg ggc 871
Leu Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser Asp Gly Leu Gly
185 190 195
tcc cgc agc atc aag caa gag atg gag gaa aag gag aat tgt cac ctg 919
Ser Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu Asn Cys His Leu
200 205 210
gag cag cga cag gtt aag gtt gag gag cct tcg aga cca tca gcg tcc 967
Glu Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg Pro Ser Ala Ser
215 220 225
tgg cag aac tct gtg tct gag cgg cca ccc tac tct tac atg gcc atg 1015
Trp Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser Tyr Met Ala Met
230 235 240
ata caa ttc gcc atc aac agc act gag agg aag cgc atg act ttg aaa 1063
Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg Met Thr Leu Lys
245 250 255 260
gac atc tat acg tgg att gag gac cac ttt ccc tac ttt aag cac att 1111
Asp Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr Phe Lys His Ile
265 270 275
gcc aag cca ggc tgg aag aac tcc atc cgc cac aac ctt tcc ctg cac 1159
Ala Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn Leu Ser Leu His
280 285 290
gac atg ttt gtc cgg gag acg tct gcc aat ggc aag gtc tcc ttc tgg 1207
Asp Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys Val Ser Phe Trp
295 300 305
acc att cac ccc agt gcc aac cgc tac ttg aca ttg gac cag gtg ttt 1255
Thr Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu Asp Gln Val Phe
310 315 320
aag cca ctg gac cca ggg tct cca caa ttg ccc gag cac ttg gaa tca 1303
Lys Pro Leu Asp Pro Gly Ser Pro Gln Leu Pro Glu His Leu Glu Ser
325 330 335 340
cag cag aaa cga ccg aat cca gag ctc cgc cgg aac atg acc atc aaa 1351
Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg Asn Met Thr Ile Lys
345 350 355
acc gaa ctc ccc ctg ggc gca cgg cgg aag atg aag cca ctg cta cca 1399
Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met Lys Pro Leu Leu Pro
360 365 370
cgg gtc agc tca tac ctg gta cct atc cag ttc ccg gtg aac cag tca 1447
Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe Pro Val Asn Gln Ser
375 380 385
ctg gtg ttg cag ccc tcg gtg aag gtg cca ttg ccc ctg gcg gct tcc 1495
Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu Pro Leu Ala Ala Ser
390 395 400
ctc atg agc tca gag ctt gcc cgc cat agc aag cga gtc cgc att gcc 1543
Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys Arg Val Arg Ile Ala
405 410 415 420
ccc aag gtg ctg cta gct gag gag ggg ata gct cct ctt tct tct gca 1591
Pro Lys Val Leu Leu Ala Glu Glu Gly Ile Ala Pro Leu Ser Ser Ala
425 430 435
gga cca ggg aaa gag gag aaa ctc ctg ttt gga gaa ggg ttt tct cct 1639
Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe Gly Glu Gly Phe Ser Pro
440 445 450
ttg ctt cca gtt cag act atc aag gag gaa gaa atc cag cct ggg gag 1687
Leu Leu Pro Val Gln Thr Ile Lys Glu Glu Glu Ile Gln Pro Gly Glu
455 460 465
gaa atg cca cac tta gcg aga ccc atc aaa gtg gag agc cct ccc ttg 1735
Glu Met Pro His Leu Ala Arg Pro Ile Lys Val Glu Ser Pro Pro Leu
470 475 480
gaa gag tgg ccc tcc ccg gcc cca tct ttc aaa gag gaa tca tct cac 1783
Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys Glu Glu Ser Ser His
485 490 495 500
tcc tgg gag gat tcg tcc caa tct ccc acc cca aga ccc aag aag tcc 1831
Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr Pro Arg Pro Lys Lys Ser
505 510 515
tac agt ggg ctt agg tcc cca acc cgg tgt gtc tcg gaa atg ctt gtg 1879
Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys Val Ser Glu Met Leu Val
520 525 530
att caa cac agg gag agg agg gag agg agc cgg tct cgg agg aaa cag 1927
Ile Gln His Arg Glu Arg Arg Glu Arg Ser Arg Ser Arg Arg Lys Gln
535 540 545
cat cta ctg cct ccc tgt gtg gat gag ccg gag ctg ctc ttc tca gag 1975
His Leu Leu Pro Pro Cys Val Asp Glu Pro Glu Leu Leu Phe Ser Glu
550 555 560
ggg ccc agt act tcc cgc tgg gcc gca gag ctc ccg ttc cca gca gac 2023
Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu Leu Pro Phe Pro Ala Asp
565 570 575 580
tcc tct gac cct gcc tcc cag ctc agc tac tcc cag gaa gtg gga gga 2071
Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr Ser Gln Glu Val Gly Gly
585 590 595
cct ttt aag aca ccc att aag gaa acg ctg ccc atc tcc tcc acc ccg 2119
Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu Pro Ile Ser Ser Thr Pro
600 605 610
agc aaa tct gtc ctc ccc aga acc cct gaa tcc tgg agg ctc acg ccc 2167
Ser Lys Ser Val Leu Pro Arg Thr Pro Glu Ser Trp Arg Leu Thr Pro
615 620 625
cca gcc aaa gta ggg gga ctg gat ttc agc cca gta caa acc tcc cag 2215
Pro Ala Lys Val Gly Gly Leu Asp Phe Ser Pro Val Gln Thr Ser Gln
630 635 640
ggt gcc tct gac ccc ttg cct gac ccc ctg ggg ctg atg gat ctc agc 2263
Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu Gly Leu Met Asp Leu Ser
645 650 655 660
acc act ccc ttg caa agt gct ccc ccc ctt gaa tca ccg caa agg ctc 2311
Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu Glu Ser Pro Gln Arg Leu
665 670 675
ctc agt tca gaa ccc tta gac ctc atc tcc gtc ccc ttt ggc aac tct 2359
Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser Val Pro Phe Gly Asn Ser
680 685 690
tct ccc tca gat ata gac gtc ccc aag cca ggc tcc ccg gag cca cag 2407
Ser Pro Ser Asp Ile Asp Val Pro Lys Pro Gly Ser Pro Glu Pro Gln
695 700 705
gtt tct ggc ctt gca gcc aat cgt tct ctg aca gaa ggc ctg gtc ctg 2455
Val Ser Gly Leu Ala Ala Asn Arg Ser Leu Thr Glu Gly Leu Val Leu
710 715 720
gac aca atg aat gac agc ctc agc aag atc ctg ctg gac atc agc ttt 2503
Asp Thr Met Asn Asp Ser Leu Ser Lys Ile Leu Leu Asp Ile Ser Phe
725 730 735 740
cct ggc ctg gac gag gac cca ctg ggc cct gac aac atc aac tgg tcc 2551
Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro Asp Asn Ile Asn Trp Ser
745 750 755
cag ttt att cct gag cta cag tag agccctgccc ttgcccctgt gctcaagctg 2605
Gln Phe Ile Pro Glu Leu Gln
760
tccaccatcc cgggcactcc aaggctcagt gcaccccaag cctctgagtg aggacagcag 2665
gcagggactg ttctgctcct catagctccc tgctgcctga ttatgcaaaa gtagcagtca 2725
caccctagcc actgctggga ccttgtgttc cccaagagta tctgattcct ctgctgtccc 2785
tgccaggagc tgaagggtgg gaacaacaaa ggcaatggtg aaaagagatt aggaaccccc 2845
cagcctgttt ccattctctg cccagcagtc tcttaccttc cctgatcttt gcagggtggt 2905
ccgtgtaaat agtataaatt ctccaaatta tcctctaatt ataaatgtaa gcttatttcc 2965
ttagatcatt atccagagac tgccagaagg tgggtaggat gacctggggt ttcaattgac 3025
ttctgttcct tgcttttagt tttgatagaa gggaagacct gcagtgcacg gtttcttcca 3085
ggctgaggta cctggatctt gggttcttca ctgcagggac ccagacaagt ggatctgctt 3145
gccagagtcc tttttgcccc tccctgccac ctccccgtgt ttccaagtca gctttcctgc 3205
aagaagaaat cctggttaaa aaagtctttt gtattgggtc aggagttgaa tttggggtgg 3265
gaggatggat gcaactgaag cagagtgtgg gtgcccagat gtgcgctatt agatgtttct 3325
ctgataatgt ccccaatcat accagggaga ctggcattga cgagaactca ggtggaggct 3385
tgagaaggcc gaaagggccc ctgacctgcc tggcttcctt agcttgcccc tcagctttgc 3445
aaagagccac cctaggcccc agctgaccgc atgggtgtga gccagcttga gaacactaac 3505
tactcaataa aagcgaaggt ggacatgaaa aaaaaaaaaa aaaaaa 3551
<210> 73
<211> 763
<212> белок
<213> Homo sapiens
<400> 73
Met Lys Thr Ser Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu
1 5 10 15
Pro Leu Pro Val Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro
20 25 30
Lys Arg Ser Pro Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys
35 40 45
Glu Val Ala Glu Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile
50 55 60
Ile Asn His Pro Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn
65 70 75 80
Asn Ala Asn Ile His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys
85 90 95
Glu Ser Gly Ser Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly
100 105 110
Gly Ala Pro Thr Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser
115 120 125
Tyr Asp Ala Lys Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys
130 135 140
Pro Ala Ala Arg Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys
145 150 155 160
Glu Gln Lys Arg Glu Thr Cys Ala Asp Gly Glu Ala Ala Gly Cys Thr
165 170 175
Ile Asn Asn Ser Leu Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser
180 185 190
Asp Gly Leu Gly Ser Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu
195 200 205
Asn Cys His Leu Glu Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg
210 215 220
Pro Ser Ala Ser Trp Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser
225 230 235 240
Tyr Met Ala Met Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg
245 250 255
Met Thr Leu Lys Asp Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr
260 265 270
Phe Lys His Ile Ala Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn
275 280 285
Leu Ser Leu His Asp Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys
290 295 300
Val Ser Phe Trp Thr Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu
305 310 315 320
Asp Gln Val Phe Lys Pro Leu Asp Pro Gly Ser Pro Gln Leu Pro Glu
325 330 335
His Leu Glu Ser Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg Asn
340 345 350
Met Thr Ile Lys Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met Lys
355 360 365
Pro Leu Leu Pro Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe Pro
370 375 380
Val Asn Gln Ser Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu Pro
385 390 395 400
Leu Ala Ala Ser Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys Arg
405 410 415
Val Arg Ile Ala Pro Lys Val Leu Leu Ala Glu Glu Gly Ile Ala Pro
420 425 430
Leu Ser Ser Ala Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe Gly Glu
435 440 445
Gly Phe Ser Pro Leu Leu Pro Val Gln Thr Ile Lys Glu Glu Glu Ile
450 455 460
Gln Pro Gly Glu Glu Met Pro His Leu Ala Arg Pro Ile Lys Val Glu
465 470 475 480
Ser Pro Pro Leu Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe Lys Glu
485 490 495
Glu Ser Ser His Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr Pro Arg
500 505 510
Pro Lys Lys Ser Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys Val Ser
515 520 525
Glu Met Leu Val Ile Gln His Arg Glu Arg Arg Glu Arg Ser Arg Ser
530 535 540
Arg Arg Lys Gln His Leu Leu Pro Pro Cys Val Asp Glu Pro Glu Leu
545 550 555 560
Leu Phe Ser Glu Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu Leu Pro
565 570 575
Phe Pro Ala Asp Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr Ser Gln
580 585 590
Glu Val Gly Gly Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu Pro Ile
595 600 605
Ser Ser Thr Pro Ser Lys Ser Val Leu Pro Arg Thr Pro Glu Ser Trp
610 615 620
Arg Leu Thr Pro Pro Ala Lys Val Gly Gly Leu Asp Phe Ser Pro Val
625 630 635 640
Gln Thr Ser Gln Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu Gly Leu
645 650 655
Met Asp Leu Ser Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu Glu Ser
660 665 670
Pro Gln Arg Leu Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser Val Pro
675 680 685
Phe Gly Asn Ser Ser Pro Ser Asp Ile Asp Val Pro Lys Pro Gly Ser
690 695 700
Pro Glu Pro Gln Val Ser Gly Leu Ala Ala Asn Arg Ser Leu Thr Glu
705 710 715 720
Gly Leu Val Leu Asp Thr Met Asn Asp Ser Leu Ser Lys Ile Leu Leu
725 730 735
Asp Ile Ser Phe Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro Asp Asn
740 745 750
Ile Asn Trp Ser Gln Phe Ile Pro Glu Leu Gln
755 760
<210> 74
<211> 3665
<212> ДНК
<213> Homo sapiens
<220>
<221> кодирующая последовательность
<222> (284)..(2689)
<400> 74
tttcaaacag cggaacaaac tgaaagctcc ggtgccagac cccacccccg gccccggccc 60
gggaccccct cccctcccgg gatcccccgg ggttcccacc ccgcccgcac cgccggggac 120
ccggccggtc cggcgcgagc ccccgtccgg ggccctggct cggcccccag gttggaggag 180
cccggagccc gccttcggag ctacggccta acggcggcgg cgactgcagt ctggagggtc 240
cacacttgtg attctcaatg gagagtgaaa acgcagattc ata atg aaa act agc 295
Met Lys Thr Ser
1
ccc cgt cgg cca ctg att ctc aaa aga cgg agg ctg ccc ctt cct gtt 343
Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu Pro Leu Pro Val
5 10 15 20
caa aat gcc cca agt gaa aca tca gag gag gaa cct aag aga tcc cct 391
Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro Lys Arg Ser Pro
25 30 35
gcc caa cag gag tct aat caa gca gag gcc tcc aag gaa gtg gca gag 439
Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys Glu Val Ala Glu
40 45 50
tcc aac tct tgc aag ttt cca gct ggg atc aag att att aac cac ccc 487
Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile Ile Asn His Pro
55 60 65
acc atg ccc aac acg caa gta gtg gcc atc ccc aac aat gct aat att 535
Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn Asn Ala Asn Ile
70 75 80
cac agc atc atc aca gca ctg act gcc aag gga aaa gag agt ggc agt 583
His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys Glu Ser Gly Ser
85 90 95 100
agt ggg ccc aac aaa ttc atc ctc atc agc tgt ggg gga gcc cca act 631
Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly Gly Ala Pro Thr
105 110 115
cag cct cca gga ctc cgg cct caa acc caa acc agc tat gat gcc aaa 679
Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser Tyr Asp Ala Lys
120 125 130
agg aca gaa gtg acc ctg gag acc ttg gga cca aaa cct gca gct agg 727
Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys Pro Ala Ala Arg
135 140 145
gat gtg aat ctt cct aga cca cct gga gcc ctt tgc gag cag aaa cgg 775
Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys Glu Gln Lys Arg
150 155 160
gag acc tgt gca gat ggt gag gca gca ggc tgc act atc aac aat agc 823
Glu Thr Cys Ala Asp Gly Glu Ala Ala Gly Cys Thr Ile Asn Asn Ser
165 170 175 180
cta tcc aac atc cag tgg ctt cga aag atg agt tct gat gga ctg ggc 871
Leu Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser Asp Gly Leu Gly
185 190 195
tcc cgc agc atc aag caa gag atg gag gaa aag gag aat tgt cac ctg 919
Ser Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu Asn Cys His Leu
200 205 210
gag cag cga cag gtt aag gtt gag gag cct tcg aga cca tca gcg tcc 967
Glu Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg Pro Ser Ala Ser
215 220 225
tgg cag aac tct gtg tct gag cgg cca ccc tac tct tac atg gcc atg 1015
Trp Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser Tyr Met Ala Met
230 235 240
ata caa ttc gcc atc aac agc act gag agg aag cgc atg act ttg aaa 1063
Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg Met Thr Leu Lys
245 250 255 260
gac atc tat acg tgg att gag gac cac ttt ccc tac ttt aag cac att 1111
Asp Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr Phe Lys His Ile
265 270 275
gcc aag cca ggc tgg aag aac tcc atc cgc cac aac ctt tcc ctg cac 1159
Ala Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn Leu Ser Leu His
280 285 290
gac atg ttt gtc cgg gag acg tct gcc aat ggc aag gtc tcc ttc tgg 1207
Asp Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys Val Ser Phe Trp
295 300 305
acc att cac ccc agt gcc aac cgc tac ttg aca ttg gac cag gtg ttt 1255
Thr Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu Asp Gln Val Phe
310 315 320
aag cca ctg gac cca ggg tct cca caa ttg ccc gag cac ttg gaa tca 1303
Lys Pro Leu Asp Pro Gly Ser Pro Gln Leu Pro Glu His Leu Glu Ser
325 330 335 340
cag cag aaa cga ccg aat cca gag ctc cgc cgg aac atg acc atc aaa 1351
Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg Asn Met Thr Ile Lys
345 350 355
acc gaa ctc ccc ctg ggc gca cgg cgg aag atg aag cca ctg cta cca 1399
Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met Lys Pro Leu Leu Pro
360 365 370
cgg gtc agc tca tac ctg gta cct atc cag ttc ccg gtg aac cag tca 1447
Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe Pro Val Asn Gln Ser
375 380 385
ctg gtg ttg cag ccc tcg gtg aag gtg cca ttg ccc ctg gcg gct tcc 1495
Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu Pro Leu Ala Ala Ser
390 395 400
ctc atg agc tca gag ctt gcc cgc cat agc aag cga gtc cgc att gcc 1543
Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys Arg Val Arg Ile Ala
405 410 415 420
ccc aag gtt ttt ggg gaa cag gtg gtg ttt ggt tac atg agt aag ttc 1591
Pro Lys Val Phe Gly Glu Gln Val Val Phe Gly Tyr Met Ser Lys Phe
425 430 435
ttt agt ggc gat ctg cga gat ttt ggt aca ccc atc acc agc ttg ttt 1639
Phe Ser Gly Asp Leu Arg Asp Phe Gly Thr Pro Ile Thr Ser Leu Phe
440 445 450
aat ttt atc ttt ctt tgt tta tca gtg ctg cta gct gag gag ggg ata 1687
Asn Phe Ile Phe Leu Cys Leu Ser Val Leu Leu Ala Glu Glu Gly Ile
455 460 465
gct cct ctt tct tct gca gga cca ggg aaa gag gag aaa ctc ctg ttt 1735
Ala Pro Leu Ser Ser Ala Gly Pro Gly Lys Glu Glu Lys Leu Leu Phe
470 475 480
gga gaa ggg ttt tct cct ttg ctt cca gtt cag act atc aag gag gaa 1783
Gly Glu Gly Phe Ser Pro Leu Leu Pro Val Gln Thr Ile Lys Glu Glu
485 490 495 500
gaa atc cag cct ggg gag gaa atg cca cac tta gcg aga ccc atc aaa 1831
Glu Ile Gln Pro Gly Glu Glu Met Pro His Leu Ala Arg Pro Ile Lys
505 510 515
gtg gag agc cct ccc ttg gaa gag tgg ccc tcc ccg gcc cca tct ttc 1879
Val Glu Ser Pro Pro Leu Glu Glu Trp Pro Ser Pro Ala Pro Ser Phe
520 525 530
aaa gag gaa tca tct cac tcc tgg gag gat tcg tcc caa tct ccc acc 1927
Lys Glu Glu Ser Ser His Ser Trp Glu Asp Ser Ser Gln Ser Pro Thr
535 540 545
cca aga ccc aag aag tcc tac agt ggg ctt agg tcc cca acc cgg tgt 1975
Pro Arg Pro Lys Lys Ser Tyr Ser Gly Leu Arg Ser Pro Thr Arg Cys
550 555 560
gtc tcg gaa atg ctt gtg att caa cac agg gag agg agg gag agg agc 2023
Val Ser Glu Met Leu Val Ile Gln His Arg Glu Arg Arg Glu Arg Ser
565 570 575 580
cgg tct cgg agg aaa cag cat cta ctg cct ccc tgt gtg gat gag ccg 2071
Arg Ser Arg Arg Lys Gln His Leu Leu Pro Pro Cys Val Asp Glu Pro
585 590 595
gag ctg ctc ttc tca gag ggg ccc agt act tcc cgc tgg gcc gca gag 2119
Glu Leu Leu Phe Ser Glu Gly Pro Ser Thr Ser Arg Trp Ala Ala Glu
600 605 610
ctc ccg ttc cca gca gac tcc tct gac cct gcc tcc cag ctc agc tac 2167
Leu Pro Phe Pro Ala Asp Ser Ser Asp Pro Ala Ser Gln Leu Ser Tyr
615 620 625
tcc cag gaa gtg gga gga cct ttt aag aca ccc att aag gaa acg ctg 2215
Ser Gln Glu Val Gly Gly Pro Phe Lys Thr Pro Ile Lys Glu Thr Leu
630 635 640
ccc atc tcc tcc acc ccg agc aaa tct gtc ctc ccc aga acc cct gaa 2263
Pro Ile Ser Ser Thr Pro Ser Lys Ser Val Leu Pro Arg Thr Pro Glu
645 650 655 660
tcc tgg agg ctc acg ccc cca gcc aaa gta ggg gga ctg gat ttc agc 2311
Ser Trp Arg Leu Thr Pro Pro Ala Lys Val Gly Gly Leu Asp Phe Ser
665 670 675
cca gta caa acc tcc cag ggt gcc tct gac ccc ttg cct gac ccc ctg 2359
Pro Val Gln Thr Ser Gln Gly Ala Ser Asp Pro Leu Pro Asp Pro Leu
680 685 690
ggg ctg atg gat ctc agc acc act ccc ttg caa agt gct ccc ccc ctt 2407
Gly Leu Met Asp Leu Ser Thr Thr Pro Leu Gln Ser Ala Pro Pro Leu
695 700 705
gaa tca ccg caa agg ctc ctc agt tca gaa ccc tta gac ctc atc tcc 2455
Glu Ser Pro Gln Arg Leu Leu Ser Ser Glu Pro Leu Asp Leu Ile Ser
710 715 720
gtc ccc ttt ggc aac tct tct ccc tca gat ata gac gtc ccc aag cca 2503
Val Pro Phe Gly Asn Ser Ser Pro Ser Asp Ile Asp Val Pro Lys Pro
725 730 735 740
ggc tcc ccg gag cca cag gtt tct ggc ctt gca gcc aat cgt tct ctg 2551
Gly Ser Pro Glu Pro Gln Val Ser Gly Leu Ala Ala Asn Arg Ser Leu
745 750 755
aca gaa ggc ctg gtc ctg gac aca atg aat gac agc ctc agc aag atc 2599
Thr Glu Gly Leu Val Leu Asp Thr Met Asn Asp Ser Leu Ser Lys Ile
760 765 770
ctg ctg gac atc agc ttt cct ggc ctg gac gag gac cca ctg ggc cct 2647
Leu Leu Asp Ile Ser Phe Pro Gly Leu Asp Glu Asp Pro Leu Gly Pro
775 780 785
gac aac atc aac tgg tcc cag ttt att cct gag cta cag tag 2689
Asp Asn Ile Asn Trp Ser Gln Phe Ile Pro Glu Leu Gln
790 795 800
agccctgccc ttgcccctgt gctcaagctg tccaccatcc cgggcactcc aaggctcagt 2749
gcaccccaag cctctgagtg aggacagcag gcagggactg ttctgctcct catagctccc 2809
tgctgcctga ttatgcaaaa gtagcagtca caccctagcc actgctggga ccttgtgttc 2869
cccaagagta tctgattcct ctgctgtccc tgccaggagc tgaagggtgg gaacaacaaa 2929
ggcaatggtg aaaagagatt aggaaccccc cagcctgttt ccattctctg cccagcagtc 2989
tcttaccttc cctgatcttt gcagggtggt ccgtgtaaat agtataaatt ctccaaatta 3049
tcctctaatt ataaatgtaa gcttatttcc ttagatcatt atccagagac tgccagaagg 3109
tgggtaggat gacctggggt ttcaattgac ttctgttcct tgcttttagt tttgatagaa 3169
gggaagacct gcagtgcacg gtttcttcca ggctgaggta cctggatctt gggttcttca 3229
ctgcagggac ccagacaagt ggatctgctt gccagagtcc tttttgcccc tccctgccac 3289
ctccccgtgt ttccaagtca gctttcctgc aagaagaaat cctggttaaa aaagtctttt 3349
gtattgggtc aggagttgaa tttggggtgg gaggatggat gcaactgaag cagagtgtgg 3409
gtgcccagat gtgcgctatt agatgtttct ctgataatgt ccccaatcat accagggaga 3469
ctggcattga cgagaactca ggtggaggct tgagaaggcc gaaagggccc ctgacctgcc 3529
tggcttcctt agcttgcccc tcagctttgc aaagagccac cctaggcccc agctgaccgc 3589
atgggtgtga gccagcttga gaacactaac tactcaataa aagcgaaggt ggacatgaaa 3649
aaaaaaaaaa aaaaaa 3665
<210> 75
<211> 801
<212> белок
<213> Homo sapiens
<400> 75
Met Lys Thr Ser Pro Arg Arg Pro Leu Ile Leu Lys Arg Arg Arg Leu
1 5 10 15
Pro Leu Pro Val Gln Asn Ala Pro Ser Glu Thr Ser Glu Glu Glu Pro
20 25 30
Lys Arg Ser Pro Ala Gln Gln Glu Ser Asn Gln Ala Glu Ala Ser Lys
35 40 45
Glu Val Ala Glu Ser Asn Ser Cys Lys Phe Pro Ala Gly Ile Lys Ile
50 55 60
Ile Asn His Pro Thr Met Pro Asn Thr Gln Val Val Ala Ile Pro Asn
65 70 75 80
Asn Ala Asn Ile His Ser Ile Ile Thr Ala Leu Thr Ala Lys Gly Lys
85 90 95
Glu Ser Gly Ser Ser Gly Pro Asn Lys Phe Ile Leu Ile Ser Cys Gly
100 105 110
Gly Ala Pro Thr Gln Pro Pro Gly Leu Arg Pro Gln Thr Gln Thr Ser
115 120 125
Tyr Asp Ala Lys Arg Thr Glu Val Thr Leu Glu Thr Leu Gly Pro Lys
130 135 140
Pro Ala Ala Arg Asp Val Asn Leu Pro Arg Pro Pro Gly Ala Leu Cys
145 150 155 160
Glu Gln Lys Arg Glu Thr Cys Ala Asp Gly Glu Ala Ala Gly Cys Thr
165 170 175
Ile Asn Asn Ser Leu Ser Asn Ile Gln Trp Leu Arg Lys Met Ser Ser
180 185 190
Asp Gly Leu Gly Ser Arg Ser Ile Lys Gln Glu Met Glu Glu Lys Glu
195 200 205
Asn Cys His Leu Glu Gln Arg Gln Val Lys Val Glu Glu Pro Ser Arg
210 215 220
Pro Ser Ala Ser Trp Gln Asn Ser Val Ser Glu Arg Pro Pro Tyr Ser
225 230 235 240
Tyr Met Ala Met Ile Gln Phe Ala Ile Asn Ser Thr Glu Arg Lys Arg
245 250 255
Met Thr Leu Lys Asp Ile Tyr Thr Trp Ile Glu Asp His Phe Pro Tyr
260 265 270
Phe Lys His Ile Ala Lys Pro Gly Trp Lys Asn Ser Ile Arg His Asn
275 280 285
Leu Ser Leu His Asp Met Phe Val Arg Glu Thr Ser Ala Asn Gly Lys
290 295 300
Val Ser Phe Trp Thr Ile His Pro Ser Ala Asn Arg Tyr Leu Thr Leu
305 310 315 320
Asp Gln Val Phe Lys Pro Leu Asp Pro Gly Ser Pro Gln Leu Pro Glu
325 330 335
His Leu Glu Ser Gln Gln Lys Arg Pro Asn Pro Glu Leu Arg Arg Asn
340 345 350
Met Thr Ile Lys Thr Glu Leu Pro Leu Gly Ala Arg Arg Lys Met Lys
355 360 365
Pro Leu Leu Pro Arg Val Ser Ser Tyr Leu Val Pro Ile Gln Phe Pro
370 375 380
Val Asn Gln Ser Leu Val Leu Gln Pro Ser Val Lys Val Pro Leu Pro
385 390 395 400
Leu Ala Ala Ser Leu Met Ser Ser Glu Leu Ala Arg His Ser Lys Arg
405 410 415
Val Arg Ile Ala Pro Lys Val Phe Gly Glu Gln Val Val Phe Gly Tyr
420 425 430
Met Ser Lys Phe Phe Ser Gly Asp Leu Arg Asp Phe Gly Thr Pro Ile
435 440 445
Thr Ser Leu Phe Asn Phe Ile Phe Leu Cys Leu Ser Val Leu Leu Ala
450 455 460
Glu Glu Gly Ile Ala Pro Leu Ser Ser Ala Gly Pro Gly Lys Glu Glu
465 470 475 480
Lys Leu Leu Phe Gly Glu Gly Phe Ser Pro Leu Leu Pro Val Gln Thr
485 490 495
Ile Lys Glu Glu Glu Ile Gln Pro Gly Glu Glu Met Pro His Leu Ala
500 505 510
Arg Pro Ile Lys Val Glu Ser Pro Pro Leu Glu Glu Trp Pro Ser Pro
515 520 525
Ala Pro Ser Phe Lys Glu Glu Ser Ser His Ser Trp Glu Asp Ser Ser
530 535 540
Gln Ser Pro Thr Pro Arg Pro Lys Lys Ser Tyr Ser Gly Leu Arg Ser
545 550 555 560
Pro Thr Arg Cys Val Ser Glu Met Leu Val Ile Gln His Arg Glu Arg
565 570 575
Arg Glu Arg Ser Arg Ser Arg Arg Lys Gln His Leu Leu Pro Pro Cys
580 585 590
Val Asp Glu Pro Glu Leu Leu Phe Ser Glu Gly Pro Ser Thr Ser Arg
595 600 605
Trp Ala Ala Glu Leu Pro Phe Pro Ala Asp Ser Ser Asp Pro Ala Ser
610 615 620
Gln Leu Ser Tyr Ser Gln Glu Val Gly Gly Pro Phe Lys Thr Pro Ile
625 630 635 640
Lys Glu Thr Leu Pro Ile Ser Ser Thr Pro Ser Lys Ser Val Leu Pro
645 650 655
Arg Thr Pro Glu Ser Trp Arg Leu Thr Pro Pro Ala Lys Val Gly Gly
660 665 670
Leu Asp Phe Ser Pro Val Gln Thr Ser Gln Gly Ala Ser Asp Pro Leu
675 680 685
Pro Asp Pro Leu Gly Leu Met Asp Leu Ser Thr Thr Pro Leu Gln Ser
690 695 700
Ala Pro Pro Leu Glu Ser Pro Gln Arg Leu Leu Ser Ser Glu Pro Leu
705 710 715 720
Asp Leu Ile Ser Val Pro Phe Gly Asn Ser Ser Pro Ser Asp Ile Asp
725 730 735
Val Pro Lys Pro Gly Ser Pro Glu Pro Gln Val Ser Gly Leu Ala Ala
740 745 750
Asn Arg Ser Leu Thr Glu Gly Leu Val Leu Asp Thr Met Asn Asp Ser
755 760 765
Leu Ser Lys Ile Leu Leu Asp Ile Ser Phe Pro Gly Leu Asp Glu Asp
770 775 780
Pro Leu Gly Pro Asp Asn Ile Asn Trp Ser Gln Phe Ile Pro Glu Leu
785 790 795 800
Gln
<210> 76
<211> 4
<212> белок
<213> искусственная последовательность
<220>
<223> линкерный пептид
<400> 76
Asn Lys Arg Lys
1
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ MPHOSPH1, И ВКЛЮЧАЮЩАЯ ЕГО ВАКЦИНА | 2016 |
|
RU2731099C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ DEPDC1, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2016 |
|
RU2765574C2 |
| НЕОАНТИГЕНЫ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2805196C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ T-КЛЕТОК И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2835034C2 |
| ИНДУКТОР ИММУНИТЕТА | 2016 |
|
RU2758112C2 |
| ИНДУКТОР ИММУНИТЕТА | 2016 |
|
RU2835947C2 |
| СПЕЦИФИЧНЫЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2020 |
|
RU2825837C2 |
| КОНСТРУКТЫ Т-КЛЕТОЧНОГО РЕЦЕПТОРА И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2785954C2 |
| НЕОАНТИГЕНЫ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2813924C2 |
| НОВЫЕ АНТИ-HLA-А2 АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2805674C2 |


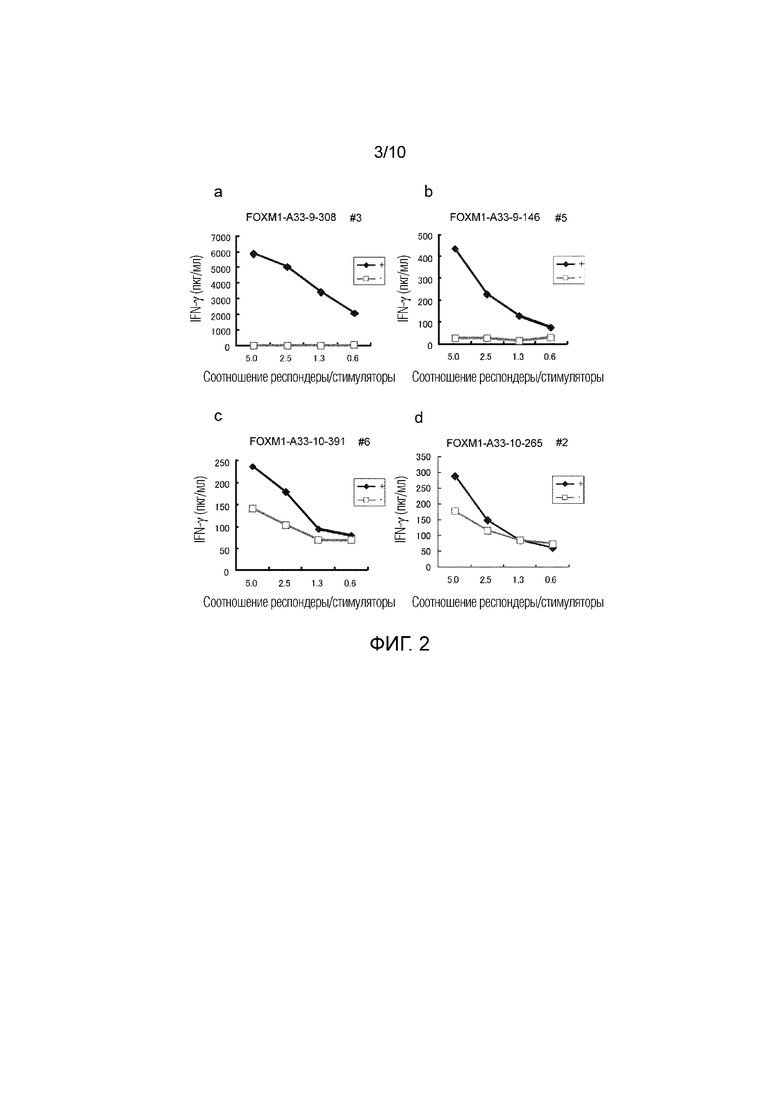

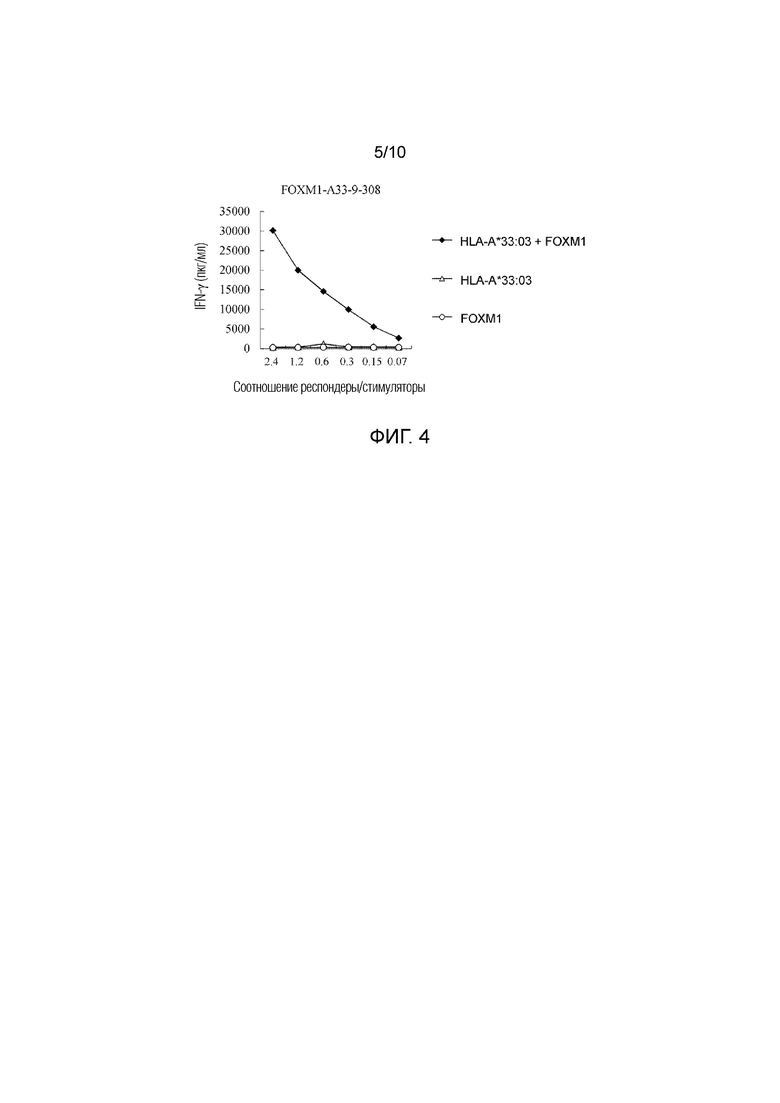

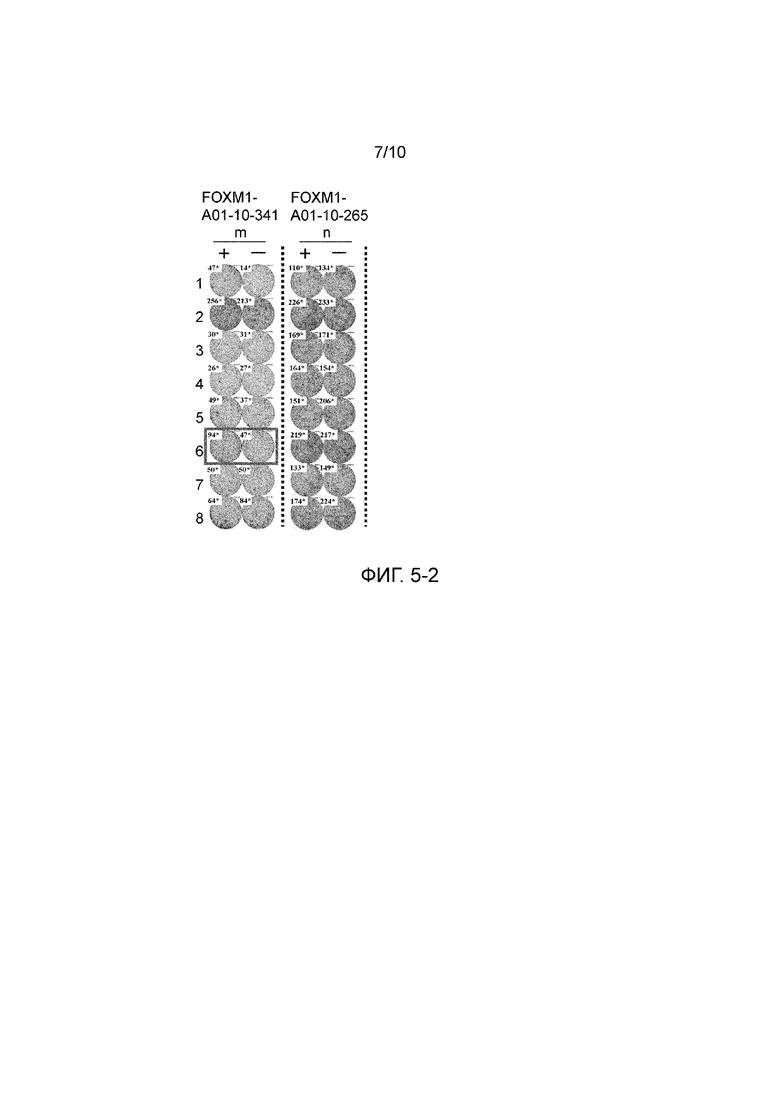
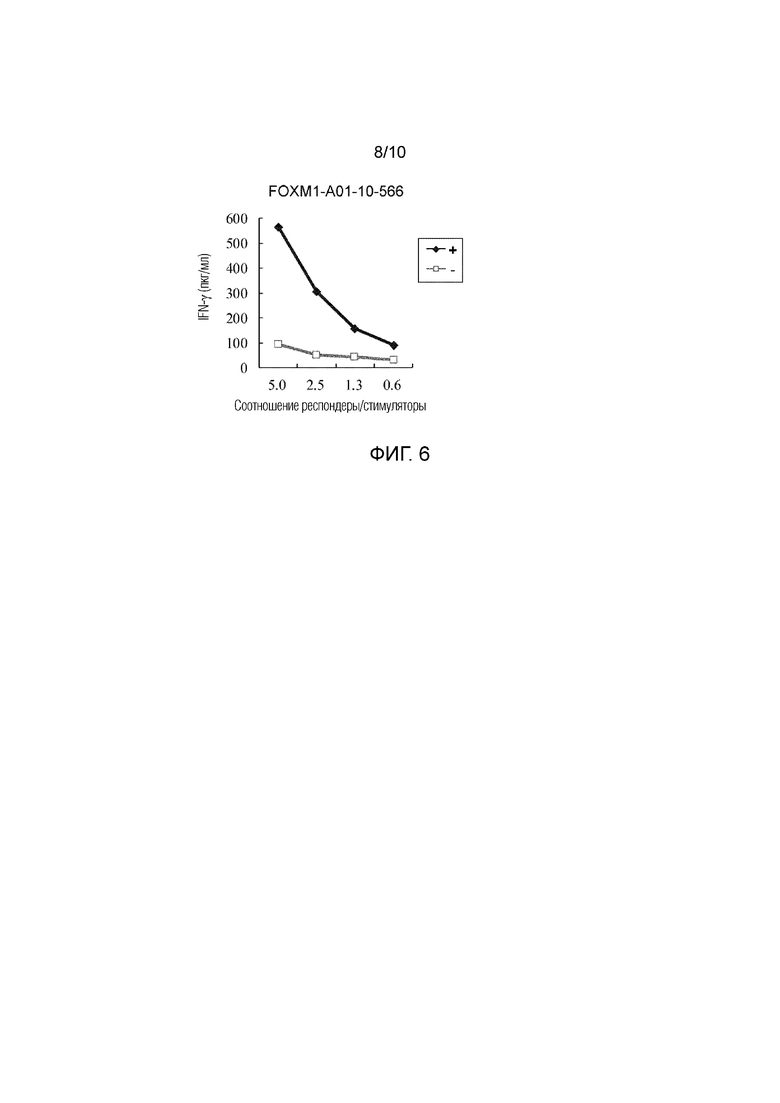
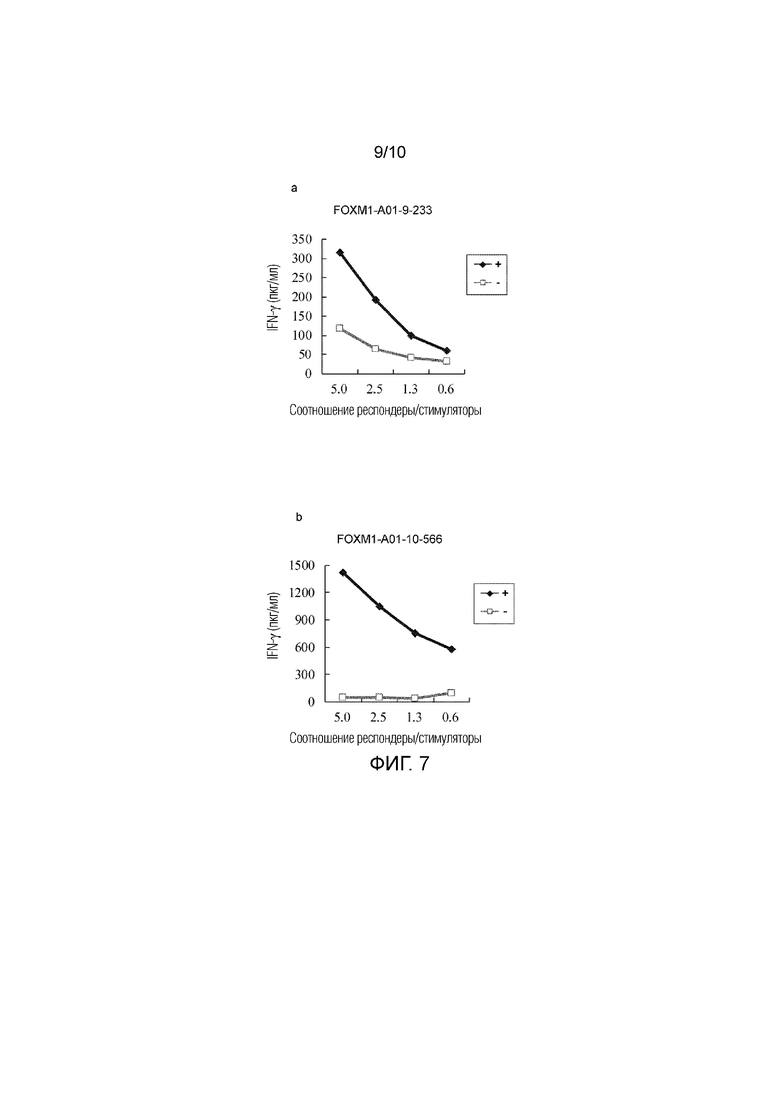
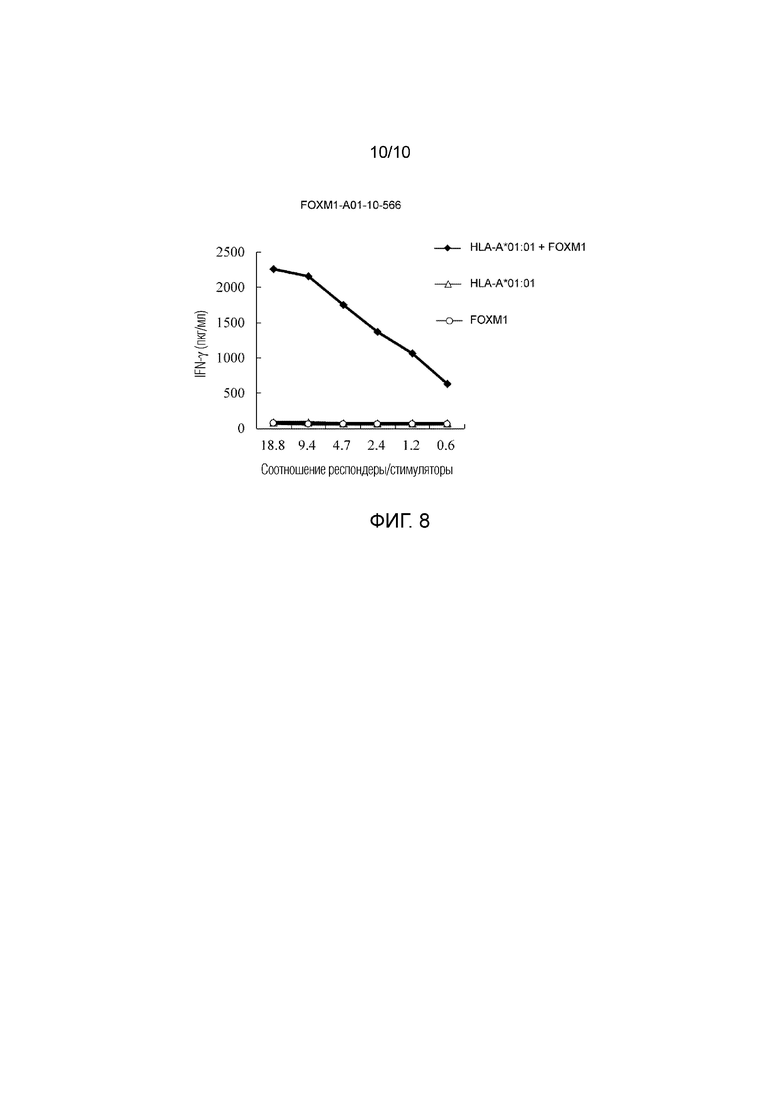
Настоящая группа изобретений относится к иммунологии. Предложены пептиды, полученные из FOXM1 и обладающие способностью индуцировать цитотоксическую T-клетку (ЦТЛ) в присутствии антигенпрезентирующей клетки (АПК), экспрессирующей HLA-A*01:01. Также описаны: кодирующий полинуклеотид; композиции; способы индуцирования АПК и ЦТЛ; АПК, презентирующая HLA-A*01:01 и пептид; способ индуцирования иммунного ответа; способ лечения и/или профилактики злокачественной опухоли и/или профилактики ее послеоперационного рецидива; эмульсия; набор; а также применение указанных изобретений при получении фармацевтической композиции и способ скрининга пептидов со способностью индуцировать ЦТЛ. Данная группа изобретений может найти применение в терапии заболеваний, связанных с FOXM1. 14 н. и 7 з.п. ф-лы, 8 ил., 2 табл., 3 пр.
1. Пептид, содержащий менее чем 15 аминокислот, со способностью индуцировать цитотоксическую T-клетку (ЦТЛ) в присутствии антигенпрезентирующей клетки(ок), экспрессирующей HLA-A*01:01, который содержит аминокислотную последовательность, выбранную из группы, состоящей из:
(a) аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 56, 20, 48, 49, 50, 52, 53, 55, 57, 58, 59, 60 и 61; и
(b) аминокислотной последовательности, в которой одна или две аминокислоты замещены в аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 56, 20, 48, 49, 50, 52, 53, 55, 57, 58, 59, 60 и 61,
где одна или две замены в аминокислотной последовательности SEQ ID NO: 56, 20, 48, 49, 50, 52, 53, 55, 57, 58, 59, 60 или 61 согласно подпункту (b) выбраны из группы, состоящей из нижеизложенных от (1) до (3):
(1) вторая аминокислота с N-конца замещена аминокислотой, выбранной из группы, состоящей из треонина и серина;
(2) третья аминокислота с N-конца замещена аминокислотой, выбранной из группы, состоящей из аспарагиновой кислоты и глутаминовой кислоты; и
(3) C-концевая аминокислота замещена тирозином.
2. Пептид по п. 1, который состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 20, 48, 49, 50, 52, 53, 55, 56, 57, 58, 59, 60 и 61.
3. Полинуклеотид, который кодирует пептид по любому из пп. 1, 2.
4. Композиция для индуцирования иммунного ответа против клеток, экспрессирующих FOXM1 и HLA-A*01:01, содержащая фармацевтически приемлемый носитель и подходящую дозу по меньшей мере одного ингредиента, выбранного из группы, состоящей из нижеизложенных от (a) до (d):
(a) один или несколько пептидов по любому из пп. 1, 2;
(b) один или несколько полинуклеотидов, кодирующих пептид(-ы) по любому из пп. 1-3, в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01; и
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. 1, 3 и антигена HLA.
5. Композиция для индуцирования ЦТЛ против клеток, экспрессирующих FOXM1 и HLA-A*01:01, содержащая фармацевтически приемлемый носитель и подходящую дозу по меньшей мере одного ингредиента, выбранного из группы, состоящей из нижеизложенных от (a) до (d):
(a) один или несколько пептидов по любому из пп. 1, 2;
(b) один или несколько полинуклеотидов, кодирующих пептид(-ы) по любому из пп. 1, 2, в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01;
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01.
6. Композиция по п. 4, которая является фармацевтической композицией.
7. Композиция по п. 6, которая предназначена для одного или нескольких применений, выбранных из группы, состоящей из (i) лечения злокачественных опухолей, (ii) предупреждения (профилактики) злокачественной опухоли и (iii) предупреждения (профилактики) послеоперационного рецидива злокачественной опухоли.
8. Композиция по п. 6, которая предназначена для индуцирования иммунного ответа против злокачественной опухоли.
9. Композиция по п. 7 или 8, где злокачественная опухоль выбрана из группы, состоящей из острого миелоидного лейкоза, рака мочевого пузыря, рака молочной железы, рака шейки матки, холангиоцеллюлярного рака, хронического миелолейкоза (ХМЛ), рака толстого кишечника, рака пищевода, рака желудка, диффузного рака желудка, немелкоклеточного рака легких (NSCLC), лимфомы, остеосаркомы, рака яичников, рака поджелудочной железы, рака предстательной железы, рака почки, мелкоклеточного рака легких (SCLC), опухоли мягких тканей и рака яичка.
10. Композиция по любому из пп. 4-9, которую формулируют для введения индивидууму, положительному по меньшей мере по одному HLA, выбранному из группы, состоящей из HLA-A*01:01.
11. Способ индуцирования АПК со способностью индуцировать ЦТЛ, который включает этап, выбранный из группы, состоящей из:
(a) контакта АПК, экспрессирующей HLA-A*01:01, с пептидом по любому из пп. 1, 2 in vitro, ex vivo или in vivo; и
(b) введения полинуклеотида, кодирующего пептид по любому из пп. 1, 2, в АПК, экспрессирующую HLA-A*01:01.
12. Способ индуцирования ЦТЛ, который включает этап, выбранный из группы, состоящей из:
(a) совместного культивирования CD8-положительной T-клетки/клеток с АПК, которые презентируют на своей поверхности комплекс из HLA-A*01:01 и пептида по любому из пп. 1, 2; и
(b) совместного культивирования CD8-положительной T-клетки/клеток с экзосомой/экзосомами, которые презентируют на своей поверхности комплекс из HLA-A*01:01 и пептида по любому из пп. 1, 2.
13. АПК, которая презентирует на своей поверхности комплекс из HLA-A*01:01 и пептида по любому из пп. 1, 2.
14. АПК по п. 13, которая индуцирована при помощи способа по п. 11.
15. Способ индуцирования иммунного ответа против злокачественной опухоли, экспрессирующей FOXM1 и HLA-A*01:01, который включает введение индивидууму подходящей дозы по меньшей мере одного ингредиента, выбранного из группы, состоящей из нижеизложенных с (a) по (d):
(a) один или несколько пептидов по любому из пп. 1, 2;
(b) один или несколько полинуклеотидов, кодирующих пептид(-ы) по любому из пп. 1, 2 в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01; и
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01.
16. Способ лечения и/или профилактики злокачественной опухоли, экспрессирующей FOXM1 и HLA-A*01:01, и/или профилактики ее послеоперационного рецидива, который включает введение индивидууму подходящей дозы по меньшей мере одного ингредиента, выбранного из группы, состоящей из нижеизложенных п/пп. (a)-(d):
(a) один или несколько пептидов по любому из пп. 1, 2;
(b) один или несколько полинуклеотидов, кодирующих пептид(-ы) по любому из пп. 1, 2, в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01; и
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01.
17. Способ скрининга на пептид со способностью индуцировать ЦТЛ, который включает этапы:
(a) создания кандидатных последовательностей, состоящих из аминокислотной последовательности, в которой один, два или несколько аминокислотных остатков замещены, удалены, вставлены и/или добавлены по сравнению с исходной аминокислотной последовательностью, состоящей из аминокислотной последовательности, выбранной из SEQ ID NO: 56, 20, 48, 49, 50, 52, 53, 55, 57, 58, 59, 60 и 61;
(b) отбор в кандидатных последовательностях, полученных в (a), кандидатной последовательности, которая не имеет значительной гомологии (идентичности последовательности) с любым известным продуктом гена человека, за исключением FOXM1;
(c) контакт АПК, экспрессирующей HLA-A*01:01, с пептидом, состоящим из кандидатной последовательности, выбранной в (b);
(d) контакт АПК из (c) с CD8-положительной T-клеткой; и
(e) отбор пептида, который имеет равную или более высокую способность индуцировать ЦТЛ по сравнению с пептидом, состоящим из исходной аминокислотной последовательности.
18. Эмульсия для индуцирования иммунного ответа против клеток, экспрессирующих FOXM1 и HLA-A*01:01, содержащая подходящую дозу одного или несколько типов пептидов по любому из пп. 1, 2, водорастворимый носитель и масляный адъювант.
19. Набор для одного или более применений, выбранных из группы, состоящей из (i) лечения злокачественных опухолей, (ii) предупреждения (профилактики) злокачественной опухоли и (iii) предупреждения (профилактики) послеоперационного рецидива злокачественной опухоли, включающий контейнер, который содержит композицию по любому из пп. 4-10, и контейнер, который содержит адъювант.
20. Применение подходящей дозы по меньшей мере одного ингредиента, выбранного из группы, состоящей из нижеизложенных п/пп. (a)-(d):
(a) один или несколько пептидов по любому из пп. 1, 2;
(b) один или несколько полинуклеотидов, кодирующих пептид(ы) по любому из пп. 1, 2, в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01; и
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01,
при получении фармацевтической композиции для индуцирования иммунного ответа злокачественной опухоли, экспрессирующей FOXM1 и HLA-A*01:01.
21. Применение подходящей дозы по меньшей мере одного ингредиента, выбранного из группы, состоящей из нижеизложенных п/пп. (a)-(d):
(a) один или несколько пептидов по любому из пп. 1, 2;
(b) один или несколько полинуклеотидов, кодирующих пептид(ы) по любому из пп. 1, 2, в экспрессируемой форме;
(c) антигенпрезентирующая клетка (АПК), которая презентирует на своей клеточной поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01; и
(d) экзосома, которая презентирует на своей поверхности комплекс из пептида по любому из пп. 1, 2 и HLA-A*01:01,
при получении фармацевтической композиции для лечения и/или профилактики злокачественной опухоли, экспрессирующей FOXM1 и HLA-A*01:01, и/или профилактики ее постоперационного послеоперационного рецидива.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| ПЕПТИД FOXM1 И ВКЛЮЧАЮЩЕЕ ЕГО МЕДИЦИНСКОЕ СРЕДСТВО | 2008 |
|
RU2487886C2 |
| KIM I.-M | |||
| et al., "The Forkhead Box m1 Transcription Factor Stimulates the Proliferation of Tumor Cells during Development of Lung Cancer", Cancer Res 2006; 66:2153-2161 | |||
| MARSH S | |||
| G | |||
| E | |||
| et al., "The HLA FactsBook", Academic Press, 2000, pp.100, 138 | |||
| TAKIGUCHI M | |||
| et al., "Polarity of the P1 | |||
Авторы
Даты
2020-12-14—Публикация
2016-10-06—Подача