Область техники изобретения
Настоящее изобретение относится к лечению субъектов, страдающих воспалительными заболеваниями кожи, включающему введение субъекту эффективного количества производного 1-аминоалкилциклогексана.
Уровень техники изобретения
Данное изобретение относится к способам лечения пациентов, страдающих воспалительными заболеваниями кожи, включающими акне, розацеа, экзему, атопический дерматит, псориаз и жирную кожу.
Акне является наиболее распространенным кожным заболеванием. Эпидемиологические данные свидетельствуют о том, что могут быть затронуты до 80% субъектов. Мужчины и женщины подвержены заболеванию акне примерно в равной степени, заболевание, как правило, возникает в возрасте 10-14 лет и снижается к 20-25 годам. У некоторых пациентов акне сохраняется на четвертом или пятом десятилетии жизни (стойкие акне). Клинический спектр акне охватывает диапазон от слабых проявлений (например, нескольких комедонов (очагов акне) со случайными воспалительными папулопустулами до «клинического» акне в более тяжелых случаях) до тяжелого воспаления и образования абсцесса на лице или верхней части туловища. Разрыв фолликул может продолжаться и приводить к возникновению реакции на чужеродные тела, включая абсцессы, свищи и системные признаки воспаления (конглобатные угри).
Повышенная выработка кожного сала, которая, как полагают, регулируется андрогенами, считается одной из основных причин развития акне (себореи). Следующей предпосылкой возникновения акне является нарушение фолликулярной кератинизации, ведущее к гиперкератозу. Факторы, ответственные за фолликулярный гиперкератоз, включают следующее: локализованный фолликулярный дефицит линолевой кислоты, комедогенные компоненты кожного сала, изменения липидного состава кожного сала, бактериальные метаболиты и медиаторы воспаления.
Пропионибактерии (Propionibacterium acnes) являются доминирующими бактериями в волосяных фолликулах. Эти бактерии предпочитают микроаэробные или анаэробные условия и преимущественно колонизируют области с повышенным производством кожного сала. На четыре порядка более высокие концентрации пропионибактерий обнаружены у 11-20-летних людей с акне по сравнению с 11-20-летними людьми без акне. Бактериальные липазы высвобождают раздражающие и провоспалительные свободные кислоты и другие потенциально провоспалительные бактериальные метаболиты, такие как протеазы, гиалуронидазы и хемотаксические факторы. Метаболиты пропионибактерий вызывают фолликулярное и околофолликулярное воспаление, особенно из-за хемотаксических веществ. Другие иммунологические и воспалительные факторы также играют важную роль в возникновении и течении акне (например, toll-подобный рецептор 2, IL-1, IL-8, LTB4, PPAR альфа).
Для лечения акне существует ряд способов, как местного, так и системного воздействия. Местные способы лечения акне включают: ретиноиды, которые нормализуют фолликулярную кератинизацию; бензоилпероксид (BPO), который является антибактериальным средством, снижающим количество Propionibacterium acnes (P. acnes) в фолликулах; и местные антибиотики с антибактериальным эффектом. Способы системного лечения акне включают антибиотики. Способы системного лечения также включают гормоны для лечения женщин.
Розацеа является общим хроническим воспалительным заболеванием кожи, преимущественно кожи лица. Обычно оно возникает на третьем и четвертом десятилетии жизни, достигая пика в возрасте от 40 до 50 лет. Причины розацеа до сих пор не выяснены. Сосудистая реактивность на лице, структура или состав кожной соединительной ткани, структура волос и сальных желез, микробная колонизация и сочетание факторов, которые изменяют кожный ответ на факторы, запускающие розацеа, соответственно, рассматриваются в качестве основных патогенных механизмов. Важными запускающими факторами, среди прочего, судя по всему, являются высокая или низкая температура, солнечные лучи, ветер, горячие напитки, острая пища, алкоголь, физические упражнения, эмоции, а также местные раздражители, которые вызывают прилив крови и покраснение. Ранняя стадия розацеа характеризуется стойкой эритемой и телеангиэктазией, в основном на щеках, часто сопровождаемой появлением папул и папулопустул. На более поздних стадиях может происходить диффузная гиперплазия соединительной ткани и сальных желез. Это может приводить к гипертрофии носа, так называемый ринофиме. Розацеа развивается поэтапно и может повлиять на глаза, чаще всего вызывая блефарит и конъюнктивит. Розацеа может возникать в других областях, помимо лица, например в позадиушной области, а также на шее, груди, спине и голове. Клиническая картина розацеа может быть похожа на акне, но отличие заключается в том, что розацеа не является первичным фолликулярным заболеванием.
Пероральные тетрациклиновые антибиотики, такие как тетрациклин, доксициклин и миноциклин, а также местные антибиотики, такие как метронидазол, которые используют при акне, также являются способом лечения розацеа и используются для уменьшения папул, пустул, воспаления и покраснения.
Экзема является общим термином, охватывающим различные воспалительные состояния кожи, такие как атопический дерматит, аллергический контактный дерматит и профессиональный дерматит.
Атопический дерматит представляет собой зуд, который обычно начинается в раннем детстве (хотя существует вариант, возникающий и во взрослом возрасте). Атопический дерматит характеризуется зудом, экзематозными очагами, ксерозом (сухой кожей) и лихенизацией (утолщением кожи и усилением кожного рисунка).
Атопический дерматит является результатом сложных взаимодействий между генами генетической предрасположенности, приводящими к дефектному кожному барьеру, дефектами врожденной иммунной системы и повышенным иммунологическим ответом на аллергены и микробные антигены. Дисфункция барьера обусловлена снижением экспрессии генов рогового конверта (филагрина и лорикрина), пониженными уровнями церамидов, повышенными уровнями эндогенных протеолитических ферментов и усиленной трансэпидермальной потерей воды. Нарушение барьера может быть также вызвано мылом и моющими средствами и/или воздействием экзогенных протеаз клещей домашней пыли и Staphylococcus aureus. Это усугубляется отсутствием некоторых эндогенных ингибиторов протеаз в атопической коже. Эти изменения эпидермиса, очевидно, способствуют увеличению абсорбции аллергена кожей и микробной колонизации. Согласно современной теории основную роль играют микробные суперантигены; они могут более легко проникать в жизнеспособные слои кожи через нарушенный барьер и вызывать приток Т-клеток (преимущественно активированных Т-клеток памяти, что предполагает предшествующее столкновение с антигеном) с отдельными макрофагами.
Зуд является характерной особенностью атопического дерматита, проявляющейся в виде кожной гиперреактивности и расчесывания после воздействия аллергенов, изменения влажности, выступившего пота и низких концентраций раздражающих веществ. Механизмы зуда плохо изучены, однако считается, что важную роль играют воспалительные клетки. Существует цикл зуда-расчесывания. Постоянное расчесывание активирует области в префронтальной коре и орбифронтальной коре. Это может объяснить гедонистические и навязчивые составляющие расчесывания и может быть связано с выделением эндогенных опиоидов. Постоянное расчесывание при атопическом дерматите вызывает секрецию нейропептидов и опиатов, что может еще больше усиливать порочный цикл зуда-расчесывания.
Псориаз является полигенным наследственным многофакторным воспалительным заболеванием кожи неизвестного патогенеза, на которое может влиять целый ряд факторов окружающей среды. Существует сильная генетическая основа, приводящая к сложным изменениям эпидермального роста и дифференциации и множественным биохимическим, иммунологическим и сосудистым аномалиям, а также плохо понимаемому взаимодействию с функцией нервной системы. Патогенез псориаза достаточно сложен, с вовлечением местных и системных факторов. В настоящее время аномальную эпидермальную гиперпролиферацию рассматривают как вторичное явление после опосредованной Т-лимфоцитами аутоиммунной реакции. Сообщали также, что свою роль также может играть иммунологическая реакция на виды Streptococcus. Эпидермальная пролиферация на поврежденной коже характеризуется повышенным рекрутингом циклирующих клеток из покоящейся популяции G0. В противоположность более старым данным, времена клеточного цикла в псориатической бляшке являются в основном нормальными. В частности, надбазальный компартмент характеризуется экспрессией молекул, которые отсутствуют или имеют ограниченную экспрессию в нормальной коже. В культурах первичных кератиноцитов растворимые факторы из клонов CD4+ T-лимфоцитов, полученных из псориатических бляшек, стимулируют пролиферацию субпопуляции псориатических CD29+ кератин-10 клеток, тогда как CD29+ кератин-10 кератиноциты от нормальных субъектов не отвечают таким ростом на растворимые факторы из тех же T-клеточных клонов. Это говорит о том, что субпопуляция эпидермальных клеток, полученных из псориатических бляшек, реагирует аномально на клоны Т-лимфоцитов из псориатических бляшек.
Жирная кожа возникает из-за чрезмерного производства кожного сала сальными железами. Чрезмерное производство кожного сала может быть вызвано гормональным дисбалансом во время беременности и менопаузы, наследственностью, диетой, противозачаточными таблетками, использованием косметики или влажной и жаркой погодой либо заболеваниями, такими как болезнь Паркинсона.
Излишки кожного сала приводят к жирной поверхности кожи, блокируют поры, обеспечивают питание для бактерий, живущих на коже (P. acnes), и способствуют вспышкам акне.
Контагиозное импетиго представляет собой поверхностную бактериальную инфекцию кожи, наиболее распространенную среди школьников. Ей подвержены также люди, занимающиеся контактными видами спорта, такими как регби и борьба, независимо от возраста. Импетиго не так часто встречается у взрослых. Она очень заразна и также известна как школьные язвы. Ее вызывает преимущественно Staphylococcus aureus и Streptococcus pyogenes. Импетиго обычно проявляется в виде струпьев медового цвета, образованных из подсохшей сыворотки, и часто находится на руках, ногах или лице. Инфекция передается при прямом контакте с очагами поражения или с назальными переносчиками. Инкубационный период составляет 1-3 дня. Высушенные стрептококки в воздухе не являются инфекционными для неповрежденной кожи. Расчесывание может способствовать распространению очагов поражения. Соблюдение гигиенических правил может помочь предотвратить распространение импетиго.
Подтипами контагиозного импетиго являются буллезное импетиго и эктима. Буллезное импетиго в первую очередь поражает младенцев и детей в возрасте до 2 лет. Оно вызывает безболезненные, наполненные жидкостью волдыри - как правило, на туловище, руках и ногах.
Кожа вокруг волдыря, как правило, красная и зудящая, но не болезненная. Волдыри, которые лопаются и покрываются желтыми струпьями, могут быть большими или маленькими и могут длиться дольше, чем язвы от других типов импетиго. Эктима является более серьезной формой импетиго, при которой инфекция проникает глубже во второй слой кожи, дерму. Признаки и симптомы включают:
- болезненные заполненные жидкостью или гноем язвочки, которые превращаются в глубокие язвы, обычно на ногах и ступнях
- жесткие, толстые, серо-желтые струпья, покрывающие язвы
- увеличенные лимфатические железы в пораженных участках
- небольшие отверстия размером от булавочной головки до пенни, появляющиеся после отпадения струпьев
- рубцы, остающиеся после заживления язв.
Для лечения контагиозного импетиго и его подтипов обычно прописывают местные или пероральные антибиотики. Легкие формы можно лечить с помощью бактерицидных мазей, например, содержащих фузидиевую кислоту, мупироцин, хлорамфеникол, клиохинол или неоспорин. Более серьезные случаи требуют применения пероральных антибиотиков, таких как диклоксациллин, флуклоксациллин или эритромицин. Альтернативно, для лечения антибиотиками можно также использовать амоксициллин в сочетании с клавуланатом калия, цефалоспорины (1-го поколения) и многое другое. Упомянутые лекарственные средства можно использовать в форме любой из фармацевтически приемлемых солей, оптических изомеров, диастереомеров, энантиомеров, гидратов и их фармацевтически приемлемых солей.
Используемые в настоящее время способы лечения воспалительных заболеваний кожи обладают различными недостатками.
Использование ретиноидов является одним из доступных способов лечения акне. Для клинического улучшения после лечения ретиноидами обычно требуется несколько недель, и ретиноиды, как известно, обладают тератогенными свойствами. Ретиноиды также могут являться раздражителями. При использовании BPO действие начинается достаточно быстро и об устойчивости к P.Acnes не сообщалось; однако BPO является отбеливающим средством и, следовательно, может происходить обесцвечивание одежды и постельных принадлежностей. Кроме того, BPO является потенциальным раздражителем и может действовать как мутаген. Использование ряда местных антибиотиков, применяемых в настоящее время, привело к появлению высокого процента устойчивости. Таким образом, существует необходимость в усовершенствованных способах лечения акне и других воспалительных заболеваний кожи.
Производные 1-аминоалкилциклогексана, такие как нерамексан (также известный как 1-амино-1,3,3,5,5-пентаметилциклогексан), были признаны полезными в терапии различных заболеваний, особенно некоторых неврологических заболеваний, включая болезнь Альцгеймера и невропатическую боль. Производные 1-аминоалкилциклогексана, такие как нерамексан, подробно раскрыты в патентах США №№6034134 и 6071966, объект изобретения этих патентов включен в данный документ посредством ссылки.
В WO 2007/062815 также раскрыто, что лекарственные формы с модифицированным высвобождением, содержащие нерамексан, могут быть полезны в лечении различных состояний, включая диабетическую невропатическую боль, боковой амиотрофический склероз, рассеянный склероз, синдром раздраженного кишечника, расстройства аппетита, ожирение, неумеренную потребность в еде, аутизм, синдром дефицита внимания, синдром дефицита внимания с гиперактивностью, биполярное расстройство, шум в ушах, микоз и псориаз.
Удивительно, но в настоящее время установлено, что производные 1-аминоалкилциклогексана, такие как нерамексан, также подходят для лечения воспалительных заболеваний кожи.
Положительное влияние производных 1-аминоалкилциклогексана, таких как нерамексан, на себоциты также способствует эффективному лечению воспалительных заболеваний кожи, включая акне, розацеа, экзему, атопический дерматит, псориаз и жирную кожу. Влияние на пролиферацию и/или дифференциацию себоцитов и, следовательно, способность уменьшать производство липидов позволяет регулировать секрецию кожного сала. В дополнение к общей регуляции производства кожного сала, влияние может оказываться и на состав кожного сала, что приводит к нормализации патофизиологического фенотипа больных волосяных фолликулов.
У пациентов с воспалительными заболеваниями кожи часто наблюдается нарушение функции кожного барьера. Производные 1-аминоалкилциклогексана, такие как нерамексан, могут улучшать функцию кожного барьера и блокировать задержку восстановления барьера, что оказывает положительное влияние на гомеостаз кожи.
Сущность изобретения
Настоящее изобретение относится к способу лечения воспалительных заболеваний кожи, таких как акне, розацеа, экзема, атопический дерматит, псориаз и жирная кожа, у субъекта, нуждающегося в этом, включающему введение субъекту эффективного количества производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат).
Настоящее изобретение также относится к способу лечения воспалительного заболевания кожи, такого как контагиозное импетиго.
Следующий аспект изобретения относится к такому способу, в котором нерамексанмезилат вводят в диапазоне от примерно 5 мг до примерно 150 мг/сутки, или нерамексанмезилат вводят в диапазоне от примерно 5 мг до примерно 100 мг/сутки, или нерамексанмезилат вводят в диапазоне от примерно 5 мг до примерно 75 мг/сутки либо в котором нерамексанмезилат вводят в дозе примерно 50 мг/сутки или в котором нерамексанмезилат вводят в дозе примерно 75 мг/сутки, например, в пероральном препарате.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят один раз в сутки, дважды в сутки (b.i.d.) или трижды в сутки.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в препарате с немедленным высвобождением.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в препарате с модифицированным высвобождением.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в местном препарате, таком как местный смываемый или несмываемый препарат.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в количестве от 0,1 до 99% по весу от препарата.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в пероральном препарате.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят системно.
Следующий аспект изобретения относится к способу лечения воспалительных заболеваний кожи у субъекта, нуждающегося в этом, включающему введение субъекту эффективного количества производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) и дополнительного фармацевтического средства (например, противомикробных препаратов, антибиотиков, ретиноидов или стероидов), которое продемонстрировало свою эффективность в лечении или предупреждении воспалительных заболеваний кожи.
Следующий аспект изобретения относится к способу лечения акне у субъекта, нуждающегося в этом, включающему введение субъекту эффективного количества производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) и дополнительного фармацевтического средства (например, противомикробных препаратов, антибиотиков, ретиноидов или стероидов), которое продемонстрировало свою эффективность в лечении или предупреждении воспалительных заболеваний кожи.
Следующий аспект изобретения относится к способу лечения акне у субъекта, нуждающегося в этом, включающему введение субъекту эффективного количества производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) и дополнительного фармацевтического средства (например, противомикробных препаратов, антибиотиков, ретиноидов, стероидов или других неспецифических средств), которое продемонстрировало свою эффективность в лечении или предупреждении акне.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят совместно.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят в одном препарате.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят в местном препарате, таком как местный смываемый или несмываемый препарат.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят системно.
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят в пероральном препарате.
Следующий аспект изобретения относится к производному 1-аминоалкилциклогексана (например, нерамексану или его фармацевтически приемлемой соли, такой как нерамексанмезилат), предназначенному для лечения воспалительных заболеваний кожи, таких как акне, розацеа, экзема, атопический дерматит, псориаз и жирная кожа.
Следующий аспект изобретения относится к производному 1-аминоалкилциклогексана (например, нерамексану или его фармацевтически приемлемой соли, такой как нерамексанмезилат), предназначенному для лечения воспалительного заболевания кожи, такого как контагиозное импетиго.
Следующий аспект изобретения относится к использованию производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) для производства лекарственного средства для лечения воспалительных заболеваний кожи.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором нерамексанмезилат вводят в диапазоне от примерно 5 мг до примерно 150 мг/сутки, или нерамексанмезилат вводят в диапазоне от примерно 5 мг до примерно 100 мг/сутки, или нерамексанмезилат вводят в диапазоне от примерно 5 мг до примерно 75 мг/сутки либо в котором нерамексанмезилат вводят в дозе примерно 50 мг/сутки или в котором нерамексанмезилат вводят в дозе примерно 75 мг/сутки, например, в пероральном препарате.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят один раз в сутки, дважды в сутки (b.i.d.) или трижды в сутки.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в препарате с немедленным высвобождением или в препарате с модифицированным высвобождением.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в местном препарате, таком как местный смываемый или несмываемый препарат.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в количестве от 0,1 до 99% по весу от препарата.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в пероральном препарате.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят системно.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором вводят по меньшей мере одно дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды), которое продемонстрировало свою эффективность в лечении или предупреждении воспалительных заболеваний кожи.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят совместно.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят в одном препарате.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят в местном препарате, таком как местный смываемый или несмываемый препарат.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят в пероральном препарате.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) и дополнительное фармацевтическое средство (например, противомикробные препараты, антибиотики, ретиноиды или стероиды) вводят системно.
Следующий аспект изобретения относится к фармацевтической композиции для лечения воспалительных заболеваний кожи, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) и, необязательно, по меньшей мере один фармацевтически приемлемый носитель или эксципиент.
Следующий аспект изобретения относится к фармацевтической композиции для лечения воспалительных заболеваний кожи, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в препарате с немедленным или модифицированным высвобождением.
Следующий аспект изобретения относится к фармацевтической композиции для лечения воспалительных заболеваний кожи, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в местном препарате.
Следующий аспект изобретения относится к фармацевтической композиции для лечения воспалительных заболеваний кожи, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в местном препарате.
Следующий аспект изобретения относится к фармацевтической композиции для лечения воспалительных заболеваний кожи, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в пероральном препарате.
Следующий аспект изобретения относится к фармацевтической композиции, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в сочетании с по меньшей мере одним дополнительным фармацевтическим средством (например, противомикробными препаратами, антибиотиками, ретиноидами или стероидами), которое продемонстрировало свою эффективность в лечении или предупреждении воспалительных заболеваний кожи, и, не обязательно, по меньшей мере одним фармацевтически приемлемым носителем или эксципиентом.
Следующий аспект изобретения относится к фармацевтической композиции, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в сочетании с по меньшей мере одним дополнительным фармацевтическим средством (например, противомикробными препаратами, антибиотиками, ретиноидами или стероидами), которое продемонстрировало свою эффективность в лечении или предупреждении воспалительных заболеваний кожи, и, не обязательно, по меньшей мере одним фармацевтически приемлемым носителем или эксципиентом.
Следующий аспект изобретения относится к фармацевтической композиции, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в сочетании с по меньшей мере одним дополнительным фармацевтическим средством (например, противомикробными препаратами, антибиотиками, ретиноидами, стероидами или другими неспецифическими средствами), которое продемонстрировало свою эффективность в лечении или предупреждении воспалительных заболеваний кожи, и, не обязательно, по меньшей мере одним фармацевтически приемлемым носителем или эксципиентом.
Следующий аспект изобретения относится к фармацевтической композиции, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в сочетании с по меньшей мере одним дополнительным фармацевтическим средством (например, противомикробными препаратами, антибиотиками, ретиноидами или стероидами), которое продемонстрировало свою эффективность в лечении или предупреждении воспалительных заболеваний кожи, и, не обязательно, по меньшей мере одним фармацевтически приемлемым носителем или эксципиентом, в форме местного или перорального препарата.
Следующий аспект изобретения относится к фармацевтической композиции, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в сочетании с по меньшей мере одним дополнительным фармацевтическим средством (например, противомикробными препаратами, антибиотиками, ретиноидами или стероидами), которое продемонстрировало свою эффективность в лечении или предупреждении воспалительных заболеваний кожи, и, не обязательно, по меньшей мере одним фармацевтически приемлемым носителем или эксципиентом, в форме местного или перорального препарата.
Следующий аспект изобретения относится к фармацевтической композиции, содержащей терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) в сочетании с по меньшей мере одним дополнительным фармацевтическим средством (например, противомикробными препаратами, антибиотиками, ретиноидами или стероидами), которое продемонстрировало свою эффективность в лечении или предупреждении акне, и, не обязательно, по меньшей мере одним фармацевтически приемлемым носителем или эксципиентом, в форме местного или перорального препарата.
Следующий аспект изобретения относится к производному 1-аминоалкилциклогексана (например, нерамексану или его фармацевтически приемлемой соли, такой как нерамексанмезилат), предназначенному для уменьшения секреции кожного сала и/или регулирования состава кожного сала.
Следующий аспект изобретения относится к использованию производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат) для производства лекарственного средства для уменьшения секреции кожного сала и/или регулирования состава кожного сала.
Следующий аспект изобретения относится к вышеуказанному производному или способу применения, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в местном препарате, таком как местный смываемый или несмываемый препарат.
Следующий аспект изобретения относится к способу уменьшения секреции кожного сала и/или регулирования состава кожного сала у субъекта, нуждающегося в этом, включающему введение субъекту эффективного количества производного 1-аминоалкилциклогексана (например, нерамексана или его фармацевтически приемлемой соли, такой как нерамексанмезилат).
Следующий аспект изобретения относится к такому способу, в котором производное 1-аминоалкилциклогексана (например, нерамексан или его фармацевтически приемлемую соль, такую как нерамексанмезилат) вводят в местном препарате, таком как местный смываемый или несмываемый препарат.
Краткое описание рисунков
На фиг.1-3 показаны эффекты нерамексана на мышиной модели контактной гиперчувствительности.
На фиг.4-5 показаны эффекты нерамексана на мышиной модели дерматита.
Подробное описание изобретения
Используемый в данном документе термин «воспалительные заболевания кожи» включает акне, экзему, атопический дерматит, розацеа, псориаз и жирную кожу.
Используемый в данном документе термин «воспалительные заболевания кожи» также включает контагиозное импетиго.
Используемый в данном документе термин «контагиозное импетиго» включает буллезное импетиго и эктиму.
Используемый в данном документе термин «акне» включает обыкновенные акне, персистирующие акне и клинические акне.
Используемый в данном документе термин «розацеа» включает розацеа с персистирующим отеком, конглобатную розацеа, розацеа фульминанс, офтальмическую розацеа, люпоидную или гранулематозную розацеа, стероидную розацеа, грамотрицательную розацеа, галогеновую розацеа, папулы при розацеа, эритематотелеангиэктатическую розацеа, папулезно-пустулезную розацеа, фиматозную розацеа и глазную розацеа.
Используемый в данном документе термин «экзема» включает атопическую экзему, контактный дерматит, аллергический контактный дерматит, профессиональный дерматит, ксеротическую экзему, себорейный дерматит, дисгидроз, дискоидную экзему, венозную экзему, герпетиформный дерматит, нейродермит и аутоэкзематизацию.
Используемый в данном документе термин «псориаз» включает обыкновенный псориаз, пятнистый псориаз, флексурный псориаз, инверсный псориаз, каплевидный псориаз, пустулезный псориаз, псориаз ногтей, эритродермический псориаз и псориатический артрит.
Используемый в данном документе термин «противомикробные препараты» включает местные противомикробные препараты, такие как BPO, триклозан, хлоргексидин, салициловая кислота, сера, резорцин, а также оптические изомеры, диастереомеры, энантиомеры, гидраты, их фармацевтически приемлемые соли и их смеси.
Используемый в данном документе термин «антибиотики» включает местные антибиотики и пероральные антибиотики.
Используемый в данном документе термин «местные антибиотики» включает эритромицин, клиндамицин, тетрациклин, метронидазол, а также оптические изомеры, диастереомеры, энантиомеры, гидраты, их фармацевтически приемлемые соли и их смеси.
Используемый в данном документе термин «пероральные антибиотики» включает эритромицин, тетрациклин, окситетрациклин, доксициклин, миноциклин, лимециклин, триметоприм, а также оптические изомеры, диастереомеры, энантиомеры, гидраты, их фармацевтически приемлемые соли и их смеси.
Используемый в данном документе термин «ретиноиды» включает местные ретиноиды и пероральные ретиноиды, такие как изотретиноин, а также оптические изомеры, диастереомеры, энантиомеры, гидраты и их фармацевтически приемлемые соли.
Используемый в данном документе термин «местные ретиноиды» включает ретинол, третиноин, изотретиноин, мотретинид, адапален, тазаротен, а также оптические изомеры, диастереомеры, энантиомеры, гидраты, их фармацевтически приемлемые соли и их смеси.
Используемый в данном документе термин «стероиды» включает спиронолактон, дроспиренон, ципротерон, ципротеронацетат, а также оптические изомеры, диастереомеры, энантиомеры, гидраты, их фармацевтически приемлемые соли и их смеси.
Используемый в данном документе термин «субъект» охватывает млекопитающих, включая животных и людей.
Термин «производное 1-аминоалкилциклогексана» используют в данном документе для обозначения 1-аминоалкилциклогексана или соединения, полученного из 1-аминоалкилциклогексана, например фармацевтически приемлемых солей 1-аминоалкилциклогексанов.
Производные 1-аминоалкилциклогексана по настоящему изобретению можно представить общей формулой (I):
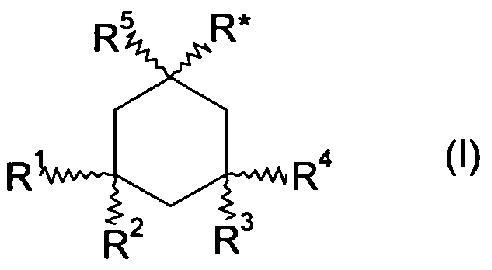
где R* представляет собой -(CH2)n-(CR6R7)m-NR8R9,
где n+m=0, 1 или 2,
где R1-R7 независимо выбраны из группы, состоящей из водорода и C1-6-алкила,
где R8 и R9 независимо выбраны из группы, состоящей из водорода и C1-6-алкила, или вместе представляют собой низший алкилен -(CH2)X-, где x равен 2-5, включительно, а также их оптические изомеры, диастереомеры, энантиомеры, гидраты и фармацевтически приемлемые соли.
Неограничивающие примеры 1-аминоалкилциклогексанов, используемых по настоящему изобретению, включают:
1-амино-1,3,5-триметилциклогексан,
1-амино-1(транс),3(транс),5-триметилциклогексан,
1-амино-1(цис),3(цис),5-триметилциклогексан,
1-амино-1,3,3,5-тетраметилциклогексан,
1-амино-1,3,3,5,5-пентаметилциклогексан (нерамексан),
1-амино-1,3,5,5-тетраметил-3-этилциклогексан,
1-амино-1,5,5-триметил-3,3-диэтилциклогексан,
1-амино-1,5,5-триметил-цис-3-этилциклогексан,
1-амино-(1S,5S)цис-3-этил-1,5,5-триметилциклогексан,
1-амино-1,5,5-триметил-транс-3-этилциклогексан,
1-амино-(1R,5S)транс-3-этил-1,5,5-триметилциклогексан,
1-амино-1-этил-3,3,5,5-тетраметилциклогексан,
1-амино-1-пропил-3,3,5,5-тетраметилциклогексан,
N-метил-1-амино-1,3,3,5,5-пентаметилциклогексан,
N-этил-1-амино-1,3,3,5,5-пентаметилциклогексан,
N-(1,3,3,5,5-пентаметилциклогексил)пирролидин,
3,3,5,5-тетраметилциклогексилметиламин,
1-амино-1-пропил-3,3,5,5-тетраметилциклогексан,
1-амино-1,3,3,5(транс)-тетраметилциклогексан (осевая аминогруппа),
3-пропил-1,3,5,5-тетраметилциклогексиламина полугидрат,
1-амино-1,3,5,5-тетраметил-3-этилциклогексан,
1-амино-1,3,5-триметилциклогексан,
1-амино-1,3-диметил-3-пропилциклогексан,
1-амино-1,3(транс),5(транс)-триметил-3(цис)-пропилциклогексан,
1-амино-1,3-диметил-3-этилциклогексан,
1-амино-1,3,3-триметилциклогексан,
цис-3-этил-1(транс)-3(транс)-5-триметилциклогексамин,
1-амино-1,3(транс)-диметилциклогексан,
1,3,3-триметил-5,5-дипропилциклогексиламин,
1-амино-1-метил-3(транс)-пропилциклогексан,
1-метил-3(цис)-пропилциклогексиламин,
1-амино-1-метил-3(транс)-этилциклогексан,
1-амино-1,3,3-триметил-5(цис)-этилциклогексан,
1-амино-1,3,3-триметил-5(транс)-этилциклогексан,
цис-3-пропил-1,5,5-триметилциклогексиламин,
транс-3-пропил-1,5,5-триметилциклогексиламин,
N-этил-1,3,3,5,5-пентаметилциклогексиламин,
N-метил-1-амино-1,3,3,5,5-пентаметилциклогексан,
1-амино-1-метилциклогексан,
N,N-диметил-1-амино-1,3,3,5,5-пентаметилциклогексан,
2-(3,3,5,5-тетраметилциклогексил)этиламин,
2-метил-1-(3,3,5,5-тетраметилциклогексил)пропил-2-амин,
2-(1,3,3,5,5-пентаметилциклогексил)этиламина полугидрат,
N-(1,3,3,5,5-пентаметилциклогексил)пирролидин,
1-амино-1,3(транс),5(транс)-триметилциклогексан,
1-амино-1,3(цис),5(цис)-триметилциклогексан,
1-амино-(1R,5S)транс-5-этил-1,3,3-триметилциклогексан,
1-амино-(1S,5S)цис-5-этил-1,3,3-триметилциклогексан,
1-амино-1,5,5-триметил-3(цис)-изопропилциклогексан,
1-амино-1,5,5-триметил-3(транс)-изопропилциклогексан,
1-амино-1-метил-3(цис)-этилциклогексан,
1-амино-1-метил-3(цис)-метилциклогексан,
1-амино-5,5-диэтил-1,3,3-триметилциклогексан,
1-амино-1,3,3,5,5-пентаметилциклогексан,
1-амино-1,5,5-триметил-3,3-диэтилциклогексан,
1-амино-1-этил-3,3,5,5-тетраметилциклогексан,
N-этил-1-амино-1,3,3,5,5-пентаметилциклогексан,
N-(1,3,5-триметилциклогексил)пирролидин или пиперидин,
N-[1,3(транс),5(транс)-триметилциклогексил]пирролидин или пиперидин,
N-[1,3(цис),5(цис)-триметилциклогексил]пирролидин или пиперидин,
N-(1,3,3,5-тетраметилциклогексил)пирролидин или пиперидин,
N-(1,3,3,5,5-пентаметилциклогексил)пирролидин или пиперидин,
N-(1,3,5,5-тетраметил-3-этилциклогексил)пирролидин или пиперидин,
N-(1,5,5-триметил-3,3-диэтилциклогексил)пирролидин или пиперидин,
N-(1,3,3-триметил-цис-5-этилциклогексил)пирролидин или пиперидин,
N-[(1S,5S)цис-5-этил-1,3,3-триметилциклогексил]пирролидин или пиперидин,
N-(1,3,3-триметил-транс-5-этилциклогексил)пирролидин или пиперидин,
N-[(1R,5S)транс-5-этил,3,3-триметилциклогексил]пирролидин или пиперидин,
N-(1-этил-3,3,5,5-тетраметилциклогексил)пирролидин или пиперидин,
N-(1-пропил-3,3,5,5-тетраметилциклогексил)пирролидин или пиперидин,
N-(1,3,3,5,5-пентаметилциклогексил)пирролидин,
а также оптические изомеры, диастереомеры, энантиомеры, гидраты, их фармацевтически приемлемые соли и их смеси.
Производные 1-аминоалкилциклогексана (например, нерамексан, 1-амино-1,3,3,5,5-пентаметилциклогексан) описаны в патентах США №№6034134 и 6071966. Производные 1-аминоалкилциклогексана (например, нерамексан) можно использовать по изобретению в форме любой из фармацевтически приемлемых солей, сольватов, изомеров, конъюгатов и пролекарств, любые ссылки на производные 1-аминоалкилциклогексана (например, нерамексан) в данном описании следует воспринимать как относящиеся также к таким солям, сольватам, изомерам, конъюгатам и пролекарствам.
Фармацевтически приемлемые соли включают, но не ограничиваются ими, кислотно-аддитивные соли, такие как те, что получены с соляной, метилсульфоновой, бромистоводородной, иодистоводородной, хлорной, серной, азотной, фосфорной, уксусной, пропионовой, гликолевой, молочной, пировиноградной, малоновой, янтарной, фумаровой, винной, лимонной, бензойной, угольной, коричной, миндальной, метансульфоновой, этансульфоновой, гидроксиэтансульфоновой, бензолсульфоновой, р-толуолсульфоновой, циклогексансульфаминовой, салициловой, p-аминосалициловой, 2-феноксибензойной и 2-ацетоксибензойной кислотой. Все эти соли (или другие аналогичные соли) можно получать общепринятыми способами. Природа соли не является критической при условии, что она не токсична и существенно не препятствует проявлению желаемой фармакологической активности.
Термин «аналог» или «производное» используют в данном документе в общепринятом фармацевтическом смысле для обозначения молекулы, которая структурно напоминает исходную молекулу (например, нерамексан), но была изменена целевым и контролируемым образом для замены одного или нескольких конкретных заместителей исходной молекулы альтернативным заместителем, в результате чего получается молекула, структурно похожая на исходную молекулу. Синтез и скрининг аналогов (например, с использованием структурного и/или биохимического анализа) для определения слегка модифицированных вариантов известного соединения, которые могут иметь улучшенные или смещенные в нужную сторону черты (такие как более высокая активность и/или избирательность в отношении конкретного целевого типа рецептора, большая способность проникать через барьеры у млекопитающих, такие как клеточные мембраны, меньше побочных эффектов и так далее), представляет собой подход в разработке лекарственных средств, хорошо известный в области фармацевтической химии.
Термин «лечить», используемый в данном документе, означает уменьшать или облегчать по меньшей мере один из симптомов заболевания у субъекта. По смыслу настоящего изобретения термин «лечить» также означает купировать, задерживать начало (то есть период до клинического проявления болезни) и/или уменьшать риск развития или усугубления болезни.
Термин «терапевтически эффективный» применительно к дозе или количеству означает такое количество соединения или фармацевтической композиции, которое достаточно для проявления нужной активности при введении млекопитающему, нуждающемуся в этом.
Словосочетание «фармацевтически приемлемый» при использовании в связи с композициями по изобретению означает молекулярные субстанции и другие ингредиенты таких композиций, которые являются физиологически переносимыми и, как правило, не вызывают неблагоприятных реакций при введении млекопитающим (например, человеку). Термин «фармацевтически приемлемый» может также означать одобренный регулирующим агентством федерального правительства или правительства штата либо перечисленный в фармакопее США или других общепризнанных фармакопеях среди разрешенных к использованию для млекопитающих, и более конкретно, для людей.
Термин «носитель» применительно к фармацевтическим композициям по изобретению означает разбавитель, эксципиент или наполнитель, с которым вводят активное соединение (например, нерамексан). Такие фармацевтические носители могут представлять собой жидкости, такие как вода, солевые растворы, водные растворы декстрозы, водные глицериновые растворы, и масла, включая масла из нефти, животного, растительного или синтетического происхождения, например арахисовое масло, соевое масло, минеральное масло, кунжутное масло и тому подобное. Подходящие фармацевтические носители описаны, например, в «Remington's Pharmaceutical Sciences» автора A.R. Gennaro, 20-е издание.
Термин «примерно» или «приблизительно», как правило, означает в пределах 20% или в пределах 10%, в том числе в пределах 5%, от данного значения или диапазона. Альтернативно, особенно в биологических системах, термин «примерно» означает в пределах примерно порядка (то есть порядка величины), в том числе, в два раза от заданного значения.
Фармацевтические препараты и введение
В сочетании со способами по настоящему изобретению также предложены фармацевтические композиции, содержащие терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана). Композиции по изобретению могут дополнительно содержать носитель или эксципиент (все фармацевтически приемлемые). Композиции могут быть сформулированы для однократного введения в сутки, двукратного введения в сутки или трехкратного введения в сутки.
Активный ингредиент (например, нерамексан, такой как нерамексанмезилат) или композицию по настоящему изобретению можно использовать для лечения по меньшей мере одного из указанных заболеваний, при этом лечение адаптировано или соответствующим образом подготовлено для конкретного введения, описанного в данном документе (например, введения один раз в сутки, дважды в сутки или трижды в сутки). С этой целью вкладыш в упаковку и/или памятка для пациента содержат соответствующую информацию.
Активный ингредиент (например, нерамексан, такой как нерамексанмезилат) или композицию по настоящему изобретению можно использовать для производства лекарственного средства для лечения по меньшей мере одного из указанных заболеваний, при этом лекарственное средство адаптировано или соответствующим образом подготовлено для конкретного введения, описанного в данном документе (например, введения один раз в сутки, дважды в сутки или трижды в сутки). С этой целью вкладыш в упаковку и/или памятка для пациента содержит соответствующую информацию.
По настоящему изобретению лекарственная форма производного 1-аминоалкилциклогексана (например, нерамексана) может представлять собой твердый, полутвердый или жидкий препарат согласно приведенному ниже.
Производные 1-аминоалкилциклогексана по настоящему изобретению (например, нерамексан) можно вводить перорально, местно, парентерально или на слизистые оболочки (например, трансбуккально, путем ингаляции или ректально) в стандартных лекарственных препаратах, содержащих общепринятые нетоксичные фармацевтически приемлемые носители. В другом варианте осуществления для введения субъектам-детям производное 1-аминоалкилциклогексана может быть сформулировано в виде ароматизированной жидкости (например, с ароматом мяты). Производные 1-аминоалкилциклогексана по настоящему изобретению можно вводить перорально в форме капсулы, таблетки или тому подобного, либо как жидкий препарат, либо местно в виде полутвердого препарата, такого как мазь, крем, гель, гидрогель (смотрите Remington's Pharmaceutical Sciences, 20-е издание, автора A.R. Gennaro).
Для перорального введения в форме таблетки или капсулы производные 1-аминоалкилциклогексана по настоящему изобретению (например, нерамексан) можно объединять с нетоксическими фармацевтически приемлемыми эксципиентами, такими как связующие вещества (например, прежелатинизированный кукурузный крахмал, поливинилпирролидон или гидроксипропилметилцеллюлоза); наполнители (например, лактоза, сахароза, глюкоза, маннит, сорбит и другие восстанавливающие и невосстанавливающие сахара, микрокристаллическая целлюлоза, сульфат кальция или вторичный кислый фосфат кальция); смазывающие вещества (например, стеарат магния, тальк или диоксид кремния, стерическая кислота, стеарилфумарат натрия, глицерилбегенат, стеарат кальция и тому подобное); разрыхлители (например, картофельный крахмал или натрийкрахмалгликолят); или увлажняющие вещества (например, лаурилсульфат натрия), красители и ароматизаторы, желатин, подсластители, природные и синтетические камеди (такие как аравийская камедь, трагакантовая камедь или альгинаты), буферные соли, карбоксиметилцеллюлоза, полиэтиленгликоль, воски и тому подобное.
Таблетки могут быть покрыты концентрированным раствором сахара, который может содержать, например, аравийскую камедь, желатин, тальк, диоксид титана и тому подобное. Альтернативно, таблетки могут быть покрыты полимером, который растворяется в легколетучем органическом растворителе или смеси органических растворителей. В конкретных вариантах осуществления препарат нерамексана сформулирован в лекарственных формах с немедленным высвобождением (IR) или модифицированным высвобождением (MR). Твердые лекарственные формы с немедленным высвобождением допускают высвобождение большей части или всего активного ингредиента в течение короткого периода времени, например 60 минут или менее, и делают возможной быструю абсорбцию лекарственного средства (препараты 1-аминоалкилциклогексанов, таких как нерамексан, с немедленным высвобождением раскрыты в опубликованных патентных заявках США №№2006/0002999 и 2006/0198884, объект изобретения которых включен в данный документ посредством ссылки). Твердые пероральные лекарственные формы с модифицированным высвобождением допускают замедленное высвобождение активного ингредиента в течение длительного периода времени в целях поддержания терапевтически эффективных уровней в плазме на протяжении аналогичных увеличенных интервалов времени и/или для изменения других фармакокинетических свойств активного ингредиента (препараты нерамексана с модифицированным высвобождением раскрыты в опубликованной патентной заявке США №2007/0141148, объект изобретения которой включен в данный документ посредством ссылки).
Для препарата в форме мягких желатиновых капсул производные 1-аминоалкилциклогексана по настоящему изобретению (например, нерамексан) можно смешивать, например, с растительным маслом или полиэтиленгликолем. Твердые желатиновые капсулы могут содержать гранулы активных веществ, полученные с применением либо вышеуказанных эксципиентов для таблеток, например лактозы, сахарозы, сорбита, маннита, крахмала (например, картофельного крахмала, кукурузного крахмала или амилопектина), производных целлюлозы, либо желатина. Твердые желатиновые капсулы можно заполнять также жидкими или полутвердыми формами лекарственного средства.
Производные 1-аминоалкилциклогексана по настоящему изобретению (например, нерамексан) можно также помещать в микросферы или микрокапсулы, например, изготовленные из смеси полигликолевой кислоты/молочной кислоты (PGLA) (смотрите, например, патенты США №№5814344, 5100669 и 4849222, PCT публикации №№ WO 95/11010 и WO 93/07861). Для достижения контролируемого высвобождения лекарственного средства можно использовать биосовместимые полимеры, включая, например, полимолочную кислоту, полигликолевую кислоту, сополимеры полимолочной и полигликолевой кислот, поли-эпсилон-капролактон, полигидроксимасляную кислоту, сложные полиортоэфиры, полиацетали, полигидропираны, полицианоакрилаты и перекрестно сшитые или амфипатические блок-сополимеры гидрогелей.
Можно также использовать препарат производных 1-аминоалкилциклогексана по настоящему изобретению в полутвердой или жидкой форме. Производное 1-аминоалкилциклогексана (например, нерамексан) может составлять от 0,1 до 99% по весу от препарата, более конкретно от 0,5 до 20% по весу для препаратов, предназначенных для инъекций, и от 0,2 до 50% по весу для препаратов, подходящих для перорального ведения.
Можно также использовать препараты производных 1-аминоалкилциклогексана по настоящему изобретению в полутвердой или жидкой форме, подходящие для местного введения.
Альтернативно, можно использовать препараты производных 1-аминоалкилциклогексана по настоящему изобретению в сухой (твердой) форме, подходящие для местного введения.
Такие препараты включают гели, кремы, мази, гидрогели, пасты, эмульсии, спреи, растворы, лосьоны и так далее.
Такие препараты также включают порошки, олеогели, суспензии, эмульсии типа «масло в воде», эмульсии типа «вода в масле», гетерогенные эмульсии, микро- и наноэмульсии, самоэмульгирующие системы, водные и неводные растворы, пластыри, или трансдермальные системы. Можно также использовать сочетание вышеуказанных препаратов.
Производное 1-аминоалкилциклогексана (например, нерамексан) может составлять от 0,1 до 99% по весу от препарата, более конкретно от 0,5 до 50% по весу от препарата, или от 1% до 25% по весу от препарата, или от 2% до 20% по весу от препарата.
В одном варианте осуществления изобретения производное 1-аминоалкилциклогексана (например, нерамексан) вводят в препарате с модифицированным высвобождением. Лекарственные формы с модифицированным высвобождением способствуют лучшему соблюдению пациентом режима и схемы лечения, а также обеспечивают эффективную и безопасную терапию за счет снижения частоты побочных реакций на лекарства. В отличие от лекарственных форм с немедленным высвобождением, лекарственные формы с модифицированным высвобождением можно использовать, чтобы продлить фармакологическое действие после введения и сократить различия в плазменных концентрациях лекарственного средства на протяжении интервала между введением доз и тем самым ликвидировать или уменьшить острые пики.
Лекарственная форма с модифицированным высвобождением может включать ядро, либо покрытое лекарственным средством, либо содержащее его. Затем ядро покрывают модифицирующим высвобождение полимером, в котором диспергировано лекарственное средство. Модифицирующий высвобождение полимер постепенно распадается, со временем высвобождая лекарственное средство. Таким образом, самый верхний слой композиции эффективно замедляет и, следовательно, регулирует диффузию лекарственного средства через слой покрытия, когда препарат подвергается воздействию водной среды, то есть в желудочно-кишечном тракте. Чистый коэффициент диффузии лекарственного средства в основном зависит от способности желудочного сока проникать в слой покрытия или в матрицу, а также от растворимости самого лекарственного средства.
В другом варианте осуществления изобретения производное 1-аминоалкилциклогексана (например, нерамексан) сформулировано в виде перорального жидкого препарата. Жидкие препараты для перорального введения могут быть в форме, например, растворов, сиропов, эмульсий или суспензий, или их можно поставлять в виде сухого продукта для разведения водой или другим подходящим носителем перед использованием. Препараты для перорального введения могут быть соответствующим образом сформулированы для обеспечения контролируемого или отложенного высвобождения активного соединения. Пероральные жидкие препараты 1-аминоалкилциклогексанов, например нерамексан, описаны в международной патентной PCT заявке № PCT/US2004/037026, объект изобретения которой включен в данный документ посредством ссылки.
Для перорального введения в жидкой форме производные 1-аминоалкилциклогексана по настоящему изобретению (например, нерамексан) можно объединять с нетоксичными фармацевтически приемлемыми инертными носителями (например, этанолом, глицерином, водой), суспендирующими веществами (например, сиропом сорбитола, производными целлюлозы или гидрогенизированными пищевыми жирами), эмульгаторами (например, лецитином или аравийской камедью), неводными наполнителями (например, миндальным маслом, сложными эфирами жирных кислот, этиловым спиртом или фракционированными растительными маслами), консервантами (например, метил- или пропил-п-гидроксибензоатами или сорбиновой кислотой) и тому подобным. Можно также добавлять стабилизаторы, такие как антиоксиданты (например, BHA, BHT, пропилгаллат, аскорбат натрия, лимонная кислота), для стабилизации лекарственных форм. Например, растворы могут содержать от примерно 0,2% до примерно 20% по весу нерамексана, притом что остальное является сахаром или смесью этанола, воды, глицерина и пропиленгликоля. При необходимости, такие жидкие препараты могут содержать красители, ароматизаторы, подсластители и загустители, такие как карбоксиметилцеллюлоза, или другие эксципиенты.
В другом варианте осуществления терапевтически эффективное количество производного 1-аминоалкилциклогексана (например, нерамексана) вводят в пероральном растворе, содержащем консервант, подсластитель, солюбилизатор и растворитель. Пероральный раствор может включать один или несколько буферов, ароматизаторов или дополнительных эксципиентов. В дополнительном варианте осуществления к пероральному жидкому препарату производного нерамексана добавляют мятный или другие ароматизаторы.
Для введения путем ингаляции производные 1-аминоалкилциклогексана (например, нерамексан) по настоящему изобретению удобно доставлять в форме распыляемого аэрозоля из находящихся под давлением упаковок или распылителя с применением подходящего пропеллента, например дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, двуокиси углерода или другого подходящего газа. В случае находящегося под давлением аэрозоля единичную дозу можно определять путем предоставления клапана для доставки дозированного количества. Можно создавать капсулы или картриджи, например, из желатина для использования в ингаляторе или инсуффляторе, содержащие порошковую смесь соединения и подходящей порошковой основы, такой как лактоза или крахмал.
Растворы для парентерального применения в виде инъекций можно получать в водном растворе водорастворимой фармацевтически приемлемой соли активных веществ, например, в концентрации от примерно 0,5% до примерно 10% по весу. Эти растворы также могут содержать стабилизаторы и/или буферные вещества и их удобно предлагать в виде ампул с различными единицами доз.
Препараты по изобретению можно доставлять парентерально, то есть путем внутривенного (i.v.), интрацеребровентрикулярного (i.c.v.), подкожного (s.c.), внутрибрюшинного (i.p.), внутримышечного (i.m.), субдермального (s.d.) или внутрикожного (i.d.) введения, прямой инъекцией с помощью, например, болюсной инъекции или непрерывной инфузии. Препараты для инъекций можно поставлять в дозированной лекарственной форме, например в ампулах или в многодозовых контейнерах с добавлением консерванта. Альтернативно, активный ингредиент может быть в виде порошка для разведения подходящим носителем, например стерильной апирогенной водой, перед использованием.
Изобретение также относится к фармацевтической упаковке или набору, включающему один или несколько контейнеров, содержащих производное 1-аминоалкилциклогексана (например, нерамексан) и, при необходимости, большее количество ингредиентов препарата. В конкретном варианте осуществления нерамексан поставляют в виде перорального раствора (2 мг/мл) для введения с использованием шприцев емкостью 2 чайные ложки (дозировка KORC®). Каждый пероральный шприц имеет штриховые метки для измерения, при этом линии на правой стороне шприца (от кончика вниз) означают единицы tsp, а линии на левой стороне означают мл.
Оптимальное терапевтически эффективное количество можно определять экспериментально с учетом конкретного способа введения лекарственного средства, показаний для применения такого введения, вовлеченного субъекта (например, вес тела, состояние здоровья, возраст, пол и так далее), а также предпочтений и опыта ответственного врача или ветеринара.
Дозированные лекарственные формы для ректального применения могут представлять собой растворы или суспензии либо могут быть изготовлены в форме суппозиториев или удерживающих клизм, содержащих нерамексан в смеси с нейтральным жирным основанием, или желатиновых ректальных капсул, содержащих активные вещества в смеси с растительным маслом или парафиновым маслом.
Токсичность и терапевтическую эффективность композиций по изобретению можно определять стандартными фармацевтическими методами на экспериментальных животных, например определяя LD50 (доза, летальная для 50% популяции) и ED50 (доза, терапевтически эффективная для 50% популяции). Отношение доз для терапевтического и токсического эффектов представляет собой терапевтический индекс и может выражаться отношением LD50/ED50. Предпочтительными являются композиции с большими терапевтическими индексами.
Подходящие суточные дозы активных соединений по изобретению для терапевтического лечения людей составляют примерно 0,01-10 мг/кг массы тела при пероральном введении и 0,001-10 мг/кг массы тела при парентеральном введении. Например, для взрослых подходящие суточные дозы нерамексана (например, нерамексанмезилата) находятся в диапазоне от примерно 5 мг до примерно 150 мг в сутки, например от примерно 5 мг до примерно 120 мг, от примерно 5 мг до примерно 100 мг или от примерно 5 мг до примерно 75 мг, или от примерно 5 мг до примерно 50 мг, например 25 мг, или 37,5 мг, или 50 мг в сутки. Например, суточная доза может быть скорректирована на массу тела, например 50 мг/сутки при массе тела до 90 кг или 75 мг/сутки для пациентов с массой тела ≥90 кг. Подходящим является также эквимолярное количество другой фармацевтически приемлемой соли, сольвата, изомера, конъюгата, пролекарства или их производных, например нерамексангидрохлорида. Для детей и подростков в возрасте 4-14 лет нерамексан (например, нерамексанмезилат) можно вводить в виде пероральной жидкой лекарственной формы в дозе примерно 0,5 мг/сутки, вплоть до максимальной дозы 10 мг/сутки.
Суточные дозы, указанные в данном документе, можно вводить, например, в количестве одной или двух единичных доз один, два или три раза в сутки. Вследствие этого подходящими дозами для единичной дозы могут быть суточные дозы, разделенные (например, поровну) на число единичных доз, вводимых в сутки, и, следовательно, они могут, как правило, быть равными суточной дозе или ее половине, одной трети, одной четверти или одной шестой части. Таким образом, дозы на единичную дозу можно рассчитывать исходя из каждой суточной дозы, указанной в данном документе. Например, суточную дозу 5 мг можно рассматривать как исходную для расчета дозы для единичной дозы, составляющей примерно 5 мг, 2,5 мг, 1,67 мг, 1,25 мг и 0,83 мг, в зависимости от выбранного режима дозирования. Соответственно доза 150 мг в сутки соответствует дозам для единичной дозы, составляющим, например, приблизительно 150 мг, 75 мг, 50 мг, 37,5 мг и 25 мг для соответствующих режимов дозирования.
Продолжительность лечения может быть краткосрочной, например несколько недель (например, 8-14 недель), или долгосрочной, пока лечащий врач не сочтет, что дальнейшее введение уже не является необходимым.
Производные 1-аминоалкилциклогексана по настоящему изобретению (например, нерамексан) можно вводить в качестве монотерапии или в сочетании с другим средством, предписанным для лечения воспалительных заболеваний кожи.
Термин «сочетание» применительно к активным ингредиентам используют в данном документе для определения одной фармацевтической композиции (препарата), содержащей два активных вещества (например, фармацевтическая композиция, содержащая производное 1-аминоалкилциклогексана, такое как нерамексан, и другое вещество, предписанное для лечения воспалительных заболеваний кожи), или двух отдельных фармацевтических композиций, из которых каждая содержит активное вещество (например, фармацевтическая композиция, содержащая производное 1-аминоалкилциклогексана, такое как нерамексан, и другая фармацевтическая композиция, содержащая другое вещество, предписанное для лечения воспалительных заболеваний кожи), для совместного введения.
По смыслу настоящего изобретения термин «совместное введение» используют для обозначения введения производного 1-аминоалкилциклогексана, такого как нерамексан, и одного или нескольких дополнительных активных веществ (например, другого вещества, предписанного для лечения воспалительных заболеваний кожи, такого как противомикробные препараты, антибиотики, ретиноиды или стероиды) одновременно в одной композиции, либо одновременно в разных композициях, либо последовательно. Однако для того, чтобы последовательное введение считать «совместным», производное 1-аминоалкилциклогексана, такое как нерамексан, и одно или несколько дополнительных активных веществ следует вводить раздельно с таким временным интервалом, который все еще допускает результирующий положительный эффект для лечения воспалительных заболеваний кожи у млекопитающего.
Примеры типичных препаратов
С помощью широко используемых растворителей, вспомогательных веществ и носителей из активных ингредиентов можно изготавливать таблетки, драже, капсулы, капельные растворы, суппозитории, инъекционные и инфузионные препараты, гели, кремы, мази и тому подобное и терапевтически применять путем перорального, ректального, парентерального, местного и других способов введения. Таблетки для перорального введения можно получать обычными методами таблетирования. Следующий пример приведен только в качестве иллюстрации и не должен быть истолкован как ограничивающий.
Пример препарата 1: Таблетки нерамексанмезилата с немедленным высвобождением
В следующих таблицах приведен состав таблеток нерамексанмезилата с немедленным высвобождением в дозах 12,5, 25,0, 37,5 и 50,0 мг, включая активные компоненты, покрывающие вещества и другие эксципиенты.
Нерамексанмезилат, таблетки 12,5 мг, покрытые оболочкой
Нерамексанмезилат, таблетки 25,0 мг, покрытые оболочкой
Нерамексанмезилат, таблетки 37,5 мг, покрытые оболочкой
Нерамексанмезилат, таблетки 50,0 мг, покрытые оболочкой
В следующих таблицах приведен состав местных препаратов нерамексана.
Пример препарата 2
«Unguentum emulsificans»
«Unguentum emulsificans aquosum», содержащая 1% нерамексан
«Unguentum emulsificans aquosum», содержащая 20% нерамексан
Пример препарата 3
«Cremor nonionicus emulsificans aquosum»
«Cremor nonionicus emulsificans aquosum», содержащий 1% нерамексан
«Cremor nonionicus emulsificans aquosum», содержащий 10% нерамексан
Пример препарата 4
«Macrogoli unguentum»
«Macrogoli unguentum», содержащая 2% нерамексан
«Macrogoli unguentum», содержащая 15% нерамексан
Пример препарата 5
«Linimentum nonionicum aquosum»
«Linimentum nonionicum aquosum», содержащая 3% нерамексан
«Linimentum nonionicum aquosum», содержащая 12% нерамексан
«Linimentum nonionicum aquosum», содержащая 25% нерамексан
ПРИМЕРЫ
Следующие примеры иллюстрируют изобретение, не ограничивая его объем.
Пример 1: Эффекты нерамексана на мышиной модели контактной гиперчувствительности
Модель контактной гиперчувствительности (CHS), индуцированной нанесением на кожу гаптенов, служит моделью реакции гиперчувствительности замедленного типа (Schwarz et al., 2004, The Journal of Immunology, 172: 1036-1043). Индуцируется появление антиген-специфических T-лимфоцитов, что можно продемонстрировать экспериментами по адоптивному переносу. Ответная реакция в виде отека уха возникает только у мышей, которые были успешно сенсибилизированы, это свидетельствует о том, что ответ является иммунным ответом, а не токсической реакцией. Отрицательные контроли, то есть несенсибилизированные мыши, не демонстрируют ответную реакцию в виде отека уха при первом нанесении гаптена на уши. Поскольку подавление сенсибилизации лекарственными средствами может указывать на иммуносупрессорную активность соответствующего вещества, модель CHS используют для проведения скрининга лекарственных средств на иммуносупрессорные свойства.
Хотя ответная реакция отека уха (провокация) также отражает иммунный ответ (Т-лимфоциты являются основными медиаторами), реакция отека уха в конечном счете опосредуется через воспалительные цитокины, которые индуцируются антиген-специфическими T-лимфоцитами. Таким образом, провокацию данной иммунной реакции также можно подавлять противовоспалительными лекарственными средствами. Следовательно, модель CHS используется для определения противовоспалительных свойств и также позволяет различать вещества с иммуносупрессорными и противовоспалительными свойствами.
Нерамексан тестировали на его способность влиять на иммунологические и/или воспалительные реакции.
МАТЕРИАЛЫ И МЕТОДЫ
Животные
Для данного исследования использовали самцов мышей C57BL/6N (6-8 недель, примерно 20 г).
Животных оставляли для акклиматизации на 5 суток до начала исследования. Контроль световых циклов, температуры и влажности осуществлялся автоматически. Световые циклы составляли 12 часов. Ежедневный мониторинг свидетельствовал, что температура и влажность оставались в пределах целевых диапазонов 21±1°C и 50±5% соответственно. Животных содержали в полипропиленовых клетках (Ebeco, тип M-3) с решетчатыми крышками (в клетке находилось до 7 мышей). Клетки, подстил и бутылочки с водой меняли на регулярной основе, то есть каждые 7 суток. Стандартный корм (продажный) предоставляли животным без ограничений. Животные имели неограниченный доступ к бытовой водопроводной воде.
Лекарственные средства
Нерамексанмезилат разводили раствором NaCl и заново готовили перед каждой инъекцией, уровни доз определяли в пилотном фармакологическом исследовании. Основываясь на пилотном исследовании, использовали дозу 5 мг/кг за 1 час до сенсибилизации с последующей дозой 3,2 мг/кг, инъецированной через 1 и 3 часа после сенсибилизации.
Лечение
При получении всех животных случайным образом распределяли по экспериментальным группам, так что экспериментальные группы были равномерно распределены среди всех клеток с животными.
Экспериментальные группы и число животных указаны в таблице 18.
Доза соответствует свободному основанию/кислоте, коэффициент преобразования из свободного основания в форму соли составляет 1,57.
Животным делали внутрибрюшинную (i.p.) инъекцию при постоянном объеме дозы, составляющем 200 мкл дозирующего раствора на кг массы тела, используя стальную дозирующую канюлю. Вводимый каждому животному объем определяли каждые сутки путем взвешивания данного животного перед введением.
Мышей сенсибилизировали, нанося 50 мкл раствора динитрофторбензола (DNFB, Sigma Corp., St. Louis, MO) (0,5% в смеси ацетон:оливковое масло, 4:1) на выбритую спину в 0 сутки. В сутки 5, 20 мкл 0,3% DNFB наносили на левое ухо. Отек уха количественно определяли при помощи пружинного микрометра через 24 часа после выявления. Контактную гиперчувствительность (CHS) определяли как величину отека обработанного гаптеном уха по сравнению с толщиной обработанного средой уха и выражали в см×10-3 (среднее±SD). Для положительного контроля животных сенсибилизировали 50 мкл 0,5% DNFB через выбритую кожу. Провокацию осуществляли через 5 суток на левом ухе (0,3% DNFB, 20 мкл). Толщину уха измеряли через 24 часа (см×10-3). Для отрицательного контроля мышам устраивали провокацию 20 мкл 0,3% DNFB и толщину уха измеряли через 24 часа (см×10-3).
Оценка данных
Результаты сенсибилизации анализировали при помощи однофакторного дисперсионного анализа ANOVA (исключая группу отрицательного контроля) с последующим применением теста Даннета в качестве апостериорного теста. Результаты представлены на фиг.1-3.
Результаты
Судя по всему, нерамексан не оказывает влияния на индукцию иммунного ответа; однако введение нерамексана до и после сенсибилизации значительно уменьшало реакцию отека уха. Данные результаты свидетельствуют о том, что нерамексан может оказывать противовоспалительное, но не иммуносупрессорное действие и что нерамексан может быть полезен для лечения воспалительных заболеваний кожи, таких как акне, розацеа, экзема, атопический дерматит, псориаз и жирная кожа.
Пример 2: Эффекты нерамексана на мышиной модели дерматита
Для дальнейшего тестирования противовоспалительных свойств использовали мышиную модель раздражительного дерматита. Индукция ответного отека уха кротоновым маслом является токсической реакцией. Данная ответная реакция является зависимым от концентрации явлением, не зависящим от сенсибилизированных лимфоцитов.
Показано, что противовоспалительные вещества до определенной степени уменьшают ответную реакцию отека уха.
Нерамексан тестировали на противовоспалительные свойства.
Животные
Для данного исследования использовали самцов мышей C57BL/6N (6-8 недель, примерно 20 г).
Животных оставляли для акклиматизации на 5 суток до начала исследования. Контроль световых циклов, температуры и влажности осуществлялся автоматически. Световые циклы составляли 12 часов. Ежедневный мониторинг свидетельствовал, что температура и влажность оставались в пределах целевых диапазонов 21±1°C и 50±5% соответственно. Животных содержали в полипропиленовых клетках (Ebeco, тип M-3) с решетчатыми крышками (в клетке находилось до 7 мышей). Клетки, подстил и бутылочки с водой меняли на регулярной основе, то есть каждые 7 суток. Стандартный корм (продажный) предоставляли животным без ограничений. Животные имели неограниченный доступ к бытовой водопроводной воде.
Лекарственные средства
Нерамексанмезилат разводили раствором NaCl и заново готовили перед каждой инъекцией, уровни доз определяли в пилотном фармакологическом исследовании. Основываясь на пилотном исследовании, использовали дозу 5 мг/кг за 1 час до сенсибилизации с последующей дозой 3,2 мг/кг, инъецированной через 1 и 3 часа после сенсибилизации.
Лечение
При получении всех животных случайным образом распределяли по экспериментальным группам, так что экспериментальные группы были равномерно распределены среди всех клеток с животными.
Экспериментальные группы и число животных указаны в таблице 19.
Доза соответствует свободному основанию/кислоте, коэффициент преобразования из свободного основания в форму соли составляет 1,57.
Животным делали внутрибрюшинную (i.p.) инъекцию при постоянном объеме дозы, составляющем 200 мкл дозирующего раствора на кг массы тела, используя стальную дозирующую канюлю. Вводимый каждому животному объем определяли каждые сутки путем взвешивания данного животного перед введением.
Животным делали внутрибрюшинную (i.p.) инъекцию при постоянном объеме дозы, составляющем 200 мкл дозирующего раствора на кг массы тела, используя стальную дозирующую канюлю. Вводимый каждому животному объем определяли каждые сутки путем взвешивания данного животного перед введением.
20 мкл 1% кротонового масла в ацетоне наносили на левое ухо. Отек уха измеряли через 7 часов и 24 часа. Отек уха количественно определяли при помощи пружинного микрометра. Реакцию на раздражитель определяли как величину отека обработанного раздражителем уха по сравнению с толщиной обработанного средой (ацетоном) уха и выражали в см×10-3. На дополнительную группу воздействовали нерамексаном (как описано выше) и кротоновым маслом.
Оценка данных
Результаты сенсибилизации анализировали при помощи критерия Стьюдента (сравнение между леченными животными и положительным контролем). Результаты представлены на фиг.4-5.
Результаты
Нерамексан до некоторой степени уменьшает ответную реакцию отека уха, вызванную кротоновым маслом, это свидетельствует о том, что нерамексан может быть полезен для лечения воспалительных заболеваний кожи, таких как акне, розацеа, экзема, атопический дерматит, псориаз и жирная кожа.
Пример 3: Противомикробные свойства нерамексана в отношении Propionibacterium acnes
Для определения эффективности нерамексана в отношении конкретной популяции микроорганизмов (то есть Propionibacterium acnes) проводили тест на логарифмическое уменьшение.
Микроорганизмы получали инокуляцией жидкого тиогликолята (FTM). Затем микроорганизмы инкубировали при 35,2±2,5°C в течение 24 часов. Микробную суспензию доводили до концентрации примерно 107-108 колониеобразующих единиц (КОЕ) (CFU) в мл и помечали как стоковую суспензию. Стоковую суспензию дополнительно разводили 1:10 с помощью PBS для достижения концентрации примерно 105-106 КОЕ в мл.
Нерамексанмезилат (1 грамм) разводили в 9,0 мл деионизованной воды для получения 10% раствора (разведение 1:10). Затем 5 мл переносили в 11 мл деионизованной воды для получения 3,125% раствора. Затем в этот раствор инокулировали микроорганизмы и тестировали через временные интервалы в 30 секунд, 1 минута и 5 минут.
Один миллилитр из каждого разведения распределяли в двойном повторе по поверхности триптического соевого агара с 5% овечьей кровью. Чашки инкубировали в анаэробных условиях при 35,2±2,5°C в течение минимум 48 часов. Ту же процедуру повторяли для контроля с фосфатно-солевым буферным раствором. После инкубации все чашки просчитывали для определения в каждой временной точке количества оставшихся микроорганизмов.
Концентрацию каждого микроорганизма в случае контроля и препарата рассчитывали для каждого интервала. Рассчитывали логарифмическое уменьшение для определения изменения (сокращения или увеличения) популяции микроорганизмов относительно исходного инокулята. Минимальную необходимую бактерицидную концентрацию определяли как уменьшение на 3 порядка от исходного инокулята. Результаты представлены в таблице 20.
Результаты
Активность, измеренная в эксперименте на логарифмическое уменьшение, указывает на то, что нерамексан обладает антибактериальной активностью в отношении Propionibacterium acnes. Данные результаты свидетельствуют, что нерамексан может быть полезен для лечения воспалительных заболеваний кожи, таких как акне, розацеа, экзема, атопический дерматит, псориаз и жирная кожа.
Пример 4: Локальная переносимость местного препарата нерамексана
Цель данного исследования заключалась в оценке локальной переносимости нерамексанмезилата в местном препарате при различных уровнях доз через 14 суток ежедневного воздействия на кожу у карликовых свиней.
Исследования проводили на 4 самках карликовых свиней линии Göttingen категории SPF (от Ellegaard Göttingen Minipigs Aps). У каждого животного было по 5 зон нанесения (25 см2), отмеченных на спине, и дозирование проводили в течение 8 часов каждые сутки. Каждую тестовую зону использовали для одного и того же тестируемого препарата или плацебо на протяжении всего исследования. На экспериментальную группу воздействовали нерамексанмезилатом в следующих концентрациях: 0, 0,5; 2,5; 5,0 и 10,0% (масс./масс.).
Клинические признаки регистрировали через 2-4 часа после начала каждой обработки и локальные кожные реакции (эритему, отек) оценивали до начала воздействия. Вес тела регистрировали еженедельно (а также на 1 каждые сутки и при вскрытии). Полное вскрытие проводили для всех животных, однако никаких макроскопических изменений не было обнаружено и вследствие этого только зоны нанесения на коже собирали и в дальнейшем подвергали макроскопическому и микроскопическому гистопатологическому изучению.
Никаких относящихся к тестируемому веществу изменений не наблюдали с точки зрения клинических признаков и прибавки массы тела у животных. Более того, никаких относящихся к тестируемому веществу кожных реакций не наблюдали на протяжении всего исследования. Результаты гистопатологического исследования зон нанесения на коже не выявили каких-либо относящихся к воздействию макроскопических или микроскопических признаков по сравнению с необработанными образцами кожи.
В заключение, обработка кожи карликовых свиней линии Göttingen в течение 14 суток нерамексанмезилатом при уровнях доз 0,5%, 2,5%, 5% и 10% в местном препарате не приводила к появлению относящихся к тестируемому веществу изменений. В условиях данного исследования местный препарат нерамексанмезилата продемонстрировал хорошую локальную (местную) переносимость.
Пример 5: Противомикробная активность нерамексана в отношении соответствующих бактерий - определение значений MIC и MBC методом разведения в агаре
Для оценки противомикробной активности нерамексана в отношении связанных с акне бактерий устанавливали минимальную ингибиторную концентрацию (MIC) и минимальную бактерицидную концентрацию (MBC) в отношении следующих бактерий:
1. Staphylococcus epidermidis ATCC 12228
2. Propionibacterium acnes ATCC 11828
3. Propionibacterium granulosum ATCC 11829
4. Propionibacterium avidum ATCC 25577
Метод
Значения MIC образцов определяли методом разведения в агаре на основании DIN 58940. Чашки Петри диаметром 5,5 см заливали 2,5 мл свежеприготовленного агара Мюллера-Хинтона (компания Merck, каталожный №1.05437) или агара Уилкинса-Чалгрена (компания Oxoid, каталожный № CM643), поддерживаемого в жидком состоянии при 50°C, к которому добавляли разведенный образец в различных концентрациях при 50,0 объемных %.
Подготовка тестируемого раствора и чашек с агаром
Для различных тестируемых соединений использовали следующие диапазоны концентраций.
Для получения исходных разведений образца 12,5%, 3,12% суспензию раствора соответствующего образца получали на очищенной воде. Из этих стоковых растворов с помощью очищенной воды готовили дальнейшие разведения. Все тестируемые соединения доводили до pH 5,5. Для тестируемого препарата №1 также готовили отдельные разведения, доведенные до pH 6,0 и pH 7,4.
Проведение теста с разведением в агаре
Для инокуляции 1 мкл соответствующей суспензии микроорганизмов помещали в центр каждой чашки с агаром. После высыхания инокулированные чашки инкубировали при 36,0±2,0°C. Основанием для продолжительности инкубационного периода служил соответствующий контроль на рост микроорганизмов, культивируемых параллельно.
Тестируемые микроорганизмы и микробное число тестируемых микробных суспензий
Чистоту и идентичность всех тестируемых микроорганизмов проверяли получением субкультур на колумбийском кровяном агаре для микроорганизмов №№1-3 (анаэробных) и микроорганизма №4 (аэробного). Затем микроорганизмы идентифицировали определением биохимического профиля при помощи ATB/API.
Тестируемую микробную суспензию получали инокуляцией нескольких отдельных колоний соответствующих бактерий в стерильный солевой раствор до достижения мутности, соответствующей стандарту McFarland 1,0 (примерно 108 КОЕ/мл). Затем тестируемые микробные суспензии дополнительно разводили 1:10 солевым раствором и определяли микробные числа (смотрите таблицу 21) методом распределения по поверхности при помощи устройства для спирального посева на чашки.
Чашки с агаром инкубировали в условиях, приведенных в таблице 22, а затем проводили оценку. Приведенные значения MIC представляют собой наименьшую концентрацию активного вещества, при которой отсутствует макроскопически видимый рост. Минимальный, едва видимый рост или несколько небольших отдельных колоний оцениваются как ингибирование.
Условия инокуляции и инкубации
Определение минимальной бактерицидной концентрации (MBC)
Все отрицательные тесты на определение минимальной бактерицидной концентрации являются основой для проверки оставшихся микроорганизмов, сегменты инокулированного агара вырезали и помещали в бульон Мюллера-Хинтона (микроорганизм 1) или бульон Уилкинса-Чалгрена (микроорганизмы 2-4). После соответствующего периода инкубации при 36,0±2,0°C (судя по контролю без тестируемого соединения) тесты проверяли вручную на микробный рост (=мутность) и определяли минимальную бактерицидную концентрацию. MBC указывает на концентрацию без выраженной мутности. Выросшие микроорганизмы проверяли на соответствие, чтобы исключить неспецифическое загрязнение.
Оценка данных
Следующие результаты суммированы и внесены в таблицу:
a) Данные по минимальной ингибиторной концентрации (MIC)*
b) Данные по минимальной бактерицидной концентрации (MBC)
* MIC представляет собой концентрацию без макроскопического роста. Едва заметный минимальный рост или несколько отдельных колоний не считаются. У контролей должен наблюдаться относительно хорошо проявляющийся рост. На чашках с агаром, контролирующих стерильность, не должно быть никакого роста.
Результаты для отдельных тестируемых соединений приведены в таблицах 23-30. В этих таблицах в последней колонке суммированы определенные значения MIC и MBC для тестируемых микроорганизмов.
Рост бактерий для чашек в двух повторах обозначен как + (то есть рост) или - (то есть нет роста), +- обозначает слабый рост на обеих чашках или рост на одной чашке и отсутствие роста на другой чашке. Все бактерии демонстрировали надлежащий рост на соответствующей контрольной чашке, не содержащей никакого тестируемого соединения. Никакого влияния используемого разбавителя (очищенная вода) не наблюдали. На контрольных чашках загрязнение отсутствовало.
Значения MIC для нерамексанмезилата при pH 5,5
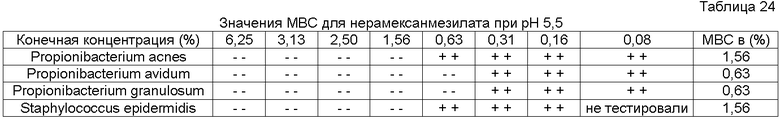
Значения MIC для нерамексанмезилата при pH 6,0
Значения MBC для нерамексанмезилата при pH 6,0
Значения MIC для нерамексанмезилата при pH 7,4
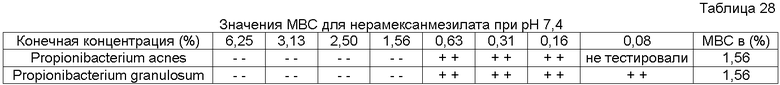
Значения MIC для нерамексан-HCl при pH 5,5
Значения MBC для нерамексан-HCl при pH 5,5
Результаты
В таблице 31 приведены значения MIC и MBC для всех тестируемых соединений, предусмотренных в данном исследовании. В целом, следует учитывать, что значения, определяемые используемым методом, могут различаться в 2 раза (для разведений 1:2).
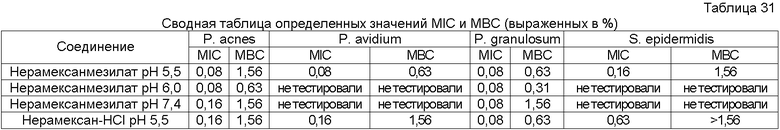
Нерамексан проявляет антибактериальную активность в отношении всех тестированных бактерий, связанных с акне. В пределах данного анализа установленные значения MIC и значения MBC при свойственном коже pH 5,5 сопоставимы для различных штаммов бактерий. Таким образом, нерамексан демонстрирует сходную эффективность в отношении всех тестируемых бактерий.
Очевидное влияние pH на эту антибактериальную активность также отсутствует. Значения MIC и MBC, установленные при pH 6,0 и pH 7,4, находятся в том же диапазоне, что и установленные при рН 5,5. То же самое относится и к значениям MIC и MBC, полученным с нерамексан-HCl. За исключением значения для S. epidermidis, эти значения отличаются максимум в 2 раза от тех, что получены с нерамексанмезилатом. Эти данные свидетельствуют, что солевая форма активного вещества имеет незначительное влияние на антибактериальную активность нерамексана.
Таким образом, наблюдаемая антибактериальная активность в отношении связанных с акне бактерий присуща нерамексану как таковому.
Пример 6: Противомикробная активность нерамексана в отношении соответствующих бактерий - определение бактерицидной активности в количественном суспензионном тесте
Для дальнейшей оценки противомикробной активности нерамексана проводили количественный суспензионный тест.
Метод
1,0 мл тестируемой бактериальной суспензии (микробное число: 1,5-5,0×108 КОЕ/мл) и 1,0 мл дистиллированной воды добавляли к 8,0 мл раствора тестируемого препарата. Запускали секундомер. В конце экспозиции 0,1 мл тестируемой смеси добавляли к 50 мл промывочной жидкости (= тестовая нейтрализующая смесь, TNM, 10°). Готовили два разведения TNM, перенося пипеткой 500 мкл TNM в 9,0 мл триптон-NaCl (соответствует разбавлению 10-2 TNM перед фильтрованием) и соответственно 50 мкл TNM в 9,0 мл триптон-NaCl (соответствует разбавлению 10-3 TNM перед фильтрованием). TNM (в двойном повторе) и каждое из разведений переносили в мембранное фильтрующее устройство, оснащенное мембранным фильтром (0,45 мкм), и немедленно фильтровали. Затем фильтр промывали 150 мл дистиллированной воды. Мембраны переносили на чашки с агаром. После инкубации при соответствующих условиях колонии подсчитывали и документировали.
Нерамексанмезилат тестировали при 4 различных концентрациях (масс./масс. 0,1%, 0,5%, 2,0%, 5,0%) для оценки его бактерицидной активности в отношении Propionibacterium acnes (ATCC 11828). В дополнение к влиянию концентрации нерамексана важность времени контакта с бактериями оценивали при 4 различных временах инкубации (5 мин, 30 мин, 6 ч, 24 ч).
После нужного времени инкубации полное удаление тестируемого соединения из анализа обеспечивали мембранной фильтрацией. Использовали бактериальные суспензии с микробным числом в диапазоне 1,5-5,0×108 КОЕ/мл. Все анализы проводили при свойственном коже pH 5,5.
Показания представляют собой уменьшение числа бактерий в тесте, выраженное в виде логарифмического уменьшения. Это уменьшение числа бактерий коррелирует со способностью соединения убивать бактерии, таким образом, соответствует его значению MBC. Более чем 5-кратное логарифмическое уменьшение необходимо для дезинфицирующего поверхность соединения и более чем 3-кратное логарифмическое уменьшение - для дезинфицирующего руки соединения.
Результаты
Сводные результаты для нерамексанмезилата представлены в таблице 32.
Сводная таблица значений логарифмического уменьшения
для нерамексанмезилата
контакта
Концентрация
Концентрация, соответствующая 0,5%, эффективно устраняет P. acnes в данном тесте через 24 часа контакта. Даже через 6 часов контакта наблюдается значительное логарифмическое уменьшение (2,6-кратное). С 2,0% раствором максимальное уменьшение в данном тесте, соответствующее >5-кратному логарифмическому уменьшению, достигалось только через 30 мин инкубации. С 5% раствором 4,33-кратное логарифмическое уменьшение было получено спустя всего 5 мин инкубации.
Эти данные подтверждают, что нерамексан эффективно устраняет связанные с акне бактерии P. acnes в суспензии. В зависимости от концентрации, достаточно лишь короткого времени инкубации для проявления этой противомикробной активности.
Пример 7: Противомикробная активность нерамексана в отношении Streptococcus pyogenes и Staphylococcus aureus - определение значений MIC методом разведения в агаре
Для оценки противомикробной активности нерамексана в отношении штаммов бактерий, связанных с атопическим дерматитом и локализованными инфекциями кожи («импетиго»), устанавливали минимальную ингибиторную концентрацию (MIC) в отношении следующий бактерий:
5. Staphylococcus aureus ATCC 6538
6. Streptococcus pyogenes ATCC 12344
Притом что инфекция Staphylococcus aureus является очень распространенным осложнением при атопическом дерматите, этот же штамм бактерий вовлечен в локализованные инфекции кожи («импетиго») наряду с Streptococcus pyogenes.
Метод
Значения MIC образцов определяли методом разведения в агаре на основании DIN 58940. Чашки Петри диаметром 5,5 см заливали 2,5 мл свежеприготовленного агара Мюллера-Хинтона, 2-кратно концентрированного (компания Merck, каталожный №1.05437), pH 5,5, поддерживаемого в жидком состоянии при 50°C, к которому добавляли разведенный образец в различных концентрациях при 50,0 объемных %.
Подготовка тестируемого раствора и чашек с агаром
Нерамексанмезилат тестировали в диапазоне концентраций 6,25-1×10-2%. Все тестируемые растворы доводили до pH 5,5.
Проведение теста с разведением в агаре
Для инокуляции 1 мкл соответствующей суспензии микроорганизмов помещали в центр каждой чашки с агаром. После высыхания инокулированные чашки инкубировали при 36,0±2,0°C. Основанием для продолжительности инкубационного периода служил соответствующий контроль на рост микроорганизмов, культивируемых параллельно.
Тестируемые микроорганизмы и микробное число тестируемых микробных суспензий
Тестируемую микробную суспензию получали инокуляцией нескольких отдельных колоний соответствующих бактерий в стерильный солевой раствор до достижения мутности, соответствующей стандарту McFarland 1,0 (примерно 108 КОЕ/мл). Затем тестируемые микробные суспензии дополнительно разводили 1:10 солевым раствором и определяли микробные числа (смотрите таблицу 33) методом распределения по поверхности при помощи устройства для спирального посева на чашки.
Чашки с агаром инкубировали в условиях, приведенных в таблице 34, а затем проводили оценку. Приведенные значения MIC представляют собой наименьшую концентрацию активного вещества, при которой отсутствует макроскопически видимый рост. Минимальный, едва видимый рост или несколько небольших отдельных колоний оцениваются как ингибирование.
Условия инокуляции и инкубации
Оценка данных и результатов
Результаты для отдельных тестируемых соединений приведены в таблице 35. Рост бактерий для чашек в двух повторах обозначен как + (то есть рост) или - (то есть нет роста), +- обозначает слабый рост на обеих чашках или рост на одной чашке и отсутствие роста на другой чашке. Оба штамма бактерий демонстрировали надлежащий рост на соответствующей контрольной чашке, не содержащей никакого тестируемого соединения. Никакого влияния используемого разбавителя (очищенная вода) не наблюдали. На контрольных чашках загрязнение отсутствовало. В целом, следует учитывать, что значения, определяемые используемым методом, могут различаться в 2 раза (для разведений 1:2).
Значения MIC для нерамексанмезилата при pH 5,5
Нерамексанмезилат обладает антибактериальной активностью в отношении Staphylococcus aureus, связанных с атопическим дерматитом и кожным заболеванием контагиозным импетиго, и действует даже в большей степени против Streptococcus pyogenes, которые также вовлечены в контагиозное импетиго.
Использованный тест с разведением в агаре является стандартным тестом для установления антибактериальной активности тестируемого соединения. Условия роста и инокулированное число бактерий позволяют избежать завышенной оценки антибактериального эффекта тестируемого соединения. Выбранное свойственное коже значение pH 5,5 дополнительно способствует получению данных, которые имеют значение для лечения кожных бактериальных инфекций. Таким образом, полученные данные являются адекватными для определения антибактериальной терапевтической активности нерамексана в отношении обоих штаммов бактерий.
Вследствие этого полученные данные позволяют предсказать терапевтическое применение нерамексана в клинических случаях, связанных с участием тестированных штаммов бактерий.
Настоящее изобретение не должно быть ограничено в объеме конкретными вариантами осуществления, описанными в данном документе. Действительно, различные модификации изобретения в дополнение к тем, что описаны в данном документе, станут очевидными для специалиста в данной области из вышеизложенного описания. Такие модификации должны входить в объем прилагающейся формулы изобретения.
Все патенты, заявки, публикации, методы тестирования, литературные источники и другие материалы, цитированные в данном документе, включены в данный документ посредством ссылки.
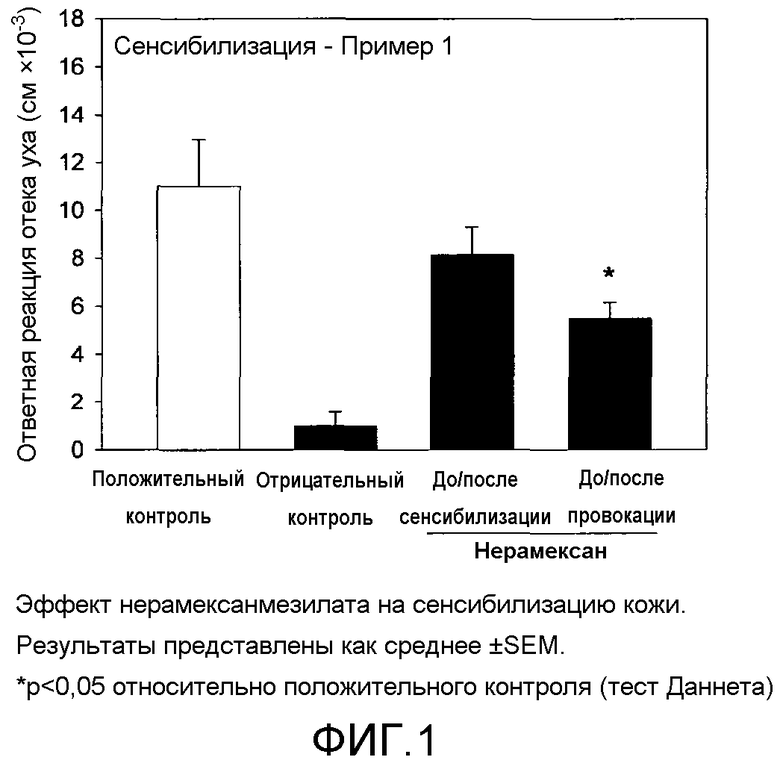
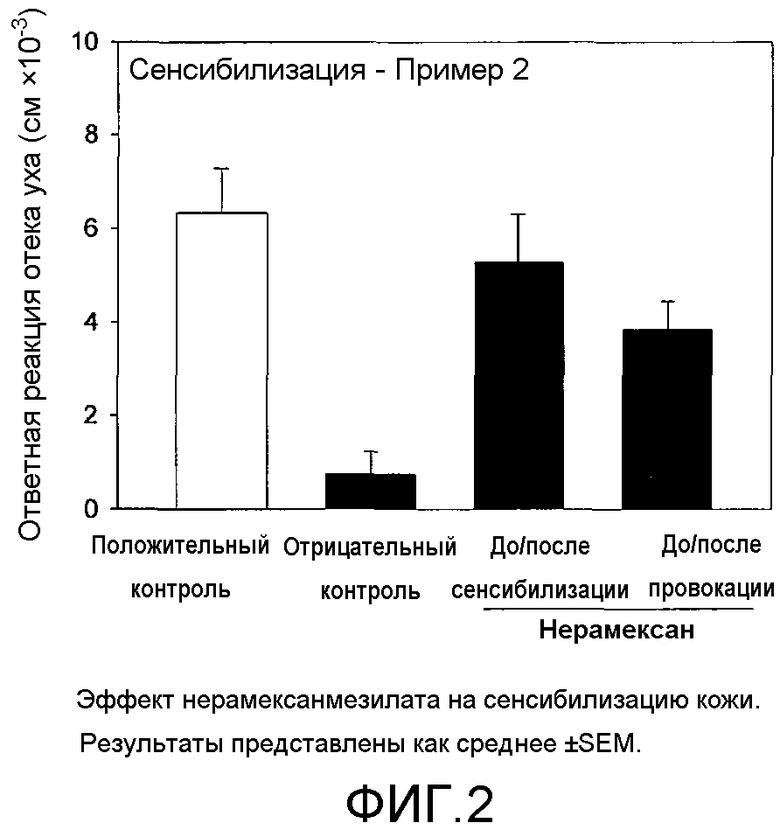
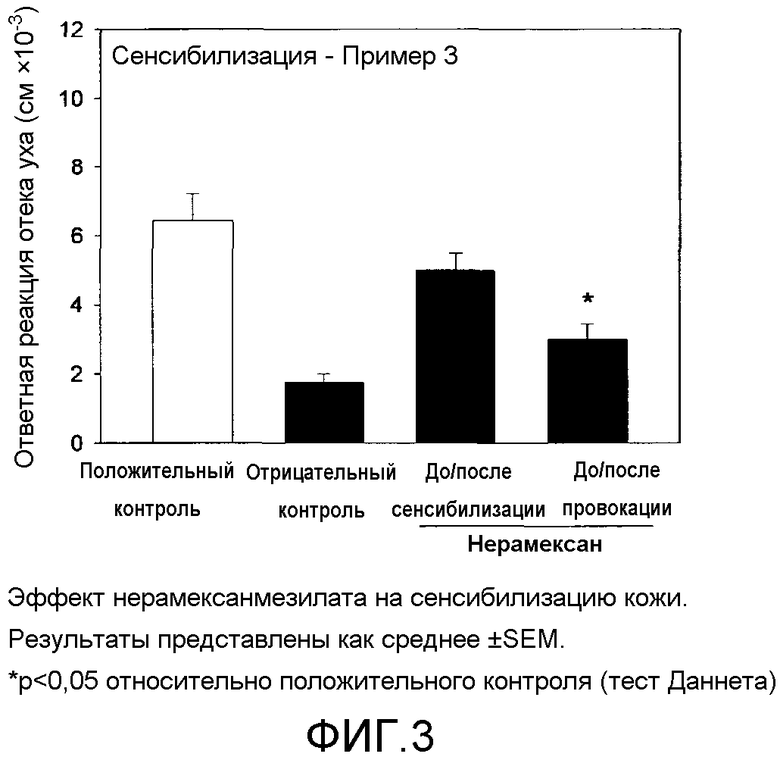
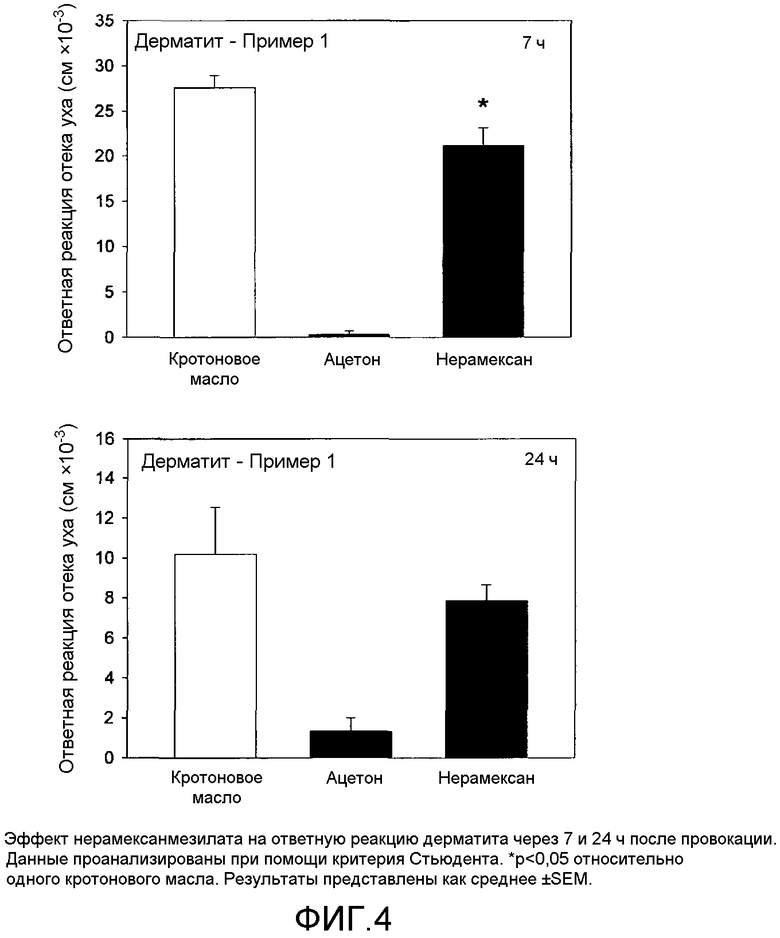
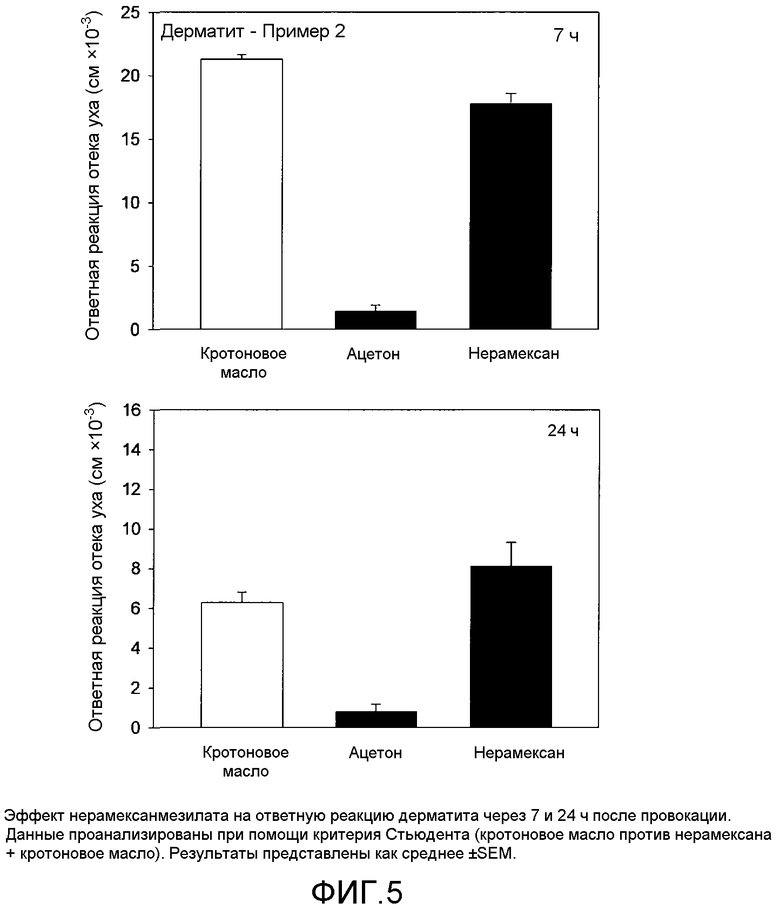
Изобретение относится к области дерматологии и представляет собой применение производного 1-аминоалкилциклогексана, выбранного из нерамексана и его фармацевтически приемлемых солей, для лечения или предупреждения воспалительных заболеваний кожи, которые представляют собой акне, раздражительный дерматит, импетиго и атопический дерматит. Изобретение обеспечивает расширение арсенала средств для лечения воспалительных заболеваний кожи. 4 н. и 35 з.п. ф-лы, 7 пр., 35 табл., 5 ил.
1. Применение производного 1-аминоалкилциклогексана, выбранного из нерамексана и его фармацевтически приемлемых солей, для лечения или предупреждения воспалительных заболеваний кожи, которые представляют собой акне, раздражительный дерматит, импетиго и атопический дерматит.
2. Применение производного 1-аминоалкилциклогексана, выбранного из нерамексана и его фармацевтически приемлемых солей, для изготовления лекарственного средства для лечения или предупреждения воспалительных заболеваний кожи, которые представляют собой акне, раздражительный дерматит, импетиго и атопический дерматит.
3. Применение по п.1, где производное 1-аминоалкилциклогексана представляет собой мезилат нерамексана.
4. Применение по п.3, где мезилат нерамексана вводят в диапазоне от примерно 5 мг до примерно 150 мг/сутки, или в диапазоне от примерно 5 мг до примерно 100 мг/сутки, или в диапазоне от примерно 5 мг до примерно 75 мг/сутки.
5. Применение по п.3, где мезилат нерамексана вводят в дозе примерно 50 мг/сутки.
6. Применение по п.3, где мезилат нерамексана вводят в дозе примерно 75 мг/сутки.
7. Применение по п.1, где производное 1-аминоалкилциклогексана вводят один раз в день, дважды в день или трижды в день.
8. Применение по любому из пп.1 или 3-7, где производное 1-аминоалкилциклогексана вводят в местном препарате.
9. Применение по п.8, где производное 1-аминоалкилциклогексана вводят в количестве от 0,1 до 99 вес.% от веса препарата.
10. Применение по любому из пп.1 или 3-7, где производное 1-аминоалкилциклогексана вводят в пероральном препарате.
11. Применение по любому из пп.1 или 3-7, где воспалительное заболевание кожи выбрано из акне, атопического дерматита и импетиго.
12. Применение по п.11, где воспалительное заболевание кожи представляет собой акне.
13. Применение по п.11, где воспалительное заболевание кожи представляет собой атопический дерматит.
14. Применение по п.11, где воспалительное заболевание кожи представляет собой контагиозное импетиго.
15. Применение по п.8, где воспалительное заболевание кожи выбрано из акне и атопического дерматита.
16. Фармацевтическая композиция, содержащая терапевтически эффективное количество производного 1-аминоалкилциклогексана, выбранного из нерамексана и его фармацевтически приемлемых солей, в сочетании с дополнительным фармацевтическим средством, которое является эффективным в лечении или предупреждении воспалительных заболеваний кожи, которые представляют собой акне, раздражительный дерматит, импетиго и атопический дерматит, и, не обязательно, по меньшей мере одним фармацевтически приемлемым носителем или эксципиентом.
17. Фармацевтическая композиция по п.16, в которой производное 1-аминоалкилциклогексана представляет собой мезилат нерамексана.
18. Применение по п.2, где производное 1-аминоалкилциклогексана представляет собой мезилат нерамексана.
19. Применение по п.2, где лекарственное средство изготовлено для введения посредством местного препарата.
20. Применение по п.2, где лекарственное средство изготовлено для введения посредством орального препарата.
21. Применение по п.2, где воспалительное заболевание кожи выбрано из акне и атопического дерматита.
22. Применение по п.2, где воспалительное заболевание кожи представляет собой акне.
23. Применение по п.2, где воспалительное заболевание кожи представляет собой атопический дерматит.
24. Применение по п.2, где воспалительное заболевание кожи представляет собой контагиозное импетиго.
25. Применение по п.19, где воспалительное заболевание кожи выбрано из акне и атопического дерматита.
26. Способ лечения или предупреждения воспалительных заболеваний кожи, которые представляют собой акне, раздражительный дерматит, импетиго и атопический дерматит у субъекта, нуждающегося в этом, включающий введение эффективного количества производного 1-аминоалкилциклогексана, выбранного из нерамексана и его фармацевтически приемлемых солей.
27. Способ по п.26, где производное 1-аминоалкилциклогексана представляет собой мезилат нерамексана.
28. Способ по п.27, где мезилат нерамексана вводят в диапазоне от примерно 5 мг до примерно 150 мг/сутки, или в диапазоне от примерно 5 мг до примерно 100 мг/сутки, или в диапазоне от примерно 5 мг до примерно 75 мг/сутки.
29. Способ по п.27, где мезилат нерамексана вводят в дозе примерно 50 мг/сутки.
30. Способ по п.27, где мезилат нерамексана вводят в дозе примерно 75 мг/сутки.
31. Способ по любому из пп.27-30, где производное 1-аминоалкилциклогексана вводят один раз в день, дважды в день или трижды в день.
32. Способ по любому из пп.27-30, где производное 1-аминоалкилциклогексана вводят в местном препарате.
33. Способ по п.32, где производное 1-аминоалкилциклогексана вводят в количестве от 0,1 до 99 вес.% от веса препарата.
34. Способ по любому из пп.27-30, где производное 1-аминоалкилциклогексана вводят в пероральном препарате.
35. Способ по любому из пп.27-30, где воспалительное заболевание кожи выбрано из акне, атопического дерматита и импетиго.
36. Способ по п.35, где воспалительное заболевание кожи представляет собой акне.
37. Способ по п.35, где воспалительное заболевание кожи представляет собой атопический дерматит.
38. Способ по п.35, где воспалительное заболевание кожи представляет собой контагиозное импетиго.
39. Способ по п.32, где воспалительное заболевание кожи выбрано из акне и атопического дерматита.
| US 2007141148 A1, 21.06.2007 | |||
| WO 2005009421 A2, 03.02.2005 | |||
| Осветительное приспособление для микроскопа | 1926 |
|
SU10430A1 |
| КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ КОЖНЫХ ЗАБОЛЕВАНИЙ | 2000 |
|
RU2199319C1 |
Авторы
Даты
2013-05-20—Публикация
2009-12-18—Подача