Настоящее изобретение относится к области душистых веществ, в частности к получению новых соединений, способу их получения и к их применению в парфюмерии благодаря их душистым свойствам. Соединения по изобретению представляют собой триметил-3,5,7-октан(ен)нитрилы и их α-замещенные производные, и они подходят для применения в парфюмерии, в частности, в качестве исходного материала. Настоящее изобретение относится также к духам и душистым продуктам, содержащим указанные соединения.
В настоящее время в области парфюмерии используется множество алифатических или ароматических нитрилов. Их разработка выгодна по причине их хорошей стабильности в агрессивных средах и из-за того, что они часто близки по запаху к соответствующим альдегидам; причем последние использовались в парфюмерии задолго до разработки нитрилов.
Заявителем было установлено, что некоторые триметил-3,5,7-октан(ен)нитрилы и их производные, имеющие заместитель в α-положении по отношению к нитрильной группе, отвечающие показанной ниже общей формуле (I), действительно могут быть выгодны в качестве отдушки, духов или в качестве исходного материала для духов или душистых композиций. Соединения по изобретению являются новыми не только в области парфюмерии, но, насколько известно заявителю, о них вообще никогда не сообщалось в литературе. Однако парфюмерная промышленность духов все больше и больше подвергается законодательному регулированию, и ведется поиск соединений, которые могли бы заменить или быть отождествлены с некоторыми соединениями, применение которых было недавно запрещено по причинам безопасности или вследствие их токсичности.
Объектом изобретения являются, в частности, соединения общей формулы (I) ниже:
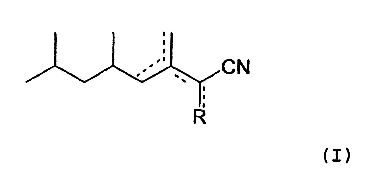
в которой R означает атом водорода, метильную группу или метиленовую группу и в которой не более одной из четырех пунктирных линий означают двойную связь углерод-углерод.
Согласно одному частному варианту осуществления изобретения основная цепь является насыщенной, а R означает атом водорода, метильную группу или метиленовую группу.
Согласно другому предпочтительному варианту осуществления соединение по изобретению отвечает следующей формуле (II):
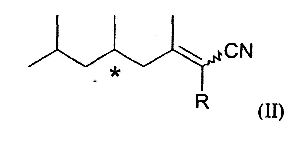
в которой R означает атом водорода или метильную группу.
Согласно другому предпочтительному варианту осуществления соединение по изобретению отвечает следующей формуле (III):
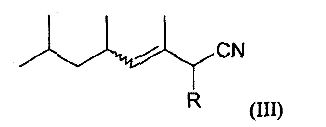
в которой R означает атом водорода или метильную группу.
Согласно другому предпочтительному варианту осуществления соединение по изобретению отвечает следующей формуле (IV):
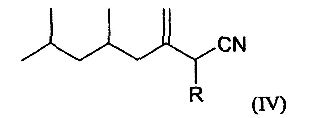
в которой R означает атом водорода или метильную группу.
Согласно другому предпочтительному варианту осуществления соединение по изобретению отвечает следующей формуле (V):
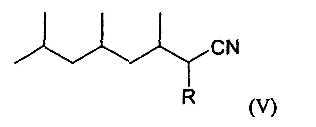
в которой R означает атом водорода или метильную группу.
Согласно другому предпочтительному варианту осуществления соединение по изобретению отвечает следующей формуле (VI):
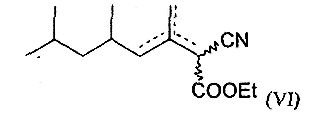
Согласно другому предпочтительному варианту осуществления соединение по изобретению отвечает следующей формуле (VII):
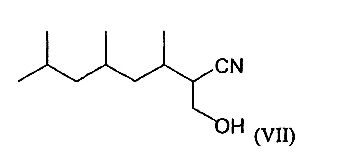
Согласно другому предпочтительному варианту осуществления соединение по изобретению отвечает следующей формуле (VIII):
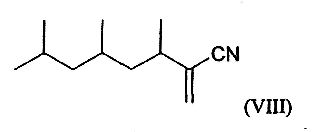
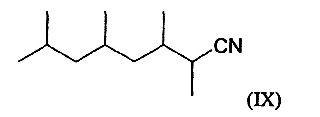
Согласно другому предпочтительному варианту осуществления соединение по изобретению отвечает следующей формуле (IX):
Соединения по изобретению содержат один или несколько асимметричных атомов углерода и поэтому могут находиться в виде смесей оптических изомеров, в частности энантиомеров и диастереомеров. Подразумевается, что настоящее изобретение включает в свой объем композиции, содержащие по меньшей мере одно соединение общей формулы (I), в виде изомера или смеси изомеров, в частности энантиомера или смеси энантиомеров, или рацемической смеси, или диастереомера или смеси диастереомеров. Таким образом, объектом изобретения является также применение соединений общей формулы (I) в качестве одорирующих агентов.
Так, объектом изобретения является композиция, отличающаяся тем, что она содержит по меньшей мере одно соединение по изобретению в виде изомера или смеси изомеров, энантиомера или смеси энантиомеров, или рацемической смеси, или диастереомера или смеси диастереомеров. Согласно одному предпочтительному варианту осуществления композиция по изобретению содержит смесь соединений формулы (II), (III), (IV), какие определены выше. Согласно другому варианту осуществления изобретения композиция содержит по меньшей мере один из двух изомеров Z и E соединения (II), какое определено выше, или смесь указанных двух изомеров. Согласно еще одному предпочтительному варианту осуществления композиция содержит по меньшей мере один из четырех диастереомеров соединения (V), какое определено выше, или смесь указанных четырех диастереомеров.
Объектом изобретения является также композиция, содержащая смесь двух изомеров Z/E по меньшей мере одного соединения формулы (II), (III) и/или (IV).
Поскольку соединения по изобретению содержат по меньшей мере один асимметрический атом углерода, объектом изобретения является также композиция, содержащая смесь энантиомеров или диастереомеров соединения (I); объектом изобретения является также композиция, содержащая смесь энантиомеров соединения (II); объектом изобретения является также композиция, содержащая смесь энантиомеров или диастереомеров соединения (III); объектом изобретения является также композиция, содержащая смесь энантиомеров или диастереоизомеров соединения (IV); объектом изобретения является также композиция, содержащая смесь энантиомеров или диастереомеров соединения (V); объектом изобретения является также композиция, содержащая смесь энантиомеров или диастереомеров соединения (VIII); объектом изобретения является также композиция, содержащая смесь энантиомеров или диастереомеров соединения (IX).
Объектом изобретения является также композиция, содержащая всего один энантиомер единственного изомера Z или E соединения (II); композиция, содержащая всего один энантиомер или диастереомер единственного изомера Z или E соединения (III); композиция, содержащая всего один энантиомер или диастереомер соединения (IV); композиция, содержащая всего один энантиомер или диастереомер соединения (V); композиция, содержащая всего один энантиомер или диастереомер соединения (VIII); композиция, содержащая всего один энантиомер или диастереомер соединения (IX).
Соединения по изобретению могут быть получены множеством способов, известных специалисту, в частности объектом изобретения является также способ получения соединений по изобретению путем конденсации по Кневенагелю [2] между кетоном, в частности диметил-4,6-гептанон-2, и цианоуксусной кислотой или ее сложными эфирами; предпочтительно за этой конденсацией идет декарбоксилирование, как показано исключительно в целях иллюстрации на схеме A. Следует понимать, что схема A показывает один способ синтеза соединений по изобретению, в которых R означает атом водорода.
Диметил-4,6-гептанон-2 легко доступен, например, как побочный продукт щелочной кетолизации ацетона в промышленном масштабе [3]. Конденсацией могут быть получены три пространственных изомера, из которых два могут иметь цис- или транс-конфигурацию, или их смесь, причем указанные изомеры отличаются друг от друга относительным положением нитрильной группы и образованной двойной связи углерод-углерод, а также геометрией относительно указанной двойной связи (α, β: изомеры E и Z; β, γ: изомеры E и Z; β: метилен).
Полученное количество различных изомеров в смеси может меняться в зависимости от рабочих условий [2]. Так, обычно увеличение времени и температуры на этапе декарбоксилирования повышает долю сопряженных изомеров (II), тогда как уменьшение количества основных катализаторов способствует образованию ненасыщенных β, γ изомеров (III E и Z, IV). Соединения (III) и (IV) могут быть отделены от смеси перегонкой в присутствии сильной кислоты, тогда как обработка в присутствии спиртового раствора едкого кали позволяет выделить ненасыщенные α, β изомеры в чистой форме (II).
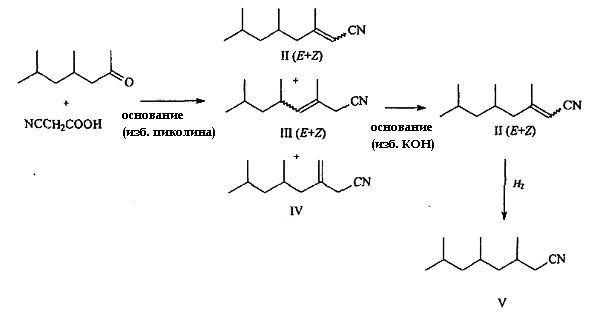
Схема A
Восстановление, например, путем каталитического гидрирования при обычных температуре и давлении изомеров (II), названных Verbetryle™, на палладии на угле ведет к насыщенному нитрилу (V) с выходом 88%. Соединение (V) названо Dihydroverbetryle™ (схема A).
Все соединения по изобретению отличаются интенсивной душистой ноткой померанца, зелени, каждый со своей особенностью: смесь изомеров II, III и IV в пропорциях (30(II): 70(III+IV)) обнаруживает фруктовую нотку (груша), Verbetryle™, полученный обработкой последнего основанием, отличается скорее чуть мятными цветочными гранями, напоминающими ирис.
Dihydroverbetryle™ (V) завершает свою обонятельную палитру цветочными, альдегидными нотками, напоминающими геранонитрил. Ощутимы также мятные штрихи.
Замена цианоуксусной кислоты ее этиловым эфиром в конденсации Кневенагеля ведет к ненасыщенному сложному нитрилоэфиру (VI) (схема B). Восстановление последнего, например, с помощью боргидрида натрия приводит к β-гидроксинитрилу (VII). Этот последний позволяет получить α, β-ненасыщенный нитрил (VIII), который образует нитрил (IX) при гидрировании в тех же условиях, какие указаны ранее.
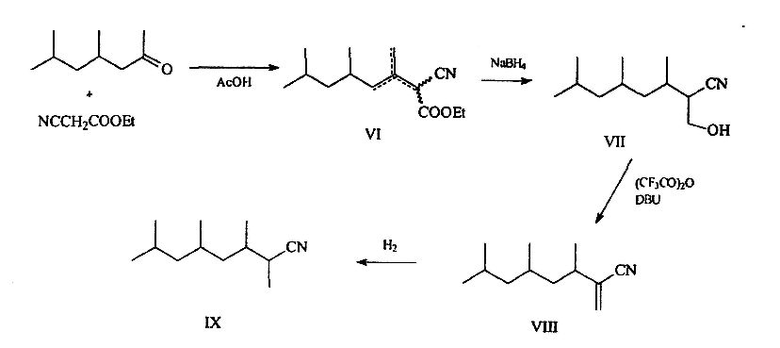
Схема B
Ненасыщенный нитрил (VIII) отличается нотками типа "эссенция мандарина, цветочная", тогда как ее насыщенный гомолог (IX) имеет нотки "молочные, фруктовые и сладкого миндаля".
Соединения по изобретению являются исходными материалами, сильными в плане душистости, поэтому они могут найти применение для придания, усиления и даже улучшения запаха широкого круга продуктов.
Таким образом, объектом изобретения является также применение по меньшей мере одного соединения формулы (I) согласно изобретению в качестве одорирующего агента, как агента, маскирующего запах, или как агента нейтрализации запаха, самостоятельно или в смеси с одним или несколькими другим душистыми соединениями, известными специалисту, и которые специалист в состоянии выбрать в зависимости от искомого эффекта. Дополнительный одорирующий агент или агенты могут быть соединениями формулы (I) или другими одорирующими агентами, известными специалисту.
В контексте настоящего изобретения термин "парфюмерия" означает не только парфюмерию в обычном смысле термина, но также другие области, в которых важен запах продуктов. Соединения по изобретению могут быть частью парфюмерных композиций в обычном смысле этого термина, такими как базовые парфюмерные композиции и концентраты, одеколон, туалетная вода, духи и сходные продукты; топических композиций, в частности косметических, таких как кремы для лица и тела, тальковая пудра, предметы по уходу за телом, в частности шампуни, продукты для мытья тела и волос, масла для волос, лосьоны для укрепления волос, соли и масла для ванны, гели для душа и ванны, туалетные мыла, антитранспиранты и дезодоранты для тела, лосьоны и кремы для бритья или после бритья, кремы, зубные пасты, ополаскиватели для рта, помады и близкие продукты; и частью средств по уходу, таких как умягчители, текстильные умягчающие средства, детергенты, жидкие моющие средства, освежители окружающей среды, продукты для уборки и дезинфекции жилища и близкие продукты.
Таким образом, соединения по изобретению являются душистыми соединениями, подходящими для применения в парфюмерии, в частности, в качестве компонентов духов. В рамках настоящего изобретения под духами понимается смесь пахучих веществ, которые могут быть растворены в или смешаны с твердой основой, чтобы придать желаемый запах коже или совсем другому основанию, для которого необходим или желателен приятный запах. Термин одорирующий используется здесь для обозначения соединения, которое источает запах.
Таким образом, объектом изобретения является парфюмерная композиция, в частности душистая базовая композиция или концентрат, одеколон, туалетная вода или духи, отличающаяся тем, что она содержит по меньшей мере одно соединение по изобретению. Объектом изобретения является, в частности, косметическая композиция, в частности крем для лица и тела, тальковая пудра, масло для волос или для тела, шампунь, лосьон для укрепления волос, соль для ванны, масло для ванны, гель для душа, гель для ванны, туалетное мыло, антитранспирант для тела, дезодорант для тела, лосьоны, крем для бритья, мыло для бритья, крем, зубная паста, полоскание для рта, помада, отличающаяся тем, что она содержит по меньшей мере одно соединение согласно изобретению. Объектом изобретения является также средство для ухода, в частности умягчитель, детергент, жидкое моющее средство, освежитель для окружающей среды, отличающееся тем, что оно содержит по меньшей мере одно соединение по изобретению. Другим объектом изобретения является профилактический или непрофилактический способ косметической обработки или ухода, в котором используется по меньшей мере одно соединение формулы (I) или по меньшей мере одна композиция, содержащая по меньшей мере одно соединение формулы (I).
Изобретение относится также к композициям, содержащим по меньшей мере одно соединение по изобретению и по меньшей мере одно другое душистое вещество, в частности выбранное из натуральных продуктов, таких как эфирные масла, абсолют, резиноиды, конкреты и т.д., а также синтетические продукты, такие как алифатические, ароматические или гетероциклические углеводороды, спирты, альдегиды, кетоны, простые эфиры, сложные эфиры, ацетали, нитрилы.
Соединения по изобретению могут применяться в парфюмерии, в частности в духах или душистых композициях, в широком диапазоне концентраций, которая зависит как от природы конечного продукта, так и от концентрации других компонентов композиции.
Предпочтительно соединения по изобретению будут присутствовать в парфюмерных композициях или духах в концентрации по меньшей мере 0,001 вес.% от полного веса композиции (при этой концентрации ее запах ощутим). Предпочтительно соединения по изобретению будут присутствовать в парфюмерных композициях или духах в концентрации по меньшей мере 0,01 вес.% от полного веса композиции. Соединения по изобретению будут присутствовать в духах предпочтительно в количестве по меньшей мере 1 в.ч. на млн, предпочтительно 10 в.ч./млн.
Изобретение относится также к применению по меньшей мере одного соединения по изобретению в качестве одорирующего агента или агента, маскирующего запах, или в качестве агента нейтрализации запаха, возможно в сочетании с другими одорирующими агентами.
Следующие примеры являются попытками показать, исключительно в целях иллюстрации, получение и применение соединений по изобретению; изобретение никоим образом не ограничено указанными примерами.
Пример 1: Синтез
1.1 Получение смеси триметил-3,5,7-октеннитрилов формул (II), (III) и (IV), в которых R означает атом водорода
Реакцию осуществляют в двухлитровой трехгорлой колбе, снабженной погружным термометром, обратным холодильником, оборудованным фазовым разделителем и капельной воронкой на 500 миллилитров с выравниванием давления.
В колбу последовательно вводят 10 г ацетата аммония (0,13 моль), 20,4 г 2-пиколина (0,22 моль), 160 г толуола и 568 г диметил-4,6-гептанон-2 (4 моль). Все это доводят до температуры кипения с обратным холодильником, при этом воду удаляют по мере выделения.
Раствор 170 г цианоуксусной кислоты (2 моль) в 70 г чистой воды (раствор 70 мас.%) выливают в капельную воронку. Этот раствор равномерно добавляют в колбу в течении 12 часов. Из-за выпаривания воды и диоксида углерода образуется пена. Воду равномерно удаляют из фазового разделителя. Кипячение с обратным холодильником продолжают еще 6 часов после окончания добавления, затем проверяют отсутствие выделения диоксида углерода. Когда дистиллят становится прозрачным, его собирают в сборный резервуар и убирают. Операцию прекращают, когда температура паров достигнет 145-150°C. Нагрев прекращают, а классическую перегонную установку заменяют на фазовый разделитель. Жидкостный кольцевой насос соединяют с полученной установкой, затем очень постепенно снижают вакуум. Постепенно собирают второй дистиллят до достижения температуры пара 60-65°C при давлении 18 Торр. Он представляет собой избыток введенного кетона.
Остаток промывают насыщенным водным раствором бикарбоната натрия, сушат, затем перегоняют (Т-ра кипения = 87-95°C/5 Торр). Собрано 210 г нитрила, что соответствует выходу 63,5%.
Соотношение между сопряженными изомерами (E+Z) (II) и несопряженными изомерами (III) и (IV) (см. схему A) было установлено путем интегрирования специфических сигналов протонного ЯМР (сигналы протона в альфа-положении к нитрилу): для изомеров (II) винильный протон находится при 5,0 ppm для одного изомера и при 5,18 ppm для другого, протоны, локализованные в положении α к нитрильной группе, находятся при 3,05 ppm для изомеров (III) и (IV), для которых R означает атом водорода.
Таким образом, можно сделать вывод, что изомеры (I) составляют 30% смеси.
1.2 Получение триметил-3,5,7-октен-2-нитрила формулы II, в которой R означает атом водорода: (Verbetryle™).
В колбу объемом 500 мл последовательно вводят 100 г этанола, 16,56 г гидроксида калия (0,295 моль), затем 210 г нитрила для равновесия (1,27 моль). Смесь перемешивают 16 часов при температуре окружающей среды, затем ее охлаждают до 0-5°C. Медленно добавляют 85%-ную фосфорную кислоту (54,4 г), pH контролируют (он должен быть почти равен 7), затем этанол отгоняют при пониженном давлении.
Остаток подвергают ректификации в вакууме через короткую колонну, затем его перегоняют в вакууме (Т-ра кипения = 85-90°C/5 Торр). Продукт перегонки весит 196 г, то есть выход равен 93,3%. Этот продукт является смесью двух изомеров E и Z в соотношении соответственно 60:40 (газовая хроматография). Он получен в виде бесцветной жидкости, имеющей очень характерный запах.
1) ИК: 3051, 2956, 2218, 1629, 1459, 1385, 1367, 829, 806, 791 см-1
2) МС (70 эВ): m/e = 165(M+·), 164, 151, 150, 122, 108, 85, 81, 69 а.е.м.
3) 1H-ЯМР: CDCl3, 200 МГц:
δ (ppm): 0,80-0,90 (м, 9H); 1,04 (д*д, 7,0/7,0 Гц, 2H); 1,12 (д*д, 7,3/7,3 Гц, 2H); 1,50-2,00 (м, 4H) 1,92 (д, 1,6 Гц, 3H); 2,02 (д, 1,0 Гц, 3H); 2,10-2,40 (м, 4H); 5,10 (м, 1H); 5,18 (м, 1H)
Подчеркнутые сигналы относятся к миноритарному изомеру.
4) 13C-ЯМР: CDCl3; 50 МГц:
δ (ppm): 19,3; 19,4; 20,8; 22,0; 22,1; 23,0; 23,3; 23,5; 25,1; 44,1; 46,2; 46,3; 46,9; 96,3; 96,7; 117,2; 164,5; 164,6.
1.3 Получение триметил-3,5,7-октаннитрила (V): (Dihydroverbetryle)
В автоклав объемом 250 мл последовательно вводят 16,5 г Verbetryle (II), 2 г палладия на угле (5%-ного), затем 150 мл сухого толуола. Полученный раствор перемешивают 24 часа в атмосфере водорода, фильтруют, затем промывают 5 н. раствором соляной кислоты. Полученный продукт перегоняют в вакууме (Температура кипения = 92-95°C/6 Торр), что дает 15 г нитрила V.
Выход 90%.
1) ИК: 2249, 1460, 1420, 1386, 1368 см-1
2) МС (70 эВ): m/e = 167(M+·); 166; 152; 124; 110(100); 96; 85; 69 а.е.м.
3) 1H-ЯМР: CDCl3, 200 МГц: смесь 4 диастереомеров
δ (ppm): 0,8-0,9 (м, 3H); 1,0-1,1 (м, 3H); 1,10-2,00 (м, 7H); 2,20-2,35 (м, 2H).
4) 13C-ЯМР: CDCl3; 50 МГц:
δ (ppm): 17,2; 17,5; 18,1; 18,2; 20,2; 20,4; 21,4; 21,6; 22,4; 23,1; 23,2; 23,4; 25,7; 25,8; 25,9; 26,0; 41,9; 42,0; 44,6; 45,2; 94,8; 116,9; 117,0.
1.4 Получение карбоэтокси-2-триметил-3,5,7-октен-2-нитрила (VI).
В колбу на 250 мл, снабженную насадкой Дина-Старка, последовательно вводят 25,6 г диметил-4,6-гептанона (0,18 моль), 14,34 г этилцианоацетата (0,127 моль), 1,95 г ацетата аммония, 6 г уксусной кислоты и 100 мл метилциклогексана. Смесь доводят до температуры кипения с обратным холодильником, отделяя воду по мере образования. Через один час смесь охлаждают до температуры окружающей среды, затем ее промывают до нейтральности насыщенным раствором бикарбоната натрия. Остаток перегоняют в вакууме (6 Торр), чтобы собрать избыток кетона (6,5 г), затем в высоком вакууме, чтобы собрать сложный цианоэфир VI. Собрано 25,8 г бесцветной жидкости (Т-ра кипения =100-104°C/2.10-1 Торр), то есть выход 85%.
Изучение спектра протонного ЯМР (см. ниже) показало отсутствие винильного протона и, следовательно, сопряженных производных. Интегрирование сигналов от метильных радикалов на двойной связи углерод-углерод (2,28 ppm для миноритарного изомера, 2,36 для мажоритарного) показывает наличие двух изомеров E/Z в пропорции 40/60.
1) ИК: 2224, 1731, 1603, 1465, 1368, 1287, 1228, 1099, 1070, 858, 777 см-1
2) МС (70 эВ): m/e = 237(M+·), 222, 192, 180, 164, 153, 135, 125, 97, 85(100), 69 а.е.м.
3) 1H-ЯМР: CDCl3, 200 МГц: подчеркнутые сигналы соответствуют миноритарному изомеру
δ (ppm): 0,8-1,0 (м, 9H), 1,0-1,3 (м, 2H), 1,34 (т, J=7,2 Гц, 3H), 1,35 (т, J=7,2 Гц, 3H), 1,5-2,1 (м, 2H), 2,28 (с, 3H), 2,36 (с, 3H), 2,48 (м, 1H), 2,76 (м, 1H), 4,27 (кв, J=7,2 Гц, 2H), 4,28 (кв, J=7,2 Гц, 2H)
4) 1H-ЯМР: CDCl3, 200 МГц: подчеркнутые сигналы соответствуют миноритарному изомеру
δ (ppm): 14,8; 19,7; 21,6; 22,4; 23,6; 23,7; 25,5; 25,7; 30,4; 30,9; 42,6; 46,7; 46,9; 48,6; 62,0; 106,0; 106,4; 116,3; 162,1; 162,4; 177,0; 177,1.
1.5 Получение гидроксиметил-2-триметил-3,5,7-октаннитрила (VII):
Реакцию проводят в трехгорлой колбе объемом 1 л, снабженной обратным холодильником, погружным термометром и капельной воронкой на 250 мл с выравниванием давления. В колбу последовательно вводят 11,4 г (0,3 моль) боргидрида натрия, затем 300 мл абсолютного этанола, охлажденного до 0°C. В капельную воронку выливают раствор 47,4 г (0,2 моль) сложного цианоэфира (VI) в 100 мл абсолютного этанола. Содержимое колбы доводят до -15°C, затем добавляют содержимое воронки, поддерживая температуру не выше 0°C. Полученную смесь перемешивают 16 часов при температуре окружающей среды, затем ее последовательно обрабатывают 50 мл ацетона и 200 мл соляной кислоты (5 н.). Смесь перемешивают 5 часов, затем этанол удаляют перегонкой. Остаток экстрагируют 3 раза 200 мл метилового эфира и трет-бутила. Органические фазы концентрируют, затем перегоняют в глубоком вакууме. Получена бесцветная жидкость (30,7 г) (Температура кипения = 100-102°C/2.10-1 Торр), что означает выход 78%.
1) ИК: 3460, 2244, 1465, 1385, 1367, 1166, 1062, 1028, 573 см-1
2) МС (70 эВ): m/e = 197 (M+·), 182, 152, 141, 140, 124, 110, 85, 68, 43(100) а.е.м.
3) 1H-ЯМР: CDCl3, 200 МГц: смесь 4 диастереомеров
δ (ppm): 0,8-0,9 (м, 3H); 1,0-1,1 (м, 3H); 1,10-2,00 (м, 7H); 2,60-2,90 (м, 1H); 3,50 (с, 1H); 3,60-4,00 (м, 2H).
4) 13С-ЯМР: CDCl3; 50 МГц: смесь 4 диастереомеров
δ (ppm) 13,6; 14,3; 15,5; 15,9; 16,9; 17,2; 17,9; 18,6; 19,5; 20,0; 20,2; 20,4; 20,9; 21,2; 21,4; 22,0; 22,9; 23,0; 23,1; 25,2; 25,3; 25,4; 25,6; 26,7; 26,9; 27,4; 27,5; 38,1; 38,4; 39,5; 39,6; 39,7; 40,1; 41,0; 41,2; 43,3; 44,3; 45,1; 45,6; 58,4; 58,5; 59,0; 59,2; 117,7; 117,9; 118,5; 118,6.
1.6 Получение метилен-2-триметил-3,5,7-октаннитрила (VIII):
В трехгорлую колбу объемом 250 мл, сухую и продутую азотом, последовательно вводят 19,7 г цианоспирта (VII) (0,1 моль), 150 мл безводного метиленхлорида, затем 18,26 г (0,11 моль) DBU (1,8-диазабицикло[5.4.0]ундек-7-ена). Раствор доводят до 0°C, затем по каплям добавляют 22,05 г (0,105 моль) трифторуксусного ангидрида, не выходя за 5°C в массе. Полученный раствор перемешивают 16 часов при температуре окружающей среды, затем его подвергают гидролизу, сушат и концентрируют. Остаток перегоняют в вакууме (6 Торр), получая 16 г ненасыщенного нитрила (VIII), который перегоняют при 105-108°C. Выход составляет 89%.
1) ИК: 2222, 1622, 1460, 1383, 935, 651 см-1
2) МС (70 эВ): m/e= 179(M+·), 178, 164, 136, 122, 108, 95, 83, 57(100) а.е.м.
3) 1H-ЯМР: CDCl3, 200 МГц: смесь 2 диастереомеров
δ (ppm): 0,8-0,9 (м, 3H) 1,00-1,80 (м, 9H); 2,5 (м, 1H); 5,70 (с, 1H); 5,80 (д, J=2 Гц, 1H)
4) 13C-ЯМР (ppm):
19,6; 19,9; 20,2; 20,7; 22,5; 22,8; 23,6; 24,0; 25,4; 25,5; 37,1; 37,4; 43,0; 43,3; 46,9; 47,3; 118,0; 118,2; 128,8; 129,2; 129,4; 130,0.
1.7 Получение тетраметил-2,3,5,7-октаннитрила (IX):
В автоклав объемом 250 мл последовательно вводят 15 г нитрила VIII, 2 г палладия на угле (5%-ного) и 100 мл сухого толуола. Смесь перемешивают под нормальным давлением водорода. Течение реакции контролируют по газовой хроматографии. Когда реакция завершается, реакционную смесь фильтруют, промывают 5 н. раствором соляной кислоты, затем концентрируют. Остаток перегоняют в вакууме и получают 13,65 г бесцветной жидкости, что соответствует выходу 90%. Т-ра кипения = 100-102°C/6 Торр.
1) ИК: 2239, 2212, 1465, 1385, 1368, 1168 см-1
2) МС (70 эВ): m/e = 181(M+·), 180, 166, 138, 125, 124, 110, 85, 71, 55, 43(100) а.е.м
3) 1H-ЯМР: CDCl3, 200 МГц: смесь 4 диастереомеров
δ (ppm): 0,8-0,9 (м, 3H); 1,10-1,90 (м, 12H); 2,60 (м, 1H);
4) 13C-ЯМР: CDCl3; 50 МГц: смесь 4 диастереомеров
δ (ppm) 14,5; 15,3; 15,6; 16,2; 16,4; 17,4; 17,6; 19,5; 19,7; 20,5; 20,9; 22,1; 22,4; 22,8; 23,4; 23,6; 23,9; 24,2; 25,4; 25,5; 25,6; 27,8; 27,9; 28,0; 31,0; 31,5; 32,2; 32,3; 33,5; 33,8; 33,9; 40,8; 41,6; 43,1; 43,6; 46,2; 46,7; 47,7; 48,0; 122,0; 122,3; 122,7; 122,9.
Пример 2: Оценка пахучести Verbetryle (II) и Dihydroverbetryle™ (V) в душистой композиции.
Описание душистых свойств
Verbetryle (II): зелень, померанец, ирис, цветочный, чуть мятный.
Dihydroverbetryle™ (V): зелень, натуральный грейпфрут, чуть мятный.
Готовили парфюмерные композиции (опыты 2 и 3), в которых изучали обонятельный эффект Verbetryle™ и Dihydroverbetryle™ в сравнении с композицией, не содержащей этих соединений (опыт 1).
(вес)
(вес)
(вес)
Verbetryle™
Dihydroverbetryle™
0
0
30
0
0
30
Эти композиции были испытаны, например, в основе перламутрового геля для душа из расчете 0,5 вес.%. Композиция из опыта 2 вносила мужскую ароматическую нотку перечной мяты, тогда как композиция из опыта 3 вносила нотку натурального грейпфрута, с легким акцентом горечи по сравнению с композицией опыта 1.
Источники информации
1. M. ERMAN; Advances in the Chemistry of Nitriles and Amides, Perfumer and Flavorist, 27, 30, (2002).
2. G.JONES; The Knoevenagel Condensation; Organic Reactions 15, 204, (1967) John Wiley and Sons Ed.; New-York, London, Sidney.
3. A. HINNEN, J.DREUX; Bull. Soc. Chim. Fr., 1964, p.1492.
Изобретение относится к новым соединениям общей формулы (I), a также к их энантиомерам, диастереомерам и изомерам Z или Е, которые могут найти применение в качестве одорирующего агента или агента, маскирующего запах. В формуле 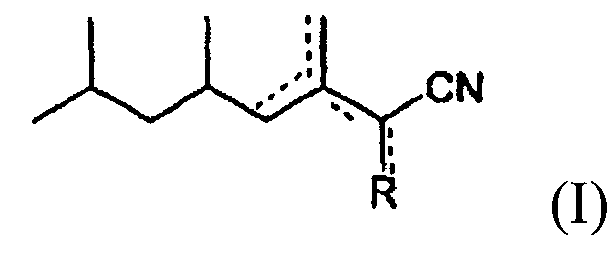 R означает атом водорода, метильную группу или метиленовую группу, и в которой не более одной из четырех пунктирных линий означает двойную связь углерод-углерод. Изобретение относится также к способам получения соединений формулы (I), композициям, в том числе парфюмерным и косметическим, средству для уборки, которые содержат указанные соединения. 8 н. и 13 з.п. ф-лы, 2 пр.
R означает атом водорода, метильную группу или метиленовую группу, и в которой не более одной из четырех пунктирных линий означает двойную связь углерод-углерод. Изобретение относится также к способам получения соединений формулы (I), композициям, в том числе парфюмерным и косметическим, средству для уборки, которые содержат указанные соединения. 8 н. и 13 з.п. ф-лы, 2 пр.
1. Соединения общей формулы (I)
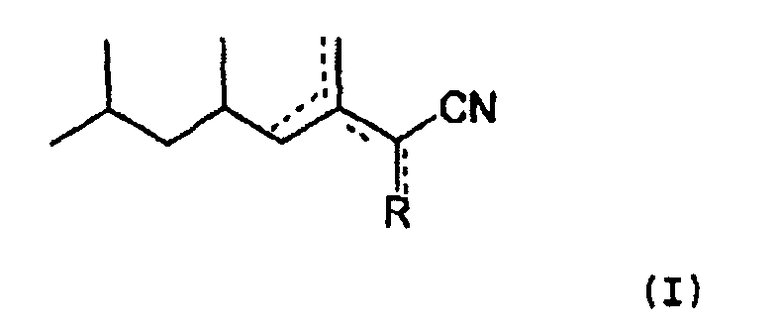
в которой R означает атом водорода, метильную группу или метиленовую группу, и в которой не более одной из четырех пунктирных линий означает двойную связь углерод-углерод, а также их энантиомеры, диастереомеры и изомеры Z или Е.
2. Соединения по п.1 следующей общей формулы (II):
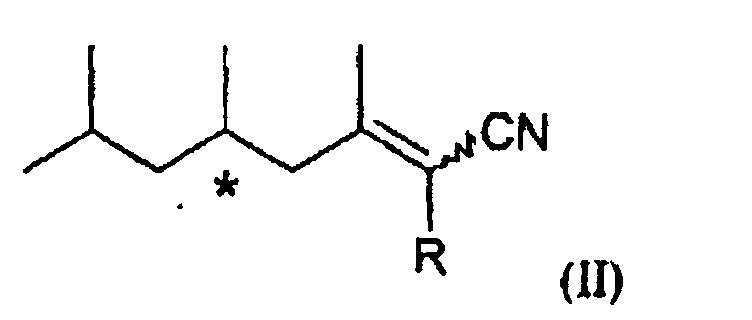
в которой R означает атом водорода или метильную группу, их изомеры Z или Е, их энантиомеры.
3. Соединения по п.1 следующей общей формулы (III):
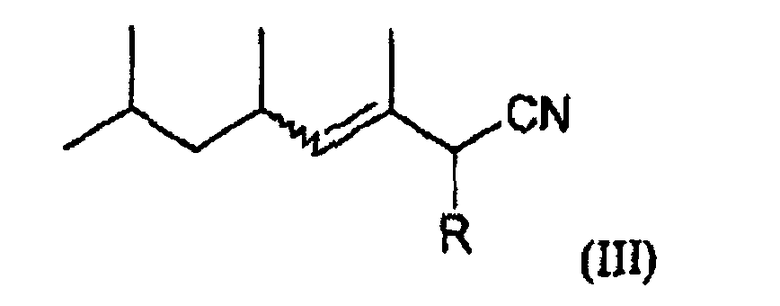
в которой R означает атом водорода или метильную группу, их изомеры Z или Е, их энантиомеры и их диастереомеры.
4. Соединения по п.1 следующей общей формулы (IV):
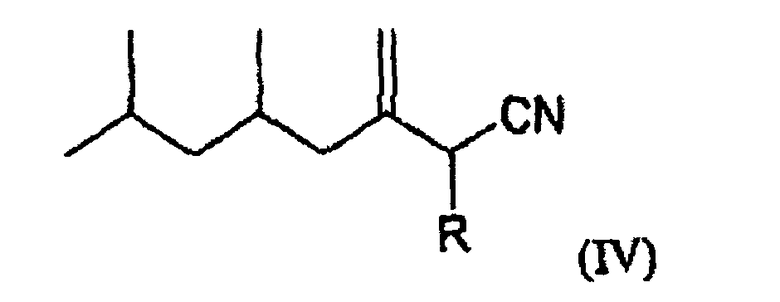
в которой R означает атом водорода или метильную группу, их энантиомеры и их диастереомеры.
5. Соединения по п.1 следующей общей формулы (V):
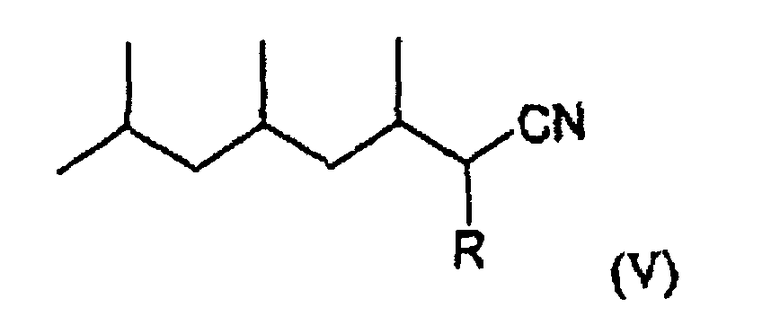
в которой R означает атом водорода или метильную группу, их энантиомеры и их диастереомеры.
6. Соединение по п.1 следующей общей формулы (VIII):
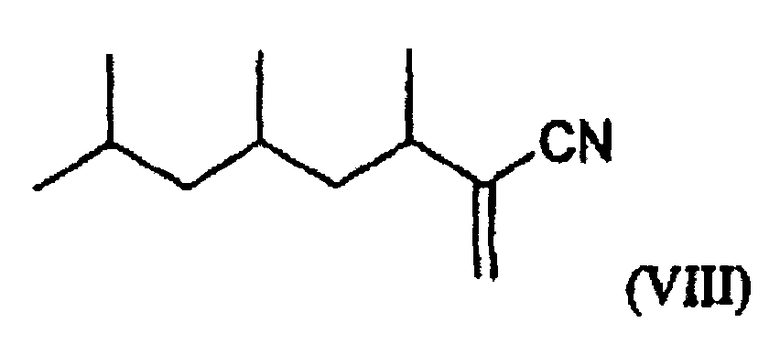
его энантиомеры и его диастереомеры.
7. Композиция, содержащая по меньшей мере соединение, какое определено в любом из пп.1-6, в виде изомера или смеси изомеров, энантиомера или смеси энантиомеров, или рацемической смеси, или диастереомера или смеси диастереомеров, или изомеры Z или Е, для применения в качестве одорирующего агента или агента, маскирующего запах, или в качестве агента нейтрализации запаха.
8. Композиция по п.7, отличающаяся тем, что она содержит смесь соединений формул (II), (III), (IV), какие определены в пп.2-4.
9. Композиция по п.7, отличающаяся тем, что она содержит по меньшей мере один из двух Z и Е изомеров соединения (II), какое определено в п.2, или смесь указанных двух изомеров.
10. Композиция по п.7, отличающаяся тем, что она содержит по меньшей мере один из четырех диастереомеров соединения (V), какое определено в п.5, или смесь указанных четырех диастереомеров.
11. Композиция по любому из пп.7-10, отличающаяся тем, что она дополнительно содержит по меньшей мере одно другое душистое вещество.
12. Парфюмерная композиция, отличающаяся тем, что она содержит по меньшей мере одно соединение, какое определено в любом из пп.1-6.
13. Парфюмерная композиция по п.12, отличающаяся тем, что она представляет собой базовую душистую композицию или концентрат, одеколон, туалетную воду или духи.
14. Косметическая композиция, отличающаяся тем, что она содержит по меньшей мере одно соединение, какое определено в любом из пп.1-6.
15. Косметическая композиция по п.14, отличающаяся тем, что она представляет собой крем для лица и тела, тальковую пудру, масло для волос или для тела, шампунь, лосьон для укрепления волос, соль для ванны, масло для ванны, гель для душа, гель для ванны, туалетное мыло, антитранспирант для тела, дезодорант для тела, лосьоны, крем для бритья, мыло для бритья, крем, зубную пасту, полоскание для рта, помаду.
16. Средство для уборки, отличающееся тем, что оно содержит по меньшей мере одно соединение, какое определено в любом из пп.1-6.
17. Средство для уборки по п.16, отличающееся тем, что оно представляет собой умягчитель, детергент, жидкое моющее средство, освежитель для окружающей среды.
18. Применение по меньшей мере одного соединения формулы (I), какое определено в любом из пп.1-6, в качестве одорирующего агента или агента, маскирующего запах, или в качестве агента нейтрализации запаха, возможно в сочетании с другими одорирующими агентами.
19. Способ получения соединений формул (II), (III) и (IV), какие описаны в любом из пп.2-4, в которых R означает атом водорода, где диметил-4,6-гептанон-2 и цианоуксусную кислоту подвергают конденсации Кневенагеля.
20. Способ по п.19, дополнительно включающий стадию восстановления для получения соединения формулы (V), где R означает атом водорода.
21. Способ получения соединения формулы (VIII), какое описано в п.6, где диметил-4,6-гептанон-2 и этиловый эфир цианоуксусной кислоты подвергают конденсации Кневенагеля с получением соединения формулы (VI) и затем осуществляют стадию восстановления для получения соединения формулы (VII), и затем осуществляют стадию дегидратации для получения соединения формулы (VIII).
| 0 |
|
SU347596A1 | |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ изменения органолептических свойств продуктов потребления | 1974 |
|
SU580804A3 |
Авторы
Даты
2013-05-20—Публикация
2008-10-28—Подача