Объектом настоящего изобретения являются новые ацетали 1-(3,3-диметилциклогекс-1-енил)этанона, обладающие амбровой или животной нотами, способ их получения и также их применение в химической промышленности и, в частности, в парфюмерии, косметике и в промышленности моющих средств, указанные соединения обладают особым запахом и особой стойкостью.
В парфюмерной промышленности постоянно ищут новые органолептические соединения, обладающие сильным запахом и наименьшей возможной стоимостью изготовления. Точнее, соединения, обладающие амбровой или животной нотами, являются редкими и их трудно получать. Кроме того, получение недорогих соединений, которые обладают амбровой или животной нотами и одновременно не обладают древесной нотой, становится все менее и менее легким.
Из обладающих запахом молекул, представляющих интерес для парфюмерии, редкими являются соединения, которым придана амбровая и/или животная ноты. Из числа чаще всего использующихся можно перечислить амбринол® (Firmenich, Switzerland) или 2,5,5-триметил-1,2,3,4,4a,5,6,7-октагидронафталин-2-ол (DE 2733928) или грисальва® (IFF, USA), или 3a-этил-6,6,9a-триметилдодекагидронафто[2,1-c]фуран (US 7468447), которые представлены ниже:
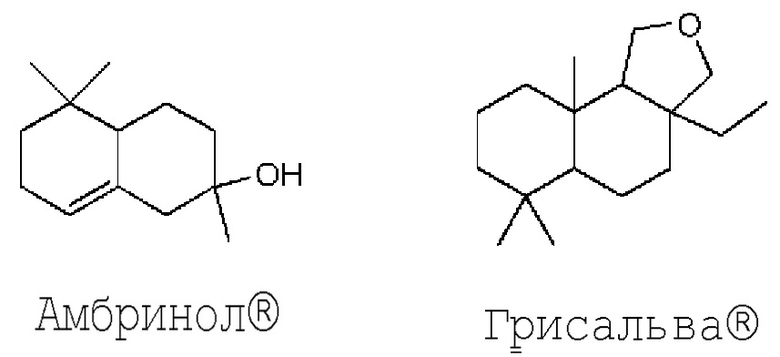
Кроме того, главным недостатком многих соединений, обладающих амбровой и/или животной нотой, является сложность способов их синтеза, что делает их очень дорогостоящим сырьем, и затрудняет их получение с высоким выходом. Например, амбринол® можно получить в две стадии из β-ионона (US 4163866); однако первая стадия термолиза, проводимая при температуре, равной от 300 до 500°C, дает промежуточный продукт дегидроамбринол (предшественник амбринола) с выходом, равным лишь 27%. Кроме того, вторая стадия гидрирования дает смесь α- и β-изомеров амбринола, тогда как требуется только α-изомер амбринола. Аналогичным образом, способ синтеза грисальва® из 1-(2,2,6,-триметилциклогексил)-пентан-3-она включает не менее девяти стадий (US 7468447).
Кроме того, для обеспечения соответствия постоянным потребностям парфюмерной и пищевкусовой промышленности заявитель выявил новые ацетали 1-(3,3-диметилциклогекс-1-енил)этанона, эти соединения обладают очень сильной и летучей амбровой или животной нотой, а также исключительной стойкостью.
Эти ацетали 1-(3,3-диметилциклогекс-1-енил)этанона описываются следующей общей формулой I:
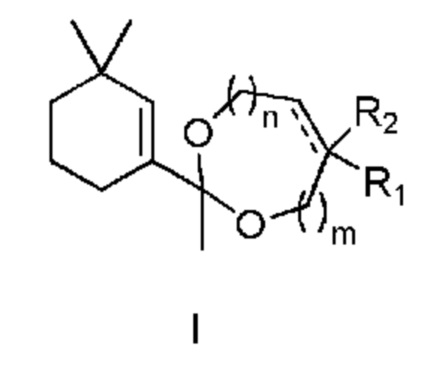
в которой:
- m и n означают количество атомов углерода (метиленовых групп) и все независимо равны 0 или 1;
- R1 означает атом водорода или насыщенную C1-C2-алкильную группу;
- углерод-углеродная связь, представленная штриховой линией, присутствует или отсутствует и
если указанная связь отсутствует, то R2 присутствует и означает атом водорода или насыщенную C1-C2-алкильную группу,
если указанная связь присутствует, то R2 отсутствует;
указанное соединение находится в форме стереоизомера, смеси стереоизомеров или рацемической смеси.
В предпочтительном варианте осуществления m и n означают количество групп -CH2- и все независимо равны 0 или 1.
Настоящее изобретение также относится к композиции, содержащей по меньшей мере одно соединение общей формулы I.
Кроме того, третьим объектом настоящего изобретения является способ получения соединения общей формулы I, указанный способ является простым, характеризуется высоким выходом и включает небольшое количество стадий и поэтому является экономичным.
Наконец, последним объектом настоящего изобретения является применение по меньшей мере одного соединения общей формулы I в качестве обладающего запахом компонента.
Насколько известно заявителю, ранее не было выявлено ни одно из соединений, описывающихся следующей общей формулой I.
Некоторые ацетали 1-(3,3-диметилциклогексил)этанона описаны в заявке на патент EP 0472966, в частности, 2-(3,3-диметилциклогексил)-2,4-диметил-1,3-диоксолан и 2-(3,3-диметилциклогексил)-2,4,4-триметил-1,3-диоксолан). Однако указанные производные описаны просто в качестве промежуточных продуктов для синтеза и с ними не связано описание запахов.
Кроме того, в предшествующем уровне техники описаны другие ацетали, представленные ниже, такие как каранал® (гиваудан, Switzerland) или 5-втор-бутил-2-(2,4-диметилциклогекс-3-енил)-5-метил-1,3-диоксан (EP 0276998), исамбер K® (Dragoco, Japan) или спиро[1,3-диоксолан-2,8'(5'h)-[2h-2,4a]метанонафталин] (EP 543470), или даже амберкетал® (Firmenich, Switzerland), или додекагидро-3,8,8,11a-тетраметил-5h-3,5a-эпоксинафт[2,1-c]оксепин (US 3144465).

Однако эти соединения обладают, с одной стороны химической структурой, сильно отличающейся от структуры соединений, предлагаемых в настоящем изобретении, и, с другой стороны, амбровыми нотами, связанными с древесными нотами. Аналогичным образом, кетоны формулы I, являющиеся объектом патента FR-B-2259091, такие как соединение 1-(3,3-диметилциклогекс-1-ен-1-ил)-1,1-этилендиоксипент-4-ен) и некоторые его ацетали, также обладают химической структурой, сильно отличающейся от структуры соединений, предлагаемых в настоящем изобретении, и также обладают древесной нотой. С другой стороны, соединения, предлагаемые в настоящем изобретении, характеризуются тем преимуществом, что обладают животными или амбровыми нотами, не включающими древесный аспект.
Поэтому объектом настоящего изобретения является соединение следующей общей формулы I:
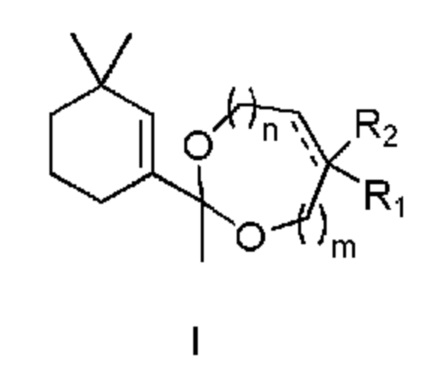
в которой:
- m и n означают количество атомов углерода (метиленовых групп) и все независимо равны 0 или 1;
- R1 означает атом водорода или насыщенную C1-C2-алкильную группу;
- углерод-углеродная связь, представленная штриховой линией, присутствует или отсутствует и
если указанная связь отсутствует, то R2 присутствует и означает атом водорода или насыщенную C1-C2-алкильную группу,
если указанная связь присутствует, то R2 отсутствует;
указанное соединение находится в форме стереоизомера, смеси стереоизомеров или рацемической смеси.
Как отмечено выше, в предпочтительном варианте осуществления m и n означают количество групп -CH2- и все независимо равны 0 или 1.
В числе терминов, использующихся в настоящем изобретении, термин "C1-C2-алкил" означает любой одновалентный радикал, образованный из насыщенной линейной углеводородной цепи, содержащей 1 или 2 атома углерода, т. е. метильную или этильную группу.
В первом варианте осуществления углерод-углеродная связь, представленная штриховой линией, отсутствует. Предпочтительно, если n равно 0 и m равно 1.
В другом предпочтительном варианте осуществления n и m равны 0.
В заключительном варианте осуществления группы R1 и R2 представляют собой C1-C2-алкильную группу.
Еще более предпочтительно, если соединение, предлагаемое в настоящем изобретении, выбрано из группы, включающей 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолан, 2-(3,3-диметилциклогекс-1-енил)-2,4-диметил-1,3-диоксолан, 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-2,5-диметил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-5,5-диэтил-2-метил-1,3-диоксан и 2-(3,3-диметилциклогекс-1-енил)-2-метил-4,7-дигидро-1,3-диоксепин.
Наличие центров асимметрии в структуре соединений формулы I, предлагаемых в настоящем изобретении, для каждого соединения приводит к существованию нескольких энантиомерных и/или диастереоизомерных форм. В объем настоящего изобретения также входят соединения, описывающиеся общей формулой I, в виде смесей энантиомеров и/или диастереоизомеров в разных соотношениях, в частности, рацемических смесей. В объем настоящего изобретения также входят соединения формулы I в форме одного энантиомера и/или диастереоизомера. Смеси энантиомеров/диастереоизомеров или чистые формы можно получить с помощью синтеза из оптически обогащенных или оптически чистых исходных веществ, или с помощью методик разделения посредством кристаллизации или хроматографии.
Вторым объектом настоящего изобретения является композиция, содержащая по меньшей мере одно соединение общей формулы I, определенное выше. Вследствие приятного запаха, который они распространяют, соединения, предлагаемые в настоящем изобретении, обладают многочисленными вариантами применения в парфюмерии. Термин "парфюмерия" используется в настоящем изобретении в его общем смысле; он означает не только традиционную парфюмерию (на основе спирта или на другой основе), но и другие области, для которых важен запах продуктов. Так, можно указать парфюмерные композиции в обычном и традиционном смысле (такие как парфюмерные основы и концентраты, духи, одеколоны, туалетную воду, дезодоранты для освежения воздуха в помещениях, отдушки для помещений, ароматизированные свечи и аналогичные продукты), композиции для местного применения, в частности, косметические (такие как кремы для лица и/или тела, тальковые пудры, масла для волос, шампуни, лосьоны для волос, соли и масла для ванны, гели для душа и/или ванны, туалетные мыла, средство от пота и дезодоранты для тела, лосьоны и кремы для бритья, мыла, зубные пасты, жидкости для полоскания рта, помады и аналогичные продукты), а также продукты для очистки, в частности, бытовые продукты (такие как моющие средства, стиральные порошки, смягчители, дезодоранты для освежения воздуха в помещениях, отдушки для помещений и аналогичные продукты).
Таким образом, настоящее изобретение относится к парфюмерной композиции, содержащей по меньшей мере одно соединение, предлагаемое в настоящем изобретении. В частности, она может быть традиционной парфюмерной композицией, косметической композицией, продуктом для очистки или даже так называемой "промежуточной композицией", предназначенной для использования для получения композиций или готовых продуктов (в особенности парфюмерных продуктов, косметических продуктов, продуктов для очистки).
Такую ароматизированную композицию обычно готовят из базового продукта, в который включено (включены) соединение (соединения), предлагаемое в настоящем изобретении. Базовый продукт должен легко определить специалист в данной области техники в зависимости от получаемой композиции и поэтому от назначения. Составы этих базовых продуктов и природа их обычных компонентов, таких как растворитель (растворители) и/или добавка (добавки), хорошо известны специалисту в данной области техники.
Соединения-компоненты этих ароматизированных композиций, в частности, соединения, предлагаемые в настоящем изобретении, можно включить в инертный материал подложки или нанести на него. Материалы подложки, которые можно использовать, являются многочисленными и разными, например, полярные растворители, масла, смазки, тонкоизмельченные твердые вещества, циклодекстрины, мальтодекстрины, камеди, смолы и любой другой материал подложки, для которого известно его применение для таких композиций (например, мыла, свечи, помады, текстильные изделия, полотенца, ароматизированные гели...).
Предпочтительно, если композиция, предлагаемая в настоящем изобретении, содержит по меньшей мере одно соединение, выбранное из группы, включающей 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолан, 2-(3,3-диметилциклогекс-1-енил)-2,4-диметил-1,3-диоксолан, 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-2,5-диметил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-5,5-диэтил-2-метил-1,3-диоксан и 2-(3,3-диметилциклогекс-1-енил)-2-метил-4,7-дигидро-1,3-диоксепин.
Эффективное количество соединений, предлагаемых в настоящем изобретении, предназначенное для включения в эти композиции, зависит от природы указанных композиций, запаха, который желательно придать, и природы любых других содержащихся душистых соединений. Его должен легко определить специалист в данной области техники и оно может меняться в очень широком диапазоне, составляющем от 0,1 до 99%, предпочтительно от 0,1 до 50%, более предпочтительно от 0,1 до 30 мас.% в пересчете на полную массу композиции. Приведенные выше содержания в процентах указаны в пересчете на полную массу композиции.
В заключительном предпочтительном варианте осуществления композиция характеризуется тем, что она дополнительно содержит по меньшей мере один другой обладающий запахом компонент/душистое вещество. Обладающие запахом компоненты/душистые вещества, которые можно использовать в комбинации с соединениями, предлагаемыми в настоящем изобретении, могут представлять собой натуральные продукты, такие как экстракты, эфирные масла, абсолю, резиноиды, смолы, конкреты и т. п., а также продукты синтеза, такие как углеводороды, спирты, альдегиды, кетоны, простые эфиры, кислоты, сложные эфиры, ацетали, нитрилы и т. п., в частности, насыщенные или ненасыщенные, алифатические, гетероциклические или карбоциклические соединения. Такие обладающие запахом компоненты/душистые вещества указаны, например, в публикациях S. Arctander, "Perfume and Flavor Chemicals" (Montclair, N.J., 1969), или в "Common Fragrance and Flavor Materials", Wiley-VCH, Weinheim, 2006. Кроме того, некоторые соединения, предлагаемые в настоящем изобретении, также можно использовать в комбинации в одной композиции.
Третьим объектом настоящего изобретения является способ синтеза соединений формулы I, определенных выше.
Указанные способ является эффективным, поскольку он позволяет использовать сырье, имеющееся в больших количествах, проводить реакцию в мягких условиях, легко адаптируемых к имеющимся производственным линиям, а также заменять реагенты, которые могут нанести вред здоровью или окружающей среде при промышленном применении.
Соединения, предлагаемые в настоящем изобретении, получают способом, включающим следующие стадии:
a) циклизация/перегруппировка дегидролиналоола с помощью кислоты с получением 1-(3,3-диметилциклогекс-1-енил)этанона и;
b) ацеталирование 1-(3,3-диметилциклогекс-1-енил)этанона с помощью диола с получением соединения формулы I.
Дегидролиналоол (DE 1643710) является недорогим, легко доступным сырьем, что обеспечивает простое приготовление, согласующееся с требованиями промышленности. Предпочтительно, если реакцию циклизации/перегруппировки дегидролиналоола проводят путем добавления кислоты, выбранной из группы, включающей фосфорную кислоту или метансульфоновую кислоту, и получают 1-(3,3-диметилциклогекс-1-енил)этанон.
Стадию b) способа, предлагаемого в настоящем изобретении, проводят путем добавления диола к соединению, полученному на стадии a), а именно, к 1-(3,3-диметилциклогекс-1-енил)этанону. Предпочтительно, если диол выбран из группы, включающей этиленгликоль, неопентилгликоль, 1,2-пропандиол, 2,2-диэтил-1,3-пропандиол, 2-метил-1,3-пропандиол, 1,3-пропандиол или даже цис-2-бутен-1,4-диол. Эту стадию ацеталирования проводят в присутствии триэтилортоформиата и небольшого количества кислоты, которая выступает в качестве катализатора и обладает тем преимуществом, что ее можно регенерировать (следовательно, уменьшить затраты способа). Небольшое количество означает количество, эквивалентное 1% массы 1-(3,3-диметилциклогекс-1-енил)этанона, введенного в реакционную среду. Например, пара-толуолсульфоновая кислота является кислотой применимой для этой стадии b).
Благоприятно, что стадию b) способа можно провести с использованием непосредственно дегидрогербака. Обычно название "дегидрогербак" означает смесь изомеров 1-(3,3-диметилциклогекс-1-енил)этанон и 1-(3,3-диметилциклогекс-6-енил)этанона (US 4264467), несущественно, каково относительно содержание этих 2 изомеров.
Чистые формы этих изомеров можно получить из дегидрогербака с помощью хорошо известных методик разделения, таких как разделение с помощью кристаллизации и/или хроматографии. Также можно использовать в качестве исходного вещества смеси дегидрогербака; в этом случае реакция будет протекать только с одним изомером, 1-(3,3-диметилциклогекс-1-енил)этаноном, с изомером 1-(3,3-диметилциклогекс-6-енил)этанон реакция протекает очень медленно.
Таким образом, способ, предлагаемый в настоящем изобретении, обладает тем преимуществом, что его проводят без растворителя, а также без воды вследствие использования триэтилортоформиата, проводят при температуре окружающей среды в течение нескольких часов и в конечном счете он обеспечивает выход, равный от 70% до 80%.
Наконец, последним объектом настоящего изобретения является применение по меньшей мере одного соединения формулы I, предлагаемого в настоящем изобретении, в качестве обладающего запахом компонента или соединения, в качестве маскирующего запах компонента или в качестве нейтрализующего запах компонента. Термин "обладающий запахом" используется в настоящем изобретении для указания на любое органолептическое соединение, приятно стимулирующее ощущение запаха. Термин "маскирующий компонент" или "маскирующий" означает ослабляющий или исключающий ощущение плохого запаха, распространяющегося одной или большим количеством молекул-компонентов продукта.
Кроме того, указанное соединение можно использовать по отдельности или в комбинации по меньшей мере с одним другим обладающим запахом компонентом/одним другим душистым веществом и/или по меньшей мере с одним растворителем, и/или по меньшей мере с одной добавкой. Дополнительный обладающий запахом/душистый компонент(ы), растворитель (растворители) и добавка (добавки) известны специалисту в данной области техники, который должен уметь выбрать наиболее подходящий (подходящие) в зависимости от желательного эффекта.
Предпочтительный вариант осуществления настоящего изобретения относится к применению соединения формулы I для изменения или улучшения органолептических характеристик вещества, композиции или продукта.
"Органолептические характеристики" означают любую характеристику, способную изменить, улучшить или усилить органолептическое восприятие вещества, композиции или продукта пользователем. Таким образом, в качестве предпочтительного примера органолептический компонент, предлагаемый в настоящем изобретении, может включать ароматизирующую добавку, способную придать, изменить, улучшить или усилить органолептическое восприятие вещества, композиции или продукта.
Приведенные ниже примеры иллюстрируют конкретную методику получения соединений, предлагаемых в настоящем изобретении, а также обонятельный профиль каждого из приведенных в качестве примеров соединений. Эти примеры приведены только для иллюстративных целей и их не следует рассматривать в качестве ограничивающих общий объем настоящего изобретения.
Пример 1: Получение 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолана.
В колбе в толуол помещают эквивалент дегидролиналоола. Этот раствор кипятят с обратным холодильником. Затем медленно по каплям добавляют фосфорную кислоту (10% от массы дегидролиналоола). После 20 ч перемешивания при кипячении с обратным холодильником и охлаждения до температуры окружающей среды реакционную смесь выливают в насыщенный водный раствор бикарбоната натрия. Фазы разделяют. Органическую фазу промывают водой до нейтральной реакции. После сушки над сульфатом магния, фильтрования и выпаривания растворителя, неочищенный продукт перегоняют при пониженном давлении: его температура кипения равна 52°C при давлении, равном 53,3 Па.
Полученный таким образом 1-(3,3-диметилциклогекс-1-енил)этанон помещают в 4 экв. этиленгликоля и 2 экв. триэтилортоформиата. При температуре окружающей среды добавляют пара-толуолсульфоновую кислоту (1% от массы введенного 1-(3,3-диметилциклогекс-1-енил)этанона). Реакционную смесь при перемешивании выдерживают в этих условиях в течение 20 ч и затем выливают в насыщенный водный раствор бикарбоната натрия. Эту водную фазу дважды экстрагируют циклогексаном. Объединенные органические фазы промывают водой до нейтральной реакции. После сушки над сульфатом магния, фильтрования и концентрирования неочищенный продукт перегоняют при пониженном давлении: его температура кипения равна 46°C при давлении, равном 53,3 Па.
Описание запахов: животный, амбровый, ароматический, терпеновый.
Полученный таким образом 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолан обладает следующими спектральными характеристиками:
1H-ЯМР (200 МГц, CDCl3): δ (част./млн) 0,94 (s, 6H), 1,34-1,37 (m, 2H), 1,41 (s, 3H), 1,57-1,61 (m, 2H), 1,91 (td, J=6,2 Гц, 1,6 Гц, 2H), 3,70-3,85 (m, 2H), 3,85-3,95 (m, 2H), 5,56 (s, 1H).
13C-ЯМР (50 МГц, CDCl3): δ (част./млн) 19,85, 23,76, 23,96, 29,92, 31,34, 36,95, 64,18, 109,31, 132,60, 134,75.
МС [e/m (%)]: 196 (M+, 0,2), 181 (100), 109 (21), 87 (82), 73 (14), 43 (32).
ИК (пленка, см-1): 859m, 946w, 1043s, 1110w, 1187m, 1209m, 1371w, 2933m.
Пример 2: Получение 2-(3,3-диметилциклогекс-1-енил)-2,4-диметил-1,3-диоксолана
2-(3,3-Диметилциклогекс-1-енил)-2,4-диметил-1,3-диоксолан получают по методике, описанной в примере 1, с использованием 1,2-пропандиола вместо этиленгликоля. Неочищенный продукт, полученный из 2-(3,3-диметилциклогекс-1-енил)-2,4-диметил-1,3-диоксолана, в форме двух диастереоизомеров в соотношении 62:38, перегоняют при пониженном давлении: его температура кипения равна 49°C при давлении, равном 66,7 Па.
Описание запахов: животный, камфорный.
Полученный таким образом 2-(3,3-диметилциклогекс-1-енил)-2,4-диметил-1,3-диоксолан обладает следующими спектральными характеристиками:
Содержащийся в наибольшем количестве изомер (62%):
1H-ЯМР (200 МГц, CDCl3): δ (част./млн) 0,93 (s, 6H), 1,25 (d, J=6,1 Гц, 3H), 1,33-1,38 (m, 2H), 1,42 (s, 3H), 1,59-1,61 (m, 2H), 1,88-1,95 (m, 2H), 3,37-3,42 (m, 1H), 3,86-3,90 (m, 1H), 4,02-4,08 (m, 1H), 5,55 (s, 1H).
13C-ЯМР (50 МГц, CDCl3): δ (част./млн) 18,99, 19,87, 24,00, 24,71, 29,92, 29,96, 31,31, 36,98, 70,58, 71,48, 109,56, 132,28, 135,11.
МС [e/m (%)]: 210 (M+, 0,3), 195 (100), 137 (24), 109 (34), 101 (998), 93 (10), 91 (14), 81 (11), 79 (15), 76 (15), 67 (16), 43 (64), 41 (16).
Содержащийся в наименьшем количестве изомер (32%):
1H-ЯМР (200 МГц, CDCl3): δ (част./млн) 0,94 (s, 6H), 1,22 (d, J=6,1 Гц, 3H), 1,33-1,38 (m, 2H), 1,39 (s, 3H), 1,59-1,61 (m, 2H), 1,88-1,95 (m, 2H), 3,28-3,33 (m, 1H), 4,00-4,04 (m, 1H), 4,18-4,25 (m, 1H), 5,60 (s, 1H).
13C-ЯМР (50 МГц, CDCl3): δ (част./млн) 18,35, 19,83, 24,00, 24,24, 29,80, 29,87, 31,35, 36,98, 70,92, 72,40, 109,50, 132,54, 136,30.
МС [e/m (%)]: 210 (M+, 0,3), 195 (100), 137 (25), 109 (33), 101 (58), 91 (13), 81 (11), 79 (14), 76 (14), 66 (14), 43 (54), 41 (15).
ИК (пленка, см-1): 866m, 937w, 953w, 1038s, 1085s, 1187s, 1210s, 1370m, 2930m.
Пример 3: Получение 2-(3,3-диметилциклогекс-1-енил)-2,5-диметил-1,3-диоксана
2-(3,3-Диметилциклогекс-1-енил)-2,5-диметил-1,3-диоксан получают по методике, описанной в примере 1, с использованием 2-метил-1,3-пропандиола вместо этиленгликоля. Неочищенный продукт, полученный из 2-(3,3-диметилциклогекс-1-енил)-2,5-диметил-1,3-диоксана, перегоняют при пониженном давлении: его температура кипения равна 46°C при давлении, равном 26,7 Па.
Описание запахов: амбровый, зелени, красноплодный.
Полученный таким образом 2-(3,3-диметилциклогекс-1-енил)-2,5-диметил-1,3-диоксан обладает следующими спектральными характеристиками:
1H-ЯМР (200 МГц, CDCl3): δ (част./млн) 0,64 (d, J=6,7 Гц, 3H), 0,85-1,06 (m, 1H), 0,98 (s, 6H), 1,32 (s, 3H), 1,41-1,43 (m, 2H), 1,61-1,65 (m, 2H), 1,84 (t, J=6,7 Гц, 1H), 1,97-2,07 (m, 1H), 3,26-3,34 (m, 2H), 3,63-3,68 (m, 2H), 5,56 (s, 1H).
13C-ЯМР (50 МГц, CDCl3): δ (част./млн) 12,60, 20,05, 24,52, 28,69, 28,87, 29,91, 31,82, 37,08, 67,41, 100,23, 132,70, 136,17.
МС [e/m (%)]: 224 (M+, 0,2), 209 (54), 137 (22), 121 (10), 115 (100), 109 (22), 93 (14), 91 (13), 79 (15), 77 (12), 67 (11), 55 (26), 43 (41), 41 (14).
ИК (пленка, см-1): 860m, 1034m, 1052m, 1100m, 1121m, 1162s, 1181s, 1225m, 1368w, 1457w, 2862w, 2930m, 2952m.
Пример 4: Получение 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксана
2-(3,3-Диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан получают по методике, описанной в примере 1, с использованием неопентилгликоля вместо этиленгликоля. Неочищенный продукт, полученный из 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксана, перегоняют при пониженном давлении: его температура кипения равна 68°C при давлении, равном 26,7 Па.
Описание запахов: амбровый, мускусный, красноплодный.
Полученный таким образом 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан обладает следующими спектральными характеристиками:
1H-ЯМР (200 МГц, CDCl3): δ (част./млн) 0,67 (s, 3H), 0,98 (s, 6H), 1,17 (s, 3H), 1,35 (s, 3H), 1,39-1,43 (m, 2H), 1,61-1,65 (m, 2H), 1,85 (t, J=6,1 Гц, 2H), 3,25-3,28 (m, 2H), 3,42-3,50 (m, 2H), 5,56 (s, 1H).
13C-ЯМР (50 МГц, CDCl3): δ (част./млн) 20,05, 22,15, 22,70, 24,42, 28,07, 29,51, 29,94, 31,79, 37,09, 71,41, 100,29, 132,63, 135,89.
МС [e/m (%)]: 238 (M+, 0,4), 223 (45), 137 (20), 129 (100), 109 (24), 93 (15), 91 (14), 81 (12), 79 (14), 77 (12), 69 (28), 67 (14), 55 (13), 43 (57), 41 (24).
ИК (пленка, см-1): 859m, 1013m, 1039m, 1083s, 1121m, 1174s, 1207w, 1239w, 1369w, 1470w, 2864w, 2951m.
Пример 5: Получение 2-(3,3-диметилциклогекс-1-енил)-5,5-диэтил-2-метил-1,3-диоксана
2-(3,3-Диметилциклогекс-1-енил)-5,5-диэтил-2-метил-1,3-диоксан получают по методике, описанной в примере 1, с использованием 2,2-диэтил-1,3-пропандиола вместо этиленгликоля. Неочищенный продукт, полученный из 2-(3,3-диметилциклогекс-1-енил)-5,5-диэтил-2-метил-1,3-диоксана, перегоняют при пониженном давлении: его температура кипения равна 78°C при давлении, равном 40,0 Па.
Описание запахов: слабый животный.
Полученный таким образом 2-(3,3-диметилциклогекс-1-енил)-5,5-диэтил-2-метил-1,3-диоксан обладает следующими спектральными характеристиками:
1H-ЯМР (200 МГц, CDCl3): δ (част./млн) 0,72 (t, J=7,5 Гц, 3H), 0,72 (t, J=7,6 Гц, 3H), 0,98 (s, 6H), 0,98-1,05 (m, 1H), 1,26-1,32 (m, 1H), 1,32 (s, 3H), 1,32-1,42 (m, 2H), 1,58-1,73 (m, 4H), 1,82-1,87 (m, 2H), 3,36-3,45 (m, 4H), 5,56 (s, 1H).
13C-ЯМР (50 МГц, CDCl3): δ (част./млн) 6,61, 7,50, 20,05, 22,58, 24,42, 24,48, 27,97, 29,93, 31,76, 34,22, 37,10, 68,38, 100,47, 132,79, 135,79.
МС [e/m (%)]: 208 (M+, 0,1), 134 (19), 133 (46), 132 (17), 121 (11), 119 (13), 110 (11), 109 (10), 108 (13), 107 (17), 97 (17), 96 (10), 95 (13), 93 (23), 92 (11), 91 (34), 81 (26), 80 (10), 79 (35), 77 (14), 67 (28), 57 (100), 55 (23), 53 (11), 41 (49), 39 (12).
ИК (пленка, см-1): 838w, 1365m, 1459m, 1726s, 2715w, 2866m, 2928s, 2951s.
Пример 6: Получение 2-(3,3-диметилциклогекс-1-енил)-2-метил-4,7-дигидро-1,3-диоксепина
2-(3,3-Диметилциклогекс-1-енил)-2-метил-4,7-дигидро-1,3-диоксепин получают по методике, описанной в примере 1, с использованием цис-2-бутен-1,4-диола вместо этиленгликоля. Неочищенный продукт, полученный из 2-(3,3-диметилциклогекс-1-енил)-2-метил-4,7-дигидро-1,3-диоксепина, перегоняют при пониженном давлении: его температура кипения равна 75°C при давлении, равном 53,3 Па.
Описание запахов: амбровый, пряный, мускатного ореха, ладана.
Полученный таким образом 2-(3,3-диметилциклогекс-1-енил)-2-метил-4,7-дигидро-1,3-диоксепин обладает следующими спектральными характеристиками:
1H-ЯМР (200 МГц, CDCl3): δ (част./млн) 0,98 (s, 6H), 1,37-1,41 (m, 2H), 1,38 (s, 3H), 1,58-1,66 (m, 2H), 1,91-1,96 (m, 2H), 4,10-4,26 (m, 4H), 5,65 (t, J=1,1, 2H), 5,76 (s, 1H).
13C-ЯМР (50 МГц, CDCl3): δ (част./млн) 19,98, 22,41, 24,44, 30,06, 31,55, 37,08, 61,49, 103,40, 129,63, 133,88, 134,33.
МС [e/m (%)]: 222 (M+, 0,1), 207 (15), 154 (33), 152 (22), 137 (58), 109 (62), 93 (14), 91 (14), 81 (18), 79 (16), 77 (14), 70 (10), 69 (13), 67 (27), 55 (14), 53 (13), 43 (100), 42 (19), 41 (38), 39 (29).
ИК (пленка, см-1): 613m, 625m, 640m, 787m, 877m, 949m, 1049s, 1082s, 1117m, 1153s, 1200w, 1231m, 1280m, 1371m, 1451w, 2861w, 2930m.
Пример 7: Парфюмерная композиция, содержащая производные, полученные в примерах 1 и 4
К розовому аккорду, полученному в соответствии с приведенной ниже таблицей (аккорд A), добавляют 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан (пример 4, аккорды B и C) и 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолан (пример 1, аккорд D).
Обычно добавление молекул усиливает аккорд, делая его более сильным.
Добавление 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолана (пример 1, аккорд D) создает ароматический, камфорный эффект (нота розы менее богатая), а добавление производного 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксана (пример 4, аккорды B и C) усиливает ноту розы, придавая ей привлекательное натуральное звучание.
В заключение аккорды B и C являются более пряными, коричными, сладкими. Однако аккорд C является сухим древесным/амбровым, нота является менее розовой, чем при использовании аккорда B (менее сбалансированной), но сухой древесный хорошо соответствует композиции, придавая силу и цветочно-древесную ноту с очень приятным бальзамическим эффектов.
Пример 8: Парфюмерная композиция, содержащая производные, полученные в примерах 1 и 4
К яблочному аккорду, полученному в соответствии с приведенной ниже таблицей (аккорд A), добавляют 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан (пример 4, аккорды B и C) и 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолан (пример 1, аккорд D).
Обычно добавление молекул усиливает аккорд, делая его более сильным и более натуральным.
Добавление 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолана (пример 1, аккорд D) создает натуральный яблочный с отшелушиванием подкисляющий эффект.
Добавление производного, 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксана (пример 4, аккорды B и C), создает фруктовый, приторный эффект свежести.
Пример 9: Парфюмерная композиция, содержащая производное, полученное в примере 4
К древесному аккорду, полученному в соответствии с приведенной ниже таблицей (аккорд A), добавляют 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан (пример 4, аккорд B).
Аккорд B, порошкообразный, является немного менее ванильным, более древесным и мужским.
Изобретение относится к ацеталям 1-(3,3-диметилциклогекс-1-енил)этанона формулы I, обладающим животными или амбровыми нотами без какого-либо древесного аспекта, способу их получения, парфюмерной композиции на их основе, а также их применению в парфюмерии. В общей формуле I m и n означают количество атомов углерода и все независимо равны 0 или 1; R1 означает атом водорода или насыщенную C1-C2-алкильную группу; углерод-углеродная связь, представленная штриховой линией, присутствует или отсутствует, и если указанная связь отсутствует, то R2 присутствует и означает атом водорода или насыщенную C1-C2-алкильную группу, если указанная связь присутствует, то R2 отсутствует. 4 н. и 13 з.п. ф-лы, 8 пр.
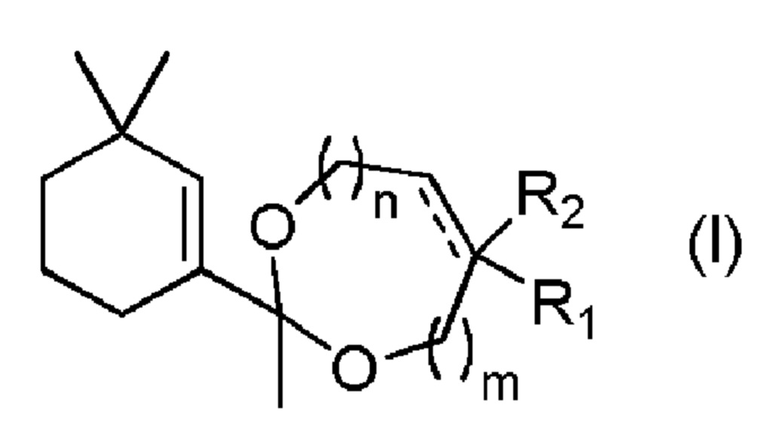
1. Соединение следующей общей формулы I:
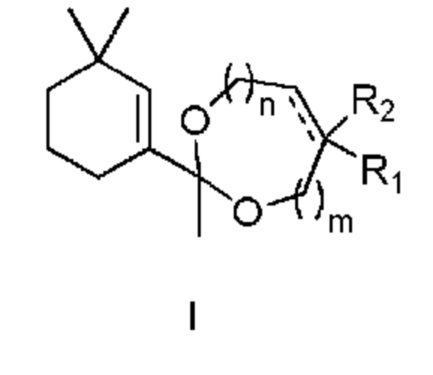
в которой:
- m и n означают количество атомов углерода и все независимо равны 0 или 1;
- R1 означает атом водорода или насыщенную C1-C2-алкильную группу;
- углерод-углеродная связь, представленная штриховой линией, присутствует или отсутствует, и
если указанная связь отсутствует, то R2 присутствует и означает атом водорода или насыщенную C1-C2-алкильную группу,
если указанная связь присутствует, то R2 отсутствует;
указанное соединение находится в форме стереоизомера, смеси стереоизомеров или рацемической смеси.
2. Соединение по п. 1, в котором указанная углерод-углеродная связь, представленная штриховой линией, отсутствует.
3. Соединение по п. 1, в котором n равно 0 и m равно 1.
4. Соединение по п. 1, в котором n и m равны 0.
5. Соединение по любому из пп. 1-4, в котором R1 и R2 означают насыщенную C1-C2-алкильную группу.
6. Соединение по любому из предыдущих пунктов, указанное соединение выбрано из группы, включающей 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолан, 2-(3,3-диметилциклогекс-1-енил)-2,4-диметил-1,3-диоксолан, 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-2,5-диметил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-5,5-диэтил-2-метил-1,3-диоксан и 2-(3,3-диметилциклогекс-1-енил)-2-метил-4,7-дигидро-1,3-диоксепин.
7. Парфюмерная композиция, содержащая эффективное количество по меньшей мере одного соединения следующей общей формулы I:

в которой:
- m и n означают количество атомов углерода и все независимо равны 0 или 1;
- R1 означает атом водорода или насыщенную C1-C2-алкильную группу;
- углерод-углеродная связь, представленная штриховой линией, присутствует или отсутствует, и
если указанная связь отсутствует, то R2 присутствует и означает атом водорода или насыщенную C1-C2-алкильную группу,
если указанная связь присутствует, то R2 отсутствует;
указанное соединение находится в форме стереоизомера, смеси стереоизомеров или рацемической смеси,
и инертный материал подложки.
8. Композиция по п. 7, указанная композиция содержит по меньшей мере одно соединение, выбранное из группы, включающей 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксолан, 2-(3,3-диметилциклогекс-1-енил)-2,4-диметил-1,3-диоксолан, 2-(3,3-диметилциклогекс-1-енил)-2-метил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-2,5-диметил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-2,5,5-триметил-1,3-диоксан, 2-(3,3-диметилциклогекс-1-енил)-5,5-диэтил-2-метил-1,3-диоксан и 2-(3,3-диметилциклогекс-1-енил)-2-метил-4,7-дигидро-1,3-диоксепин.
9. Композиция по п. 7 или 8, в которой указанное соединение представляет собой обладающий запахом компонент; указанная композиция дополнительно содержит по меньшей мере один другой обладающий запахом компонент.
10. Композиция по любому из пп. 7-9, в которой соединение общей формулы I содержится в концентрации, равной от 0,01 до 99 мас.% в пересчете на полную массу композиции, более предпочтительно от 0,1 до 30 мас.% в пересчете на полную массу композиции.
11. Композиция по одному из пп. 7-10, указанная композиция является парфюмерной композицией.
12. Способ получения соединения общей формулы I по одному из пп. 1-6, указанный способ включает следующие стадии:
a) циклизация/перегруппировка дегидролиналоола с помощью кислоты с получением 1-(3,3-диметилциклогекс-1-енил)этанона и
b) ацеталирование 1-(3,3-диметилциклогекс-1-енил)этанона с помощью диола с получением соединения общей формулы I.
13. Способ по п. 12, в котором кислота на стадии a) выбрана из группы, включающей фосфорную кислоту и метансульфоновую кислоту.
14. Способ по одному из пп. 12 или 13, в котором диол на стадии b) выбран из группы, включающей этиленгликоль, неопентилгликоль, 1,2-пропандиол, 2,2-диэтил-1,3-пропандиол, 2-метил-1,3-пропандиол, 1,3-пропандиол или цис-2-бутен-1,4-диол.
15. Применение по меньшей мере одного соединения общей формулы I по одному из пп. 1-6 в качестве обладающего запахом компонента.
16. Применение по п. 15, в котором указанное соединение общей формулы I используют в комбинации по меньшей мере с одним другим обладающим запахом компонентом, и/или по меньшей мере с одним растворителем, и/или по меньшей мере с одной добавкой.
17. Применение по одному из пп. 15 или 16 для придания, изменения или улучшения органолептических характеристик вещества, композиции или продукта.
| СПОСОБ ПОЛУЧЕНИЯ САЖИСТОГО ЖЕЛЕЗА | 2006 |
|
RU2322511C1 |
| WO 2001085713 A1, 15.11.2001 | |||
| WO 2010122451 A1, 28.10.2010 | |||
| СПОСОБ ПРОИЗВОДСТВА ЖЕЛЕЙНОГО МАРМЕЛАДА | 2003 |
|
RU2259091C2 |
| US 6348618 B1, 19.02.2002 | |||
| Этиленацеталь -толилпропинового альдегида в виде смеси о- и п-изомеров в качестве душистого вещества | 1977 |
|
SU644773A1 |
Авторы
Даты
2020-04-15—Публикация
2015-12-14—Подача