Область техники, к которой относится изобретение
Настоящее изобретение относится к способу диагностики карциномы предстательной железы, включающему определение аннексина A3 (ANXA3) и/или аутоантител против аннексина A3 с использованием специфического реагента. Этот способ позволяет различать доброкачественное, предраковое и злокачественное (рак) состояния. Данный способ также имеет прогнозное значение.
Уровень техники
Ранее при количественном исследовании дифференцированной экспрессии белков было показано, что аннексин A3 в значительной степени ассоциирован с раком предстательной железы (1). Однако мало что известно о биологической роли аннексина A3 в предстательной железе у человека. К настоящему времени показано, что аннексин A3 является частью так называемых экзосом - небольших везикул, высвобождающихся из различных эпителиальных структур (2), и что эти экзосомы играют какую-то неясную роль в регуляции врожденной иммунной системы (3), а недавно обнаружено, что они обладают противоопухолевой активностью (4). В последних публикациях сообщалось об аутоиммунной атаке так называемых простасом - экзосом из предстательной железы (5).
Белковые биологические маркеры для лечения и диагностики рака предстательной железы и других раковых поражений эпителиальных структур мочеполового тракта описаны в патенте США 2005130876 и публикациях WO 03086461, WO 2005078124, EP 05011042.8, EP 05026092.6. Содержание этих документов включено в настоящий документ путем отсылки. В патентах США 60/812,089 и 60/859,489 раскрывается диагностика рака, при которой в образце определяют присутствие и/или количество аннексина A3 при помощи высокоспецифичных моноклональных антител. Содержание этих документов включено в настоящий документ путем отсылки.
Хотя аннексин A3 известен как маркер рака предстательной железы, есть нужда в усовершенствованных методах дифференциальной диагностики, позволяющей различить доброкачественное, предраковое и злокачественное (рак) состояния.
Раскрытие изобретения
Одной из целей настоящего исследования было изучение экспрессии и локализации аннексина A3 в эпителиальных компонентах при доброкачественном состоянии эпителия предстательной железы, при простатической интраэпителиальной неоплазии высокой степени и при раке предстательной железы, а также выяснение различий и изменений локализации в ходе трансформации предстательной железы.
По данному изобретению было обнаружено, что при помощи антител к аннексину A3 доброкачественная ткань предстательной железы окрашивается интенсивно в апикальной области, тогда как при раке предстательной железы окрашивание слабее и смещено к базальной области. Изучение серийных срезов ткани в более чем 1900 случаях показало, что картина экспрессии аннексина A3 в доброкачественной, предраковой и злокачественной (раковой) ткани предстательной железы различна, имея прогностическое значение и обеспечивая механистическое понимание.
При далеко зашедшем раке предстательной железы присутствие аннексина A3 наблюдалось в разбросанных неэпителиальных клетках, совпадая по локализации с контрастным окрашиванием на регуляторные Т-клетки (Tregs). Также у больных раком предстательной железы может выявляться присутствие аутоантител против аннексина A3. Эти аутоантитела против аннексина A3, вероятно, индуцируются при оксидативном (окислительном) стрессе в раковых клетках. Это служит доказательством того, что высвобождение аннексина A3 через экзосомы представляет защитный механизм, который у больных раком предстательной железы раковые клетки «стараются» обратить вспять, вызывая аутоиммунную реакцию против простасом, содержащих аннексии A3. Таким образом, сигнальные процессы в регуляторных Т-клетках могут модулироваться ANXA3-экзосомами и/или раковыми клетками. Кроме того, аутоиммунные антитела против простасом/экзосом могут индуцироваться/регулироваться ANXA3-положительными Т-клетками.
Все это вместе взятое убедительно указывает на то, что высвобождение аннексина A3 во внеклеточные компартменты предстательной железы в процессе доброкачественной гиперплазии предстательной железы (ВРН) представляет механизм защиты от рака и что в раковой ткани это высвобождение в конце концов прекращается в результате индукции аутоиммунных антител против аннексина A3 и при помощи механизма с участием регуляторных Т-клеток (Tregs). Также различные паттерны окрашивания на аннексин A3 впервые дают возможность предсказывать выживание без повышения уровня PSA у больных промежуточной группы риска, определенного по шкале Глисона, рТ-стадии и уровню простатического антигена (PSA).
В первом аспекте данное изобретение относится к способу диагностики рака, предпочтительно рака предстательной железы, при котором в образце ткани определяют внутриклеточное распределение аннексина A3.
В следующем аспекте данное изобретение относится к способу диагностики рака, предпочтительно рака предстательной железы, при котором в образце, а именно в образце ткани или жидкости тела, определяют присутствие, количество и/или внутриклеточное распределение аннексина A3 и аутоиммунный ответ на аннексин A3, причем аутоиммунный ответ предпочтительно оценивается по присутствию аутоантител против аннексина A3 и/или присутствию регуляторных Т-клеток.
В следующем аспекте данное изобретение относится к способу диагностики рака, предпочтительно рака предстательной железы, при котором в образце определяют присутствие и/или количество аутоантител против аннексина A3 и (при необходимости) присутствие и/или количество регуляторных Т-клеток.
В еще одном аспекте данное изобретение относится к способу дальнейшего дифференцирования пациентов, причисленных к промежуточной группе риска развития рака предстательной железы, при котором в образцах, взятых у указанных пациентов, определяют присутствие, локализацию и/или количество аннексина A3.
Еще одним аспектом данного изобретения является аналитический реактив для диагностики рака, предпочтительно рака предстательной железы, содержащий (i) реагент для определения аннексина A3 и (ii) реагент для определения аутоантител против аннексина A3 и/или реагент для определения регуляторных Т-клеток.
Еще одним аспектом данного изобретения является аналитический реактив для диагностики рака предстательной железы, содержащий реагент для определения аутоантител против аннексина A3.
К раковым заболеваниям, которые могут быть диагностированы по данному изобретению, принадлежат раковые поражения мочеполового и/или желудочно-кишечного тракта, как, например, рак предстательной железы, мочевого пузыря, почек, мочеиспускательного канала, яичников, матки или толстого кишечника. В частности, это эпителиальный рак. В особенно предпочтительном воплощении данного изобретения это рак предстательной железы.
В одном из предпочтительных воплощений данное изобретение включает дифференциальную диагностику стадии заболевания и/или прогностическую оценку. Например, данное изобретение позволяет проводить дифференциальную диагностику стадий заболевания, выбираемых из:
(i) доброкачественные состояния, в частности доброкачественные состояния предстательной железы, как, например, доброкачественная гиперплазия предстательной железы (ВРН), фиброз и хронический простатит;
(ii) предраковые состояния, как, например, различные стадии интраэпителиальной неоплазии предстательной железы (PIN 1-3), включая интраэпителиальную неоплазию предстательной железы высокой степени (HGPIN), и/или
(iii) злокачественные состояния (рак), например, предстательной железы, в частности далеко зашедший прогрессирующий рак предстательной железы, диагностированный по шкале Глисона или стадиям рТ.
Более предпочтительно, данное изобретение позволяет проводить дифференциальное диагностирование доброкачественных и/или предраковых состояний, с одной стороны, и злокачественных состояний (рака) - с другой.
В одном из предпочтительных воплощений данного изобретения присутствие, количество и/или распределение аннексина A3 определяют в образце, которым может быть образец ткани или жидкости тела. Более предпочтительно, образец является образцом ткани, например срезом ткани или биоптатом предстательной железы. В дальнейшем воплощении определяют внутриклеточное распределение/локализацию аннексина A3 в образце, в качестве которого берут образец ткани, предпочтительно срез ткани или биоптат, например, из предстательной железы. Предпочтительно, внутриклеточную локализацию аннексина A3 определяют в эпителиальных клетках, в частности в эпителиальных клетках предстательной железы. Следует отметить, что присутствие, количество и внутриклеточную локализацию можно определять в одном образце или же в разных образцах, например в образце жидкости тела и в образце ткани того же пациента.
Большое количество аннексина A3 в образце, чему соответствует выраженное окрашивание образца ткани, указывает в основном на доброкачественное состояние. Умеренное/малое количество аннексина A3, чему соответствует слабое/умеренное окрашивание образца ткани, указывает на предраковое состояние или на раннюю/раннюю - промежуточную стадию злокачественного состояния (рака). Отсутствие аннексина A3 в образце указывает на злокачественное состояние, в основном на уже достаточно далеко зашедший рак, на промежуточной или поздней стадии. Также отсутствие аннексина A3 в образце указывает на агрессивный вариант рака предстательной железы, в частности с высоким риском прогрессирования после хирургического лечения, например после радикальной простатэктомии.
Апикальная внутриклеточная локализация аннексина A3, в частности присутствие аннексина A3 в везикулах, находящихся в апикальной части клеток - в экзосомах и/или простасомах, в основном свидетельствует о доброкачественном или предраковом состоянии. Диффузная внутриклеточная локализация аннексина A3, в особенности в сочетании с отсутствием везикул в апикальной части клеток, свидетельствует о злокачественном состоянии (раке).
Наличие аутоиммунного ответа против аннексина A3, т.е. присутствие аутоантител против аннексина A3 и/или присутствие выражение ANXA3-положительных (но внутриклеточно, а не апикально) регуляторных Т-клеток в основном указывает на далеко зашедшее злокачественное состояние (рак).
Настоящее изобретение касается определения полипептидов или клеток в образце. Предпочтительно, это определение включает иммунологические методы, при которых присутствие, количество и/или локализацию того или иного компонента определяют при помощи иммунологических аналитических реактивов (тест-реагентов).
Реагентом для определения аннексина A3 в образце предпочтительно являются антитела, специфичные к аннексину A3, например поли- или моноклональные антитела. Особенно предпочтительны высокоспецифичные моноклональные антитела, описанные в заявках на патент США 60/812089 и 60/859489, которые включены в настоящий документ путем отсылки.
Реагентом для определения аутоантител против аннексина A3 в образце предпочтительно является полипептид ANXA3 или его фрагмент, содержащие эпитопы, узнаваемые аутоантителами. Более предпочтительно, чтобы полипептид ANXA3 был рекомбинантным.
Реагентом для определения регуляторных Т-клеток в образце предпочтительно являются антитела, направленные против маркера регуляторных Т-клеток, например CD25 или Foxp3 или других таких маркеров.
Способ по данному изобретению может осуществляться в любом аналитическом формате, подходящем для иммунологического определения, включая аналитические форматы, подходящие для автоматизированного оборудования. В некоторых аналитических форматах может быть предпочтительным использовать реагенты, несущие группы-метки, например визуальные маркеры, такие как частицы латекса или золота, флуоресцирующие маркерные группировки, ферментные маркерные группировки и т.д. Конъюгаты реагентов и групп-меток можно получить стандартными методами, например сшиванием ковалентными связями с реакционноспособными боковыми группами аминокислотных остатков реагента, как, например, карбокси-, амино- и/или SH-группами, с группами-метками, например, через бифункциональные молекулы-спейсеры.
Образец предпочтительно берут у пациента-человека. В некоторых воплощениях способ по данному изобретению является неинвазивной диагностической процедурой, при которой образец может быть образцом мочи, в частности экскрементом, или образцом каловых масс. Если необходимо, образец может быть подвергнут предварительной обработке, например гель-фильтрации. В других воплощениях способ по данному изобретению может быть гистохимической процедурой, при которой образец может быть образцом ткани, в частности биоптатом, например материалом, полученным путем пункции или иссечения, или образцом, полученным в результате трансуретральной резекции предстательной железы (TUR-P). При гистохимической процедуре избирательное определение внури- или внеклеточного аннексина A3 может осуществляться путем определения локализации аннексина A3 в образце.
В предпочтительном воплощении данное изобретение включает полуколичественное или количественное определение аннексина A3. В это количественное или полуколичественное определение может входить оценка результатов анализа на основе предварительно определенных пренебрегаемых величин и соотнесение результатов оценки со стадией заболевания. Пренебрегаемые величины могут быть установлены путем определения аннексина A3 в образцах, взятых у здоровых людей и/или у больных с ранее выясненной стадией заболевания, с использованием известных методов. Далее, количество аннексина A3 в образце может быть также определено путем оценки окрашенных образцов ткани и соотнесения результатов оценки со стадией заболевания.
Настоящее изобретение также относится к определению аутоиммунного ответа, т.е. аутоантител, направленных против аннексина A3, и/или присутствия регуляторных Т-клеток. Это определение может осуществляться само по себе или в сочетании с определением аннексина A3. Присутствие аутоантител свидетельствует о злокачественном состоянии, в частности о выраженном раке. Определение аутоантител при необходимости можно сочетать с определением регуляторных Т-клеток. Присутствие регуляторных Т-клеток свидетельствует о злокачественном состоянии, в частности о выраженном раке.
Образец может быть подвергнут фракционированию, которое позволяет разделить определение внеклеточного и внутриклеточного аннексина A3. Например, образец можно центрифугировать, чтобы получить осадок клеток и супернатант, так что внутриклеточный аннексин A3 определяют в осадке клеток, а внеклеточный аннексин A3 определяют в супернатанте. В особенно предпочтительном воплощении способ по данному изобретению включает избирательное определение внеклеточного аннексина A3. В другом воплощении особенно предпочтительный способ по данному изобретению включает избирательное определение внутриклеточного аннексина A3.
Способ по данному изобретению может дополнительно включать определение добавочных маркеров, например других маркеров рака. Определение добавочных маркеров может осуществляться в том же образце, в котором определяли аннексин A3, или в других образцах, например в образцах крови, сыворотки и/или плазмы. Особенно предпочтительно определение маркеров, присутствующих в крови, сыворотке или плазме, в частности, по меньшей мере, одной протеазы из семейства калликреинов, как, например, специфический антиген предстательной железы (PSA), и/или по меньшей мере один маркер эпителиальных клеток, в частности специфический мембранный антиген предстательной железы (PSMA).
Настоящее изобретение может представлять собой процедуру скрининга, когда у отдельно взятого индивида или группы индивидов определяют наличие ракового заболевания, в частности рака предстательной железы. С другой стороны, способ по данному изобретению может также включать прогнозную оценку или катамнестическое исследование после курса лечения, когда пациент, которому уже поставили диагноз «рак», в частности рак предстательной железы, или «предраковое состояние», проходит прогнозную оценку и/или контрольное обследование в ходе лечения.
В особенно предпочтительном воплощении данное изобретение относится к прогнозной оценке прогрессирования заболевания, давая ценный инструмент для любого диагностического исследования, в частности для контролирования лечения. Прогнозная оценка может основываться на определении только аннексина A3 или же аннексина A3 в сочетании с другими маркерами, как, например, PSA. Так, путем гистологического исследования и/или определения уровней PSA и дополнительных маркеров рака пациент может быть отнесен к группе низкого риска (например, уровень PSA не более 10 нг/мл), к промежуточной группе (например, уровень PSA>10, но <20 нг/мл) или высокого риска (например, уровень PSA>20 нг/мл). Определение аннексина A3 у лиц из этих групп может дать дополнительную ценную информацию, в частности у тех пациентов, которые ранее были отнесены к промежуточной группе. Если у таких пациентов обнаруживается аннексин A3, выживаемость без повышения уровня PSA оказывается значительно выше, чем среди тех, у кого аннексин А3 отсутствует. Таким образом, данное изобретение дает возможность более точного подразделения групп риска. Предпочтительно, лица, первоначально отнесенные к промежуточной группе, могут быть заново подразделены на основании результатов определения аннексина A3. Индивидов, у которых имеется аннексин A3, можно отнести к группе низкого риска, а тех, у кого он не обнаруживается (и у кого выявляется аутоиммунная реакция против аннексина A3, что определяют по желанию), можно отнести к группе высокого риска.
Далее настоящее изобретение будет раскрыто подробнее в нижеследующих чертежах и примерах.
Описание чертежей
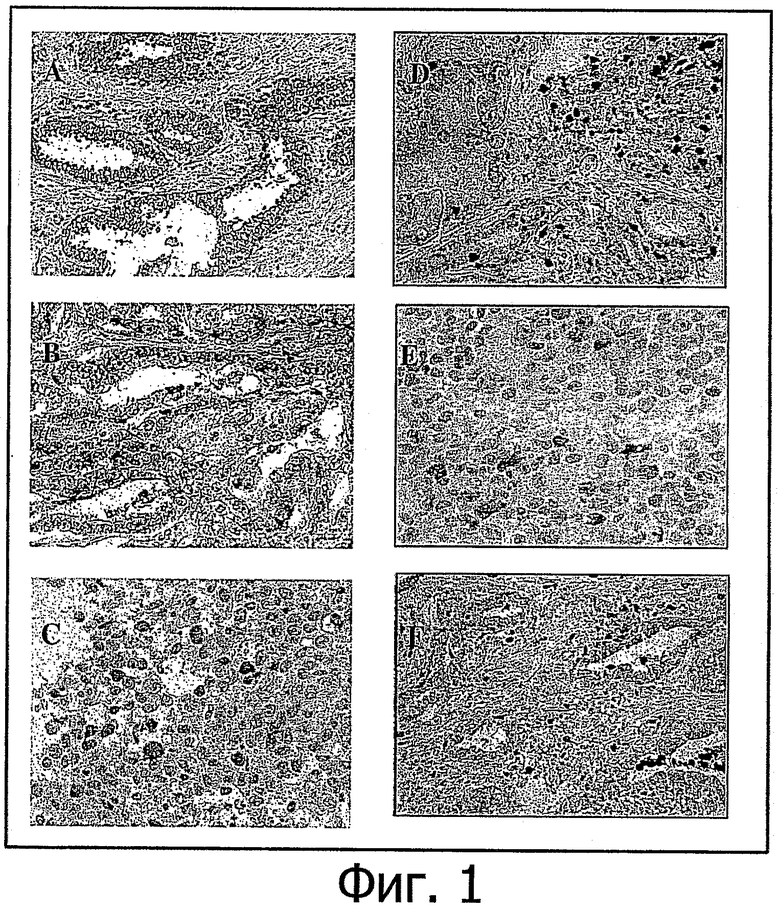
Фигура 1 показывает разницу в интенсивности и локализации окрашивания на аннексин A3 образца ткани при доброкачественной гиперплазии предстательной железы (1А), раке предстательной железы с промежуточной суммой баллов по шкале Глисона (1В) и далеко зашедшем раке с наличием разбросанных ANXA3-положительных клеток (1C; срез ткани). Такие клетки также окрашиваются на CD3-общий маркер Т-клеток (1D), на CD25 - специфический маркер регуляторных Т-клеток (Tregs, 1E) и Foxp3 - другой специфический маркер регуляторных Т-клеток (Tregs, 1F).
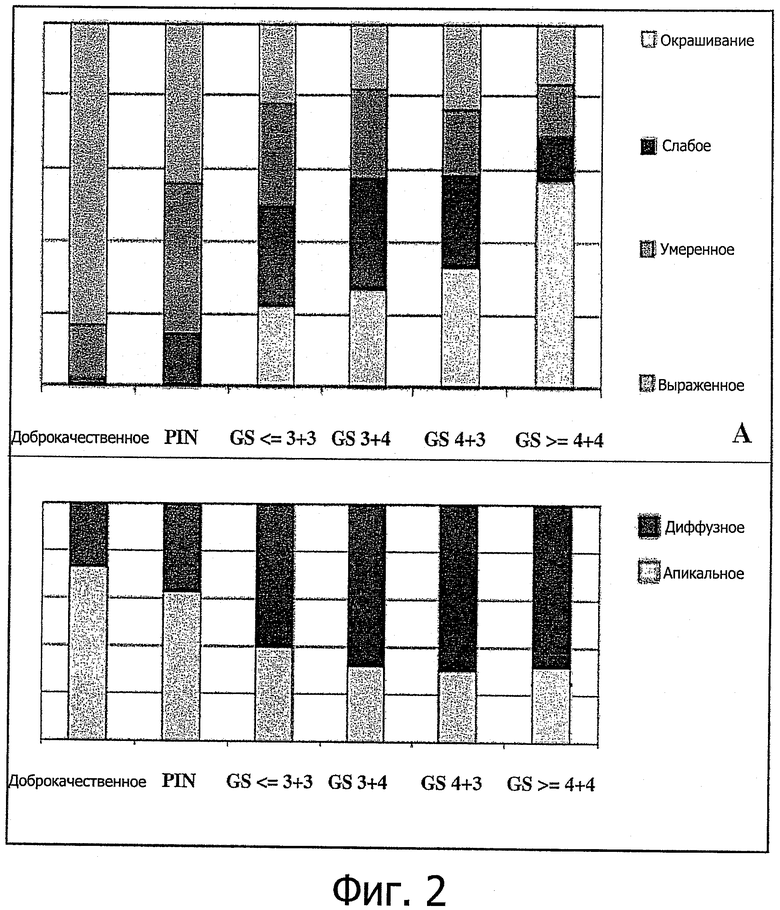
Фигура 2 суммирует данные по окрашиванию на аннексин A3 (отсутствует, слабое, умеренное, выраженное) в зависимости от состояния пациента: доброкачественное, предраковое (интраэпителиальная неоплазия предстательной железы - PIN), злокачественное (рак, классифицируемый по шкале Глисона - GS). Наиболее интенсивно окрашивается доброкачественный эпителий.
(a) Интенсивность окрашивания меньше при PIN и при карциноме с нарастающей дедифференцировкой клеток.
(b) Апикальное окрашивание на ANXA3 отрицательно коррелирует с тяжестью ракового заболевания. Корреляция обоих параметров со стадией трансформации предстательной железы высокозначимая (р<0,001). ANXA3 - аннексии A3; PIN - интраэпителиальная неоплазия предстательной железы.
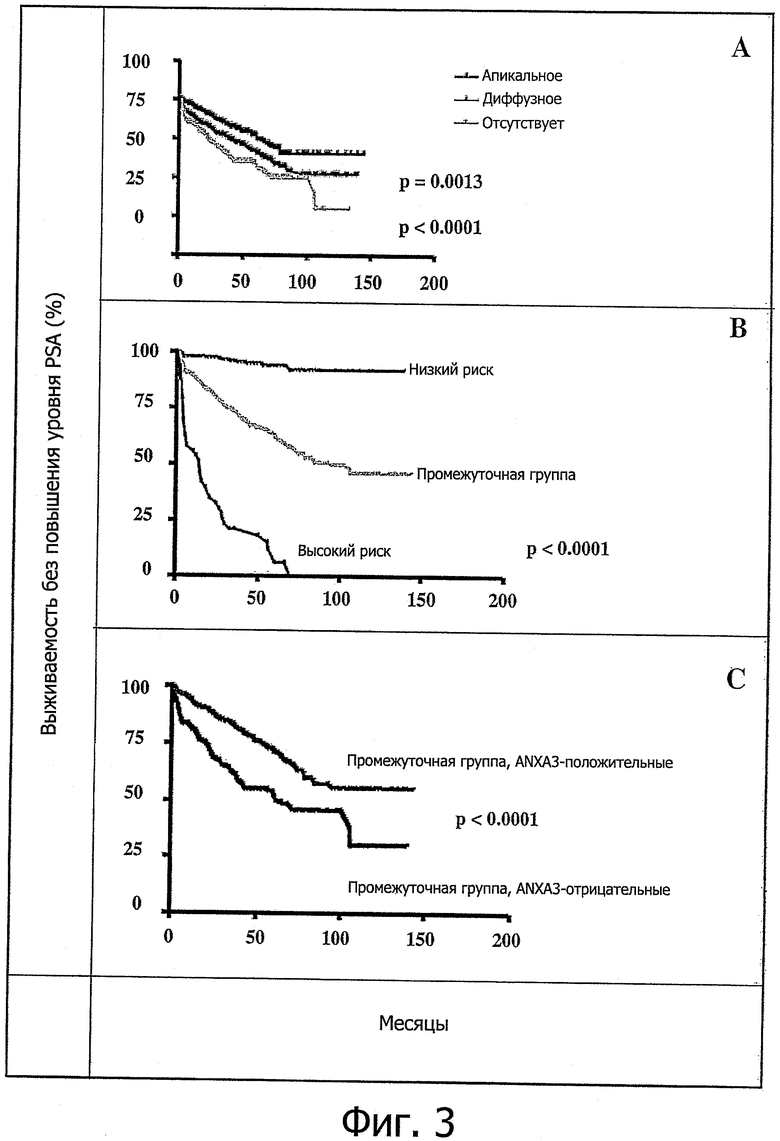
Фигура 3 показывает связь между продолжительностью жизни без повышения уровня PSA и окрашиванием на ANXA3 в различных группах пациентов.
(a) Подразделение ANXA3-положительных опухолей по паттерну окрашивания (апикальное/диффузное) позволило выделить подгруппы, соответствующие прогнозу.
(b) Вероятность выживания без повышения уровня PSA согласно подразделению на группы риска.
(c) Подразделение в зависимости от присутствия ANXA3 (положительное/отрицательное) позволило разделить промежуточную группу риска, составлявшую самую большую когорту (n=969), на подгруппы высокого и низкого риска (р=0,0001). ANXA3 - аннексин A3; PSA - специфический антиген предстательной железы.
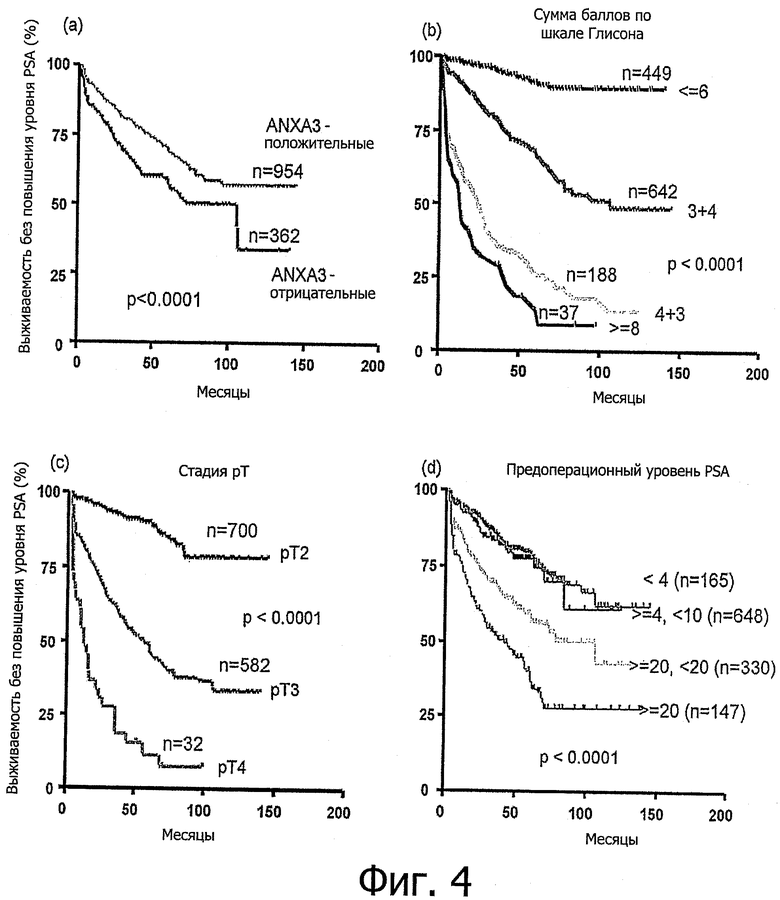
Фигура 4 показывает связь между продолжительностью жизни без повышения уровня PSA и присутствием/отсутствием аннексина A3. Отсутствие окрашивания на ANXA3 выраженно коррелирует с выживанием без повышения уровня PSA. Вероятность выживания без повышения уровня PSA согласно сумме баллов по шкале Глисона (b), стадии рТ (с) и предоперационному уровню PSA (нг/мл). ANXA3 - аннексин A3; PSA - специфический антиген предстательной железы.
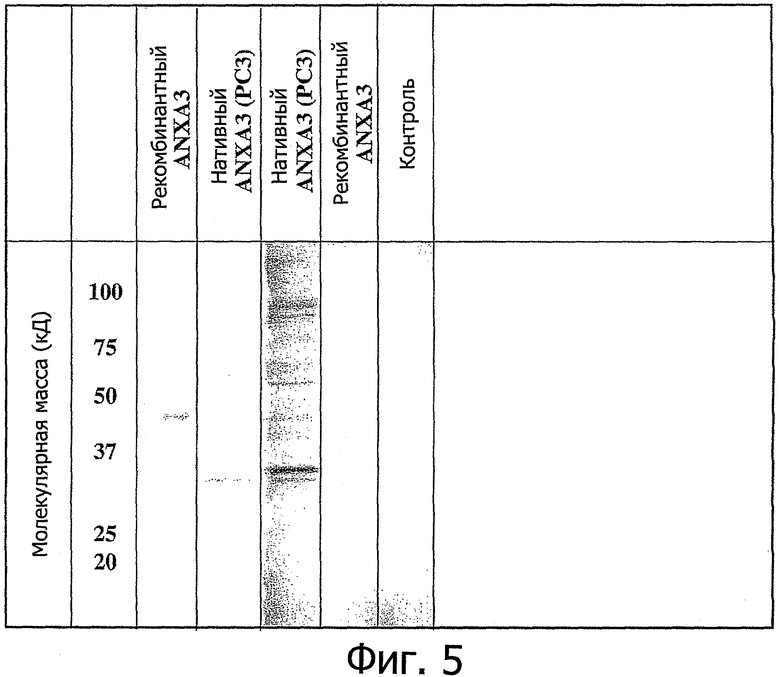
Фигура 5 показывает присутствие аутоантител в сыворотке крови у больных раком предстательной железы.
Примеры
1. Материалы и методы
1.1 Антитела
В данном исследовании использовались следующие антитела.
Клон tgc7 ProVII5C5 (DSM АСС2780), моноклональные; 2,4 мг/мл; направленные против белка-мишени ANXA3.
1.2 Ткани
Для анализа брали готовые ТМА раковой опухоли предстательной железы, содержащие >3000 образцов ткани. Подробное описание состава представлено в разделе «Результаты».
1.3. Иммуногистохимические методы (IHC)
Был разработан протокол IHC, подходящий для определения аннексина A3 в фиксированных формалином образцах ткани. Подробный протокол приведен ниже.
Протокол иммунохимического окрашивания на ANXA3
ПОДГОТОВКА ПРЕПАРАТОВ
- Депарафинизация ТМА по меньшей мере 1 час в ксилоле, GFS 2×5 мин ксилол.
- Регидратация в водном растворе этилового спирта убывающей концентрации вплоть до дистиллированной воды.
- Промывание 5 мин буферным раствором (PBS)
ПРЕДВАРИТЕЛЬНАЯ ОБРАБОТКА (восстановление эпитопов)
- Автоклавирование в течение 5 мин в уксусной кислоте рН2.
- Промывание 5 мин буферным раствором PBS.
БЛОКИРОВАНИЕ ПЕРОКСИДАЗНОЙ АКТИВНОСТИ
- Инкубация 10 мин в растворе H2O2 (1%)/метанол.
- Промывание 2×5 мин в PBS.
ИНКУБАЦИЯ АНТИТЕЛ
- Разведение первичных антител (ANXA3) 1:8100 (0,3 мкг/мл) в PBS.
- Нанесение на ткань/срез ТМА 100-200 мкл разведенных антител.
- Инкубация 2 ч при 30°С во влажной камере.
- Промывание 2×5 мин буферным раствором Tris-PBS (1:10).
- Нанесение вторичных антител (EnVision DAKO K4003, антикроличьи), конъюгированных с HRP, на 30 мин при 30°С.
- Промывание 2×5 мин буферным раствором Tris-PBS.
ХРОМОГЕН
- Наносят на препараты DAB-Chromogen (Liquid DAB DAKO Code No.: К 3467) на 10 мин при комнатной температуре.
- Препараты тщательно промывают буферным раствором PBS.
- Контрастное окрашивание гематоксилином в течение 1 мин sec (Harris Hamatoxylin HTX 31000, Medite Gmbh).
- Промывание водой.
- Дифференцировка в HCl-Ethanolblue в течение 5 мин в водном растворе этилового спирта убывающей концентрации.
- Нанесение ксилола.
1.4. Иммуногистохимическая оценка
Все окрашенные препараты оценивал один и тот же патологоанатом. Вариант а) Для каждого образца ткани и антитела интенсивность мембранного окрашивания оценивали визуально по 4-балльной шкале (0, 1, 2, 3). Кроме того, окрасившиеся части опухолевых клеток оценивали по 4-балльной шкале (<20%, > или =20% < 40%, > или =40% - <90%, >90%). Окончательную иммуногистохимическую оценку проводили по этим двум параметрам.
Определение оценок
Для некоторых вариантов статистического анализа случаи рака группировали как отрицательные (отсутствие) либо положительные (слабое, умеренное, выраженное).
1.5. Описание файла данных
Все данные, полученные в этом исследовании, собрали в один файл, сгруппировав следующим образом.
1.6. Статистическая обработка данных
Для расчета вероятности различий в экспрессии аннексина A3 между разными подгруппами опухолей применяли критерий хи-квадрат. Для определения влияния экспрессии аннексина A3 на прогноз для данного пациента строили кривые Каплана-Мейера. Для мультивариантного анализа осуществляли регрессионный анализ по методу Кокса.
2. Результаты
Основанные на исследовании ТМА-блоков, содержащих столбики опухолевой ткани из 1679 образцов, полученных в результате радикальной простатэктомии, репрезентативные изображения, полученные при помощи иммуноцитохимических методов с использованием специфических антител против ANXA3 (Фигура 1), показывают разницу в интенсивности и локализации окрашивания на ANXA3 в типичных образцах ткани предстательной железы при доброкачественной гиперплазии (1А), раке предстательной железы с умеренной суммой баллов по шкале Глисона (1В) и далеко зашедшем раке (1C). Кроме того, были исследованы 135 случаев доброкачественных состояний и 125 случаев пренеопластических поражений (PIN высокой степени).
В целом окрашивание на аннексии A3 было локализовано преимущественно в цитоплазме, причем имела место внутриклеточная дифференциация - цитоплазматическое окрашивание и связанное с мембранами/везикулярное. В доброкачественном железистом эпителии наблюдалось выраженное клеточное и ядерное окрашивание на аннексин A3. Кроме того, окрашивание обнаруживалось в мелких цитоплазматических везикулах, сосредоточенных в верхушках клеток, так что получался выражение апикальный цитоплазматический паттерн окрашивания. В верхушках клеток образование ANXA3-положительных везикул часто наблюдалось в соответствии с процессом апокриновой секреции в протоки железы.
В доброкачественных секреторных клетках и поражениях PIN высокой степени окрашивание было равномерным, преимущественно выраженно апикальным цитоплазматическим. Однако при PIN высокой степени интенсивность окрашивания значительно уменьшалась (р<0,0001). При раке интенсивность окрашивания на ANXA3 еще более уменьшалась (включая отсутствие окрашивания в 27% случаев, р<0,0001) и наблюдался явный сдвиг паттерна окрашивания от апикального цитоплазматического к диффузному цитоплазматическому (р<0,0001). Эти результаты суммированы на Фигуре 2.
Отсутствие окрашивания на ANXA3 было ассоциировано с рТ-стадией и суммой баллов по шкале Глисона (р<0,0001), но не с уровнем PSA (р=029). Анализ по методу Каплана-Мейера выявил значительное сокращение выживаемости без повышения уровня PSA (р<0,001; логарифмичекий ранговый критерий). Мультивариантный анализ показал, что отсутствие окрашивания на аннексин A3 является независимым прогностическим показателем (HR 1,20; р=0,002). Подробнее см. Таблицы 1 и 2.
Дальнейшее исследование отдельных разбросанных клеток при далеко зашедшем раке путем окрашивания с использованием антител показало, что эти клетки являются преимущественно Т-лимфоцитами (1D), а точнее регуляторными Т-клетками (Tregs), поскольку в них экспрессируются CD25 (1Е) и Eохр3 (1F) (6). Недавно сообщалось, что регуляторные Т-клетки играют роль в опухолеспецифической толерантности (7).
Что касается исследования ANXA3-положительных случаев рака, то имеется корреляция с суммой баллов по шкале Глисона (р=0,04), однако вопреки ожидаемому среди случаев рака высокой степени злокачественности оказалась наибольшая доля выраженного окрашивания (35,6%), а доля слабого окрашивания была почти одинаковой при раке низкой и высокой степени (35,6% и 36,3% соответственно). Интенсивность окрашивания также коррелировала с уровнем PSA (р=0,0029). Случаи выраженного окрашивания опухолевой ткани на ANXA3 чаще всего попадали в группу с уровнем PSA не менее 20 нг/мл (41,1%), а случаи слабого окрашивания на ANXA3 чаще всего оказывались в группе с уровнем PSA ниже 20 нг/мл. Имела место тенденция к ослаблению интенсивности окрашивания в случаях локально прогрессировавшего рака, однако она не достигала статистической значимости (р=0,0630).
За уровнем PSA после лечения следили у 1317 пациентов. Биохимическим рецидивом считалось достижение или превышение уровнем PSA величины 0,1 нг/мл в двух последовательных определениях. Рецидив по PSA наблюдался у 354 пациентов. В среднем наблюдение после лечения велось 33 месяца. Пациентов без рецидива наблюдали 39 месяцев. Путем унивариантного анализа нам удалось показать, что отсутствие окрашивания на аннексин A3 ассоциировано со значительным сокращением продолжительности жизни без возрастания уровня PSA по сравнению со случаями ANXA3-положительных опухолей (р<0,0001). Более тонкая характеристика ANXA3-положительных опухолей по паттерну окрашивания позволила подразделить эту группу пациентов на две подгруппы, соответствующие прогнозу развития заболевания. Прогноз был значительно хуже при ANXA3-положительных опухолях с диффузным окрашиванием эпителия нежели при апикальном окрашивании (логарифмический ранговый критерий, р=0,0013; Фигура 3А).
Чтобы далее изучить, соотносится ли присутствие/отсутствие ANXA3 с прогнозом, дополняя сочетанное использование хорошо известных классических прогностических параметров (уровень PSA, оценка по Глисону, стадия рТ) мы разделили нашу когорту пациентов на три группы риска. По уровню PSA, сумме баллов по шкале Глисона и стадии рТ пациентов характеризовали как имеющих низкий либо высокий риск прогрессирования рака или же относили к промежуточной группе. В группе низкого риска предоперационный уровень PSA был не выше 10 нг/мл, сумма баллов по шкале Глисона образцов материала, полученных в результате простатэктомии, составляла не более 6, а раковое поражение ограничивалось предстательной железой. В группе высокого риска прогрессирования рака предстательной железы предоперационный уровень PSA был выше 20 нг/мл, сумма баллов по шкале Глисона образцов материала, полученных в результате простатэктомии, составляла не менее 7, а стадия опухоли не менее рТ3. Тех пациентов, которые не попадали ни в группу высокого риска, ни в группу низкого риска, объединяли в промежуточную группу.
Как показано на Фигуре 3В, категории по риску существенно различались вероятностью прогрессирования рака ((р<0,0001). Дальнейшее подразделение в зависимости от присутствия/отсутствия аннексина A3 (ANXA3-положительные/ANXA3-отрицательные) позволили рассортировать промежуточную группу, составлявшую самую многочисленную когорту (n=922), по подгруппам высокого и низкого риска (р=0,0001). В группах высокого и низкого риска невозможно было определить подгруппы (Таблица 3). Анализ по методу Каплана-Мейера применительно к промежуточной группе также показал, что при отсутствии аннексина A3 выживаемость без повышения уровня PSA значительно ниже (Фигура 3С).
Отсутствие окрашивания на аннексин A3 было ассоциировано со значительным сокращением продолжительности жизни без повышения уровня PSA по сравнению со случаями ANXA3-положительных опухолей (р<0,0001); см. Фигуру 4А. Однако подразделение группы ANXA3-положительных опухолей в зависимости от степени окрашивания (слабое - умеренное - выраженное) не имело прогностического соответствия (логарифмический ранговый критерий, р=0,642; данные не показаны). Помимо факта наличия окрашивания на аннексин A3 (отрицательное-положительное), унивариантный анализ также продемонстрировал прогностическое значение установленных прогностических факторов - суммы баллов по шкале Глисона, стадии рТ и предоперационного уровня PSA в сыворотке крови (р<0,0001; Фигура 4B-D).
Мы изучили возможность аутоиммунной реакции против аннексина A3 у больных раком, исследуя иммунную реактивность против рекомбинантного ANXA3 в сыворотке крови пациентов с помощью метода твердофазного иммуноферментного анализа в варианте «сэндвич». Контроли включали ANXA5, MCV, Ana с фосфосерином и без него. Действительно, у некоторых больных с раком предстательной железы были обнаружены очень высокие титры специфичных анти-АНХА3-антител. Как показано на Фигуре 4, у одного из этих пациентов поликлональная сыворотка окрашивается рекомбинантным ANXA3, натуральным ANXA3 и ANXA3 из линии опухолевых клеток предстательной железы (клетки РС3) сравнительно с окрашиванием соответствующих моноклональных анти-ANXA3-антител. У этого пациента выделили из цельной крови В-клетки и использовали специфичные моноклональные антитела, рекомбинантный ANXA3 и экстракты клеток РС3 в качестве положительных контролей; в результате удалось выделить и культивировать соответствующие клоны В-клеток, продуцирующих анти-ANXA3-антитела, и таким образом перейти к человеческим моноклональным антителам. Результаты вестерн-блоттинга показаны на Фигуре 5.
3. Обсуждение
Изменения в локализации и внутриклеточном распределении аннексина A3, сообразные превращению доброкачественного эпителия предстательной железы в злокачественный, и их прогностическое значение указывают на важную биологическую роль аннексина A3 в жизнедеятельности предстательной железы. Присутствие секретируемого аннексина A3 во внеклеточных пространствах ткани предстательной железы в согласии с тем, что сообщалось о присутствии этого белка в экзосомах/простосомах (2) и о предполагаемой противораковой активности этих везикул (4) побудило нас проверить, доступен ли аннексин A3 для антител в моче или экстрактах клеток РСЗ у больных раком предстательной железы. Исследование при помощи клеточного сортера с возбуждением флуоресценции (FACS) показало, что, действительно, аннексии A3 является потенциально антигенным поверхностным белком (данные не приводятся). Проверка образцов сыворотки крови у больных раком и у пациентов с ВРН (участвовавших в широкомасштабном клиническом исследовании, в котором оценивалось диагностическое значение аннексина A3), показала, что в небольшой группе больных раком имеются аутоантитела, и мы выделили соответствующие клоны В-клеток, продуцирующих анти-ANXA3-антитела.
Обычно используемый в настоящее время биомаркер для определения ранних стадий рака предстательной железы - PSA (8, 9) имеет ряд недостатков, и трудно принимать решения, оценивая риск по данным исследования материала биопсии или образцов, полученных в результате тотальной простатэктомии (10, 11); аннексин A3 представляется потенциально исчерпывающим диагностическим белковым биомаркером.
Одной из ключевых особенностей аннексина A3 явялется то, что его внутри- и внеклеточное распределение и локализация не только дают возможность стабильного неинвазивного исследования жидкостей тела в целях раннего выявления рака предстательной железы, но также отражают важную сторону биологии опухолей, которая не поддается изучению аналитическими методами на основе ДНК/РНК (которые, в принципе, могут выявить лишь заменители суммарного аннексина A3). Полученные нами результаты согласуются с противораковой и защитной ролью аннексина A3, секретируемого эпителием предстательной железы при ВРН, вероятно, в экзосмах/простасомах, которые постепенно теряются в ходе трансформации предстательной железы от доброкачественной гиперплазии (ВРН) через простатическую интраэпителиальную неоплазию (PIN) к раку предстательной железы с высокой суммой баллов по шкале Глисона. Сокращение экзосомального аннексина A3 обусловлено аутоиммунным механизмом, который инициируется при далеко зашедшем раке регуляторными Т-клетками, нацеленными на поверхностный антиген внеклеточных простасом.
Впервые появилась возможность дальнейшего подразделения большого числа пациентов «промежуточной» группы риска и предсказания прогрессирования рака предстательной железы на основании анализа на аннексин A3, что представляет большой интерес для врачебного наблюдения больных после прохождения курса лечения.
С учетом молекулярного окружения аннексина A3 при раке предстательной железы (1) и его предполагаемой роли в иммунологической регуляции злокачественной трансформации ткани предстательной железы до стадий рака, а также участия аннексина A3 в мембранном транспорте, миграции лимфоцитов, подвижности клеток и передаче сигналов (12), его присутствие в экзосомах (12) и простасомах (13) вызывает особенный интерес. Считается, что простасомы участвуют в регуляции врожденной иммунной защиты (14, 15), а в последнее время их стали связывать с различными стадиями рака предстательной железы (15, 16).
Корреляция между тканевым аннексином A3 и аннексином A3, содержащимся в моче, может способствовать пониманию связанной с раком кинетики локализации и высвобождения аннексина A3. Вполне вероятно, что представленное здесь открытие использования аннексина A3 в качестве маркера рака предстательной железы имеет более широкое применение, так как недавно появились сообщения о сходных с нашими результатах исследования аннексина A3 как обратно коррелирующего маркера при светлоклеточной аденокарциноме яичника (17) и колоректальном раке (18, 19). Таким образом, гипотеза о том, что высвобождение аннексина A3 играет связанную с раком общую роль при эпителиальных аденокарциномах, заслуживает повышенного внимания.
Тот факт, что отсутствие окрашивания на аннексин A3 является независимым прогностическим фактором при раке предстательной железы, представляется наиболее важным открытием, сделанным в наших исследованиях. Отсутствие окрашивания на аннексин A3 характеризует подгруппу биологически агрессивных раковых поражений предстательной железы с высоким риском прогрессирования после радикальной простатэктомии. И, наконец, аннексин A3 является многообещающим кандидатом на роль тканевого маркера, который в сочетании со стандартными прогностическими параметрами обеспечивает, как мы полагаем, более точный индивидуальный прогноз, что способствует дальнейшему ведению больного.
Таблицы
ная группа

| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ АННЕКСИНА А3 ДЛЯ ОБНАРУЖЕНИЯ КАРЦИНОМЫ ПРОСТАТЫ | 2007 |
|
RU2467335C2 |
| РЕГИСТРАЦИЯ РАХ2 ДЛЯ ДИАГНОСТИКИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2009 |
|
RU2522485C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ БИОХИМИЧЕСКОГО РЕЦИДИВА У БОЛЬНЫХ РАКОМ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ПОСЛЕ ГОРМОНОЛУЧЕВОЙ ТЕРАПИИ | 2015 |
|
RU2605838C1 |
| КОНТРАСТНЫЕ ВЕЩЕСТВА ДЛЯ ДЕТЕКЦИИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2007 |
|
RU2450832C2 |
| БИОМАРКЕРЫ РАКА | 2007 |
|
RU2460075C2 |
| АНТИТЕЛО К ФАКТОРУ HLDF, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ), ПЕПТИД С АНТИГЕННЫМИ И НК-ГИДРОЛИЗУЮЩИМИ СВОЙСТВАМИ И СПОСОБ ДИАГНОСТИКИ АНАПЛАСТИЧЕСКОГО СОСТОЯНИЯ КЛЕТКИ ЧЕЛОВЕКА | 2000 |
|
RU2276672C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА ЗЛОКАЧЕСТВЕННОЙ ТРАНСФОРМАЦИИ КЛЕТОК ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2022 |
|
RU2806518C1 |
| СПОСОБЫ И СРЕДСТВА ДЛЯ МОНИТОРИНГА НАРУШЕНИЯ ТКАНЕВОГО ГОМЕОСТАЗА В ОРГАНИЗМЕ | 2012 |
|
RU2635767C2 |
| ФОСФОДИЭСТЕРАЗА 4D7 В КАЧЕСТВЕ МАРКЕРА ДЛЯ АГРЕССИВНОГО ГОРМОН-ЧУВСТВИТЕЛЬНОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2010 |
|
RU2575076C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИНТРАЭПИТЕЛИАЛЬНОЙ НЕОПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ КОМПОЗИЦИЯМИ НА ОСНОВЕ ТРАВ | 2004 |
|
RU2373948C2 |
Группа изобретений относится к медицине и касается способа диагностики рака предстательной железы, включающего определение в биологическом образце внутриклеточного распределения аннексина A3 и в котором при обнаружении апикальной внутриклеточной локализации аннексина A3 диагностируют доброкачественное состояние или предраковое состояние или при обнаружении диффузной внутриклеточной локализации аннексина A3 диагностируют злокачественное состояние. Способ диагностики рака предстательной железы также может включать определение в образце присутствия и/или количества аутоантител против аннексина A3 и при необходимости присутствия и/или количества регуляторных Т-клеток, причем присутствие аутоантител против ANXA3 и/или присутствие значительного количества внутриклеточных ANXA3-положительных, но не апикальных регуляторных Т-клеток, прежде всего, свидетельствует о злокачественном состоянии. Группа изобретений касается также аналитического реактива для диагностики рака предстательной железы; способа уточнения диагноза у субъекта, отнесенного к промежуточной группе риска развития рака простаты. Группа изобретений обеспечивает различение доброкачественного и злокачественного состояния. 6 н. и 10 з.п. ф-лы, 5 ил., 3 табл., 1 пр.
1. Способ диагностики рака предстательной железы, включающий определение в биологическом образце внутриклеточное распределение аннексина А3, и в котором при
(a) обнаружении апикальной внутриклеточной локализации аннексина A3 диагностируют доброкачественное состояние или предраковое состояние, или при
(b) обнаружении диффузной внутриклеточной локализации аннексина A3 диагностируют злокачественное состояние.
2. Способ по п.1, в котором реагентом являются антитела.
3. Способ по п.2, в котором антитела являются моноклональными антителами.
4. Способ по п.1, который является гистохимической процедурой.
5. Способ по п.4, в котором анализируемый образец является образцом ткани, биоптатом.
6. Способ по п.1, в котором внутриклеточное распределение аннексина A3 определяют в клетках эпителия предстательной железы.
7. Способ по п.1, включающий дифференциальное диагностирование стадий заболевания, выбираемых из:
(i) доброкачественное состояние,
(ii) предраковое состояние и
(iii) злокачественное состояние (рак).
8. Способ по п.1, в котором определяют, по меньшей мере, один дополнительный маркер.
9. Способ по п.8, в котором дополнительным маркером является специфический антиген предстательной железы (PSA) и/или специфический мембранный антиген предстательной железы (PSMA).
10. Способ по п.1, в котором определяют также аутоантитела против аннексина А3.
11. Способ диагностики рака предстательной железы, включающий анализ образца, например, ткани или биологической жидкости, на присутствие, количество и/или внутриклеточное распределение аннексина A3, в котором
(a) обнаружение апикальной внутриклеточной локализации аннексина A3 свидетельствует о доброкачественном или предраковом состоянии;
(b) обнаружение диффузной внутриклеточной локализации аннексина A3 свидетельствует о злокачественном состоянии и об аутоиммунном ответе на аннексин A3, причем этот аутоиммунный ответ предпочтительно характеризуется присутствием аутоантител против аннексина A3, и/или простасом/экзосом или присутствия АМХА3-положительных регуляторных Т-клеток, и причем это присутствие аутоантител против ANXA3 и/или наличие значительного количества внутриклеточных, но не апикальных, АМХА3-положительных регуляторных Т-клеток прежде всего свидетельствует о злокачественном состоянии.
12. Способ диагностики рака предстательной железы, включающий определение в образце присутствие и/или количество аутоантител против аннексина A3 и при необходимости присутствие и/или количество регуляторных Т-клеток, причем присутствие аутоантител против ANXA3 и/или присутствие значительного количества внутриклеточных ANXA3-положительных, но не апикальных регуляторных Т-клеток прежде всего свидетельствует о злокачественном состоянии.
13. Способ по п.1, в котором отсутствие аннексина A3 является указанием на то, что рак предстательной железы относится к агрессивной подгруппе к подгруппе с высоким риском прогрессирования после хирургического лечения.
14. Способ уточнения диагноза у субъекта, отнесенного к промежуточной группе риска развития рака простаты, включающий анализ образца от этого субъекта на присутствие и/или количество аннексина A3, причем
(a) обнаружение апикальной внутриклеточной локализации аннексина A3 свидетельствует о доброкачественном или предраковом состоянии; и
(b) обнаружение диффузной внутриклеточной локализации аннексина A3 свидетельствует о злокачественном состоянии.
15. Аналитический реактив для диагностики рака предстательной железы, содержащий
(i) реагент для определения аннексина A3 и
(ii) реагент для определения аутоантител против аннексина A3 и/или реагент для определения регуляторных Т-клеток.
16. Аналитический реактив для диагностики рака предстательной железы, содержащий реагент для определения аутоантител против аннексина A3.
| Способ опреснения воды | 1988 |
|
SU1724586A1 |
| Madoz-Gúrpide J., et al., "Proteomics-based validation of genomic data: applications in colorectal cancer diagnosis." Mol Cell Proteomics | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Wozny W., et al., "Differential radioactive quantification of protein abundance ratios between benign and malignant prostate tissues: | |||
Авторы
Даты
2013-06-10—Публикация
2008-04-09—Подача