Изобретение относится к органической химии и предназначено для получения 4-аминостирола из 4-нитростирола.
В настоящее время известно несколько принципиальных методов синтеза 4-аминостирола:
1) дегидратация в газовой [1] и жидкой [2] фазах 1-(4-аминофенил)этанола;
2) жидкофазная дегидратация 2-(4-аминофенил)этанола [3, 4];
3) неселективное гидрирование 4-нитроацетофенона над палладиевым или платиновым катализатором [5] с образованием сложной трудноразделимой смеси аминов, содержащей 0-43% 4-аминостирола;
4) каталитическое селективное гидрирование 4-нитростирола над золотосодержащими катализаторами [6, 7].
Таким образом, в периодической и патентной литературе отсутствуют данные по получению 4-аминостирола из 4-нитростирола без использования процесса гидрирования над Au.
Необходимо отметить, что особенность распределения ē-плотности в структуре 4-нитростирола обуславливает существенное его отличие в химических превращениях от двух других региоизомеров и, особенно, от других нитропроизводных бензола. В частности, восстановление с использованием восстановленного железа приводит к осмолению (образованию олигомерных сополимеров 4-нитростирола с 4-аминостиролом), при этом удается выделить очень незначительное количество смеси 4-аминостирола с 1-амино-4-этилбензолом, а восстановление с помощью Fe(OH)2 дает в результате сложную многокомпонентную смесь низкомолекулярных аминов неизвестного состава, содержащую следы 4-аминостирола.
Технической задачей способа является разработка метода синтеза 4-аминостирола посредством восстановления 4-нитростирола без использования катализаторов.
Указанная задача и эффективность достигаются за счет того, что восстановление 4-нитростирола проводят в соответствии с уравнением реакции

где М - щелочной металл,
при этом проводят восстановление 4-нитростирола, находящегося в растворе, при перемешивании в среде растворителей при 15-50°C в течение 1-15 мин, при этом в качестве восстановителя используют дитионит щелочного металла в количестве 500-1000 мол. % по отношению к 4-нитростиролу, который добавляют в один прием к раствору 4-нитростирола. В качестве растворителей используют такие компоненты, которые в условиях процесса не реагируют химически с исходным 4-нитростиролом, промежуточными и конечным продуктами его восстановления и подобраны в таких соотношениях, чтобы обеспечивались однородность жидкой фазы, растворимость 4-нитростирола и диффузия восстанавливающего агента (аниона 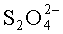 ). После окончания восстановления проводят выделение целевого продукта путем перевода его в объем органической жидкости при 10-50°C, представляющей собой растворитель или их смесь, не растворяющей неорганические продукты, а именно экстракция органическим растворителем целевого продукта или экстракция неорганическим растворителем, например водой, побочных продуктов реакции из однородной жидкой фазы. После получения органического раствора 4-аминостирола его, при необходимости, высушивают и удаляют экстрагент в вакууме.
). После окончания восстановления проводят выделение целевого продукта путем перевода его в объем органической жидкости при 10-50°C, представляющей собой растворитель или их смесь, не растворяющей неорганические продукты, а именно экстракция органическим растворителем целевого продукта или экстракция неорганическим растворителем, например водой, побочных продуктов реакции из однородной жидкой фазы. После получения органического раствора 4-аминостирола его, при необходимости, высушивают и удаляют экстрагент в вакууме.
Способ получения 4-аминостирола раскрывается далее на примерах восстановления 4-нитростирола с помощью Na2S2O4.
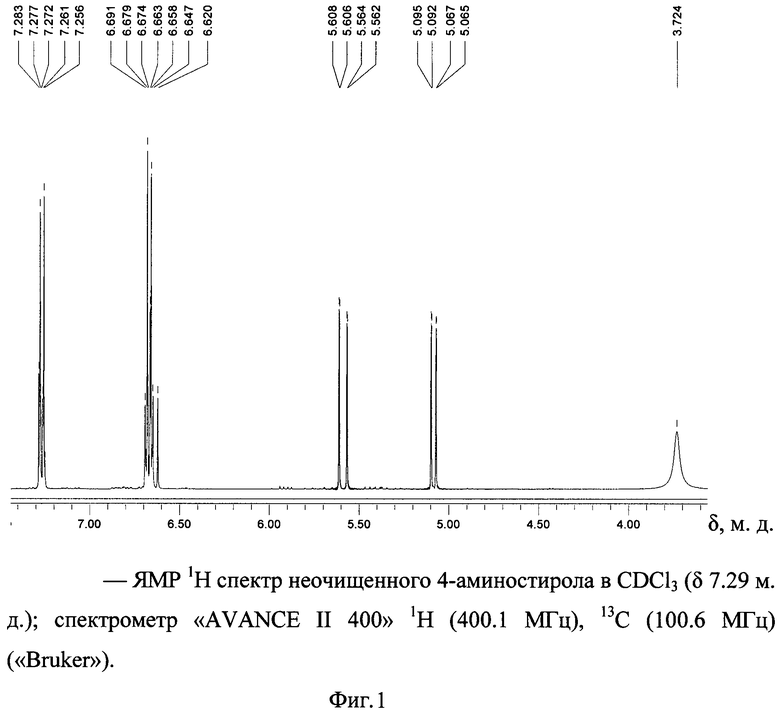
Пример 1. К раствору 2.24 г (0.015 моль) перегнанного 4-нитростирола в 100 мл ацетона добавляют 50 мл H2O и затем 19.70 г (0.113 моль) Na2S2O4, после чего смесь интенсивно перемешивают в течение 10 мин. При перемешивании появляется окраска, через 2 мин окрашенный изначально в желтый цвет раствор обесцвечивается и происходит разогревание смеси. По прошествии всего времени реакционную массу охлаждают до 20-25°C, добавляют к ней 150 мл диэтилового эфира и 50 мл H2O, отделяют органический слой и экстрагируют его 150 мл воды, затем дважды по 100 мл. Эфирно-ацетоновый раствор высушивают над Na2SO4, декантируют, а осушитель промывают 40 мл диэтилового эфира. Органические растворы объединяют, отгоняют растворители в вакууме, к полученной желтой жидкости добавляют 8 мл H2O, массу перемешивают, добавляют к ней 5 мл диэтилового эфира, сливают жидкость в делительную воронку, промывают колбу из-под остатка после упаривания 5 мл диэтилового эфира, который сливают в воронку. К жидкости в делительной воронке добавляют еще 10 мл диэтилового эфира, смесь, не перемешивая, разделяют, эфирный раствор высушивают над KOH, декантируют, затем отфильтровывают образовавшуюся взвесь и удаляют растворитель в вакууме. Выход: 0.44 г (24.6%), жидкость, кристаллизующаяся при охлаждении. Спектр ЯМР 1H, δ, м.д.: 3.724 ш. с (2Н, NH2), 5.085, 5.087, 5.092, 5.095 д. д (1Н, J 10.884 Гц, цис-Н), 5.582, 5.584, 5.606, 5.608 д. д (1Н, J 17.603 Гц, транс-H), 6.620, 6.647, 6.651, 6.686, 6.691 м (1Н, виц-H), 6.658, 6.663, 6.674, 6.679 д (2Н, J 8.455 Гц, 2,6-Ar), 7.256, 7.261, 7.272, 7.277 д (2Н, J 8.455 Гц, 3,5-Ar).
Полученный таким образом 4-аминостирол имеет высокую степень чистоты, что следует из данных ЯМР 1Н спектроскопии (фиг.1), полученных для продукта, который не подвергался дальнейшей очистке.
Пример 2. К смеси 1.08 г (0.0072 моль) 4-нитростирола, 48.2 мл ацетона и 24.1 мл H2O добавляют 9.50 г (0.0546 моль) Na2S2O4, после чего реакционную массу перемешивают в течение 10 мин. При этом образование промежуточных продуктов заканчивается уже через 1 мин. Затем реакционную массу охлаждают до 20-25°C, добавляют к ней 25 мл диэтилового эфира, осадок отфильтровывают, промывают его 25 мл диэтилового эфира, отгоняют из фильтрата растворители в вакууме, затем экстрагируют из полученной суспензии 4-аминостирол 100 мл диэтилового эфира, органический слой отделяют, а водный экстрагируют 50 мл диэтилового эфира. Полученные экстракты объединяют, высушивают над KOH и отгоняют эфир в вакууме. Выход: 0.23 г (26.7%), окрашенная жидкость, кристаллизующаяся при охлаждении.
При необходимости продукт может быть очищен посредством перегонки при пониженном давлении, кислотно-щелочной экстракции (при условии использования растворов слабых органических кислот и быстрого выделения свободного основания) или перегонки с водяным паром.
Таким образом, заявляемый способ является оригинальным и позволяет получать 4-аминостирол, используя в качестве исходного реагента 4-нитростирол и доступные  содержащие восстановители.
содержащие восстановители.
Список источников информации
1. Mowry D.Т., Renoll M., Huber W.F. Vinyl aromatic compounds. I. The vapor phase dehydration of arylmethylcarbinols // J. Am. Chem. Soc. - 1946. - Vol.68. - P.1105-1109.
2. Шульцев А.Л., Панарин Е.Ф. Исследование жидкофазной дегидратации d,1-1-(4-аминофенил)этанола // ЖОХ. - 2010. - Т.80. - Вып.7. - С.1143-1147 // J. General Chem. - 2010. - Vol.80. - N. 7. - P.1309- 1313.
3. Шульцев А.Л. Термическая дегидратация 2-(4-аминофенил)этанола // ЖОХ. - 2011. - Т.81. - №11. - С.1849-1852 // J. General Chem. - Vol.81. - N. 11. - P.2300-2303.
4. Патент RU по З. №2010107931/04, МПК C07B 35/00, C07B 47/00, C07C 15/00, C07C 85/00, C07C 87/00. Шульцев А.Л. Способ получения 1-винил-4-аминобензола; заявл. 15.06.2011.
5. Kittredge K.W., Marine S.S., Taylor R.T. Combinatorial partial hydrogenation reactions of 4-nitroacetophenone // J. Chem. Ed. - 2004. - Vol.81. - N. 10 - P.1494-1496.
6. Avelino Corma, Serna P. Chemoselective hydrogenation of nitro compounds with supported gold catalysts // Science. - 2006. - Vol.313. - P.332-333.
7. Chemoselective hydrogenation of nitroaromatics by supported gold catalysts: Mechanistic reasons of size- and support-dependent activity and selectivity / Shimizu K., Mijamoto Y., Kawasaki Т., Tanji Т., Tai Y., Satsuma A. // J. Phis. Chem. C. - 2009.- Vol.113. - N. 41 - P.17803-17810.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1-АМИНО-4-ВИНИЛБЕНЗОЛА | 2011 |
|
RU2472773C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-НИТРОСТИРОЛА | 2010 |
|
RU2432351C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ КАРБОНОВЫХ КИСЛОТ | 2013 |
|
RU2529026C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРЕТИЧНЫХ АМИНОВ | 2012 |
|
RU2499793C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРПЕРГАЛОГЕНАЛКИЛТИОЭФИРОВ | 1989 |
|
RU2045517C1 |
| Способ получения катализаторов полимеризации этилена с 1-(4-третбутилфенил)этильным фрагментом | 2024 |
|
RU2827710C1 |
| СПОСОБ ЭНАНТИОСЕЛЕКТИВНОГО СИНТЕЗА (R)-ДИЭТИЛ(2-НИТРО-1-ФЕНИЛЭТИЛ) МАЛОНАТА В ПРИСУТСТВИИ КОМПЛЕКСА НИКЕЛЯ | 2011 |
|
RU2488576C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРВИЧНЫХ ИЛИ ВТОРИЧНЫЙ СПИРТОВ | 2013 |
|
RU2519950C1 |
| Способ получения -аминофенилэтиловых спиртов | 1975 |
|
SU535290A1 |
| УЛУЧШЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ ТИГЕЦИКЛИНА И СПОСОБ ПОЛУЧЕНИЯ ИЗ НЕГО ТИГЕЦИКЛИНА | 2021 |
|
RU2819296C1 |
Изобретение относится к новому способу получения 4-аминостирола из 4-нитростирола. Способ включает восстановление 4-нитростирола, находящегося в растворе, при 15-50°C при перемешивании в среде растворителей в течение 1-15 мин, при этом в качестве восстановителя используют дитионит щелочного металла в количестве 500-1000 мол.% по отношению к 4-нитростиролу, который в один прием добавляют к раствору 4-нитростирола, после окончания восстановления проводят выделение целевого продукта путем перевода его в объем органической жидкости при 10-50°C, не растворяющей неорганические продукты, после чего удаляют жидкость в вакууме. Способ позволяет получать продукт с высокой степенью чистоты без использования катализаторов. 1 ил., 2 пр.
Способ получения 4-аминостирола, характеризующийся тем, что в соответствии с уравнением реакции:
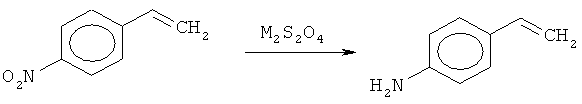 ,
,
где М - щелочной металл,
проводят восстановление 4-нитростирола, находящегося в растворе, при 15-50°C при перемешивании в среде растворителей в течение 1-15 мин, при этом в качестве восстановителя используют дитионит щелочного металла, в количестве 500-1000 мол.% по отношению к 4-нитростиролу, который в один прием добавляют к раствору 4-нитростирола, после окончания восстановления проводят выделение целевого продукта путем перевода его в объем органической жидкости при 10-50°C, не растворяющей неорганические продукты, после чего удаляют жидкость в вакууме.
| SHIMIZU K | |||
| ЕТ AL., «Chemoselective hydrogenation of nitroaromatics by supported gold catalysts: Mechanistic reasons of size- and support-dependent activity and selectivity», J | |||
| Phys | |||
| Chem, 113 (41), 2009, pp.17803-17810 | |||
| WO 2007126262 A1, 08.11.2007 | |||
| WO 2009060886 A1, 14.05.2009 | |||
| ШУЛЬЦЕВ А.Л | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| - Журнал общей химии, т.81, №11, 2011, с.1849-1852. | |||
Авторы
Даты
2013-06-20—Публикация
2012-06-07—Подача