Изобретение относиться к области микробиологической промышленности и касается производства кристаллического λ-лизина. Лизин используется в качестве кормовой добавки для улучшения усвояемости зерновых белков, в которых не хватает 30-35% лизина для полноценного белкового синтеза в организме птицы и свиней. В настоящее время в мире производиться более 900 тыс.т кристаллического лизина для кормовых целей и 15 тыс.т высокоочищенного лизина для пищевых и медицинских целей.
Впервые кристаллический лизин стали производить в 60-х годах прошлого века японские фирмы Аджиномото Ко и Киова Хакко. Технология включала ферментативный биосинтез лизина сепарирование биомассы, подкисление нативного раствора серной кислотой, сорбцию лизина в виде двухзарядного иона на неподвижном слое сульфостирольного катионита элюцию лизина аммиаком, удаление избыточного аммиака путем вакуум-выпарки, подкисления лизина концентрированной HCl, кристаллизацию лизина, центрифугирование и сушку.
Основным недостатком этого способа было использование больших количеств катионита, воды и теплоэнергии при выпарке элюата. Эти недостатки устранены в способе выделения лизина, предложенной бельгийской инжиниринговой компанией CHemviron Carbon (www.chemvironcarbon.com). Данный способ внедрен на заводах основных производителей лизина Аджиномото Ко, Киова Хакко (Япония), ADM (США) и С J (Южная Корея). Способ предусматривает непрерывно работающую ионообменную систему (ISEP) из 30-ти ионообменных колонн, соединенных последовательно в виде замкнутого круга, в которой культуральная жидкость, вода и элюент движутся навстречу движущемуся иониту.
Ионообменные колонны механическим способом перемещаются по часовой стрелке по кругу в виде карусели и тем самым попадают под подачу и сток обрабатываемых жидкостей.
В установке ионообмена имеются 4 зоны воздействия:
- зона промывки;
- зона адсорбции;
- зона споласкивания;
- зона элюирования продукта.
Все остальные стадии производственного процесса: отделение биомасссы, подкисление нативного раствора перед сорбцией, аммиачная элюция - осветление элюата, вакуум-выпарка элюата, кристаллизация лизина, центрифугирование кристаллов и сушка не отличаются от ранее используемого способа.
Несмотря на то, что система ISEP сокращает количество катионита в 17 раз по сравнению с неподвижным слоем смолы. У данного метода есть недостатки. Прежде всего, это отсутствие избирательности обмена и хроматографии веществ, благодаря чему лизин, катионы и пигменты идут одним фронтом, и весь пигмент попадает в элюат. Для удаления пигмента используют большое количество активированного угля. Но даже при этом раствор лизина упаривают только до концентрации 50%.
В этом случае можно получить более крупные кристаллы, чем при концентрации лизина 65%, даже в сильно окрашенном растворе, однако кристаллизуется только половина лизина, а лизин, остающийся в маточнике, возвращается в технологический процесс. Таким образом, компактная ионообменная установка не делает лизин чище и дешевле.
Другая технологическая концепция отражена в авторских свидетельствах СССР №677501, №1112779 и Патента РФ №1578196. Она состоит в том, что подкисленный до pH 1,5 нативный раствор, содеращий лизин Л2+, пропускают через колонны с катеонитом в Na+- форме, с половины колонн лизин элюируют щелочью и элюат пропускают через вторую половину колонн. При этом количество лизина на колоннах удваивается по уравнению Л2++Л±=2Л+
- Л2+ - сорб.
- Л± - эл.
- 2Л+ - сорб.
В этом процессе пигментные вещества проходят вместе со стоками и не сорбируются на смоле.
Отличие щелочной элюции от аммиачной состоит в том, что щелочь элюирует лизин эквивалентно и элюат лизина имеет pH, соответствующий изоэлектрической точке лизина, т.е. 9,7. При этом значении pH, которое не меняется в течение всего процесса элюции, пигмент не десорбируется и элюат остается чистым.
Для десорбции лизина аммиаком необходим значительный избыток элюента, pH элюата достигает 12-12,5 и вместе с лизином десорбируется пигмент. Процесс перезарядки лизина на колонне позволяет получить вдвое более концентрированный элюат лизина, а следовательно, сократить количество выпариваемой воды. В предлагаемом изобретении используется щелочная элюция и неподвижный слой катионита, поэтому наиболее близким прототипом является способ, описанный в Патенте РФ №1578196. Способ включает следующие операции. Культуральную жидкость по окончании ферментации фильтруют на установке микрофильтрации на керамических мембранах с размером пор 100 кДа. Фильтрат подкисляют до pH 1,5 азотной кислотой и пропускают через шесть колонн с катионитом Ку-2×8 в Н+-форме до их полного насыщения. Через три колонны пропускают раствор щелочи, дозированной так, что ее количество в г-экв. соответствует 95% обменной емкости смолы в колонне. Элюат с каждой колонны с pH 10,2 пропускают через насыщенную лизином колонну. В этом процессе перезарядки лизина на смоле pH фильтрата с колонн находится на уровне 5-7. Лизин в фильтрате отсутствует. Колонны с лизином элюируют раствором щелочи, количество которой в г-экв. составляет 105% от обменной емкости смолы в колонне. Элюат с трех колонн объединяют и под вакуумом отпаривают некоторое количество аммиака, сорбированного на смоле вместе с лизином. Затем лизин нейтрализуют концентрированной HCl, осветляют на микропористом оиносорбенте ИА-4, доупаривают раствор лизина до концентрации 65%, кристаллизуют при температуре 15-18°С, центрифугируют на фильтрующей центрифуге при 5000 об/мин и сушат на сушилке во взвешенном слое. Маточник от кристаллизации возвращают в процесс на стадии осветления. Концентрат биомассы высушивают на распылительной сушилке. Конечный продукт представляет собой белый порошок с содержанием лизина монохлоргидрата 98,5-98,7%. Продукт можно использовать в пищевых условиях в качестве добавок в хлеб, макаронные изделия и другие продукты. Выход продукта - 85-88%.
Недостатком этого способа является большое количество катеонита, необходимость упаривания большого количества воды и многостадийность. Целью настоящего изобретения является усовершенствование ионообменной технологии и устранение этих недостатков. Это достигается тем, что после микрофильтрации культуральной жидкости фильтрат обессоливают с помощью специальной ионообменной колонны, состоящей из десяти слоев ионита, которые могут вращаться относительно друг друга. В одном положении слой катеонита чередуется со слоем анионита. Пропуская раствор со скоростью 2 объема на общий объем колонны, из раствора лизина удаляют все неорганические соли. При регенерации слои катеонита и анионита, заключенные в цилиндрические емкости, вращаются относительно друг друга на 90°С и переходят в другое положение. При этом слой катеонита оказывается под слоем катеонита, а слой анионита под слоем анионита, т.е. практически образуются две колонны. Слои катионита регенерируют 2н HNO3, а слои анионита - раствором щелочи. После промывки водой слои снова перемещают в исходное состояние.
Обессоленный раствор пропускают через колонну с осветляющей смолой ИА-4 в Cl--форме. Осветленный раствор пропускают через колонну с анионитом ЭДЕ - 10п, на которой сорбируется анион, связанный с лизином (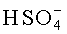 или Cl-). Таким образом получают цвиттер-ион лизина Л±. Пропуская обесцвеченный раствор цвиттер-иона через колонну с катионитом Ку-2×8 в Н+-форме, смолу полностью переводят в лизиновую форму. По сравнению с сорбцией цвиттер-иона лизина, идущей по уравнению: Л±+Н+R→ЛН+R, сорбция на катионите двухзарядного лизина из подкисленного нативного раствора требует в 2,7 раза больше смолы. Другое преимущество данного способа состоит в том, что пропуская через колонну, насыщенную лизином, 4н раствор щелочи, подогретый до 50°С, получают элюат лизина с концентрацией до 70% лизина основания. Кристаллизацию осуществляют, подавая в раствор газообразный HCl или концентрированный раствор HCl. После центрифугирования и сушки кристаллов получают белый негигроскопический порошок с содержанием основного вещества более 98,5%.
или Cl-). Таким образом получают цвиттер-ион лизина Л±. Пропуская обесцвеченный раствор цвиттер-иона через колонну с катионитом Ку-2×8 в Н+-форме, смолу полностью переводят в лизиновую форму. По сравнению с сорбцией цвиттер-иона лизина, идущей по уравнению: Л±+Н+R→ЛН+R, сорбция на катионите двухзарядного лизина из подкисленного нативного раствора требует в 2,7 раза больше смолы. Другое преимущество данного способа состоит в том, что пропуская через колонну, насыщенную лизином, 4н раствор щелочи, подогретый до 50°С, получают элюат лизина с концентрацией до 70% лизина основания. Кристаллизацию осуществляют, подавая в раствор газообразный HCl или концентрированный раствор HCl. После центрифугирования и сушки кристаллов получают белый негигроскопический порошок с содержанием основного вещества более 98,5%.
Примеры осуществления изобретения
Пример 1
400 л культуральной жидкости с концентрацией лизина 100 г/л и биомассы 45 г/л, полученной путем биосинтеза культуры Brevibacterium на среде, содержащей глюкозный сироп, сернокислый аммоний, калий гидрофосфат, витамины и микроэлементы, подвергают микрофильтрации на установке с полимерной мембраной с порами 100 кДа. Концентрат биомассы разбавляют водой (100 л) и продолжают микрофильтрацию до концентрации биомассы 25%. Получают 80 л концентрата, содержащего 18 кг сухой биомассы и 2 кг лизина. Концентрат высушивают на распылительной сушилке производительностью 10 л/час по испаренной влаге. Получают 20 кг протеина, содержащего 10% лизина. Продукт представляет собой полноценную кормовую белковую добавку. 420 л пермеата пропускают через обессоливающую ионообменную систему, состоящую их десяти двухлитровых колонн диаметром 15 см, высотой 12 см, загруженных анионитом ЭДЕ - 10п в Н--форме и катионитом Ку-2×20 в Н+-форме. Колонны соединены последовательно: Анионит-Катионит. Скорость раствора составляет 2-2,5 объемов на объем системы, т.е. 40-45 л/час. Раствор вытесняют с колонн водой с той же скоростью. Получают 440 л раствора с pH 6,8 светло-коричневого цвета, не содержащего неорганических солей. Обессоленный раствор пропускают через колонну, загруженную 50 л осветляющей микропористой смолы ИА-4, со скоростью 40 л/час. Раствор вытесняют с колонны водой с той же скоростью. Сульфат лизина превращают в цвиттер-ион, пропуская раствор лизина через колонну со смолой ЭДЕ - 10п в Н--форме диаметром 25 см, высотой 200 см и объемом 100 л. Скорость раствора в колонне составляет 75 л/час. Раствор вытесняют с колонны водой с той же скоростью. Получают 530 л бесцветного прозрачного раствора с pH 9,8. Сорбция цвиттер-иона лизина на катионите Ку-2×8 в Н+-форме происходит по механизму хемосорбции и идет с выделением энергии. Благодаря этому лизин заполняет все обменные места на смоле, т.е. емкость смолы по лизину фактически равна теоретической, 5,1 мг-экв/г. Лизин элюируют с катеонита с помощью 4н раствора NaOH, подогретого до 50°С. Скорость элюента составляет 30 л/час. В процессе элюции раствор подают сверху, чтобы не размывать фронт элюции. Снизу колонны выходит вязкий светло-желтый раствор лизина основания. Всего после вытеснения щелочи с колонны деионизованной водой собирают 55 л элюата.
Газообразный хлористый водород получают в стеклянном реакторе объемом 100 л, постепенно приливая в 30 л концентрированной HCl концентрированную H2SO4. Кристаллизацию лизина осуществляют в стеклянном реакторе объемом 100 л. Аппарат снабжен барбатером, соединенным полиэтиленовым шлангом с источником хлористого водорода. При барботаже HCl при перемешивании начинается кристаллизация лизинмонохлоргидрата. Суспензия белых кристаллов становиться вязкой, а pH смеси достигает 5,2. Концентрация лизина в суспензии составляет 64%. Суспензию центрифугируют на капроновой ткани при 5000 об/мин. 41,7 кг сырых кристаллов лизина с влажностью 18% сушат на сушилке во взвешенном слое при температуре входящего воздуха 110°С. 16 л маточника, содержащего 7 кг лизина, возвращают в процесс на стадии пропускания раствора через анионит. Выход сухих кристаллов лизинамонохлоргидрата составляет 34,2 кг, или 86%. Качество порошка полностью соответствует сертификату на пищевой лизин.
Преимущество данного процесса перед действующими производствами состоит в том, что в нем используется мало воды и отсутствуют процессы выпарки, которые требуют больших энергетических затрат.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АМИНОКИСЛОТНОЙ СМЕСИ ИЗ БЕЛКОВОГО ГИДРОЛИЗАТА | 2005 |
|
RU2317331C2 |
| Способ получения полностью гидролизованного коллагена | 2018 |
|
RU2680968C1 |
| Способ выделения глутамина | 1990 |
|
SU1740419A1 |
| Способ выделения лизина | 1988 |
|
SU1578196A1 |
| Способ выделения глутаминовой кислоты из культуральной жидкости | 1988 |
|
SU1682393A1 |
| СПОСОБ ВЫДЕЛЕНИЯ L-ЛИЗИНА ИЗ КУЛЬТУРАЛЬНОЙ ЖИДКОСТИ | 2009 |
|
RU2410435C1 |
| Способ получения осветляющего ионообменного сорбента | 2018 |
|
RU2713828C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИЗИНА ФАРМАКОПЕЙНОЙ КОНДИЦИИ ИЗ КОРМОВОГО ЛИЗИНА | 2014 |
|
RU2624002C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТИЛОЗИНА | 1993 |
|
RU2108392C1 |
| ШТАММ ДРОЖЖЕЙ YARROWIA LIPOLYTICA - ПРОДУЦЕНТ ЛИМОННОЙ КИСЛОТЫ, СПОСОБ ПОЛУЧЕНИЯ ЛИМОННОЙ КИСЛОТЫ И СПОСОБ ВЫДЕЛЕНИЯ ЦИТРАТА НАТРИЯ | 1996 |
|
RU2090611C1 |
Изобретение относится к области биохимии. Предложен способ ионообменного выделения лизина из культуральной жидкости. Отделяют биомассу путем микрофильтрации. Осветляют нативный раствор. Осветленный раствор обессоливают, пропуская через ионообменную систему из 10 одинаковых колонн с соотношением высоты к диаметру 0,8, соединенных в последовательности: анионит в ОН-форме - катионит в H+-форме, со скоростью 2-2,5 объема раствора на объем системы. Обессоленный раствор пропускают через колонну с анионитом в ОН-форме. Образующийся раствор лизина-основания пропускают через колонну с катионитом. Осуществляют элюцию лизина с катионита 3-5н, предпочтительнее 4н, раствором щелочи. В полученный концентрированный элюат лизина барботируют газообразный хлористый водород, вызывая одновременно нейтрализацию и кристаллизацию лизина. Способ позволяет обойтись в технологическом процессе без операций выпарки, что приводит к экономии энергозатрат. 1 з.п. ф-лы, 1 пр.
1. Способ ионообменного выделения лизина из культуральной жидкости, включающий отделение биомассы путем микрофильтрации, осветление нативного раствора, сорбцию лизина на сульфополистирольном катионите, элюцию лизина раствором щелочи, кристаллизацию лизина, центрифугирование кристаллов и сушку, отличающийся тем, что перед сорбцией на катионите раствор обессоливают, пропуская через ионообменную систему из 10 одинаковых колонн с отношением высоты к диаметру 0,8, соединенных в последовательности: анионит в OH--форме - катионит в Н+-форме, со скоростью 2-2,5 объема раствора на объем системы; обессоленный раствор пропускают через колонну с анионитом в ОН--форме, образующийся раствор лизина-основания пропускают через колонну с катионитом и в концентрированный элюат лизина барботируют газообразный хлористый водород, вызывая одновременно нейтрализацию и кристаллизацию лизина.
2. Способ по п.1, отличающийся тем, что для элюции лизина с катионита используют 3-5н, предпочтительнее 4н, раствор щелочи.
| Способ выделения лизина | 1988 |
|
SU1578196A1 |
| Способ выделения глутамина | 1990 |
|
SU1740419A1 |
| Способ получения смеси аминокислот | 1977 |
|
SU698980A1 |
| CZ 9202341 A3, 17.02.1993 | |||
| ГАЛЬВАНИЧЕСКОГО ПОКРЫТИЯ ДЕТАЛЕЙ | 0 |
|
SU337440A1 |
Авторы
Даты
2013-06-20—Публикация
2008-08-27—Подача