Область техники, к которой относится изобретение
Изобретение относится к использованию бактериальных пробиотиков в производстве питательной композиции для ожидающих потомства самок млекопитающих для усиления иммунологического статуса их новорожденного потомства.
Уровень техники
Иммунологический статус новорожденных является важной проблемой. Этот статус включает защиту, присутствующую при рождении ребенка, и приобретение такой иммунологической защиты в течение первых часов, дней или недель жизни ребенка. Способность приобретать и поддерживать такую защиту является критическим фактором для здоровья ребенка, столкнувшегося с новой для него средой. У людей данные проблемы имеют первостепенное значение для здоровья населения.
Поддержание хорошего состояния здоровья будущих матерей во время беременности является ключевым фактором укрепления здоровья потомства в течение беременности и после рождения. К известным факторам общего состояния здоровья относятся привычки питания будущих матерей, потребление ими питательных микроэлементов, их инфекционная история, а также их иммунологический статус. Например, дефицит некоторых минеральных веществ, витаминов или соединений (таких как фолиевая кислота) могут повлиять на развитие плода, а также на послеродовое развитие ребенка. В связи с этим питание матерей играет ключевую роль в здоровье детей в будущем, и для отслеживания и улучшения баланса питания будущих матерей был приложен максимум усилий. В связи с этим важное значение имеют биологически активные добавки к пище или просто общие принципы питания.
Наряду с общими принципами питания будущих матерей, в настоящее время признано, что некоторые конкретные виды пищи могут способствовать распространению специфичной микробиоты в желудочно-кишечном тракте будущей матери. Сбалансированная микробиота, в свою очередь, может оказывать влияние на хозяина. Использование пребиотиков, т.е. питательных веществ для улучшения кишечной микробиоты хозяина, было описано, например, в WO 02/07533 в контексте пользы микробиоты для здоровья особей женского пола.
Кроме того, в WO 2007/105945 утверждается, что включение в питание будущих матерей пребиотических ингредиентов, особенно включение неперевариваемых сахаридов определенного типа, может улучшить микробиоту и/или иммунную систему потомства.
Использование в качестве дополнения при приеме пищи микроорганизмов, предпочтительно живых микроорганизмов, также продемонстрировало улучшение баланса микробиоты кишечного тракта хозяина. Было показано, что модуляция микробиоты кишечного тракта определенными живыми микроорганизмами привносит определенные положительные физиологические эффекты. Так, например, широко изучен и описан иммунный ответ, индуцированный специфическими типами пробиотических бактерий ("Cross talk between probiotics bacteria and the host immune system", The journal of nutrition, Blaise Corthesy et al., supplement, 2007, pages 781S-790S). Обладающие благоприятными эффектами определенные штаммы микроорганизмов более конкретно представлены в научной литературе. Bifidobacterium, Lactobacillus acidophilus и Lactobacillus caseii являются общеизвестными примерами семейств, демонстрирующих пробиотические эффекты.
Высказано предположение, что пробиотики, как и другие комменсалы, будут оказывать влияние на иммунные функции хозяина либо посредством модуляции композиции микробиоты и/или метаболической активности, либо через прямое взаимодействие с частью иммунной системы, базирующейся в слизистой кишечника. После этого взаимодействия иммунные функции будут активированы, отражением чего являются высвобождение иммунных модуляторов (цитокинов), производство антител и активация лимфоцитов, а также других иммунных клеток. Данные активированные клетки, цитокины и/или бактериальные соединения через кровоток будут выполнять иммуномодулирующие функции в различных участках тела. В этой связи предполагается, что оказанный пробиотической добавкой благоприятный эффект на иммунный статус матери также может повлиять на развитие иммунитета плода. Кроме того, также известно, что клетки иммунной системы и другие биологически активные факторы, образованные в кишечнике матери, могут переноситься в грудное молоко через транспортный путь кишечник-молочная железа и передаваться новорожденному в период лактации. Поэтому стоит предположить, что дополнительная подкормка беременных матерей может способствовать обогащению грудного молока факторами иммунной системы, которые будет вносить вклад в поддержание развития иммунитета новорожденного.
Обеспечение здорового будущего потомству является общепризнанной необходимостью. В частности, первостепенным значением обладает обеспечение наилучшего развития и созревания иммунной системы потомства.
Обычно, помимо оказания медицинской помощи в ответ на конкретные медицинские состояния, упор делается на хорошем балансе питания будущих матерей. Однако не так много известно о том, как конкретно усилить иммунный статус потомства в течение периода беременности.
Однако для обеспечения потомству здорового будущего существует необходимость включения дополнительной стадии, основанной на использовании последних данных о питании.
Следовательно, существует необходимость в оказании положительного воздействия на здоровье потомства с помощью целевой питательной диеты будущих матерей.
В частности, для того чтобы наилучшим образом подготовить потомство к антигенным стимулам на ранних этапах жизни, а также для усиления дальнейшего созревания их иммунной системы в целях более эффективного содействия защите в поздний период раннего детского возраста существует необходимость в оказании помощи, гарантирующей потомству наилучшую иммунную систему.
Существует необходимость оказания воздействия на построение иммунной системы потомства на как можно более ранней стадии беременности и в течение всей беременности, а также на ранних этапах жизни новорожденного, когда созревание иммунной системы идет высокими темпами.
Существует необходимость укрепления способности иммунной системы потомства реагировать на антигены, в общем, и на инфекционные болезни, в частности.
Существует необходимость донести это благоприятное действие посредством эффективного и лишенного негативных аспектов воздействия будущим матерям и/или их потомству.
Сущность изобретения
В первом аспекте настоящее изобретение обеспечивает при производстве композиции применение пробиотиков для ожидающих потомства самок млекопитающих для усиления иммунитета их потомства после рождения.
Во втором аспекте настоящее изобретение обеспечивает применение конкретных пробиотических организмов, таких как Bifidobacterium, Lactobacillus, Streptococcus, Enterococcus и Saccharomyces, ожидающими потомства самками млекопитающих для повышения иммунитета их потомства после рождения.
В третьем аспекте, настоящее изобретение обеспечивает применение пробиотиков в период беременности и/или в период грудного кормления потомства.
В другом аспекте изобретения пробиотики вводятся будущим матерям совместно с другими активными ингредиентами, такими как пребиотики или другие диетические добавки, в или с пищей или напитками.
Изобретение также распространяется на используемую вышеупомянутыми способами композицию для указанных целей.
Краткое описание чертежей
На Фигурах 1 и 3 соответственно схематично представлены порядки проведения экспериментов описанных исследований 1 и 2.
На Фигурах 2 и 4 представлены результаты исследований, демонстрирующих усиление иммунитета у потомства.
Раскрытие изобретения
Определения. В настоящем описании следующие термины имеют следующие значения.
«Ожидающие потомства самки млекопитающих» являются особями женского пола млекопитающих, у которых в матке находится, по меньшей мере, одна оплодотворенная, развивающаяся яйцеклетка. Предпочтительно, в настоящем изобретении рассматриваются особи женского пола человека (т.е. матери или потенциальные матери).
«Пробиотик» означает препараты микробных клеток или компоненты микробных клеток с благоприятным влиянием на здоровье или самочувствие организма-хозяина. (Salminen S., Ouwehand A., Benno Y. et al. "Probiotics: how should they be defined". Trends Food Sci. Technol. 1999:10, 107-10). Пробиотик может содержать уникальный штамм микроорганизма, смесь различных штаммов и/или смесь различных микроорганизмов. В случае смесей сингулярный термин «Пробиотик» еще может использоваться для обозначения пробиотической смеси или препарата.
«Пребиотик», как правило, обозначает неперевариваемый пищевой ингредиент, который благоприятно действует на организм хозяина путем селективной стимуляции роста и/или активности микроорганизмов, присутствующих в кишечнике организма-хозяина, посредством чего предпринимается попытка улучшить здоровье организма-хозяина.
«Потомство» относится к новорожденному ребенку или будущему новорожденному целевых самок млекопитающих. В частности, термин включает потомство еще на стадии беременности. Настоящим изобретением рассматривается ювенильная фаза/детский возраст (т.е. вплоть до подросткового возраста человека - 12-14 лет), более предпочтительно настоящее изобретение относится к иммунному статусу потомства в раннем детском возрасте (вплоть до 2-4 летнего возраста человека).
Изобретатели обнаружили, что введение пробиотиков ожидающим потомства самкам млекопитающих может оказывать влияние на иммунную систему потомства, а более конкретно может активизировать иммунную систему потомства таким образом, чтобы позволить системе лучше и сильнее отвечать на воздействие антигенами.
Модуляция иммунной системы потомства может произойти на очень раннем периоде их внутриматочной жизни или на раннем этапе жизни вне матки, когда их иммунная система созревает.
Изобретатели получили свидетельства активирующего эффекта в отсутствии обычного прямого контакта между кишечной системой потомства и пробиотической композицией, введенной ожидающим потомства самкам, т.е. в течение внутриматочного периода жизни потомства.
Дополнительно изобретатели обнаружили, что такая содержащая пробиотики композиция может также оказывать благоприятное влияние на иммунную систему потомства в течение периода лактации.
Без какой-либо связи с теорией, предполагается, что частичная колонизация пробиотиками кишечного тракта ожидающих потомства самок индуцирует образование молекулярного сигнала. Считается, что потомство получает и реагирует на этот молекулярный сигнал. Кроме того, считается, что иммунная система потомства зависит от этого сигнала. Этот сигнал имеет положительный эффект на созревание иммунной системы потомства, что в свою очередь может привести к лучшей способности реагировать на антигены после рождения. Кроме того, предполагается, что сигнал может быть передан потомству в течение периода лактации, в частности, если была проведена предварительная подготовка к получению сигнала в течение внутриутробного периода жизни потомства.
Ожидающие потомства самки
Применение композиции настоящего изобретения осуществляется путем введения ожидающим потомства самкам млекопитающих, т.е. особям женского пола, которые должны принести приплод. Рассматриваемое настоящим изобретением применение распространяется на период от зачатия потомства (оплодотворение) и на весь внутриутробный период вплоть до рождения потомства. Использование также распространяется на период лактации вплоть до отлучения от груди. Частичное отлучение от груди, вплоть до полного окончания лактации, также включено в настоящее изобретение. Не исключено, что рассматриваемое изобретением применение также распространяется на период, непосредственно предшествующий зачатию, так чтобы оказать влияние на состояние здоровья самок и косвенным образом на состояние здоровья потомства.
Млекопитающими могут быть беременные женщины. В таком случае период беременности составляет около 9 месяцев, а период лактации может значительно варьировать в соответствии с привычками, культурой и состоянием здоровья женщин. Самками млекопитающих также могут быть особи женского пола других млекопитающих, включая лошадей, домашних животных, таких как кошки и собаки. Ожидающие потомства самки других млекопитающих не исключаются из настоящего изобретения.
Пробиотические микроорганизмы
Пробиотические микроорганизмы, рассматриваемые в настоящем изобретении, могут включать любые пробиотики выбранные из группы, содержащей Bifidobacterium, Lactobacillus, Streptococcus, Enterococcus и Saccharomyces или их смеси, предпочтительно выбранные из группы состоящей из Bifidobacterium longum, Bifidobacterium lactis, Lactobacillus acidophilus, Lactobacillus rhamnosus, Lactobacillus paracasei, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus salivarius, Lactobacillus reuteri, Enterococcus faecium, Streptococcus sp. и Saccharomyces boulardii или их смесей. Другие пробиотические микроорганизмы не исключаются из настоящего изобретения в том случае, если они обеспечивают способность привносить описанный эффект, активирующий иммунитет.
Более предпочтительно, если пробиотик выбирается из группы, содержащей Lactobacillus rhamnosus CGMCC 1.3724 (сокращенное название NCC4007 и LPR), Bifidobacterium lactis CNCM 1-3446, предлагаемый на рынке среди прочего компанией «Christian Hansen» в Дании под торговой маркой «Bbl2» (сокращенное название NCC2818), Bifidobacterium longum АТСС ВАА-999, предлагаемый на рынке компанией «Morinaga Milk Industry Co. Ltd.» из Японии под торговой маркой «ВВ536», Lactobacillus johnsonii CNCM I-1225 (сокращенное название NCC533 и Lal), Lactobacillus fermentum VRI 003, предлагаемый на рынке фирмой «Probiomics» (Австралия) под торговой маркой «РСС», Bifidobacterium longum CNCM 1-2170, Bifidobacterium longum CNCM 1-2618, Bifidobacterium breve, предлагаемый на рынке фирмой «Danisco» (Дания) под торговой маркой «Bb-03», Bifidobacterium breve, предлагаемый на рынке фирмой «Morinaga» (Япония) под торговой маркой «М-16V» и штамм Bifidobacterium breve, предлагаемый на рынке «Institut Rosell» (Лаллеманд) (Канада) под торговой маркой R0070, Lactobacillus paracasei CNCM 1-1292, Lactobacillus rhamnosus ATCC 53103, предоставляемые среди прочего фирмой «Valio Oy», Финляндия, под торговой маркой «LGG», Enterococcus faecium SF 68 и их смеси. Предпочтительным пробиотиком является Lactobacillus rhamnosus CGMCC 1.3724.
Дозы пробиотика
Пробиотик может присутствовать в композиции в широком процентном диапазоне при условии, что определенный используемый пробиотик привносит описанный эффект, активирующий иммунитет. Однако предпочтительно, если пробиотик присутствует в композиции в количестве, эквивалентном диапазону от 103 до 1010 КОЕ/г сухого вещества композиции. Данное выражение включает возможность того, что бактерии являются живыми, инактивированными или мертвыми или даже присутствуют в виде фрагментов, таких как ДНК или материалы клеточной стенки. Другими словами, формула содержит количество бактерий, выраженное в терминах колониеобразующей способности, как если бы все бактерии были живыми независимо от того, являются ли они, по сути, живыми, инактивированными или мертвыми, фрагментированными или смесью любых из представленных состояний. Предпочтительно, если пробиотик присутствует в количестве в диапазоне от 104 до 109 КОЕ/г сухого вещества композиции, а еще более предпочтительно в количестве в диапазоне от 106 до 108 КОЕ/г сухой композиции.
Способ введения
Композиция может быть введена ожидающим потомства самкам различными путями, при условии возникновения взаимодействия между композицией и желудочно-кишечным трактом самок. Предпочтительно, если композиция вводится самкам как часть пищевого продукта или диетической добавки. Композиция также может быть введена в фармацевтическую композицию. Предпочтительно, если введение является пероральным или энтеральным. Пероральное введение является наиболее предпочтительным, поскольку оно оказывает наименее травматическое воздействие на самок. Однако в патологических условиях или когда энтеральное питание используется по иным основаниям, введение композиции может быть осуществлено вместе с энтеральным питанием.
Введение с другими соединениями
В любом случае, композиция может быть введена отдельно (в чистом виде или, например, разведенная в воде) или в смеси с другими соединениями (такими как диетические добавки, биологически активные добавки к пище, лекарства, носители, ароматизаторы, перевариваемые или неперевариваемые ингредиенты). Витамины и минералы являются примерами типичных диетических добавок. В предпочтительном воплощении композиция вводится вместе с другими соединениями, которые усиливают описанный эффект на иммунитет потомства. Такие синергетически активные соединения могут быть носителями или матрицей, которые облегчают доставку пробиотиков в кишечный тракт особей женского пола, предпочтительно в активной форме. Такие синергетически активные соединения могут также повлиять на состояние здоровья или метаболизм ожидающих потомства самок таким образом, чтобы усилить эффект композиции на иммунную систему потомства. Такие синергетически активные соединения могут быть другими активными соединениями, которые синергетично или отдельно влияют на иммунный ответ ребенка и/или потенцируют эффект пробиотика. Примером таких синергетически активных соединений является мальтодекстрин. Один из эффектов мальтодекстрина заключается в обеспечении носителя для пробиотика, в обеспечении усиления эффекта пробиотика и в предотвращении агрегации. Другие примеры включают известные пребиотические соединения, такие как углеводные соединения, выбранные из группы, состоящей из инулина, фруктоолигосахарида (ФОС), фруктоолигосахарида с короткой цепью (ФОС с короткой цепью), галактоолигосахарида (ГОС), ксилоолигосахарида (КОС), ганглиозида, частично гидролизованной гуаровой камеди (ЧГГК), камеди акации, соевой камеди, молочной композиции с ягодой годжи (Lactowolfberry), экстракта ягоды годжи или их смеси. Могут присутствовать другие углеводы, например, вторичный углевод, действующий в синергии с первичным углеводом, выбираемый из группы, состоящей из ксилоолигосахарида (КОС), камеди, камеди акации, крахмала, частично гидролизованной гуаровой камеди или их смеси.
Углевод или углеводы могут присутствовать в количестве от около 1 г до 20 г, или от 1% до 80%, или от 20% до 60% ежедневной дозы композиции. В ином случае, углеводы присутствуют в количестве от 10% до 80% сухого вещества композиции. В любом случае, однако, ежедневная доза углевода должна соответствовать опубликованным правилам техники безопасности и нормативным требованиям. Для детей типичным ограничением, например, является максимум, равный 6 г/л/день.
В воплощении пищевая композиция предпочтительно содержит источник белка. Источником белка предпочтительно является диетический белок. Диетический белок может быть любым подходящим диетическим белком; например животным белком (таким как молочный белок, мясной белок или яичный белок); растительным белком (таким как соевый белок, пшеничный белок, рисовый белок и гороховый белок); смесью свободных аминокислот или их комбинацией. Особенно предпочтительными являются молочные (такие как казеин), сывороточные и соевые белки.
Композиция также может содержать источники углеводов и/или жиров.
Если композиция изобретения является пищевой композицией и включает источник жира, то источник жира предпочтительно обеспечивает от около 5% до около 55% энергии пищевой композиции; например от около 20% до около 50% энергии. Липид, входящий в источник жира, может быть любым подходящим жиром или жировой смесью. Особенно подходящим является растительный жир; такой как, например, соевое масло, пальмовое масло, кокосовое масло, сафлоровое масло, подсолнечное масло, кукурузное масло, каноловое масло, лецитин и т.п. Животный жир, такой как молочный жир, также может быть добавлен при необходимости.
В пищевую композицию может быть добавлен дополнительный источник углеводов. Предпочтительно обеспечивается от около 40% до около 80% энергии пищевой композиции. Может быть использован любой подходящий углевод, например сахароза, лактоза, глюкоза, фруктоза, сухая кукурузная патока, мальтодекстрин или их смеси.
Также при необходимости могут быть добавлены дополнительные диетические волокна. Если они добавлены, то предпочтительно содержат вплоть до около 5% энергии пищевой композиции. Диетическое волокно может быть из любого подходящего источника, включая, например, сою, горох, овес, пектин, гуаровую камедь, камедь акации, фруктоолигосахариды или их смесь.
Подходящие витамины и минеральные вещества могут быть включены в пищевую композицию в количествах, рекомендуемых соответствующими руководствами.
При необходимости в пищевую композицию могут быть включены один или несколько пищевых эмульгаторов; например эфиры моно- и диглицеридов диацетилвиннокаменной кислоты, лецитин или диглицериды или их смесь. Таким же образом могут быть включены подходящие соли и/или стабилизаторы. В композицию может быть включено вкусо-ароматизирующее вещество.
Период введения
Период введения начинается с оплодотворения или на как можно более раннем сроке после оплодотворения (соотв., после того как потенциальная мать начинает осознавать свою беременность). Однако период введения также может начинаться раньше. Например, период введения может предшествовать оплодотворению на 1 или 2 месяца. В таком случае, считается, что состояние здоровья оплодотворенной потенциальной матери оказывает влияние на состояние здоровья потенциального потомства. Период введения также может начинаться поздно относительно течения беременности, предпочтительно на 3, 5 или 7 месяце беременности (если рассматривать женщин) или на соответствующих им периодах беременности других млекопитающих. Также может рассматриваться очень позднее начало введения композиции, т.е. начало около 8 и 9 месяца (за несколько недель до рождения). В таком случае, предполагается, что воздействие на иммунную систему потомства является кратковременным и быстрым, наилучшим образом подготавливая ее к представлению антигенов после рождения. Период введения может быть непрерывным (например, период до лактации, период лактации вплоть до отлучения от груди) или прерывающимся. Предпочтительно, если период введения является непрерывным для более лучшего, пролонгированного эффекта. Однако предполагается, что схема введения с перерывами (например, ежедневное введение в течение 1 недели в месяц) может обеспечить «прерывистые активирующие иммунитет сигналы», которые индуцируют положительные эффекты у потомства. Продолжительность введения может варьировать. Если положительные эффекты ожидаются при относительно короткой продолжительности введения (например, ежедневное введение в течение 1 недели или 1 месяца), считается, что большая длительность обеспечивает усиленный эффект (например, длительность в 3, 5 или 8 месяцев у человека или соответствующие периоды у других млекопитающих). Предпочтительно, если период введения по существу покрывает полностью весь период беременности. В одном воплощении период введения охватывает период беременности более чем на 50%, более чем на 70% или более чем на 80%. Продолжительность введения может охватывать весь или часть периода лактации.
Наиболее предпочтительно, если период введения также охватывает весь период лактации. Продолжительность может покрыть 0%, 30% или больше, 50% или больше или 80% или больше периода лактации. В одном конкретном воплощении период введения композиции может охватывать период лактации (весь или часть), но не период беременности; и в этом случае благоприятное действие композиции передается потомству через женское молоко. Наиболее предпочтительно, если период введения охватывает часть (или весь) период беременности и часть (или весь) период лактации. Предпочтительно, если введение проводится в виде ежедневного приема (прием один или два раза в день) или в виде еженедельного приема (прием один или два раза в неделю).
В одном воплощении, композиция также вводится напрямую потомству при условии, что мать получала композицию в течение беременности. Предпочтительно, если композиция вводится (наиболее предпочтительно перорально) напрямую потомству в течение лактации или после частичного или полного отлучения от груди. Двойное воздействие композицией на мать (во время беременности) и на потомство (прямое введение) может быть действительно синергетично и оказать улучшенное благоприятное действие. Предполагается, что воздействие в течение беременности индуцирует предварительное кондиционирование потомства для лучшего ответа на более позднее прямое введение.
Эффект композиции
Композиция изобретения, вводимая ожидающим потомства самкам млекопитающих, индуцирует усиление иммунитета потомства. Конкретно это усиление поддается измерению после рождения, но само по себе оно может начаться в течение внутриутробного периода.
В частности, термин «усиление иммунитета», используемый здесь, исключает аллергические реакции. Термин «усиление иммунитета» определяется как усиление врожденных иммунных функций и содействие специфическому иммунному ответу на антигены. Врожденный иммунный ответ может быть представлен клеточными ответами, фагоцитарной активностью, лейкоцитарной активностью и/или полиреактивными антителами. Специфический иммунный ответ может быть представлен клеточной активацией и/или специфическим гуморальным иммунным ответом. Термин «усиление иммунитета» может содержать или может быть определен как усиление иммунной защиты организма и/или как усиление возможности организма реагировать на инфекционные антигенные стимулы. Указанные антигенные стимулы могут быть представлены вирусными, и/или бактериальными, и/или паразитарными агентами или производными, субъединицами, соединениями их поверхностных антигенов и/или токсинами.
В одном воплощении композиция изобретения усиливает передачу иммунной компетентности от указанных самок указанному потомству. Действуя таким образом, композиция способна обеспечить потомство лучшими шансами выдержать воздействие стимулами на ранних этапах жизни. В конечном счете, композиция помогает потомству получить лучшие условия в начале жизни и/или лучшую защиту от инфекций.
В одном воплощении, такой усиливающий эффект является усилением способности потомства отвечать на антигенное воздействие. При рождении иммунная система ребенка находится одновременно в состоянии, позволяющем ему адекватно отвечать на антигенные воздействия, так и в состоянии быстрого созревания. Воздействие антигенами также участвует в усилении созревания иммунной системы. После рождения все дети естественным образом подвергаются воздействию антигенами окружающей среды и патогенов. Иммунная система потомства реагирует на такое воздействие. В одном воплощении настоящего изобретения иммунная система потомства в состоянии реагировать более эффективно на воздействие антигенами. В одном воплощении ответ на воздействие антигенами может быть измерен по содержанию антител, специфичных к указанному антигену. В контексте изобретения повышение содержания специфических антител может быть измерено как количественно, так и качественно. В одном воплощении такое повышение может быть измерено в сыворотке, и/или в слюне, и/или в экскрементах потомства, подвергнутого воздействию антигенов. В одном воплощении, ответ на антигенное воздействие содержит повышение общего количества полиреактивных антител, предпочтительно в сыворотке, и/или в слюне, и/или в экскрементах потомства. В одном воплощении ответ на антигенное воздействие содержит повышение клеточного иммунного ответа в крови потомства, предпочтительно увеличение числа и/или повышение активности лейкоцитов указанного потомства (для иллюстрации, см. результаты примера 2). Понятно, что тип ответа сильно зависит от типа воздействия, хотя некоторые антигены могут индуцировать комплексный иммунный ответ, измеряемый по более чем одному из приведенных выше эффектов (например, повышение специфических антител и повышение полиреактивных антител и/или повышение клеточного иммунного ответа). Измерение иммунного ответа может быть проведено с помощью общеизвестных количественных иммунологических методов, таких как подсчет клеток, количественные анализы антител, фагоцитарная активность, а также цитотоксическая клеточная активность (активность нейтрофилов и естественных клеток-киллеров), количество иммунных маркеров, включая цитокины, факторы роста, а также иммунные маркеры поверхности клеток и т.п. Повышение измеряется относительно уровней в образцах соответствующего потомства, матери которых не подвергались воздействию композиции изобретения (=контрольные образцы).
Антигенное воздействие, обладающее конкретной правомочностью в контексте изобретения, включает, в частности, воздействие вирусами, предпочтительно ротавирусами и аденовирусами, или воздействие инфекционными бактериями, предпочтительно Escherichia coli., Vibrio cholerae, сальмонеллами, клостридиями, шигеллами, или воздействие инфекцией контагиозных паразитов, предпочтительно Giardia lamblia, Entamoeba histolytica и Cryptosporidium spp или их смесями. Это особенно интересно для состояния здоровья детей, в целях демонстрации улучшенной способности отвечать на такие патогенные воздействия. Все это может участвовать в более эффективной защите потомства от данных патогенов и в конечном итоге лучше защитить их от соответствующих инфекций, индуцируемых данными патогенами. В более общем плане, антигенное воздействие может участвовать в создании лучшей защиты потомства от многих типов патогенов (=в общем случае, усиленной иммунной системы). В рамках этого изобретения также может быть рассмотрено положительное влияние на аллергии, поскольку данное влияние на иммунную систему может заключаться в лучших балансе и контроле ответа на аллергены.
Усиливающий эффект на иммунную систему потомства может достигать максимума в течение периода грудного вскармливания или в течение ювенильной фазы/детства. Для человека максимум повышения предпочтительно достигается между рождением (день 0) и 24-мя месяцами жизни, более предпочтительно между рождением (день 0) и 180-м днем жизни. Не исключается, что усиливающий эффект может длиться до достижения фазы раннего совершеннолетия жизни потомства. Для млекопитающих, не являющихся человеком, рассматриваются соответствующие периоды.
Далее изобретение будет проиллюстрировано ссылкой на следующий пример.
Пример 1, исследование на мышах 1
Материалы и методы: Использованные во всех экспериментах обычные шестинедельные самки мышей BALB/c (18-20 г) были приобретены у «Charles River» (Domaine Des Oncins, BP 010969592, L'Arbresle Cedex, Франция). Мышей размещали в специальных, беспатогенных условиях, в виварии медицинской клиники университета Женевы (Clinique Medical Universitaire of Geneva) (CMU-Geneva), и от 6 до 8 детенышей мышей из каждого помета распределяли на каждую группу для изучения.
Животные имели свободный доступ к обычному общепринятому рациону. Беременные мыши получали растворенные в питьевой воде порошки с пробиотиком или плацебо. Питьевая вода менялась ежедневно. Сравнивали три группы:
- группа А, контроль (мальтодекстрин);
- группа В, Lactobacillus paracasei CNCM 1-2116 (ST 11);
- группа С, Lactobacillus rhamnosus CGMCC 1,3724 (LPR).
Все препараты были получены из обычного публичного источника. Названия «ST11» и «LPR» являются аббревиатурами или сокращенными названиями для цитируемых микроорганизмов.
Живая ослабленная противокоревая вакцина (MV-S) была приобретена у «Aventis Pasteur» (Лион, Франция).
Измерения
Определение антител к вирусу кори (изотипов IgGI и IgG2a) и общего количества IgG в сыворотке проводили методом ИФА в центре вакцинологии и неонатальной иммунологии (Center for vaccinology and Neonatal Immunology (CVNI)) медицинского центра университета Женевы (Швейцария), в соответствии со стандартами.
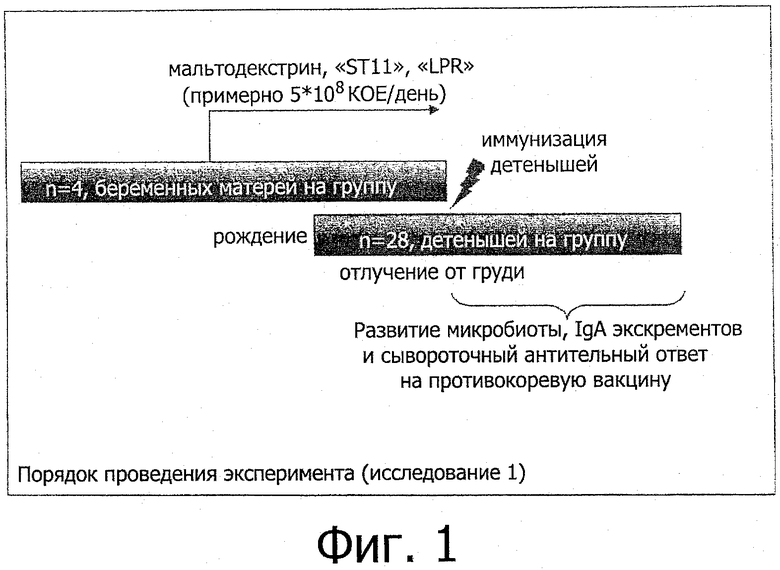
Порядок проведения эксперимента: (на Фигуре 1 представлена схема процедуры):
1. Четыре беременные мыши на группу получали питьевую воду содержащую А, В или С на всем протяжении беременности и в течение периода до отлучения от груди.
2. При отлучении от груди (3 недели) и далее все детеныши получали обычную воду без каких-либо добавок. Матерей умерщвляли.
3. На 3 неделе (детская иммунизация) детенышей (5-8 детенышей в помете, 28 детенышей в группе) иммунизировали с помощью живого ослабленного вируса кори (5×105 CCID50).
4. Еженедельно (с 3 по 8 неделю жизни) отслеживали прибавку массы детенышей и один раз в неделю проводили сбор экскрементов (с 3 по 8 неделю жизни).
5. Через 3 и 5 недель после иммунизации для определения общего содержания IgG и содержания специфичных к кори антител IgGI и IgG2a у детенышей отбирали кровь.
6. Через пять недель после иммунизации всех мышей умерщвляли.
Для оценки различий в действии противокоревой вакцины были проведены анализ Краскера-Уоллеса с последующим проведением анализа Манна-Уитни (Уилкоксона).
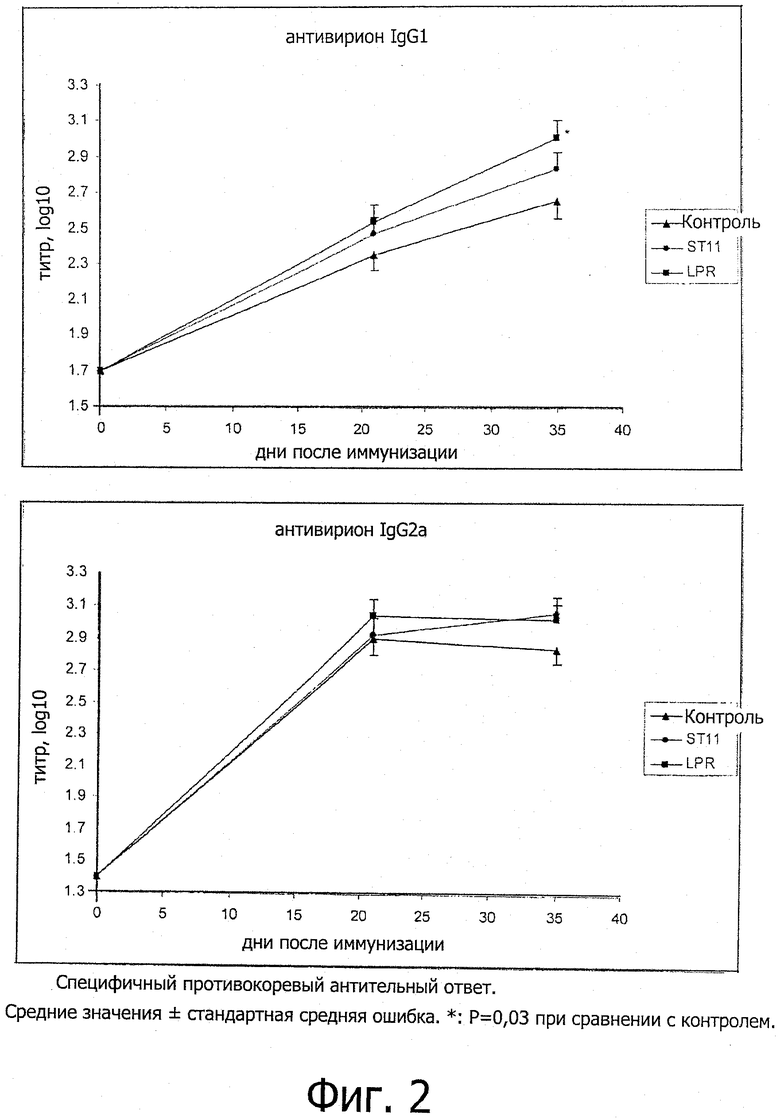
Результаты: На Фигуре 2 представлена графическая иллюстрация полученных результатов. Не было выявлено влияния на рост новорожденных. Не наблюдалось каких-либо различий в вакцинных ответах, связанных с пометами, полом или удельным весом тела. Значительное увеличение антительных ответов после противокоревой вакцинации наблюдали во всех группах, что отражает нормальный процесс созревания антител. Иммунный ответ характеризовали по смешанным ответам Th1:Th2, что проиллюстрировано сбалансированными уровнями IgG1 и IgG2a, наблюдаемыми во всех группах. Подкормка матерей «ST11» не дала какого-либо статистически значимого эффекта на отзывчивость детенышей к противокоревой вакцине (в условиях проведения теста). Однако подкормка беременных матерей «LPR» способствовала более высокому титру IgG по сравнению с контролями, без изменения в общем иммунном профиле ответа на противокоревую вакцину.
Вывод: Данные результаты, по всей видимости, указывают на то, что данные эффекты являются специфичными по отношению к пробиотическому штамму. Действительно, «ST11», no всей видимости, слабо влияет на созревание иммунитета кишечника детенышей и на реакцию в ответ на противокоревую вакцину. В отличие от этого, подкормка беременных матерей «LPR» способствует усилению ответов периферальными IgG на противокоревую вакцину у молодых взрослых мышей.
Пример 2, исследование на мышах 2
Материалы и методы: Использованные во всех экспериментах обычные шестинедельные самки мышей BALB/c (18-20 г) были приобретены у «Janvier», Франция. Мышей размещали в специальных, беспатогенных условиях в виварии исследовательского центра «Nestle» и от 10 до 12 детенышей из каждого помета распределяли в каждую группу для изучения.
Животные имели свободный доступ к обычному общепринятому рациону. Беременные мыши получали растворенные в питьевой воде порошки с пробиотиком или плацебо. Питьевая вода менялась ежедневно. Сравнивали две группы:
- группа А, контроль (мальтодекстрин);
- группа В, Bifidobacterium lactis CNCM 1 -3446 (BL).
Все препараты были получены из обычного публичного источника. Название «BL» является аббревиатурой для цитируемого микроорганизма.
Противостолбнячная вакцина, «Tetanol Pur» (40 ME), была приобретена у «Novartis» (Швейцария).
Измерения
Определение пролиферации Т-клеток селезенки в присутствии антитела анти-CD3 проводили в соответствии с общепринятыми процедурами. Вкратце, спленоциты инкубировали с пришитыми к подложке антимышиными CD3 (2,5 мкг/мл, инкубация в течение 2 часов при 37°С, «BD Pharmingen», каталожный №553056) в 96-луночных планшетах при 37°С в течение 72 ч. Пролиферацию клеток определяли по включению [метил-3H] тимидина («Amersham Pharmacia Biosciences»), как описано ранее (DeCicco, К.L., Youngdahl, J.D. and Ross, А.С. 2001 Immunology 104, 341-348). Данные представлены в виде импульсов в минуту, нормированных к процентному содержанию CD3-позитивных клеток, фактически присутствующих в селезенках тестируемых мышей.
Определение доз антител IgG специфичных к столбняку в сыворотке проводили методом ИФА. Вкратце, 96-луночные планшеты для микротитрования покрывали полным антигеном столбнячного токсина в концентрации 0,1 мкг («Calbiochem», столбнячный токсин из Clostridium tetani, каталожный №582231) в фосфатно-солевом буферном растворе. После 3 отмывок фосфатно-солевым буферным раствором с 0,05% «Tween 20» планшеты блокировали с помощью буфера, содержащего фосфатно-солевой буферный раствор с 20% фетальной телячьей сывороткой и 0,05% «Tween 20», в течение 1 часа при 37°С и затем снова отмывали 3 раза. Серийные разведения сыворотки мышей в блокирующем буфере инкубировали в течение 2 часов при 37°С. После 3 отмывок связанные специфичные к столбнячному токсину IgG детектировали инкубацией с конъюгированными с биотином козьими антимышиными антителами IgG («SouthernBiotech», каталожный №1034-08) в течение 1 часа при 37°С. После 3 отмывок пластины для ИФА инкубировали с меченным пероксидазой стрептавидином («KPL», каталожный №14-30-00) в течение 30 минут при 37°С. После 3-кратной окончательной отмывки добавляли субстрат перокисидазы («KPL», каталожный №50-76-00). Колориметрическую реакцию останавливали с помощью серной кислоты и измеряли оптическую плотность при 450 нм с помощью спектрофотометра. Затем расчитывали титры антител, как описано ранее (Ма, Y. and Ross, А.С, 2005, Proc Natl Acad Sci. 2005 Sep 20; 102(38): 13556-61).
Порядок проведения эксперимента (на Фигуре 3 представлена схема процедуры):
1. От двух до трех беременных мышей в каждой группе получали питьевую воду, содержащую плацебо или BL, на протяжении всей беременности и в течение первых двух недель лактации.
2. При отлучении от груди (3 недели) и в дальнейшем все детеныши получали обычную воду без каких-либо добавок. Матерей умерщвляли.
3. Через 3 недели подгруппу детенышей в каждой группе (5-6 детенышей на группу) умерщвляли для оценки пролиферации клеток селезенки.
4. Через 3 недели (детская иммунизация) оставшихся детенышей (5-6 детенышей на группу) иммунизировали подкожно противостолбнячной вакциной (1/4 от человеческой дозы).
5. Спустя четыре недели после первой иммунизации детенышам вводили вакцинный стимулятор.
6. Через 4 недели после первой иммунизации и через 2 недели после стимулятора для определения титра антител IgG против столбнячного токсина у детенышей отбирали кровь, после чего мышей умерщвляли.
Для оценки различий в пролиферации Т-клеток и в действии противостолбнячной вакцины проводили анализы Манна-Уитни (Уилкоксона).
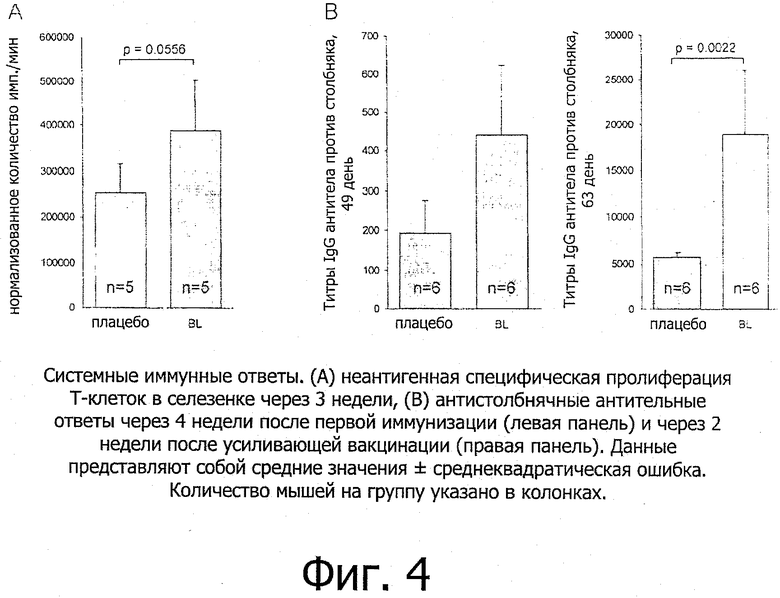
Результаты: На Фигуре 4 показано, что значительное увеличение антительных ответов после вакцинации столбнячным токсином наблюдали во всех группах, что отражает нормальный процесс созревания антител. Подкормка матерей «BL» в течение беременности и лактации способствует более высокой системной Т-клеточной реактивности и значительно повышает титры IgG по сравнению с плацебо.
Выводы: Два исследования в примерах 1 и 2 подчеркивают факт того, что возможно способствовать развитию иммунитета в потомстве посредством перинатального вмешательства, в частности через подкормку пробиотиками матерей в течение беременности и лактации. Данные эффекты являются зависимыми от штамма, о чем свидетельствует Исследование 1, однако они, по всей видимости, не являются зависимыми от вида. Действительно, подкормка беременных матерей «LPR» или «BL», по всей видимости, способствует более интенсивному созреванию иммунитета у потомства.

Изобретение относится к использованию пробиотиков для усиления иммунного статуса потомства, ожидаемого самками млекопитающих. Предложено применение пробиотиков - Lactobacillus rhamnosus CGMCC 1.3724 и/или Bifidobacterium lactis CNCM 1-3446 в производстве композиции для введения ожидающим потомства самкам млекопитающих для повышения после рождения иммунитета их потомства. Изобретение позволяет вызвать у потомства после рождения усиленный ответ на воздействие инфекционными антигенами, а также индуцировать у потомства лучшую защиту от инфекционных заболеваний. 15 з.п. ф-лы, 4 ил., 2 пр.
1. Применение пробиотиков Lactobacillus rhamnosus CGMCC 1.3724 и/или Bifidobacterium lactis CNCM 1-3446 в производстве композиции для введения ожидающим потомства самкам млекопитающих для повышения после рождения иммунитета их потомства.
2. Применение по п.1 для усиления функций врожденного иммунитета и/или содействия специфическому иммунному ответу на инфекционные антигены у указанного потомства.
3. Применение по п.1, где указанная композиция укрепляет передачу иммунной компетентности от указанных самок к указанному потомству.
4. Применение по п.1, где указанные самки млекопитающих являются людьми.
5. Применение по любому из пп. 1-4, где указанная композиция вводится указанным самкам перорально, предпочтительно с пищей, напитками, диетическими добавками или фармацевтическими композициями.
6. Применение по любому из пп. 1-4, где указанная композиция вводится в течение периода введения, где указанный период введения содержит часть периода беременности указанных самок.
7. Применение по п.6, где указанный период введения включает часть периода грудного вскармливания указанного потомства.
8. Применение по п.6, где указанный период введения включает часть указанной беременности и часть периодов лактации.
9. Применение по любому из пп. 1-4, где указанная композиция содержит дополнительные ингредиенты или пребиотики, предпочтительно выбранные из инулина, фруктоолигосахарида (ФОС), фруктоолигосахарида с короткой цепью (ФОС с короткой цепью), галактоолигосахарида (ГОС), ксилоолигосахарида (КОС), ганглиозида, частично гидролизованной гуаровой камеди, камеди акации, камеди соевых бобов, молочной композиции с ягодой годжи, экстракта ягоды годжи или их смесей.
10. Применение по любому из пп. 1-4, где указанное усиление иммунитета включает увеличение способности потомства отвечать на воздействие антигенами.
11. Применение по п.2, где указанный ответ на указанное воздействие антигенами содержит увеличение специфических антител на указанные антигены, предпочтительно в сыворотке, и/или в слюне, и/или в экскрементах указанного потомства.
12. Применение по п.2, где указанный ответ на упомянутое воздействие антигенами содержит увеличение общего количества полиреактивных антител, предпочтительно в сыворотке, и/или в слюне, и/или в экскрементах указанного потомства.
13. Применение по п.2, где указанный ответ на упомянутое воздействие антигенами содержит увеличение клеточного иммунного ответа в крови указанного потомства, предпочтительно увеличение количества и/или увеличение активности лейкоцитов указанного потомства.
14. Применение по любому из пп. 2, 11, 12 или 13, где указанное воздействие антигенами содержит воздействие вирусами, предпочтительно ротавирусами и аденовирусами, или воздействие инфекционными бактериями, предпочтительно Escherichia coli, Vibrio cholerae, сальмонеллами, клостридиями, шигеллами, или воздействие инфекцией контагиозных паразитов, предпочтительно Giardia lamblia, Entamoeba histolytica и Cryptosporidium spp. или их смесей.
15. Применение по п.2, где указанная способность к ответу на указанное воздействие антигенами вносит свой вклад в улучшенную защиту указанного потомства от инфекций в ранний период жизни, предпочтительно указанные инфекции содержат вирусные инфекции, такие как ротавирусные инфекции и аденовирусные инфекции, или бактериальные инфекции, такие как инфекция Escherichia coli, инфекция Vibrio cholerae, инфекция сальмонелл, инфекция клостридий, инфекция шигелл или паразитные инфекции, такие как инфекции Giardia lamblia, Entamoeba histolytica и Cryptosporidium spp.
16. Применение по п.1, где указанное усиление иммунитета достигает своего максимума в течение указанного периода лактации или в течение ювенильной фазы указанного потомства, предпочтительно между рождением (день 0) и 24 месяцами жизни, более предпочтительно между рождением (день 0) и 180-м днем жизни.
| WO 2007105945 А2, 20.09.2007 | |||
| WO 2007039313, 12.04.2007 | |||
| WO 2007144334 A1, 21.12.2007 | |||
| US 2006165669 A1, 27.07.2006. |
Авторы
Даты
2013-06-27—Публикация
2009-03-11—Подача