Область техники
Настоящее изобретение имеет отношение к улучшению толерантности у младенцев млекопитающих, в частности младенцев человека, к вновь вводимым продуктам питания в течение периода отлучения от груди путем введения пробиотика или смеси пробиотиков.
Уровень техники
Постнатальное созревание иммунной системы кишечника
Младенцы, как и другие детеныши млекопитающих, рождаются с функциональной, однако ранее не подвергавшейся воздействию, «наивной» (не тренированной) иммунной системой кишечника. Полная иммунная компетентность достигается постепенно после рождения и может достигаться только посредством развития иммунной системы при постепенном взаимодействии с внешними стимулами, такими как поглощенные белки и/или кишечная микрофлора. Такое постепенное созревание иммунокомпетентности в конечном счете приводит к способности различать вредные и безопасные воздействия (стимулы) и формировать соответствующие иммунные ответы (что означает воспаление после столкновения с патогенами и толерантность при столкновении с пищевыми компонентами и симбиотическими бактериями). Таким образом, младенчество является нестабильным временем для иммунной системы с возможным двойственным результатом, приводящим или к толерантности и защитному иммунитету, или к патологическим аллергическим иммунным ответам (Cummins и Thompson; 1997; Immunology и Cell Biology; 75, 419-29).
В течение постнатального созревания иммунной системы кишечника материнское молоко обеспечивает иммунную защиту и компенсирует отсутствие иммунной активности в кишечнике. Однако кормление исключительно грудным молоком может обеспечивать достаточное питание только в течение ограниченного времени после рождения, т.е. от 4 до 6 месяцев у младенцев человека. После этого периода в диету постепенно вводятся другие продукты питания для обеспечения пищевых потребностей младенца, и, таким образом, зависимость от молока или молочной смеси для обеспечения всех питательных веществ уменьшается. Этот процесс обычно называют периодом отлучения от груди. У младенцев человека введение прикорма и отлучение от груди происходит постепенно в возрасте от 3 до 12 месяцев. Однако возраст, в котором вводится прикорм, может варьировать в зависимости от географического местоположения и культурных различий (Aggett, P.J., Research priorities in complementary feeding: International Paediatric Association (IPА) и European Society of Paediatric Gastroenterology, Hepatology, и Nutrition (ESPGHAN) workshop. Pediatrics 2000; 106: 1271). Другие млекопитающие, такие как собаки и кошки, сами постепенно отучаются от материнского молока, начиная поедать прикорм в возрасте 3-4 недель, и становятся независимыми от молока в 8-10-недельном возрасте.
Созревание желудочно-кишечного тракта у младенцев и молодых млекопитающих включает целый ряд физиологических механизмов, которые протекают в младенческом возрасте и которые способствуют развитию незрелого желудочно-кишечного тракта в зрелый. Одной из ключевых стадий является адаптация к новой пище, которая в основном происходит в период отлучения от груди. Следовательно, адаптация к новым продуктам питания при отлучении от груди расценивается как важная часть созревания желудочно-кишечного тракта.
Иммунная система и физиология кишечника претерпевают изменения в период отлучения от груди
Иммунная система кишечника здорового молодого млекопитающего активируется в период отлучения от груди. Эта активация включает гуморальные и клеточные механизмы и представляет собой ответ на большое количество вновь встречающихся антигенов в результате изменения источников питания (при переходе от молока к твердой пище). Показано, что эта первоначальная иммунная активация при отлучении от груди, в ответ на воздействие нового питания у млекопитающих, является транзиторной (преходящей). У крыс, например, отлучение связано с увеличенным количеством клеток в мезентериальных лимфатических узлах (MLN), увеличенным количеством лимфоцитов в тощей кишке и дегрануляцией мастоцитов. У младенцев человека наблюдается распространение дуоденальных мастоцитов и увеличение интраэпителиальных лимфоцитов (Thompson, F.M., Mayrhofer G, Cummins A.G., Dependence of epithelial growth of the small intestine on T-cell activation during weaning in the rat, Gastroenterology 1996; 111:37-44). Кроме того, у мышей было обнаружено, что количество клеток, спонтанно секретирующих цитокины, постепенно увеличивается в ходе отлучения от груди (Vazquez, Е., Gil, A., Garcia-Olivares, Е., Rueda, R., Weaning induces an increase in the number of specific cytokine-secreting intestinal lymphocytes in mice, Cytokine 2000; 12: 1267-70).
Полагают, что транзиторная иммунная активация во время отлучения от груди необходима для развития интестинальной (кишечной) иммунной системы, которая в дальнейшем переходит в состояние толерантности у растущего младенца в отношении безвредных стимулов (например, пищи, симбиотических бактерий). Широко известно, что одним из путей физиологического достижения интестинальной толерантности является применение понижающей регуляции первоначальных локальных иммунных ответов в отношении новых стимулов.
Отлучение от груди не только оказывает влияние на интестинальную иммунную систему, но также стимулирует существенные, вызванные питанием изменения в метаболизме и морфологии в кишечнике. Интестинальную морфологию обычно оценивают с помощью морфометрии ворсинок (длина ворсинок или площадь ворсинок) и крипт (длина и деление крипт). Например, у младенцев человека наблюдается увеличение деления крипт в возрасте 6-12 месяцев, а также увеличение длины крипт в возрасте от 12 до 24 месяцев и уменьшение площади ворсинок в период отлучения (Cummins, A.G., Catto-Smith A.G., Cameron, D.J. et al., Crypt fission peaks early during infancy и crypt hyperplasia broadly peaks during infancy и childhood in the small intestine of humans, J. Pediatr. Gastroenterol. Nutr., 2008; 47: 153-7). Как и в случае иммунной системы, большая часть этих морфологических изменений является транзиторной и достигает равновесия у детей в возрасте около 4 лет, напоминая взрослое состояние.
К сожалению, активированный иммунный статус здорового молодого млекопитающего при отлучении от груди (необходимый для соответствующих иммунных ответов в течение последующей жизни), а также морфологические изменения в кишечнике делают молодое млекопитающее более восприимчивым к стрессовым воздействиям, с которым оно может встретиться в это время. Эта восприимчивость может привести к осложнениям, связанным с отлучением от груди, таким как весьма распространенная хроническая неспецифическая диарея у детей (Kleinman, R.E., Chronic nonspecific diarrhea of childhood, Nestle Nutr. Workshop Ser. Pediatr. Program, 2005; 56: 73-9) или неадекватный ответ иммунной системы на пищевые белки, а именно пищевой аллергии, гиперчувствительности и энтероколиту, индуцированному пищевыми белками (FPIES) (Nowak-Wegrzyn, A., Muraro, A., Food protein-induced enterocolitis syndrome, Curr. Opin. Allergy Clin. Immunol., 2009; 9: 371-7). Несомненно, упомянутые выше патологические состояния, связанные с отлучением от груди, являются причиной дискомфорта для молодого млекопитающего.
Кроме того, с увеличением потребления прикорма младенец подвергается действию большего числа потенциально патогенных микроорганизмов (Sheth, М., Dwivedi, R., Complementary foods associated diarrhea, Indian J. Pediatr., 2006; 73: 61-4), при этом увеличивается риск инфекции. Во время отлучения от груди потребление пищи увеличивается, тогда как потребление грудного молока постепенно уменьшается. Таким образом, имеет место меньшее потребление иммунных защитных веществ, обнаруженных в человеческом молоке, в то время когда эти вещества являются наиболее необходимыми, а иммунная система молодого млекопитающего еще не способна полностью обеспечить эти факторы.
Осложнения в период отлучения от груди являются особенно вредоносными, так как формирование иммунной системы в это время может иметь продолжительное влияние на то, как будут решаться связанные с иммунитетом проблемы в дальнейшей жизни. Например, это было показано при пищевой аллергии, диабете 1 типа и глютеиновой болезни.
Микрофлора желудочно-кишечного тракта и отлучение от груди
Одним из основных факторов, управляющих развитием и созреванием иммунной системы, является раннее образование колоний микроорганизмов. Показано, что животные, выращенные в безмикробных (стерильных) условиях, имеют сильно недоразвитую иммунную систему кишечника, которая может быть восстановлена путем введения симбиотических бактерий и/или пробиотиков. Кроме того, было показано, что в течение первых месяцев жизни млекопитающие претерпевают значительное изменение в составе кишечной микрофлоры. Тогда как во время грудного вскармливания доминируют бифидобактерии (Bifidobacteria), с введением прикорма микрофлора становится более сложной. После отлучения от груди преобладают Bacteroitedes, Enterococci и анаэробные кокки.
Так как процесс отлучения от груди связан с изменением характера кишечного микробного сообщества, этот период является промежутком времени для вмешательства, например, с использованием пробиотиков. Более того, изменение развития микрофлоры путем воздействия пробиотиками во время отлучения от груди может иметь более явно выраженное влияние на последующую функцию иммунной системы, чем введение пробиотиков взрослым людям.
Таким образом, не удивительно, что отлучение от груди является решающим и физиологически сложным временем в ходе нормального развития и рассматривается как стресс для молодого млекопитающего. Соответственно, существует необходимость оказания помощи молодому млекопитающему на всем протяжении критического периода отлучения от груди при минимальном возможном дискомфорте, в то же время, обеспечивая потребление соответствующей пищи для удовлетворения пищевых потребностей. Существует необходимость обеспечить терапевтическое лечение, которое может предотвратить состояния, связанные с отлучением от груди, в частности упомянутые в параграфе выше, включая хроническую неспецифическую диарею у детей и энтероколит, индуцированный пищевыми белками (FPIES). Существует необходимость обеспечить профилактическое терапевтическое лечение, чтобы предотвратить или ослабить симптомы состояний, связанных с отлучением от груди.
В дополнение к этому, существует необходимость в облегчении и ускорении адаптации кишечника молодого млекопитающего к новым продуктам питания, вводимым в течение периода отлучения от груди.
Существует необходимость в индуцировании или поддержании толерантности к вновь вводимым в течение периода отлучения от груди продуктам питания.
Существует необходимость в предотвращении и лечении дискомфорта в кишечнике, который испытывают молодые млекопитающие в период отлучения от груди. Этот дискомфорт может быть незначительным и может не указывать на определенное патологическое состояние. Альтернативно, этот дискомфорт может быть тяжелым, являющимся причиной боли и продолжительного плача младенца. Этот дискомфорт может быть связан с тяжелыми патологическими состояниями.
Сущность изобретения
Настоящее изобретение отвечает описанным выше потребностям. Изобретение основывается на введении пробиотика здоровым молодым млекопитающим в течение критического периода отлучения от груди (у младенцев этот период обычно приходится на возраст примерно от 3 месяцев до 12, 18 или 24 месяцев), для того чтобы ускорить адаптацию молодого млекопитающего к новой пище. Эффективность изобретения явствует из морфологических и иммунологических изменений, наблюдаемых на модели отлучения от груди поросят, при этом были определены физиология ворсинок слизистой кишечника, уровни антиген специфических IgG1 и IgG2 в сыворотке и количество и тип В-клеточных фолликулов в клетках MLN (мезентериального лимфатического узла).
Таким образом, введение пробиотика приводит к стимулированию транзиторного повышения гуморального иммунного ответа, в частности выработке иммуноглобулина класса G, после воздействия вновь введенных пищевых продуктов. Это увеличение происходит более быстро и/или в большей степени по сравнению с увеличением, происходящим у молодых млекопитающих, не получавших пробиотик.
Таким образом, введение пробиотика во время отлучения от груди приводит к увеличению более чем на 15% высоты и/или площади ворсинок слизистой кишечника по сравнению с молодыми млекопитающими, не получавшими пробиотик.
Изобретение касается предотвращения патологических состояний, связанных с отлучением от груди, таких как хроническая неспецифическая диарея у детей, неадекватный ответ иммунной системы на пищевые белки, а именно пищевой аллергии, гиперчувствительности и FPIES. Таким образом, симптомы, связанные с отсутствием толерантности к вновь введенной пище во время отлучения от груди, предотвращаются или уменьшаются в период отлучения от груди и в дальнейшей жизни. В то же время, воздействие делает возможной нормальную иммунную адаптацию молодого млекопитающего. Таким образом, период, в течение которого молодое млекопитающее имеет повышенную чувствительность вследствие отлучения от груди, уменьшается.
Таким образом, введение пробиотика согласно изобретению обладает профилактическим действием, предотвращая тяжелый дискомфорт и патологические состояния, связанные с введением новых продуктов питания в течение периода отлучения от груди.
Изобретение также преследует цель предотвращения минимального дискомфорта в кишечнике, связанного с отлучением от груди.
Введенный пробиотик предпочтительно представляет собой Bifidobacterium animalis подвид lactis (В. lactis), штамм В. lactis CNCM-I-3446, также известный как В. lactis NCC2818. Пробиотик может быть живым или инактивированным (т.е. приведенным в состояние, при котором он не способен воспроизводиться). Ежедневная доза, которая может использоваться, составляет от 102 до 1×1011, предпочтительно от 1×106 до 1×109 КОЕ или эквивалент КОЕ в случае неспособных к воспроизведению микроорганизмов.
Пробиотик может вводиться в чистом виде, или разведенным в воде, или в составе композиции, подходящей для введения молодым млекопитающим. Композиция может содержать другие дополнительные пробиотики, предпочтительно выбранные из Bifidobacterium longum ВВ536 (АТСС ВАА-999), Lactobacillus rhamnosus fCGMCC 1.3724), Lactobacilus reuteri или их смесей. Композиция также может содержать такие пребиотики, как инулин, фруктоолигосахарид (FOS), фруктоолигосахарид с короткой цепью (FOS с короткой цепью), галактоолигосахарид (GOS), ксилоолигосахарид (XOS), арабиноксилан-олигосахариды (AXOS), ганглиозиды, в частности гидролизованную гуаровую камедь, аравийскую камедь, соевую камедь. Композиция также может содержать не пребиотики, подобные молочной смеси ягод годжи, экстрактам ягод годжи или их смеси.
Композиция может быть молочной смесью, детской смесью в период прикорма или молочной смесью для детей 1-3 лет, детским зерновым продуктом или йогуртом, детским питанием, пудингом или сыром, молочным и фруктовым напитком, смузи, легкой закуской, или сухим печеньем, или другим хлебобулочным изделием. Композиция может быть в форме продукта длительного хранения или высушенного сублимацией продукта, или может быть получена с помощью экструзии, асептического процесса или автоклавирования.
Краткое описание чертежей
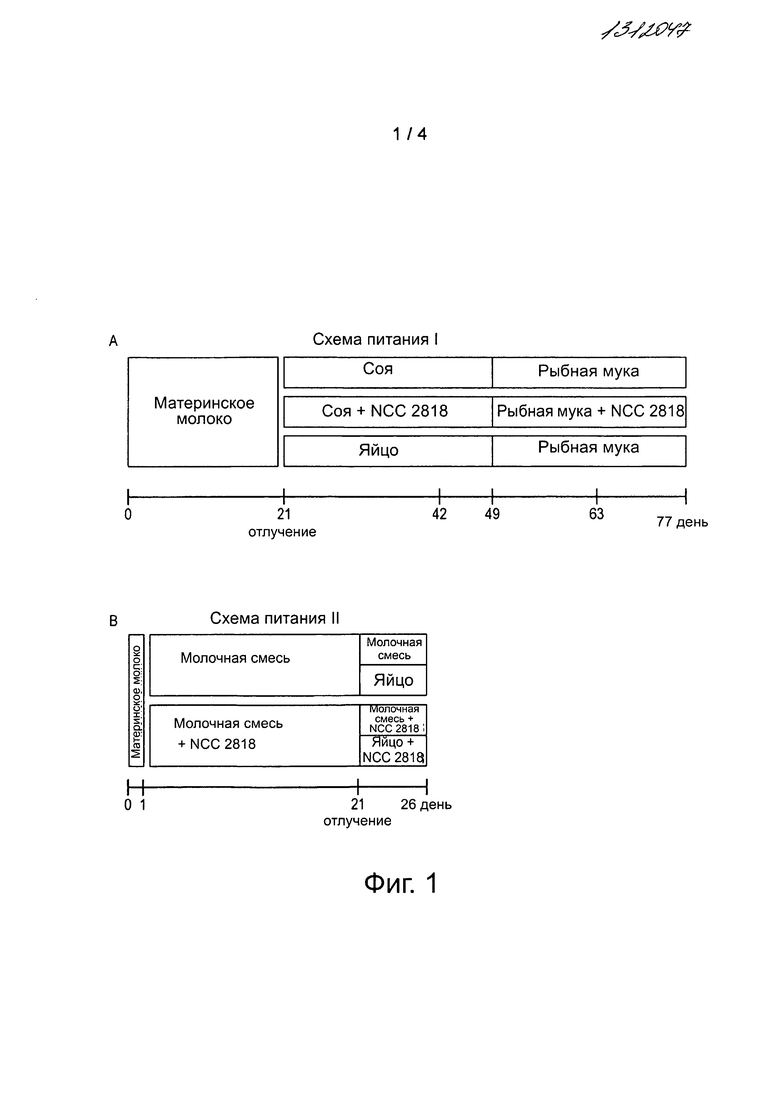
Фигура 1: Схемы кормления
А: Схема кормления I: Поросят отлучали от материнского молока и переводили на твердую пищу (соя или белки на основе OVA (яиц) соответственно), а одной группе добавляли NCC2818. Все группы получали рыбную муку с 49 дня до завершения эксперимента на 77 день, n=6.
В: Схема кормления II: Поросят кормили молочной смесью с возраста 24 часа с добавлением или без добавления NCC2818. Затем половину поросят из каждой группы или переводили на диету на основе яичного белка или продолжали кормить молочной смесью. Эксперимент заканчивался в 25-дневном возрасте, n=6.
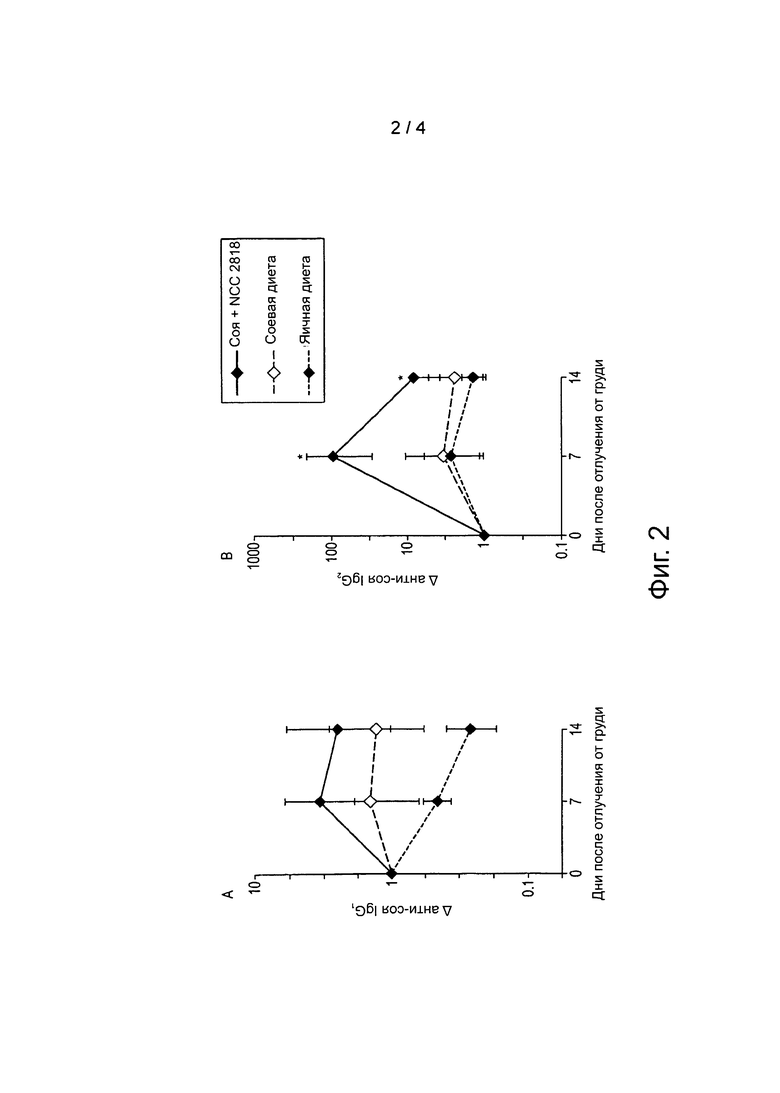
Фигура 2: Ответ сывороточного IgG на кормление соей
Изменение сояспецифических IgG1 (А) и IgG2 (В) в сыворотке поросят, которых кормили соей с добавлением NCC2818 (Соя + NCC2818), или без добавления NCC2818 (Соевая диета), или яичным белком (Яичная диета). Планки погрешностей = SEM (стандартная ошибка среднего) (n=14). Результаты выражены как изменение уровней антител к сое после воздействия по сравнению с уровнями до воздействия (кратное изменение антител).
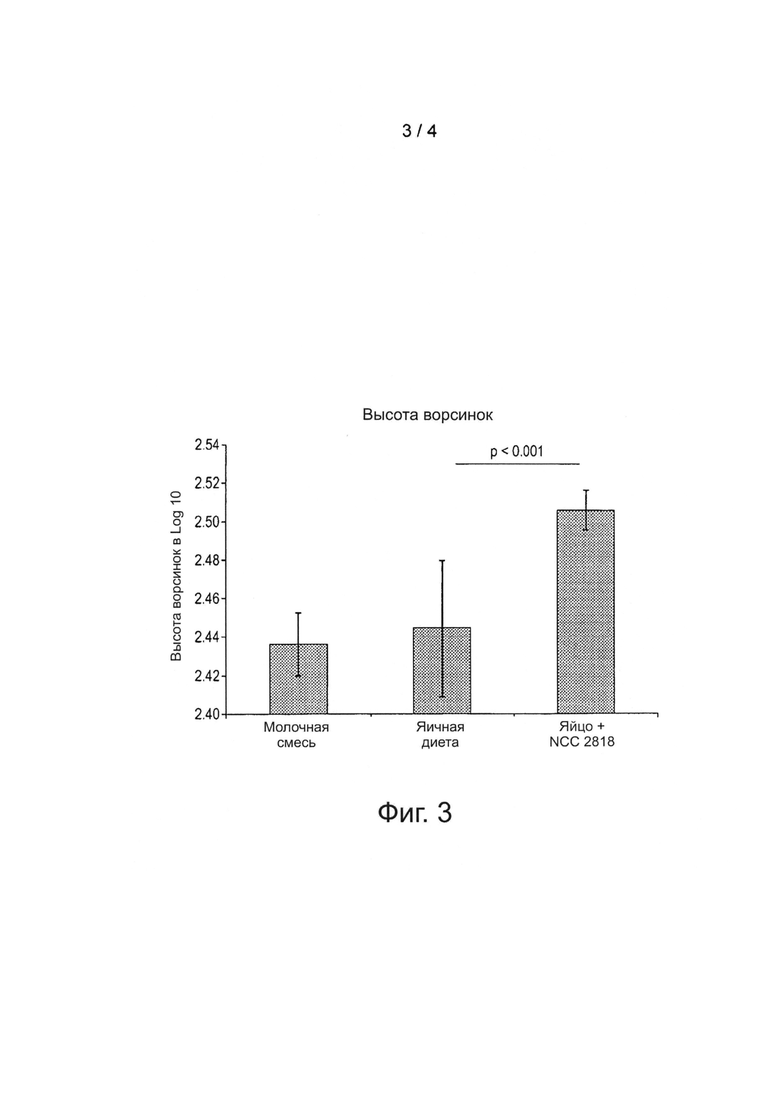
Фигура 3: Гистоморфометрия интестинальной слизистой (дистальный тонкий кишечник)
Высота ворсинок у поросят, которых кормили соей с добавлением или без добавления NCC2818, начиная с возраста 24 часа. Поросят или переводили на твердую пищу (Яичная диета, Яичная диета + NCC2818) на 21 день, или держали на молочной смеси для поросят (Молочная смесь). Гистоморфометрические исследования проводили после завершения эксперимента на 25 день. Результаты представлены как среднее Iog10 мм ± стандартная ошибка (SE).
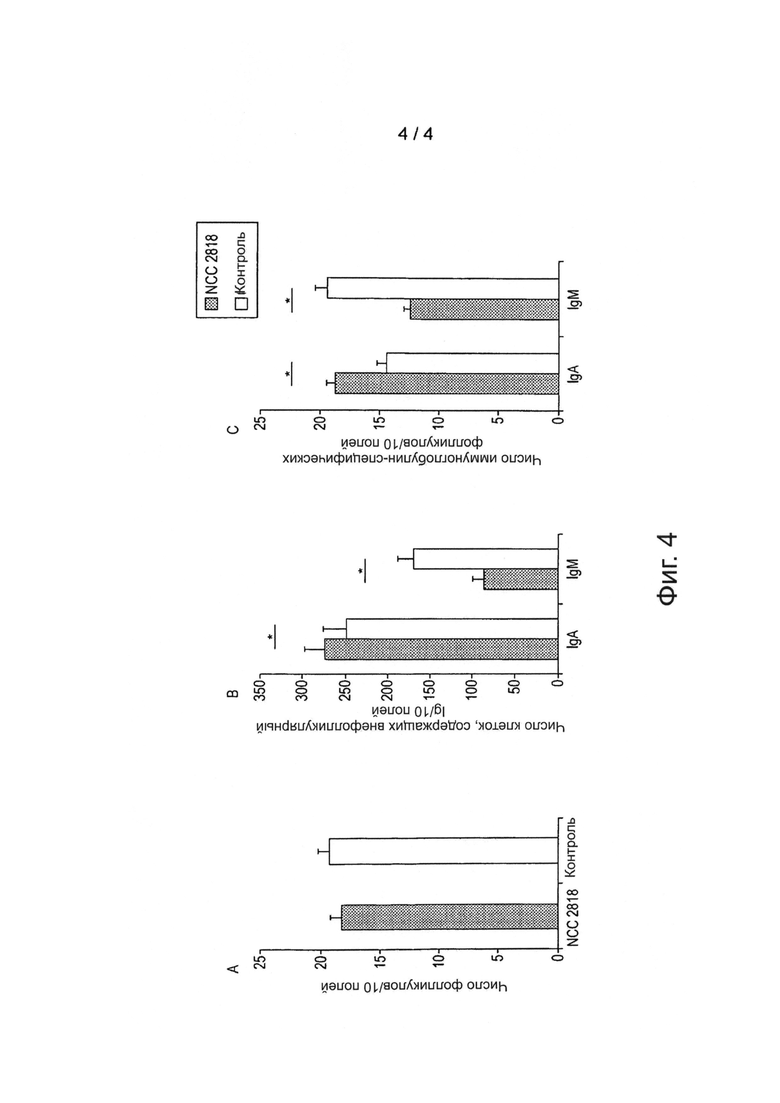
Фигура 4: Флуоресцентная иммуногистология В-клеточных фолликулов в клетках мезентериального лимфатического узла (MLN)
Общее число фолликулов (А), экспрессирующих IgA и IgM во внефолликулярных клетках (В), и число IgA или IgM положительных фолликулов (С) у поросят, которых кормили соей с добавлением или без добавления В. lactis NCC2818 с начала периода отлучения на день 21. Планки погрешностей = SEM (n=6).
Раскрытие изобретения
Определения
В настоящем описании следующие термины имеют следующие значения.
"Период отлучения от груди" - это период, в течение которого молодые млекопитающие адаптируются при переходе от питания на основе чистого жидкого молока к полутвердым или твердым продуктам питания и адаптируются при переходе от единственно возможного типа питания (как правило, в случае младенцев, материнского молока или молочной смеси) к целому ряду продуктов питания.
"Толерантность" означает активное состояние низкой реактивности на пищевые продукты.
"Пробиотик" означает препараты микробных клеток или компоненты микробных клеток, оказывающие благоприятное воздействие на здоровье или самочувствие хозяина (Salminen, S., Ouwehand, A. Benno, Y. et al., Probiotics: how should they be defined, Trends Food Sci. Technol. (1999): 10 107-10). Определение пробиотика является общепризнанным и согласуется с определением ВОЗ. Пробиотик может включать один штамм микроорганизма, смесь различных штаммов и/или смесь разных видов и родов бактерий. В случае смесей термин "пробиотик" в единственном числе может тем не менее использоваться для обозначения пробиотической смеси или препарата. Для цели настоящего изобретения микроорганизмы рода Bifidobacterium считаются пробиотиками.
"Пребиотик", как правило, означает неусвояемый пищевой ингредиент, оказывающий благотворное действие на хозяина путем селективного стимулирования роста и/или активности микроорганизмов, присутствующих в кишечнике хозяина, и таким образом предпринимается попытка улучшить здоровье хозяина.
Bifidobacterium animalis подвид lactis (В. lactis) штамм NCC2818 (коллекция культур Nestle) представляет собой В. lactis, размещенный на хранение под международным идентификационным обозначением CNCM-I-3446 (Французская национальная коллекция культур микроорганизмов института Пастера, Париж, Франция). На всем протяжении текста используется В. lactis NCC2818. Маркировка CNCM имеет отношение к Национальной коллекции культур микроорганизмов при институте Пастера, 22 rue du docteur Roux, 75724 Paris, France.
Изобретение касается введения пробиотика, в частности В. lactis NCC2818 (В. lactis CNCM-I-3446), здоровым молодым млекопитающим во время периода отлучения от груди, т.е. когда молодое млекопитающее начинает потреблять немолочные продукты и все меньше и меньше зависит от молока при удовлетворении пищевых потребностей. У младенцев человека этот период обычно происходит при достижении младенцем возраста приблизительно от 3 до 12 месяцев, хотя этот период может продолжаться до 18, 24 или даже до 36-месячного возраста. В большинстве случаев младенцы продолжают регулярно сталкиваться с новыми продуктами питания до достижения этого и даже более старшего возраста.
Подробности способа введения пробиотика даны в следующих параграфах.
Как показывают экспериментальные данные, полученные в Примере 1, введение В. lactis NCC2818 поросятам в период отлучения от груди может заметно влиять на структуру и функции иммунной системы, связанной со слизистой кишечника. Введение пробиотика согласно изобретению ускоряет адаптацию молодого млекопитающего к вновь вводимым пищевым продуктам и улучшает толерантность молодого млекопитающего к вновь вводимым пищевым продуктам. Таким образом, такое воздействие обеспечивает способ оказания содействия иммунной адаптации младенцев во время периода отлучения от груди. Все младенцы могут получить пользу от настоящего изобретения, включая младенцев, имеющих риск развития атопических болезней вследствие семейного анамнеза.
Дозы пробиотиков
Ежедневные дозы В. lactis NCC2818, предназначенные для введения молодому млекопитающему, составляют примерно от 1×106 до 1×1011 КОЕ, предпочтительно от 1×106 до 1×109 КОЕ.
В. lactis NCC2818 может присутствовать в композиции, предназначенной для введения молодому млекопитающему, в разных процентных содержаниях при условии, что наблюдается описанное положительное воздействие. Таким образом, количество присутствующего пробиотика на грамм сухой композиции, предназначенной для введения, может варьировать при условии, что описанные выше ежедневные дозы не нарушаются. Однако предпочтительно В. lactis NCC2818 присутствует в композиции в количестве, эквивалентном в пределах от 1×102 до 1×1011 КОЕ/г сухой композиции, предпочтительно от 1×104 до 1×109 КОЕ/г сухой композиции. Это включает возможность того, что бактерии являются живыми, инактивированными, или убитыми, или даже присутствуют в виде фрагментов, таких как ДНК или материалы клеточных стенок. Для перевода пробиотика в состояние неспособности к воспроизведению могут использоваться известные в данной области техники методы. Таким образом, количество бактерий, содержащихся в молочной смеси, выражается в виде количества бактерий, способных к колониеобразованию, как если бы все бактерии были живыми, независимо от того являются ли они в действительности живыми, инактивированными или убитыми, фрагментированными или смесью любых или всех из этих состояний.
Способ введения
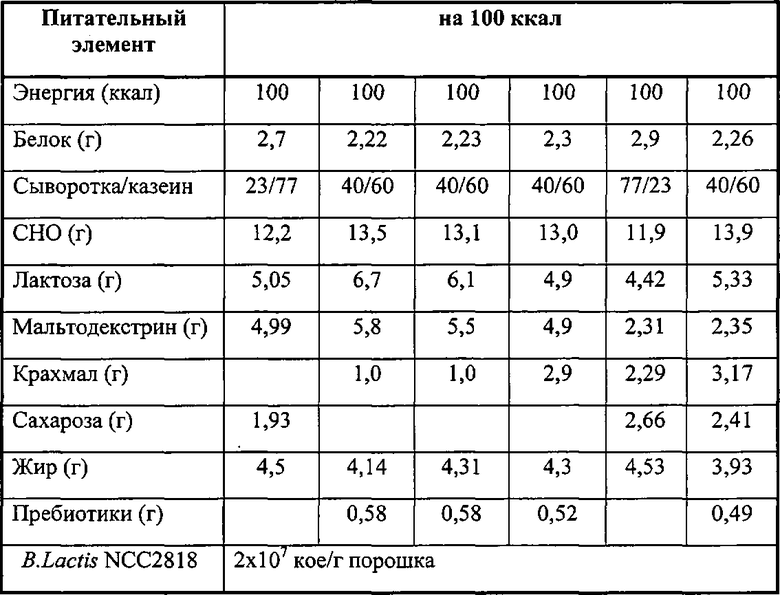
В. lactis NCC2818 может вводиться молодому млекопитающему перорально; он может быть в чистом виде или разведенным в воде или материнском молоке, например, в виде диетической добавки или в виде ингредиента в молочной смеси для детского питания. Такая смесь может быть "первичной молочной смесью" для младенцев, если введение пробиотика начинается до достижения младенцем 6-месячного возраста, или "детской смесью в период прикорма", если младенец старше 6-месячного возраста. Пример такой «первичной молочной смеси» представлен в Примере 2. Смесь также может быть гипоаллергенной (НА) смесью, в которой белки коровьего молока являются гидролизованными.
Если молодое млекопитающее находится в возрасте от 12 до 24 месяцев, пробиотик может вводиться в молочной смеси для детей 1-3 лет, детском зерновом продукте или йогурте, детском питании, пудинге или сыре, молочном и фруктовом напитке, смузи, легкой закуске, или сухом печенье, или другом хлебобулочном изделии. Пример такой молочной смеси для детей 1-3 лет дан в Примере 3. Композиция может быть в форме продукта длительного хранения или высушенного сублимацией продукта или может быть получена с помощью экструзии, асептического процесса или автоклавирования.
Введение с другими составами
В. lactis NCC2818 может вводиться вместе с одним или более дополнительными пробиотиками. Эти пробиотики предпочтительно выбирают из Bifidobacterium longum ВВ536 (АТСС ВАА-999); Lactobacillus rhamnosus (CGMCC 1.3724); Lactobacilus reuteri или их смесей.
В. lactis NCC2818 может быть введен отдельно (в чистом виде или разведенным в воде или молоке, включая, например, грудное молоко) или в смеси с другими соединениями (такими как диетические добавки, питательные добавки, лекарственные средства, носители, ароматические вещества, усвояемыми или трудноусваиваемыми ингредиентами). Витамины и минералы являются примерами типичных диетических добавок. В предпочтительном варианте изобретения композицию вводят вместе с другими соединениями, усиливающими описанное действие на иммунитет потомства. Такие синергетические (взаимоусиливающие) соединения могут быть носителями или матрицей, облегчающей доставку В. lactis NCC2818 в кишечник молодого млекопитающего. Такие соединения могут представлять собой другие активные соединения, которые влияют на иммунный ответ младенца синергетически или в отдельности, и/или усиливать действие пробиотика. Примером таких синергетических соединений является мальтодекстрин. Одно свойство мальтодекстрина состоит в том, чтобы обеспечивать носитель для пробиотика, усиливая его действие, и предотвращать агрегацию.
Другие примеры включают известные пробиотические соединения, такие как углеводные соединения, выбранные из группы, состоящей из инулина, фруктоолигосахарида (FOS), фруктоолигосахарида с короткой цепью (FOS с короткой цепью), галактоолигосахарида (GOS), ксилоолигосахарида (XOS), арабиноксилан-олигосахаридов (AXOS), ганглиозидов, частично гидролизованной гуаровой камеди (PHGG), аравийской камеди, соевой камеди, яблочного экстракта и непребиотических соединений, таких как молочные смеси ягод годжи, экстракты ягод годжи или их смеси. Могут присутствовать другие углеводы, такие как второй углевод, который может действовать в синергизме с первым углеводом. Углевод или углеводы могут присутствовать в количестве примерно от 1 г до 20 г, или от 1% до 80%, или от 20% до 60% в ежедневных дозах композиции. Альтернативно, углеводы могут составлять от 10% до 80% сухой композиции.
Ежедневные дозы углеводов и всех других соединений, вводимых вместе с В. lactis NCC2818, всегда должны соответствовать опубликованным руководствам по безопасности и нормативным требованиям. Это особенно важно в отношении введения младенцам в возрасте до одного года.
В одном варианте осуществления питательная композиция предпочтительно содержит источник белка. В качестве источника белка предпочтительным является пищевой белок. Пищевой белок может быть любым подходящим пищевым белком, например, животными белками (такими как белки молока или белки мяса), растительными белками (такими как белки сои, белки пшеницы, белки риса или белки гороха), смесью свободных аминокислот или их комбинацией. Особенно предпочтительными являются молочные белки, такие как казеин и белки пшеницы.
Композиция может содержать источник углеводов и/или источник жира.
Если композиция изобретения является питательной композицией и включает источник жира, предпочтительно источник жира обеспечивает примерно от 5% до 55% энергии питательной композиции, например примерно от 20% до 50% энергии.
Источником липидов может быть любой подходящий жир или смесь жиров. Растительный жир является особенно предпочтительным, например соевое масло, пальмовое масло, кокосовое масло, сафлоровое масло, подсолнечное масло, кукурузное масло, масло канолы, лецитин и тому подобное. При желании также может быть добавлен животный жир, такой как молочный жир.
В питательную композицию может быть добавлен дополнительный источник углевода. Предпочтительно он обеспечивает примерно от 40% до 80% энергии питательной композиции. Может использоваться любой подходящий углевод, например сахароза, лактоза, глюкоза, фруктоза, сухая кукурузная патока, мальтодекстрин или их смеси. При желании также может быть добавлено дополнительное пищевое волокно (клетчатка). Если его добавляют, оно предпочтительно содержит примерно до 5% энергии питательной композиции. Пищевое волокно может быть из любого подходящего источника, включая, например, сою, горох, овес, пектин, гуаровую камедь, аравийскую камедь, фруктоолигосахарид или их смесь. В питательную композицию могут включаться подходящие витамины и минералы в количестве, необходимом для выполнения соответствующих указаний.
В композицию может быть включена одна или более незаменимых жирных кислот с длинной цепью (LC-PUFA). Примеры LC-PUFA, которые можно добавлять, включают докозагексаеновую кислоту (DHA) и арахидоновую кислоту (АА). LC-PUFA могут быть добавлены в таких концентрациях, чтобы они составляли больше чем 0,01% жирных кислот, присутствующих в композиции.
При необходимости в питательную композицию может быть включено одно или более пищевых эмульгирующих веществ, например сложные эфиры диацетилвинной кислоты и моно- и ди- глицеридов, лецитин и моно- или диглицериды или их смеси. Аналогично, могут быть включены подходящие соли и/или стабилизирующие вещества. К композиции могут быть добавлены ароматические вещества.
Период введения
Начало периода введения, как правило, совпадает с началом периода отлучения от груди, т.е. в тот момент, когда вводится первый немолочный продукт питания. Альтернативно, введение В. lactis NCC2818 может начинаться незадолго до этого времени, например за одну или две недели до введения первого немолочного продукта питания. Кроме того, это может происходить вскоре после введения первого немолочного продукта питания. Однако считается, что положительные эффекты являются наиболее значительными, если воздействие пробиотиком совпадает с первым введением новых продуктов питания или происходит до этого момента.
Что касается младенцев человека, возраст, при котором начинается отлучение от груди, может зависеть от культуры, в которой рождается младенец, ввиду того, что отлучение от груди в различных культурах совершается в разном возрасте. Во многих случаях отлучение начинается в 3-7-месячном возрасте младенца. Таким образом, в таком случае введение пробиотика может начинаться, когда начинается отлучение, т.е. примерно в 3-7-месячном возрасте младенца или за 1-4 недель до этого момента.
Введение может начинаться даже раньше, например, за 3, 4, 5, 6, 7, 8, 9 или 10 недель до начала отлучения от груди.
Период введения пробиотиков может быть непрерывным, например каждый день вплоть до достижения младенцем возраста, по меньшей мере, 12 месяцев. Непрерывное введение является предпочтительным для достижения более продолжительного эффекта. Однако предполагается, что введение с перерывами (например, ежедневное введение в течение одной недели в месяц, или введение через неделю) может оказывать благотворное воздействие на младенца.
Продолжительность введения пробиотика может варьировать и различается в соответствии с культурой, в которой рожден младенец. Положительные эффекты ожидаются даже при короткой продолжительности введения, например в течение одного, двух или трех месяцев, если введение начинается в то же самое время, когда начинается отлучение или немного раньше. Более длительное введение будет обеспечивать положительный эффект у молодого млекопитающего в течение более длительного периода. Как правило, введение пробиотика продолжается до достижения младенцем, по меньшей мере, 12-месячного возраста. Введение может продолжаться вплоть до достижения ребенком возраста 18 месяцев, или 24 месяцев, или даже вплоть до 3-летнего возраста. В большинстве случаев дети продолжают регулярно сталкиваться с новыми продуктами питания вплоть до 4-летнего возраста.
Предпочтительно введение младенцу осуществляется ежедневно или через день, пробиотик принимается внутрь один или два раза в день.
Эффект введения пробиотика
Введение В. lactis NCC2818 младенцам во время периода отлучения от груди улучшает толерантность к вновь вводимым продуктам питания. Это было продемонстрировано в ряде экспериментов с использованием модели отлучения от груди поросят, как подробно показано в Примере 1. Модель на поросятах была использована изобретателями для изучения влияния В. lactis NCC2818 при отлучении от груди, потому что поросята в большей мере сопоставимы с людьми, чем грызуны, в их развитии при рождении и постнатально. Кроме того, последнее сравнение 147 генотипических, фенотипических и функциональных параметров у мышей, свиней и людей показало, что 80% этих параметров были более похожими между свиньями и людьми, чем между мышами и людьми (Wernersson R, Schierup МН, Jorgensen FG, et al., 2005, Pigs in sequence space: A 0.66X coverage pig genome survey based on shotgun sequencing. BMC Genomics, 6: 70).
Представленные здесь результаты ясно показывают, что введение В. lactis NCC2818 поросятам в период отлучения от груди может оказывать заметное воздействие на структуру и функцию иммунной системы, связанной со слизистой кишечника.
В одном варианте изобретения транзиторное увеличение общих IgG, специфичных к вновь вводимому белку, которое в норме наблюдается в период отлучения от груди, усиливается. Это увеличение происходит более быстро и/или в большей степени в том случае, когда отлучение от груди сопровождается введением В. lactis NCC2818.
Таким образом, в Примере 1 поросята, которых кормили согласно Схеме кормления 1 (Фигура 1А), были отлучены от материнского молока через 3 недели и переведены на соевую диету, соевую диету с добавлением В. lactis NCC2818, смешанного со смесью, в концентрации 4.2×106 КОЕ/мл (приблизительно 2×109 КОЕ/кг метаболический вес/день), или на яичную диету. Уровни специфических к сое IgG1 и IgG2 в сыворотке животного в каждой группе определяли на 0, 7 и 14 дни после отлучения (см. Фигура 2). Это соответствует 21, 28 и 35 дням после рождения (Фигура 1А). Было обнаружено, что кормление поросят в период отлучения белком, ранее неизвестным для иммунной системы, приводит к транзиторному увеличению специфического IgG в сыворотке через одну и две недели после отлучения от груди. Также было обнаружено, что при добавлении В. lactis NCC2818 в соевую диету у поросят наблюдается значительно более высокое увеличение в сыворотке специфического к сое IgG2 (p=0.03; Фигура 2 В) и тенденция к более высокому увеличению специфического к сое IgG1 (Фигура 2А).
Ответные реакции на пищевые белки в виде повышения сывороточных IgG антител связаны со сниженной восприимчивостью к аллергической болезни, опосредованной IgE, у людей и к диарее у свиней после отъема от матки (Li, D.F. et al., Interrelationship between Hypersensitivity to Soybean Proteins и Growth-Performance in Early-Weaned Pigs, Journal of Animal Science, 1991; 69: 4062-4069 и Strait, R.T., et al. Ingested allergens must be absorbed systemically to induce systemic anaphylaxis, Journal of Allergy и Clinical Immunology; 127: 982-989.el.).
Таким образом, более высокое транзиторное увеличение специфических к сое IgG, которое наблюдалось у поросят при добавлении В. lactis NCC2818 в Примере 1, показывает, что введение В. lactis NCC2818 во время отлучения от груди ускоряет и повышает уровень адаптации иммунной системы поросят к вновь вводимому белку.
В другом варианте осуществления высота ворсинок у молодого млекопитающего увеличивается в том случае, когда отлучение сопровождается введением В.lactis NCC2818.
Высота ворсинок может служить индикатором хорошего здоровья у младенцев. Атрофия ворсинок нередко наблюдается при сопутствующих болезнях желудочно-кишечного тракта, таких как глютеиновая болезнь, или вирусных инфекциях (Cummins, А. et al., American Journal of Gastroenterology, 2011, 106, 145-50; и Boshuizen, et al.; Journal of Virology, 2003, 77 (24), 13005-16). Также у поросят было показано, что на сильное нарушение целостности кишечника указывает, в числе прочего, уменьшение длины ворсинок. Напротив, следующая за этим адаптация характеризуется увеличением длины ворсинок в тощей кишке (Montagne, L. et al., British Journal of Nutrition, 2007, 97, 45-57). Таким образом, большая высота ворсинок соответствует адаптированному к новым продуктам питания кишечнику.
Фигура 3 показывает гистоморфометрию интестинальной слизистой (дистальный тонкий кишечник) у животных после применения схемы кормления II (Фигура 1). Сильные изменения в морфологии слизистой вследствие отлучения происходят в пределах 2-5 дней после отлучения. Так как целью эксперимента было продемонстрировать благоприятное воздействие В. lactis NC2818 на морфологию слизистой кишечника, экспериментальный протокол схемы кормления II был соответствующим образом скорректирован. Учитывая, что для достижения эффекта пробиотика необходима некоторая длительность кормления, кормление этих животных было начато в возрасте 24 часа. Таким образом, была измерена длина ворсинок (А) у поросят, которых кормили, начиная с 24 часов после рождения и дальше с добавлением В. lactis NCC2828 или без добавления. Свиней или переводили на твердую пищу (яичная диета, яичная диета+NCC2818) на 21 день, или оставляли на смеси для поросят (молочная смесь).
Высоту ворсинок определяли на 25 день. Панель А демонстрирует увеличение высоты ворсинок в группе, которую кормили яичной диетой с добавлением В. lactis NCC2818, по сравнению с группой без добавления. Достаточная высота ворсинок обычно считается одним из признаков физиологически функциональной и хорошо развитой слизистой кишечника. Обеспечение высоты ворсинок обычно рассматривается как защитное средство. Следовательно, увеличение высоты ворсинок при использовании В. lactis NCC2818 может считаться признаком мукозальной защиты.
В другом варианте осуществления добавление В. lactis NCC2818 при отлучении от груди, по-видимому, способствует сдвигу к определенным иммунным процессам в мезентериальных лимфатических узлах (MLN): от менее зрелого ответа с доминированием IgM антител к более зрелому ответу с преобладанием IgA.
Фигура 4 показывает флуоресцентную иммуногистологию В-клеточных фолликулов в MLN животных, Пример 1 Схема кормления I. При сравнении группы с добавлением В. lactis NCC2818) с группой без добавления видно, что общее число фолликулов в лимфатическом узле остается неизменным (Фигура 4А). Однако в группе с добавлением наблюдаются значительные различия в количестве и IgM-специфических фолликулов, и клеток, продуцирующих внефолликулярный IgM (p<0,0001; Фигура 4В, С). Кроме того, наблюдается значительное увеличение числа IgA-специфических фолликулов (p=0,04 и p<0,0001 соответственно; Фигура 4В, С), по сравнению с группой без добавления.
Эти результаты свидетельствуют о сдвиге к более "зрелому" иммунному ответу на вновь введенный пищевой белок у животных, получавших пищу с добавлением В. lactis NCC2818 во время периода отлучения от груди. Этот более зрелый ответ может рассматриваться как улучшение толерантности к вновь вводимым продуктам питания. Пищеварительная система молодого млекопитающего быстрее адаптируется к новым пищевым продуктам. Таким образом, изобретатели предполагают, что эта более быстрая адаптация будет обуславливать уменьшение уязвимого периода, связанного со временем отлучения от груди. Таким образом, патологические состояния, связанные с отлучением от груди, предотвращаются или уменьшается их тяжесть. Кроме того, предотвращаются и/или уменьшаются отдаленные последствия этих состояний в дальнейшей жизни.
Таким образом, введение пробиотика согласно изобретению оказывает профилактическое действие на молодого млекопитающего, предотвращая умеренный дискомфорт или тяжелый дискомфорт, связанный с патологическими состояниями, которые могут являться результатом введения новых пищевых продуктов во время периода отлучения от груди.
Примеры
Пример 1: Модель изучения влияния В. lactis NCC2818 на поросят в период отлучения.
Были проведены два эксперимента.
В первом эксперименте в соответствии со Схемой кормления I (Фигура 1А) в течение первых трех недель жизни поросята сосали материнское молоко. На 3 неделе животные были переведены на твердую пищу с содержанием белка на основе сои с добавлением В. lactis (NCC2818) или без добавления, или на овальбуминовую (OVA) диету без добавления В. lactis (NCC2818). Все животные были переведены на диету из рыбьей муки на 7 неделе, при этом одна группа продолжала получать диету с добавлением В. lactis NCC2818. Животных забивали в возрасте 11 недель.
Уровни системных специфичных к сое IgG измеряли на 0, 7 и 14 дни после отлучения (Фигура 2), а уровни IgA, IgM и CD21 в клетках мезентериального лимфатического узла (MLN) (Фигура 4) определяли на стадии умерщвления.
Во втором эксперименте в соответствии со Схемой кормления II (Фигура 1В) поросят кормили смесью или с добавлением В. lactis NCC2828, или без добавления, начиная от 24 ч и далее. Поросят или переводили на твердую пищу (яичная диета, яичная диета + NCC2818) на 21 день, или держали на смеси для поросят (молочной смеси). Высоту ворсинок на образцах слизистой кишечника измеряли на 25 день, когда поросята были умерщвлены. Результаты показаны на Фигуре 3.
Подробности эксперимента приведены ниже.
Животная модель
Содержание животных и экспериментальные методики осуществлялись в соответствии с местным этическим руководством: все эксперименты были проведены по лицензии МВД Великобритании и были одобрены местной группой этической экспертизы. Семь беспородных свиней были искусственно оплодотворены семенем одного борова (поставленного компанией Hermitage-Seaborough Ltd, North Tawton, Девон, Великобритания). Свиней транспортировали в отделение Клинической ветеринарии за шесть недель до родов и кормили диетой на основе пшеницы (ВОСМ Pauls Ltd, Wherstead, UK).
Схема кормления I (Фигура 1А)
В 3-недельном возрасте поросят отлучили и разделили детенышей на три группы. На данный момент одна группа получала Bifidobacterium animalis подвид lactis (CNCM I-3446), иначе известный как В. lactis NCC2818, пробиотическую добавку в виде высушенной распылением культуры, примешанной к молочной смеси в концентрации 4.2×106 КОЕ/мл (приблизительно 2×109 КОЕ/кг метаболический вес/день). Требуемое количество корма с добавлением свежих пробиотиков скармливали два раза в день соответствующей группе до завершения эксперимента при достижении поросятами 11-недельного возраста. Остальные две группы не получили пробиотическую добавку. Животные, которых кормили пробиотиком, и контрольные животные содержались в разных помещениях, разделенных обеспечивающим биобезопасность барьером. Поросят, получающих пробиотики, перевели на диету на основе сои, в то время как поросят, не получающих пробиотики, перевели на соевую диету или овальбумин (яичную диету). Все диеты были дополнены соответствующими уровнями витаминов и минералов и производились на заказ компанией Parnutt Foods Ltd (Sleaford, Lincolnshire, Великобритания).
С 7-недельного возраста все три группы получали диету на основе рыбы, без яиц и сои, или вместе с пробиотиком, или без пробиотика в соответствующих случаях.
У всех поросят брали кровь с помощью венопункции в 3, 4 и 5 недельном возрасте для сбора сыворотки. В 11-недельном возрасте поросят усыпляли азапероном и подвергали эвтаназии смертельной дозой барбитурата. После смерти отбирали образцы тканей и кровь из сердца.
Схема кормления II (Фигура 1В)
В 1-дневном возрасте поросят отлучили и разделили детенышей на две группы. Затем, вплоть до 21 дня, одну группу кормили смесью с добавлением Bifidobacterium animalis подвид lactis (CNCM 1-3446), еще известного как В. lactis NCC2818, в виде высушенной распылением культуры, примешанной к молочной смеси в концентрации 4.2×106 КОЕ/мл (приблизительно 2×109 КОЕ/кг метаболический вес/день). Вторую группу кормили смесью без добавления В. lactis NCC2818 вплоть до 21 дня. Требуемое количество корма с добавлением свежих пробиотиков скармливали два раза в день соответствующей группе до завершения эксперимента при достижении поросятами 25-дневного возраста.
Когда поросята достигли трехнедельного возраста группу с добавлением В. lactis NCC2818 разделили на две группы: одну перевели на яичную диету с добавлением В. lactis NCC2818, а другую не отлучали вообще. Аналогично, группа без добавления была поделена на две группы, одну из них переводили на яичную диету, а другую не отлучали вообще. Все диеты были дополнены соответствующими уровнями витаминов и минералов и производились на заказ компанией Parnutt Foods Ltd (Sleaford, Lincolnshire, Великобритания). Эта диета была создана так, что она содержала 21% яичного белка.
В 25-дневном возрасте поросят усыпляли азапероном и подвергали эвтаназии смертельной дозой барбитурата. После смерти отбирали образцы тканей и кровь из сердца.
Измерение антиген-специфического иммуноглобулина (Фигура 2)
Образцы сыворотки были взяты у животных, которых кормили по Схеме кормления I, в дни 0, 7 и 14. Образцы были исследованы на антиовальбумин IgG1 и IgG2 антитела с помощью ELISA, как подробно описано в Bailey М, et al. Effects of infection with transmissible gastroenteritis virus on concomitant immune responses to dietary и injected antigens, Clin. Diagn. Lab. Immunol. 2004; 11:337-43. Коротко, 96-луночные микропланшеты покрывали овальбумином из белка куриного яйца (Sigma) до того, как неспецифические сайты связывания были блокированы 2%-ным альбумином бычьей сыворотки (BSA) (Sigma) в PBS-твин20. После промывки к планшетам были добавлены серийные разведения образцов сыворотки и стандартного образца. Стандартным образцом служила сыворотка поросят, полученная после гипериммунизации овальбумином. Связанные антисоевые IgG1 и IgG2 антитела обнаруживали с помощью изотипспецифических моноклональных антител, а затем HRP-конъюгированными козьими антимышь, как указано выше, при этом относительные концентрации антитела были определены путем интерполяции образцов к стандартным образцам.
Для того чтобы сравнить изменения антител, образованных в сыворотке, при отлучении аутбредных животных, у которых исходные уровни отличаются, результаты выражаются как отношение антител после обработки к антителам до обработки (кратное изменение антител).
Иммуногистология
Сбор образцов
Ткань MLN была взята у каждого из экспериментальных животных вскоре после смерти. Ткани закладывали в OCT (Tissue ТЕК, BDH, Lutterworth, Лестершир, Великобритания) и быстро замораживали в изопентане, предварительно охлажденном приблизительно до -70°C в парах жидкого азота. Образцы хранили при -80°C до изготовления срезов. Серийные срезы 5 мкм этих тканей нарезали, используя микротом Model OTF (Brights Instrument Company Ltd., Хантингдон, Великобритания). Срезы сушили на воздухе в течение 24 ч, затем фиксировали погружением в ацетон в течение 15 минут. Слайдам давали высохнуть перед хранением при -80°C.
Флуоресцентное иммуногистологическое исследование
Для проведения 2-цветного флуоресцентного иммуногистологического исследования использовали мышиные антисвинья моноклональные антитела (IgA и IgM, как для ELISA) с целью определения свободного и связанного с клетками IgA и IgM положительных клеток (Фигура 4). Были использованы конъюгированные вторичные реагенты: козий анти-мышь IgG1, конъюгированный с FITC (Southern Biotechnology, AMS Biotechnology, Oxon, Великобритания), и козий анти-мышь IgG2b, конъюгированный с TRITC (Southern Biotechnology). Окрашивание тканей, запись изображения и автоматизированный анализ изображения проводили, как описано Inman et al., 2010, Inman, C.F., Rees, L.E.N., Barker E., Haverson, K., Stokes, C.R., Bailey, M., Validation of computer-assisted, pixel-based analysis of multiple-colour immunofluorescence histology, Journal of Immunological Methods, 2005; 302: 156-167, за исключением того, что блокирование Fc рецептора достигалось с помощью 10%-ной козьей сыворотки в PBS.
Гистоморфометрическое исследование
Образцы были приготовлены, как описано выше в разделе сбор образцов, окрашены гематоксилином и эозином, а потом исследованы с использованием записи изображения и автоматизированного анализа изображения с помощью программного обеспечения Image для определения длины ворсинок.
Пример 2
Первичная молочная смесь
Пример 3
Молочные смеси для детей 1-3 лет
Дополнительным подтверждающим доказательством настоящего изобретения является содержание статьи "Weaning diet induces sustained metabolic phenotype shift in the pig и influences host response to Bifidobacterium lactis NCC2818C" (Merrifield и M. Lewis et al., 2012, Gut doi:10.1136/gutjnl-2011-301656), которая включается в описание путем отсылки. Сделана конкретная ссылка на Фигуру 3 панель A Merrifield и М. Lewis et al. Данные, представленные в Merrifield и М. Lewis et al., обеспечивают доказательство того, что пробиотик, в частности Bifidobacterium animalis подвид lactis, оказывает действие на иммунную адаптацию при введении здоровым молодым млекопитающим в течение периода отлучения от груди.
Изобретение имеет отношение к улучшению толерантности у младенцев млекопитающих к вновь вводимым продуктам питания. Предложено применение пробиотического штамма В. lactis NCC2818 в профилактике энтероколита, индуцированного пищевыми белками (FPIES), при введении здоровым молодым млекопитающим во время периода отлучения от груди. Изобретение позволяет ускорить адаптацию молодого млекопитающего к новой пище. 9 з.п. ф-лы, 4 ил., 3 пр.
1. Применение пробиотического штамма В. lactis NCC2818 в профилактике энтероколита, индуцированного пищевыми белками (FPIES), при введении здоровым молодым млекопитающим во время периода отлучения от груди.
2. Применение по п. 1, где пробиотический штамм усиливает транзиторное увеличение гуморального иммунного ответа, в частности выработку иммуноглобулина класса G, после воздействия вновь введенных продуктов питания.
3. Применение по п. 1 или 2, где пробиотический штамм вводят в качестве ежедневной дозы в диапазоне от 1×102 до 1×1011, предпочтительно от 1×106 до 1×109 КОЕ.
4. Применение по п. 1 или 2, где пробиотический штамм вводят здоровым младенцам человека в возрасте примерно от 3 месяцев до 24 месяцев.
5. Применение по п. 1 или 2, где пробиотический штамм вводят в чистом виде, или разведенным в воде, или в композиции, подходящей для введения молодым млекопитающим.
6. Применение по п. 1 или 2, где пробиотический штамм вводят в комбинации с одним или более дополнительными пробиотиками.
7. Применение по п. 6, где один или более дополнительных пробиотиков предпочтительно выбирают из Bifidobacterium longum ВВ536 (АТСС ВАА-999), Lactobacillus rhamnosus (CGMCC 1.3724) или их смесей.
8. Применение по п. 1 или 2, где пробиотический штамм вводят в композиции, которая содержит дополнительные ингредиенты или пребиотики, предпочтительно выбранные из инулина, фруктоолигосахарида (FOS), фруктоолигосахарида с короткой цепью (FOS с короткой цепью), галактоолигосахарида (GOS), ксилоолигосахарида (XOS), арабиноксилан-олигосахаридов (AXOS), ганглиозидов, частично гидролизованной гуаровой камеди (PHGG), аравийской камеди, соевой камеди, молочной смеси ягод годжи, экстрактов ягод годжи или их смесей.
9. Применение по п. 1 или 2, где пробиотический штамм инактивирован, т.е. переведен в состояние, в котором он не способен к воспроизводству.
10. Применение по п. 1 или 2, где пробиотический штамм вводят в виде молочной смеси, детской смеси в период прикорма или молочной смеси для детей 1-3 лет, детского зернового продукта или йогурта, детского питания, пудинга или сыра, молочного и фруктового напитка, смузи, легкой закуски или сухого печенья, или другого хлебобулочного изделия.
| ISOLAURI E ET AL: "Probiotics in the management of atopic eczema", CLINICAL AND EXPERIMENTAL ALLERGY", vol | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| Регенеративная с капельниковым нефтяным отоплением печь | 1925 |
|
SU1604A1 |
| Устройство для обеспыливания при загрузке сыпучих материалов в транспортные средства | 1986 |
|
SU1364586A1 |
| СИНБИОТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ДЕТЕЙ | 2004 |
|
RU2373769C2 |
| KIRJAVAINEN P V ET AL: "Aberrant composition of gut microbiota of allergic infant: a target of bifidobacterial therapy at weaning?", GUT, BRITISH MEDICAL ASSOCIATION, | |||
Авторы
Даты
2016-04-10—Публикация
2012-07-11—Подача