Перекрестная ссылка на родственные заявки
Настоящая заявка испрашивает приоритет предварительной заявки на патент США № 61/016614, поданной 26 декабря 2007 г., предварительной заявки на патент США № 61/087466, поданной 8 августа 2008 г., и предварительной заявки на патент США № 61/087590, поданной 8 августа 2008 г., которые полностью включены в настоящее описание изобретения в качестве ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к применению иммуноконъюгатов против антигена CD138 и композиций, включающих указанные иммуноконъюгаты, для уменьшения адгезии стромальных клеток к CD138-экспрессирующим клеткам-мишеням и, таким образом, для более эффективного лечения заболеваний, обусловленных СD138-экспрессирующими клетками.
Уровень техники
CD138, действующий в качестве рецептора внеклеточного матрикса, сверхэкспрессирован на клетках множественной миеломы (ММ) и, как было установлено, влияет на развитие и/или пролиферацию клеток ММ. CD138 экспрессирован также на клетках рака яичника, рака почки, рака желчного пузыря, рака молочной железы, рака предстательной железы, рака легкого, рака ободочной кишки, лимфомы Ходжкина и неходжкинской лимфомы, хронического лимфолейкоза (CLL) и многих других.
Публикации и другие материалы, включая патенты, использованные в настоящем описании изобретения для иллюстрации изобретения и, в частности, для более подробного описания возможностей осуществления настоящего изобретения, включены в качестве ссылки. Публикации, приведенные в нижеследующем описании изобретения только с указанием автора и даты публикации, перечислены в алфавитном порядке по имени автора в прилагаемом библиографическом разделе.
Тассон и др. (2004) сообщили в превосходном связывании антитела В-В4 IgG1 мыши с антигеном CD138, экспрессированным на поверхности клеток ММ. Тассон также отметил высокую цитотоксическую активность иммуноконъюгата В-В4-DM1, включающего митанзиноид DM1 в качестве эффекторной молекулы, против клеток множественной миеломы (см. также публикацию патента США 20070183971).
Тассон также показал, что конъюгат антитела В-В4 эффективно действует даже в микросреде костного мозга, которая вызывает устойчивость клеток множественной миеломы (ММ) ко многим лекарственным средствам, вводимым субъектам, страдающим множественной миеломой, таким как, например, дексаметазон. Иммуноконъюгаты, созданные Тассоном, были способны эффективно разрушать опухолевые клетки ММ в среде костномозговой стромы.
Несмотря на то, что Тассон и др. создали эффективный метод лечения множественной миеломы и композицию, которая может быть использована при осуществлении такого метода лечения, в данной области существует большая потребность в новых методах и лекарственных средствах.
Существует потребность в усовершенствованных методах лечения с использованием иммуноконъюгатов на основе антитела В-В4. Кроме того, существует потребность в эффективных методах лечения с использованием иммуноконъюгатов на основе антитела В-В4, обладающих одним или несколькими преимуществами. Такие иммуноконъюгаты предпочтительно характеризуются лучшим связыванием с антигеном, лучшим лизисом опухолевых клеток, включая, в частности, CD138-экспрессирующие опухолевые клетки и А-клетки, или более гомогенным связыванием с мишенью и, в частности, способностью более эффективно лечить заболевания, ассоциированные с CD138-экспрессирующими клетками.
Сущность изобретения
Настоящее изобретение относится к способу уменьшения адгезии стромальных клеток к CD138-экспрессирующим опухолевым клеткам в опухолевых клетках нуждающегося субъекта, который включает:
введение в указанные опухолевые клетки иммуноконъюгата против CD138-экспрессирующих опухолевых клеток, в частности, иммуноконъюгата, содержащего расщепляемый линкер и эффектор, рассмотренные в настоящем описании изобретения, в количестве, эффективном для уменьшения адгезии стромальных клеток к CD138-экспрессирующим опухолевым клеткам, и необязательно введение в указанные опухолевые клетки дополнительного цитотоксического средства в количестве, обеспечивающем ингибирование, задержку и/или предотвращение роста опухолевых клеток.
Адгезия может быть уменьшена по меньшей мере примерно на 10%, примерно на 20%, примерно на 30%, примерно на 40%, примерно на 50%, примерно на 60%, примерно на 70%, примерно на 80% или больше, и/или может быть достигнуто ослабление лекарственной устойчивости, опосредованной указанной адгезией, включая опосредованную адгезией лекарственную устойчивость к дополнительному цитотоксическому средству (которое не является одним из вышеуказанных иммуноконъюгатов), вводимому в количестве, обеспечивающем ингибирование, задержку и/или предотвращение роста опухолевых клеток. Иммуноконъюгат и один или несколько цитотоксических средств можно вводить последовательно, при этом цитотоксическое средство можно вводить после введения иммуноконъюгата или одновременно с ним.
Иммуноконъюгат по настоящему изобретению, в частности, включает:
(а) генетически созданное антитело против клетки-мишени и
(b) эффекторную молекулу,
при этом указанный иммуноконъюгат гомогенно и направленно воздействует на CD138-экспрессирующие клетки-мишени.
Генетически созданное антитело против клетки-мишени по настоящему изобретению может
(i) по существу состоять из антигенсвязывающей области (ABR) против CD138 антитела, отличного от человеческого, или
(ii) включать антигенсвязывающую область (ABR) против CD138, выделенную из антитела, отличного от человеческого, и
дополнительную область антитела, по меньшей мере часть которой выделена из человеческого антитела.
Антигенсвязывающая область (ABR) может включать:
(а) CDR3 вариабельной области тяжелой цепи, включающую аминокислотные остатки 99-111 SEQ ID NO:1, и
(b) CDR3 вариабельной области легкой цепи, включающую аминокислотные остатки 89-97 SEQ ID NO:2.
Антигенсвязывающая область (ABR) может далее включать:
(а) CDR1 и CDR2 вариабельной области тяжелой цепи, включающие соответственно аминокислотные остатки 31-35 и 51-68 SEQ ID NO:1, и/или
(b) CDR1 и CDR2 вариабельной области легкой цепи, включающие соответственно аминокислотные остатки 24-34 и 50-56 SEQ ID NO:2.
Дополнительная область антитела может включать:
(а) аминокислотные остатки 123-448 SEQ ID NO:1 и/или
(b) аминокислотные остатки 108-214 SEQ ID NO:2
и их мутанты, которые
(i) сохраняют или снижают антителозависимую цитотоксичность и/или комплементзависимую цитотоксичность генетически созданного антитела против клетки-мишени и/или
(ii) стабилизируют генетически созданное антитело против клетки-мишени.
Эффекторная молекула может быть присоединена к указанному генетически созданному антителу против клетки-мишени с помощью линкера. Линкер может включать дисульфидную связь. Эффекторная молекула (например, DM4) может создавать стерическое препятствие между антителом против клетки-мишени и эффекторной молекулой. Эффекторная молекула может быть по меньшей мере одним майтанзиноидом (например, DM1, DM3 или DM4), таксаном, СС1065 или их аналогом.
Иммуноконъюгат может связываться с CD138 с изменчивостью направленного воздействия менее 150%, 140%, 130%, 120%, 110%, 100%, 90%, 80%, 70%, 60% или 50%.
Настоящее изобретение относится также к иммуноконъюгату, который включает:
агент против антигена CD138, включающий:
выделенный полипептид, содержащий аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, которая по меньшей мере на 70% идентична SEQ ID NO:1. Константная область указанной тяжелой цепи иммуноглобулина или ее части может быть константной областью изотипа IgG4.
Настоящее изобретение относится также к способу лечения множественной миеломы у субъекта, который включает:
получение одного или нескольких иммуноконъюгатов по настоящему изобретению и
введение субъекту указанного иммуноконъюгата в количестве, обеспечивающем эффективное лечение множественной миеломы.
Агент против клетки-мишени иммуноконъюгата может включать последовательность легкой цепи, которая по меньшей мере примерно на 70% идентична SEQ ID NO:2. Агент против клетки-мишени иммуноконъюгата может также включать последовательность тяжелой цепи, которая по меньшей мере примерно на 70% идентична SEQ ID NO:1.
Настоящее изобретение относится также к способу доставки лекарственного средства иммуноконъюгатом, который включает:
получение одного или нескольких иммуноконъюгатов по настоящему изобретению и
введение указанного иммуноконъюгата в терапевтически эффективном количестве, при этом указанный изотип IgG4 ослабляет антителозависимую клеточно-опосредованную цитотоксичность (АDCC), комплементзависимую цитотоксичность и/или Fс-опосредованное направленное воздействие на FcR печени.
Настоящее изобретение относится также к способу ингибирования, задержки и/или предотвращения роста опухолевых клеток в культуре клеток, который включает:
введение в указанную культуру клеток одного или нескольких иммуноконъюгатов по настоящему изобретению в эффективном количестве, ингибирующем, задерживающем и/или предотвращающем рост опухолевых клеток. Эффективное количество может индуцировать гибель клеток или остановку непрерывного клеточного цикла в CD138-экспрессирующих опухолевых клетках и необязательно А-клетках, не экспрессирующих антиген CD138, в частности, стромальных клетках опухоли. Клетки в указанной культуре клеток могут быть получены у субъекта, страдающего раком, и после введения эффективного количества иммуноконъюгата клетки указанной культуры клеток могут быть вновь имплантированы субъекту, страдающему раком.
Настоящее изобретение относится также к способу ингибирования, задержки и/или предотвращения роста опухоли, содержащей CD138-экспрессирующие опухолевые клетки, и/или распространения опухолевых клеток такой опухоли у нуждающегося субъекта, который включает:
введение указанному субъекту по меньшей мере одного или нескольких иммуноконъюгатов по настоящему изобретению в количестве, ингибирующем или задерживающем рост опухоли и/или распространение опухолевых клеток,
при этом указанный иммуноконъюгат ингибирует, задерживает или предотвращает рост и/или распространение указанных опухолевых клеток.
Эффекторная молекула указанного иммуноконъюгата может быть токсином, цитотоксическим ферментом, низкомолекулярным цитотоксическим лекарственным средством, порообразующим агентом, модификатором биологической реакции, ферментом, активирующим пролекарство, антителом, цитокином или радиоактивным изотопом.
Иммуноконъюгаты по настоящему изобретению можно вводить в виде однократной дозы от 5 мг/м2 до около 300 мг/м2 необязательно с интервалом в несколько часов, дней, недель или, комбинируя указанные интервалы.
Схемы введения многократных доз с интервалами в несколько часов, дней и недель, также входят в объем настоящего изобретения и, в частности, включают введение с интервалами в 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 часа, 1, 2, 3, 4, 5, 6, 7 дней, 1, 2, 3, 4, 5, 6, 7 или 8 недель.
Настоящее изобретение относится также к способу ингибирования, задержки и/или предотвращения роста опухоли и/или распространения злокачественных опухолевых клеток у нуждающегося субъекта, который включает:
(а) введение указанному субъекту одного или нескольких цитотоксических средств и/или проведение лучевой терапии в дозе, необходимой для уменьшения опухолевой массы; и
(b) введение указанному субъекту по меньшей мере одного из иммуноконъюгатов по настоящему изобретению в количестве, ингибирующем, задерживающем или предотвращающем рост опухоли и/или распространение опухолевых клеток,
при этом указанный иммуноконъюгат ингибирует, задерживает или предотвращает рост и/или распространение опухолевых клеток, включающих CD138-экспрессирующие клетки.
Цитотоксическое средство по любому из вариантов осуществления настоящего изобретения может быть, в частности, мефаланом, винкристином, доксорубицином, дексаметазоном, циклофосфамидом, этопозидом, цитарабином, цисплатином, талидомидом, преднизоном, талидомидом, бортезомибом, леналидомидом, сорафенибом, ромидепсином или их комбиациями, либо может быть создано на основе антитела.
Настоящее изобретение относится также к способу лечения субъекта, страдающего заболеванием, на которое может оказать благоприятное воздействие подавление миеломных клеток, который включает:
(а) получение по меньшей мере одного из иммуноконъюгатов по настоящему изобретению и
(b) введение указанного иммуноконъюгата субъекту для селективного уменьшения выживания или роста миеломных клеток у указанного субъекта.
Настоящее изобретение относится также к фармацевтической композиции, включающей любые иммуноконъюгаты по настоящему изобретению для ингибирования, задержки и/или предотвращения роста опухоли и/или распространения опухолевых клеток, и один или несколько фармацевтически приемлемых наполнителей.
Фармацевтическая композиция может включать цитотоксические средства, рассмотренные в настоящем описании изобретения.
Настоящее изобретение относится также к набору, в комплект которого входят отдельные контейнеры с фармацевтическими композициями, предназначенными для использования в комбинации для ингибирования, задержки и/или предотвращения роста опухолей и/или распространения опухолевых клеток, при этом в одном контейнере находится эффективное количество вышеуказанной фармацевтической композиции и в другом контейнере находится вторая фармацевтическая композиция, включающая эффективное количество средства, предпочтительно цитотоксического средства, предназначенного для ингибирования, задержки и/или предотвращения роста опухоли и/или распространения опухолевых клеток, и один или несколько фармацевтически приемлемых наполнителей.
Настоящее изобретение относится также к способу ингибирования, задержки и/или предотвращения роста опухоли, включающей CD138-экспрессирующие опухолевые клетки, и/или распространения опухолевых клеток такой опухоли у нуждающегося субъекта, который включает:
(а) получение иммуноконъюгата, включающего
генетически созданное антитело против CD138, присоединнное к эффекторной молекуле при помощи расщепляемого линкера, причем указанная эффекторная молекула имеет стерическое препятствие, и
(b) введение указанному субъекту иммуноконъюгата (а) в количестве, обеспечивающем ингибирование, задержку и/или предотвращение роста опухоли и/или распространение опухолевых клеток, при этом указанный иммуноконъюгат (а) обладает ингибирующей рост опухоли активностью, которая превышает активность иммуноконъюгата без стерического препятствия, примерно на 10%, примерно на 20%, перимерно на 30%, примерно на 40% или больше.
Ингибирующая рост опухоли активность иммуноконъюгата без стерического препятствия, включающего нерасщепляемый линкер, может превышать ингибирующую рост опухоли активность иммуноконъюгата без стерического препятствия, включающего расщепляемый линкер, по меньшей мере примерно на 5%, по меньшей мере примерно на 10%, примерно до 15%.
Указанное генетически созданное антитело против CD138 может по существу состоять из антигенсвязывающей области против CD138 антитела, отличного от человеческого, или может включать антигенсвязывающую область против CD138 антитела, отличного от человеческого, и дополнительную область антитела, по меньшей мере часть которой выделена из человеческого антитела.
Указанный расщепляемый линкер может включать дисульфидную связь. Эффекторная молекула может быть DM4. Иммуноконъюгат может быть частью фармацевтической композиции и может быть введен субъекту по меньшей мере в виде одной дозы в количестве от около 5 мг/м2 до около 300 мг/м2.
Настоящее изобретение относится к иммуноконъюгату, предназначенному для использования в качестве лекарственного средства, который включает:
(а) генетически созданное антитело против клетки-мишени,
(i) состоящее в основном из антигенсвязывающей области против CD138 антитела, отличного от человеческого; или
(ii) включающее антигенсвязывающую область против CD138, выделенную из антитела, отличного от человеческого, и
дополнительную область антитела, по меньшей мере часть которой выделена из человеческого антитела, и
(b) эффекторную молекулу,
при этом указанный иммуноконъюгат гомогенно связывается с CD138.
Настоящее изобретение относится к другому иммуноконъюгату, предназначенному для использования в качестве лекарственного средства, который включает:
агент против антигена CD138, включающий
выделенный полипептид, содержащий аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, которая по меньшей мере на 70% идентична SEQ ID NO:1.
В частности, одним объектом настоящего изобретения является иммуноконъюгат по настоящему изобретению, предназначенный для лечения множественной миеломы. Указанный иммуноконъюгат может быть использован для приготовления лекарственного средства, предназначенного для лечения множественной миеломы.
Настоящее изобретение относится также к иммуноконъюгату, используемому для доставки лекарственного средства субъекту, в частности, для ослабления антителозависимой клеточно-опосредованной цитотоксичности, комплементзависимой цитотоксичности и/или Fc-опосредованного направленного воздействия на FcR печени, при этом указанный иммуноконъюгат включает агент против CD138, включающий выделенный полипептид, содержащий аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, которая по меньшей мере на 70% идентична SEQ ID NO:1, и константную область тяжелой цепи иммуноглобулина или ее части, которая является константной областью изотипа IgG4.
Настоящее изобретение относится также к опухолевым клеткам, используемым при лечении рака у субъекта, которые обрабатывают в культуре клеток иммуноконъюгатом, включающим:
(а) генетически созданное антитело против клетки-мишени,
(i) состоящее в основном из антигенсвязывающей области против CD138 антитела, отличного от человеческого; или
(ii) включающее антигенсвязывающую область против CD138, выделенную из антитела, отличного от человеческого; и
дополнительную область антитела, по меньшей мере часть которой выделена из человеческого антитела, и
(b) эффекторную молекулу,
при этом указанный иммуноконъюгат гомогенно связывается с CD138.
Настоящее изобретение относится также к опухолевым клеткам, используемым при лечении рака у субъекта, которые обрабатывают в культуре клеток иммуноконъюгатом, включающем:
агент против гена CD138, который включает
выделенный полипептид, содежащий аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, которая по меньшей мере на 70% идентична SEQ ID NO:1.
Настоящее изобретение относится к иммуноконъюгату, предназначенному для ингибирования, задержки и/или предотвращения роста опухоли, содержащей CD138-экспрессирующие опухолевые клетки, и/или распространения опухолевых клеток такой опухоли у субъекта, который включает:
(а) генетически созданное антитело против клетки-мишени,
(i) состоящее в основном из антигенсвязывающей области против CD138 антитела, отличного от человеческого; или
(ii) включающее антигенсвязывающую область против CD138, выделенную из антитела, отличного от человеческого; и
дополнительную область антитела, по меньшей мере часть которой выделена из человеческого антитела, и
(b) эффекторную молекулу,
при этом указанный иммуноконъюгат гомогенно связывается с CD138.
Альтернативно настоящее изобретение относится к иммуноконъюгату, предназначенному для ингибирования, задержки и/или предотвращения роста опухоли, включающей CD138-экспрессирующие опухолевые клетки, и/или распространения опухолевых клеток такой опухоли у субъекта, который включает:
агент против антигена CD138, включающий
выделенный полипептид, содержащий аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, которая по меньшей мере на 70% идентичная SEQ ID NO:1.
Настоящее изобретение далее относится к лекарственному средству, включающему иммуноконъюгат и одно или несколько противораковых средств в виде комбинированного препарата, предназначенного для одновременного, раздельного или последовательного введения при лечении опухоли, содержащей CD138-экспрессирующие клетки, в котором иммуноконъюгат включает:
(а) генетически созданное антитело против клетки-мишени,
(i) состоящее в основном из антигенсвязывающей области против CD138 антитела, отличного от человеческого; или
(ii) включающее антигенсвязывающую область против CD138, выделенную из антитела, отличного от человеческого; и
дополнительную область антитела, по меньшей мере часть которой выделена из человеческого антитела, и
(b) эффекторную молекулу,
при этом указанный иммуноконъюгат гомогенно связывается с CD138 и одно или несколько противораковых средств могут уменьшать опухолевую массу.
Альтернативно настоящее изобретение относится к лекарственному средству, включающему иммуноконъюгат и одно или несколько противораковых средств в виде комбинированного препарата, предназначенного для одновременного, раздельного или последовательного введения при лечении опухоли, содержащей CD138-экспрессирующие клетки, в котором иммуноконъюгат включает:
агент против антигена CD138, включающий
выделенный полипептид, содержащий аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, которая по меньшей мере на 70% идентична SEQ ID NO:1,
и одно или несколько противораковых средств могут уменьшать опухолевую массу.
В соответствии с другим объектом изобретения комбинированный препарат, рассмотренный в двух вышеуказанных абзацах, вводят субъекту, прошедшему курс лучевой терапии.
Альтернативным объектом настоящего изобретения является использование иммуноконъюгата для приготовления лекарственного средства, предназначенного для лечения у субъекта опухоли, содержащей CD138-экспрессирующие клетки, в котором иммуноконъюгат включает:
(а) генетически созданное антитело против клетки-мишени,
(i) состоящее в основном из антигенсвязывающей области против CD138 антитела, отличного от человеческого; или
(ii) включающее антигенсвязывающую область против CD138, выделенную из антитела, отличного от человеческого; и
дополнительную область антитела, по меньшей мере часть которой выделена из человеческого антитела, и
(b) эффекторную молекулу,
при этом указанный иммуноконъюгат гомогенно связывается с CD138 и лекарственное средство вводят субъекту, прошедшему курс лучевой терапии, для уменьшения опухолевой массы.
Настоящее изобретение далее относится к использованию иммуноконъюгата для приготовления лекарственного средства для лечения у субъекта опухоли, содержащей CD138-экспрессирующие клетки, в котором иммуноконъюгат включает:
агент против антигена CD138, включающий
выделенный полипептид, содержащий аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, которая по меньшей мере на 70% идентична SEQ ID NO:1,
и лекарственное средство предназначено для введения субъекту, прошедшему курс лучевой терапии, для уменьшения опухолевой массы.
Рассмотренное в вышеуказанных абзацах лекарственное средство может ингибировать, задерживать и/или предотвращать рост опухоли и/или распространение злокачественных опухолевых клеток у субъекта.
Настоящее изобретение далее относится к иммуноконъюгату, предназначенному для подавления выживания миеломных клеток у субъекта, который включает:
(а) генетически созданное антитело против клетки-мишени,
(i) состоящее в основном из антигенсвязывающей области против CD138 антитела, отличного от человеческого; или
(ii) включающее антигенсвязывающую область против CD138, выделенную из антитела, отличного от человеческого; и
дополнительную область антитела, по меньшей мере часть которой выделена из человеческого антитела, и
(b) эффекторную молекулу,
при этом указанный иммуноконъюгат гомогенно связывается с CD138.
Настоящее изобретение далее относится к иммуноконъюгату, предназначенному для подавления выживания миеломных клеток у субъекта, который включает:
агент против антигена CD138, включающий
выделенный полипептид, содержащий аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, которая по меньшей мере на 70% идентична SEQ ID NO:1.
Рассмотренный в вышеуказанных двух абзацах иммуноконъюгат, в частности, способен селективно уменьшать выживание или рост указанных миеломных клеток у субъекта.
Настоящее изобретение далее относится к иммуноконъюгату, предназначенному для ингибирования, задержки и/или предотвращения роста опухоли, включающей CD138-экспрессирующие опухолевые клетки, и распространения опухолевых клеток такой опухоли у субъекта, при этом иммуноконъюгат включает генетически созданное антитело против CD138, присоединенное к эффекторной молекуле при помощи расщепляемого линкера, и эффекторная молекула имеет стерическое препятствие.
Рассмотренный в вышеуказанном абзаце иммуноконъюгат, в частности, способен проявлять ингибирующую рост опухоли активность, которая превышает активность иммуноконъюгата без стерического препятствия, примерно на 10%, примерно на 20%, перимерно на 30%, примерно на 40% или больше.
Настоящее изобретение относится также к агенту против CD138, который предназначен для использования в способе уменьшения адгезии стромальных клеток к CD138-экспрессирующим опухолевым клеткам в опухолевых клетках субъекта.
Настоящее изобретение далее относится к лекарственному средству, включающему агент против CD138 и другой агент, такой как иммуноконъюгат против клетки-мишени или цитостатическое средство, в виде комбинированного препарата для одновременного (совместного введения), раздельного или последовательного введения в способе уменьшения адгезии стромальных клеток к CD138-экспрессирующим опухолевым клеткам в опухолевых клетках субъекта.
Рассмотренный в вышеуказанном абзаце комбинированный препарат, в частности, способен ингибировать, задерживать и/или предотвращать рост опухолевых клеток у субъекта.
Краткое описание чертежей
На Фиг.1 схематически изображено антитело nBT062 с присоединенными эффекторными молекулами.
На Фиг.2 показана химическая структура ВТ062.
На Фиг.3 показано превращение ансамитоцина Р-3 в майтанзинол (стереохимия опущена для более простого представления).
На Фиг.4 показана типичная схема синтеза DM4.
На Фиг.5 схематически изображена конъюгация антитела (nBT062 с DM4).
На Фиг.6 показан анализ связывания nBT062-SPDB-DM4, nBT062-SPP-DM1, nBT062-SMCC-DМ1 и антитела nBT062 с клетками ОРМ-2. Клетки подвергали воздействию антитела nBT062 и конъюгатов в разных концентрациях и измеряли среднее значение флуоресценции при помощи анализа методом FACS.
На Фиг.7А-7D показана цитотоксичность in vitro конъюгатов nBT062-DMx в отношении клеток MOLP-8 (CD138+) и BJAB (CD138-). Клетки культивировали на плоскодонных планшетах и инкубировали с иммуноконъюгатами в указанных концентрациях в течение 5 дней. Реагент WST добавляли в течение дополнительных 3 часов для оценки жизнеспособности клеток. На Фиг.7D показан анализ цитотоксической активности иммуноконъюгата nBT062-SPDB-DM4 в присутствии или отсутствии блокирующего антитела (1 мкМ nBT062).
На Фиг.8 показаны объемы опухолей у отдельных мышей, которым вводили (А) PBS, (В) антитело nBT062, (С) свободный DM4 или (D) конъюгат huC242-DM4 ненаправленного действия, образовавшихся в течение определенного периода времени (дни) после инокуляции опухолевыми клетками MOLP-8.
На Фиг.9 показаны объемы опухолей у отдельных мышей, которым вводили (А) PBS, (B) nBT062-SPDB-DM4, (C) B-B4-SPP-DM1 или (D) nBT062-SPP-DM1, образовавшихся в течение определенного периода времени (дни) после инокуляции опухолевыми клетками MOLP-8.
На Фиг.10 показан средний объем опухоли (± стандартное отклонение) ксенотрансплантатов клеток множественной миеломы человека MOLP-8 у мышей SCID CB.17, образовавшейся в течение определенного периода времени (дни) после инокуляции.
На Фиг.11А и В показана противоопухолевая активность nBT062-DMx в отношении CD138+ опухолевых клеток MOLP-8 в объемной модели опухоли MOLP-8 у мышей SCID. Объем опухоли выражен в виде среднего значения (± стандартное отклонение) для каждой группы.
На Фиг.12 представлен график противоопухолевой эффективности конъюгатов DMx, содержащих антитело nBT062, в модели SCIDhu/INA-6 в отношении клеток множественной миеломы в среде костного мозга человека. Растворимый рецептор IL-6 человека, продуцируемый клетками множественной миеломы, (shulL-6R), был использован в качестве индикатора опухолевой массы. Треугольник: nBT062-SPP-DM1, квадрат: nBT062-SPDB-DM4, ромб: контрольный наполнитель.
На Фиг.13 показан опосредованный nBT062-SPDB-DM4 лизис опухолевых клеток in vitro. CD138-положительные клетки ОРМ2 и CD138-отрицательные клетки Namawla культивировали с nBT062-SPDB-DM4 в разных концентрациях и измеряли жизнеспособность клеток. Значения ОD450 являются мерой жизнеспособности клеток.
На Фиг.14А показана экспрессия CD138 разными клетками ММ, и на Фиг.14В показан микроскопический анализ клеток DOX40 (верхний блок) и клеток ОРМ1 (нижний блок). Экспрессия CD138 показана с правой стороны, и нуклеиновые кислоты показаны с левой стороны.
На Фиг.15А показана цитотоксичность nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 в отношении клеток ММ через 40, 80 и 120 часов. На Фиг.15В показана жизнеспособность клеток ММ, выделенных у трех разных субъектов после лечения nBT062-SPDB-DM4 в течение 2 дней. На Фиг.15С показаны мононуклеарные клетки периферической крови (РВМС), выделенные у 3 здоровых субъектов, которые культивировали с nBT062-SPDB-DM4 в течение 72 часов до определения жизнеспособности клеток.
На Фиг.16А показан анализ клеточного цикла, при выполнении которого клетки ОРМ1 обрабатывали иммуноконъюгатами в течение 0, 12 или 24 часов и анализировали профили клеточных циклов путем окрашивания PI. На Фиг.16В показаны клетки ОРМ1, которые культивировали в присутствии или отсутствии иммуноконъюгатов в течение 24, 48 или 72 часов. Процентное содержание апоптических клеток определяли путем окрашивания антителом Аро 2.7 и выполнения проточного цитометрического анализа. На Фиг.16С показаны клетки ОРМ1, которые культивировали в присутствии 885 мкг/мл nBT062-SPDB-DM4 в течение указанных периодов времени (левый блок) или с иммуноконъюгатом в разных концентрациях (средний блок). Ингибитор панкаспазы zVAD-fmk блокировал индуцируемую nBT062-SPDB-DM4 каспазу-8, -9 и -3 и расщеплял поли(ADP-рибоза)полимеразу (PARP) в клетках ОРМ1 (правый блок).
На Фиг.17А-17С показано воздействие IL-6, IGF-1 и BMSC на рост и чувствительность клеток ММ к иммуноконъюгатам. На Фиг.17D показаны эксперименты с использованием дексаметазона вместо иммуноконъюгата. На Фиг.17Е показаны результаты эксперимента по адгезии клеток к сокультурам опухолевых клеток и BMSC в присутствии или отсутствии иммуноконъюгатов.
На Фиг.18А показан анализ экспрессии GFP клетками ОРМ1GFP. На Фиг.18В показано воздействие nBT062-SPDB-DM4, nBT062-SPP-DM1 или контрольного буфера на размеры опухолей в группах мышей SCID, которым инъецировали клетки ОРМ1GFP в количестве 5×106. На Фиг.18С показано значительно более высокое выживание животных, которым вводили nBT062-SPDB-DM4, (Р <0,0023, пунктирная линия, n=5) по сравнению с контрольной группой, которой вводили только наполнитель (сплошная линия; нормальный физиологический раствор, n=5). На Фиг.18D показано, что nBT062-SPDB-DM4 вызывает апоптоз клеток in vivo.
Подробное описание разных и предпочтительных вариантов осуществления изобретения
Настоящее изобретение относится к иммуноконъюгатам, включающим агенты против CD138, к доставке эффекторных молекул иммуноконъюгатов к мишени и сайтспецифическому высвобождению эффекторных молекул в клетках-мишенях, тканях и органах или рядом с ними. Эффекторные молекулы могут быть активированы отщеплением/диссоциацией от агента против клетки-мишени иммуноконъюгата на сайте-мишени. Настоящее изобретение, в частности, относится к применению указанных иммуноконъюгатов для прекращения роста опухоли in vivo и преодоления или ослабления защитных механизмов, действующих в микросреде костного мозга.
Иммуноконъюгаты по настоящему изобретению можно вводить субъекту, нуждающемуся в терапевтическом лечении, или в клетки, выделенные у такого субъекта. Одна или несколько эффекторных молекул могут высвобождаться из иммуноконъюгата в результате отщепления/диссоциации в клетках-мишенях, тканях и органах или рядом с ними.
В соответствии с одним примером субъекту, страдающему раком, вводят иммуноконъюгат, включающий антитело nВT062 против CD138-экспрессирующих клеток и по меньшей мере одно высокотоксичное лекарственное средство или токсин в качестве эффекторной молекулы. В данном примере терапевтически эффективное количество иммуноконъюгата вводят субъекту внутривенно для концентрирования в раковых клетках. Одна или несколько эффекторных молекул затем высвобождаются из антитела естественным путем. После или во время отщепления эффекторная молекула может быть стабилизирована алкилированием и может диффундировать в окружающие А-клетки, такие как стромальные клетки, не экспрессирующие CD138.
В соответствии со вторым примером субъекту, страдающему раком, вводят иммуноконъюгат, включающий антитело nBT062 против CD138-экспрессирующих клеток, по меньшей мере одно вывокотоксичное лекарственное средство или токсин в качестве эффекторной молекулы и дополнительное цитотоксическое средство. В данном примере терапевтически эффективное количество иммуноконъюгата и цитотоксического средства вводят последовательно. Сначала субъекту внутривенно вводят иммуноконъюгат, который концентрируется в раковых клетках микросреды костного мозга. Иммуноконъюгат преодолевает лекарственную устойчивость, опосредуемую межклеточной адгезией (CAM-DR), и разрушает значительную часть CD138- экспрессирующих опухолевых клеток в микросреде костного мозга. Эффекторные молекулы отделяются от антитела естественным путем и разрушают опухолевые клетки. Иммуноконъюгат по меньшей мере частично предотвращает адгезию опухолевых клеток к стромальным клеткам, некоторые из которых могут быть разрушены диффундирующей эффекторной молекулой. Через 12 часов вводят цитотоксическое средство. Цитотоксическое средство, активность которого обычно по меньшей мере частично уменьшается вследствие САМ-DR, может воздействовать на опухолевые клетки, не ассоциированные со стромальными клетками, и разрушать CD138-экспрессирующие опухолевые клетки, которые не поддаются воздействию иммуноконъюгата.
CD138 или синдекан-1 (определяемый также как SYND1, СИНДЕКАН, SDC, SCD1, АНТИГЕН CD138, номер доступа SwissProt: Р18827 человека) является мембранным гликопротеином, который, как первоначально было указано, присутствует на клетках эпителиального происхождения и затем был обнаружен на гемопоэтических клетках (Sanderson, 1989). CD138 имеет длинный внеклеточный домен, который связывается с растворимыми молекулами (например, факторами роста EGF, FGF, HGF) и нерастворимыми молекулами (например, с компонентами внеклеточного матрикса коллагеном и фибронектином) при помощи цепей, образуемых сульфатом гепарана (Langford, 1998; Yang, 2007), и действует в качестве рецептора внеклеточного матрикса. CD138 также опосредует межклеточную адгезию при помощи гепарин-связывающих молекул, экспрессируемых смежными клетками. Установлено, что CD138 является корецептором факторов роста миеломных клеток (Bisping, 2006). Исследования дифференцировки плазмоцитов показали, что CD138 следует также считать дифференцировочным антигеном (Batаille, 2006).
В случае злокачественного гемопоэза антиген CD138 высоко экспрессирован на большинстве клеток ММ, клетках рака яичника, рака почки, рака желчного пузыря, рака молочной железы, рака предстательной железы, рака легкого, рака ободочной кишки, клетках лммфомы Ходжкина и неходжскинской лимфомы, хронического лимфолейкоза (CLL) (Horvathova, 1995), острого лимфобластного лейкоза (ALL), острого миелобластного лейкоза (AML) (Seftalioglu, 2003 (a); Deftalioglu, 2003 (b)), клетках солидных тканевых сарком, рака ободочной кишки и других гематологических злокачественных новообразований и солидных опухолей, экспрессирующих антиген CD138 (Carbone et al., 1999; Sebestyen et al., 1999; Han et al., 2004; Charnaux et al., 2004; O'Connell et al., 2004; Orosz and Kopper, 2001).
Другими видами рака, которые, как было установлено, экспрессируют CD138, являются многие аденокарциномы яичника, переходно-клеточный рак мочевого пузыря, светлоклеточный рак почки, плоскоклеточный рак легкого, рак молочной железы и рак матки (см., например, публикации Davies et al., 2004; Barbareschi et al., 2003; Mennerich et al., 2004; Anttonen et al., 2001; Wijdenes, 2002).
В нормальном гемопоэтическом компартменте человека экспрессия CD138 ограничивается плазмоцитами (Wijdenes, 1996; Chilosi, 1999), и CD138 не экспрессирован на лимфоцитах, моноцитах, гранулоцитах и эритроцитах периферической крови. В частности, CD34+ стволовые клетки и клетки-предшественники не экспрессируют CD138, и моноклональные антитела против CD138 не воздействуют на ряд колониеобразующих единиц в культурах гемопоэтических стволовых клеток (Wijdenes, 1996). В негемопоэтических компартментах антиген CD138 в основном экспрессирован на простом и многослойном эпителии в легком, печени, коже, почке и кишечнике. На эндотелиальных клетках было обнаружено только слабое окрашивание (Bernfield, 1992; Vooijs, 1996). В научной литературе было отмечено, что CD138 существует в полиморфных формах в клетках лимфомы человека (Gattei, 1999).
Моноклональные антитела В-В4, ВС/В-В4, B-B2, DL-101, 1D4, MI15, 1.BB.210, 2Q1484, 5F7, 104-9, 281-2, в частности, В-В4, как было указано в научной литературе, являются специфичными к CD138. Из вышеуказанных моноклональных антител В-В4, 1D4 и MI15 узнают как интактную молекулу, так и центральный белок CD138, и могут узнавать одинаковые или близко родственные эпитопы (Gattei, 1999). Предшествующие исследования показали, что В-В4 не узнает растворимый CD138 и узнает только CD138 в мембраносвязанной форме (Wijdenes, 2002).
В-В4, мышиное моноклональное антитело IgG1, связывается с линейным эпитопом между остатками 90-95 центрального белка на синдекане-1 человека (CD138) (Wijdenes, 1996; Dore, 1998). Было установлено, что в соответствии с паттерном экспрессии CD138 антитело В-В4 активно взаимодействует с линией плазмоцитов RPMI8226, но не взаимодействует с эндотелиальными клетками. Также в соответствии с паттерном экспрессии CD138 антитело В-В4 взаимодействует с линиями эпителиальных клеток А431 (выделенными из кератиноцитов) и HepG2 (выделенными из гепатоцитов). Иммунотоксин В-В4-сапорин также являлся высокотоксичным для линии плазмоцитов RPMI8226, фактически более токсичным, чем свободный сапорин. Однако при исследовании двух линий эпителиальных клеток В-В4-сапорин был токсичен только для линии клеток А431, хотя при выполнении клоногенного анализа В-В4-сапорин не оказывал ингибирующего воздействия на рост клеток А431 (Vooijs, 1996). Друие исследователи сообщали об отсутствии специфичности ММ-ассоциированных антигенов в отношении опухолей (Couturier, 1999).
Термин ”антитело/иммуноконъюгат, по существу состоящий из” определенных компонентов, в контексте настоящего изобретения означает, что данное антитело/иммуноконъюгат состоит из точно определенных компонентов и любых дополнительных веществ или компонентов, которые не влияют на основные характеристики антитела.
В настоящем изобретении использован термин ”опухолевая клетка”, который означает раковые клетки, а также предраковые клетки, которые могут образовывать или не образовывать часть солидной опухоли.
“Агент против клетки-мишени” по настоящему изобретению может связываться с молекулой, экспрессированной клеткой-мишенью, и включает пептиды и непептиды. В частности, агенты против клетки-мишени по настоящему изобретению являются антителами против клетки-мишени и молекулами против клетки-мишени, отличными от иммуноглобулина, которые могут быть созданы на основе белков, отличных от иммуноглобулина, и включают, не ограничиваясь ими, молекулы АФФИЛИН®, АНТИКАЛИН® и АФФИБОДИ®. Молекулы против клетки-мишени, отличные от иммуноглобулина, включают также непептидные молекулы против клетки-мишени, такие как олигонуклеотиды ДНК и РНК против клетки-мишени (аптамеры), а также физиологические лиганды, в частности, лиганды рассматриваемого антигена, такого как CD138.
“Антитело против клетки-мишени” по настоящему изобретению является природным антителом или антителом, созданным на его основе, синтезированным или генетически созданным антителом и связывается с антигеном на представляющей интерес клетке или клетках (клетках-мишенях). Антитело против клетки-мишени по настоящему изобретению включает моноклональное антитело, поликлональное антитело, полиспецифическое антитело, например, биспецифическое антитело) или фрагмент антитела. Антитело против клетки-мишени может быть создано, например, для улучшения сродства к клеткам-мишеням (Ross, 2003) или уменьшения иммуногенности. Антитело против клетки-мишени может быть присоединено к липосомному препарату, включающему эффекторные молекулы (Carter, 2003). Фрагмент антитела включает часть интактного антитела, предпочтительно антигенсвязывающую или вариабельную область интактного антитела. Примеры фрагментов антител по настоящему изобретению включают Fab, Fab', F(ab')2 и Fv фрагменты, а также диатела; домен-специфические антитела (dAb) (Ward, 1989; патент США № 6005079); линейные антитела; одноцепочечные антитела и полиспецифические антитела, образованные из фрагментов антител. В антителе, включающем одноцепочечный фрагмент (scFv) вариабельной области, тяжелая и легкая цепи (VH и VL) могут быть связаны коротким аминокислотным линкером, например, последовательностью (глицин4серин)n, которая обладает достаточной гибкостью, чтобы собрать из двух доменов функциональный антигенсвязывающий карман. Добавление разных сигнальных последовательностей может обеспечить более точную направленную доставку антитела против клетки-мишени. Добавление константной области легкой цепи (CL) обеспечивает димеризацию при помощи дисульфидных связей, в результате чего достигается более высокая устойчивость и авидность. Вариабельные области для создания sсFv, если имеется моноклональное антитело против представляющей интерес мишени, могут быть получены методом ПЦР с обратной транскрипцией, который позволяет клонировать вариабельные области из мРНК, экстрагированной из родительской гибридомы. Альтернативно, scFv может быть создан de novo методом отображения на фаге (Smith, 2001). В использованном здесь значении термин “функциональный фрагмент” применительно к антителу против клетки-мишени означает часть антитела против клетки-мишени, которая может специфически связываться с антигеном, с которым специфически связывается указанное антитело. Биспецифическое антитело по настоящему изобретению может, например, иметь по меньшей мере одно плечо, которое взаимодействует с тканью-мишенью, и одно плечо, которое взаимодействует с линкером (публикация патента США 20020006379). Биспецифическое антитело по настоящему изобретению может также связываться с несколькими антигенами на клетке-мишени (Carter, 2003). Антитело по настоящему изобретению может быть модифицировано, например, путем введения остатков цистеина для введения тиоловых групп (Olafsen, 2004).
В соответствии с настоящим изобретением антитело против клетки-мишени может быть выделено из любого источника и может быть, не ограничиваясь ими, верблюжьим антителом, мышиным антителом, химерным антителом ”мышь-человек” или химерным антителом ”обезьяна-человек”, в частности, химерным антителом ”мышь-человек”, таким как nBT062.
Гуманизированные антитела являются антителами, которые содержат последовательности, выделенные из человеческого антитела и антитела, отличного от человеческого, и также входят в объем настоящего изобретения. Приемлемые методы гуманизации антител включают трансплантацию CDR-области (трансплантация области, определяющей комплементарность) (европейский патент 0239400; WO 91/09967; патенты США №№ 5530101 и 5585089), маскировку и облицовку (европейский патент 0592106; европейский патент 0519596; Padlan, 199; Studnicka et al., 1994; Roguska et al., 1994), перестановку цепи (патент США № 5565332) и делммуносацию™ (Biovation, LTD). В соответствии с методом трансплантации CDR-области определяющие комплементарность области (CDR) мыши, например, из моноклонального антитела В-В4, трансплантируют в остовные области вариабельных областей человека, которые затем соединяют с константными областями человека с созданием человеческого антитела В-В4 (hB-B4). В настоящее время в клинической практике используют несколько антител, гуманизированных методом трансплантации CDR-области, включая МИЛОТАРГ (Sievers et al., 2001) и ГЕЦЕПТИН (Pagran et al., 1998).
Метод маскировки предполагает использование комбинации молекулярного моделирования, статистического анализа и мутагенеза для изменения не являющихся CDR-областями поверхностей вариабельных областей антитела с целью имитации поверхностей известных антител хозяина-мишени. Стратегии и методы маскировки антител и другие методы уменьшения иммуногенности антител в другом хозяине описаны, например, в патенте США № 5639641. Человеческие антитела могут быть получены разными методами, известными в данной области, включая методы отображения на фаге. См. также патенты США №№ 4444887, 4716111, 5545806 и 5814318 и публикации международных заявок на патент WO 98/46645, WO 98/50433, WO 98/24893, WO 98/16654, WO 96/34096, WO 96/33735 и WO 91/10741.
Антитела против клетки-мишени, которые были подвергнуты любым неприродным модификациям, такие как химерные антитела ”мышь-человек” или химерные антитела ”обезьяна-человек”, гуманизированные антитела или антитела, которые были созданы, например, для улучшения их сродства к клеткам-мишеням или уменьшения иммуногенности, а также фрагменты антител, в частности, функциональные фрагменты таких антител против клетки-мишени, которые были подвергнуты любым неприродным модификациям, диатела, домен-специфические антитела, линейные антитела, одноцепочечные антитела и полиспецифические антитела, определяются в настоящем описании изобретения как генетически созданные антитела против клетки-мишени.
Химерные антитела сохраняют область связывания (ABR или Fab-область) антитела, отличного от человеческого, например, мышиного антитела, на основе которого они созданы, в то время как любые константные области могут быть выделены, например, из человеческого антитела. Как правило, химеризация и/или замена константных областей антитела не влияет на сродство антитела, так как области антитела, участвующие в связывании антигена, не затрагиваются такой заменой. В предпочтительном варианте осуществления настоящего изобретения генетически созданное, в частности, химерное антитело по настоящему изобретению, может обладать более высоким сродством связывания (выраженным значениями КD) по сравнению с соответствующим антителом, отличным от человеческого, на основе которого оно создано. В частности, антитело nBT062 и антитела на его основе могут обладать более высоким сродством связывания, чем мышиное антитело В-В4. В другом предпочтительном варианте осуществления настоящего изобретения иммуноконъюгаты, содержащие указанные генетически созданные/химерные антитела, также характеризуются более высоким сродством связывания. В некоторых вариантах осуществления изобретения указанные иммуноконъюгаты могут также обладать другими полезными свойствами, такими как лучшее уменьшение опухолевой массы, по сравнению с иммуноконъюгатами, содержащими мышиное антитело В-В4. В предпочтительном варианте осуществления изобретения генетически созданные, в частности, химерные антитела против клетки-мишени обладают сродством связывания, которое определяется константами диссоциации КD (нМ) менее 1,6, менее 1,5 или около или менее 1,4, в то время как мышиные антитела характеризуются константами диссоциации КD (нМ) около или более 1,6. Иммуноконъюгаты, включающие агенты против клетки-мишени, такие как антитела против клетки-мишени, могут характеризоваться константами диссоциации КD (нМ) менее 2,6, менее 2,5, менее 2,4, менее 2,3, менее 2,2, менее 2,1, менее 2,0, менее или около 1,9, в то время как иммуноконъюгаты, включающие мышиные антитела, могут характеризоваться константами диссоциации КD (нМ) около или более 2,6 (сравните данные, приведенные в таблице 3 раздела ”Вещества и методы”).
Могут быть также использованы полностью человеческие антитела. Указанные антитела могут быть отобраны методом отображения на фаге, при осуществлении которого используют CD138 или его антигенную детерминанту для селективного связывания с фагом, экспрессирующим, например, вариабельные области антитела В-В4 (см. публикацию Krebs, 2001). Данный метод успешно сочетается с методом созревания аффинности для улучшения сродства антитела. Все антитела, рассмотренные в настоящем описании изобретения, являются выделенными антителами.
В одном варианте осуществления изобретения антитело против клетки-мишени является в неконъюгированном виде умеренно или плохо интернализированным. Умеренная интернализация предполагает интернализацию антитела от около 30% до около 75%, плохая интернализация предполагает интернализацию от около 0,01% до около 30% после инкубации в течение 3 часов при 37°С. В другом предпочтительном варианте осуществления изобретения антитело против клетки-мишени связывается с антигеном CD138; такими антителами являются, например, антитела В-В4, ВС/B-B4, B-B2, DL-101, 1D4, MI15, 1.BB.210, 2Q1484, 5F7, 104-9, 281-2, в частности, В-В4. Клетки гибридомы, полученные путем гибридизации миеломных клеток SP02/0 с клетками селезенки мышей Balb/c, депонированы в DSMZ-Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Mascheroder Weg 1, D-38124 Braunschweig 11 декабря 2007 г. Указанные клетки гибридомы, экспрессирующие В-В4, имеют идентифицирующий номер DSM ACC2874. В другом варианте осуществления изобретения антитело против клетки-мишени по существу не связывается с CD138, экспрессированным не на поверхности клетки. Название конкретного антитела, определяемое в контексте настоящего изобретения термином ”антитело против клетки-мишени”, таким как ”антитело против клетки-мишени nBT062”, означает, что данное антитело против клетки-мишени обладает специфичностью связывания антитела nBT062. Указание на то, что антитело против клетки-мишени создано ”на основе” конкретного антитела, означает, что данное антитело против клетки-мишени обладает специфичностью связывания указанного антитела, но может принимать любую форму, сопоставимую с приведенным выше описанием антитела против клетки-мишени. Название конкретного антитела, объединенное в контексте настоящего изобретения с термином ”антитело против клетки-мишени”, таким как ”антитело против CD138”, означает, что антитело против клетки-мишени обладает специфичностью связывания с CD138. Указание в контексте настоящего изобретения на то, что антитело против клетки-мишени делает что-то ”селективно”, например, ”селективно воздействует на экспрессированный на поверхности клетки CD138”, или является ”селективным” в отношении чего-то, означает, что для данного антитела характерна значительная селективность (то есть более высокое сродство к CD138-положительным клеткам по сравнению с CD138-отрицательными клетками), например, в данном примере, к экспрессированному на поверхности клетки CD138 по сравнению с любыми другими антигенами. Благодаря такой селективности значительно уменьшаются или даже полностью устраняются вредные побочные эффекты в данной среде.
Термин ”молекулы против клетки-мишени, отличные от иммуноглобулина” по настоящему изобретению означают молекулы против клетки-мишени, выделенные из белков, отличных от иммуноглобулина, а также непептидные молекулы против клетки-мишени. Мелкие белки, отличные от иммуноглобулина, входящие в данное определение, обладают специфическим сродством, например, в отношении экспрессированного на поверхности CD138. Указанные мелкие белки, отличные от иммуноглобулина, включают молекулы, созданные на основе каркаса, такие как молекулы аффилин®, которые имеют относительно небольшую молекулярную массу, например, в пределах от 10 кДа до 20 кДа. Соответствующий каркас включает, например, кристаллическую гамма-структуру. Указанные молекулы в естественном состоянии не обладают специфической активностью связывания в отношении молекул-мишеней. Благодаря созданию белковых поверхностей путем локальной рандомизации аминокислот, подвергаемых воздействию растворителя, могут быть созданы совершенно новые сайты связывания. Таким образом, исходные не связывающиеся белки превращаются в специфически связывающиеся белки. Такие молекулы могут быть специально созданы для связывания с мишенью, такой как CD138, и могут обеспечивать специфическую доставку одной или нескольких эффекторных молекул (см. scil Proteins GmbH на сайте www.scilproteins.com, 2004). Молекулы против клетки-мишени, отличные от иммуноглобулина, другого типа, получаемые из липокалинов, включают, например, АНТИКАЛИНЫ®, которые имеют структуру, подобную в некоторой степени иммуноглобулинам. Однако липокалины состоят из одной полипептидной цепи, содержащей 160-180 аминокислотных остатков. Связывающий карман липокалинов может быть изменен для узнавания представляющей интерес молекулы с высоким сродством и специфичностью (см., например, публикацию Beste et al., 1999). В объем настоящего изобретения входят также искусственные бактериальные рецепторы, такие как продаваемые на рынке под торговым названием аффибоди® (аффибоди АВ). Указанные молекулы искусственных бактериальных рецепторов являются мелкими простыми белками и могут состоять из трех спиралей, полученных на каркасе из одного из IgG-связывающих доменов белка А (Staphylococcus aureus). Свойства связывания указанных молекул подобны многим иммуноглобулинам, но такие молекулы значительно меньше и имеют молекулярную массу, которая часто не превышает 10 кДа, и являются сравнительно устойчивыми. Приемлемые молекулы искусственных бактериальных рецепторов описаны, например, в патентах США №№ 5831012, 6534628 и 6740734.
Другие ”молекулы против клетки-мишени, отличные от иммуноглобулина” являются физиологическими лигандами рассматриваемого антигена. Физиологические лиганды CD138 включают, например, не ограничиваясь ими, ADAMTS4 (агреканаза-1), антитромбин-3, bFGF, катепсин G, CCL5 (RANTES), CCL7, CCL11, CCL17, CD44, коллагены (коллаген типа 1, коллаген типа 2, коллаген типа 3, коллаген типа 4, коллаген типа 5, коллаген типа 6), CXCL1, эластазу, gp120, HGF [фактор роста гепатоцитов], ламинин-1, ламинин-2, ламинин-5, мидкин, ММР-7, эластазу нейрофилов и плеиотрофин (HBNF, HBGF-8). Непептидные молекулы против клетки-мишени включают, не ограничиваясь ими, олигонуклеотиды ДНК и РРК, которые связываются с CD138 (аптамеры).
“Эффекторная молекула” по настоящему изобретению является молекулой, ее производным или аналогом, которая присоединена к агенту против клетки-мишени, в частности, к антителу против клетки-мишени и/или генетически созданному антителу против клетки-мишени, и оказывает требуемое действие, например, вызывает апоптоз или гибель клетки другого типа, остановку непрерывного клеточного цикла в одной или нескольких клетках-мишенях. Эффекторные молекулы по настоящему изобретению являются молекулами, которые могут оказывать требуемое действие в клетке-мишени, и включают, не ограничиваясь ими, токсины, лекарственные средства, в частности, низкомолекулярные цитотоксические лекарственные средства, радиоактивные изотопы, модификаторы биологических реакций, порообразующие агенты, рибонуклеазы, белки сигнальных путей активации апоптоза, способные индуцировать апоптоз, цитотоксические ферменты, ферменты, активирующие пролекарства, антисмысловые олигонуклеотиды, антитела или цитокины, а также их функциональные производные или аналоги/фрагменты. Токсины могут быть бактериальными токсинами, включающими, не ограничиваясь ими, дифтерийный токсин или экзотоксин А, растительными токсинами, такими как, рицин, но не ограничиваясь им. Белки сигнальных путей активации апоптоза, способные индуцировать апоптоз, включают, не ограничиваясь ими, гранзим В, гранзим А, каспазу-3, каспазу-7, каспазу-8, каспазу-9, усеченный бид (tBid), бакс и бак.
В предпочтительном варианте осуществления изобретения эффектор повышает доставку эффектора иммуноконъюгатом, в частности, тогда, когда природное антитело, на основе которого создано антитело против клетки-мишени иммуноконъюгата, плохо интернализировано. В другом предпочтитиельном варианте осуществления изобретения эффектор в нативной форме является неселективным. В определенных вариантах осуществления изобретения эффектор в нативной форме обладает высокой неселективной токсичностью, включая системную токсичность. Термин ”нативная форма” эффекторной молекулы по настоящему изобретению означает форму эффекторной молекулы до присоединения к агенту против клетки-мишени с образованием иммуноконъюгата. В другом предпочтительном варианте осуществления изобретения неселективная токсичность эффекторной молекулы по существу полностью устраняется при конъюгации с агентом против клетки-мишени. В другом предпочтительном варианте осуществления изобретения эффекторная молекула вызывает при достижении клетки-мишени гибель или остановку непрерывного клеточного цикла в клетке-мишени. Эффекторная молекула, являющаяся лекарственным средством, включает, не ограничиваясь ими, такие лекарственные средства как, например, низкомолекулярные высокотоксичные лекарственные средства, которые действуют в качестве ингибиторов полимеризации тубулина, например, майтанзиноиды, доластатины, ауристатин и критофицин; ДНК-алкилирующие агенты, подобные аналогам или производным СС-1065 (патенты США №№ 5475092, 5585499, 6716821) и дуокармицин, энедииновые антибиотики, такие как калихеамицин и эсперамицин, и сильнодействующие таксоидные (таксан) лекарственные средства (Payne, 2003). Майтанзиноиды и калихеамицины являются особенно предпочтительными. Майтанзиноидный эффектор включает майтанзиноиды любого происхождения, в том числе, не ограничиваясь ими, синтетический майтанзинол, аналог и производное майтанзинола. Доксорубицин, дауномицин, метотрексат, винбластин, неокарзиностатин, макромицин, тренимон и α-аманитин являются некоторыми другими эффекторными молекулами, входящими в объем настоящего изобретения. Кроме того, в объем настоящего изобретения в качестве эффекторных молекул входят также молекулы антисмысловой ДНК. Когда название, например, конкретного лекарственного средства или класса лекарственных средств использовано в сочетании с термином ”эффектор” или “эффекторная молекула”, имеется в виду эффектор иммуноконъюгата по настоящему изобретению, созданный на основе указанного лекарственного средства или класса лекарственных средств.
Майтанзин является природным продуктом, первоначально выделенным из эфиопского кустарника Maytenus serrata (Remillard, 1975; патент США № 3896111). Указанное лекарственное средство ингибирует полимеризацию тубулина, что вызывает митотическую блокаду и гибель клетки (Remillard, 1975; Bhattacharyya, 1977; Kupchan, 1978). Цитотоксичность майтанзина в 200-1000 раз выше, чем у противораковых средств, используемых в клинической практике, которые воздействуют на полимеризацию тубулина, таких как алкалоиды барвинка или таксол. Однако клинические испытания майтанзина показали, что он не может быть использован в клинической медицине из-за высокой системной токсичности. Майтанзин и майтанзиноиды являются высокоцитотоксическими веществами, но их клиническое применение при лечении рака сильно ограничено из-за тяжелых системных побочных эффектов, связанных главным образом с плохой селективностью в отношении опухолей. Клинические испытания майтанзина выявили серьезное вредное влияние на центральную нервную систему и желудочно-кишечный тракт.
Майтанзиноиды были также выделены из других растений, в том числе из семян Trewia nudiflora (патент США № 4418064).
Некоторые микробы также продуцируют майтанзиноиды, такие как майтанзинол и сложные эфиры майтанзинола С-3 (патент США № 4151042).
Настоящее изобретение относится к майтанзиноидам любого происхождения, включая синтетический майтанзинол и аналоги майтанзинола, описанные, например, в патентах США № 4137230, 4248870, 4256746, 4260608, 4265814, 4294757, 4307016, 4308268, 4308269, 4309428, 4313946, 4315929, 4317821, 4322348, 4331598, 4361650, 4362663, 4364866, 4371533, 4424219 и 4151042.
В предпочтительном варианте осуществления изобретения майтанзиноид является тиолсодержащим майтанзиноидом, который более предпочтительно получают способами, описанными в патенте США № 6333410, выданном Chari et al., или в публикации Chari et al. (Chari, 1992).
DM-1 (N2-деацетил-N2-(3-меркапто-1-оксопропил)майтанзин) является предпочтительной эффекторной молекулой в контексте настоящего изобретения. DM-1 в 3-10 раз более цитотоксичен, чем майтанзин, и превращается в пролекарство при связывании дисульфидной связью с моноклональным антителом против опухолеспецифического антигена. Некоторые такие конъюгаты (иногда именуемые ”опухолеактивируемыми пролекарствами” (TAP)) не являются цитотоксическими в кровяном русле, так как указанные конъюгаты активируются при связывании с клетками-мишенями и интернализируются, высвобождая лекарственное средство (Blattler, 2001). Было создано несколько конъюгатов антитело-DM1 (Payne, 2003), которые прошли клинические испытания. Например, субъекты, страдающие колоректальным раком, хорошо переносили лечение конъюгатом huC242-DM1, который не вызывал какой-либо обнаруживаемой иммунной реакции и характеризовался продолжительным временем нахождения в кровотоке (Tolcher, 2003).
Другие особенно предпочтительные майтанзиноиды имеют боковую цепь, содержащую тиоловую связь со стерическим препятствием, и включают, не ограничиваясь ими, такие майтанзиноиды как N2'-деацетил-N2'-(4-меркапто-1-оксопентил)майтанзин, именуемый также ”DM3”, и N2'-деацетил-N2'-(4-метил-4-меркапто-1-оксопентил)майтанзин, именуемый также ”DM4”. Синтез DM4 показан на Фиг.3 и 4 и описан в настоящем описании изобретения. DM4 отличается от DM1 и DM3 тем, что содержит метильные группы в положении αС. Благодаря этому образуется стерическое препятствие при присоединении DM4 с помощью линкера, который включает, не ограничиваясь им, линкер, имеющий дисульфидную связь, к агенту против клетки-мишени, такому как антитело nBT062. Целый ряд майтанзиноидов, содержащих тиоловую группу со стерическим препятствием (имеющую один или два заместителя, в частности, алкильных заместителя, таких как метильные заместители DM4), описан в публикации патента США 2004/0235840, опубликованной 25 ноября 2004 г., которая полностью включена в настоящее описание изобретения в качестве ссылки. Стерическое препятствие, образуемое алкильными группами, такими как метильные группы в положении атома углерода, смежного с атомом серы, в DM3 и DM4, может влиять на скорость внутриклеточного расщепления иммуноконъюгата. Таким образом, переменное алкильное звено может влиять на силу воздействия, эффективность и безопасность/токсичность in vitro и in vivo.
Как отмечали Голдмахер и др. в публикации патента США 2006/0233814, такое препятствие вызывает алкилирование (например, метилирование) свободного лекарственного средства после высвобождения лекарственного средства в клетке-мишени. Алкилирование может повышать устойчивость лекарственного средства, вызывая так называемый эффект неспецифического цитолиза. Однако, как должно быть понятно специалисту в данной области, другие эффекторные молекулы, включающие такие заместители как алкильные группы в положениях, образующих стерическое препятствие при присоединении эффектора к агенту против клетки-мишени с помощью линкера, также входят в объем настоящего изобретения (публикация патента США 2004/0235840). Указанное препятствие предпочтительно вызывает химическую модификацию, такую как алкилирование свободного лекарственного средства, что повышает его устойчивость, благодаря чему лекарственное средство не только индуцирует гибель клетки или остановку непрерывного клеточного цикла в CD138-экспрессирующих опухолевых клетках, но также необязательно воздействует на А-клетки, которые, например, поддерживают или защищают опухоль от лекарственных средств, в частности, клетки стромы и сосудистой сети опухоли, и обычно не экспрессируют CD138, обеспечивая ослабление или утрату поддерживающей или защитной функции таких клеток.
ДНК-алкилирующие агенты также являются особенно предпочтительными эффекторными молекулами и включают, не ограничиваясь ими, аналоги или производные СС-1065. СС-1065 является сильнодействующим противоопухолевым антибиотиком, выделенным из культур Streptomyces zelensis, и, как установлено, обладают исключительно высокой цитотоксичностью in vitro (патент США № 4169888). В объем настоящего изобретения входят, например, аналоги или производные СС-1065, описанные в патентах США №№ 5475092, 5585499 и 5739350. Как должно быть понятно специалисту в данной области, в объем настоящего изобретения входят также модифицированные аналоги или производные СС-1065, описанные в патенте США № 5846545, и пролекарства аналогов или производных СС-1065, описанные, например, в патенте США № 6756397. В некоторых вариантах осуществления изобретения аналоги или производные СС-1065, например, могут быть синтезированы способом, описанным в патенте США № 6534660.
К другой группе соединений, являющихся предпочтительными эффекторными молекулами, относятся таксаны, особенно сильнодействующие таксаны и таксаны, содержащие тиоловые или дисульфидные группы. Таксаны являются митотическими веретенообразными ядами, которые ингибируют деполимеризацию тубулина, увеличивая таким образом скорость сборки микротрубочек и гибель клетки. Таксаны, входящие в объем настоящего изобретения, описаны, например, в патентах США №№ 6436931, 6340701, 6706708 и публикациях патентов США 20040087649, 20040024049 и 20030004210. Другие таксаны описаны, например, в патенте США № 6002023, патенте США № 5998656, патенте США № 5892063, патенте США № 5763477, патенте США № 5705508, патенте США № 5703247 и патенте США № 5367086. Как должно быть понятно специалисту в данной области, в объем настоящего изобретения входят также пегилированные таксаны, аналогичные описанным в патенте США № 6596757.
Эффекторные молекулы калихеамицина по настоящему изобретению включают гамма 1I, N-ацетилкалихеамицин и другие производные калихеамицина. Калихеамицин связывается специфично к последовательности с малой бороздкой ДНК, реаранжируется и открывает свободные радикалы, разрывая таким образом двухцепочечную ДНК, что вызывает апоптоз и гибель клетки. Один пример эффекторной молекулы калихеамицина, которая может быть использована в контексте настоящего изобретения, приведен в патенте США № 5053394.
Иммуноконъюгат по настоящему изобретению включает по меньшей мере один агент против клетки-мишени, в частности, антитело против клетки-мишени, такое как генетически созданное антитело против клетки-мишени, и одну эффекторную молекулу. Иммуноконъюгат может далее включать, например, стабилизирующие молекулы. Для иммуноконъюгатов термин ”конъюгация” обычно используется для определения функционального связывания агента против клетки-мишени с одной или несколькими эффекторными молекулами и не относится к какому-либо одному типу функционального связывания, в частности, не ограничивается химическим ”сопряжением”. Любой способ присоединения является приемлемым, если агент против клетки-мишени способен связываться с сайтом-мишенью и присоединенный эффектор действует должным образом, особенно после доставки к сайту-мишени. Методы конъюгации по настоящему изобретению включают, не ограничиваясь ими, прямое присоединение эффекторной молекулы к антителу против клетки-мишени с выполнением предварительной модификации или без предварительной модификации эффекторной молекулы и/или антитела против клетки-мишени, или присоединение с помощью линкеров. Линкеры могут быть классифицированы с точки зрения функциональности, например, на кислотолабильные линкеры, фотолабильные линкеры, линкеры, расщепляемые ферментами, например, линкеры, расщепляемые пептидазами. Расщепляемые линкеры являются предпочтительными во многих вариантах осуществления изобретения. Такие расщепляемые линкеры могут расщепляться в условиях клеточной среды, в частности, внутриклеточной среды, и не оказывают вредного влияния на лекарственное средство, высвобождаемое в результате расщепления. Кислотолабильные линкеры могут расщепляться при низких значениях рН, таких как рН 4-5, имеющих место в определенных внутриклеточных отделах, в то время как фотолабильные линкеры могут расщепляться, например, под воздействием инфракрасного света. Однако линкеры, которые расщепляются в физиологических условиях, имеющих место в большинстве клеток, являются более предпочтительными и определяются в настоящем описании изобретения как физиологически расщепляемые линкеры. Таким образом, дисульфидные линкеры являются предпочтительными во многих вариантах осуществления изобретения. Указанные линкеры расщепляются в результате дисульфидного обмена, который может происходить в физиологических условиях. Предпочтительные гетеробифункциональные дисульфидные линкеры включают, не ограничиваясь ими, N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP) (см., например, публикацию Carisson et al., 1978), N-сукцинимидил-4-(2-пиридилдитио)бутаноат (SPDB) (см., например, патент США № 4563304), N-сукцинимидил-4-(2-пиридилдитио)пентаноат (SPP) (см., например, регистрационную запись CAS № 341498-08-6), N-сукцинимидил-4-(N-малеимидометил)-циклогексан-1-карбоксилат (SMCC) (см., например, публикацию Yoshitake et al., (1979) и N-сукцинимидил-4-метил-4-[2-(5-нитропиридил)дитио]пентаноат (SMNP) (см., например, патент США № 4563304). Наиболее предпочтительными линкерными молекулами, пригодными для использования в настоящем изобретении, являются SPP, SMCC и SPDB.
Другие приемлемые линкеры могут включать ”нерасщепляемые” связи, такие как, например, сульфосукцинимидилмалеимидометилциклогексанкарбоксилат (SMCC), который является гетеробифункциональным линкером, способным связывать соединения с SH-содержащими соединениями. В объем настоящего изобретения входят также бифункциональные и гетеробифункциональные линкерные молекулы, в частности, углевод-направленные гетеробифункциональные линкерные молекулы, такие как S-(2-тиопиридил)-L-цистеингидразид (ТРСН) (Vogel, 2004). Эффекторная молекула, такая как майтанзиноид, может быть конъюгирована с антителом против клетки-мишени двухстадийным способом, на первой стадии которого антитело против клетки-мишени модифицируют перекрестносшивающим реагентом, таким как N-сукцинимидилпиридилдитиопропионат (SPDP), для введения дитиопиридильных групп в антитело против клетки-мишени. На второй стадии к модифицированному антителу может быть добавлен реакционноспособный майтанзиноид, содержащий тиоловую группу, такой как DM1, в результате чего происходит замещение тиопиридильных групп в модифицированном антителе и образование цитотоксического конъюгата майтанзиноид-антитело, связанного дисульфидной связью (патент США № 5208020). Однако в объем настоящего изобретения входят также одностадийные способы конъюгации, аналогичные описанным в публикации патента США 20030055226, выданного Чари и др. В одном варианте осуществления настоящего изобретения к антителу против клетки-мишени присоединяют несколько эффекторных молекул одинакового или разного типа. Как указано в настоящем описании изобретения, характер используемых линкеров может влиять на неспецифический цитолиз. См. также фиг.13.
Аналоги или производные СС-1065 могут быть конъюгированы с агентом против клетки-мишени при помощи полиэтиленгликолевых (PEG) связующих групп, описанных в патенте США № 6716821.
Калихеамицины могут быть конъюгированы с антителами против клетки-мишени при помощи линкеров (патент США № 5877296 и патент США № 5773001) или методами конъюгации, описанными в патенте США № 5712374 и патенте США № 5714586. Другой предпочтительный способ получения конъюгатов калихеамицина описан в публикации патента США 20040082764. Иммуноконъюгаты по настоящему изобретению могут иметь форму рекомбинантных слитых белков.
Термин ”цитотоксические средства” означает ”цитотоксические/противораковые средства”, включающие химиотерапевтические средства, такие как мелфалан, циклофосфамид, винкристин, доксорубицин и липосомный доксорубицин (DOXIL), циклофосфамид, этопозид, цитарабин и цисплатин, кортикостероиды, такие как прендизон и дексаметазон, такие средства как талидомид, бортезомиб, леналидомид, ингибиторы киназы, такие как сорафениб, или ингибиторы HDAC (гистондеацетилаза), такие как ромидепсин, а также ингибиторы роста, антигормональные средства, средства, препятствующие развитию кровеносных сосудов, кардиопротекторы, иммуностимулирующие средства, иммунодепрессивные средства, ингибиторы ангиогенеза, ингибиторы протеин-тирозинкиназы (РТК). Данный термин также означает цитотоксические средства на основе антитела, включающие иммуноконъюгаты и антитела, обладающие известным цитотоксическим действием. Антитело против CD40 является предпочтительным антителом. Другие антитела включают, не ограничиваясь ими, например, АВАСТИН (бевацизуаб) или МИЕЛОМАЦИД (милатузумаб).
ТАЛОМИД (α-(N-фталимидо(глутаримид; талиомид) является иммуномодулирующим средством. Талидомид имеет эмпирическую формулу С13Н10N2O4 и грамм-молекулярную массу, равную 258,2. Номер талидомида по классификации CAS 50-35-1. Талидомид выполняет разные функции, включая способность ингибировать рост и выживание миеломных клеток разными способами и ингибировать рост новых кровеносных сосудов.
ВЕЛКАД является ингибитором протеасомы, используемым для лечения множественной миеломы. Считается, что ВЕЛКАД воздействует на миеломные клетки, вызывая гибель клетки, и/или опосредованно ингибирует рост и выживание миеломных клеток, воздействуя на микросреду костного мозга. Не ограничиваясь конкретной теорией или способом действия, можно отметить, что ВЕЛКАД нарушает нормальные клеточные процессы, в результате чего происходит ингибирование протеасомы, вызывающее апоптоз клетки.
РУВЛИМИД является иммуномодулирующим средством. Считается, что РУВЛИМИД влияет на многие пути в миеломных клетках, вызывая апоптоз, ингибируя рост миеломных клеток, подавляя эндотелиальный фактор роста сосудистой сети (VEGF) и ингибируя таким образом развитие кровеносных сосудов, уменьшая адгезию миеломных клеток к стромальным клеткам костного мозга.
Дексаметазон является синтетическим глюкокортикоидным стероидным гормоном, который действует в качестве противовоспалительного средства и иммунодепрессанта. При введении субъектам, страдающим раком, дексаметазон может противодействовать возникновению побочных эффектов при лечении рака. Дексаметазон может быть введен отдельно или вместе с другими противораковыми средствами, включающими талидомид, адриамицин или винкристин.
Термин ”в комбинации с” не ограничен введением точно в одно время. Наоборот, данный термин предполагает последовательное введение иммуноконъюгата по настоящему изобретению и другого средства, в частности, вышеописанных цитотоксических средств, или проведение другого лечения (например, лучевой терапии) в течение периода времени, обеспечивающего совместное действие с достижением более высокого благоприятного воздействия по сравнению с использованием только иммуноконъюгата по настоящему изобретению или, например, другого средства или средств. Желательно, чтобы иммуноконъюгат и другое средство или средства вызывали аддитивный эффект, и особенно желательно, чтобы они оказывали синергическое действие. Такие молекулы получают в количествах, обеспечивающих эффективное достижение предполагаемой цели. Квалифицированный лечащий врач может определить эмпирически или с учетом фармакокинетики и характера действия указанных средств соответствующую дозу или дозы каждого терапевтического средства, а также соответствующее время и способы введения. В значении, использованном в контексте настоящего изобретения, термин ”совместное введение” означает введение одновременно с иммуноконъюгатом, часто в комбинированной лекарственной форме.
Термин “идентичность последовательностей” означает меру идентичности нуклеотидных последовательностей или аминокислотных последовательностей. Последовательности обычно подвергают сравнительному анализу до достижения соответствия высшего порядка. Термин ”идентичность” сам по себе имеет известное значение в данной области, при этом идентичность может быть вычислена при помощи опубликованных методов. (См., например, публикации
Несмотря на то, что существует много методов измерения идентичности двух полинуклеотидных или полипептидных последовательностей, термин ”идентичность” хорошо известен квалифицированным специалистам (Carillo, H. & Lipton, D., SIAM J. Applied Math. 48:1073 (1988)).
То, что любая конкретная молекула нуклеиновой кислоты по меньшей мере на 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентична, например, последовательности нуклеиновой кислоты антитела nBT062 или ее части, можно определить при помощи известных компьютерных программ, таких как программное обеспечение DNAsis (Hitachi Software, San Bruno, Calif.), предназначенных для выполнения первоначального сравнительного анализа последовательностей, с последующим выполнением программы ESEE, версия 3.0, для анализа ДНК/белковых последовательностей (cabot@trog.mbb.sfu.ca), предназначенной для сравнительного анализа множества последовательностей.
То, что аминокислотная последовательность по меньшей мере на 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентична, например, SEQ ID NO:1 или SEQ ID NO:2 или ее части, можно определить при помощи известных компьютерных программ, таких как программа BESTFIT (Wisconsin Sequence Analysis Package, Version 8 for Unix, Genetics Computer Group, University Research Park, 575 Science Drive, Madison, Wis. 53711). В программе BESTFIT использован алгоритм локальной гомологии, представленный в публикации Smith and Waterman, Advances in Applied Mathematics 2:482-489 (1981), который предназначен для поиска лучшего гомологичного сегмента в двух последовательностях.
При использовании программ DNAsis, ESEE, BESTFIT или любой другой программы для сравнительного анализа последовательностей с целью определения того, что конкретная последовательность, например, на 95% идентична эталонной последовательности по настоящему изобретению, параметры задают с возможностью вычисления процентного значения идентичности на протяжении всей длины эталонной последовательности нуклеиновой кислоты или аминокислотной последовательности, при этом допускаются разрывы гомологии до 5% от общего числа нуклеотидов в эталонной последовательности.
Если в контексте настоящего изобретения указана идентичность определенной последовательности с комбинацией остатков конкретной последовательности, это значит, что идентичность последовательности относится к сумме всех указанных остатков.
Основная молекула антитела имеет бифункциональную структуру, в которой вариабельные области связываются с антигеном, в то время как реакции оставшихся константных областей не зависят от антигена. Основные классы антител, IgA, IgD, IgE, IgG и IgM, определяются по константным областям. Указанные классы могут быть далее разделены на подклассы (изотипы). Например, класс IgG имеет четыре изотипа, а именно IgG1, IgG2, IgG3 и IgG4, которые определяются по константным областям. Известно, что из разных классов человеческих антител только IgG1, IgG2, IgG3 и IgM человека эффективно активируют систему комплементов. Несмотря на то, что константные области не образуют антигенсвязывающих центров, расположение константных областей и шарнирной области может сообщать молекуле сегментную гибкость, которая позволяет молекуле связываться с антигеном.
Разные изотипы IgG могут связываться с Fc-рецепторами на таких клетках как моноциты, В-клетки и NK-клетки, активируя таким образом клетки с целью высвобождения цитокинов. Разные изотипы могут также активировать комплемент, вызывая местное или системное воспаление. В частности, разные изотипы IgG могут связываться с FcγR в разной степени. FcγR представляют собой группу поверхностных гликопротеинов, относящихся к надсемейству Ig и экспрессированных главным образом на лейкоцитах. Гликопротеины FcγR разделены на три класса, обозначенные FcγRI (СD64), FcγRII (CD32) и FcγRIII (CD16). В то время как IgG1, IgG2 и IgG3 сильно связываются с разными гликопротеинами FcγR указанных классов, IgG4 отличается гораздо более слабым связыванием. В частности, IgG4 связывается с FcγRI со средней силой, что является причиной относительно низкой ADCC или даже полного отсутствия ADCC (антителозависимая клеточно-опосредованная цитотоксичность), и не связывается с FcγRIIIA или FcγRIIА. IgG4 также слабо связывается с FcγRIIВ, который является ингибирующим рецептором. Кроме того, IgG4 опосредует только слабую фиксацию комплемента или не опосредует такую фиксацию и вызывает слабую комплементзависимую цитотоксичность (CDC) или не вызывает такую цитотоксичность. В контексте настоящего изобретения IgG4 может быть специально использован для предотвращения Fc-опосредованного направленного воздействия на FcR печени, так как IgG4 не взаимодействует с FcRγII на клетках LSEC (синусоидальные эндотелиальные клетки печени), не взаимодействует или слабо взаимодействует с FcRγI-III на клетках Капффера (макрофаги) и не взаимодействует с FcRγIII на NK-клетках печени. В объем настоящего изобретения входят также определенные мутации, которые еще больше уменьшают CDC. Например, известно, что остатки IgG4 в положениях 327, 330 и 331 уменьшают ADCC (антителозависимая клеточно-опосредованная цитотоксичность) и CDC (Amour, 1999; Shields, 2001). Одна или несколько мутаций, стабилизирующих антитело, также являются частью настоящего изобретения (в настоящем описании изобретения определяются также как ”стабилизирующие мутации”). Указанные мутации, в частности, включают мутации с заменой лейцина глутаминовой кислотой в СН2-области IgG4 и с заменой серина пролином в шарнирной области IgG4. В некоторых вариантах осуществления изобретения указанные мутации уменьшают количество полумолекул до менее 10%, менее 5% и предпочтительно менее 2% или 1%. Кроме того, время полужизни in vivo стабилизированных антител может быть увеличено на несколько дней, в том числе на 1, 2, 3, 4 или больше, чем на 5 дней (Schuurman, 1999).
Агенты против клетки-мишени, включающие антитела против клетки-мишени, в частности, генетически созданные антитела против клетки-мишени, рассмотренные в настоящем описании изобретения, могут быть также определены с учетом их сродства связывания с антигеном, в частности, с CD138. Предпочтительное сродство связывания агентов против клетки-мишени, таких как антитела против клетки-мишени, характеризуется константами диссоциации КD (нМ) менее 1,6, менее 1,5 или около или менее 1,4. Для иммуноконъюгатов, включающих указанные агенты против клетки-мишени, такие как антитела против клетки-мишени, предпочтительными являются константы диссоциации КD (нМ) менее 1,6, менее 1,5, менее 2,5, менее 2,4, менее 2,3, менее 2,2, менее 2,1, менее 2,0, менее или около 1,9.
Антигенсвязывающая область (ABR) по настоящему изобретению может изменяться в зависимости от типа антитела против клетки-мишени или генетически созданного антитела против клетки-мишени. В природном антителе и в большинстве химерных и гуманизированных антител антигенсвязывающая область состоит из легкой цепи и первых двух доменов тяжелой цепи. Однако в антителе с тяжелой цепью, не имеющем легких цепей, антигенсвязывающая область может состоять, например, только из первых двух доменов тяжелой цепи, в то время как в одноцепочечных антителах (ScFv), которые объединяют в одной полипептидной цепи вариабельные области легкой и тяжелой цепей, ABR образуется только одной полипептидной молекулой. FAB-фрагменты, обычно получаемые в результате расщепления папаином, имеют одну легкую цепь и часть тяжелой цепи и, таким образом, включают ABR только с одним антигенсвязывающим центром. С другой стороны, диатела являются мелкими фрагментами антитела с двумя антигенсвязывающими областями. Однако в контексте настоящего изобретения антигенсвязывающая область антитела против клетки-мишени или генетически созданного антитела против клетки-мишени является любой областью, которая определяет главным образом специфичность связывания антитела против клетки-мишени или генетически созданного антитела против клетки-мишени.
Если указано, что антигенсвязывающая область или другая область антитела против клетки-мишени является областью ”определенного антитела”, например, человеческого антитела или антитела, отличного от человеческого, это значит в контексте настоящего изобретения, что антигенсвязывающая область (ABR) или идентична соответствующей природной ABR, или создана на ее основе. Антигенсвязывающая область считается созданной на основе природной ABR, если она обладает специфичностью связывания природной ABR. Однако такая антигенсвязывающая область может включать, например, точковые мутации, добавления, делеции или посттрансляционную модификацию, такую как гликозилирование. Такая антигенсвязывающая область, в частности, может иметь последовательность, которая более, чем на 70%, более, чем на 80%, более, чем на 90%, предпочтительно более, чем на 95%, более, чем на 98% или более, чем на 99% идентична последовательности природной ABR.
Гомогенное направленное воздействие агента против клетки-мишени, такого как антитело против клетки-мишени, и, в частности, иммуноконъюгата, содержащего такой агент, в контексте настоящего изобретения является мерой дисперсии при достижении требуемого результата указанного направленного воздействия агента против клетки-мишени. В определенных вариантах осуществления изобретения требуемый результат достигается при простом связывании с мишенью. Именно так обстоит дело, например, в тех вариантах осуществления изобретения, в которых определенный агент против клетки-мишени обеспечивает защиту от последующего связывания. Однако гомогенность агента против клетки-мишени можно легко оценить, например, путем определения эффективности иммуноконъюгата, включающего указанный агент против клетки-мишени. Например, эффективность указанного иммуноконъюгата против опухолевого антигена, такого как CD138, который включает эффектор, нацеленный на разрушение опухолевых клеток и/или остановку роста опухоли, можно определить по степени подавления роста опухоли, включающей клетки, экспрессирующие антиген CD138. Такой иммуноконъюгат может характеризоваться высокой дисперсией эффективности. Например, в одних случаях иммуноконъюгат может останавливать рост опухоли с высокой эффективностью, а в других случаях с эффективностью, едва превышающей эффективность контрольного вещества. Низкая дисперсия эффективности конъюгата, с другой стороны, показывает, что данный иммуноконъюгат и/или соответственно агент против клетки-мишени обеспечивают согласованное достижение требуемого результата. Одним способом количественного определения гомогенности направленного воздействия является вычисление изменчивости направленного воздействия. Применительно к остановке роста опухоли иммуноконъюгатом, включающим определенный агент против клетки-мишени, изменчивость направленного воздействия можно вычислить, определяя время, необходимое для достижения опухолью заранее определенного объема, например, 300 мм3. Заранее определенный объем предпочтительно выбирают таким образом, чтобы рост опухоли до и после достижения указанного заранее определенного объема постоянно увеличивался с примерно одинаковой скоростью. После определения такого времени для группы субъектов вычисляют среднее значение указанного времени (Тm) в группе субъектов (например, у мышей SCID или в другой приемлемой модели, характеризующейся гомогенным ростом опухоли). Затем значение Тm коррелируют с данными наблюдений, полученными у субъекта в группе с наименьшей эффективностью направленного воздействия и, следовательно, с наименьшим временем (Тf), необходимым для достижения опухолью заранее определенного объем, и, с другой стороны, у субъекта в группе с наибольшей эффективностью направленного воздействия и, следовательно, с наибольшим временем (Тs), необходимым для достижения опухолью заранее определенного объема, вычисляя изменчивость направленного воздействия для заранее определенного объема по следующей формуле:
Изменчивость направленного воздействия [%]=Ts-Tf/Tm×100
В предпочтительном варианте осуществления изобретения изменчивость направленного воздействия иммуноконъюгата, включающего генетически созданное антитело против клетки-мишени по настоящему изобретению, составляет менее 150%, менее 140%, менее 130%, менее 120%, менее 110%, менее 100%, менее 90%, менее 80%, менее 70%, менее 60% или менее 50% и в определенных вариантах осуществления изобретения даже менее 45%. Изменчивость направленного воздействия предпочтительно находится в пределах от около 10% до около 150%, предпочтительно от около 10% до около 100%, от около 10% до около 80%, от около 10% до около 70%, от около 10% до около 60%, от около 10% до около 50%.
Гомогенность направленного воздействия можно также количественно определить другим способом, например, путем определения задержки роста опухоли. Кроме того, специалисту в данной области должно быть понятно, что объем опухоли определенного размера является только одним параметром, на основании которого можно определить изменчивость направленного воздействия. В зависимости от требуемого результата можно использовать другие парамеры, которые включают время (например, для измерения задержки роста опухоли) или % связывания. Специалист в данной области может легко определить такие параметры.
На Фиг.9С и 9D показаны различия в гомогенности направленного воздействия/связывания иммуноконъюгатов, включающих мышиное антитело ВВ4 (ВВ4-SPP-DM1; Фиг.9С) и созданное на его основе антитело против клетки-мишени nBT062 (nBT062-SPP-DM1; Фиг.9D). Как видно из приведенных графиков, результаты, полученные при использовании иммуноконъюгата, включающего генетически созданное антитело против клетки-мишени, являются значительно более гомогенными по сравнению с результатами, полученными для иммуноконъюгатов, включающих мышиное антитело. Это особенно заметно, так как область связывания антитела ВВ4 не была модифицирована в антителе nBT062. Таким образом, иммуноконъюгат, включающий область связывания мышиного антитела при отсутствии других частей мышиного антитела, обладает свойствами, которые намного превосходят результаты, ожидаемые специалистом в данной области.
Антитело nBT062 (см. также Фиг.1) является химерным моноклональным антителом IgG4 ”мышь-человек”, химерным вариантом антитела В-В4. Химерный вариант антитела В-В4 был создан с целью ослабления реакции НАМА (антитела человека против антитела мыши) при сохранении функциональности области связывания антитела В-В4 в отношении CD138. Удивительным было то, что результаты, полученные при использовании иммуноконъюгата, включающего генетически созданное антитело против клетки-мишени, были гораздо более гомогенными (уменьшилось расхождение результатов). Ниже описан способ получения антитела nBT062. Клетки яичника китайского хомячка, экспрессирующие антитело nBT062, были депонированы в DSMZ-Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Mascheroder Weg 1, D-38124 Braunschweig 11 декабря 2007 г. Указанные клетки имеют идентифицирующий номер DSM ACC2875. CD138-специфическое химерное антитело, созданное на основе антитела В-В4, определяется в настоящем описании изобретения как с-В-В4.
Аминокислотная последовательность для тяжелой и легкой цепей была прогнозирована в результате трансляции нуклеотидной последовательности для nBT062. Аминокислотные последовательности, прогнозированные для тяжелой цепи и легкой цепи, приведены в таблице 1. Прогнозированные вариабельные области выделены жирным шрифтом, прогнозированные CDR-области подчеркнуты.
Прогнозированная аминокислотная последовательность для антитела nBT062



Сравнение общих определений CDR Кабата и Хотиа и прогнозированных CDR-областей для антитела ВТ062
ВТ062 является иммуноконъюгатом, включающим химерное антитело nBT062 против CD138, присоединенное с помощью линкера, в данном случае SPDB, к цитостатическому производному майтанзиноида DM4. Химическая структура ВТ062 показана на Фиг.1 и 2. Иммуноконъюгаты, включающие антитело nBT062 и эффекторную молекулу майтанзиноида, часто определяются с указанием линкера и эффектора майтанзиноида, например, nBT062-SMCC-DM1 является иммуноконъюгатом, включающим nBT062, SMCC (“нерасщепляемый” линкер, содержащий сложную тиоэфирную связь) и DM1 в качестве эффектора. Иммуноконъюгат, содержащий nBT062 и эффекторную молекулу, может быть также описан как nBT062-линкер-эффектор или просто как nBT062-эффектор (nBT062N, где N означает любой эффектор, рассмотренный в настоящем описании изобретения).
В настоящем описании изобретения рассмотрен иммуноконъюгат без стерического препятствия (UI: иммуноконъюгат без стерического препятствия), включающий генетически созданное антитело против CD138, присоединенное к эффекторной молекуле с помощью расщепляемого линкера (CL); такой иммуноконъюгат, определяемый как UICL, противопоставлен иммуноконъюгату, в котором указанная эффекторная молекула имеет стерическое препятствие и содержит расщепляемый линкер (HICL - иммуноконъюгат со стерическим препятствием и расщепляемым линкером). Иммуноконъюгат UICL эквивалентен иммуноконъюгату HICL, включающему генетически созданное антитело против клетки-мишени и эффекторную молекулу, которая, однако, не имеет стерического препятствия. Примерами двух иммуноконъюгатов HICL/UICL являются ВТ062 и nBT062-SPP-DM1. Иммуноконъюгат без стерического препятствия, включающий нерасщепляемый линкер, (UINCL) эквивалентен иммуноконъюгату, включающему генетически созданное антитело против клетки-мишени, в котором эффекторная молекула не имеет стерического препятствия и включает нерасщепляемый линкер. Для ВТ062 иммуноконъюгат nBT062-SMCC-DM1 является примером такого иммуноконъюгата без стерического препятствия, включающего нерасщепляемый линкер.
Активность иммуноконъюгата, ингибирующая рост опухоли, является относительной единицей измерения. Данная единица измерения определяет активность иммуноконъюгата, ингибирующую рост опухоли, относительно активности наиболее эффективного иммуноконъюгата, активность которого принята равной 100%. Например, если активность наиболее эффективного иммуноконъюгата, скажем, ВТ062, который задерживает рост опухоли (TGD) на 32 дня, принята равной 100%, то активность, например, nBT062-DM1, который задерживает рост опухоли (TGD) на 18 дней, вычисляют следующим образом:
Активность, ингибирующая рост опухоли =
100×(TGDnBT062-DM1/TGDBT062),
в более общем представлении:
Активность, ингибирующая рост опухоли =
100×TGDобразца/TGDэталона).
Приемлемые примеры результатов, приведенных на Фиг.11В
(*) Задержка роста опухоли в днях (TGD) в виде среднего времени в днях для экспериментальной группы до достижения заранее определенного размера (160 мм3) минус среднее время для контрольной группы до достижения указанного заранее определенного размера.
(**) Активность, ингибирующая рост опухоли = 100×TGDобразца/TGDэталона). Активность ВТ062 определена равной 100%.
В примере, приведенном в таблице 2, ВТ062 обладает активностью, ингибирующей рост опухоли, которая выше, чем у иммуноконъюгата без стерического препятствия (nBT062-SPP-DM1) на 60%, и активностью, ингибирующей рост опухоли, которая выше, чем у иммуноконъюгата без стерического препятствия с нерасщепляемым линкером (nBT062-SMCC-DM1) на 44%.
Ранее сообщалось, что расщепляемый линкер в иммуноконъюгате может создавать так называемый эффект неспецифического цитолиза. Голдмахер и др. (публикация патента США 2006/0233814) также указали, что эффект неспецифического цитолиза является особенно выраженным, когда эффекторная молекула подвергается дальнейшей модификации, в частности, алкилированию, после отщепления от агента против клетки-мишени. Голдмахер и др. также показали, что UICL характеризуется лучшей TGD по сравнению с соответствующим иммуноконъюгатом UINCL, что также было объяснено эффектом неспецифического цитолиза (см., например, Фиг.6 в публикации патента США № 2006/0233814).
Однако общая эффективность иммуноконъюгатов HICL/UICL/UINCL, по-видимому, отличается у разных иммуноконъюгатов и/или при воздействии на разные мишени. Например, иммуноконъюгат HICL трастузумаб-SPP-DM4 превосходил по своей способности уменьшать размер опухоли иммуноконъюгат UINCL трастузумаб-SMCC-DM1, в то время как рабочие характеристики иммуноконъюгата UICL трастузумаб-SPP-DM1 по существу были такими же, как у соответствующего иммуноконъюгата HICL (см. публикацию патента США 2008/0171040, выданного Эбертсу и др.), таким образом, полученные результаты зависели от иммуноконъюгата и мишени.
На Фиг.11А показано, что иммуноконъюгат HICL превосходит иммуноконъюгаты UIUCL и UNICL, при этом было установлено, что результаты введения иммуноконъюгата UICL в высокой однократной дозе (250 мкг/кг) фактически не были лучше, чем у UINCL. Значение TGD в днях, которое было получено для иммуноконъюгата UICL при введении в указанном режиме, было ниже аналогичного значения иммуноконъюгата UINCL. Данное наблюдение было более выраженным при увеличении дозы (450 мкг/кг). Как показано на Фиг.11А, иммуноконъюгат HICL превосходил иммуноконъюгат UICL в экспериментах по введению однократной дозы в неожиданной степени. В соответствии с указанными результатами в экспериментах по повторному введению дозы иммуноконъюгат HICL значительно превосходил иммуноконъюгат UICL, причем результаты иммуноконъюгата UICL лишь ненамного превосходили результаты контрольного вещества. Кроме того, иммуноконъюгат UICL превосходил иммуноконъюгат UINCL при введении в более высоких дозах.
Адгезия клеток множественной миеломы к стромальным клеткам, в частности, к стромальным клеткам костного мозга, определяет лекарственную устойчивость, опосредованную адгезией (CAM-DR), которая наблюдается у субъектов, страдающих множественной миеломой. В определенных вариантах осуществления изобретения иммуноконъюгаты по настоящему изобретению могут ослаблять CAM-DR. В частности, в некоторых вариантах осуществления настоящего изобретения указанная адгезия уменьшается при введении иммуноконъюгата в указанные клетки множественной миеломы, например, по меньшей мере примерно на 10%, примерно на 20%, примерно на 30%, примерно на 40%, примерно на 50%, примерно на 60%, примерно на 70%, примерно на 80% или больше. Как показано на Фиг.17Е, иммуноконъюгаты UICL и HICL были особенно способны ингибировать адгезию клеток множественной миеломы к BMSC (стромальные клетки костного мозга) в образцах, в которых обрабатывали только стромальные клетки (а также в образцах, в которых стромальные клетки не обрабатывали), в то время как иммуноконъюгат UINCL не вызывал такого эффекта. Полученные результаты позволяют предположить, что эффект уменьшения адгезии зависит от характера линкера иммуноконъюгата, при этом предпочтительным является расщепляемый линкер, который позволяет легче диссоциировать эффекторной молекуле. То, что клетки множественной миеломы по меньшей мере частично не сцепляются с BMSC, делает их более доступными для других цитотоксических средств, включая те средства, которые обычно не воздействуют, по меньшей мере с полной эффективностью, на клетки множественной миеломы вследствие САМ-DR. Таким образом, введение иммуноконъюгата предпочтительно объединяют с одновременным или последующим введением цитотоксического средства. Интервалы времени между введением иммуноконъюгата и цитотоксического средства могут составлять от 12 часов до 6 дней, включая 12 часов, 24 часа, 2, 3, 4 или 5 дней.
Иммуноконъюгаты по настоящему изоборетению можно вводить любым способом, включая внутривенное, парентеральное, пероральное, внутримышечное, интратекальное введение или введение в виде аэрозоля. Способ доставки зависит от требуемого эффекта. Специалист в данной области может легко определить лучший способ введения для проведения конкретного лечения по настоящему изобретению. Соответствующая доза зависит от способа введения и назначенного лечения и может быть легко определена специалистом в данной области с учетом современных методов лечения.
Фармацевтические композиции, содержащие иммуноконъюгат по настоящему изобретению и/или любое дополнительное цитотоксическое средство в качестве активных ингредиентов, могут быть получены стандартными методами приготовления фармацевтических препаратов. См., например, публикацию Remington's Pharmaceutical Sciences, 17th Ed. (1985, Mack Publishing Co., Easton, Pa.). Активные ингредиенты в эффективных количествах обычно смешивают с фармацевтически приемлемым носителем. Носитель может быть использован в разных видах в зависимости от формы препарата, предназначенного, например, для внутривенного, перорального, парентерального, интратекального, чрескожного введения или для введения в виде аэрозоля.
В случае перорального введения иммуноконъюгат и/или цитотоксическое средство могут быть получены в виде твердых или жидких препаратов, таких как капсулы, пилюли, таблетки, лепешки, расплавы, порошки, суспензии или эмульсии. При получении композиций в виде лекарственной формы для перорального введения могут быть использованы любые обычно применяемые фармацевтические среды, такие как, например, вода, гликоли, масла, спирты, ароматизаторы, консерванты, охлаждающие агенты, суспендирующие агенты и тому подобные, в случае жидких препаратов для перорального введения (таких как, например, суспензии, эликсиры и растворы); или такие носители как крахмалы, сахара, разбавители, гранулирующие агенты, смазывающие вещества, связывающие вещества, дезинтеграторы и тому подобные, в случае твердых препаратов для перорального введения (таких как, например, порошки, капсулы и таблетки). Благодаря простоте введения таблетки и капсулы являются наиболее предпочтительными лекарственными формами для перорального введения, в которых использованы твердые фармацевтические носители. При желании на таблетки может быть нанесено сахарное покрытие или энтеросолюбильное покрытие стандартными методами. Активный агент должен оставаться устойчивым при прохождении через желудочно-кишечный тракт. При необходимости могут быть использованы приемлемые агенты, обеспечивающие устойчивое прохождение, которые могут включать фосфолипиды или производные лецитина, описанные в научной литературе, а также липосомы, микрочастицы (в том числе микросферы и макросферы).
В случае парентерального введения иммунгоконъюгат и/или цитотоксическое средство могут быть растворены в фармацевтическом носителе и введены в виде раствора или суспензии. Примерами приемлемых носителей являются вода, физиологический раствор, физиологический раствор с фосфатным буфером (PBS), растворы декстрозы, растворы фруктозы, этанол или животные, растительные или синтетические масла. Носитель может также содержать другие ингредиенты, например, консерванты, суспендирующие агенты, растворители, буферы и тому подобные. При церебровентрикулярном или интратекальном введении указанные вещества могут быть также растворены в цереброспинальной жидкости.
Дозы, вводимые субъекту, могут быть определены в виде количества на площадь поверхности субъекта (данное положение относится как к человеку, так и к животным, отличным от человека). Субъекту может быть введена доза в количестве, которое предпочтительно равно, не исключая других количеств, от около 5 мг/м2 до около 300 мг/м2, включая примерно 20 мг/м2, примерно 50 мг/м2, примерно 100 мг/м2, примерно 150 мг/м2, примерно 200 мг/м2 и примерно 250 мг/м2. В определенных вариантах осуществления изобретения, в которых иммуноконъюгат вводят в комбинации с цитотоксическим средством, доза иммуноконъюгата может быть ниже. Иммуноконъюгаты вводят один или несколько раз. В случае введения нескольких доз указанные количества можно вводить один раз в день, один раз в неделю, один раз в две недели, один раз в три недели, один раз в четыре недели, один раз в пять недель или один раз в шесть недель. В соответствии с предпочтительным вариантом осуществления изобретения вводят одну высокую дозу или альтернативно более низкие дозы через короткие промежутки времени с последующим введением доз через более продолжительные периоды времени. В препочтительном варианте осуществления изобретения время введения доз определяется для субъекта таким образом, чтобы перед введением второй и/или любой последующей дозы прошло достаточно времени для метаболизации предшествующей дозы, но при этом количество иммуноконъюгата, присутствующего в организме субъекта, по-прежнему позволяло ингибировать, задерживать и/или предотвращать рост опухоли. Типичная схема ”повторного введения однократной дозы” включает введения первоначальной дозы иммуноконъюгата, равной примерно 200 мг/м2, один раз в три недели. Альтернативно после высокой первоначальной дозы два раза в неделю вводят поддерживающую дозу, равную примерно 150 мкг/м2. Однако могут быть использованы другие схемы введения доз. Ход лечения можно легко контролировать при помощи известных методов и анализов. Доза может изменяться в зависимости от профилактического или терапевтического введения, предшествующего лечения, клинической истории субъекта, реакции на воздействие агента против клетки-мишени/иммуноконъюгата и решения лечащего врача.
В одном варианте осуществления изобретения иммуноконъюгат вводят с одним или несколькими дополнительными цитотоксическим средствами, которые оказывают эффективное воздействие при лечении того же заболевания, но при введении без иммуноконъюгата часто характеризуются ограниченной эффективностью с точки зрения CAM-DR; например, иммуноконъюгат, специфичный к CD138, можно вводить в комбинации с дексаметазоном. В частности, дексаметазон вводят нуждающемуся субъекту в эффективном количестве через два часа после введения иммуноконъюгата.
Таким образом, иммуноконъюгат по настоящему изобретению можно также вводить при химиотерапии высокими дозами (предпочтительно с использованием мелфалана, мелфалана/преднизона (МР), винкристина/доксорубицина/дексаметазона (VAD), липосомного доксорубицина/винкристина, дексаметазона (DVd), циклофосфамида, этоподиза/дексаметазона/цитарабина, цисплатина (EDAP)), при трансплантации стволовых клеток (например, аутологической трансплантации стволовых клеток, аллогенной трансплантации стволовых клеток и/или миниаллогенной (немиелоабластической) трансплантации стволовых клеток), при использовании стероидов (например, кортикостероидов, дексаметазона, талидомида/дексаметазона, преднизона, мелфалана/преднизона), при поддерживающей терапии (например, с помощью бисфосфонатов, факторов роста, антибиотиков, внутривенного введения иммуноглобулина, лучевой терапии в низких дозах и/или ортопедического вмешательства), при лечении таломидом (талидомид, Celgene), велкадом (бортезомиб, Millennium) и/или ревлимидом (леналидомид) (Chelgene Corporation) и/или при других видах лечения множественной миеломы, включая лучевую терапиию.
При введении иммуноконъюгата по настоящему изобретению в комбинации с цитотоксическими средствами часто используются вышеуказанные дозы и схемы введения. Однако при совместном введении иммуноконъюгата и цитотоксического средства в некоторых вариантах осуществления изобретения предпочтительны низкие дозы каждого из указанных терапевтических компонентов. В таком случае иммуноконъюгат можно вводить в дозах от около 5 мг/м2 до около 100 мг/м2, включая примерно 20 мг/м2, примерно 50 мг/м2, при этом цитотоксическое средство вводят в дозах, рекомендуемых при отдельном введении.
Экспериментальные данные, полученные в процессе исследований с использованием культур клеток (Фиг.7) и мышей (Фиг.8-11), были подтверждены последующим экспериментам.
Патогенез множественной миеломы включает связывание миеломных клеток при помощи адгезивных молекул на поверхности клеток не только со стромальными клетками костного мозга (BMSC), но также с внеклеточным матриксом (ЕСМ). Указанное связывание запускает и, таким образом, в конечном счете определяет рост клеток множественной миеломы, лекарственную устойчивость и миграцию клеток ММ в среду костного мозга (Munshi et al., 2008). В частности, адгезия клеток множественной миеломы при помощм синдекана-1 (CD138) к ЕСМ, коллагену типа I, вызывает экспрессию металлопротеиназы 1 в матриксе, стимулируюя таким образом резорбцию кости и инвазию опухоли (Hideshima et al., 2007). Взаимодействие между клетками множественной миеломы и микросредой костного мозда активирует плеотропный пролиферативный и антиапоптозный процесс.
Вслед за внедрением клеток множественной миеломы в стромальный компартмент костного мозга адгезия между клетками множественной миеломы и BMSC увеличивает количество многих цитокинов, таких как интерлейкин-6 (IL-6) и инсулиноподобный фактор роста 1 (IGF-1), которые обладают активностью, стимулирующей развитие кровеносных сосудов и рост опухоли (Hideshima et al., 2007). Пути передачи сигналов, инициируемых указанными цитокинами, в конечном счете вызывают устойчивость клеток ММ к общепринятым методами лечения (Anderson et al., 2000; Hideshima et al., 2006).
Эффективность nBT062-SPDB-DM4 и nBT062-SPP-DM1 in vivo против CD138-положительных опухолевых клеток в присутствии костного мозга человека анализировали с использованием мышиной модели, и результаты данного анализа приведены на Фиг.12. На данной фигуре показано, что как HICL, так и UICL эффективно действуют в указанной среде. Вышеуказанные иммуноконъюгаты снижали уровень shulL-6R, который может быть использован в данной моделе в качестве параметра роста клеток ММ.
В соответствии с настоящим изобретением множественную миелому лечили следующим образом, используя ВТ062 в качестве примера. Данный пример никоим образом не ограничивает настоящее изобретение, и специалист в данной области может легко определить другие системы на основе иммуноконъюгата или антитела nBT062, которые входят в объем настоящего изобретения, и другие схемы лечения, которые могут быть использованы для лечения таких заболеваний как множественная миелома.
Благодаря селективной экспрессии CD138 в клетках множественной миеломы субъекта, доступности клеток в кровотоке, специфичности антитела nBT062 и устойчивости ВТ062 в кровотоке, ВТ062 устраняет системную токсичность DM4 и создает возможность для направленной доставки эффекторной молекулы DM4. Иммуноконъюгаты по настоящему изобретению являются средством эффективной доставки эффекторных молекул к сайтам на клетках, где эффекторные молекулы могут высвобождаться из иммуноконъюгатов.
Субъекту, которому вводят одно или несколько цитотоксических средств в дозах и лекарственных формах в соответствии со схемами лечения, установленными для указанных цитотоксических средств, также вводят иммуноконъюгат по настоящему изобретению.
В частности, субъекту вводят соответствующую дозу ВТ062, например, равную 100 мг/м2, по настоящему изобретению через определенные периоды времени, например, первоначально ежедневно и затем один раз в неделю. Через двенадцать часов после введения иммуноконъюгата один раз в неделю субъекту также вводят мелфалан, например, в виде пероральной дозы в соответствии с инструкцией производителя (например, в виде пилюли, продаваемой под торговым знаком АЛКЕРАН).
В соответствии с настоящим изобретением солидные опухоли можно также лечить следующим образом, используя ВТ062 в качестве примера. Данный пример никоим образом не ограничивает настоящее изобретение, и специалист в данной области может легко определить иммуноконъюгаты по настоящему изобретению и другие схемы лечения, которые могут быть использованы для лечения солидных опухолей. Сначала уменьшают размер опухоли, например, при помощи лучевой терапии. Последующее введение ВТ062 и затем дозы цитотоксического средства, например, в виде пилюли АЛКЕРАН, является высокоэффективным способом устранения остаточных раковых клеток. Введение иммуноконъюгата позволяет направленно воздействовать на указанные остаточные клетки и высвобождать эффекторные молекулы на сайте мишени. Иммуноконъюгат преодолевает или уменьшает САМ-DR не только благодаря собственной активности, но и вследствие ингибирования адгезии миеломных клеток к стромальным клеткам, причем указанный иммуноконъюгат преодолевает или уменьшает САМ-DR также для других цитотоксических средств. Высокая эффективность иммуноконъюгата позволяет в предпочтительных вариантах осуществления изобретения применять схему введения однократной дозы.
Настоящее изобретение далее описано со ссылкой на нижеследующие примеры, которые приведены в качестве иллюстрации и не ограничивают объем настоящего изобретения. Использованы стандартные методы, хорошо известные в данной области, или методы, специально описанные ниже.
Материалы и методы
Создание химерного антитела (сВ-В4:nBT062)
В-В4
В описанных экспериментах было использовано ранее исследованное мышиное антитело В-В4 (Wijdenes et al., Br. J. Haematol., 94 (1996), 318).
Клонирование и экспрессия В-В4 и сВ-В4/nBT062
Выполняли стандартные методики рекомбинантных ДНК, подробно описанные в учебниках, например, в J. Sambrook; Molecular Cloning, A Laboratory Manual; 2nd Ed. (1989), Cold Spring Harbor Laboratory Press, USA, или рекомендованные в инструкции производителя в случае использования наборов. Клонирование и модификацию вариабельных областей мыши выполняли с помощью стандартных методов ПЦР. Были использованы праймеры, указанные в соответствующем разделе “Результаты”.
Экспрессия сВ-В4/nBT062
Клетки COS в экспоненциальной фазе роста, культивируемые в среде DMEM, содержащей 10% FCS, 580 мкг/мл L-глутамина, 50 ед/мл пенициллина и 50 мкг/мл стрептомицина, собирали, обрабатывая трипсином, центрифугировали и промывали в PBS. Клетки повторно взвешивали в РBS до конечной концентрации, равной 1×107 клеток/мл. 700 мкл взвеси клеток COS переносили в кювету импульсного генератора Gene Pulser и смешивали с ДНК вектора экспрессии тяжелой цепи и легкой каппа-цепи (по 10 мкм каждого вектора или 13 мкг супервектора). Клетки электропорировали при 1900 В, 25 мкф с помощью импульсного генератора Gene Pulser компании Bio-Rad. Трансформированные клетки культивировали в среде DMEM, содержащей 10% FBS без гамма-глобулина, 580 мкг/мл L-глутамина, 50 ед/мл пенициллина и 50 мкг/мл стрептомицина, в течение 72 часов, после чего собирали супернатанты культур клеток, содержащих антитело.
Метод ELISA с захватом антитела для измерения уровней экспрессии сВ-В4/nBT062
96-луночные планшеты покрывали 100 мкл аликвотами 0,4 мкг/мл антитела козы против IgG человека, разведенного в PBS (4°С, в течение ночи). Планшеты трижды промывали 200 мкл/лунку промывочного буфера (PBS+0,1% твина-20). Лунки блокировали 0,2% BSA, 0,02% твина-20 в PBS и добавляли 200 мкл супернатантов культур клеток, содержащих секретированное антитело (инкубация при 37°С в течение одного часа). Лунки шесть раз промывали промывочным буфером и обнаруживали связанное антитело, используя конъюгат антитела козы против легкой каппа-цепи человека с пероксидазой.
Очистка сВ-В4/nBT062 от супернатантов культур клеток
Антитело сВ-В4 очищали от супернатантов трансформированных клеток COS 7, используя набор ImmunoPure Plus, содержащий белок А (Pierce, Rockdord, IL), в соответствии с рекомендациями производителя.
Конкурентно-связывающий анализ антитела сВ-В4
Анализ активности связывания антител В-В4 и сВ-В4 с CD138 выполняли, используя набор Diaclone, содержащий sCD138 (Besancon, France), в соответствии с рекомендациями производителя, принимая во внимание изменения, описанные в разделе “Результаты”.
Получение РНК и синтез кДНК
Клетки гибридомы В-В4 выращивали и обрабатывали с помощью набора Qiagen Midi (Hilden, Germany) для выделения РНК в соответствии с инструкциями производителя. Примерно 5 мкг РНК клеток В-В4 подвергали обратной транскрипции для получения кДНК В-В4, используя набор для синтеза 1-й цепи Amersham Biosciences (Piscataway, NJ) в соответствии с инструкциями производителя.
Клонирование кДНК иммуноглобулина В-В4
кДНК тяжелой цепи иммуноглобулина (IgH) амплифицировали методом ПЦР, используя праймер MHV7 для IgH (5'-ATGGGCATCAAGATGGAGTCACAGACCCAGG-3') [SEQ ID NO:3] и праймер MHCG1 для константной области IgG1 (5'-CAGTGGATAGACAGATGGGGG-3') [SEQ ID NO:4]. Легкую цепь иммуноглобулина (IgL) амплифицировали аналогичным образом, используя три разных праймера для Igκ, а именно MKV2 (5'-ATGGAGACAGACACACTCCTGCTATGGGTG-3') [SEQ ID NO:5], MKV4 (5'-ATGAGGGCCCCTGCTCAGTTTTTTGGCTTCTTG-3') [SEQ ID NO:6] и MKV9 (5'-ATGGTATCCACACCTCAGTTCCTTG-3') [SEQ ID NO:7], в комбинации с праймером МКС (5'-ACTGGATGGTGGGAAGATGG-3') [SEQ ID NO:8]. Все продукты амплификации лигировали в вектор pCR2.1-TOPO, используя набор для клонирования TOPO-TA (Invitrogen, Carlsbad, CA), в соответствии с инструкциями производителя.
Бактерии ТОР10 E. coli (Invitrogen), трансформированные лигированными конструкциями вектора pCR2.1, отбирали на агаровых пластинках с LB-ампициллин-Xgal. Небольшие культуры инокулировали единичными белыми колониями, выращивали в течение ночи и выделяли плазмиды, используя набор QIAprep Spin Miniprep в соответствии с инструкциями производителя.
Определение последовательности кДНК
Плазмиды секвенировали, используя готовый реакционный набор для циклического секвенирования BigDye Termination v3.0 (ABI, Foster City, CA). Каждую отобранную плазмиду секвенировали в обоих направлениях, используя праймеры 1210 и 1233, циклизованные в устройстве для ПЦР GeneAmp9600. Электрофоретический анализ последовательности выполняли в капиллярном секвенаторе ABI.
Полный цикл ПЦР с обратной транскрипцией, клонирование и анализ последовательности ДНК повторяли для получения трех полностью независимых наборов информации о последовательности для каждой цепи иммуноглобулина.
Последовательность ДНК вариабельной области каппа-цепи (Vκ) В-В4
1-ю цепь синтезировали, выполняя три независимые реакции. Продукты ПЦР, полученные при использовании праймеров МКС и MKV2 (приведенные выше последовательности), лигировали в векторы pCR2.1-TOPO в соответствии с инструкциями производителя. Клоны, полученные в результате выполнения независимых серий ПЦР с обратной транскрипцией, секвенировали в обоих направлениях. Последовательность продукта, полученная с помощью праймера MKV2, была в высшей степени подобна стерильным транскриптам каппа-цепи, полученным из миеломной клетки-партнера, таким как МОРС-21, SP2 и Ag8 (Carroll et al., Mol. Immunol., 25 (1988), 991; Cabilly et al., Gene, 40 (1985); 157), и поэтому не принимались во внимание.
Продукты ПЦР, полученные при использовании праймера МКС с праймерами MKV4 и MKV9, были подобны друг другу и отличались только неоднозначными положениями в праймере для лидерной последовательности.
Последовательность ДНК вариабельной области тяжелой цепи (VH) В-В4
1-ю цепь синтезировали, выполняя три независимые реакции, затем продукты ПЦР клонировали и секвенировали из каждого продукта 1-й цепи. Из каждой 1-й цепи секвенировали пять клонов.
Создание векторов экспрессии химерного антитела сВ-В4
Создание векторов экспрессии химерного антитела предполагает добавление приемлемой лидерной последовательности к VH и Vκ, которой предшествует сайт рестрикции BamHI и последовательность Козака. Консенсусная последовательность Козака имеет важное значение для эффективной трансляции последовательности вариабельной области. Данная последовательность определяет правильный кодон AUG, из которого рибосома может начать трансляцию, при этом единственным наиболее значимым основанием является аденин (или менее предпочтительно гуанин) в положении -3, вверху от начала AUG. Лидерную последовательность выбирают как наиболее подобную последовательность в базе данных Кабата (Kabat et al., NIH National Technical Information Service, 1991). Указанные добавления кодируют в верхних (For) праймерах (имеющих последовательность 5'-AGAGAAGCTTGCCGCCACCATGATTGCCTCTGCTCAGTTCCTTGGTCTCC-3' [SEQ ID NO:9]; сайт рестрикции подчеркнут; последовательность Козака выделена жирным шрифтом). Кроме того, создание векторов экспрессии химерного антитела предполагает введение 5'-концевого фрагмента константной области гамма-цепи 1 человека до природного сайта рестрикции Apal, смежного с 3'-концом J-области антитела В-В4, и добавление сайта донора сплайсированного фрагмента и сайта HindIII для легкой цепи. Последовательность донора сплайсированного фрагмента имеет важное значение для правильного присоединения в остове вариабельной области к соответствующей константной области, сплайсируя таким образом интрон V:C. Интрон каппа-цепи + СК кодированы экспрессирующей конструкцией, расположенной внизу от последовательности Vκ В-В4. Аналогичным образом СН гамма-цепи 4 кодирована экспрессирующей конструкцией, расположенной внизу от последовательности VH В-В4.
Гены VH и Vκ В-В4 сначала тщательно анализировали для идентификации любых нежелательных сайтов донора сплайсированного фрагмента, сайтов акцептора сплайсированного фрагмента, последовательностей Козака и наличия любых дополнительных сайтов рестрикции субклонирования, которые позднее могут мешать субклонированию и/или экспрессии функционального полного антитела. Нежелательный сайт HindIII, обнаруженный в последовательности Vκ, был удален путем сайтнаправленного мутагенеза при помощи ПЦР без изменения аминокислотной последовательности. Для выполнения указанных реакций были использованы олигонуклеотидные праймеры ВТ03 (5'-CAACAGTATAGTAAGCTCCCTCGGACGTTCGGTGG-3') [SEQ ID NO:10] и ВТ04 (5'-CCACCGAACGTCCGAGGGAGCTTACTATACTGTTA-3') [SEQ ID NO:11], и мутагенез выполняли в соответствии с инструкциями к набору для мутагенеза Quickсhange компании Stratagene (La Jolla, CA).
Праймеры для химеризации каппа-цепи
Не вызывающую сомнений лидерную последовательность Vκ В-В4, независимо от последовательности праймера для ПЦР, подвергали сравнительному анализу с мышиными лидерными последовательностями в базе данных Кабата. Ближайшей совместимой последовательностью для лидерной последовательности VH В-В4 была последовательность VK-10 ARS-A (Sanz et al., PNAS, 84 (1987), 1085). Указанная лидерная последовательность была точно вырезана в соответствии с прогнозом, сделанным с помощью алгоритма SignaIP (Nielsen et al., Protein Eng, 10 (1997); 1). Праймеры СВВ4Kfor (см. выше) и g2258 (5'-CGCGGGATCCACTCACGTTTGATTTCCAGCTTGGTGCCTCC-3' [SEQ ID NO:12]; сайт рестрикции подчеркнут) были созданы для получения продукта ПЦР, содержащего указанную полную лидерную последовательность, Vκ-область В-В4 и концевые сайты рестрикции HindIII и BamHI, с целью клонирования в экспрессирующем векторе pKN100. Верхний праймер СВВ4К вводит сайт рестрикции HindIII, сайт инициации трансляции Козака и лидерную последовательность VK-10 ARS-A. Нижний праймер g2258 вводит сайт донора сплайсированного фрагмента и сайт рестрикции BamHI. Полученный фрагмент клонировали в сайты рестрикции HindIII/BamHI вектора pKN100.
Праймеры для химеризации тяжелой цепи
Не вызывающую сомнений лидерную последовательность VH В-В4, независимо от последовательности праймера для ПЦР, подвергали сравнительному анализу с мышиными лидерными последовательностями в базе данных Кабата. Ближайшей совместимой последовательностью для лидерной последовательности VK В-В4 была последовательность VH17-1A (Sun et al., PNAS, 84 (1987), 214). Указанная лидерная последовательность была точно вырезана в соответствии с прогнозом, сделанным с помощью алгоритма SignaIP. Праймеры cBB4Hfor (см. выше) и g22949 (5'-CGATGGGCCCTTGGTGGAGGCTGAGGAGACGGTGACTGAGGTTСС-3' [SEQ ID NO:13]; сайт рестрикции подчеркнут) были созданы для получения продукта ПЦР, содержащего лидерную последовательность VH17-1A, VH-область В-В4 и концевые сайты рестрикции HindIII и AlaI, с целью клонирования в экспрессирующем векторе pG4D200. Верхний праймер cBBHfor вводит сайт рестрикции HindIII, сайт инициации трансляции Козака и лидерную последовательность VH17-1A. Нижний праймер g22949 вводит 5'-конец С-области гамма-цепи 4 и природный сайт рестрикции AlaI. Полученный фрагмент клонировали в сайты рестрикции HindIII/ApaI вектора pG4D200, в результате чего был получен вектор pG4D200cBB4.
Получение антитела сВВ4
Одну пробирку с клетками COS 7 оттаивали и клетки выращивали в среде DMEM, содержащей 10% фетальной сыворотки клона I с антибиотиками. Через одну неделю клетки (0,7 мл в количестве 107 клеток/мл) электропорировали вектором pG4D200cBB4 с pKN100cBB4 (10 мкг ДНК каждого) или без ДНК. Клетки культивировали в 8 мл питательной среды в течение 4 дней. Электропорацию повторяли семь раз.
Обнаружение химерного антитела
Сэндвич-метод ELISA использовали для измерения концентраций антител в супернатантах клеток COS 7. Временно трансформированные клетки COS 7 секретировали примерно 6956 нг/мл антитела (данные не показаны).
Связывающая активность антитела сВ-В4
Cвязывающую активность антитела сВ-В4 в супернатантах культур клеток COS 7 анализировали при помощи твердофазного сэндвич-метода ELISA с использованием набора Diaclone, содержащего sCD138. Моноклональным антителом, специфичным к sCD138, сенсибилизировали лунки титровального микропланшета. Во время первой инкубации sCD138 и биотинилированное антитело В-В4 (био-В-В4) инкубировали вместе, выполняя серию разведений немеченого испытуемого антитела (В-В4 или сВ-В4).
Концентрации био-В-В4 при выполнении данного анализа были уменьшены для конкуренции с немеченым антителом в низких концентрациях (концентрация сВ-В4 в супернатантах культур клеток COS 7 в противном случае была слишком низкой для достижения достаточной конкуренции). Результаты данного анализа показывают, что оба антитела обладают одинаковой специфичностью к CD138 (данные не показаны).
Очистка антитела сВ-В4
Химерное антитело В-В4 очищали от супернатантов клеток COS 7, используя набор ImmunoPure Plus, содержащий белок А (Pierce), в соответствии с рекомендациями производителя (данные не показаны).
Определение К D : сравнение nBT062/BB4
Очистка растворимого антигена CD138
Растворимый антиген CD138 из супернатанта культуры клеток U-266 очищали методом FPLC, используя 1 мл NHS-активируемую НР колонку HiTrap, связанную с В-В4. В колонку вводили супернатант культуры клеток в физиологическом растворе с фосфатным буфером при рН 7,4 и антиген CD138 элюировали 50 мМ триэтиламина с рН 11 в 2 мл фракциях. Элюированный антиген CD138 сразу же нейтрализовали 375 мкл 1 М раствора трис-буфера с HCl, рН 3, для предотвращения структурных и/или функциональных разрушений.
Биотинилирование антигена CD138
Антиген CD138 метили сульфо-NHS-LC (Pierce). NHS-активируемые биотины эффективно взаимодействуют с первичными аминогруппами, такими как остатки лизина, в буферах с рН 7-9 с образованием устойчивых амидных связей.
Для биотинилирования антигена CD138 50 мкл CD138 обессоливали, используя центрифужные колонки для обессоливания белка (Pierce). Биотинилирующий реагент (сульфо-NHS-LC-биотин с EZ-линкером, Pierce) растворяли в ожлаждаемой льдом деионизированной Н2О до конечной концентрации 0,5 мг/мл. Раствор биотинилирующего реагента и улавливающего реагента смешивали с 12-кратным молярным избытком биотинилирующего реагента по сравнению с улавливающим реагентом (50 пмоль антигена CD138 на 600 пмоль биотинилирующего реагента) и инкубировали в течение 1 часа при комнатной температуре, осторожно встряхивая пробирку. Несвязанный биотинилирующий реагент удаляли в колонках для обессоливания белка.
Иммобилизация bCD138
Сенсорный чип (сенсорный чип SA, Biacore AB), использованный в анализе BIACORE, предназначен для связывания биотинилированных молекул с целью выполнения анализа взаимодействия в системах BIACORE. Поверхность состоит из матрицы из карбоксиметилированного декстрана, предварительно иммобилизованной стрептавидином, которая готова для высокоаффинного улавливания биотинилированных лигандов. Антиген bCD138 иммобилизовали на сенсорном чипе SA со скоростью потока 10 мкл/мин путем ручного введения. Поверхность чипа обрабатывали, производя три последовательных одноминутных впрыскивания 1 М раствора NaCl в 50 мМ NaOH. Затем в течение 1 минуты вводили биотинилированный антиген CD138.
Определение К D разных антител с использованием программы BIACORE
В программном обеспечении BIACORE C использованы заранее определенные маски, так называемые ”мастера”, предназначенные для разных экспериментов, в которых могут быть изменены только определенные установки. Так как программное обеспечение BIACORE C было первоначально разработано для измерения концентраций, в нем отсутствует мастер, служащий для выполнения измерений сродства. Однако при соответствующих установках мастер для измерения ”неспецифического связывания” может быть использован для измерения констант сродства и следовательно для определения КD. С помощью данного мастера было произведено измерение двух проточных кювет при установке фазы диссоциации на 90 сек путем выполнения ”регенерации 1” с помощью разделяющего буфера BIACORE. “Регенерацию 2”, которая эквивалента действительной регенерации, выполняли, используя 10 мМ гидрохлорида глицина, рН 2,5. После выполнения данной стадии лиганд CD138 снова находился в компетентном состоянии связывания. В течение всей процедуры в качестве разделяющего и разбавляющего буфера использовали HBS-EP. Для определения связывания разных антител (~150 кДа) с CD138 анализировали ассоциацию и диссоциацию при разных концентрациях (100, 50, 25, 12,5, 6,25 и 3,13 нМ). Константы равновесия диссоциации определяли, вычисляя константы скорости kа и kd. Значения КD веществ, определяемых при анализе, вычисляли с учетом коэффициента kd и ka при помощи программного обеспечения BIAevaluation. Результаты приведены в таблице 4.
Сравнительный анализ значений КD антител nBT062 и В-В4. Для средних значений КD указаны стандартные отклонения
1,4
1,5
1,7
1,6
1,9
1,9
2,7
2,6
Рассмотрение результатов
Средние значения КD для каждого антитела были вычислены по результатам трех независимых экспериментов. Полученные данные показывают, что при выполнении всех измерений антитело nBT062 характеризуется несколько меньшими значениями КD по сравнению с В-В4 (средние значения КD были соответственно равны 1,4 и 1,6 нМ).
Получение иммуноконъюгатов
nBT062-DM1 и huC242-DM1
Тиолсодержащий майтанзиноид DM1 синтезировали из продукта ферментации микробов ансамитоцина Р-3 способом, описанными Чари (Chari et al., Cancer Res. 1 (1992), 127). Получение гуманизированного антитела С242 (huC242) было описано ранее (Roguska et al., PNAS, 91 (1994), 969). Конъюгаты антитела с лекарственным средством были получены ранее описанным способом (Liu еt al., PNAS, 93 (1996), 8618). С одной молекулой антитела в среднем было связано 3,5 молекулы DM1.
nBT062-DM4
ВТ062 является конъюгатом антитела с лекарственным средством, состоящим из цитотоксического майтанзиноида DM4, связанного дисульфидными связями при помощи линкера с химерным моноклональным антителом nBT062. Майтанзиноиды являются антимитотическими агентами, ингибирующими полимеризацию тубулина и сборку микротрубочек (Remillard et al., Science 189 (1977), 1002). Химическая структура и схематическое изображение ВТ062 (nBT062-DM4) показаны на Фиг.1 и 2.
Синтез DM4
DM4 получают из хорошо известного производного майтанзинола (Kupchan et al., J. Med. Chem., 21 (1978), 31). Майтанзинол получают путем восстановительного расщепления сложноэфирной части продукта ферментации микробов ансамитоцина Р3 с помощью триметоксиалюмогидрида лития (см. Фиг.3).
DM4 синтезируют путем ацилирования майтанзинола N-метил-N-(4-метилдитиопентаноил)-L-аланином (боковая цепь DM4) в присутствии дициклогексилкарбодиимида (DCC) и хлорида цинка с образованием дисульфид-содержащего майтанзиноида DM4-SMe. DM4-SMe восстанавливают дитиотреитолом (DTT), получая при этом требуемый тиол-содержащий майтанзиноид DM4 (см. Фиг.4 для ознакомления с блок-схемой процесса получения DM4).
Иммуноконъюгат ВТ062
Способ получения nBT062-DM4 показан на Фиг.5. Антитело nBT062 модифицируют N-сукцинимидил-4-(2-пиридилдитио)бутиратом (линкер SPDB) для введения дитиопиридильных групп. DM4 смешивают с модифицированным антителом в концентрации, превышающей эквиваленты дитиопиридильных групп. Конъюгат ВТ062 получают путем реакции дисульфидного обмена между тиоловой группой DM4 и дитиопиридильными группами, введенными в антитело с помощью линкера. Хроматографическая очистка и диафильтрация позволяют удалить низкомолекулярные реагенты (DM4) и продукты реакции (тиопиридин), а также агрегаты конъюгированного антитела с образованием нерасфасованного лекарственного средства.
Анализ методом FACS и анализы цитотоксичности с использованием водорастворимой соли тетразолия (WST)
Анализ методом FACS
Клетки ОРМ-2 представляют собой линии клеток плазмаклеточного лейкоза, экспрессирующие антиген CD138 на высоком уровне. Клетки ОРМ-2 инкубировали с nBT062, nBT062-SPDB-DM4, nBT062-SPP-DM1 или nBT062-SMCC-DM1 в разных концентрациях (указанных на Фиг.6). Клетки промывали и CD138-связанное антитело или конъюгаты обнаруживали, используя вторичное антитело, меченное флуоресцином, при помощи анализа методом клеточного сортинга с возбуждением флуоресценции (FACS). Средние значения флуоресценции, измеренные в указанных экспериментах, представлены в виде графика зависимости от концентрации антитела.
Анализ жизнеспособности клеток
CD138+ клетки MOLP-8 высевали на плоскодонные планшеты в количестве 3000 клеток/лунку. Контрольные CD138- клетки BJAB высевали в количестве 1000 клеток/лунку. Клетки обрабатывали nBT062-SPDB-DM4, nBT062-SPP-DM1 или nBT062-SMCC-DM1 в разных концентрациях (указанных на Фиг.7) в течение пяти дней. Реагент WST (водорастворимая соль тетразолия, ROCHE), используемый для измерения жизнеспособности клеток, добавляли в соответствии с инструкциями производителя (ROCHE). Указанный реагент инкубировали в течение 7,5 часа на клетках MOLP-8 и в течение 2 часов на клетках BJAB. Фракцию выживших клеток вычисляли на основании оптической плотности, которую измеряли в спектрометре для прочтения микропланшетов стандартными методами.
Рассмотрение результатов
Связывание nBT062-SPDB-DM4, nBT062-SPP-DM1, nBT062-SMCC-DM1 или nBT062 анализировали методом FACS. CD138+ клетки ОРМ-2, используемые в качестве клеток-мишеней, инкубировали с nBT062 или иммуноконъюгатами и связанные с клетками молекулы обнаруживали с помощью вторичного антитела, меченного флуоресцеином. На Фиг.6 средние значения флуоресценции в качестве меры количества связанного с клетками антитела представлены в виде графика зависимости от разных концентраций антитела или конъюгата. Полученные данные показывают, что nBT062-SPDB-DM4, nBT062-SPP-DM1 и nBT062-SMCC-DM1 имеют очень схожие характеристики связывания. Кроме того, полученные результаты позволяют предположить, что на характеристики связывания неконъюгированного антитела не влияют конъюгированные токсины.
При выполнении анализов жизнеспособности клеток анализировали цитотоксическую активность антитела против CD138+ клеток-мишеней MOLP-8 и против контрольных CD138- клеток В-лимфобластомы BJAB. Обе линии клеток высевали на плоскодонные планшеты и инкубировали с иммуноконъюгатами в возрастающих концентрациях. Неконъюгированное антитело было использовано в качестве контрольного антитела. Цитотоксическую активность анализировали в течение пяти дней после добавления иммуноконъюгатов, используя реагент WST для измерения жизнеспособности клеток. На Фиг.7А-7С фракция выживших клеток по сравнению с контрольными клетками, которые обрабатывали контрольным наполнителем, представлена в виде графика зависимости от возрастающих концентраций иммуноконъюгатов. Полученные данные показывают, что цитотоксическая активность nBT062-SPDB-DM4, nBT062-SPP-DM1 и nBT062-SMCC-DM1 против клеток MOLP-8 является очень схожей. Как ожидалось, контрольные CD138- клетки BJAB не были уничтожены иммуноконъюгатами, из чего следует, что все иммуноконъюгаты действуют путем клеточно-специфического связывания с CD138. При выполнении экспериментов по конкурентному связыванию клетки MOLP-8 предварительно инкубировали с молярным избытком неконъюгированного антитела nBT062. Предварительная инкубация по существу блокировала цитотоксичность nBT062-SPDB-DM4, что стало еще одним свидетельством того, что иммуноконъюгаты уничтожают клетки путем специфического связывания с CD138 на поверхности клетки (Фиг.7D).
Эксперименты с использованием мышей, несущих ксенотрансплантаты
Для оценки важности направленного воздействия на CD138 для противоопухолевой активности конъюгатов антитела с майтанзиноидом при использовании человеческого химерного варианта антитела В-В4, nBT062, выполняли эксперименты с использованием мышей, несущих ксенотрансплантаты. Были получены два варианта конъюгатов антитела nBT062 с майтанзиноидом, которые отличались химической стойкостью дисульфидных связей (nBT062-SPP-DM1 и nBT062-SPDB-DM4). Противоопухолевую активность указанных конъюгатов антитела с лекарственным средством сравнивали с активностью конъюгата В-В4-SPP-DM1 (включающего мышиное родительское антитело), а также неконъюгированного свободного майтанзиноида (DM4), нативного немодифицированного антитела nBT062 и конъюгата IgG1 с майтанзиноидом ненаправленного действия (нерелевантный конъюгат). Конъюгаты оценивали с использованием CD138-положительной модели ксенотрансплантата (MOLP-8) множественной миеломы человека у мышей с тяжелым комбинированным иммунодефицитом (SCID).
У указанных мышей вызывали образование подкожных опухолей (самки мышей SCID CB.17) путем инокуляции взвеси клеток MOLP-8. Лечение в виде однократной внутривенной инъекции ударной дозы проводили, когда объем опухоли достигал в среднем 113 мм3. Изменение объма опухоли и массы тела контролировали два раза в неделю. Эксперименты выполняли в течение 68 дней после инокуляции опухолевых клеток.
Эксперименты А с использованием мышей, несущих ксенотрансплантаты
Мыши
Самки мышей SCID CB.17 в возрасте пяти недель были приобретены в компании Сharles River Laboratories.
Линии опухолевых клеток человека
MOLP-8, линия клеток множественной миеломы человека, была получена из АТСС. Клетки MOLP-8, экспрессирующие антиген CD138 на поверхности клеток и образующие ксенотрансплантаты опухолей у мышей SCID, сохраняли в среде RPMI-1640, содержащей 4 мМ L-глутамина (Biowhittaker, Walkersville, MD), 10% фетальной телячьей сыворотки (Hyclone, Logan, Utah) и 1% стрептомицина/пенициллина, при 37°С во влажной атмосфере, содержащей 5% СО2.
Часть I
Рост опухолей у мышей
Каждой мыши подкожно инокулировали 1×107 клеток MOLP-8 в область под правым плечом. Общий объем клеток составлял 0,2 мл/мышь, при этом отношение бессывороточной среды к матригелю (BD Bioscience, Bedford, MA) было равно 1/1 (об./об.). До начала лечения ежедневно контролировали образование ксенотрансплантатов опухолей. Объем опухолей достигал почти 113 мм3 примерно через 11 дней после инокуляции опухолевых клеток. Образование опухолей у мышей SCID CB.17 было равно 100%.
Через одиннадцать дней после инокуляции опухолевых клеток отбирали 42 мыши с учетом объемов опухолей и массы тела. Объем опухоли находился в пределах от 68,2 до 135,9 мм3. Сорок две мыши произвольно распределяли в семь групп (А-G) по шесть животных в каждой группе с учетом объема опухоли.
Каждой из шести мышей в группе А вводили 200 мкл PBS в качестве контрольного наполнителя. Каждой мыши в группе В вводили 13,8 мг/кг голого антитела nBT062. Указанная доза эквивалента количеству антитела nBT062 в 250 мкг/кг связанного майтанзиноида. Отношение молекулярных масс майтанзиноидов к антителу nBT062 в молекуле конъюгата равно примерно 1/55. Каждой мыши в группе С вводили 250 мкг/ко DM4. Каждой мыши в группе D вводили 250 мкг/кг huC242-DM4. Мышам в группах Е, F и G вводили соответственно 250 мкг/кг nBT062-SPDB-DM4, B-B4-SPP-DM1 и nBT062-SPP-DM1.
Все агенты вводили внутривенно в виде одной инъекции ударной дозы через боковую хвостовую вену с помощью 1 мл шприца, оснащенного иглой 27 калибра длиной 1,25 см (1/2 дюйма). Перед введением исходные растворы антитела nBT062, конъюгатов nBT062-SPDB-DM4 и nBT062-SPP-DM1 разбавляли стерильным PBS до концентраций 2 мг/мл, 28,1 мкг/мл и 28,1 мкг/мл таким образом, чтобы объем, вводимый каждой мыши, был равен 120-220 мкл.
Часть II
Во второй серии экспериментов клетки MOLP-8 (1,5×107 клеток/мышь), взвешенные в смеси бессывороточной среды и матригеля в соотношении 50:50, инъецировали подкожно в количестве 100 мкл в область под правым плечом. На 11-й день объемы опухолей достигли примерно 80 мм3, при этом среднее значение у контрольных животных было равно примерно 750 мм3 на 25-й день после инокуляции клеток. Время удвоения опухоли было равно 4,58 дня. Каждой мыши в контрольной группе (n=6) вводили (внутривенно) 0,2 мл стерильного PBS в боковую хвостовую вену в виде инъекции ударной дозы. Все дозы определяли на основании конъюгированного майтанзиноида. Животным в девяти группах (n=6) делали одну внутривенную инъекцию nBТ062-SMCC-DM1, nBT062-SPDB-DM4 или nBT062-SPP-DM1 в дозах, равных 450, 250 и 100 мкг/кг. Животным в дополнительной группе (n=6) вводили 250 мкг/кг nBT062-SMCC-DM1 в виде повторных доз (один раз в неделю в течение пяти недель). Мышей произвольно распределяли в одиннадцать групп (n=6) с учетом объема опухоли в соответствии с программой LabCat. Объемы опухолей находились в пределах от 40,0 до 152,5 мм3. Дозы для мышей определяли на основании массы тела.
Размер опухоли измеряли два раза в неделю в трех направлениях, используя систему LabCat (Tumor Measurement and Tracking, Innovative Programming Associated, Inc., Princeton, NJ). Объем опухоли в мм3 вычисляли с помощью метода, описанного в публикации Tomayko et al., Cancer Chemother. Pharmacol. 24 (1989), 148:
Объем = Длина×ширина×высота×½
Log10 лизиса клеток вычисляли по формуле, описанной в публикации Bissery et al., Cancer Res., 51 (1991), 4845:
Log10 лизиса клеток = (Т-С)/Td×3,32
где (Т-С) или задержка роста опухоли означает среднее время в днях, необходимое для достижения опухолями заранее определенного размера (600 мм3) в экспериментальной группе (Т) и контрольной группе (С). Td означает время удвоения опухоли, определяемое на основании среднего объема опухоли у контрольных мышей, и 3,32 означает число удвоений клеток на Log роста опухоли.
Результаты
Рост опухолей у отдельных мышей показан на Фиг.8 и 9. Среднее значение (± стандартное отклонение) роста опухолей для каждой группы показано на Фиг.10.
При сравнении с ростом опухолей у животных, которым вводили PBS, введение антитела nBT062, неконъюгированного свободного DM4 или нерелевантного конъюгата ненаправленного действия huC242-DM4 не вызывало значительного ингибирования роста опухолей.
Все три конъюгата против CD138, nBT062-SPDB-DM4, B-B4-SPP-DM1 и nBT062-SPP-DM1, вводимые в дозе 250 мкг/кг, вызывали значительную задержку роста опухоли. С учетом средних объемов опухолей, измеренных в экспериментальных группах, конъюгат с DM4 nBT062-SPDB-DM4 был наиболее активным, в то время как конъюгат nBT062-SPP-DM1 характеризовался несколько более высокой активностью по сравнению с мышиным конъюгатом В-В4-SPP-DM1 (Фиг.10). Результаты, полученные у отдельных мышей, кроме того, показывают, что противоопухолевая активность конъюгата В-В4-SPP-DM1 являются более гетерогенной и поэтому менее прогнозируемой по сравнению с конъюгатом nBT062-SPP-DM1. С точки зрения гомогенности противоопухолевой активности другой конъюгат, в котором использовано антитело nBT062 в качестве антитела против клетки-мишени, nBT062-SPDB-DM4 действовал подобно конъюгату nBT062-SPP-DM1.
Ни в одной экспериментальной группе не было отмечено уменьшение массы тела, из чего следует, что мыши хорошо переносили лечение.
Рассмотрение результатов
Результаты анализа трех конъюгатов против CD138, вводимых экспериментальным животным, показывают важное значение направленной доставки противоопухолевой активности. В то время, как конъюгаты майтанзиноида с человеческим химерным антителом nBT062 и мышиным антителом В-В4 характеризовались значительной активностью при измерении с помощью Log лизиса клеток, при лечении неконъюгированным DM4, немодифицированным нативным антителом huBT062 или контрольным конъюгатом ненаправленного действия (huC242-DM4) не было отмечено значительного воздействия на рост опухоли.
Иммуноконъюгат, полученный из человеческого химерного антитела, nBT062-SPP-DM1 характеризовался несколько более высокой противоопухолевой активностью по сравнению с конъюгатом, полученным из мышиного антитела В-В4-SPP-DM1. Кроме того, введение nBT062-SPP-DM1 и nBT062-SPDB-DM4 вызвало более гомогенные реакции у отдельных мышей по сравнению с введением В-В4-SPP-DM1. То, что для В-В4-SPP-DM1 фактически были получены несколько лучшие результаты, чем для nBT062-SPP-DM1 (данные не показаны) при измерении среднего объема опухолей (± стандартное отклонение) ксенотрансплантатов множественной миеломы человека MOLP-8 у мышей SCID CB.17 через некоторое время (дней) после инокуляции, объяснялось высокой изменчивостью связывания В-В4-SPP-DM1. Рассмотренная особенность иммуноконъюгатов с использованием nBT062 в качестве антитела против клетки-мишени кажется особенно полезной для терапевтического использования указанных конъюгатов.
И наконец, самым сильнодействующим из конъюгатов майтанзиноида после однократного внутривенного введения в моделях ксенотрансплантатов MOLP-8 у мышей SCID был конъюгат nBT062-SPDB-DM4.
Неспецифический цитолиз (анализ жинеспособности клеток)
CD138+ клетки ОРМ2 и CD138- клетки Namalwa высевали на круглодонные планшеты в отдельные лунки или в виде сокультуры. Клетки обрабатывали nBT062-SPDB-DM4 в концентрациях от 1×10-8 до 1×10-9 М. Фракцию жизнеспособных клеток обнаруживали с помощью реагента WST (водорастворимая соль тетразолия, ROCHE) в соответствии с инструкцией производителя (ROCHE). Фракцию выживших клеток вычисляли на основании оптической плотности, которую измеряли в спектрометре для прочтения микропланшетов стандартными методами.
Рассмотрение результатов
Неспецифический цитолиз клеток, не являющихся мишенями, в непосредственной близости (находящихся в круглодонных лунках) от клеток множественной миеломы под воздействием nBT062-SPDB-DM4 анализировали при выполнении исследования in vitro, в соответствии с которых CD138-положительные клетки ОРМ-2 культивировали в виде сокультуры вместе с CD138-отрицательными клетками Namawla (Фиг.13). Как правило, в то время как nBT062-SPDB-DM4 эффективно уничтожал CD138-положительные клетки, указанный конъюгат не воздействовал на CD138-отрицательные клетки. Однако в сокультуре, находящейся в круглодонных лунках, конъюгат nBT062-SPDB-DM4 уничтожил также антигенотрицательные клетки, находящиеся в непосредственной близости от антигенположительных клеток (эффект, который часто определяется как неспецифический цитолиз). Ковтун и др. (2006) отметили, что неспецифический цитолиз, опосредуемый конъюгатами майтанзиноида, происходит только в непосредственной близости от антигенположительных клеток. В публикации Kovtun et al. (2006), которая полностью включена в настоящее описание изобретения в качестве ссылки, также отмечено важное значение линкера иммуноконъюгата. In vivo неспецифический цитолоиз может способствовать 1) уничтожению опухолевых клеток, которые гетерогенно экспрессируют CD138, 2) разрушению микросреды опухоли в результате лизиса стромальных клеток опухоли и 3) предотвращению отбора CD138-отрицательных клеток, устойчивых к nBT062-SPDB-DM4.
Эффект неспецифического цитолиза имеет особенно важное значение, если активность иммуноконъюгата нарушена антигеном-мишенью, который гетерогенно экспрессирован в опухолях. В данном случае определенная клетка опухоли экспрессирует антиген в количестве, если такая экспрессия вообще имеет место, которое не позволяет эффективно направленно воздействовать и уничтожать указанную клетку соответствующим иммуноконъюгатом. Противоопухолевая активность nBT062-SPDB-DM4 в отношении CD138-отрицательных клеток в сокультуре с CD138-положительными клетками показала, что присутствие клеток-мишеней влияет в определенных условиях на цитотоксическую активность nBT062-SPDB-DM4 в отношении клеток, не являющихся мишенями.
Эксперименты В с использованием мышей, несущих ксенотрансплантаты
В данной серии экспериментов восьмидесяти пяти мышам подкожно инокулировали клетки MOLP-8 (1,5×107 клеток/мышь) в правое плечо. Опухоль образовалась у 100% мышей. Шестьдесят шесть мышей SCID, имеющих объемные опухоли MOLP-8 со средним объемом опухоли около 80 мм3, произвольно распределяли в одиннадцать экспериментальных групп (n=6). Мышам вводили однократную дозу одного из трех конъюгатов (nBT062-SMCC-DM1, nBT062-SPDB-DM4 или nBT062-SPP-DM1). Дополнительной группе вводили пять еженедельных доз nBT062-SMCC-DM1 и контрольной группе вводили однократную дозу PBS. Средние объемы опухолей показаны на Фиг.11А. Определяли реакцию на дозу каждого конъюгата. У мышей, которым вводили PBS, опухоль достигла среднего объема, равного 750 мм3, на 25-й день. Время удвоения опухоли, определенное методом наилучшего приближения линейной регрессионной кривой на логарифмическом линейном графике роста контрольной опухоли, было равно 4,58 дня. Животные, которым вводили nBT062-SPDB-DM4 в дозе 450 мкг/кг, характеризовались наибольшим Log лизиса клеток (LCK=2,89), несколько более низкий показатель имели животные, которым еженедельно вводили nBT062-SMCC-DM1 в дозе 250 мкг/кг (LCK=2,1; см. таблицу 5). Сравнение кривых среднего роста опухолей для экспериментальных групп при повторных измерениях методом ANOVА с использованием множественного t-критерия сравнения Даннетта свидетельствовало о значительном расхождении между контрольной группой, которой вводили PBS, и группами, которым вводили 450 мкг/кг nBT062-SPDB-DM4 (p<0,01), 250 мкг/кг nBT062-SPDB-DM4 (р<0,05) и пять еженедельных доз, равных 250 мкг/кг nBT062-SMCC-DM1 (р<0,05). Ни в одной из экспериментальных групп не произошла частичная или полная регрессия опухоли за исключением одного животного, которому вводили 450 мкг/кг nBT062-SPDB-DM4, у которого наблюдалась частичная регрессия опухоли до 85-го дня после инокуляции.
Значения Log лизиса клеток (LCK) в качестве меры противоопухолевой активности разных конъюгатов nBT062-DMx при использовании разных схем введения. Обратитесь к разделу ”Вещества и методы” для ознакомления с информацией по вычислению значений LCK
Эффективность in vivo nBT062-SPDВ-DM4 и nBT062-SPP-DM1 в среде костного мозга
Получение мышей SCID с имплантами костей плода человека
Длинные кости плода человека (крошка костей плода человека) имплантировали в верхнюю часть тела мышей SCID СВ17 (SCID-hu) в соответствии с ранее описанным способом (Urashima et al., 1997), получив таким образом мышиную модель для введения клеток ММ человека в клетки ВМ человека.
Схема лечения (мыши SCID-hu/INA-6)
Через 4 недели после имплантации костей мышам SCID-hu непосредственно в полость костного мозга человека вводили 2,5×106 клеток INA-6 в конечном объеме, равном 100 мкл, в культуральной среде для клеток RPMI-1640 в соответствии с приведенным выше описанием. Повышение уровня растворимого рецептора IL-6 человека (shulL-6R), высвобождаемого клетками INA-6, использовали в качестве параметра роста клеток ММ и развития болезни.
Измеряемое количество shulL-6R в сыворотке мышей было обнаружено примерно через 4 недели после введения клеток INA-6, после чего мышам вводили 0,176 мг конъюгата или контрольного наполнителя в виде инъекции в хвостовую вену один раз в неделю в течение 7 недель. После каждого введения у мышей брали пробы крови и измеряли уровни shulL-6R при помощи твердофазного иммуноферментного анализа (ELISA, R&D Systems, Minneapolis, MN). Результаты приведены на Фиг.12.
Рассмотрение результатов
Интерлейкин 6 (IL-6) является фактором роста и выживания для клеток множественной миеломы. Клетки INA-6 являются IL-6-зависимой линией миеломных клеток человека, которая требует для пролиферации также наличия стромальных клеток костного мозга (BMSC). Линии клеток INA-6 продуцируют растворимый рецептор IL-6 (shulL-6R). Увеличение уровня shulL-6R можно испольозовать в качестве параметра роста клеток ММ и развития болезни.
Таким образом, мыши SCID-hu/INA-6 представляют собой модель клеток множественной миеломы, растущих в нормальной среде костного мозга. Опухолевые клетки данной модели, которые прямо взаимодействуют с костным мозгом человека, близко напоминают ситуацию у субъектов, у которых рост опухолевых клеток также стимулируется присутствием стромальных клеток. По мере того, как клетки INA-6 высвобождают растворимый рецептор интерлейкин-6 человека (shulL-6R), концентрации указанного белка в сыворотке могут быть использованы в качестве меры количества опухолевых клеток у указанных мышей. Действие in vivo nBT062-SPDB-DM4 и nBT062-SPP-DM1 испытывали в указанной среде.
Внутривенное введение мышам SCID-hu/INA-6 один раз в неделю nBT062-SPDB-DM4 или nBT062-SPP-DM1 в течение семи недель вызвало эффективную регрессию опухоли, определяемую по уменьшению в сыворотке уровней shulL-6R по сравнению с контрольной группой, что свидетельствует о хорошей эффективности конъюгатов даже в среде костного мозга человека, отражающей подобную ситуацию у субъектов (Фиг.12).
Анализ эффективности nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 in vitro и у экспериментальных животных in vivo
Вещества и методы
Культура клеток
Чувствительные к доксорубицину (ММ.1S) и устойчивые (ММ.1R) линии клеток ММ человека были любезно предоставлены д-ром Стивеном Розеном (Northwestern University, Chicago, IL). Линии клеток ММ человека RPMI8226 и U266 были получены из Американской коллекции типовых культур (Manassas, VA). Устойчивые к доксорубицину (Dox) (RPMI-Dox40) и устойчивые к мелфалану (LR5) клетки были любезно предоставлены д-ром Вильямом Далтоном (Lee Moffitt Cancer Center, Tampa, FL). Клетки плазмаклеточного лейкоза ОРМ1 и ОРМ2 были любезно предоставлены д-ром Эдвардом Томпсоном (University of Texas Medical Branch, Galveston).
Все линии клеток ММ и стромальных клеток костного мозга (ВМ) культивировали в модифицированной по способу Дульбекко среде Игла (DMEM) (Sigma), содержащей 10% фетальной телячьей сыворотки, 2 мМ L-глутамина (Life Technologies), 100 ед/мл пенициллина и 100 Aг/мл стрептомицина (Life Technologies). Пробы крови, взятые у здоровых добровольцев, обрабатывали градиентами фиколл-пака для получения мононуклеарных клеток периферической крови (РВМС). Клетки ММ и ВМ субъектов были выделены из образцов ВМ после получения письменного согласия в соответствии с Хельсинской декларацией и одобрения Консультативного совета Института рака Дана-Фарбера (Boston, MA). Мононуклеарные клетки ВМ отделяли путем осаждения в градиенте плотности фиколл-пака и плазмациты очищали (>95% CD138+) путем положительного отбора с помощью активируемых магнитным полем микрогранул против CD138 для разделения клеток (Miltenyi Biotec Auburn, CA). Опухолевые клетки очищали от костного мозга субъектов, страдающих множественной миеломой, используя систему отрицательного отбора RosetteSep (StemCell Technologies, Vancouver, BC, Canada), ранее описанным способом (Hideshima, 2001). В образцы костного мозга вводили смесь антител RosetteSep. CD138-отрицательные клетки перекрестно связывали с эритроцитами (розеткообразующие клетки) при помощи реагентов RosetteSep, инкубировали в течение 20 минут при комнатной температуре и разделяли путем центрифугирования в градиенте плотности фиколла.
Анализ ингибирования роста и пролиферации клеток
Ингибирующее действие nBT062-SMCC-DM1, nBT062-SPDB-DM4, nBT062-SPP-DM1 и дексаметазона на рост линий клеток ММ, PBMC и BMSC оценивали при помощи анализов на основе МТТ, измеряя метаболизацию красителя 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетранатрийбромида (МТТ; Chemicon International, Temecula, CA) ранее описанным способом (Hideshima, 2003).
Воздействие nBT062-SMCC-DM1, nBT062-SPDB-DM4, nBT062-SPP-DM1 на рост клеток ММ в костном мозге
Для оценки стимулирующего рост воздействия клеток костного мозга на чувствительность клеток ММ к иммуноконъюгатам клетки ММ (2×104 клеток/лунку) в течение 48 часов культивировали вместе со стромальными клетками костного мозга (BMSC, 1×104 клеток/лунку) на 96-луночных планшетах (Costar, Cambridge, MA) в присутствии или отсутствии лекарственного средства. Синтез ДНК измеряли с учетом поглощения [3H]-тимидина (Perkin-Elmer, Boston, MA). [3H]-Тимидин (0,5 мкCi/лунку) добавляли в последние 8 часов эксперимента. Все эксперименты повторяли четыре раза.
Анализ клеточного цикла
Клетки ММ (1×106 клеток) инкубировали в течение 48 часов в присутствии или отсутствии иммуноконъюгатов, промывали физиологическим раствором с фосфатным буфером (PBS), сообщали проницаемость в результате 30-минутного воздействия 70% этанола при -20°С и инкубировали с иодидом пропидия (PI) (50 мкг/мл) в 0,5 мл PBS, содержащего 20 ед/мл РНКазы А (Roche Diagnostics), в течение 30 минут при комнатной температуре. Содержание ДНК анализировали с помощью проточного цитометра.
Иммунофлуоресценция
Клетки, выращенные на покровных стеклах, фиксировали в холодном абсолютном ацетоне в течение 10 минут, промывали в PBS и блокировали в течение 60 минут 5% FBS в PBS. Затем покровные стекла инкубировали с антителом против CD138 (sc12765, Santa Cruz Biuotechnology, Santa Cruz, CA) в течение 24 часов при 4°С. Клетки снова промывали PBS, инкубировали с меченным флуоресцином антителом козы против IgG мыши в течение 1 часа при 4°С и анализировали с помощью флуоресцентного микроскопа Nikon E800 ранее описанным способом (Ikeda, 2005; Kiziltepe, 2007).
Модель ксенотрансплантата ММ человека, положительно реагирующая на автофлуоресцирующий зеленый флуоресцентный белок (GFP) и мышиная модель ксенотрансплантата ММ человека
Клетки ОРМ1 трансфецировали зеленым флуоресцентным белком (ОРМ1DFP), используя вектор на основе лентивируса, ранее описанным способом (Zufferey, 1998). Мыши SCID CD17 (в возрасте 48-54 дней) были приобретены в компании Сharles River Laboratories (Wilmington, MA). Все исследования с использованием животных выполняли в соответствии с протоколами, одобренными Комитетом по этике обращения с животными Института рака Дана-Фарбера. Мышам подкожно инокулировали в правый бок 5×106 клеток ММ ОРМ1GFP в 100 мкл среды RPMI-1640. Когда опухоли можно было пальпировать, была сформирована экспериментальная группа мышей, которым вводили 176 мкг/мышь конъюгата с учетом молекулярной массы один раз в неделю в течение 4 недель в виде инъекции в боковую хвостовую вену, и 5 мышей были включены в контрольную группу, которой вводили только наполнитель. Наибольшие перпендикулярные диаметры опухоли измеряли штангенциркулем через день для определения объема опухоли по нижеследующей формуле, представляющей трехмерный объем эллипса: 4/3×(ширина/2)2×(длина/2). Животных умерщвляли, когда опухоль достигала 2 см или если мыши находились в агональном состоянии. Выживание определяли с первого дня лечения до смерти. Рост опухоли измеряли штангенциркулем с первого дня лечения до дня смерти, который был 10-м днем для контрольной группы и 21-м днем для группы, которой вводили ВТ062-SPDB-DM4. Мышам сбривали шерсть с кожи в месте опухоли и исследовали методом флуоресцентной визуализации, используя систему Illumatool Bright Light System LT-9900 (Lightools Research, Encinitas, CA). Изображения были получены с помощью цифровой видеокамеры 700 Сanon IXY. Изображения анализа опухолей ex vivo были получены с помощью микроскопа LEICA DM IL, соединенного с камерой LEICA DFC300 FX, при 40u/0,60 (Leica, Heidelberg, Germany).
Обнаружение апоптических клеток
Клетки ММ (1×106) промывали РBS и инкубировали в присутствии или отсутствии иммуноконъюгатов. Апоптические клетки окрашивали РЕ-конъюгированным антителом Аро 2.7 (7А6, Beckman Coulter, Inc.). Клетки анализировали методом проточной цитометрии в проточном цитометре Epics (Beckman Coulter, Inc.), используя программное обеспечение RXP Cytomics.
Анализ методом вестерн-блоттинга
Клетки ММ культивировали в присутствии или отсутствии nBT062-SMCC-DM1, nBT062-SPDB-DM1 или BT062-SPP-DM1, собирали, промывали и лизировали, используя буфер для радиоиммунопреципитационного анализа (RIPA), содержащий 2 мМ Na3VO4, 5 мМ NaF, 1 мМ фенилметилсульфонилфторида, 5 мг/мл полного ингибитора протеазы, ранее описанным способом (Yasui, 2005; Hayashi, 2002). Цельноклеточные лизаты (20 мкг/полосу) разделяли электрофорезом в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE), переносили на чистые нитроцеллюлозные мембраны (Bio-Rad Laboratories, Hercules, CA) и анализировали методом иммуноблоттинга с использованием антител против поли-ADP аденозиндифосфат-рибозополимераза (PARP), каспазы-8, каспазы-3, каспазы-9, АКТ и фосфо(Ser 473) Akt (Cell Sigaling), а также антител против тубулина и против CD138 (Santa Cruz Biotechnology).
Анализ межклеточной адгезии
Стромальные клетки костного мозга в количестве 1×104 клеток пипетировали в каждую лунку 96-луночного планшета и инкубировали в течение 12 часов в присутствии или отсутствии иммуноконъюгатов при 37°С. Во время инкубации к стромальным клеткам костного мозга добавляли клетки ММ в присутствии или отсутствии лекарственных средств. Клетки ММ трижды промывали РBS и повторно взвешивали в бессывороточной среде RPMI с плотностью 2×105 клеток в 100 мкл в присутствии или отсутствии лекарственных средств. Исследование каждой группы образцов повторяли три или четыре раза. После совместного культивирования в течение 2 часов при 37°С несцепленные, плохо сцепленные клетки и среду удаляли, переворачивая планшет. Затем лунки трижды промывали РBS. Оставшиеся сцепленные клетки культивировали в среде RPMI, содержавшей 10% FBS, в присутствии [3H]-тимидина (0,5 мкСi/лунку, Perkin Elmer, Boston, MA, USA) еще в течение 8 часов для измерения синтеза ДНК.
Статистический анализ
Статистическую значимость различий, наблюдаемых в культуре, обработанной иммуноконъюгатом (IC), по сравнению с контрольной культурой определяли с использованием множественных t-критериев сравнения Данна. Минимальный уровень значимости был равен значению Р менее 0,5. При выполнении экспериментов in vivo объемы опухолей сравнивали при помощи одномерного анализа с использованием множественных t-критериев сравнения Данна. Выживание клеток определяли при помощи кривых Каплана-Майера и логарифмического анализа.
Результаты
Экспрессия CD138 в линиях клеток ММ
Уровни экспрессии CD138 в линиях клеток множественной миеломы анализировали методом вестерн-блоттинга с использованием цельноклеточных лизатов клеток MM1S, OPM1, OPM2, RPMI8226, DOX40, MM1R, LR5 и U266 (Фиг.14А).
Как показано на Фиг.14А, клетки MM1S и LR5 характеризовались слабой экспрессией CD138, и клетки DОХ40 не экспрессировали CD138. Другие линии клеток характеризовались высокими уровнями экспрессии CD138. Было установлено, что антиген CD138 экспрессирован в 7 из 8 (87,5%) линий клеток множественной миеломы.
На Фиг.14В показан анализ методом иммунофлуоресцентного окрашивания с использованием антител, специфичных к CD138. Выполняли микроскопический анализ клеток DOX40 (верхний блок) и клеток ОРМ1 (нижний блок). Экспрессия CD138 показана слева, и экспрессия нуклеиновых кислот показана справа. На Фиг.14В показано, что в клетках DOX40 почти отсутствует обнаруживаемая экспрессия антигена CD138. В отличие от этого клетки ОРМ1 характеризовались высокой иммунореактивностью CD138.
Иммуноконъюгаты nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 характеризуются селективной цитотоксичностью в отношении линий CD138-положительных клеток.
Эффективность конъюгатов антитела против CD138 с майтанзиноидом также определяли при помощи анализов жизнеспособности клеток. Иммуноконъюгаты nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 исследовали в отношении цитотоксической активности против CD138-положительных клеток (ОРМ1, RPMI8226), клеток, слабо экспрессирующих CD138 (MM1S), и CD138-отрицательных клеток (DOX40) при помощи анализа на основе бромида 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия (МТТ). На Фиг.15А показаны клетки ОРМ1 (■), RPMI8226 (♦), DOX40 (□) и MM1S (∆), подвергнутые соответственно воздействию nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1. Выживание клеток определяли при помощи анализов на основе МТТ. Жизнеспособность клеток после инкубации в течение указанных периодов времени (40, 80, 120 часов) представлена в % от жизнеспособности необработанных контрольных клеток. Обработка клеток иммуноконъюгатами nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 в концентрациях от 3 до 354 нг/мл вызывала ингибирование роста CD138-положительных клеток. Данный эффект имаел место в зависимости от времени и дозы и был наиболее выраженным после инкубации в течение 120 часов в двух линиях клеток, экспрессирующих CD138 на высоком уровне. В аналогичных условиях было установлено почти полное отсутствие цитотоксичности в отношении CD138-отрицательных клеток DOX40 (Фиг.15А). Важно отметить, что все три иммуноконъюгата проявляли цитотоксичность в отношении выделенных у субъектов отобранных CD138-отрицательных клеток ММ при использовании в концентрации 111-442 нг/мл после инкубации в течение 48 часов (Фиг.15В). На Фиг.15С показаны клетки PBMC, выделенные у 3 здоровых субъектов, жизнеспособность которых определяли после культивирования с nBT062-SPDB-DM4 в течение 72 часов. Жизнеспособность клеток ОРМ1, обработанных в аналогичных условиях, приведена в качестве контрольного значения (закрашенные квадраты). Как показано на Фиг.15С, иммуноконъюгаты не оказывали цитотоксического действия в клетках PBMC (мононуклеарные клетки периферической крови), выделенных у 3 здоровых добровольцев (Фиг.15С). Полученные результаты показывают, что nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 селективно уничтожают CD138-положительные клетки ММ (все данные, приведенные на данной фигуре, представляют собой средние значения, полученные в результате выполнения трех одинаковых экспериментов. Стандартные отклонения показаны планками погрешностей).
Иммуноконъюгаты nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 индуцируют остановку клеточного цикла в G2/M-фазе в клетках ОРМ1
Поскольку майтанзиноид подавляет полимеризацию микротрубочек, то ранее было показано, что DM1 и DM4 индуцируют остановку клеточного цикла опухолевых клеток в G2/M-фазе (Erickson, 2006). Поэтому после обработки иммуноконъюгатами nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 исследовали профиль клеточного цикла клеток ОРМ1. Клетки инкубировали с иммуноконъюгатами в течение 0-72 часов, метили иодидом пропидия (PI) и анализировали методом проточной цитометрии. На Фиг.16А показаны клетки ОРМ1, обработанные иммуноконъюгатами в течение 0, 12 или 24 часов, и представлен анализ профилей клеточного цикла путем окрашивания иодидом пропидия. Как показано на Фиг.16А, указанные соединения оказывали значительное воздействие на долю клеток в G2/M-фазе по сравнению с необработанными клеткамии. Обработка клеток ОРМ1 иммуноконъюгатом nBT062-SPDB-DM4 вызывала более быструю и более сильную реакцию по сравнению с клетками, обработанными двумя другими лекарственными средствамии.
nBT062-SPDB-DM4 индуцирует апоптоз клеток ОРМ1
Затем определяли способность иммуноконъюгата nBT062-SPDB-DM4 вызывать апоптоз клеток-мишеней. На Фиг.16В показаны клетки ОРМ1, которые культивировали в присутствии или отсутствии иммуноконъюгатов в течение 24, 48 или 72 часов. Процентное количество апоптических клеток определяли путем окрашивания антителом Аро 2.7 и выполнения проточного цитометрического анализа. Как показано на Фиг.16В, окрашивание клеток антителом Аро 2.7 свидетельствовало об индукции апоптоза клеток, обработанных иммуноконъюгатами.
На Фиг.16С показаны клетки ОРМ1, которые культивировали в присутствии 885 мкг/мл nBT062-SPDB-DM4 в течение указанных периодов времени (левый блок) или с иммуноконъюгатом в разных концентрациях (средний блок). На данной фигуре FL означает полосы, соответствующие непроцессированным формам каспаз и PARР; CL означает полосы, соответствующие расщепляемым продуктам. Клетки ОРМ1 предварительно инкубировали с zVAD-fmk (50 мкмоль/л) в течение 60 минут и затем обрабатывали иммуноконъюгатом nBT062-SPDB-DM4 в указанных дозах в течение 24 часов. Все клеточные лизаты анализировали методом иммуноблоттинга с использованием каспазы-3, -8, -9, PARP и антител против тубулина. Как показано на Фиг.16С, обработка клеток ОРМ1 иммуноконъюгатом nBT062-SPDB-DM4 вызывала расщепление какспазы-8, -9, -3 и PARP в зависимости от дозы и времени воздействия (левый и средний блоки). Ингибитор панкаспазы zVAD-fmk блокировал вызываемое иммуноконъюгатом nBT062-SPDB-DM4 расщепление каспазы-3, -8, -9 и PARP в клетках ОРМ1 (Фиг.16С, правый блок). Полученные результаты показывают, что nBT062-SPDB-DM4 активирует каспазы и вызывает апоптоз клеток-мишеней.
Иммуноконъюгаты nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 ингибируют защитное действие BMSC
У субъектов, страдающих множественной миеломой, микросреда костного мозга индуцирует рост, выживание и лекарственную устойчивость клеток ММ в результате действия по меньшей мере двух разных механизмов: адгезия клеток ММ к фибронектину сообщает лекарственную устойчивость, опосредуемую межклеточной адгезией (CAM-DR); и цитокины, такие как интерлейкин-6 (IL-6) и инсулиноподобный фактор роста 1 (IGF-1) в среде костного мозга индуцируют важные сигнальные пути, которые в конечном счете опосредуют устойчивость клеток ММ к стандартным лекарственным средствам. Цитотоксичность иммуноконъюгатов в отношении клеток ММ в сокультуре с BMSC анализировали в присутствии IL-6 или стромальных клеток костного мозга (BMSC).
Клетки ОРМ1, показанные на Фиг.17А-17С, культивировали в течение 48 часов с контрольной средой (черные столбцы) или с иммуноконъюгатом nBT062-SPDB-DM4 в возрастающих концентрациях: 55 нг/мл (темно-серые столбцы; *), 111 нг/мл (серые столбцы; **), 221 нг/мл (светло-серые столбцы; ***), 442 нг/мл (очень светло-серые столбцы; ****), 885 нг/мл (белые столбцы, *****). Клетки, показанные на Фиг.17D, обрабатывали контрольной средой (черные столбцы) в течение 72 часов или дексаметазоном в возрастающих концентрациях: 250 нМ (серые столбцы; +), 500 нМ (светло-серые столбцы; ++), 100 нМ (белые столбцы; +++). IL-6 присутствовал в некоторых культурах в концентрациях 1 или 10 нг/мл (Фиг.17А). IGF-1 использовали в концентрациях 10 или 50 нг/мл (Фиг.17В). Ни один из указанных цитокинов не вызывал устойчивости клеток к иммуноконъюгатам.
Для анализа влияния микросреды костного мозга на рост и устойчивость клеток ОРМ1 к иммуноконъюгатам клетки культивировали в присутствии или отсутствии BMSC в соответствии с приведенным выше описанием.
Сокультивирование клеток ОРМ1 в присутствии или отсутствии BMSC показано в блоках (С) и (D) Фиг.17. Во всех экспериментах синтез ДНК определяли путем измерения включения [3H]-тимидина в течение последних 8 часов культивирования. Адгезия клеток ОРМ1 к BMSC вызывала повышенное поглощение [3H]-тимидина. Важно отметить, что на токсичность иммуноконъюгатов не влияло присутствие BMSC (Фиг.17С). В отличие от этого дексаметазон, который был использован в качестве контрольного вещества, не мог преодолеть защитное действия, вызываемое BMSC (Фиг.17D).
Иммуноконъюгаты nBT062-SPDB-DM4 и nBT062-SPP-DM1 ингибируют адгезию клеток ММ1S к BMSC
Анализировали способность иммуноконъюгатов ингибировать адгезию клеток множественной миеломы к BMSC. Клетки MM1S, которые экспрессируют CD138 только на среднем уровне и демонстрируют лишь слабую чувствительность к ВТ062 (Фиг.14А и Фиг.15А), культивировали в присутствии или отсутствии иммуноконъюгатов nBT062-SMCC-DM1, nBT062-SPDB-DM4 или nBT062-SPP-M1 в течение 2 часов (885 нг/мл). После указанной обработки клетки MM1S сокультивировали с BMSC в течение еще 2 часов. В некоторых случаях стромальные клетки костного мозга (BMSC) сначала обрабатывали иммуноконъюгатами в течение 12 часов (885 нг/мл) и затем сокультивировали (обработка стромальных клеток). Клетки трижды промывали PBS и измеряли адгезию клеток по поглощению [3H]-тимидина.
Стромальные клетки костного мозга, показанные на Фиг.17Е, культивировали в течение 24 часов на 96-луночных плоскодонных планшетах в присутствии или отсутствии иммуноконъюгатов. BMSC трижды промывали PBS. Клетки MM1S, которые инкубировали с иммуноконъюгатами в течение 2 часов, подвергали воздействию BMSC. Синтез ДНК измеряли по поглощению [3H]-тимидина.
Как показано на Фиг.17Е, иммуноконъюгаты nBT062-SPDB-DM4 и nBT062-SPP-DM1 ингибировали адгезию клеток множественной миеломы к BMSC по сравнению с образцами, в которых обрабатывали только стромальные клетки (соответственно 3,6-кратное и 2,5-кратное увеличение). Иммуноконъюгат nBT062-SMCC-DM1 почти не воздействовал на межклеточную адгезию. Полученные результаты позволяют предположить, что иммуноконъюгаты nBT062-SPDB-DM4 и nBT062-SPP-DM1 могут мешать адгезии клеток ММ к BMSC и что указанные иммуноконъюгаты способны преодолевать лекарственную устойчивость, опосредуемую межклеточной адгезией (CAM-DR).
Иммуноконъюгат nBT062-SPDB-DM4 ингибирует рост опухоли в модели ксенострансплантата ММ человека у мышей SCID
Активность иммуноконъюгатов nBT062-SPDB-DM4 и nBT062-SPP-DM1 in vivo определяли в модели GFP-положительного ксенотрансплоантата ММ человека у мышей SCID.
На Фиг.18А показан анализ экспрессии GFP клетками ОРМ1GFP. Как показано на данной фигуре, может быть создан сильно флуоресцирующий клон клеток ММ ОРМ1 (ОРМ1GFP), который используют для исследования противоопухолевой активности иммуноконъюгатов в указанных клетках экспериментальных животных. На Фиг.18В 5 мышам/группе инъецировали 5×106 клеток ОРМ1GFP. Мышам подкожно инокулировали 5×106 клеток ОРМ1GFP в 100 мкл среды RPMI-1640. После образования опухолей животным начинали вводить nBT062-SPDB-DM4 (квадраты), nBT062-SPP-DM1 (треугольники) или контрольный буфер. Размеры опухолей определяли путем измерения перпендикулярных диаметров с помощью штангенциркуля. Планки погрешностей показывают стандартные отклонения. У всех мышей образовались измеряемые опухоли через 14 дней после инъекции опухолевых клеток, после чего мышей произвольно распределяли в группы, которым один раз в неделю вводили nBT062-SPDB-DM4, nBT062-SPP-DM1 или контрольный наполнитель (PBS). Для вычисления объема опухоли через день с помощью штангенциркуля измеряли перпендикулярные диаметры. Введение мышам, имеющим опухоли, иммуноконъюгата nBT062-SPDB-DM4 (176 мкг/мышь на основании молекулярной массы конъюгата, один раз в неделю в течение 4 недель) существенно ингибировало рост опухоли ММ по сравнению с контрольными животными, которым вводили наполнитель PBS (множественный t-критерий сравнения Данна; контрольный наполнитель по сравнению с nBT062-SPDB-DM4; P<0,01, Фиг.16В). Конъюгат nBT062-SPP-DM1 был менее эффективен, чем nBT062-SPDB-DM4 (множественный t-критерий сравнения Данна; nBT062-SPP-DM1 по сравнению с nBT062-SPDB-DM4; Р<0,05, Фиг.5В). Всех контрольных мышей пришлось умертвить на 19-й день после начала лечения из-за больших размеров опухолей. При построении кривых Каплана-Майера и выполнении логарифмического анализа среднее значение OS было равно 13,6 дня (95% доверительный интервал [CI], 10-19 дней) в контрольной группе по сравнению с 26 днями (95% CI, 23-42 дня) в группах, которым вводили nBT062-SPDB-DM4 (Фиг.5С). Как показано на Фиг.18С, иммуноконъюгат nBT062-SPDB-DM4 значительно увеличивал выживание (Р<0,0023, пунктирная линия, n=5) по сравнению с контрольной группой, которой вводили только наполнитель (сплошная линия; нормальный физиологический раствор, n=5). Мышей умерщвляли и у мышей, которым вводили nBT062-SPDB-DM4, и у контрольных мышей, которым вводили буфер, иссекали опухоли для выполнения анализа TUNEL. Анализ ex vivo опухолей, удаленных у мышей, несущих клетки ОРМ1GFP, показал значительно более высокий апоптоз клеток у животных, которым вводили ВТ062, по сравнению с контрольными мышами (Фиг.18D). Таким образом, иммуноконъюгат nBT062-SPDB-DM4 индуцировал апоптоз in vivo. Ни одно из введенных соединений не повлияло на массу тела в данном исследовании.
Рассмотрение результатов
Была продемонстрирована селективная противоопухолевая активность иммуноконъюгатов nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 против CD138-экспрессирующих клеток ММ in vitro и у экспериментальных животных in vivo. При помощи анализа методом иммуноблоттинга и иммунофлуоресцентного анализа было установлено, что большинство анализированных линий клеток ММ экспрессирует CD138. Однако клетки DOX40 не экспрессировали белок CD138 и клетки MM1S и LR5 характеризовались слабой экспрессией указанного белка. В остальных пяти линиях клеток наблюдалась экспрессия CD138 на высоком уровне. Иммуноконъюгаты nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 проявляли значительную цитотоксичность в отношении линий клеток ММ, при этом иммуноконъюгат nBT062-SPDB-DM4 является наиболее сильнодействующим соединением из указанных трех агентов. Клетки ОРМ1 и RPMI8226, экспрессирующие CD138 на высоком уровне, были более чувствительны к иммуноконъюгатам, чем клетки MM1S, слабо экспрессирующие CD138, или CD138-отрицательные клетки DOX40. Важно отметить, что указанные агенты также проявляли цитотоксичность в отношении опухолевых клеток, выделенных у субъектов, страдающих множественной миеломой. При этом указанные иммуноконъюгаты не проявляли цитотоксичности в отношении мононуклеарных клеток периферической крови или костного мозга, взятых у здоровых добровольцев. Полученные результаты позволяют предположить, что иммуноконъюгаты обладают антиген-селективной активностью против опухолевых клеток ММ. Можно продемонстрировать, что nBT062-SMCC-DM1, nBT062-SPDB-DM4 и nBT062-SPP-DM1 ингибируют пролиферацию клеток ММ путем остановки клеточного цикла в G2/M-фазе, вызывая апоптоз клетки. Расщепление каспазы-3, -8, -9 и каспазы-3 внизу от PARP-мишени можно обнаружить в клетках ОРМ1, обработанных иммуноконъюгатами. Кроме того, количество антигенположительных клеток, окрашенных антителом АРО 2.7, увеличилось после инкубации с указанными лекарственными средствами в течение двадцати четырех часов.
Ранее сообщалось, что IL-6 запускает пролиферацию клеток множественной миеломы в результате активации сигнальных путей PI3-K/Akt, MEK/ERK и JAK2/STAT3. В научной литературе отмечено, что IGF-1 также стимулирует пролиферацию и выживание клеток множественной миеломы, используя те же пути. IL-6 защищает клетки от апоптоза, вызываемого дексаметазоном, индуцируя передачу сигнала PI3-K/Akt. Была исследована способность экзогенных IL-6 и IGF-1 ингибировать индуцируемую иммуноконъюгатами цитотоксичность в клетках множественной миеломы. Хотя в клетках, обработанных IL-6 или IGF-1, была отмечена повышенная пролиферация, указанные цитокины не были способны ингибировать апоптоз клеток ОРМ1, вызванный иммуноконъюгатом nBT062-SPDB-DM4, из чего следует, что агенты по настоящему изобретению могут преодолевать защитное действие указанных цитокинов. Важно отметить, что иммуноконъюгаты ингибируют рост и адгезию клеток MM1S к BMSC, что подтверждает способность иммуноконъюгатов преодолевать лекарственную устойчивость, опосредуемую межклеточной адгезией (CAM-DR). Иммуноконъюгат nBT062-SPDB-DM4 вызывал значительную задержку роста ксенотрансплантатов ММ, не влияя при этом на массу тела мышей.
Все испытанные конъюгаты продемонстрировали высокую цитотоксическую активность против линий клеток ММ и против первичных клеток ММ, выделенных у субъектов, в то время как мононуклеарные клетки периферической крови, полученные у здоровых добровольцев, не были восприимчимы к воздействию указанных конъюгатов.
Иммуноконъюгаты, специфичные к CD138, вызывали остановку клеточного цикла в G2/M-фазе и индуцировали апоптоз клеток-мишений, обусловленный расщеплением каспазы-8, -9 и -3 внизу от PARP-мишени. Важно отметитть, что интерлейкин-6-, инсулиноподобный фактор роста 1 или присутствие стромальных клеток костного мозга не защищали клетки ММ от опосредуемой иммуноконъюгатами цитотоксичности.
Конъюгат nBT062-SРDB-DM4 существенно ингибировал рост опухоли ММ (р<0,01) и продлевал жизнь мышей.
Следует отметить, что способы и композиции по настоящему изобретению могут быть использованы в разных вариантах осуществления изобретения, причем в настоящем описании изобретения рассмотрены лишь некоторые из них. Специалисту в данной области должно быть понятно, что существуют другие варианты осуществления изобретения, которые входят в объем настоящего изобретения. Таким образом, описанные варианты осуществления изобретения являются иллюстративными и не ограничивают объем настоящего изобретения.
Библиография







| название | год | авторы | номер документа |
|---|---|---|---|
| АГЕНТЫ ПРОТИВ КЛЕТКИ-МИШЕНИ, НАЦЕЛЕННЫЕ НА CD138, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2537265C2 |
| ИММУНОКОНЪЮГАТЫ, НАПРАВЛЕННЫЕ НА CD138, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2547939C2 |
| ПРИМЕНЕНИЯ ИММУНОКОНЪЮГАТОВ, МИШЕНЬЮ КОТОРЫХ ЯВЛЯЕТСЯ CD138 | 2010 |
|
RU2561041C2 |
| ПРИМЕНЕНИЯ ИММУНОКОНЪЮГАТОВ, МИШЕНЬЮ КОТОРЫХ ЯВЛЯЕТСЯ CD138 | 2012 |
|
RU2632108C2 |
| АНТИТЕЛА ПРОТИВ РЕЦЕПТОРА ФОЛИЕВОЙ КИСЛОТЫ 1, ИХ ИММУНОКОНЪЮГАТЫ И ИСПОЛЬЗОВАНИЕ | 2011 |
|
RU2610663C2 |
| CD37-СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ И ИХ ИММУНОКОНЪЮГАТЫ | 2011 |
|
RU2610662C9 |
| НОВЫЕ СИНЕРГИЧЕСКИЕ ЭФФЕКТЫ | 2009 |
|
RU2471499C2 |
| СПОСОБЫ КОНЪЮГАЦИИ | 2010 |
|
RU2765240C2 |
| АНТИТЕЛА ПРОТИВ CD20 И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2573994C2 |
| СПОСОБЫ КОНЪЮГАЦИИ | 2010 |
|
RU2595424C2 |






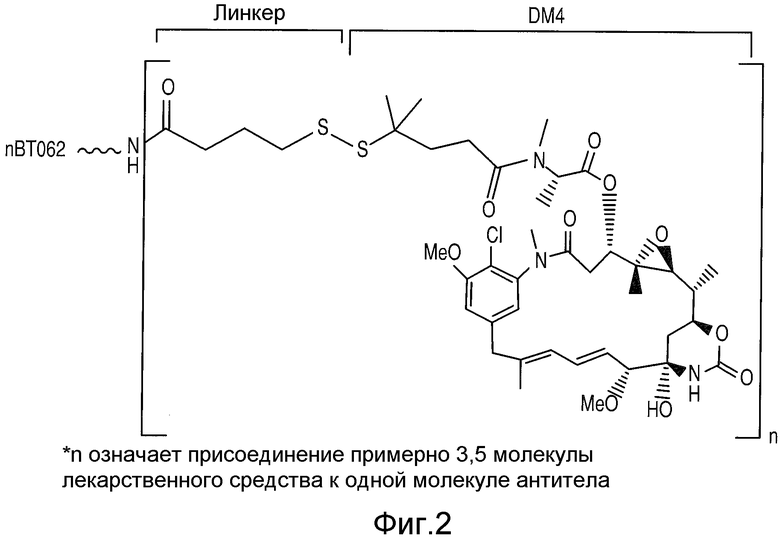

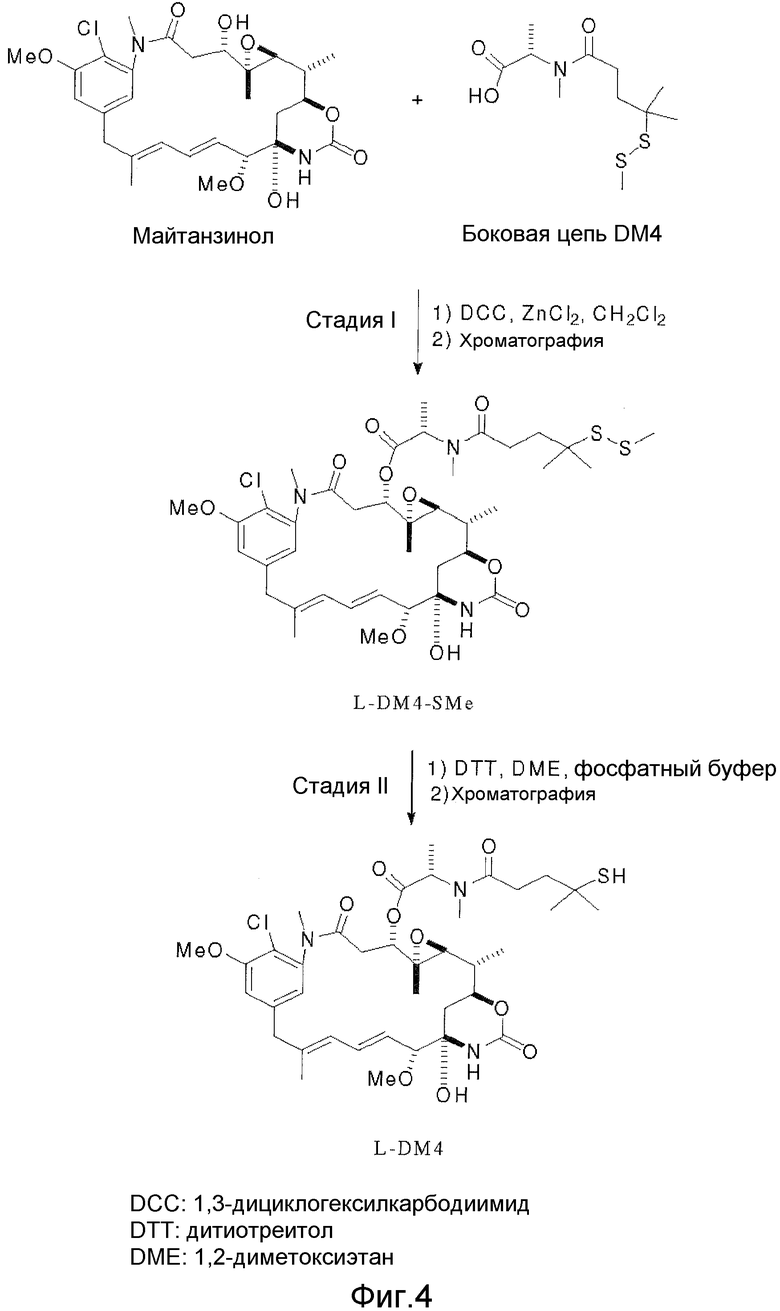
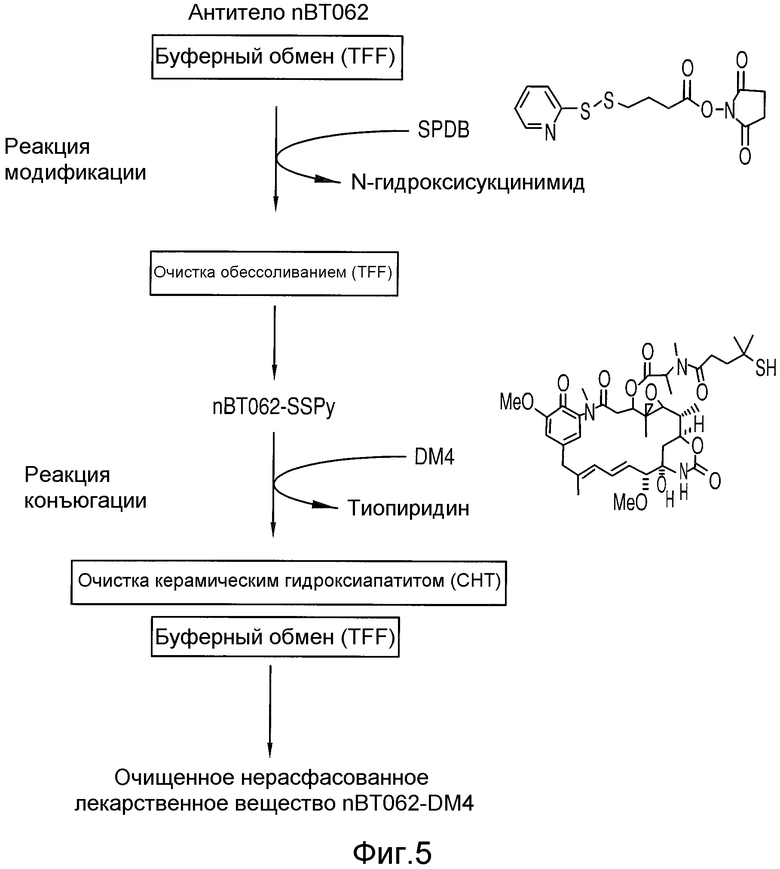
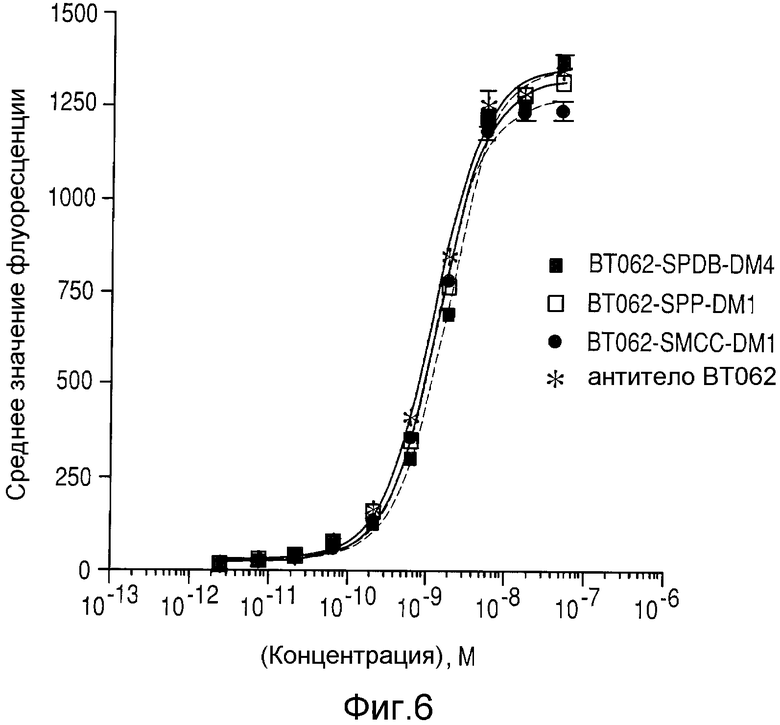
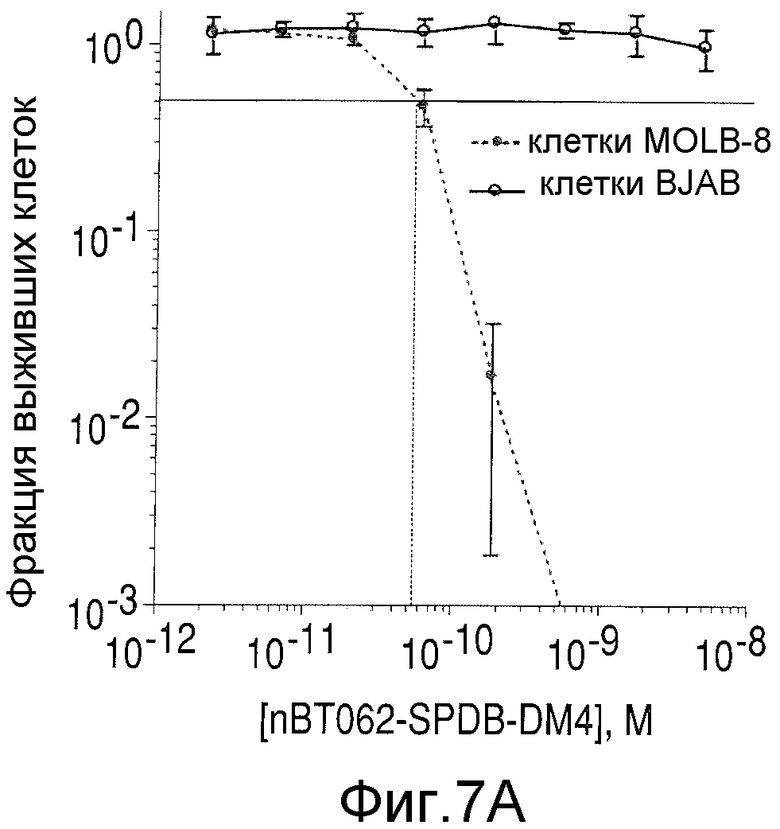

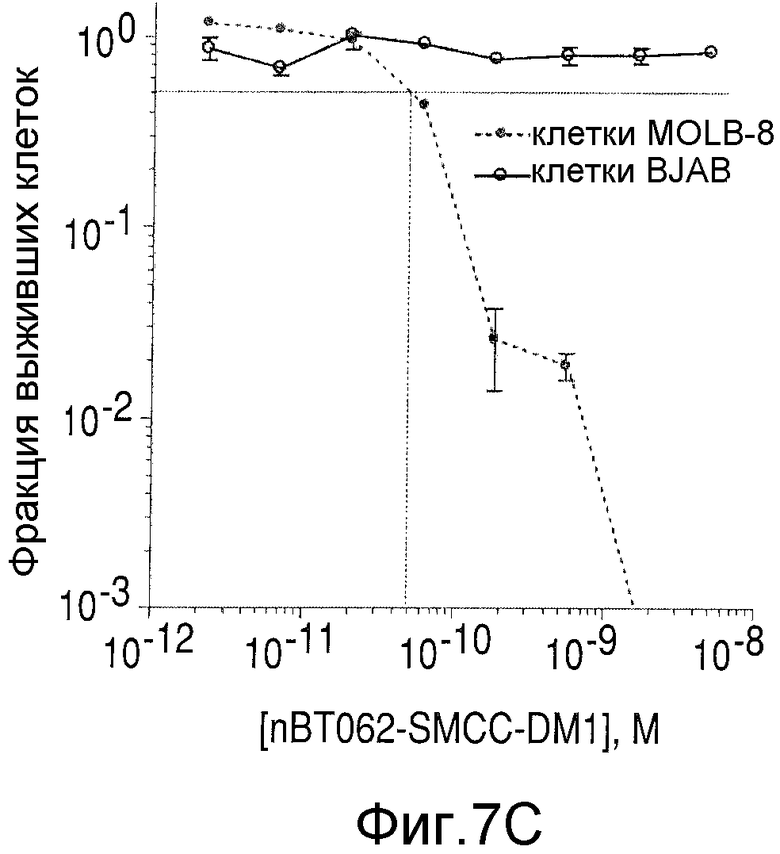
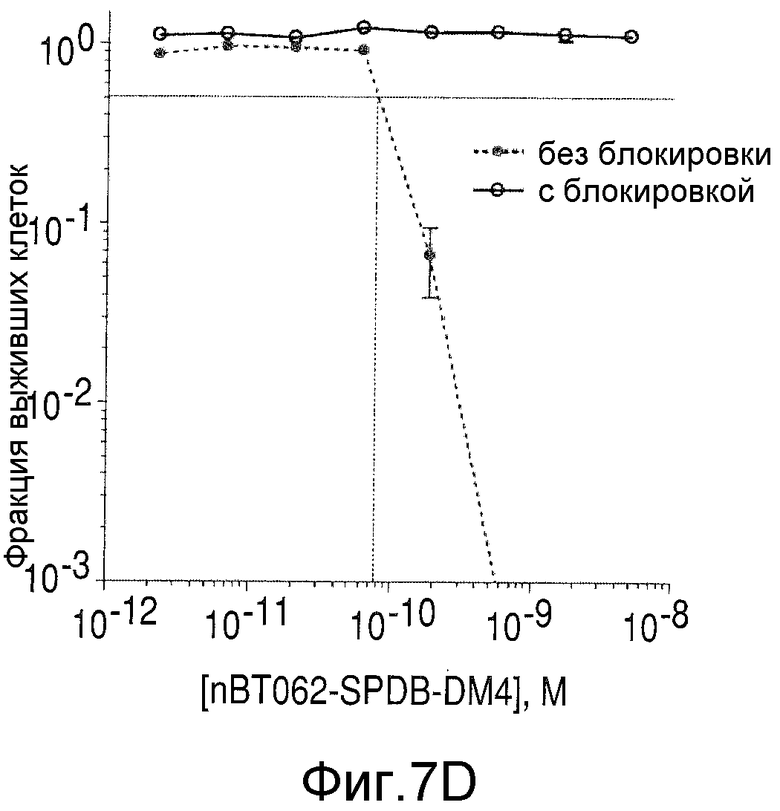
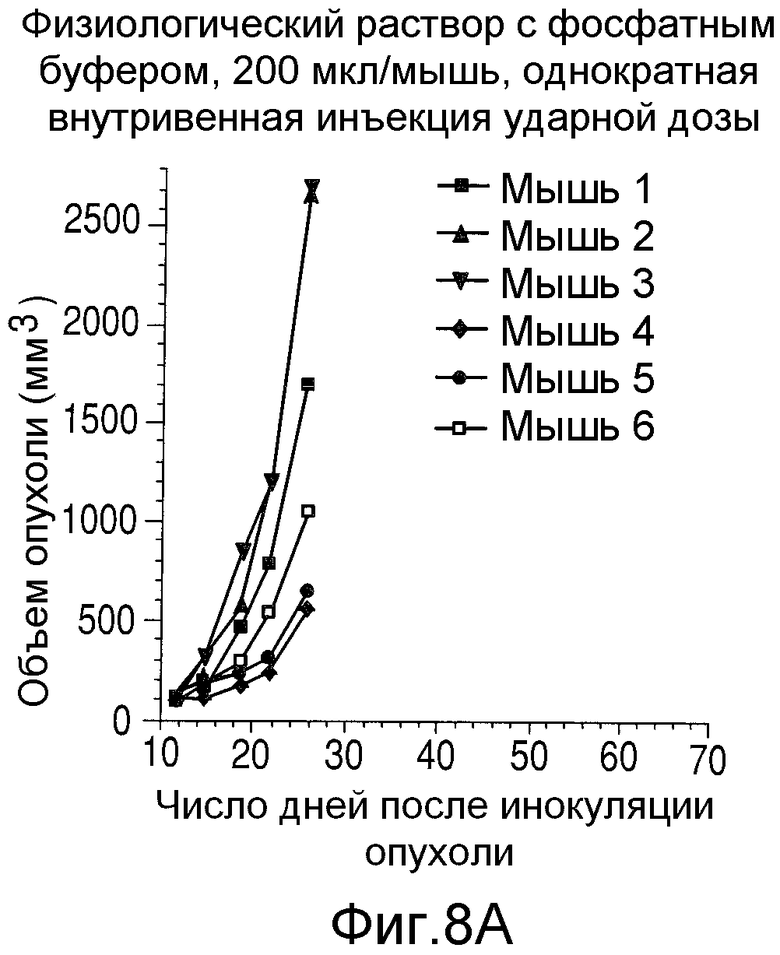
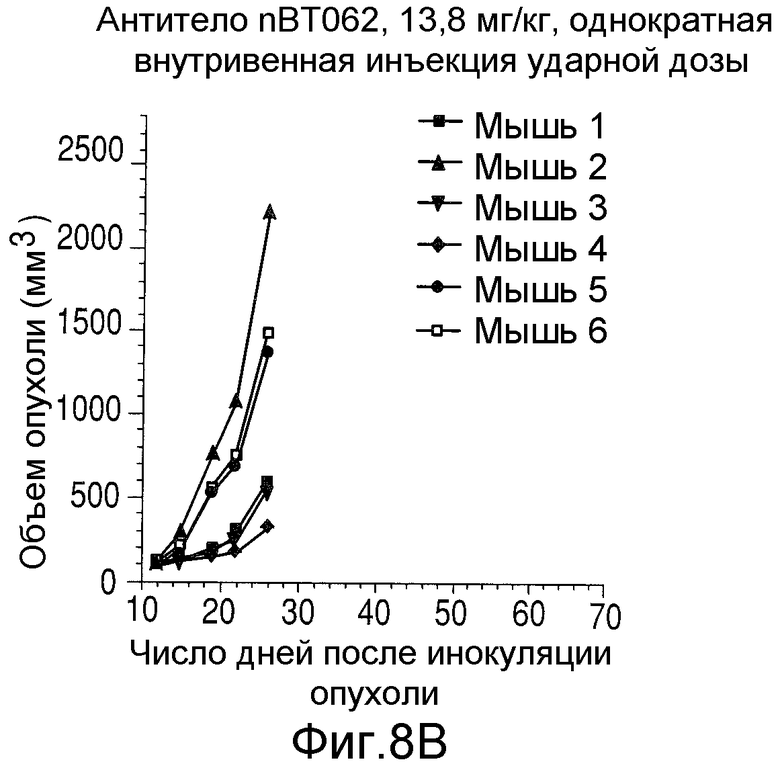
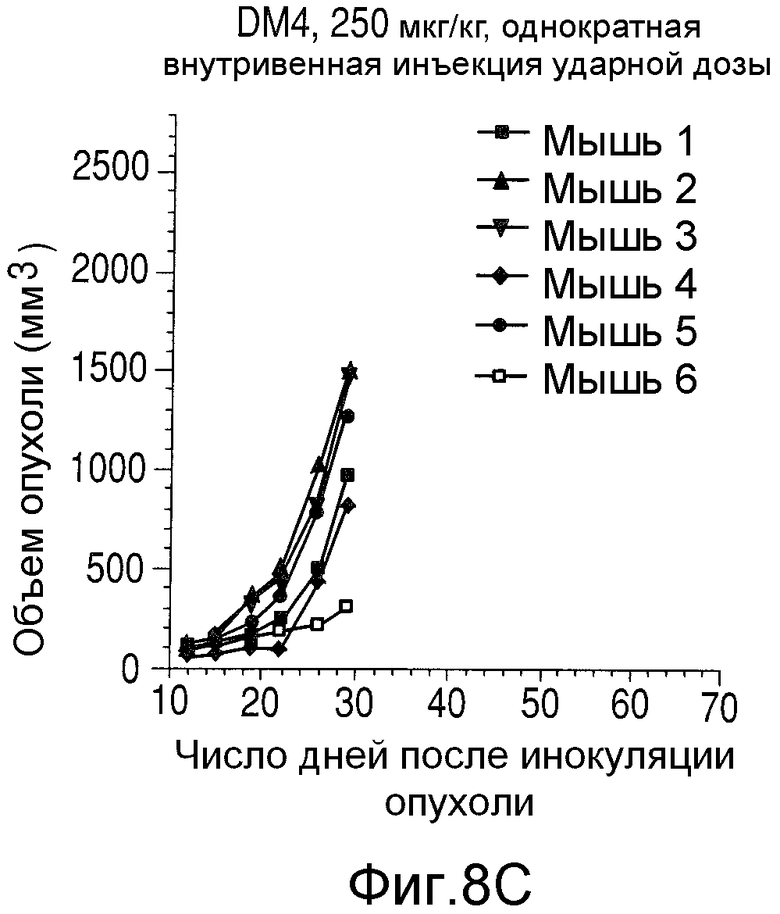
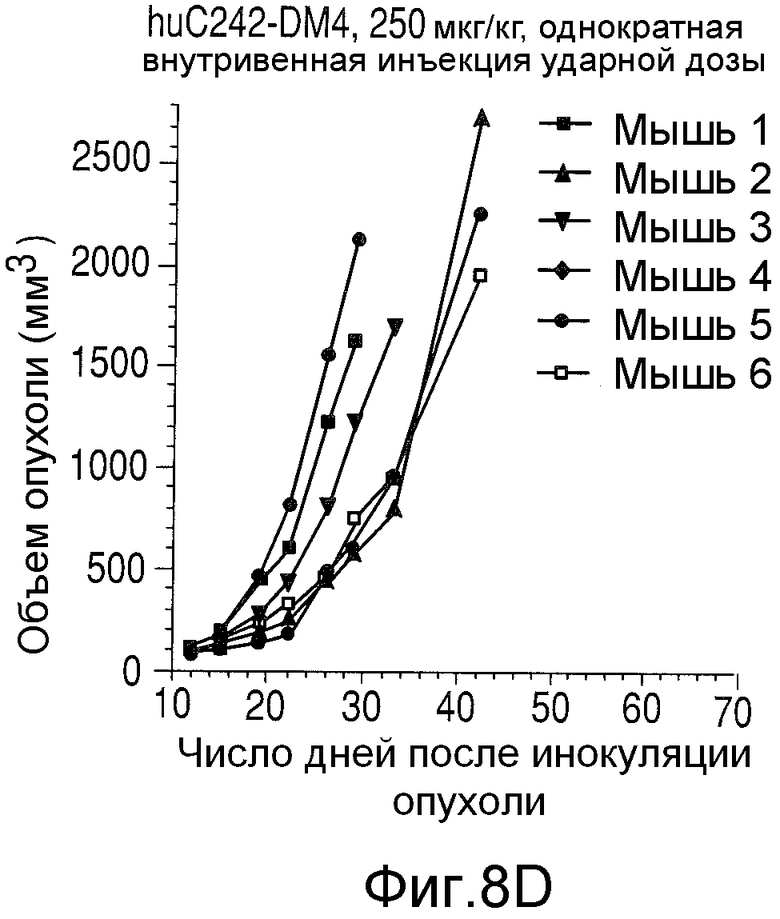
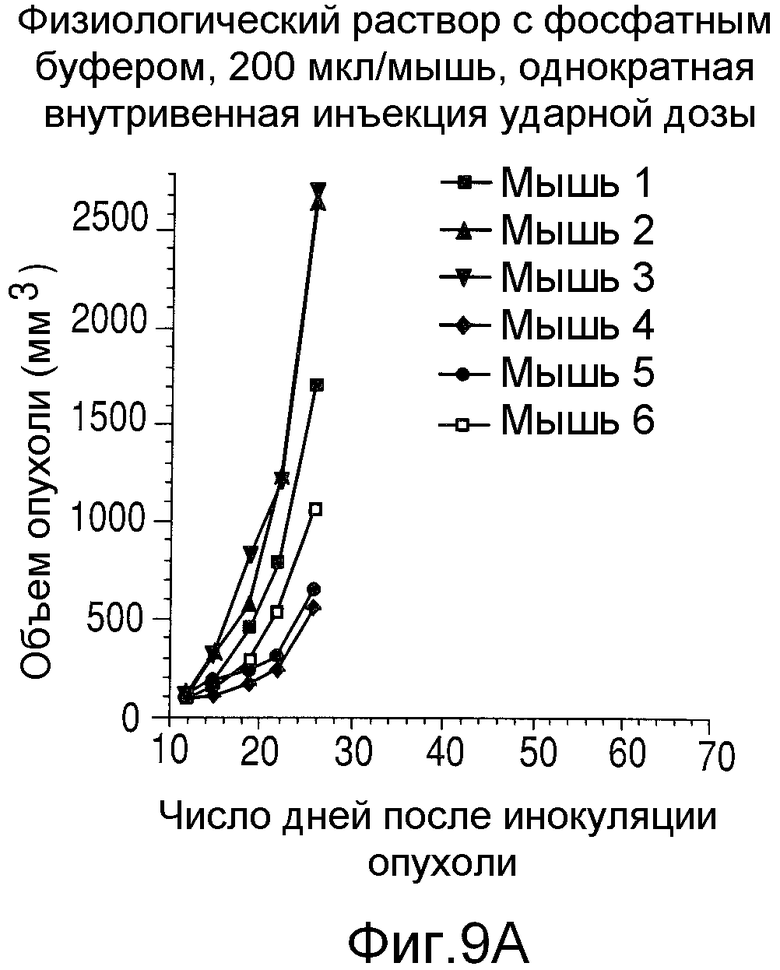
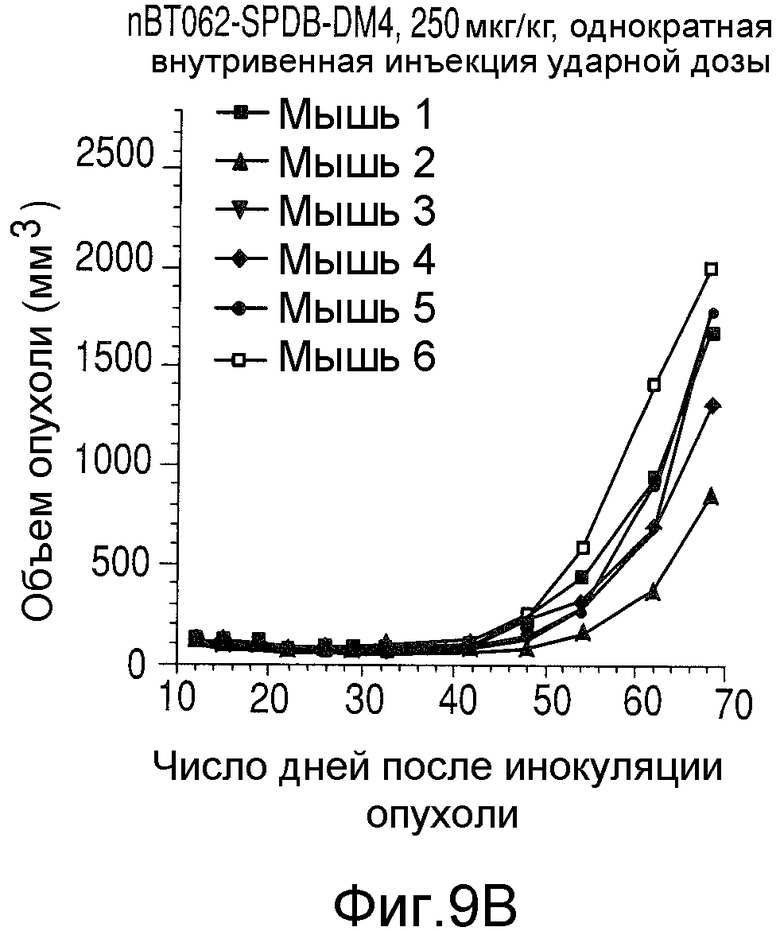

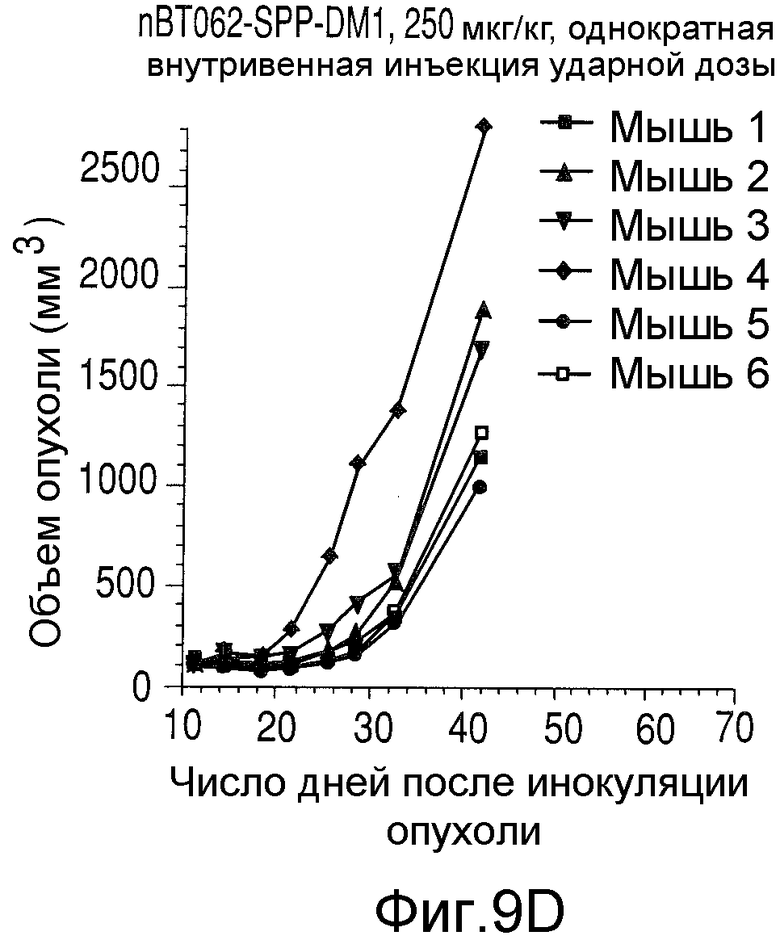
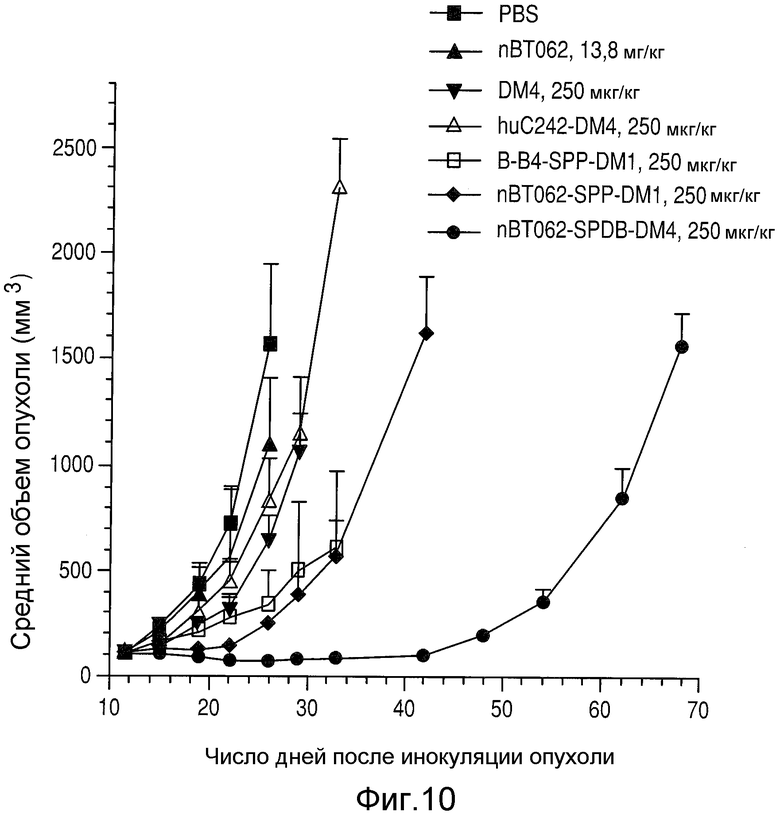
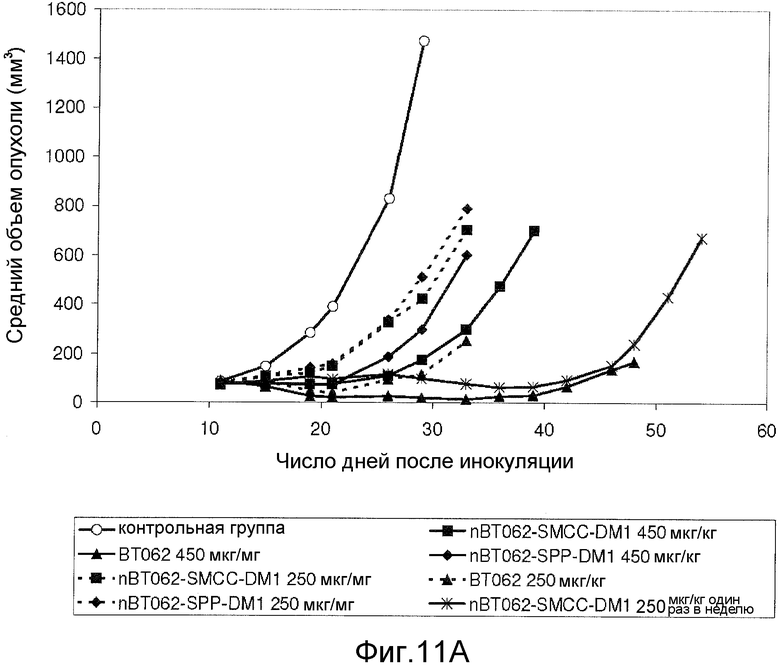
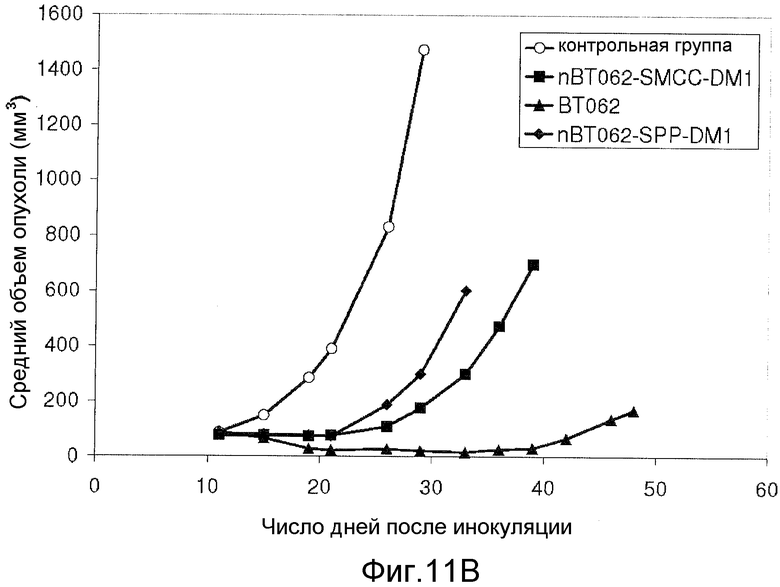
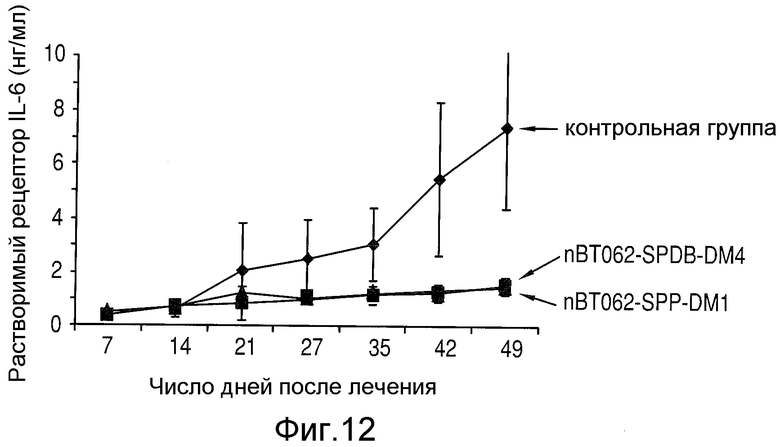
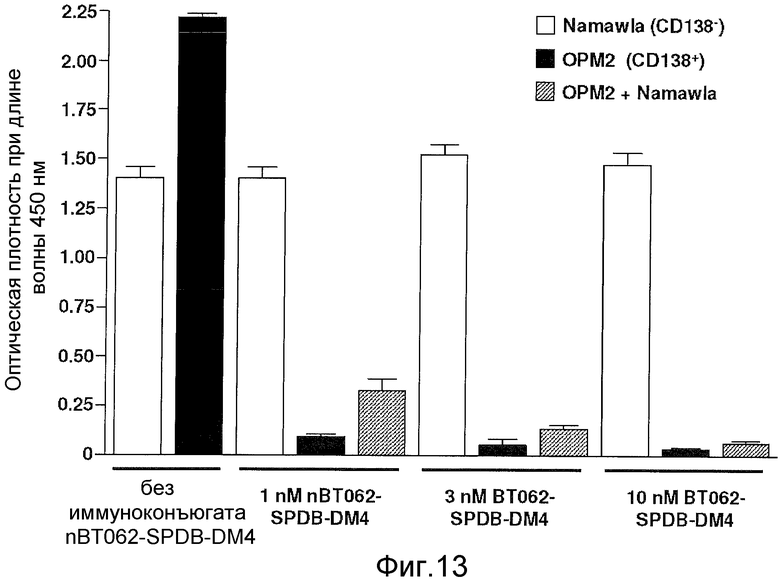

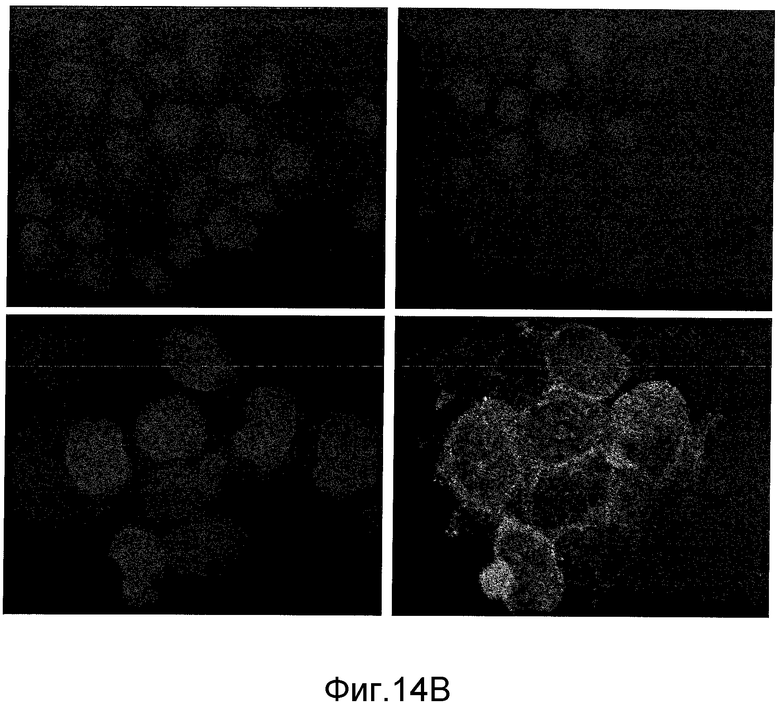
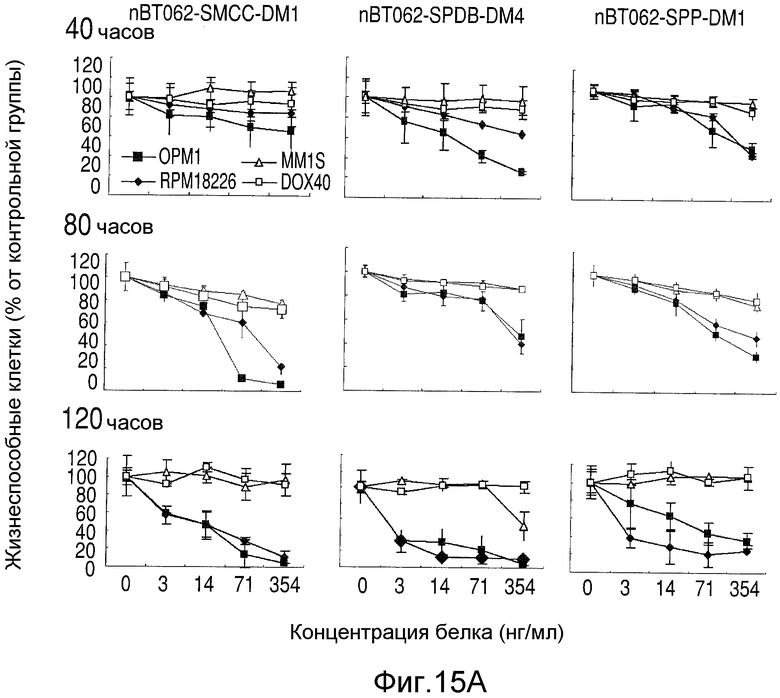
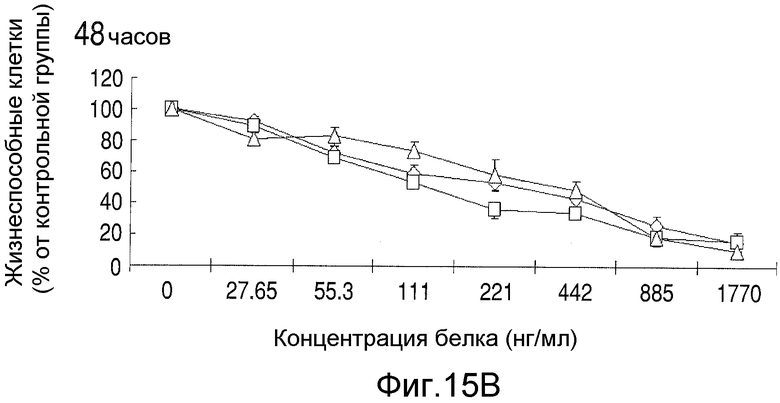
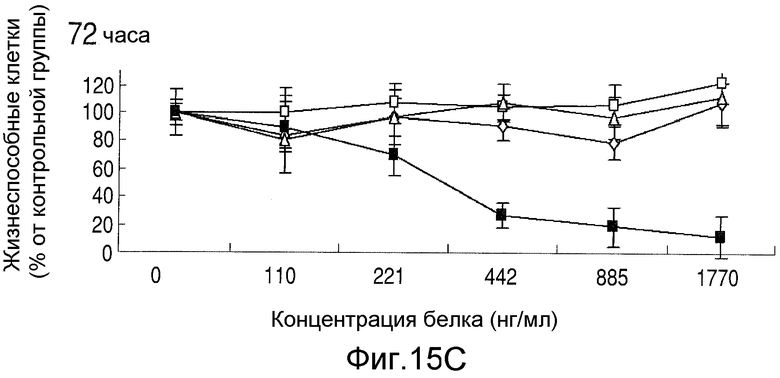
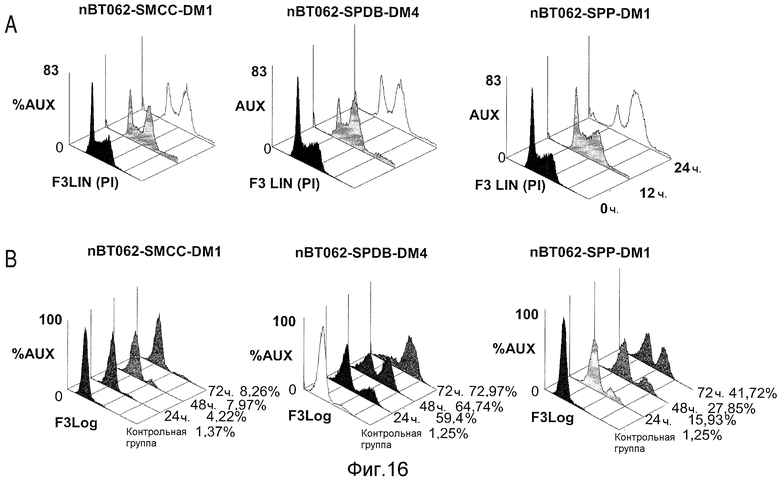
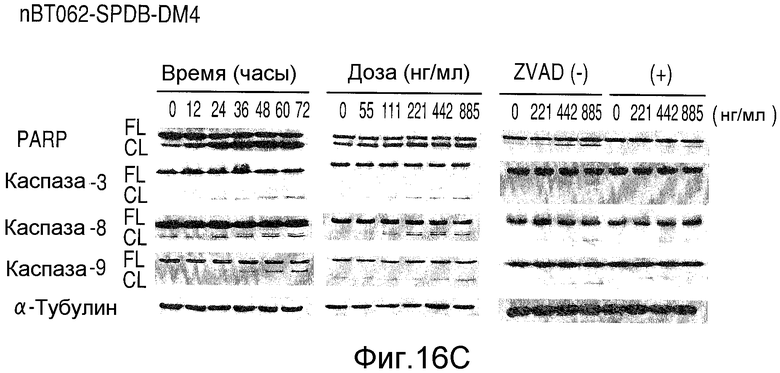
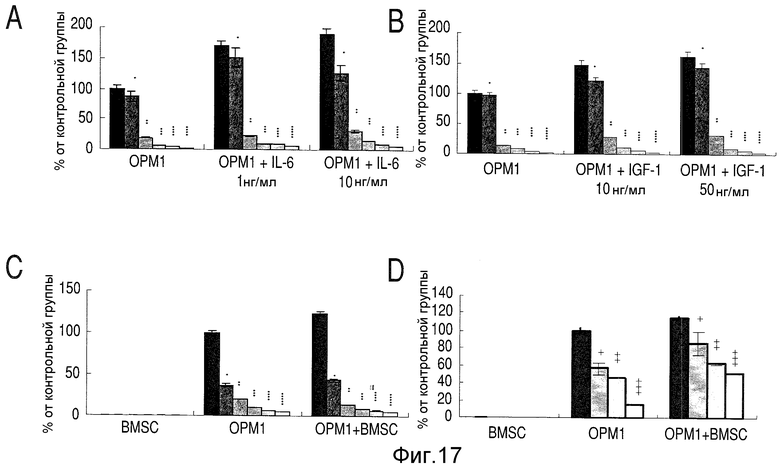
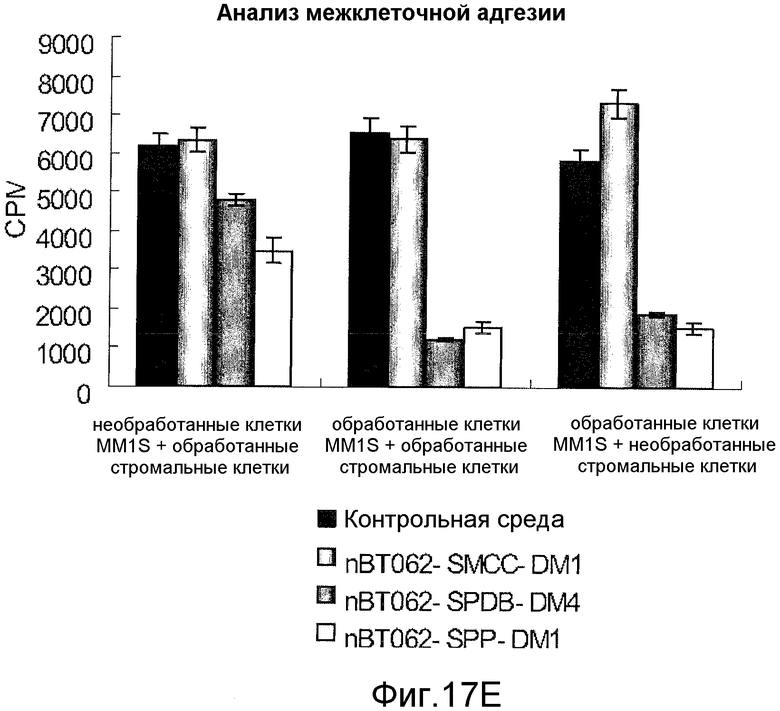
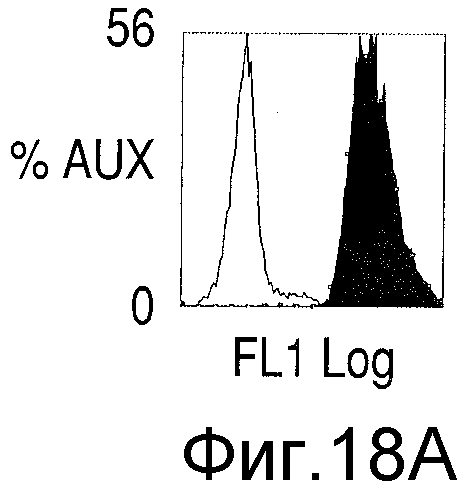
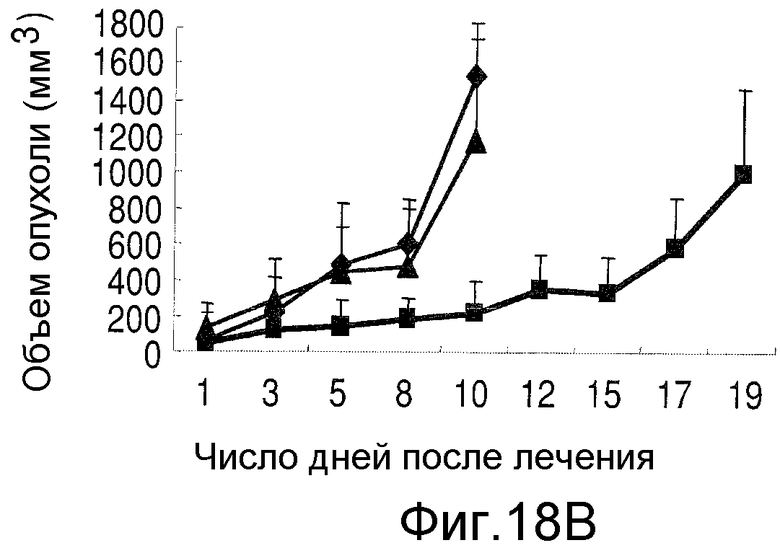
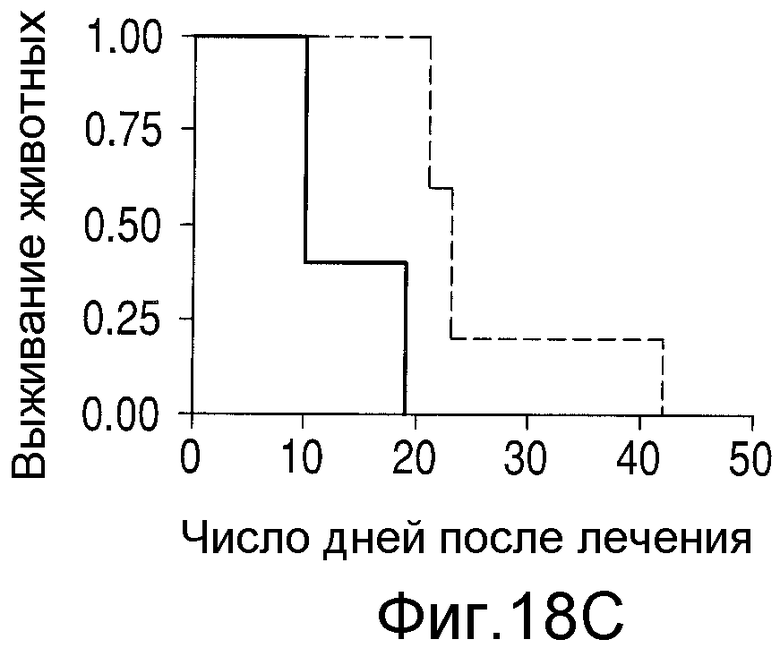

Изобретение относится к области биотехнологии, конкретно к клеточным технологиям и агентам для уменьшения адгезии клеток, и может быть использовано в медицине. Способ уменьшения адгезии стромальных клеток к СD138-экспрессирующим опухолевым клеткам в опухолевых клетках нуждающегося субъекта включает введение в указанные опухолевые клетки иммуноконъюгата, включающего сконструированное антитело нацеленного действия против СD138-экспрессирующих опухолевых клеток и эффекторную молекулу. Сконструированное антитело по существу состоит или включает антигенсвязывающую область против CD138, включающую (а) вариабельную область тяжелой цепи, включающую аминокислотные остатки 31-35 (CDR1), 51-68 (CDR2) и 99-111 (CDR3) SEQ ID NO:1, и (b) вариабельную область легкой цепи, включающую аминокислотные остатки 24-34 (CDR1), 50-56 (CDR2) и 89-97 (CDR3) SEQ ID NO:2. Способ также может включать введение в указанные опухолевые клетки дополнительного цитотоксического средства в количестве, ингибирующем, задерживающем и/или предотвращающем рост опухолевых клеток. Изобретение позволяет за счет уменьшения адгезии опухолевых клеток повысить их восприимчивость к воздействию эффекторной молекулы в составе иммуноконъюгата и других агентов, в частности, цитотоксических средств. 17 з.п. ф-лы, 18 ил.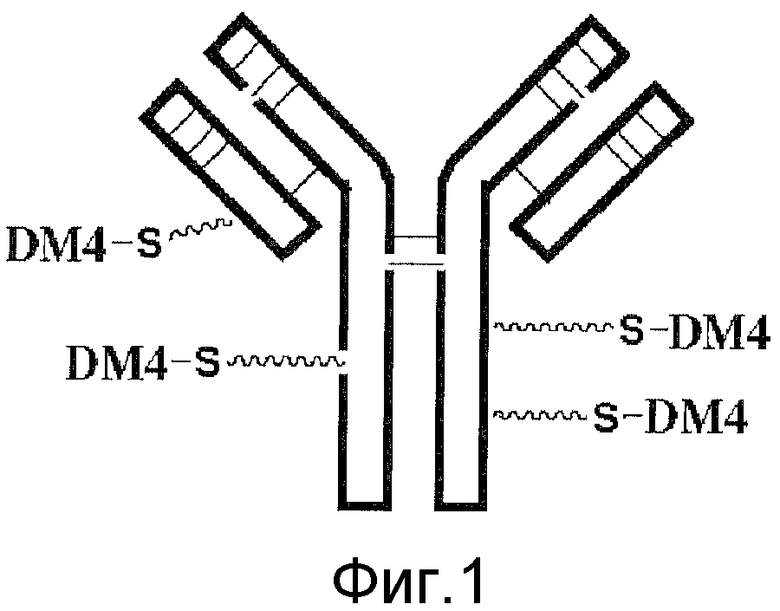
1. Способ уменьшения адгезии стромальных клеток к CD138-экспрессирующим опухолевым клеткам в опухолевых клетках нуждающегося субъекта, который включает:
введение в указанные опухолевые клетки иммуноконъюгата, включающего сконструированное антитело нацеленного действия и эффекторную молекулу, где указанный иммуноконъюгат нацеленно действует против CD138-экспрессирующих опухолевых клеток в количестве, эффективном для уменьшения адгезии стромальных клеток к CD138-экспрессирующим опухолевым клеткам, и, необязательно, введение в указанные опухолевые клетки дополнительного цитотоксического средства в количестве, ингибирующем, задерживающем и/или предотвращающем рост опухолевых клеток, где сконструированное созданное антитело нацеленного действия
(i) по существу, состоит из антигенсвязывающей области против CD138 антитела, отличного от человеческого, или
(ii) включает антигенсвязывающую область против CD138, где указанная антигенсвязывающая область взята от антитела, отличного от человеческого, и дополнительную область антитела, где, по меньшей мере, часть указанной дополнительной области антитела взята из человеческого антитела,
где антигенсвязывающая область включает:
(a) вариабельную область тяжелой цепи, включающую аминокислотные остатки 31-35 (CDR1), 51-68 (CDR2) и 99-111 (CDR3) SEQ ID NO:1, и
(b) вариабельную область легкой цепи, включающую аминокислотные остатки 24-34 (CDR1), 50-56 (CDR2) и 89-97 (CDR3) SEQ ID NO:2.
2. Способ по п.1, в котором указанная эффекторная молекула и указанное антитело нацеленного действия связаны друг с другом при помощи расщепляемого линкера.
3. Способ по п.2, в котором расщепляемый линкер содержит дисульфидную связь.
4. Способ по п.3, в котором линкер является SPP или SPDB.
5. Способ по любому из пп.1-4, в котором адгезия уменьшена, по меньшей мере, примерно на 10%, примерно на 20%, примерно на 30%, примерно на 40%, примерно на 50%, примерно на 60%, примерно на 70%, примерно на 80% или больше.
6. Способ по любому из пп.1-4, в котором указанная уменьшенная адгезия вызывает ослабление опосредуемой адгезией устойчивости к лекарствам.
7. Способ по п.6, в котором уменьшена опосредуемая адгезией устойчивость к лекарствам в отношении дополнительного цитотоксического средства, не являющегося указанным иммуноконъюгатом, и в котором указанное дополнительное цитотоксическое средство вводят в количестве, ингибирующем, задерживающем и/или предотвращающем рост опухолевых клеток.
8. Способ по п.7, в котором указанное цитотоксическое средство представляет собой мефалан, винкристин, доксорубицин, дексаметазон, циклофосфамид, этопозид, цитарабин, цисплатин, талидомид, прендизон, бортезомиб, леналидомид, сорафениб, ромидепсин или их комбинации.
9. Способ по п.7, в котором цитотоксическое средство создано на основе антитела.
10. Способ по п.1 или 2, в котором указанная эффекторная молекула имеет стерическое препятствие.
11. Способ по п.1 или 2, в котором эффекторная молекула представляет собой, по меньшей мере, один майтанзиноид, таксан, СС1065 или их аналог.
12. Способ по п.11, в котором эффекторная молекула представляет собой, по меньшей мере, один майтанзиноид, такой как DM1, DM3 или DM4.
13. Способ по п.12, в котором указанная эффекторная молекула представляет собой DM4.
14. Способ по любому из пп.1-4, в котором указанное сконструированное антитело нацеленного действия иммуноконъюгата включает:
аминокислотную последовательность тяжелой цепи иммуноглобулина или ее части, где указанная тяжелая цепь иммуноглобулина или ее части, по меньшей мере, на 70%, по меньшей мере, на 80%, по меньшей мере, на 90%, по меньшей мере, на 95% или, по меньшей мере, на 98% идентичны SEQ ID NO:1.
15. Способ по п.7, в котором иммуноконъюгат и цитотоксическое средство вводят последовательно, где цитотоксическое средство вводят после введения иммуноконъюгата.
16. Способ по п.7, в котором иммуноконъюгат и цитотоксическое средство вводят одновременно.
17. Способ по любому из пп.1-4 и 7-9, в котором указанный субъект является раковым пациентом, страдающим одним из следующих заболеваний: множественная миелома, карцинома яичника, карцинома почки, карцинома желчного пузыря, карцинома молочной железы, рак предстательной железы, рак легкого, карцинома толстой кишки, лимфома Ходжкина и неходжкинская лимфома, хронический лимфолейкоз (CLL), острый лимфобластный лейкоз (ALL), острый миелобластный лейкоз (AML) и солидная тканевая саркома.
18. Способ по п.17, в котором указанный пациент страдает множественной миеломой.
| US 20060045877, 02.03.2006 | |||
| WO 2006099875, 28.09.2006 | |||
| POST J | |||
| et al., Efficacy of an anti-CD138 immunotoxin and doxorubicin on drug-resistant and drug-sensitive myeloma cells, Int | |||
| J | |||
| Cancer, 1999, v.83, n.4, p.571-576 | |||
| БАЙКОВ B.B | |||
| и др | |||
| Пролиферация клеток миеломных клеточных линий при действии цитокинов и ингибиторов основных узлов |
Авторы
Даты
2013-06-27—Публикация
2008-12-23—Подача