Область изобретения, к которой относится изобретение
Настоящее изобретение относится к новым применениям анти-CD40-антител в лечении заболеваний или состояний, ассоциированных с ростом неопластических В-клеток. Изобретение особенно применимо для лечения пациентов, которым предварительно вводили (i) СНОР, (ii) химерное моноклональное анти-CD20-антитело ритуксимаб или (iii) CHOP и ритуксимаб в виде комбинированной терапии.
Уровень техники
CD40 является антигеном клеточной поверхности 50-55 кДа, присутствующим на поверхности как нормальных, так и неопластических В-клеток человека. Злокачественные В-клетки из опухолей В-клеточного направления дифференцировки экспрессируют CD40 и, по-видимому, зависят от передачи сигнала CD40 для выживания и пролиферации. Трансформированные клетки от пациентов с В-клеточными лимфомами низкой и высокой степени, В-клеточным острым лимфобластным лейкозом, множественной миеломой, хроническим лимфоцитарным лейкозом и болезнью Ходжкина экспрессируют CD40. Экспрессия CD40 детектируется также в остром миелобластном лейкозе и 50% связанных со СПИДом лимфом.
Анти-CD40-антитела и их применения были описаны, например, в совместных международных заявках на патент, опубликованных в виде WO 2005/044294, WO 2005/044304, WO 2005/044305, WO 2005/044306, WO 2005/044307, WO 2004/044854, WO 2005/044855, WO 2006/073443, WO 2006/125117, WO 2006/125143, WO 2007/053661 и WO 2007/053767. Эти заявки описывают конкретно моноклональное анти-CD40-антитело IgG1 человека, называемое в этих заявках CHIR-12 (но теперь известное как HCD122), генерируемое иммунизацией трансгенных мышей, несущих локус тяжелой цепи IgG1 человека и локус легкой цепи κ человека (XenoMouse® technology; Abgenix, California). Эти заявки раскрывают также применение анти-CD40-антител, таких как HCD122, для лечения заболеваний и состояний, ассоциированных с ростом неопластических В-клеток.
Хотя любой один терапевтический агент может обеспечивать пользу пациенту, требуются дополнительные способы для уменьшения токсичности и для улучшения результатов лечения. Кроме того, заболевания или состояния часто могут становиться не поддающимися лечению монотерапией (резистентными к монотерапии) либо в результате исходной устойчивости, либо устойчивости, развивающейся во время терапии. Таким образом, любое обнаружение комбинированной терапии, которая может улучшать лечение относительно монотерапии, представляет большой интерес.
Краткое описание фигур
Фиг.1 иллюстрирует результаты исследования противоопухолевой активности, обеспечиваемой различными обработками в модели ксенотрансплантата RL DLBCL (см. пример 1).
Фиг.2 иллюстрирует результаты исследования действий CD40L и HCD122 на цитотоксичность CHOP на клетках SU-DHL-4.
Фиг.3 иллюстрирует результаты исследования действий CD40L и HCD122 на передачу сигнала NFκB в клеточных линиях RL и SU-DHL-4.
Фиг.4 иллюстрирует результаты исследования действий CD40L и HCD122 на экспрессию некоторых молекул адгезии клеточной поверхности в клетках RL.
Фиг.5 иллюстрирует результаты исследования действий CD40L и HCD122 на экспрессию некоторых молекул адгезии клеточной поверхности в клетках SU-DHL-4.
Фиг.6 иллюстрирует результаты исследования действий CD40L и HCD122 на агрегацию in vitro клеток SU-DHL-4.
Подробное описание изобретения
Настоящее изобретение обеспечивает способы лечения пациентов-людей в отношении заболеваний или состояний, ассоциированных с ростом неопластических В-клеток. Эти способы включают комбинированную терапию с использованием (i) анти-CD40-антитела и (ii) циклофосфамида, доксорубицина, винкристина и преднизона (CHOP). Авторы изобретения обнаружили, что введение этих двух известных терапий в комбинации приводит к неожиданно сильнодействующей терапевтической эффективности in vivo. Авторы изобретения обнаружили, что объединенное действие этих двух терапий может быть более эффективным, чем сумма отдельных действий каждой терапии, т.е. что комбинация анти-CD40-антитела (такого как HCD122) с CHOP может обеспечивать синергическое терапевтическое действие. Не желая быть связанными какой-либо определенной теорией, авторы изобретения считают, что эта неожиданно сильная терапевтическая эффективность обусловлена способностью анти-CD40-антител сенсибилизировать В-клетки к цитотоксичности CHOP посредством подавления активации NF-κB и/или ингибированием CD40L-индуцированной экспрессии молекул адгезии.
Настоящее изобретение обеспечивает способ лечения пациента-человека в отношении заболевания или состояния, ассоциированного с ростом неопластических В-клеток, включающий введение указанному пациенту циклофосфамида, доксорубицина, винкристина и преднизона (CHOP) в комбинации с анти-CD40-антителом.
В некоторых вариантах осуществления анти-CD40-антитело (в настоящем документе "лечение антителами (пассивная иммунотерапия)") и циклофосфамид, доксорубицин, винкристин и преднизон (CHOP; здесь "химиотерапия") вводят пациенту одновременно. В этих вариантах осуществления введение антител пациенту (пассивная терапия) может проводиться точно в то же самое время, что и химиотерапия (т.е. эти два типа терапевтических веществ вводят одновременно). Альтернативно введение антител пациенту может проводиться приблизительно в то же самое время, что и химиотерапия (т.е. эти два типа терапевтических веществ не вводят точно в то же самое время), например, во время одного и того же визита к врачу или другому медицинскому работнику.
В других вариантах осуществления лечение антителами пациента и химиотерапию проводят не в одно и то же время, а последовательно в любом порядке. В этих вариантах осуществления способы по настоящему изобретению могут предусматривать первый цикл химиотерапии пациенту перед введением первой дозы анти-CD40-антитела этому пациенту. Альтернативно эти способы могут предусматривать проведение первого цикла химиотерапии пациенту после введения первой дозы анти-CD40-антитела этому пациенту. В вариантах, в которых лечение антителами и химиотерапию выполняют последовательно, эти терапевтические вещества могут вводиться таким образом, что обе эти терапии проявляют терапевтическое действие на пациента в одно и то же время (т.е. периоды, в которых каждое терапевтическое вещество является эффективным, могут перекрываться), хотя это и не является существенным.
Таким образом, изобретение обеспечивает способ лечения пациента-человека в отношении заболевания или состояния, ассоциированного с ростом неопластических В-клеток, включающий введение пациенту анти-CD40-антитела до, во время или после введения одного и/или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона. Ссылки здесь в отношении использования одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона являются ссылками на использование одного или более, двух или более, трех или более или всех четырех из циклофосфамида, доксорубицина, винкристина и преднизона.
В вариантах осуществления, в которых первый цикл химиотерапии проводят для пациента до первой дозы анти-CD40-антитела, первый цикл химиотерапии может проводиться от приблизительно одной недели до приблизительно одного года, от приблизительно одной недели до приблизительно десяти месяцев, от приблизительно одной недели до приблизительно восьми месяцев, от приблизительно одной недели до приблизительно шести месяцев, от приблизительно одной недели до приблизительно четырех месяцев, от приблизительно одной недели до приблизительно двух месяцев, от приблизительно одной недели до приблизительно одного месяца, от приблизительно одной недели до приблизительно трех недель, от приблизительно одной недели до приблизительно двух недель или приблизительно одной недели, прежде чем первую дозу анти-CD40-антитела вводят этому пациенту. Другими словами, лечение антителами может проводиться от приблизительно одной недели до приблизительно одного года, от приблизительно одной недели до приблизительно десяти месяцев, от приблизительно одной недели до приблизительно восьми месяцев, от приблизительно одной недели до приблизительно шести месяцев, от приблизительно одной недели до приблизительно четырех месяцев, от приблизительно одной недели до приблизительно двух месяцев, от приблизительно одной недели до приблизительно одного месяца, от приблизительно одной недели до приблизительно трех недель, от приблизительно одной недели до приблизительно двух недель или приблизительно одной недели после первого цикла химиотерапии.
В вариантах осуществления, в которых первый цикл химиотерапии проводят для пациента после первой дозы анти-CD40-антитела, первый цикл химиотерапии может проводиться от приблизительно одной недели до приблизительно одного года, от приблизительно одной недели до приблизительно десяти месяцев, от приблизительно одной недели до приблизительно восьми месяцев, от приблизительно одной недели до приблизительно шести месяцев, от приблизительно одной недели до приблизительно четырех месяцев, от приблизительно одной недели до приблизительно двух месяцев, от приблизительно одной недели до приблизительно одного месяца, от приблизительно одной недели до приблизительно трех недель, от приблизительно одной недели до приблизительно двух недель или приблизительно одной недели, после введения первой дозы анти-CD40-антитела этому пациенту. Другими словами, лечение антителами может проводиться от приблизительно одной недели до приблизительно одного года, от приблизительно одной недели до приблизительно десяти месяцев, от приблизительно одной недели до приблизительно восьми месяцев, от приблизительно одной недели до приблизительно шести месяцев, от приблизительно одной недели до приблизительно четырех месяцев, от приблизительно одной недели до приблизительно двух месяцев, от приблизительно одной недели до приблизительно одного месяца, от приблизительно одной недели до приблизительно трех недель, от приблизительно одной недели до приблизительно двух недель или приблизительно одной недели, перед первым циклом химиотерапии.
Когда эти терапевтические вещества вводят одновременно, они могут вводиться в виде единой фармацевтической композиции или в виде двух или более отдельных фармацевтических композиций. Когда эти терапевтические вещества не вводят одновременно, их вводят в виде двух или более отдельных фармацевтических композиций.
При использовании двух или более фармацевтических композиций, может быть использована любая подходящая комбинация терапевтического антитела и химиотерапевтического вещества. Например, одна фармацевтическая композиция может содержать терапевтическое антитело, тогда как другая фармацевтическая композиция (другие фармацевтические композиции) содержит химиотерапевтические агенты циклофосфамид, доксорубицин, винкристин и преднизон. Альтернативно одна фармацевтическая композиция может содержать терапевтическое антитело и один или несколько химиотерапевтических агентов, тогда как другая фармацевтическая композиция (другие фармацевтические композиции) содержит другой химиотерапевтический агент (другие фармацевтические агенты). В вариантах осуществления, в которых фармацевтическая композиция содержит терапевтическое антитело и один или несколько химиотерапевтических агентов, эта фармацевтическая композиция может быть получена способом, предусматривающим стадии (i) получения композиции лиофилизированного анти-CD40-антитела, (ii) получения композиции, содержащей один или несколько химиотерапевтических агентов в стерильном разбавителе и (iii) воссоздания композиции лиофилизированного антитела с использованием композиции, содержащей один или несколько из этих химиотерапевтических агентов.
Таким образом, изобретение обеспечивает фармацевтическую композицию (i) одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона, (ii) анти-CD40-антитела и (iii) фармацевтически приемлемого носителя или эксципиента.
Изобретение обеспечивает также применение (i) одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона и (ii) анти-CD40-антитела в производстве лекарственного средства для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток. В других вариантах осуществления изобретение обеспечивает применение (i) одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона и (ii) анти-CD40-антитела в производстве по меньшей мере двух отдельных лекарственных средств (двух, трех, четырех или пяти лекарственных средств) для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, комбинированной терапией. Циклофосфамид, винкристин, преднизон, доксорубицин и анти-CD40-антитело могут быть использованы в производстве по меньшей мере трех, по меньшей мере четырех или пяти раздельных лекарственных средств.
Изобретение обеспечивает также набор для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем указанный набор содержит (i) один или несколько из циклофосфамида, доксорубицина, винкристина и преднизона и (ii) анти-CD40-антитело. Этот набор может дополнительно содержать одно или несколько устройств для введения комбинированного терапевтического средства пациенту-человеку, таких как одна или несколько стерильных игл и один или несколько стерильных шприцов, (ii) стерильный контейнер (например, стеклянный флакон, пластиковый флакон или пластиковый мешок) и отстойник, (iii) стерильная трубка с регулировочным зажимом и (iv) катетер.
Изобретение обеспечивает способ лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, включающий введение указанному пациенту одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона, при этом пациенту предварительно вводили анти-CD40-антитело. Настоящее изобретение обеспечивает также способ лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, включающий введение указанному пациенту анти-CD40-антитела, при этом пациенту предварительно вводили один или несколько из циклофосфамида, доксорубицина, винкристина и преднизона.
Изобретение обеспечивает дополнительно применение анти-CD40-антитела в производстве лекарственного средства для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем указанному пациенту-человеку предварительно вводили один или несколько из циклофосфамида, доксорубицина, винкристина и преднизона. Изобретение обеспечивает также применение одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона в производстве лекарственного средства для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем указанному пациенту-человеку предварительно вводили анти-CD40-антитело.
Под терминами "предварительно вводили" или "предварительное введение" имеют в виду, что субъект получал одну или несколько доз первого лекарственного средства перед получением второго лекарственного средства. Субъект, которому "предварительно вводили" или которому обеспечивали "предварительное введение", включает пациентов, которых лечили первым терапевтическим средством в пределах 2 лет, в пределах 18 месяцев, в пределах 1 года, в пределах 6 месяцев, в пределах 2 месяцев, в пределах 6 недель, в пределах 1 месяца, в пределах 4 недель, в пределах 3 недель, в пределах 2 недель, в пределах 1 недели, в пределах 6 дней, в пределах 5 дней, в пределах 4 дней, в пределах 3 дней, в пределах 2 дней или в пределах 1 дня перед началом лечения вторым терапевтическим средством. В комбинированных способах по настоящему изобретению термины "предварительно вводили" или "предварительное введение" относятся также к пациентам, которых лечили анти-CD40-антителом в пределах 2 лет, в пределах 18 месяцев, в пределах 1 года, в пределах 6 месяцев, в пределах 2 месяцев, в пределах 6 недель, в пределах 1 месяца, в пределах 4 недель, в пределах 3 недель, в пределах 2 недель, в пределах 1 недели, в пределах 6 дней, в пределах 5 дней, в пределах 4 дней, в пределах 3 дней, в пределах 2 дней или в пределах 1 дня перед началом лечения с использованием химиотерапии. В комбинированных способах по настоящему изобретению термины "предварительно вводили" или "предварительное введение" относятся также к пациентам, которых лечили химиотерапией в пределах 2 лет, в пределах 18 месяцев, в пределах 1 года, в пределах 6 месяцев, в пределах 2 месяцев, в пределах 6 недель, в пределах 1 месяца, в пределах 4 недель, в пределах 3 недель, в пределах 2 недель, в пределах 1 недели, в пределах 6 дней, в пределах 5 дней, в пределах 4 дней, в пределах 3 дней, в пределах 2 дней или в пределах 1 дня перед началом лечения анти-CD40-антителом.
Пациентов, которым предварительно вводили анти-CD40-антитело, можно отличать от других пациентов, например, с использованием медицинских карт пациентов или проведением подходящего теста (подходящих тестов) in vitro. Пациентов, которым предварительно вводили один или несколько из циклофосфамида, доксорубицина, винкристина и преднизона, можно отличать от других пациентов, например, с использованием медицинских карт пациентов или проведением подходящего теста (подходящих тестов) in vitro.
Изобретение обеспечивает также применение анти-CD40-антитела в производстве лекарственного средства для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем лекарственное средство вводят перед циклофосфамидом, доксорубицином, винкристином или преднизоном. В альтернативных вариантах осуществления изобретение обеспечивает также применение анти-CD40-антитела в производстве лекарственного средства для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем лекарственное средство вводят после циклофосфамида, доксорубицина, винкристина или преднизона. Изобретение обеспечивает также применение одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона в производстве лекарственного средства для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем лекарственное средство вводят перед анти-CD40-антителом. В альтернативных вариантах осуществления изобретение обеспечивает применение одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона в производстве лекарственного средства для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем лекарственное средство вводят после анти-CD40-антитела.
Изобретение обеспечивает также анти-CD40-антитело и один или несколько из циклофосфамида, доксорубицина, винкристина и преднизона для одновременного, раздельного или последовательного применения в лечении пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, комбинированной терапией. Изобретение обеспечивает также применение анти-CD40-антитела в производстве лекарственного средства для одновременного или последовательного применения в комбинации с одним или несколькими из циклофосфамида, доксорубицина, винкристина и преднизона для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток. Изобретение обеспечивает применение одного или нескольких из циклофосфамида, доксорубицина, винкристина и преднизона в производстве лекарственного средства для одновременного или последовательного применения в комбинации с анти-CD40-антителом для лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток.
Способы по изобретению могут предусматривать введение дозы анти-CD40-антитела в любой момент во время первого или последующего цикла химиотерапии. Альтернативно способы по изобретению могут предусматривать введение дозы анти-CD40-антитела между циклами химиотерапии.
Как отмечалось выше, авторы изобретения нашли, что комбинированная терапия анти-CD40-антителом и CHOP может обеспечивать синергическое терапевтическое действие. Таким образом, в некоторых вариантах осуществления способов, применений, композиций и наборов, описанных в настоящем документе, комбинированная терапия обеспечивает синергическое улучшение терапевтической эффективности относительно индивидуальных терапевтических агентов при введении раздельно. Термин "синергия" используется для описания комбинированного действия двух или более активных агентов, которое является более высоким, чем сумма индивидуальных действий каждого соответствующего активного агента. Таким образом, если объединенное действие двух или более агентов приводит к "синергическому ингибированию" активности или процесса, например, роста опухоли, предполагается, что это ингибирование активности или процесса является более высоким, чем сумма ингибирующих действий каждого соответствующего активного агента. Таким образом, термин "синергическое терапевтическое действие" относится к терапевтическому действию, наблюдаемому с комбинацией двух или более терапий, где это терапевтическое действие (измеренное по любому из ряда параметров, например, задержке роста опухоли, как в примере 1 в данном описании) является более высоким, чем сумма индивидуальных терапевтических действий, наблюдаемых с соответствующими индивидуальными терапиями.
Как отмечалось выше, авторы изобретения считают, что эта неожиданно сильная терапевтическая эффективность, обеспечиваемая комбинированной терапией по изобретению, обусловлена способностью анти-CD40-антител сенсибилизировать В-клетки к цитотоксичности CHOP посредством подавления активации NF-κB и/или ингибированием CD40L-индуцированной экспрессии молекул адгезии (см. примеры 2-4 данного описания). Приведенные примеры демонстрируют, что передача сигнала через CD40 может способствовать развитию резистентности В-клеток к цитотоксичности CHOP, и что эта устойчивость может предотвращаться или уменьшаться использованием антагонистического анти-CD40-антитела (такого как HCD122) с уменьшением передачи сигнала CD40. Приведенные примеры дополнительно демонстрируют, что экспрессия молекул адгезии клеточной поверхности на В-клетках, индуцируемая передачей сигнала CD40, может способствовать развитию резистентности В-клеток к цитотоксичности CHOP, позволяющей В-клеткам агрегироваться и взаимодействовать с их микроокружением. Приведенные здесь примеры предполагают, что экспрессия молекул адгезии клеточной поверхности на В-клетках может быть предотвращена или уменьшена с использованием анти-CD40-антитела (такого как HCD122).
Таким образом, изобретение обеспечивает применение анти-CD40-антитела для предотвращения или уменьшения резистентности к цитотоксичности CHOP в неопластических В-клетках человека (т.е. для сенсибилизации неопластических В-клеток к цитотоксичности CHOP). Изобретение обеспечивает также способ предотвращения или уменьшения резистентности к цитотоксичности CHOP в неопластических В-клетках человека (т.е. сенсибилизации неопластических В-клеток к цитотоксичности CHOP), предусматривающий стадию контактирования in vitro одной или нескольких неопластических В-клеток человека с анти-CD40-антителом.
Кроме того, изобретение обеспечивает способ предотвращения или уменьшения резистентности В-клеток к цитотоксичности CHOP в пациенте-человеке, предусматривающий стадию введения анти-CD40-антитела этому пациенту. Изобретение обеспечивает также способ лечения пациента-человека от заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем указанный способ предусматривает стадию уменьшения резистентности В-клеток к цитотоксичности CHOP в указанном пациенте (т.е. сенсибилизации неопластических В-клеток этого пациента к цитотоксичности CHOP) введением анти-CD40-антитела пациенту.
Изобретение обеспечивает также анти-CD40-антитело для предотвращения или уменьшения резистентности В-клеток к цитотоксичности CHOP в неопластических В-клетках человека in vitro (т.е. для сенсибилизации неопластических В-клеток этого пациента к цитотоксичности CHOP) или в пациенте-человеке in vivo (т.е. сенсибилизации неопластических В-клеток пациента к цитотоксичности CHOP). Изобретение обеспечивает также применение анти-CD40-человека в производстве лекарственного средства для предотвращения или уменьшения резистентности В-клеток к цитотоксичности CHOP в пациенте-человеке (т.е. сенсибилизации неопластических В-клеток пациента к цитотоксичности CHOP).
Предпочтительно анти-CD40-антитело, используемое в этих экспериментах, подавляет активацию NF-κB. В частности, антитело может подавлять активацию NF-κB в В-клетках, которая индуцируется передачей сигнала CD40 и которая способствует развитию резистентности В-клеток к цитотоксичности CHOP.
Предпочтительно анти-CD40-антитело, используемое в этих экспериментах, является антителом, которое ингибирует экспрессию одной или нескольких молекул адгезии клеточной поверхности на В-клетках. В частности, это антитело может ингибировать экспрессию одной или нескольких молекул адгезии клеточной поверхности на В-клетках, которая индуцируется передачей сигнала CD40 и которая способствует развитию резистентности В-клеток к цитотоксичности CHOP. В некоторых вариантах осуществления анти-CD40-антитело ингибирует индуцированную CD40-L экспрессию одного или нескольких из CD54, CD80, CD86 и CD95 (или двух или более, трех или более или всех четырех из CD54, CD80, CD86 и CD95).
Таким образом, композиции, применения и наборы по изобретению могут использовать анти-CD40-антитело, которое способно подавлять активацию NF-κB и/или которое способно ингибировать экспрессию одной или нескольких молекул адгезии клеточной поверхности на В-клетках.
Суммирование стандартных способов и процедур, которые могут быть использованы для применения изобретения, приведены ниже. Должно быть понятно, что настоящее изобретение не ограничивается описанными конкретными методологией, протоколами, клеточными линиями, векторами и реагентами. Должно быть также понятно, что используемая здесь терминология является терминологией только для цели описания конкретных вариантов осуществления, и не предполагается, что эта терминология должна ограничивать объем настоящего изобретения. Объем изобретения ограничивается только прилагаемой формулой изобретения.
В данном описании используются стандартные аббревиатуры для нуклеотидов и аминокислот. Применение на практике настоящего изобретения будет использовать, если нет других указаний, общепринятые способы молекулярной биологии, микробиологии, технологии рекомбинантных ДНК и иммунологии, которые находятся в рамках квалификации специалистов, работающих в данной области. Такие способы полностью описаны в литературе.
Изобретение включает применение анти-CD40-антител для лечения пациентов, имеющих заболевания или состояния, ассоциированные с ростом неопластических В-клеток. Под терминами "CD40", "CD40-антиген" или "CD40-рецептор" имеется в виду трансмембранный гликопротеин 50-55 кДа семейства рецепторов фактора некроза опухолей (TNF) (см., например, патенты США №№ 5674492 и 4708871; Stamenkovic et al. (1989) EMBO 8:1403; Clark (1990) Tissue Antigens 36:33; Barclay et al. (1997) The Leucocyte Antigen Facts Book (2d ed.; Academic Press, San Diego)). Были идентифицированы две изоформы CD40 человека, кодируемые вариантами альтернативно сплайсированных транскриптов этого гена. Первая изоформа (также известная как "длинная изоформа" или "изоформа 1") экспрессируется в виде состоящего из 277 аминокислот полипептида-предшественника (SEQ ID NO:9; впервые сообщенного в виде GenBank Accession № CAA43045, и идентифицированного как изоформа 1 в GenBank Accession № NP_001241), кодируемого SEQ ID NO:8 (см. GenBank Accession №№ X60592 и NM_001250), который имеет сигнальную последовательность, представленную первыми 19 остатками. Вторая изоформа (также известная как "короткая изоформа" или "изоформа 2") экспрессируется в виде состоящего из 203 аминокислот полипептида-предшественника (SEQ ID NO:7; GenBank Accession № NP_690593), кодируемого SEQ ID NO:6 (GenBank Accession № NM_152854), который также имеет сигнальную последовательность, представленную первыми 19 остатками. Полипептиды-предшественники этих двух изоформ CD40 человека имеют общие первые 165 остатков (т.е. остатки 1-165 SEQ ID NO:7 и SEQ ID NO:9). Полипептид-предшественник короткой изоформы (показанной в SEQ ID NO:7) кодируется вариантом транскрипта (SEQ ID NO:6), который лишен кодирующего сегмента, что приводит к смещению рамки трансляции; полученная изоформа CD40 содержит более короткий С-конец (остатки 166-203 SEQ ID NO:7), отличающийся от С-конца длинной изоформы CD40 (C-конца, показанного в остатках 166-277 SEQ ID NO:9). Для целей данного изобретения термин "CD40" или "CD40-антиген", "антиген CD40 клеточной поверхности" или "CD40-рецептор" включает в себя как короткую, так и длинную изоформы CD40.
Под термином "CD40-экспрессирующие клетки" здесь имеют в виду любые нормальные или злокачественные клетки, которые экспрессируют детектируемые уровни CD40-антигена. Способы детектирования CD40-антигена хорошо известны в данной области и включают, но не ограничиваются ими, ПЦР-способы, иммуногистохимию, проточную цитометрию, Вестерн-блоттинг, ELISA и т.п. Эти способы позволяют детектировать мРНК CD40, CD40-антиген и CD40-антиген клеточной поверхности. Предпочтительно CD40-экспрессирующие клетки являются клетками, которые экспрессируют детектируемые уровни CD40-антигена клеточной поверхности.
Под терминами "CD40-лиганд" или "CD40L" имеют в виду трансмембранный белок 32-33 кДа, который также существует в двух меньших биологически активных растворимых формах, 18 кДа и 31 кДа, соответственно (Graf et al. (1995) Eur. J. Immunol. 25:1749-1754; Mazzei et al. (1995) J. Biol. Chem. 270:7025-7028; Pietravalle et al. (1996) J. Biol. Chem. 271:5965-5967). CD40L человека известен также как CD154 или gp39.
Под термином "пациент-человек" имеют в виду человека, который поражен любым заболеванием или состоянием, ассоциированным с ростом неопластических В-клеток или имеет риск развития или рецидива этого заболевания или состояния.
Под термином "заболевание или состояние, ассоциированное с ростом неопластических В-клеток" имеют в виду любое заболевание или состояние (в том числе предраковые состояния), включающее неконтролируемый рост клеток В-клеточного направления дифференцировки. Такие заболевания и состояния включают, но не ограничиваются ими, острый лимфобластный лейкоз (ALL), острый миелогенный лейкоз (AML), хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL), пролимфоцитарный лейкоз (PLL), мелкоклеточный лимфоцитарный лейкоз (SLL), диффузный мелкоклеточный лимфоцитарный лейкоз (DSLL), диффузную крупноклеточную В-клеточную лимфому (DLBCL), злокачественный гистиоцитарный ретикулоэндотелиоз, неходжкинские лимфомы, болезнь Ходжкина, индуцированные вирусом Эпштейна-Барра (EBV) лимфомы, миеломы, такие как множественная миелома, макроглобулинемию Вальденстрема, болезнь тяжелых цепей, связанную со слизистой оболочкой лимфому лимфоидной ткани, моноцитоидную В-клеточную лимфому, селезеночную лимфому, лимфогрануломатоз, внутрисосудистый лимфоматоз, иммунобластные лимфомы, связанные со СПИДом лимфомы и т.п.
Способы по изобретению находят применение в лечении субъектов, имеющих неходжкинские лимфомы, связанные с аномальными пролиферацией или накоплением В-клеток. Для целей данного изобретения такие лимфомы будут называться в соответствии со схемой классификации (Working Formulation classification scheme), т.е. эти В-клеточные лимфомы будут классифицироваться как лимфомы низкой степени, промежуточной степени и высокой степени (см. "The Non-Hodgkin's Lymphoma Pathologic Classification Project", Cancer 49(1982):2112-2135). Таким образом, В-клеточные лимфомы низкой степени включают мелкоклеточные лимфоцитарные, фолликулярные мелкоклеточные дифференцированные и фолликулярные смешанно-клеточные дифференцированные и крупноклеточные лимфомы; лимфомы промежуточной степени включают фолликулярные крупноклеточные, диффузные мелкоклеточные дифференцированные, диффузные смешанные мелкоклеточные и крупноклеточные и диффузные крупноклеточные лимфомы; и лимфомы высокой степени включают крупноклеточные иммунобластные, лимфобластные и мелкоклеточные недифференцированные лимфомы типа Беркитта и не-Беркитта. Способы изобретения могут быть использованы для лечения В-клеточных лимфом низкой, промежуточной и высокой степени.
Способы по изобретению применимы в терапевтическом лечении В-клеточных лимфом, которые классифицируются в соответствии с системой классификации Revised European and American Lymphoma Classification (REAL). Такие В-клеточные лимфомы включают, но не ограничиваются ими, лимфомы, классифицируемые как В-клеточные неоплазмы-предшественники, такие как В-лимфобластные лейкоз/лимфома; периферические B-клеточные неоплазмы, включающие B-клеточный хронический лимфоцитарный лейкоз/мелкоклеточную лейкоцитарную лимфому, лимфоплазмацитоидную лимфому/иммуноцитому, лимфому клеток мантии (коры головного мозга) (MCL), фолликулярную лимфому (в том числе диффузные мелкоклеточные, диффузные смешанные мелкоклеточные и крупноклеточные и диффузные крупноклеточные лимфомы), В-клеточную лимфому маргинальной зоны (в том числе внеузловые (нефолликулярные), нодулярные и селезеночные типы, например, внеузловую (нефолликулярную) В-клеточную лимфому маргинальной зоны ассоциированной со слизистой оболочкой ткани), плазмацитому/миелому, диффузную крупноклеточную В-клеточную лимфому подтипа первичной медиастинальной (тимусовой) лимфомы, лимфому Беркитта и подобную лимфоме Беркитта В-клеточную лимфому высокой степени; и неклассифицируемые В-клеточные лимфомы низкой степени или высокой степени.
В способах по изобретению комбинированную терапию используют для обеспечения положительной терапевтической реакции в отношении заболевания или состояния. Под "положительной терапевтической реакцией" имеют в виду улучшение в этом заболевании или состоянии в результате терапевтической активности комбинированной терапии. То есть, могут наблюдаться антипролиферативное действие, предотвращение дополнительного разрастания опухоли, уменьшение размера опухоли, уменьшение количества неопластических клеток и/или уменьшение одного или нескольких симптомов, связанных с CD40-экспрессирующими клетками. Так, например, положительной терапевтической реакцией можно было бы назвать одно или несколько следующих изменений в заболевании: (1) уменьшение размера опухоли; (2) уменьшение количества неопластических клеток; (3) увеличение гибели неопластических клеток; (4) ингибирование выживания неопластических клеток; (4) ингибирование (т.е. замедление до некоторой степени, предпочтительно остановка) роста опухоли; (5) ингибирование (т.е. замедление до некоторой степени, предпочтительно остановка) инфильтрации неопластических клеток в периферические органы; (6) ингибирование (т.е. замедление до некоторой степени, предпочтительно остановка) метастазирования опухоли; (7) предотвращение дополнительных разрастаний опухоли; (8) увеличенная скорость выживания пациентов; и (9) некоторое ослабление одного или нескольких симптомов, ассоциированных с этим заболеванием или состоянием.
Положительные терапевтические реакции в любом конкретном заболевании или состоянии могут быть определены стандартизованными критериями реакции, специфическими в отношении заболевания или состояния. Реакция опухоли может оцениваться в отношении изменений в морфологии опухоли (например, отягощенности опухолью (общей массе опухолевой ткани в организме), размере опухоли и т.п.) с использованием способов скрининга, таких как сканирование магнитно-резонансного изображения (MRI), x-радиографическая томография, компьютерно-томографическое (CT) сканирование, сканирование кости, эндоскопия и взятие проб биопсии опухоли, включающее костно-мозговую аспирацию (BMA) и счет опухолевых клеток в кровотоке. Кроме этих положительных терапевтических реакций, субъект, подвергающийся терапии, может испытывать благоприятное действие улучшения в симптомах, ассоциированных с заболеванием. Так, что касается В-клеточных опухолей, субъект может испытывать уменьшение так называемых В-симптомов, т.е. ночной потливости, жара, потери массы и/или крапивницы. Что касается предраковых состояний, терапия с использованием анти-CD40-терапевтического агента может блокировать и/или продлевать время перед развитием соответствующего злокачественного состояния, например, развитием множественной миеломы в субъектах, страдающих от моноклональной гаммопатии неопределенного значения (MGUS).
Улучшение в этом заболевании может быть охарактеризовано как полная реакция. Под "полной реакцией" имеют в виду отсутствие клинически детектируемого заболевания с нормализацией любых ранее отклоняющихся от нормы радиографических исследований, костного мозга и цереброспинальной жидкости (CSF) или отклоняющегося от нормы моноклонального белка в случае миеломы. Такая реакция может сохраняться в течение по меньшей мере 4-8 недель или иногда 6-8 недель после лечения в соответствии со способами по настоящему изобретению. Альтернативно улучшение в этом заболевании может классифицироваться как частичная реакция. Под "частичной реакцией" имеют в виду по меньшей мере 50% уменьшение во всей измеримой отягощенности опухолью (т.е. количестве злокачественных клеток, присутствующих в субъекте, или измеримом объеме масс опухоли или количестве отклоняющегося от нормы моноклонального белка) при отсутствии новых повреждений, которое может сохраняться в течение 4-8 недель или 6-8 недель.
Способы и продукты по изобретению включают применение терапевтически или профилактически эффективных количеств анти-CD40-антитела и каждого из четырех компонентов CHOP. Под "эффективным количеством" или "терапевтически или профилактически эффективным количеством" имеют в виду количество терапевтического агента или химиотерапевтического агента, которое, при введении в виде части комбинированной терапии, вызывает положительную терапевтическую реакцию в отношении лечения пациента. Подходящие количества описаны более подробно в другом месте в данном документе.
Термин "опухоль", в данном контексте, относится ко всем случаям неопластического роста и пролиферации клеток, независимо от того, являются ли они злокачественными или доброкачественными, и ко всем предраковым и раковым клеткам и тканям. "Неопластические", в данном контексте, обозначает любой регулируемый нарушенным образом или нерегулируемый рост клеток, независимо от того, являются ли они злокачественными или доброкачественными клетками, приводящий к аномальному росту. Таким образом, термин "неопластические клетки" включает злокачественные и доброкачественные клетки, имеющие регулируемый нарушенным образом или нерегулируемый рост клеток. Термины "рак" и "раковое" относятся к физиологическому состоянию или описывают физиологическое состояние у млекопитающих, которое обычно характеризуется нерегулируемым ростом клеток.
"Лечение" определяется как применение комбинированной терапии к пациенту или к изолированной ткани из пациента или введение агентов комбинированной терапии пациенту или в изолированную ткань из пациента, где этот пациент имеет заболевание, симптом заболевания или предрасположение к заболеванию, где целью этого является лечение, исцеление, смягчение, облегчение симптомов, изменение, вылечивание или воздействие на заболевание, симптомы этого заболевания или предрасположение к этому заболеванию.
Способы по изобретению применимы, в частности, для лечения пациентов, которым ранее вводили другие онкотерапевтические агенты. Эти пациенты включают таких, которым ранее вводили другие агенты онкотерапевтического лечения в любой момент перед началом комбинированной терапии в соответствии с настоящим изобретением, например, в пределах 15 лет, в пределах 14 лет, в пределах 13 лет, в пределах 12 лет, в пределах 11 лет, в пределах 10 лет, в пределах 9 лет, в пределах 8 лет, в пределах 7 лет, в пределах 6 лет, в пределах 5 лет, в пределах 4 лет, в пределах 3 лет, в пределах 2 лет, в пределах 18 месяцев, в пределах 1 года, в пределах 6 месяцев, в пределах 2 месяцев, в пределах 6 недель, в пределах 1 месяца, в пределах 4 недель, в пределах 3 недель, в пределах 2 недель, в пределах 1 недели, в пределах 6 дней, в пределах 5 дней, в пределах 4 дней, в пределах 3 дней, в пределах 2 дней или в пределах 1 дня перед началом комбинированной терапии в соответствии с настоящим изобретением.
В частности, комбинированная терапия по изобретению может быть полезной для лечения пациента-человека, которому ранее вводили (i) только CHOP, (ii) только анти-CD40-антитело (такое как HCD122), (iii) только анти-CD20-антитело (такое как химерное анти-CD20-антитело ритуксимаб), или (iv) использовали комбинированную терапию с CHOP и анти-CD20-антителом (таким как ритуксимаб, где эту комбинированную терапию обычно называют R-CHOP).
Изобретение может быть особенно полезным для лечения заболеваний и состояний, которые не поддаются терапии другими онкотерапевтическими обработками. Таким образом, настоящее изобретение может быть полезным в лечении заболеваний или состояний, которые не поддаются терапии с использованием (i) только CHOP, (ii) только анти-CD40-антитела (такого как HCD122), (iii) только анти-CD20-антитела (такого как ритуксимаб) или (iv) комбинированной терапии с CHOP и анти-CD20-антителом (R-CHOP). "Не поддающимся лечению" называют конкретное заболевание или состояние, которое является резистентным (не поддающимся лечению) или не отвечающим на терапию конкретным онкотерапевтическим агентом. Заболевание или состояние может быть не отвечающим на лечение конкретным терапевтическим агентом либо с начала терапии этим конкретным терапевтическим агентом (т.е. не отвечающим на начальное подвергание действию этого терапевтического агента), либо в результате развития устойчивости к этому терапевтическому агенту либо на протяжении хода первого периода лечения этим терапевтическим агентом, либо во время последующего периода лечения этим терапевтическим агентом. Таким образом, изобретение обеспечивает способы, композиции, применения и наборы для лечения пациента-человека в отношении заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем указанное заболевание или состояние является не поддающимся онкотерапевтическому лечению, другому, чем комбинированная терапия по настоящему изобретению. Термин "онкотерапевтическое" обозначает любое лечение в отношении заболевания или состояния, включающее химиотерапию, пассивную иммунотерапию (лечение антителами), хирургию, лучевую терапию и их комбинации.
Изобретение может быть также особенно полезным для лечения пациентов, которые имели рецидив после терапии с использованием (i) только CHOP, (ii) только анти-CD40-антитела (такого как HCD122), (iii) только анти-CD20-антитела (такого как ритуксимаб) или (iv) комбинированной терапии с CHOP и анти-CD20-антителом (R-CHOP). Под термином "имевший рецидив" имеют в виду, что этот пациент обнаруживал полную или частичную реакцию на предыдущее онкотерапевтическое лечение, но затем имел рецидив этого заболевания или состояния. Таким образом, изобретение обеспечивает способы, композиции, применения и наборы для лечения пациента-человека в отношении заболевания или состояния, ассоциированного с ростом неопластических В-клеток, причем указанный пациент имел рецидив после терапии с использованием онкотерапевтического лечения, другого, чем комбинированная терапия по настоящему изобретению.
Комбинированная терапия по изобретению нацелена на проблемы, ассоциированные с терапией с использованием ритуксимаба (моноклонального антитела IDEC-C2B8 (Biogen Idee или Genentech), коммерчески доступного под товарным названием Rituxan®). Ритуксимаб является химерным моноклональным анти-CD20-антителом, содержащим IgG1 и константные области каппа человека с мышиными вариабельными областями, выделенными из мышиного моноклонального анти-CD20-антитела (Reffet al. (1994) Blood 83:435-445). Способы по настоящему изобретению делают возможным лечение пациентов, имеющих заболевание или состояние, ассоциированное с CD40-экспрессирующими B-клетками, которые могут в противном случае лечиться ритуксимабом или комбинированной терапией с ритуксимабом и химиотерапевтическими агентами (например, CHOP).
Таким образом, изобретение обеспечивает способы, композиции, применения и наборы для лечения пациента-человека в отношении заболевания или состояния, ассоциированного с ростом неопластических В-клеток, в случае, когда этому пациенту ранее вводили химерное анти-CD20-антитело ритуксимаб. Изобретение может быть полезным в лечении заболеваний или состояний, которые не поддаются терапии с использованием (i) одного ритуксимаба или (ii) комбинированной терапии с CHOP и ритуксимабом (R-CHOP). Изобретение может быть также полезным в лечении пациентов, которые имели рецидив после терапии с использованием (i) одного ритуксимаба или (ii) комбинированной терапии с CHOP и ритуксимабом (R-CHOP).
Пациентов, которых предварительно лечили ритуксимабом, можно отличать от других пациентов, например, с использованием медицинских карт пациентов или проведения подходящего теста (подходящих тестов) in vitro. Например, количество циркулирующих в кровотоке CD19+ B-клеток является истощенным в пациентах, лечившихся ритуксимабом, и количества циркулирующих CD19+ B-клеток может быть подвергнуто мониторингу с использованием подходящих способов, например, FACS (McLaughlin et al. (1998) J. Clin. Oncol. 16(8):2825-2833; Maloney et al. (1997) Blood 90(6):2188-2195).
Способы по изобретению включают применение анти-CD40-антител. Природные антитела являются обычно гетеротетрамерными гликопротеинами приблизительно 150000 дальтон, состоящими из двух идентичных легких (L) цепей и двух идентичных тяжелых (H) цепей. Каждая легкая цепь связана с тяжелой цепью одной ковалентной дисульфидной связью, тогда как число дисульфидных связей варьируется среди тяжелых цепей различных изотипов. Каждая тяжелая цепь и легкая цепь имеет также расположенные с регулярными интервалами межцепочечные дисульфидные мостики. Каждая тяжелая и легкая цепь имеет также расположенные с регулярными интервалами внутрицепочечные дисульфидные мостики. Каждая тяжелая цепь имеет на одном конце вариабельный домен (VH), за которым следует ряд константных доменов. Каждая легкая цепь имеет вариабельный домен на одном конце (VL) и константный домен на ее другом конце; константный домен легкой цепи выровнен с вариабельным доменом тяжелой цепи, а вариабельный домен легкой цепи выровнен с вариабельным доменом тяжелой цепи. Считается, что конкретные аминокислотные остатки образуют границу раздела между вариабельными доменами легкой цепи и тяжелой цепи. Термин "вариабельные" относится к тому факту, что некоторые части вариабельных доменов в сильной степени различаются в их последовательности среди антител. Эти вариабельные домены придают антигенсвязывающую специфичность. Константные домены не участвуют непосредственно в связывании антитела с антигеном, но обнаруживают различные эффекторные функции, такие как связывание Fc-рецептора (FcR), участие антитела в антителозависимой клеточной токсичности, инициации комплементзависимой цитотоксичности и дегрануляции мастоцитов (тучных клеток).
"Легкие цепи" антител из любых видов позвоночных могут быть отнесены к одному из двух явно отличающихся типов, называемых каппа (κ) и лямбда (λ), на основе аминокислотных последовательностей их константных доменов.
В зависимости от аминокислотной последовательности константного домена их "тяжелых цепей", антитела могут быть отнесены к различным классам. Имеются пять основных классов антител человека: IgA, IgD, IgE, IgG и IgM, и несколько из них могут быть дополнительно разделены на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные домены тяжелой цепи, которые соответствуют различным классам антител, называют альфа, дельта, эпсилон, гамма и мю, соответственно. Структуры субъединиц и трехмерные конфигурации различных классов антител хорошо известны. Разные изотипы имеют разные эффекторные функции. Например, изотипы IgG1 и IgG3 человека имеют ADCC-активность (активность антителозависимой клеточноопосредованной цитотоксичности). IgG1-антитела, в частности, IgG1-антитела человека, особенно полезны в способах по данному изобретению.
"Эффекторные клетки человека" являются лейкоцитами, которые экспрессируют один или несколько FcR и выполняют эффекторные функции. Предпочтительно, эти клетки экспрессируют по меньшей мере FcγRIII и выполняют эффекторную функцию антителозависимой клеточноопосредованной цитотоксичности (ADCC). Примеры лейкоцитов человека, которые опосредуют ADCC, включают мононуклеарные клетки периферической крови (PBMC), природные клетки-киллеры (NK-клетки), моноциты, макрофаги, эозинофилы и нейтрофилы, причем предпочтительными являются PBMC и NK-клетки. Антитела, которые имеют ADCC-активность, обычно являются антителами изотипов IgG1 или IgG3. Обратите внимание на то, что, наряду с выделением антител IgG1 и IgG3, ADCC-опосредующие антитела могут быть получены объединением вариабельной области из не-ADCC-антитела с константной областью изотипа IgG1 или IgG3.
Термины "Fc-рецептор" или "FcR" используются для описания рецептора, который связывает Fc-район антитела. Предпочтительным FcR является природная последовательность FcR человека. Кроме того, предпочтительным FcR является FcR, который связывает IgG-антитело (гамма-рецептор) и включает рецепторы подклассов FcγRI, FcγRII и FcγRIII, в том числе аллельные варианты и альтернативно сплайсированные формы этих рецепторов. FcγRII-рецепторы включают FcγRIIA ("активирующий рецептор") и FcγRIIB ("ингибирующий рецептор"), которые имеют сходные аминокислотные последовательности, которые различаются прежде всего в их цитоплазматических доменах. Активирующий рецептор FcγRIIA содержит иммунорецепторный мотив активации на основе тирозина (ITAM) в его цитоплазматическом домене. Ингибирующий рецептор FcγRIIB содержит иммунорецепторный мотив ингибирования (ITIM) в его цитоплазматическом домене (см. Daeron (1997) Annu. Rev. Immunol. 15:203-234). FcR обсуждаются в обзоре Ravetch and Kinet (1991) Annu. Rev. Immunol. 9:457-492 (1991); Capel et al. (1994) Immunomethods 4:25-34; и de Haas et al. (1995) J. Lab. Clin. Med. 126:330-341. Другие FcR, включающие FcR, которые будут идентифицированы в будущем, включены в приведенный здесь термин "FcR". Этот термин включает также неонатальный рецептор, FcRn, который является ответственным за перенос материнских IgG в плод (Guyer et al. (1976) J. Immunol. 117:587 and Kim et al. (1994) J. Immunol. 24:249 (1994)).
Термин "антитело" используется в настоящем документе в самом широком смысле и включает полностью собранные антитела, фрагменты антител, которые сохраняют способность специфически связываться с CD40-антигеном (например, Fab, F(ab')2, Fv и другие фрагменты), одноцепочечные антитела (scFv), диатела, биспецифические антитела, химерные антитела, гуманизированные антитела, полные антитела человека и т.п., и рекомбинантные пептиды, содержащие вышеописанные фрагменты. Термин "антитело" включает как поликлональные, так и моноклональные антитела.
В данном контексте "анти-CD40-антитело" включает любое антитело, которое специфически узнает антиген CD40. В некоторых вариантах осуществления анти-CD40-антитела для применения в способах по настоящему изобретению, в частности, моноклональные анти-CD40-антитела, проявляют сильную односайтовую аффинность связывания в отношении антигена CD40. Такие моноклональные антитела проявляют аффинность в отношении CD40 (KD) по меньшей мере 10-5 M, предпочтительно по меньшей мере 10-6 M, по меньшей мере 10-7 M, по меньшей мере 10-8 M, по меньшей мере 10-9 M, по меньшей мере 10-10 M, по меньшей мере 10-11 M или по меньшей мере 10-12 M при измерении с использованием стандартного анализа, такого как Biacore™. Анализ Biacore известен в данной области и подробности обеспечены в руководстве "BIAapplications handbook".
Под фразами "специфически узнает" или "специфически связывается с" имеется в виду, что это анти-CD40-антитело связывается с антигеном CD40 на поверхности В-клеток человека, но не связывается значимо с другими антигенами на поверхности В-клеток человека, такими как антиген CD20.
Анти-CD40-антитела для применения в способах по настоящему изобретению могут быть получены с использованием любого подходящего способа получения антител, известного квалифицированным в данной области специалистам.
Анти-CD40-антитело, используемое в способах по настоящему изобретению, может быть моноклональным антителом. Термин "моноклональное антитело" (и "mAb") относится в данном контексте к антителу, полученному из по существу гомогенной популяции антител, т.е. индивидуальные антитела, содержащие эту популяцию, являются идентичными, за исключением возможных природно-встречающихся мутаций, которые могут присутствовать в минорных количествах. Этот термин не ограничивается в отношении вида этого антитела и не требует получения этого антитела каким-либо конкретным способом. В противоположность препаратам поликлональных антител, которые обычно включают разные антитела, направленные против разных антигенных детерминант (эпитопов), каждое моноклональное антитело направлено против единственной детерминанты (единственного эпитопа) на этом антигене.
Термин "моноклональные", первоначально используемый в отношении антител, относился к антителам, продуцируемым единственной клональной линией иммунных клеток, в противоположность "поликлональным" антителам, которые, хотя все они узнавали один и тот же белок-мишень, продуцировались разными В-клетками и могли быть направлены на различные эпитопы на этом белке. В этом контексте слово "моноклональные" имеет в виду не какое-либо конкретное клеточное происхождение, а относится к любой популяции антител, все из которых имеют одну и ту же аминокислотную последовательность и узнают один и тот же эпитоп в одном и том же белке-мишени. Таким образом, моноклональное антитело может быть получено с использованием любой подходящей системы синтеза, включающей иммунные клетки, неиммунные клетки, бесклеточные системы и т.д. Это применение является обычным в данной области, например, таблицы данных продуктов для CDR-трансплантированного гуманизированного антитела Synagis™, экспрессируемых в линии клеток NSO мышиной миеломы, гуманизированное антитело Herceptin™, экспрессируемое в линии клеток СНО, и находящееся в фаговом дисплее антитело Humira™, экспрессируемое в линии клеток СНО, все называют продуктами, являющиимся моноклональными антителами.
Под термином "эпитоп" имеется в виду часть антигенной молекулы, к которой получено антитело и с которой это антитело будет связываться. Эпитопы могут содержать линейные аминокислотные остатки (т.е. остатки в пределах этого эпитопа расположены последовательно линейным образом), нелинейные аминокислотные остатки (называемые здесь "нелинейными эпитопами"; эти эпитопы не расположены последовательно) или как линейные, так и нелинейные аминокислотные остатки.
Моноклональные антитела могут быть получены гибридомным способом, впервые описанным Kohler et al. (1975) Nature 256:495, или могут быть получены способами рекомбинантных ДНК (см., например, патент США № 4816567). Моноклональные антитела могут быть также выделены из фаговых библиотек антител, полученных с использованием способов, описанных, например, в McCafferty et al. (1990) Nature 348:552-554 (1990) и патенте США № 5514548. Clackson et al. (1991) Nature 352:624-628 и Marks et al. (1991) J. Mol. Biol. 222:581-597 описывают выделение мышиных антител и антител человека, соответственно, с использованием фаговых библиотек. Последующие публикации описывают получение высокоаффинных (диапазона нМ) антител человека перетасовкой цепи (Marks et al. (1992) Bio/Technology 10:779-783), а также комбинаторной инфекцией и рекомбинацией in vivo в качестве стратегии конструирования очень больших фаговых библиотек (Waterhouse et al. (1993) Nucleic. Acids Res. 21:2265-2266). Таким образом, эти способы являются жизнеспособными альтернативами традиционным гибридомным способам получения моноклональных антител для выделения моноклональных антител.
Когда анти-CD40-антитела для применения в способах по изобретению должны быть получены с использованием способов рекомбинантных ДНК, ДНК, кодирующую эти моноклональные антитела с легкостью выделяют и секвенируют с использованием общепринятых процедур. После выделения эта ДНК может быть помещена в экспрессирующие векторы, которые затем трансфицируют в клетки-хозяева, такие как клетки E. coli, клетки COS обезьян, клетки яичника Китайского хомячка (CHO) или клетки миеломы, которые обычно не продуцируют белок иммуноглобулина, для получения синтеза моноклональных антител в этих рекомбинантных клетках-хозяевах. Обзорные статьи по рекомбинантной экспрессии в бактериях ДНК, кодирующей это антитело, включают Skerra et al. (1993) Curr. Opinion in Immunol. 5:256 и Phickthun (1992) Immunol. Revs. 130:151. Альтернативно антитело может быть получено в линии клеток, такой как линия клеток СНО, как описано в патентах США с номерами 5545403, 5545405 и 5998144. Вкратце, эту линию клеток трансфицируют векторами, способными экспрессировать легкую цепь и тяжелую цепь, соответственно. Посредством трансфекции этих двух белков на раздельных векторах получают химерные антитела. Другим преимуществом является гликозилирование млекопитающими этого антитела в клетках СНО. Клетки СНО являются предпочтительным источником рекомбинантных антител для применения в комбинированной терапии изобретения.
Термин "клетка-хозяин" в данном контексте относится к микроорганизму или эукариотической клетке или линии клеток, культивируемой в виде одноклеточной организации, которые могут быть или были использованы в качестве реципиента для рекомбинантного вектора или других полинуклеотидов-переносчиков и включают в себя потомство первоначальной клетки, которая была трансфицирована. Понятно, что потомство отдельной клетки необязательно может быть полностью идентичным в морфологии или в комплементе геномной или общей ДНК первоначального родителя вследствие природной, случайной или произвольной мутации.
Моноклональные антитела к CD40 известны в данной области. См., например, разделы, посвященные В-клеточному антигену, в McMichael, ed. (1987; 1989) Leukocyte Typing III and IV (Oxford University Press, New York); патенты США с номерами 5674492; 5874082; 5677165; 6056959; WO 00/63395; Международные публикации с номерами WO 02/28905 и WO 02/28904; Gordon et al. (1988) J. Immunol. 140:1425; Valle et al. (1989) Eur. J. Immunol. 19:1463; Clark et al. (1986) PNAS 83:4494; Paulie et al. (1989) J. Immunol. 142:590; Gordon et al. (1987) Eur. J. Immunol. 17:1535; Jabara et al. (1990) J. Exp. Med. 172:1861; Zhang et al. (1991) J. Immunol. 146:1836; Gascan et al., (1991) J. Immunol. 147:8; Banchereau et al. (1991) Clin. Immunol. Spectrum 3:8; и Banchereau et al. (1991) Science 251:70.
Как отмечалось выше, термин «антитело» в данном контексте включает химерные антитела. Под термином "химерные" подразумеваются антитела, которые наиболее предпочтительно получены с использованием способов рекомбинантных ДНК и которые содержат как компоненты человека (включающие компоненты иммунологически родственных видов, например, шимпанзе), так и компоненты не человека. Таким образом, константная область химерного антитела является наиболее предпочтительно по существу идентичной константной области природного антитела человека; вариабельная область химерного антитела произведена наиболее предпочтительно из источника не человека и имеет желаемую антигенную специфичность в отношении CD40. Этим источником, не являющимся человеком, может быть источник любого позвоночного животного, которое может быть использовано для генерирования антител к антигену CD40. Такие источники не человека включают, но не ограничиваются ими, грызунов (например, кролика, крысу, мышь и т.д.; см., например, патент США № 4816567) и приматов (не человека) (например, низшую узконосую обезьяну, мартышку и т.д.; см., например, патенты США с номерами 5750105 и 5756096). Фраза "константная область" относится к части белка молекулы антитела, которая придает эффекторные функции. В предыдущем исследовании, направленном на получение неиммуногенных антител для применения в терапии заболевания человека, мышиные константные области заменяли константными областями человека. Эти константные области рассматриваемых гуманизированных антител происходили из антител человека. Однако эти антитела могут индуцировать нежелательную и потенциально опасную иммунную реакцию в людях, и наблюдали потерю аффинности.
Как отмечалось выше, термин «антитело» в данном контексте включает гуманизированные антитела. Под термином "гуманизированные" подразумеваются антитела, которые содержат минимальную последовательность, происходящую из последовательностей антитела не человека. В большей части, гуманизированные антитела являются антителами человека (реципиентным антителом), в которых остатки из гипервариабельного района (также известного как определяющий комплементарность район или CDR) реципиента заменены остатками из гипервариабельного района вида не человека (донорского антитела), такого как мышь, крыса или примат (не человек), имеющими желаемую специфичность, аффинность и эффективность. Фраза "определяющий комплементарность район" относится к аминокислотным последовательностям, которые вместе определяют аффинность и специфичность связывания природного Fv-района связывающего сайта природного антитела. См., например, Chothia et al. (1987) J. Mol. Biol. 196:901-917; Kabat et al. (1991) U. S. Dept. of Health and Human Services, NIH Publication № 91-3242).
Гуманизация может выполняться согласно способу Winter and co-workers (Jones et al. (1986) Nature 321:522-525; Riechmann et al. (1988) Nature 332:323-327; Verhoeyen et al. (1988) Science 239:1534-1536) заменой CDR или последовательностями CDR грызуна или мутанта соответствующих последовательностей антитела человека. См. также патенты США с номерами 5225539; 5585089; 5693761; 5693762; 5859205. В некоторых случаях остатки в каркасных районах одной или нескольких вариабельных областей антитела человека заменены соответствующими остатками не человека (см., например, патенты США с номерами 5585089; 5693761; 5693762 и 6180370). Кроме того, гуманизированные антитела могут содержать остатки, которые не обнаруживаются в реципиентном антителе или в донорском антителе. Эти модификации производят для дополнительного улучшения эффективности антитела (например, для получения желаемой аффинности). Обычно гуманизированное антитело будет содержать по существу все из по меньшей мере одного и обычно двух вариабельных доменов, в которых все или по существу все из гипервариабельных районов соответствуют гипервариабельным районам антитела не человека и все или по существу все из каркасных районов являются последовательностью антитела человека. Гуманизированное антитело необязательно будет также содержать по меньшей мере часть константной области антитела (Fc), обычно часть константной области антитела человека. В отношении дополнительных подробностей см. Jones et al. (1986) Nature 331:522-525; Riechmann et al. (1988) Nature 332:323-329; и Presta (1992) Curr. Op. Struct. Biol. 2:593-596. Таким образом, такие "гуманизированные" антитела могут включать антитела, в которых по существу менее чем природный вариабельный домен человека был заменен соответствующей последовательностью из последовательности вида не человека. На практике, гуманизированные антитела являются обычно антителами человека, в которых несколько остатков CDR и, возможно, некоторые каркасные остатки заменены остатками из аналогичных сайтов в антителах грызунов. См., например, патенты США с номерами 5225539; 5585089; 5693761; 5693762; 5859205. См. также патент США № 6180370 и Международную публикацию № WO 01/27160, где описаны гуманизированные антитела и способы получения гуманизированных антител, имеющих улучшенную аффинность в отношении предварительно определенного антигена.
Гуманизированные анти-CD40-антитела могут быть также получены с использованием способа Human Engineering™ (Xoma Ltd., Berkeley, California), который был описан в качестве способа уменьшения иммуногенности при сохранении связывающей активности молекул антител (например, см. Studnicka et al. (1994) Protein Engineering 7:805-814 и патент США № 5766886).
Гуманизированные моноклональные анти-CD40-антитела включают такие антитела, как SGN-40 (Tai et al. (2004) Cancer Res. 64:2846-52; патент США № 6838261), которое является гуманизированной формой мышиного анти-CD40-антитела SGN-14 (Francisco et al. (2000) Cancer Res. 60:3225-31), и антитела, описанные в публикации заявки на патент США № 2004/0120948.
Данное изобретение может также использоваться на практике с использованием ксеногенных или модифицированных антител, продуцируемых клеткой-хозяином млекопитающего не человека, более конкретно трансгенной мышью, характеризующейся инактивированными локусами эндогенного иммуноглобулина (Ig). В таких трансгенных животных компетентные эндогенные гены для экспрессии легкой и тяжелой субъединиц иммуноглобулинов хозяина сделаны нефункциональными и заменены аналогичными локусами иммуноглобулина человека. Эти трансгенные животные продуцируют антитела человека по существу в отсутствие легкой или тяжелой субъединиц иммуноглобулина хозяина. См., например, патенты США с номерами 5877397 и 5939598.
Таким образом, в некоторых вариантах осуществления полные антитела человека против CD40 получают иммунизацией трансгенной мыши. Одна такая мышь получена с использованием технологии XenoMouse® (Abgenix; Fremont, California) и описана в патентах США с номерами 6075181, 6091001 и 6114598. Например, для получения антитела HCD122 мышей, трансгенных в отношении локуса тяжелой цепи IgG1 человека и локуса легкой цепи κ человека, иммунизировали клетками Sf9, экспрессирующими CD40 человека. Мыши могут быть также трансгенными в отношении других изотипов.
В некоторых вариантах осуществления анти-CD40-антитело будет иметь вариабельный домен легкой цепи (VL), который содержит последовательности CDR легкой цепи HCD122. Таким образом, в некоторых вариантах осуществления анти-CD40-антитело будет содержать вариабельный домен легкой цепи (VL), который содержит аминокислотную последовательность, показанную в SEQ ID NO:10, для CDR-L1, аминокислотную последовательность, показанную в SEQ ID NO:11, для CDR-L2, и аминокислотную последовательность, показанную в SEQ ID NO:12, для CDR-L3. В других вариантах осуществления анти-CD40-антитело будет иметь вариабельный домен тяжелой цепи (VH), который содержит последовательности CDR тяжелой цепи HCD122. Таким образом, в некоторых вариантах осуществления анти-CD40-антитело будет содержать вариабельный домен тяжелой цепи (VH), который содержит аминокислотную последовательность, показанную в SEQ ID NO:13, для CDR-Н1, аминокислотную последовательность, показанную в SEQ ID NO:14, для CDR-Н2, и аминокислотную последовательность, показанную в SEQ ID NO:15, для CDR-Н3.
В следующих вариантах осуществления анти-CD40-антитело будет иметь вариабельный домен легкой цепи (VL), который содержит последовательности CDR легкой цепи HCD122, и вариабельный домен тяжелой цепи (VH), который содержит последовательности CDR тяжелой цепи HCD122. Таким образом, в следующих вариантах осуществления анти-CD40-антитело будет содержать вариабельный домен легкой цепи (VL), который содержит аминокислотную последовательность, показанную в SEQ ID NO:10, для CDR-L1, аминокислотную последовательность, показанную в SEQ ID NO:11, для CDR-L2, и аминокислотную последовательность, показанную в SEQ ID NO:12, для CDR-L3, и вариабельный домен тяжелой цепи (VH), который содержит аминокислотную последовательность, показанную в SEQ ID NO:13, для CDR-Н1, аминокислотную последовательность, показанную в SEQ ID NO:14, для CDR-Н2, и аминокислотную последовательность, показанную в SEQ ID NO:15, для CDR-Н3.
Имеются различные схемы для определения остатков CDR в конкретном вариабельном домене антитела (например, см. Web-сайт, названный "bioinf.org.uk/abs", расположенный на World Wide Web (www)). Наиболее часто используемой является схема нумерации Кабата (Kabat et al. (1991) Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD). Согласно схеме нумерации Кабата эти CDR в вариабельном районе легкой цепи являются аминокислотами 24-34 (CDR-L1), 50-56 (CDR-L2) и 89-97 (CDR-L3), а эти CDR в вариабельном районе тяжелой цепи являются аминокислотами 31-35 (CDR-H1), 50-65 (CDR-H2) и 95-102 (CDR-H3). Другой хорошо известной схемой является схема нумерации Хотиа (Chothia & Lesk (1987) Mol. Biol. 196:901-917). По нумерации Хотиа эти остатки CDR в вариабельном районе легкой цепи являются аминокислотами 26-32 (CDR-L1), 50-52 (CDR-L2) и 91-96 (CDR-L3), а этими CDR в вариабельном районе тяжелой цепи являются аминокислоты 26-32 (CDR-H1), 53-55 (CDR-H2) и 96-101 (CDR-H3). С использованием одной или нескольких из этих известных схем квалифицированный в данной области специалист будет вполне способен определить, удовлетворяет ли конкретное антитело требованиям в отношении последовательности CDR легкой цепи и тяжелой цепи, указанных выше.
"Фрагменты антител" содержат часть природного антитела, предпочтительно антигенсвязывающий или вариабельный район природного антитела. Примеры фрагментов антител включают фрагменты Fab, F(ab')2 и Fv.
Под "Fab" имеют в виду моновалентный антигенсвязывающий фрагмент антитела, который содержит константный домен легкой цепи и первый константный домен (CH1) тяжелой цепи. Расщепление антител папаином продуцирует два идентичных Fab-фрагмента и оставшийся "Fc"-фрагмент, название которого отражает его способность легко кристаллизоваться. Под "F(ab')2" имеют в виду бивалентный антигенсвязывающий фрагмент антитела, который содержит как легкие цепи, так и часть тяжелых цепей, который сохраняет способность сшивания антигена. Обработка пепсином дает фрагмент F(ab')2. "Fv" является минимальным фрагментом антитела, который содержит полный сайт узнавания и связывания антигена. Этот район состоит из димера одного вариабельного района тяжелой цепи и одного вариабельного домена легкой цепи в прочной, нековалентной ассоциации. Именно в этой конфигурации эти три CDR каждого вариабельного домена взаимодействуют для определения антигенсвязывающего сайта на поверхности этого димера VH-VL. В совокупности эти шесть CDR придают антигенсвязывающую специфичность этому антителу. Однако даже единственный вариабельный домен (или половина Fv, содержащая только три CDR, специфических в отношении антигена) имеет способность узнавания и связывания антигена, хотя и при более низкой аффинности, чем весь связывающий сайт.
Изобретение может также использовать одноцепочечный Fv (scFv), который является полипептидом, содержащим домены VH и VL антитела, где эти домены присутствуют в одной полипептидной цепи (см., например, патенты США 4946778, 5260203, 5455030 и 5856456). Обычно полипептид scFv содержит полипептидный линкер между доменами VH и VL, который позволяет фрагменту scFv образовывать желаемую структуру для связывания антигена. В отношении обзора scFv см. Pluckthun (1994) в The Pharmacology of Monoclonal Antibodies, Vol.113, ed. Rosenburg and Moore (Springer-Verlag, New York), pp.269-315.
Фрагменты анти-CD40-антитела пригодны для применения в способах изобретения, пока они сохраняют способность связывания с антигеном CD40 на поверхности В-клеток человека. Такие фрагменты называют здесь "антигенсвязывающими" фрагментами. Такие фрагменты предпочтительно характеризуются функциональными свойствами, сходными со свойствами соответствующего полноразмерного антитела. Так, например, фрагмент полноразмерного анти-CD40-антитела предпочтительно будет способен специфически связывать антиген CD40 человека, экспрессируемый на поверхности клетки человека, и не содержит значимой агонистической активности, как описано в другом месте в данном документе. Фрагменты анти-CD40-антитела для применения в способах по изобретению, могут в некоторых случаях сохранять способность связывания одного или нескольких релевантных FcR.
Различные способы были разработаны для получения фрагментов антител. Традиционно, эти фрагменты получают посредством протеолитического расщепления интактных антител (см., например, Morimoto et al. (1992) Journal of Biochemical and Biophysical Methods 24:107-117 (1992) и Brennan et al. (1985) Science 229:81). Однако эти фрагменты могут быть теперь продуцированы непосредственно рекомбинантными клетками-хозяевами. Например, эти фрагменты антител могут быть теперь выделены из фаговых библиотек антител, обсуждаемых выше. Альтернативно Fab'-SH-фрагменты могут быть непосредственно извлечены из E. coli и химически связаны с образованием F(ab')2-фрагментов (Carter et al. (1992) Bio/Technology 10:163-167). В соответствии с другим подходом, F(ab')2-фрагменты могут быть выделены непосредственно из культуры рекомбинантных клеток-хозяев. Другие способы получения фрагментов антител будут очевидными для квалифицированного в данной области практика.
Анти-CD40-антитела, используемые в комбинированной терапии по изобретению, не содержат значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека. В некоторых вариантах осуществления их связывание с CD40 на поверхности В-клеток человека может приводить к ингибированию пролиферации и дифференцировки этих В-клеток. Анти-CD40-антитела, подходящие для применения в способах по настоящему изобретению, включают антитела, которые могут проявлять свойства агониста при объединении с рецептором на клетке и инициировать реакцию или активность, которая является сходной или той же самой активностью, инициируемой природным лигандом этого рецептора. Агонист CD40 индуцирует любую или все, но не только, из следующих реакций: пролиферацию и/или дифференцировку В-клеток; повышающую регуляцию межклеточной адгезии посредством таких молекул, как ICAM-1, E-селектин, VCAM и т.п.; секрецию провоспалительных цитокинов, таких как IL-1, IL-6, IL-8, IL-12, TNF и т.п.; трансдукцию сигнала через CD40-рецептор такими путями, как TRAF (например, TRAF2 и/или TRAF3), MAP-киназы, такие как NIK (NF-κB индуцирующая киназа), I-каппа B-киназы (IKK α/β), фактор транскрипции NF-κB, Ras и путь MEK/ERK, путь PI3K/AKT, путь P38 MAPK и т.п.; трансдукцию антиапоптотического сигнала такими молекулами, как XIAP, mcl-1, bcl-x и т.п.; генерирование B- и/или T-клеток памяти; продуцирование антител B-клетками; переключение изотипа В-клетками, повышающую регуляцию MHC класса II и CD80/86 и т.п.
Под "значимой" агонистической активностью имеют в виду агонистическую активность по меньшей мере на 30%, 35%, 40%, 45%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95% или 100% более высокую, чем агонистическая активность, индуцируемая отрицательным контролем, при измерении в анализе В-клеточной реакции. Предпочтительно значимой агонистической активностью является агонистическая активность, которая является по меньшей мере в 2 раза или по меньшей мере в 3 раза более высокой, чем агонистическая активность, индуцируемая отрицательным контролем, при измерении в анализе В-клеточной реакции. Так, например, когда представляющей интерес реакцией является пролиферация В-клеток, "значимой" агонистической реакцией была бы индукция уровня пролиферации В-клеток, который является по меньшей мере в 2 раза или по меньшей мере в 3 раза более высоким, чем уровень пролиферации В-клеток, индуцируемый отрицательным контролем. Вещество "свободное от значимой агонистической активности" проявляло бы агонистическую активность не более чем на приблизительно 25% более высокую, чем агонистическая активность, индуцируемая отрицательным контролем, предпочтительно не более чем приблизительно на 20% более высокую, на 15% более высокую, на 10% более высокую, на 5% более высокую, на 1% более высокую, на 0,5% более высокую или даже на не более чем приблизительно на 0,1% более высокую, чем агонистическая активность, индуцируемая отрицательным контролем, при измерении в анализе В-клеточной реакции.
"Антагонист" CD40 предотвращает или уменьшает индукцию любой из этих реакций, индуцируемых связыванием CD40-рецептора с лигандом-агонистом, в частности, CD40L. Этот антагонист может уменьшать индукцию реакции на связывание CD40L на 5%, 10%, 15%, 20%, 25%, 30%, 35%, предпочтительно 40%, 45%, 50%, 55%, 60%, более предпочтительно 70%, 80%, 85% и наиболее предпочтительно 90%, 95%, 99% или 100%.
Предпочтительные антитела и фрагменты для применения в способах по изобретению являются анти-CD40-антителами, которые не имеют значимой агонистической активности при связывании с антигеном CD40 на В-клетках человека и которые проявляют антагонистическую активность при связывании с антигеном CD40 на В-клетках человека. В некоторых вариантах осуществления анти-CD40-антитело не имеет значимой агонистической активности в одной реакции В-клеток. В других вариантах осуществления анти-CD40-антитело не имеет значимой агонистической активности в анализах более чем одной реакции В-клеток (например, пролиферации и дифференцировки или пролиферации, дифференцировки и продуцирования антител).
Способы измерения антагонистической активности анти-CD40-терапевтического агента (например, анти-CD40-антитела) известны в данной области и включают, но не ограничиваются ими, стандартные конкурентные анализы связывания, анализы мониторинга секреции антител В-клетками, анализы пролиферации В-клеток, Banchereau-подобные анализы пролиферации В-клеток, анализы T-клеток-хелперов на продуцирование антител, анализы костимуляции пролиферации В-клеток и анализы на повышающую регуляцию маркеров активации В-клеток. Релевантные анализы описаны, например, в патенте США № 6087329 и международных заявках на патент, опубликованных в виде WO 00/75348, WO 2005/044294, WO 2005/044304, WO 2005/044305, WO 2005/044306, WO 2005/044307, WO 2005/044854, WO 2005/044855, WO 2006/073443, WO 2006/125117, WO 2006/125143, WO 2007/053661 и WO 2007/053767.
Любые из анализов, известных в данной области, могут быть использованы для определения, действует ли анти-CD40-антитело как антагонист в одной или нескольких В-клеточных реакциях. В некоторых вариантах осуществления анти-CD40-антитело действует как антагонист по меньшей мере одной реакции В-клеток, выбранной из группы, состоящей из пролиферации В-клеток, дифференцировки В-клеток, продуцирования антител, межклеточной адгезии, генерирования В-клеток памяти, переключения изотипа, повышающей регуляции экспрессии на клеточной поверхности MHC класса II и CD80/86 и секреции провоспалительных цитокинов, таких как IL-8, IL-12 и TNF. Особый интерес представляют антагонистические анти-CD40-антитела, которые не имеют значимой агонистической активности в отношении пролиферации В-клеток при связывании с антигеном CD40 человека на поверхности В-клетки человека.
Анти-CD40-антитело может быть антагонистом пролиферации В-клеток, индуцированной растворимым или находящимся на клеточной поверхности лигандом CD40L, как измерено в анализе пролиферации В-клеток. Подходящие анализы пролиферации В-клеток известны в данной области. Подходящие анализы пролиферации В-клеток также описаны ниже. В некоторых вариантах осуществления антагонистическое анти-CD40-антитело стимулирует пролиферацию В-клеток на уровне, который является не более чем приблизительно на 25% более высоким, чем уровень пролиферации В-клеток, индуцируемый отрицательным контролем (т.е. по меньшей мере 75%-ое ингибирование), предпочтительно не более чем приблизительно на 20% более высоким, 15% более высоким, 10% более высоким, 5% более высоким, 1% более высоким, 0,5% более высоким или даже не более чем приблизительно на 0,1% более высоким, чем пролиферация В-клеток, индуцируемая отрицательным контролем.
В других вариантах осуществления анти-CD40-антитело является антагонистом пролиферации В-клеток, индуцируемой другим анти-CD40-антителом (например, анти-CD40-антителом S2C6; Kwekkeboom et al. (1993) Immunology 79:439-444), как измерено в анализе пролиферации В-клеток, и уровень пролиферации В-клеток, стимулируемой этим другим анти-CD40-антителом в присутствии антагонистического анти-CD40-антитела, равен не более чем 25% пролиферации В-клеток, индуцируемой этим другим анти-CD40-антителом в отсутствие этого антагонистического анти-CD40-антитела (т.е. по меньшей мере 75% ингибирование), предпочтительно не более чем приблизительно 20%, 15%, 10%, 5%, 1%, 0,5% или даже не более чем приблизительно 0,1% пролиферации В-клеток, индуцированной другим анти-CD40-антителом в отсутствие этого антагонистического анти-CD40-антитела.
В других вариантах осуществления анти-CD40-антитело является антагонистом пролиферации В-клеток, которая индуцируется клеточной линией EL4B5 (Kwekkeboom et al. (1993) Immunology 79:439-444), как измерено в анализе пролиферации В-клеток, и уровень пролиферации В-клеток, стимулируемой клеточной линией EL4B5, в присутствии антагонистического анти-CD40-антитела равен не более чем 25% пролиферации В-клеток, индуцируемой этой клеточной линией в отсутствие этого антагонистического анти-CD40-антитела (т.е. по меньшей мере 75% ингибирование), предпочтительно не более чем приблизительно 20%, 15%, 10%, 5%, 1%, 0,5% или даже не более чем приблизительно 0,1% пролиферации В-клеток, индуцированной этой клеточной линией в отсутствие этого антагонистического анти-CD40-антитела.
В других вариантах осуществления это анти-CD40-антитело является антагонистом индуцируемого Т-клетками человека продуцирования антител В-клетками человека, как измерено в анализе Т-клеток-хелперов на продуцирование антител В-клетками. В таком способе уровень продуцирования IgG-антитела, продуцирования IgM-антитела или продуцирования как IgG-, так и IgM-антитела В-клетками, стимулируемого Т-клетками в присутствии этого антагонистического анти-CD40-антитела, равен не более чем приблизительно 50% продуцирования соответствующего антитела В-клетками, стимулируемого Т-клетками в отсутствие этого антагонистического анти-CD40-антитела (т.е. по меньшей мере 75%-ое ингибирование), предпочтительно не более чем приблизительно 25%, 20%, 15%, 10%, 5%, 1%, 0,5%, или даже не более чем 0,1% продуцирования соответствующего антитела В-клетками, стимулируемыми Т-клетками в отсутствие этого антагонистического анти-CD40-антитела.
Например, могут быть использованы следующие анализы для оценивания антагонистической активности анти-CD40-антитела. Могут быть получены В-клетки человека для этих анализов, например, выделением из миндалин, полученных от индивидуумов, подвергнутых тонзилэктомии, в основном, как описано в De Groot et al. (1990) Lymphokine Research (1990) 9:321. Вкратце, эту ткань диспергируют лезвиями скальпелей, фагоцитарные клетки и NK-клетки истощают обработкой 5 мМ метиловым эфиром L-лейцина, и Т-клетки удаляют одним циклом розеткообразования с овечьими эритроцитами (SRBC), обработанными бромидом 2-аминоэтилизотиоурония. Чистота этих полученных препаратов В-лимфоцитов может быть проверена непосредственным иммунофлуоресцентным мечением анти-(CD20)-mAb В1 (Coulter Clone, Hialeah, FA) или анти-(CD3)-mAb OKT3 (Ortho, Raritan, NJ) и FITC-конъюгированным фрагментом F(ab')2 крысиного антитела против Ig мыши (Zymed, San Francisco, CA), и FACS-анализом.
Анализ пролиферации В-клеток
B-клетки (4×104 на лунку) культивируют в 200 мкл IMDM, дополненной 10% фетальной телячьей сывороткой, в плоскодонных 96-луночных микротитрационных планшетах. В-клетки стимулируют добавлением иммобилизованных анти-(IgM)-антител (Immunobeads; 5 мкг/мл; BioRad, Richmond, California). Если желательно, добавляют 100 Е/мл рекомбинантного IL-2. Варьирующиеся концентрации тестируемых моноклональных антител (mAb) добавляют в начале этих микрокультур, и пролиферацию оценивают в день 3 измерением включения (3Н)-тимидина после 18 часов импульсного мечения. Антагонистическое анти-CD40-антитело не костимулирует значимо пролиферацию В-клеток человека в присутствии иммобилизованного анти-IgM-антитела или в присутствии иммобилизованного анти-IgM-антитела и IL-2.
Banchereau-подобный анализ пролиферации В-клеток
Для тестирования способности моноклональных анти-CD40-антител стимулировать пролиферацию В-клеток в культуральной системе, аналогичной системе, описанной Banchereau et al. (1991) Science (1991) 251:70, используют клетки трансфектанта мыши 3T6, экспрессирующие аллельную форму HR FcγRII человека. B-клетки (2×104 на лунку) культивируют в плоскодонных микролунках в присутствии 1×104 клеток-трансфектантов (облученных 5000 Рад) в 200 мкл IMDM, дополненной 10% фетальной телячьей сывороткой и 100 Е/мл рекомбинантного IL-4. Перед добавлением В-клеток клеткам 3T6 давали прикрепляться к пластику культуры в течение приблизительно 5 часов. Анти-CD40-mAb добавляют в концентрациях, варьирующихся от 15 нг/мл до 2000 нг/мл, и пролиферацию В-клеток оценивают измерением включения тимидина в день 7, после 18 часов импульсного мечения [3Н]-тимидином.
Ингибирование S2C6-стимулированной пролиферации В-клеток с использованием антагонистических анти-CD40-антител
Антагонистические моноклональные анти-CD40-антитела (mAb) могут также характеризоваться по их способности ингибировать стимуляцию пролиферации В-клеток анти-CD40-антителом, таким как S2C6 (также известным как SGN-14, которое, как сообщалось, является агонистом CD40-стимуляции пролиферации нормальных В-клеток; Francisco et al. (2000) Cancer Res. 60:3225-3231), с использованием анализа пролиферации В-клеток, описанного выше. В-клетки миндалин человека (4×104 на лунку) культивируют в 200 мкл в микролунках в присутствии анти-IgM, связанного с гранулами Сефарозы (5 мкг/мл), и анти-CD40-mAb S2C6 (1,25 мкг/мл). Добавляют варьирующиеся концентрации представляющего интерес анти-CD40-mAb, и включение [3Н]-тимидина оценивают спустя 3 дня. В качестве контроля может быть добавлено анти-(глюкоцереброзидаза)-mAb 8E4 в сходных концентрациях, Barneveld et al. (1983) Eur. J. Biochem. 134:585. Антагонистическое анти-CD40-антитело может ингибировать костимуляцию анти-IgM-индуцированной пролиферации В-клеток антителом mAb S2C6, например, по меньшей мере на 75% или более (т.е. S2C6-стимулированная пролиферация в присутствии антагонистического анти-CD40-антитела составляет не более чем 25% стимуляции, наблюдаемой в отсутствие антагонистического анти-CD40-антитела). В отличие от этого, не наблюдали значимого ингибирования с эквивалентными количествами постороннего mAb 8Е4, направленного на β-глюкоцереброзидазу. Barneveld et al., выше. Такой результат показывает, что анти-CD40-mAb не доставляет стимулирующие сигналы для пролиферации В-клеток человека, а, напротив, может ингибировать стимулирующие сигналы, вызываемые запуском CD40 другим mAb.
Анализ активации В-клеток с использованием клеток EL4B5
Zubler et al. (1985) J. Immunol. (1985) 134:3662 наблюдали, что мутантный субклон линии EL-4 тимомы мыши, известный как EL4B5, мог сильно стимулировать как В-клетки мышиного происхождения, так и происходящие из человека В-клетки в отношении пролиферации и дифференцировки в секретирующие иммуноглобулин плазматические клетки in vitro. Было обнаружено, что эта активация была антиген-независимой и не рестриктированной по антигенам МНС. Для оптимальной стимуляции В-клеток человека было необходимо присутствие супернатанта от активированных Т-клеток человека, но В-клеточная реакция также имела место, когда клетки EL4B5 предварительно активировали форбол-12-миристат-13-ацетатом (РМА) или IL-1. Zubler et al. (1987) Immunological Reviews 99:281; и Zhang et al. (1990) J. Immunol. 144:2955. Активация В-клеток в этой культуральной системе является эффективной: эксперименты с серийным разведением показали, что большинство В-клеток человека могут активироваться в отношении пролиферации и дифференцировки в секретирующие антитело клетки. Wen et al. (1987) Eur. J. Immunol. 17:887.
В-клетки (1000 на лунку) культивируют вместе с облученными (5000 Рад) клетками EL4B5 (5×104 на лунку) в плоскодонных микротитрационных планшетах в 200 мкл IMDM, дополненной 10% инактивированной нагреванием фетальной телячьей сывороткой, 5 нг/мл форбол-12-миристат-13-ацетата и 5% супернатантом Т-клеток человека. mAb добавляют при варьирующихся концентрациях в начале этих культур, и включение тимидина оценивают в день 6 после 18-часового импульсного мечения [3H]-тимидином. Для получения супернатанта Т-клеток очищенные Т-клетки культивируют при плотности 106/мл в течение 36 часов в присутствии 1 мкг/мл PHA и 10 нг/мл PMA. Wen et al. (1987) Eur. J. Immunol. (1987) 17:887. Супернатант T-клеток получают центрифугированием и хранят при -20°C. Тестируют эффективность Т-клеточных супернатантов в усилении пролиферации В-клеток человека в культурах клеток EL4B5-B-клеток, и наиболее эффективные супернатанты объединяют для применения в экспериментах. При оценивании действия анти-CD40-антитела на индуцированную EL4B5 пролиферацию В-клеток человека, в качестве контроля может быть добавлено моноклональное антитело, такое как MOPC-141 (IgG2b).
Анализ с использованием Т-клеток-хелперов человека на продуцирование антител В-клетками
Антагонистическое анти-CD40-антитело может функционировать в качестве антагониста продуцирования антител В-клетками. Анти-CD40-антитело может быть тестировано на этот тип антагонистической активности оцениванием способности этого антитела ингибировать продуцирование антител В-клетками, которые были стимулированы контакт-зависимым образом активированными Т-клетками в анализе Т-клеток-хелперов. В этом способе 96-луночные планшеты для культуры ткани покрывают разведением 1:500 асцитной жидкости анти-CD3-mAb CLB-T3/3 (CLB, Amsterdam, The Netherlands). Как указано, добавляют костимуляторные mAb: анти-CD2-mAb CLB-T11.1/1 и CLB-T11.2/1 (CLB, Amsterdam, The Netherlands), как асциты 1:1000, так и анти-CD28-mAb CLB-28/1 (CLB, Amsterdam, The Netherlands). Затем добавляют Т-клетки миндалин (облученные, 3000 Рад; 105 на лунку), В-клетки миндалин (104 на клетку) и rIL-2 (20 Е/мл). Конечный объем каждой культуры равен 200 мкл. Спустя 8 дней клетки отделяют, и не содержащий клеток супернатант собирают. Концентрации IgM и IgG в (разведенных) пробах определяют при помощи ELISA, как описано ниже.
В одном варианте осуществления В-клетки миндалин человека (104 на лунку) культивируют вместе с облученными очищенными Т-клетками (3000 Рад, 105 на лунку) в 96-луночных планшетах, покрытых анти-CD40-антителом и с различными или без различных mAb для костимуляции этих Т-клеток. Спустя 8 дней культивирования супернатанты собирают для определения продуцирования антител В-клетками. Продуцирование антител этими В-клетками оценивают при помощи анализа ELISA, описанного ниже. Представляющее интерес анти-CD40-антитело добавляют в варьирующихся концентрациях от начала этих культур. В качестве контроля может быть добавлено антитело mAb MOPC-141.
Антагонистическое анти-CD40-антитело может ингибировать продуцирование IgG- и IgM-антител В-клеток, стимулированных Т-клетками человека, по меньшей мере на 50% или более (т.е. индуцированное Т-клетками продуцирование антител В-клетками в присутствии анти-CD40-антитела равно не более чем 50% продуцирования, наблюдаемого в отсутствие этого антагонистического анти-CD40-антитела). В отличие от этого, контрольное антитело, такое как MOPC-141, не оказывает значимого действия на индуцированное Т-клетками продуцирование антител В-клетками.
Анализ ELISA для количественного определения антител
Концентрации IgM и IgG человека оценивают при помощи ELISA. 96-луночные планшеты ELISA покрывают 4 мкг/мл антитела MH 16-01 против человеческого IgG (CLB, Amsterdam, The Netherlands) или 1,2 мкг/мл мышиного mAb 4102 против IgM человека (Tago, Burlingame, CA) в 0,05 M карбонатном буфере (pH=9,6), инкубированием в течение 16 часов при 4°C. Планшеты промывают 3 раза ЗФР-0,05% Твин-20 (ЗФР-Твин) и насыщают БСА в течение 1 часа. После 2 промывок планшеты инкубируют в течение 1 часа при 37°С с различными разведениями тест-проб. После 3 промывок связанный Ig детектируют инкубированием в течение 1 часа при 37°С с 1 мкг/мл меченного пероксидазой мышиного mAb МН 16-01 против IgG человека (CLB) или мышиного mAb МН 15-01 против IgM человека (CLB). Планшеты промывают 4 раза и связанную пероксидазную активность выявляют добавлением О-фенилендиамина в качестве субстрата. Для создания калибровочной кривой для каждого анализа используют стандартную сыворотку человека (H00, CLB).
Антагонистические анти-CD40-антитела известны в данной области. См., например, анти-CD40-антитело человека, продуцируемое гибридомой, названное F4-465, описанное в публикациях заявок на патент США с номерами 20020142358 и 20030059427. F4-465 получали из мыши HAC (Kuroiwa et al. (2000) Nature Biotech. 10:1086 (2000)), и, следовательно, оно экспрессирует легкую цепь лямбда человека.
Кроме антагонистической активности, анти-CD40-антитело для применения в способах по настоящему изобретению будет предпочтительно иметь другой механизм действия против клетки-мишени. Анти-CD40-антитело будет предпочтительно иметь ADCC-активность.
Особый интерес для настоящего изобретения представляют анти-CD40-антитела, которые имеют общие характеристики связывания с HCD122 (продуцируемого гибридомной клеточной линией, депонированной ATCC (Американской Коллекцией Типовых культур; 10801 University Blvd., Manassas, Virginia 20110-2209 (USA)) 17 сентября, 2003 г., под номером депозита PTA-5543). Такие антитела включают, но не ограничиваются ими:
a) моноклональное антитело HCD122, продуцируемое гибридомной клеточной линией, депонированной ATCC под номером депозита № PTA-5543;
b) антитело, содержащее аминокислотную последовательность, выбранную из группы, состоящей из последовательности, показанной в SEQ ID NO:2, последовательности, показанной в SEQ ID NO:4, последовательности, показанной в SEQ ID NO:5, обеих последовательностей, показанных в SEQ ID NO:2 и SEQ ID NO:4, и обеих последовательностей, показанных в SEQ ID NO:2 и SEQ ID NO:5;
c) антитело, содержащее аминокислотную последовательность, выбранную из группы, состоящей из последовательности, показанной в SEQ ID NO:17, последовательности, показанной в SEQ ID NO:19, последовательности, показанной в SEQ ID NO:20, обеих последовательностей, показанных в SEQ ID NO:17 и SEQ ID NO:19, и обеих последовательностей, показанных в SEQ ID NO:17 и SEQ ID NO:20;
d) антитело, содержащее аминокислотную последовательность, выбранную из группы, состоящей из последовательности, показанной в SEQ ID NO:16, последовательности, показанной в SEQ ID NO:18, и обеих последовательностей, показанных в SEQ ID NO:16 и SEQ ID NO:18;
e) антитело, имеющее аминокислотную последовательность, кодируемую молекулой нуклеиновой кислоты, содержащей нуклеотидную последовательность, выбранную из группы, состоящей из последовательности, показанной в SEQ ID NO:1, последовательности, показанной в SEQ ID NO:3, и обеих последовательностей, показанных в SEQ ID NO:1 и SEQ ID NO:3;
f) антитело, имеющее вариабельный домен легкой цепи (VL), который содержит аминокислотную последовательность, показанную в SEQ ID NO:10, для CDR-L1, аминокислотную последовательность, показанную в SEQ ID NO:11, для CDR-L2, и аминокислотную последовательность, показанную в SEQ ID NO:12, для CDR-L3;
g) антитело, имеющее вариабельный домен тяжелой цепи (VH), который содержит аминокислотную последовательность, показанную в SEQ ID NO:13, для CDR-Н1, аминокислотную последовательность, показанную в SEQ ID NO:14, для CDR-Н2, и аминокислотную последовательность, показанную в SEQ ID NO:15, для CDR-Н3;
h) антитело, имеющее вариабельный домен легкой цепи (VL), который содержит аминокислотную последовательность, показанную в SEQ ID NO:10, для CDR-L1, аминокислотную последовательность, показанную в SEQ ID NO:11, для CDR-L2, и аминокислотную последовательность, показанную в SEQ ID NO:12, для CDR-L3, и имеющее вариабельный домен тяжелой цепи (VH), который содержит аминокислотную последовательность, показанную в SEQ ID NO:13, для CDR-H1, аминокислотную последовательность, показанную в SEQ ID NO:14, для CDR-H2, и аминокислотную последовательность, показанную в SEQ ID NO:15, для CDR-H3;
i) антитело, которое связывает домен 2 антигена CD40 человека;
j) антитело, которое связывается с эпитопом CD40, способным связывать моноклональное антитело HCD122;
k) антитело, которое связывается с эпитопом, содержащим остатки 82-87 последовательности CD40 человека, показанной в SEQ ID NO:7 или SEQ ID NO:9; и
l) антитело, которое конкурирует с моноклональным антителом HCD122 в конкурентном анализе связывания.
Анти-CD40-антитело, полученное из клетки СНО, содержащей один или несколько экспрессирующих векторов, кодирующих это антитело, может быть использовано в способах по настоящему изобретению.
Моноклональное антитело HCD122, продуцируемое гибридомной клеточной линией, депонированной ATCC под номером депозита PTA-5543, является особенно предпочтительным для применения в способах по изобретению.
Моноклональное антитело HCD122 связывает домен 2 антигена CD40 человека, тогда как было обнаружено, что более ранние анти-CD40-антитела, имеющие антагонистические свойства, связываются с другими доменами CD40 человека.
Моноклональное антитело HCD122 связывает растворимый CD40 в анализах типа ELISA, предотвращает связывание CD40-лиганда с CD40 клеточной поверхности и вытесняет ранее связанный CD40-лиганд, как определено проточными цитометрическими анализами. При тестировании in vitro на действия на пролиферацию В-клеток от здоровых субъектов-людей, HCD122 действует в качестве антагонистического анти-CD40-антитела. Кроме того, HCD122 не индуцирует сильную пролиферацию лимфоцитов человека от здоровых субъектов. Антитело способно убивать CD40-экспрессирующие клетки-мишени посредством антителозависимой клеточной цитотоксичности (ADCC). Связывающая аффинность HCD122 в отношении CD40 человека равна 5×10-10 M, как определено при помощи анализа Biacore™.
Нуклеотидная и аминокислотная последовательности антитела HCD122 известны (например, см. WO 2005/044854). Кроме того, мышиная гибридомная линия 153.8E2.D10.D6.12.12 (CMCC#12056), которая экспрессирует антитело HCD122, была депонирована Американской Коллекцией Типовых Культур [ATCC; 10801 University Blvd., Manassas, Virginia 20110-2209 (USA)] 17 сентября 2003 года под номером депозита PTA-5543.
Полная последовательность легкой цепи HCD122 представлена в SEQ ID NO:2, которая включает лидерную последовательность (остатки 1-20 SEQ ID NO:2), вариабельный район (остатки 21-132 SEQ ID NO:2) и константный район (остатки 133-239 SEQ ID NO:2). Полная последовательность тяжелой цепи HCD122 представлена в SEQ ID NO:4, которая включает лидерную последовательность (остатки 1-19 SEQ ID NO:4), вариабельный район (остатки 20-139 SEQ ID NO:4) и константный район (остатки 140-469 SEQ ID NO:4). Полная последовательность для варианта HCD122 представлена в SEQ ID NO:5, которая включает лидерную последовательность (остатки 1-19 SEQ ID NO:5), вариабельный район (остатки 20-139 SEQ ID NO:5) и константные районы (остатки 140-469 SEQ ID NO:5). Этот вариант отличается от HCD122 тем, что он содержит замену остатком серина остатка аланина в положении 153 SEQ ID NO:4, которое находится в этих константных районах. Нуклеотидные последовательности, кодирующие легкую и тяжелую цепи HCD122, представлены в SEQ ID NO:1 (кодирующей последовательности легкой цепи HCD122) и SEQ ID NO:3 (кодирующей последовательности тяжелой цепи HCD122).
Аминокислотная последовательность для вариабельного района легкой цепи HCD122 без лидерной последовательности (т.е. остатки 21-132 SEQ ID NO:2) представлена в SEQ ID NO:16. Аминокислотная последовательность для вариабельного и константного районов легкой цепи HCD122 без лидерной последовательности (т.е. остатки 21-239 SEQ ID NO:2) представлена в SEQ ID NO:17. Аминокислотная последовательность для вариабельного района тяжелой цепи HCD122 без лидерной последовательности (т.е. остатки 20-139 SEQ ID NO:4) представлена в SEQ ID NO:18. Аминокислотная последовательность для вариабельного и константного районов тяжелой цепи HCD122 без лидерной последовательности (т.е. остатки 20-469 SEQ ID NO:4) представлена в SEQ ID NO:19. Аминокислотная последовательность для вариабельного и константного районов варианта тяжелой цепи HCD122 (т.е. остатки 20-469 SEQ ID NO:5) представлена в SEQ ID NO:20.
Анти-CD40-антитела для применения в способах по данному изобретению включают антитела, отличающиеся от моноклонального антитела HCD122, но сохраняющие CDR, и антитела с одной или несколькими добавлениями, делециями или заменами аминокислот. HCD122 является полностью человеческим антителом, но может быть дополнительно деиммунизировано, если желательно. Деиммунизированные анти-CD40-антитела могут быть получены с использованием известных способов, например, описанных в WO 98/52976 и WO 00/34317. Таким образом, остатки в анти-CD40-антителах могут быть модифицированы так, что они делают эти антитела менее иммуногенными для людей при сохранении их терапевтической активности.
Любое известное антитело, имеющее представляющую интерес специфичность связывания, может иметь вариации последовательности, получаемые с использованием способов, например, описанных в EP 0983303, WO 00/34317 и WO 98/52976. Например, было показано, что последовательности в CDR могут вызывать связывание антитела с МНС класса II и запускать нежелательную реакцию Т-клеток-хелперов в некоторых пациентах. Консервативная замена может позволить этому антителу сохранять связывающую активность, но терять его способность запускать нежелательную реакцию Т-клеток. Любые такие консервативные или неконсервативные замены могут быть произведены с использованием общепринятых в данной области способом, таких как способы, указанные здесь в другом месте, и полученные антитела могут быть также использованы в способах по данному изобретению. Эти вариантные антитела могут быть рутинно тестированы на конкретную активность, например, на антагонистическую активность, аффинность и специфичность, с использованием описанных здесь способов.
Например, варианты аминокислотных последовательностей антагонистического анти-CD40-антитела, например, моноклонального антитела HCD122, могут быть получены посредством мутаций в клонированной ДНК-последовательности, кодирующей представляющее интерес антитело. Способы мутагенеза и изменений нуклеотидных последовательностей хорошо известны в данной области. См., например, Walker and Gaastra, eds. (1983) Techniques in Molecular Biology (MacMillan Publishing Company, New York); Kunkel (1985) Proc. Natl. Acad. Sci USA 82:488-492; Kunkel et al. (1987) Methods Enzymol. 154:367-382; Sambrook et al. (1989) Molecular Cloning: A Laboratory Manual (Cold Spring Harbor, New York); U.S. Patent № 4873192; и цитируемые в них ссылки. Руководство в отношении аминокислотных замен, которые не влияют на биологическую активность представляющего интерес полипептида, может быть найдено в модели Dayhoff et al. (1978) in Atlas of Protein Sequence and Structure (Natl. Biomed. Res. Found., Washington, D.C). Консервативные замены, такие как замена одной аминокислоты другой, имеющей сходные свойства, могут быть предпочтительными. Примеры консервативных замен включают, но не ограничиваются ими, Gly⇔Ala, Val⇔Ile⇔Leu, Asp⇔Glu, Lys⇔Arg, Asn⇔Gln и Phe⇔Trp⇔Tyr.
В конструировании вариантов представляющего интерес антитела, например, представляющего интерес полипептида анти-CD40-антитела, модификации могут быть произведены таким образом, что варианты продолжают иметь желаемую активность, т.е. сходную активность связывания, и в случае антагонистических анти-CD40-антител способны специфически связываться с антигеном CD40 человека, экспрессируемым на поверхности клетки человека, и не содержать значимой агонистической активности, но проявлять антагонистическую активность при связывании с антигеном CD40 на CD40-экспрессирующей клетке человека. Очевидно, любые мутации, произведенные в ДНК, кодирующей этот вариантный полипептид, не должны помещать эту последовательность вне рамки считывания и предпочтительно не будут создавать комплементарные районы, которые могли бы продуцировать вторичную структуру мРНК (например, см. EP 0075444).
Кроме того, константный район антитела, например, антагонистического анти-CD40-антитела, может быть мутирован таким образом, что он изменяет эффекторную функцию несколькими путями. Например, см. патент США № 6737056 B1 и публикацию заявки на патент США № 2004/0132101 A1, которые описывают мутации Fc, которые оптимизируют связывание антитела с Fc-рецепторами.
Предпочтительно варианты ссылочного антитела, например, антагонистическое анти-CD40-антитело, имеют аминокислотные последовательности, которые имеют по меньшей мере 70% или 75% идентичность последовательности, предпочтительно по меньшей мере 80% или 85% идентичность последовательности, более предпочтительно по меньшей мере 90%, 91%, 92%, 93%, 94% или 95% идентичность последовательности с аминокислотной последовательностью для молекулы ссылочного антитела, например, молекулы антагонистического анти-CD40-антитела, например, описанного здесь моноклонального антитела HCD122. Более предпочтительно, эти молекулы разделяют по меньшей мере 96%, 97%, 98% или 99% идентичность последовательности. Для целей данного изобретения процентную идентичность последовательности определяют с использованием алгоритма поиска гомологии Смита-Уотермана, использующего поиск аффинного гэпа с пенальти (штрафом) 12 за открывание гэпа 12 и пенальти (штрафом) 2 за удлинение гэпа, BLOSUM матрицы 62. Алгоритм поиска гомологии Смита-Уотермана описан в Smith and Waterman (1981) Adv. Appl. Math. 2:482-489. Вариант может, например, отличаться от ссылочного антитела, например, от антагонистического анти-CD40-антитела, всего лишь 1-15 аминокислотными остатками, всего лишь 1-10 аминокислотными остатками, например, 6-10 аминокислотными остатками, всего лишь 5, всего лишь 4, 3, 2 остатками или даже 1 аминокислотным остатком.
Что касается оптимального сопоставления двух аминокислотных последовательностей, сегмент смежных аминокислотных остатков вариантной аминокислотной последовательности может иметь дополнительные аминокислотные остатки или делетированные аминокислотные остатки. Сегмент смежных аминокислотных остатков, используемый для сравнения со ссылочной аминокислотной последовательностью, будет включать по меньшей мере 20 смежных аминокислотных остатков и может иметь 30, 40, 50 или более аминокислотных остатков. Могут быть произведены корректирования в отношении идентичности последовательности, ассоциированные с консервативными заменами остатков или гэпами (см. алгоритм поиска гомологии Смита-Уотремана).
Точная химическая структура антитела, способного специфически связывать CD40 и сохранять антагонистическую активность, в частности, при связывании с антигеном CD40 на злокачественных В-клетках, зависит от ряда факторов. Когда в молекуле антитела присутствуют ионизируемые аминогруппы и карбоксильные группы, конкретный полипептид может быть получен в виде кислой или щелочной соли или в нейтральной форме. Все такие препараты, которые сохраняют их биологическую активность при помещении в подходящие условия окружающей среды, включены в определение антагонистических анти-CD40-антител, в данном контексте. Далее, первичная аминокислотная последовательность полипептида может быть увеличена дериватизацией с использованием сахарных частей (гликозилированием) или другими дополнительными молекулами, такими как липиды, фосфатные, ацетильные группы и т.п. Она может быть увеличена конъюгацией с сахаридами. Определенные аспекты такого увеличения выполняются посредством систем посттрансляционного процессинга продуцирующего хозяина; другие такие модификации могут вводиться in vitro. В любом событии такие модификации включены в определение анти-CD40-антитела, используемого в данном описании. Предполагается, что такие модификации могут количественно или качественно влиять на активность, либо увеличением, либо уменьшением активности этого полипептида, в различных анализах. Кроме того, отдельные аминокислотные остатки в цепи могут быть модифицированы окислением, восстановлением или другой дериватизацией, и эти полипептиды могут расщепляться для получения фрагментов, которые сохраняют активность.
Эта область обеспечивает значительное количество рекомендаций в отношении получения и применения вариантов антител. В получении вариантов анти-CD40-антител специалист в данной области может легко определить, какие модификации в отношении нуклеотидной или аминокислотной последовательности природного белка будут приводить к варианту, который является подходящим для применения в качестве терапевтически активного компонента фармацевтической композиции, используемой в способах по настоящему изобретению.
Анти-CD40-антитело для применения в способах по изобретению предпочтительно имеет по меньшей мере одну из следующих биологических активностей in vitro и/или in vivo: ингибирование секреции антител нормальными периферическими В-клетками человека, стимулируемыми Т-клетками; ингибирование выживания и/или пролиферации нормальных В-клеток, стимулируемых CD40L-экспрессирующими клетками или растворимым лигандом CD40 (sCD40L); ингибирование выживания и/или пролиферации нормальных периферических В-клеток человека, стимулируемых Т-клетками Jurkat; ингибирование "выживания" анти-апоптотических внутриклеточных сигналов в любой клетке, стимулируемой sCD40L или твердофазным CD40L; и ингибирование трансдукции сигнала CD40 в любой клетке после лигирования с sCD40L или твердофазным CD40L, делецию, индукцию анергии (иммунологическую толерантность) и/или индукцию толерантности CD40-несущих клеток-мишеней или клеток, несущих когнатные лиганды, к CD40, в том числе, но не только, к Т-клеткам и В-клеткам, индукцию экспансии или активации регуляторных CD4+CD25+-T-клеток (см., например, специфическое в отношении донорского аллоантигена отторжение ткани посредством CD40-CD40L-интерференции, van Maurik et al. (2002) J. Immunol. 169:5401-5404), цитотоксичность, вызываемую любым механизмом (включающим, но не ограничивающимся ими, антителозависимую клеточноопосредованную цитотоксичность (ADCC), комплементзависимую цитотоксичность (CDC), понижающую регуляцию пролиферации и/или апоптоз в клетках-мишенях), модуляцию секреции цитокинов клеток-мишеней и/или экспрессию молекул клеточной поверхности, и их комбинации. См. также анализы, описанные в Schultze et al. (1998) Proc. Natl. Acad. Sci USA 92:8200-8204; Denton et al. (1998) Pediatr. Transplant. 2:6-15; Evans et al. (2000) J. Immunol. 164:688-697; Noelle (1998) Agents Actions Suppl. 49:17-22; Lederman et al. (1996) Curr. Opin. Hematol. 3:77-86; Coligan et al. (1991) Current Protocols in Immunology 13:12; Kwekkeboom et al. (1993) Immunology 79:439-444; и патенты США с номерами 5674492 и 5847082.
Можно сконструировать антитело, которое будет иметь увеличенную активность ADCC. В частности, для ADCC, опосредуемой через FcRIII-рецептор, важной является карбокси-концевая половина СН2-домена. Поскольку районы CH2 и шарнирные районы имеют важную роль в эффекторных функциях, могут быть созданы антитела с множественными доменами, которые содержат дополнительные районы СН2 и/или шарнирные районы, и исследованы на любые изменения эффекторной активности (см. Greenwood et al. (1994) Ther. Immunol. 1(5):247-55). Альтернативным подходом может быть конструирование параллельно дополнительных доменов, например, посредством создания димеров введением цистеина в H-цепь химерного Ig (см. Shopes (1992) J. Immunol. 148(9):2918-2922). Кроме того, изменения для увеличения активности ADCC могут быть сконструированы введением мутаций в Fc-район (см., например, патент США № 6737056 B1), экспрессией клеток в недостаточных в отношении фукозилтрансферазы клеточных линиях (см., например, публикацию заявки на патент США № 2003/0115614) или выполнением других изменений в отношении гликозилирования антител (см., например, патент США № 6602684).
Одним репрезентативным анализом для детектирования антагонистических анти-CD40-антител, специфических в отношении эпитопов CD40-антигена, идентифицированных в данном описании, является "анализ конкурентного связывания". Анализы конкурентного связывания являются серологическими анализами, в которых неизвестные компоненты детектируют и определяют количественно по их способности ингибировать связывание меченого известного лиганда с его специфическим антителом. Этот анализ называют также анализом конкурентного ингибирования. В репрезентативном анализе конкурентного связывания меченый полипептид CD40 осаждается кандидатными антителами в пробе, например, в комбинации с моноклональными антителами, индуцированными против одного или нескольких эпитопов моноклональных анти-CD40-антител. Анти-CD40-антитела, которые специфически взаимодействуют с представляющим интерес эпитопом, могут быть идентифицированы скринингом ряда антител, полученных против белка или фрагмента CD40 белка, содержащего конкретный эпитоп представляющего интерес белка CD40. Например, для CD40 человека представляющие интерес эпитопы включают эпитопы, содержащие линейные и/или нелинейные аминокислотные остатки короткой изоформы CD40 человека (см. GenBank Accession № NP_690593), представленной в SEQ ID NO:7, кодируемой последовательностью, представленной в SEQ ID NO:6; см. также GenBank Accession № NM_152854), или длинной изоформы CD40 человека (см. GenBank Accession №№ CAA43045 и NP_001241, представленной в SEQ ID NO:9, кодируемой последовательностью, представленной в SEQ ID NO:8; см. GenBank Accession №№ X60592 и NM_001250). Альтернативно анализы конкурентного связывания с предварительно идентифицированными подходящими антагонистическими анти-CD40-антителами могут быть использованы для отбора моноклональных антител, сравнимых с ранее идентифицированными антителами.
Антитела, используемые в таких иммуноанализах, могут быть мечеными или немечеными. Немеченые антитела могут быть использованы в агглютинации; меченые антитела могут быть использованы в широком диапазоне анализов, использующих большой диапазон меток. Детектирование образования комплекса антитело-антиген между анти-CD40-антителом и представляющим интерес эпитопом может облегчаться присоединением детектируемого вещества к этому антителу. Подходящие способы детектирования включают применение меток, таких как радионуклиды, ферменты, коферменты, флуоресцирующие агенты, хемилюминесцирующие агенты, хромогены, субстраты или кофакторы ферментов, ингибиторы ферментов, комплексы простетических групп, свободные радикалы, частицы, красители и т.п. Примеры подходящих ферментов включают пероксидазу хрена, щелочную фосфатазу, β-галактозидазу или ацетилхолинэстеразу; примеры подходящих комплексов простетических групп включают в себя стептавидин/биотин и авидин/биотин; примеры подходящих флуоресцентных материалов включают умбеллиферон, флуоресцеин, флуоресцеинизотиоциант, родамин, дихлортриазиниламин-флуоресцеин, дансилхлорид или фикоэритрин; примером люминесцентного материала является люминол; примеры биолюминесцентных материалов включают люциферазу, люциферин и экворин; и примеры подходящего радиоактивного материала включают 125I, 131I, 35S или 3H. Такие меченые реагенты могут быть использованы в различных хорошо известных анализах, таких как радиоиммуноанализы, ферментные иммуноанализы, например, ELISA, флуоресцентные иммуноанализы и т.п. См., например, патенты США с номерами 3766162, 3791932, 3817837 и 4233402.
Как отмечалось выше, комбинированная терапия по изобретению направлена на проблемы, ассоциированные с известными терапиями для заболеваний или состояний, ассоциированных с ростом неопластических В-клеток, включающими терапию с использованием ритуксимаба (коммерчески доступного под товарным названием Ритуксан®). Было показано, что ритуксимаб является эффективным лекарственным средством для неходжкинской лимфомы (NHL) низкой, промежуточной и высокой степени и является активным в других В-клеточных злокачественностях (см., например, Maloney et al. (1994) Blood 84:2457-2466), McLaughlin et al. (1998) J. Clin. Oncol. 16:2825-2833, Maloney et al. (1997) Blood 90:2188-2195, Hainsworth et al. (2000) Blood 95:3052-3056, Colombat et al. (2001) Blood 97:101-106, Coiffer et al. (1998) Blood 92:1927-1932), Foran et al. (2000) J. Clin. Oncol. 18:317-324, Anderson et al. (1991) Biochem. Soc. Trans. 25:705-708 или Vose et al. (1999) Ann. Oncol. 10:58a). Ритуксимаб лицензирован для лечения В-клеточной неходжкинской лимфомы низкой степени или фолликулярной неходжкинской лимфомы (NHL). Некоторые пациенты становятся резистентными к лечению ритуксимабом (см. Witzig et al. (2002) J. Clin. Oncol. 20:3262, Grillo-Lopez et al. (1998) J. Clin. Oncol. 16:2825 или Jazirehi et al. (2003) Mol. Cancer Ther 2:1183-1193). Например, некоторые пациенты утрачивают экспрессию CD20 на злокачественных В-клетках после терапии анти-CD20-антителами (Davis et al. (1999) Clin. Cancer Res. 5:611). Кроме того, 30%-50% пациентов с NHL низкой степени не проявляют клинической реакции на это моноклональное антитело (Hainsworth et al. (2000) Blood 95:3052-3056; Colombat et al. (2001) Blood 97:101-106). Для пациентов, развивающих резистентность к этому моноклональному антителу или имеющих В-клеточную лимфому, которая является резистентной к начальной терапии с использованием этого антитела, требуются альтернативные формы терапевтического вмешательства. Альтернативные терапии желательны также для пациентов с рецидивом после терапии с использованием ритуксимаба. Обнаружение антител с лучшей терапевтической, в частности, противоопухолевой, активностью в сравнении с ритуксимабом могло бы разительно улучшать способы терапии для заболевания или состояния, ассоциированного с ростом неопластических В-клеток, таких как В-клеточные лимфомы, в частности, В-клеточная неходжкинская лимфома.
В некоторых вариантах осуществления комбинированная терапия по изобретению обеспечивает более сильное терапевтическое действие, чем ритуксимаб, например, когда противоопухолевую активность анализируют с эквивалентными количествами этих антител в модели ксенотрансплантата опухоли голой мыши с использованием линий клеток лимфомы или миеломы человека. В других экспериментах комбинированная терапия по изобретению обеспечивает более сильное терапевтическое действие, чем комбинированная терапия с использованием ритуксимаба и CHOP (обычно известного как R-CHOP), например, когда противоопухолевую активность анализируют с эквивалентными количествами этих антител в модели ксенотрансплантата опухоли голой мыши с использованием линий клеток лимфомы или миеломы человека.
Подходящие модели ксенотрансплантата опухоли голой мыши включают модели, использующие линии клеток лимфомы Беркитта человека, известные как Namalwa и Daudi. Предпочтительные варианты анализируют противоопухолевую активность в стадийной модели ксенотрансплантата опухоли голой мыши с использованием линии клеток Daudi лимфомы человека. Стадийная модель ксенотрансплантата опухоли голой мыши, использующая линию клеток Daudi лимфомы человека, является более эффективной в различении терапевтической эффективности конкретного антитела, чем нестадийная модель, так как в этой стадийной модели введение доз антитела начинают только после достижения этой опухолью измеряемого размера. В нестадийной модели введение доз антитела начинают приблизительно в пределах 1 дня инокуляции опухоли и до того, как развивается пальпируемая опухоль. Способность антитела превзойти ритуксимаб или R-CHOP (т.е. обнаруживать увеличенную терапевтическую активность) в стадийной модели является веским указанием на то, что это антитело будет более терапевтически эффективным, чем ритуксимаб. Кроме того, в модели Daudi анти-CD20, мишень для ритуксимаба, экспрессируется на поверхности клеток при более высоком уровне, чем CD40.
В описанных здесь примерах, авторы изобретения использовали клеточные линии В-клеточной лимфомы человека RL (ATCC; CRL-2261) и SU-DHL-4 (DSMZ; ACC 495). Сообщалось, что обе эти клеточные линии являются отрицательными в отношении генома вируса Эпштейна-Барра, в противоположность обычным линиям клеток лимфомы, используемых в данной области. Использование клеточных линий, которые являются положительными в отношении вируса Эпштейна-Барра, может приводить к проблемам при интерпретации экспериментальных данных вследствие влияния на передачу сигнала онкогенного EBV в этих клеточных линиях. Клеточные линии лимфомы RL и SU-DHL-4 были специально выбраны авторами изобретения, так как они являются EBV-отрицательными, что дает большую уверенность в том, что эти результаты являются действительно достоверными, т.е. предсказательными в отношении терапевтической эффективности в людях.
Таким образом, в некоторых вариантах осуществления комбинированная терапия по изобретению обеспечивает более сильное терапевтическое действие, чем ритуксимаб, где противоопухолевую активность анализируют с эквивалентными количествами антител в модели ксенотрансплантата опухоли голой мыши с использованием линии клеток лимфомы человека, которая является отрицательной в отношении генома вируса Эпштейна-Барра. В следующих вариантах осуществления комбинированная терапия по изобретению обеспечивает более сильное терапевтическое действие, чем комбинированная терапия с ритуксимабом и CHOP, где противоопухолевую активность анализируют с эквивалентными количествами этих антител в модели ксенотрансплантата опухоли голой мыши с использованием линии клеток лимфомы человека, которая является отрицательной в отношении генома вируса Эпштейна-Барра. В этих экспериментах могут быть использованы линии клеток RL или SU-DHL-4 лимфомы.
Под "эквивалентным количеством" анти-CD40-антитела и ритуксимаба имеют в виду, что одну и ту же дозу вводят в расчете на массу или в расчете на объем. Таким образом, если анти-CD40-антитело вводят в дозе 0,01 мг/кг массы тела мыши, используемой в этой модели опухоли, ритуксимаб также вводят в дозе 0,01 мг/кг массы тела этой мыши.
Другим различием в эффективности антител является мера концентрации in vitro антитела, необходимая для получения максимального лизиса опухолевых клеток in vitro в присутствии NK-клеток. Например, анти-CD40-антитела могут достигать максимального лизиса клеток Daudi при EC50, меньшей ½ и предпочтительно ¼ и наиболее предпочтительно 1/10 концентрации ритуксимаба. Таким образом, анти-CD40-антитело или его антигенсвязывающий фрагмент может быть более сильнодействующим, чем эквивалентное количество ритуксимаба, в анализе антителозависимой клеточноопосредованной цитотоксичности (ADCC), например, в анализе, который предусматривает инкубирование CD40-экспрессирующих клеток и CD20-экспрессирующих клеток с выделенными природными клетками-киллерами (NK) в присутствии релевантного антитела, как описано в WO 2007/053767.
Изобретение использует анти-CD40-антитела для лечения заболеваний или состояний, ассоциированных с ростом неопластических В-клеток.
Анти-CD40-антитела по настоящему изобретению вводят при концентрации, которая является терапевтически эффективной для лечения заболевания или состояния, ассоциированного с неопластическими экспрессирующими CD40 В-клетками. Для выполнения этой задачи антитела могут быть приготовлены с использованием разнообразия приемлемых носителей и/или эксципиентов, известных в данной области. Анти-CD40-антитело может вводиться парентеральным способом введения. Обычно антитела вводят инъекцией, внутривенно или подкожно. Способы выполнения этого введения известны специалистам с обычной квалификацией в данной области.
Внутривенное введение выполняют предпочтительно инфузией (вливанием) на протяжении периода приблизительно менее 1 часа-приблизительно 10 часов (более предпочтительно менее 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 часов). Последующие инфузии могут вводиться на протяжении периода приблизительно менее 1 часа-приблизительно 6 часов, в том числе приблизительно 1-приблизительно 4 часов, приблизительно 1-приблизительно 3 часов или приблизительно 1-приблизительно 2 часов. Альтернативно доза может вводиться подкожно.
Фармацевтическую композицию по изобретению готовят таким образом, что она является совместимой с предполагаемым способом введения. Растворы или суспензии, используемые для парентерального применения, могут включать следующие компоненты: стерильный разбавитель, такой как вода для инъекций, солевой раствор; антибактериальные компоненты, такие как бензиловый спирт или метилпарабены; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатообразующие агенты, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты, и агенты для доведения тоничности, такие как хлорид натрия или декстроза. pH может корректироваться кислотами или щелочами, такими как соляная кислота или гидроксид натрия. Парентеральный препарат может быть заключен в ампулы, одноразовые шприцы или многодозовые флаконы, выполненные из стекла или пластика.
Анти-CD40-антитела обычно обеспечивают стандартным способом в фармацевтически приемлемом буфере, например, стерильном солевом растворе, стерильной забуференной воде, их комбинациях и т.д. Способы приготовления парентерально вводимых агентов описаны в Remington: The Science and Practice of Pharmacy (21st edition, Lippincott Williams & Wilkins, May 2005). См. также, например, WO 98/56418, который описывает стабилизированные фармацевтические готовые формы антител, подходящие для применения в способах по настоящему изобретению.
Количество по меньшей мере одного анти-CD40-антитела, подлежащего введению, может быть легко определено специалистом с обычной квалификацией в данной области. Факторы, влияющие на способ введения и соответствующее количество по меньшей мере одного анти-CD40-антитела, включают, но не ограничиваются ими, тяжесть этого заболевания, историю заболевания и возраст, рост, массу, здоровье, тип заболевания и физическое состояние индивидуума, подвергающегося терапии, и реакцию на инфузию антитела. Подобным образом, количество анти-CD40-антитела, которое должно вводиться, будет зависеть от способа введения и от того, будет ли этот субъект получать единичную дозу или множественные дозы этого противоопухолевого агента. Обычно более высокая доза анти-CD40-антитела является предпочтительной по мере увеличения массы субъекта, получающего терапию.
Для единичной дозы вводимое анти-CD40-антитело может быть в диапазоне от приблизительно 0,1 мг/кг до приблизительно 35 мг/кг, от приблизительно 0,5 мг/кг до приблизительно 30 мг/кг, от приблизительно 1 мг/кг до приблизительно 30 мг/кг, от приблизительно 3 мг/кг до приблизительно 30 мг/кг, от приблизительно 3 мг/кг до приблизительно 25 мг/кг, от приблизительно 3 мг/кг до приблизительно 20 мг/кг, от приблизительно 5 мг/кг до приблизительно 15 мг/кг. Так, например, эта доза может быть 0,3 мг/кг, 0,5 мг/кг, 1 мг/кг, 1,5 мг/кг, 2 мг/кг, 2,5 мг/кг, 3 мг/кг, 5 мг/кг, 7 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг или 35 мг/кг, или другими такими дозами, которые находятся в пределах диапазона от приблизительно 0,3 мг/кг до приблизительно 35 мг/кг.
Лечение субъекта терапевтически эффективным количеством антитела может включать единичную обработку или ряд обработок. Так, способы по настоящему изобретению могут включать введение множественных доз анти-CD40-антитела. Способ может включать введение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40 или более терапевтически эффективных отдельных доз фармацевтической композиции, содержащей анти-CD40-антитело. Частота и продолжительность введения множественных доз фармацевтических композиций, содержащих анти-CD40-антитело, могут быть легко определены квалифицированным в данной области специалистом без чрезмерного экспериментирования. Одна и та же терапевтически эффективная доза анти-CD40-антитела может вводиться на протяжении хода периода лечения. Альтернативно разные терапевтически эффективные дозы анти-CD40-антитела могут быть использованы на протяжении хода периода лечения.
В одном примере субъекта лечат анти-CD40-антителом в диапазоне приблизительно 0,1-20 мг/кг массы тела, один раз в неделю в течение приблизительно 1-10 недель, предпочтительно приблизительно 2-8 недель, более предпочтительно в течение приблизительно 3-7 недель и даже более предпочтительно в течение приблизительно 4, 5 или 6 недель. Лечение может иметь место с интервалами каждые 2-12 месяцев для предотвращения рецидива. Будет также понятно, что эффективная доза антитела, используемая для лечения, может увеличиваться или уменьшаться в ходе конкретного лечения. Изменения дозы могут происходить и становиться очевидными из результатов диагностических анализов.
Так, в одном варианте осуществления схема введения доз включает первое введение терапевтически эффективной дозы по меньшей мере одного анти-CD40-антитела в дни 1, 8, 15 и 22 периода лечения.
В другом варианте осуществления схема введения доз включает первое введение терапевтически эффективной дозы по меньшей мере одного анти-CD40-антитела ежедневно или в дни 1, 3, 5 и 7 одной недели в периоде лечения; причем схема введения включает первое введение терапевтически эффективной дозы по меньшей мере одного анти-CD40-антитела в дни 1 и 3-4 одной недели в периоде лечения; и предпочтительная схема введения включает первое введение терапевтически эффективной дозы по меньшей мере одного анти-CD40-антитела в день 1 недели в периоде лечения. Период лечения может составлять по меньшей мере 1 неделю, по меньшей мере 2 недели, по меньшей мере 3 недели, по меньшей мере месяц, по меньшей мере 2 месяца, по меньшей мере 3 месяца, по меньшей мере 6 месяцев, по меньшей мере 1 год. Периоды лечения могут быть последующими или отдельными и составлять каждый по меньшей мере 1 неделю, по меньшей мере 2 недели, по меньшей мере месяц, по меньшей мере 3 месяца, по меньшей мере 6 месяцев, по меньшей мере 1 год.
В других вариантах осуществления начальная терапевтически эффективная доза анти-CD40-антитела, как определено в другом месте в данном описании, может находиться в более низком диапазоне доз (т.е. от приблизительно 0,3 мг/кг приблизительно 20 мг/кг) с последующими дозами, находящимися в диапазоне более высоких доз (т.е. от приблизительно 20 мг/кг до приблизительно 50 мг/кг).
В альтернативных вариантах осуществления начальная терапевтически эффективная доза анти-CD40-антитела, как определено в другом месте в данном описании, может находиться в более высоком диапазоне доз (т.е. приблизительно 20 мг/кг-приблизительно 50 мг/кг) с последующими дозами, находящимися в диапазоне более низких доз (т.е. от приблизительно 0,3 мг/кг до приблизительно 20 мг/кг). Так, в некоторых вариантах осуществления изобретения терапия с использованием анти-CD40-антитела может начинаться введением "ударной (нагрузочной) дозы" антитела субъекту, нуждающемуся в терапии. Под "ударной дозой" имеется в виду начальная доза анти-CD40-антитела, которую вводят субъекту, причем доза вводимого антитела находится в более высоком диапазоне доз (т.е. от приблизительно 20 мг/кг до приблизительно 50 мг/кг). Эта "ударная доза" может вводиться в виде единственного введения, например, единственной инфузии, в которой это антитело вводят IV (внутривенно), или множественных введений, например, множественных инфузий, в которых это антитело вводят IV (внутривенно), пока полная "ударная доза" вводится в пределах приблизительно 24-часового периода. После введения "ударной дозы" субъекту вводят одну или несколько дополнительных терапевтически эффективных доз анти-CD40-антитела. Последующие терапевтически эффективные дозы могут вводиться, например, в соответствии со схемой один раз в неделю или один раз каждые две недели, один раз каждые три недели или один раз каждые четыре недели. В таких экспериментах последующие терапевтически эффективные дозы обычно находятся в диапазоне более низких доз (т.е. от 0,3 мг/кг до приблизительно 20 мг/кг).
Альтернативно, в некоторых вариантах осуществления, после "ударной дозы" последующие терапевтически эффективные дозы анти-CD40-антитела вводят в соответствии со "схемой поддержания", где терапевтически эффективную дозу антитела вводят один раз в месяц, один раз каждые 6 недель, один раз каждые два месяца, один раз каждые 10 недель, один раз каждые 3 месяца, один раз каждые 14 недель, один раз каждые четыре месяца, один раз каждые 18 недель, один раз каждые пять месяцев, один раз каждые 22 недели, один раз каждые шесть месяцев, один раз каждые 7 месяцев, один раз каждые 8 месяцев, один раз каждые 9 месяцев, один раз каждые 10 месяцев, один раз каждые 11 месяцев или один раз каждые 12 месяцев. В таких вариантах осуществления терапевтически эффективные дозы анти-CD40-антитела находятся в диапазоне более низких доз (т.е. от 0,3 мг/кг до приблизительно 20 мг/кг), в частности, когда последующие дозы вводят при более частых интервалах, например, один раз каждые две недели-один раз каждый месяц, или в пределах диапазона более высоких доз (т.е. от приблизительно 20 мг/кг до приблизительно 50 мг/кг), в частности, когда последующие дозы вводят при менее частых интервалах, например, когда последующие дозы вводят с интервалами приблизительно один месяц-приблизительно 12 месяцев.
Анти-CD40-антитела, присутствующие в описанных здесь фармацевтических композициях, для применения в способах по изобретению, могут быть природными или полученными рекомбинантными способами и могут происходить из любого источника, в том числе источников млекопитающих, таких как, например, мышь, крыса, кролик, свинья и человек. Предпочтительно такие полипептиды происходят из человека и более предпочтительно являются рекомбинантными белками человека из гибридомных линий клеток.
Любая фармацевтическая композиция, содержащая анти-CD40-антитело, имеющее описанные здесь связывающие свойства, может быть использована в качестве терапевтически активного компонента в способах по изобретению. Таким образом, жидкие, лиофилизированные или высушенные распылительной сушкой композиции, содержащие одно или несколько анти-CD40-антител, могут быть приготовлены в виде водного или неводного раствора или суспензии для последующего введения субъекту в соответствии со способами по изобретению. Каждая из этих композиций будет содержать по меньшей мере одно анти-CD40-антитело в качестве терапевтически или профилактически активного компонента. Под термином "терапевтически или профилактически активный компонент" имеют в виду, что анти-CD40-антитело специфически включено в композицию для вызывания желаемой терапевтической или профилактической реакции относительно лечения, предупреждения или диагностики заболевания или состояния субъекта при введении этой фармацевтической композиции этому субъекту. Предпочтительно фармацевтические композиции содержат подходящие стабилизирующие агенты, наполнители или и то, и другое, для минимизации проблем, ассоциированных с потерей стабильности белка и биологической активности во время приготовления и хранения.
К фармацевтическим композициям, содержащим анти-CD40-антитело, могут быть добавлены способствующие приготовлению агенты. Эти дополнительные компоненты могут включать, но не ограничиваются ими, масла, полимеры, витамины, углеводы, аминокислоты, соли, буферы, альбумин, поверхностно-активные вещества или наполнители. Предпочтительно углеводы включают сахар или сахароспирты, такие как моно-, ди- или полисахариды или водорастворимые глюканы. Сахариды или глюканы могут включать фруктозу, глюкозу, трегалозу, маннозу, сорбозу, ксилозу, мальтозу, сахарозу, декстран, пуллулан, декстрин, α- и β-циклодекстрин, растворимый крахмал, гидроксиэтилкрахмал и карбоксиметилцеллюлозу или их смеси. "Сахароспирт" определен как C4-C8 углеводород, имеющий гидроксильную группу, и включает галактит, инозит, маннит, ксилит, сорбит, глицерин и арабит. Эти сахара или сахароспирты могут использоваться индивидуально или в комбинации. Концентрация сахаров и сахароспиртов равна 1,0%-7% масс./об., более предпочтительно 2,0%-6,0% масс./об. Предпочтительно аминокислоты включают левовращающие (L) формы карнитина, аргинина и бетаина; однако, могут добавляться и другие аминокислоты. Предпочтительные полимеры включают поливинилпирролидон (PVP) со средней молекулярной массой между 2000 и 3000 или полиэтиленгликоль (PEG) со средней молекулярной массой между 3000 и 5000. Поверхностно-активные вещества, которые могут быть добавлены к этим композициям, показаны в EP №№ 270799 и 268110.
Эти способствующие приготовлению агенты, которые должны быть включены в фармацевтическую композицию, должны обеспечивать стабильность анти-CD40-антитела. То есть, анти-CD40-антитело должно сохранять его физическую и/или химическую стабильность и иметь желаемую биологическую активность, т.е. одну или несколько антагонистических активностей, определенных в данном описании выше.
Способы мониторинга стабильности белков хорошо известны в данной области. См., например, Jones (1993) Adv. Drug Delivery Rev. 10:29-90; Lee, ed. (1991) Peptide and Protein Drug Delivery (Marcel Dekker, Inc., New York, New York); и анализы стабильности, описанные ниже. Обычно стабильность белка измеряют при выбранной температуре в течение указанного периода времени. В предпочтительных вариантах осуществления стабильная фармацевтическая композиция антитела обеспечивает стабильность анти-CD40-антитела при хранении при комнатной температуре (приблизительно 25°C) в течение по меньшей мере 1 месяца, по меньшей мере 3 месяцев или по меньшей мере 6 месяцев, и/или является стабильной при приблизительно 2-8°C в течение по меньшей мере 6 месяцев, по меньшей мере 9 месяцев, по меньшей мере 12 месяцев, по меньшей мере 18 месяцев, по меньшей мере 24 месяцев.
Считается, что белок, такой как антитело, при приготовлении в фармацевтической композиции, сохраняет его физическую стабильность в конкретной точке времени, если он не обнаруживает видимых признаков (т.е. обесцвечивания или потери прозрачности) или измеримых признаков (например, с использованием вытеснительной хроматографии (SEC) или УФ-рассеяния) преципитации, агрегации и/или денатурации в этой фармацевтической композиции. Что касается химической стабильности, считается, что белок, такой как антитело, при приготовлении в фармацевтической композиции, сохраняет его химическую стабильность в конкретной точке времени, если измерения химической стабильности показывают, что этот белок (т.е. антитело) сохраняет представляющую интерес биологическую активность в этой фармацевтической композиции. Способы мониторинга изменений химической стабильности хорошо известны в данной области и включают, но не ограничиваются ими, способы детектирования химически измененных форм белка, таких, которые происходят из клиппирования, с использованием, например, электрофореза в ДСН-ПААГ, SEC и/или масс-спектрометрии MALDI-TOF-MS (масс-спектрометрии с измерением времени полета ионов, получаемых лазерной десорбцией/ионизацией из матрикса (поглощающих лазерный свет малых органических молекул, высушенных вместе с белком-мишенью); и деградации, ассоциированной с изменениями в молекулярном заряде (например, связанных с дезамидированием), с использованием, например, ионообменной хроматографии. См., например, способы, описанные ниже.
Считается, что анти-CD40-антитело, при приготовлении в фармацевтической композиции, сохраняет желаемую биологическую активность в конкретной точке времени, если эта желаемая биологическая активность в это время находится в пределах приблизительно 30%, предпочтительно а пределах приблизительно 20% желаемой биологической активности, проявляемой во время приготовления этой фармацевтической композиции, при определении в подходящем анализе для желаемой биологической активности. Анализы для измерения желаемой биологической активности анти-CD40-антител могут выполняться, как описано в примерах в данном описании. См. также анализы, описанные в Schultze et al. (1998) Proc. Natl. Acad. ScL USA 92:8200-8204; Denton et al. (1998) Pediatr. Transplant. 2:6-15; Evans et al. (2000) J. Immunol. 164:688-697; Noelle (1998) Agents Actions Suppl. 49:17-22; Lederman et al. (1996) Curr. Opin. Hematol. 3:77-86; Coligan et al. (1991) Current Protocols in Immunology 13:12; Kwekkeboom et al. (1993) Immunology 79:439-444; и патенты США с номерами 5674492 и 5847082.
В некоторых вариантах осуществления изобретения анти-CD40-антитело готовят в виде жидкой фармацевтической композиции. Анти-CD40-антитело может быть приготовлено с использованием любого способа, известного в данной области, в том числе с использованием способов, описанных в данном документе выше. Анти-CD40-антитело может быть рекомбинантно продуцировано в линии клеток СНО.
Когда анти-CD40-антитело должно храниться перед его приготовлением в виде композиции, оно может быть заморожено, например, при ≤-20°C, и затем оттаяно при комнатной температуре для дополнительного приготовления. Эта жидкая фармацевтическая композиция содержит терапевтически эффективное количество анти-CD40-антитела. Количество антитела, присутствующего в композиции, зависит от способа введения и желаемого объема дозы.
Таким образом, жидкая фармацевтическая композиция содержит анти-CD40-антитело в концентрации приблизительно 0,1 мг/мл-приблизительно 50,0 мг/мл, приблизительно 0,5 мг/мл-приблизительно 40,0 мг/мл, приблизительно 1,0 мг/мл-приблизительно 30,0 мг/мл, приблизительно 5,0 мг/мл-приблизительно 25,0 мг/мл, приблизительно 5,0 мг/мл-приблизительно 20,0 мг/мл или приблизительно 15,0 мг/мл-приблизительно 25,0 мг/мл. В некоторых вариантах осуществления жидкая фармацевтическая композиция содержит анти-CD40-антитело в концентрации приблизительно 0,1 мг/мл-приблизительно 5,0 мг/мл, приблизительно 5 мг/мл-приблизительно 10,0 мг/мл, приблизительно 10 мг/мл-приблизительно 15,0 мг/мл, приблизительно 15 мг/мл-приблизительно 20,0 мг/мл, приблизительно 20,0 мг/мл-приблизительно 25,0 мг/мл, приблизительно 25,0 мг/мл-приблизительно 30,0 мг/мл, приблизительно 30,0 мг/мл-приблизительно 35 мг/мл, приблизительно 35 мг/мл-приблизительно 40,0 мг/мл, приблизительно 40,0 мг/мл-приблизительно 45,0 мг/мл или приблизительно 45,0 мг/мл-приблизительно 50,0 мг/мл. В других вариантах осуществления жидкая фармацевтическая композиция содержит анти-CD40-антитело в концентрации приблизительно 15,0 мг/мл, приблизительно 16,0 мг/мл, приблизительно 17,0 мг/мл, приблизительно 18,0 мг/мл, приблизительно 19,0 мг/мл, приблизительно 20,0 мг/мл, приблизительно 21,0 мг/мл, приблизительно 22,0 мг/мл, приблизительно 23,0 мг/мл, приблизительно 24,0 мг/мл или приблизительно 25,0 мг/мл. Жидкая фармацевтическая композиция содержит анти-CD40-антитело и буфер, который поддерживает pH композиции в диапазоне приблизительно pH 5,0-приблизительно pH 7,0, в том числе приблизительно pH 5,0, 5,1, 5,2, 5,3, 5,4, 5,5, 5,6, 5,7, 5,8, 5,9, 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9, 7,0. В некоторых вариантах осуществления буфер поддерживает pH этой композиции в диапазоне приблизительно pH 5,0-приблизительно pH 6,5, приблизительно pH 5,0 до приблизительно pH 6,0, приблизительно pH 5,0 до приблизительно pH 5,5, приблизительно pH 5,5 до приблизительно pH 7,0, приблизительно pH 5,5-приблизительно pH 6,5 или приблизительно pH 5,5-приблизительно pH 6,0.
Любой подходящий буфер, который поддерживает pH жидкой композиции анти-CD40-антитела в диапазоне приблизительно pH 5,0-приблизительно pH 7,0, может быть использован в этой композиции, пока сохраняются физико-химическая стабильность и желаемая биологическая активность этого антитела, как отмечалось выше. Подходящие буферы включают, но не ограничиваются ими, общепринятые кислоты и их соли, в которых противоионом может быть, например, натрий, калий, аммоний, кальций или магний. Примеры общепринятых кислот и их солей, которые могут быть использованы для забуферивания фармацевтической жидкой композиции, включают, но не ограничиваются ими, янтарную кислоту или сукцинат, лимонную кислоту или цитрат, уксусную кислоту или ацетат, винную кислоту или тартрат, фосфорную кислоту или фосфат, глюконовую кислоту или глюконат, глутаминовую кислоту или глутамат, аспарагиновую кислоту или аспартат, малеиновую кислоту или малеат и яблочную кислоту или малат в качестве буферов. Концентрация буфера в композиции может быть от приблизительно 1 мМ до приблизительно 50 мМ, в том числе приблизительно 1 мМ, 2 мМ, 5 мМ, 8 мМ, 10 мМ, 15 мМ, 20 мМ, 25 мМ, 30 мМ, 35 мМ, 40 мМ, 45 мМ, 50 мМ или может быть другими такими величинами в диапазоне приблизительно 1 мМ-приблизительно 50 мМ. В некоторых вариантах осуществления концентрация буфера в композиции равна приблизительно 5 мМ до приблизительно 15 мМ, в том числе приблизительно 5 мМ, 6 мМ, 7 мМ, 8 мМ, 9 мМ, 10 мМ, 11 мМ, 12 мМ, 13 мМ, 14 мМ, 15 мМ или другим таким величинам в диапазоне приблизительно 5 мМ-приблизительно 15 мМ.
В некоторых вариантах осуществления изобретения жидкая фармацевтическая композиция содержит терапевтически эффективное количество анти-CD40-антитела и сукцинатного буфера или цитратного буфера в концентрации, которая поддерживает pH этой композиции в диапазоне приблизительно pH 5,0-приблизительно pH 7,0, предпочтительно приблизительно pH 5,0-приблизительно pH 6,5. Под "сукцинатным буфером" или "цитратным буфером" имеется в виду буфер, содержащий соль янтарной кислоты или соль лимонной кислоты, соответственно. В одном предпочтительном варианте осуществления противоионом сукцината или цитрата является катион натрия, и, следовательно, этот буфер является сукцинатом натрия или цитратом натрия, соответственно. Однако ожидается, что любой катион является эффективным. Другие возможные катионы сукцината или цитрата включают, но не ограничиваются ими, калий, аммоний, кальций и магний. Как отмечалось выше, концентрация сукцинатного или цитратного буфера в этой композиции может быть от приблизительно 1 мМ до приблизительно 50 мМ, в том числе приблизительно 1 мМ, 2 мМ, 5 мМ, 8 мМ, 10 мМ, 15 мМ, 20 мМ, 25 мМ, 30 мМ, 35 мМ, 40 мМ, 45 мМ, 50 мМ, или может быть другими такими величинами в диапазоне приблизительно 1 мМ до приблизительно 50 мМ. В некоторых вариантах осуществления концентрация буфера в композиции равна приблизительно 5 мМ до приблизительно 15 мМ, в том числе приблизительно 5 мМ, 6 мМ, 7 мМ, 8 мМ, 9 мМ, 10 мМ, 11 мМ, 12 мМ, 13 мМ, 14 мМ или приблизительно 15 мМ. В других вариантах осуществления жидкая фармацевтическая композиция содержит анти-CD40-антитело в концентрации приблизительно 0,1 мг/мл-приблизительно 50,0 мг/мл или приблизительно 5,0 мг/мл-приблизительно 25,0 мг/мл, и сукцинатный или цитратный буфер в концентрации приблизительно 1 мМ-приблизительно 20 мМ, приблизительно 5 мМ-приблизительно 15 мМ, предпочтительно приблизительно 10 мМ.
Если желательно, чтобы эта жидкая фармацевтическая композиция была почти изотонической, жидкая фармацевтическая композиция, содержащая анти-CD40-антитело и буфер, может дополнительно содержать количество изотонизирующего агента, достаточное для того, чтобы она стала почти изотонической. Под термином "почти изотоническая" имеется в виду, что эта водная композиция имеет осмолярность приблизительно 240 ммоль/кг-приблизительно 360 ммоль/кг, предпочтительно приблизительно 240-приблизительно 340 ммоль/кг, более предпочтительно приблизительно 250-приблизительно 330 ммоль/кг, даже более предпочтительно приблизительно 260-приблизительно 320 ммоль/кг, еще более предпочтительно приблизительно 270-приблизительно 310 ммоль/кг. Способы определения изотоничности раствора известны квалифицированным в данной области специалистам.
Квалифицированным в данной области специалистам известны различные фармацевтически приемлемые растворенные вещества, применимые в обеспечении изотоничности в фармацевтических композициях. Этим изотонизирующим агентом может быть любой реагент, способный корректировать осмотическое давление жидкой фармацевтической композиции по настоящему изобретению до величины, почти равной величине осмотического давления воды (биологической жидкости) организма. Желательным является применение физиологически приемлемого изотонизирующего агента. Таким образом, жидкая фармацевтическая композиция по настоящему изобретению, содержащая терапевтически эффективное количество анти-CD40-антитела и буфер, может дополнительно содержать компоненты, которые могут быть использованы для обеспечения изотоничности, например, хлорид натрия; аминокислоты, такие как аланин, валин и глицин; сахара и сахароспирты (полиолы), включающие, но не ограничивающиеся ими, глюкозу, декстрозу, фруктозу, сахарозу, мальтозу, маннит, трегалозу, глицерин, сорбит и ксилит; уксусную кислоту, другие органические кислоты и относительно минорные количества цитратов или фосфатов. Лицу с обычной квалификацией в данной области будут известны дополнительные агенты, которые пригодны для обеспечения оптимальной тоничности этой жидкой композиции.
В некоторых вариантах осуществления жидкая фармацевтическая композиция, содержащая анти-CD40-антитело и буфер, дополнительно содержит хлорид натрия в качестве изотонизирующего агента. Концентрация хлорида натрия в композиции будет зависеть от вклада других компонентов в тоничность. В некоторых вариантах осуществления концентрация хлорида натрия равна приблизительно 50 мМ-приблизительно 300 мМ, приблизительно 50 мМ-приблизительно 250 мМ, приблизительно 50 мМ-приблизительно 200 мМ, приблизительно 50 мМ-приблизительно 175 мМ, приблизительно 50 мМ-приблизительно 150 мМ, приблизительно 75 мМ-приблизительно 175 мМ, приблизительно 75 мМ-приблизительно 150 мМ, приблизительно 100 мМ-приблизительно 175 мМ, приблизительно 100 мМ-приблизительно 200 мМ, приблизительно 100 мМ-приблизительно 150 мМ, приблизительно 125 мМ-приблизительно 175 мМ, приблизительно 125 мМ-приблизительно 150 мМ, приблизительно 130 мМ-приблизительно 170 мМ, приблизительно 130 мМ-приблизительно 160 мМ, приблизительно 135 мМ-приблизительно 155 мМ, приблизительно 140 мМ-приблизительно 155 мМ или приблизительно 145 мМ-приблизительно 155 мМ. В одном таком варианте осуществления концентрация хлорида натрия равна приблизительно 150 мМ. В других таких вариантах осуществления концентрация хлорида натрия равна приблизительно 150 мМ, буфер является натрий-сукцинатным или натрий-цитратным буфером в концентрации приблизительно 5 мМ-приблизительно 15 мМ, эта жидкая композиция содержит терапевтически эффективное количество анти-CD40-антитела и имеет pH приблизительно pH 5,0-приблизительно pH 7,0, приблизительно pH 5,0-приблизительно pH 6,0 или приблизительно pH 5,5-приблизительно pH 6,5. В других вариантах осуществления эта жидкая фармацевтическая композиция содержит анти-CD40-антитело в концентрации приблизительно 0,1 мг/мл-приблизительно 50,0 мг/мл или приблизительно 5,0 мг/мл-приблизительно 25,0 мг/мл, приблизительно 150 мМ хлорида натрия и приблизительно 10 мМ сукцината натрия или цитрата натрия при pH приблизительно 5,5.
Деградация белка вследствие замораживания-оттаивания или механического сдвигающего усилия во время обработки жидкой фармацевтической композиции по данному изобретению может быть ингибирована включением поверхностно-активных веществ в композицию для снижения поверхностного натяжения на границе раздела раствор-воздух. Таким образом, в некоторых вариантах осуществления жидкая фармацевтическая композиция содержит терапевтически эффективное количество анти-CD40-антитела, буфер и дополнительно содержит поверхностно-активное вещество. В других вариантах осуществления жидкая фармацевтическая композиция содержит анти-CD40-антитело, буфер, изотонизирующий агент и дополнительно содержит поверхностно-активное вещество.
Типичными поверхностно-активными веществами являются неионогенные поверхностно-активные вещества, включающие сложные эфиры полиэтиленсорбита, такие как полисорбат 80 (Твин 80) и полисорбат 20 (Твин 20); сложные эфиры полиоксипропилен-полиоксиэтилена, такие как Плюроник F68; полиоксиэтилированные спирты, такие как Brij 35; симетикон; полиэтиленгликоль, такой как PEG400; лизофосфатидилхолин; и полиоксиэтилен-п-т-октилфенол, такой как Тритон Х-100. Классическая стабилизация фармацевтических веществ поверхностно-активными веществами или эмульгаторами описана, например, в Levine et al. (199I) J. Parenteral Sd. Technol. 45(3):160-165. Одним предпочтительным поверхностно-активным веществом, используемым в практике данного изобретения, является полисорбат 80. При включении поверхностно-активного вещества, его обычно добавляют в количестве от приблизительно 0,001% до приблизительно 1,0% (масс./об.), приблизительно 0,001% до приблизительно 0,5%, приблизительно 0,001% до приблизительно 0,4%, приблизительно 0,001% до приблизительно 0,3%, приблизительно 0,001% до приблизительно 0,2%, приблизительно 0,005% до приблизительно 0,5%, приблизительно 0,005% до приблизительно 0,2%, приблизительно 0,01% до приблизительно 0,5%, приблизительно 0,01% до приблизительно 0,2%, приблизительно 0,03% до приблизительно 0,5%, приблизительно 0,03% до приблизительно 0,3%, приблизительно 0,05% до приблизительно 0,5% или приблизительно 0,05% до приблизительно 0,2%.
Таким образом, в некоторых вариантах осуществления жидкая фармацевтическая композиция содержит терапевтически эффективное количество анти-CD40-антитела, буфером является натрий-сукцинатный или натрий-цитратный буфер в концентрации приблизительно 1 мМ-приблизительно 50 мМ, приблизительно 5 мМ-приблизительно 25 мМ или приблизительно 5 мМ-приблизительно 15 мМ; эта композиция имеет pH приблизительно pH 5,0-приблизительно pH 7,0, приблизительно pH 5,0-приблизительно pH 6,0 или приблизительно pH 5,5-приблизительно pH 6,5; и композиция дополнительно содержит поверхностно-активное вещество, например, полисорбат 80, в количестве от приблизительно 0,001% до приблизительно 1,0 или приблизительно от 0,001% до приблизительно 0,5%. Такие композиции могут необязательно содержать изотонирующий агент, такой как хлорид натрия, в концентрации приблизительно 50 мМ-приблизительно 300 мМ, приблизительно 50 мМ-приблизительно 200 мМ или приблизительно 50 мМ-приблизительно 150 мМ. В других вариантах осуществления жидкая фармацевтическая композиция содержит анти-CD40-антитело в концентрации приблизительно 0,1 мг/мл-приблизительно 50,0 мг/мл или приблизительно 5,0 мг/мл до приблизительно 25,0 мг/мл, в том числе приблизительно 20,0 мг/мл; приблизительно 50 мМ-приблизительно 200 мМ хлорида натрия, в том числе приблизительно 150 мМ хлорида натрия; сукцинат натрия или цитрат натрия в концентрации приблизительно 5 мМ-приблизительно 20 мМ, в том числе приблизительно 10 мМ сукцината натрия или цитрата натрия; хлорид натрия в концентрации приблизительно 50 мМ-приблизительно 200 мМ, в том числе приблизительно 150 мМ; и необязательно поверхностно-активное вещество, например, полисорбат 80, в концентрации от приблизительно 0,001% до приблизительно 1,0%, в том числе приблизительно 0,001%-приблизительно 0,5%; где жидкая фармацевтическая композиция имеет pH приблизительно pH 5,0-приблизительно pH 7,0, приблизительно pH 5,0-приблизительно pH 6,0, приблизительно pH 5,0-приблизительно pH 5,5, приблизительно pH 5,5-приблизительно pH 6,5 или приблизительно pH 5,5-приблизительно pH 6,0.
Эта жидкая фармацевтическая композиция может по существу не содержать никаких консервантов и других носителей, эксципиентов или стабилизаторов, указанных выше. Альтернативно композиция может включать один или несколько конвервантов, например, антибактериальных агентов, фармацевтически приемлемых носителей, эксципиентов или стабилизаторов, описанных здесь выше, при условии, что они не действуют вредным образом на физико-химическую стабильность анти-CD40-антитела. Примеры приемлемых носителей, эксципиентов и стабилизаторов включают, но не ограничиваются ими, дополнительные буферные агенты, сорастворители, поверхностно-активные вещества, антиоксиданты, в том числе аскорбиновую кислоту и метионин, хелатообразующие агенты, такие как ЭДТА, комплексы металлов (например, комплексы Zn-белок) и биодеградируемые полимеры. Подробное обсуждение композиции и выбора фармацевтически приемлемых носителей, стабилизаторов и изомолитов может быть найдено в Remington: The Science and Practice of Pharmacy (21st edition, Lippincott Williams & Wilkins, May 2005).
"Носители", в данном контексте, включают фармацевтически приемлемые носители, эксципиенты или стабилизаторы, которые являются нетоксичными для клеток или млекопитающих, подвергающихся их действию, при используемых дозах и концентрациях. Физиологически приемлемым носителем часто является водный раствор с забуференным pH. Примеры физиологически приемлемых носителей включают буферы, такие как фосфатный, цитратный, сукцинатный буферы, и другие органические кислоты; антиоксиданты, в том числе аскорбиновую кислоту; полипептиды с низкой молекулярной массой (менее приблизительно 10 остатков); белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включающие глюкозу, маннозу или декстрины; хелатообразующие агенты, такие как ЭДТА; сахароспирты, такие как маннит или сорбит; солеобразующие противоионы, такие как натрий; и/или неионогенные поверхностно-активные вещества, такие как Твин, полиэтиленгликоль (PEG) и Плюроники.
После приготовления этой жидкой фармацевтической композиции или другой описанной здесь композиции, она может быть лиофилизирована для предотвращения деградации. Способы для лиофилизации жидких композиций известны специалистам с обычной квалификацией в данной области. Непосредственно перед использованием эта композиция может быть воссоздана при помощи стерильного разбавителя (например, раствора Рингера, дистиллированной воды или стерильного солевого раствора), который может включать дополнительные ингредиенты. После воссоздания эту композицию предпочтительно вводят субъектам с использованием способов, которые известны квалифицированным в данной области специалистам.
Содержащей анти-CD40-антитело фармацевтической композицией может быть композиция, описанная в находящейся в совместном владении публикации международной заявки на патент № PCT/US2007/066757, опубликованной в виде WO 2007/124299. В частности, фармацевтическая композиция для применения в комбинированной терапии по настоящему изобретению может содержать (i) анти-CD40-антитело, (ii) буферный агент для поддержания pH этой композиции между приблизительно pH 5,0 и pH 7,0, и (iii) количество аргинин-HCl, достаточное для того, чтобы эта жидкая композиция стала почти изотонической. В таких композициях буферным агентом может быть буфер, состоящий из цитрата/лимонной кислоты. Композиции могут дополнительно содержать неионогенное поверхностно-активное вещество и/или L-метионин в качестве дополнительных стабилизирующих агентов. Композиция может иметь осмолярность приблизительно 240 ммоль/кг до приблизительно 360 ммоль/кг. Концентрация буферного агента может быть от приблизительно 5 мМ до приблизительно 100 мМ, от приблизительно 5 мМ до приблизительно 20 мМ или от приблизительно 5 мМ до приблизительно 15 мМ (например, 10 мМ). Композиция может иметь pH от pH 5,0 до pH 6,0 (например, около pH 5,5). Эта композиция может содержать аргинин-HCl в концентрации приблизительно 50 мМ-приблизительно 200 мМ или приблизительно 100 мМ-приблизительно 175 мМ (например, приблизительно 150 мМ). Композиция может дополнительно содержать поверхностно-активное вещество полисорбат, например, в концентрации приблизительно 0,001%-приблизительно 1,0% (масс./об.) или в концентрации приблизительно 0,025%-приблизительно 0,1% (масс./об.). Эта композиция может дополнительно содержать метионин в концентрации приблизительно 0,5 мМ-приблизительно 20,0 мМ или в концентрации приблизительно 1,0 мМ-приблизительно 20,0 мМ (например, приблизительно 5,0 мМ). Анти-CD40-антитело может присутствовать в композиции при 0,1 мг/мл-приблизительно 50,0 мг/мл или при приблизительно 1,0 мг/мл-приблизительно 35,0 мг/мл, или при приблизительно 10,0 мг/мл-приблизительно 35,0 мг/мл.
Изобретение включает также применение химиотерапевтических агентов циклофосфамида (фабричная марка Цитоксан), доксорубицина (фабричная марка Адриамицин), винкристина (фабричная марка Онковин) и преднизона (фабричная марка Дельтазон). Применение этих четырех химиотерапевтических агентов в комбинации называют CHOP. Схемы введения CHOP обычно используют для лечения пациентов с неходжкинской лимфомой, и CHOP считался стандартной терапией для пациентов с диффузной крупноклеточной недифференцированной B-клеточной лимфомой (DLBCL) в течение более двадцати пяти лет. (Feugier et al. (2005) J. Clin. Oncol. 23(18):4117-4126; Habermann et al. (2006) J. Clin. Oncol. 24(19):3121-3127). CHOP использовали в комбинации с ритуксимабом в лечении DLBCL (Feugier et al. (2005) J. Clin. Oncol. 23(18):4117-4126; Habermann et al. (2006) J. Clin. Oncol. 24(19):3121-3127).
CHOP является комбинацией трех химиотерапевтических лекарственных средств (циклофосфамида, доксорубицина и винкристина) и стероида (преднизона). Химиотерапия CHOP ассоциирована в многочисленными побочными действиями, причем наиболее частыми являются усталость, уменьшенное число клеток крови вследствие воздействий на костный мозг, тошнота, выпадение волос, бесплодие, повреждения и язвы в полости рта, потеря аппетита и симптомы нервной системы (например, покалывания или боль в области живота). Способы по настоящему изобретению могут позволить уменьшать или элиминировать одно или несколько из этих побочных действий, позволяя использовать схемы введения более низкой дозы CHOP. Таким образом, в некоторых вариантах осуществления способы, применения, композиции и наборы по изобретению могут быть использованы для лечения пациентов-людей в отношении заболевания или состояния, ассоциированного с ростом неопластических В-клеток, с устранением или уменьшением одного или нескольких побочных действий, обычно ассоциированных с введением CHOP.
Комбинированная терапия по изобретению может также позволить уменьшать или элиминировать одно или несколько из побочных действий, ассоциированных с введением анти-CD40-антител, позволяя использовать схемы введения более низких доз анти-CD40-антител. Таким образом, в некоторых вариантах осуществления способы, применения, композиции и наборы по настоящему изобретению могут быть использованы для лечения пациентов-людей в отношении заболевания или состояния, ассоциированного с ростом неопластических В-клеток, с устранением или уменьшением одного или нескольких побочных действий, обычно ассоциированных с введением анти-CD40-антитела.
Любые фармацевтические композиции, содержащие компоненты CHOP в качестве терапевтически активных компонентов, могут быть использованы в способах по настоящему изобретению. Они будут содержать один или несколько компонентов CHOP и фармацевтически приемлемый носитель или эксципиент, например, фармацевтически приемлемый носитель или эксципиент, описанные в другом месте в данном описании. Подходящие фармацевтические композиции хорошо известны в данной области. Под термином "терапевтические активный компонент" имеется в виду, что релевантный терапевтический агент (агенты) специально включен(ы) в эту комбинацию для вызывания желаемой терапевтической реакции в отношении лечения заболевания или состояния у субъекта при введении фармацевтической композиции этому субъекту. Компоненты CHOP вводят в концентрациях, которые являются "терапевтически эффективными" для лечения заболевания или состояния, ассоциированного с ростом неопластических В-клеток.
Компоненты CHOP могут вводиться любым подходящим способом введения. Циклофосфамид, доксорубицин и винкристин вводят обычно внутривенно, тогда как преднизон обычно вводят перорально. Способы выполнения такого введения известны специалистам с обычной квалификацией в данной области.
CHOP обычно вводят в виде циклов лечения, причем каждый цикл предусматривает введение циклофосфамида в дозе 750 мг/м2 в день 1, доксорубицина 50 мг/м2 в день 1, винкристина 1,4 мг/м2 в день 1 и преднизона 100 мг/м2 в дни 1-5. Этот цикл обычно повторяют каждые три недели (21 день). Обычный курс лечения состоит из шести-восьми циклов в целом.
В этих способах, применениях, композициях и наборах по изобретению циклофосфамид может использоваться в дозе 75-1000 мг/м2 или 185-1000 мг/м2, или 500-1000 мг/м2 или 700-800 мг/м2 (например, 750 мг/м2). Доксорубицин может использоваться в дозе 5-70 мг/м2 или 12-70 мг/м2, или 35-70 мг/м2, или 45-55 мг/м2 (например, 50 мг/м2). Винкристин может использоваться в дозе 0,1-2,0 мг/м2 или 0,7-2,0 мг/м2, или 1,0-2,0 мг/м2, или 1,0-1,6 мг/м2 (например, 1,4 мг/м2). Преднизон может использоваться в дозе 10-130 мг/м2 или 50-130 мг/м2, или 65-130 мг/м2, или 85-125 мг/м2 (например, 100 мг/м2). Квалифицированный специалист будет вполне способен выбрать подходящую схему введения CHOP для применения в комбинированной терапии изобретения.
В этих способах, применениях, композициях и наборах по настоящему изобретению схема введения CHOP будет повторяться каждые три недели, но может повторяться каждые четыре недели, каждые пять недель, каждые шесть недель, каждые семь недель, каждые восемь недель, каждые девять недель или каждые десять недель, если желательно. Комбинированная терапия по изобретению может позволить применение более низких доз CHOP при сохранении терапевтической эффективности, позволяя тем самым повторять схему введения CHOP более часто, например, каждую неделю или каждые две недели. CHOP может вводиться в течение любого количества циклов, например, 1-20 циклов, предпочтительно 3-15 циклов, более предпочтительно 5-10 циклов.
Термин "содержащий" включает в себя "включающий", а также "состоящий". Например, композиция, "содержащая" X, может состоять исключительно из Х или может включать что-нибудь дополнительное, например, X + Y.
Слово "по существу" не исключает "полностью", например, композиция, которая является "по существу не содержащей" Y, может полностью не содержать Y. При необходимости, слово "по существу" может быть опущено из определения настоящего изобретения.
Термин "приблизительно" в отношении численной величины x обозначает, например, x±10%.
Теперь различные аспекты и варианты осуществления данного изобретения будут описаны более подробно только при помощи примеров. Будет понятно, что может быть произведена модификация деталей без отклонения от объема настоящего изобретения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Анти-CD40-антитело, используемое в примерах ниже, является моноклональным антителом HCD122 (ранее известным как CHIR-12.12). Получение, секвенирование и характеристика HCD122 уже были описаны.
Пример 1
Противоопухолевая активность HCD122 в комбинации с CHOP (H-CHOP)
Как моноклональное антитело HCD122 человека, так и CHOP показали противоопухолевую эффективность в моделях лимфомы RL и SU-DHL-4 при использовании раздельно. Линия клеток RL (ATCC; CRL-2261) является линией клеток В-клеточной лимфомы человека, установленной от 52-летнего пациента мужского пола Индо-Европейской группы населения с NHL. Линия клеток SU-DHL-4 (DSMZ; ACC 495) является линией клеток В-клеточной лимфомы человека, установленной из перитонеального выпота 38-летнего пациента мужского пола с B-NHL (диффузного крупноклеточного, дифференцированного типа). Сообщалось, что обе эти линии клеток являются отрицательными в отношении генома вируса Эпштейна-Барра в противоположность многим обычным клеточным линиям лимфом, используемым в данной области. Применение клеточных линий, которые являются положительными в отношении вируса Эпштейна-Барра, может приводить к проблемам при интерпретации экспериментальных данных вследствие влияний на передачу сигнала онкогенным EBV в этих клеточных линиях. Клеточные линии лимфомы RL и SU-DHL-4 были специально выбраны авторами настоящего изобретения, так как они являются EBV-отрицательными, что позволяет иметь более высокую уверенность в том, что эти результаты действительно являются достоверными.
Активность HCD122 в комбинации с CHOP оценивали в модели ксенотрансплантата диффузной крупноклеточной В-клеточной лимфомы RL (DLBCL) и сравнивали с активностями HCD122 отдельно и CHOP отдельно. Эту комбинацию HCD122 и CHOP называют ниже H-CHOP. Терапевтическую эффективность H-CHOP сравнивали также с известной комбинацией CHOP с химерным моноклональным анти-CD20-антителом ритуксимабом, обычно называемым R-CHOP.
Материалы и способы
Противоопухолевую активность HCD122 тестировали в моделях ксенотрансплантата RL DLBCL в комбинации с CHOP в мышах CB17/SCID. 10×106 клеток RL имплантировали подкожно с равным объемом Matrigel™ в срединной торакально-вертебральной области животного в объеме 200 мкл. Введение антитела начинали, когда средний объем опухоли был равен 150-200 мм3 (отмечено как день 1 на фиг.1). HCD122, ритуксимаб и IgG1-антитело человека в качестве отрицательного контроля, в каждом случае, вводили внутрибрюшинной инъекцией. Все моноклональные антитела вводили по схеме один раз в неделю и длительность обработки была равна 4 неделям. Протокол CHOP вводили при дозах и схеме введения: преднизон, 0,2 мг/кг перорально (p.o.) в дни 1-5; цитоксан, 40 мг/кг, внутривенно (i.v.), в день 1; доксорубицин, 3,3 мг/кг, i.v., в день 1; винкристин, 0,5 мг/кг, i.v., в день 1. Размер группы был n=12. Для измерений объема опухоли длину и затем ширину измеряли цифровым калипером. Эти измерения регистрировали дважды в неделю, как только опухоли становились видимыми. Объемы опухолей и время удвоения рассчитывали на основе формулы, Объем = L×W2/2. Массы животных регистрировали и оценивали в виде среднего на группу.
Результаты
Результаты этих экспериментов показаны на фиг.1 и в таблицах 1 и 2 ниже.
Ингибирование роста опухолей в день 25
Все из этих терапий значимо уменьшали рост опухолей в день 25 при сравнении с лечением контрольным huIgG1-антителом. Наблюдаемое ингибирование роста опухолей (TGI) только с CHOP или только с HCD122 (при 1 мг/кг) было 77% и 71%, соответственно (р<0,001; критерий Тьюки). В отличие от этого, наблюдаемое TGI для комбинации H-CHOP (с использованием HCD122 при 1 мг/кг) было равно 95% (p<0,001; критерий Тьюки). Наблюдаемое TGI для комбинации R-CHOP (с использованием ритуксимаба при 10 мг/кг) было равно 90% (p<0,001; критерий Тьюки).
Задержка роста опухоли
Задержка роста опухоли (время достижения размера опухоли 500 мм3) была значимо более длинной для H-CHOP (17,5 дней), чем для одного CHOP (8 дней) или одного HCD122 (6 дней) (p<0,001). Не наблюдали токсичности с комбинацией H-CHOP. В конце этого исследования (день 35) уменьшение роста опухоли было значимо большим в группе обработки, получавшей H-CHOP (1 мг/кг HCD122), чем в группах, получавших R-CHOP (10 мг/кг ритуксимаб, p<0,05; критерий Тьюки) или только CHOP (p<0,001; критерий Тьюки).
Эти данные показывают, что лечение комбинацией H-CHOP приводит к большей противоопухолевой эффективности, чем лечение либо только HCD122, либо только CHOP. При использовании HCD122 в дозе 1 мг/кг комбинация H-CHOP обеспечивала большую терапевтическую эффективность, чем эффективность, которая ожидалась бы, если действия каждого агента были бы лишь аддитивными, т.е. было обнаружено, что эта комбинация H-CHOP обеспечивает синергическое терапевтическое действие. Таким образом, эти данные предполагают, что комбинация H-CHOP может быть использована для улучшения противоопухолевой терапии в пациентах-людях, которые могли в противном случае лечиться только CHOP или только HCD122, например, обеспечением повышенного терапевтического эффекта или позволением уменьшения доз CHOP для уменьшения или элиминации одного или нескольких побочных эффектов, ассоциированных с введением CHOP.
Эти данные показывают также, что такое лечение комбинацией H-CHOP приводит к большей противоопухолевой эффективности, чем лечение только ритуксимабом или известной комбинацией ритуксимаба и CHOP (R-CHOP). Таким образом, эти данные предполагают, что комбинация H-CHOP может быть использована для улучшения противоопухолевой терапии в пациентах-людях, которые могли в противном случае лечиться только ритуксимабом или R-CHOP, например, обеспечением повышенного терапевтического эффекта или позволением уменьшения доз CHOP для уменьшения или элиминации одного или нескольких побочных эффектов, ассоциированных с введением CHOP.
Пример 2
HCD122 обращает CD40L-индуцированную резистентность к CHOP
Проводили эксперименты для выяснения механизма, при помощи которого комбинация H-CHOP обеспечивает неожиданно сильную противоопухолевую эффективность in vivo. Клетки SU-DHL-4 культивировали в присутствии (i) отрицательного контрольного huIgG1-антитела, (ii) HCD122, (iii) huIgG1 и CD40L или (iv) HCD122 и CD40L. Клетки SU-DHL-4 высевали при 30000 клеток на лунку. Все антитела использовали при 10 мкг/мл. Рекомбинантный растворимый CD40L человека использовали при 1 мкг/мл с усилителем лиганда при 2 мкг/мл. Все клетки обрабатывали цитоксаном в дозе 1 мкг/мл, преднизоном - 15 мкг/мл, доксорубицином - 2,5 нг/мл и винкристином - 1 пг/мл. Клетки культивировали в течение 3 дней, и процент жизнеспособных клеток определяли с использованием CellTiter-Glo. Результаты этих экспериментов показаны на фиг.2. Эти данные показывают, что CD40L индуцирует резистентность к цитотоксичности CHOP против клеток SU-DHL-4, но эта резистентность может быть преодолена с использованием HCD122, что позволяет CHOP иметь его полное цитотоксическое действие. Эти данные помогают объяснить эту неожиданно сильную противоопухолевую эффективность H-CHOP.
Пример 3
Действие HCD122 на активацию NF-κB
Клетки RL и SU-DHL-4 стимулировали CD40L в течение 0, 10, 30 и 90 минут и выполняли Вестерн-блоты (фиг.3). Было обнаружено, что фосфорилирование р65 индуцировалось в пределах минут стимуляции клеток RL или SU-DHL-4 посредством CD40L. Фосфорилирование сохранялось в этих клеточных линиях по меньшей мере в течение 90 минут. Кроме того, было обнаружено, что фосфорилирование р65 как в клетках RL, так и в клетках SU-DHL-4, стимулированных CD40L, сильно ингибировалось в присутствии HCD122 (фиг.3). Эти данные демонстрируют, что активация NF-κB, индуцированная CD40L, полностью блокируется HCD122 как в клетках RL, так и в клетках SU-DHL-4. Понижающая регуляция активации NF-κB в клетке может сенсибилизировать эту клетку к цитотоксичности CHOP (Chuang et al. (2002) Biochemical Pharmacology 63:1709-1716; Cheng et al. (2000) Oncogene 19:4936-4940). Таким образом, эти данные, показывающие, что HCD122 понижающим образом регулирует активацию NF-κB, помогают объяснить, почему CD40L-индуцируемая резистентность к цитотоксичности CHOP может быть преодолена с использованием HCD122.
Пример 4
Действие HCD122 на молекулы адгезии клеточной поверхности
Для дополнительного выяснения механизма, посредством которого комбинация H-CHOP приводит к неожиданно сильной противоопухолевой эффективности in vivo, выполняли дополнительные эксперименты. Способность В-клеток агрегироваться и взаимодействовать с их микроокружением может влиять на эффективность терапевтических агентов. Таким образом, исследовали действия HCD122 на экспрессию молекул адгезии в клеточных линиях RL и SU-DHL-4. В этих исследованиях было обнаружено, что HCD122 ингибирует CD40L-индуцированную экспрессию CD54, CD86 и CD95 в клеточных линиях как RL, так и SU-DHL-4. Результаты для клеточной линии RL показаны на фиг.4. Результаты для клеточных линий SU-DHL-4 показаны на фиг.5.
Действие HCD122 на CD40L-индуцированной агрегации клеток SU-DHL-4 анализировали микроскопией, и было обнаружено, что антитело HCD122 ингибировало эту агрегацию. Результаты этих экспериментов показаны на фиг.6A-6D. Фиг.6A показывает клетки, обработанные huIgG1. Фиг.6В показывает клетки, обработанные HCD122. Фиг.6С показывает клетки, обработанные huIgG1 и CD40L. Фиг.6D показывает клетки, обработанные HCD122 и CD40L.
Эти данные предполагают, что CD40L может уменьшать эффективность терапевтических средств, таких как CHOP, in vivo, заставляя В-клетки агрегироваться, и что эта агрегация может быть предотвращена с использованием HCD122. Эти данные помогают дополнительно объяснить, почему комбинация H-CHOP приводит к неожиданно сильной противоопухолевой эффективности in vivo.
Многочисленные модификации и другие варианты изобретения, представленного здесь, могут придти на ум специалисту, квалифицированному в области, к которой относятся эти изобретения, имеющему преимущество объяснений, представленных в предыдущих описаниях и прилагаемых фигурах. Таким образом, должно быть понятно, что эти изобретения не ограничиваются конкретными описанными вариантами и что предполагается, что модификации и другие варианты также включены в объем перечня вариантов и прилагаемой формулы изобретения. Хотя здесь используются конкретные термины, они используются только в общем и описательном смысле, а не с целью ограничения.
Все публикации и заявки на патент, цитируемые здесь, включены в полном объеме в качестве ссылки в такой же степени, как если бы каждая отдельная публикация или публикация патента была конкретно и отдельно указана как включенная в качестве ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ АНТИ-CD40-АНТИТЕЛ | 2006 |
|
RU2442606C2 |
| КОМБИНАЦИЯ СЛИТОГО БЕЛКА АНТИТЕЛО ПРОТИВ EDb ФИБРОНЕКТИНА-IL-2 И МОЛЕКУЛЫ, СВЯЗЫВАЮЩЕЙСЯ С В-КЛЕТКАМИ, ПРЕДШЕСТВЕННИКАМИ В-КЛЕТОК И/ИЛИ ИХ ЗЛОКАЧЕСТВЕННЫМ АНАЛОГОМ | 2008 |
|
RU2484845C2 |
| АНТИ-CD40-АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2012 |
|
RU2609647C2 |
| СПОСОБ ЛЕЧЕНИЯ ВАСКУЛИТА | 2005 |
|
RU2411956C2 |
| АНТИТЕЛА К CD40 ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ СИНДРОМА ШЕГРЕНА | 2018 |
|
RU2790558C2 |
| КОНЪЮГАТЫ "ПРОИЗВОДНОЕ КАЛИХЕАМИЦИНА-НОСИТЕЛЬ" | 2003 |
|
RU2422157C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИ-CD40-АНТИТЕЛА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2407544C2 |
| ОЧИСТКА АНТИТЕЛ С ПОМОЩЬЮ КАТИОНООБМЕННОЙ ХРОМАТОГРАФИИ | 2008 |
|
RU2498991C2 |
| АНТИ-CD40-АНТИТЕЛА, ПРИМЕНЕНИЕ И МЕТОДЫ | 2012 |
|
RU2649055C2 |
| СПОСОБ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 2005 |
|
RU2384345C2 |














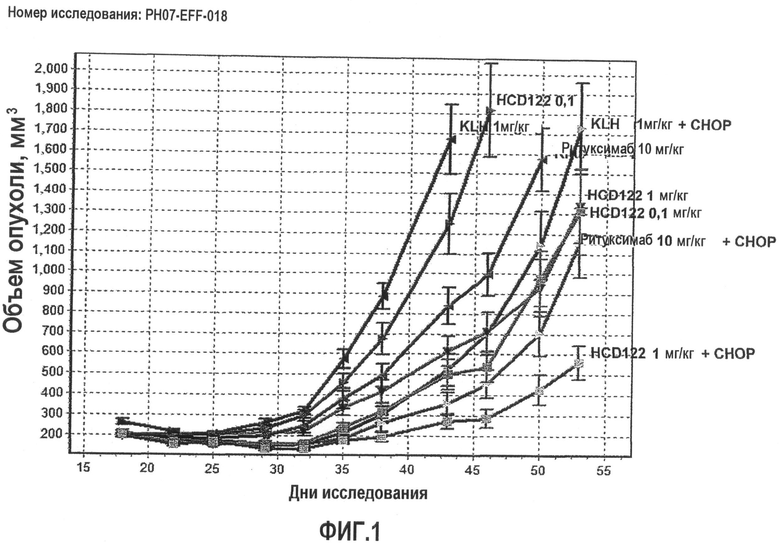
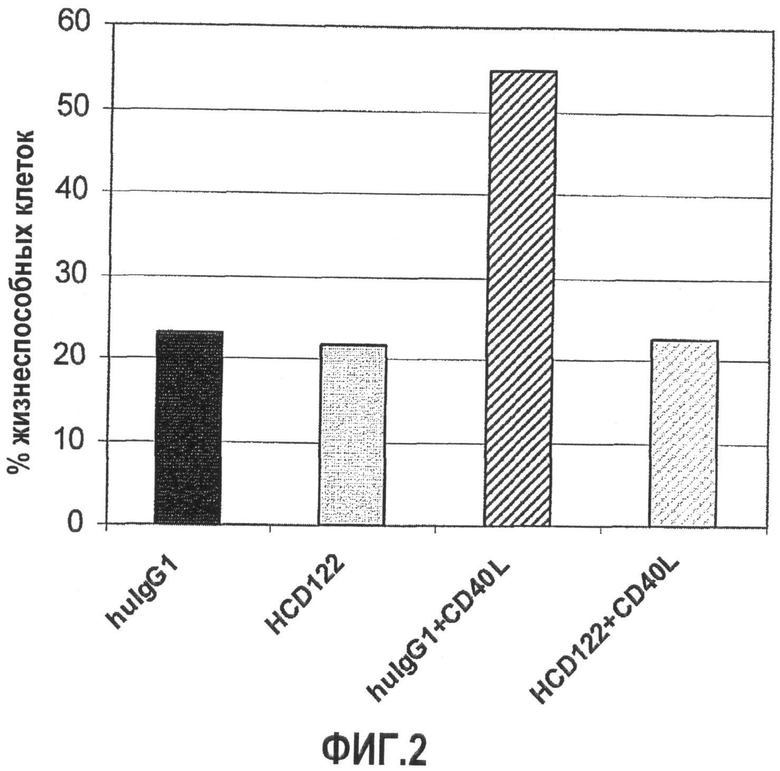
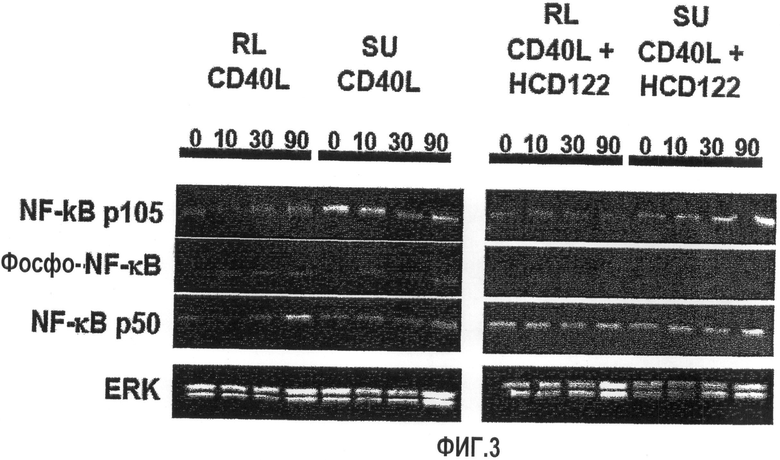
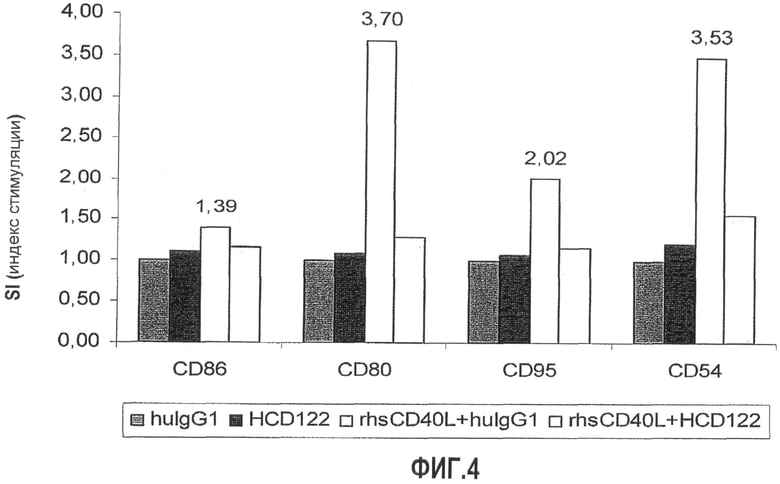
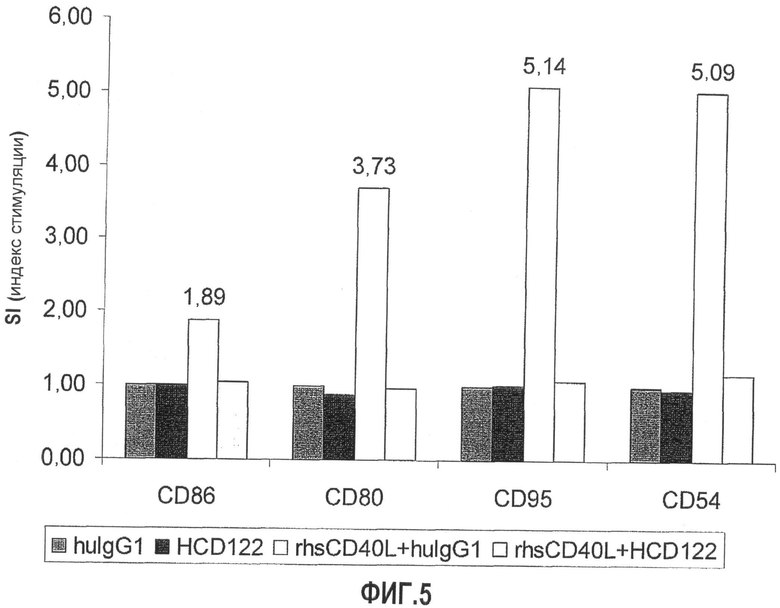



Группа изобретений относится к медицине и касается применения анти-CD40-антител в комбинации с CHOP для лечения заболеваний или состояний, ассоциированных с ростом неопластических B-клеток; где указанное заболевание или состояние является резистентным к терапии с использованием (i) CHOP, (ii) химерного моноклонального анти-CD20-антитела ритуксимаба или (iii) CHOP и ритуксимаба в виде комбинированной терапии, или пациент имел рецидив после терапии с использованием (i) CHOP, (ii) химерного моноклонального анти-CD20-антитела ритуксимаба или (iii) CHOP и ритуксимаба в виде комбинированной терапии. Группа изобретений обеспечивает синергическое терапевтическое действие при использовании комбинации по изобретению. 4 н. и 22 з.п. ф-лы, 4 пр., 6 ил., 2 табл.
1. Способ лечения пациента-человека в отношении заболевания или состояния, ассоциированного с ростом неопластических B-клеток, включающий введение указанному пациенту циклофосфамида, доксорубицина, винкристина и преднизона (CHOP) в комбинации с анти-CD40-антителом, где указанное анти-CD40-антитело не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека и указанное анти-CD40-антитело выбрано из группы, состоящей из:
a) моноклонального антитела HCD122, продуцируемого гибридомной клеточной линией, депонированной АТСС под номером депозита РТА-5543:
b) антитела, содержащего обе последовательности, показанные в SEQ ID NO:2 и SEQ ID NO:4, или обе последовательности, показанные в SEQ ID NO:2 и SEQ ID NO:5;
c) антитела, содержащего обе последовательности, показанные в SEQ ID NO:17 и SEQ ID NO:19, или обе последовательности, показанные в SEQ ID NO:17 и SEQ ID NO:20;
d) антитела, содержащего обе последовательности, показанные в SEQ ID NO:16 и SEQ ID NO:18;
e) антитела, имеющего аминокислотную последовательность, кодируемую последовательностью, показанной в SEQ ID NO:1, и амнокислотную последовательность, кодируемую последовательностью, показанной в SEQ ID NO:3, и;
f) антитела, имеющего вариабельный домен легкой цепи (VL), который содержит аминокислотную последовательность, показанную в SEQ ID NO:10, для CDR-L1, аминокислотную последовательность, показанную в SEQ ID NO:11, для CDR-L2, и аминокислотную последовательность, показанную в SEQ ID NO:12, для CDR-L3, и имеющего вариабельный домен тяжелой цепи (VH), который содержит аминокислотную последовательность, показанную в SEQ ID NO:13, для CDR-H1, аминокислотную последовательность, показанную в SEQ ID NO:14, для CDR-H2, и аминокислотную последовательность, показанную в SEQ ID NO:15, для CDR-H3;
где указанному пациенту ранее вводили (i) CHOP, (ii) химерное моноклональное анти-CD20-антитело ритуксимаба или (iii) терапевтическую комбинацию CHOP и ритуксимаба, и где указанное заболевание или состояние является резистентным к терапии с использованием (i) CHOP, (ii) химерного моноклонального анти-CD20-антитела ритуксимаба или (iii) комбинированной терапии с CHOP и ритуксимабом, или указанный пациент имел рецидив после терапии с использованием (i) CHOP, (ii) химерного моноклонального анти-CD20-антитела ритуксимаба или (iii) комбинированной терапии с CHOP и ритуксимабом.
2. Способ по п.1, где CHOP и анти-CD40-антитело вводят пациенту одновременно или последовательно.
3. Способ по п.2, где первый цикл CHOP вводят пациенту перед введением этому пациенту первой дозы анти-CD40-антитело.
4. Способ по п.2, где первый цикл CHOP вводят пациенту после введения этому пациенту первой дозы анти-CD40-антитело.
5. Способ по п.1, где указанное заболевание или состояние выбрано из группы, состоящей из острого лимфобластного лейкоза (ALL), острого миелогенного лейкоза (AML), хронического миелогенного лейкоза (CML), хронического лимфоцитарного лейкоза (CLL), пролимфоцитарного лейкоза (PLL), мелкоклеточного лимфоцитарного лейкоза (SLL), диффузного мелкоклеточного лимфоцитарного лейкоза (DSLL), диффузной крупноклеточной В-клеточной лимфомы (DLBCL), злокачественного гистиоцитарного ретикулоэндотелиоза, неходжкинских лимфом, болезни Ходжкина, индуцированных вирусом Эпштейна-Барра (EBV) лимфом, миелом, таких как множественная миелома, макроглобулинемин Вальденстрема, болезни тяжелых цепей, связанной со слизистой оболочкой лимфомы лимфоидной ткани, моноцитоидной В-клеточной лимфомы, селезеночной лимфомы, лимфогранулематоза, внутрисосудистого лимфоматоза, иммунобластных лимфом и связанных со СПИДом лимфом.
6. Способ по п.5, где указанным заболеванием или состоянием является неходжкинская лимфома.
7. Способ по п.6, где указанной неходжкинской лимфомой является диффузная крупноклеточная В-клеточная лимфома (DLBCL).
8. Способ по любому из пп.1-7, где указанное анти-CD40-антитело получают из клетки CHO, содержащей один или несколько экспрессирующих векторов, кодирующих это антитело.
9. Способ по любому из пп.1-7, где указанным анти-CD40-антителом является моноклональное антитело HCD122 (CHIR-12.12), продуцируемое гибридомной клеточной линией, депонированной АТСС под номером депозита РТА-5543.
10. Способ по любому из пп.1-7, где указанным анти-CD40-антителом является антигенсвязующий фрагмент антитела, выбранный из группы, состоящей из Fab-фрагмента, F(ab')2-фрагмента и Fv-фрагмента, где этот фрагмент не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека.
11. Способ предотвращения или уменьшения резистентности к цитотоксичности CHOP в неопластических В-клетках человека, включающий стадию контактирования одной или нескольких неопластических В-клеток человека с анти-CD40-антителом, где указанное анти-СD40-антнтело не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека и указанное анти-CD40-антитело выбрано из группы, состоящей из:
a) моноклонального антитела HCD 122, продуцируемого гибридомной клеточной линией, депонированной ATCC под номером депозита РТА-5543;
b) антитела, содержащего обе последовательности, показанные в SEQ ID NO:2 и SEQ ID NO:4, или обе последовательности, показанные в SEQ ID NO:2 и SEQ ID NO:5;
c) антитела, содержащего обе последовательности, показанные в SEQ ID NO:17 и SEQ ID NO:19, или обе последовательности, показанные в SEQ ID NO:17 и SEQ ID NO:20;
d) антитела, содержащего обе последовательности, показанные в SEQ ID NO:16 и SEQ ID NO:18;
e) антитела, имеющего аминокислотную последовательность, кодируемую последовательностью, показанной в SEQ ID NO:1, и аминокислотную последовательность, кодируемую последовательностью, показанной в SEQ ID NO:3, и;
f) антитела, имеющего вариабельный домен легкой цепи (VL), который содержит аминокислотную последовательность, показанную в SEQ ID NO:10, для CDR-L1, аминокислотную последовательность, показанную в SEQ ID NO:11, для CDR-L2, и аминокислотную последовательность, показанную в SEQ ID NO:12, для CDR-L3, и имеющего вариабельный домен тяжелой цепи (VH), который содержит аминокислотную последовательность, показанную в SEQ ID NO:13, для CDR-H1, аминокислотную последовательность, показанную в SEQ ID NO:14, для CDR-H2, и аминокислотную последовательность, показанную в SEQ ID NO:15, для CDR-H3.
12. Способ по п.11, где указанное антн-CD40-антитело получают из клетки СНО, содержащей один или несколько экспрессирующих векторов, кодирующих это антитело.
13. Способ по п.11, где указанным анти-CD40-антителом является моноклональное антитело HCD122 (CHIR-12.12), продуцируемое гибридомной клеточной линией, депонированной АТСС под номером депозита РТА-5543.
14. Способ по п.11, где указанным анти-CD40-антителом является антигенсвязующий фрагмент антитела, выбранный из группы, состоящей из Fab-фрагмента. F(ab')2-фрагмента и Fv-фрагмента, где этот фрагмент не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека.
15. Способ предотвращения или уменьшения резистентности B-клеток к цитотоксичности CHOP у пациента-человека, включающий стадию введения указанному пациенту анти-CD40-антитела, где указанное анти-CD40-антитело не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека, и указанное анти-CD40-антитело выбрано из группы, состоящей из:
a) моноклонального антитела HCD122, продуцируемого гибридомной клеточной линией, депонированной АТСС под номером депозита РТА-5543;
b) антитела, содержащего обе последовательности, показанные в SEQ ID NO:2 и SEQ ID NO:4, или обе последовательности, показанные в SEQ ID NO:2 и SEQ ID NO:5;
c) антитела, содержащего обе последовательности, показанные в SEQ ID NO:17 и SEQ ID NO:19, или обе последовательности, показанные в SEQ ID NO:17 и SEQ ID NO:20;
d) антитела, содержащего обе последовательности, показанные в SEQ ID NO:16 и SEQ ID NO:18;
е) антитела, имеющего аминокислотную последовательность, кодируемую последовательностью, показанной в SEQ ID NO:1, и аминокислотную последовательность, кодируемую последовательностью, показанной в SEQ ID NO:3, и;
f) антитела, имеющего вариабельный домен легкой цепи (VL), который содержит аминокислотную последовательность, показанную в SEQ ID NO:10, для CDR-L1, аминокислотную последовательность, показанную в SEQ ID NO:11, для CDR-L2, и аминокислотную последовательность, показанную в SEQ ID NO:12, для CDR-L3, и имеющего вариабельный домен тяжелой цепи (VH), который содержит аминокислотную последовательность, показанную в SEQ ID NO:13, для CDR-H1, аминокислотную последовательность, показанную в SEQ ID NO:14, для CDR-H2, и аминокислотную последовательность, показанную в SEQ ID NO:15, для CDR-H3.
16. Способ по п.15, где указанное анти-CD40-антитело получают из клетки CHO, содержащей один или несколько экспрессирующих векторов, кодирующих это антитело.
17. Способ по п.15, где указанным анти-CD40-антителом является моноклональное антитело HCD122 (CHIP-12.12), продуцируемое гибридомной клеточной линией, депонированной АТСС под номером депозита РТА-5543.
18. Способ по п.15, где указанным анти-CD40-антителом является антигенсвязующий фрагмент антитела, выбранный из группы, состоящей из Fab-фрагмента, F(ab')2- фрагмента и Fv-фрагмента, где этот фрагмент не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека.
19. Применение (i) циклофосфамида, доксорубицина, винкристина и преднизона и (ii) анти-CD40-антитела в производстве по меньшей мере двух отдельных лекарственных средств для лечения пациента-человека в отношении заболевания или состояния, ассоциированного с ростом неопластических В-клеток, комбинированной терапией, где указанное анти-CD40-аптитело не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека и указанное анти-CD40-антнтело выбрано из группы, состоящей из:
a) моноклонального антитела HCD122, продуцируемого гибридомной клеточной линией, депонированной АТСС под номером депозита РТА-5543;
b) антитела, содержащего обе последовательности, показанные в SEQ ID NO:2 и SEQ ID NO:4, или обе последовательности, показанные в SEQ ID NO:2 и SEQ ID NO:5;
c) антитела, содержащего обе последовательности, показанные в SEQ ID NO:17 и SEQ ID NO:19, или обе последовательности, показанные в SEQ ID NO:17 и SEQ ID NO:20:
d) антитела, содержащего обе последовательности, показанные в SEQ ID NO:16 и SEQ ID NO:18;
e) антитела, имеющего аминокислотную последовательность, кодируемую последовательностью, показанной в SEQ ID NO:1, и аминокислотную последовательность, кодируемую последовательностью, показанной в SEQ ID NO:3, и;
f) антитела, имеющего вариабельный домен легкой цепи (VL), который содержит аминокислотную последовательность, показанную в SEQ ID NO:10, для CDR-L1, аминокислотную последовательность, показанную в SEQ ID NO:11, для CDR-L2, и аминокислотную последовательность, показанную в SEQ ID NO:12, для CDR-L3, и имеющего вариабельный домен тяжелой цепи (VH), который содержит аминокислотную последовательность, показанную в SEQ ID NO:13, для CDR-H1, аминокислотную последовательность, показанную в SEQ ID NO:14, для CDR-H2, и аминокислотную последовательность, показанную в SEQ ID NO:15, для CDR-H3;
где указанному пациенту ранее вводили (i) CHOP, (ii) химерное моноклональное анти-CD20-антитело ритуксимаба или (iii) терапевтическую комбинацию CHOP и ритуксимаба, и где указанное заболевание или состояние является резистентным к терапии с использованием (i) CHOP, (ii) химерного моноклонального анти-CD20-антитела ритуксимаба или (iii) комбинированной терапии с CHOP и ритуксимабом, или указанный пациент имел рецидив после терапии с использованием (i) CHOP, (ii) химерного моноклонального анти-CD20-антитела ритуксимаба или (iii) комбинированной терапии с CHOP и ритуксимабом.
20. Применение по п.19, где указанное заболевание или состояние выбрано из группы, состоящей из острого лимфобластного лейкоза (ALL), острого миелогенного лейкоза (AML), хронического миелогенного лейкоза (CML), хронического лимфоцитарного лейкоза (CLL), пролимфоцитарного лейкоза (PLL), мелкоклеточного лимфоцитарного лейкоза (SLL), диффузного мелкоклеточного лимфоцитарного лейкоза (DSLL), диффузной крупноклеточной В-клеточной лимфомы (DLBCL), злокачественного гистиоцитарного ретикулоэндотелиоза, неходжкинских лимфом, болезни Ходжкина, индуцированных вирусом Эпштейна-Барра (EBV) лимфом, миелом, таких как множественная миелома, макроглобулинемии Вальденстрема, болезни тяжелых цепей, связанной со слизистой оболочкой лимфомы лимфоидной ткани, моноцитоидной В-клеточной лимфомы, селезеночной лимфомы, лимфогранулематоза, внутрисосудистого лимфоматоза, иммунобластных лимфом и связанных со СПИДом лимфом.
21. Применение по п.19, где указанное анти-CD40-антитело получают из клетки CHO, содержащей один или несколько экспрессирующих векторов, кодирующих это антитело.
22. Применение по п.19, где указанным анти-CD40-антителом является моноклональное антитело HCD122 (CHIR-12.12), продуцируемое гибридомной клеточной линией, депонированной ATCC под номером депозита РТА-5543.
23. Применение по п.19, где указанным анти-CD40-антителом является антигенсвязующий фрагмент антитела, выбранный из группы, состоящей из Fab-фрагмента, F(ab')2-фрагмента и Fv-фрагмента, где этот фрагмент не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека.
24. Применение по п.20, где указанное анти-CD40-антитело получают из клетки CHO, содержащей один или несколько экспрессирующих векторов, кодирующих это антитело.
25. Применение по п.20, где указанным анти-CD40-антителом является моноклональное антитело HCD122 (CHIP-12.12), продуцируемое гибридомной клеточной линией, депонированной АТСС под номером депозита РТА-5543.
26. Применение по п.20, где указанным анти-CD40-антителом является антигенсвязующий фрагмент антитела, выбранный из группы, состоящей из Fab-фрагмента, F(ab')2-фрагмента и Fv-фрагмента, где этот фрагмент не имеет значимой агонистической активности при связывании с антигеном CD40 на поверхности В-клеток человека.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Mohammad RM | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| RU 2005103824 A, 27.08.2005. | |||
Авторы
Даты
2013-08-27—Публикация
2008-11-07—Подача