Известны способы переработки отходов металлического бериллия с получением гидроксида путем растворения в различных средах: растворах щелочей, кислот, фторидных солей [С.С.Коровин, Г.В. Зулина, A.M. Резник, В.И. Букин, В.Ф. Корнюшко. Редкие и рассеянные элементы. Химия и технологии. М.: МИСИС, 1996, с.126].
Недостатком этих способов является высокая пожаровзрывоопасность, связанная с выделением водорода:
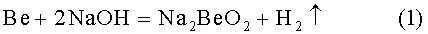
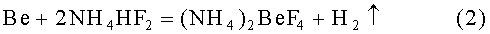
Известны способы электроэрозионного и электрохимического растворения металлов. Электроэрозионная обработка основана на разрушении металла под действием электрического разряда, проходящего через диэлектрическую среду, например, воду [Материаловедение и технология металлов / Сост. Г.П. Фетисов, М.Г. Карпман, В.М. Матюнин и др. М.: Высшая школа, 2000. С.598-599]. После накопления необходимого заряда между катодом и анодом происходит электрический пробой жидкости, в результате чего происходит диспергирование металла В зависимости от силы тока и частоты импульсов в процессе переработки металла могут быть получены либо гидроксид металла, либо порошок самого металла. При диспергировании металла с получением гидроксида выделяется водород, что не позволяет рекомендовать его для внедрения в промышленном производстве.
В основе электрохимического растворения лежит метод анодного растворения металла. В качестве электролита используются растворы сульфатов натрия или аммония. [Отчет ВНИИХТ, арх. №2107, 1984 г.]. Недостатком данного способа является значительное выделение аммиака в процессе электролиза и последующего кипячения раствора, большой расход электроэнергии, а также низкая производительность процесса.
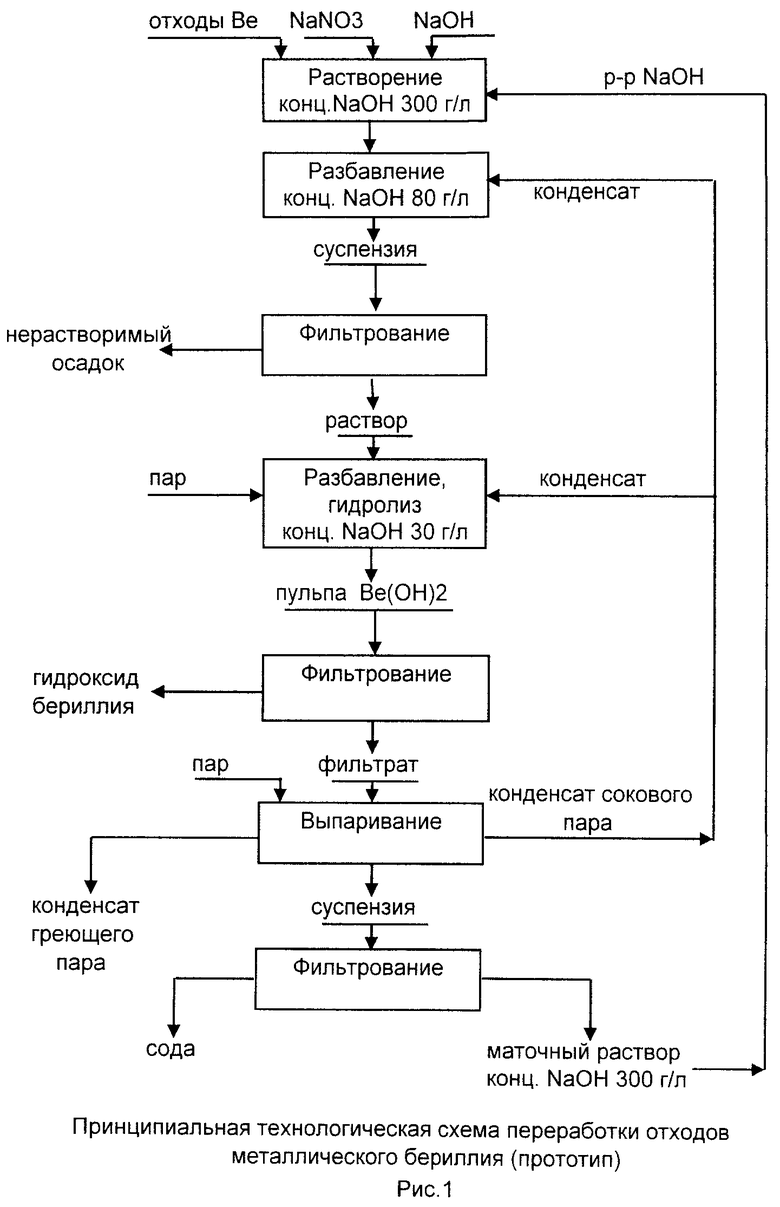
Наиболее близким является способ переработки металлических бериллиевых отходов, [патент РФ №2315714, МПК C01F 3/00]. Способ основан на растворении отходов бериллия в щелочном растворе с концентрацией 300 г/дм3 при температуре 85-110°С в присутствии нитрата натрия или калия, взятых в количестве 120-150% от стехиометрически необходимого по реакции образования газообразного аммиака, при продолжительности процесса 4 ч (реакция 3).
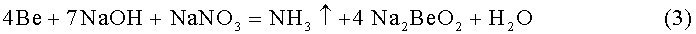
Выделение гидроксида бериллия осуществляют путем гидролиза бериллата натрия при его разбавлении до конц. 30 г/л NaOH и кипячении:
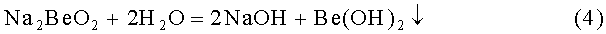
После отделения гидроксида бериллия фильтрованием маточный раствор выпаривают с целью концентрирования раствора щелочи с 30 до ~300 г/л NaOH. В процессе выпаривания происходит карбонизация части щелочи по реакции (5), в результате чего ~7% NaOH теряется в виде соды, которая отделяется при фильтровании упаренного раствора и выводится из технологического процесса.
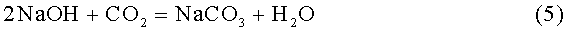
Концентрированный раствор щелочи вновь используют в процессе растворения следующей партии отходов.
Этот способ выбран в качестве прототипа.
Преимущество данного способа заключается в том, что вместо водорода в процессе реакции (3) выделяется аммиак. При этом его количество составляет 0,25 моль/моль бериллия вместо 1 моля по реакции (1). К недостаткам данного способа следует отнести высокую энергоемкость процесса, связанную с необходимостью нагрева и выпаривания больших объемов раствора, а также значительное обводнение процесса.
Предлагаемое техническое решение направлено на снижение энергопотребления, сокращение обводнения процесса и реализацию попутно получаемой товарной продукции - нитрата натрия.
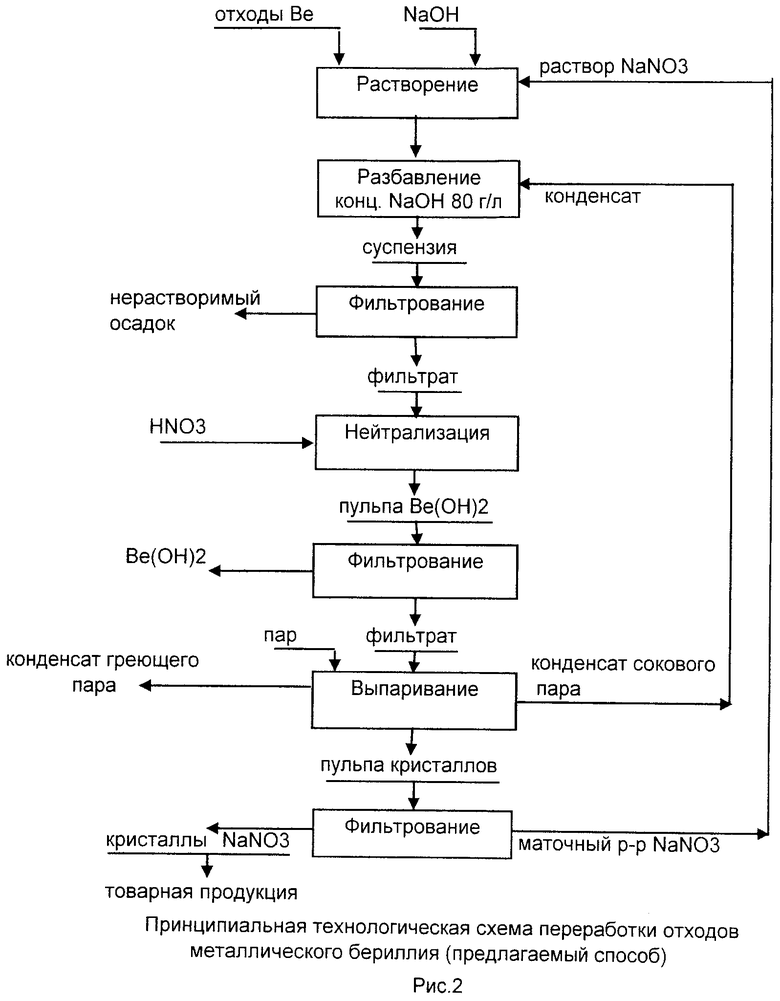
Технический результат достигается за счет того, что в способе переработки металлических бериллиевых отходов, включающем их растворение в щелочном растворе в присутствии нитрата натрия или калия с последующим выделением кристаллического гидроксида бериллия, в процесс дополнительно вводят азотную кислоту в количестве 2,09-2,26 моль/моль бериллия, которая нейтрализует избыток щелочи и бериллата натрия или калия с образованием нитрата натрия или калия и кристаллического гидроксида бериллия, причем часть нитрата натрия или калия используют для растворения следующей порции отходов, а остальной нитрат натрия или калия реализуют как попутно получаемую товарную продукцию.
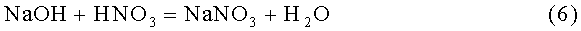
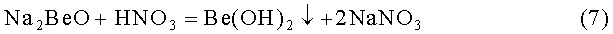
Нитрат натрия или калия не вносят непосредственно при каждой загрузке отходов бериллия на растворение, а вводят как оборотный продукт, полученный на последующих операциях технологического цикла;
После отделения гидроксида бериллия фильтрованием, раствор выпаривают с получением соли нитрата натрия. Часть полученного NaNO3 в количестве 105-115% от стехиометрически необходимого по реакции (3), что соответствует 0,26-0,29 моль/моль Be, направляют в «голову» процесса на растворение следующей партии отходов, остальной нитрат натрия может быть реализован как побочный товарный продукт. Натрий азотнокислый широко применяется в металлургической промышленности как компонент шихты закалочных ванн при обработке режущего инструмента, в производстве стекла и сельском хозяйстве (азотное удобрение).
Пример 1. Прототип
В качестве исходного материала использовали отходы с содержанием бериллия 95%, масса бериллия 100 г. Опыт проводили в герметичном аппарате. Навеску отходов массой 105,3 г помещали в аппарат, заливали насыщенный раствор нитрата натрия, затем добавляли раствор щелочи (конц. NaOH 300 г/л). Избыток реагентов брали из расчета 150% от стехиометрии по реакции (3). Растворение отходов проводили при температуре 85-110°C в течение 4 ч. После растворения отходов раствор бериллата натрия разбавляли до 80 г/л NaOH (для сохранения стойкости фильтрующего материала) и отфильтровывали нерастворимые примеси. Затем раствор бериллата натрия подвергали гидролизу (реакция 4). С целью обеспечения максимального выделения бериллия в виде гидроксида, раствор Na2BeO2 разбавляли до 30 г/л NaOH и проводили гидролиз в течение 1 часа при температуре кипения раствора. После охлаждения суспензии гидроксид бериллия отфильтровывали. Полученный при этом маточный раствор выпаривали до получения раствора NaOH конц. 300 г/л, который затем использовали в следующем цикле растворения отходов.
Пример 2. Предлагаемый способ
Опыт по растворению указанных выше отходов (100 г по бериллию, 105,3 по массе) проводили в аналогичных условиях: в герметичном аппарате при температуре 85-110°C в течение 4 ч, расход щелочи и нитрата натрия брали из расчета 110% от стехиометрии по реакции (3). После растворения отходов раствор бериллата натрия разбавляли до 80 г/л NaOH и отфильтровывали нерастворимые примеси. Затем полученный фильтрат нейтрализовали азотной кислотой в количестве 2,16 моль/моль Be до значения рН~7 (реакции 6 и 7). При этом осаждался гидроксид бериллия, который отфильтровывали. Фильтрат, представляющий собой раствор нитрат натрия, выпаривали с целью получения насыщенного раствора нитрата натрия, который использовали в следующем цикле растворения отходов бериллия и выделения товарных кристаллов нитрата натрия.
На рис.1 и 2 приведены принципиальные технологические схемы переработки отходов бериллия. Результаты экспериментов в равновесном режиме работы по прототипу и предлагаемому способу приведены в табл.1 и 2.
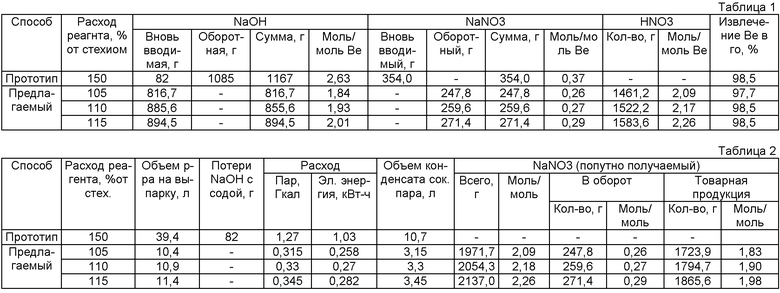
Сравнение данных, приведенных в табл.1, позволяет сделать вывод о достаточно высоком извлечении бериллия в гидроксид как по прототипу, так и предлагаемому способу. Однако расход NaOH и NaNOs во втором случае значительно меньше. Введение же сравнительно дешевой азотной кислоты обеспечивает существенное сокращение энергопотребления в случае работы по предлагаемому способу (табл.2), т.к. исключается необходимость значительного разбавления растворов при гидролизе бериллата натрия (по прототипу). Кроме того, при этом сокращается объем конденсата, образующегося в процессе выпаривания (~ в 3 раза), и появляется возможность получить дополнительную прибыль за счет реализации попутно получаемой продукции - соли нитрата натрия. Оптимальным в предлагаемом способе следует считать расход NaOH, NaNO3 и HNO3 соответственно 1,93, 0,27 и 2,17 моль/моль бериллия, поскольку при этом достигается высокое извлечение бериллия при меньшем расходе реагентов. Отклонение в сторону снижения расхода реагентов приводит к неполноте растворения отходов и, следовательно, к потере извлечения бериллия в гидроксид. Повышение же расхода реагентов неоправданно, т.к. оно не способствует повышению излечения бериллия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРЕРАБОТКИ МЕТАЛЛИЧЕСКИХ БЕРИЛЛИЕВЫХ ОТХОДОВ | 2006 |
|
RU2315714C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА БЕРИЛЛИЯ ИЗ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ | 2015 |
|
RU2598444C1 |
| Способ получения гидроксида бериллия из бериллийсодержащих концентратов | 2017 |
|
RU2668914C2 |
| СПОСОБ ПЕРЕРАБОТКИ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ | 2006 |
|
RU2309122C2 |
| СЛОИСТЫЕ ТИТАНАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2010 |
|
RU2564339C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИОЛИТА ИЗ АЛЮМИНИЙСОДЕРЖАЩЕГО РУДНОГО СЫРЬЯ | 2006 |
|
RU2317256C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА БЕРИЛЛИЯ | 2004 |
|
RU2264986C1 |
| Способ переработки жидких отходов АЭС с борным регулированием | 2017 |
|
RU2652978C1 |
| СПОСОБ ПЕРЕРАБОТКИ МЕТАЛЛИЧЕСКИХ ОТХОДОВ БЕРИЛЛИЯ | 2007 |
|
RU2351538C1 |
| СПОСОБ ПЕРЕРАБОТКИ ОТХОДОВ МЕТАЛЛИЧЕСКОГО БЕРИЛЛИЯ И СПЕЦКЕРАМИКИ НА ОСНОВЕ ОКСИДА БЕРИЛЛИЯ | 2012 |
|
RU2493101C1 |
Изобретение относится к переработке бериллийсодержащих металлических отходов. Способ включает растворение металлических бериллиевых отходов в щелочном растворе в присутствии нитрата натрия или калия. Вводят в процесс азотную кислоту в количестве 2,09-2,26 моль/моль бериллия. Азотная кислота нейтрализует избыток щелочи и бериллата натрия или калия с образованием нитрата натрия или калия и кристаллического гидроксида бериллия. Часть нитрата натрия или калия используют для растворения следующей порции отходов, а остальной нитрат натрия или калия реализуют как попутно получаемую товарную продукцию. Изобретение обеспечивает снижение энергопотребления, сокращение обводнения процесса и реализацию попутно получаемой товарной продукции - нитрата натрия. 2 з.п. ф-лы, 2 табл., 2 пр., 2 ил.
1. Способ переработки металлических бериллиевых отходов, включающий их растворение в щелочном растворе в присутствии нитрата натрия или калия с последующим выделением кристаллического гидроксида бериллия, отличающийся тем, что после растворения отходов в процесс дополнительно вводят азотную кислоту в количестве 2,09-2,26 моль/моль бериллия, которая нейтрализует избыток щелочи и бериллата натрия или калия с образованием нитрата натрия или калия и кристаллического гидроксида бериллия, причем часть нитрата натрия или калия используют для растворения следующей порции отходов, а остальной нитрат натрия или калия реализуют как попутно получаемую товарную продукцию.
2. Способ по п.1, отличающийся тем, что количество нитрата натрия или калия, возвращаемого на растворение бериллиевых отходов, составляет 0,26-0,29 моль/моль бериллия, а количество нитрата натрия или калия, реализуемого как попутный товарный продукт составляет 1,83-1,98 моль/моль бериллия.
3. Способ по п.1, отличающийся тем, что на растворение отходов расход щелочи составляет 1,84-2,01 моль/моль бериллия.
| СПОСОБ ПЕРЕРАБОТКИ МЕТАЛЛИЧЕСКИХ БЕРИЛЛИЕВЫХ ОТХОДОВ | 2006 |
|
RU2315714C1 |
| GB 1056825 A, 01.02.1967 | |||
| US 3615260 A, 26.10.1971 | |||
| Способ получения нитрида бериллия | 1974 |
|
SU535217A1 |
| СПОСОБ ПЕРЕРАБОТКИ МЕТАЛЛИЧЕСКИХ ОТХОДОВ БЕРИЛЛИЯ | 2007 |
|
RU2351538C1 |
Авторы
Даты
2013-09-10—Публикация
2012-05-23—Подача