Изобретение относится к области получения соединений бериллия, а именно гидроксида бериллия, широко используемого в производстве металлического бериллия, медно-бериллиевой лигатуры, керамики из оксида бериллия и солей бериллия.
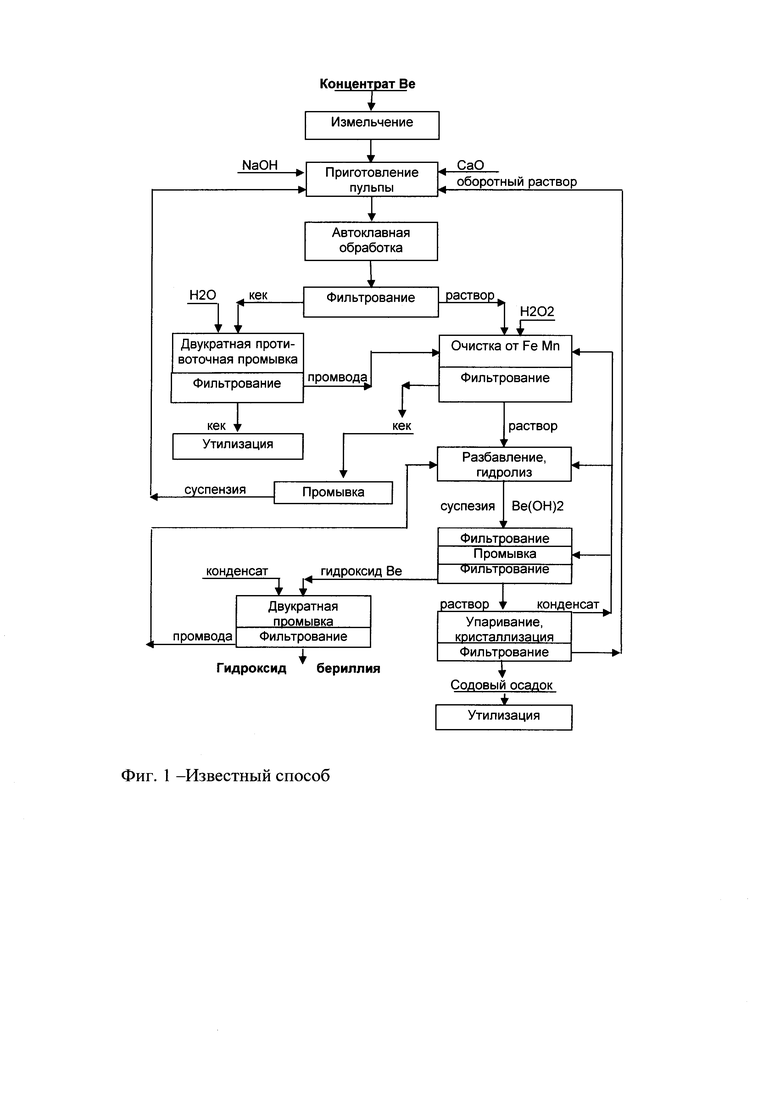
Известен способ [Патент RU №2264986, МПК CO1F 3/02] получения гидроксида бериллия из бериллийсодержащих концентратов путем воздействия гидроксида натрия с последующим разделением продуктов реакции. Концентрат или смесь концентратов обрабатывают в автоклаве гидроксидом натрия с концентрацией 400-450 г/дм3 в присутствии оксида кальция при мольном отношении CaO:SiO2=1,1-1,3, температуре 250-260°С и отношении Na2O:ВеО=12-13 в течение 4-5 ч. Принципиальная технологическая схема переработки концентратов по данному способу приведена на фиг. 1.
Недостатками указанного способа являются:
- значительные затраты энергии, связанные с разбавлением основного технологического раствора в 15 раз с 450 до 30 г /дм3 NaOH и необходимость ее последующего выпаривания из маточных растворов после выделения гидроксида бериллия;
- большое обводнение технологического процесса получения гидроксида бериллия;
- необходимость применения реагента (пероксида водорода) для очистки технологического раствора от примесей железа и марганца;
- необходимость организации участка утилизации бериллийсодержащей соды, образующейся в процессе выпаривания щелочного раствора (карбонизация щелочи).
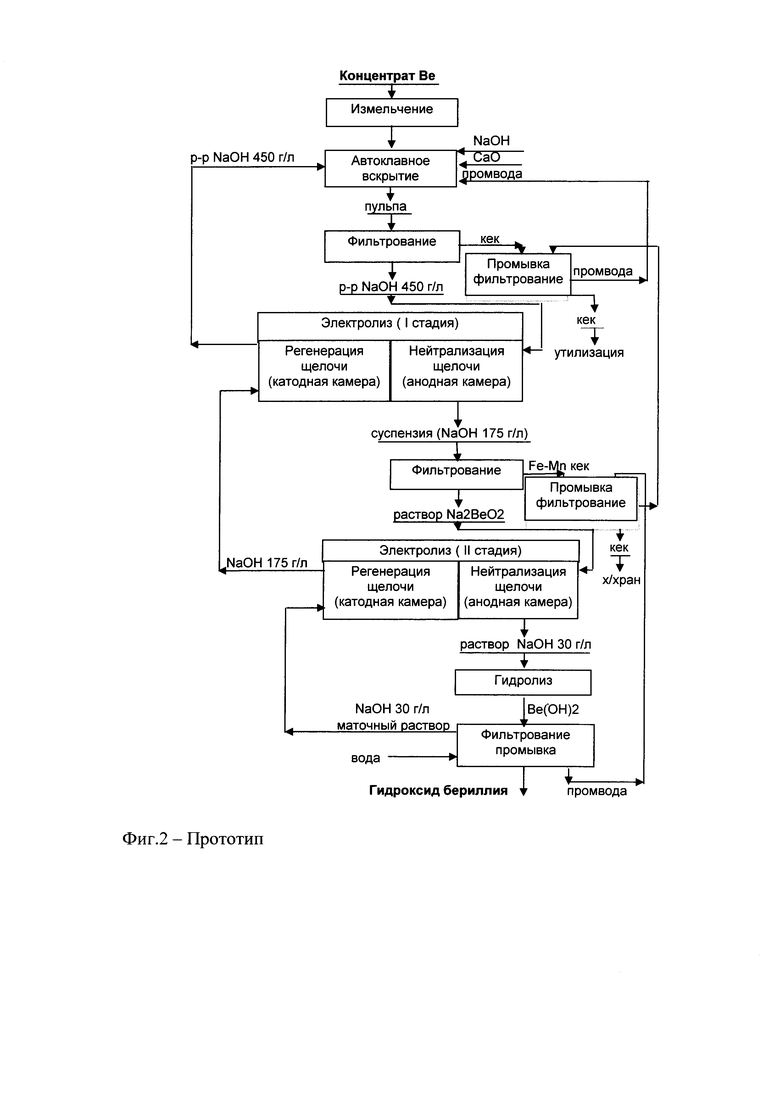
Наиболее близким является способ получения гидроксида бериллия методом щелочного автоклавного вскрытия с последующей переработкой щелочных растворов методом двухстадийного мембранного электролиза, (патент RU №2598444, МПК C01F 3/02). При этом электрохимическая нейтрализация щелочи в растворе осуществляется в анодных камерах электролизеров с одновременной регенерацией ее в катодных камерах после выделения целевого продукта (фиг. 2).
Недостатками данного способа (прототипа) являются:
- образование и выделение в осадок непосредственно в анодной камере нерастворимых гидроксидов железа и марганца в процессе электрохимической нейтрализации избытка щелочи на первой стадии электродиализа (исходная концентрация NaOH 450 г/л, конечная - 175 г/л NaOH);
- образование и выделение в осадок на второй стадии нейтрализации щелочи в анодной камере осадка гидроксида бериллия при постепенном снижении концентрации щелочи (исходная концентрация NaOH 175 г/л, конечная - 30 г/л NaOH).
- образование осадков непосредственно в камерах значительно затрудняет процесс электродиализа из-за необходимости периодической остановки процесса, зачистки поверхности камер и электродов от осадков гидроксидов железа и марганца на первой стадии электродиализа и от высокотоксичного гидроксида бериллия на второй;
- использование ручного труда для зачистки поверхности камер и электродов от токсичных продуктов значительно ухудшает санитарную обстановку на данном переделе;
- прерывание технологического процесса снижает производительность, технико-экономические показатели процесса и делает невозможным создание современного, отвечающего требованиям времени автоматизированного и экологически безопасного производства гидроксида бериллия.
Техническим результатом предлагаемого способа является упрощение технологии переработки концентрата за счет сокращения числа операций фильтрования, проведения нейтрализации и регенерации щелочи методом электродиализа в одну стадию, упрощения аппаратурной схемы, повышения производительности процесса получения гидроксида бериллия, снижения энергозатрат, возможности организации непрерывного процесса и его автоматизации.
Технический результат данного изобретения достигается за счет того, что в способе получения гидроксида бериллия из бериллийсодержащих концентратов путем воздействия на них концентрированных растворов гидроксида натрия предлагается:
1. Очистку щелочного раствора от железа и марганца проводить перед поступлением его в электродиализатор путем подачи кислорода в шламовую пульпу, полученную после автоклавного вскрытия, с последующим разделением фаз фильтрованием. При этом гидроксиды железа и марганца выводятся из системы вместе с натриево-кальциевым силикатным осадком, образующимся в процессе автоклавного вскрытия.
2. Для окисления железа и марганца использовать кислород, выделяющийся в анодной камере электродиализатора при прохождении тока через раствор щелочи за счет разряда ионов гидроксида на положительном заряженном аноде:
4 ОН--4е-=O2↑+2H2O
3. Нейтрализацию избытка щелочи в электролизере проводить в одну стадию с исходной концентрации 450 г/дм3 до границы устойчивости раствора бериллата натрия в интервале концентрации щелочи 100-70 г/дм3 (среднее значение ≈ 90 г/дм3 NaOH) (до начала выпадения осадка гидроксида бериллия). Предел устойчивости зависит от концентрации бериллия в растворе, его температуры, вязкости, общего солевого состава раствора, получаемого при переработке различных бериллийсодержащих концентратов.
4. После электролитического снижения концентрации щелочи в технологическом растворе с ≈450 г/л до ≈90 г/л NaOH, раствор бериллата натрия выводить из анодной камеры на операцию гидролиза.
5. Для сокращения времени гидролиза и обеспечения требуемой полноты извлечения бериллия процесс гидролиза проводить с введением затравки.
6. В качестве затравки использовать свежеосажденный гидроксид бериллия от предыдущего цикла гидролиза в количестве 10-30% от массы бериллия в исходном растворе.
7. Маточный раствор после отделения осадка гидроксида бериллия разделять на две части в соотношении 2:1, меньшую направлять на промывку кека после вскрытия концентрата, а большую часть - в катодную камеру электролизера для концентрирования щелочи до 450 г/дм3, требуемой для автоклавного вскрытия. Для обеспечения требуемой степени вскрытия бериллиевого концентрата в процессе автоклавного вскрытия используют щелочь (NaOH), количество которой определяется отношением Na2O:BeO - 1,1-1,3. В процессе автоклавного вскрытия происходит взаимодействие минералов, содержащихся в концентрате, с NaOH с образованием химических соединений типа криолитов, натриево-кальциевых силикатов, которые переходят в нерастворимый осадок (кек). С этими осадками безвозвратно теряется щелочь. Содержание щелочи в кеке в пересчете на натрий составляет 10-15%. Следовательно, на последующие операции поступает меньше щелочи, чем было ее в исходной загрузке на автоклавное вскрытие. Соответственно с оборотным раствором после прохождения всех последующих операций технологической цепочки на автоклавное вскрытие поступает меньше щелочи. Для обеспечения заданного соотношения Na2O:BeO в указанных выше пределах вводится гидроксид натрия в том количестве, которое теряется с отвальным кеком.
8. Предлагаемый способ может быть использован при переработке бериллийсодержащих отходов.
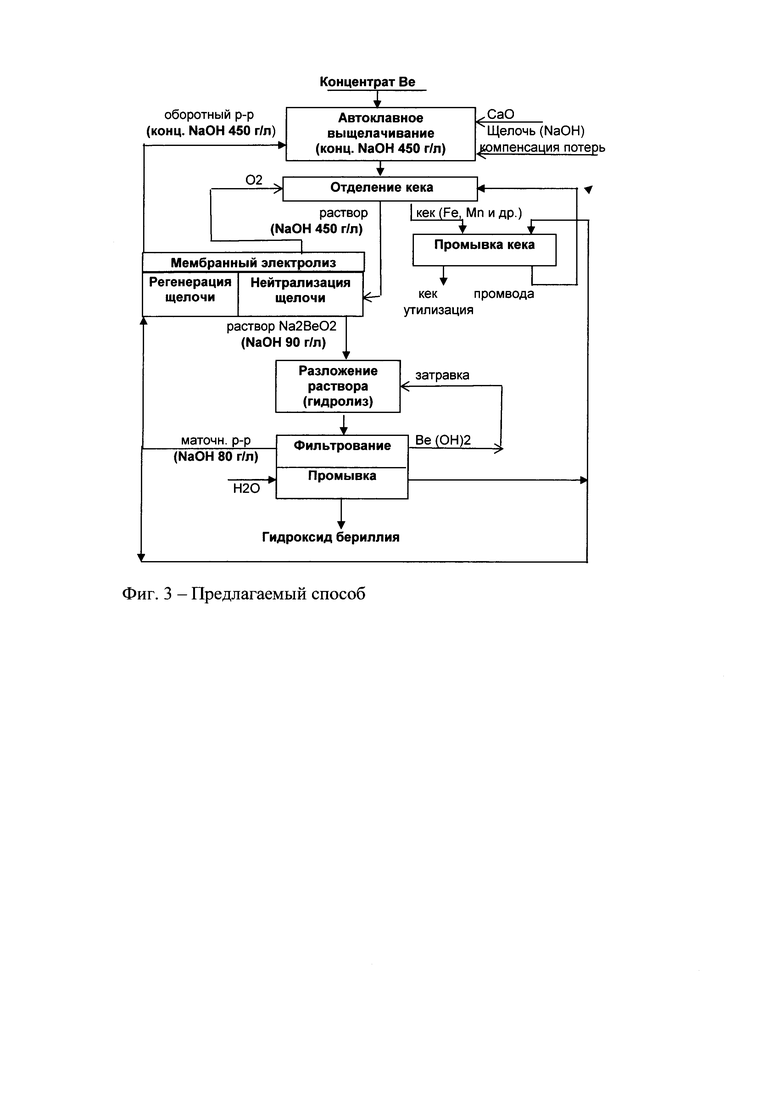
Принципиальная технологическая схема получения гидроксида бериллия из концентратов по предлагаемому способу приведена на фиг. 3.
Примеры осуществления способа
Исходный фенакит-бертрандитовый концентрат после измельчения до крупности 0,05 мм (95%) в количестве 110 г. смешивали с оксидом кальция в соотношении СаО:SiO2=1,2 и подвергали обработке растворами щелочи (концентрация NaOH 400-600 г/дм3, объемом 1 дм3) в автоклаве при температуре 250-260°С в течение 4 ч. После разгрузки автоклава полученную пульпу делили на 2 части: часть пульпы перерабатывали по способу-прототипу, а другую часть - по предлагаемому способу.
Пример 1. Получение гидроксида бериллия по способу-прототипу.
После охлаждения полученную пульпу фильтровали: кек подвергали отмывке от водорастворимого бериллия, а щелочной раствор направляли в анодную камеру электролизера для проведения 1-й стадии электрохимической нейтрализации щелочи. В ходе эксперимента использовали источник постоянного тока (Б5-46). Материал электродов: анод выполнен из никеля, катод - из нержавеющей стали. Анодные и катодные камеры электролизеров разделены катионообменными мембранами МК-40 на основе сорбента КУ-2. При пропускании постоянного тока в количестве 188 А⋅ч/дм3 в анодной камере содержание NaOH снижали до ~ 175 г/дм3. При этом кислород, выделяющийся в процессе электродиализа, окислял железо и марганец. Полученную суспензию фильтровали: Fe-Mn-кек отмывали от водорастворимого бериллия, а раствор направляли в анодную камеру электролизера для проведения 2-й стадии электрохимической нейтрализации щелочи до концентрации NaOH ~30 г/дм3 при пропускании тока в количестве 93,8 А⋅ч/дм3, после чего раствор бериллата натрия подвергали гидролизу при кипячении в течение 1 ч. Суммарный расход тока за 2 стадии нейтрализации составил 281,8 А⋅ч/дм3.
Выделившийся осадок гидроксида бериллия отделяли фильтрованием, промывали от избытка щелочи, высушивали и рассчитывали извлечение бериллия в гидроксид. Маточный раствор после гидролиза направляли в катодную камеру электролизера 2-й стадии, где под действием тока происходил обратный процесс образования гидроксильных ионов. При этом содержание щелочи повышалось до 170-180 г/дм3 NaOH. Полученный раствор направляли в катодную камеру электролизера 1-й стадии, где происходила регенерация реагента до требуемой концентрации (400-600 г/дм3 NaOH).
Пример 2. Получение гидроксида бериллия по предлагаемому способу.
Вторую часть пульпы, полученной после автоклавного вскрытия, охлаждали до ≈ 70°С, после чего с помощью полого керамического барботера в пульпу подавали кислород со скоростью 5 мл/мин в течение 30 мин. Затем пульпу фильтровали: кек подвергали отмывке от водорастворимого бериллия (фиг. 3).
Раствор с исходной щелочностью 450 г/л NaOH направляли в анодную камеру электролизера для нейтрализации. В ходе эксперимента использовали источник постоянного тока (Б5-46). Материал электродов: анод выполнен из никеля, катод - из нержавеющей стали. Анодные и катодные камеры электролизеров разделены катионообменными мембранами МК-40 на основе сорбента КУ-2. При пропускании постоянного тока в анодной камере в количестве 237 А⋅ч/дм3 содержание NaOH снижали до границы устойчивости раствора бериллата натрия (≈ 90 г/дм3), после чего раствор из анодной камеры разделяли по объему на 4 равных части, и затем каждую часть раствора подвергали гидролизу. Гидролиз проводили при температуре кипения в присутствии затравки в течение различного времени. В качестве затравки использовали заранее полученный свежеосажденный гидроксид бериллия (от предыдущего цикла получения гидроксида бериллия). Опыты проводили при введении затравки в количестве 5, 10, 20 и 30% по бериллию от содержания его в исходном растворе. При этом затравочное отношение (ЗО - массовое отношение ВеО в затравке к ВеО в бериллатном растворе) составляло соответственно 0,05; 0,1; 0,2; 0,3.
Выделившиеся в процессе гидролиза осадки гидроксида бериллия отделяли фильтрованием, промывали от избытка щелочи, высушивали и рассчитывали извлечение бериллия в гидроксид. Маточный раствор после гидролиза направляли в катодную камеру электролизера, где под действием тока происходил обратный процесс образования гидроксильных ионов. При этом содержание щелочи повышалось до требуемой концентрации (400-600 г/дм3 NaOH).
Сравнительные результаты получения гидроксида бериллия из концентрата по предложенному способу и прототипу приведены в таблицах 1-3.
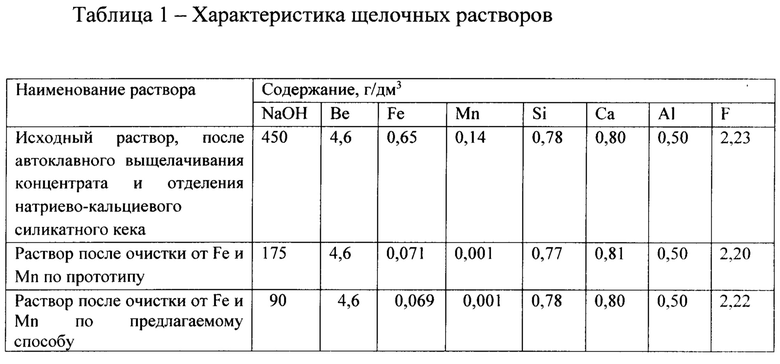
Как видно из таблицы, предложенный способ очистки технологического раствора от примеси железа и марганца путем барботирования кислорода непосредственно в пульпу после автоклавного вскрытия концентрата обеспечивает эффективную очистку от указанных примесей. Высокой степени очистки способствует также эффект соосаждения гидроксидов железа и марганца с натриево-кальциевым силикатным кеком автоклавного вскрытия концентрата.
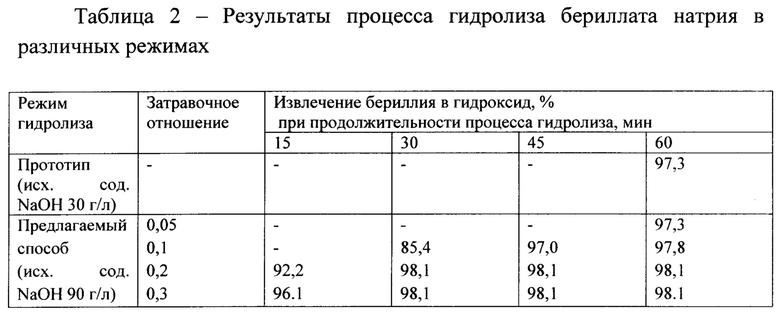
Как следует из таблицы 2, при проведении гидролиза бериллата натрия введение затравки обеспечивает сокращение продолжительности процесса и повышение извлечения бериллия в гидроксид до 98,1%.
Оптимальным затравочным отношением (ЗО) следует считать 0,2, при котором полнота осаждения бериллия достигается за 30 мин. В присутствии затравочных зерен кристаллизуемого вещества происходит образование новых дополнительных центров кристаллизации (вторичное зародышеобразование), что приводит к массовому и наиболее полному осаждению гидроксида бериллия за более короткое время. Дальнейшее увеличение затравочного отношения до 0,3 не оказывает существенного влияния на степень извлечения бериллия в гидроксид.
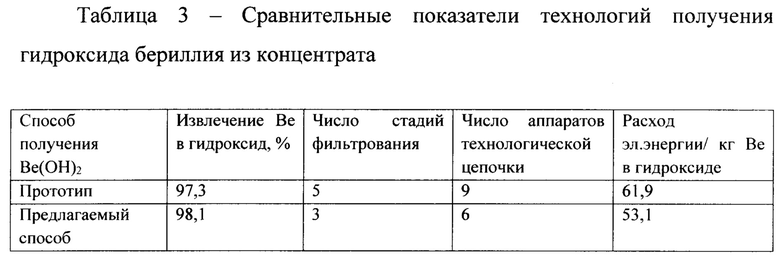
Примечание: водород, выделяющийся в катодных камерах электролизеров как по способу-прототипу, так и по предлагаемому способу, может быть аккумулирован геттерами или использован для получения пара.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА БЕРИЛЛИЯ ИЗ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ | 2015 |
|
RU2598444C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА БЕРИЛЛИЯ | 2004 |
|
RU2264986C1 |
| СПОСОБ ПЕРЕРАБОТКИ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ | 2006 |
|
RU2309122C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ БЕРИЛЛИЯ ИЗ БЕРИЛЛСОДЕРЖАЩЕГО СПОДУМЕНОВОГО КОНЦЕНТРАТА | 2008 |
|
RU2356963C2 |
| СПОСОБ ПЕРЕРАБОТКИ МЕТАЛЛИЧЕСКИХ БЕРИЛЛИЕВЫХ ОТХОДОВ | 2006 |
|
RU2315714C1 |
| СПОСОБ ПЕРЕРАБОТКИ МЕТАЛЛИЧЕСКИХ БЕРИЛЛИЕВЫХ ОТХОДОВ | 2012 |
|
RU2492144C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ БЕРИЛЛИЯ МЕТОДОМ ИОННОГО ОБМЕНА | 2014 |
|
RU2571763C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ БЕРИЛЛИЯ ИЗ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ | 2008 |
|
RU2350562C2 |
| СПОСОБ ПЕРЕРАБОТКИ БЕРТРАНДИТ-ФЕНАКИТ-ФЛЮОРИТОВЫХ КОНЦЕНТРАТОВ | 2006 |
|
RU2324653C2 |
| СПОСОБ ПЕРЕРАБОТКИ БЕРИЛЛИЕВОГО СЫРЬЯ | 1991 |
|
RU2040567C1 |
Изобретение может быть использовано при получении гидроксида бериллия, используемого в производстве металлического бериллия, медно-бериллиевой лигатуры, керамики из оксида бериллия и солей бериллия. Способ получения гидроксида бериллия из бериллийсодержащих концентратов включает воздействие концентрированным раствором гидроксида натрия, отделение раствора от кека, очистку раствора от железа и марганца. Затем проводят гидролиз бериллата натрия с получением гидроксида бериллия. Укрепляют маточные растворы после гидролиза добавлением твердого гидроксида натрия. Электрохимическую нейтрализацию избытка щелочи с исходной концентрацией 450 г/дм3 проводят в одну стадию до границы устойчивости раствора бериллата натрия в интервале концентрации щелочи 100-70 г/дм3 с последующим гидролизом раствора бериллата натрия. Очистку щелочного раствора от примесей железа и марганца проводят перед поступлением его в электродиализатор путем подачи кислорода в шламовую пульпу, полученную после автоклавного вскрытия, с последующим разделением фаз фильтрованием. Изобретение позволяет упростить технологию переработки бериллийсодержащих концентратов за счет сокращения числа операций, упрощения аппаратурной схемы, повышения производительности процесса получения гидроксида бериллия. 2 з.п. ф-лы, 3 ил., 3 табл., 2 пр.
1. Способ получения гидроксида бериллия из бериллийсодержащих концентратов путем воздействия на них концентрированным раствором гидроксида натрия, отделения раствора от кека, очистки раствора от железа и марганца, проведения гидролиза бериллата натрия с получением гидроксида бериллия и укрепления маточных растворов после гидролиза до концентрации, требуемой для вскрытия концентрата при прохождении его через катодные камеры электролизеров с компенсацией потерь щелочи добавлением твердого гидроксида натрия, отличающийся тем, что электрохимическую нейтрализацию избытка щелочи с исходной концентрацией 450 г/дм3 проводят в одну стадию до границы устойчивости раствора бериллата натрия в интервале концентрации щелочи 100-70 г/дм3 с последующим гидролизом раствора бериллата натрия, причем очистку щелочного раствора от примесей железа и марганца проводят перед поступлением его в электродиализатор путем подачи кислорода в шламовую пульпу, полученную после автоклавного вскрытия, с последующим разделением фаз фильтрованием.
2. Способ по п. 1, отличающийся тем, что для окисления железа и марганца методом барботажа пульпы используют кислород, выделяющийся в анодной камере электролизера при прохождении тока через раствор щелочи.
3. Способ по п. 1, отличающийся тем, что гидролиз раствора бериллата натрия проводят в присутствии свежеосажденной затравки от предыдущего цикла получения гидроксида бериллия, которую берут в количестве 20% от массы бериллия в исходном растворе, поступающем на гидролиз.
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА БЕРИЛЛИЯ ИЗ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ | 2015 |
|
RU2598444C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРИОЛИТА ИЗ АЛЮМИНИЙСОДЕРЖАЩЕГО РУДНОГО СЫРЬЯ | 2006 |
|
RU2317256C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА БЕРИЛЛИЯ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2338688C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ БЕРИЛЛИЯ МЕТОДОМ ИОННОГО ОБМЕНА | 2014 |
|
RU2571763C1 |
| US 5091160 A1, 25.02.1992 | |||
| CN 105585034 A, 18.05.2016. | |||
Авторы
Даты
2018-10-04—Публикация
2017-03-03—Подача