Текст описания приведен в факсимильном виде.




















































































































































































































































































































































































































| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ПОВЫШЕНИЯ УСИЛИВАЮЩЕЙ ЦЕЛЛЮЛОЛИТИЧЕСКОЙ АКТИВНОСТИ ПОЛИПЕПТИДА | 2008 |
|
RU2510417C2 |
| СПОСОБЫ УСИЛЕНИЯ ДЕГРАДАЦИИ ИЛИ ПРЕВРАЩЕНИЯ ЦЕЛЛЮЛОЗНОГО МАТЕРИАЛА | 2006 |
|
RU2441912C2 |
| СПОСОБ ОБРАБОТКИ ЦЕЛЛЮЛОЗНОГО МАТЕРИАЛА И ИСПОЛЬЗУЕМЫЕ В НЕМ ФЕРМЕНТЫ | 2006 |
|
RU2458128C2 |
| МОЮЩАЯ КОМПОЗИЦИЯ | 2015 |
|
RU2737535C2 |
| ЦЕЛЛЮЛОЗНЫЕ БЕЛКИ СЛИЯНИЯ И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2458127C2 |
| ГЕН ABFB-2 PENICILLIUM FUNICULOSUM | 2006 |
|
RU2388820C2 |
| ПОЛИПЕПТИДЫ, ОБЛАДАЮЩИЕ ЭНДОПЕПТИДАЗНОЙ АКТИВНОСТЬЮ, И КОДИРУЮЩИЕ ИХ ПОЛИНУКЛЕОТИДЫ | 2011 |
|
RU2583293C2 |
| ПОЛИПЕПТИДЫ С ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ И КОДИРУЮЩИЕ ИХ ПОЛИНУКЛЕОТИДЫ | 2005 |
|
RU2393224C2 |
| ПОЛИПЕПТИДЫ, ОБЛАДАЮЩИЕ АНТИМИКРОБНОЙ АКТИВНОВНОСТЬЮ, И ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ ИХ | 2006 |
|
RU2512525C2 |
| Композиции, содержащие липазы, и способы обработки поверхности | 2013 |
|
RU2612215C2 |
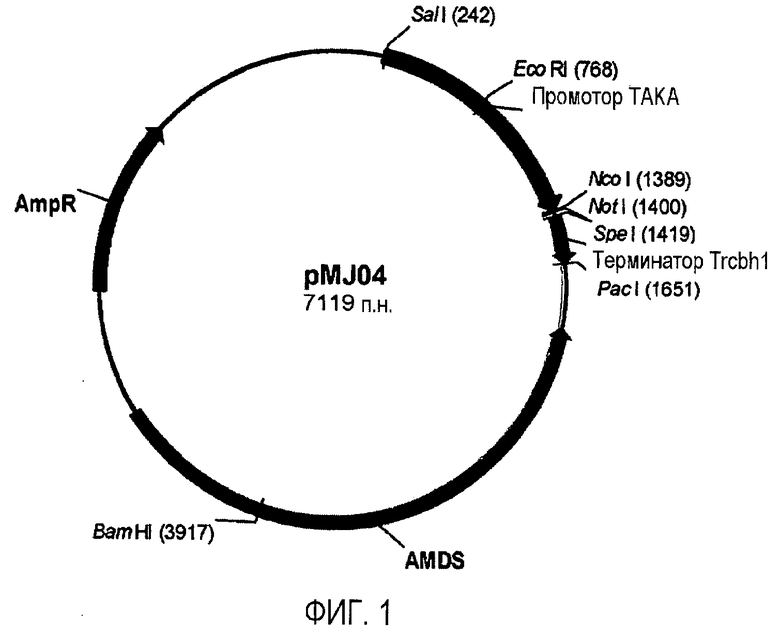
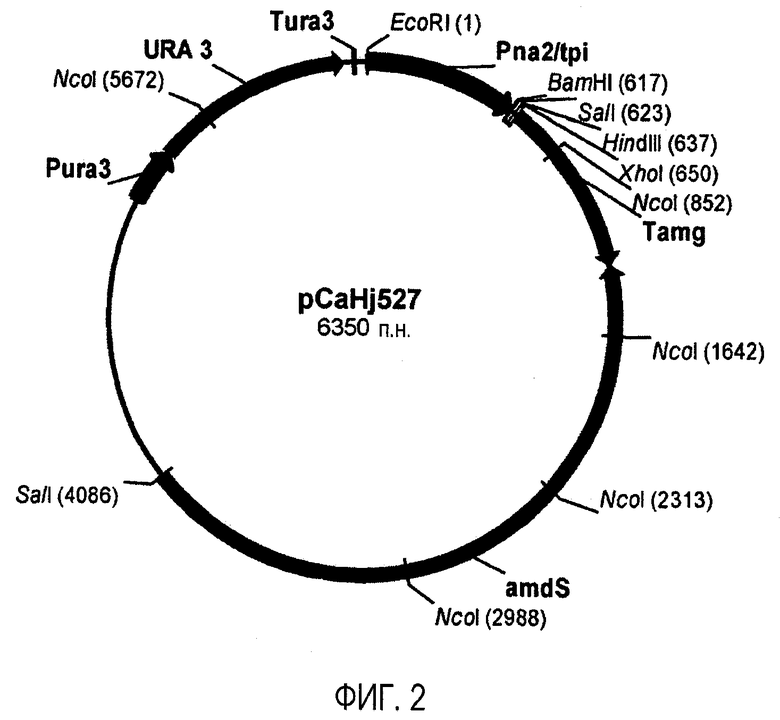
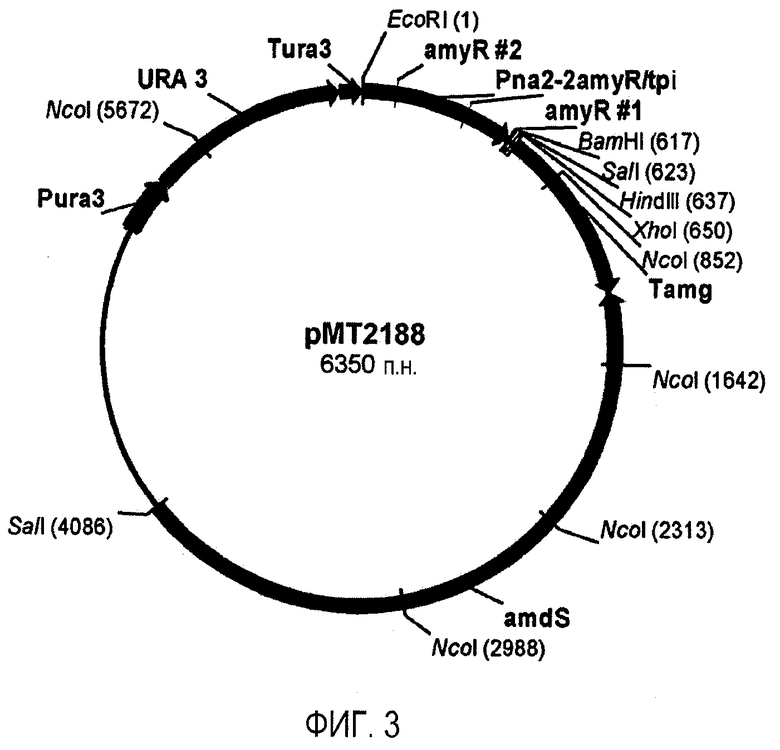
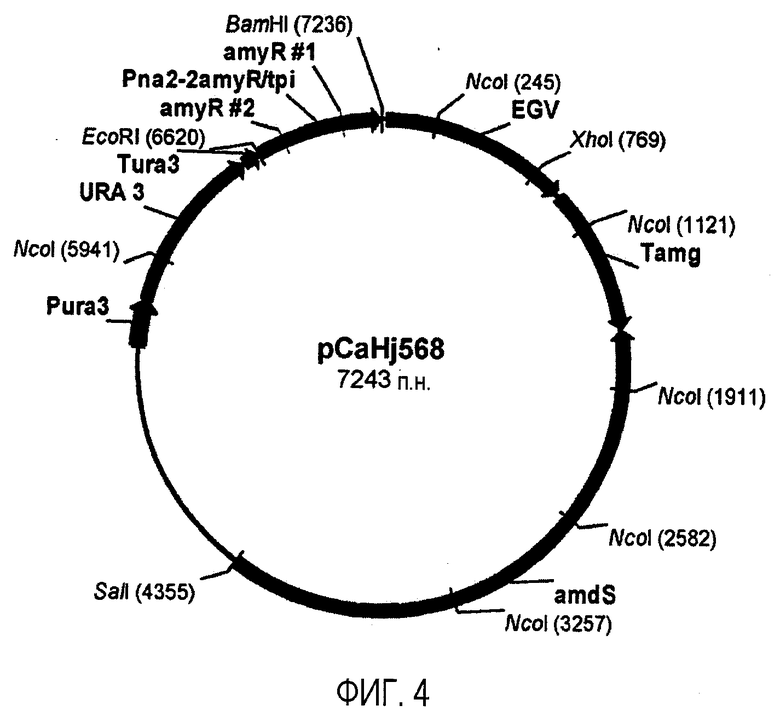
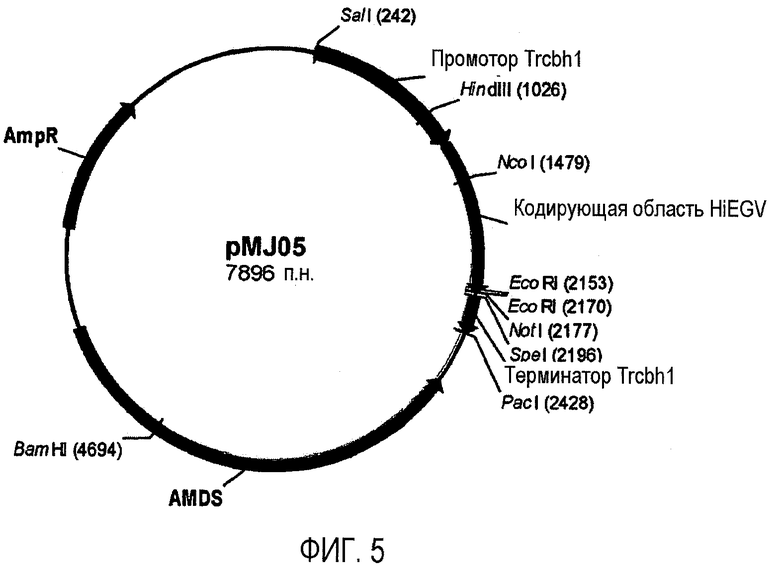
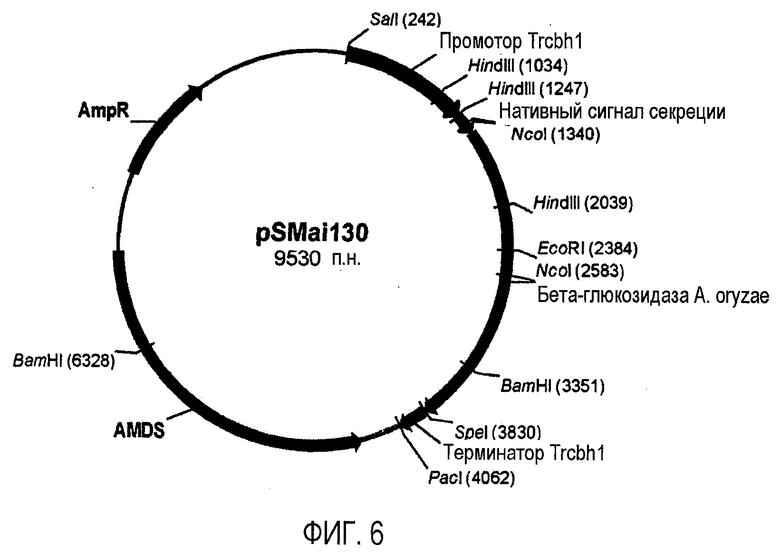
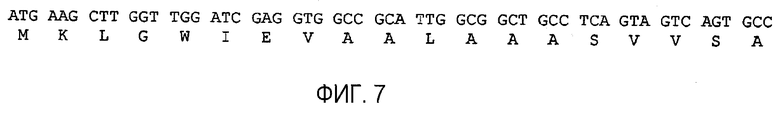

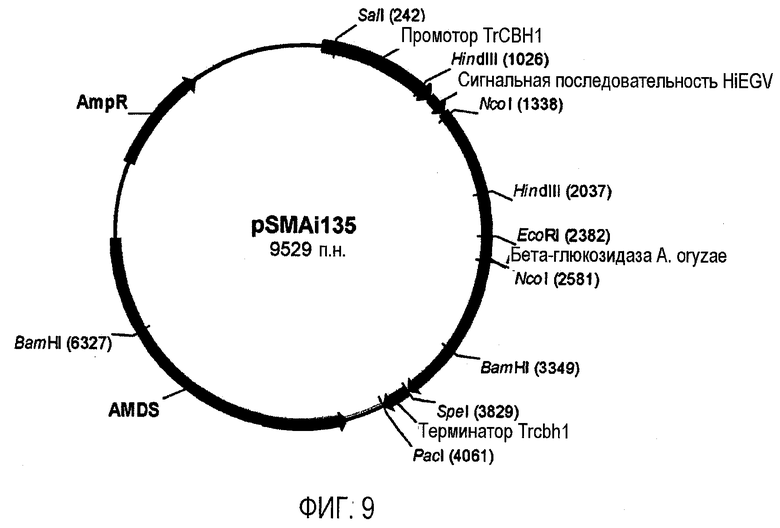
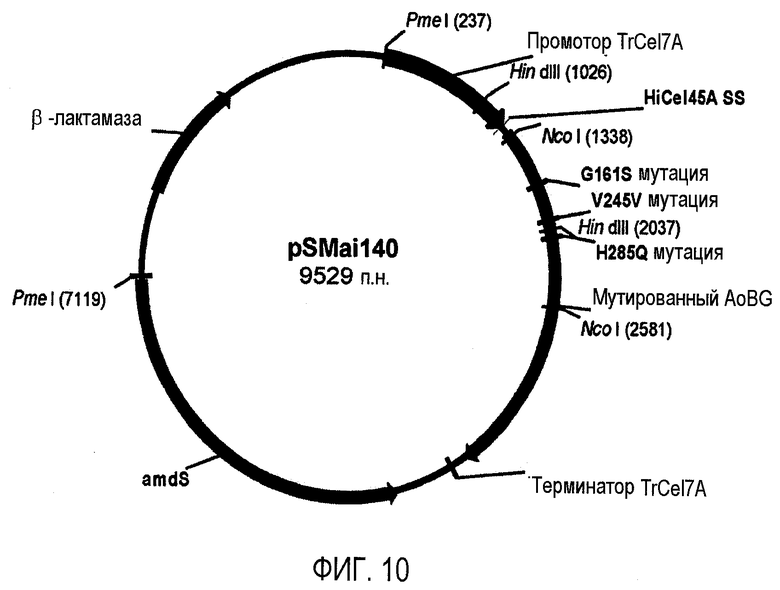
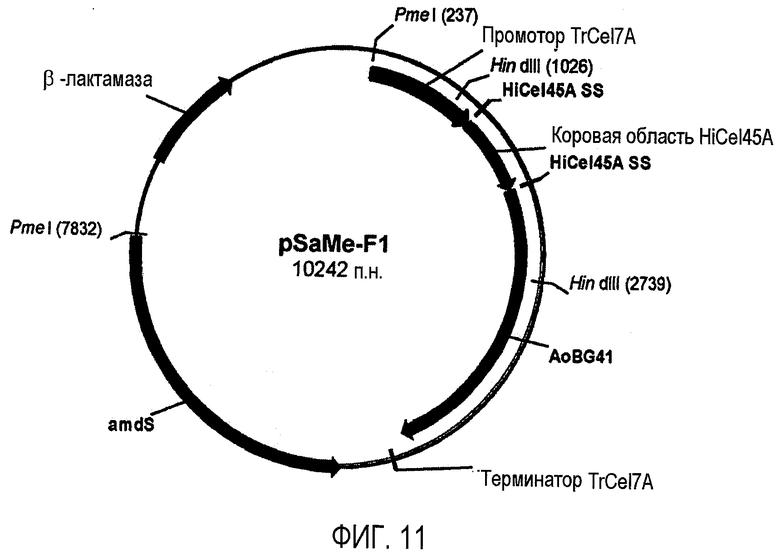

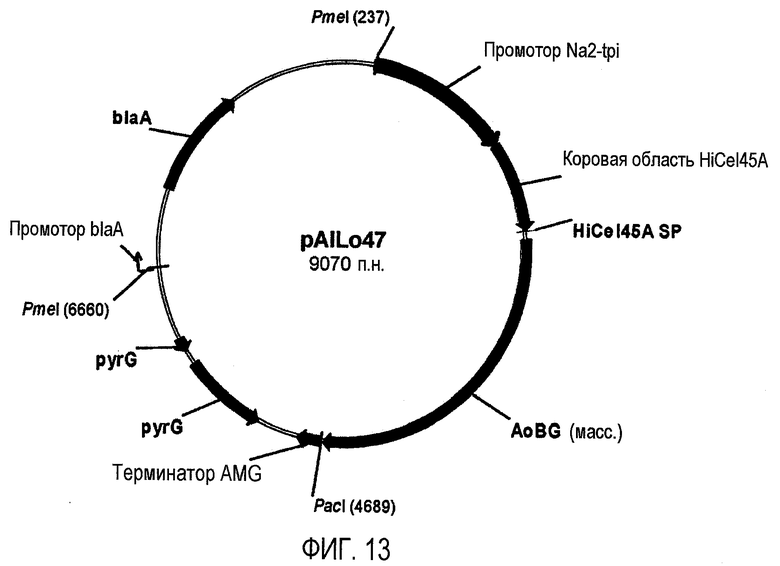
Изобретение относится к области биотехнологии, а именно к клетке-хозяину Trichoderma reesei для получения целлюлолитической белковой композиции, целлюлолитической белковой композиции, способам получения и применения композиции. Клетка-хозяин Trichoderma reesei содержит полинуклеотиды, кодирующие гетерологичный полипептид GH61, слитый белок бета-глюкозидазы, целлюлолитические ферменты. Способ получения композиции включает культивирование клетки-хозяина Trichoderma reesei и выделение композиции. Композиция содержит полипептид GH61, слитый белок бета-глюкозидазы и один или более целлюлолитических ферментов. Способ разложения материала, содержащего целлюлозу, характеризуется обработкой материала целлюлолитической белковой композицией. Способ получения продукта ферментации включает осахаривание материала, ферментацию осахаренного материала сбраживающими микроорганизмами и выделение продуктов ферментации. Представленные изобретения могут быть использованы для разложения или преобразования материала, содержащего целлюлозу. 5 н. и 7 з.п. ф-лы, 14 ил., 23 пр.
1. Клетка-хозяин Trichoderma reesei, использующаяся для получения целлюлолитической ферментной композиции, содержащая: (a) первый полинуклеотид, кодирующий гетерологичный полипептид GH61, обладающий усиливающей целлюлолитическое действие активностью; (b) второй полинуклеотид, кодирующий слитый белок бета-глюкозидазы с последовательностью SEQ ID NO:104 и SEQ ID NO:106; и (c) третий полинуклеотид, один или несколько, кодирующий целлюлолитические ферменты, выбранные из группы, состоящей из целлобиогидролазы I (CEL7A) Trichoderma reesei, целлобиогидролазы II (CEL6A) Trichoderma reesei и эндоглюканазы I (CEL7B) Trichoderma reesei, и их ортолога или варианта;
где Trichoderma reesei целлобиогидролаза I (CEL7A) или ее ортолог или ее вариант, кодируемые одним или несколькими третьими полинуклеотидами, выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:52;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:51, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:51, кодирующий зрелый полипептид;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:52; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:52;
где целлобиогидролазы II (CEL6A) Trichoderma reesei или ее ортолог или ее вариант, кодируемые одним или несколькими третьими полинуклеотидами, выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:54;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:53, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:53, кодирующий зрелый полипептид;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:54; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:54;
где эндоглюканаза Trichoderma reesei (CEL7B) или ее ортолог или вариант, кодируемые одним или несколькими третьими полинуклеотидами, выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:56;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:55, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом белке с последовательностью SEQ ID NO:56; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:56;
где клетка-хозяин Trichoderma reesei трансформирована первым и вторым полинуклеотидом, а также одним или несколькими третьими полинуклеотидами, кодирующими указанный ортолог или вариант, где каждый функционально связан с контрольными последовательностями, которые контролируют их экспрессию; и
где клетка-хозяин Trichoderma reesei продуцирует целлюлолитическую ферментную композицию, содержащую полипептиды, которые кодируются первым, вторым или третьим нуклеотидами,
где полипептид GH61, обладающий усиливающей целлюлолитическое действие активностью, выбран из группы, состоящей из:
(a) полипептида GH61, обладающего усиливающей целлюлолитическое действие активностью и содержащего [ILMV]-P-X(4,5)-G-X-Y-[ILMV]-X-R-X-[EQ]-X(4)-A-[HNQ] и [FW]-[TF]-K-[AIV], где X представляет собой любую аминокислоту, X(4,5) представляет собой любую аминокислоту в 4 или 5 смежных положениях и X(4) представляет собой любую аминокислоту в 4 смежных положениях;
(b) полипептида GH61, обладающего усиливающей целлюлолитическое действие активностью и содержащего [ILMV]-P-x(4,5)-G-x-Y-[ILMV]-x-R-x-[EQ]-x(3)-A-[HNQ], где x означает любую аминокислоту, x(4,5) означает любую аминокислоту в 4 или 5 смежных положениях и x(3) означает любую аминокислоту в 3 смежных положениях;
где указанный полипептид, обладающий усиливающей целлюлолитическое действие активностью и содержащий [ILMV]-P-X(4,5)-G-X-Y-[ILMV]-X-R-X-[EQ]-X(4)-[HNQ] и [FW]-[TF]-K-[AIV], необязательно дополнительно содержит:
Н-Х(1,2)-G-P-X(3)-[YW]-[AILMV],
[EQ]-X-Y-X(2)-C-X-[EHQN]-[FILV]-X-[ILV] или
H-X(1,2)-G-P-X(3)-[YW]-[AILMV] и [EQ]-X-Y-X(2)-C-X-[EHQN]-[FILV]-X-[ILV],
где X представляет собой любую аминокислоту, X(1,2) представляет собой любую аминокислоту в 1 положении или 2 смежных положениях, X(3) представляет собой любую аминокислоту в 3 смежных положениях и X(2) представляет собой любую аминокислоту в 2 смежных положениях;
(c) полипептида GH61, содержащего аминокислотную последовательность, которая, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% и по меньшей мере на 95% или на 100% идентична последовательности зрелого полипептида SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8 или SEQ ID NO:10, SEQ ID NO:12 или SEQ ID NO:14;
(d) полипептида GH61, кодируемого полинуклеотидом, который гибридизуется по меньшей мере в условиях умеренной жесткости, по меньшей мере в условиях умеренно-высокой жесткости, по меньшей мере в условиях высокой жесткости или по меньшей мере в условиях очень высокой жесткости с последовательностью SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:11 или SEQ ID NO:13, или с их полноразмерными комплементарными цепями;
(e) полипептида GH61, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или на 100% идентична последовательности SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:11 или SEQ ID NO:13, кодирующей зрелый полипептид;
(f) варианта полипептида GH61, обладающего усиливающей целлюлолитическое действие активностью, содержащего замену, делецию и/или инсерцию одной или нескольких аминокислот зрелого полипептида с последовательностью SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8 или SEQ ID NO:10, SEQ ID NO:12 или SEQ ID NO:14; и
(g) полипептида GH61, обладающего усиливающей целлюлолитическое действие активностью и содержащего или состоящего из зрелого полипептида с последовательностью SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8 или SEQ ID NO:10, SEQ ID NO:12 или SEQ ID NO:14; или их фрагмента, обладающего усиливающей целлюлолитическое действие активностью.
2. Клетка-хозяин Trichoderma reesei по п.1, которая дополнительно содержит один или несколько четвертых полинуклеотидов, кодирующих целлюлолитические ферменты, выбранные из группы, состоящей из эндоглюканазы II (CEL5A) Trichoderma reesei, эндоглюканазы III (CEL12A) Trichoderma reesei и эндоглюканазы V (CEL45A) Trichoderma reesei, и их ортолога или варианта,
где эндоглюканаза II Trichoderma reesei (CEL5A) или ее ортолог или ее вариант, кодируемые одним или несколькими четвертыми полинуклеотидами, выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:58;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:57, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:57, кодирующий зрелый полипептид;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:58; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:58;
где эндоглюканаза III Trichoderma reesei (CEL12A) или ее ортолог, или ее вариант, кодируемые одним или несколькими четвертыми полинуклеотидами, выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:60;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:59, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:59, кодирующий зрелый полипептид;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:60; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:60; и
где эндоглюканаза V Trichoderma reesei (CEL45A) или ее ортолог, или ее вариант, кодируемые одним или несколькими четвертыми полинуклеотидами, выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:62;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:61, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:61, кодирующий зрелый полипептид; и
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:62; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:62.
3. Клетка-хозяин Trichoderma reesei по п.1, которая продуцирует целлюлолитическую белковую композицию, содержащую полипептид GH61, обладающий усиливающей целлюлолитическое действие активностью зрелого полипептида с последовательностью SEQ ID NO:12, бета-глюкозидазный слитый белок с последовательностью SEQ ID NO:104 и SEQ ID NO:106; целлобиогидролазу I (CEL7A) Trichoderma reesei зрелого полипептида SEQ ID NO:52, целлобиогидролазу II (CEL6A) Trichoderma reesei зрелого полипептида с последовательностью SEQ ID NO:54 и эндоглюканазу I (CEL7B) Trichoderma reesei зрелого полипептида с последовательностью SEQ ID NO:56.
4. Клетка-хозяин Trichoderma reesei по п.3, которая дополнительно продуцирует один или более ферментов, выбранных из группы, состоящей из эндонуклеазы II (CEL5A) Trichoderma reesei SEQ ID NO:58, эндоглюканазы V (CEL45A) Trichoderma reesei с последовательностью SEQ ID NO:62 и эндоглюканазы III (CEL12A) Trichoderma reesei с последовательностью SEQ ID NO:60.
5. Способ получения целлюлолитической белковой композиции, включающий: (а) культивирование клетки-хозяина Trichoderma reesei по любому из пп.1-4 в условиях, способствующих получению указанной композиции; и (b) выделение указанной композиции.
6. Целлюлолитическая белковая композиция, содержащая: (a) полипептид GH61, обладающий усиливающей целлюлолитическое действие активностью; (b) слитый белок бета-глюкозидазы с последовательностью SEQ ID NO:104 или SEQ ID NO:106; и (c) один или более целлюлолитических ферментов, выбранных из группы, состоящей из целлобиогидролазы I (CEL7A) Trichoderma reesei, целлобиогидролазы II (CEL6A) Trichoderma reesei и эндоглюканазы I (CEL7B) Trichoderma reesei, и его ортолог или вариант;
где целлобиогидролаза I Trichoderma reesei (CEL7A) или ее ортолог или ее вариант выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:52;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:51, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:51, кодирующий зрелый полипептид;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:52; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:52;
где целлобиогидролаза II Trichoderma reesei (CEL6A) или ее ортолог или ее вариант выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:54;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:53, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:53, кодирующий зрелый полипептид;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:54; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:54;
где эндоглюканаза I Trichoderma reesei (CEL7B) или ее ортолог или ее вариант выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:56;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:55, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:55, кодирующий зрелый полипептид;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:56; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:56.
7. Целлюлолитическая белковая композиция по п.6, где полипептид GH61, обладающий усиливающей целлюлолитическое действие активностью, выбран из группы, состоящей из:
(a) полипептида GH61, обладающего усиливающей целлюлолитическое действие активностью и содержащего [ILMV]-P-X(4,5)-G-X-Y-[ILMV]-X-R-X-[EQ]-X(4)-[HNQ] и [FW]-[TF]-K-[AIV], где Х представляет собой любую аминокислоту, Х(4,5) представляет собой любую аминокислоту в 4 или 5 смежных положениях и Х(4) представляет собой любую аминокислоту в 4 смежных положениях;
(b) полипептида GH61, обладающего усиливающей целлюлолитическое действие активностью и содержащего [ILMV]-P-x(4,5)-G-x-Y-[ILMV]-x-R-x-[EQ]-x(3)-A-[HNQ], где x означает любую аминокислоту, x(4,5) означает любую аминокислоту в 4 или 5 смежных положениях и x(3) означает любую аминокислоту в 3 смежных положениях;
где указанный полипептид, обладающий усиливающей целлюлолитическое действие активностью и содержащий [ILMV]-P-X(4,5)-G-X-Y-[ILMV]-X-R-X-[EQ]-X(4)-[HNQ] и [FW]-[TF]-K-[AIV], необязательно дополнительно содержит:
H-X(1,2)-G-P-X(3)-[YW]-[AILMV],
[EQ]-X-Y-X(2)-C-X-[EHQN]-[FILV]-X-[ILV] или
H-X(1,2)-G-P-X(3)-[YW]-[AILMV]H[EQ]-X-Y-X(2)-C-X-[EHQN]-[FILV]-X-[ILV],
где X представляет собой любую аминокислоту, Х(1,2) представляет собой любую аминокислоту в 1 положении или 2 смежных положениях, Х(3) представляет собой любую аминокислоту в 3 смежных положениях и Х(2) представляет собой любую аминокислоту в 2 смежных положениях;
(c) полипептида GH61, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% и по меньшей мере на 95% или на 100% идентична последовательности зрелого полипептида SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8 или SEQ ID NO:10, SEQ ID NO:12 или SEQ ID NO:14;
(d) полипептида GH61, кодируемого полинуклеотидом, который гибридизуется по меньшей мере в условиях умеренной жесткости, по меньшей мере в условиях умеренно-высокой жесткости, по меньшей мере в условиях высокой жесткости или по меньшей мере в условиях очень высокой жесткости с последовательностью SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:11 или SEQ ID NO:13, или с ее полноразмерной комплементарной цепью;
(e) полипептида GH61, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или на 100% идентична последовательности SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:11 или SEQ ID NO:13, кодирующей зрелый полипептид;
(f) варианта полипептида GH61, обладающего усиливающей целлюлолитическое действие активностью, содержащего замену, делецию и/или инсерцию одной или нескольких аминокислот зрелого полипептида с последовательностью SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8 или SEQ ID NO:10, SEQ ID NO:12 или SEQ ID NO:14; и
(g) полипептида GH61, обладающего усиливающей целлюлолитическое действие активностью и содержащего или состоящего из зрелого полипептида с последовательностью SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8 или SEQ ID NO:10, SEQ ID NO:12 или SEQ ID NO:14; или его фрагмента, обладающего усиливающей целлюлолитическое действие активностью.
8. Целлюлолитическая белковая композиция по п.6, которая дополнительно содержит один или несколько целлюлолитических ферментов, выбранных из группы, состоящей из эндоглюканазы II (CEL5A) Trichoderma reesei, эндоглюканазы III (CEL12A) Trichoderma reesei и эндоглюканазы V(CEL45A) Trichoderma reesei, и его ортолог или его вариант;
где целлобиогидролаза II Trichoderma reesei (CEL5A) или ее ортолог или ее вариант выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:58;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:57, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:57, кодирующий зрелый полипептид;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:58; и
(е) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:58;
где эндоглюканаза III Trichoderma reesei (CEL12A) или ее ортолог или ее вариант, выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:60;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:59, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду, кодирующегося последовательностью SEQ ID NO:59;
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом белке с последовательностью SEQ ID NO:60; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:60; и
где эндоглюканаза V Trichoderma reesei (CEL45A) или ее ортолог или ее вариант выбраны из группы, состоящей из:
(a) полипептида, содержащего аминокислотную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична зрелому полипептиду с последовательностью SEQ ID NO:62;
(b) полипептида, кодируемого полинуклеотидом, который гибридизуется в условиях по меньшей мере средней жесткости, в условиях по меньшей мере жесткости выше средней, в условиях по меньшей мере высокой жесткости или в условиях по меньшей мере очень высокой жесткости с последовательностью SEQ ID NO:61, кодирующей зрелый полипептид, и с ее полноразмерной комплементарной цепью;
(c) полипептида, кодируемого полинуклеотидом, содержащим нуклеотидную последовательность, которая по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 97% идентична последовательности SEQ ID NO:61, кодирующей зрелый полипептид; и
(d) варианта, содержащего замену, делецию и/или вставку одной или нескольких аминокислот в зрелом полипептиде с последовательностью SEQ ID NO:62; и
(e) полипептида, содержащего зрелый полипептид с последовательностью SEQ ID NO:62.
9. Целлюлолитическая белковая композиция по п.6, которая содержит полипептид, обладающий усиливающей целлюлолитическое действие активностью зрелого полипептида с последовательностью SEQ ID NO:12; бета-глюкозидазный слитый белок SEQ ID NO:104 или SEQ ID NO:106; целлобиогидролазу I (CEL7A) Trichoderma reesei зрелого полипептида с последовательностью SEQ ID NO:52, целлобиогидролазу II (CEL6A) Trichoderma reesei зрелого полипептида с последовательностью SEQ ID NO:54 и эндоглюканазу I (CEL7B) Trichoderma reesei зрелого полипептида с последовательностью SEQ ID NO:56.
10. Целлюлолитическая белковая композиция по п.9, которая дополнительно содержит один или более ферментов, выбранных из группы, состоящей из эндоглюканазы II (CEL5A) Trichoderma reesei SEQ ID NO:58, эндоглюканазы V (CEL45A) Trichoderma reesei с последовательностью SEQ ID NO:62 и эндоглюканазы III (CEL12A) Trichoderma reesei с последовательностью SEQ ID NO:60.
11. Способ разложения материала, содержащего целлюлозу, включающий обработку материала, содержащего целлюлозу, эффективным количеством композиции целлюлолитического белка по любому из пп.6-10.
12. Способ получения продукта ферментации материала, содержащего целлюлозу, включающий:
(a) осахаривание материала, содержащего целлюлозу, указанной композицией целлюлолитического белка по любому из пп.6-10;
(b) ферментацию содержащего целлюлозу осахаренного материала одним или более сбраживающими микроорганизмами с получением продукта ферментации; и
(c) выделение продукта ферментации, полученного в результате реакции ферментации.
| WO 2005074656 A2, 18.08.2005 | |||
| US 20070077630 A1, 05.04.2007 | |||
| US 20050191736 A1, 01.09.2005 | |||
| YASUYA FUJITA et al., Synergistic Saccharification, and Direct Fermentation to Ethanol, of Amorphous Cellulose by Use of an Engineered Yeast Strain Codisplaying Three Types of Cellulolytic Enzyme, Appl | |||
| Environ | |||
| Microbiol | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ШТАММ Penicillium funiculosum, ПРОДУЦИРУЮЩИИЙ КОМПЛЕКС ФЕРМЕНТОВ - ЦЕЛЛЮЛАЗУ, ЭНДО-1,4-β-КСИЛАНАЗУ, ЦЕЛЛОБИОГИДРОЛАЗУ, β-ГЛЮКОЗИДАЗУ, ЭНДО-1,3(4)- β-ГЛЮКАНАЗУ, ФЕРУЛОИЛ-ЭСТЕРАЗУ, ЖИДКАЯ КОРМОВАЯ ДОБАВКА И СУХОЙ КОРМ ДЛЯ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 1999 |
|
RU2261910C2 |
Авторы
Даты
2013-09-27—Публикация
2008-05-30—Подача