Область техники
Данное изобретение относится к новым производным неоникотиноида, к способу их получения и к их применениям.
Предшествующий уровень техники
Представленный имидаклопридом, неоникотиноидный инсектицид стал пусковым фактором открытия пестицидов, со свойством высокой инсектицидной активности, широким инсектицидным спектром, низкой токсичностью для млекопитающих и водных животных, хорошими системными свойствами, подходящей полевой стабильностью и благоприятностью для окружающей среды. После имидаклоприда была разработана серия неоникотиноидных инсектицидов, таких как тиоклоприд, клотианидин, тиаметоксам, ацетамиприд, нитенпирам и динотефуран (ЕР 247477, 296453, 685477, 235725, 235725, 315826, 192060, 244777, 0386565, 580553, 1031566, JP 62292765, 8259568, 8291171 и 7242633).
Однако применение и разработка этих соединений ограничены вследствие устойчивости, вызванной слишком частым применением имидаклоприда, и перекрестной устойчивости среди неоникотиноидных инсектицидов, вызванной структурным сходством. Тем не менее, неоникотиноидные инсектициды, в основном, проявляют высокую активность в отношении вредителей Homoptera и Coleoptera, и узкий инсектицидный спектр ограничивает их широкое применение в борьбе с вредителями.
Таким образом, в данной области техники крайне необходимо разработать соединения с эффективными активностями из высокоактивных нитрометиленовых соединений, чтобы решить проблему устойчивости, расширить инсектицидный спектр и применять их в инсектицидных композициях.
Краткое описание изобретения
В данном изобретении предложены новые эффективные инсектициды, которые позволяют решить проблему устойчивости к неоникотиноидным инсектицидам, расширить инсектицидный спектр и решить проблемы, существующие в данной области техники.
Одной целью изобретения является разработка производных для эффективной борьбы с вредителями и их получение.
Другой целью изобретения является разработка защиты растущих и собранных растений и предупреждение их инвазии насекомыми.
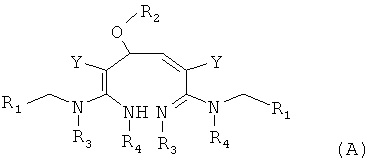
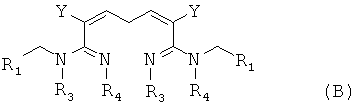
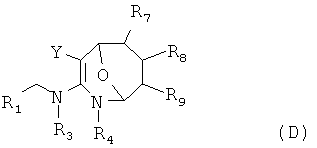
В соответствии с первым аспектом изобретения предложено соединение формулы (А), (В), (С) или (D), его оптический изомер, цис-транс-изомер или его агрохимически приемлемые соли
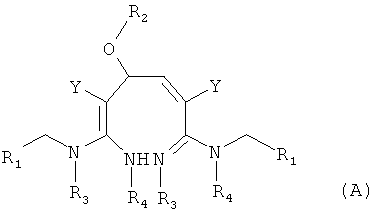
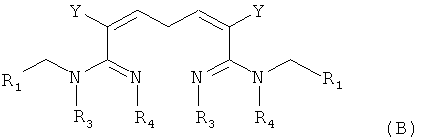
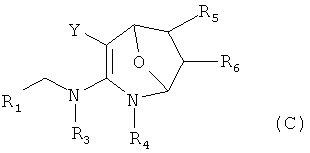
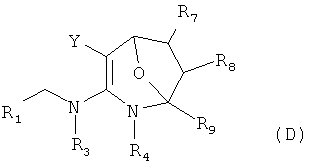
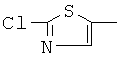
где R1 представляет собой 5- или 6-членный гетероцикл, содержащий атом азота, кислорода и/или серы, замещенный галогеном 5- или 6-членный гетероцикл, содержащий атом азота, кислорода и/или серы, замещенный или незамещенный фенил, где заместители представляют собой одну или более чем одну группу, выбранную из группы, состоящей из атомов галогена, C1-4 галогеноалкила или C1-4 хлороалкоксила;
R2 представляет собой Н, C1-8 насыщенный или ненасыщенный алкил, замещенный галогеном C1-8 насыщенный или ненасыщенный алкил, -CH2CH2OCH2CH3, -CH2CH2OCH3, C1-8 насыщенный или ненасыщенный алкоксил, фенил, бензил, C1-4 алкилкарбонил или С1-4 алкилсульфонил;
R3 и R4 независимо выбраны из Н, C1-6 алкила, аллила, бензила, C1-4алкоксил-С1-4алкила, С1-4алкоксилкарбонила, феноксикарбонила, С2-6алкинилкарбонила, C2-3алкенилкарбонила, С3-6циклоалкилкарбонила, незамещенной бензоильной группы или бензоильной группы, замещенной одной или более чем одной группой, выбранной из группы, состоящей из атомов галогена, С1-4алкила, С1-4галогеноалкила, С1-4алкоксила или C1-4алкилкарбонила, фуранкарбонила или N,N-диметилкарбонила; либо R3 и R4 вместе образуют -СН2-СН2-, -СН2-СН2-СН2- или -CH2-XR-CH2-, где Х представляет собой N, О, S или другой гетероатом; R представляет собой заместитель на Х и выбран из Н, С1-6алкила, аллила, бензила, фенила, C1-4алкоксил-С1-4алкила, С1-4алкоксилкарбонила, феноксикарбонила, C2-6алкинилкарбонила, С2-3алкенилкарбонила, С3-6циклоалкилкарбонила, незамещенной бензоильной группы или бензоильной группы, замещенной одной или более чем одной группой, выбранной из группы, состоящей из атомов галогена, С1-4галогеноалкила, C1-8 насыщенного или ненасыщенного алкила или алкоксила, либо С1-4алкилкарбонила, фуранкарбонила или N,N-диметилкарбонила.
R5, R6, R7, R8 и R9 представляют собой Н, насыщенный или ненасыщенный С1-4алкил, атом галогена, насыщенный или ненасыщенный C1-8алкоксил, насыщенный или ненасыщенный С1-4галогеноалкоксил, C1-4алкилкарбонил, C1-8алкилэфир, С1-4алкилсульфонил, фенил или бензил;
Y представляет собой нитро, циано, трифторметил, трифторацетил или трифторметилсульфонил.
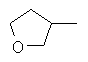
В одном воплощении предпочтительно R1 выбран из пиридила, тиазолила, пиримидинила, тетрагидрофурила, оксазолила или их галогенированных групп.
В одном воплощении предпочтительный R1 представляет собой галогенопиридил, галогенотиазолил, галогенопиримидинил, галогенотетрагидрофурил или галогенооксазолил. Предпочтительными галогенированными группами являются хлориды.
В другом воплощении R1 представляет собой 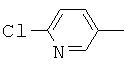 ,
, 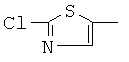 или
или 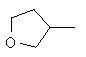 .
.
В другом воплощении R2 представляет собой Н, насыщенный или ненасыщенный С1-4алкил, насыщенный или ненасыщенный С1-4галогеноалкил, С1-4алкилкарбонил, незамещенный бензил или бензил, замещенный одной или более чем одной группой, выбранной из группы, состоящей из атома галогена, С1-4галогеноалкила или С1-4хлороалкоксила.
В одном воплощении R2 представляет собой Н или С1-3алкил. Более предпочтительно R2 представляет собой Н или метил.
В другом воплощении R3 и R4 представляют собой Н, С1-6алкил, либо R3 и R4 вместе образуют -CH2-CH2- или -СН2-СН2-СН2-.
В одном воплощении R3 и R4 представляют собой атом водорода или C1-3алкил, и предпочтительно Н, метил или этил. Альтернативно R3 и R4 вместе образуют -СН2-СН2- или -СН2-СН2-СН2-.
В другом воплощении R5, R6, R7, R8 и R9 представляют собой Н, насыщенный или ненасыщенный С1-2алкил, атом галогена, насыщенный или ненасыщенный С1-4алкоксил, насыщенный или ненасыщенный C1-2 галогеноалкоксил, С1-4алкилэфирную группу (RCOO-), С1-2алкилсульфонил или трифторметансульфонилэфирную группу.
В одном воплощении R5, R6, R7, R8 и R9 представляют собой Н, метил, атом хлора, атом брома, метоксил или этоксил и предпочтительно представляют собой Н, метил и метоксил.
В другом воплощении Y представляет собой нитрогруппу или цианогруппу.
В одном воплощении Y представляет собой нитрогруппу.
В соответствии со вторым аспектом изобретения предложена агрохимическая композиция, содержащая:
(a) 0,001-99,99 масс.% вышеупомянутого соединения, его оптического изомера, цис-транс-изомера, его агрохимически приемлемых солей или их комбинации; и
(b) агрохимически приемлемый носитель или эксципиент.
В одном воплощении концентрация компонента (а) составляет 0,01-99,9 масс.%, и предпочтительно 0,05-90 масс.%.
В одном воплощении агрохимическую композицию применяют для уничтожения или борьбы с насекомыми, выбранными из группы, состоящей из Coleoptera, Lepidoptera, Hemiptera, Orthoptera, Isoptera и двукрылых насекомых.
В одном воплощении вредители имеют ротовой аппарат колюще-сосущего типа или грызущего типа.
В другом воплощении вредители включают настоящую тлю, коричневую рисовую цикаду, белокрылку, цикадку, трипсов, совку хлопковую, гусеницу, поражающую капусту, капустную моль, совку литура или гусеницу злаковых растений.
В другом воплощении агрохимическая композиция дополнительно содержит другие активные соединения, которые выбраны из группы, состоящей из инсектицида, кобальта, бактерицидного агента, акарицида, нематицида, фунгицида и регуляторов роста.
В соответствии с третьим аспектом изобретения предложено применение агрохимической композиции при уничтожении или борьбе с сельскохозяйственными вредителями, санитарными вредителями и вредителями, вредными для здоровья животных; либо агрохимическую композицию применяют как инсектицидную композицию для уничтожения или борьбы с сельскохозяйственными вредителями, санитарными вредителями и вредителями, вредными для здоровья животных.
В соответствии с четвертым аспектом изобретения предложен способ уничтожения или борьбы с сельскохозяйственными вредителями, санитарными вредителями и вредителями, вредными для здоровья животных, включающий нанесение вышеописанной агрохимической или инсектицидной композиции на растения, окружающую их почву или окружающую среду, которая атакована или будет атакована насекомыми.
В соответствии с пятым аспектом изобретения предложено применение соединения, его оптического изомера или цис-транс-изомера, его агрохимически приемлемых солей или их комбинации при получении инсектицидной композиции.
В соответствии с шестым аспектом изобретения предложен способ получения соединения, его оптического изомера или цис-транс-изомера, его агрохимически приемлемых солей, включающий приведенные ниже стадии:
В присутствии каталитической кислоты и при 0-60°С взаимодействие соединения формулы (а) с соединением (b), (с) или (d), в результате чего образуется соединение (А), (В), (С) или (D), где R2 представляет собой Н,
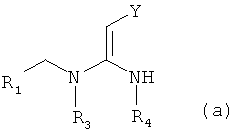
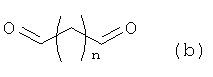
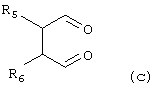
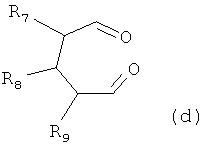
где R1, R3, R4, R5, R6, R7, R8, R9 и Y являются такими, как определено выше, и n равно 0 или 1.
В одном воплощении температура реакции составляет 15-45°С, и предпочтительно 20-30°С.
В другом воплощении растворитель выбран из ацетонитрила или этанола, и предпочтительно ацетонитрила.
В другом воплощении каталитическая кислота выбрана из концентрированной соляной кислоты, концентрированной серной кислоты или бензойной кислоты, и предпочтительно концентрированной соляной кислоты.
В одном воплощении способ включает:
в присутствии каталитической кислоты приведенную ниже реакцию проводят при 20-30°С в ацетонитриле в течение 2-24 часов, в результате чего образуется соединение (А), где R2 представляет собой Н:
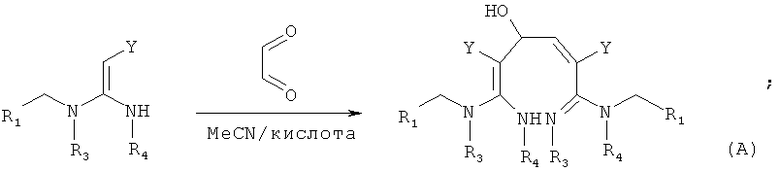
в присутствии каталитической кислоты приведенную ниже реакцию проводят при 20-30°С в ацетонитриле в течение 2-24 часов, в результате чего образуется соединение (В):
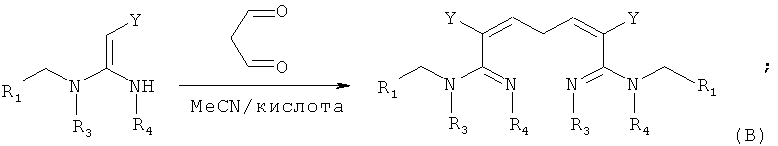
в присутствии каталитической кислоты приведенную ниже реакцию проводят при 10-50°С в ацетонитриле в течение 2-24 часов, в результате чего образуется соединение (С):
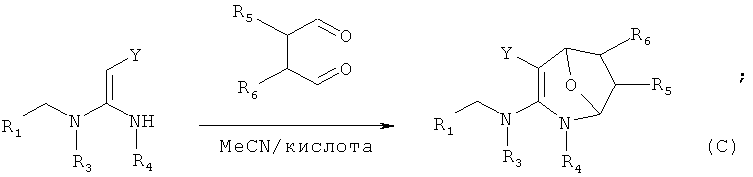
в присутствии каталитической кислоты приведенную ниже реакцию проводят при 10-50°С в ацетонитриле в течение 2-24 часов, в результате чего образуется соединение (D):
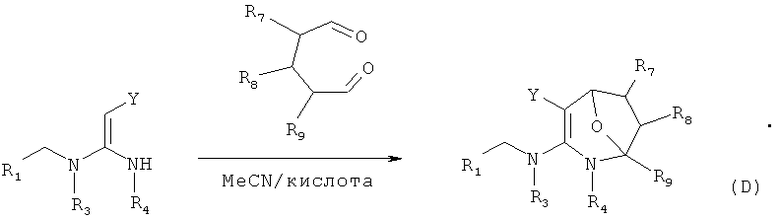
Подробное описание изобретения
После долговременного и глубокого исследования авторы изобретения синтезировали новый класс неоникотиноидных производных, которые получают путем взаимодействия нитрометиленовых соединений с диальдегидом, основанный на нитрометиленовой группе современных нитрометиленовых неоникотиноидных инсектицидов. Эти новые производные проявляют значимо высокие активности и расширенный инсектицидный спектр. Авторы изобретения выполнили настоящее изобретение на основе вышеописанного.
Определение заместителей
Термин «C1-6алкил» относится к прямоцепочечному или разветвленному алкилу с 1-6 атомами углерода, такому как метил, этил, пропил, изопропил, бутил, изобутил, emop-бутил, mpem-бутил или некоторые подобные группы.
Термин «С1-6алкоксил» относится к прямоцепочечному или разветвленному алкоксилу с 1-6 атомами углерода, такому как метоксил, этоксил, пропоксил, изопропоксил, бутоксил, изобутоксил, втор-бутоксил, трет-бутоксил или некоторые подобные группы.
Термин «галоген» относится к атому фтора, хлора, брома или йода. Термин «галогенированный» относится к одному или более чем одному замещению одним и тем же или другим атомом «галогена», как упомянуто выше, такому кактрифторметил, пентафторэтил или подобные группы.
Термин «5- или 6-членный гетероциклический алкил» относится к 5- или 6-членному кольцевому циклическому алкилу, содержащему один или более чем один гетероатом, выбранный из атома азота, кислорода или серы, такому как пиридил, тиазил, пиримидинил, тетрагидрофурил, оксазолил и т.д.
Получение соединения по изобретению
Соединения по изобретению можно синтезировать, как описано выше. Соединение (а) может быть получено в соответствии с техническими ссылками в данной области техники, такими как WO 2006056108 A1, WO 2007101369 A1 и PCT/CN 2008/071115.
В одном воплощении соединение формулы (А) можно синтезировать, следуя приведенной ниже методике, где R2 представляет собой Н;
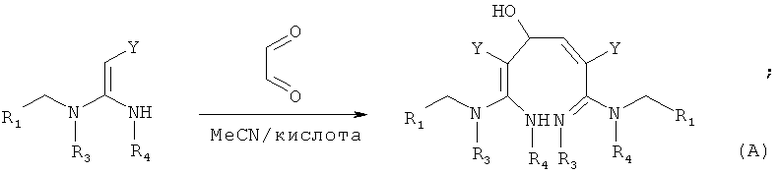
В одном воплощении соединение формулы (В) можно синтезировать, следуя приведенной ниже методике:
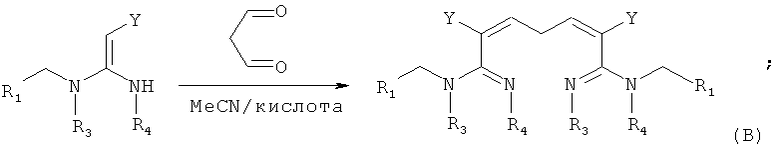
В одном воплощении соединение формулы (С) можно синтезировать, следуя приведенной ниже методике:
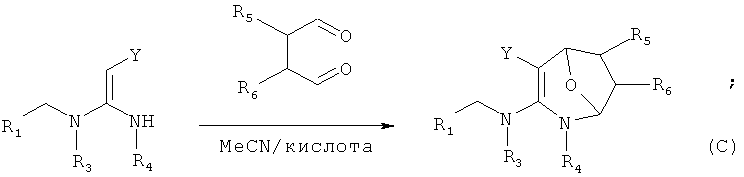
В одном воплощении соединение формулы (D) можно синтезировать, следуя приведенной ниже методике:
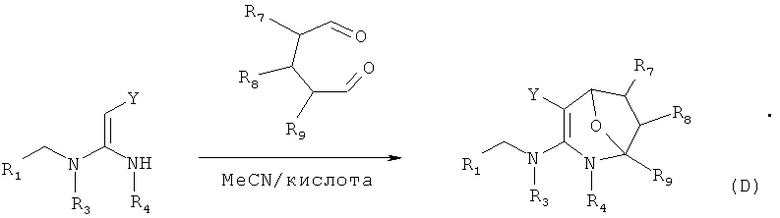
В одном воплощении соединение формулы (А) можно синтезировать, следуя приведенной ниже методике:
(1) Раствор 2-хлор-5-(хлорметил)пиридина в ацетонитриле добавляют по каплям к раствору 5-10 моль диамина. Реакцию проводят при 0-50°С в течение 5-10 часов. После завершения смесь перегоняют при пониженном давлении для удаления диамина, растворяют в этилацетате и выпаривают с получением N-((6-хлорпиридин-3-ил)метил)диамина.
(2) Смесь N-((6-хлорпиридин-3-ил)метил)диамина и 1,1-диметилтио-2-нитроэтена растворяют в этаноле и кипятят с обратным холодильником в течение 4-8 часов с получением нитрометиленового соединения.
(3) В присутствии кислотного катализатора, такого как соляная кислота, серная кислота, гетерополикислоты и т.д., нитрометиленовое соединение взаимодействует с оксальдегидом (глиоксалем) с получением соединения формулы (А).
В другом воплощении соединение формулы (В) можно синтезировать, следуя приведенной ниже методике:
(1) К водному раствору этиламина добавляют соответствующее количество ацетонитрила. Затем 2-хлор-5-(хлорметил)пиридин в ацетонитриле добавляют по каплям в ледяной бане. Мониторинг реакции осуществляют с помощью ТСХ (тонкослойной хроматографии). После завершения в смесь добавляют большое количество воды, экстрагируют ДХМ (дихрорметаном), высушивают, фильтруют и выпаривают с получением N-((6-хлорпиридин-3-ил)метил)этенамина в виде масла.
(2) Смесь N-((6-хлорпиридин-3-ил)метил)этенамина и 1,1-диметилтио-2-нитроэтена растворяют в этаноле и кипятят с обратным холодильником в течение 4-8 часов. После завершения смесь концентрируют и очищают колоночной хроматографией с получением N-((6-хлорпиридин-3-ил)метил)-N-этил-1-(метилтио)-2-нитроэтенамина.
(3) Смесь спиртового раствора метиламина и N-((6-хлорпиридин-3-ил)метил)-N-этил-1-(метилтио)-2-нитроэтенамина растворяют в этаноле и подвергают взаимодействию в течение 4-8 часов в ледяной бане. После завершения смесь концентрируют и очищают колоночной хроматографией с получением N-((6-хлорпиридин-3-ил)метил)-N-этил-N'-метил-2-нитроэтен-1,1-диамина.
(4) В присутствии кислотного катализатора, такого как соляная кислота, серная кислота, гетерополикислоты и т.д., N-((6-хлорпиридин-3-ил)метил)-N-этил-N'-метил-2-нитроэтен-1,1-диамин взаимодействует с малоновым альдегидом с получением соединения формулы (В).
В другом воплощении соединение формулы (С) можно синтезировать, следуя приведенной ниже методике:
(1) Раствор 2-хлор-5-(хлорметил)пиридина в ацетонитриле добавляют по каплям к раствору 5-10 моль диамина. Реакцию проводят при 0-50°С в течение 5-10 часов. После завершения смесь перегоняют при пониженном давлении для удаления диамина, растворяют в этилацетате и выпаривают с получением N-((6-хлорпиридин-3-ил)метил)диамина.
(2) Смесь N-((6-хлорпиридин-3-ил)метил)диамина и 1,1-диметилтио-2-нитроэтена растворяют в этаноле и кипятят с обратным холодильником в течение 4-8 часов с получением нитрометиленового соединения.
(3) В присутствии кислотного катализатора, такого как соляная кислота, серная кислота, гетерополикислоты и т.д., нитрометиленовое соединение взаимодействует с янтарным альдегидом с получением соединения формулы (С).
В другом воплощении соединение формулы (D) можно синтезировать, следуя приведенной ниже методике:
(1) Раствор 2-хлор-5-(хлорметил)пиридина в ацетонитриле добавляют по каплям к раствору 5-10 моль диамина. Реакцию проводят при 0-50°С в течение 5-10 часов. После завершения смесь перегоняют при пониженном давлении для удаления диамина, растворяют в этилацетате и выпаривают с получением N-((6-хлорпиридин-3-ил)метил)диамина.
(2) Смесь N-((6-хлорпиридин-3-ил)метил)диамина и 1,1-диметилтио-2-нитроэтена растворяют в этаноле и кипятят с обратным холодильником в течение 4-8 часов с получением нитрометиленового соединения.
(3) В присутствии кислотного катализатора, такого как соляная кислота, серная кислота, гетерополикислоты и т.д., нитрометиленовое соединение взаимодействует с глутаральдегидом с получением соединения формулы (D).
Инсектиидная активность активных соединений по изобретению
Термины «активный ингредиент по изобретению» или «активное соединение по изобретению» представляют собой соединение по изобретению, его оптически изомер или цис-транс-изомер, или его агрохимически приемлемые соли. «Активное соединение по изобретению» проявляет значительно повышенные активности и расширенный инсектицидный спектр.
Термин «агрохимически приемлемые соли» означает, что анион соли является известным или приемлемым при образовании инсектицидно приемлемой соли. Предпочтительно соль растворима в воде. Соли, образованные соединениями формулы (А), (В), (С) и (D), включают соли, образованные с неорганической кислотой (например, гидрохлорат, фосфат, сульфат и нитрат) и соли, образованные с органической кислотой (например, ацетат и бензоат).
Активное соединение по данному изобретению можно применять для борьбы и уничтожения обычных насекомых-вредителей сельскохозяйственных культур и растений, насекомых-вредителей зернохранилищ, насекомых, вредных для здоровья населения, и насекомых, вредных для здоровья животных. В данном изобретении термин «инсектицид» представляет собой любое соединение, которое предотвращает появление или борется с любым из вышеупомянутых насекомых. Примерные насекомые включают, но не ограничены ими;
Coleoptera: Sitophilus zeamai, Tribolium castaneum, Henosepilachna vigintioctomaculata, Henosepilachna spars, Agriotes fuscicollis, Anomala cupripes, Popillia quadriguttata, Monolepta hieroglyphica, Monochamus alternatus, Echinocnemus squameus, Basiprionota bisignata, Anoplophora chinensis, Apripona gennari, Scolytus schevy, Agriotes fuscicollis.
Lepidoptera: Lymantria dispar, Malacosoma neustria testacea, Diaphania perspectalis, Clania variegate, Cnidocampa flauescens, Dendrolimus punctatus, Orgyia gonostigma, Paranthrene tabaniformis, Spodoptera litura, Chilo suppressalis, Ostrinia nubilalis, Ephestia cautella, Adoxophyes orana, Laspyresia splendana, Agrotis fucosa, Galleria mellonella, Plutella xylostella, Phyllocnistis citrella, or Mythimna separate.
Homoptera: Nephotettix cincticeps, Nilaparvata lugens, Pseudococcus comstocki, Unaspis yanonensis, Myzus persicae, Aphis gossydii, Lipaphis erysimi pseudobrassicae, Stephanitis nashi, or Bemisia tabaci.
Orthoptera: Blattella germanica, Periplaneta americana, Gryllotalpa africana, or Locusta migratoria.
Isoptera: Solenopsis invicta, Coptotermes formosanus.
Diptera: Musca domestica, Aedes aegypti, Delia platura, Culex sp., Anopheles sinensis.
Насекомые, вредные для здоровья человека: Boophilus microplus, Haemaphysalis longicornis, Hyalomma anatolicum, Hypoderma spp., Fasciola hepatica, Moniezia Blanchard, Ostertagia spp., Trypanosoma enansi, Babesia bigemina, etc.
Соединения по изобретению обладают специфичными эффектами на насмекомых-вредителей сельскохозяйственных культур и растений, имеющих колюще-сосущий или грызущий ротовой аппарат, таких как тля, цикадка, коричневая рисовая цикада, трипсы, белокрылка и т.д.
Инсектицидная композиция, содержащая соединение по изобретению
Активные соединения по изобретению можно обычно включать в инсектицидную композицию. Активные соединения по изобретению можно включать в общепринятые препараты, такие как растворы, эмульсии, суспензии, порошки, пенки, пасты, гранулы, аэрозоли, натуральные и синтетические материалы, пропитанные активными соединениями, и микрокапсулы в полимерах, покрывающий комплекс для семян, препараты, используемые с камерой сгорания (такой как дымовой цилиндр, дымовая коробка и дымовая пластина) и препараты холодного аэрозоля и теплого аэрозоля ULV.
Эти препараты могут быть получены известным способом, например, путем смешивания активных соединений с наполнителями, которые являются жидкими или в виде сжиженного газа, твердыми разбавителями или носителями, необязательно с использованием поверхностно-активных агентов, которые являются эмульгирующими агентами и/или диспергирующими агентами, и/или пенообразующими агентами. В случае использования воды в качестве наполнителя органические растворители можно также использовать как вспомогательные растворители.
Обычно правильно использовать жидкие растворители в качестве разбавителя или носителя, например, ароматические углеводороды, такие как ксилол, толуол и алкилнафталины; хлорированные ароматические или хлорированные алифатические углеводороды, такие как хлорбензолы, хлорэтилены и метиленхлорид; алифатические углеводороды, такие как циклогексан или парафины, например, нефтяные фракции; спирты, такие как этанол или гликоль, а также их простые эфиры и сложные эфиры; кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон или циклогексанон; либо нераспространенные полярные растворители, такие как диметилформаммид и диметилсульфоксид, а также вода. Под сжиженными газообразными разбавителями или носителями подразумевают жидкости, которые являются газообразными при нормальной температуре и при нормальном давлении, например, аэрозольные пропелленты, такие как галогенированные углеводороды, а также бутан, пропан, азот и диоксид углерода.
Твердый носитель включает измельченные природные минералы, такие как каолины, глины, тальки, кварцы, аттапульгиты, монтмориллониты или кизельгуры; измельченные синтетические минералы, такие как высокодисперсная кремниевая кислота, оксид алюминия и силикат. Твердый носитель, используемый для частиц, представляет собой дробленые и фракционированные природные камни, такие как кальцит, мрамор, пемза, сепиолит и доломит, а также синтетические гранулы неорганического или органического крупного порошка и гранулы органического материала, такого как древесные опилки, скорлупа кокосовых орехов, кукурузные початки и стебли табака и тому подобное.
В качестве эмульгирующих и/или пенообразующих агентов можно использовать неионные и анионные эмульгаторы, такие как сложные эфиры полиоксиэтилена и жирных кислот, простые эфиры полиоксиэтилена и жирных спиртов, например, алкиларилполигликолевые эфиры, алкилсульфонаты, алкилсульфаты, арилсульфонаты, а также продукты гидролиза альбумина. Диспергирующие агенты включают, например, лигнин, отработанные сульфитные щелоки и метилцеллюлозу.
Клеящие вещества, такие как карбоксиметилцеллюлоза и природные и синтетические полимеры (такие как аравийская камедь, поливиниловый спирт и поливинилацетат) в форме порошков, гранул или эмульсий можно использовать в препаратах. Возможно использовать красители, такие как неорганические красящие вещества, например, оксид железа, оксид кобальта и берлинская лазурь, и органические красящие вещества, такие как красящие вещества, представляющие собой диазосоединения, или красящие вещества, представляющие собой фталоцианины металлов, и питательные микроэлементы, такие как соли железа, марганца, бора, меди, кобальта, алюминия и цинка.
Активное соединение по изобретению может быть представлено в виде смеси с другими активными соединениями в коммерческом препарате или в форме применения, полученной из коммерческого препарата. Другие соединения могут представлять собой инсектицид, бактерицидный агент, акарицид, нематоцид, фунгицид, регулятор роста и тому подобное. Инсектицид включает, например, фосфаты, карбаматы, пиретроиды, хлорированные углеводороды, бензоилмочевину, нереистоксин и вещество, продуцируемое микроорганизмами, такое как авермектин.
Кроме того, активное соединение по изобретению может быть представлено в виде смеси с синергистом в коммерческом препарате или в форме применения, полученной из коммерческого препарата. Синергист используют для усиления действия активного соединения, если само соединение активно, необязательно использовать синергист.
Как правило, препараты содержат 0,001-99,99 мас.%, предпочтительно 0,01-99,9 мас.% и более предпочтительно 0,05-90 мас.% активного соединения по изобретению. Концентрация активного соединения в форме применения, полученной из коммерческого препарата, может варьировать в широком диапазоне. Концентрация активного соединения в препарате для применения составляет, например, 0,0000001-100% (мас./об.) и предпочтительно 0,0001-1%.
Примеры
Далее изобретение проиллюстрировано приведенными ниже примерами. Должно быть понятно, что эти примеры предназначены только для иллюстрации изобретения, и не ограничивают объема изобретения. Что касается экспериментальных методов в приведенных ниже примерах, их осуществляют в обычных условиях или в соответствии с инструкциями изготовителей, если не указано иное. Процентное содержание и доли вычислены по массе. Термин «к.т.» представляет собой комнатную температуру.
Пример 1
Синтез 4-(1-((6-хлорпиридин-3-ил)метил)-4,5-дигидро-1Н-имидазол-2-ил)-1-(1-((6-хлорпиридин-3-ил)метил)имидазолидин-2-илиден)-1,4-динитробут-3-ен-2-ола (соединение 13)
В соответствии со способом, описанным в WO 2006056108 А1 и WO 2007101369 А1, 2-хлор-5-((2-(нитрометилен)имидазолидин-1-ил)метил)пиридин был получен из 2-хлор-5-(хлорметил)пиридина (0,03 моль) при выходе 56%. Rf=0,46 (петролейный эфир: EtOAc=1:1); т.пл.=156,9°С-161,8°С; ЖХ-МС (m/s): 220 (25), 126 (100), 90 (9).
Синтез 4-(1-((6-хлорпиридин-3-ил)метил)-4,5-дигидро-1Н-имидазол-2-ил)-1-(1-((6-хлорпиридин-3-ил)метил)имидазолидин-2-илиден)-1,4-динитробут-3-ен-2-ола
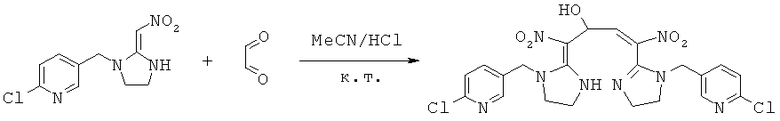
В 50 мл круглодонную колбу добавляли 1,27 г (0,005 моль) 2-хлор-5-((2-(нитрометилен)имидазолидин-1-ил)метил)пиридина, 30 мл ацетонитрила и 3 мл 30% водного раствора оксальдегида. После перемешивания в течение 0,5 часа добавляли катализатор - концентрированную HCl. Затем реакционную смесь перемешивали и проводили мониторинг по ТСХ до завершения. После этого смесь фильтровали с получением белого порошка, который кристаллизовали с получением 1,05 г чистого конечного продукта в виде белого порошкообразного твердого вещества. Выход: примерно 76%.
Т.пл.=164,6-165,3°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 9,01 (s, 1H), 8,41 (d, J=2,0 Гц, 1H), 8,38 (d, J=2,0 Гц, 1H), 7,80-7,86 (m, 2H), 7,51-7,54 (m, 2H), 6,50 (d, J=7,2 Гц, 1H), 5,34 (d, J=15,2 Гц, 1H), 5,18 (d, J=15,2 Гц, 1H), 4,84 (dd, J1=2,4 Гц, J2=7,2 Гц, 1H), 4,77 (d, J=16,8 Гц, 1H), 4,67 (d, J=16,8 Гц, 1H), 3,98 (d, J=2,4 Гц, 1H), 3,86-3,95 (m, 2H), 3,61-3,80 (m, 5H), 3,40-3,47 (m, 1H) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 162,7, 158,7, 148,3, 148,2, 148,0, 147,7, 138,1, 137,7, 130,9, 130,2, 123,1, 123,0, 102,5, 101,4, 81,4, 53,8, 52,6, 49,4, 48,8, 46,4, 41,2, 41,0 млн-1; МСВР (масс-спектрометрия высокого разрешения) (ES+) вычислено для C22H23N8O5 35Cl2 (М+Н)+ 549,1168; обнаружено 549,1178. вычислено для C22H23N8O5 35Cl37Cl (M+H)+ 551,1139; обнаружено 551,1152. вычислено для C22H23N8O5 37Cl2 (М+Н)+ 553,1109; обнаружено 553,1108.
Пример 2
Синтез 2-хлор-5-((4-(1-((6-хлорпиридин-3-ил)метил)имидазолидин-2-илиден)-2-метокси-1,4-динитробут-3-енил)-4,5-дигидроимидазол-1-ил)метил) пиридина (соединение 14)
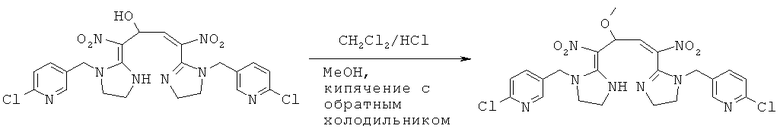
В 50 мл круглодонную колбу добавляли 0,549 г (0,001 моль) соединения 13, 10 мл метанола, 50 мл дихлорметана и каталитическое количество концентрированной HCl. Реакционную смесь кипятили с обратным холодильником и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде желтого порошка (выход 62%).
Т.пл.=151,6-153,1°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 9,03 (s, 1H), 8,38 (d, J=2,0 Гц, 1H), 8,36 (d, J=2,0 Гц, 1H), 7,81-7,85 (m, 2H), 7,49-7,51 (m, 2H), 6,50 (d, J=7,2 Гц, 1H), 5,35 (d, J=15,2 Гц, 1H), 5,19 (d, J=15,2 Гц, 1H), 4,80 (d, J1=7,2 Гц, 1H), 4,77 (d, J=16,8 Гц, 1H), 4,69 (d, J=16,8 Гц, 1H), 3,68 (s, 3Н), 3,88-3,95 (m, 2H), 3,61-3,85 (m, 5H), 3,38-3,41 (m, 1H) млн-1; 13C ЯМР (100 МГц, ДМСО-d6): δ 162,6, 158,7, 148,9, 148,3, 148,1, 147,6, 138,1, 137,8, 130,9, 129,9, 122,8, 123,1, 102,2, 101,6, 81,6, 58,7, 53,8, 52,6, 49,6, 48,9, 46,4, 41,3, 41,0 млн-1; MCBP (ES+) вычислено для C23H25N8O5 35Cl2 (М+Н)+ 563,1325; обнаружено 563,1311. вычислено для C23H25N8O5 35Cl37Cl (M+H)+ 565,1295.
Пример 3
Синтез N1,N7-бис((6-хлорпиридин-3-ил)метил)-N1,N7-диэтил-N1,N7-диметил-2,6-динитрогепта-2,5-диендиамина (Соединение 37)
(1): Синтез N-((6-хлорпиридин-3-ил)метил)этанамина
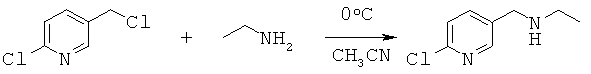
65-70% раствор этиламина (70 г, 1 моль), ацетонитрил 50 мл, добавляли в трехгорлую круглодонную колбу, оборудованную капельной воронкой с выравниванием давления и термометром. Раствор перемешивали в ледяной бане в течение 15 мин с контролем температуры около 0°С. Затем добавляли 2-хлор-5-(хлорметил)пиридин (16,10 г, 0,10 моль) в 25 мл ацетонитрила с помощью капельной воронки с выравниванием давления в течение 3,5 ч со скоростью 3 капли/мин. После завершения добавляли воду, и реакционную смесь экстрагировали ДХМ. Органическую фазу собирали с получением, таким образом, 14 г N-((6-хлорпиридин-3-ил)метил)этанамина в виде масла при выходе 70%. ЖХ-МС: m/z (%)=170 ([М]+, 20), 155 (80), 126 (100), 114 (10), 90 (12).
(2): Синтез N-((6-хлорпиридин-3-ил)метил)-N-этил-1-(метилтио)-2-нитроэтенамина
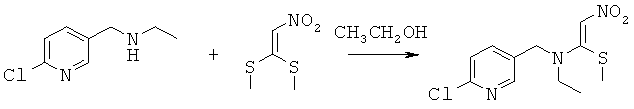
В 100 мл трехгорлую круглодонную колбу добавляли N-((6-хлорпиридин-3-ил)метил)этанамин (17,0 г, 0,1 моль), (2-нитроэтен-1,1-диил)бис(метилсульфан) (15,0 г, 0,09 моль), сухой этанол (50 мл). Смесь кипятили с обратным холодильником. После завершения реакционную смесь охлаждали до к.т. и концентрировали при пониженном давлении с получением сырого продукта в виде масла, которое очищали колоночной хроматографией с получением 5,3 г N-((6-хлорпиридин-3-ил)метил)-М-этил-1-(метилтио)-2-нитроэтенамина при выходе 18,5%.
ЖХ-МС: m/z (%)=242 ([М]+-46, 53), 227 (15), 213 (100), 169 (45), 155 (28), 141 (29), 126 (91), 90 (12).
(3): Синтез N-((6-хлорпиридин-3-ил)метил)-N-этил-N'-метил-2-нитроэтен-1,1-диамина
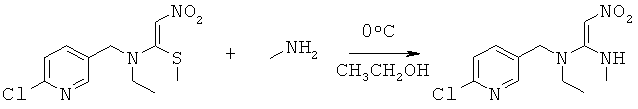
В 100 мл круглодонную колбу добавляли N-((6-хлорпиридин-3-ил)метил)-N-этил-1-(метилтио)-2-нитроэтенамин (5 г, 0,017 моль), спиртовой раствор метиламина (1,8 г, 0,017 моль), сухой этанол (30 мл). Смесь перемешивали в бане со льдом до снижения температуры до 0°С и постоянно перемешивали до завершения реакции. Реакционную смесь выпаривали при пониженном давлении для удаления растворителя и концентрировали с получением сиропа, который растворяли в некотором количестве ДХМ и очищали колоночной хроматографией, используя ДХМ/МеОН=25:1 в качестве элюента и силикагель в качестве наполнителя. Получали 0,9 г N-((6-хлорпиридин-3-ил)метил)-N-этил-N-метил-2-нитроэтен-1,1-диамина при выходе 19,1%. Rf=0,23 (ДХМ/ацетон=5:1,); т.пл.=78-80°С, (лит. [67] 79-81°С); ЖХ-МС: m/z (%)=236 ([М]+-34, 32), 207 (49), 169 (52), 126 (49), 110 (20), 90 (16), 67 (100). 16,65.
(4): Синтез N1,N7-бис((6-хлорпиридин-3-ил)метил)-N1,N7-диэтил-N1',N7'-диметил-2,6-динитрогепта-2,5-диенамидина (соединение 37)
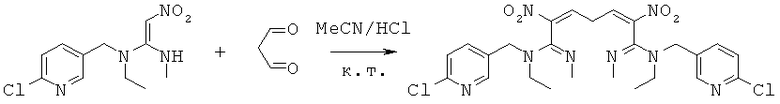
В 50 мл круглодонную колбу добавляли 1,35 г (0,005 моль) N-((6-хлорпиридин-3-ил)метил)-N-этил-N-метил-2-нитроэтен-1,1-диамина, 30 мл сухого ацетонитрила, 0,72 г (0,01 моль) малонового альдегида и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 56%.
Т.пл.=117,3-118,7°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 8,36 (d, J=2,4 Гц, 2Н), 7,88 (dd, J1=2,4 Гц, J2=8,4 Гц, 2Н), 7,51 (d, J=8,4 Гц, 2Н), 4,97 (t, J=2,8 Гц, 2Н), 4,86 (d, J=15,2 Гц, 2Н), 4,49 (d, J=15,2 Гц, 2Н), 3,95-3,99 (m, 4H), 3,66-3,78 (m, 6H), 3,12-3,21 (m, 2Н), 1,91-1,93 (m, 6H) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 156,3, 148,5, 148,1, 137,3, 131,9, 122,5, 104,8, 49,2, 48,9, 48,0, 48,5, 28,1, 20,2 млн-1; МСВР (EI+) вычислено для C25H30N8O4 35Cl2 (М+) 576,1767; обнаружено 576,1751.
Пример 4
Синтез 2-хлор-5-((5-(1-((6-хлорпиридин-3-ил)метил)-4,5-дигидро-1Н-имидазол-2-ил)-1,5-динитропента-1,4-диенил)-4,5-дигидроимидазол-1-ил)метил)пиридина (соединение 39)
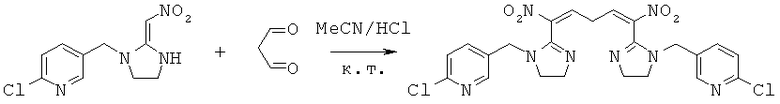
В 50 мл круглодонную колбу добавляли 1,27 г (0,005 моль) 2-хлор-5-((2-(нитрометилен)имидазолидин-1-ил)метил)пиридина, 30 мл сухого ацетонитрила, 0,720 г (0,01 моль) малонового альдегида и каталитическое количество HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 52%.
Т.пл.=136,5-137,8°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 8,34 (d, J=2,4 Гц, 2Н), 7,82 (dd, J1=2,4 Гц, J2=8,4 Гц, 2Н), 7,47 (d, J=8,4 Гц, 2Н), 4,96 (t, J=2,8 Гц, 2Н), 4,81 (d, J=15,8 Гц, 2Н), 4,44 (d, J=15,8 Гц, 2Н), 3,92-3,97 (m, 4H), 3,65-3,72 (m, 2Н), 3,49-3,56 (m, 2Н), 1,92-1,93 (m, 2Н) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 155,3, 147,9, 147,8, 138,0, 130,9, 122,7, 104,8, 50,2, 48,9, 48,5, 48,5, 28,1 млн-1; МСВР (ES+) вычислено для C23H23N8O4 35Cl2 (М+Н)+ 545,1219; обнаружено 545,1201. Вычислено для C23H23N8O4 35Cl37Cl (M+H)+ 547,1190; обнаружено 547,1178. Вычислено для C23H23N8O4 37Cl2 (М+Н)+ 549,1160; обнаружено 549,1181.
Пример 5
Синтез 1-((2-хлортиазол-5-ил)метил)-5-(1-((2-хлортиазол-5-ил)метил)-4,5-дигидро-1Н-имидазол-2-ил)-1,5-динитропента-1,4-диенил)-4,5-дигидро-1Н-имидазола (соединение 41)
Следуя способу, описанному в Примере 1, 0,03 моль 2-хлор-5-(хлорметил)тиазола использовали вместо 2-хлор-5-(хлорметил)пиридина в качестве исходного вещества и получили 1-((2-хлортиазол-5-ил)метил)-2-(нитрометилен)имидазолидин при выходе 56%. ЖХ-МС (m/s) 226 (24), 132 (100), 77 (9).
Синтез 1-((2-хлортиазол-5-ил)метил)-5-(1-((2-хлортиазол-5-ил)метил)-4,5-дигидро-1Н-имидазол-2-ил)-1,5-динитропента-1,4-диенил)-4,5-дигидро-1Н-имидазола
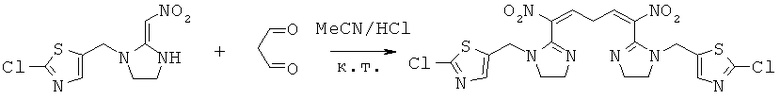
В 50 мл круглодонную колбу добавляли 1,30 г (0,005 моль) 1-((2-хлортиазол-5-ил)метил)-2-(нитрометилен)имидазолидина, 30 мл сухого ацетонитрила, 0,720 г (0,01 моль) малонового альдегида и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг no TCX. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 44%.
Т.пл.=138,6-139,9°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 7,63 (s, 1H), 4,98 (t, J=2,8 Гц, 2Н), 4,85 (d, J=15,8 Гц, 2Н), 4,43 (d, J=15,8 Гц, 2Н), 3,96-3,99 (m, 4H), 3,67-3,71 (m, 2Н), 3,51-3,56 (m, 2Н), 1,95-1,97 (m, 2Н) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 157,6, 149,3, 138,3, 105,8, 50,6, 48,9, 48,4, 48,1, 29,1 млн-1; MCBP (ES+) вычислено для C19H19N8O4S2 35Cl2 (М+Н)+ 557,0348; обнаружено 557,0363, вычислено для C19H19N8O4S2 35Cl37Cl (М+Н)+ 559,0318; обнаружено 559,0620.
Пример 6
Синтез 1-((6-хлорпиридин-3-ил)метил)-5-(1-((6-хлорпиридин-3-ил)метил)-1,4,5,6-тетрагидропиримидин-2-ил)-1,5-динитропента-1,4-диенил)-1,4,5,6-тетрагидропиримидина (соединение 43)
В соответствии со способом, описанным в WO 2006056108 А1 и WO 2007101369 A1, 1-((6-хлорпиридин-3-ил)метил)-2-(нитрометилен)-гексагидропиримидин получали из 2,42 г (0,015 ммоль) 2-хлор-5-(хлорметил)пиридина при выходе 56%; Rf=0,19 (EtOH: ДХМ=1:1); т.пл.=175,7°С-182,6°С; ЖХ-МС (m/s): 225 (100), 196 (9), 154 (10), 139 (11), 126 (31), 113 (10), 90 (31).
Синтез 1-((6-хлорпиридин-3-ил)метил)-5-(1-((6-хлорпиридин-3-ил)метил)-1,4,5,6-тетрагидропиримидин-2-ил)-1,5-динитропента-1,4-диенил)-1,4,5,6-тетрагидропиримидина
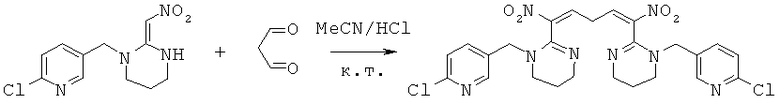
В 50 мл круглодонную колбу добавляли 1,34 г (0,005 моль) 1-((6-хлорпиридин-3-ил)метил)-2-(нитрометилен)-гексагидропиримидина, 30 мл сухого ацетонитрила и 0,720 г (0,01 моль) малонового альдегида и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 55%.
Т.пл.=133,7-134,9°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 8,32 (d, J=2,4 Гц, 2Н), 7,81 (dd, J1=2,4 Гц, J2=8,4 Гц, 2Н), 7,49 (d, J=8,4 Гц, 2Н), 4,93 (t, J=2,8 Гц, 2Н), 4,78 (d, J=15,8 Гц, 2Н), 4,40 (d, J=15,8 Гц, 2Н), 3,91-3,96 (m, 4H), 3,63-3,71 (m, 2Н), 3,49-3,53 (m, 2Н), 2,32-2,37 (m, 2Н), 1,92-1,93 (m, 2Н) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 155,6, 148,3, 147,9, 138,0, 130,7, 122,7, 105,1, 50,2, 48,8, 48,5, 48,1, 36,2, 28,0 млн-1; МСВР (ES+) вычислено для C25H27N8O4 35Cl2 (M+H)+ 572,1454; обнаружено 572,1468; вычислено для C25H27N8O4 35Cl37Cl (M+H)+ 574,1425; обнаружено 574,1416.
Пример 7
Синтез N-((6-хлорпиридин-3-ил)метил)-N-этил-2-метил-4-нитро-8-окса-2-аза-бицикло[3.2.1]окт-3-ен-3-амина (соединение 46)
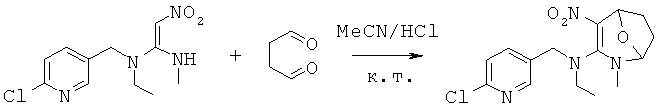
В 50 мл круглодонную колбу добавляли 1,35 г (0,005 моль) N-((6-хлорпиридин-3-ил)метил)-N-этил-N'-метил-2-нитроэтен-1,1-диамина, 30 мл сухого ацетонитрила, 0,860 г (0,01 моль) янтарного альдегида и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 40%.
Т.пл.=125,3-125,7°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 8,72 (s, 1H), 8,27 (d, J=2,4 Гц, 1H), 7,75 (dd, J1=2,4 Гц, J2=8,4 Гц, 1H), 7,58 (d, J=8,4 Гц, 1H), 5,25-5,30 (s, 2Н), 4,41-4,50 (m, 2Н), 2,96-3,26 (m, 2Н), 2,86 (s, 3H), 2,36-2,41 (m, 2H), 1,81-1,5 (m, 4H), 1,16-1,26 (m, 3H) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 158,5, 154,4, 151,6, 150,8, 148,1, 139,3, 137,1, 107,8, 89,5, 65,8, 49,8, 46,9, 40,6, 21,9, 20,3 млн-1; МСВР (EI+) вычислено для C15H21N4O3 35Cl (M+) 339,1224; обнаружено 339,1257. вычислено для C15H21N4O3 37Cl (M+) 341,1194; обнаружено 341,1213.
Пример 8
Синтез 1-((6-хлорпиридин-3-ил)метил)-9-нитро-2,3,5,6,7,8-гексагидро-1Н-5,8-эпоксиимидазо[1,2-а]азепина (соединение 52)
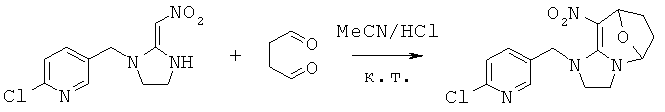
В 50 мл круглодонную колбу добавляли 1,27 г (0,005 моль) 2-хлор-5-((2-(нитрометилен)имидазолидин-1-ил)метил)пиридина, 30 мл сухого ацетонитрила, 0,860 г (0,01 моль) янтарного альдегида и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 71%.
Т.пл.=149,0-150,0°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 8,35 (d, J=2,4 Гц, 1Н), 7,81 (dd, J1=2,4 Гц, J2=8,4 Гц, 1Н), 7,51 (d, J=8,4 Гц, 1Н), 5,36-5,39 (s, 2H), 5,00 (d, J=15,6 Гц, 1Н), 4,68 (d, J=15,6 Гц, 1Н), 3,57-3,73 (m, 4H), 1,94-2,04 (m, 4H) ppm; 13C ЯМР (100 МГц, ДМСО-d6): δ 155,6, 149,7, 149,6, 139,7, 132,6, 124,5, 109,6, 87,0, 75,1, 51,2, 50,3, 46,6, 31,9, 31,7 млн-1; МСВР (ES+) вычислено для C14H16N4O3 35Cl (М+Н)+ 323,0911; обнаружено 323,0912; вычислено для C14H16N4O3 37Cl (М+Н)+ 325.0811; обнаружено 325,0895; вычислено для C14H15N4O3 35ClNa (M+Na)+ 345,0730; обнаружено 345,0722; вычислено для C14H15N4O3 37ClNa (M+Na)+ 347,0701; обнаружено 347,0692.
Пример 9
Синтез 1-((2-хлортиазол-5-ил)метил)-9-нитро-2,3,5,6,7,8-гексагидро-1Н-5,8-эпоксиимидазо[1,2-а]азепина (соединение 53)
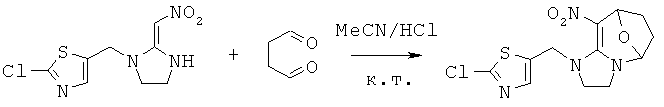
В 50 мл круглодонную колбу добавляли 1,30 г (0,005 моль) 1-((2-хлортиазол-5-ил)метил)-2-(нитрометилен)имидазолидина, 30 мл сухого ацетонитрила, 0,860 г (0,01 моль) янтарного альдегида и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при кт и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 63%.
Т.пл.=151,7-152,1°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 7.65 (s, 1H), 5.33-5.37 (s, 2H), 5.01 (d, J=15.6 Гц, 1H), 4.69 (d, J=15.6 Гц, 1H), 3.52-3.70 (m, 4H), 1.90-2.01 (m, 4H) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 155.2, 149.6, 139.1, 124.5, 110.6, 87.1, 75.6, 51.3, 50.6, 46.9, 31.9, 31.2 млн-1; МСВР (ES+) вычислено для C12H15N4O3S35Cl (M+H)+ 329,0475; обнаружено 329,0412; вычислено для C12H15N4O3S37Cl (M+Н)+ 331,0446; обнаружено 331,0423.
Пример 10
Синтез 1-((6-хлорпиридин-3-ил)метил)-10-нитро-1,2,3,4,6,7,8,9-октагидро-6,9-эпоксипиримидо[1,2-а]азепина (соединение 61)
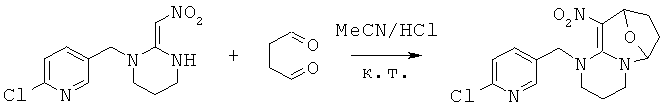
В 50 мл круглодонную колбу добавляли 1,34 г (0,005 моль) (Е)-1-((6-хлорпиридин-3-ил)метил)-2-(нитрометилен)-гексагидропиримидина, 30 мл сухого ацетонитрила и 0,860 г (0,01 моль) янтарного альдегида и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 38%.
Т.пл.=143,2-144,9°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 8,33 (d, J=2,4 Гц, 1Н), 7,80 (dd, J1=2,4 Гц, J2=8,4 Гц, 1Н), 7,49 (d, J=8,4 Гц, 1Н), 5,32-5,35 (s, 2H), 5,00 (d, J=15,6 Гц, 1Н), 4,66 (d, J=15,6 Гц, 1Н), 3,51-3,68 (m, 4H), 2,33-2,41 (m, 2H), 1,89-2,00 (m, 4H) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 155,5, 149,6, 149,3, 139,7, 132,6, 124,1, 109,3, 86,6, 75,1, 51,2, 50,7, 46,6, 32,1, 31,7, 26,9 млн-1; МСВР (ES+) вычислено для C15H19N4O3 35Cl (М+H)+ 337,1067; обнаружено 337,1015; вычислено для C15H19N4O3 37Cl (M+H)+ 339,1038; обнаружено 339,0995.
Пример 11
Синтез 1-((6-хлорпиридин-3-ил)метил)-2,3,5,6,7,8-гексагидро-1Н-5,8-эпоксиимидазо[1,2-а]азепин-9-карбонитрила (соединение 64)
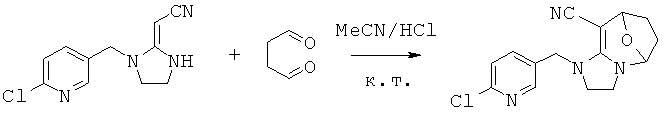
В 50 мл круглодонную колбу добавляли 1,17 г (0,005 моль) 2-(1-((6-хлорпиридин-3-ил)метил)имидазолидин-2-илиден)ацетонитрила, 30 мл сухого ацетонитрила и 0,860 г (0,01 моль) янтарного альдегида и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 66%.
Т.пл.=125,1-126,8°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 8,34 (d, J=2,4 Гц, 1Н), 7,82 (dd, J1=2,4 Гц, J2=8,4 Гц, 1Н), 7,55 (d, J=8,4 Гц, 1Н), 5,33 (s, 1Н), 5,25 (s, 1Н), 5,00 (d, J=15,6 Гц, 1Н), 4,78 (d, J=15,6 Гц, 1Н), 3,56-3,78 (m, 4H), 1,91-2,00 (m, 4H) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 153,6, 149,0, 148,6, 139,7, 132,3, 121,5, 99,6, 87,3, 75,7, 51,3, 50,2, 46,6, 31,5, 29,7 млн-1; МСВР (ES+) вычислено для C15H16N4O35Cl (М+Н)+ 303,1013; обнаружено 303,0992; вычислено для C15H16N4O37Cl (M+H)+ 305,0983; обнаружено 305,0957.
Пример 12
Синтез 1-((6-хлорпиридин-3-ил)метил)-10-нитро-1,2,3,5,6,7,8,9-октагидро-5,9-эпоксиимидазо[1,2-а]азоцина (соединение 77)
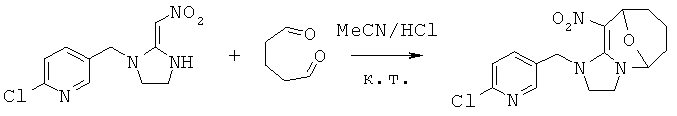
В 50 мл круглодонную колбу добавляли 1,27 г (0,005 моль) 2-хлор-5-((2-(нитрометилен)имидазолидин-1-ил)метил)пиридина, 30 мл ацетонитрила, 3 мл 25% водного раствора глутаральдегида (0,0075 моль глутаральдегида) и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при кт и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 86%.
Т.пл.=174,7-175,4°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 8,38 (dd, J1=0,6 Гц, J2=2,4 Гц, 1Н), 7,84 (dd, J1=2,4 Гц, J2=8,4 Гц, 1Н), 7,52 (dd, J1=0,6 Гц, J2=8,4 Гц, 1Н), 5,12 (s, 1Н), 5,04-5,05 (m, 1Н), 4,97 (d, J=15,6 Гц, 1Н), 4,71 (d, J=15,6 Гц, 1Н), 3,62-3,74 (m, 4H), 1,66-1,81 (m, 4H), 1,51-1,55 (m, 1Н), 1,32-1,44 (m, 1Н) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): δ 156,6, 149,7, 149,6, 139,7, 132,9, 124,5, 105,8, 81,7, 68,9, 51,7, 50,0, 46,3, 28,8, 27,2, 14,8 млн-1; МСВР (EI+) вычислено для C15H17N4O3 35Cl (М+) 336,0989; обнаружено 336,0988; вычислено для C15H17N4O3 37Cl (M+) 338,0960; обнаружено 338,0968.
Пример 13
Синтез 10-нитро-1-((тетрагидрофуран-3-ил)метил)-1,2,3,5,6,7,8,9-октагидро-5,9-эпоксиимидазо[1,2-а]азоцина (соединение 80)
Следуя способу, описанному в Примере 1, 0,2 моль 3-(хлорметил)тетрагидрофурана использовали вместо 2-хлор-5-(хлорметил)пиридина в качестве исходного вещества. Получали 2-(нитрометилен)-1-((тетрагидрофуран-3-ил)метил)имидазолидин при выходе 51%. ЖХ-МС (m/s) 177 (29), 99 (100), 56 (9).
Синтез 10-нитро-1-((тетрагидрофуран-3-ил)метил)-1,2,3,5,6,7,8,9-октагидро-5,9-эпоксиимидазо[1,2-а]азоцина
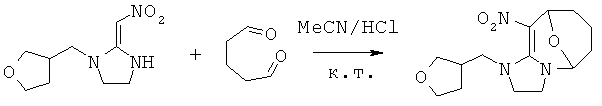
В 50 мл круглодонную колбу добавляли 1,065 г (0,005 моль) 2-(нитрометилен)-1-((тетрагидрофуран-3-ил)метил)имидазолидина, 30 мл ацетонитрила, 3 мл 25% водного раствора глутаральдегида (0,0075 моль глутаральдегида) и каталитическое количество концентрированной HCl. Реакционную смесь перемешивали при к.т. и проводили мониторинг по ТСХ. После завершения смесь выпаривали для удаления растворителя и очищали колоночной хроматографией с получением конечного продукта в виде бледно-желтого порошка при выходе 36%.
Т.пл.=115,3-116,9°С; 1H ЯМР (400 МГц, ДМСО-d6): δ 5,11 (s, 1H), 5,00-5,03 (m, 1H), 4,18 (d, J=3,2 Гц, 2H), 4,05-4,25 (m, 2H), 3,85-3,96 (m, 4H), 2,25 (m, 1H), 1,66-1,81 (m, 4H), 1,63 -1,64 (m, 2H), 1,57-1,59 (m, 2H), 1,51-1,55 (m, 1H), 1,32-1,44 (m, 1H) млн-1; 13С ЯМР (100 МГц, ДМСО-d6): 6 81,7, 80,6, 78,5, 68,9, 50,0, 49,7, 46,9, 44,6, 36,8, 33,9, 28,8, 27,2, 17,8, 14,8 млн-1; МСВР (EI+) вычислено для C14H21N3O4 (М+) 295,1532; обнаружено 295,1598.
Пример 14
Тест на инсектицидную активность соединений по изобретению
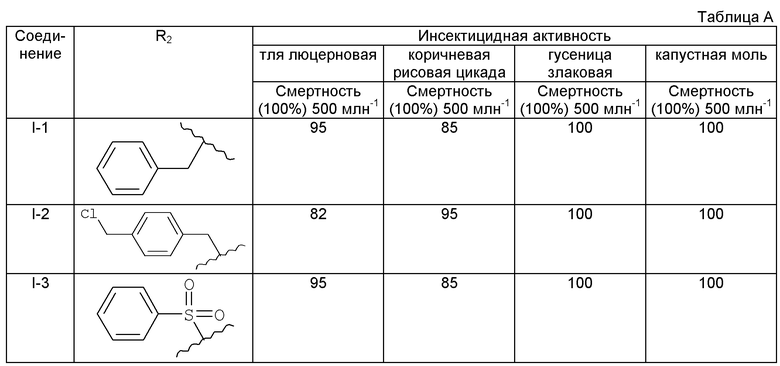
(1) Тест на активность в отношении тли люцерновой (Aphis craccivoral)
Тли, которые принадлежат к Homoptera и имеют колюще-сосущий ротовой аппарат, являются распространенными насекомыми для сельскохозяйственных растений. Aphis craccivoral тестировали путем погружения.
Метод тестирования: точно взвешенные различные образцы независимо добавляли к N,N-диметилформамиду с получением 10 г/л маточного раствора. Смесь разводили 0,2 мл/л водным раствором Тритона Х-100 до концентрации 500 м.д. После стабильного сосания на проростках фасоли взрослых тлей без крыльев вместе с проростками фасоли погружали в разведение 500 м.д., вынимали через 5 секунд, и избыточное разведение отсасывали промокательной бумагой, и взрослых тлей без крыльев инкубировали в чистом сосуде при постоянной температуре 23°С. Каждую концентрацию повторяли 3 раза, и контрольная группа содержала 0,2 мл/л водного раствора Тритон Х-100. Число погибших тлей подсчитывали через 24 часа для вычисления смертности по следующей формуле:
смертность (%) = (число контрольных живых тлей - число обработанных живых тлей)/число контрольных живых тлей × 100%.
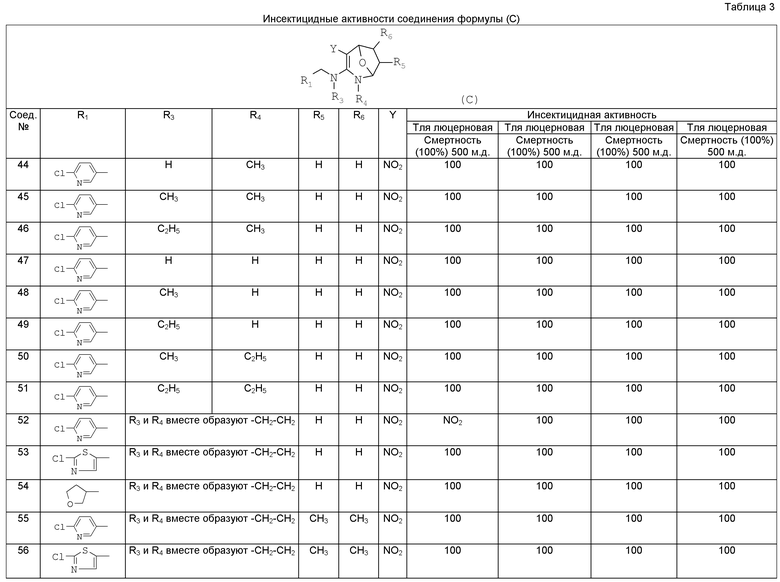
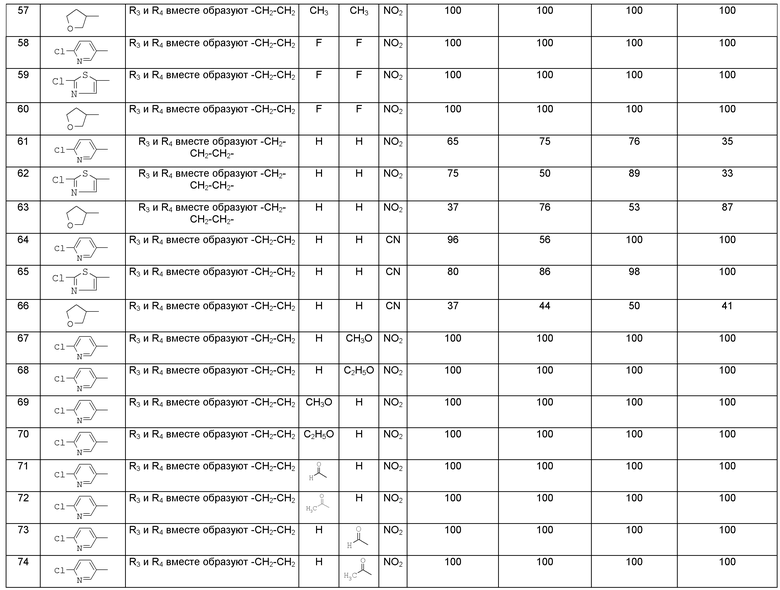
Результаты приведены ниже в таблицах 1-4.
(2) Тест на активность в отношении коричневых рисовых цикад {Nilaparvata lugens)
Коричневые рисовые цикады, которые принадлежат к Homoptera и имеют колюще-сосущий ротовой аппарат, являются распространенными насекомыми для сельскохозяйственных растений. Nilaparvata lugens тестировали путем распыления.
Метод тестирования; тестируемое соединение точно готовили в растворе ацетона до конечной концентрации 500, 250, 100, 50, 25, 12,5, 6,25, 3,13, 1,57 и 0,79 м.д. Водный раствор ацетона использовали в качестве контроля. Каждый процесс повторяли в 3 сосудах (3 раза). 2 мл раствора равномерно распыляли на каждую чашку с помощью ручного мини-опрыскивателя. 10 Nilaparvata lugens вводили в каждую ванночку за 6 часов до распыления. Проводили три серии экспериментов. Число погибших Nilaparvata lugens подсчитывали через 24 часа для вычисления смертности с использованием вышеупомянутой формулы. Результаты представлены ниже в таблицах 1-4.
(3) Тест на активность в отношении гусеницы, поражающей злаковые растения (Pseudaletia separate Walker)
Гусениц, поражающих злаковые растения, тестировали путем скармливания погруженных листьев. Тестируемое соединение точно готовили в растворе ацетона до конечной концентрации 500, 250, 100, 50, 25, 12,5, 6,25, 3,13, 1,57 и 0,79 м.д. Водный раствор ацетона использовали в качестве контроля. Свежие листья кукурузы погружали в раствор на 3 секунды и высушивали при комнатной температуре и использовали для скармливания тестируемым насекомым. Каждый процесс повторяли 3 раза, причем в каждом эксперименте тестировали 10 гусениц. Число погибших гусениц подсчитывали через 24 часа для вычисления смертности с использованием вышеупомянутой формулы. Результаты представлены ниже в таблицах 1-4.
(4) Тест на активность в отношении капустной моли (Plutella xylostella)
Капустную моль тестировали путем скармливания погруженных листьев. Свежие листья капусты погружали в вышеупомянутый раствор на 3 секунды и и высушивали при комнатной температуре и использовали для скармливания тестируемым насекомым. Каждый процесс повторяли 3 раза, причем в каждом эксперименте тестировали 10 капустных молей. Число погибших капустных молей подсчитывали через 24 часа для вычисления смертности с использованием вышеупомянутой формулы. Результаты представлены ниже в таблицах 1-4.
















































Пример 15
Получение инсектицидной композиции, содержащей активное соединение по изобретению
а) Масляная суспензия
Готовили следующие ингредиенты: 25 масс.% любого соединения, выбранного из соединений 1-73; 5 масс.% полиоксиэтиленсорбитана гексаолеата и 70 масс.% высшего алифатического углеводородного масла. Все компоненты измельчали в песочной мельнице до тех пор, пока твердые гранулы не уменьшались до размера менее чем примерно 5 микрометров. Полученную в результате вязкую суспензию можно было использовать непосредственно, либо использовать после эмульгирования в воде.
б) Водная суспензия
Готовили следующие компоненты: 25 масс.% любого соединения, выбранного из соединений 1-73; 3 масс.% гидрата аттапульгита; 10 масс.% кальция лигносульфоната; 0,5 масс.% натрия дигидрофосфата и 61,5 масс.% воды. Все компоненты измельчали в шаровой мельнице до тех пор, пока твердые гранулы не уменьшались до размера менее чем примерно 10 микрометров. Водную суспензию можно было использовать непосредственно.
в) Препарат приманки
Готовили следующие ингредиенты: 0,1-10 масс.% любого соединения, выбранного из соединений 1-73; 80 масс.% пшеничной муки и 19,9-10 масс.% мелассы. Все ингредиенты в достаточной степени смешивали и по необходимости формовали. Пищевая приманка может быть проглочена, или ее можно распределять в домашних или промышленных помещениях, таких как кухня, больница, хранилище, а также на открытом воздухе в области, пораженной насекомыми, вредными для здоровья населения.
Все документы, цитируемые в данной заявке, включены в изобретение в виде ссылки, как если бы каждый из них был включен индивидуально. Кроме того, должно быть понятно, что в свете вышеописанных положений изобретения специалист в данной области техники может произвести различные изменения или модификации изобретения, и эти эквиваленты будут, тем не менее, находиться в пределах объема изобретения, определенного прилагаемой ниже формулой изобретения.
Дополнительный пример 1:
Стадия 1. Синтез N-бензил-1,2-этандиамина
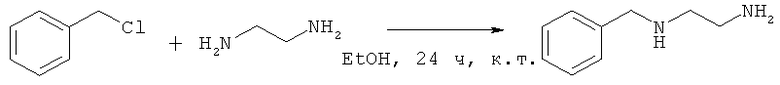
Бензилхлорид (1,26 г, 10 ммоль) растворяли в безводном этаноле (40 мл), смесь перемешивали в ледяной бане и добавляли безводный этандиамин (50 ммоль). Раствор становился желтым. После добавления смесь перемешивали при комнатной температуре в течение 24 часов и проводили мониторинг по ТСХ. После завершения смесь фильтровали, и фильтрат упаривали для удаления этанола. К остатку добавляли воду и экстрагировали смесь с помощью CH2Cl2 (30 мл × 10). Органические фазы объединяли, сушили над Na2SO4 и концентрировали с получением конечного продукта в виде желтого масла (0,627 г. Выход: 41,8%).
Стадия 2. Синтез ((2-(нитрометилен)имидазолин-1-ил)метил)бензола
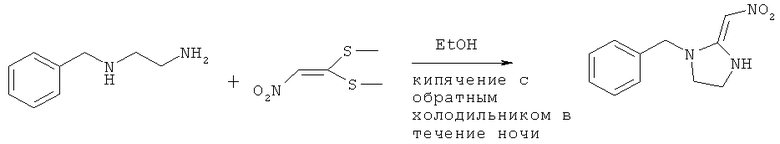
N-бензил-1,2-этандиамин (10 ммоль) растворяли в безводном этаноле (10 мл) и добавляли (2-нитроэтилен-1,1-диил)бис(метилсульфана) (1,61 г, 10 ммоль). Смесь кипятили с обратным холодильником и проводили мониторинг по ТСХ. После завершения смесь охлаждали до комнатной температуры и фильтровали. Отфильтрованный осадок промывали этилацетатом трижды и осушали с получением целевого продукта (1,012 г. Выход: 46%).
Стадия 3. Синтез 1-бензил-9-нитро-2,3,5,6,7,8-гексагидро-1Н-5,8-эпоксиимидазо[1,2-а]азепина
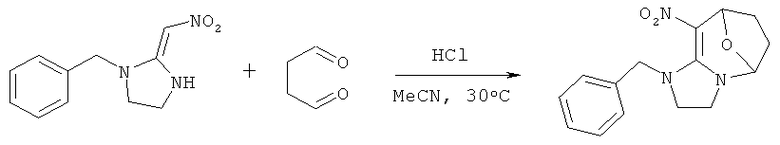
Целевое соединение получали способом согласно Примеру 8 за исключением того, что 2-хлор-5-((2-(нитрометилен)имидазолидин-1-ил)метил)пиридин заменяли ((2-(нитрометилен)имилазолидин-1-ил)метил)бензолом. Выход составил 30%.
Т.Пл. 124,7-125,6°С,
1H ЯМР (400 МГц, ДМСО-d6) δ 8,54 (d, J=2,2 Гц, 1 Н), 8,51 (dd, J=4,8, 1,7 Гц, 1Н), 7,74 (dt, J=7,8, 2,0 Гц, 2Н), 7,39 (dd, J=7,8, 4,7 Гц, 1Н), 5,39 (d, J=4,5 Гц, 2Н), 5,03 (d,J=15,4 Гц, 1Н), 4,76 (d, aJ=15,4 Гц, 1Н), 3,76-3,59 (m, 4H), 2,07-1,92 (m,4H). 13С ЯМР (100 МГц, ДМСО) δ 155,60; 149,44; 149,15; 135,95; 135,95; 132,81; 124,00; 109,66; 87,00; 75,19; 51,75; 50,23; 46,67; 31,84; 31,65. (ES+) вычислено для C14H16N4O3 (М+Н)+, 288,1270; обнаружено 288,1301.
Дополнительный пример 2:
1. Синтез N-((пиридин-3-ил)метил)-1,2-этандиамина
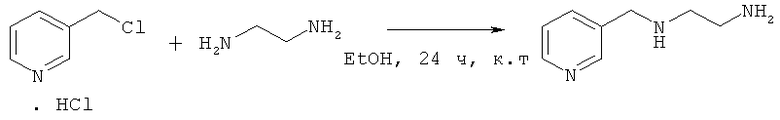
Указанное в заголовке соединение получали согласно Стадии 1 Дополнительного примера 1, за исключением того, что бензилхлорид заменяли 3-хлорметил-пиридин гидрохлоридом. Выход составил 41,8%.
2. 3-((2-(трифторметил)сульфурил-винил)имидазолидин-1-ил)метил)пиридин
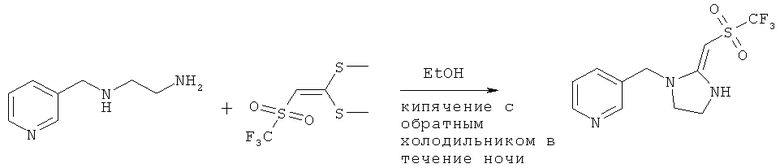
Соединение, указанное в заголовке, получали согласно Стадии 2 Дополнительного примера 1, за исключением того, что использовали другие исходные вещества, как указано на реакционной схеме. Выход составил 48%.
3. Синтез 1-(пиридин-3-ил)метил)-9-(трифторметил)сульфурил-2,3,5,6,7,8-гексагидро-1Н-5,8-эпоксимидазо[1,2-а]азепина
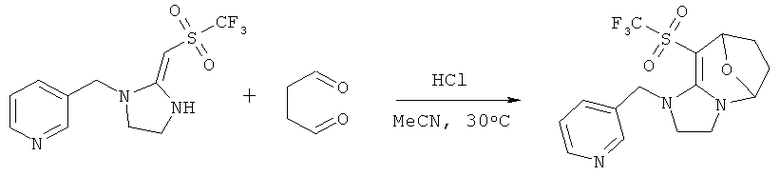
Соединение, указанное в заголовке, получали согласно Стадии 3 Дополнительного примера 1, за исключением того, что использовали другие исходные вещества, как указано на реакционной схеме. Выход составил 36%.
1H ЯМР (400 МГц, ДМСО-d6) δ 8,52 (d, J=2,2 Гц, 1 Н), 8,45 (dd, J=4,8, 1,7 Гц, 1Н), 7,86 (dt, J=7,8, 2,0 Гц, 1Н), 7,38 (dd, J=7,8, 4,7 Гц, 1Н), 4,88 (d, J=4,5 Гц, 2Н), 4,43 (d, J=15,4 Гц, 1Н), 4,26 (d, J=15,4 Гц, 1Н), 2,76-2,59 (m, 4H), 2,05-1,73 (m, 4H). 13С ЯМР (100 МГц, ДМСО) δ 157,80; 154,70; 148,55; 147,35; 135,51; 135,60; 123,06; 107,90; 88,71; 66,51; 58,30; 53,76; 51,49; 35,51; 27,52.
Дополнительный пример 3:
1. Синтез N-((2-хлор-пиридин-5-ил)метил)-1,2-этандиамина
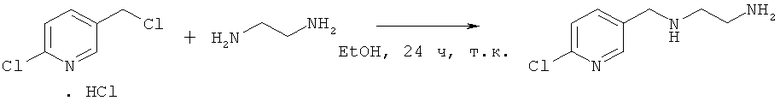
Соединение, указанное в заголовке, получали согласно Стадии 1 Дополнительного примера 1, за исключением того, что использовали другие исходные вещества, как указано на реакционной схеме. Выход составил 47,2%.
2. Синтез 2-хлор-5-((2-(трифторметил-винил)имидазолидин-1-ил)метил)пиридина
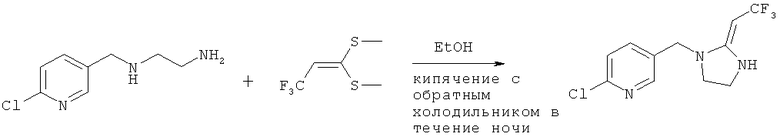
Соединение, указанное в заголовке, получали согласно Стадии 2 Дополнительного примера 1, за исключением того, что использовали другие исходные вещества, как указано на реакционной схеме. Выход составил 57%.
3. Синтез 1-(2-хлор-пиридин-5-ил)метил)-9-трифторметил-2,3,5,6,7,8-гексагидро-1Н-5,8-эпоксимидазо[1,2-а]азепина
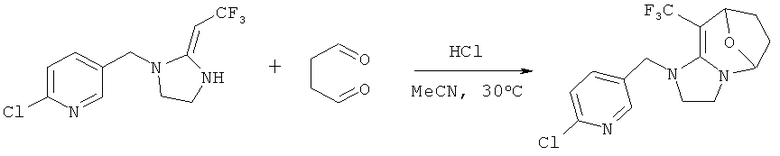
Соединение, указанное в заголовке, получали согласно Стадии 3 Дополнительного примера 1, за исключением того, что использовали другие исходные вещества, как указано на реакционной схеме. Выход составил 61%.
1H ЯМР (400 МГц, ДМСО-d6) δ 8,52 (d, J=2,2 Гц, 1 Н), 7,86 (dt, J=7,8, 2,0 Гц, 1Н), 7,38 (dd, J=7,8, 4,7 Гц, 1Н), 4,82 (d, J=4,5 Гц, 2H), 4,34 (d, J=15,4 Гц, 1 Н), 4,26 (d,J=15,4 Гц, 1Н), 2,67-2,59 (m, 4H), 2,15-1,73 (m, 4H).
13С ЯМР (100 МГц, ДМСО) δ 155,00; 148,50; 147,53; 135,51; 135,60; 123,06; 113,73; 108,29; 86,01; 58,57; 58,31; 53,96; 52,24; 35,45; 28,62.
Дополнительный пример 4:
1. Синтез N-((5-хлортиазол-2-ил)метил)-1,2-этандиамина
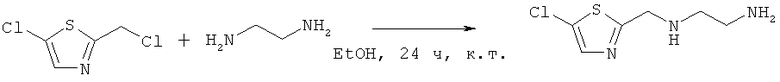
Соединение, указанное в заголовке, получали согласно Стадии 1 Дополнительного примера 1, за исключением того, что использовали другие исходные вещества, как указано на реакционной схеме. Выход составил 39.1%.
2. Синтез 5-хлор-2-((2-(трифторметокси-винил)имидазолидин-1-ил)метил)тиазола
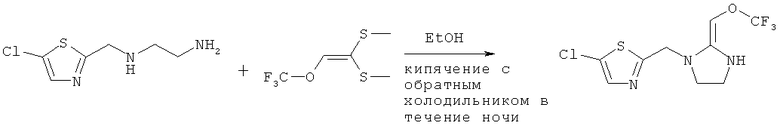
Соединение, указанное в заголовке, получали согласно Стадии 2 Дополнительного примера 1, за исключением того, что использовали другие исходные вещества, как указано на реакционной схеме. Выход составил 44%.
3. Синтез 1-(5-хлортиазол-2-ил)метил)-9-три фторметокси-2,3,5,6,7,8-гескагидро-1Н-5,8-эпоскимидазо[1,2-а]азепина
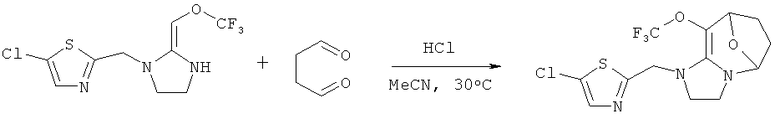
Соединение, указанное в заголовке, получали согласно Стадии 3 Дополнительного примера 1, за исключением того, что использовали другие исходные вещества, как указано на реакционной схеме. Выход составил 48%.
1Н ЯМР (400 МГц, ДМСО-d6) δ 7,49 (s, 1H), 4,88 (d, J=4,5 Гц, 2Н), 4,43 (d, J=15,4 Гц, 1H), 4,26 (d, J=15,4 Гц, 1Н), 2,67-2,59 (m, 4H), 2,15-1,73 (m, 4H).
13С ЯМР (100 МГц, ДМСО) δ 168,60; 138,53; 121,30; 123,05; 115,70; 108,29; 106,04; 79,11; 58,35; 53,96; 52,24; 35,45; 25,26.
Дополнительный пример 5:
Инсектицидную активность соединений, полученных согласно Дополнительным примерам 1-4 тестировали тем же способом, что и в Примере 14.
Результаты испытаний показали, что смертность тли люцерновой, коричневой рисовой цикады, гусениц, поражающих злаковые растения, и капустной моли составила 90~100% при 500 млн-1.
Дополнительный пример 6: Синтез соединения I-1
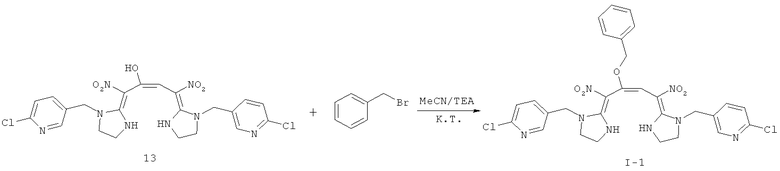
Соединение 13 (0,01 моль) подвергали реакции с бензил бромидом (0,01 моль) в присутствии триэтаноламина (TEA) (0,01 моль) в MeCN (30 мл) при комнатной температуре. Проводили мониторинг реакции по ТСХ. После завершения смесь упаривали для удаления растворителя, и полученную смесь очищали колоночной хроматографией с получением конечного соединения. Выход: 85%.
т.пл.=168,1-168,9°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,42 (d; J=2,0 Гц; 1Н); 8,39 (d; J=2,0 Гц; 1Н); 7,81-7,86 (m; 2H); 7,64 (d; J=8,0 Гц; 2Н); 7,49-7,53 (m; 2H); 7,47 (t; J=8,0 Гц; 1Н); 7,41 (d; J=8,0 Гц; 2H); 6,51(d; J=7,2 Гц; 1Н); 6,22 (s; 2H); 5,34 (d; J=15,2 Гц; 1Н); 5,18 (d; J=15,2 Гц; 1Н); 4,84 (dd; J1=2,4 Гц; J2=7,2 Гц; 1Н); 4,75 (d; J=16,8 Гц; 1Н); 4,63 (d; J=16,8 Гц; 1Н); 3,96 (d; J=2,4 Гц; 1H); 3,84-3,92 (m; 2H); 3,63-3,81 (m; 5H); 3,35-3,45 (m; 1Н) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 154,9; 151,3; 150,0; 149,3; 137,1; 136,0; 128,3; 128,2; 125,2; 104,3; 84,6; 71,1; 54,6; 52,6; 44,5 ppm;
Масс-спектрометрия высокого разрешения (ES+) вычислено для C29H29 35Cl2N8O5 (M+H)+ 639,1560; обнаружено 639,1566. Вычислено для C29H29 37Cl2N8O5 (M+H)+ 643,1560; обнаружено 643,1560.
Дополнительный пример 7: Синтез соединения I-2
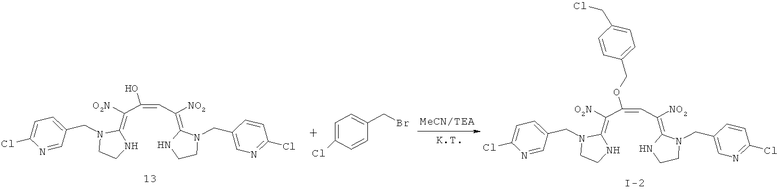
Соединение I-2 получили согласно Дополнительному примеру 5, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 83%.
т.пл.=169,5-171,2°С;
1H ЯМР (400 МГц, ДМСО-d6): δ 8,41 (d; J=2,0 Гц; 1Н); 8,34 (d; J=2,0 Гц; 1Н); 7,80-7,85 (m; 2H); 7,63 (d; J=8,0 Гц; 2H); 7,47-7,52 (m; 2H); 7,40 (d; J=8,0 Гц; 2Н); 6,50 (d; J=7,2 Гц; 1Н); 6,21 (s; 2H); 5,62 (s; 2H); 5,34 (d; J=15,2 Гц; 1Н); 5,15 (d; J=15,2 Гц; 1Н); 4,80 (dd; J1=2,4 Гц; J2=7,2 Гц; 1Н); 4,81 (d; J=16,8 Гц; 1Н); 4,62 (d; J=16,8 Гц; 1Н); 3,92 (d; J=2,4 Гц; 1Н); 3,82-3,92 (m; 2H); 3,62-3,81 (m; 5H); 3,32-3,39 (m; 1Н) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 154,9; 151,4; 151,3; 150,0; 149,3; 136,0; 135,4; 130,4; 129,7; 128,7; 125,2; 104,3; 84,5; 71,1; 54,6; 52,8; 47,1; 44,5 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C30H30N8O5 35Cl3 (M+H)+ 687,1326; обнаружено 687,1320. Вычислено для C30H30N8O5 37Cl3 (M+H)+ 689,1326; обнаружено 689,1320.
Дополнительный пример 8: Синтез соединения I-3
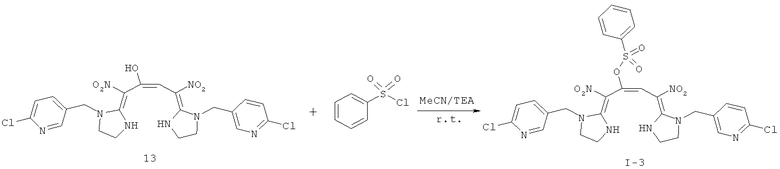
Соединение I-3 получали согласно Дополнительному примеру 5 за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 73%.
т.пл.=202,2-203,1°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,43 (d; J=2,0 Гц; 1Н); 8,37 (d; J=2,0 Гц; 1Н); 7,82-7,85 (m; 2H); 7,65 (d; J=8,0 Гц; 2H); 7,44-7,50 (m; 2H); 7,48 (t; J=8,0 Гц; 1Н); 7,40 (d; J=8,0 Гц; 2H); 6,61 (d; J=7,2 Гц; 1Н); 5,35 (d; J=15,2 Гц; 1Н); 5,18 (d; J=15,2 Гц; 1Н); 4,82 (dd; J1=2,4 Гц; J2=7,2 Гц; 1Н); 4,72 (d; J=16,8 Гц; 1Н); 4,64 (d; J=16,8 Гц; 1Н); 3,93 (d; J=2,4 Гц; 1Н); 3,84-3,92 (m; 2Н); 3,67-3,81 (m; 5Н); 3,25-3,35 (m; 1H) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 151,4; 150,0; 149,3; 146,9; 136,0; 133,0; 130,0; 129,1; 128,7; 125,2; 102,7; 97,3; 54,6; 52,7; 44,5 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C28H27N8O7 35Cl2S (М+Н)+ 689,1022; обнаружено 689,1008. Вычислено для C28H27N8O7 37Cl2S (M+H)+ 691,1022; обнаружено 691,1008.
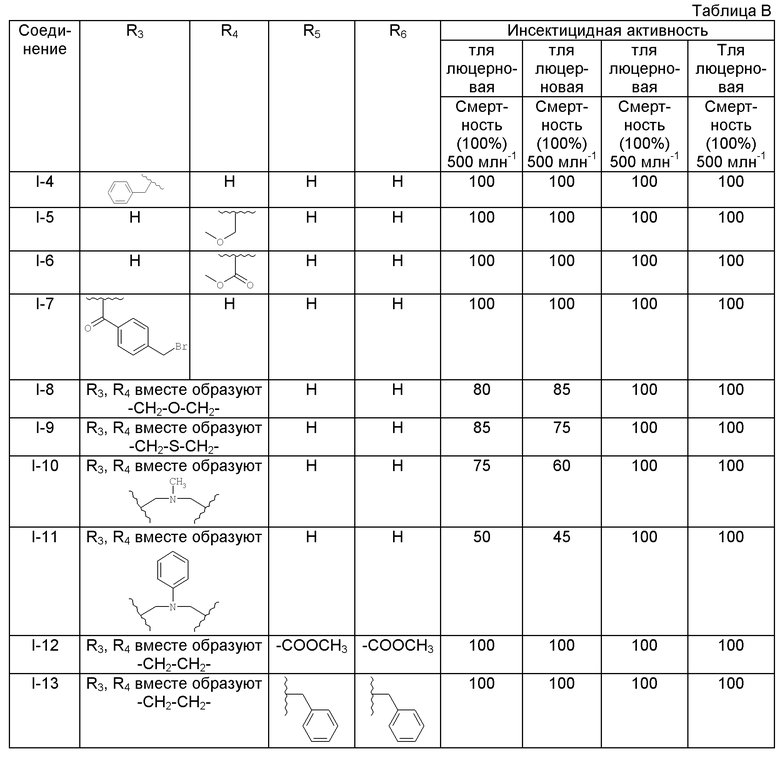
Дополнительный пример 9: Синтез соединения I-4
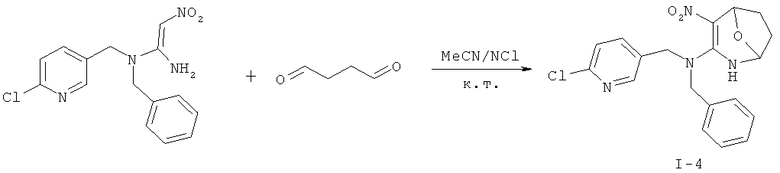
Соединение I-4 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 62%.
т.пл.=128,2-129,8°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,35 (d; J=2,4 Гц; 1H); 7,81 (dd; Л=2,4 Гц; J2=8,4 Гц; 1H); 7,51 (d; J=8,4 Гц; 1H); 7,47 (d; J=8,0 Гц; 1H); 7,32 (t; J=8,0 Гц; 2Н); 7,28 (d; J=8,0 Гц; 2Н); 5,36 (s; 2Н); 5,18 (s; 2Н); 5,00 (d; J=15,6 Гц; 1H); 4,68 (d; J=15,6 Гц; 1Н); 1,94-2,04 (m; 4H) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 155,6:149,7; 149,6; 139,7; 132,6; 124,5; 109,6; 87,0; 75,1; 51,2; 50,3; 46,6; 31,9; 31,7 ppm; 13С ЯМР (100 МГц; ДМСО-d6): δ 152,2; 150,0; 149,3; 144,7; 129,8; 125,2; 118,7; 84,4; 74,6; 56,9; 55,78; 31,6; 29,4; 14,2 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C19H20N4O3 35Cl (М+Н)+ 387,1146; обнаружено 387,1139. Вычислено для C19H20N4O3 37Cl (M+H)+ 389,1146; обнаружено 389,1139.
Дополнительный пример 10: Синтез соединения I-5
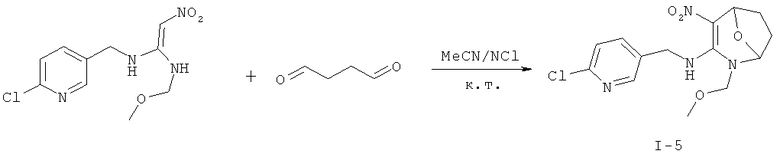
Соединение I-5 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 68%.
т.пл.=130,2-130,8°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,35 (d; J=2,4 Гц; 1Н); 7,81 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н);7,51 (d; J=8,4 Гц; 1Н); 5,36 (s; 2Н); 5,18 (s; 2H); 5,00 (d; J=15,6 Гц; 1Н); 4,68 (d; J=15,6 Гц; 1Н); 3,35 (s; ЗН); 2,85 (s; 2H);1,94-2,04 (m; 4H) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 156,1; 149,2; 135,4; 132,3; 124,7; 88,4; 81,4; 74,6; 56,6; 48,8; 30,8; 27,9 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C14H18N4O4 35Cl (M+H)+ 341,0938; обнаружено 341,0933. Вычислено для C14H18N4O4 37Cl (M+H)+ 343,0938; обнаружено 343,0933.
Дополнительный пример 11: Синтез соединения I-6
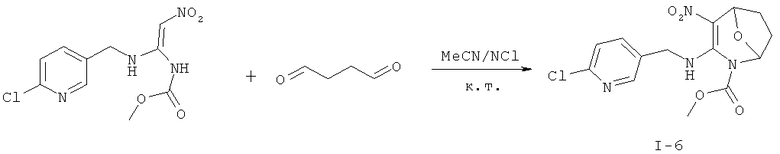
Соединение I-6 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 71%.
т.пл.=144,2-145,8°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,32 (d; J=2,4 Гц; 1Н); 7,84 (dd; Л=2,4 Гц; J2=8,4 Гц; 1H); 7,57 (d; J=8,4 Гц; 1Н); 5,29 (s; 2H); 5,15(s; 2H); 5,10 (d; J=15,6 Гц; 1Н); 4,78 (d; J=15,6 Гц; 1Н); 3,37 (s; 3Н); 1,94-2,00 (m; 4H) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 162,4; 156,5; 149,2; 135,4; 124,7; 88,1; 74,6; 53,5; 48,8; 31,3; 27,9 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C14H16N4O5 35Cl (М+Н)+ 355,0731; обнаружено 355,0723. Вычислено для C14H16N4O5 37Cl (М+Н)+ 357,0731; обнаружено 357,0723.
Дополнительный пример 12: Синтез соединения I-7
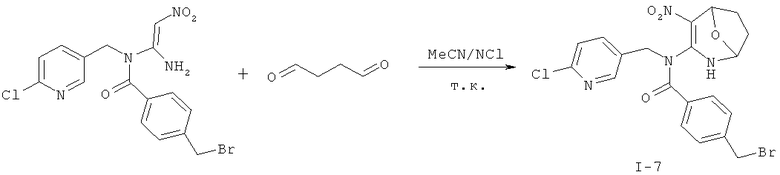
Соединение I-7 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 72%.
т.пл.=158,2-159,8°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,32 (d; J=2,4 Гц; 1Н); 7,80 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н); 7,54 (d; J=8,4 Гц; 1Н); 7,42 (d; J=8,0 Гц; 1Н); 7,22 (d; J=8,0 Гц; 2Н); 5,34 (s; 2Н); 5,11 (s; 2H); 5,02 (d; J=15,6 Гц; 1Н); 4,67 (d; J=15,6 Гц; 1Н); 1,92-2,01 (m; 4H) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 155,6; 149,7; 149,6; 139,7; 132,6; 124,5; 109,6; 87,0; 75,1; 51,2; 50,3; 46,6; 31,9; 31,7 ppm; 13С ЯМР (100 МГц; ДМСО-d6): δ 170,3; 151,0; 150,2; 148,6; 143,5; 135,8; 134,9; 129,8; 129,0; 127,7; 124,8; 84,4; 74,6; 47,9; 31,6; 30,8; 29,4 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C20H19N4O4Br35Cl (M+H)+ 493,0200; обнаружено 493,0191. Вычислено для C20H19N4O4Br37Cl (M+H)+ 495,0200; обнаружено 495,0191.
Дополнительный пример 13: Синтез соединения I-8
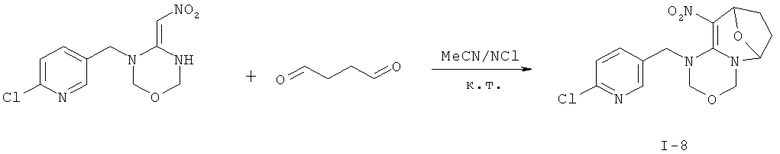
Соединение I-8 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме.
Выход: 66%.
т.пл.=138,2-139,7°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,32 (d; J=2,4 Гц; 1Н); 7,81 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н); 7,55 (d; J=8,4 Гц; 1Н); 5,70 (s; 2Н); 5,57 (s; 2Н); 5,32 (s; 2H); 5,04 (d; J=15,6 Гц; 1Н); 4,61 (d; J=15,6 Гц; 1Н); 1,92-2,04 (m; 4H) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 155,6; 149,7; 149,6; 139,7; 132,6; 124,5; 109,6; 87,0; 75,1; 51,2; 50,3; 46,6; 31,9; 31,7 ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 155,8; 150,0; 149,3; 136,0; 130,4; 125,2; 77,3; 70,9; 63,3; 53,9; 24,7 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C14H16N4O4 35Cl (M+H)+ 339,0784; обнаружено 3390789. Вычислено для C14H16N4O4 37Cl (M+H)+, 341,0784; обнаружено 341,0789.
Дополнительный пример 14: Синтез соединения I-9
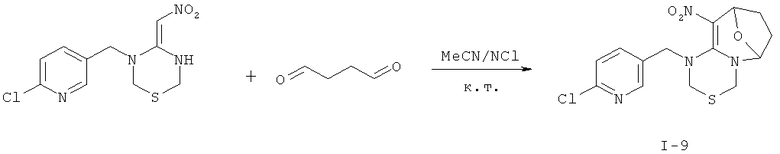
Соединение I-9 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 63%,
т.пл.=168,2-169,4°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,31 (d; J=2,4 Гц; 1Н); 7,84 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н); 7,52 (d; J=8,4 Гц; 1Н); 5,71 (s; 2Н); 5,57 (s; 2Н); 5,31 (s; 2Н); 5,05 (d; J=15,6 Гц; 1Н); 4,61 (d; J=15,6 Гц; 1Н); 1,93-2,07 (m; 4H) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 155,6; 149,7; 149,6; 139,7; 132,6; 124,5; 109,6; 87,0; 75,1; 51,2; 50,3; 46,6; 31,9; 31,7 ppm; 13С ЯМР (100 МГц; ДМСО-d6): δ 178,2; 150,0; 149,3; 136,0; 130,4; 125,2; 89,2; 73,9; 57,5; 53,9; 51,5; 30,9; 27,9 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C14H16N4O3S35Cl (М+Н)+ 355,0553; обнаружено 355,0559. Вычислено для C14H16N4O3S37Cl (M+H)+ 357,0553; обнаружено 357,0559.
Дополнительный пример 15: Синтез соединения I-10
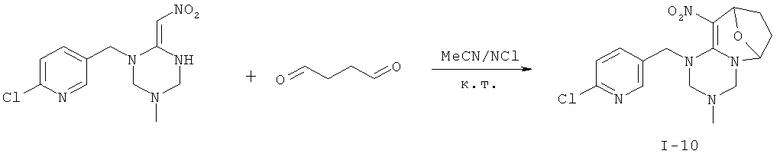
Соединение I-10 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 68%.
т.пл.=155,2-156,7°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,32 (d; J=2,4 Гц; 1Н); 7,82 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н); 7,54 (d; J=8,4 Гц; 1Н); 5,72 (s; 2Н); 5,57 (s; 2Н); 5,35 (s; 2H); 5,02 (d; J=15,6 Гц; 1Н); 4,64 (d; J=15,6 Гц; 1Н); 1,94-2,07 (m; 4H); 1,15 (s; 3H) ppm; 13C ЯМР (100 МГц; ДМСО-d6): 6 162,1; 150,0; 149,3; 136,0; 130,4; 125,2; 89,5; 73,9; 67,2; 56,4; 42,9; 30,9; 27,9 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C15H19N6O3 35Cl (М+Н)+ 352,1098; обнаружено 352,1092. Вычислено для C15H19N5O3 37Cl (М+Н)+ 354,1092; обнаружено 354,1098.
Дополнительный пример 16: Синтез соединения I-11
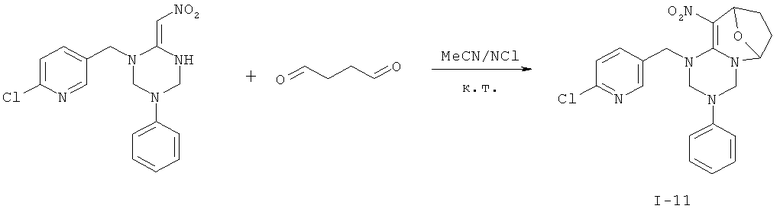
Соединение I-11 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 71%.
т.пл.=142,2-143,8°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,35 (d; J=2,4 Гц; 1Н); 7,82 (dd; J1=2,4 Гц; J2=8,4 Гц; 1H); 7,52 (d; J=8,4 Гц; 1Н); 7,43 (d; J=8,4 Гц; 2Н); 7,32 (t; J=8,4 Гц; 1Н); 7,29 (d; J=8,4 Гц; 2Н); 5,72 (s; 2Н); 5,54 (s; 2Н); 5,32 (s; 2Н); 5,05 (d; J=15,6 Гц; 1Н); 4,62 (d; J=15,6 Гц; 1Н); 1,95-2,07 (m; 4H) ppm; 13С ЯМР (100 МГц; ДМСО-d6): δ 162,1; 150,0; 149,3; 146,9; 136,0; 130,4; 130,3; 125,2; 122,5; 117,7; 89,5; 73,9; 62,2; 60,5; 56,4; 30,9; 27,8 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C20H21N5O3 35Cl (М+Н)+ 414,1255; обнаружено 414,1263. Вычислено для C20H21N5O3 37Cl (М+Н)+ 416,1255; обнаружено 416,1263.
Дополнительный пример 17: Синтез соединения I-12
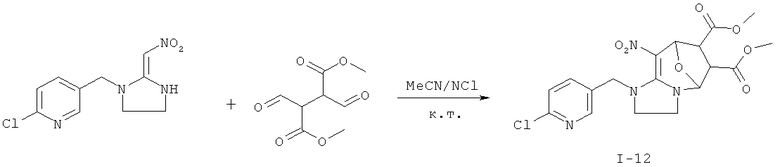
Соединение I-12 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 58%.
т.пл.=151,2-152,9°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,32 (d; J=2,4 Гц; 1Н); 7,84 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н); 7,53 (d; J=8,4 Гц; 1Н); 5,32 (s; 2Н); 5,03 (d; J=15,6 Гц; 1Н); 4,64 (d; J=15,6 Гц; 1Н); 3,52-3,73 (m; 4H); 2,32 (s; 2Н); 3,17 (s; 2Н); 1,95-2,04 (m; 2Н) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 155,6; 149,7; 149,6; 139,7; 132,6; 124,5; 109,6; 87,0; 75,1; 51,2; 50,3; 46,6; 31,9; 31,7 ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 171,7; 171,5; 150,0; 149,3; 136,0; 130,4; 125,2; 89,0; 71,6; 54,9; 52,2; 51,5; 50,6; 49,0; 46,9 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C18H19N4O35Cl (M+H)+ 439.0942; обнаружено 439,0933. Вычислено для C18H19N4O35Cl (M+H)+, 441,0942; обнаружено 441,0933.
Дополнительный пример 18: Синтез соединения I-13
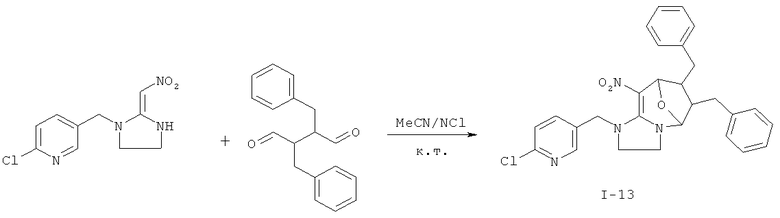
Соединение I-13 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 69%.
т.пл.=145,2-146,8°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,33 (d; J=2,4 Гц; 1Н); 7,81 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н); 7,51 (d; J=8,4 Гц; 1Н); 7,43 (t; J=8,4 Гц; 1Н); 7,25-7,38 (m; 8Н); 7,14 (t; J=8,4 Гц; 1Н); 6,57 (s; 2Н); 6,51 (s; 2H); 5,33 (s; 2Н); 5,05 (d; J=15,6 Гц; 1Н); 4,67 (d; J=15,6 Гц; 1Н); 3,54-3,73 (m; 2Н); 2,32 (s; 2Н); 3,21 (s; 2Н); 1,98-2,04 (m; 2Н) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 150,0; 149,3; 136,0; 130,4; 129,1; 128,7; 127,0; 125,2; 90,5; 76,8; 58,2; 50,6; 48,1; 46,9; 34,9; 33,2 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C28H28N4O3 35Cl (М+Н)+ 503,1772; обнаружено 503,1763. Вычислено для C28H28N4O3 37Cl (М+Н)+, 505,1772; обнаружено 505,1763.
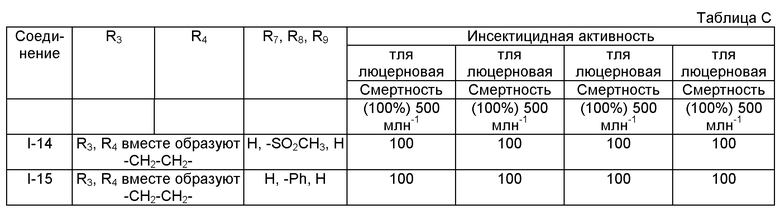
Дополнительный пример 19: Синтез соединения I-14
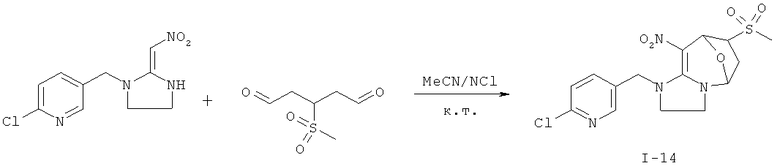
Соединение I-14 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 64%.
т.пл.=188,2-189,8°С;
1Н ЯМР (400 МГц; ДМСО-d6): δ 8,35 (dd; J1=0,6 Гц; J2=2,4 Гц; 1Н); 7,82 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н); 7,53 (dd; J1=0,6 Гц; J2=8,4 Гц; 1Н); 5,12 (s; 1H); 5,04-5,06 (m; 1Н); 4,92 (d; J=15,6 Гц; 1Н); 4,72 (d; J=15,6 Гц; 1Н); 3,64-3,74 (m; 4H); 3,55 (s; 3H); 1,71-1,84 (m; 3Н); 1,51-1,56 (m; 1Н); 1,31-1,40 (m; 1Н) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 157,6; 150,0; 149,3; 136,0; 130,4; 125,2; 75,6; 66,3; 54,9; 50,6; 47,7; 39,2; 32,5; 26,8 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C16H20N4O5S35Cl (М+Н)+ 415,0765; обнаружено 415,0760. Вычислено для C16H20N4O5S37Cl (М+Н)+, 417,0765; обнаружено 417,0760.
Дополнительный пример 20: Синтез соединения I-15
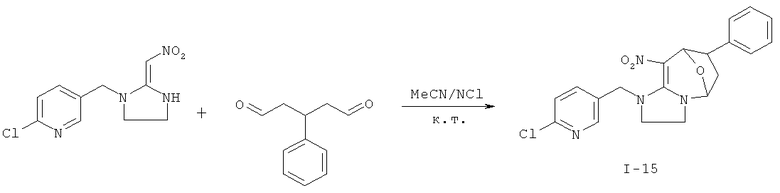
Соединение I-15 получали согласно Примеру 8, за исключением того, что использовали другие исходные вещества, как показано на реакционной схеме. Выход: 63%.
т.пл.=148,2-149,8°С;
1H ЯМР (400 МГц; ДМСО-d6): δ 8,33 (dd; J1=0,6 Гц; J2=2,4 Гц; 1Н); 7,84 (dd; J1=2,4 Гц; J2=8,4 Гц; 1Н); 7,63 (d; J=8,4 Гц; 1Н); 7,41 (t; J=8,4 Гц; 2H); 7,52 (dd; J1=0,6 Гц; J2=8,4 Гц; 1Н); 7,29 (d; J=8,4 Гц; 2H); 5,15 (s; 1H); 5,04-5,06 (m; 1Н); 4,98 (d; J=15,6 Гц; 1Н); 4,72(d; J=15,6 Гц; 1Н); 3,66-3,74 (m; 4H); 1,78-1,88 (m; 3Н); 1,52-1,55 (m; 1Н); 1,32-1,41 (m; 1Н) ppm; 13C ЯМР (100 МГц; ДМСО-d6): δ 155,9; 150,4; 149,2; 142,8; 140,2; 137,4; 136,1; 130,4; 125,6; 75,8; 66,5; 54,4; 50,8; 47,1; 32,8; 26,8 ppm;
Масс-спектрометрия высокого разрешения (ES+), вычислено для C21H22N4O3 35Cl (M+H)+ 413,1302; обнаружено 413,1311. Вычислено C21H22N4O3 37Cl (M+H)+ 415,1295; обнаружено 415,1304.
Дополнительный пример 21:
Инсектицидную активность соединений, полученных согласно Дополнительным Примерам 5-20 определяли тем же способом, что и в Примере 14 настоящей заявки.
Тест показал, что все соединения с I-1 по I-15 обладают очень хорошей инсектицидной активностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2001 |
|
RU2340611C2 |
| ПРОТИВОФИБРОЗНЫЕ ПИРИДИНОНЫ | 2015 |
|
RU2692485C2 |
| ФОСФОИНДОЛЫ КАК ИНГИБИТОРЫ ВИЧ | 2005 |
|
RU2393163C2 |
| СОЕДИНЕНИЯ, ОБРАЗУЮЩИЕ ПРОЛЕКАРСТВА | 2014 |
|
RU2667942C2 |
| СИММЕТРИЧНЫЕ И НЕСИММЕТРИЧНЫЕ ПРОИЗВОДНЫЕ ДИФЕНИЛМОЧЕВИНЫ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПОДАВЛЕНИЯ РОСТА ОПУХОЛЕВЫХ КЛЕТОК, ОПОСРЕДОВАННОГО КИНАЗОЙ RAF | 1998 |
|
RU2247109C9 |
| ПИРРОЛОПИРИДИНЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2006 |
|
RU2435769C2 |
| ИНДАЗОЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ FGFR, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2015 |
|
RU2719428C2 |
| ИНГИБИТОРЫ МЕТАЛЛОПРОТЕИНАЗ, ИХ ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2002 |
|
RU2288228C2 |
| N-9-ЗАМЕЩЕННЫЕ ПУРИНОВЫЕ СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2607635C2 |
| ИНГИБИТОРЫ АРОМАТАЗЫ | 2010 |
|
RU2572244C2 |
Изобретение относится к новым гетероциклическим азот- и кислородсодержащим соединениям, обладающим инсектицидной активностью. В формулах (А), (В), (С), (D):


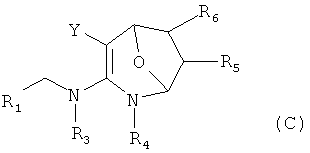

R1 представляет собой 5- или 6-членный гетероцикл, содержащий атом азота, кислорода и/или серы, галогенозамещенный 5- или 6-членный гетероцикл, содержащий атом азота, кислорода и/или серы, замещенный или незамещенный фенил, где заместители представляют собой одну или более чем одну группу, выбранную из группы, состоящей из атомов галогена, С1-4галогеноалкила или С1-4хлоралкоксила; R5, R6, R7, R8 и R9 представляют собой Н, насыщенный или ненасыщенный С1-4алкил, атом галогена, насыщенный или ненасыщенный С1-8алкоксил, насыщенный С1-4галогеноалкоксил, С1-4алкилкарбонил, С1-8алкиловый сложный эфир, С1-4алкилсульфонил, фенил, бензил или трифторметансульфонильную эфирную группу; Y представляет собой нитро, циано, трифторметил, трифторацетил или трифторметилсульфонил. Значения радикалов R, R2-R4 приведены в формуле изобретения. Изобретение также относится к агрохимической композиции, содержащей указанные соединения, к применению агрохимической композиции для борьбы с сельскохозяйственными вредителями и к способу получения указанных соединений. 5 н. и 7 з.п. ф-лы, 7 табл., 36 пр.
1. Соединение формулы (А), (В), (С) или (D), или его агрохимически приемлемые соли,




где R1 представляет собой 5- или 6-членный гетероцикл, содержащий атом азота, кислорода и/или серы, галогенозамещенный 5- или 6-членный гетероцикл, содержащий атом азота, кислорода и/или серы, замещенный или незамещенный фенил, где заместители представляют собой одну или более чем одну группу, выбранную из группы, состоящей из атомов галогена, С1-4галогеноалкила или С1-4хлоралкоксила;
R2 представляет собой Н, C1-8 насыщенный или ненасыщенный алкил, галогенозамещенный C1-8 насыщенный или ненасыщенный алкил, -CH2CH2OCH2CH3, -СН2СН2ОСН3, фенил, незамещенный бензил или бензил, замещенный одной или более чем одной группой, выбранной из группы, состоящей из атома галогена, C1-4галогеноалкила или С1-4хлоралкоксила, С1-4алкилкарбонил или С1-4алкилсульфонил;
R3 и R4 независимо выбраны из Н, C1-6 алкила, аллила, бензила, С1-4алкоксил-С1-4 алкила, С1-4алкоксилкарбонила, незамещенной бензоильной группы или бензоильной группы, замещенной одной или более чем одной группой, выбранной из группы, состоящей из атомов галогена, С1-4алкила, С1-4галогеноалкила, С1-4алкоксила или C1-4алкилкарбонила; либо R3 и R4 вместе образуют -СН2-СН2-, -СН2-СН2-СН2- или -CH2-XR-CH2-, где Х представляет собой гетероатом N, О и S; R представляет собой заместитель на Х и выбран из H, C1-6алкила, аллила, бензила, фенила, С1-4алкоксил-С1-4алкила, С1-4алкоксилкарбонила, незамещенной бензоильной группы или бензоильной группы, замещенной одной или более чем одной группой, выбранной из группы, состоящей из атомов галогена, С1-4галогеноалкила, C1-8 насыщенного или ненасыщенного алкила или алкоксила, либо С1-4алкилкарбонила,
R5, R6, R7, R8 и R9 представляют собой Н, насыщенный или ненасыщенный C1-4алкил, атом галогена, насыщенный или ненасыщенный С1-8алкоксил, насыщенный C1-4галогеноалкоксил, С1-4алкилкарбонил, С1-8алкиловый сложный эфир, C1-4алкилсульфонил, фенил, бензил или трифторметансульфонильную эфирную группу;
Y представляет собой нитро, циано, трифторметил, трифторацетил или трифторметилсульфонил.
2. Соединение или его агрохимически приемлемые соли по п.1, где R1 выбран из пиридила, тиазолила, тетрагидрофурила, оксазолила или их галогенированных групп.
3. Соединение или его агрохимически приемлемые соли по п.1, где R2 представляет собой H, насыщенный или ненасыщенный С1-4алкил, насыщенный или ненасыщенный С1-4галогеноалкил, С1-4алкилкарбонил, незамещенный бензил или бензил, замещенный одной или более чем одной группой, выбранной из группы, состоящей из атома галогена, С1-4галогеноалкила или С1-4хлоралкоксила.
4. Соединение или его агрохимически приемлемые соли по п.1, отличающиеся тем, что R3 и R4 представляют собой Н, C1-6алкильную группу, либо R3 и R4 вместе образуют -СН2-СН2- или -CH2-CH2-CH2-.
5. Соединение или его агрохимически приемлемые соли по п.1, где R5, R6, R7, R8 и R9 представляют собой Н, насыщенный С1-2алкил, атом галогена, насыщенный или ненасыщенный С1-4алкоксил, насыщенный С1-2галогеноалкоксил, С1-2алкилсульфонил или трифторметансульфонильную эфирную группу.
6. Соединение или его агрохимически приемлемые соли по п.1, где Y представляет собой нитрогруппу или цианогруппу.
7. Агрохимическая композиция, имеющая инсектицидную активность, содержащая:
(а) 0,001-99,99 мас.% соединения или его агрохимически приемлемых солей по любому из пп.1-6 или их комбинации; и
(б) агрохимически приемлемый носитель или эксципиент.
8. Применение агрохимической композиции по п.7 для уничтожения или борьбы с сельскохозяйственными вредителями, санитарными вредителями и вредителями, вредными для здоровья животных.
9. Способ получения соединения или его агрохимически приемлемых солей по любому из пп.1-6, включающий приведенные ниже стадии:
в присутствии каталитической кислоты и при 0-60°С взаимодействие соединения формулы (а) с соединением (b) посредством чего получают соединение (А) или (В), где R2 представляет собой Н,


где R1, R3, R4, R5, R6, R7, R8, R9 и Y являются такими, как определено в п.1, и n равно 0 или 1.
10. Способ по п.9, включающий:
в присутствии каталитической кислоты проводят приведенную ниже реакцию при 20-30°С в ацетонитриле в течение 2-24 ч, посредством чего получают соединение (А), где R2 представляет собой Н:
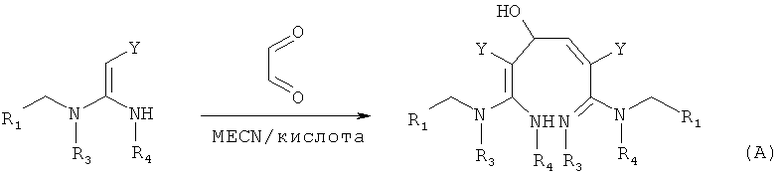 ;
;
в присутствии каталитической кислоты, проводят приведенную ниже реакцию при 20-30°С в ацетонитриле в течение 2-24 ч, посредством чего получают соединение (В):
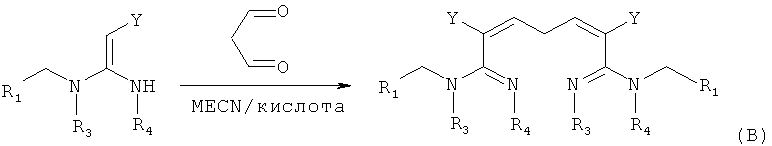 .
.
11. Способ получения соединения или его агрохимически приемлемых солей по любому из пп.1-6, включающий приведенные ниже стадии:
в присутствии каталитической кислоты и при 0-60°С взаимодействие соединения формулы (а) с соединением (с) или (d), посредством чего получают соединение (С) или (D)



где R1, R3, R4, R5, R6, R7, R8, R9 и Y являются такими, как определено в п.1, и n равно 0 или 1.
12. Способ по п.11, включающий:
в присутствии каталитической кислоты проводят приведенную ниже реакцию при 10-50°С в ацетонитриле в течение 2-24 ч, посредством чего получают соединение (С):
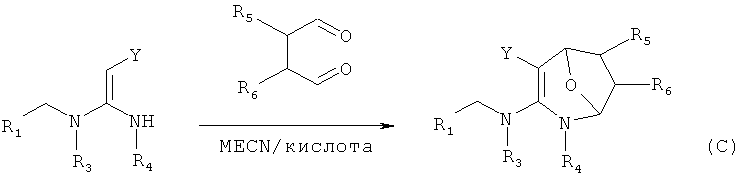 ;
;
в присутствии каталитической кислоты проводят приведенную ниже реакцию при 10-50°С в ацетонитриле в течение 2-24 ч, посредством чего получают соединение (D):
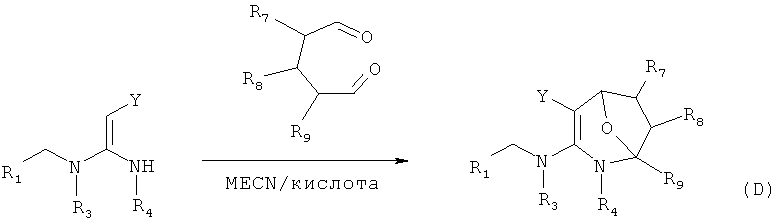 .
.
| WO 2004056178 А2, 08.07.2004 | |||
| WO 2007101369 A1, 13.09.2007 | |||
| Устройство в наливных баржах для выкачивания из них обезвоженного мазута | 1927 |
|
SU10019A1 |
| M | |||
| NOGUCHI ET AL., «Chirality transfer in the ene-reactions of 3-{2-(2S)-[2-(substituted)vinyl]pyrrolidin-l-yl}-2-(substituted)acrolein derivatives» | |||
| Tetrahedron letters, 41, 2000, pp.8489-8493 | |||
| M | |||
| NOGUCHI ET AL., «Thermal ene reactions of | |||
Авторы
Даты
2013-10-10—Публикация
2009-12-18—Подача