Перекрестная ссылка на родственные заявки
По данной заявке испрашивается приоритет на основании предварительных заявок США №60/611061, поданной 17 сентября 2004, 60/711445, поданной 25 августа 2005, и 60/711565, поданной 26 августа 2005, все названы "Фосфоиндолы как ингибиторы HIV".
Область техники, к которой относится изобретение
В данном изобретении представлены соединения - ингибиторы обратной транскриптазы вируса иммунодефицита человека (HIV; ВИЧ) и их фармацевтически приемлемые соли, пролекарства, аналоги и производные. Также изобретение включает в себя способы применения названных соединений для профилактики и лечения ВИЧ-инфекции и AIDS (СПИДа) и фармацевтических композиций, которые содержат названные соединения.
Уровень техники изобретения
Многочисленные соединения были синтезированы против вируса иммунодефицита человека (HIV; ВИЧ), так как, как было установлено в 1983 году, он является этиологической причиной синдрома приобретенного иммунного дефицита (AIDS; СПИД). Главным направлением работы по изучению СПИДа было и продолжает оставаться разработка ингибиторов обратной транскриптазы вируса иммунодефицита человека (HIV-1; ВИЧ-1), фермента, ответственного за обратную транскрипцию ретровирусной РНК до провирусной ДНК (W.C.Greene, New England Journal of Medicine (1991), 324: 308-17; Mitsuya et al., Science (1990), 249: 1533-44; EJ. DeClercq, Retrovirus (1992), 8: 119-34). Ингибиторы включают в себя ненуклеозидные ингибиторы обратной транскриптазы или NNRTI, которые связывают специфический аллостерический участок обратной транскриптазы ВИЧ около полимеразного участка и препятствуют обратной транскрипции посредством или изменения конформации, или подвижности обратной транскриптазы, таким образом, приводя к неконкурентному ингибированию фермента (Kohlstaedt et al., Science (1992), 256:1783-90).
Некоторые классы соединений идентифицировали как NNRTI для ВИЧ. Примеры упомянутых соединений включают в себя:
1) 1-[(2-гидроксиэтокси)метил]-6-(фенилтио)тимины (HEPT) (Tanaka et al., J. Med. Chem. (1991), 34:349-57; Pontikis et al., J. Med. Chem. (1997), 40:1845-54; Danel et al., J. Med. Chem. (1996), 39:2427-31; Baba et al., Antiviral Res. (1992), 17:245-64);
2) бис(гетероарил)пиперазины (BHAP) (Romero et al., J. Med. Chem. (1993), 36:1505-8);
3) дигидроалкоксибензилоксипиримидин (DABO) (Danel et al., Acta Chemica Scandinavica (1997), 51:426-30; Mai et al., J. Med. Chem. (1997), 40:1447-54);
4) 2',5'-бис-О-(третбутилдиметилсилил)-3'-спиро-5''-(4''-амино-1'',2''-оксатиол-2'',2''-диоксид)пиримидины (TSAO) (Balzarini et al., PNAS USA (1992), 89:4392-96);
5) производные фенилэтилтиазолилтиомочевины (PETT) (Bell et al., J. Med. Chem. (1995), 38:4929-36; Cantrell et al., J. Med. Chem. (1996), 39:4261-74);
6) производные тетрагидро-имидазо[4,5,1-jk][1,4]-бензодиазепин-2(1Н)-она и -тиона (TIBO) (Pauwels et al., Nature (1990), 343:470-4);
7) фосфор-замещенные производные имидазола (публикация PCT № WO 03/091264 A2 от Gilead Sciences, Inc.);
8) производные альфа-анилинфенилацетамида (альфа-АРА) (Pauwels et al., PNAS USA (1993), 90:1711-15) и
9) производные индола (патент США № 5527819 от Merck & Co, и дополняющая публикация РСТ № WO 94/19321).
Производные индола, описываемые в патенте США № 5527819 фирмы Merck & Co., как показано, являются ингибиторами обратной транскриптазы ВИЧ. Некоторые из упомянутых соединений имеют величины IC50 для обратной транскриптазы при концентрациях 3-35 нМ. Способ синтеза необязательно замещенных индолов в результате катализируемого паладием аннелирования между кетоном и иоданилином также разработан Merck & Co. (Chen et al., J. Org. Chem. (1997), 62(9):2676-77).
Соединения, обсуждаемые в патенте '819, обычно представляют следующей общей структурной формулой (III):
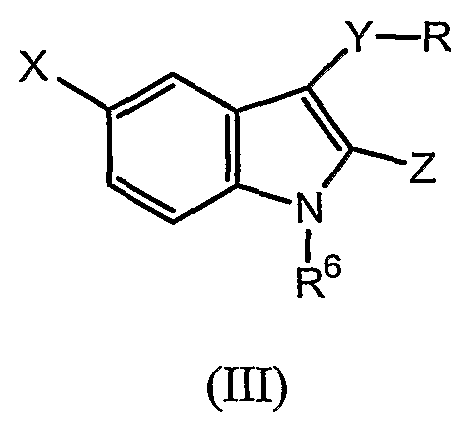
для которой переменные значения X, Y, Z, R и R6 определяют в общих чертах.
В патенте США № 5124327 от Merck & Co. рассматривают класс необязательно замещенных соединений сульфонилфенилиндола. В патенте сообщают, что соединения являются активными как ингибиторы обратной транскриптазы, и их можно применять для лечения ВИЧ-инфекции и СПИДа.
В патенте США № 6710068 от Idenix Pharmaceuticals, Ltd., обсуждают класс фенилиндолов, замещенных, по крайней мере, двумя фрагментами помимо водорода на любом или обоих кольцах. Смотри также публикацию PCT № WO 02/083126.
В публикации PCT WO 2004/014364 от Idenix Pharmaceuticals описывают другой класс фенилиндолов, которые обладают повышенной анти-ВИЧ-активностью. Названные соединения также замещают, по крайней мере, двумя фрагментами кроме водорода на любом кольце или обоих кольцах. Кроме того, в названные соединения вводят ряд различных заместителей с функциональностью карбоксамида по положению 2 на индоле, положение показано в формуле (II) выше как "Z". Типичными положениями присоединения заместителей являются 3'' и 5'' в фенильном кольце и положения 4' и 5',5' и 6', или положения 5' и 7' в бензокольце фрагмента индола.
Bristol Myers Squibb описывают различные необязательно замещенные индолы, азаиндолы, пиперазины и пирролидины для лечения ВИЧ и/или СПИДа в нескольких патентах США и публикациях США и РСТ. Смотри публикации США №№ 2004/0006090, 2004/0063746, 2003/0096825, 2003/0236277 и WO 03/068221.
В WO 01/02388 от SmithKline Beecham S.P.A рассматривают необязательно замещенные фенилиндолы с карбамильным заместителем, которые, как утверждают, имеют применение при лечении ВИЧ-инфекции, СПИДа, остеопороза, раковых заболеваний и болезни Альцгеймера.
Компания Warner-Lambert Company представляет различные индол-тиазепиноны, оксазепиноны, диазепиноны, бензотиофены, бензофураны и индол-2-карбоксамиды для лечения ВИЧ в патентах США 5424329, 5565446, 5703069 и WO 96/29077.
Shinogi & Co. описывает необязательно замещенные производные индола, которые являются ингибиторами вирусной интегразы, применяемые как анти-ВИЧ лекарственные средства, в публикации США № 2002/0019434 и патенте США № 6716605 и 6506787.
В патенте США № 5945440 Kleinschroth et al. рассматривают класс индолкарбазол-амидов для лечения заболеваний, включающих в себя рак, вирусные заболевания (включая ВИЧ), сердечные и сосудистые заболевания, бронхопульмональные заболевания, воспалительные заболевания, дегенеративные заболевания центральной нервной системы и другие болезни.
В патенте США № 4866084 Gunasekera et al. рассматривает некоторые алкалоидные соединения бис-индола, которые имеют противовирусную и противоопухолевую активность, включая HSV (вирус простого герпеса). В патенте США 5935982 Dykstra et al. описывает другой класс бис-индолов, который применяют против ретровирусных инфекций и особенно ВИЧ-инфекции.
В патенте США № 5852011 Matsunaga et al. обсуждает класс производных индола, замещенных гетероарильной группой и амидной группой. Соединения, как отмечают, проявляют противоопухолевую, противовирусную и противомикробную активность.
В патенте США № 5935982 Dykstra et al. рассматривает класс бис-индолов и, в частности, предлагает применять их для лечения ретровирусных инфекций и особенно инфекции ВИЧ.
В патенте США № 5929114 Domagala et al. обсуждает класс соединений арилтио и битиобисариламида, включающих в себя производное индола, которое косвенно проявляет противобактериальную и противовирусную активность.
В патенте США № 5830894 Pevear et al. описывает класс производных триазининдола, которые обладают анти-пествирусной активностью, особенно активностью против BVDV.
Индолы использовали при лечении заболеваний помимо ВИЧ. В патенте США № 5981525 Farina et al. описывает комплексный ряд индолов для применения при лечении остеопороза на основании их способности ингибировать остеокластную Н+-АТФ-азу и, таким образом, уменьшать костную резорбцию. В патенте США № 6025390 Farina et al. также рассматривает другую группу производных индола, названных гетероароматические производные пентадиеноевой кислоты, также для лечения остеопороза. В патенте США № 5489685 Houpis et al. описывает серию соединений, которые представляют собой сложные эфиры фуро(2,3-b)пиридин-карбоновой кислоты, якобы приемлемые для лечения ВИЧ.
Известно, что со временем противовирусные средства, которые активны в отношении ВИЧ, вызывают мутации в вирусе, которые снижают эффективность лекарственного средства. Так, явно возникла проблема, доказанная фирмой Merck с помощью индолов в патенте США № 5527819 (Williams et al., J. Med. Chem., 1993, 36(9), 1291-94). Устойчивость к лекарственному средству чаще всего возникает в результате мутации гена, который кодирует фермент, участвующий в вирусной репликации, и обычно в случае ВИЧ, обратную транскриптазу, протеазу или интегразу ДНК. Обнаружено, что эффективность лекарственного средства против ВИЧ-инфекции можно пролонгировать, увеличивать или восстанавливать введением соединения в комбинации или при чередовании со вторым и, необязательно, третьим противовирусным соединением, которое индуцирует мутацию, отличающуюся от мутации, вызванной основным лекарственным средством. Альтернативно, фармакокинетику, биораспределение или другие параметры лекарственного средства можно изменять с помощью такой комбинированной или чередующейся терапии. Вообще, комбинированная терапия является общепринятой терапией скорее, чем переменная терапия, так как комбинированная терапия индуцирует многочисленные одновременные воздействия на вирус. Однако нельзя предсказать, какие мутации будут индуцированы в геноме ВИЧ-1 данным лекарственным средством, будут ли мутации постоянными или временными, или как инфицированная клетка с мутантной последовательностью ВИЧ-1 будет отвечать на терапию другими средствами в комбинации или при чередовании. Приведенные факторы осложняются тем фактом, что имеется небольшое количество данных по кинетике устойчивости к лекарственному средству в долгосрочных клеточных культурах, обработанных современными противоретровирусными средствами.
Поэтому, существует потребность в обеспечении новыми соединениями и способами для лечения ВИЧ-инфекции.
Таким образом, цель данного изобретения заключается в обеспечении новыми соединениями, композициями, способами и применениями для лечения пациентов, инфицированных ВИЧ.
Другое направление данного изобретения заключается в обеспечении новыми композициями и способами для лечения пациентов, инфицированных ВИЧ, которые проявляют активность против форм вируса, устойчивых к лекарственному средству.
Краткое изложение изобретения
Соединения 3-фосфоиндола проявляют противовирусную активность против ВИЧ, в частности, против штаммов ВИЧ, в которых развивается перекрестная резистентность к другим анти-ВИЧ лекарственным средствам. Разработаны соединения, композиции и способы лечения ВИЧ-инфекции, которые включают в себя соединения 3-фосфоиндола. 3-Фосфоиндол может находиться в виде большого разнообразия составляющих фрагментов, без ограничений, включающих в себя фосфаты, фосфонаты, фосфортиолат, включая тиофосфаты, тиофосфонаты, фосфат, и фосфорамидат, включая иминофосфаты и иминофосфонаты.
В одном осуществлении, соединения, которые проявляют анти-ВИЧ-активность, имеют формулу (А), представленную ниже. Названные соединения включают в себя связанный с фосфором заместитель в положении-3 и особенно заместители в положении-2 на индоле, и монозамещение в положении R5' или дизамещения в положениях R4' и R5', R5' и R6', или R5' и R7' в бензокольце.
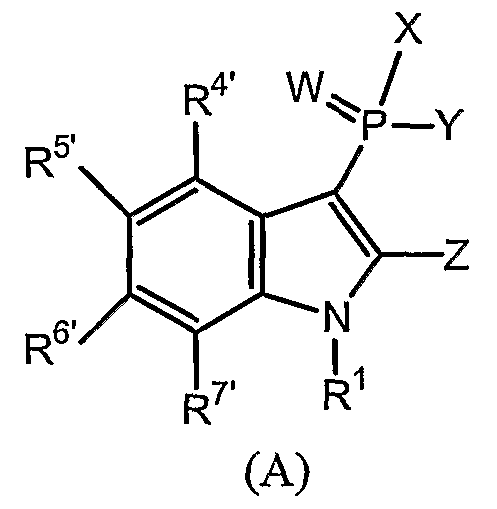
В одном особом осуществлении заместитель "Х" представляет собой кольцо фенила, которое не замещают или замещают одним или более галогенами или группами низшего алкила, такими как метил или этил. Определенные заместители в положении 2 фрагмента индола, например водород, гидрокси, галоген, алкил, арил, гетероарил, и особенно заместители, содержащие карбоксамид или фрагмент карбоксамида, показаны в формуле (А) как "Z". Заместители для бензокольца фрагмента индола, без ограничений, включают в себя хлор, фтор, бром, иод, CF3, CN, NO2 и метокси.
Активное соединение может быть солью или пролекарством, которое при введении доставляет непосредственно или косвенно родительское соединение или которое само проявляет желаемую активность. В другом осуществлении соединение формулы А содержит заряженный гетероатом, а в особом осуществлении, соединение содержит группу N-оксида. Модификации, влияющие на биологическую активность соединения данного изобретения, также включены в данное изобретение, так как представляют собой любые изменения, которые продуцируют увеличенную активность по сравнению с активностью исходного соединения.
Краткое описание чертежей
Фигура 1 представляет собой изображение трех (3) общих структур данного изобретения, представленных как формула (А), формула (В) и формула (С).
Фигура 2 является изображением фосфорилированных соединений (I)-(X) общих формул (А) и (В).
Фигура 3 является изображением 9- и 10-членных бициклических фосфорилированных соединений (XI)-(XX) общей формулы (С).
Подробное описание изобретения
Описаны состав вещества, способ применения и фармацевтическая композиция для лечения ретровирусных инфекций у млекопитающих и, в частности, ВИЧ-инфекции у человека. Данное изобретение включает в себя следующие критерии:
- 3-фосфоиндолы и их фармацевтически приемлемые соли и пролекарства, которые описывают в изобретении, необязательно, по существу не содержат других химических элементов;
- 3-фосфоиндолы формул А-С и их фармацевтически приемлемые соли и пролекарства, которые описывают в изобретении, необязательно, по существу не содержат других химических элементов;
- 3-фосфоиндолы и их фармацевтически приемлемые соли и пролекарства, которые описывают в изобретении, являются эффективными против ВИЧ у хозяина;
- 3-фосфоиндолы и их фармацевтически приемлемые соли и пролекарства, которые описывают в изобретении, являются эффективными против устойчивых к лекарственному средству штаммов ВИЧ у хозяина и, в некоторых осуществлениях, когда устойчивые к лекарственному средству штаммы ВИЧ обусловлены мутацией обратной транскриптазы, такой как лизин 103 → аспарагин и/или тирозин 181 → цистеин;
- 3-фосфоиндолы и их фармацевтически приемлемые соли и пролекарства, которые описывают в изобретении для применения при лечении или профилактики ВИЧ-инфекции у хозяина или в производстве лекарственного средства для лечения или профилактики ВИЧ-инфекции у хозяина, особенно у индивидуумов, у которых установлена ВИЧ-инфекция или которые относятся к группе риска относительно такой инфекции;
- 3-фосфоиндолы и их фармацевтически приемлемые соли и пролекарства, которые описывают в изобретении для применения при лечении или профилактики ВИЧ-инфекции, или в производстве лекарственного средства для лечения или профилактики ВИЧ-инфекции, которая резистентна к одному или более ингибиторам обратной транскриптазы, у хозяина;
- 3-фосфоиндолы и их фармацевтически приемлемые соли и пролекарства, которые описывают в изобретении для применения при лечении или профилактики ВИЧ-инфекции в виде восстановительной терапии у хозяина или в производстве медикамента для лечения или профилактики ВИЧ-инфекции в виде восстановительной терапии у хозяина, особенно у индивидуумов, у которых выявлена ВИЧ-инфекция или которые относятся к группе риска в отношении такой инфекции;
- 3-фосфоиндолы и их фармацевтически приемлемые соли и пролекарства, которые описывают в изобретении для применения при лечении или профилактики или в производстве лекарственного средства для лечения или профилактики ВИЧ-инфекции, которая резистентна к одному или более ингибиторам обратной транскриптазы вследствие мутации обратной транскриптазы, такой как мутация лизина 103 → аспарагин и/или тирозина 181 → цистеин, у хозяина, особенно у индивидуумов, у которых выявлена ВИЧ-инфекция или которые относятся к группе риска относительно такой инфекции;
- способы получения 3-фосфоиндолов, необязательно по существу отделенных от других химических элементов;
- фармацевтические композиции, содержащие эффективное анти-ВИЧ терапевтическое количество 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства вместе с фармацевтически приемлемым носителем или разбавителем;
- фармацевтические композиции, содержащие эффективное анти-ВИЧ терапевтическое количество 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства в комбинации с одним или более другими анти-ВИЧ-средствами, необязательно с фармацевтически приемлемым носителем или разбавителем;
- фармацевтические композиции для лечения или профилактики ВИЧ-инфекции, которая резистентна к одному или более ингибиторам обратной транскриптазы у хозяина, содержащие эффективное анти-ВИЧ терапевтическое количество 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства, необязательно в комбинации, по крайней мере, с одним другим анти-ВИЧ-средством, необязательно с фармацевтически приемлемым носителем или разбавителем;
- фармацевтические композиции для лечения или профилактики ВИЧ-инфекции у хозяина в виде восстановительной терапии, содержащие эффективное анти-ВИЧ терапевтическое количество 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства, необязательно в комбинации, по крайней мере, с одним другим анти-ВИЧ-средством, и необязательно с фармацевтически приемлемым носителем или разбавителем;
- фармацевтические композиции для лечения или профилактики ВИЧ-инфекции, которая резистентна к одному или более ингибиторам обратной транскриптазы вследствие мутации обратной транскриптазы, такой как лизин 103 → аспарагин и/или тирозин 181 → цистеин, у хозяина, содержащие эффективное анти-ВИЧ терапевтическое количество 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства, необязательно в комбинации, по крайней мере, с одним другим анти-ВИЧ-средством, и необязательно с фармацевтически приемлемым носителем или разбавителем;
- способы лечения или профилактики ВИЧ-инфекции у хозяина, при этом ВИЧ может быть устойчивым к одному или более ингибиторам обратной транскриптазы, включающие в себя введение названному хозяину эффективного анти-ВИЧ терапевтического количества 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства, необязательно в комбинации или при чередовании, по крайней мере, с одним другим анти-ВИЧ-средством, и необязательно с фармацевтически приемлемым носителем или разбавителем;
- способы лечения или профилактики ВИЧ-инфекции у хозяина в виде восстановительной терапии, включающие в себя введение названному хозяину эффективного анти-ВИЧ терапевтического количества 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства, необязательно в комбинации или при чередовании, по крайней мере, с одним другим анти-ВИЧ-средством, и необязательно с фармацевтически приемлемым носителем или разбавителем;
- способы лечения или профилактики ВИЧ-инфекции, которая резистентна к одному или более ингибиторам обратной транскриптазы вследствие мутации обратной транскриптазы, такой как лизин 103 → аспарагин и/или тирозин 181 → цистеин, у хозяина, включающие в себя введение названному хозяину эффективного анти-ВИЧ терапевтического количества 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства, необязательно в комбинации или при чередовании, по крайней мере, с одним другим анти-ВИЧ-средством и необязательно с фармацевтически приемлемым носителем или разбавителем;
- применение 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства, необязательно в комбинации или при чередовании, по крайней мере, с одним другим анти-ВИЧ-средством и необязательно с фармацевтически приемлемым носителем или разбавителем, для лечения или профилактики ВИЧ-инфекции у хозяина;
- применение 3-фосфоиндола или его фармацевтически приемлемой соли или пролекарства, необязательно в комбинации или при чередовании, по крайней мере, с одним другим анти-ВИЧ-средством и необязательно с фармацевтически приемлемым носителем или разбавителем, для лечения или профилактики ВИЧ-инфекции или при производстве лекарственного средства для лечения или профилактики ВИЧ-инфекции, которая резистентна к одному или более ингибиторам обратной транскриптазы, что может быть обусловлено мутацией обратной транскриптазы, такой как лизин 103 → аспарагин и/или тирозин 181 → цистеин, у хозяина. Описанное применение может быть в виде восстановительной терапии; и
- любой или все из вышеприведенных критериев, при которых хозяин является человеком.
I. Активные соединения данного изобретения
В главном осуществлении изобретение обеспечивает 3-фосфоиндол или его фармацевтически приемлемую соль, пролекарство, N-оксид, четвертичный амин, стереохимический изомер или таутомер. 3-Фосфоиндол может быть в виде фосфата, фосфоната, тиофосфата, тиофосфоната, иминофосфата или иминофосфоната.
В первом осуществлении данного изобретения соединение обычно изображают следующей химической формулой (А):
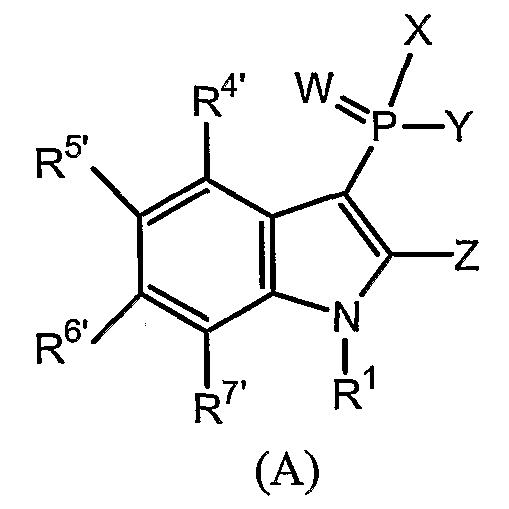
или его фармацевтически приемлемая соль, пролекарство, N-оксид, четвертичный амин, стереохимический изомер или таутомер, в которых:
каждый X и Y независимо представляет собой
а) Н;
b) галоген (F, Cl, Br или I), обычно F;
с) R3;
d) CF3;
e) С1-6 алкил;
f) С2-6 алкенил;
g) С2-6 алкинил;
h) алкилгетероцикл;
i) 3-14-членный карбоцикл, арил, гетероцикл, любой из которых может содержать моноциклическую, бициклическую, трициклическую или спироструктуру;
j) OH;
k) OR2;
l) О-алкил;
m) О-алкенил;
n) О-алкинил;
o) О-алкиларил;
p) О-арил;
q) О-гетероцикл;
r) О-аралкил;
s) О-карбоцикл;
t) SH;
u) SR2;
v) S-алкил;
w) S-алкенил;
x) S-алкинил;
y) S-алкиларил;
z) S-арил;
aa) S-гетероцикл;
bb) S-аралкил;
cc) S-карбоцикл;
dd) NH2;
ee) NHR2;
ff) NR2R2;
gg) NH-алкил;
hh) N-диалкил;
ii) NH-арил;
jj) N-алкарил;
kk) N-аралкил;
ll) NH-гетероцикл;
mm) N-алкил-гетероцикл;
nn) N-алкенил-гетероцикл;
oo) N-алкинил-гетероцикл; или
альтернативно, X и Y могут присутствовать вместе для образования необязательно замещенного бициклического или трициклического фосфорилированного гетероцикла, в котором каждое кольцо содержит 3-7 элементов;
Z представляет собой:
a) H;
b) CN;
c) NO2;
d) С1-6 алкил;
e) С2-6 алкенил;
f) С2-6 алкинил;
g) алкарил;
h) аралкил;
i) гетероцикл;
j) алкил-гетероцикл;
k) арил;
l) алкокси;
m) OR2;
n) SR2;
o) S(O)nR2;
p) S(O)n-NR2R3;
q) N(R2)(R3);
r) карбоксамидо;
s) амидо;
t) ацил;
u) C(=W)-R3;
v) C(=W)NH-C(R3)(R3)-C(=W)-N(R2)(R2);
w) C(=W)NH-P(=W)(R3)-A-R3;
x) C(=W)NH-A-S(O)n-NR2;
y) C(=W)NH-CR3R3-S(O)n-NR2R2;
z) C(=W)-NH-A-C(=W)-N(R2)(R2);
aa) C(=W)-N(R2)(R2);
bb) C(=W)-NH-A-R3;
cc) C(=W)-NH-NH-R3;
dd) C(=W)-NH-C(R3)(R3)-C(=W)NH-C(R3)(R3)C(=W)-N(R2)(R2);
ee) C(=W)-NH-R2;
ff) C(=W)-NH-A-C(=W)-NH-A-C(=W)-NH2;
gg) C(R2)(R3)(R3);
hh) C(R2)(R3)-NH-R2;
ii) A-S(O)n-R3;
jj) C(=W)-A-C(=W)-A-C(=W)R3;
kk) A-R3;
ll) C(=W)-(O)R2;
mm) C(=W)-A-C(=W)-NH2;
nn) аминокислотный остаток;
oo) C(=W)-N(R2)-A-(аминокислотный остаток);
pp) C(=W)-N(R2)-A-(аминокислотный остаток)-C(=W)-R3;
qq) C(=W)-аминокислотный остаток;
rr) C(=W)-N(R2)-A-(аминокислотный остаток)-A-C(=W)-R3;
ss) C(=W)-OR2;
tt) C(=W)-S(R2);
uu) C(=W)-NH-NH-R2;
vv) C(=W)-NH-N(R2)-A-C(=W)R3;
ww) C(=W)-N(R2)-C(=W)-R3;
xx) C(=W)-A-NH-C(=W)R3;
yy) C(=W)-A-NH-C(=W)OR2;
zz) C(=W)-A-R3;
aaa) C(=W)-NH-NH-CH2-C(=W)R3;
bbb) P(=W)(R3)(R3); или
ccc) A-P(=W)(R3)(R3);
ddd) C(=W)-NH-C1-10алкил-гетероарил;
eee) C(=W)-NH-C1-4алкил-гетероарил;
fff) C(=W)-NH-CH2-гетероарил;
ggg) 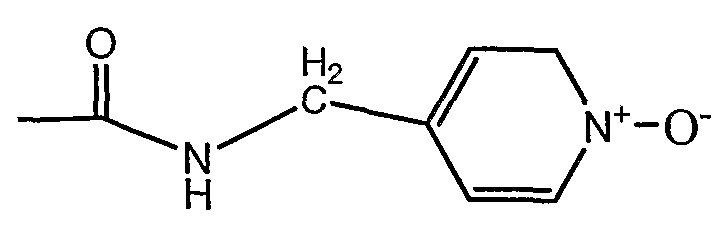
где в осуществлениях (ddd), (eee) и (fff) гетероарил, необязательно, может включать в себя заряженный гетероатом и, в частности, может включать в себя N-оксид;
где каждый X, Y и Z независимо может быть незамещенным или замещенным одним или более С1-6 алкилом; алкокси; ОН; оксо; галогеном (F, Cl, Br или I); NR2R2; необязательно замещенным арилом; необязательно замещенным гетероциклом; O-C(=W)-алкилом; C(=W)-OR2; CN; NO2; NH-C(=W)-алкилом; NH-S(O)n-алкилом; NH-S(O)n-NR2R2; или С3-6циклоалкилом;
каждый W независимо представляет собой:
a) O;
b) S;
c) NH;
d) N-N(R2)(R2);
e) N(R2);
f) N-OH;
g) N-O-алкил; или
h) N-O-R2;
R1 представляет собой:
a) H;
b) -R2;
c) C(=W)-R3;
d) C(=W)-O(R2);
e) C(=W)-S(R2);
f) C(=W)-NH-R2;
g) C(=W)-N(R2)(R2);
h) C(=W)-NH-A-(аминокислотный остаток);
i) A-(аминокислотный остаток)-R3;
j) S(O)n-R3; или
k) S(O)2-N(R2)(R2);
любой из которых, необязательно, может быть замещен одним или более С1-6 алкилом; ОН; алкокси; арилом; галогеном; CN; NO2; или N(R2)(R2);
каждый R2 независимо представляет собой:
a) H;
b) CF3;
c) CN;
d) необязательно замещенный алкил с разветвленной или неразветвленной цепью, такой как С1-6 алкил;
e) необязательно замещенный алкенил с разветвленной или неразветвленно цепью, такой как С2-6 алкенил;
f) необязательно замещенный алкинил с разветвленной или неразветвленной цепью, такой как С2-6 алкинил;
g) 3-14-членный карбоцикл;
h) необязательно замещенный арил;
i) необязательно замещенный аралкил;
j) необязательно замещенный алкиларил;
k) необязательно замещенный гетероцикл;
l) необязательно замещенный алкилгетероцикл;
m) необязательно замещенный гетероцикл-алкил;
n) А-гетероцикл;
o) ацил;
p) алкокси;
q) CH2-S(O)nR3;
r) C(алкил)2-S(O)nалкил;
s) CH(алкил)-S(O)nалкил;
t) CH2NH2;
u) CH2NH(алкил);
v) CH2N(алкил)2;
w) CH(алкил)-NH2;
x) CH(алкил)-NH(алкил);
y) CH(алкил)-N(алкил)2;
z) C(алкил)2-NH2;
aa) C(алкил)2-NH(алкил);
bb) C(алкил)2-N(алкил)2;
cc) CH2-C(=W)H;
dd) CH2-C(=W)алкил;
ee) A-алкил;
ff) C(алкил)2-C(=W)алкил;
gg) CH2-C(=W)H;
hh) CH2-C(=W)алкенил;
ii) CH(алкенил)-C(=W)H;
jj) A-S(O)алкил;
kk) CH(NH)-S(O)nалкил; или
ll) A-N(NH)алкил;
mm) C(R3)(R3)-S(O)nNH2;
nn) C(R3)(R3)-S(O)nCF3;
oo) C(R3)(R3)-NH2;
каждый R3 независимо представляет собой:
a) H;
b) OH;
c) галоген (F, Cl, Br или I);
d) CF3;
e) CN;
f) необязательно замещенный, разветвленный или неразветвленный алкил, такой как С1-6 алкил;
g) необязательно замещенный, разветвленный или неразветвленный алкенил, такой как С2-6 алкенил;
h) необязательно замещенный, разветвленный или неразветвленный алкинил, такой как С2-6 алкинил;
i) 3-14-членный карбоцикл;
j) необязательно замещенный арил;
k) необязательно замещенный аралкил;
l) необязательно замещенный алкиларил;
m) необязательно замещенный гетероцикл;
n) необязательно замещенный алкилгетероцикл;
o) необязательно замещенный гетероцикл-алкил;
p) А-гетероцикл;
q) ацил;
r) карбоксамидо;
s) карбамоил;
t) алкокси;
u) OH;
v) OR2;
w) О-алкил;
x) О-алкенил;
y) О-алкинил;
z) О-алкарил;
aa) О-аралкил;
bb) О-карбоцикл;
cc) О-гетероцикл;
dd) О-арил;
ee) SH;
ff) SR2;
gg) S-алкил;
hh) S-алкенил;
ii) S-алкинил;
jj) S-алкарил;
kk) S-аралкил;
ll) S-карбоцикл;
mm) S-гетероцикл;
nn) S-арил;
oo) S(O)n-R2;
pp) амино;
qq) NH2;
rr) NHR2;
ss) N(R2)(R2);
tt) NH-S(O)n-R2;
uu) NHC(=W)-арил;
vv) NHC(=W)-алкил;
ww) NH-C(=W)-гетероцикл;
xx) CH2-S(O)nR2;
yy) C(=W)R2;
zz) C(=W)-N(R2)-R2;
aaa) C(алкил)2-S(O)nR2;
bbb) CH(алкил)-S(O)nR2;
ccc) C(алкил)2-NH2;
ddd) CH(алкил)-N(алкил)R2;
eee) C(R2)(R2)-NR2R2;
fff) CH2N(алкил)R2;
ggg) CH(алкил)-NHR2;
hhh) C(алкил)2-NHR2;
iii) C(алкил)2-N(алкил)R2;
jjj) CH2-C(=W)H;
kkk) CH2-C(=W)алкил;
lll) CR2R2-C(=W)R2;
mmm) A-R2;
nnn) C(R2)2-C(=W)R2;
ooo) CH2-C(=W)H;
ppp) CH2-C(=W)алкенил;
qqq) CH(алкенил)-C(=W)H;
rrr) A-S(O)R2;
sss) CH(NH)-S(O)nR2; или
ttt) A-N(NH)R2;
uuu) C(R2)(R2)-S(O)nNH2;
vvv) C(R2)(R2)-S(O)nCF3;
www) C(R2)(R2)-NH2;
где необязательное замещение содержит один или более из:
а) замещенного или незамещенного гетероцикла
b) C(=W)O-арила;
c) C(=W)O-алкила;
d) C(=W)NH2;
e) C(=W)NH-алкила;
f) C(=W)NH-арила;
g) C(=W)N-ди-алкила;
h) C(=W)N(алкил)-арила;
i) α-аминокислоты;
j) сложного α-аминоэфира
k) α-амино-карбоксамида;
l) β-аминокислоты;
m) сложного β-аминоэфира;
n) β-амино-карбоксамида;
при этом, если необязательное замещение включает в себя замещенный гетероцикл, тогда гетероциклическое замещение выбирают из группы, состоящей из:
a) C(=W)O-арила;
b) C(=W)O-алкила;
c) C(=W)NH2;
d) C(=W)NH-арила;
e) C(=W)NH-алкила;
f) C(=W)N-ди-алкила;
g) C(=W)N(алкил)-арила;
h) α-аминокислоты;
i) сложного α-аминоэфира;
j) α-амино-карбоксамида;
k) β-аминокислоты;
l) сложного β-аминоэфира; и
m) β-амино-карбоксамида;
n) галогена; или
o) циано;
отдельно или в любой комбинации;
n независимо равно 0, 1 или 2;
каждый А независимо представляет собой дизамещенное промежуточное звено, выбранное из группы, состоящей из:
а) С1-6 алкилена, с разветвленной или неразветвленной цепью и необязательно содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
b) С2-12 алкенилена, с разветвленной или неразветвленной цепью и необязательно содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
с) С2-12 алкинилена, с разветвленной или неразветвленной цепью и необязательно содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
d) необязательно замещенного арилена;
e) О-алкилена, разветвленного или неразветвленного и, необязательно, содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
f) аралкилена, разветвленного или неразветвленного и, необязательно, содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
g) необязательно замещенного циклоалкила; и
h) необязательно замещенного гетероцикла;
в которой "А" можно присоединять с помощью любой требуемой связи, такой как простая эфирная, тиоэфирная связь, амино-связь, карбоксамидная, сложная эфирная или углерод-углерод связь, или любой их комбинацией;
каждый R4', R5', R6' и R7' независимо представляет собой:
a) H;
b) галоген (F, Cl, Br, I);
c) NO2;
d) CN;
e) CF3;
f) OH;
g) OR2;
h) SH;
i) SR2;
j) NR2R2;
k) NHS(O)nR2;
l) NHCO-C1-3 алкил;
m) S(O)nR2;
n) арил;
o) гетероцикл;
p) С1-6 алкил;
q) С2-6 алкенил;
r) С2-6 алкинил;
s) C(=W)-S(O)nR2;
t) C(=W)-S(O)n-NR2R2;
u) C(=W)-арил;
v) C(=W)-алкил;
w) C(=W)-гетероцикл; или
x) C(=W)-NR2R2;
каждый из которых, необязательно, можно замещать одним или более из:
a) OR2;
b) S(O)nR2;
c) C(=W)-S(O)nR2;
d) C(=W)-S(O)nNR2R2;
e) C(=W)-арила;
f) C(=W)-алкила;
g) C(=W)-гетероцикла;
h) C(=W)NR2R2;
i) NO2;
j) CN;
k) CF3;
l) галогена (F, Cl, Br, I);
m) NHS(O)nR2;
n) NHCO-C1-3 алкила;
o) арила;
p) гетероцикла;
q) С1-6 алкила;
r) С2-6 алкенила;
s) С2-6 алкинила; или
t) NR2R2.
В одном осуществлении формулы (А), Х представляет собой необязательно замещенный фенил; Y представляет собой любое из его определений; R1, R4', R6' и R7', все означают водород; R5' означает галоген, а Z представляет собой карбоксамидный фрагмент.
В альтернативном осуществлении R1 представляет собой ацил, алкил, арил, алкарил или аралкил.
В еще одном альтернативном осуществлении R4' представляет собой фтор, нитро или циано, W означает кислород, а Y означает О-алкил.
Во втором осуществлении формулы (А, Х представляет собой необязательно замещенный фенил; Y представляет собой любое из его определений; R1, R4', R6' и R7', все означают водород; R5' означает хлор, и Z представляет собой фрагмент карбоксамида или карбоксамидо-гетероциклила.
В еще одном осуществлении формулы (А) Х представляет собой толил, тиазолил или пиридил; Y представляет собой Н, ОН или О-алкил; R1, R4', R6' и R7', все означают водород; R5' означает галоген, а Z представляет собой группу карбоксамида, ацила, алкил-сульфонильную группу или производное карбоновой кислоты.
В альтернативном предшествующему осуществлению X, Y, R1, R4', R6', R7' и R5', все являются такими как описано выше, а Z представляет собой группу карбоксамидо-алкилен-гетероцикла, обычно карбоксамидо-алкилен-пиридила; тиоамидо-пиридила, в котором пиридил не замещают или замещают OH, OMe или низшим алкилом; группу имино-нитрила или алкилсульфонил-арила.
В другом осуществлении Z представляет собой карбоксамидо-алкилен-гетероцикл, в котором гетероцикл включает в себя, по крайней мере, одну N-оксидную группу.
Во втором осуществлении в изобретении представляют фенилиндол для применения при лечении ВИЧ-инфекции, изображаемый следующей общей формулой (В):
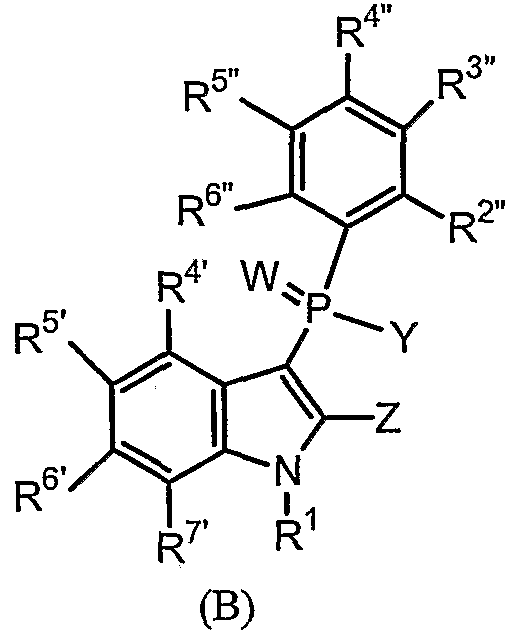
или его фармацевтически приемлемую соль, пролекарство, N-оксид, четвертичный амин, стереохимический изомер или таутомер, в которых:
каждый W, Y, Z, R1 R2, R3, A, n, R4', R5', R6' и R7' являются такими, как определяют выше для формулы (А); и
каждый R2'', R3'', R4'', R5'' и R6'' независимо представляют собой:
a) H;
b) галоген;
c) NO2;
d) CN;
e) OR2;
f) SR2;
g) NH2;
h) NR2R3;
i) N(R2)-C(=W)-C1-4 алкил;
j) N(R2)-SO2-C1-4 алкил;
k) С1-6 алкил;
l) С2-6 алкенил;
m) С2-6 алкинил;
n) арил;
o) CF3;
p) CR2R2-S(O)n-R3;
q) CR2R2NR2R3;
r) C-OH;
s) CR2R2-C(=W)R2;
t) ацил;
u) C(=W)R2;
v) C(=W)OR2;
w) C(=W)SR2;
x) C(=W)-NR2R3;
y) C(=W)NH(CH2)p-(аминокислотный остаток);
z) амино; или
aa) А-(аминокислотный остаток);
где любой из приведенных выше, необязательно, может быть замещен; или
альтернативно, R2'' или R6'' можно присоединять к Y с образованием необязательно замещенного бициклического или трициклического фосфорилированного гетероцикла, в котором каждое кольцо содержит 3-14 элементов.
Следующее представляет собой не ограничивающие изобретение примеры осуществлений формулы (В):
a) Y означает алкил; W означает O, S(O)n, или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген, а Z представляет собой карбоксамид;
b) Y означает алкил; W означает O, S(O)n, или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает амино-алкил, тиоамино-алкил или аминокарбонил-алкил, а Z означает карбоксамид;
c) Y означает -OH или -SR2; W означает O, S(O)n, или N-NH2; R1, R4', R6', R7', R2'', R4'' и R6'', все представляют собой водород; R5' означает гелоген; R3'' и R5'' представляют собой метил, а Z означает карбоксамид;
d) Y означает -OH; W означает O, S(O)n или NH; R1, R6', R7', R2'', R4'' и R6'', все представляют собой водород; R4' и R5' означают галоген; R3'' и R5 представляют собой метил, а Z означает карбоксамид;
e) Y означает -OH; W означает O, S(O)n или N-NR2R2; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z означает карбоксамид;
f) Y означает алкенил; W означает O, S(O)n или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z означает карбоксамид или карбоксамид-гетероцикл;
g) Y означает алкинил или -NR2R3; W означает O, S(O)n или N-O-алкил; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z означает карбоксамид;
h) Y означает алкенилен; W означает O, S(O)n или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z означает карбоксамид;
i) Y означает этил; W означает O, S(O)n или N-OH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает хлор; а Z означает карбоксамид;
j) Y означает -O-метил; W означает O, S(O)n или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z означает карбоксамид;
k) Y означает -O-этил; W означает O, S(O)n или N-NH2; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z означает карбоксамид-гетероцикл;
l) Y означает -O-этил; W означает O, S(O)n или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает хлор; а Z означает карбоксамид;
m) Y означает -O-H; W означает O, S(O)n или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z представляет собой группу карбоксамид-алкила, которая является незамещенной или замещенной одним или более -NO2, -NH-C(=O)-алкилом или -NH-S(O)n-алкилом;
n) Y означает -O-H; W означает O, S(O)n или N-NH2; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z представляет собой группу карбоксамидо-алкилен-гетероциклила, в которой названный гетероцикл представляет собой имидазол, тиазол, пиридил или фуран и в которой гетероцикл не замещают или замещают одним или более галогеном, оксо, -OH, -NO2, -MeOH, -NH-C(=O)-алкилом или -NH-S(O)n-алкилом;
o) Y означает -O-H; W означает O, S(O)n или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z представляет собой карбоксамид-циклопропил или карбоксамид-циклобутил;
p) Y означает -O-метил; W означает O, S(O)n или NH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z представляет собой карбоксамид-этил, карбоксамид-этанол или карбоксамид-этил-метокси;
q) Y означает -OH или NR2R3; W означает O, S(O)n или N-O-алкил; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z представляет собой группу карбоксамид-алкил-фенила, в которой фенил еще замещают одной или более группами галогена, оксо, -OH, -OCH3, -NO2, -MeOH или -NH-C(=O)-алкила;
r) Y означает -OH или SR2; W означает O, S(O)n или N-NR2R2; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z представляет собой фрагмент изопропанол-карбоксамида; и
s) Y означает -OH; W означает O, S(O)n или N-OH; R1, R4', R6', R7', R2'', R3'', R4'', R5'' и R6'', все представляют собой водород; R5' означает галоген; а Z представляет собой группу тиоацетамида.
В третьем осуществлении в данном изобретении представляют необязательно замещенный 9-11-членный бициклический 3-фосфоиндол для применения при лечении ВИЧ-инфекции, изображаемый следующей общей формулой (С):
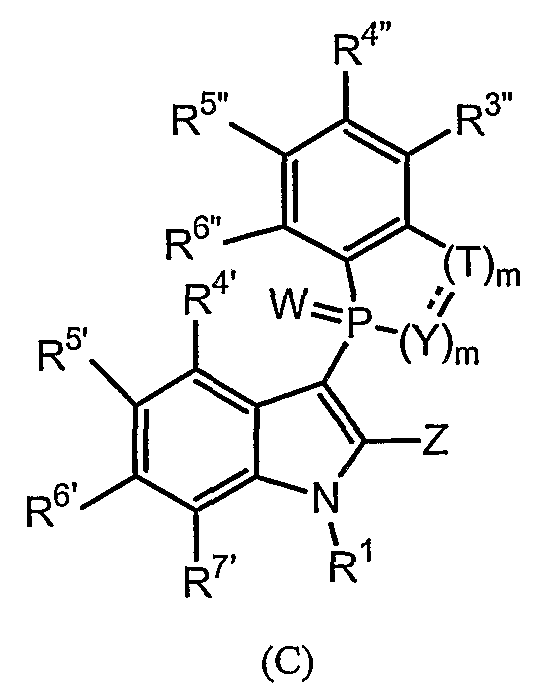
или его фармацевтически приемлемую соль, пролекарство, N-оксид, четвертичный амин, стереохимический изомер или таутомер, в которых:
каждый W, Z, R1, R2, R3, A, n, R4', R5', R6' и R7' являются такими, как описывают выше для формулы (А);
каждый R3'', R4'', R5'' и R6'' являются такими, как описывают выше для формулы (В);
 указывает на наличие ординарной или двойной связи, где:
указывает на наличие ординарной или двойной связи, где:
если  указывает на наличие двойной связи, каждый Y и T независимо означает:
указывает на наличие двойной связи, каждый Y и T независимо означает:
a) CR3;
b) N; или
c) S(=W);
так что, по крайней мере, один из Y и T означает CR3; и
если  указывает на наличие ординарной связи, тогда каждый Y и T независимо означает:
указывает на наличие ординарной связи, тогда каждый Y и T независимо означает:
a) CHR3;
b) C(R3)(R3);
c) O;
d) S; или
e) NR2;
так что, по крайней мере, один из Y и T означает C(R3)(R3); и
m равно 1 или 2 при условии, что m может быть только 2 для T или Y = CR2.
Следующее представляет собой не ограничивающие изобретение примеры осуществлений формулы (С):
a) W означает O, Y означает CR2, T представляет собой (CH2)2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой карбоксамид;
b) W означает S, Y означает O, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой карбоксамидо-гетероцикл, в котором названный гетероцикл представляет собой необязательно замещенный фуран, имидазол, тиазол или пиридил;
c) W означает S, Y означает NR2, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой карбоксамид;
d) W означает O, Y означает SR2, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой алкил-карбоксамид;
e) W означает S, Y означает SR2, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой карбоксамид;
f) W означает O, Y означает CR2, T представляет собой C-C(=W)R3, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой метоксиметил-карбоксамид;
g) W означает S, Y означает O, T представляет собой C-C(=W)R3, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой карбоксамид-циклобутил;
h) W означает O, Y означает SR2, T представляет собой C-C(=W)R3, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает хлор, а Z представляет собой алкил-карбоксамид, в котором алкил необязательно замещен одним или более галогеном, оксо, -OH, -NO2, -MeOH, -NH-C(=O)алкилом или -NH-S(O)n-алкилом;
i) W означает S, Y означает NR2, T представляет собой C-C(=W)R3, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает хлор, а Z представляет собой карбоксамид;
j) W означает S, Y означает N, T представляет собой C-C(=W)R3, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает фтор, а Z представляет собой карбоксамид;
k) W означает NH, Y означает CR2, T представляет собой NR2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает амино-алкил, а Z представляет собой карбоксамид;
l) W означает NR2, Y означает O, T представляет собой (CH2)2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает хлор, а Z представляет собой карбоксамид;
m) W означает N-OH, Y означает O, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает тиоамино-алкил, а Z представляет собой карбоксамид;
n) W означает S, Y означает SR2, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой группу карбоксамид-гетероциклила, в которой гетероцикл представляет собой необязательно замещенный пиридин, тиазол, имидазол или фуран;
o) W означает N-O-алкил, Y означает NR2, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой группу карбоксамид-алкила, в которой алкил необязательно замещен одним или более -NO2, -NH2, -NH-C(=W)алкилом или -NH-S(O)n-алкилом;
p) W означает NH, Y означает SR2, T представляет собой (CH2)2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой карбоксамид-алкил-фенил, где фенил необязательно замещен одним или более группами галогена, оксо, OH, NO2, MeOH, -NH-C(=O)алкила или -NH-S(O)n-алкила;
q) W означает NR2, Y означает (CH2)2, T представляет собой NR2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой группу карбоксамид-циклопропила;
r) W означает N-OH, Y означает CH, T представляет собой O, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой группу карбоксамид-циклопропила;
s) W означает N-O-алкил, Y означает O, T представляет собой (CH2)2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает хлор, а Z представляет собой группу карбоксамид-метоксиэтила;
t) W означает O, Y означает N, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой группу карбоксамид-этанола;
u) W означает N-NR2R2, Y означает NR2, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает галоген, а Z представляет собой карбоксамид; и
v) W означает O, Y означает CR2, T представляет собой CH2, R1, R4', R6', R7', R3'', R4'', R5'' и R6'', все означают Н; R5' означает аминокарбонил-алкил, а Z представляет собой карбоксамид.
В одной серии осуществлений формулы А, В или С, Z означает C(=W)-R3; C(=W)-NH-A-C(=W)-N(R2)(R2); C(=W)-NH-A-R3; C(=W)-NH-R2 или C(=W)-A-R3.
В одном осуществлении формулы А, В или С, соединение содержит заряженный гетероатом. В частности, заряженный азот, такой как N-оксид, является частью соединения. Заряженный гетероатом может присутствовать на гетероароматическом кольце, которое присоединяют к индолу, например через C(O)NH-алкил или специально через C(O)NH-CH2.
В особом осуществлении формулы А, В или С, Z означает C(=O)-NH-R2, где R2 представляет собой необязательно замещенный алкилгетероцикл, в котором гетероцикл имеет формулу 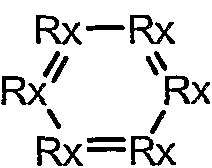 , в которой каждый Rx независимо означает CH или N+-O-. В отдельном осуществлении, один из Rx представляет собой N+-O-. Группа алкила может представлять собой С1-10 алкил или С1-4 алкил, или может представлять собой, в частности, метилен или этилен. В специальном осуществлении, R2 имеет формулу
, в которой каждый Rx независимо означает CH или N+-O-. В отдельном осуществлении, один из Rx представляет собой N+-O-. Группа алкила может представлять собой С1-10 алкил или С1-4 алкил, или может представлять собой, в частности, метилен или этилен. В специальном осуществлении, R2 имеет формулу 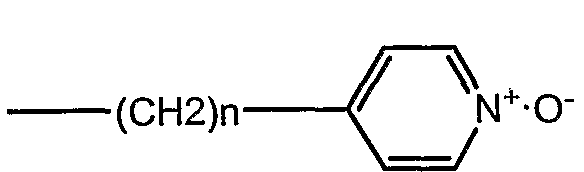 , в которой n равно 0, 1 или 2.
, в которой n равно 0, 1 или 2.
В определенных осуществлениях формулы А, В или С, соединение представляет собой:
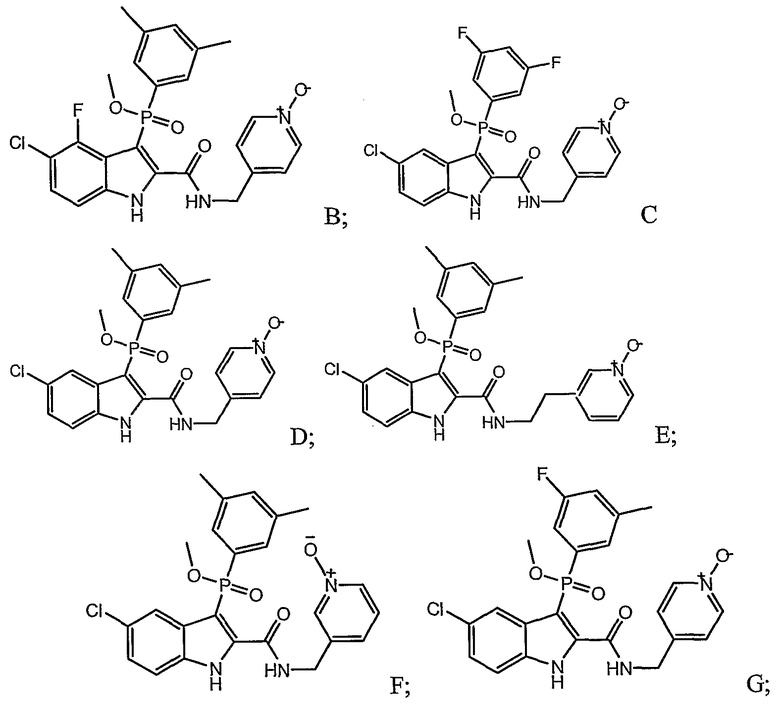
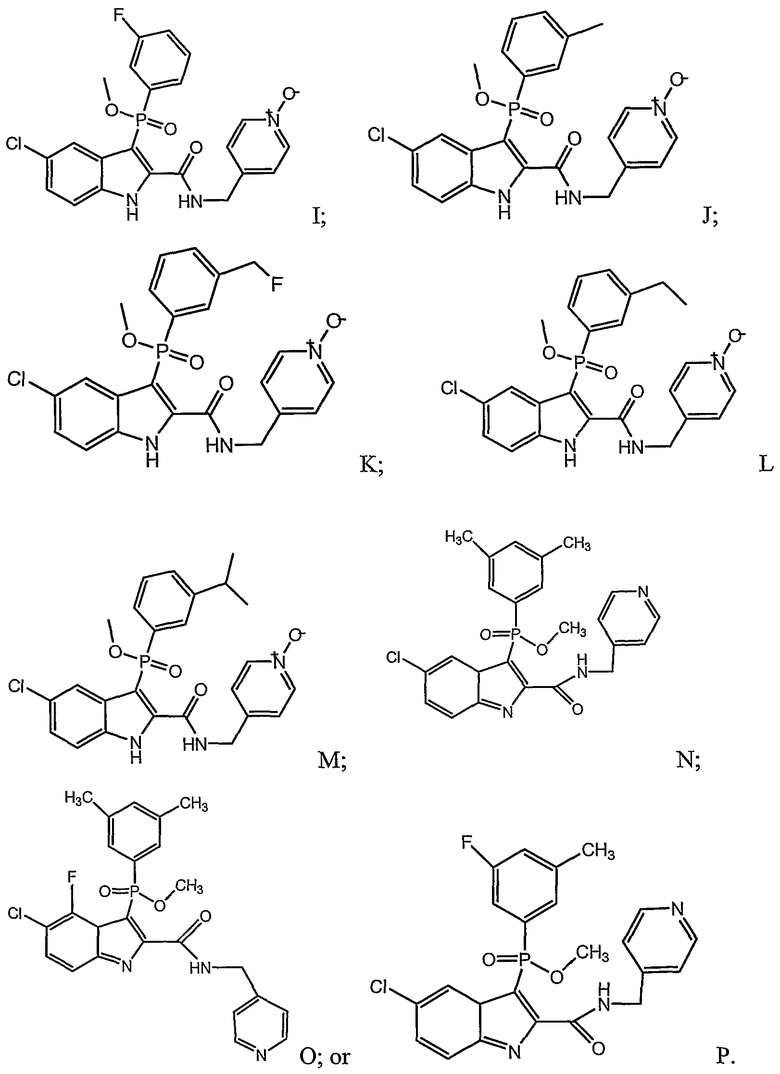
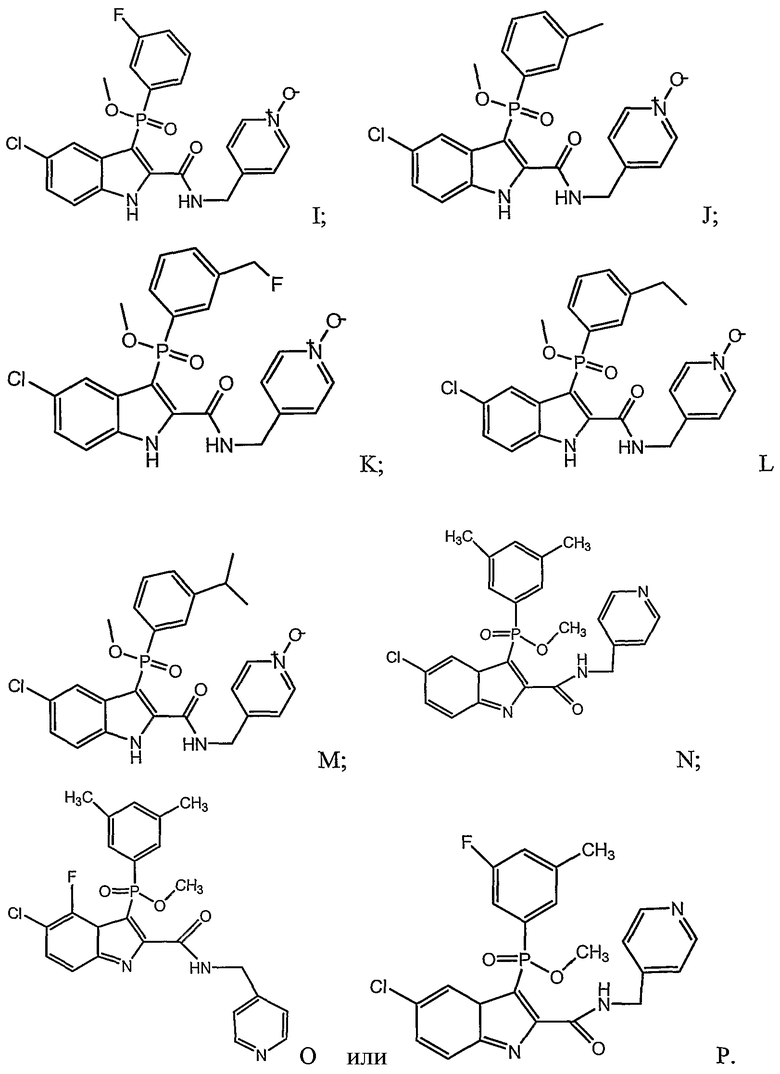
Дополнительными примерами осуществления соединения формулы А, В или С в виде N-оксида являются:
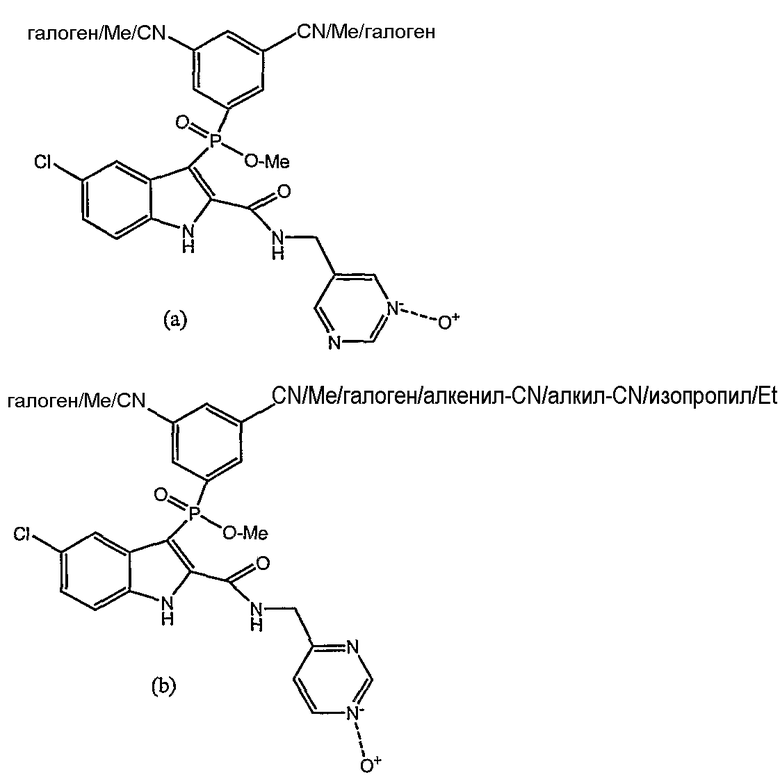 . Любой заместитель на кольце фенила можно замещать CN, Me, галогеном, алкилом, алкенилом, алкинилом, алкил-CN или алкенил-CN, как наиболее синтезируемых и тестируемых N-оксидов в серии в настоящее время.
. Любой заместитель на кольце фенила можно замещать CN, Me, галогеном, алкилом, алкенилом, алкинилом, алкил-CN или алкенил-CN, как наиболее синтезируемых и тестируемых N-оксидов в серии в настоящее время.
II. Особые субварианты данного изобретения
В первом осуществлении изобретения соединения обычно представляют формулой (А):
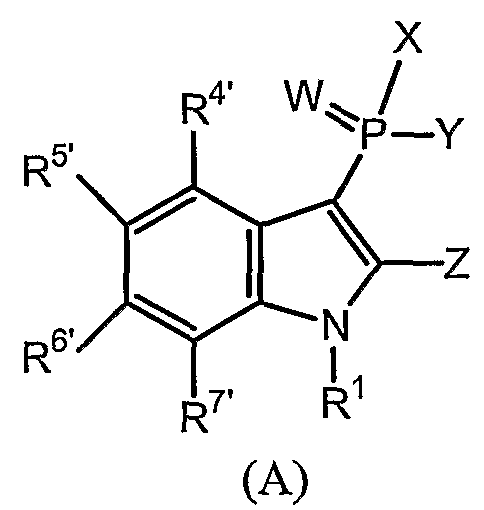
или их фармацевтически приемлемая соль, пролекарство, N-оксид, четвертичный амин, стереохимический изомер или таутомер, в которых:
X и Y, каждый независимо представляет собой:
a) 3-14-членный карбоцикл, арил, гетероцикл, любой из которых может содержать моноциклическую, бициклическую, трициклическую или спироструктуру, или может быть замещен;
b) H;
c) OH;
d) Cl, Br, I, F;
e) CF3;
f) С1-6 алкил;
g) С2-6 алкенил;
h) С2-6 алкинил;
i) алкилгетероцикл;
j) NH2;
k) NH-алкил;
l) N-диалкил;
m) NH-арил;
n) N-алкарил;
o) N-аралкил;
p) NH-гетероцикл;
q) N-алкил-гетероцикл;
r) N-алкенил-гетероцикл;
s) N-алкинил-гетероцикл;
t) O-алкил;
u) О-алкенил;
v) О-алкинил;
w) О-алкиларил;
x) О-арил;
y) О-гетероцикл;
z) О-аралкил;
aa) О-карбоцикл;
bb) SR2; или
cc) NR2R3;
альтернативно, X и Y можно соединять с образованием необязательно замещенного бициклического или трициклического фосфорилированного гетероцикла, в котором каждое кольцо содержит 3-7 элементов;
Z представляет собой:
a) H;
b) алкокси;
c) NO2;
d) N(R2)(R3);
e) OR2;
f) карбоксамидо;
g) амидо;
h) ацил;
i) S(O)nR2;
j) S(O)nNR2R3;
k) С1-6 алкил;
l) С2-6 алкенил;
m) С2-6 алкинил;
n) алкарил;
o) аралкил;
p) гетероцикл;
q) алкил-гетероцикл;
r) арил;
s) CN;
t) C(=W)-R2;
u) C(=W)NH-C(R2)(R2)-C(=W)-N(R2)(R2);
v) C(=W)NH-P(=W)(R2)-A-R2;
w) C(=W)NH-A-S(O)n-NR2;
x) C(=W)NH-CR2R3-S(O)n-NR2R3;
y) C(=W)-NH-A-C(=W)-N(R2)(R3);
z) C(=W)-N(R2)(R3);
aa) C(=W)-NH-A-R2;
bb) C(=W)-NH-NH-R2;
cc) C(=W)-NH-C(R2)(R2)-C(=W)NH-C(R2)(R3)C(=W)-N(R2)(R3);
dd) C(=W)-NH-R2;
ee) C(=W)-NH-A-C(=W)-NH-A-C(=W)-NH2;
ff) C(R2)(R2)(R3);
gg) C(R2)(R2)-NH-R2;
hh) A-S(O)n-R2;
ii) C(=W)-A-C(=W)-A-C(=W)R3;
jj) A-R2;
kk) C(=W)-(O)R2;
ll) C(=W)-A-C(=W)-NH2;
mm) аминокислотный остаток;
nn) C(=W)-N(R2)-A-(аминокислотный остаток);
oo) C(=W)-N(R2)-A-(аминокислотный остаток)-C(=W)-R2;
pp) C(=W)-аминокислотный остаток;
qq) C(=W)-N(R2)-A-(аминокислотный остаток)-A-C(=W)-R2;
rr) C(=W)-OR3;
ss) C(=W)-S(R2);
tt) C(=W)-NH-NH-R2;
uu) C(=W)-NH-N(R2)-A-C(=W)R2;
vv) C(=W)-N(R2)-C(=W)-R3;
ww) C(=W)-A-NH-C(=W)R2;
xx) C(=W)-A-NH-C(=W)OR3;
yy) C(=W)-A-R3;
zz) C(=W)-NH-NH-CH2-C(=W)R2;
aaa) P(=W)(R2)(R2); или
bbb) A-P(=W)(R2)(R2);
где каждый вышеприведенный X, Y и Z независимо можно не замещать или замещать одним или более из:
a) H;
b) С1-6 алкила;
c) алкокси;
d) OH;
e) оксо;
f) галогена;
g) NR2R2;
h) необязательно замещенного арила;
i) необязательно замещенного гетероциклила;
j) O-C(=W)-алкила;
k) C(=W)-OR2;
l) CN;
m) NO2;
n) NH-C(=W)алкила;
o) NH-S(O)n-алкила;
p) NH-S(O)n-NR2R2; или
q) С3-6 циклоалкила;
W представляет собой:
a)O;
b) S;
c) NH;
d) N-N(R2)(R2);
e) N(R2);
f) N-OH; или
g) N-O-алкила;
R1 представляет собой:
a) H;
b) R2;
c)C(=W)-R2;
d) C(=W)-O(R2);
e) C(=W)-S(R2);
f) C(=W)-NH-R2;
g) C(=W)-N(R2)(R2);
h) C(=W)-NH-A-(аминокислотный остаток);
i) A-(аминокислотный остаток)-R2;
j) S(O)nR3; или
k) S(O)2-N(R2)(R2);
любой из которых, необязательно, можно замещать одним или более:
a) С1-6 алкилом;
b) OH;
c) алкокси;
d) арилом;
e) галогеном;
f) CN;
g) NO2; или
h) N(R2)(R2);
R2 представляет собой:
a) H;
b) OH;
c) галоген;
d) необязательно замещенный алкил с разветвленной или неразветвленной цепью;
e) необязательно замещенный алкенил с разветвленной или неразветвленной цепью;
f) необязательно замещенный алкинил с разветвленной или неразветвленной цепью;
g) 3-14-членный карбоцикл;
h) алкилгетероцикл;
i) ацил;
j) карбоксамидо;
k) карбамоил;
l) алкокси;
m) необязательно замещенный арил;
n) необязательно замещенный аралкил;
o) необязательно замещенный алкиларил;
p) О-алкил;
q) О-алкенил;
r) О-алкинил;
s) О-алкарил;
t) О-аралкил;
u) О-карбоцикл;
v) О-гетероцикл;
w) О-арил;
x) CF3;
y) CN;
z) S(O)n-R3;
aa) N(R3)(R3);
bb) NH-S(O)n-R3;
cc) NHC(=W)-арил;
dd) NHC-(=W)-алкил;
ee) NHC(=W)-гетероцикл;
ff) CH2-S(O)nR3;
gg) C(=W)R3;
hh) C(=W)NR3R3;
ii) C(алкил)2-S(O)nR3;
jj) CH(алкил)-S(O)nR3;
kk) C(алкил)2-NH2;
ll) CH(алкил)-N(алкил)R3;
mm) CR3R3-NR3R3;
nn) CH2N(алкил)R3;
oo) CH(алкил)-NHR3;
pp) C(алкил)2-NHR3;
qq) C(алкил)2-N(алкил)R3;
rr) CH2-C(=W)H;
ss) CH2-C(=W)алкил;
tt) CR3R3-C(=W)R3;
uu) A-R3;
vv) C(R3)2-C(=W)R3;
ww) CH2-C(=W)H;
xx) CH2-C(=W)алкенил;
yy) CH(алкенил)-C(=W)H;
zz) A-S(O)R3;
aaa) CH(NH)-S(O)nR3; или
bbb) A-N(NH)R3;
где названное необязательное замещение включает один или более из:
a) замещенного или незамещенного гетероцикла;
b) C(=W)O-арила;
c) C(=W)O-алкила;
d) C(=W)NH2;
e) C(=W)NH-алкила;
f) C(=W)NH-арила;
g) C(=W)N-ди-алкила;
h) C(=W)N-(алкил)-арила;
i) α-аминокислоты;
j) сложного α-аминоэфира;
k) α-амино-карбоксамида;
l) β-аминокислоты;
m) сложного β-аминоэфира; или
n) β-амино-карбоксамида;
R3 представляет собой:
a) H;
b) OH;
c) С1-6 алкил;
d) С2-6 алкенил;
e) С2-6 алкинил;
f) алкокси;
g) CF3;
h) CN;
i) амино;
j) NR2R2;
k) О-алкил;
l) О-алкенил;
m) О-алкинил;
n) C(R2)(R2)-S(O)nNH2;
o) C(R2)(R2)-S(O)nCF3;
p) C(R2)(R2)-NH2;
q) А-гетероцикл;
r) C(R2)(R2)-NR2R2;
s) C(R2)(R2)-C(=W)R2;
t) арил;
u) карбоцикл;
v) гетероцикл;
w) циклоалкил;
x) алкарил;
y) алкилгетероцикл;
z) аралкил; или
aa) гетероцикл-алкил;
любой из которых может быть незамещенным или замещенным одним или более из следующих, взятых в любой комбинации:
a) галогена;
b) OH;
c) OR2;
d) SR2;
e) COOH;
f) сложного эфира карбоновой кислоты;
g) C(=W)R2;
h) C(=W)OR2;
i) C(=W)OR3;
j) C(=W)SR2;
k) A-C(=W)NH2;
l) C(=W)NR2R3;
m) NR2R2;
n) NR2R3;
o) NR2-S(O)nR3;
p) NR2-C(=W)-C1-6 алкила;
q) S(O)nR3;
r) С1-6-алкокси;
s) простого С1-6 тиоэфира;
t) аминокислотного остатка;
u) NH-A-(аминокислотный остаток);
v) C(=W)NH-A-(аминокислотный остаток); и
где, если названное необязательное замещение включает в себя замещенный гетероцикл, тогда замещение выбирают из группы, состоящей из:
a) C(=W)O-арила;
b) C(=W)O-алкила;
c) C(=W)NH2;
d) C(=W)NH-арила;
e) C(=W)NH-алкила;
f) C(=W)N-ди-алкила;
g) C(=W)N(алкил)-арила;
h) α-аминокислоты;
i) сложного α-аминоэфира;
j) α-амино-карбоксамида;
k) β-аминокислоты;
l) сложного β-аминоэфира; или
m) β-амино-карбоксамида;
n) галогена; или
o) циано,
взятых отдельно или в любой комбинации;
n независимо равно 0, 1 или 2;
каждый А независимо представляет собой дизамещенный промежуточный мостик, выбранный из группы, состоящей из:
a) С1-6 алкилена, с разветвленной или неразветвленной цепью и, необязательно, содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
b) С2-12 алкенилена, с разветвленной или неразветвленной цепью и, необязательно, содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
c) С2-12 алкинилена, с разветвленной или неразветвленной цепью и, необязательно, содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
d) необязательно замещенного арилена;
e) О-алкилена, с разветвленной или неразветвленной цепью и, необязательно, содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
f) аралкилена, с разветвленной или неразветвленной цепью и, необязательно, содержащего один или более гетероатомов, арил, циклоалкил или гетероциклил в цепи или присоединенные к ней;
g) необязательно замещенного циклоалкила; и
h) необязательно замещенного гетероцикла;
в которых "А" можно присоединять любой приемлемой связью, например, такой как простая эфирная, тиоэфирная, амино, карбоксамидная, сложная эфирная связь или связь углерод-углерод, или любой их комбинацией;
каждый R4', R5', R6' и R7' независимо представляет собой:
a) H;
b) галоген;
c) NO2;
d) CN;
e) CF3;
f) OR2;
g) NR2R2;
h) NHS(O)nR2;
i) NHCO-C1-3 алкил;
j) S(O)nR2;
k) арил;
l) гетероцикл;
m) С1-6 алкил;
n) С2-6 алкенил;
o) С2-6 алкинил;
p) C(=W)-S(O)nR2;
q) C(=W)-S(O)n-NR2R2;
r) C(=W)-арил;
s) C(=W)-алкил;
t) C(=W)-гетероцикл; или
u) C(=W)-NR2R2;
каждый из которых, необязательно, можно замещать одним или более из:
a) OR2;
b) S(O)nR2;
c) C(=W)-S(O)nR2;
d) C(=W)-S(O)n-NR2R2;
e) C(=W)-арила;
f) C(=W)-алкила;
g) C(=W)-гетероцикла;
h) C(=W)NR2R2;
i) H;
j) NO2;
k) CN;
l) CF3;
m) галогена;
n) NHS(O)nR2;
o) NHCO-C1-3 алкила;
p) арила;
q) гетероцикла;
r) С1-6 алкила;
s) С2-6 алкенила;
t) С2-6 алкинила; или
u) NR2R2.
В одном осуществлении формулы (А) Х представляет собой необязательно замещенный фенил; Y означает любое из его определений; R1, R4', R6' и R7', все представляют собой водород; R5' означает галоген, а Z представляет собой фрагмент карбоксамида.
В альтернативном осуществлении R1 означает ацил, алкил, арил, алкарил или аралкил.
В еще одном альтернативном осуществлении R4' означает фтор, нитро или циано, W означает кислород, а Y представляет собой О-алкил.
Во втором осуществлении формулы (А) Х представляет собой необязательно замещенный фенил; Y означает любое из его определений; R1, R4', R6' и R7', все представляют собой водород; R5' означает хлор, а Z представляет собой фрагмент карбоксамида или карбоксамидо-гетероциклила.
В еще одном осуществлении формулы (А) Х представляет собой толил, тиазолил или пиридил; Y означает H, OH или О-алкил; R1, R4', R6' и R7', все представляют собой водород; R5' означает галоген, а Z представляет собой группу карбоксамида, ацила, алкил-сульфонила или производное карбоновой кислоты.
В качестве альтернативы предшествующему осуществлению X, Y, R1, R4', R6', R7' и R5', все являются такими, как определяют выше, а Z представляет собой группу карбоксамидо-алкилен-гетероциклила, в котором гетероциклил обычно означает имидазол, фуран, пиридин, пиримидин или тиазол, которые, необязательно, могут быть замещенными; тиоамидо-пиридила, в котором пиридил не замещают или замещают OH, OMe или низшим алкилом; группу имино-нитрила или алкилсульфонил-арила.
В первой серии субвариантов данного изобретения приводят осуществления, в которых формула (А) является такой, как представляют выше, а W, X и Y определяют как:
a) W означает O, X означает алкил, а Y представляет собой -О алкил;
b) W означает O, X означает -О-арил, а Y представляет собой алкил;
c) W означает O, X означает -О-арил, а Y представляет собой -NR2R3;
d) W означает O, X означает -О-алкил, а Y представляет собой алкил;
e) W означает O, X означает -О-алкил, а Y представляет собой галоген;
f) W означает O, X означает -О-гетероциклил, а Y представляет собой алкил;
g) W означает O, X означает арил, а Y представляет собой -О-алкил;
h) W означает O, X означает гетероциклил, а Y представляет собой -О-арил;
i) W означает O, X означает алкил, а Y представляет собой -О-гетероциклил;
j) W означает -NR2R2, X означает гетероциклил, а Y представляет собой -О-арил;
k) W означает -NR2R2, X означает алкил, а Y представляет собой галоген;
l) W означает S, X означает алкил, а Y представляет собой -О-алкил;
m) W означает S, X означает алкил, а Y представляет собой -NR2R3;
n) W означает S, X означает -О-арил, а Y представляет собой алкил;
o) W означает S, X означает -О-арил, а Y представляет собой С-галоген;
p) W означает S, X означает -О-алкил, а Y представляет собой алкил;
q) W означает S, X означает -О-гетероциклил, а Y представляет собой алкил;
r) W означает S, X означает арил, а Y представляет собой -О-алкил;
s) W означает S, X означает гетероциклил, а Y представляет собой -О-арил;
t) W означает S, X означает алкил, а Y представляет собой -О-гетероциклил;
u) W означает S, X означает арил, а Y представляет собой -О-арил;
v) W означает -NR2, X означает -О-алкил, а Y представляет собой -NR2R3;
w) W означает O, X означает -О-арил, а Y представляет собой -О-арил;
x) W означает O, X означает алкил, а Y представляет собой алкил; и
y) W означает -NR2, X означает -О-алкил, а Y представляет собой алкил.
Во второй серии субвариантов данного изобретения приводят осуществления, в которых формула (А) является такой, как представляют, R1 означает H, алкил, ацил, арил, аралкил или алкарил, а Z определяют как:
a) -C(=W)NR2R3, R2 означает H, а R3 означает NR2R2;
b) -C(=W)NR2R3, R2 означает H, а R3 означает NR2R2, или R2 означает С1-5 алкил, необязательно замещенный OH, а R3 означает -NH2;
c) -C(=W)NR2R3, R2 означает H, а R3 означает (CH2)mC(=W)NR2R2;
d) -C(=W)NR2R3, R2 означает H, а R3 означает алкил, замещенный необязательно замещенным арилом или гетероциклом;
e) -C(=W)R3, R3 означает остаток аминокислоты или -NH(CH2)p-(аминокислотный остаток);
f) -C(=W)NHNHC2H5OH;
g) -C(=W)NHCH2C(=W)NH2;
h) -C(=W)NHCH2CONHNH2;
i) -C(=W)NHCH2CH2-(2-NO2, 5-метилимидазол);
j) -C(=W)NHCH2NHCH(CH3)C(=W)OH;
k) -C(=W)NHCH=CHC(=W)NH2;
l) -C(=W)NR2R5NR2R3, R5 означает (=O), R2 и R3 являются такими, как определяют выше;
m) -C(=W)NR2NR2-C(=W)R3, R2 означает H или алкил, а R3 означает арил;
n) -C(=W)N(-NR2R3)-N(-NR2R3)R3, R2 означает H, а R3 означает R2 или алкокси;
o) -C(=W)NHR2C(=W)-Q, Q означает гетероциклил, а R2 является таким, как описывают выше;
p) -C(=W)NR2R3, R2 является таким, как описывают выше, а R3 означает -OH;
q) -COR2R3, R2 означает амино, а R3 означает гетероцикл;
r) -C(=W)NHNHC(=W)R2, а R2 означает NH2;
s) -C(=W)-R2-CH-A-C(=W)NH2, а R2 означает NH;
t) -C(=W)-R2-CH-A-C(=W)H, а R2 означает NH;
u) -C(=W)-R2-CH-A-C(=W)OH, а R2 означает NH;
v) -C(=W)-R2-CH-A-R3, R2 означает NH, а R3 означает CH3;
w) -C(=W)NHR2C(=W)NH2, а R2 необязательно представляет собой замещенный алкил с разветвленной цепью;
x) -C(=W)R2R3, R2 означает NH или алкил, а R3 означает NH2;
y) -C(=W)R2-C(=W)OR3, а R2 и R3 являются такими, как определяют выше;
z) -C(=W)R2-NH-C(=W)C1-4 алкокси, а R2 является таким, как определяют выше;
aa) -C(=W)R2C(=W)C1-4 алкокси, а R2 является таким, как определяют выше;
bb) -C(=W)R2, а R2 означает NH2;
cc) -C(=W)R2-NH-C(=W)OR3, а R2 и R3 являются такими, как определяют выше;
dd) -C(=W)R2-C(=W)R2, а R2 является таким, как определяют выше;
ee) -C(=W)NHR2, в котором R2 необязательно представляет собой замещенный арил, циклоалкил или кольцо гетероциклила;
ff) -C(=W)R2-W-R3, где R2 и R3 являются такими, как определяют выше;
gg) -C(=W)-NH-CH(R2)-C(=W)-NH2, а R2 является таким, как определяют выше;
hh) -C(=W)-NH-NH2;
ii) -C(=W)-NH-NH(R2), а R2 является таким, как определяют выше;
jj) -C(=W)-NH-CH(C[=W]NH2)(CH2-C[=W]-O-арил);
kk) -C(=W)-NH-CH(-[CH2]4-NH-C[=W]-t-BuO)(-C[=W]-NH2);
ll) -C(=W)-NH-CH(-CH2-CH2C[=W]-t-BuO)(-C[=W]-NH2);
mm) -C(=W)-NH-CH(R3)(-C[=W]-NH2), и R3 является таким, как определяют выше;
nn) -C(=W)-NH-CH(-CH2-R3)(-C[=W]-NH2), а R3 является таким, как определяют выше;
oo) -C(=W)-NH-CH(-CH2OH)(-C[=W]-NH2);
pp) -C(=W)-NH-CH(C[=W]-NH2)(C[=W]-NH2);
qq) -C(=W)-NHR2-C[=W]NH2, а R2 является таким, как определяют выше;
rr) -C(=W)-NH-CH(-[CH2]4-NH-C[=W]-O-CH2-R3)(-C[=W]-NH2), а R3 является таким, как определяют выше;
ss) -C(=W)-NH-CH(-CH2-C[=W]-NH2)(-C[=W]-NH2);
tt) -C(=W)-NH-CH(-CH2-R3)(-C[=W]-NH2), где R3 является таким, как определяют выше;
uu) -C(=W)-NH-CH(-[CH2]4-NH2)(-C[=W]-NH2);
vv) -C(=W)-NH-CH(-CH[R2][OH])(-C[=W]-NH2), а R2 является таким, как определяют выше;
ww) -C(=W)-NH-CH(-R2)(-C[=W]-NH2), а R2 является таким, как определяют выше;
xx) -C(=W)-NH-CH(-R2-C[=W]-NH2)(-C[=W]-NH2), а R2 является таким, как определяют выше;
yy) -C(=W)-NH-CH(-R2SCH3)(-C[=W]-NH2), а R2 является таким, как определяют выше;
zz) -C(=W)-NH-CH(-C[=N]-NH2)(-C[=W]-NH2);
aaa) -C(=W)-NH-CH(-R3)(-C[=W]-NH2), а R3 является таким, как определяют выше;
bbb) -C(=W)-NH-CH(-CH2-R3)(-C[=W]-NH2), а R3 является таким, как определяют выше;
ccc) -C(=W)-NH-CH(-R2)(-C[=W]-NH2), а R2 является таким, как определяют выше;
ddd) -C(=W)-NH-R2-C[=W]R3, и R2 означает алкилен, а R3 представляет собой арил или гетероарил;
eee) -C(=W)-NH-R2-R3-C[=W]-NH2, где R2 означает алкилен, а R3 представляет собой арил или гетероарил;
fff) -C(=W)-NH-NH-R2-R3-C(=W)NH2, где R2 означает алкилен, а R3 представляет собой арил или гетероарил;
ggg) -C(=W)-NH-NH-CH(R3)-C(=W)R2, а R2 означает NH2, и R3 представляет собой необязательно замещенный арил или гетероарил;
hhh) -C(=W)NHR2(-R3)-C(=W)NH2, где R2 означает алкилен, а R3 представляет собой необязательно замещенный алкил, арил или гетероарил;
iii) -C(=W)NHR2(-R3)-C(=W)NH-R2-C(=W)OH, где R2 означает изоалкилен, а R3 представляет собой необязательно замещенный алкил, арил или гетероарил;
jjj) -C(=W)NHR2(-R3)-C(=W)NH-R2NH2, где R2 означает алкилен, а R3 представляет собой необязательно замещенный алкил, арил или гетероарил;
kkk) -C(=W)NHR2(-R3)-C(=W)NH-R3, где R2 означает алкилен, а R3 представляет собой необязательно замещенный алкил, арил или гетероарил;
lll) -C(=W)-R2-(CH2)p-A-C(=W)-NH2, где R2 означает -NH, p равно 0-10, A представляет собой двухвалентный линкер или необязательно замещенный арил или гетероарил, а W означает O или S;
mmm) -C(=W)NH-R3, где R3 представляет собой необязательно замещенный гетероцикл;
nnn) -C(=W)-NH-R2-R5-R3, где W означает O или S, R2 представляет собой алкилен, алкенилен или алкинилен, R5 означает -SO2, а R3 означает -NH2;
ooo) -C(=W)-NH-NH-R2(R3)-R5-NH2, где W означает O или S, R2 представляет собой алкилен, алкенилен или алкинилен, R3 означает арил, арилен или гетероарил, а R5 означает -SO2;
ppp) -C(=W)-NH-R3(R5-NH2), где W означает O или S, R3 представляет собой арил, арилен или гетероарил, и R5 означает SO2;
qqq) -C(=W)-NH-R2-R3(R5-NH2), где W означает O или S, R2 представляет собой алкилен, алкенилен или алкинилен, R3 означает арил, арилен или гетероарил, а R5 означает SO2;
rrr) -C(=W)-NH-R3(R2R5-NH2), где W означает O или S, R2 представляет собой алкилен, алкенилен или алкинилен, R3 означает арил, арилен или гетероарил, а R5 означает SO2;
sss) -C(=W)-NHR2(-R3)-C(=W)NH-R2-C(=W)OH, где R2 представляет собой необязательно замещенный алкилен, алкенилен или алкинилен, а R3 представляет собой любое из его значений, которые представлены выше;
ttt) -C(=W)-NHR2(R3)-C(=W)NH-R2-C(=W)NH2, где R2 представляет собой необязательно замещенный алкилен, алкенилен или алкинилен, а R3 означает любое из его значений, которые представлены выше;
uuu) -C(=W)-NHR2-C(=W)NH-R2-C(=W)OH, где R2 представляет собой необязательно замещенный алкилен, алкенилен или алкинилен, а R3 означает любое из его значений, которые представлены выше; или
vvv) -C(=W)-NHR2-C(=W)NH-R2-C(=W)NH2, где R2 представляет собой необязательно замещенный алкилен, алкенилен или алкинилен, а R3 означает любое из его значений, которые представлены выше;
в которых R2, R3 и A, каждый является таким, как описывают ранее.
Третья серия субвариантов данного изобретения приведена для формулы (А), которую характеризуют выше, для которой R4', R5', R6' и R7' определяют как:
a) R6' и R7', оба означают водород, а R4' и R5' независимо представляют собой галоген, -NO2, -N, -OR2, -NR2R2, -NH-R5-C1-3 алкил, -NHCO-C1-3 алкил, оксим, гидразин, -N(SO2)C1-3 алкил, -NH-O-C1-3 алкил, -NHOH или C1-3 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)H, -C(=W)OH, галогеном, -NR2R2, С1-3 алкокси или простым С1-3 тиоэфиром;
b) R4' и R7', оба означают водород, а R5' и R6' независимо представляют собой галоген, -NO2, -N, -OR2, -NR2R2, -NHSO2-C1-6 алкил, -NHCO-C1-6 алкил, оксим, гидразин, -H-O-C1-6 алкил, -NH-OH или С1-3 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)H, -(=W)OH, галогеном, -NR2R2, С1-3 алкокси или простым С1-3 тиоэфиром;
c) R4' и R6', оба означают водород, а R5' и R7' независимо представляют собой галоген, -NO2, -N, -OR2, -NR2R2, -NHSO2-C1-6 алкил, -NHCO-C1-6 алкил, оксим, гидразин, -H-O-C1-6 алкил, -NH-OH, или С1-6 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)H, -(=W)OH, галогеном, -NR2R2, С1-3 алкокси или простым С1-3 тиоэфиром;
d) R4' и R7', оба означают водород, а R5' и R6' независимо представляют собой галоген, -NO2, -N, -OR2, -NR2R2, -NH-C-O-C1-6 алкил, -NHOH, или С1-6 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)H, -C(=W)OH, галогеном или -NH2;
e) R4' и R6', оба означают водород, а R5 и R7' независимо представляют собой галоген, -NO2, -N, -OR2, -NR2R2, -NH-O-C1-3 алкил, -NHOH, или С1-6 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)H, -C(=W)OH, галогеном или -NH2;
f) R6' и R7', оба означают водород, а R4' и R5' независимо представляют собой галоген, -С1-6 алкил, алкенил или алкинил, необязательно замещенный одним или более галогеном;
g) R4' и R7', оба означают водород, а R5' и R6' независимо представляют собой галоген, -С1-6 алкил, алкенил или алкинил, необязательно замещенный одним или более галогеном;
h) R4' и R6', оба означают водород, а R5' и R7' независимо представляют собой галоген, -С1-6 алкил, алкенил или алкинил, необязательно замещенный одним или более галогеном;
i) R6' и R7', оба означают водород, а R4' и R5' независимо представляют собой Cl, F, Br, I, метил, этил или CF3;
j) R4' и R7', оба означают водород, а R5' и R6' независимо представляют собой Cl, F, Br, I, метил, этил или CF3;
k) R4' и R6', оба означают водород, а R5' и R7' независимо представляют собой Cl, F, Br, I, метил, этил или CF3; и
где А является таким, как определяют выше.
Охарактеризована четвертая серия субвариантов для формулы (А), в которой W, X и Y являются такими, как определяют в первой серии субвариантов, а Z является таким, как установлено во второй серии субвариантов.
Охарактеризована пятая серия субвариантов для формулы (А), в которой W, X и Y являются такими, как определяют в первой серии субвариантов, а R4', R5', R6' и R7' являются такими, как устанавливают в третьей серии осуществлений.
Охарактеризована шестая серия субвариантов для формулы (А), в которой Z является таким, как определяют во второй серии субвариантов, а R4', R5', R6' и R7' являются такими, как устанавливают в третьей серии осуществлений.
Не ограничивающую серию первого осуществления, которая представлена формулой (А) выше, определяют, если:
1) Z означает -C(=W)NHNHC2H5OH, R4', R6' и R7' означают Н, R5' означает Cl, X означает H, а Y означает H;
2) Z означает -C(=W)NHCH2C(=W)NH2, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает OH;
3) Z означает -C(=W)NHCH2CONHNH2, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает -O-алкил;
4) Z означает -C(=W)NHCH2CH2-(2-NO2, 5-Me-имидазол), R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает -O-алкенил;
5) Z означает -C(=W)NHCH2NHCH(CH3)C(=W)OH, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает -O-алкинил;
6) Z означает -C(=W)CH=CHC(=W)NH2, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает -O-алкарил;
7) Z означает -C(=W)NHNHCH2C(=W)NH2, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает -O-арил;
8) Z означает -C(=W)NHCH2C(=W)R2, где R2 означает NH2, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает -O-гетероцикл;
9) Z означает -C(=W)NHCH2-A-C(=W)NH2, где A представляет собой двухвалентное промежуточное звено, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает С1-6 алкил;
10) Z означает -C(=W)R2CH-A-C(=W)H, где A представляет собой двухвалентное промежуточное звено, R2 означает NH, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает С2-6 алкинил;
11) Z означает -C(=W)R2CH-A-C(=W)OH, где A представляет собой двухвалентное промежуточное звено, R2 означает NH, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает С2-6 алкинил;
12) Z означает -C(=W)R2-CH-A-R3, где A представляет собой двухвалентное промежуточное звено, R2 означает NH, R3 означает CH3, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает арил;
13) Z означает -C(=W)NHR2-C(=W)R2, где R2 представляет собой необязательно замещенный алкилен с разветвленной цепью или NH, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает гетероцикл;
14) Z означает -C(=W)R2, где R2 представляет собой NH, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает H, а Y означает H;
15) Z означает -C(=W)R2R3-гетероцикл, где R2 представляет собой NH, R3 означает CH3, гетероцикл представляет собой необязательно замещенный морфолин, имидазол или пиррол, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает С1-6 алкил, а Y означает H;
16) Z означает -C(=W)R2C(=W)-O-R3, где R2 представляет собой необязательно замещенный алкил, R3 означает бензилокси, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -O-алкил, а Y означает H;
17) Z означает -C(=W)R2-NH-C(=W)-C1-4 алкокси, где R2 представляет собой необязательно замещенный алкил, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -O-алкенил, а Y означает H;
18) Z означает -C(=W)R3-C(=W)R2, где R2 представляет собой С1-4 алкокси, R3 означает необязательно замещенный алкил, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -O-алкинил, а Y означает H;
19) Z означает -C(=W)R2R3, где R2 представляет собой необязательно замещенный алкил, R3 представляет собой необязательно замещенный фенил, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -O-алкарил, а Y означает H;
20) Z означает -C(=W)R2-NH-C(=W)-O-R3, где R2 представляет собой необязательно замещенный алкил, R3 представляет собой бензил, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -O-аралкил, а Y означает H;
21) Z означает -C(=W)R2C(=W)-NH2, где R2 представляет собой необязательно замещенный алкил, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -O-арил, а Y означает H;
22) Z означает -C(=W)R2-W-R3, где R2 и R3 представляют собой необязательно замещенный алкил, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -O-гетероцикл, а Y означает H;
23) Z означает -C(=W)R2C(=W)-O-R3, где R2 представляет собой необязательно замещенный алкил, R3 представляет собой бензилокси, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -O-алкенил, а Y означает H;
24) Z означает -C(=W)-NH-CH(R2)-C(=W)-NH2, где R2 представляет собой NH2, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает -С2-6 алкинил, а Y означает H;
25) Z означает -C(=W)-NH-NH2, где R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает арил, а Y означает H;
26) Z означает -C(=W)-NH-NH(R2), где R2 представляет собой NH2, R4' означает F или Cl, R6' и R7' означают Н, R5' означает F или Cl, X означает гетероцикл, а Y означает H;
27) Z означает -C(=W)-NH-CH(C[=W]NH2)(CH2-C[=W]-O-CH2-арил), где R4' и R5' независимо означают F или Cl, R6' и R7' означают Н, X означает карбоцикл, а Y означает H;
28) Z означает -C(=W)-NH-CH(-[CH2]4-NH-C[=W]-t-BuO)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' означают Н, X означает -O-алкарил, а Y означает С1-С6-алкил;
29) Z означает -C(=W)-NH-CH(-CH2-CH2-C[=W]-t-BuO)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' означают Н, X означает -O-арил, а Y означает -O-алкил;
30) Z означает -C(=W)-NH-CH(-CH2R3)(-C[=W]-NH2), где R3 означает CF3, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -С2-6 алкенил, а Y означает -OH;
31) Z означает -C(=W)-NH-CH(-CH2R3)(-C[=W]-NH2), где R3 является таким, как определяют в первом осуществлении, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -С2-6 алкинил, а Y означает H;
32) Z означает -C(=W)-NH-CH(-CH2OH)(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -O-алкиларил, а Y означает -О-алкил;
33) Z означает -C(=W)-NH-CH(-C[=W]-NH2)(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает гетероцикл, а Y означает -OH;
34) Z означает -C(=W)-NH-CH(-R3)(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкенил, а Y означает -О-алкил;
35) Z означает -C(=W)-NH-CH(-[CH2]4-NH-C[=W]-O-CH2-R3)(-C[=W]-NH2), где R3 является таким, как определяют в первом осуществлении, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -OH, а Y означает -О-алкилен;
36) Z означает -C(=W)-NH-CH(-CH2-C[=W]-NH2)(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -карбоцикл, а Y означает -О-алкил;
37) Z означает -C(=W)-NH-CH(-CH2-R3)(-C[=W]-NH2), где R3 является таким, как определяют в первом осуществлении, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкил, а Y означает -гетероцикл;
38) Z означает -C(=W)-NH-CH(-[CH2]4-NH2)(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкенил, а Y означает -OH;
39) Z означает -C(=W)-NH-CH(-CH[R2][OH])(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкинил, а Y означает -О-алкил;
40) Z означает -C(=W)-NH-CH(R2)(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -OH, а Y означает -О-алкилен;
41) Z означает -C(=W)-NH-CH(-R2-C[=W]-NH2)(-C[=W]-NH2), где R2 означает NH2, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -С2-6 алкилен, а Y означает -OH;
42) Z означает -C(=W)-NH-CH(-C[=NH]-NH2)(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает карбоцикл, а Y означает -О-алкил;
43) Z означает -C(=W)-NH-CH(-C[=NH]-NH2)(-C[=W]-NH2), где R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -OH, а Y означает -О-алкилен;
44) Z означает -C(=W)-NH-CH(-R3)(-C[=W]-NH2), где R3 является таким, как определяют в первом общем осуществлении, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-арил, а Y означает -С1-6 алкил;
45) Z означает -C(=W)-NH-CH(-CH2-R3)(-C[=W]-NH2), где R3 является таким, как определяют в первом общем осуществлении, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -OH, а Y означает -С1-6 алкилен;
46) Z означает -C(=W)-NH-CH(-R2)(-C[=W]-NH2), где R2 означает NH2, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -С1-6 алкинил, а Y означает -О-арил;
47) Z означает -C(=W)-NH-NH-CH(R3)-C[=W]R2, где R2 означает -NH2, R3 представляет собой необязательно замещенный арил или гетероцикл, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкиларил, а Y означает -OH;
48) Z означает -C(=W)-NHR2(-R3)-C[=W]NH2, где R2 означает -алкилен, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкинил, а Y означает -OH;
49) Z означает -C(=W)NHR2(-R3)-C(=W)NH-R2-C(=W)OH, где R2 означает алкилен, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкенил, а Y означает -О-алкил;
50) Z означает -C(=W)NHR2(-R3)-C(=W)NH-R2-NH2, где R2 означает алкилен, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает H, а Y означает -О-алкил;
51) Z означает -C(=W)-NHR2(-R3)-C(=W)NH-R3-C(=W)OH, где R2 означает алкилен, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -OH, а Y означает -О-алкилен;
52) Z означает -C(=W)R2(CH2)p-A-C(=W)NH2, где R2 означает -NH, p равно 0-10, A означает двухвалентный, необязательно замещенный арил или гетероцикл, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -C1-6 алкил, а Y означает -О-алкенил;
53) Z означает -C(=W)NH-R3, где R3 представляет собой необязательно замещенный гетероцикл, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкил, а Y означает -OH;
54) Z означает -C(=W)NH-R2-R5-R3, где R2 представляет собой алкилен, алкенилен или алкинилен, R5 означает -SO2, R3 означает -NH2, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-арил, а Y означает -О-алкил;
55) Z означает -C(=W)NH-NH-R2(R3)-R5-NH2, где R2 означает алкилен, алкенилен или алкинилен, R3 означает арил, арилен или гетероциклил, R5 представляет собой -SO2, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -О-алкинил, а Y означает -OH;
56) Z означает -C(=W)NH-R3(R5-NH2), где R3 означает арил, арилен или гетероциклил, R5 представляет собой -SO2, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -гетероциклил, а Y означает -О-алкил;
57) Z означает -C(=W)NH-R2R3(R5-NH2), где R2 означает алкилен, алкенилен или алкинилен, R3 означает арил, арилен или гетероциклил, R5 представляет собой -SO2, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -арил, а Y означает -О-алкенил;
58) Z означает -C(=W)NH-R3(R2R5-NH2), где R2 представляет собой алкилен, алкенилен или алкинилен, R3 означает арил, арилен или гетероциклил, R5 представляет собой -SO2, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -OH, а Y означает -О-алкиларил;
59) Z означает -C(=W)NHR2(-R3)-C(=W)NH-R2-C(=W)OH, где R2 представляет собой необязательно замещенный алкилен, алкенилен или алкинилен, R3 означает любое из определений, приведенных в первом общем осуществлении, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -С2-6 алкинил, а Y означает -О-алкенил;
60) Z означает -C(=W)NHR2(-R3)-C(=W)NH-R2-C(=W)NH2, где R2 представляет собой необязательно замещенный алкилен, алкенилен или алкинилен, R3 означает любое из определений, приведенных в первом общем осуществлении, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -С2-6 алкенил, а Y означает -H;
61) Z означает -C(=W)NHR2-C(=W)NH-R2-C(=W)OH, где R2 представляет собой необязательно замещенный алкилен, алкенилен или алкинилен, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -С1-6 алкил, а Y означает -H;
62) Z означает -C(=W)NHR2-C(=W)NH-R2-C(=W)NH2, где R2 представляет собой необязательно замещенный алкилен, алкенилен или алкинилен, R4' и R5' независимо представляют собой F или Cl, R6' и R7' означают Н, X означает -H, а Y означает -О-алкил;
63) Z означает -C(=W)NH-R3, где W означает O, и R3 представляет собой гетероцикл и, в частности, пиридил, пиримидил или имидазол, который необязательно замещен одним или более группами галогена, циано, алкила, алкенила, алкинила или цианоалкила, R4' и R5' независимо представляют собой H, F или Cl, R6' и R7' означают Н, X означает необязательно замещенный фенил, а Y означает -О-алкил; и
где W является таким, как определяют для формулы (А).
Во втором осуществлении в изобретении представляют фенилиндол для применения при лечении ВИЧ-инфекции, имеющий следующую общую формулу (В):
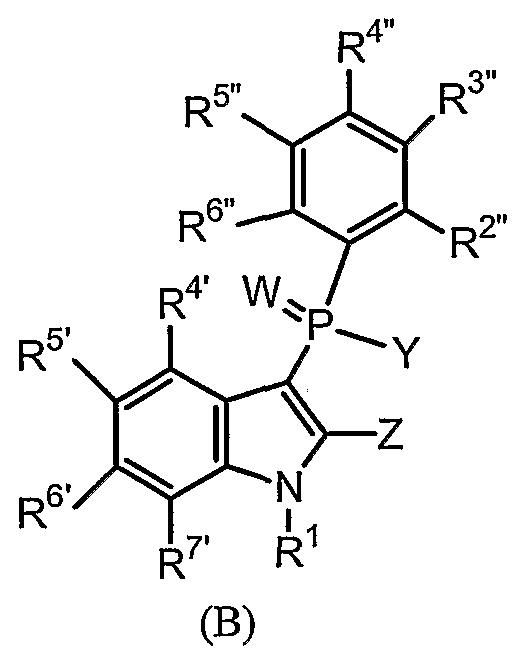
или его фармацевтически приемлемую соль, пролекарство, N-оксид, четвертичный амин, стереохимический изомер или таутомер, в которых:
каждый W, Y, Z, R1, R2, R3, A, n, R4', R5', R6' и R7' является таким, как определяют выше для формулы (А); и
каждый R2'', R3'', R4'', R5'' и R6'' независимо представляет собой:
a) H;
b) галоген;
c) NO2;
d) CN;
e) OR2;
f) SR2;
g) NH2;
h) NR2R3;
i) N(R2)-C(=W)-C1-4 алкил;
j) N(R2)-SO2-C1-4 алкил;
k) С1-6 алкил;
l) С2-6 алкенил;
m) С2-6 алкинил;
n) арил;
o) CF3;
p) CR2R2-S(O)n-R3;
q) CR2R2NR2R3;
r) C-OH;
s) CR2R2-C(=W)R2;
t) ацил;
u) C(=W)R2;
v) C(=W)OR2;
w) C(=W)SR2;
x) C(=W)-NR2R3;
y) C(=W)NH(CH2)p-(аминокислотный остаток);
z) аминокислотный остаток; или
aa) А-(аминокислотный остаток);
bb) цианоалкил;
cc) цианоалкенил; или
dd) цианоалкинил,
где любой из вышеприведенных, необязательно, можно замещать; или
альтернативно, R2'' или R6'' можно присоединять к Y с образованием необязательно замещенного бициклического или трициклического фосфорилированного гетероцикла, содержащего 4-14 элементов.
Первая серия вариантов субформулы (В) включает в себя все субварианты, приведенные для формулы (А) выше.
Вторая серия субвариантов данного изобретения приведена для осуществления формулы (В), которая представлена выше, для которой R2'', R3'', R4'', R5'' и R6'' определяют как:
a) R2'', R4'' и R6'' означают водород, а R3'' и R5'', каждый независимо представляет собой галоген, -NO2, -CN, -OR2, -NH-R5-C1-6 алкил, -NHCO-C1-6 алкил, оксим, гидразин, -N(OH)C1-6 алкил, С1-6 алкокси, -OH, -NR2R2 или -С1-6 алкил, алкенил или алкинил, необязательно замещенный одним или более из -OH, -SR, -CN, -галогеном, -C(=W)H, -C(=W)OH, NR2R2, простым -С1-6 тиоэфиром или -С1-6 алкокси;
b) R2'', R4'' и R6'' означают водород, а R3'' и R5'', каждый независимо представляет собой галоген или -С1-6 алкил, алкенил, алкинил, необязательно замещенный одним или более галогеном;
c) R2'', R3'', R4'', R5'' и R6'' означают водород;
d) R2'', R4'' и R6'' означают водород, а R3'' и R5'' означают метил;
e) R2'', R4'' и R6'' означают водород, а R3'' и R5'' означают хлор;
f) R2'', R4'' и R6'' означают водород, а R3'' и R5'' означают фтор;
g) R2'', R4'' и R6'' означают водород, а R3'' означает иод, а R5'' представляет собой бром;
h) R2'', R4'' и R6'' означают водород, а R3'' означает метил, а R5'' представляет собой хлор; и
i) R2'', R4'' и R6'' означают водород, а R3'' означает хлор, а R5'' представляет собой метил.
Третья серия субвариантов данного изобретения приведена для осуществления формулы (В), которая представлена выше, в которой W, Y, R2'', R3'', R4'', R5'' и R6'' характеризуют как:
a) W означает O, Y означает -О-алкил, R2'', R4'' и R6'' означают водород, а R3'' и R5'', каждый независимо представляет собой галоген, -NO2, -CN, -OR2, -NH-R5-C1-6 алкил, -NHCO-C1-6 алкил, оксим, гидразин, -N(OH)C1-6 алкил, С1-6 алкокси, -OH, -NR2R2 или -С1-6 алкил, алкенил или алкинил, необязательно замещенный одним или более из -OH, -SR, -C(=W)H, -C(=W)OH, галогеном, NR2R2, простым -С1-6 тиоэфиром или -С1-6 алкокси;
b) W означает S, Y означает OH, R2'', R4'' и R6'' означают водород, а R3'' и R5'', каждый независимо представляет собой галоген или -С1-6 алкил, алкенил, алкинил, необязательно замещенный одним или более галогеном;
c) W означает O, Y означает С1-6 алкил, R2'', R3'', R4'', R5'' и R6'' означают водород;
d) W означает S, Y означает С1-6 алкилен, R2'', R4'' и R6'' означают водород, а R3'' и R5'' представляют собой метил;
e) W означает NH, Y означает -О-алкил, R2'', R4'' и R6'' означают водород, а R3'' и
f) R5'' означают хлор;
g) W означает S, Y означает -О-алкенил, R2'', R4'' и R6'' означают водород, а R3'' и
h) R5'' означают фтор;
i) W означает O, Y означает арил, R2'', R4'' и R6'' означают водород, а R3'' и R5'' означают фтор;
j) W означает NH, Y означает -О-алкинил, R2'', R4'' и R6'' означают водород, а R3'' и R5'' означают фтор;
k) W означает S, Y означает S, R2'', R4'' и R6'' означают водород, а R3'' и R5'' означают фтор;
l) W означает O, Y означает -О-алкил, R2'', R4'' и R6'' означают водород, а R3'' означает иод, а R5'' представляет собой бром;
m) W означает O, Y означает -О-алкарил, R2'', R3'', R5'' и R6'' означают водород, а R4'' означает -OH;
n) W означает S, Y означает -NR2R3, R2'', R3'', R5'' и R6'' означают водород, а R4'' означает -NH2;
o) W означает S, Y означает -SR2, R2'', R3'', R5'' и R6'' означают водород, а R4'' означает -NO2; и
p) W означает O, Y означает -О-аралкил, R2'', R4'', и R6'' означают водород, а R3'' означает хлор, а R5'' означает метил.
Характеризуют четвертую серию субвариантов, в которой Z является таким, как определяют в любом осуществлении из второй серии субвариантов для формулы (А), R4', R5', R6' и R7' являются такими, как устанавливают в третьей серии субвариантов для формулы (А), а R2'', R3'', R4'', R5'' и R6'', все характеризуют также, как во второй серии субвариантов для формулы (В).
Характеризуют пятую серию субвариантов, в которой W и Y являются такими, как описывают в первой серии субвариантов для формулы (А), Z является таким, как описывают в любом осуществлении второй серии субвариантов для формулы (А), R4', R5', R6' и R7' являются такими, как устанавливают в третьей серии субвариантов для формулы (А), а R2'', R3'', R4'', R5'' и R6'', все характеризуют также, как в третьей серии субвариантов для формулы (В).
Характеризуют шестую серию субвариантов, в которой Z является таким, как описывают в любом осуществлении второй серии субвариантов для формулы (А), R4', R5', R6' и R7' являются такими, как устанавливают в третьей серии субвариантов для формулы (А), а W, Y, R2'', R3'', R4'', R5'' и R6'', все характеризуют также, как в третьей серии субвариантов для формулы (В).
Не ограничивающую серию второго осуществления, которая приведена для формулы (В) выше, определяют, когда:
A) Z означает C(=W)NHNHC2H5OH, R4', R6' и R7' представляют собой H, R5' означает Cl, Y означает H, R2'', R4'' и R6'' означают H, R3''и R5'' означают метил;
B) Z означает C(=W)NHCH2C(=W)NH2, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает OH, R2'', R4'' и R6'' означают H, а R3''и R5'' означают метил;
C) Z означает -C(=W)NHCH2CONHNH2, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3''и R5'' означают метил;
D) Z означает -C(=W)NHCH2CH2-(2-NO2, 5-Me-имидазол), R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает -О-алкенил, R2'', R4'' и R6'' означают H, а R3''и R5'' означают метил;
E) Z означает -C(=W)NHCH2NHC(=W)OH, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает -О-алкинил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
F) Z означает -C(=W)CH=CHC(=W)NH2, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает -О-алкарил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
G) Z означает -C(=W)NHNHCH2C(=W)NH2, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает -О-арил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
H) Z означает -C(=W)NHCH2C(=W)R2, где R2 представляет собой NH2, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает -О-гетероцикл, R2'', R4'' и R6'' означают H, а R3''и R5'' означают метил;
I) Z означает -C(=W)NHCH2-A-C(=W)NH2, где A представляет собой двухвалентное промежуточное звено, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает С1-6 алкил, R2'', R3'', R5'' и R6'' означают H, а R4'' означает -NH2;
J) Z означает -C(=W)R2CH-A-C(=W)H, где A представляет собой двухвалентное промежуточное звено, R2 означает NH, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает С2-6 алкинил, R2'', R4'' и R6'' означают H, а R3''и R5'' означают метил;
K) Z означает -C(=W)R2CH-A-C(=W)OH, где A представляет собой двухвалентное промежуточное звено, R2 означает NH, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает С2-6 алкинил, R2'', R3'', R5'' и R6'' означают H, а R4'' означает -NO2;
L) Z означает -C(=W)R2-CH-A-R3, где A представляет собой двухвалентное промежуточное звено, R2 означает NH, R3 означает CH3, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает арил, R2'', R4'' и R6'' означают H, а R3''и R5'' означают метил;
M) Z означает -C(=W)NHR2-C(=W)R2, где R2 представляет собой необязательно замещенный алкенил с разветвленной цепью или NH, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает гетероцикл, R2'', R4'' и R6'' означают H, а R3''и R5'' означают метил;
N) Z означает -C(=W)R2, где R2 представляет собой NH, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R3'', R5'' и R6'' означают H, а R4'' означает -OH;
O) Z означает -C(=W)R2R3-гетероцикл, где R2 представляет собой NH, R3 означает CH2, гетероцикл представляет собой необязательно замещенный морфолин, имидазол или пиррол, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
P) Z означает -C(=W)R2NH-C(=W)-O-R3, где R2 представляет собой необязательно замещенный алкил, R3 означает бензилокси, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают -метил;
Q) Z означает -C(=W)R2-NH-C(=W)-C1-4 алкокси, где R2 представляет собой необязательно замещенный алкил, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
R) Z означает -C(=W)R3-C(=W)R2, где R2 представляет собой С1-4 алкокси, R3 означает необязательно замещенный алкил, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
S) Z означает -C(=W)R2R3, где R2 представляет собой необязательно замещенный алкил, R3 означает необязательно замещенный фенил, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
T) Z означает -C(=W)R2-NH-C(=W)-O-R3, где R2 представляет собой необязательно замещенный алкил, R3 означает бензил, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
U) Z означает -C(=W)R2C(=W)-NH2, где R2 представляет собой необязательно замещенный алкил, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
V) Z означает -C(=W)-A-R3, где R3 представляет собой необязательно замещенный алкил, A означает алкиленовый линкер, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
X) Z означает -C(=W)R2C(=W)-O-R3, где R2 представляет собой необязательно замещенный алкил, R3 означает бензилокси, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
Y) Z означает -C(=W)-NH-CH(R2)-C(=W)-NH2, где R2 представляет собой NH2, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
Z) Z означает -C(=W)-NH-NH2, где R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
AA) Z означает -C(=W)-NH-NH(R2), где R2 представляет собой NH2, R4' означает F или Cl, R6' и R7' представляют собой H, R5' означает F или Cl, Y означает H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
BB) Z означает -C(=W)-NH-CH(C[=W]NH2)CH2-C[=W]-O-NR2R2, где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, R2 означает алкил или арил, Y означает H, R2'', R3'', R5'' и R6'' означают H, R4'' означает -NH2;
CC) Z означает -C(=W)-NH-CH(-[CH2]4-NH-C[=W]-t-BuO)(-C[=W]=NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает C1-6 алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
DD) Z означает -C(=W)-NH-CH(-CH2CH2-C[=W]-t-BuO)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
EE) Z означает -C(=W)-NH-CH(-CH2R3)(-C[=W]-NH2), где R3 представляет собой CF3, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -OH, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
FF) Z означает -C(=W)-NH-CH(-CH2R3)(-C[=W]-NH2), где R3 является таким, как описывают в первом осуществлении, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает H, R2'', R3'', R5'' и R6'' означают H, а R4'' означает -NO2;
GG) Z означает -C(=W)-NH-CH(-ацил)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
HH) Z означает -C(=W)-NH-CH(-C[=W]-NH2)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -OH, R2'', R3'', R5'' и R6'' означают H, а R4'' означает -OH;
II) Z означает -C(=W)-NH-CH(-R3)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
JJ) Z означает -C(=W)-NH-CH(-CH2-R3)(-C[=W]-NH2), где R3 является таким, как описывают в первом осуществлении, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -гетероцикл, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
KK) Z означает -C(=W)-NH-CH(-[CH2]4-NH2)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -OH, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
LL) Z означает -C(=W)-NH-CH(-CR2R2)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
MM) Z означает -C(=W)-NH-CH(R2)(-C[=W]-NH2), где R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкилен, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
NN) Z означает -C(=W)-NH-CH(-R3)(-C[=W]-NH2), где R3 является таким, как описывают в первом общем осуществлении, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -С1-6 алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
OO) Z означает -C(=W)-NH-CH(-CH2-R3)(-C[=W]-NH2), где R3 является таким, как описывают в первом общем осуществлении, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкилен, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
PP) Z означает -C(=W)-NH-CH(-R2)(-C[=W]-NH2), где R2 означает NH2, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-арил, R2'', R3'', R5'' и R6'' означают H, а R4'' означает -NH2;
UU) Z означает -C(=W)-NH-NH-CH(R3)-C[=W]R2, где R2 означает -NH2, R3 представляет собой необязательно замещенный арил или гетероцикл, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -OH, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
VV) Z означает -C(=W)-NHR2(-R3)-C[=W]NH2, где R2 означает алкилен, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -OH, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
WW) Z означает -C(=W)-NHR2(-R3)-C(=W)NH-R2-C(=W)OH, где R2 означает алкилен, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
XX) Z означает -C(=W)-NHR2(-R3)-C(=W)NH-R2-NH2, где R2 означает алкилен, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
YY) Z означает -C(=W)-NHR2(-R3)-C(=W)NH-R3-C(=W)OH, где R2 означает алкилен, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкилен, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
ZZ) Z означает -C(=W)R2(CH2)p-A-C(=W)NH2, где R2 означает -NH, p равно 0-10, A представляет собой двухвалентный необязательно замещенный арил или гетероцикл, R3 представляет собой необязательно замещенный алкил, арил или гетероцикл, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкенил, R2'', R3'', R5'' и R6'' означают H, а R4'' означает -NO2;
AAA) Z означает -C(=W)NH-R3, где R3 представляет собой необязательно замещенный гетероцикл, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -OH, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
BBB) Z означает -C(=W)NH-A-S(O)n-R2, где A представляет собой алкилен, алкенилен или алкинилен, R2 означает -NH2, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
CCC) Z означает -C(=W)NH-NH-R2(R3)-A-C(=W)NH2, где R2 означает алкил, A представляет собой алкилен, алкенилен или алкинилен, R3 означает арил, арилен или гетероциклил, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -OH, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
DDD) Z означает -C(=W)NH-A-[S(O)2-NH2], где A представляет собой алкилен, алкенилен или алкинилен, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкенил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
EEE) Z означает -C(=W)NH-A-C(=W)NH-R2-C(=W)OH, где R2 и R3 представляют собой любое из значений, приведенных в первом общем осуществлении, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкенил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
FFF) Z означает -C(=W)NHR2(-R3)-C(=W)NH-R2-C(=W)NH2, где R2 означает необязательно замещенный алкилен, алкенилен или алкинилен, R3 представляет собой любое из значений, приведенных в первом общем осуществлении, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
GGG) Z означает -C(=W)NHR2-C(=W)NH-R2-C(=W)OH, где R2 означает необязательно замещенный алкилен, алкенилен или алкинилен, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -H, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил;
HHH) Z означает -C(=W)NHR2-C(=W)NH-R2-C(=W)NH2, где R2 означает необязательно замещенный алкилен, алкенилен или алкинилен, R4' и R5' независимо означают F или Cl, R6' и R7' представляют собой H, Y означает -О-алкил, R2'', R4'' и R6'' означают H, а R3'' и R5'' означают метил; и
где W является таким, как устанавливают для формулы (А).
В третьем осуществлении, в данном изобретении представляют необязательно замещенный 9-11-членный бициклический 3-фосфоиндол для применения при лечении ВИЧ-инфекции, который имеет следующую общую формулу (С):
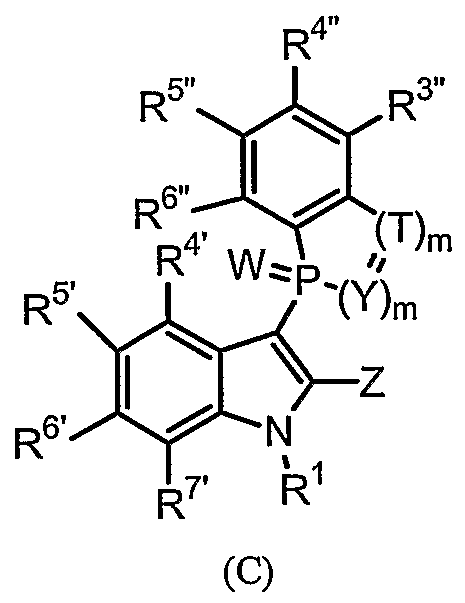
или его фармацевтически приемлемую соль, пролекарство, N-оксид, четвертичный амин, стереохимический изомер или таутомер, в которых:
каждый W, Z, R1, R2, R3, A, n, R4', R5', R6' и R7' являются такими, как описывают выше для формулы (А);
каждый R3'', R4'', R5'' и R6'' являются такими, как описывают выше для формулы (В);
 указывает на наличие ординарной или двойной связи, где:
указывает на наличие ординарной или двойной связи, где:
если  указывает на присутствие двойной связи, каждый Y и T независимо представляет собой:
указывает на присутствие двойной связи, каждый Y и T независимо представляет собой:
a) CR2;
b) N; или
c) SR2;
с предостережением, что один из Y и T должен быть CR2;
если  указывает на присутствие ординарной связи, тогда каждый Y и T независимо представляет собой:
указывает на присутствие ординарной связи, тогда каждый Y и T независимо представляет собой:
a) CR2;
b) O;
c) NR2; или
d) SR2;
с предостережением, что один из Y и T должен быть CR2; и
m равно 1 или 2 при условии, что m может быть только 2 для T или Y = CR2.
Первая серия субвариантов формулы (С) включает в себя все субварианты, приведенные для формулы (А) выше, в которых заместитель "Х" представляет собой арил, гетероциклил, О-арил и О-гетероциклил.
Вторую серию субвариантов данного изобретения приводят для осуществления формулы (С), которая представлена выше, для которой Y и T устанавливают как:
j) T означает -CH2, а Y означает -O-;
k) T означает -C-C(=O)-OCH3, а Y означает -O-;
l) T означает -O, а Y означает -CR2;
m) T означает (-CH2)2, а Y означает -NR2;
n) T означает -CH2, а Y означает -SR2;
o) T означает -O, а Y означает -C-арил;
p) T означает -NR2, а Y означает -C-галоген;
g) T означает -SR2, а Y означает -C-гетероцикл;
r) T означает -С-С1-6 алкил, а Y означает -O-;
s) T означает -C-C(=S)CH2, а Y означает -CH2-;
t) T означает -CH-OCH3, а Y означает -SR2;
u) T означает -C-OH, а Y означает -CH2-;
v) T означает -C-O-C1-6 алкил, а Y означает -CH2-;
w) T означает -C-NH2, а Y означает -CH2-;
x) T означает -C-NH-C1-6 алкил, а Y означает -CH2-; и
y) T означает (-CH2)2, а Y означает (-CH2)2.
Третью серию субвариантов данного изобретения приводят для осуществления формулы (С), которую представляют выше, для которой R3'', R4'', R5'' и R6'' определяют как:
a) R4'' и R6'' означают водород, а R3'' и R5'', каждый независимо представляет собой галоген, -NO2, -CN, -OR2, -NH-R5-C1-6 алкил, -NHCO-C1-6 алкил, гидразин, -N(OH)C1-6 алкил, С1-6 алкокси, -OH, -NR2R2, или -С1-6 алкил, алкенил или алкинил, необязательно замещенный одним или более из -OH, -SR, -C(=W)H, -C(=W)OH, галогена, NR2R2, простого -C1-6 тиоэфира или -С1-6 алкокси;
b) R4'' и R6'' означают водород, а R3'' и R5'', каждый независимо представляет собой галоген или -С1-6 алкил, алкенил, алкинил, необязательно замещенный одним или более галогеном;
c) R3'', R4'', R5'' и R6'' означают водород;
d) R4'' и R6'' означают водород, а R3'' и R5'' означают метил;
e) R4'' и R6'' означают водород, а R3'' и R5'' означают хлор;
f) R4'' и R6'' означают водород, а R3'' и R5'' означают фтор;
g) R4'' и R6'' означают водород, а R3'' и R5'' означают бром;
h) R3'', R4'' и R6'' означают водород, а R5'' означает хлор;
i) R4'' и R6'' означают водород, R3'' означает хлор, а R5'' означает метил;
i) R3'', R5'' и R6'' означают водород, а R4'' представляет собой галоген, -NO2, -CN, -OR2, -NH-R5-C1-6 алкил, -NHCO-C1-6 алкил, гидразин, -N(OH)C1-6 алкил, С1-6 алкокси, -OH, -NR2R2, или -С1-6 алкил, алкенил или алкинил, необязательно замещенный одним или более из -OH, -SR, -C(=W)H, -C(=W)OH, галогена, NR2R2, простого -C1-6 тиоэфира или -С1-6 алкокси;
j) R3'', R5'' и R6'' означают водород, а R4'' представляет собой -NO2;
k) R3'', R5'' и R6'' означают водород, а R4'' представляет собой -OR2;
l) R3'', R5'' и R6'' означают водород, а R4'' представляет собой галоген; и
m) R3'', R5'' и R6'' означают водород, а R4'' представляет собой -NH2.
Характеризуют четвертую серию субвариантов формулы (С), где Z является таким, как описывают в любом осуществлении второй серии субвариантов для формулы (А), R4', R5', R6' и R7' являются такими, как определяют в третьей серии субвариантов для формулы (А), а R3'', R4'', R5'' и R6'', все являются такими, как определяют в третьей серии субвариантов для формулы (С).
Характеризуют пятую серию субвариантов, где Z является таким, как описывают в любом осуществлении второй серии субвариантов для формулы (А), R4', R5', R6' и R7' являются такими, как определяют в третьей серии субвариантов для формулы (А), а Y и T являются такими, как определяют во второй серии субвариантов для формулы (С).
Характеризуют шестую серию субвариантов для формулы (С), где Z является таким, как описывают в любом осуществлении второй серии субвариантов для формулы (А), R4', R5', R6' и R7' являются такими, как определяют в третьей серии субвариантов для формулы (А), а R3'', R4'', R5'' и R6'', все являются такими, как определяют во второй серии субвариантов для формулы (В).
Разновидность третьего осуществления, которое представляют формулой (С) выше, характеризуют, если:
a) Z означает -C(=W)N(2R3)C(=W)NH2, где R2 означает NH, а R3 означает алкил, R1, R4', R6' и R7' означают H, R5' означает галоген или -NO2, R4'' и R6'' означают H, R3'' и R5'' независимо представляют собой -OH или -NR2R2, Y означает O, а T означает CH2;
b) Z означает -C(=W)-NH-CH(-C[=W]NH2)(-CH2-C[=W]-O-CH3-арил); R1, R4', R6' и R7' означают H; R5' означает галоген или -CN; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой -C1-5 алкокси или -C1-5 алкил, необязательно замещенный -С1-5 алкокси, Y означает SR2, а T означает CH2;
c) Z означает -C(=W)NHNH2, R1, R4', R6' и R7' означают H; R5' означает галоген или -NR2R2, R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой -NO2 или -CN; Y означает CH2, а T-R2-R3 означает CH2;
d) Z означает -C(=W)NH-CH2-C(=W)NHNH2, R1, R4', R6' и R7' означают H, R5' означает галоген или -NH-R5-C1-6 алкил, где R5 означает -C(O) или -S(O)n, а n равно 0, 1 или 2, R4'' и R6'' означают H, R3'' и R5'' независимо представляют собой -OR2 или -CN, Y означает C-C1-6 алкил, а T означает N;
e) Z означает -C(=W)NH-CH2-C(=W)NHNH2, R1, R4', R6' и R7' означают H; R5' означает галоген или -NH-R5-C1-6 алкил, где R5 означает -C(O) или -S(O)n, а n равно 0, 1 или 2; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой -OR2 или -CN; Y означает C-C1-6 алкил, T означает SR2, а R2 является таким, как описывают для формулы (А);
f) Z означает -C(=W)NH-CH(R2)-C(=W)NH2, где R2 означает -NH2 или алкил; R1, R4', R6' и R7' означают H; R5' означает галоген или -NHCO-C1-6 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой -NHOH; Y означает C-алкенил, а T означает (CH2)2;
g) Z означает -C(=W)NR2-C(=W)R3, где R2 означает необязательно замещенный алкил, алкенил или алкинил; R3 означает NH2; R1, R4', R6' и R7' означают H; R5' означает галоген или оксим; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NH-R5-C1-6 алкил, где R5 означает -C(O) или S(O)n, а n равно 0, 1 или 2; Y означает C-алкинил, а T означает -O;
h) Z означает -C(=W)NH-R2-SR2, где R2 означает необязательно замещенный алкил, алкенил или алкинил; R1, R4', R6' и R7' означают H; R5' означает галоген или гидразин; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NHCO-C1-6 алкил; Y означает C-карбоцикл, а T означает -NR2, где R2 является таким, как описывают для формулы (А);
i) Z означает -C(=W)NH-N(R3)(R2), где R2 означает гидрокси или алкокси, а R3 означает H или алкил; R1, R4', R6' и R7' означают H; R5' означает галоген или С1-6 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)H, -C(=W)OH, галогеном, -NR2R2, C1-3 алкокси или простым С1-3 тиоэфиром; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -CN; Y означает C-арил, а T означает N;
j) Z означает -C(=W)NH-CH2NH-CH(CH3)C(=W)OH, R1, R4', R6' и R7' означают H; R5' означает галоген или CF3; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NH-O-C1-3 алкил; Y означает O, а T означает CH2;
k) Z означает -C(=W)NH-N(R2)-C(=W)R2, где R2 означает H или NH2, R1, R4', R6' и R7' означают H; R5' означает галоген или H; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или галоген; Y означает -NR2, а T означает CR2, где R2 является таким, как определяют в первом общем осуществлении;
l) Z означает -C(=W)-N(R2)-C(=W)R3, где R2 означает NH, а R3 означает CH3; R1, R4', R6' и R7' означают H; R5' означает галоген или H; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или галоген; Y означает -O, а T означает (C-O-алкил);
m) Z означает -C(=W)-NH-CH=CH-C(=W)R2, где R2 означает NH2; R1, R6' и R7' означают H; R4' и R5' означает галоген или H; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -OR2, где R2 является таким, как определяют в первом общем осуществлении; Y означает -O, а T означает (C-CH2-CH3);
n) Z означает -C(=W)-NH-CH=CH-C(=W)R2, где R2 означает NH2; R1, R6' и R7' означают H; R4' и R5' означает галоген или -NO2; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NHOH; Y означает -O, а T означает C-CH3;
o) Z означает -C(=W)R2(CH)2-C(=W)R2, где R2 означает NH или NH2; R1, R6' и R7' означают H; R4' и R5' означает галоген или -OR2, где R2 является таким, как определяют в первом общем осуществлении; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -С1-3 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)OH, галогеном или -NH2; Y означает -SR2, а T означает CH2;
p) Z означает -C(=W)-R2-CH2-A-C(=W)R2, где R2 является таким, как определяют в первом общем осуществлении, A представляет собой двухвалентный линкер, который описывают в первом общем осуществлении; R1, R6' и R7' означают H; R4' и R5' означает галоген или -CN; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -С1-3 алкокси; Y означает -NR2, где R2 является таким, как описывают в первом общем осуществлении, а T означает (CH2)2;
q) Z означает -C(=W)-R2-CH2-A-C(=W)R2, где R2 означает алкил или -NH2, а A представляет собой двухвалентный линкер; R1, R6' и R7' означают H; R4' и R5' означает галоген или -NR2R2, где R2 является таким, как описывают в первом общем осуществлении; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -OH; Y означает -CH2, а T означает (CH2)2;
r) Z означает -C(=W)-A-R2-C(=W)OR3, где R2 означает -NH, а R3 означает -H или алкил; R1, R6' и R7' означают H; R4' и R5' означает галоген или -NHR5-С1-3 алкил, где R5 является таким, как описывают в первом общем осуществлении; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NR2R2, где R2 является таким, как описывают в первом общем осуществлении; Y означает -C-C1-6 алкил, а T означает CH2;
s) Z означает -C(=W)-NH-C(=W)OR3, где R3 является таким, как описывают для формулы (А); R1, R6' и R7' означают H; R4' и R5' означает галоген или -NHCO-С1-3 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой галоген или H; Y означает -C-алкенил, а T означает O2;
t) Z означает -C(=W)R3-NH-C(=W)-R2, где R2 означает -NH2, а R3 означает -NH; R1, R6' и R7' означают H; R4' и R5' означает галоген или оксим; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -С1-3 алкил или алкенил, необязательно замещенный одним или более галогеном; Y означает -C-алкинил, а T означает (CH2)2;
u) Z означает -C(=W)-N(C=O)-N(R2)-R3, где R2 означает -H, а R3 означает -NH2, R1, R6' и R7' означают H; R4' и R5' означает галоген или гидразин; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H; Y означает -C-арил, а T означает (CH2)2;
v) Z означает -C(=W)-N(R2)-N(R2)-C(=W)R3, где R2 означает H или алкил, а R3 означает NH2, R1, R6' и R7' означают H; R4' и R5' означает галоген или -NHS(O)2-C1-3 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -метил; Y означает -C-гетероцикл, а T означает O;
w) Z означает -C(=W)-N(-N[R2][R3])-R3, где R2 означает H или алкил, а R3 означает NH2; R1, R6' и R7' означают H; R4' и R5' означает галоген или -C1-6 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)H, -C(=W)OH, галогеном, NR2R2, C1-3 алкокси или простым С1-3 тиоэфиром, где R2 является таким, как описывают в первом общем осуществлении; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NR2R2, где R2 является таким, как описывают в первом общем осуществлении; Y означает -C-карбоцикл, а T означает NR2, где R2 является таким, как представляют выше;
x) Z означает -C(=W)R2-C(=W)NH2, где R2 означает алкил; R1, R6' и R7' означают H; R4' и R5' означает галоген или -H; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или хлор; Y означает -SR2, а T означает CH2;
y) Z означает -C(=W)R2-SR2, где R2 означает -NH или алкил; R1, R6' и R7' означают H; R4' и R5' означают галоген или -CF3; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или фтор; Y означает -O, а T означает (CH2)2;
z) Z означает -C(=W)-CH(R2)-C(=NH)R2, где R2 означает H или NH2; R1, R4' и R7' означают H; R5' и R6' означают галоген или -H; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -CF3; Y означает -NR2, а T означает CR2, где R2 является таким, как определяют для формулы (А);
aa) Z означает -C(=W)-NH-A-NH-C(=W)-A-C(=W)-R2, где R2 означает NH2, а A представляет собой двухвалентный линкер; R1, R4' и R7' означают H; R5' и R6' означают -CN или -NO2; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NO2; Y означает -CH2, а T означает NR2, где R2 является таким, как определяют для формулы (А);
bb) Z означает -C(=W)-R2-CH-(-A-C[=W]R2)(-C[=W]-NH2), где R2 означает H, алкил или NH; A представляет собой двухвалентное промежуточное звено, как описывают для формулы (А); R1, R4' и R7' означают H; R5' и R6' означают H или -NHCO-C1-6 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или гидразинил; Y означает (CH2)2, а T означает N;
cc) Z означает -C(=W)-NH-A(-C[=W]-NH2), где A представляет собой алкиленовое или ариленовое двухвалентное промежуточное звено; R1, R4' и R7' означают H; R5' и R6' означают H или -NH(SO2)C1-6 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NHOH; Y означает -С-алкенил, а T означает N;
dd) Z означает -C(=W)-NH-CH(-A-R3)(-C[=W]-NH2), где A представляет собой алкиленовое или алкениленовое промежуточное звено; R3 означает OH; R1, R4' и R7' означают H; R5' и R6' означают H или CF3; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NR2R2, где R2 является таким, как определяют для формулы (А); Y означает -С-карбоцикл, а T означает SR2;
ee) Z означает -C(=W)-NH-CH(R2)(R3), где R2 и R3, каждый представляет собой C(=W)NH2; R1, R6' и R7' означают H; R5' и R4' означают H или галоген; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -С1-5 алкокси, Y означает -O, а T означает CH2;
ff) Z означает -C(=W)-A-CH-(R2-C[=W]-NH2)(-C[=W]-NH2), где A представляет собой промежуточное звено, как описывают для формулы (А); R2 означает NH; R1, R6' и R7' означают H; R5' и R4' означают H или -NO2; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -OH; Y означает -N, а T означает CH2;
gg) Z означает -C(=W)-NH-CH(-CH-R2-OH)(-C[=W]-NH2), где R2 означает NH или алкилен; R1, R6' и R7' означают H; R5' и R4' означают H или -галоген; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -галоген; Y означает -SR2, а T означает CH-OCH3;
hh) Z означает -C(=W)-NH-CH(-R2)(-C[=W]-NH2), где R2 означает алкил; R1, R6' и R7' означают H; R5' и R4' означают H или -NO2; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -CN; Y означает -С-арил, а T означает N;
ii) Z означает -C(=W)-NH-CH(-R2)(-C[=W]-NH2), где R2 означает алкил; R1, R6' и R7' означают H; R5' и R4' означают H или -OH; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -CN; Y означает -С-гетероцикл, а T означает (CH2)2;
jj) Z означает -C(=W)-NH-CH(-R2-C[=W]-NH2)(-C[=W]-NH2), где R2 означает алкилен; R1, R6' и R7' означают H; R4' и R5' означают H или -NO2; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NHOH; Y означает -O, а T означает CH2;
kk) Z означает -C(=W)-NH-CH(-R2)(-C[=W]-NH2), где R2 означает -S(O)R3, а R3 является таким, как описывают для формулы (А); R1, R6' и R7' означают H; R4' и R5' означают H или -OR2; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -C1-3 алкокси; Y означает -NR2, где R2 является таким, как определяют в первом общем осуществлении, а T означает CH2;
ll) Z означает -C(=W)-NH-CH(-C[=NH]-NH2)(-C[=W]-NH2); R1, R6' и R7' означают H; R4' и R5' означают H или -NR2R2, где R2 является таким, как описывают в первом общем осуществлении; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -OH; Y означает -SR2, а T означает (CH2)2;
mm) Z означает -C(=W)-NH-NH-CH(R3)-C[=W]R2, где R2 означает -NH2, и R3 представляет собой необязательно замещенный арил или гетероарил; R1, R6' и R7' означают H; R4' и R5' означают H или -CN; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NR2R2, где R2 является таким, как описывают в первом общем осуществлении; Y означает -С-С1-6 алкил, а T означает N;
nn) Z означает -C(=W)-NHR2(-R3)-C[=W]NH2, где R2 означает алкил, а R3 представляет собой необязательно замещенный алкил, арил или гетероарил; R1, R6' и R7' означают H; R4' и R5' означают H или -NH-R5-C1-3 алкил, где R5 является таким, как устанавливают в первом общем осуществлении; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -С1-6 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, -C(=W)OH, галогеном или NH2; Y означает -С-алкенил, а T означает SR2, где R2 является таким, как описывают для формулы (А);
oo) Z означает -C(=W)-NHR2(-R3)-C[=W]NH-R2-C(=W)OH, где R2 означает алкил, а R3 представляет собой необязательно замещенный алкил, арил или гетероарил; R1, R6' и R7' означают H; R4' и R5' означают H или -NHCO-C1-3 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -С1-6 алкил или алкенил, необязательно замещенный одним или более галогеном; Y означает -С-алкинил, а T означает CH2;
pp) Z означает -C(=W)-NHR2(-R3)-C[=W]NH-R2-NH2, где R2 означает алкил, а R3 представляет собой необязательно замещенный алкил, арил или гетероарил; R1, R6' и R7' означают H; R4' и R5' означают H или -оксим; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или галоген; Y означает -CH2, а T означает -NR2, где R2 является таким, как определяют для формулы (А);
qq) Z означает -C(=W)-NHR2(-R3)-C(=W)NH-R3, где R2 означает алкил, а R3 представляет собой необязательно замещенный алкил, арил или гетероарил; R1, R6' и R7' означают H; R4' и R5' означают H или -гидразин; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H; Y означает -NR2, где R2 является таким, как определяют в первом общем осуществлении, а T означает (CH2)2;
rr) Z означает -C(=W)-R2-A-C(=W)-NH2, где R2 означает -NH, а A представляет собой двухвалентное промежуточное звено, которая представляет собой необязательно замещенный арил или гетероарил; R1, R6' и R7' означают H; R4' и R5' означают H или -NH(SO2)C1-6 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или метил; Y означает -С-С1-6 алкил, а T означает N;
ss) Z означает -C(=W)NH-R3, где R3 представляет собой необязательно замещенный гетероцикл; R1, R6' и R7' означают H; R4' и R5' означают H или -C1-6 алкил или алкенил, необязательно замещенный одним или более -OH, -SR, C(=W)H, C(=W)OH, галогеном, NR2R2, C1-3 алкокси или простым С1-3 тиоэфиром; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или хлор; Y означает -С-алкенил, а T означает NR2, где R2 является таким, как определяют для формулы (А);
tt) Z означает -C(=W)NH-A-S(O)2-R3, где A означает алкиленовое, алкениленовое или алкиниленовое двухвалентное промежуточное звено, R3 представляет собой -NH2, а R5 означает -SO2; R1, R6' и R7' означают H; R4' и R5' означают H; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или фтор; Y означает -(CH2)2, а T означает -(CH2)2;
uu) Z означает -C(=W)NH-NH-A-(R3)-S(O)2-NH2, где A означает алкиленовое, алкениленовое или алкиниленовое двухвалентное промежуточное звено, R3 представляет собой арил, арилен или гетероарил, а R5 означает -SO2; R1, R6' и R7' означают H; R4' и R5' означают H или CF3; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или CF3; Y означает -O, а T означает CH2;
vv) Z означает -C(=W)NH-R3(SO2-NH2), где R3 представляет собой арил, арилен или гетероарил; R1, R4' и R7' означают H; R5' и R6' означают H или -галоген; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NO2; Y означает -O, а T означает CR2, где R2 является таким, как определяют для формулы (А);
ww) Z означает -C(=W)NH-A-(NH2), где A означает алкиленовое, алкениленовое или алкиниленовое двухвалентное промежуточное звено; R1, R4' и R7' означают H; R5' и R6' означают H или -NO2; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -галоген; Y означает -O, а T означает С-карбоцикл;
xx) Z означает -C(=W)NH-R3(-A-SO2-NH2), где A означает алкиленовое, алкениленовое или алкиниленовое двухвалентное промежуточное звено; R3 представляет собой арил, арилен или гетероарил, R1, R4' и R7' означают H; R5' и R6' означают H или -CN; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NH-R5-C1-3 алкил, где R5 является таким, как определяют в первом общем осуществлении; Y означает -С-карбоцикл; а T означает NR2, где R2 является таким, как описывают для формулы (А);
yy) Z означает -C(=W)NH-(-R3)-C(=W)NH-A-C(=W)OH, где A представляет собой необязательно замещенное алкиленовое, алкениленовое или алкиниленовое двухвалентное промежуточное звено, R3 является таким, как определяют в первом общем осуществлении; R1, R4' и R7' означают H; R5' и R6' означают H или -OR2, где R2 является таким, как определяют в первом общем осуществлении; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -CN; Y означает -С-арил, а T означает CH2;
zz) Z означает -C(=W)NH(-R3)-C(=W)NH-A-C(=W)NH2, где A представляет собой необязательно замещенное двухвалентное промежуточное звено, которую описывают для формулы (А); R3 является таким, как определяют в первом общем осуществлении; R1, R4' и R7' означают H; R5' и R6' означают H или -NR2R2, где R2 является таким, как определяют в первом общем осуществлении; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -NH-R5-C1-6 алкил, где R5 является таким, как определяют в первом общем осуществлении; Y означает -С-гетероцикл, а T означает SR2;
aaa) Z означает -C(=W)NHR2-C(=W)NH-R2-C(=W)OH, где R2 является таким, как описывают для формулы (А); A представляет собой необязательно замещенное двухвалентное промежуточное звено; R1, R4' и R7' означают H; R5' и R6' означают H или -NHSO2-C1-6 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или гидразин; Y означает -O, а T означает (CH2)2; и
bbb) Z означает -C(=W)NHR2-C(=W)NH-R2-C(=W)NH2, где R2 является таким, как описывают для формулы (А); A представляет собой необязательно замещенное двухвалентное промежуточное звено; R1, R4' и R7' означают H; R5' и R6' означают H или -NHCO-C1-6 алкил; R4'' и R6'' означают H; R3'' и R5'' независимо представляют собой H или -OH; Y означает -NR2, где R2 является таким, как определяют в первом общем осуществлении, а T означает CH2;
где W является таким, как определяют выше для первого общего осуществления формулы (А).
Все осуществления, субварианты определяют, если:
1) Z означает -C(=W)-NH-R2; -C(=W)-NR2R3; -C-R2R3; -CR2-C(=W)R3; -R2-C(=W)R3; -R2-C(=W)R2; -R2R3; R3; или C(=W)-NH-CR2R2-C(=W)-NH-CR2R3-C(=W)-NR2R3;
2) R4', R6' и R7' означают H, а R5' означает i) галоген и, в частности, хлор; ii) гидразин; iii) С1-6 алкил, алкенил, амино-алкил, тиоамино-алкил или аминокарбонил-алкил, каждый из которых, необязательно, можно замещать одним или более -OH, -C(=W)H, -C(=W)OH, -NR2R3, -C1-3 алкокси или простым -С1-3 тиоэфиром; или одной из следующих комбинаций:
a) R5', R6' и R7' означают водород, а R4' означает галоген;
b) R4', R5' и R7' означают водород, а R6' означает галоген;
c) R4', R5' и R6' означают водород, а R7' означает галоген;
d) R5', R6' и R7' означают водород, а R4' означает CF3;
e) R4', R5' и R7' означают водород, а R6' означает CF3; и
f) R4', R5' и R6' означают водород, а R7' означает CF3.
III. Определения
Подразумевают следующие определения и терминологические конструкции, если не указывают особо.
Диапазоны, специфические значения и обычные значения, приведенные для радикалов, заместителей и производных являются только иллюстрацией и не исключают другие определенные значения или величины в пределах установленных диапазонов для радикалов, заместителей и производных. Когда диапазон оказывается описанным в заявке, диапазон независимо включает в себя каждый элемент диапазона. В качестве иллюстративного примера, когда упоминают С1-6-алкил, этот перечень независимо включает в себя С1-алкил, С2-алкил, С3-алкил, С4-алкил, С5-алкил и С6-алкил.
"Галоген" означает фтор, хлор, бром или иод.
"Алкил", "алкокси", алкенил", "алкинил" и так далее включает в себя группы как с прямой, так и с разветвленной цепью. Однако ссылка на индивидуальный радикал, такой как "пропил" охватывает только такой радикал с прямой цепью, тогда как изомер с разветвленной цепью, такой как "изопропил", должен быть назван именно так.
Термин "алкил", который используют в заявке и если не указывают особо, представляет собой насыщенный, прямой, разветвленный или циклический, первичный, вторичный или третичный углеводород, например, из С1-10, а точнее включает в себя метил, этил, пропил, изопропил, циклопропил, бутил, изобутил, трет-бутил, пентил, циклопентил, изопентил, неопентил, гексил, изогексил, циклогексил, циклогексилметил, 3-метилпентил, 2,2-диметилбутил и 2,3-диметилбутил. Если контекст данного описания позволяет, алкил замещают, фрагменты, которыми можно замещать группу алкила, без ограничений, включают в себя гидроксил, амино, алкиламино, ариламино, алкокси, арилокси, арил, гетероциклил, галоген, карбокси, ацил, ацилокси, амидо, нитро, циано, сульфоновую кислоту, сульфат, фосфоновую кислоту, фосфат или фосфонат, простой эфир, защищенный или незащищенный, когда требуется, которые известны специалистам в данной области и которые описывают, например, в Greene et al., Protective Groups in Organic Synthesis, John Wiley and Sons, Third Ed., 1999.
Термин "низший алкил", который используют в заявке и если не указывают особо, включает в себя С1-4 насыщенную, прямую, разветвленную или, если уместно, циклическую (например, циклопропил) группу алкила, включая как замещенные, так и незамещенные формы. Если не указывают особо в данной заявке, когда алкил является подходящим фрагментом, обычно используют низший алкил. Аналогично, когда алкил или низший алкил оказывается подходящим фрагментом, незамещенный алкил или низший алкил является типичным.
Термины "алкенил" и "алкинил" относятся к фрагментам алкила, включающими в себя как замещенные, так и незамещенные формы, в которых, по крайней мере, одну насыщенную связь С-С замещают двойной или тройной связью. Так, С2-6 алкенил может представлять собой винил, аллил, 1-пропенил, 2-пропенил, 1-бутенил, 2-бутенил, 3-бутенил, 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-гексенил, 2-гексенил, 3-гексенил, 4-гексенил или 5-гексенил. Аналогично, С2-6 алкинил может представлять собой этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 1-пентинил, 2-пентинил, 3-пентинил, 4-пентинил, 1-гексинил, 2-гексинил, 3-гексинил, 4-гексинил или 5-гексинил.
Термин "алкилен" относится к насыщенному, с прямой цепью, двухвалентному алкильному радикалу формулы -(CH2)n-, в которой n может быть любым целым числом от 1 до 10.
Используемый за исключением, которое указывают, термин "арил" означает любое стабильное моноциклическое, бициклическое или трициклическое углеродное кольцо из вплоть до 8 элементов в каждом кольце, при этом, по крайней мере, одно кольцо является ароматическим, что определяют по правилу 4n + 2 Хюккеля. Примеры кольцевых систем арила включают в себя фенил, нафтил, тетрагидронафтил и бифенил. Группа арила может быть замещенной одним или более фрагментами, без ограничений, включающими в себя гидроксил, амино, алкиламино, ариламино, алкокси, арилокси, алкил, гетероциклил, галоген, карбокси, ацил, ацилокси, амидо, нитро, циано, сульфонамидо, сульфоновую кислоту, сульфат, фосфоновую кислоту, фосфат или фосфонат, простой эфир, защищенный или незащищенный, когда требуется, которые известны специалистам в данной области и которые обсуждают в Greene et al., Protective Groups in Organic Synthesis, John Wiley and Sons, Third Ed., 1999.
Используемый термин "гетероцикл" или "гетероциклический", за исключением при необходимости, относится к стабильному 5-7-членному моноциклическому или стабильному 8-11-членному бициклическому гетероциклическому кольцу, которое является или насыщенным, или ненасыщенным, включая гетероарил, и которое состоит из атома(ов) углерода и от одного до четырех гетероатомов, без ограничений, включающих в себя O, S, N и P, и в котором гетероатомы азота и серы, необязательно, могут быть окисленными и/или гетероатом азота кватернизованным, и которое включает в себя бициклическую группу, в которой любое из идентифицированных выше гетероциклических колец конденсировано с кольцом бензола. Гетероциклическое кольцо можно присоединять к любому гетероатому или атому углерода, что приводит к созданию стабильной структуры. Гетероароматическое кольцо можно частично или полностью гидрировать, когда требуется. Например, дигидропиридин можно использовать вместо пиридина. Функциональные группы кислорода и азота на гетероариле можно замещать при необходимости или по желанию. Подходящие защитные группы для кислорода или азота включают в себя триметилсилил, диметилгексилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, тритил, замещенный тритил, алкил, метансульфонил, п-толуолсульфонил или группы ацила, такие как ацетил и пропионил.
Не ограничивающие примеры гетероарильных и гетероциклических групп включают в себя фурил, пиридил, пиримидил, пиридазинил, пиразинил, пиперидинил, пиперазинил, тиенил, пирролил, пирролинил, пирролидинил, имидазолил, тетразолил, тиазолил, тиазинил, тиазинил, оксазолил, пуринил, карбазолил, хинолинил, пиразолил, морфолинил, бензимидазолил и тому подобные. Любые из гетероарматических и гетероциклических фрагментов, необязательно, можно замещать, как описывают выше для арила, включая замещение(я) одним или более гидроксилом, амино, алкиламино, ариламино, алкокси, арилокси, алкилом, гетероциклилом, галогеном, карбокси, ацилом, ацилокси, амидо, нитро, циано, сульфоновой кислотой, сульфатом, фосфоновой кислотой, фосфатом или фосфонатом, простым эфиром, защищенным или незащищенным, когда требуется, которые известны специалистам в данной области и которые обсуждают, например, в Greene et al., Protective Groups in Organic Synthesis, John Wiley and Sons, Third Ed., 1999.
Термин "ацил" относится к соединению формулы "RC(O)-", в которой R замещают или не замещают алкилом или арилом, как описывают в заявке.
Термин "карбоксил" относится к соединению формулы "RCOOH", в которой R замещают или не замещают алкилом или арилом, как описывают в заявке.
Термин "аралкил", используемый в заявке, если не указывают особо, относится к группе арила, которую описывают выше, связанной с молекулой через группу алкила, которую описывают выше.
Термин "алкарил", используемый в заявке, если не указывают особо, относится к группе алкила, которую описывают выше, связанной с молекулой через группу арила, которую определяют выше.
Термин "алкокси", используемый в заявке, если не указывают особо, относится к фрагменту структуры "-O-алкил", где алкил является таким, как определяют выше.
Термин "амино", используемый в заявке, если не указывают особо, относится к фрагменту, представляемому структурой "-NR2", и включает в себя первичные амины и вторичные и третичные амины, необязательно замещенные группами алкила, арила, гетероциклила и/или сульфонила. Так, R2 может представлять собой два водорода, два алкильных фрагмента или один водород и один фрагмент алкила.
Термин "амидо", используемый в заявке, если не указывают особо, относится к фрагменту, представляемому структурой "-C(O)NR2", в которой R2 означает Н, группу алкила, арила, ацила, гетероциклила и/или сульфонила.
Используемые термины "аминокислота" или "аминокислотный остаток" относится к природной аминокислоте или некоторой ее части (то есть Ala, Arg, Asn, Asp, Cys, Glu, Gln, Cly, His, Hyl, Hyp, Ile, Leu, Lys, Met, Phe, Pro, Ser, Thr, Trp, Tyr и Val) в D- или L-форме, или к неприродной аминокислоте, имеющей одну или более доступных валентностей, например, такой как трет-бутилглицин, орнитин, гиппуровая кислоты и фосфотреонин. Другими неприродными аминокислотами являются кислоты, представляемые формулой "NH2(CH2)yCOOH", в которой y равно 2-12, и включают в себя аминоалкановые кислоты, такие как ε-аминокапроновая кислота (H2N-(CH2)5-COOH). Термин также охватывает природные и неприродные аминокислоты, несущие амино-защитные группы, такие как ацил, трифторацетил и бензилоксикарбонил, а также природные и неприродные аминокислоты, защищенные по карбокси-фрагментам защитными группами, такими как С1-6 алкил, сложный фениловый или бензиловый эфир и амид, и защитными группами, известными специалистам в данной области. Во всех случаях, когда природные или неприродные аминокислоты содержат один или более хиральных центров, все возможные стереохимические конфигурации, включая как "D"-, так и "L"-формы и их смеси, включая рацемические смеси, включены в заявку.
Используемый термин "четвертичный амин" включает в себя соли четвертичного аммония, которые содержат положительно заряженный азот. Они образуются в результате реакции между основным азотом в соединении, представляющем интерес, и соответствующим кватернизирующим агентом, например, таким как метилиодид или бензилиодид. Соответствующие противоионы, сопутствующие четвертичному амину, включают в себя ацетат, трифторацетат, ионы хлора, брома и иода.
Используемый в заявке термин "N-оксиды" обозначает состояние соединений данного изобретения, при котором один или более атомов азота окислены атомом кислорода.
Используемый в заявке термин "ретровирус" включает в себя любой вирус, который экспрессирует обратную транскриптазу. Примеры ретровируса, без ограничений, включают в себя HIV-1, HIV-2, HTLV-I, HTLV-II, FeLV, FIV, SIV, AMV, MMTV и MoMuLV.
Используемый термин "обратная транскриптаза" или "RT" относится к ферменту, имеющему участок, связывающий ненуклеозидный ингибитор, подобный участку RT HIV-1 (ВИЧ-1), и в котором лиганды, которые связывают композиционный связывающий карман соединений данного изобретения, также будут связываться. Одним показателем активности RT является вирусная репликация. Оценку репликации вируса ВИЧ-1 осуществляют с помощью автоматизированного анализа, в котором используют MTT, что описано ранее в данном описании. Другой оценкой является иммуноферментный анализ ядерного антигена р24, например, такой как анализ, коммерчески предоставляемый фирмой Coulter Corporation/Immunotech, Inc.® (Westbrook, MI). Другие способы оценки активности RT представляют собой исследование активности рекомбинантной обратной транскриптазы ВИЧ-1, например, такое как использование системы исследования Quan-T-RT™ фирмы Amersham® (Arlington Heights, IL) и которая описана Bosworth et al., Nature, 1989, 341:167-168.
Используемое в заявке выражение “соединение, которое "ингибирует репликацию вируса иммунодефицита человека (ВИЧ)"” подразумевает соединение, которое при контакте с ВИЧ-1, например, через ВИЧ-инфицированные клетки, осуществляет снижение количества ВИЧ-1 по сравнению с необработанным контролем. Ингибирование репликации ВИЧ-1 можно оценивать по любому способу, известному специалистам в данной области, например, такому как анализ р24, упомянутый выше.
Реагент, отмеченный в схеме синтеза "mCPBA", представляет собой мета-хлор-пероксибензойную кислоту.
Используемый термин "восстановительная терапия" подразумевает соединение, которое может быть взято при любой схеме после того, как первичная схема лечения пациента не имела успеха.
Используемый термин "хозяин" относится к многоклеточному или одноклеточному организму, в котором может реплицироваться вирус. Таким образом, термин "хозяин" включает в себя клеточную линию, млекопитающее, предпочтительно человека. Альтернативно, хозяин может нести часть генома ВИЧ, чью репликацию или функцию можно изменять соединениями данного изобретения. Точнее термин "хозяин" относится к инфицированным клеткам, клеткам, трансфицированным всем или частью генома ВИЧ, и млекопитающим, особенно приматам, включая шимпанзе и человека. В случае большинства применений данного изобретения млекипитающему, хозяином является человек. Однако в данном изобретении четко предполагают применения в ветеринарии, например, у шимпанзе.
IV. Фармацевтически приемлемые соли, пролекарства, стереоизомеры и таутомеры
Активное соединение можно вводить в виде соли или пролекарства, которое при введении реципиенту, способно доставлять непосредственно или косвенно родительское соединение или которое само проявляет активность. Не ограничивающие примеры включают в себя фармацевтически приемлемую соль, альтернативно называемую "физиологически приемлемая соль". Кроме того, модификации, произведенные с соединением, могут влиять на его биологическую активность, в некоторых случаях увеличивая активность по сравнению с исходным соединением. Упомянутую активность можно оценивать при получении солевой или пролекарственной формы соединения и тестировании его противовирусной активности, используя способы, описанные в заявке, или другие способы, известные любым специалистам в области NNRTI.
Фразу "фармацевтически приемлемая соль или пролекарство" используют во всем описании, чтобы определить любую фармацевтически приемлемую форму (такую как сложный эфир, амид, соль сложного эфира, соль амида или родственной группы) соединения, которое при введении пациенту обеспечивает активное соединение изобретения. Используемые в заявке термины "стереоизомер" и "таутомер" включают в себя все стереоизомерные и таутомерные формы соединений данного изобретения, а также его четвертичный амин, соль, сольват, производное и N-оксидные формы. В случае, когда соединения общей формулы (I) и (II) содержат один или более хиральных центров, все возможные энантиомерные и диастереомерные формы включены в изобретение.
Термин "фармацевтически приемлемая соль" относится к состоянию соединения, при котором соединение несет противоион, который является фармацевтически приемлемым, и при котором соль сохраняет желаемую биологическую активность идентифицированных в изобретении соединений при проявлении минимальных нежелательных токсических эффектов. Такие соли представляют собой нетоксические, терапевтически используемые формы соединений данного изобретения. Любую соль, которая сохраняет желаемую биологическую активность соединений, включенных в заявку, и которая проявляет минимальные или не проявляет никаких нежелательных или токсических эффектов, имеют в виду для включения в изобретение. Фармацевтически приемлемые соли включают в себя соли, полученные из фармацевтически приемлемых органических или неорганических кислот и оснований. Фармацевтически не приемлемые кислоты и основания также находят применение в изобретении, например, в синтезе и/или очистке соединений, представляющих интерес. Таким образом, все "соли" предполагают применять в изобретении.
Не ограничивающие примеры приемлемых солей включают в себя соли, полученные из неорганических кислот, например, таких как хлористоводородная кислота, бромистоводородная кислота, серная кислота, фосфорная кислота, азотная кислота, однозамещенная угольная кислота, угольная кислота; и соли, образованные с органическими кислотами, например, такими как муравьиная кислота, уксусная кислота, щавелевая кислота, винная кислота, янтарная кислота, яблочная кислота, малоновая кислота, аскорбиновая кислота, лимонная кислота, бензойная кислота, дубильная кислота, памовая кислота, альгиновая кислота, полиглутаминовая кислота, толуолсульфоновая кислота, метансульфоновая кислота, нафталинсульфоновая кислота, нафталиндисульфоновая кислота, α-кетоглутаровая кислота, α-глицерофосфорная кислота и полигалактуроновая кислота. Подходящие соли включают в себя соли, полученные с щелочными металлами, такими как литий, калий и натрий, с щелочноземельными металлами, такими как кальций и магний, а также с другими основаниями, хорошо известными любым специалистам в фармацевтической области. Другие приемлемые соли включают в себя соли, полученные с катионами металлов, таких как цинк, висмут, барий или алюминий, или с катионом, образованным из амина, такого как аммиак, NN-дибензилэтилен-диамина, D-глюкозамина, тетраэтиламмония или этилендиамина. Кроме того, приемлемые соли включают в себя соли, полученные из комбинации кислот и оснований, например, такие как таннат цинка.
Фармацевтически приемлемое пролекарство относится к соединению, которое метаболизирует (то есть гидролизуется или окисляется, например) в организме хозяина с образованием соединения данного изобретения. Типичные примеры пролекарств включают соединения, которые имеют биологически лабильные защитные группы на функциональном фрагменте активного соединения. Пролекарства включают в себя соединения, которые можно окислять, восстанавливать, аминировать, деаминировать, гидроксилировать, дегидроксилировать, гидролизовать, дегидролизовать, алкилировать, деалкилировать, ацилировать, деацилировать, фосфорилировать и/или дефосфорилировать, чтобы получить активное соединение.
Соединения данного изобретения или обладают противовирусной активностью против ретровирусов и, в частности, ВИЧ, или метаболизируют до соединения, которое проявляет такую активность.
Любое из соединений оксо-пиримидина, описываемых в заявке, можно вводить в виде пролекарства, чтобы увеличить активность, биодоступность, стабильность или иным образом изменить свойства оксо-пиримидина. Ряд пролекарственных лигандов также известен. Вообще, ацилирование, алкилирование и другие липофильные модификации гетероатома оксо-пиримидина будут повышать стабильность соединения. Примеры заместительных групп, которые могут замещать один или более водородов на гетероцикле, без ограничений, включают в себя алкил, арил, стероид, углеводород, включая сахара, 1,2-диацилглицерин, фосфолипид, фосфотидилхолин, фосфохолин и/или спирт. Любую из названных групп можно использовать в комбинации с обсуждаемым соединением оксо-пиримидина, чтобы достигнуть желаемого эффекта.
V. Способы лечения
В одном осуществлении представляют способ лечения или профилактики ВИЧ-инфекции у хозяина, включающий в себя введение соединения 3-фосфоиндола хозяину при необходимости. В одном особом осуществлении соединение вводят перорально, парентерально, энтерально, внутривенно, внутрикожно, подкожно, чрескожно, трансдермально, интраназально, местно или с помощью ингаляционной терапии. Соединение можно вводить хозяину, у которого установлена ВИЧ-инфекция, титрованием зараженности вирусом в крови или ткани хозяина. В других осуществлениях хозяину ставили диагноз при титровании титра анти-ВИЧ антител в крови. В другом осуществлении соединения вводят, чтобы снизить или предупредить симптомы СПИДа (синдром приобретенного иммунного дефицита) у хозяина. В еще одном осуществлении соединения изобретения вводят хозяину при риске инфекции ВИЧ.
В другом осуществлении активное соединение проявляет активность против форм ВИЧ, резистентных к лекарственному средству, и, таким образом, проявляет сниженную перекрестную резистентность против современных одобренных противовирусных терапий. Фраза "активность против формы ВИЧ, устойчивой к лекарственному средству", означает, что соединение (или его пролекарство или фармацевтически приемлемая соль) активно против мутантного штамма с EC50 приблизительно менее чем 50, 25, 10 или 1 микромолярная концентрация. В одном осуществлении ненуклеозидный ингибитор обратной транскриптазы (NNRTI) демонстрирует EC50 (при молярной концентрации) против мутантного штамма ВИЧ приблизительно менее чем 5, 2,5, 1 или 0,1 микромолярные количества. В одном не ограничивающем осуществлении мутантный штамм ВИЧ имеет мутацию обратной транскриптазы по лизину 103 → аспарагин и/или тирозину 181 → цистеин.
3-Фосфоиндолы можно оценивать по их способности ингибировать активность обратной транскриптазы in vitro стандартными скрининговыми способами. Спектр активности, проявляемой любым определенным соединением, устанавливают при оценке соединения при исследовании, описанном в данном описании или другими одобренными исследованиями, известными специалистам в области анти-ВИЧ-соединений. Соединения обычно имеют EC50 менее 10-15 мкМ.
В одном осуществлении эффективность 3-фосфоиндолов оценивали с помощью ВИЧ-специфического твердофазного иммуноферментного анализа, ELISA p24. Эффективность лекарственного средства выражали как процент ингибирования антигена р24 ВИЧ в упомянутом быстром и чувствительном исследовании. В родственном осуществлении, подходящем для специальных экспериментов, эффективность анти-ВИЧ-соединения определяют с помощью "анализа снижения бляшек", при котором оценивают концентрацию соединения, необходимую, чтобы уменьшить количество бляшек вируса in vitro, в соответствии со способами, изложенными более подробно в заявке, на 50% (то есть EC50 соединения). В некоторых осуществлениях соединение имеет EC50 менее 15 или менее 10 микромолярного к наномолярному количеству in vitro.
VI. Комбинированная терапия или терапия с чередованием лекарственных средств
В некоторых осуществлениях соединение 3-фосфоиндола вводят в комбинации или при чередовании с одним или более другими анти-ретровирусными или анти-ВИЧ средствами. В одном осуществлении результатом введения двух или более таких средств в комбинации и/или при чередовании оказывается синергическое действие при ингибировании репликации ВИЧ. В другом осуществлении результатом введения двух или более таких средств в комбинации и/или при чередовании оказывается аддитивное действие при ингибировании репликации ВИЧ.
При комбинированной терапии эффективные дозировки двух и более средств вводят вместе, тогда как во время переменной терапии эффективную дозу каждого средства вводят последовательно. Дозировки зависят от скоростей всасывания, инактивации и выведения лекарственных средств, а также других факторов, известных специалистам в данной области. Величины доз также варьируют в зависимости от тяжести состояния, которое должны облегчить. Что касается любого отдельного индивидуума, специальные схемы приема и применения лекарственных средств следует корректировать в течение периода времени, чтобы удовлетворить потребности индивидуума и профессиональную оценку специалиста, который осуществляет введение и контроль применения композиций.
Устойчивость к лекарственному средству чаще всего возникает в результате мутации гена, который кодирует фермент, участвующий в цикле вирусной репликации, и обычно в случае ВИЧ, в генах или обратной транскриптазы, или протеазы. Установлено, что эффективность лекарственного средства против ВИЧ можно пролонгировать, увеличивать или восстанавливать введением соединения в комбинации или при чередовании со вторым, а необязательно третьим, противовирусным соединением, которое индуцирует другую(ие) мутацию(и) помимо мутации, выбранной основным лекарственным средством. Такие лекарственные комбинации одновременно снижают вероятность резистентности к любому одному лекарственному средству и любые ассоциированные токсические реакции. Альтернативно, фармакокинетика, биораспределение и другие параметры лекарственного средства можно изменять такой комбинированной терапией или терапией с чередованием лекарственных средств. Например, применение комбинации лекарственных средств позволяет назначать индивидуальное лекарственное средство в пределах такой комбинации в дозе более низкой, чем доза, которая потребуется, если лекарственное средство будут вводить в виде монотерапии. Подобным образом, когда лекарственные средства, которые таргетируют различные стадии цикла жизни вируса, комбинируют, существует возможность для потенцирования их действий. Кроме того, применение комбинаций лекарственных средств может снижать или устранять нежелательные побочные эффекты отдельного лекарственного средства, при этом еще продуцируя противовирусную активность. Вообще, комбинированная терапия является обычной терапией по сравнению с терапией с чередованием лекарственных средств, так как при комбинированной терапии имеют место многочисленные, одновременные воздействия на вирус.
Вторым противовирусным средством для лечения ВИЧ-инфекции может быть, например, протеазный ингибитор, ингибитор ВИЧ-интегразы, ингибитор хемокина или ингибитор обратной транскриптазы ("RTI"), последний из которых может быть или синтетическим нуклеозидным ингибитором обратной транскриптазы ("NRTI") или ненуклеозидным ингибитором обратной транскриптазы ("NNRTI"). В другом осуществлении, вторым или третьим соединением может быть аналог пирофосфата или ингибитор слияния-связывания. Список собранных данных по резистентности, полученных in vitro и in vivo для некоторых противовирусных соединений, имеется в Schinazi et al., Mutation in retroviral genes associated with drug resistance, International Antiviral News, 1997, 5(8).
В некоторых осуществлениях соединение индола вводят в комбинации и/или при чередовании с FTC (2',3'-дидезокси-3'-тиа-5-фторцитидин); 141W94 (ампренавир, Glaxo Wellcome, Inc.); вирамун (невирапин); рескриптор (делавирдин); DMP-266 (эфавиренз); DDI (2'3'-дидезоксиинозин); 3ТС (3'-тиа-2',3'-дидезоксицитидин); DDC (2',3'-дидезоксицитидин); абакавир (1592U89), который представляет собой (1S,4R)-4-[(2-амино-6-циклопропил-амино)-9Н-пурин-9-ил]-2-циклопентен-1-метанол сукцинат, тенофовир DF (виреад), D4T или AZT.
Другие примеры противовирусных средств, которые можно использовать в комбинации и/или при чередовании с соединениями, обсуждаемыми в заявке, без ограничений, включают в себя фоскарнет, карбовир, ацикловир, интерферон, ингибиторы слияния, такие как энфувиртид; и β-D-диоксолан-нуклеозиды, такие как β-D-диоксоланилгуанин (DXG), β-D-диоксоланил-2,6-диаминопурин (DAPD) и β-D-диоксоланил-6-хлорпурин (ACP). Интерфероны, которые можно использовать, включают в себя продукты альфа интерферон-2b фирмы Schering-Plough, интрон® А и ПЭГ-интрон™; и Со-Pegasus и PEGASYS (пегилированный интерферон альфа-2а) фирмы Hoffman La Roche. Комбинации, с которыми можно вводить 3-фосфоиндолы, включают в себя эпзиком (АВС+3ТС), тризивир (ABC+3TC+AZT), трувада (FTC+виреад) и комбивир (AZT+3TC).
Примеры протеазных ингибиторов, которые можно использовать в комбинации и/или при чередовании с соединениями, рассматриваемыми в заявке, без ограничений, включают в себя индинавир {1(1S,2R),5(S)}-2,3,5-тридезокси-N-(2,3-дигидро-2-гидрокси-1Н-инден-1-ил)-5-[2-[[(1,1-диметилэтил)амино]-карбонил]-4-(3-пиридинилметил)-1-пиперазинил]-2-(фенилметил)-D-эритро-пентоамид сульфат; Merck & Co., Inc.); нельфинавир (Agouron); ритонавир (Abbott Labs), саквинавир (Roche); ампренавир; атазанавир; фосампренавир; калетра; и DMP-450 {[4R-4(r-a,5-a,6-b,7-6)-гексагидро-5,6-бис(гидрокси)-1,3-бис(3-амино)фенил]метил-4,7-бис(фенилметил)-2Н-1,3-диазепин-2-он}-бисмезилат (Triangle Pharmaceuticals, Inc.).
Другие соединения, которые можно вводить в комбинации или при чередовании с фенилиндолом, чтобы повысить его противовирусные свойства, включают в себя (1S, 4R)-4-[2-амино-6-циклопропил-амино-9Н-пурин-9-ил]-2-циклопентен-1-метанол сукцинат (1592U89, аналог карбовира от GlaxoSmithKline); BILA 1906 (N-{1S-[[[3-[2S-{(1,1-диметилэтил)амино]карбонил}-4R-]3-пириндинилметил)тио]-1-пиперидинил]-2R-гидрокси-1S-фенилметил)пропил]амино]карбонил]-2-метилпропил}-2-хинолинкарбоксамид) (Bio Mega/Boehringer Ingelheim); BILA 2185 (N-(1,1-диметилэтил)-1-[2S-[[[2-2,6-диметил-фенокси]-1-оксоэтил]амино]-2R-гидрокси-4-фенилбутил]4R-пиридинилтио-2-пиперидин-карбоксамид) (Bio Mega/Boehringer Ingelheim); BM+51.0836 (производное триазолоизо-индолинона) и BMS 186318 (производное аминодиола, ингибитор протеазы ВИЧ-1) (Bristol-Myers Squibb); d4API (9-[2,5-дигидро-5-(фосфонометокси)-2-фуранил]-аденин) (Gilead); HBY097 (S-4-изопропоксикарбонил-6-метокси-3-[метилтио-метил]-3,4-дигидрохиноксалин-2(1Н)-тион); HEPT (1-[(2-гидрокси-этокси)метил]6-[фенилтио]-тимин); KNI-272 ((2S,3S)-3-амино-2-гидрокси-4-фенилмасляная кислота, содержащая трипептид); L-697593 (5-этил-6-метил-3-(2-фталимидо-этил)пиридин-2(1Н)-он); L-732524 (гидрокси-аминопентан амид, протеазный ингибитор ВИЧ-1) (Merck & Co.); L-697661 (3-{[(-4,7-дихлор-1,3-бензоксазол-2-ил)метил]амино}-5-этил-6-метил-пиридин-2(1Н)-он); L-FDDC ((-)-β-L-5-фтор-2',3'-дидезоксицитидин); L-FDOC ((-)-β-L-5-фтор-диоксолан цитозин); PFA (фосфоноформиат; "фоскарнет"; Astra); PMEA (9-(2-фосфонилметоксиэтил)аденин) (Gilead); PMPA ((R)-9-(2-фосфонилметокси-пропил)аденин) (Gilead); Ro 31-8959 (производное гидроксиэтиламина, ингибитор протеазы ВИЧ-1) (Roche); RPI-3121 (ингибитор пептидил-протеазы, 1-[(3S)-3-(н-альфа-бензилокси-карбонил)-1-аспарагинил)-амино-2-гидрокси-4-фенилбутирил]-н-трет-бутил-1-пролин амид); 2720 (6-хлор-3,3-диметил-4-(изопропенилоксикарбонил)-3,4-дигидрохиноксалин-2(1Н)тион); SC-52151 (гидроксиэтилмочевина изостер, протеазный ингибитор) (G.D. Searle); SC-55389A (гидроксиэтилмочевина изостер, протеазный ингибитор) (G.D. Searle)); TIBO R82150 ((+)-(5S)-4,5,6,7-тетрагидро-5-метил-6-(3-метил-2-бутенил)-имидазо-[4,5,1-jk]-[1,4]-бензодиазепин-2(1Н)-тион) (Janssen Pharmaceuticals); TIBO 82913 ((+)-(5S)-4,5,6,7-тетрагидро-9-хлор-5-метил-6-(3-метил-2-бутенил)имидазо[4,5,1-jk]-[1,4]-бензо-диазепин-2(1Н)-тион (Janssen Pharmaceuticals); TSAO-m3T ([2',5'-бис-О-(трет-бутилдиметилсилил)-3'-спиро-5'-(4'-амино-1',2'-оксатиол-2',2'-диоксид)]-β-D-пентофуранозил-N3-метил-тимин); U90152 (1-[3-[(1-метилэтил-амино)-2-пиридинил]-4[[5-[(метилсульфонил)амино]-1Н-индол-2-ил]карбонил]пиперазин); UC (производные тио-карбоксамида) (Uniroyal); UC-781 (N-[4-хлор-3-(3-метил-2-бутенилокси)фенил]-2-метил-3-фуранкарбо-тиоамид); UC-82 (N-[4-хлор-3-(3-метил-2-бутенилокси)фенил]-2-метил-3-тиофенкарботиоамид); VB 11328 (протеазный ингибитор, гидроксиэтил-сульфонамид) (Vertex/Glaxo Wellcome); XM 323 (протеазный ингибитор, циклическая мочевина) (Dupont Merck); и пенцикловир. В еще одном осуществлении, соединение индола согласно изобретению вводят в комбинации с протеазным ингибитором LG 1350.
Следующие лекарственные средства одобрены FDA или в настоящее время проходят клинические испытания для применения при лечении ВИЧ-инфекции, и поэтому, в одном осуществлении, их можно использовать в комбинации и/или при чередовании с соединениями данного изобретения.
Дополнительные лекарственные средства, проходящие клинические испытания, которые можно использовать в комбинации и/или при чередовании с 3-фосфоиндолами, включают в себя:
Следующие лекарственные средства одобрены FDA для применения при лечении осложнений ВИЧ-инфекции и СПИДа, которые можно использовать в комбинации и/или при чередовании с соединениями данного изобретения.
Некоторые продукты допущены к рассмотрению FDA как исследуемые новые лекарственные средства (IND) для лечения осложнений ВИЧ-инфекции и СПИДа. Поэтому, следующие лекарственные средства можно использовать в комбинации и/или при чередовании с соединениями данного изобретения.
- Триметрексат глюкуронат для лечения пневмонии Pneumocystis carinii у больных СПИДом, которые не могут переносить стандартные формы лечения.
- Ганцикловир для лечения цитомегаловирусного ретинита у больных СПИДом.
- Аэрозольный пентамидин для предупреждения пневмонии Pneumocystis carinii у больных СПИДом.
- Эритропоэтин для лечения анемии, ассоциированной с зидовудином.
- Атоваквион для лечения больных СПИДом с пневмонией Pneumocystis carinii, которые не чувствительны или не отвечают на триметоприм-сульфаметоксазол.
- Рифабутин для профилактики против комплексной бактериемии, вызванной Mycobacterium avium, у больных СПИДом.
- Вистид, внутривенный цидофовир, для ВИЧ-инфицированных субъектов с рецидивирующим цитомегаловирусным (CMV) ретинитом, который прогрессирует несмотря на лечение (Hoffmann-La Riche).
- Серостин, рекомбинантный гормон роста человека, полученный от млекопитающего, для лечения истощения, связанного со СПИДом (Serono Laboratories).
Обычно при терапии с чередованием лекарственных средств эффективную дозу каждого средства вводят последовательно. Во время комбинированной терапии, эффективные дозы двух или более средств вводят вместе. Вводимые дозы зависят от факторов, таких как скорости всасывания, биораспределения, метаболизма и выведения для каждого лекарственного средства, а также других факторов, известных специалистам в данной области. Следует отметить, что дозовые количества будут варьировать в зависимости от тяжести состояния, которое необходимо облегчить, возраста, веса и общего физического состояния субъекта, которому назначают лекарственное средство. Кроме того, понятно, что для любого определенного субъекта специальные схемы и применения лекарственного средства следует корректировать с течением времени в соответствии с ответом субъекта на лекарственное средство, потребности субъекта и профессиональной оценки специалиста, осуществляющего введение или контроль введения композиции. Примеры подходящих диапазонов доз для анти-ВИЧ соединений, включающих в себя нуклеозидные производные, например, такие как D4T, DDI и 3TC, или протеазные ингибиторы, подобные нельфинавиру и индинавиру, следует искать в научной литературе и справочнике по рецептуре для врачей. Предполагаемые диапазоны для эффективных дозировок соединений данного изобретения являются только руководством и не предназначены для ограничения сферы или применения изобретения.
Обсуждаемые комбинированная схема или схема чередования средств подходит для лечения и предупреждения ретровирусных инфекций и других родственных состояний, например, таких как СПИД-ассоциированный комплекс (ARC), устойчивая генерализованная лимфаденопатия (PGL), СПИД-ассоциированные неврологические состояния, анти-ВИЧ-антитело-позитивные и ВИЧ-позитивные состояния, саркома Капоши, тромбоцитопеническая пурпура и оппортунистические инфекции. Кроме того, названные соединения и препараты можно использовать профилактически, чтобы предупредить или замедлить прогрессирование клинических проявлений заболевания у индивидуумов, которые являются анти-ВИЧ-антитело- или ВИЧ-антиген-позитивными, или которые подверглись действию ВИЧ.
VII. Фармацевтические композиции
Соединения индола согласно данному изобретению, при необходимости, необязательно, можно вводить субъекту в комбинации или при чередовании с другим анти-ВИЧ или противоретровирусным средством и/или с фармацевтически приемлемым носителем, разбавителем или наполнителем. В одном осуществлении, субъекта, инфицированного ВИЧ, можно лечить введением такому субъекту эффективного количества производного индола, его соли, пролекарства, стереоизомера или таутомера в присутствии фармацевтически приемлемого носителя или разбавителя. Субъектам с поливалентной устойчивостью к лекарственным средствам, соединение оксо-пиримидина вводят или отдельно или в комбинации с одним или более другими противоретровирусными средствами или анти-ВИЧ-средствами. Активные соединения можно вводить любым подходящим способом, например, перорально, парентерально, энтерально, внутривенно, внутрикожно, подкожно, чрескожно, трансдермально, интраназально, местно или с помощью ингаляционной терапии, и они могут быть в твердой, жидкой или парообразной форме.
Активное соединение(я) заключают в фармацевтически приемлемый носитель, разбавитель или наполнитель в количестве, достаточном, чтобы доставить пациенту терапевтически эффективное количество активного соединения для того, чтобы ингибировать репликацию вируса in vivo, особенно репликацию ВИЧ, не вызывая серьезных токсических реакций у субъекта, которого лечат. Выражение "количество ингибитора" означает количество активного ингредиента, достаточное, чтобы остановить вирусную репликацию, которую оценивают, например, исследованием, таким как исследования, упомянутые в заявке.
Доза соединения индола для всех упомянутых состояний соответствует диапазону приблизительно от 0,1 до 100 мг/кг веса тела на день, или от 1 до 75 мг/кг веса тела на день, и даже обычно приблизительно от 1 до 20 мг/кг веса тела на день. Диапазон эффективных доз фармацевтически приемлемых производных рассчитывают на основании веса исходного соединения производного индола, которое вводят. Если преобразованное соединение само проявляет активность, тогда эффективную дозу можно установить, как описано выше, используя вес производного или другие способы, известные специалистам в данной области.
Соединения обычно вводят в единицах любой подходящей лекарственной формы, без ограничений, включающей в себя форму, содержащую приблизительно от 7 до 3000 мг или приблизительно от 70 до 1400 мг или более типично приблизительно от 25 до 1000 мг активного ингредиента на единицу лекарственной формы. Например, пероральная доза приблизительно от 50 до 1000 мг является общепринятой.
Идеально, активный ингредиент вводят, чтобы достигнуть в плазме пиковых концентраций активного соединения приблизительно от 0,02 до 70 мкМ и обычно приблизительно от 0,5 до 10 мкМ. Например, этого можно достигнуть внутривенной инъекцией от 0,1 до 25% раствора активного ингредиента, необязательно в физиологическом растворе, или введенного в виде ударной дозы активного ингредиента. Следует понимать, что для любого определенного субъекта, специальную схему приема лекарственного средства со временем нужно корректировать, чтобы удовлетворить индивидуальные потребности. Концентрации, приведенные в заявке, являются только показательными и не предназначены для ограничения объема или практического применения заявленной композиции. Активный ингредиент можно вводить весь сразу или можно разделять на ряд меньших доз, которые вводят в различные интервалы времени.
Одним способом введения активного соединения является пероральный. Пероральные композиции обычно включают в себя инертный разбавитель или съедобный носитель. Их можно заключать в желатиновые капсулы, прессовать в таблетки или доставлять в жидкой форме. Для перорального терапевтического введения, активное соединение можно заключать в наполнители или готовить в виде твердых дисперсий или твердых растворов и использовать в виде таблеток, пастилок или капсул. Термин "твердая дисперсия" означает твердое состояние, содержащее, по крайней мере, два компонента, где один компонент диспергирован более или менее равномерно по всему второму компоненту. Термин "твердый раствор" означает твердое состояние, включающее в себя, по крайней мере, два компонента, которые химически или физически интегрированы с образованием однородного продукта. Твердый раствор является более приемлемым по сравнению с твердой дисперсией, так как он легче образует жидкий раствор при контакте с соответствующей жидкой средой, таким образом, увеличивая биодоступность лекарственного средства. Фармацевтически совместимые связующие средства и/или адъювантные вещества также можно включать в виде части такой композиции.
Таблетки, пилюли, капсулы, пастилки и тому подобное могут содержать любой из следующих ингредиентов и соединений подобной природы: связующее вещество, такое как микрокристаллическая целлюлоза, трагакантовая камедь или желатин; наполнитель, такой как крахмал или лактоза; дезинтегрирующее средство, такое как альгиновая кислота, примогель или кукурузный крахмал; смазка, такая как стеарат магния или стероты; вещество, обеспечивающее скольжение, такое как коллоидный диоксид кремния; подсластитель, такой как сахароза сахарина; и вкусовое вещество, такое как перечная мята, метил-салицилат или апельсиновый ароматизатор. Если лекарственная стандартная форма представляет собой капсулу, она может содержать жидкий носитель, такой как жирное масло помимо любого из веществ, приведенных выше. Кроме того, лекарственные стандартные формы могут содержать различные другие вещества, которые изменяют физическую форму лекарственной единицы, например, такие как покрытия сахаром, щеллак и другие энтерические вещества.
Соединения индола можно вводить в виде компонента эликсира, суспензии, сиропа, облаток, жевательной резинки и тому подобного. Сироп может содержать сахарозу как подсластитель, консерванты, красители, окрашивающие вещества и вкусовые вещества помимо активных соединений.
Активные соединения и их фармацевтически приемлемые соли или пролекарства можно смешивать с другими активными веществами, которые не ухудшают желаемое действие, или с веществами, которые дополняют желаемый эффект, такими как антибиотики, противогрибковые средства, противовоспалительные средства, протеазные ингибиторы или другие нуклеозидные или ненуклеозидные противовирусные средства. Растворы или суспензии, используемые для парентерального, внутрикожного, подкожного или местного применения, могут включать в себя следующие компоненты: стерильный разбавитель, такой как вода для инъекции, физиологический раствор, нелетучие масла, полиэтиленгликоли, глицерин, пропиленгликоль или другие синтетические растворители; противобактериальные средства, такие как бензиловый спирт или метил-парабены; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатообразующие средства, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты, и средства для корректировки тонуса, такие как хлорид натрия или декстроза. Парентеральные препараты обычно включают в себя стерильную воду, и могут быть заключены в ампулы, шприцы одноразового применения, или во флаконы с многократной дозой, сделанные из стекла или пластика.
Если вводят внутривенно, типичными носителями являются физиологический раствор, забуференный фосфатом физиологический раствор (PBS), раствор глюкозы или смешанный раствор, содержащий глюкозу и физиологический раствор. Если введение осуществляют подкожно, например, такое как с применением пластыря или мази, ассоциированный носитель может содержать средство, усиливающее проникновение и/или подходящее смачивающее вещество, которое не является вредным для кожи. Если ингаляция или инсуффляция оказывается требуемым способом введения, тогда композиция данного изобретения включает в себя соединение в виде раствора, суспензии или сухого порошка, которые можно доставлять через ротовое и/или носовое отверстие.
Липосомные суспензии, которые включают в себя липосомы, нацеленные на инфицированные клетки, с моноклональными антителами к вирусным антигенам, также являются общепринятыми в качестве фармацевтически приемлемых носителей. Липосомные суспензии можно получать по способам, известным специалистам в данной области, например, которые описывают в патенте США № 4522811, который включен в заявку цитированием в его полном объеме. Например, липосомные препараты можно получать растворением соответствующего липида(ов), такого как стеароил-фосфатидил-этаноламин, стеароил-фосфатидил-холин, арахадоил-фосфатидил-холин и холестерин, в неорганическом растворителе, который позднее выпаривают, оставляя после него тонкую пленку высушенного липида на поверхности контейнера. Водный раствор активного соединения или его соли или пролекарства затем вводят в контейнер. Контейнер вращают, чтобы снять липидное вещество с его стенок и диспергировать липидные агрегаты, таким образом, формируя липосомную суспензию.
VIII. Способы получения активных соединений
Общие схемы
Схема 1:
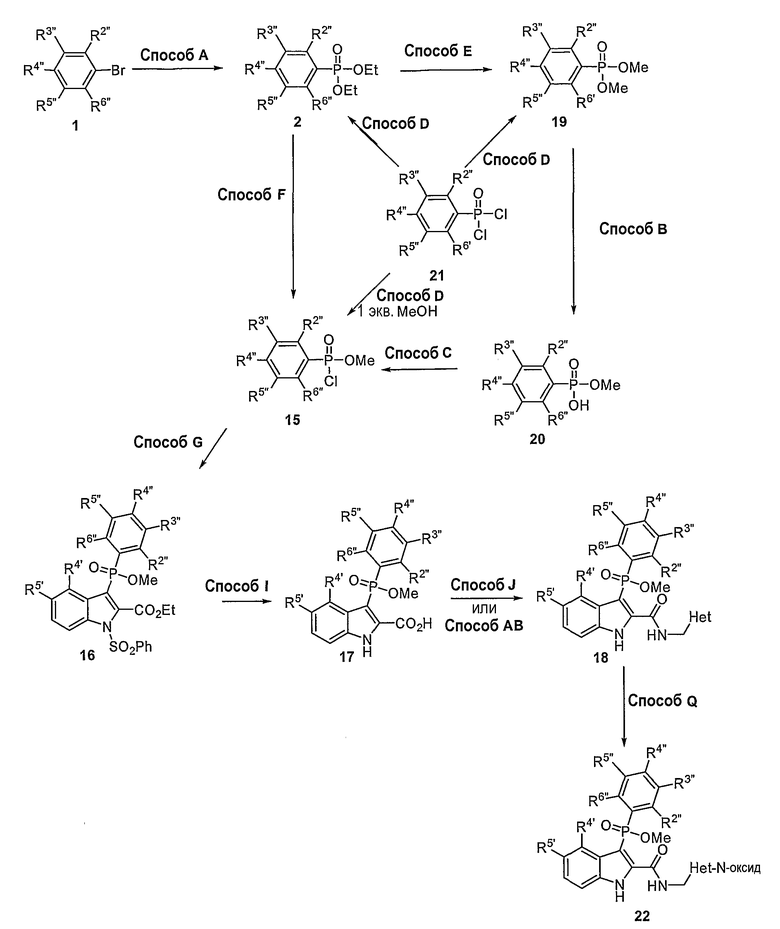
Схема 2:
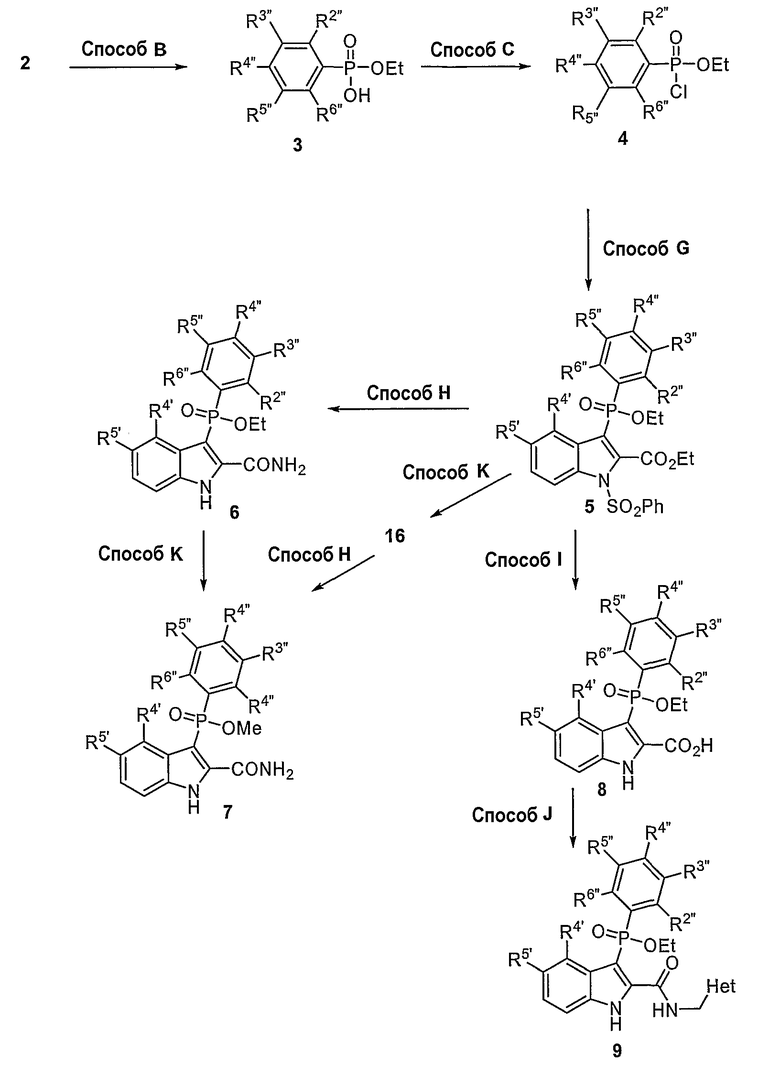
Схема 3:
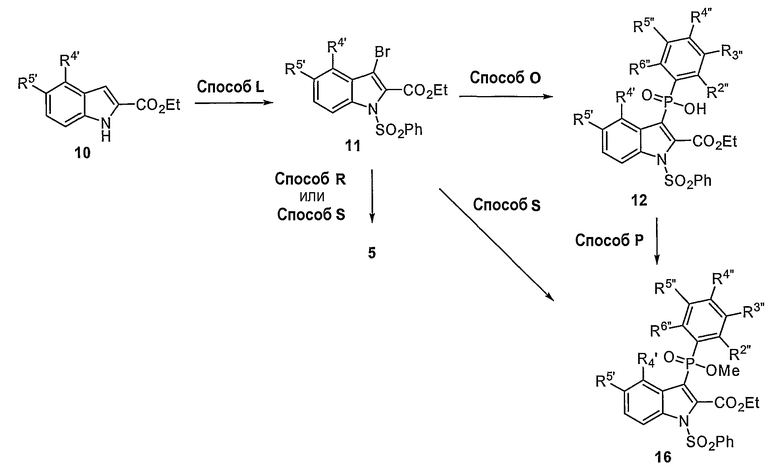
Схема 4:

Схема 5:
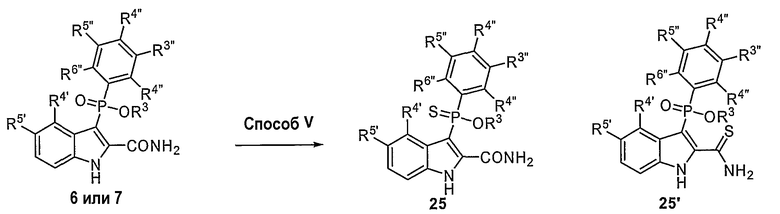
Схема 6:
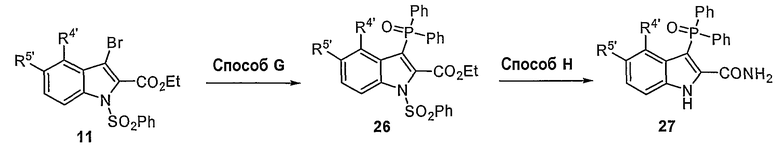
Схема 7:
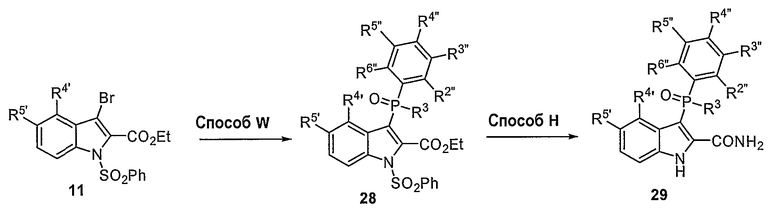
Схема 8:
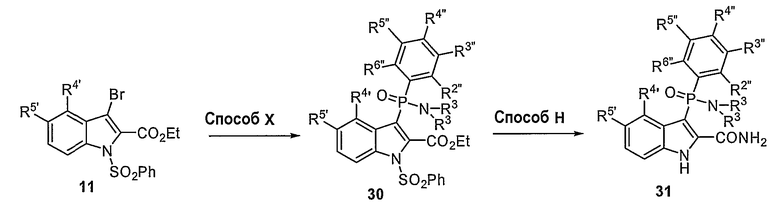
Схема 9:
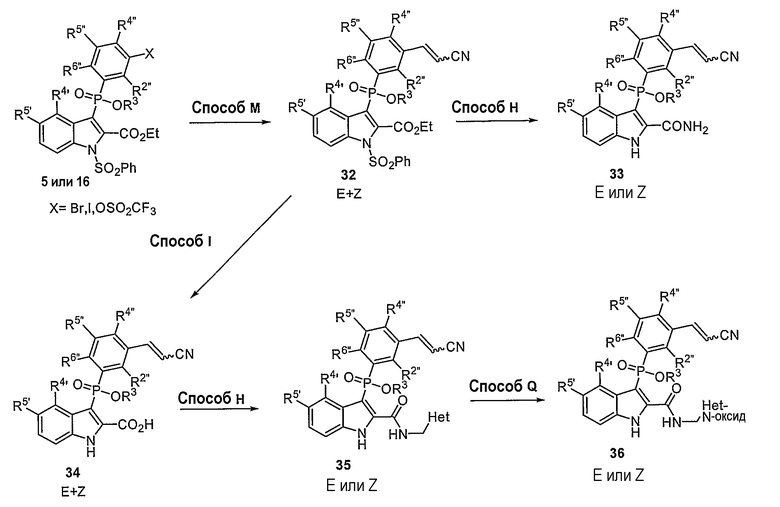
Схема 10:
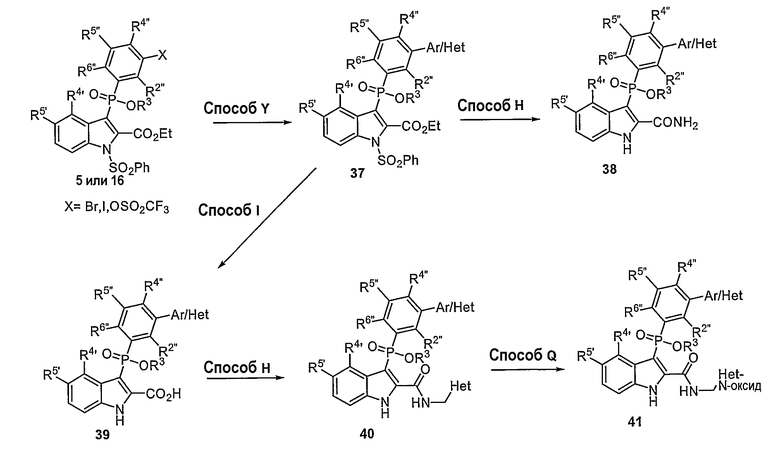
Подробно описанные схемы
Схема 11: N-разветвленные гетероциклы
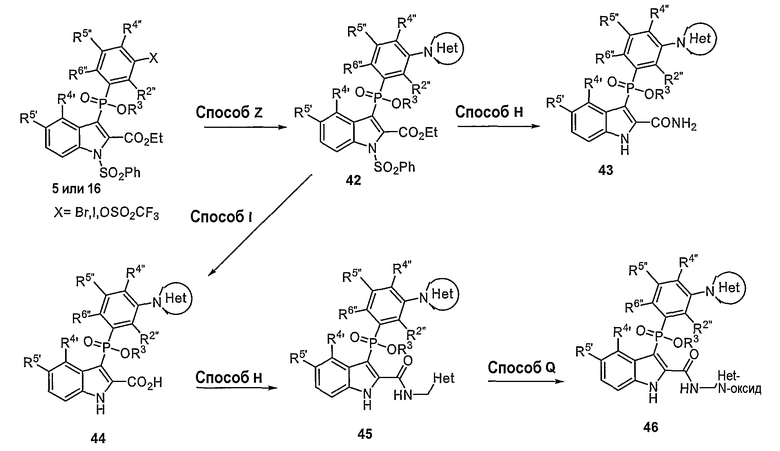
Схема 12: Фосфинатные гетероциклы
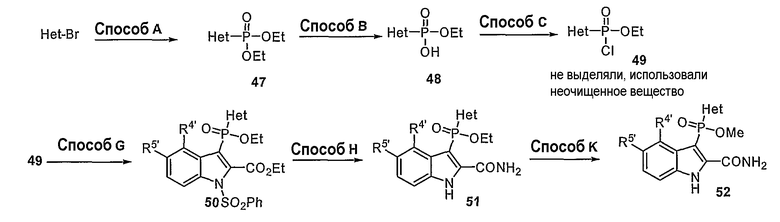
Схема 13: Алкил/алкенил/алкинил-фосфинаты
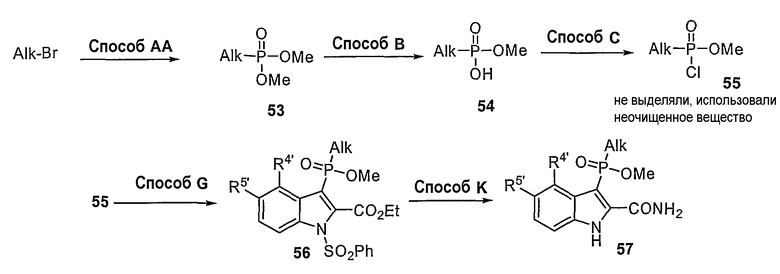
Схема 14: Алкил-фосфинаты
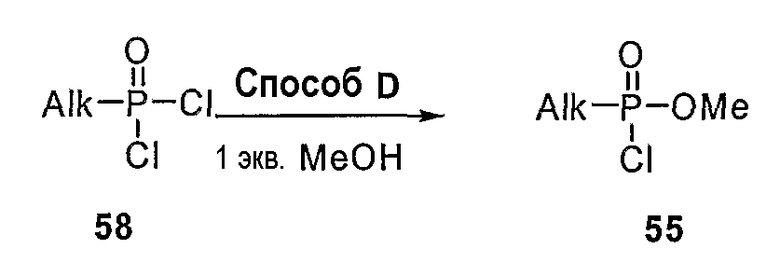
Схема 15: Алкил-метил-карбоксамиды
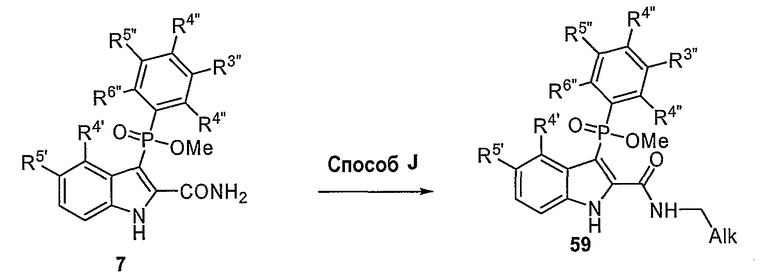
Схема 16: Фосфиновые кислоты
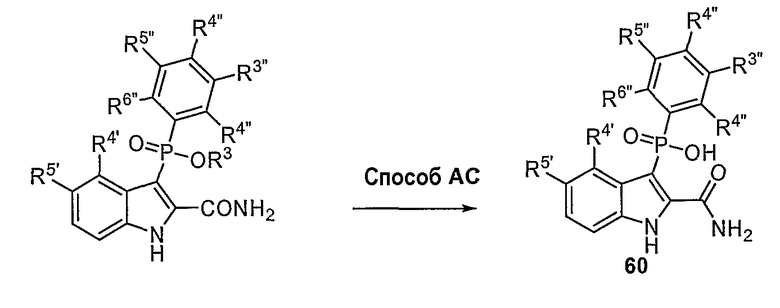
Способы
Следующее представляет собой описания методологий, используемых в предшествующих схемах. Номера, обозначенные жирным шрифтом, соответствуют пронумерованным соединениям, приведенным в схемах 1-16. Способы A, B, C, D, F, L, N, T, U и AA известны всем специалистам в области создания таких общих классов соединений, но они приспособлены для получения специфических соединений данного изобретения. Это также верно для способов H, I, J, M, P, Q, Y, Z, AB и AC. Способы E, G, K, O, R, S, W, V и X являются новыми способами получения соединений изобретения.
СПОСОБ А
Бромбензол 1 (1 экв.) перемешивали с диэтилфосфином (1,1 экв.) и триэтиламином (1,1 экв.) в трубчатом автоклаве, и смесь дегазировали с N2 приблизительно в течение 15 минут. Затем добавляли тетракис палладий (0,05 экв.), и смесь перемешивали под давлением приблизительно при 85°С в течение ночи. На следующее утро Et2O добавляли в реакционную смесь и смесь фильтровали. Фильтрат выпаривали, и неочищенное вещество очищали хроматографией на силикагеле (элюент: петролейный эфир/EtOAc от 8/2 до 6/4). Альтернативно, реакцию проводили, используя 10 объемов 1,2-диэтоксиэтана в тех же условиях.
СПОСОБ В
Все реагенты (1 экв. диэтилфосфоната 2 или диметилфосфоната 19, 6 экв. гидроксида натрия и этанол или метанол (3 мл/ммоль)) перемешивали при комнатной температуре приблизительно в течение 5 часов. Затем этанол (или метанол) выпаривали в вакууме, и смесь подкисляли HCl 2,5 н., чтобы получить рН 1. Затем смесь насыщали NaCl и экстрагировали этилацетатом. Объединенные органические слои высушивали над Na2SO4, фильтровали и концентрировали, чтобы получить требуемые продукты 3 или 20.
СПОСОБ С
Соединение 20 или 3 (1,2 экв.) перемешивали при комнатной температуре в атмосфере N2 с тионилхлоридом (3,6 экв.), дихлорметаном (5 мл/ммоль) и несколькими каплями диметилформамида приблизительно в течение 5 часов. Брали аликвоту и помещали в сухой метанол и Et3N, чтобы контролировать реакцию. Когда реакция завершалась, дихлорметан и тионилхлорид, выпариваемые одновременно с толуолом, выпаривали в вакууме, чтобы получить масло, которое хранили в атмосфере N2.
СПОСОБ D
К раствору арилфосфонилдихлорида 21 (1 мл, 6,35 ммоль) в безводном дихлорметане (25 мл) по каплям добавляли этанол или метанол (1,12 мл, 19,04 ммоль) приблизительно при 0°С с последующим добавлением триэтиламина (2,65 мл, 19,04 ммоль). Реакционную смесь перемешивали при комнатной температуре приблизительно в течение 2 часов, и затем промывали раствором HCl 1 н. (50 мл). Водный слой экстрагировали дихлорметаном. Объединенные органические фазы высушивали и концентрировали при пониженном давлении. Неочищенное масло очищали методом хроматографиии на силикагеле (элюент: C6H12/EtOAc 6/4), чтобы получить диметиларилфосфонат 19 или диэтиларилфенилфосфонат 2.
СПОСОБ Е
Диэтиларилфосфонат 2 (1 экв.) перемешивали в атмосфере N2 при комнатной температуре с бромтриметилсиланом (10 экв.) и дихлорметаном (5 мл/ммоль) приблизительно в течение 5 часов. Затем бромтриметилсилан и дихлорметан выпаривали, чтобы получить желтое масло. Затем оксалилхлорид, диметилформамид и дихлорметан добавляли в атмосфере N2, и смесь перемешивали при комнатной температуре в течение ночи, после этого оксалилхлорид и растворители выпаривали. Масло в растворе дихлорметана перемешивали и оставляли для охлаждения приблизительно до 0°С и добавляли этанол или метанол (1,12 мл, 19,04 ммоль) в атмосфере N2 с последующим добавлением по каплям триэтиламина. Смесь потом нагревали до комнатной температуры. Растворитель выпаривали, и полученный продукт очищали методом хроматографии на силикагеле (элюент: CH2Cl2/EtOAc : 8/2), чтобы получить соединение 14.
СПОСОБ F
К перемешиваемому раствору диэтиларилфосфоната 2 (1 экв.) в дихлорметане (5 мл/ммоль) добавляли бромтриметилсилан (5 экв.) при комнатной температуре в атмосфере N2. Приблизительно после 3-х часов перемешивания при комнатной температуре растворитель выпаривали и добавляли дихлорметан (5 мл/ммоль), несколько капель диметилформамида и оксалилхлорид (2,5 экв.). Полученную смесь перемешивали при комнатной температуре в течение ночи, растворитель выпаривали, чтобы получить масло. Раствор масла (1,2 экв.) в простом диэтиловом эфире (3 мл/ммоль) перемешивали и охлаждали приблизительно до -17°С, после этого безводный метанол (1,2 экв.) добавляли по каплям, чтобы удалить компоненты двойного присоединения и триэтиламин. Полученную смесь нагревали до комнатной температуры, перемешивали приблизительно в течение 1 часа, и затем фильтровали на автоматическом устройстве в атмосфере N2, чтобы удалить соли триэтиламина. Растворитель выпаривали, чтобы получить соединение 15.
СПОСОБ G
n-BuLi (2,5 М в гексане, 1,2 экв.) добавляли по каплям к перемешиваемому и охлажденному (приблизительно до -90°С) раствору броминдола 11 (1 экв.) в безводном THF (10 мл/ммоль) в атмосфере N2. После содержания раствора приблизительно при -90°С приблизительно в течение 5 минут, соответствующий хлорфосфорный реагент 15, 4 или хлорангидрид дифенилфосфоновой кислоты (1,2 экв.) добавляли по каплям к раствору при той же самой температуре. Реакционную смесь оставляли для медленного нагревания приблизительно до -40°С (контролировали TLC; ТСХ, элюент CH2Cl2/ETOAc 9/1). Затем добавляли воду. Экстракция этилацетатом, высушивание и выпаривание давали неочищенное масло, которое очищали хроматографией на силикагеле, чтобы получить соединение 16, 5 или 26.
СПОСОБ Н
Перемешиваемый и охлажденный (приблизительно до 0°С) раствор соединения 5, 16, 26, 28 или 30 в метаноле в трубчатом автоклаве насыщали газом NH3 приблизительно в течение 10 минут. Затем смесь перемешивали приблизительно при 50°С в течение ночи, и после контроля методом ТСХ избыток аммиака и метанола выпаривали в вакууме, и неочищенное вещество очищали методом хроматографии на силикагеле, чтобы получить карбоксамид 6, 7, 27, 29 или 31.
СПОСОБ I
Гидрооксид лития (14 экв.) добавляли к перемешиваемому раствору соединения 16 или 5 в тетрагидрофуране (20 мл/ммоль) и воде (20 мл/ммоль). Полученную смесь затем перемешивали при комнатной температуре и контролировали с помощью ТСХ. Если необходимо, эквиваленты гидроксида лития добавляли до тех пор, пока реакция не завершалась. Затем THF выпаривали, и HCl (1 н.) добавляли, чтобы получить рН 1. Водный слой экстрагировали этилацетатом, и объединенные органические фазы высушивали, фильтровали и концентрировали при пониженном давлении, чтобы получить соединение 17 или 8.
СПОСОБ J
Соединение 17 или 8 (1 экв.) перемешивали с дихлорметаном (20 мл/ммоль) или DMF и добавляли 1-гидроксибензотриазол (1 экв.) с последующим добавлением EDCI (1 экв.), за которым следовало добавление амина (1 экв.). Полученную смесь перемешивали при комнатной температуре в течение ночи. На следующее утро смесь промывали водой (до рН 5-6), и органические слои высушивали, фильтровали и концентрировали при пониженном давлении. Полученное масло очищали методом хроматографии на силикагеле (элюент: CH2Cl2/EtOAc), чтобы получить порошок 18 или 9.
СПОСОБ К
В микроволновой трубке соединение 5 или 6 (1 экв.) перемешивали с DMF (5 мл/ммоль) и добавляли TMSBr (5 экв.). Трубку нагревали при облучении микроволнами при пониженном давлении приблизительно при 60°С (максимальная мощность 100 Вт, устройство для обнаружения СЕМ) приблизительно в течение 50 минут. DMF выпаривали в вакууме, и смесь помещали в трубчатый автоклав. Триметилфосфит (4 мл/ммоль) добавляли и смесь перемешивали и нагревали приблизительно при 90°С в течение ночи. Затем смесь охлаждали в ледяной водной бане и добавляли по каплям HCl (1 н.). Смесь экстрагировали этилацетатом, и объединенные органические слои промывали HCl (1 н.) до тех пор, пока не оставалось никакого HP(OMe)2. Затем полученное вещество высушивали, фильтровали и концентрировали при пониженном давлении, чтобы получить масло, и полученное масло очищали хроматографией на силикагеле, чтобы получить соединение 16 или 7.
СПОСОБ L
К перемешиваемому и охлажденному (приблизительно до 0°С) раствору этил индол-2-карбоксилата 10 (1 экв.) в DMF (2 мл/ммоль) в атмосфере N2 добавляли порциями NaH (60% в масле, 1,2 экв.). Когда выделение газа прекращалось, добавляли бензолсульфонилхлорид (1,2 экв.). Реакционную смесь перемешивали приблизительно в течение 1 часа (контроль посредством ТСХ, элюент - дихлорметан); затем осторожно добавляли небольшое количество воды, и DMF выпаривали. Неочищенный остаток растворяли в этилацетате и промывали водой или солевым раствором. После высушивания и выпаривания растворителей, соединение очищали хроматографией на силикагеле (элюент: C6H12/EtOAc от 9/1 до 7/3), чтобы получить этил 1-фенилсульфонилиндол-2-карбоксилат.
К перемешиваемому раствору этил 1-фенилсульфонилиндол-2-карбоксилата (1 экв.) в DMF (2,5 мл/ммоль) в атмосфере N2 добавляли раствор брома (4 экв.) в DMF (0,5 мл/ммоль). Реакционную смесь перемешивали при комнатной температуре приблизительно в течение 4 часов, вслед за этим добавляли воду, и смесь экстрагировали дихлорметаном (×3). Органический слой промывали насыщенным раствором Na2SO5, высушивали и выпаривали, чтобы получить неочищенное желтое масло. Очистка хроматографией на силикагеле (элюент: C6H12/EtOAc 9/1) давала 3-бромированный индол 11.
СПОСОБ М
Смесь 5 или 6 (1 экв.), акрилонитрила (10 экв.), ацетата палладия (20% моль), триэтиламина (1 экв.) и три-орто-толилфосфина (1 экв.) в дегазированном ацетонитриле (30 мл/ммоль) перемешивали и нагревали при облучении микроволнами в трубчатом автоклаве приблизительно в течение 45 минут. Затем добавляли воду, и водный слой экстрагировали дихлорметаном. Объединенные органические слои высушивали и концентрировали, и очищали хроматографией на силикагеле (элюент: петролейный эфир/EtOAc 8/2), чтобы получить соединение 32 в виде смеси энантиомеров Е и Z (которые разделяли методом препаративной ВЭЖХ).
СПОСОБ N
Бромбензол 1 (1 экв.), диметилформамид (1 мл/ммоль), триэтиламин (3 экв.) и соль анилиния* (1,25 экв.) помещали в трубчатый автоклав и дегазировали N2 приблизительно в течение 15 минут. Затем добавляли тетракис палладий, и полученную смесь перемешивали приблизительно при 85°С в течение ночи, после этого растворитель выпаривали и добавляли воду, чтобы достигнуть рН приблизительно 5-6. Смесь подщелачивали NaHCO3 до тех пор, пока не достигали рН 8, и потом экстрагировали диэтиловым эфиром. Водный слой подкисляли HCl (1 н.), чтобы получить рН 1 и экстрагировали этилацетатом. Объединенные органические слои высушивали, фильтровали и концентрировали при пониженном давлении, чтобы получить соединение 14.
*Соль анилиния синтезировали по способу Montchamp et al., (J. Am. Chem. Soc., 2001, 123, 510-511).
СПОСОБ О
Тетраметилортосиликат (1,2 экв.) добавляли к перемешиваемому раствору соединения 14 (1,2 экв.) в толуоле (4 мл/ммоль) в атмосфере N2. Полученную смесь нагревали с обратным холодильником приблизительно в течение 1,5 часов, и затем охлаждали до комнатной температуры. Затем смесь дегазировали с N2 перед добавлением триэтиламина (3,3 экв.), броминдола 11 (1 экв.) и тетракис палладия (0,05 экв.). Смесь перемешивали приблизительно при 100°С в течение периода с субботы до понедельника (приблизительно 48 часов), вслед за этим реакционную смесь охлаждали до комнатной температуры и добавляли воду, чтобы получить рН приблизительно 8-9. Смесь затем экстрагировали этилацетатом, и органические фазы промывали KHSO4 (1 н.), насыщенным NaCl. Затем полученное вещество высушивали, фильтровали и концентрировали при пониженном давлении, чтобы получить масло, которое очищали хроматографией на силикагеле (элюент: CH2Cl2/MeOH), чтобы получить соединение 12.
СПОСОБ Р
К перемешиваемому раствору соединения 12 (1 экв.) в метаноле (25 мл/ммоль) добавляли триметилсилилдиазометан (13 экв.) в нескольких порциях при комнатной температуре в атмосфере N2. Полученную смесь перемешивали в течение ночи, после этого добавляли воду, и метанол выпаривали при пониженном давлении. Потом NaHCO3 добавляли, чтобы достигнуть рН 8, и смесь экстрагировали этилацетатом. Органические фазы высушивали, фильтровали и концентрировали при пониженном давлении. Неочищенное вещество очищали хроматографией на силикагеле (элюент: C6H12/EtOAc), чтобы получить соединение 16.
СПОСОБ Q
Соединение 18 растворяли в хлороформе (или в CH2Cl2) при перемешивании при комнатной температуре; добавляли м-хлорпероксибензойную кислоту, и реакционную смесь оставляли для перемешивания в течение ночи (приблизительно 15 часов). Затем смесь разбавляли дихлорметаном и экстрагировали смесью насыщенного K2CO3/H2O (1/3). Водный слой экстрагировали три раза дихлорметаном. Объединенные органические слои высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении (ТСХ: дихлорметан/метанол = 9/1). Неочищенный продукт очищали хроматографией на силикагеле, чтобы получить соединение 22.
СПОСОБ R
В микроволновой запаянной трубке соединения 11 (1 экв.) и 23 (1,1 экв.) добавляли к толуолу (8 мл/ммоль) и триэтиламину (3,3 экв.) и дегазировали с N2 приблизительно в течение 10 минут. Затем добавляли Pd(PPh3)2, и трубку нагревали при облучении микроволнами при давлении приблизительно при 120°С (максимальная мощность 200 Вт, устройство для обнаружения СЕМ) приблизительно в течение 30 минут. Реакцию контролировали с помощью ТСХ, и сосуд нагревали приблизительно в течение 30 минут, если необходимо. Растворитель выпаривали, и неочищенный продукт очищали методом хроматографии на силикагеле (элюент: C6H12/EtOAc : 8/2), чтобы получить соединение 5.
СПОСОБ S
В микроволновой запаянной трубке соединения 11 (1 экв.) и 24 (2 экв.) добавляли к толуолу (8 мл/ммоль), и затем дегазировали с N2 приблизительно в течение 10-минутного периода времени. Потом добавляли Pd(OAc)2 приблизительно в 20% растворе, и трубку нагревали при облучении микроволнами при давлении приблизительно при 150°С (максимальная мощность 200 Вт, устройство для обнаружения СЕМ) приблизительно в течение 45 минут. Реакцию контролировали с помощью ТСХ и, если любое исходное вещество присутствовало, сосуд нагревали приблизительно в течение еще 45 минут приблизительно при 170°С. Затем добавляли HCl (1 н.) (8 мл/ммоль), и раствор экстрагировали этилацетатом. Объединенные органические слои высушивали, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали методом хроматографии на силикагеле (элюент: петролейный эфир/EtOAc : 1/1), чтобы получить соединение 5 или 16.
Альтернативно, реакцию проводили приблизительно при 150°С в ксилоле приблизительно в течение 5 часов.
СПОСОБ Т
Пиридин (1 экв.) осторожно добавляли к энергично перемешиваемому раствору алкилхлорформиата (1 экв.) и арилфосфиновой кислоты (1 экв.) в дихлорметане (2 мл/ммоль) при комнатной температуре. Как только прекращалось выделение газа, раствор кипятили с обратным холодильником приблизительно в течение 15 минут, а затем оставляли охлаждаться до комнатной температуры. Раствор вливали в 0,1 М хлористоводородную кислоту (1 мл/ммоль), и органический слой отделяли. После промывания водой и высушивания над Na2SO4, растворитель удаляли в вакууме, чтобы получить соединение 23.
СПОСОБ U
Алкил- или арилбромид (0,15 моль) добавляли по каплям к смеси магния (3,6 г) и сухого тетрагидрофурана (40 мл) в атмосфере N2 приблизительно при 50°С. После описанного добавления реакционную смесь перемешивали приблизительно при 50°С в течение дополнительных 1-2 часов, чтобы позволить завершиться реакции. Затем смесь добавляли по каплям к раствору триэтилфосфита (0,1 моль) и THF (25 мл) при температуре от 40°С до 50°С в атмосфере N2 и перемешивали приблизительно в течение 3 часов приблизительно при 50°С. После удаления растворителя при пониженном давлении неочищенный продукт отгоняли из полутвердого остатка в вакууме, чтобы получить соединение 24.
СПОСОБ V
Соединение 6 или 7 (1 экв.) и реагент Лавессона (Lawesson) (4 экв.) нагревали в толуоле (10 мл/ммоль) приблизительно при 90°С в атмосфере N2 в трубчатом автоклаве. За реакцией следили с помощью ТСХ и нагревание продолжали до тех пор, пока не оставалось никакого исходного вещества (приблизительно 5,5 часов). Неочищенный раствор фильтровали, и фильтрат выпаривали досуха и очищали методом хроматографии на силикагеле, чтобы получить соединение 25 и соединение 25'.
СПОСОБ W
К перемешиваемому и охлажденному (приблизительно до -90°С) раствору броминдола 11 (1 экв.) добавляли по каплям н-бутиллитий (1,2 экв.) в атмосфере N2. Приблизительно через 10 минут бензолфосфонилдихлорид 21 (1,1 экв.) в тетрагидрофуране (15 мл/ммоль) добавляли по каплям при температуре приблизительно -70°С, и температуру потом повышали приблизительно до -90°С и поддерживали приблизительно в течение 15 минут. За этим следовало добавление бромида метилмагния (1,1 экв.), и смесь оставляли для нагревания приблизительно до -40°С приблизительно в течение 1 часа, после этого смесь гасили водой и экстрагировали этилацетатом, потом дихлорметаном. Органический слой высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали методом хроматографии на силикагеле (элюент: CH2Cl2/AcOEt : от 9/1 до 7/3), чтобы получить соединение 28.
СПОСОБ Х
Диметиламин (1 экв.) добавляли по каплям к перемешиваемому и охлажденному (приблизительно до -55°С) раствору дихлорангидрида фенилфосфоновой кислоты 21 (1 экв.) в диэтиловом эфире (1,5 мл/ммоль). Затем добавляли триэтиламин (1 экв.) и смесь оставляли для нагревания до комнатной температуры. Смесь затем фильтровали, в фильтрат выпаривали, чтобы получить масло/смесь. Чтобы масло/смесь отделить от (дихлорангидрид)фенилфосфоновой кислоты, масло/смесь растворяли в EtOAc и дважды промывали раствором HCl рН 4-5. Органические фазы высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении, чтобы получить масло. Затем н-бутиллитий (1,2 экв.) добавляли по каплям к перемешиваемому и охлажденному (приблизительно до -80°С) раствору броминдола 11 (1 экв.) в тетрагидрофуране (5 мл/ммоль) в атмосфере N2. В конце добавления смесь нагревали приблизительно до -60°С, и тетрагидрофуран (1,2 экв.; 3 мл/ммоль) добавляли по каплям к маслу. Потом смесь медленно нагревали приблизительно до -10°С, и реакцию гасили водой (8 мл/ммоль). HCl (1 н.) добавляли, чтобы привести к рН приблизительно 5, и растворитель выпаривали в вакууме. Водную фазу экстрагировали этилацетатом, и объединенные органические слои промывали солевым раствором, высушивали над Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали методом хроматографии на силикагеле (элюент: C6H12/EtOAc : от 9/1 до 0/10), чтобы получить соединение 30.
СПОСОБ Y Образование поперечных связей по Suzuki
Pd(PPh3)4 (10% мас.), раствор Na2CO3 (6 экв.) в H2O (2 М) и раствор арил-, алкил- или гетероарилбороновой кислоты (2 экв.) в EtOH (0,3 М) добавляли к перемешиваемому раствору 5 или 16 (имеющим галогеновый или трифталатный заместитель) в дегазированном толуоле в атмосфере N2. Реакционный сосуд затем нагревали при облучении микроволнами приблизительно при 110°С до тех пор, пока никакого исходного вещества не оставалось. Добавляли воду и реакционную среду экстрагировали EtOAc, высушивали и концентрировали. Неочищенный остаток очищали методом колоночной хроматографии на силикагеле (PE/EtOAc 8/2), чтобы получить 37.
СПОСОБ Z
В атмосфере азота сухой реакционный сосуд загружали оксидом меди (10% моль), лигандом (20% моль), нуклеофилом (1,5 экв.), карбонатом цезия (2 экв.) и арилгалогенидом 5 или 16 (несущим галогеновый или трифталатный заместитель) (1 экв.) с последующим добавлением безводного и дегазированного ацетонитрила (0,6 мл на ммоль арилгалогенида). Сосуд герметически закрывали и проводили перемешивание приблизительно при 80°С до завершения реакции. Реакционную смесь затем охлаждали до комнатной температуры, разбавляли трет-бутилметиловым эфиром и фильтровали через слой из целита, осадок после фильтрования промывали еще простым бутилметиловым эфиром. Фильтрат концентрировали, чтобы удалить ацетонитрил, и повторно растворяли в трет-бутилметиловом эфире. Полученный фильтрат органического слоя дважды промывали водой, один раз солевым раствором перед высушиванием над Na2SO4 и фильтровали. Растворитель удаляли в вакууме, чтобы получить неочищенный продукт, который очищали методом хроматографии на силикагеле, чтобы получить соединение 42.
СПОСОБ АА
Алкилгалогенид нагревали приблизительно при 90°С в течение ночи в триметилфосфите (10 мл/ммоль). Реакционную смесь охлаждали приблизительно до 0°С в бане со льдом и осторожно добавляли раствор HCl (1 н.). Водный слой экстрагировали EtOAc. Объединенные органические слои промывали HCl (1 н.) и водой, и затем высушивали и концентрировали, чтобы получить соединение 53 в виде бесцветного масла.
СПОСОБ АВ
В микроволновую запаянную трубку добавляли соединения 17 (1 экв.), формальдегид (37% мас. в воде, 1 экв.) и морфолин (1 экв.) к трет-бутиловому спирту (4 мл/ммоль). Трубку нагревали при облучении микроволнами при давлении приблизительно при 170°С (максимальная мощность 200 Вт, устройство для обнаружения CEM) приблизительно в течение 60 минут. Реакцию контролировали с помощью ТСХ и, если оставалось какое-либо исходное вещество, сосуд нагревали приблизительно в течение 45 минут приблизительно при 170°С. Растворители выпаривали в вакууме, и неочищенный остаток очищали методом хроматографии на силикагеле (MeOH/EtOAc : 2/98), чтобы получить соединение 18.
СПОСОБ АС
В микроволновой трубке соединение 5 или 6 (1 экв.) перемешивали с DMF (5 мл/ммоль) и добавляли TMSBr (5 экв.). Трубку нагревали при облучении микроволнами при давлении приблизительно при 60°С (максимальная мощность 100 Вт, устройство для обнаружения CEM) приблизительно в течение 50 минут. После охлаждения добавляли воду, и соединение 60 собирали фильтрованием.
IX. Репрезентативные примеры активных соединений
В таблицах 1 и 2 представлен не ограничивающий список репрезентативных соединений, которые можно получать по способам и в соответствии со схемами 1-16, приведенными выше.
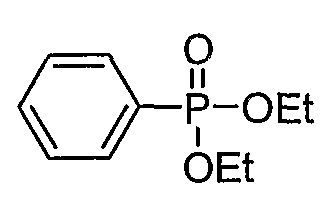
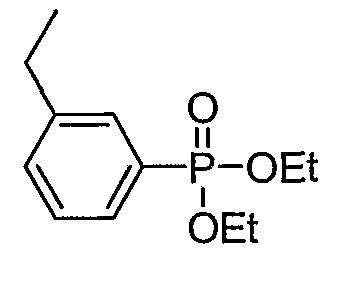
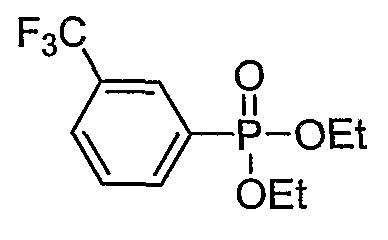
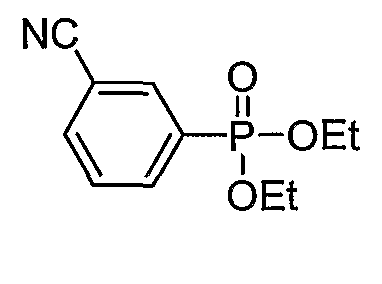
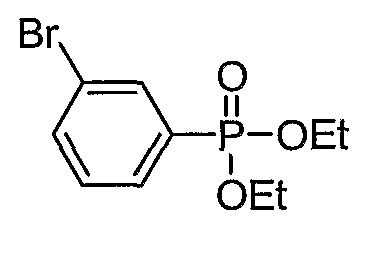
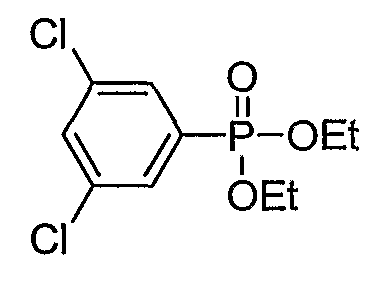
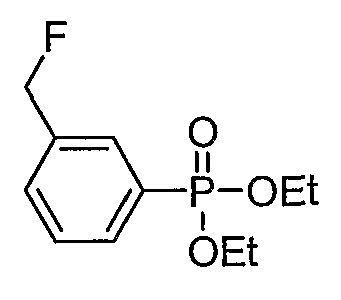
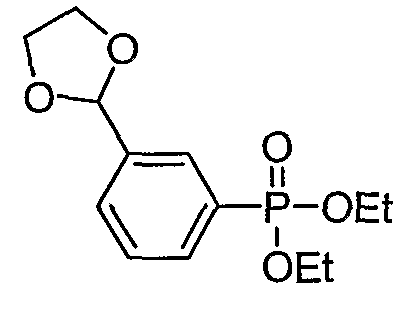
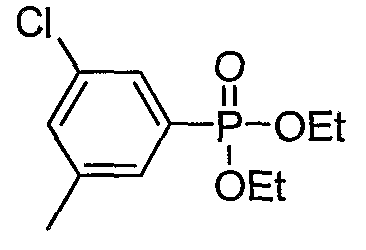
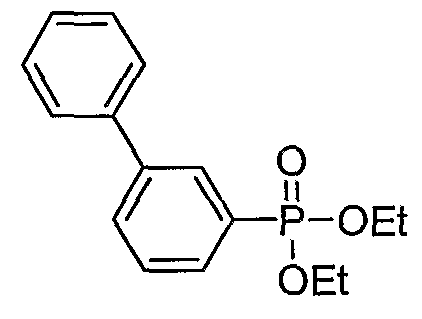
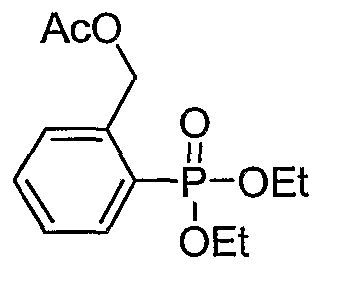
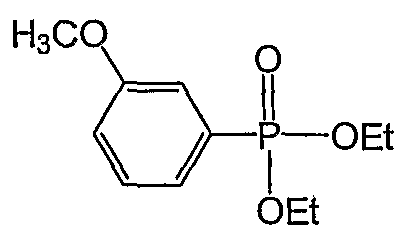
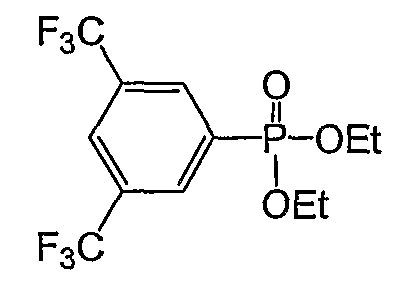
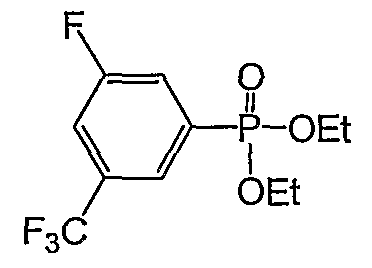
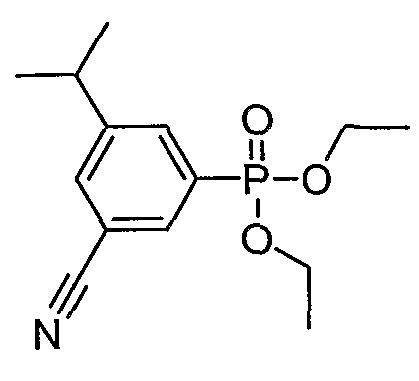
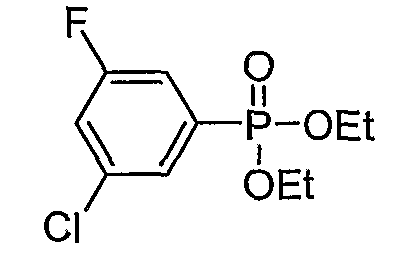
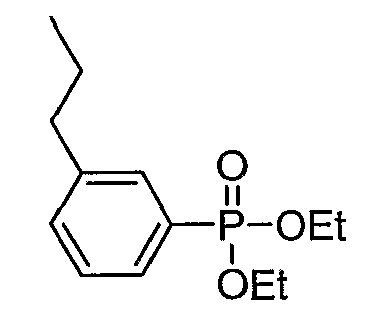
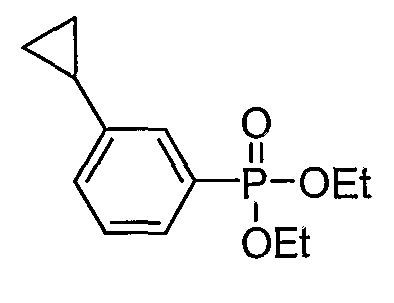
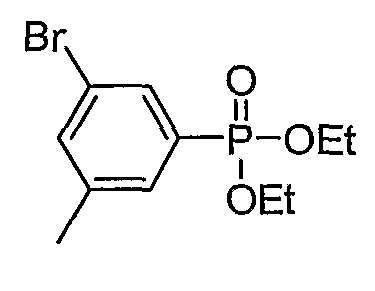
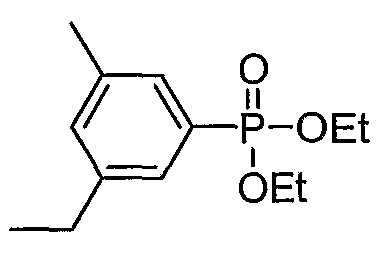
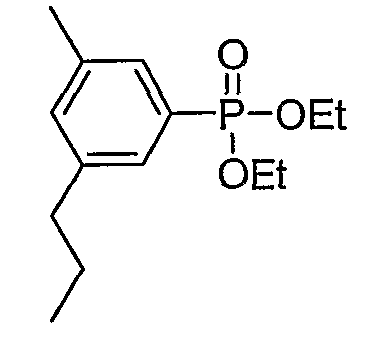
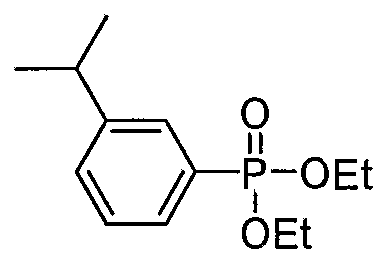
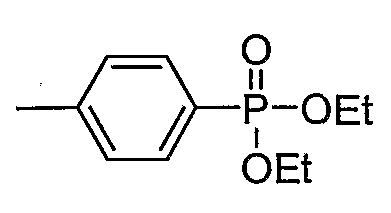
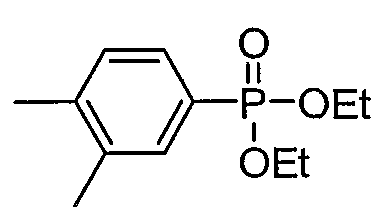
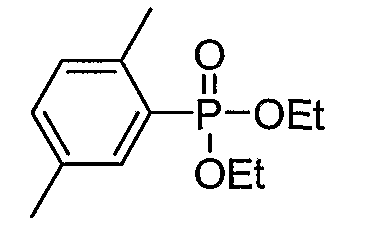
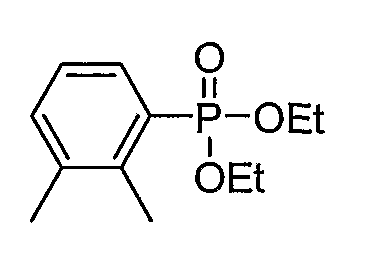
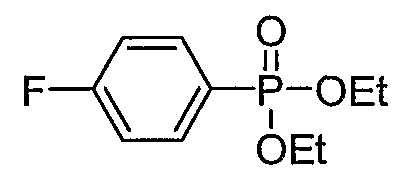
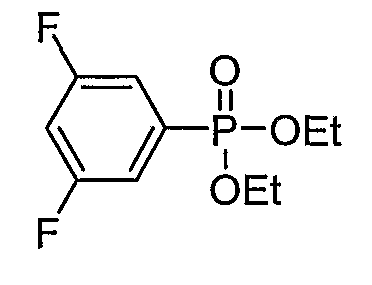
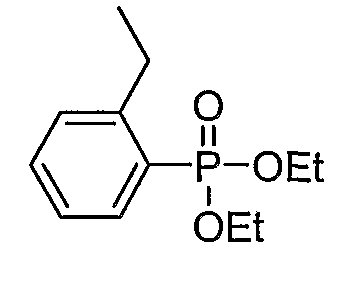
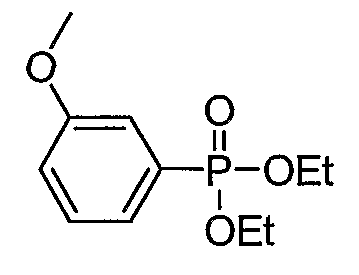
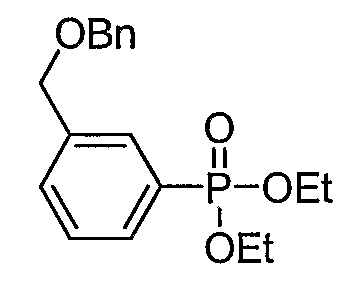
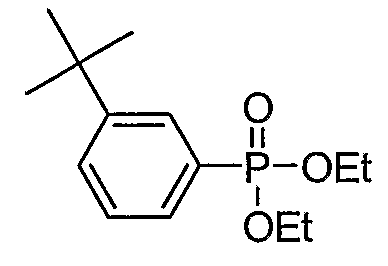
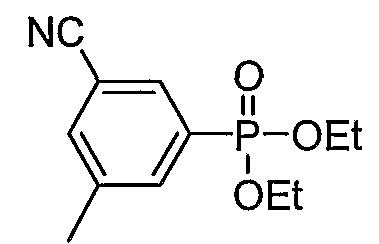
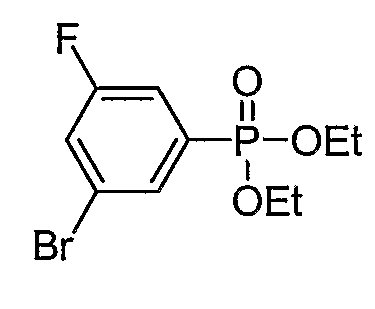
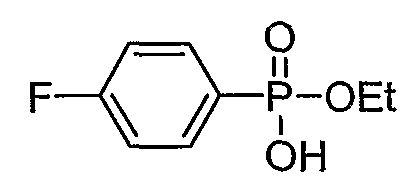

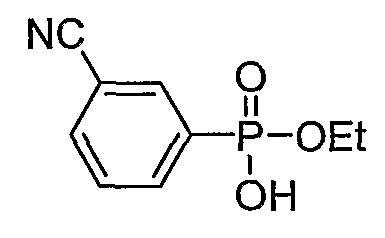
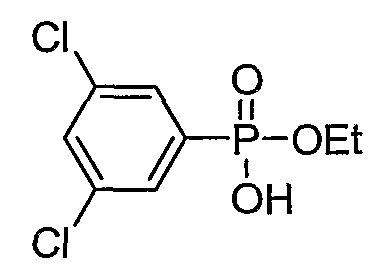
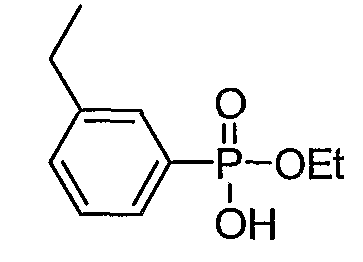
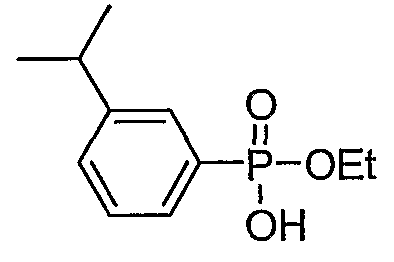
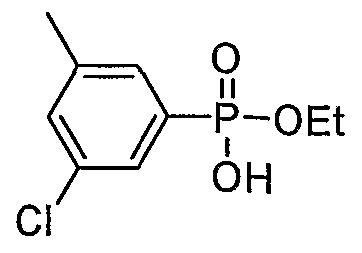
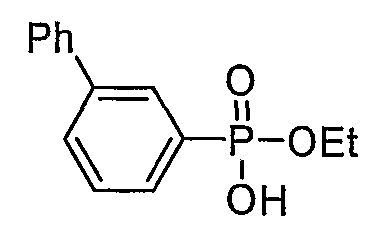
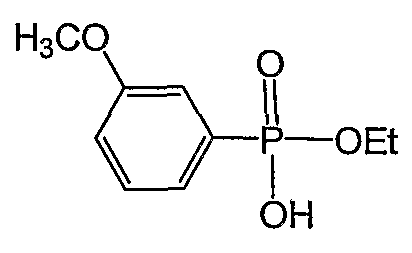
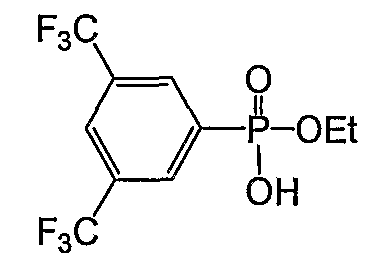
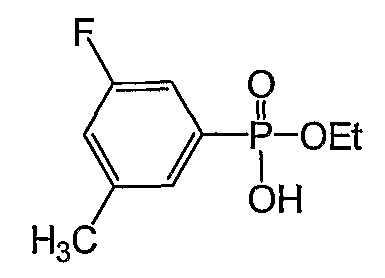
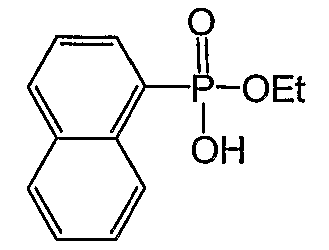
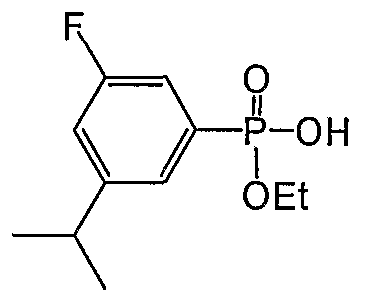
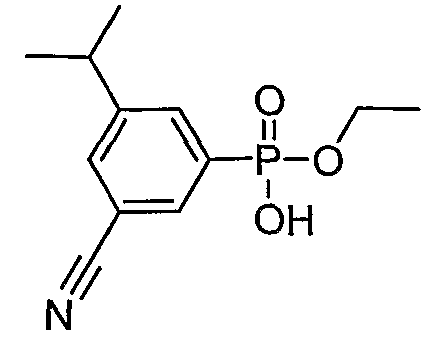
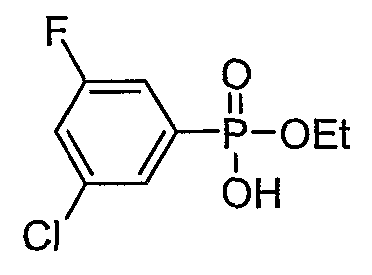
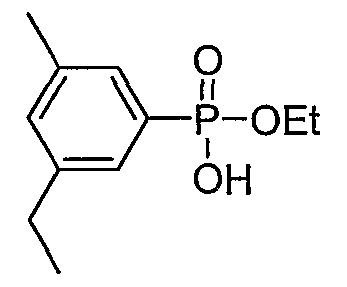
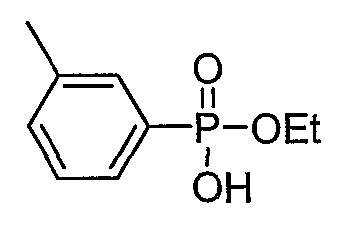
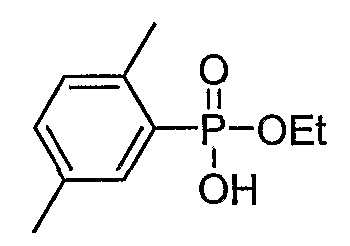
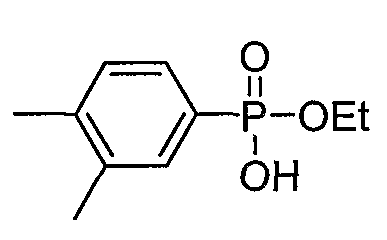
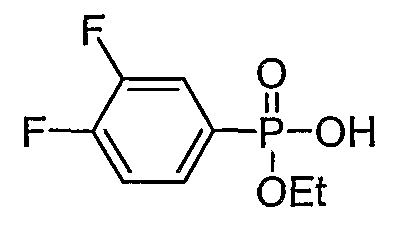
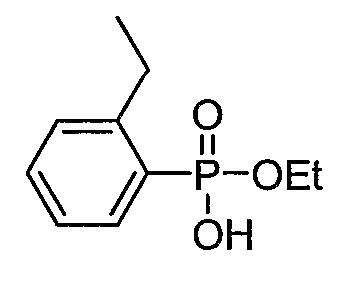
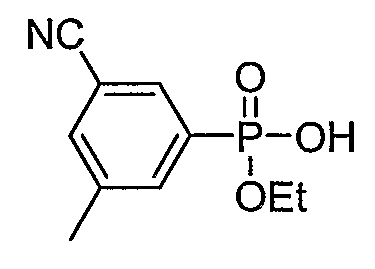
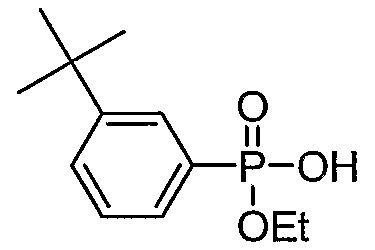
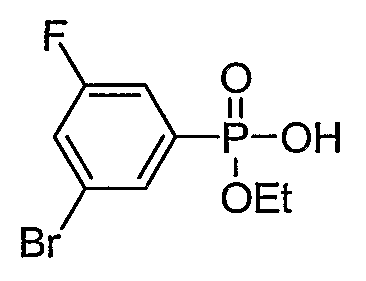
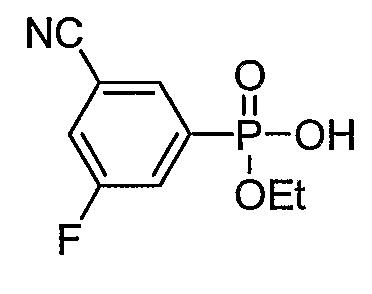
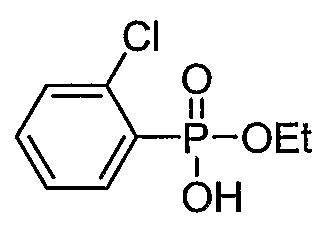
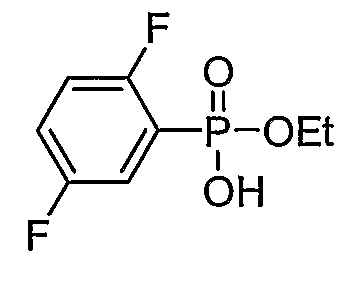
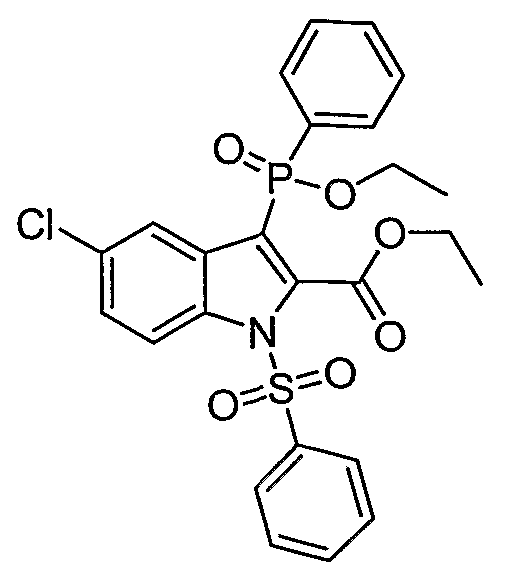
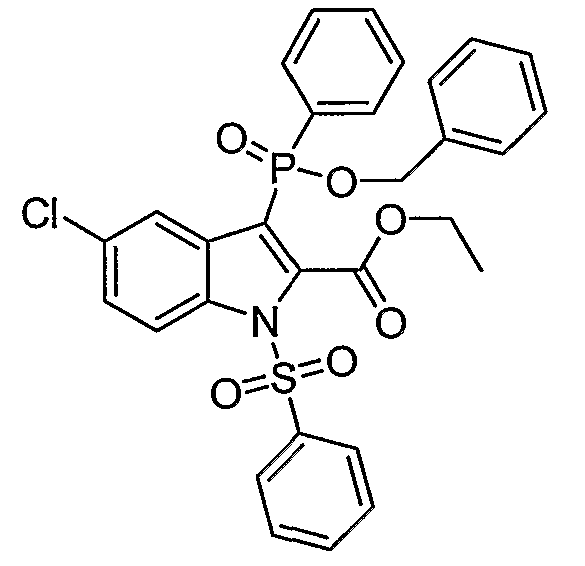
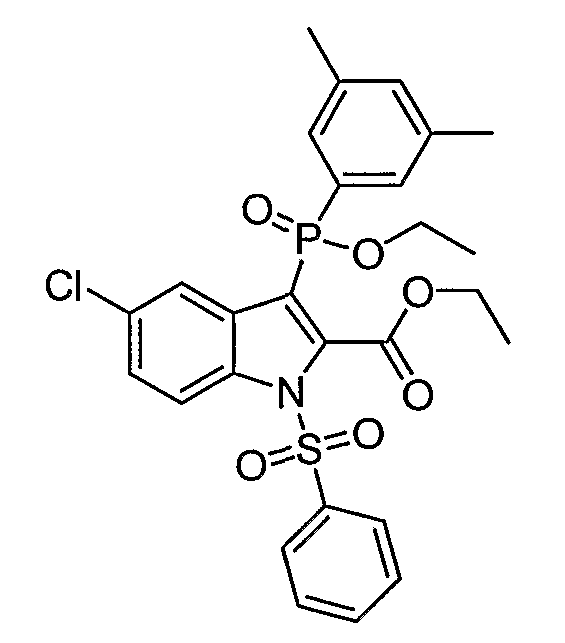
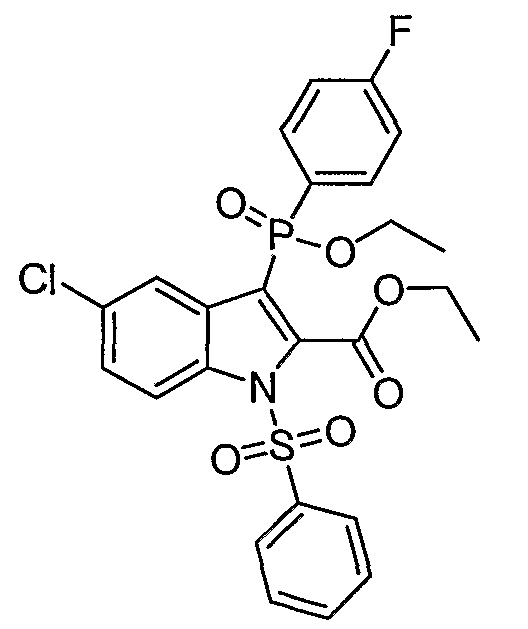
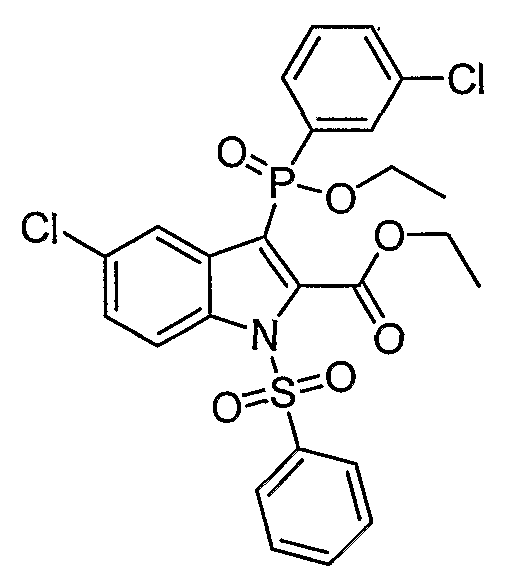
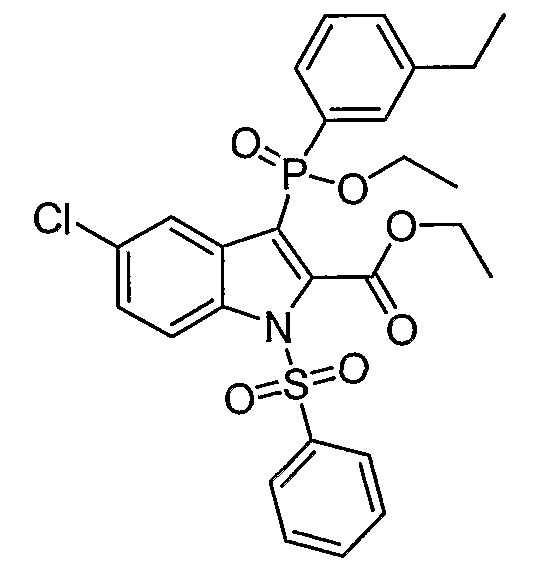
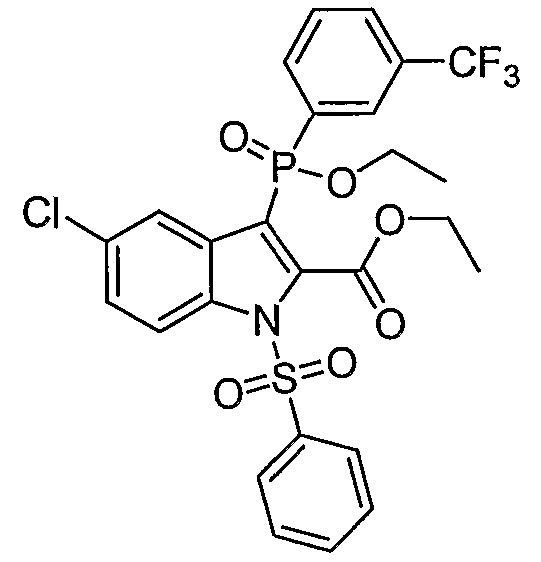
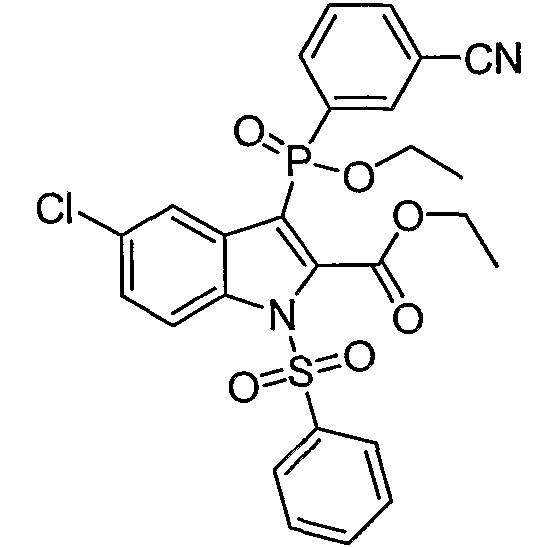
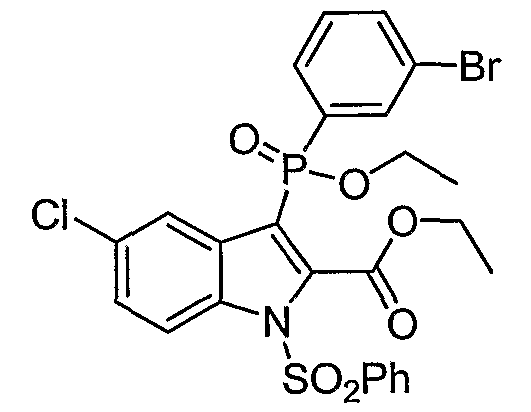
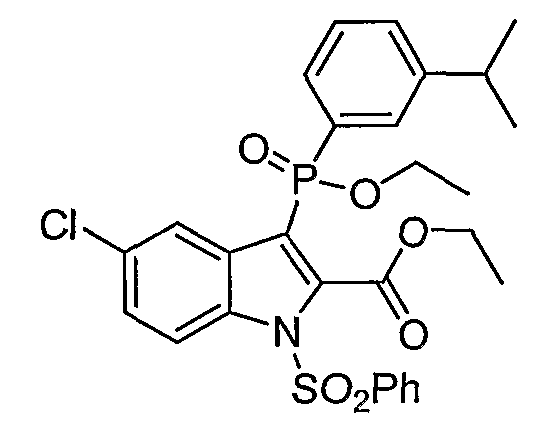
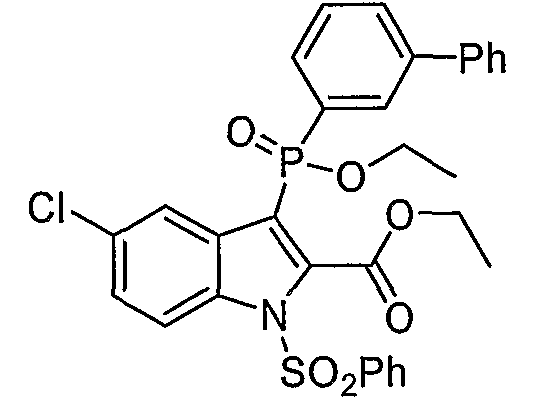
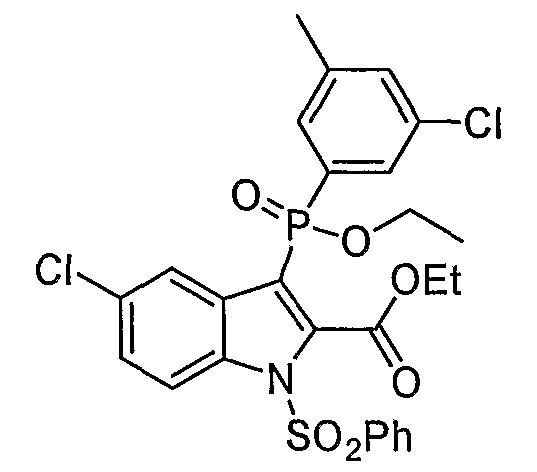
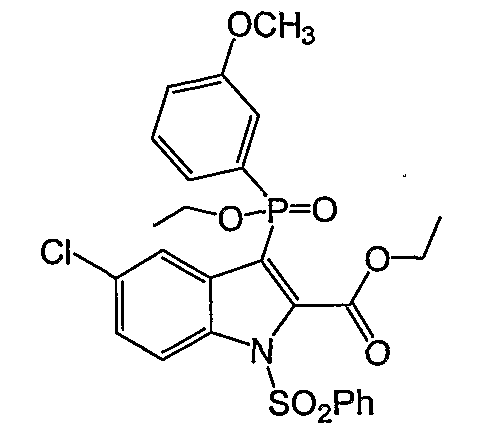
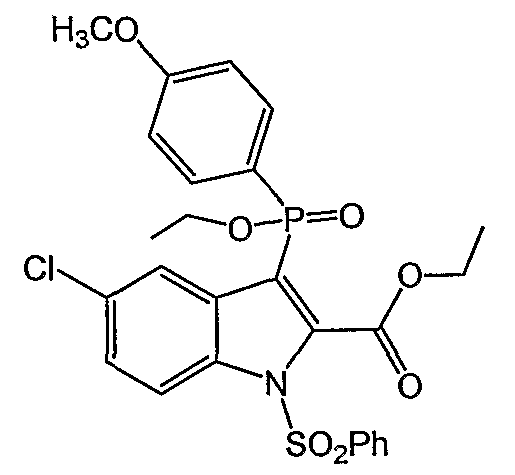
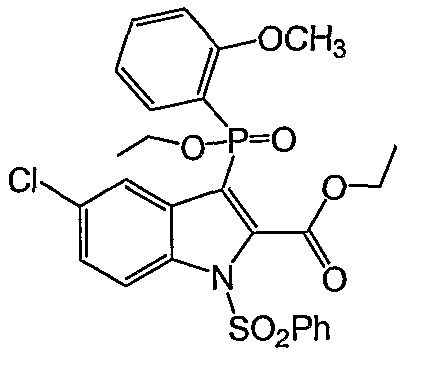
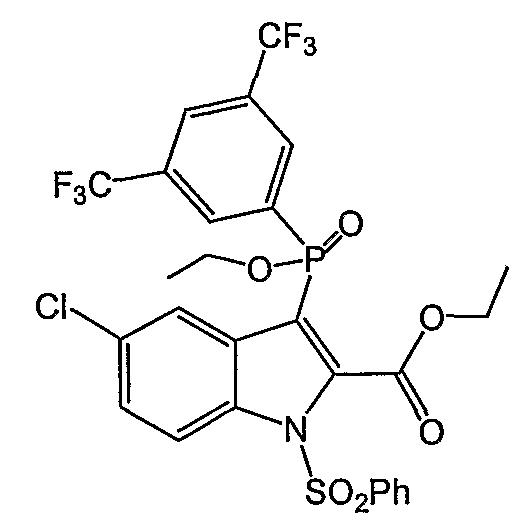
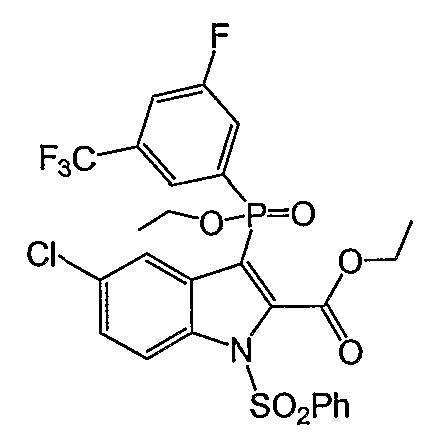
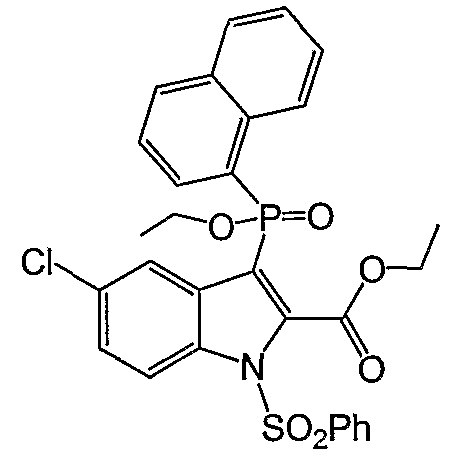
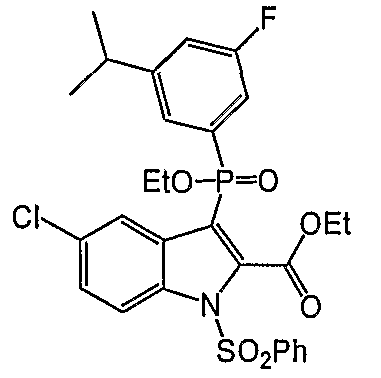
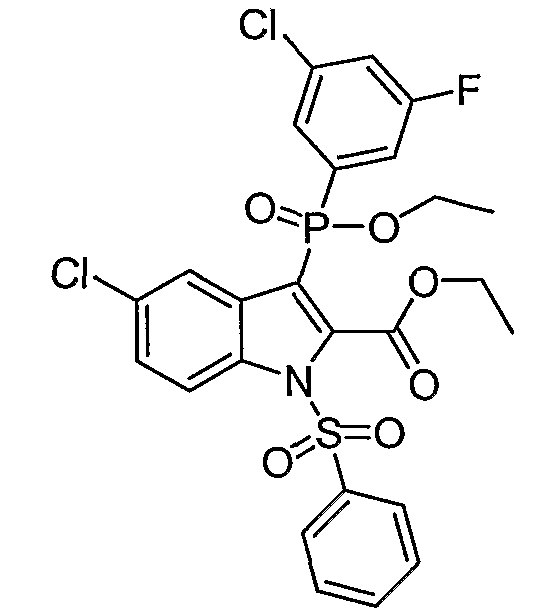
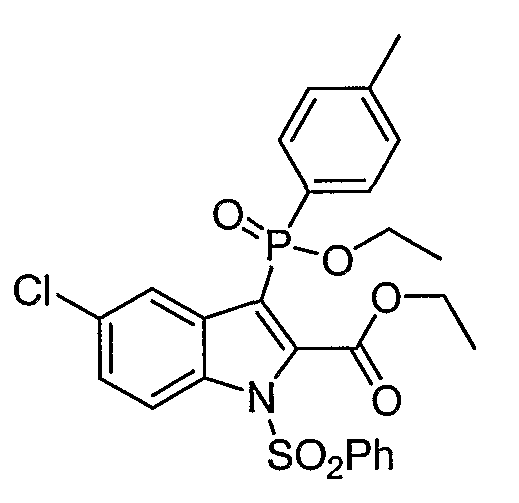
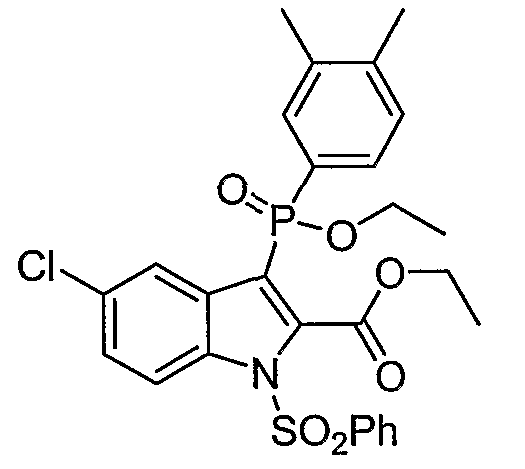
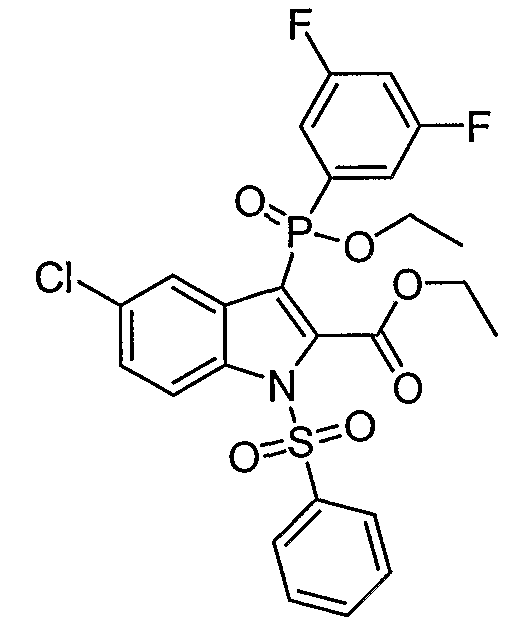
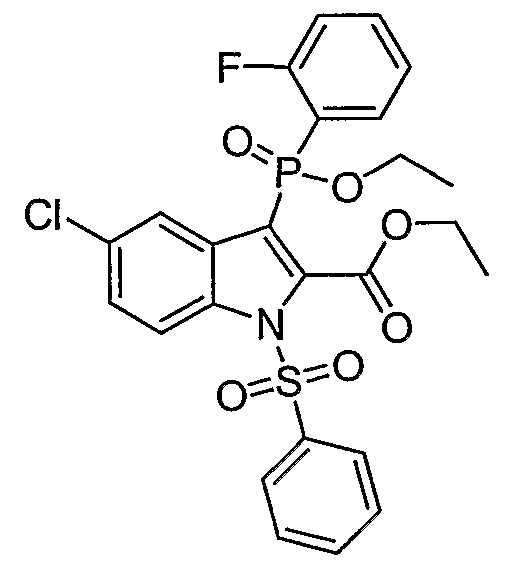
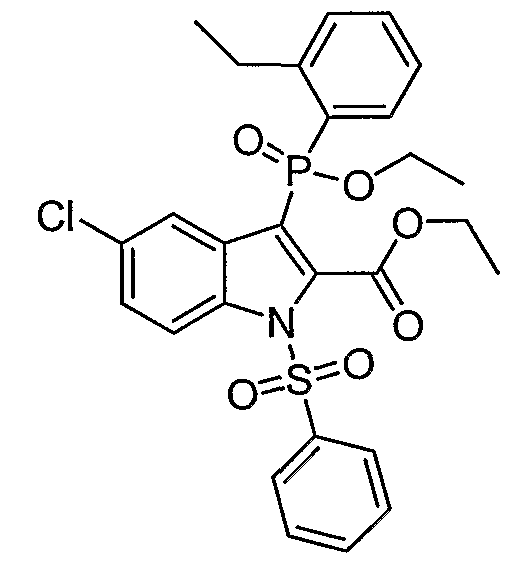
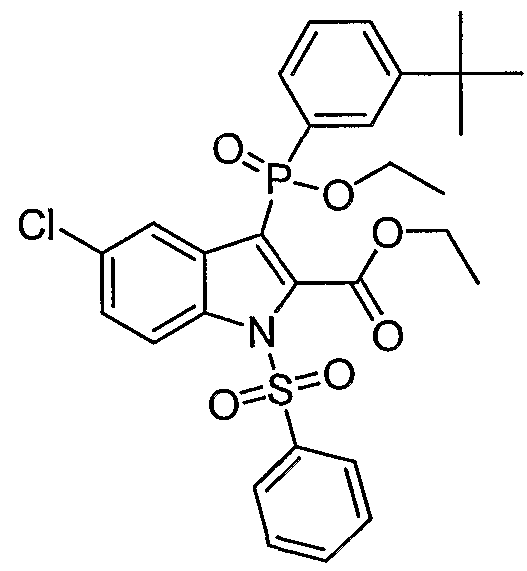
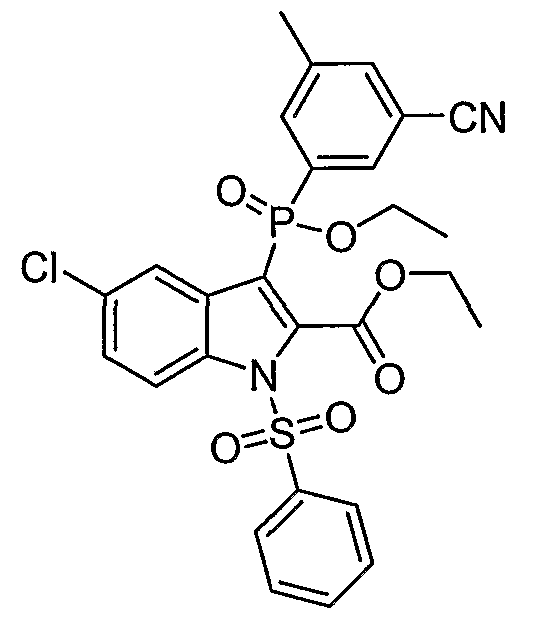
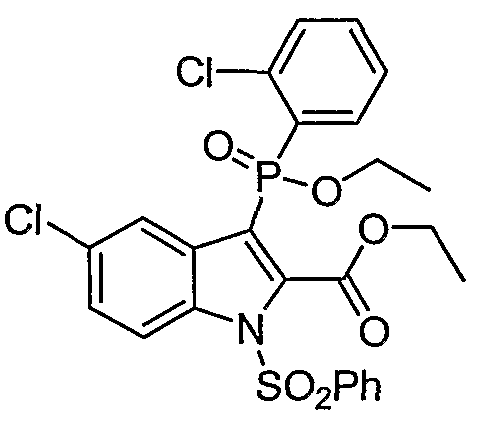
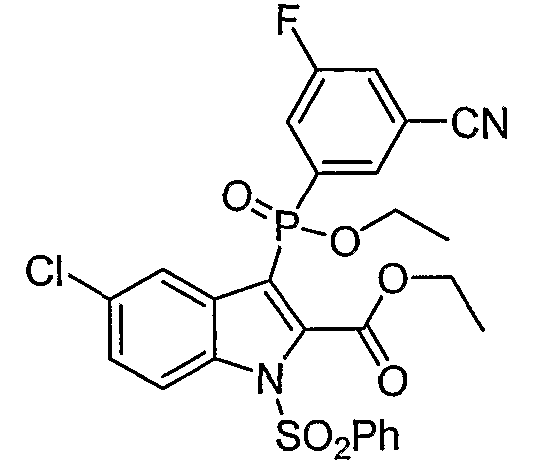
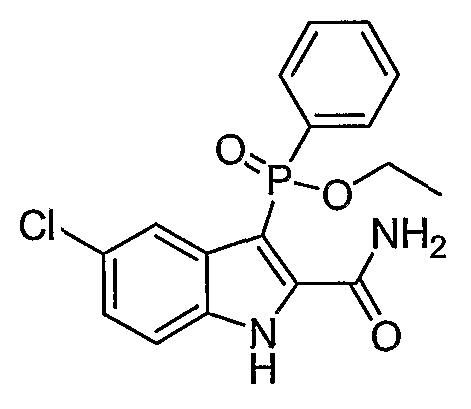
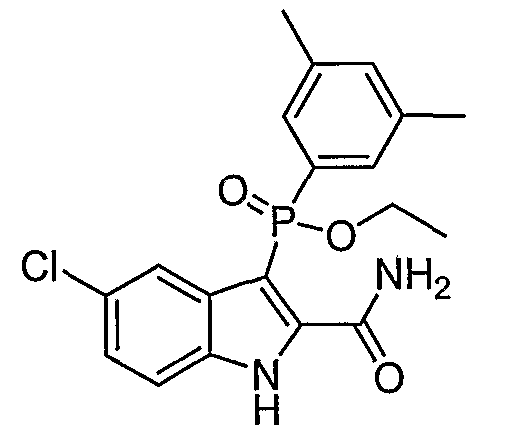
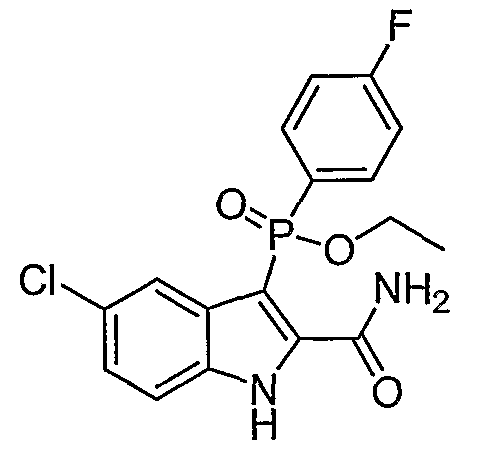
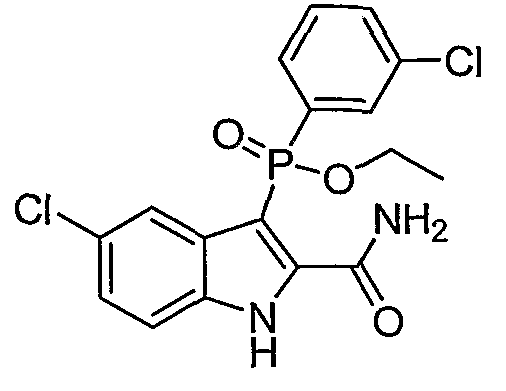
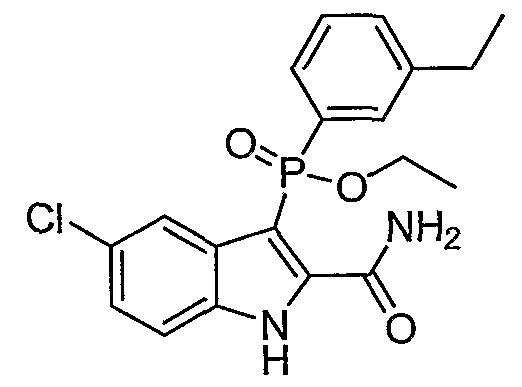
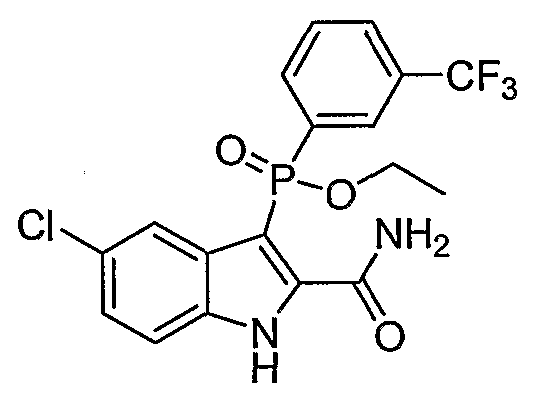
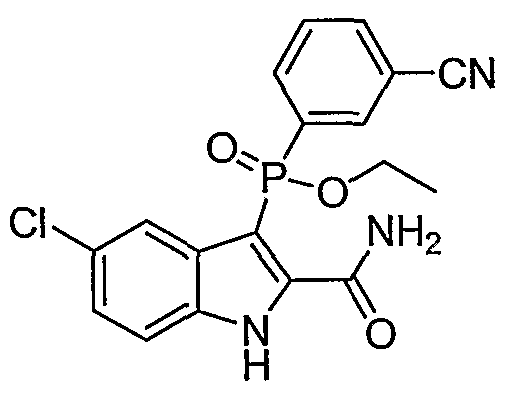
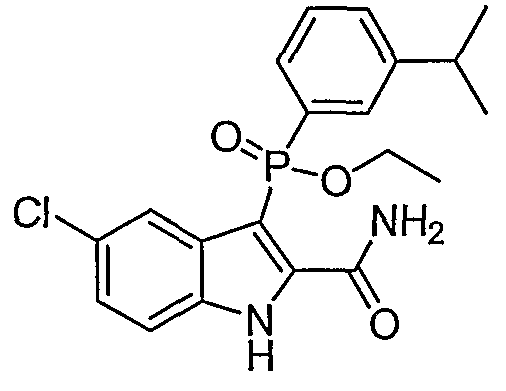
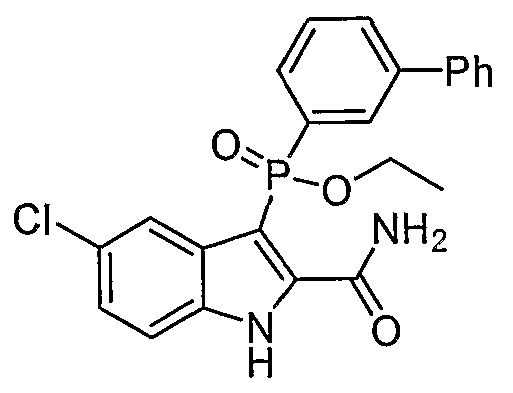
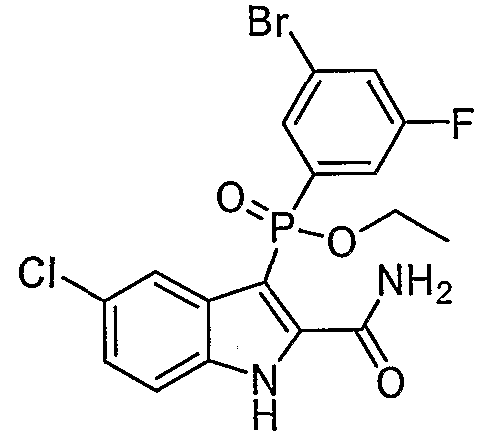
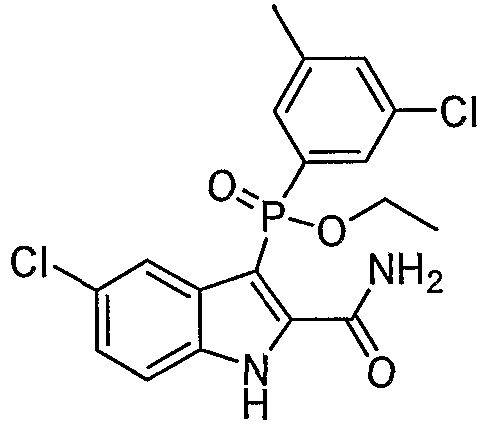
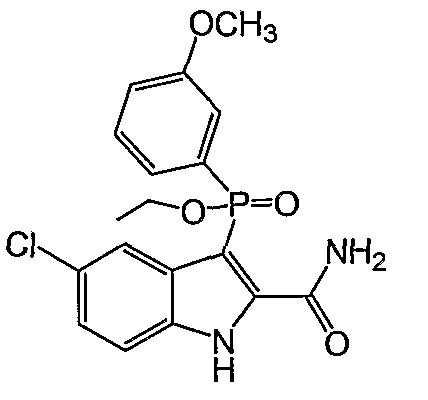
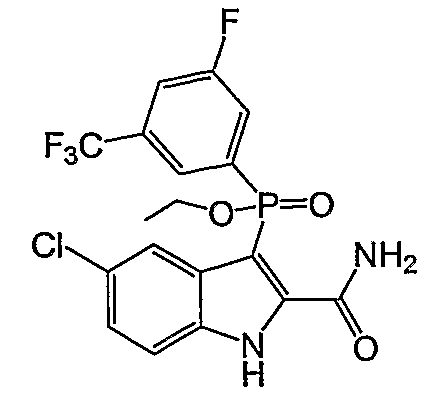
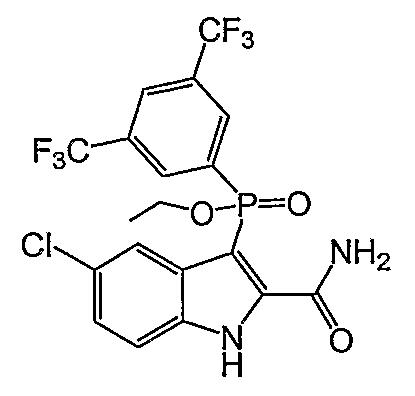
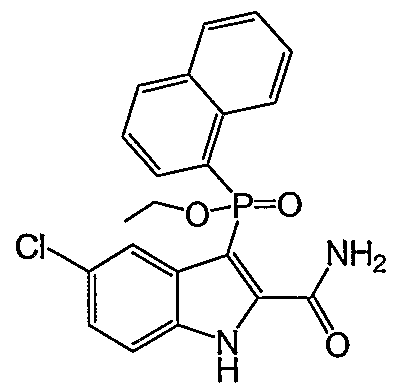
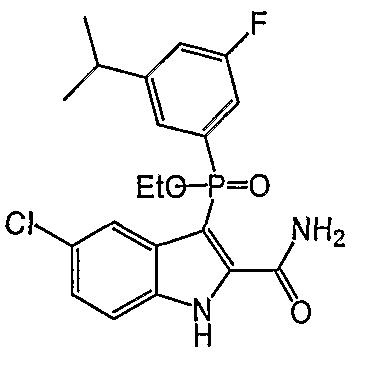
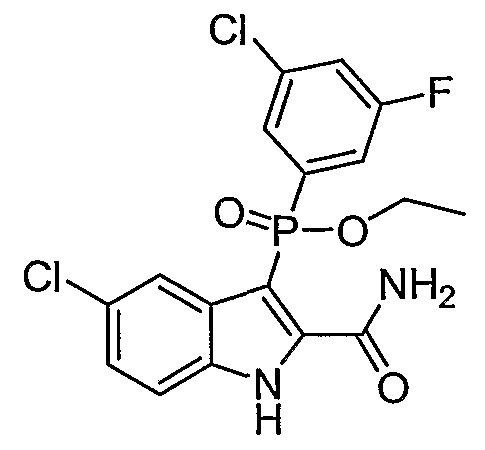
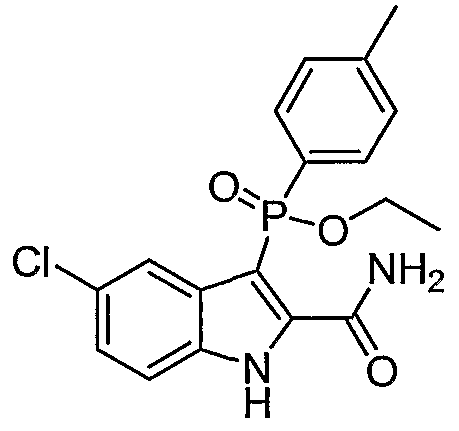
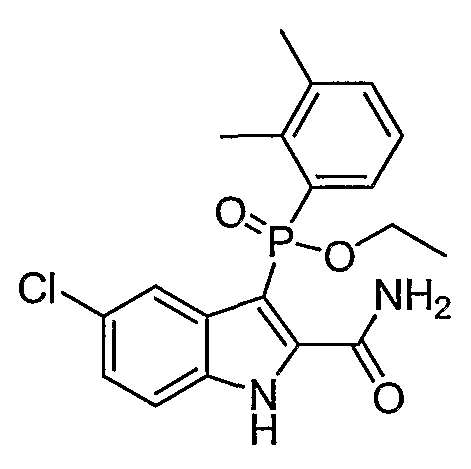
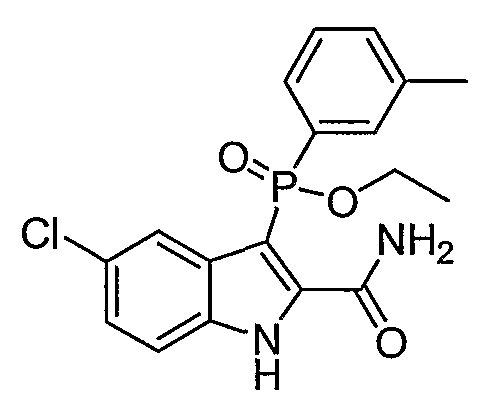
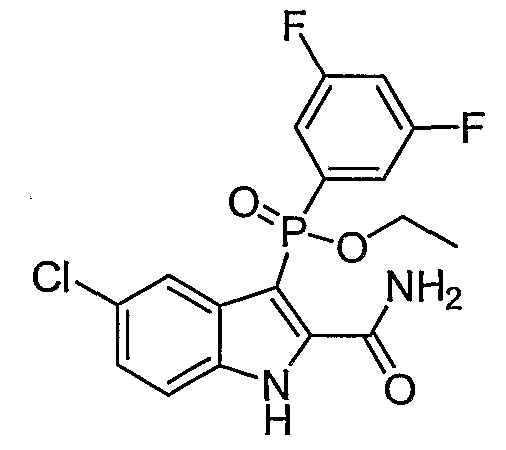
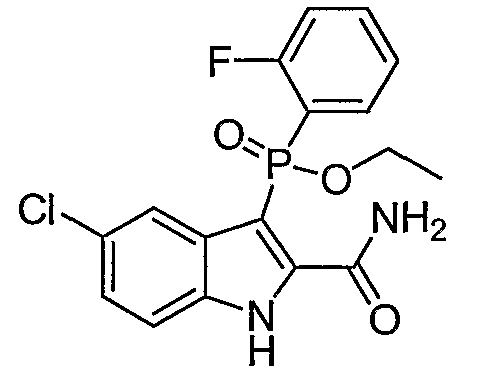
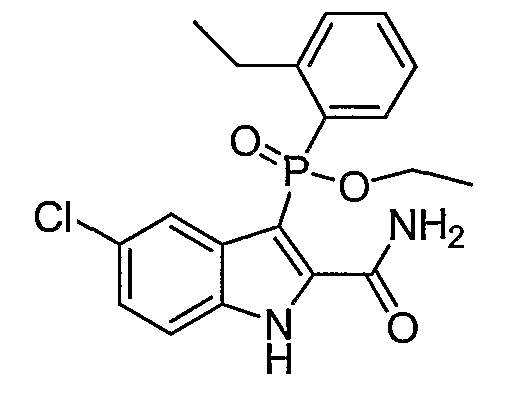
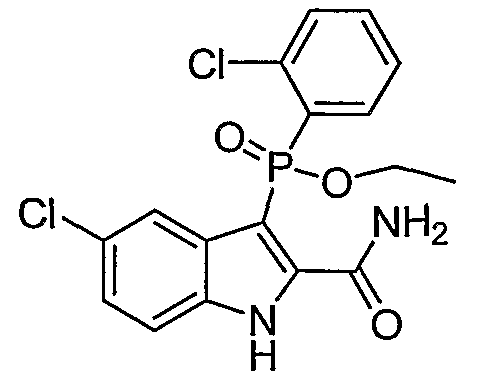
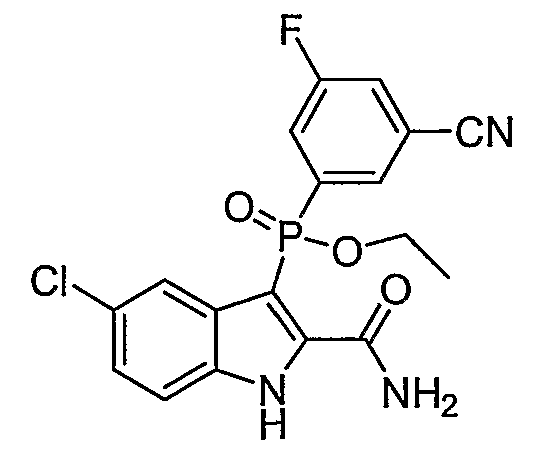
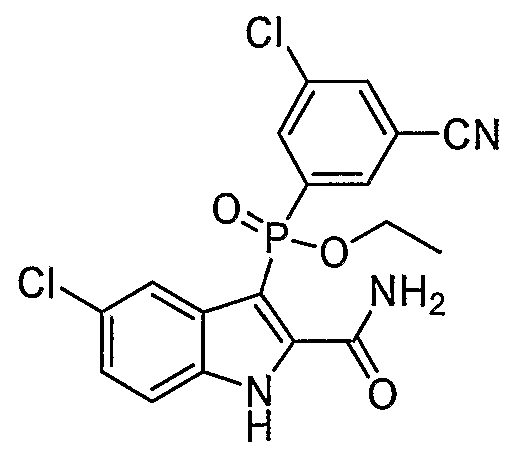
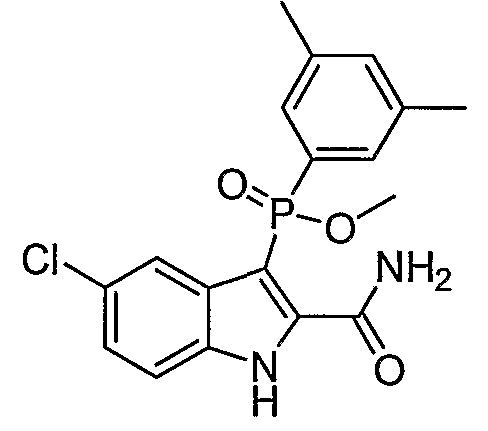
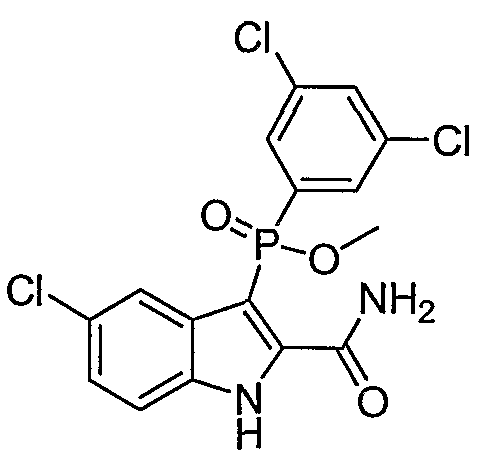
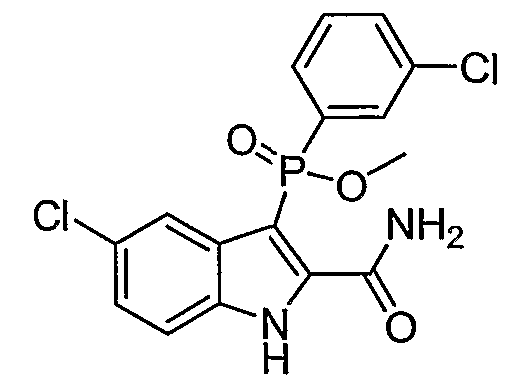
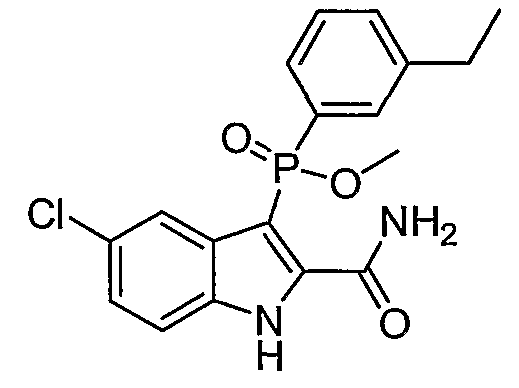
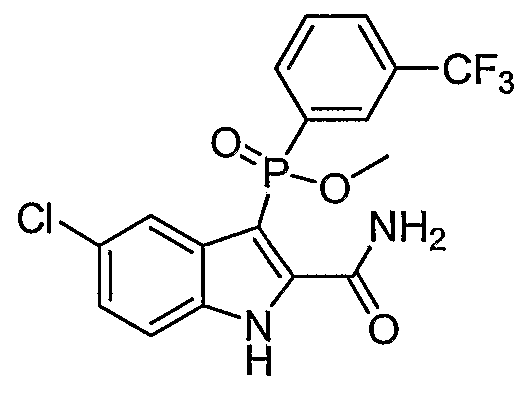
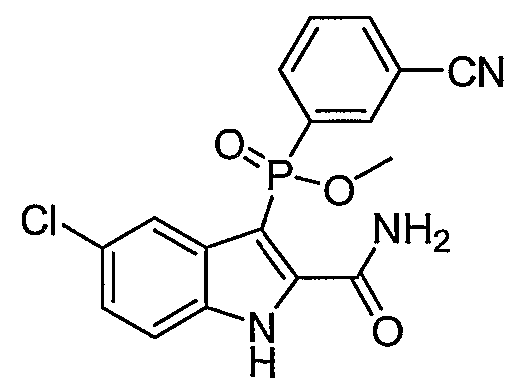
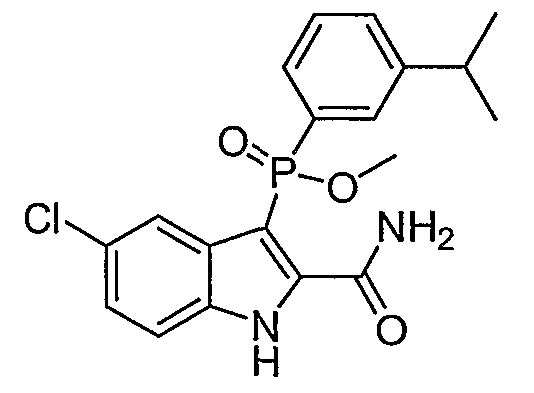
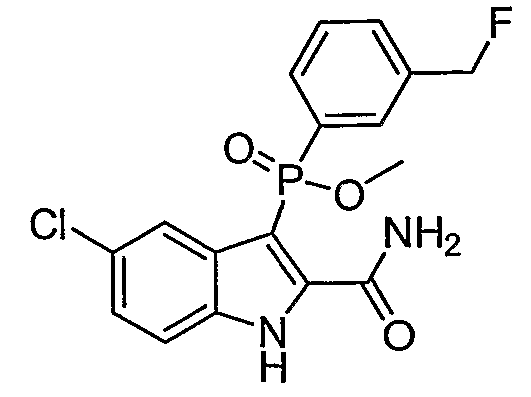
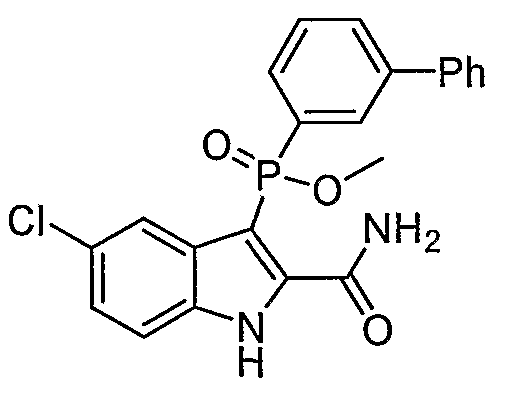
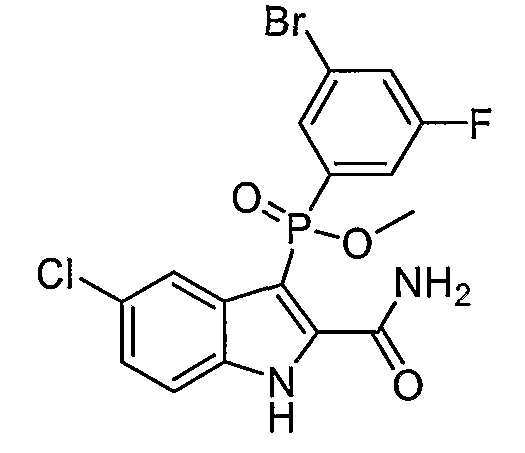
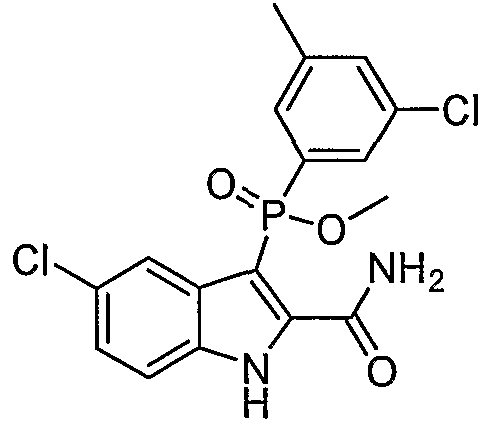
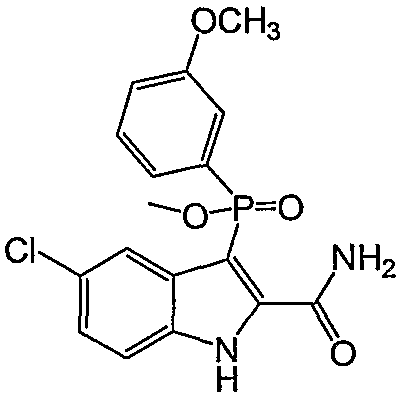
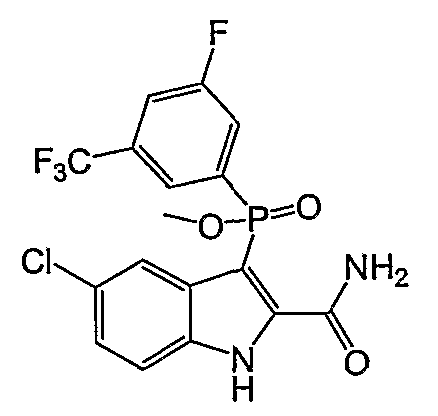
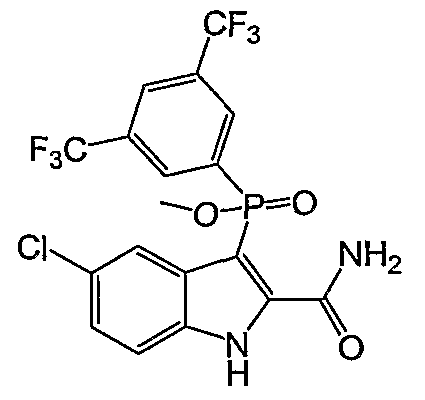
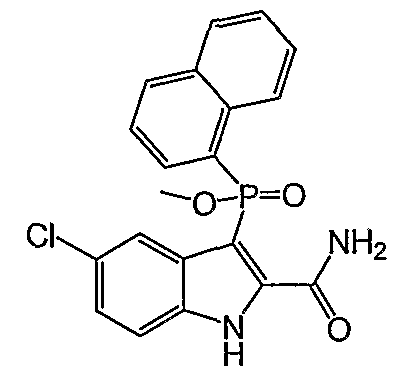
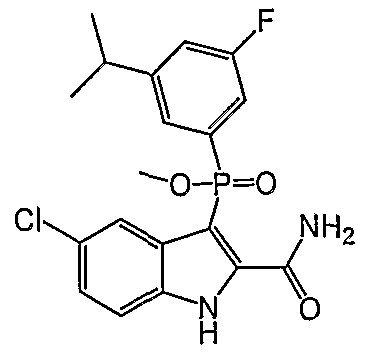
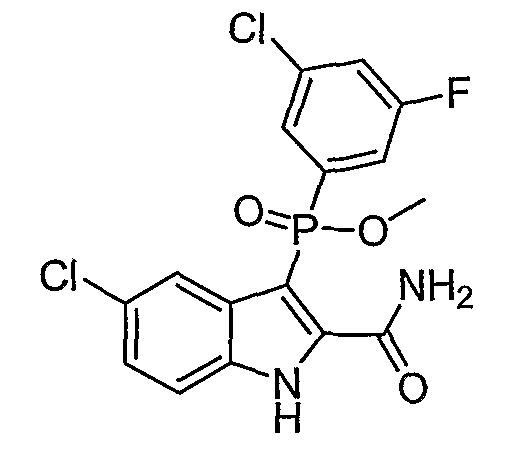
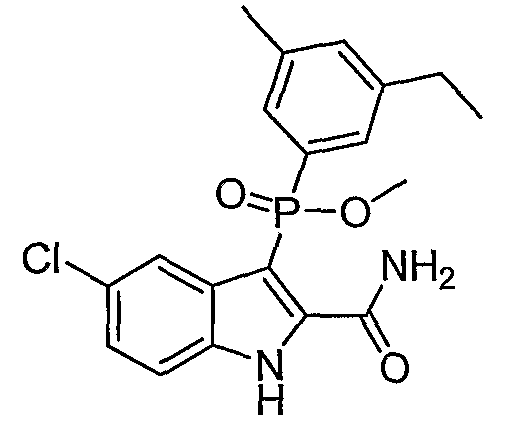
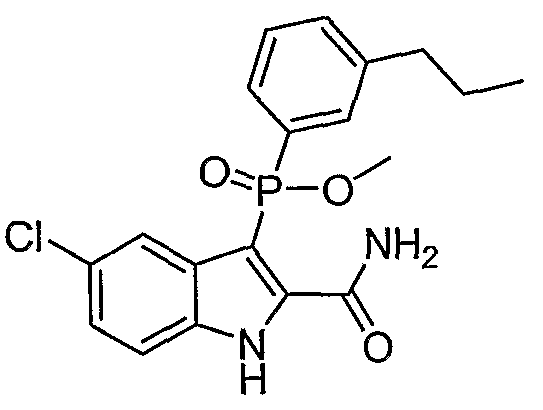
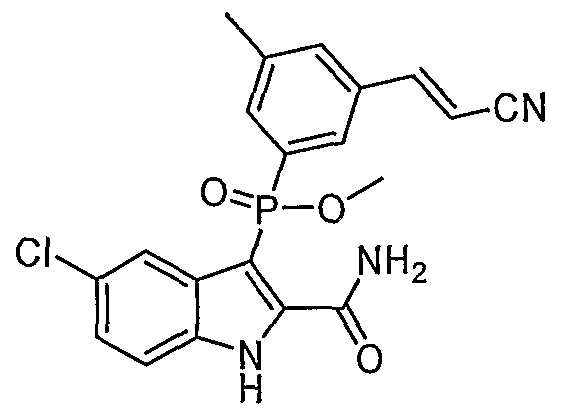
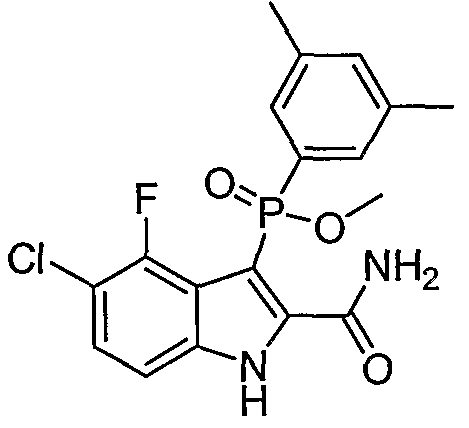
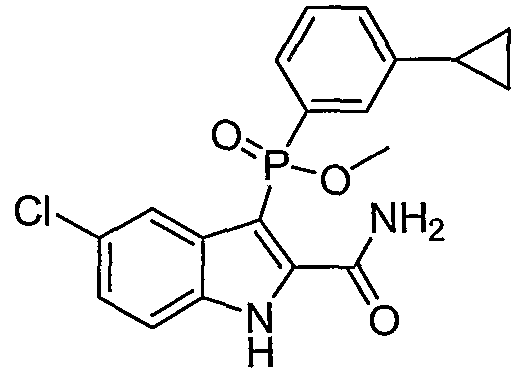
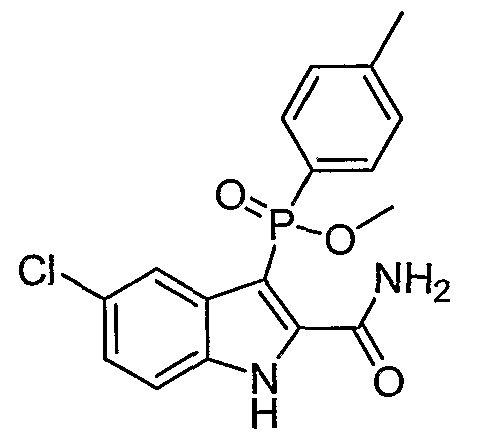
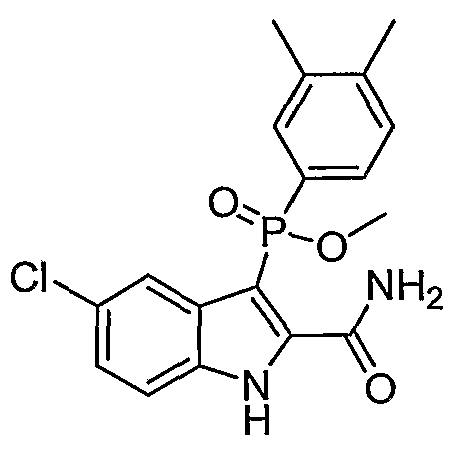
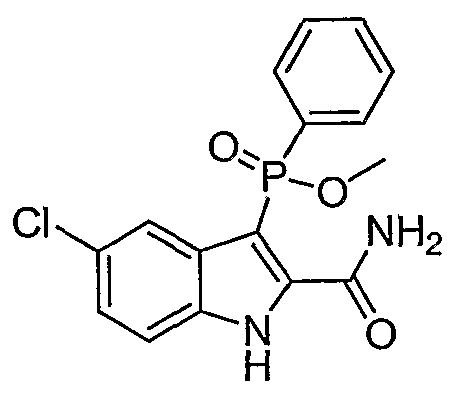
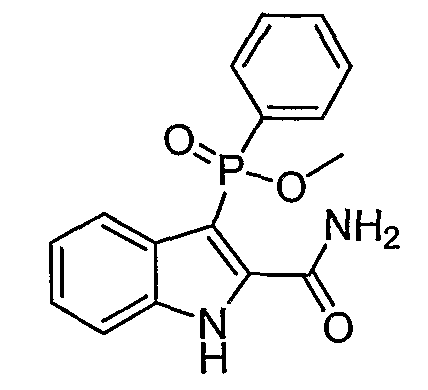
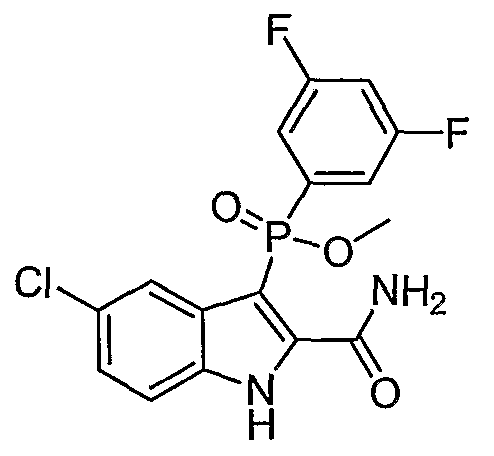
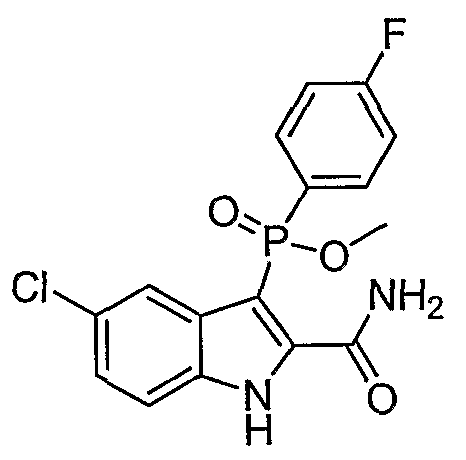
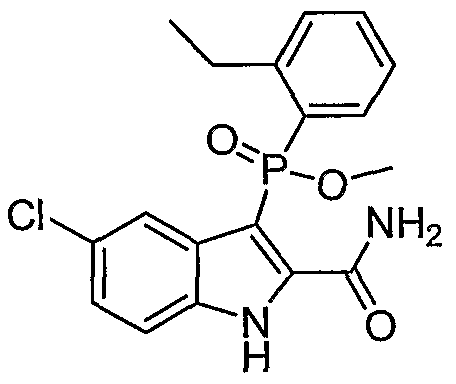
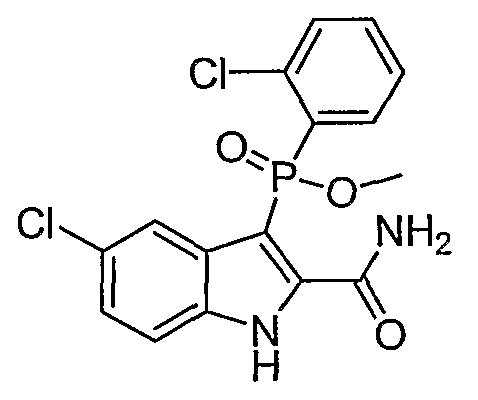
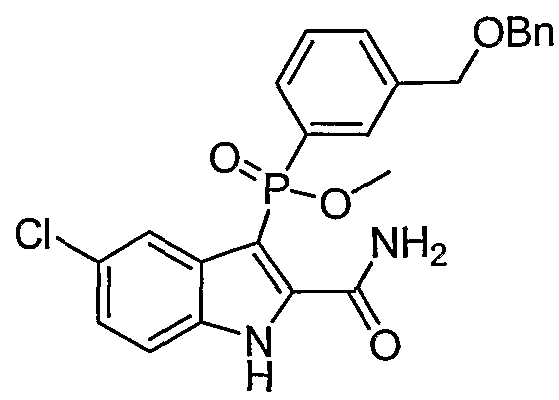
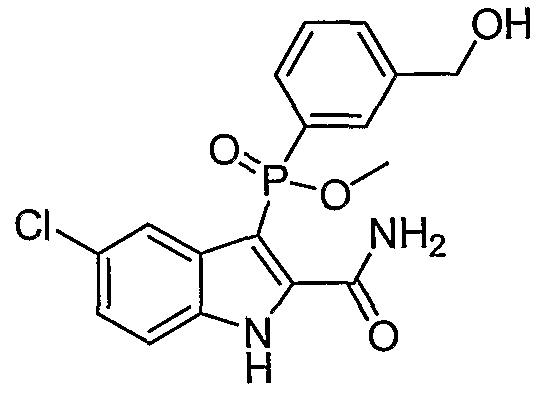
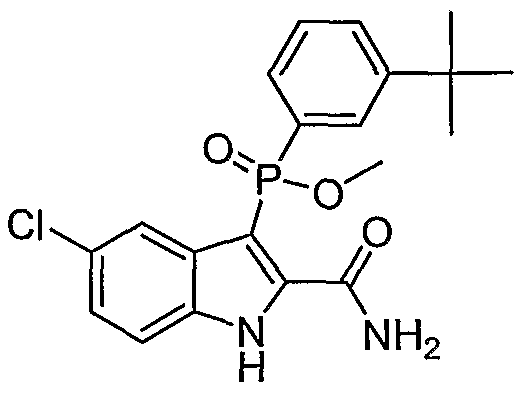
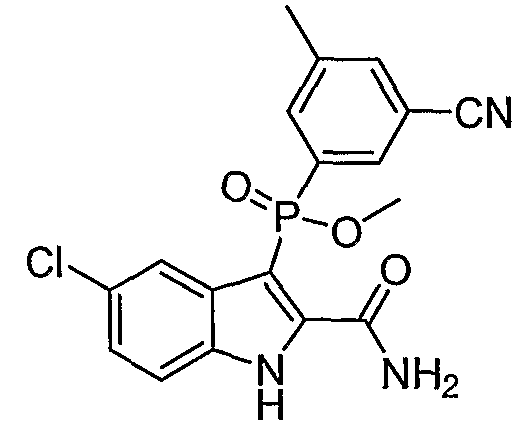
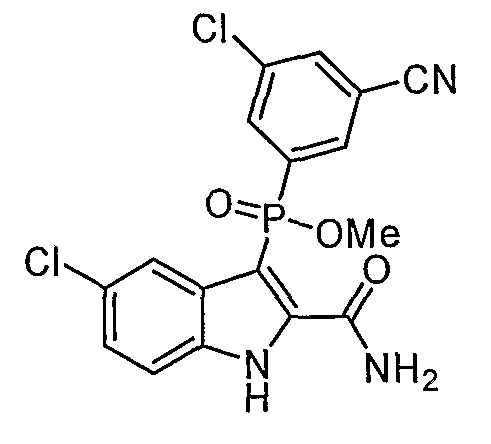
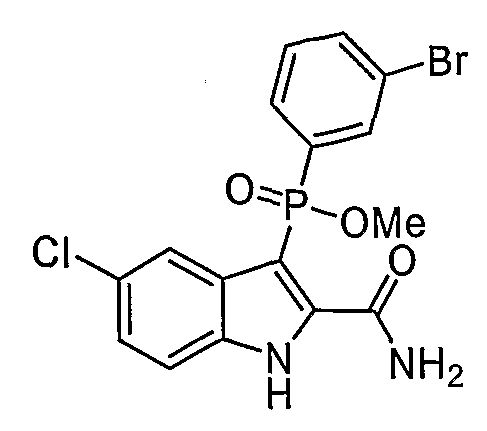
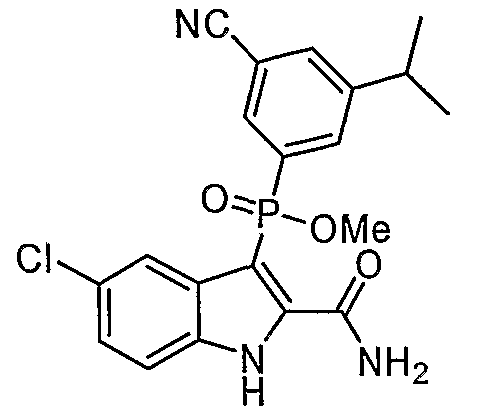
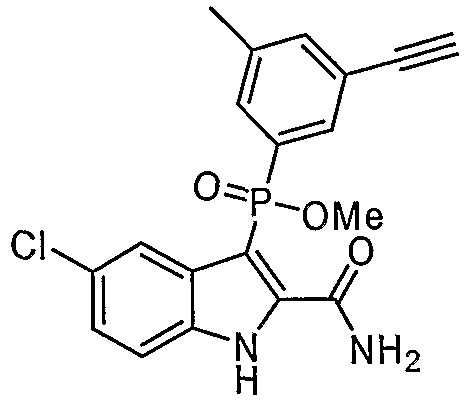
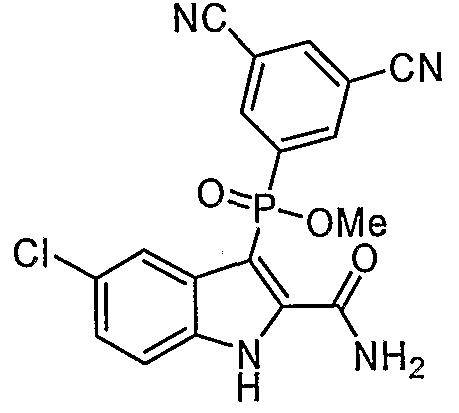
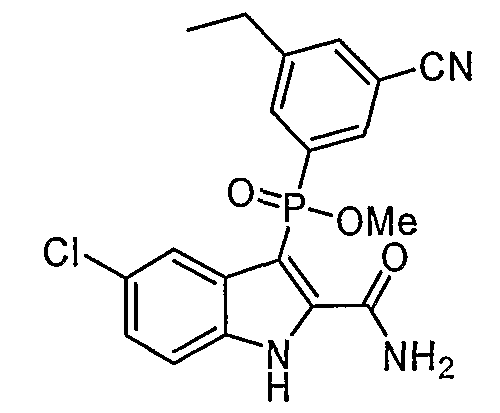
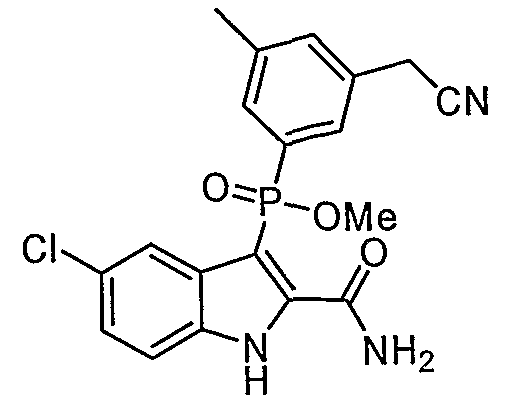
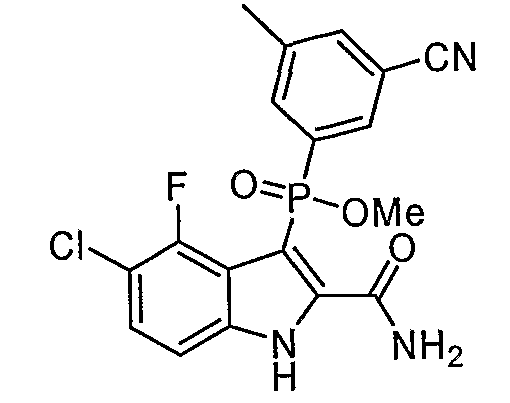
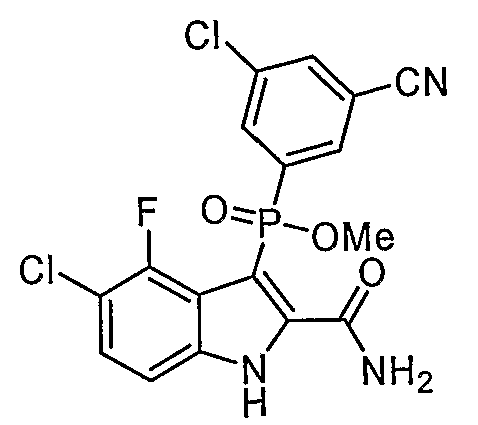
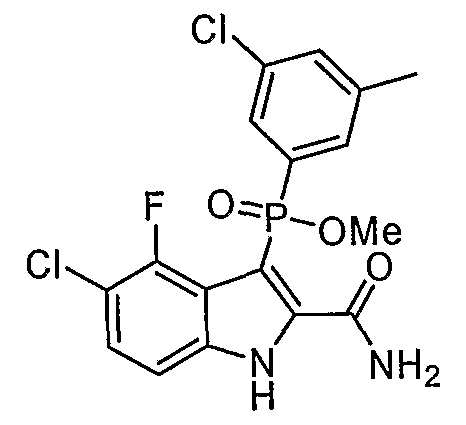
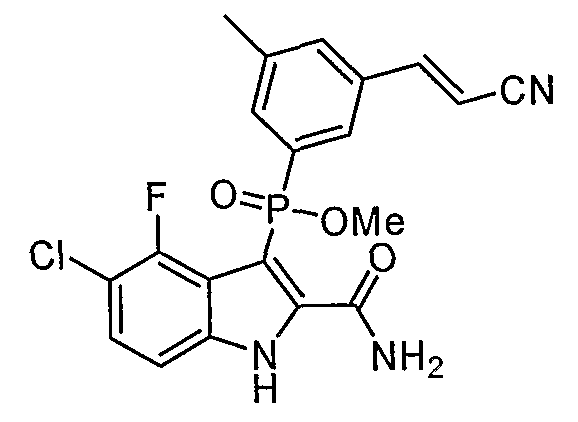
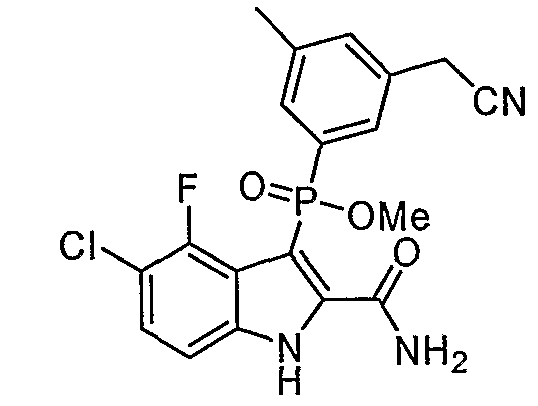
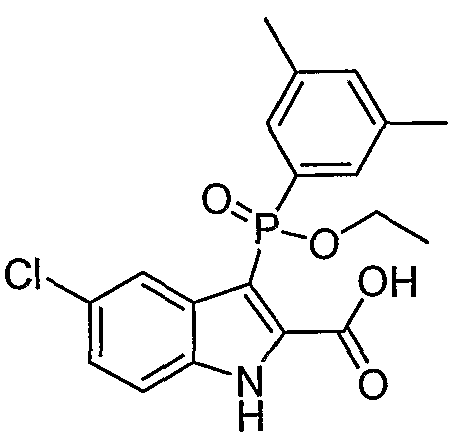
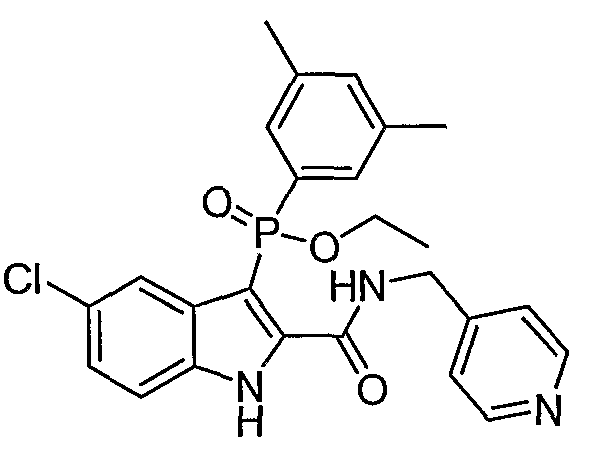
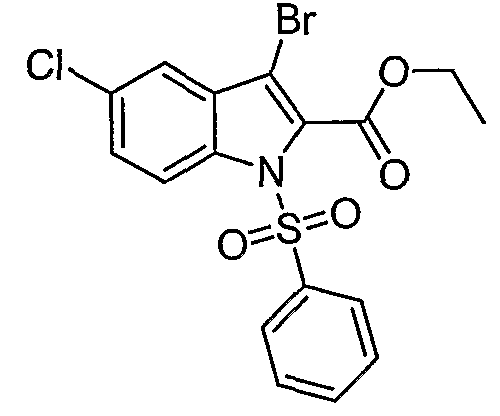
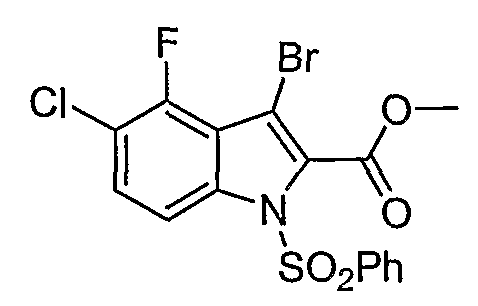
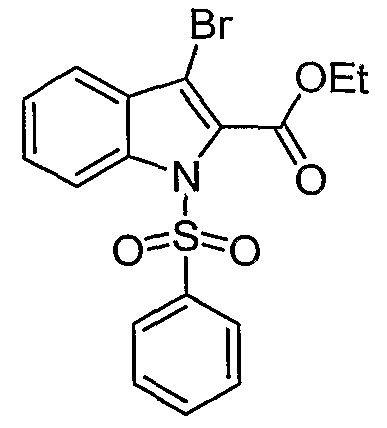
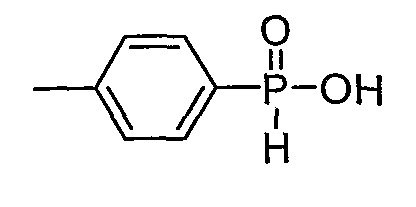
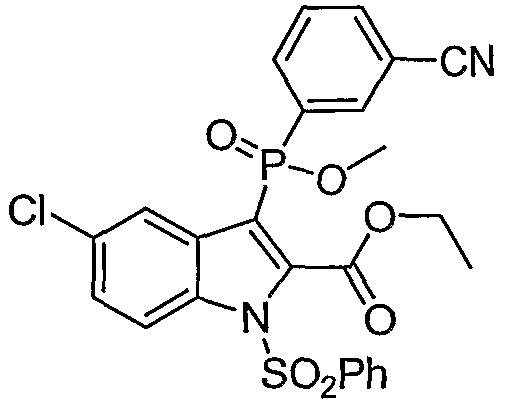
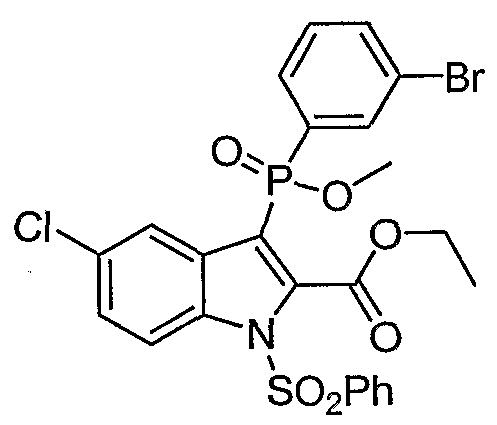
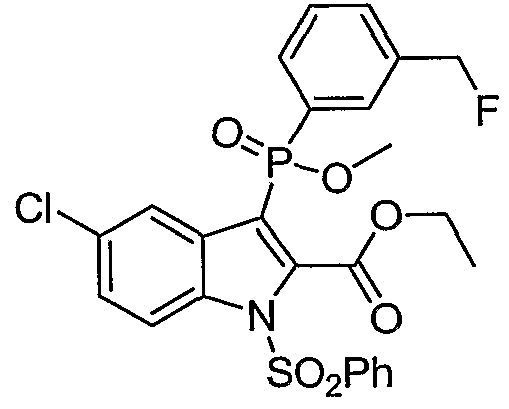
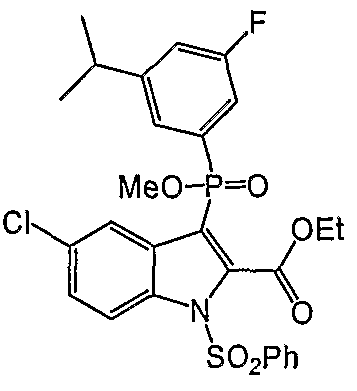
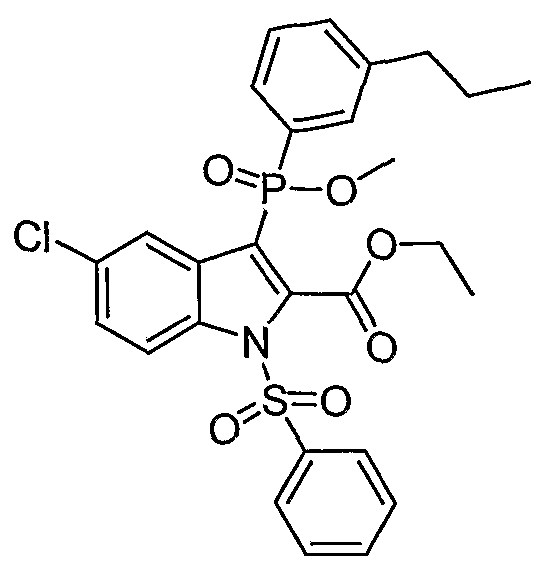
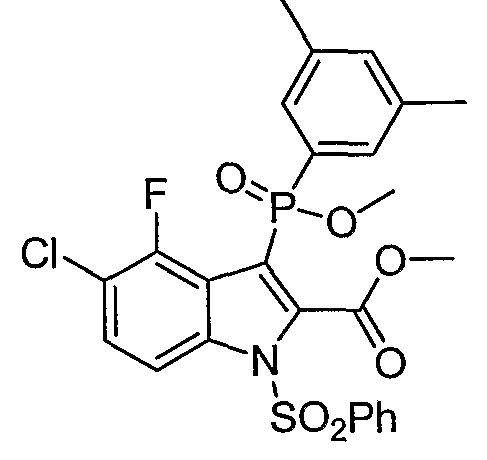
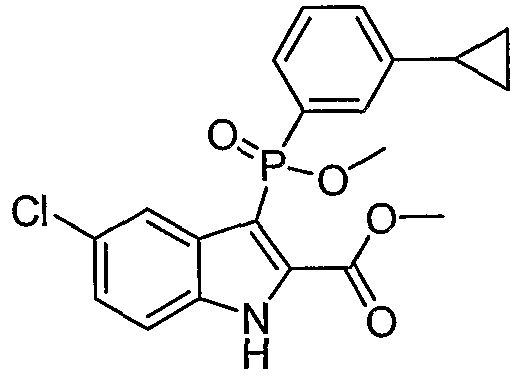
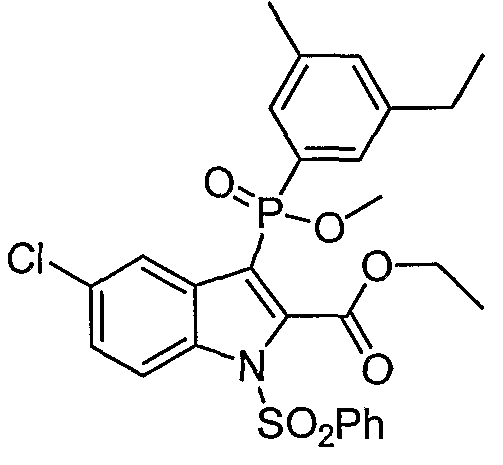
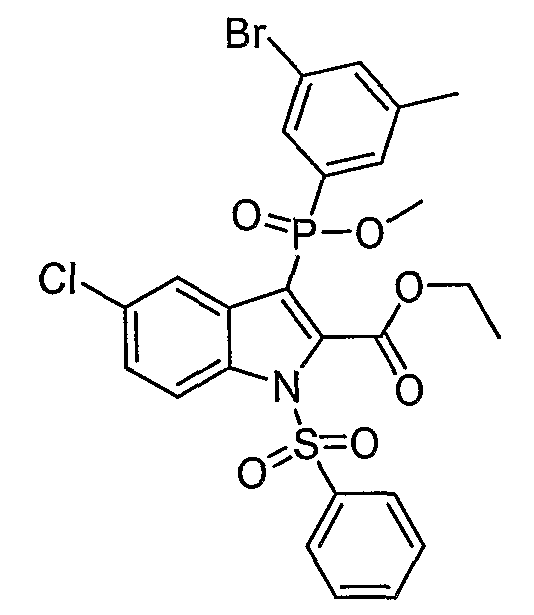
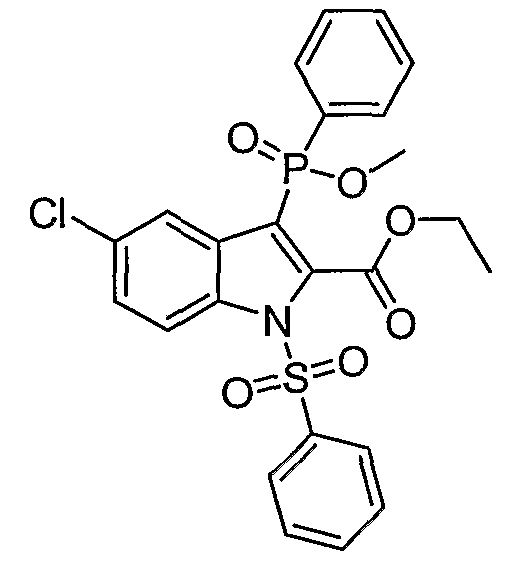
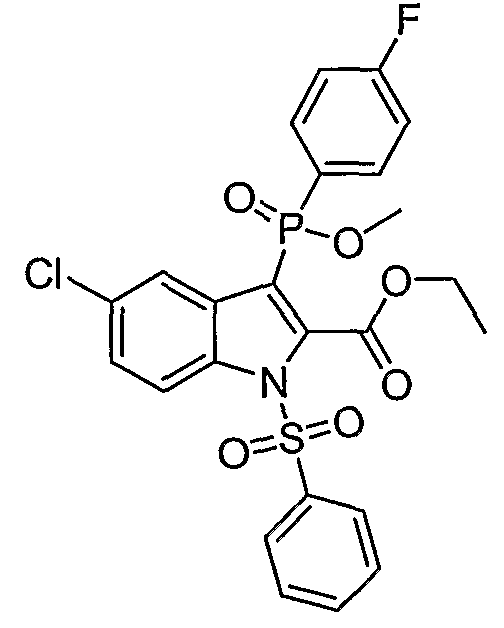
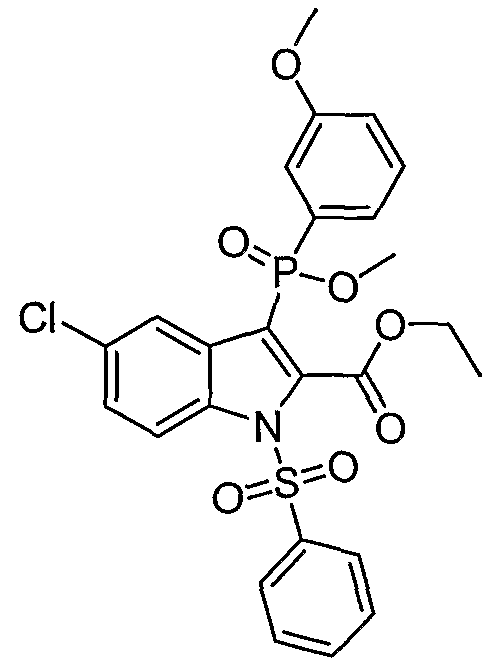
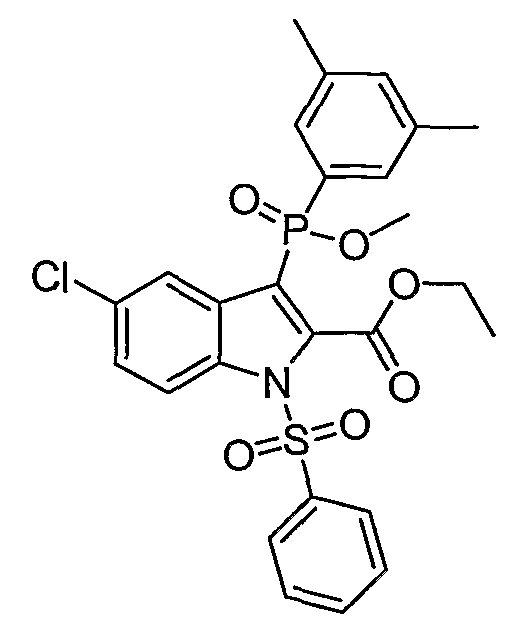
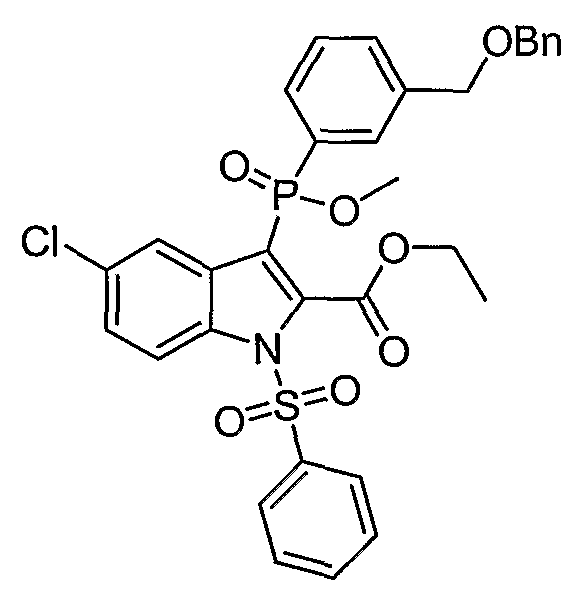
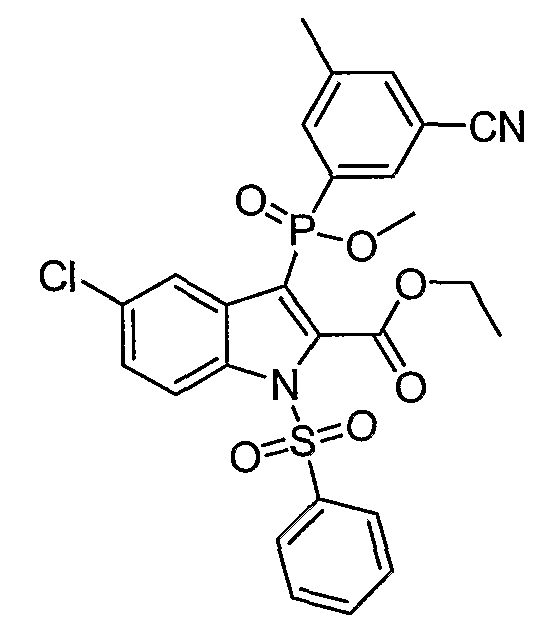
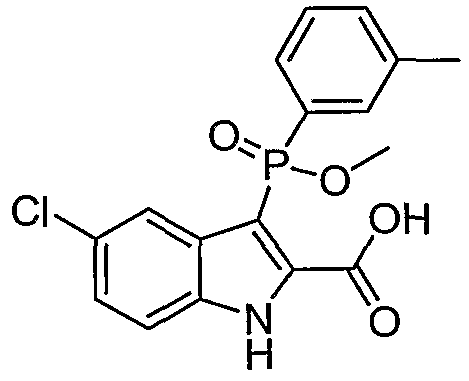
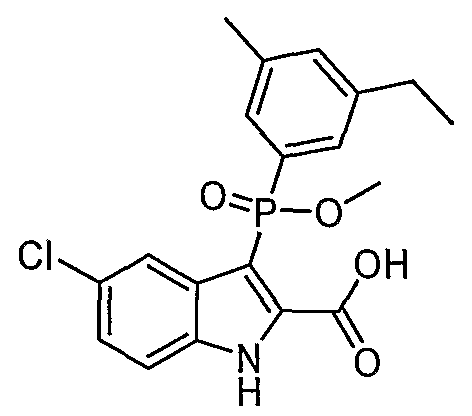
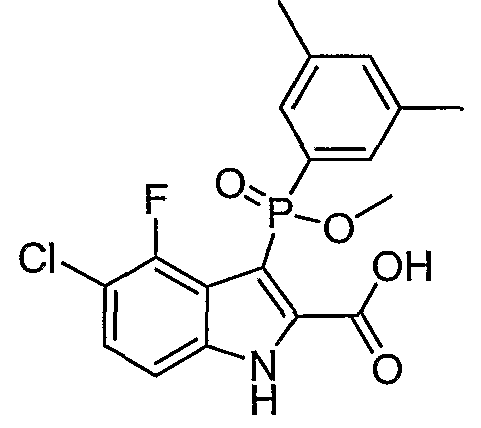
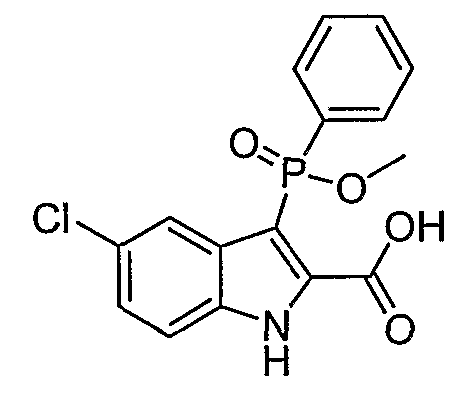

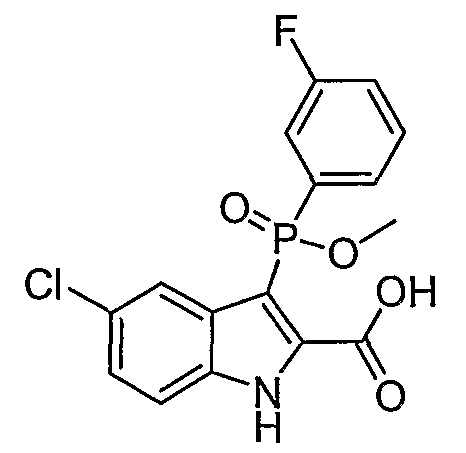
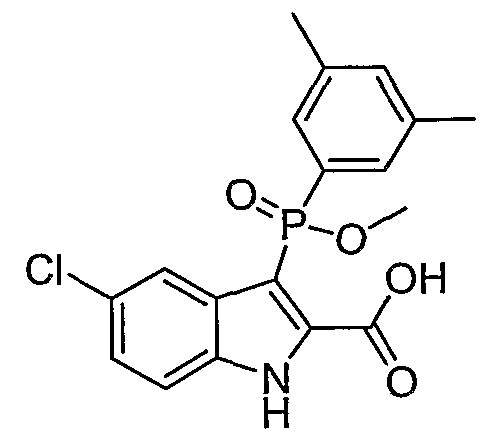
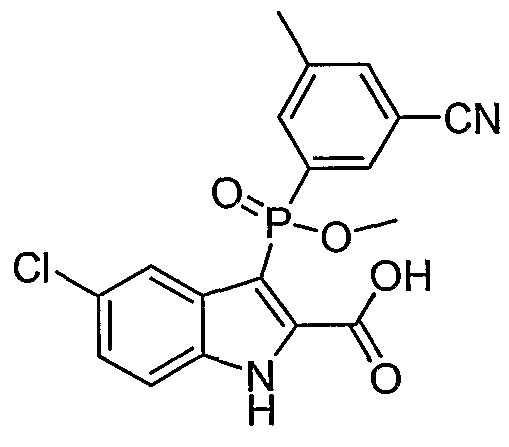
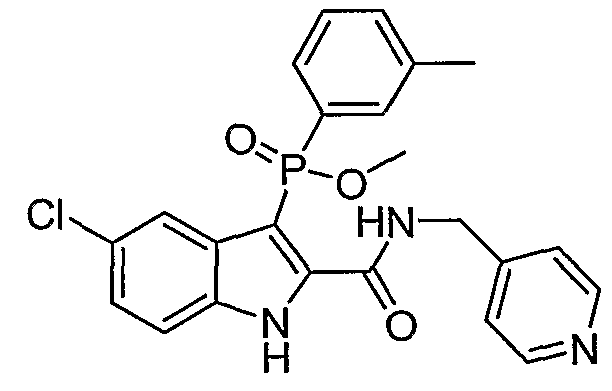
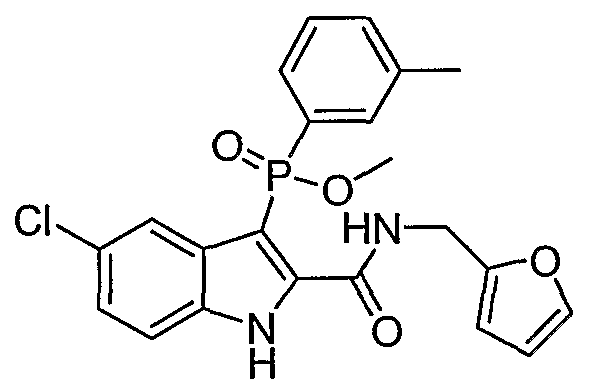
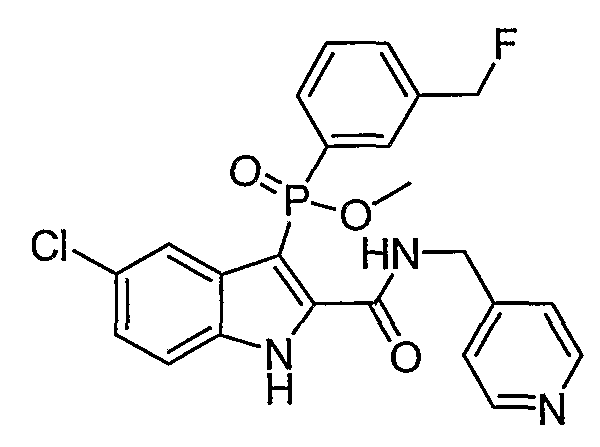
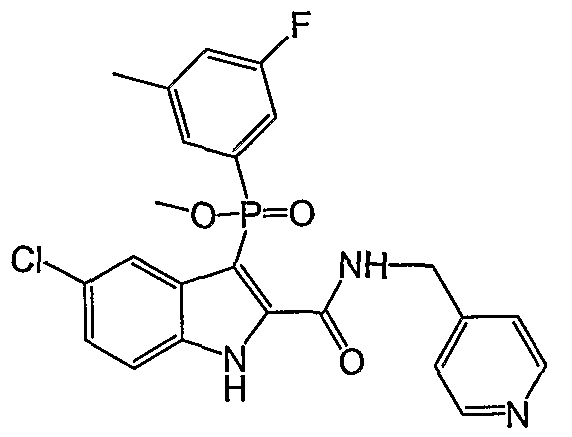
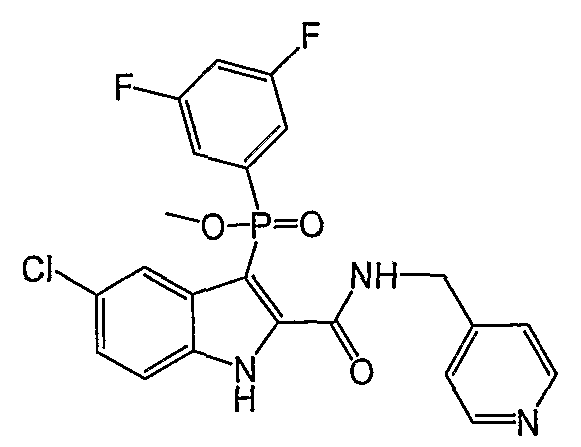
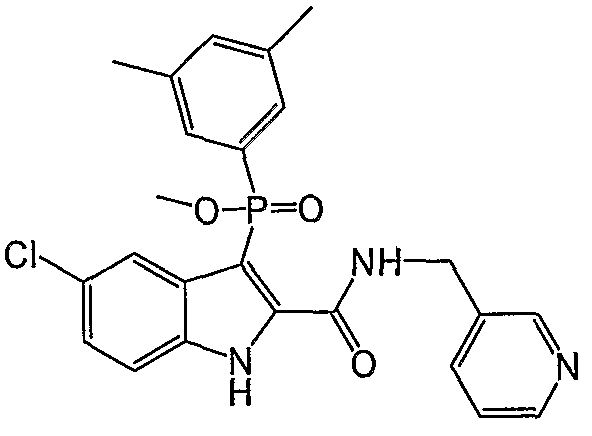
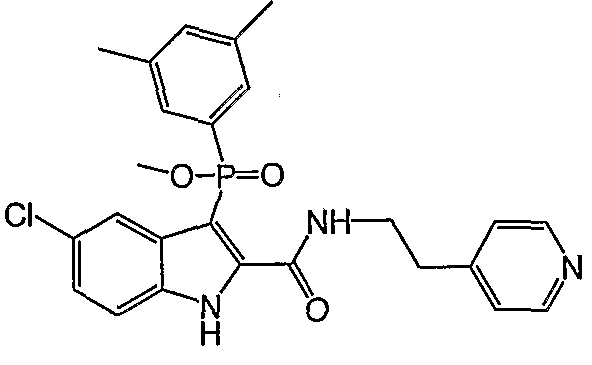
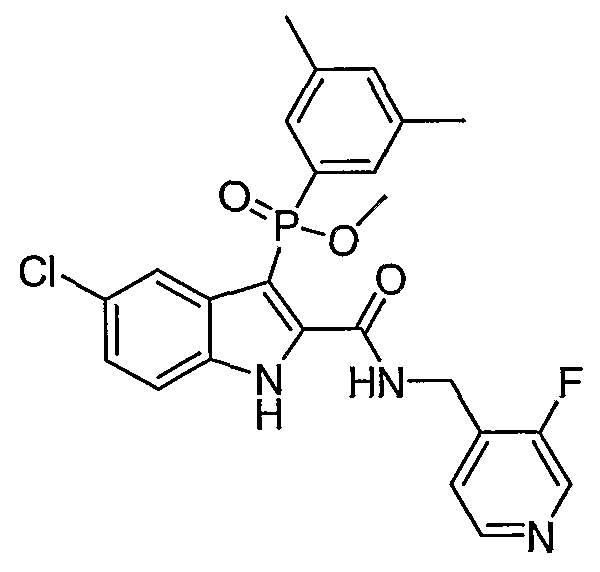
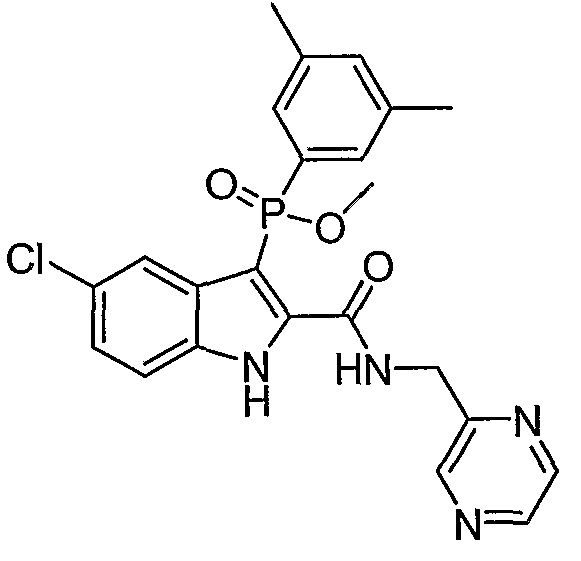
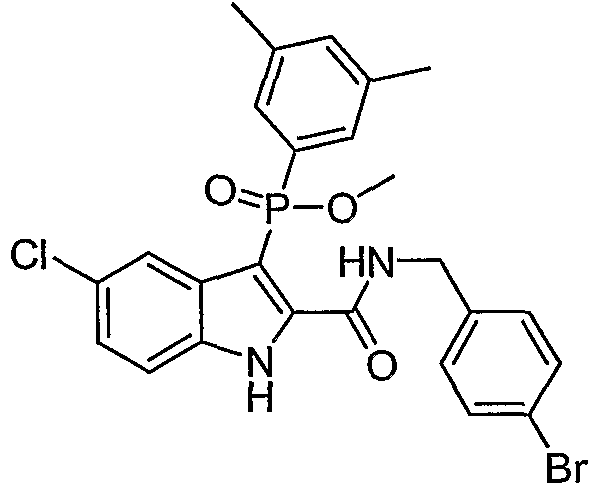
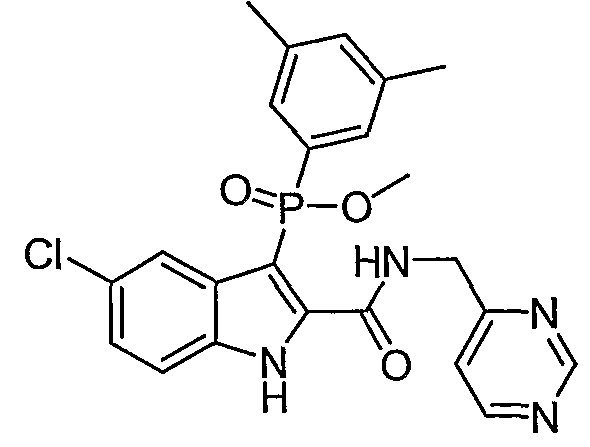
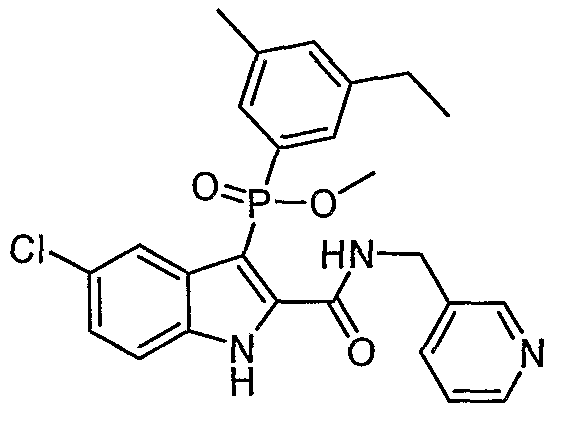
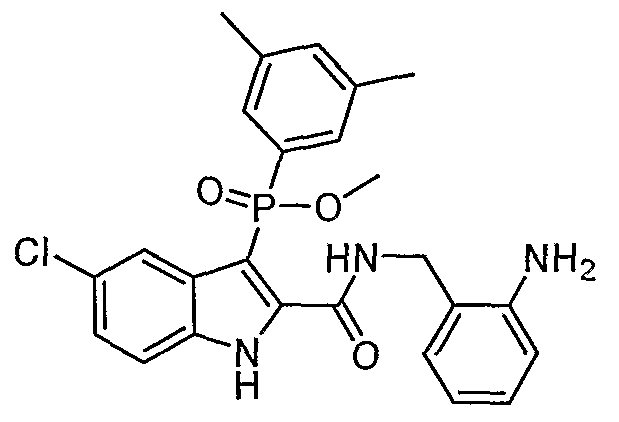
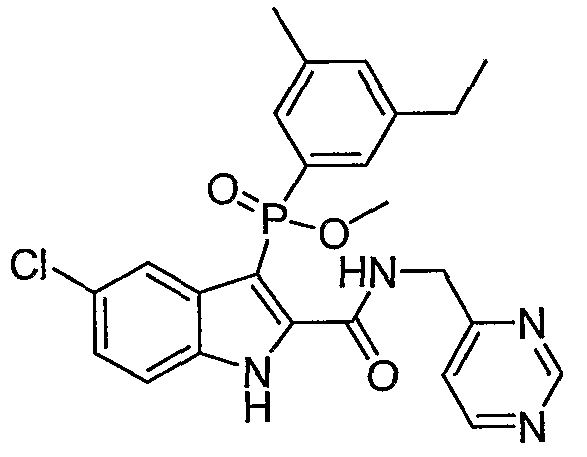
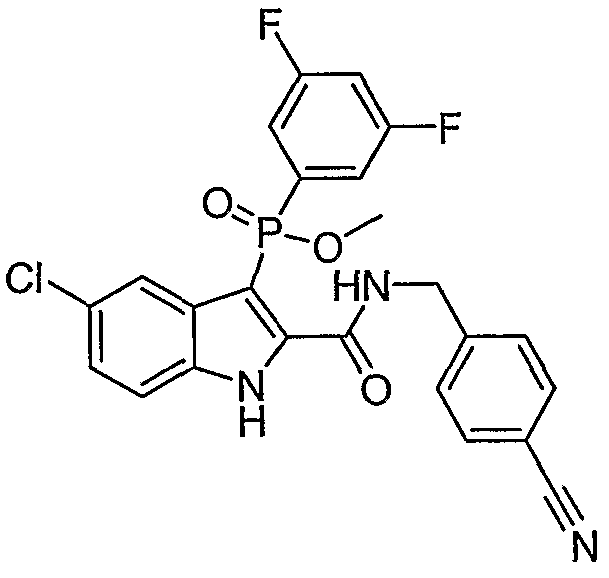
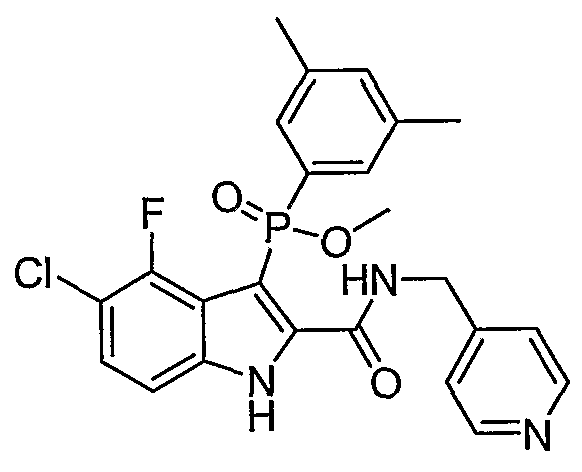
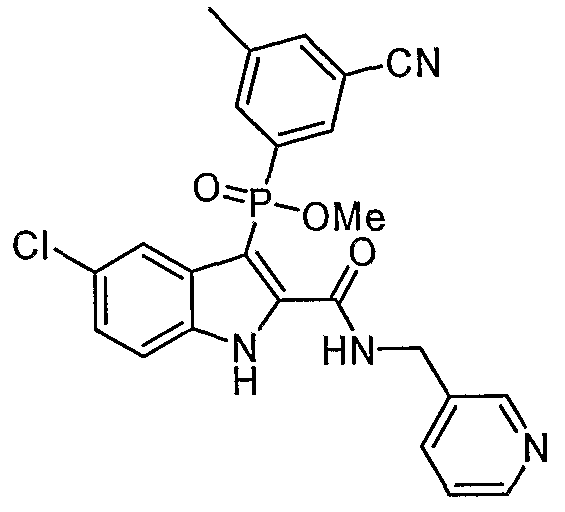
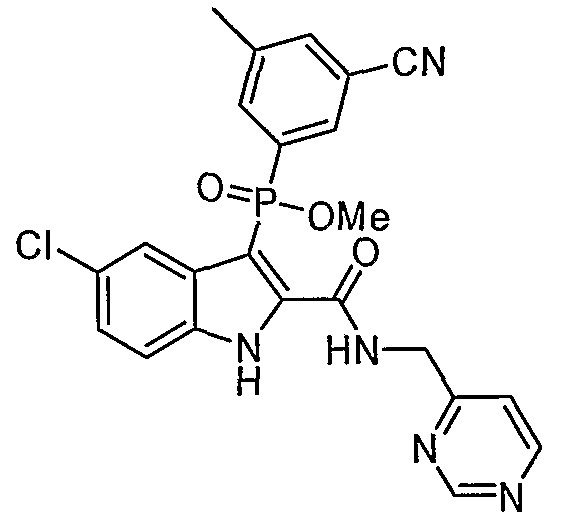
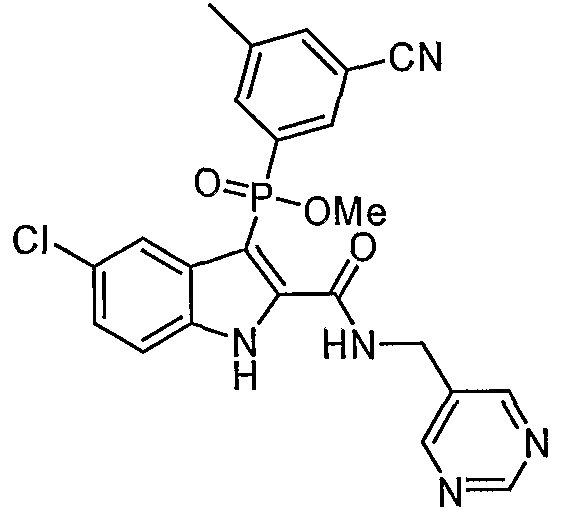
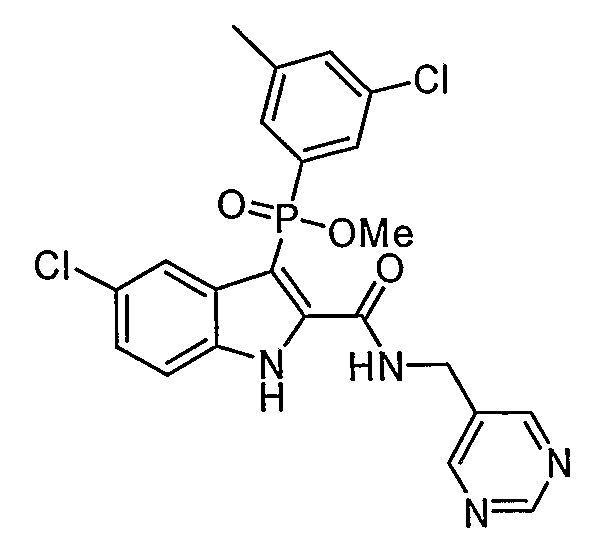
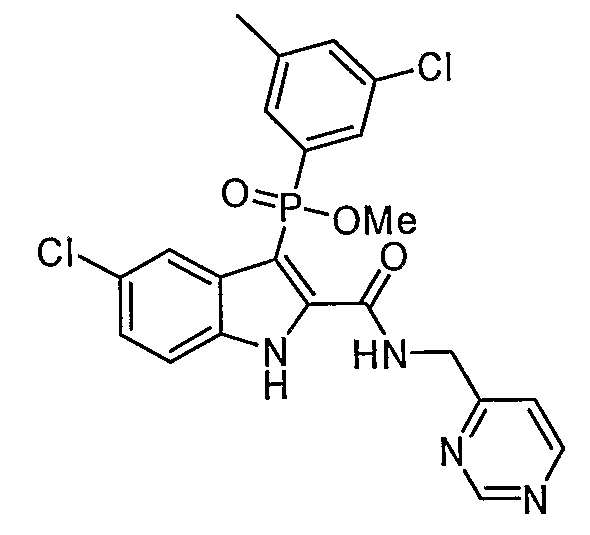
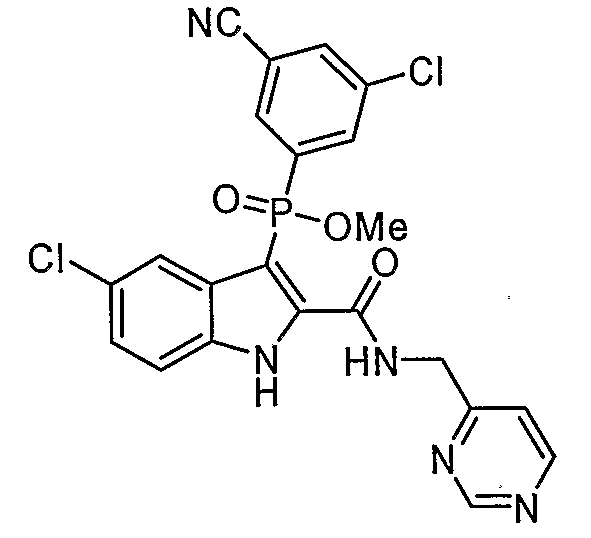
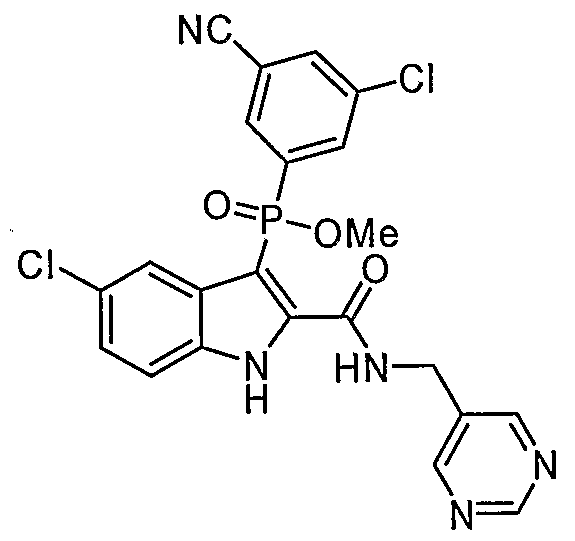
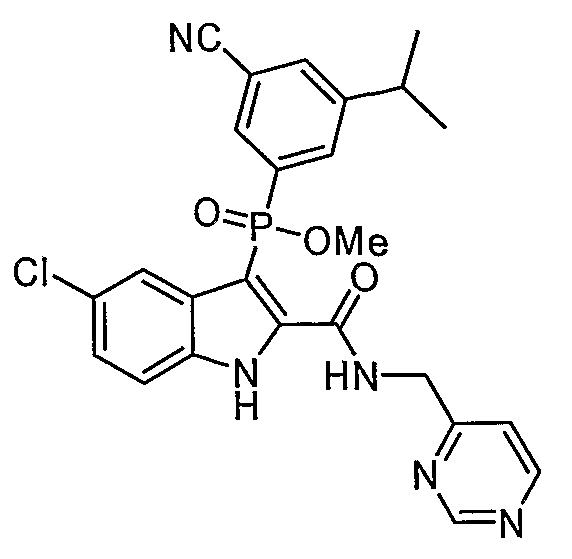
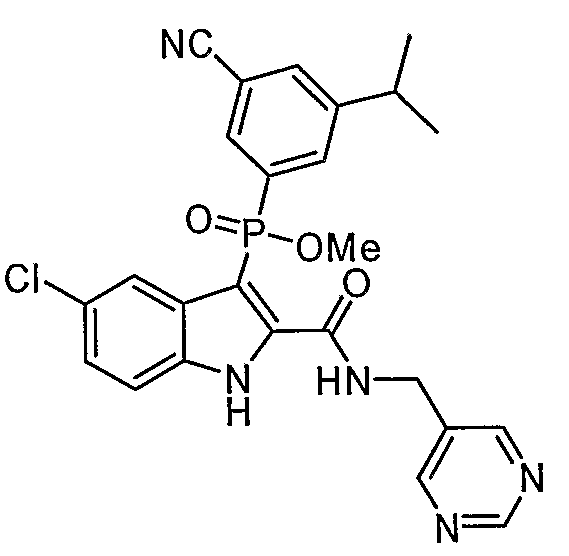
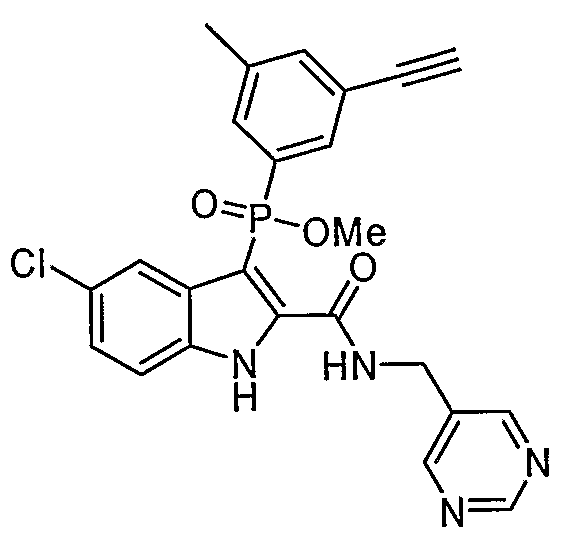
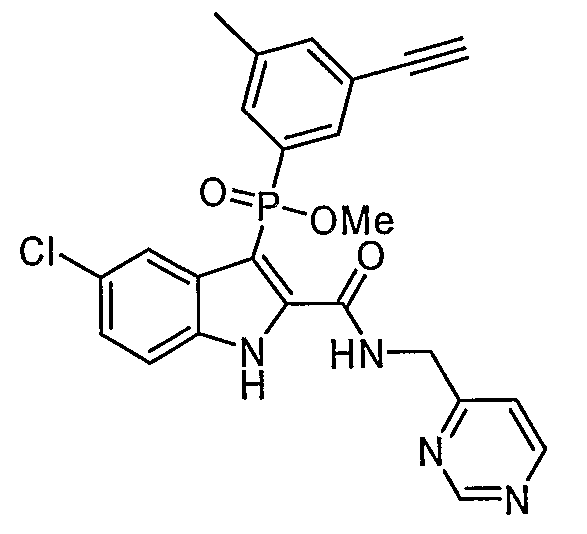
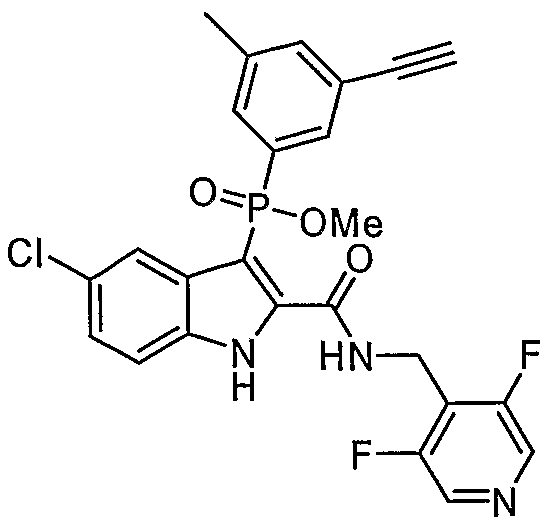
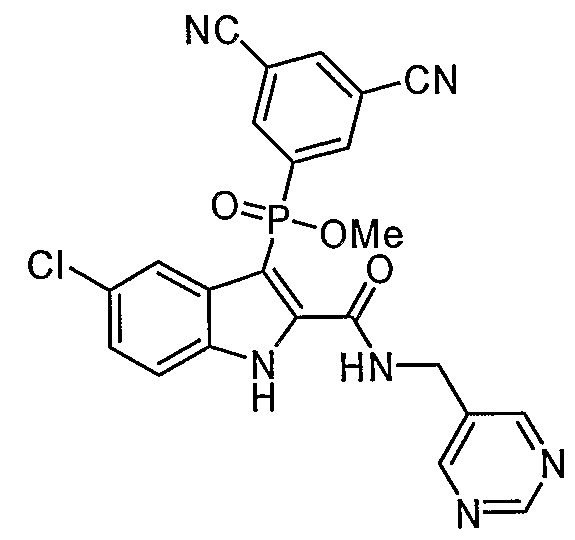
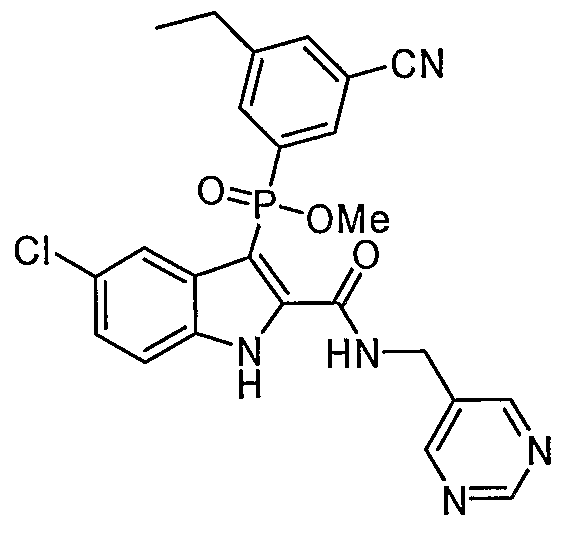
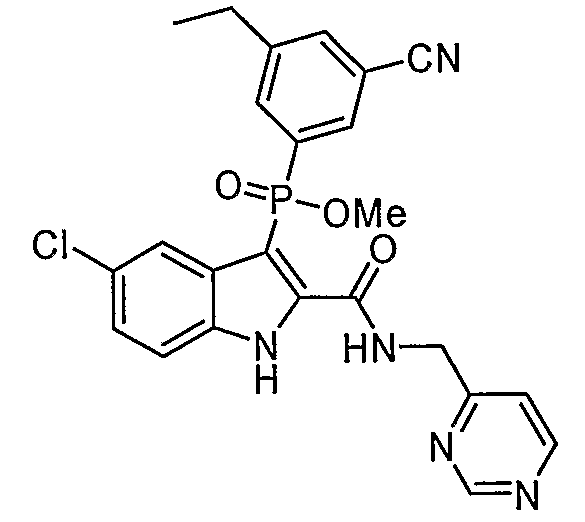
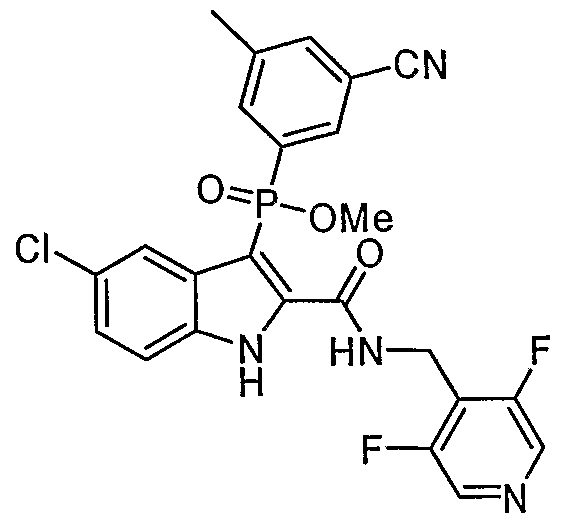
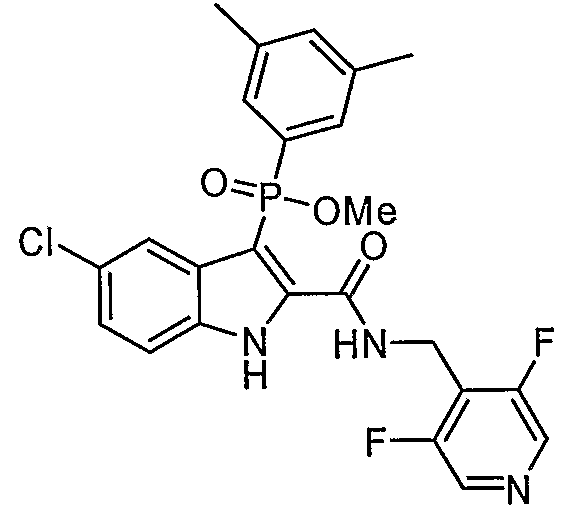
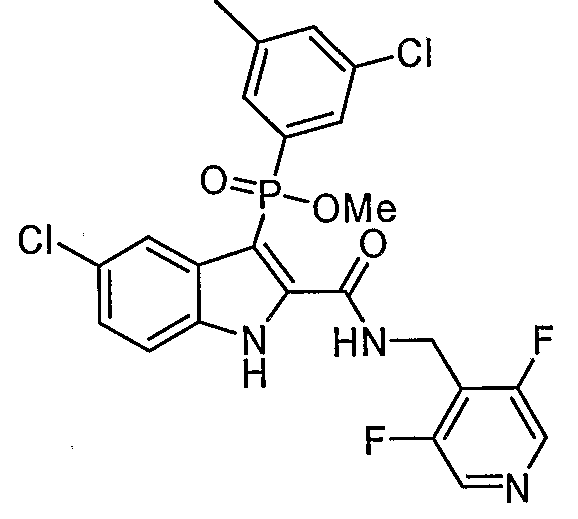
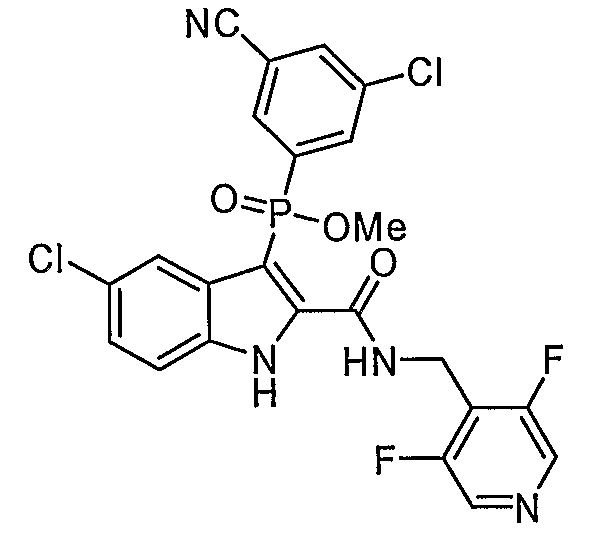
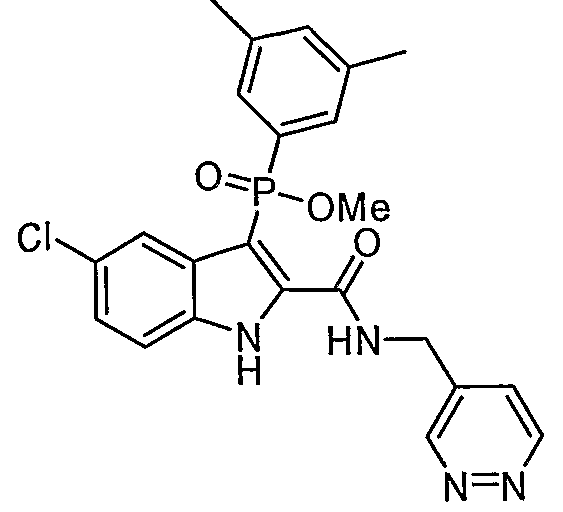
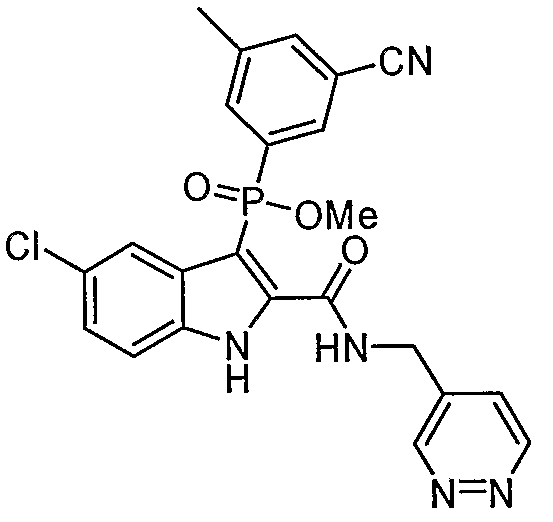
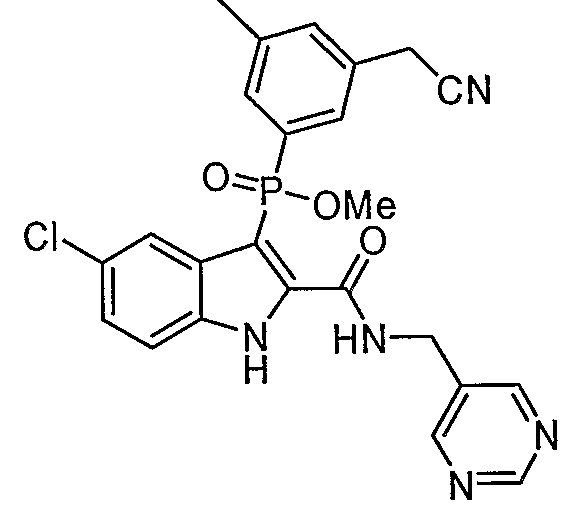
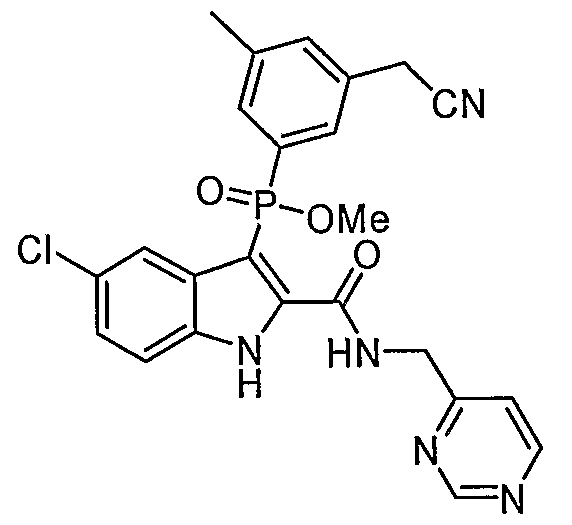
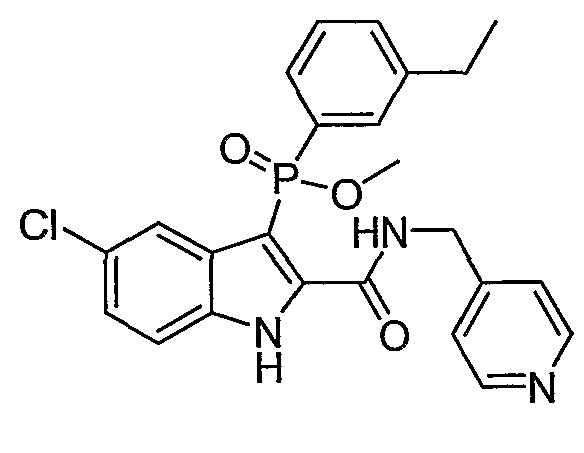

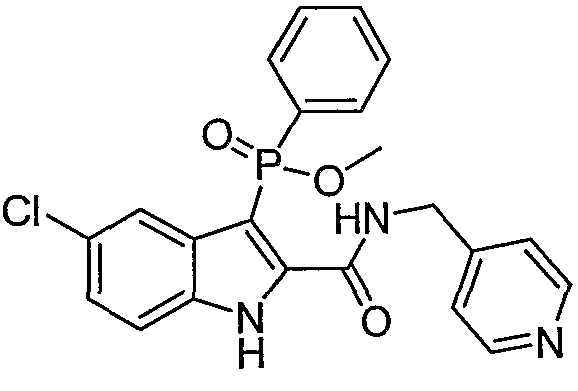
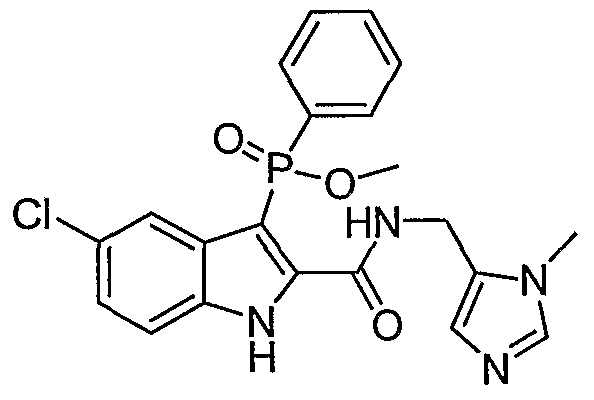
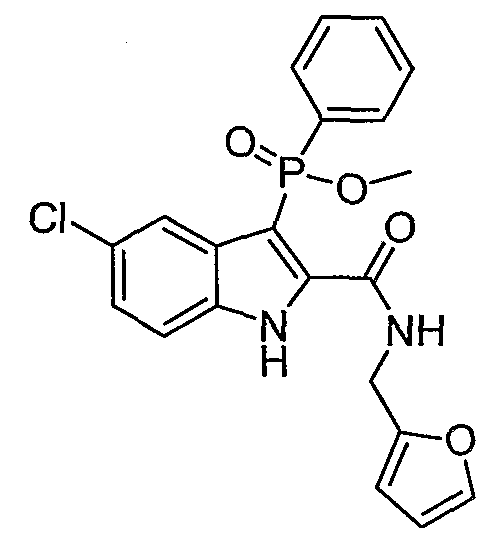
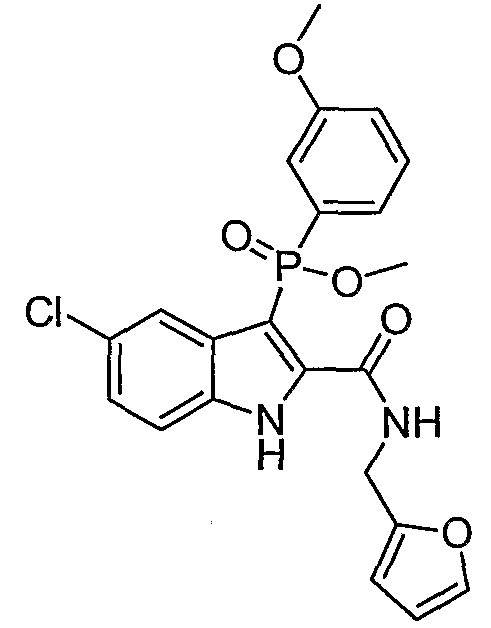
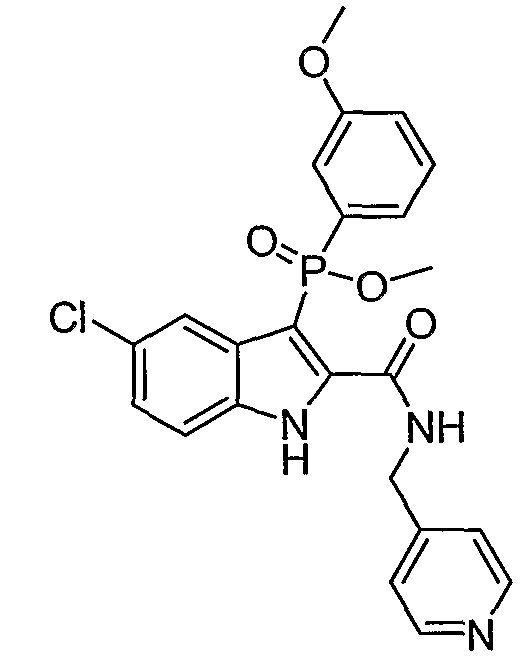
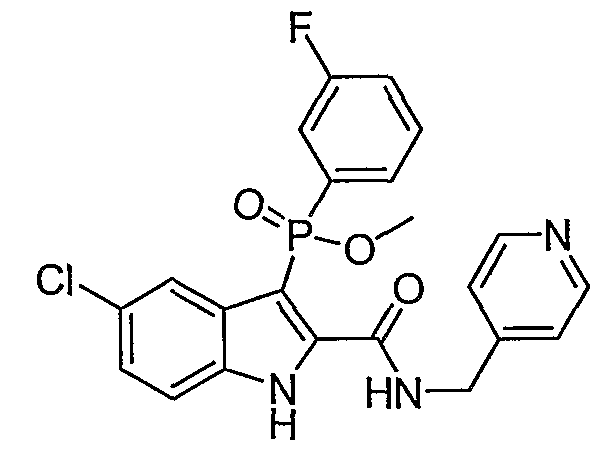
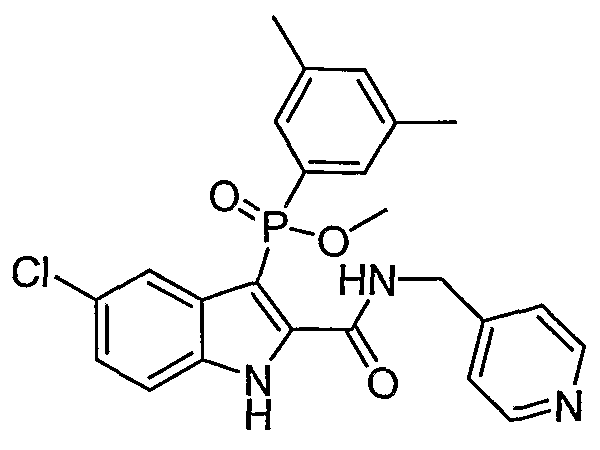
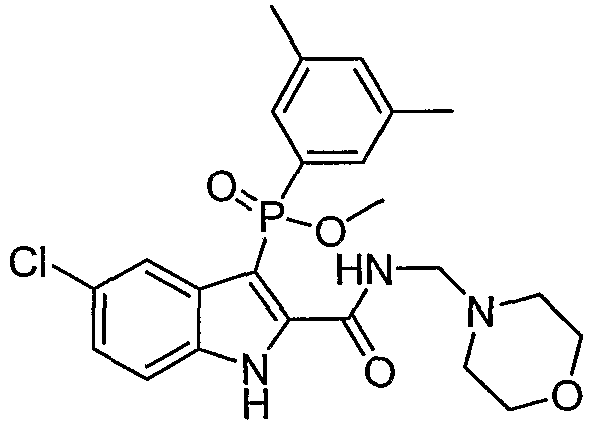
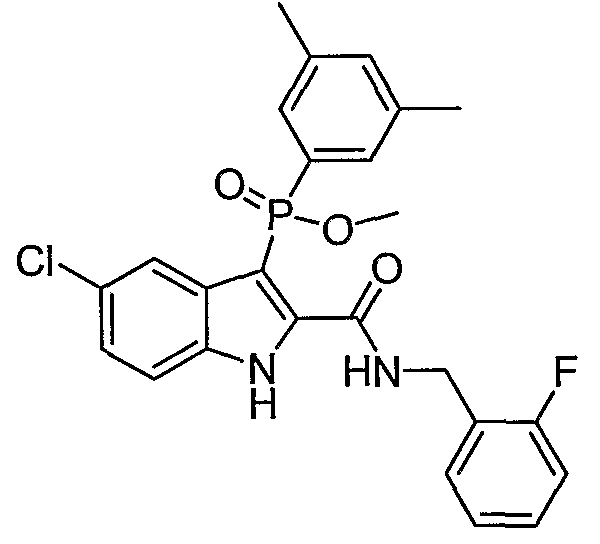
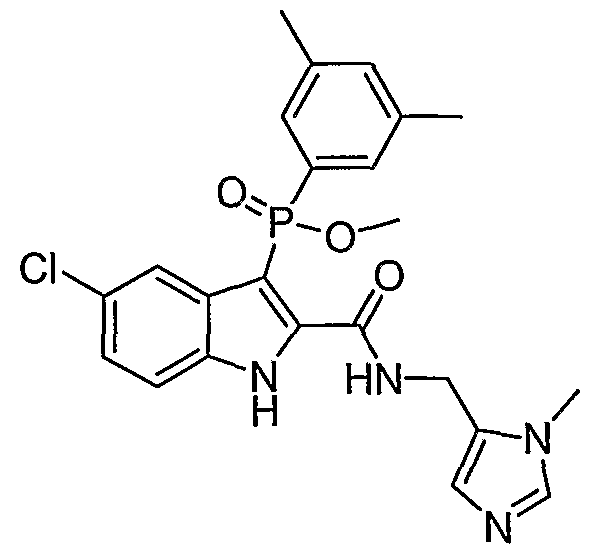
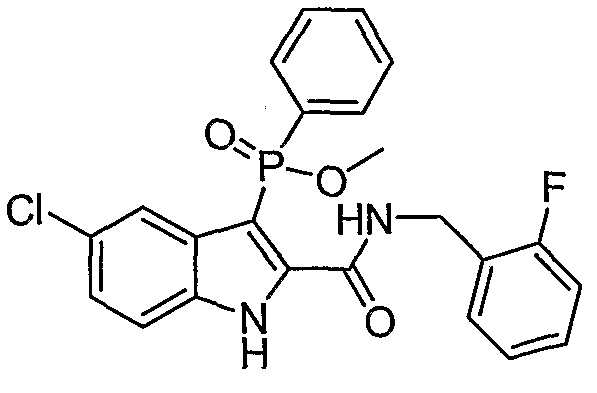
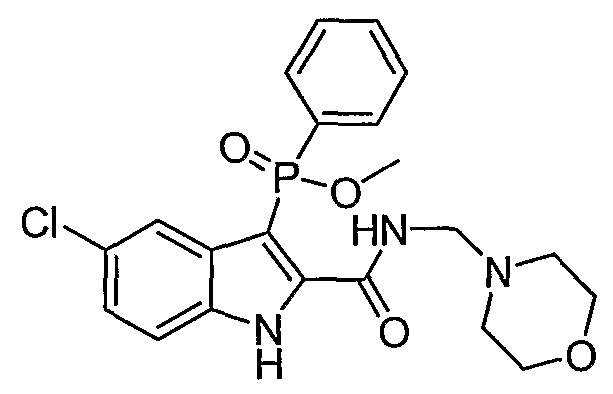
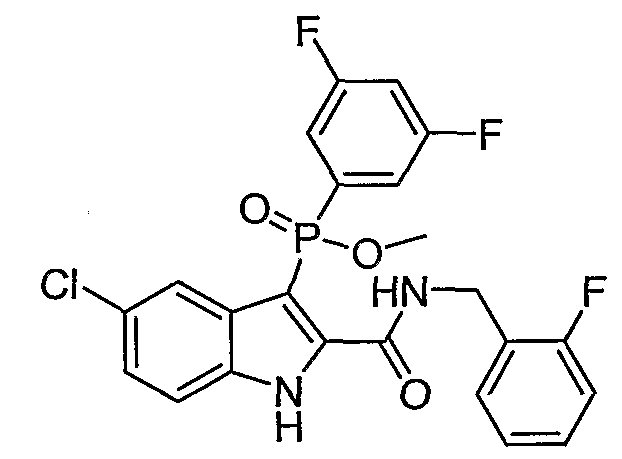
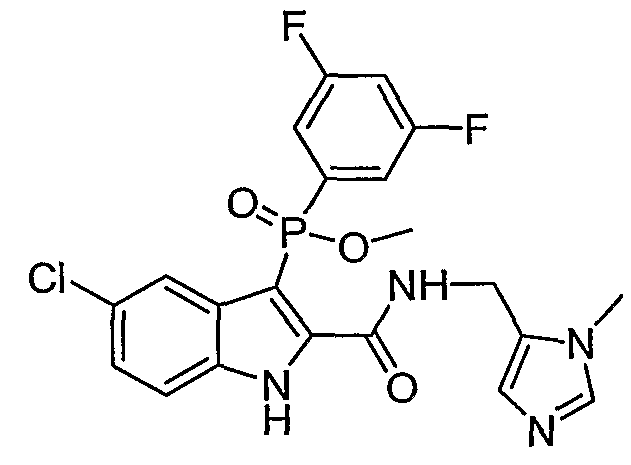
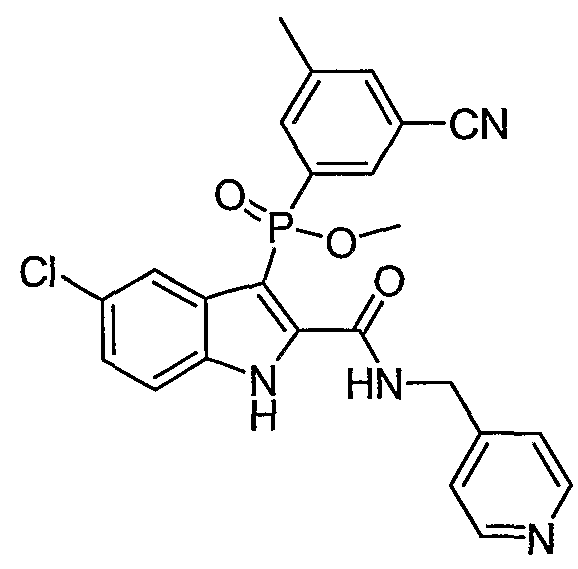
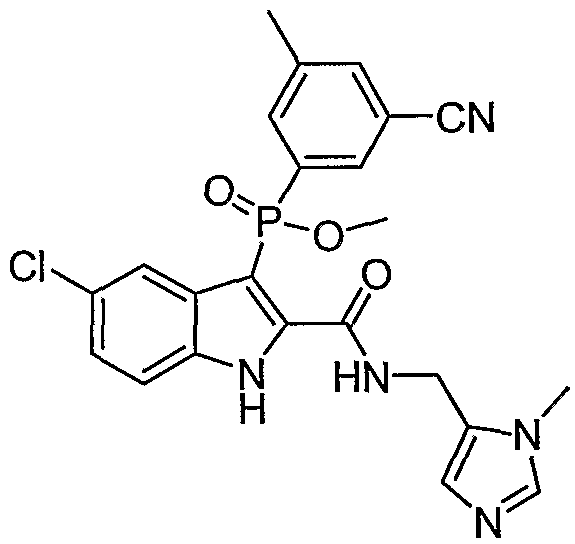
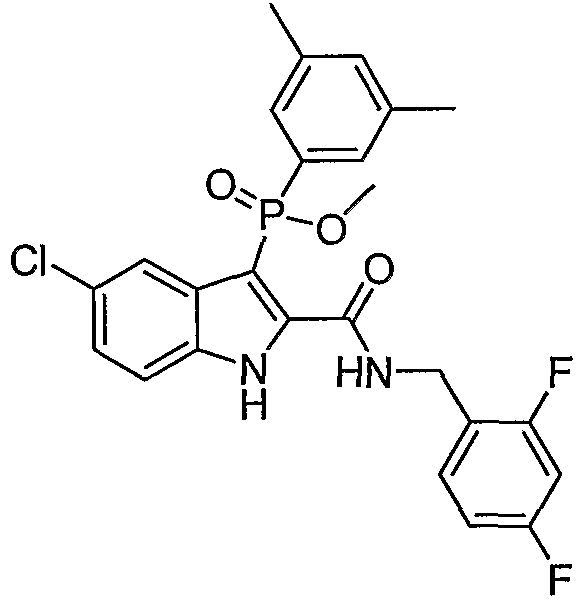
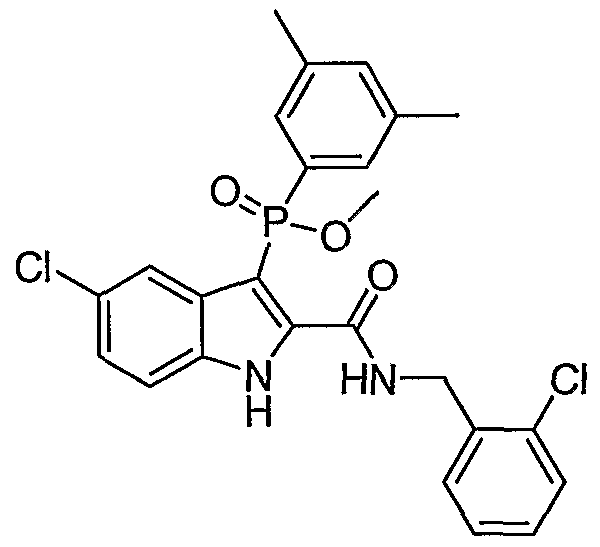
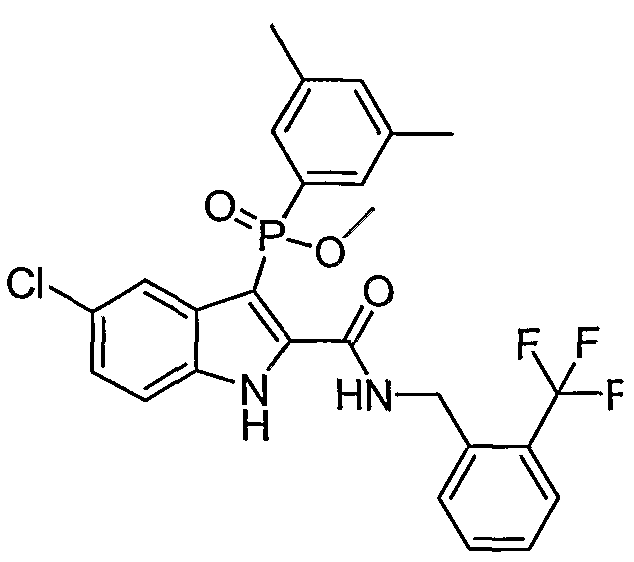
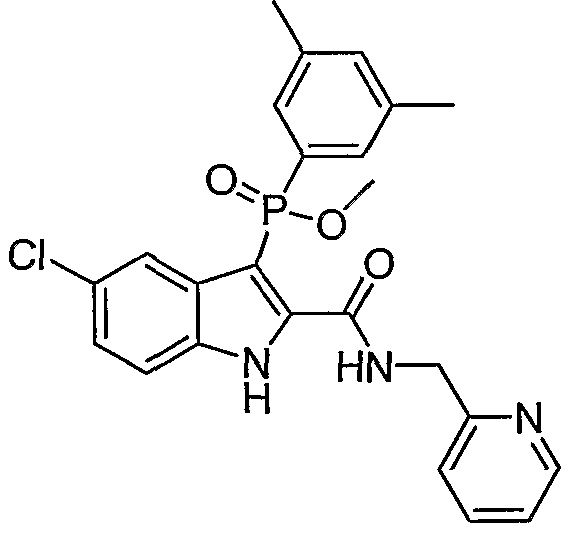
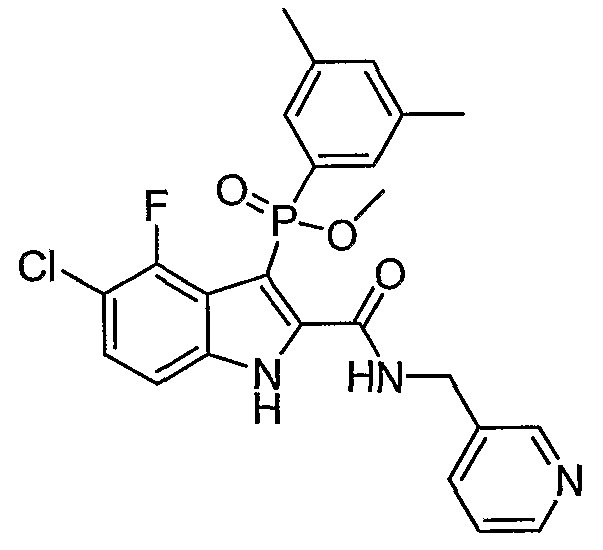
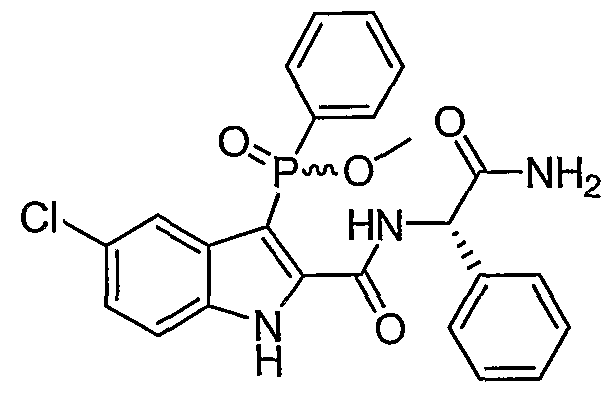
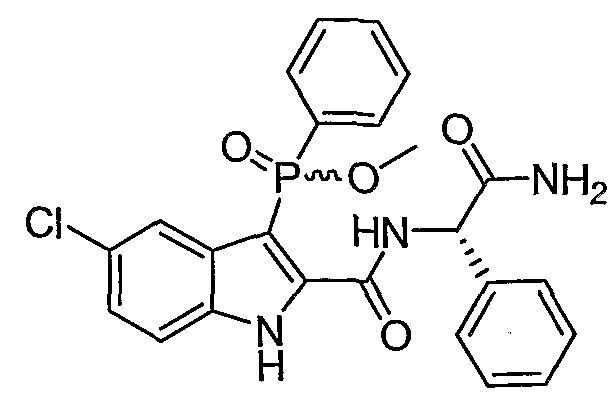
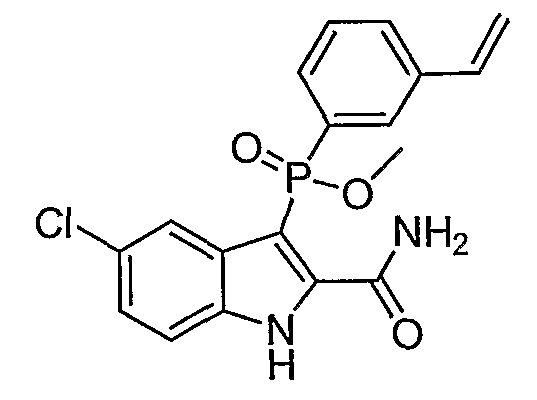
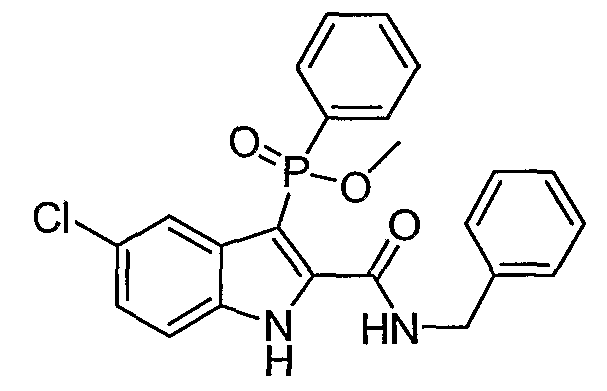
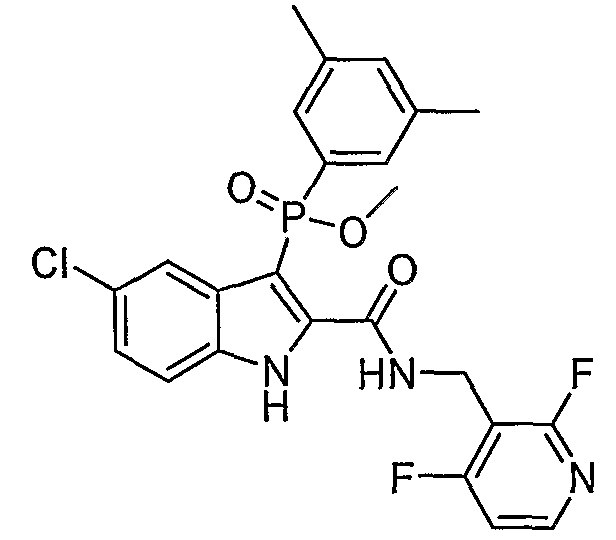
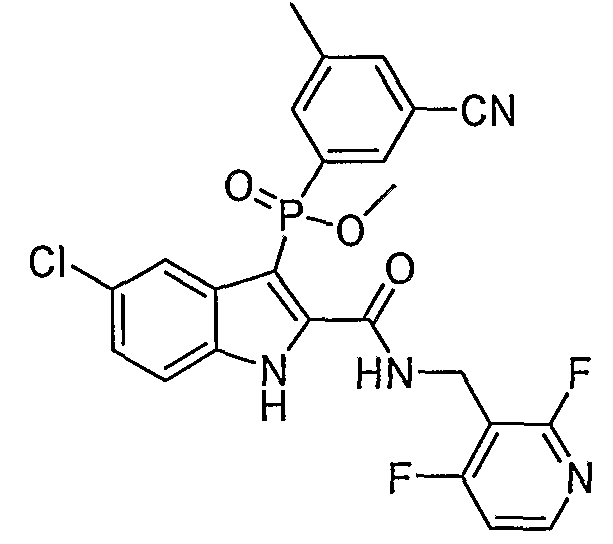
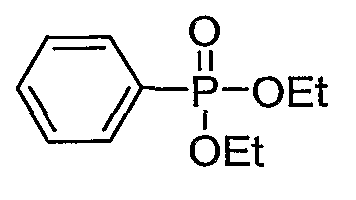
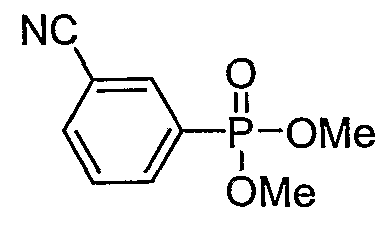
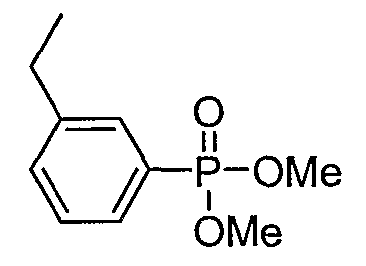
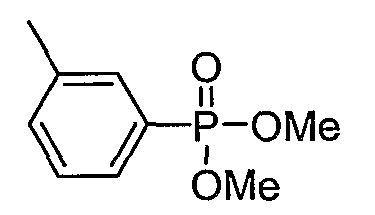
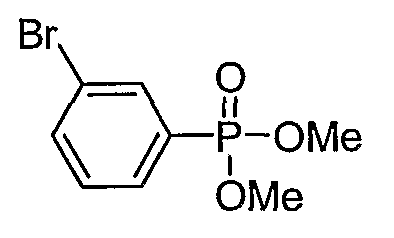
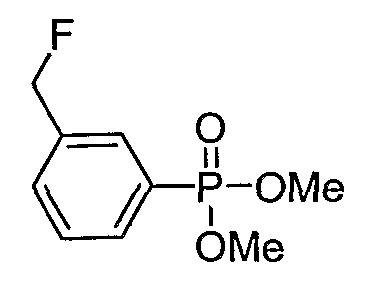
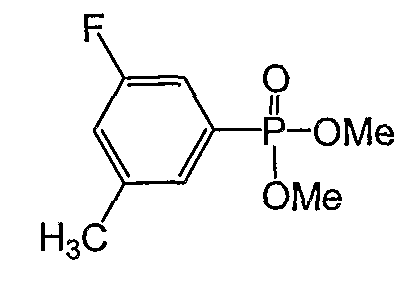
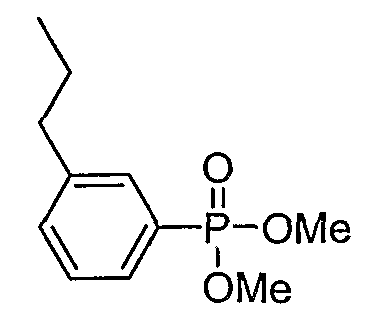
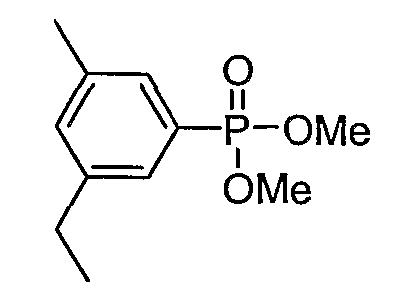
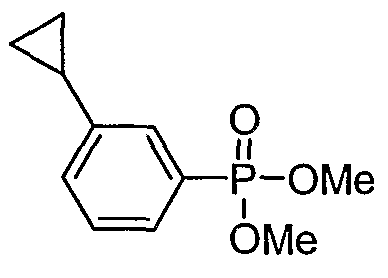
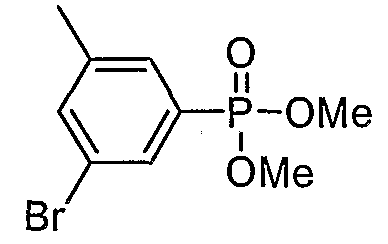
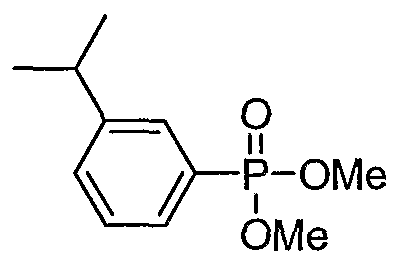
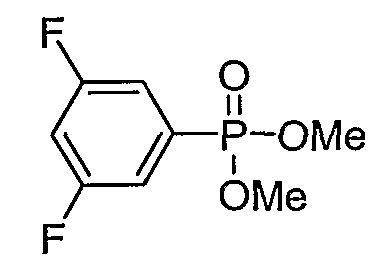
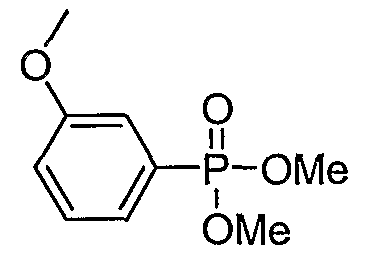
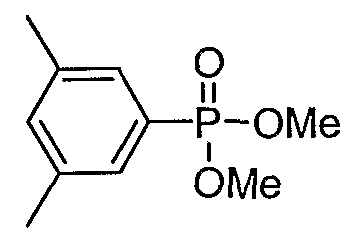
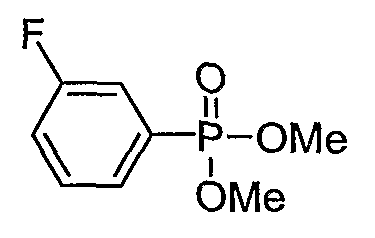
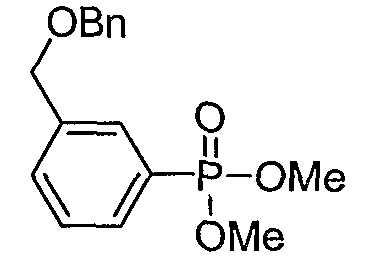
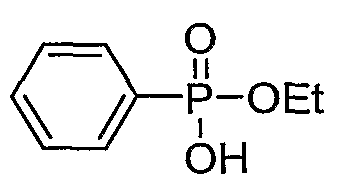
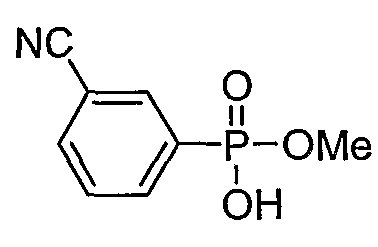
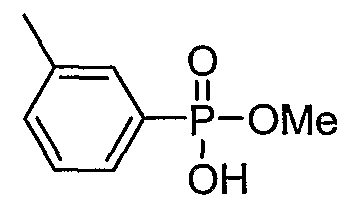
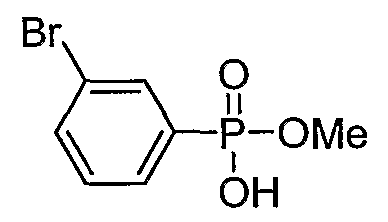
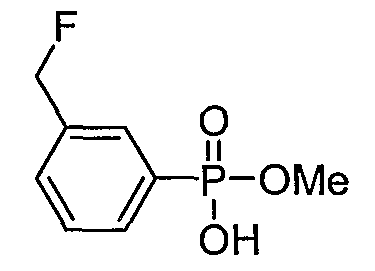
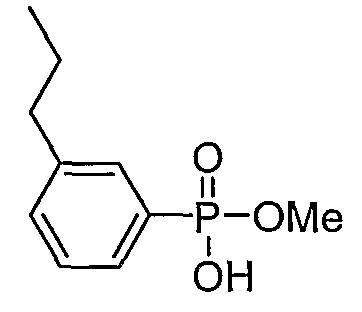
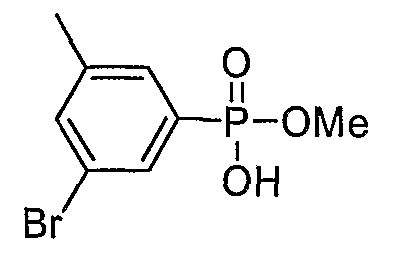
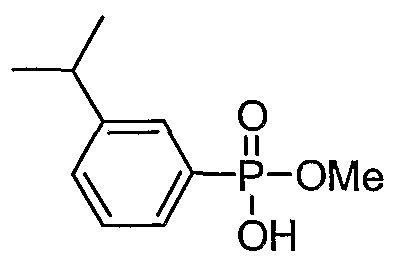
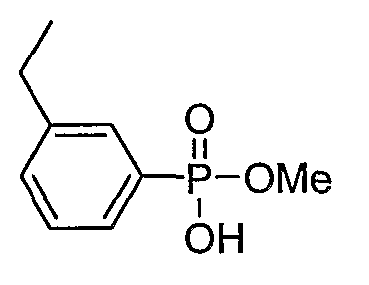
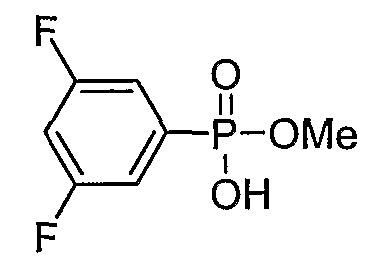
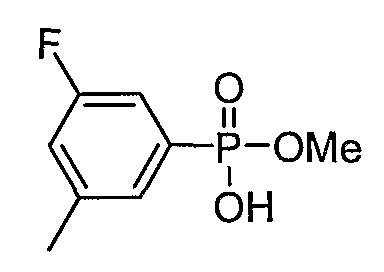
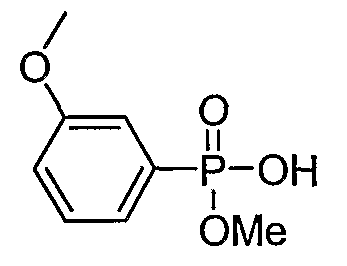

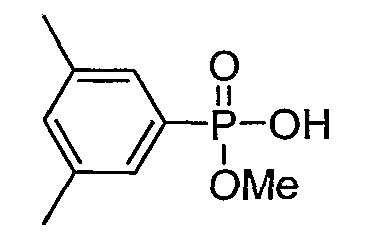
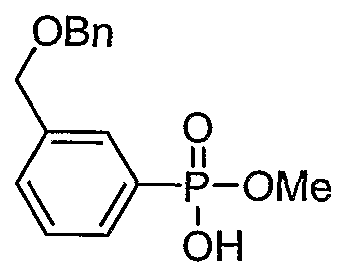
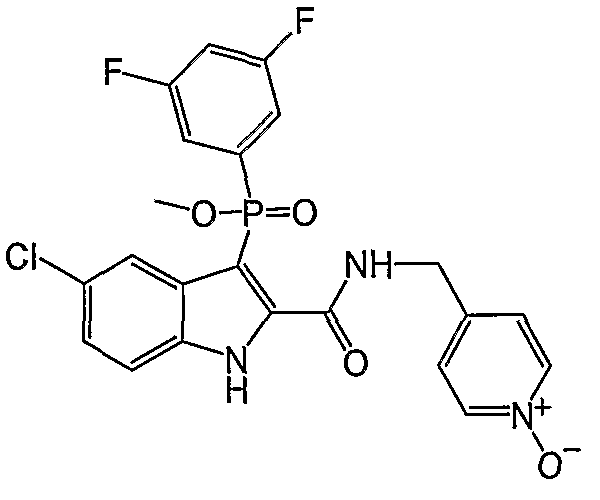
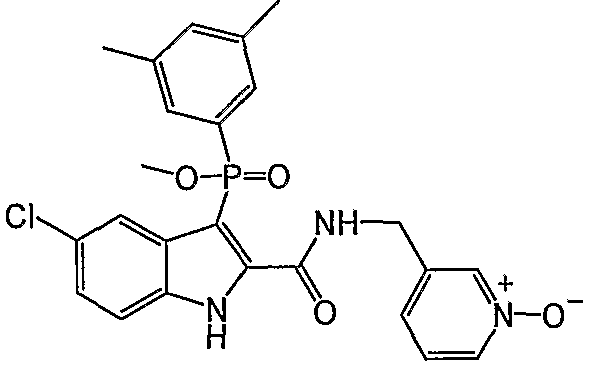
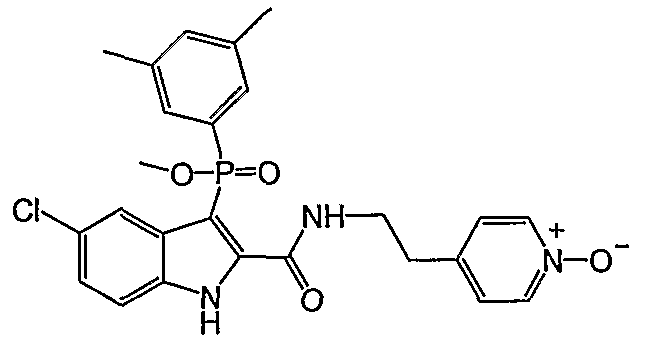
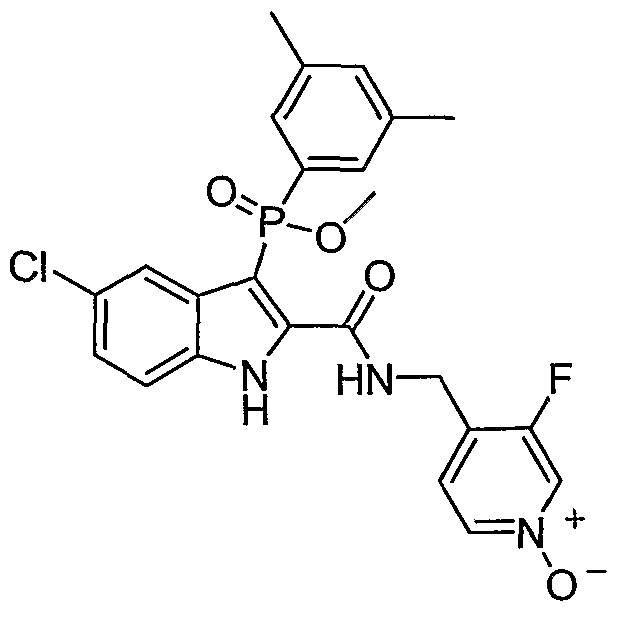
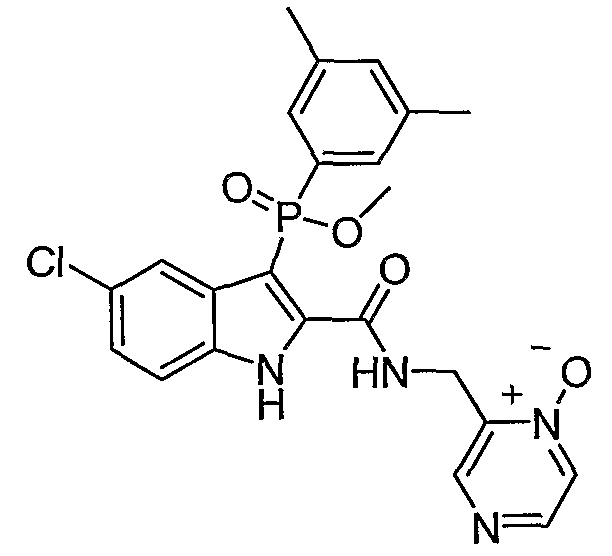
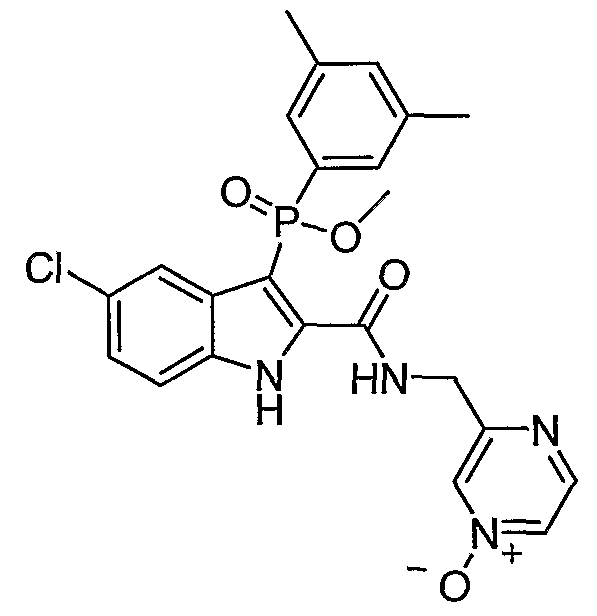
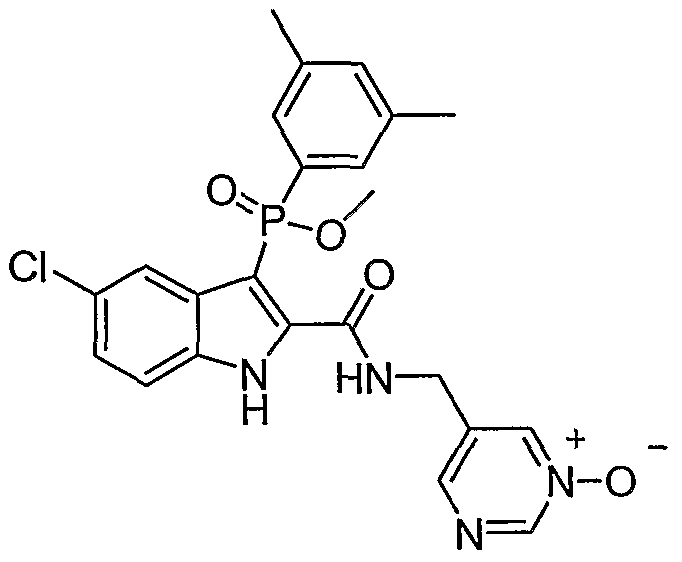
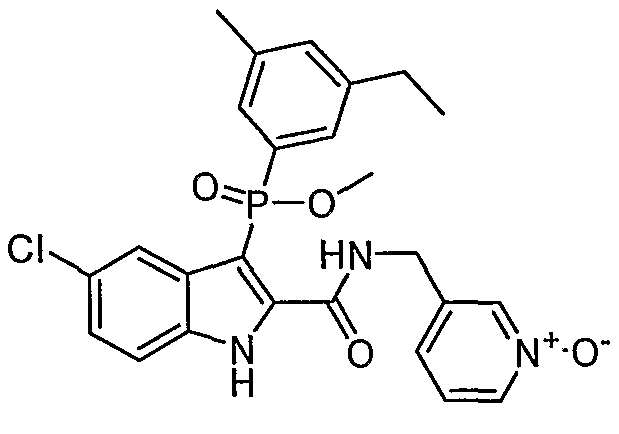
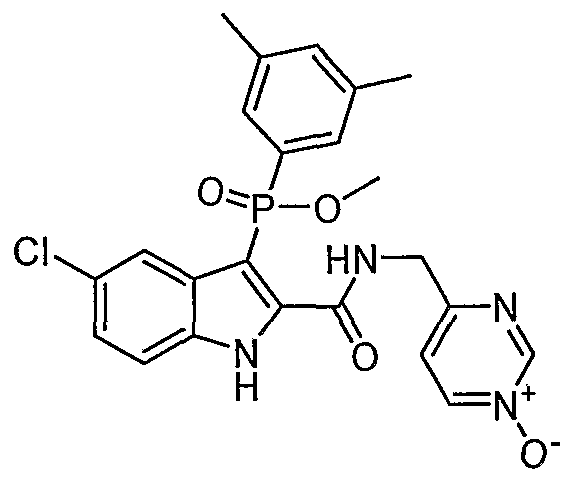
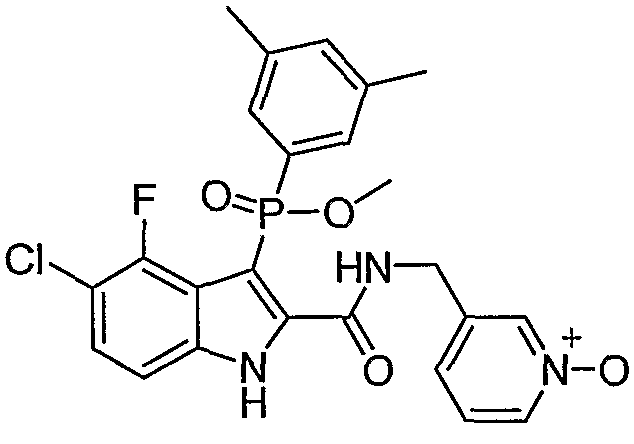
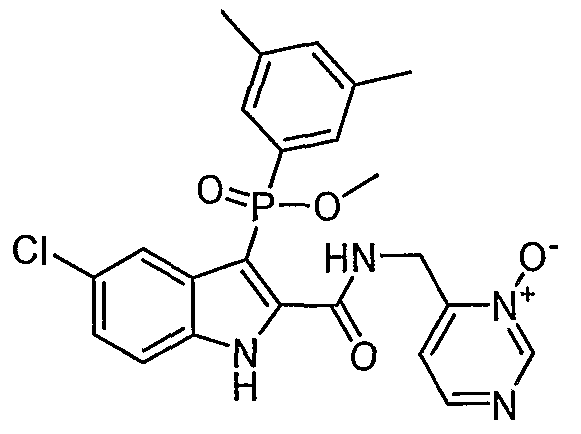
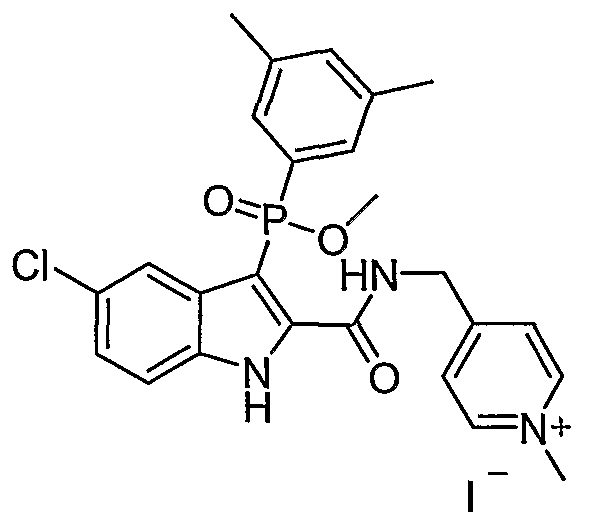
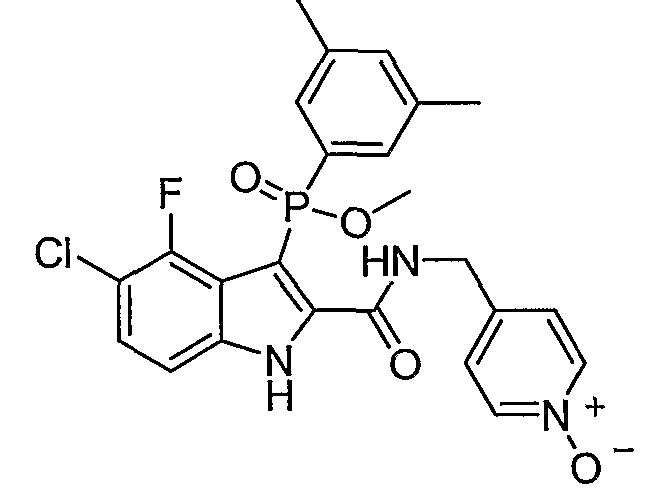
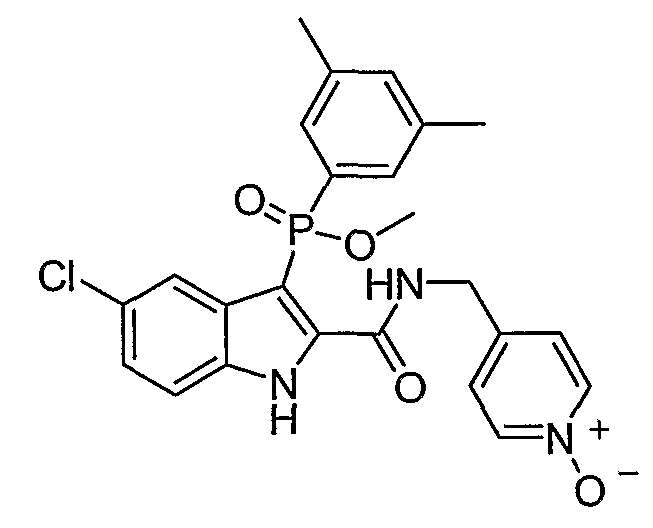
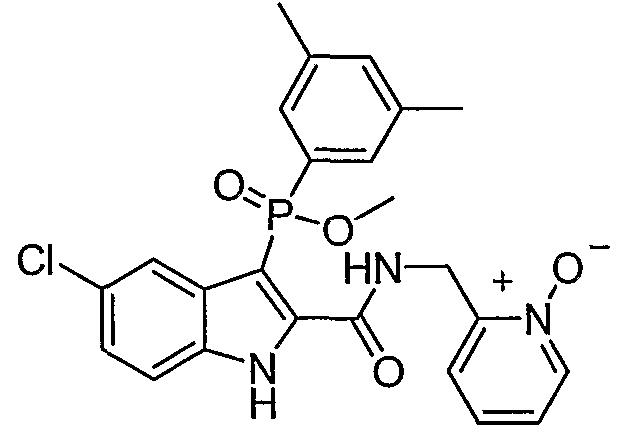
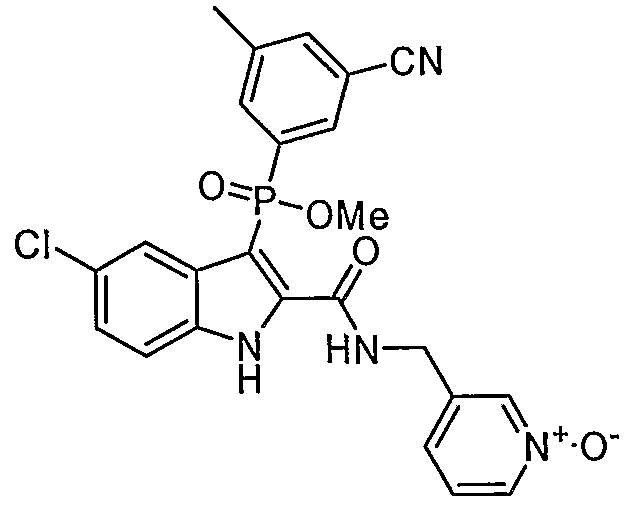
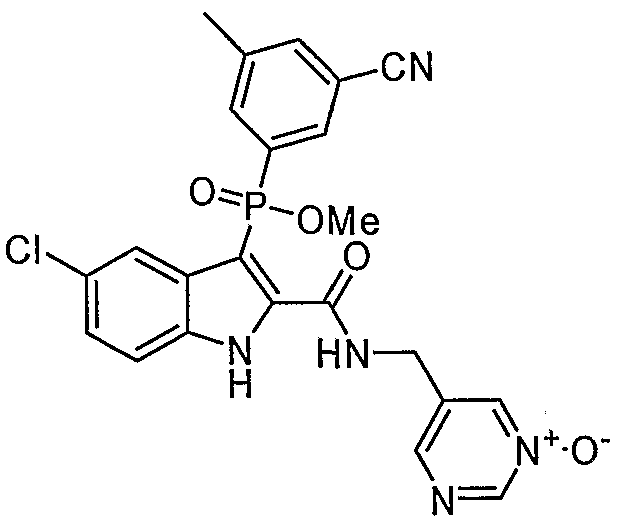
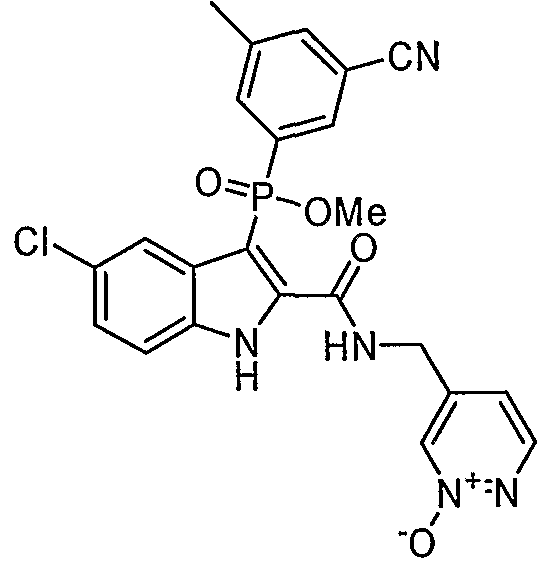
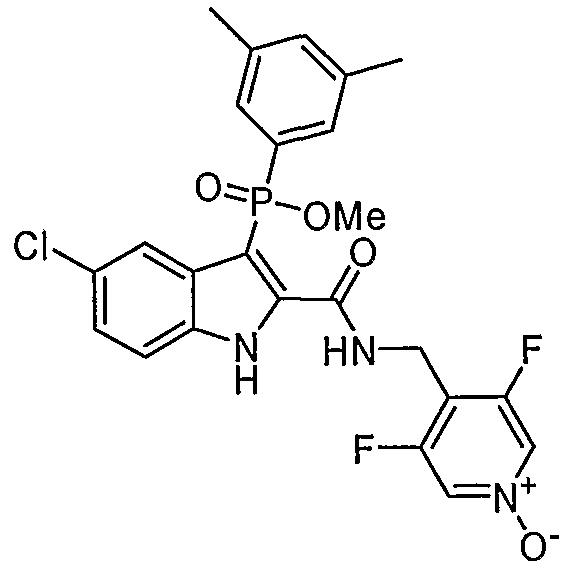
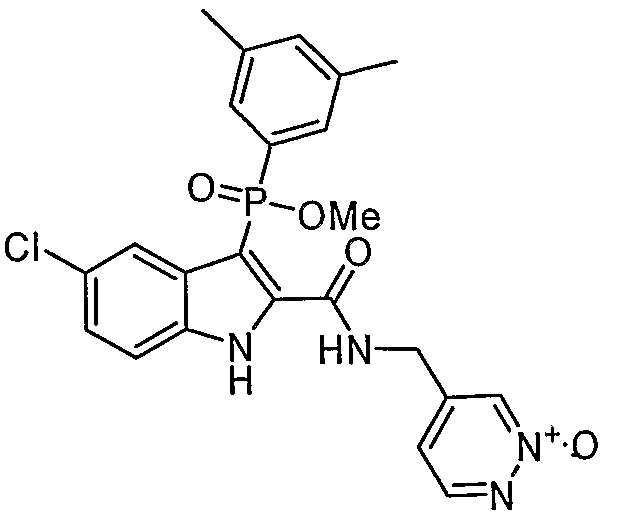
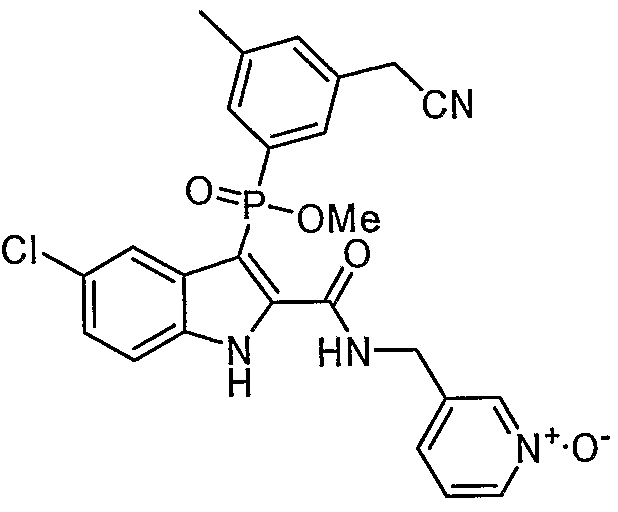
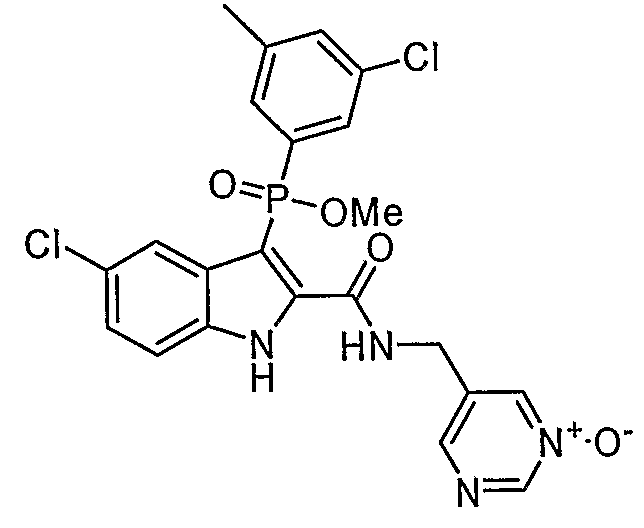
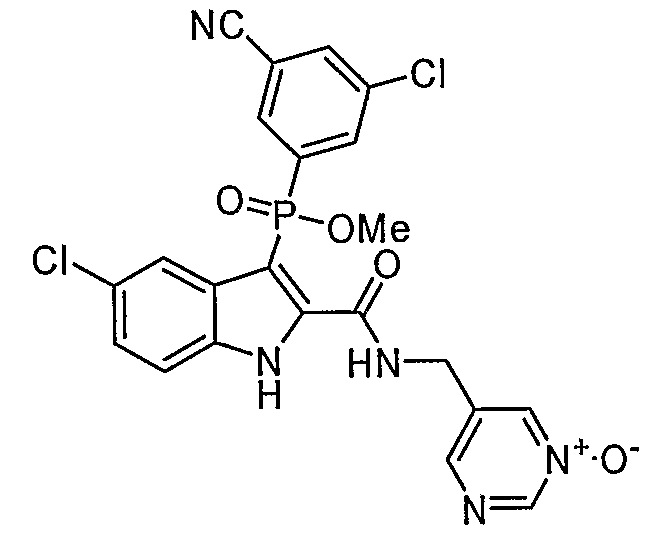
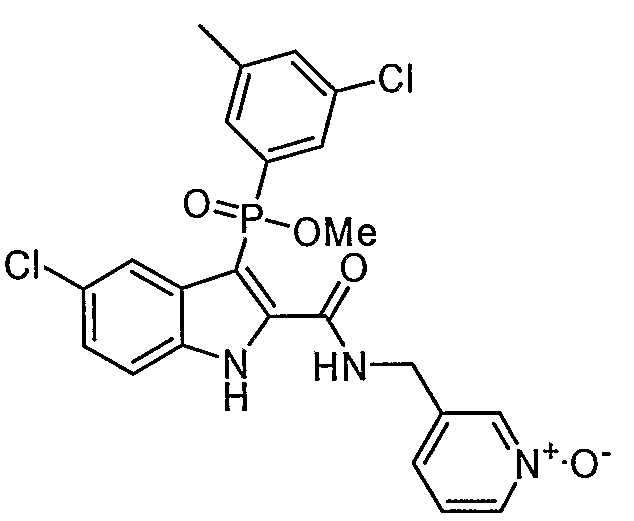
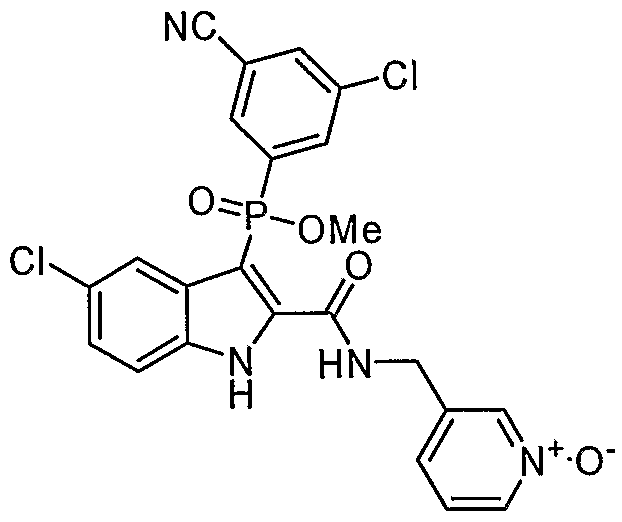
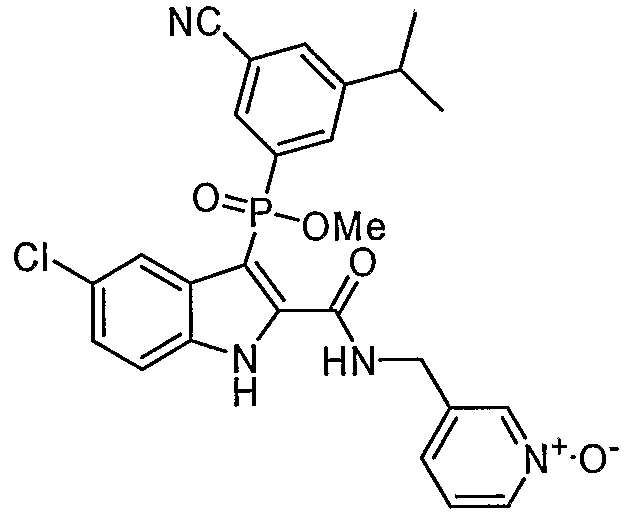
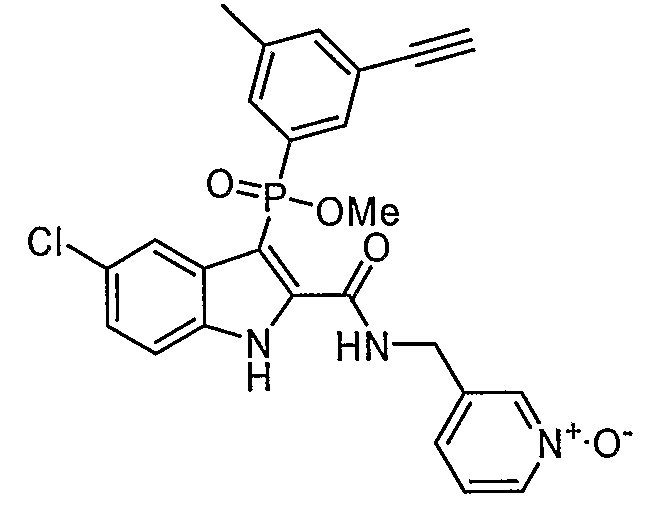
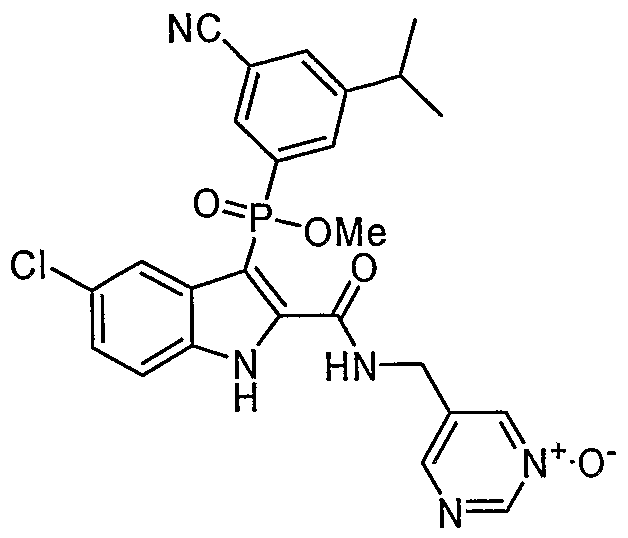
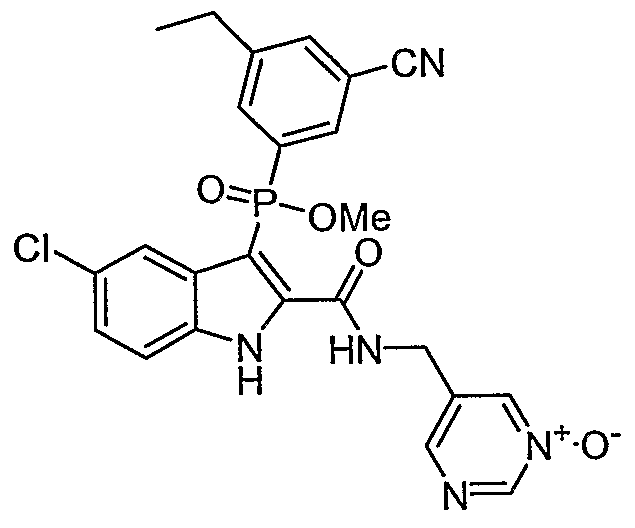
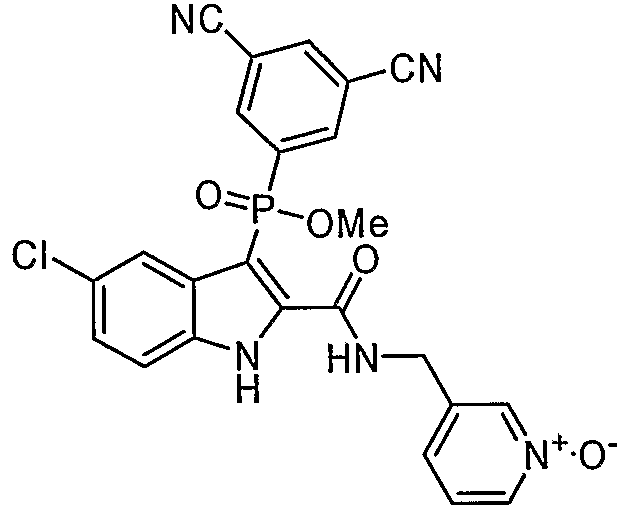
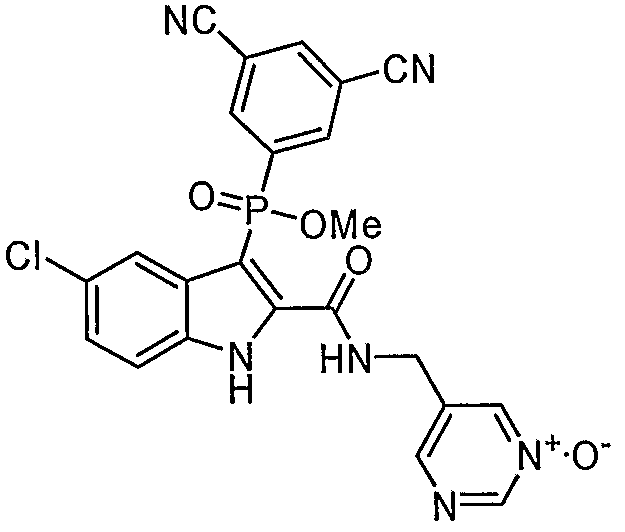
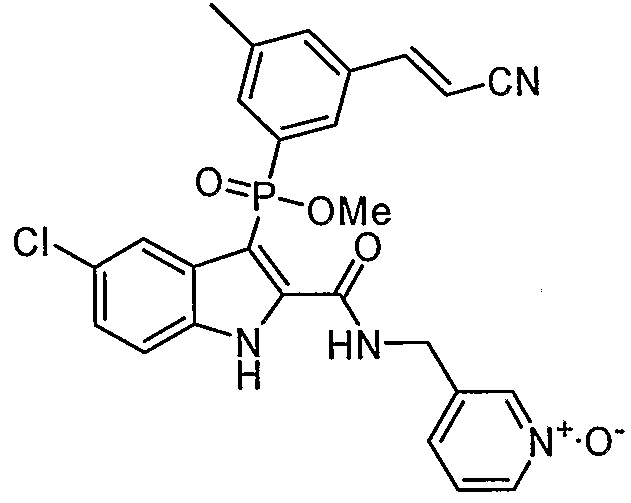
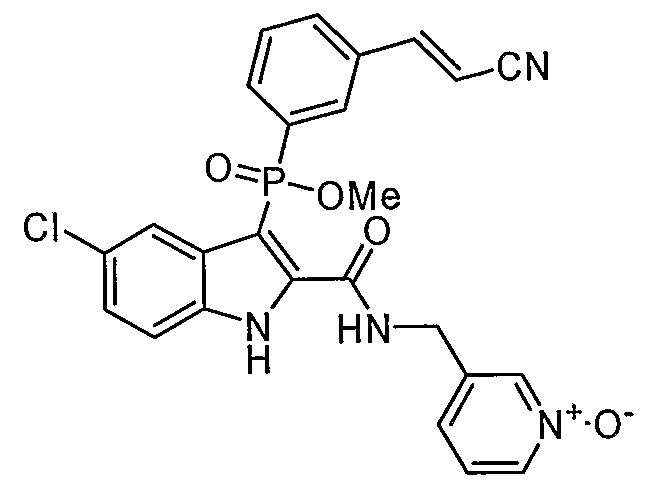
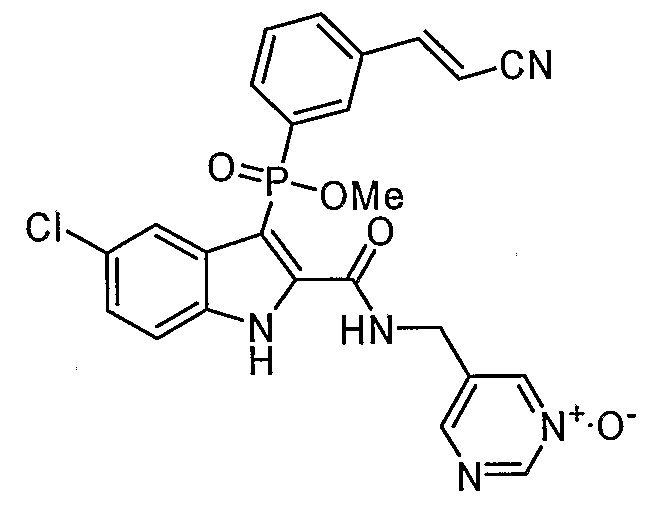
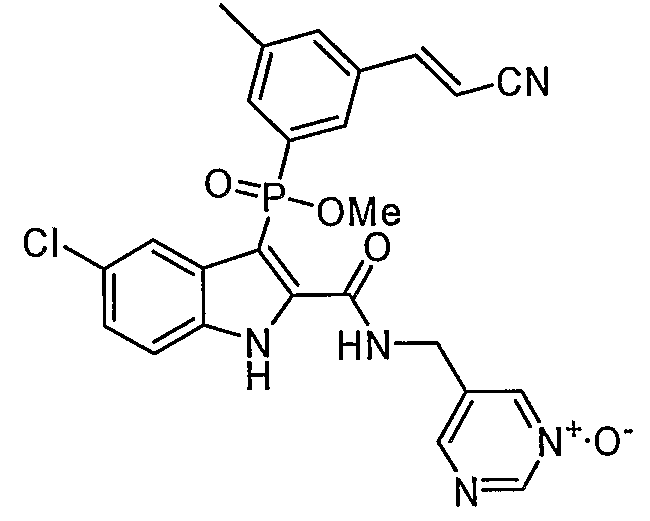
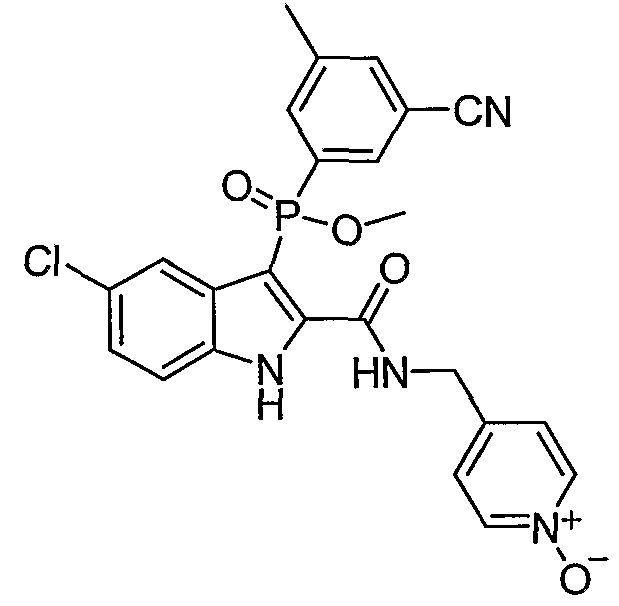
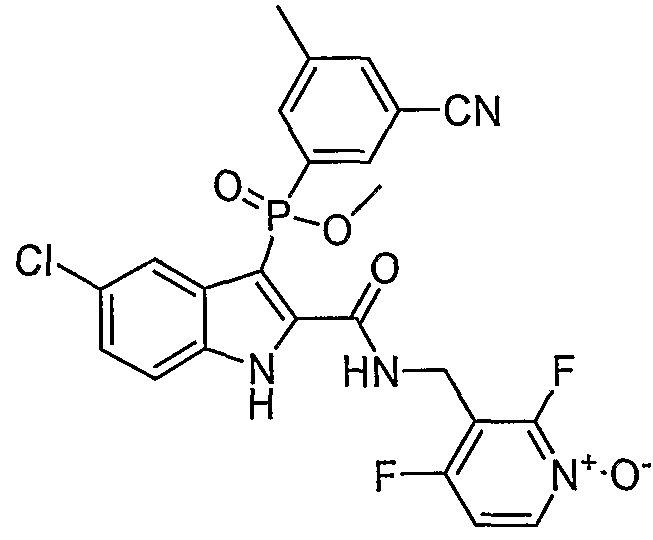
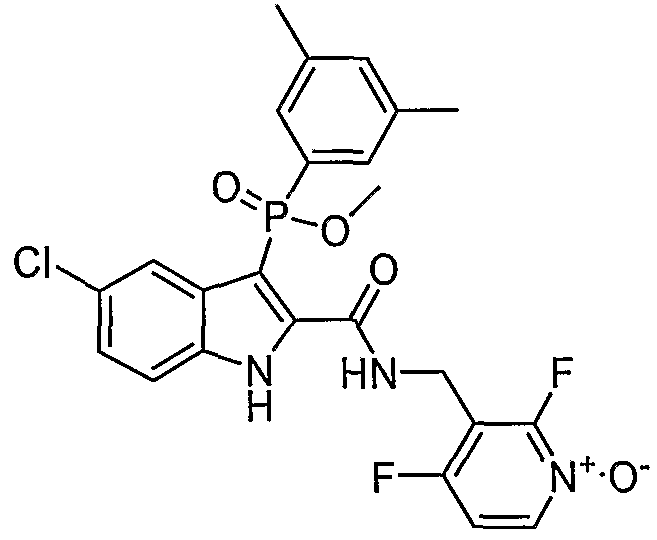
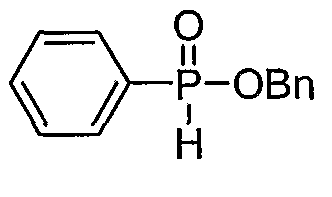
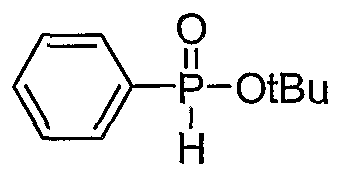
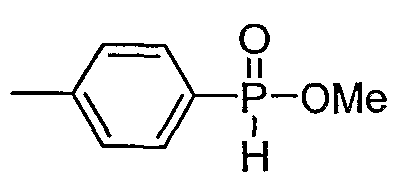
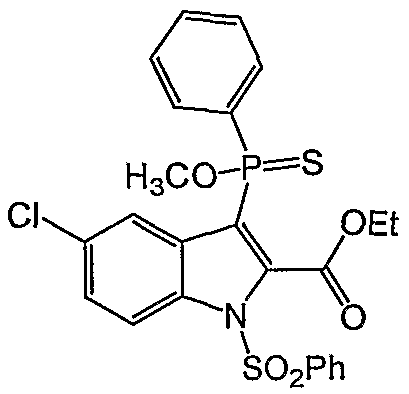
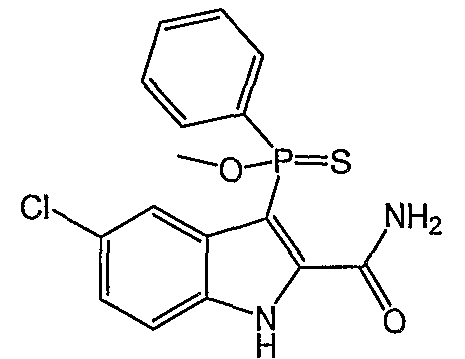
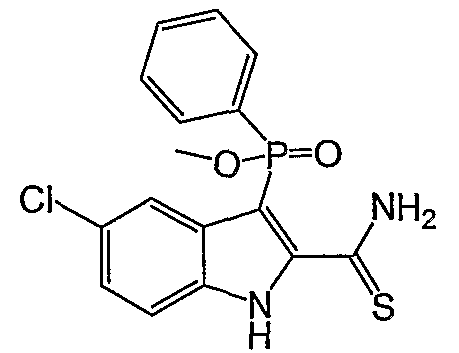
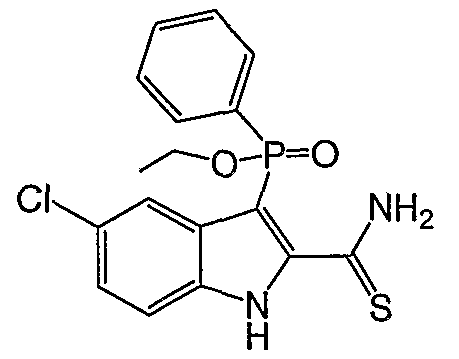
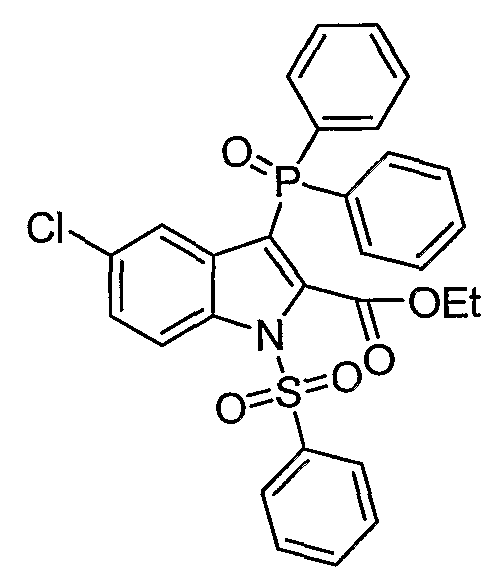
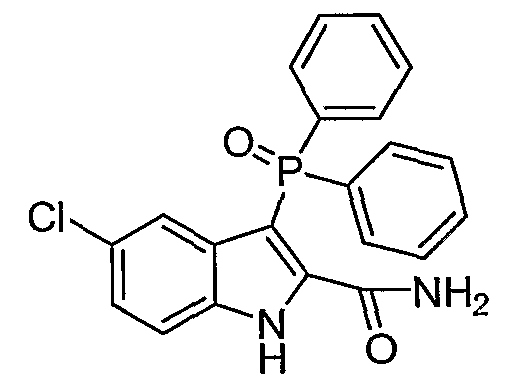
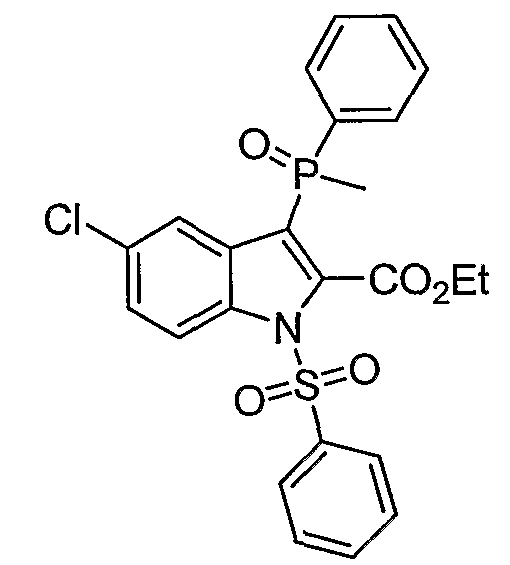
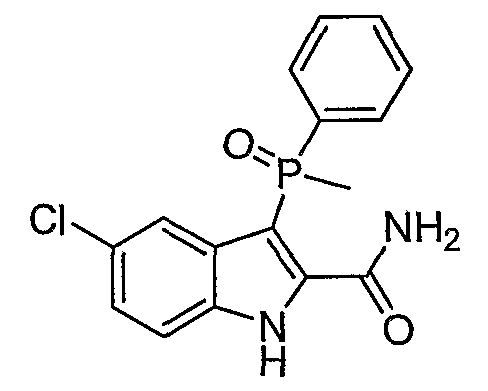
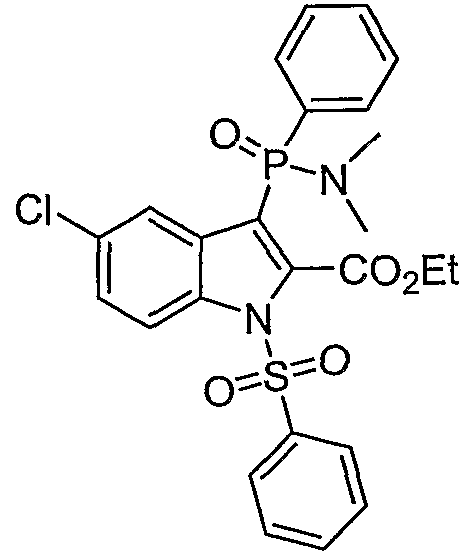
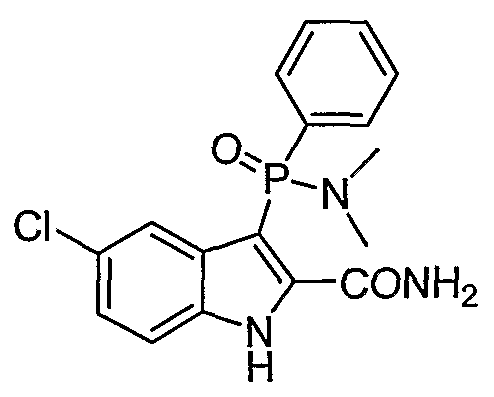
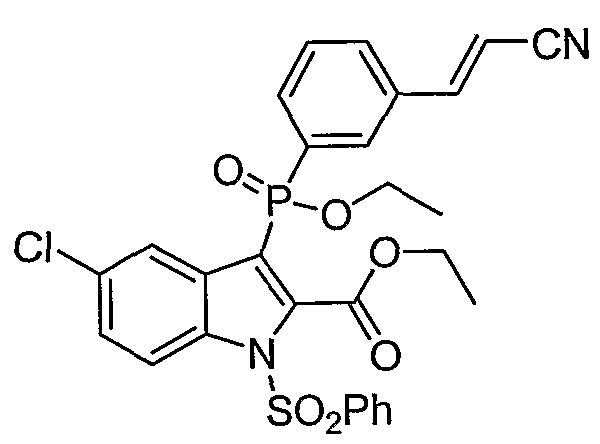
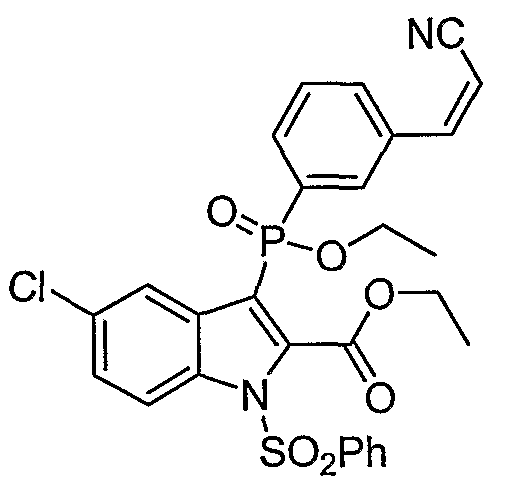
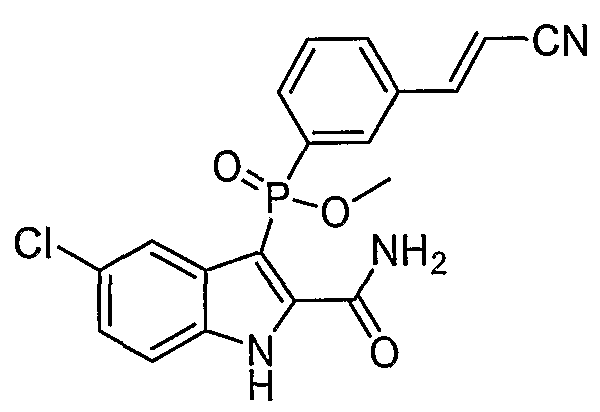
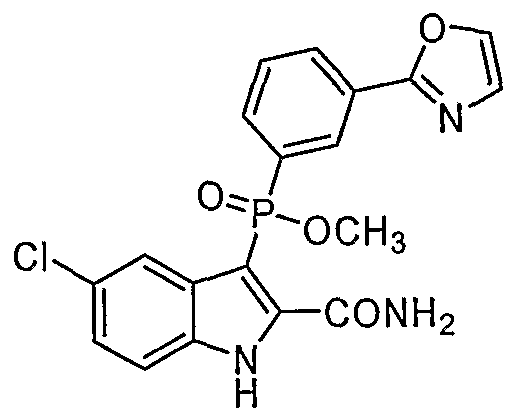
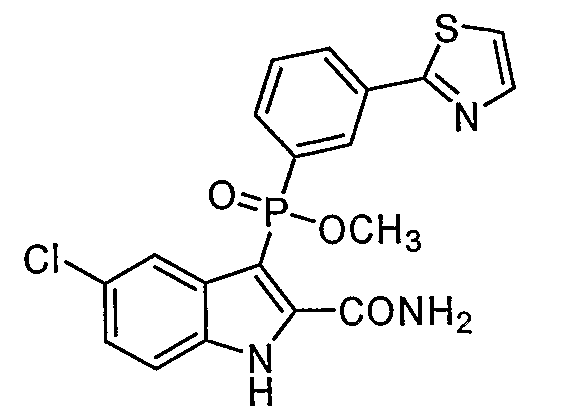
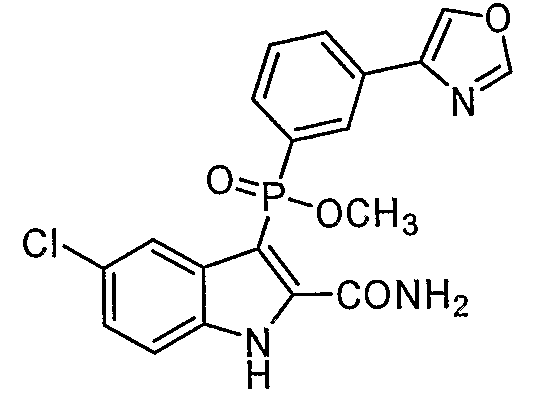
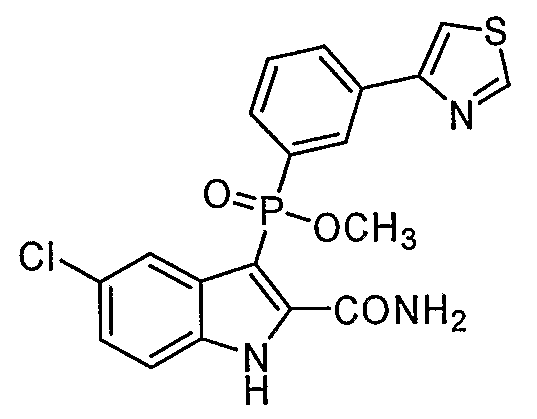
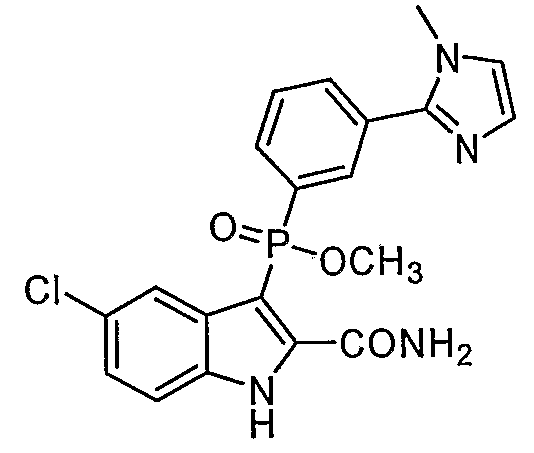
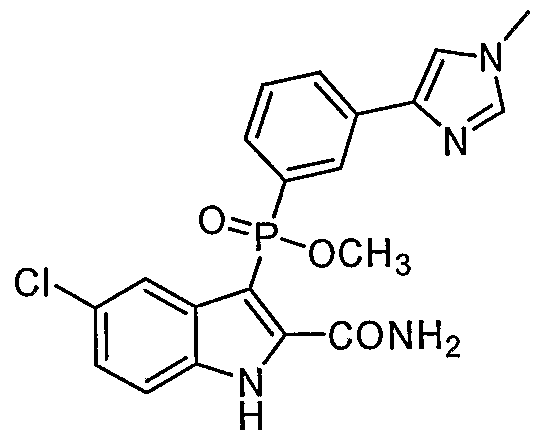
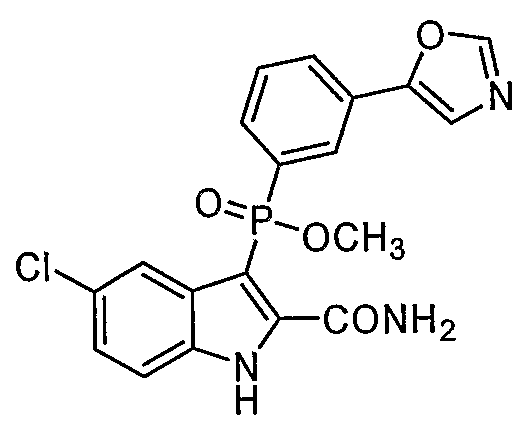
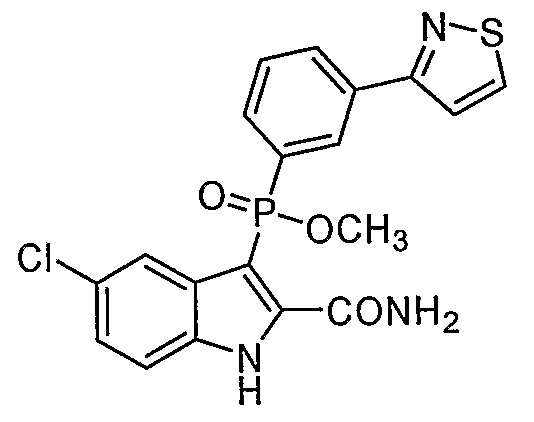
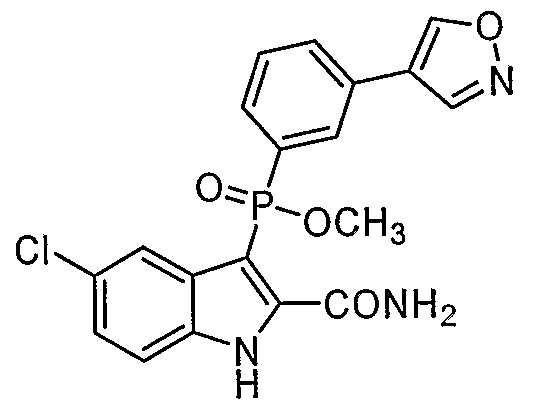
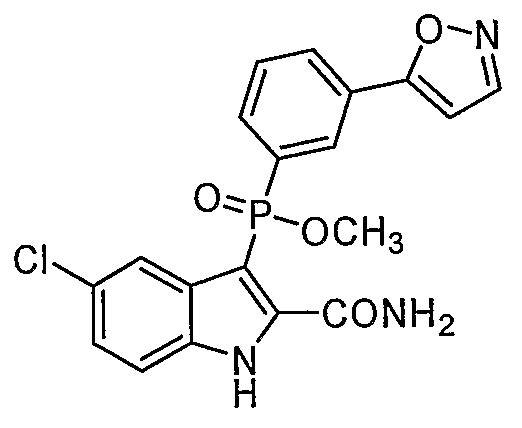
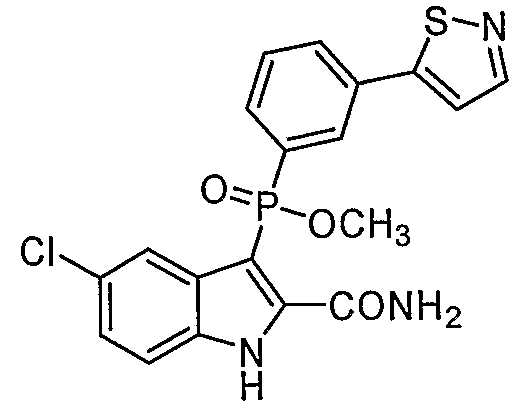
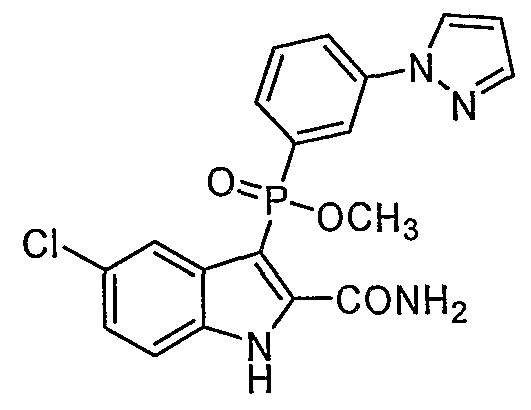
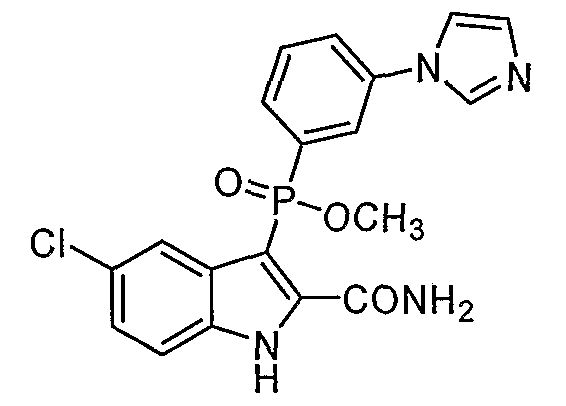
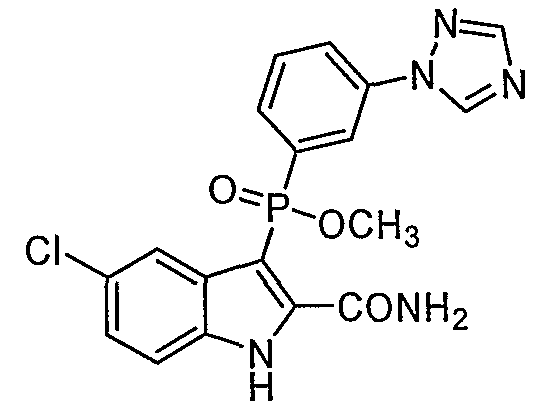
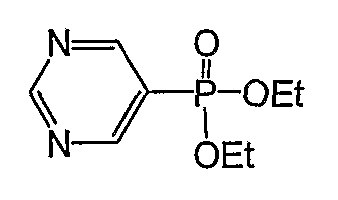
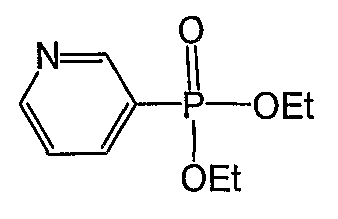
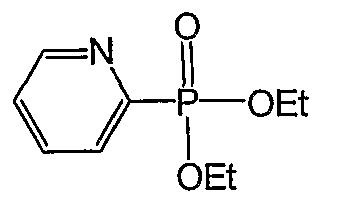
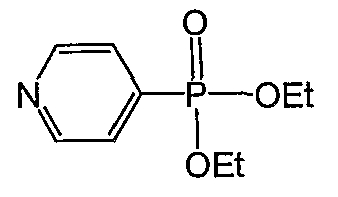
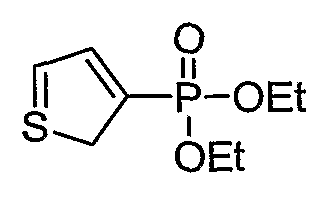
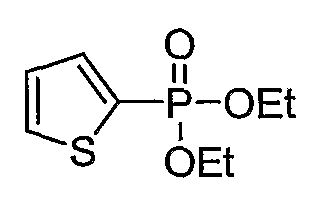
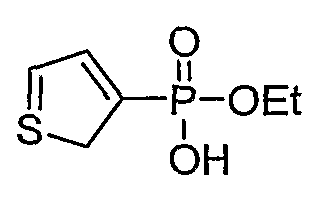
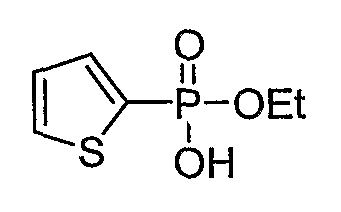
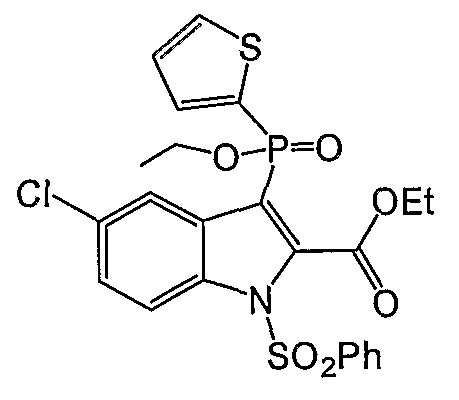
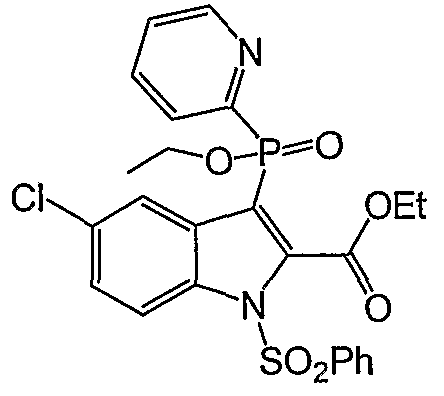
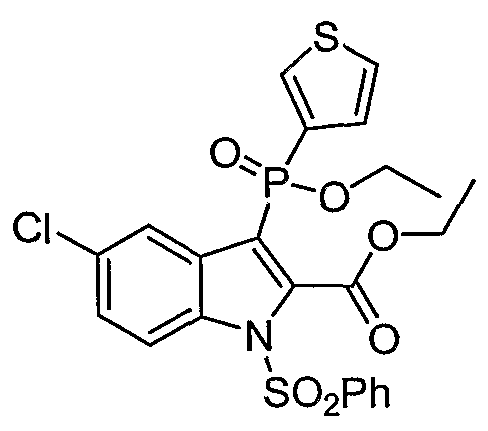
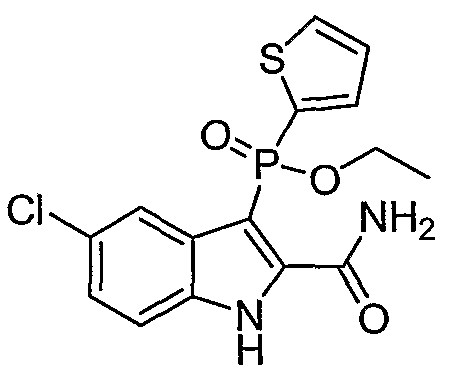
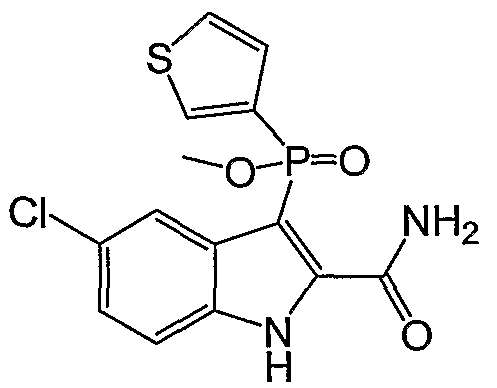
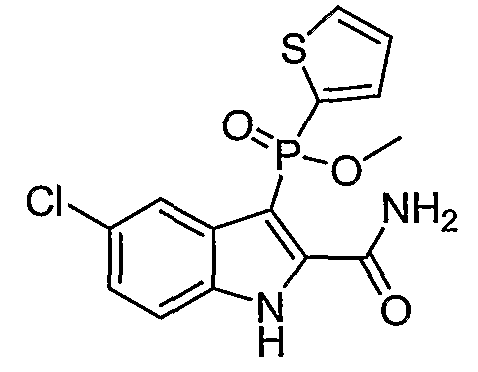
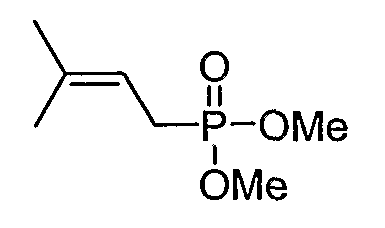
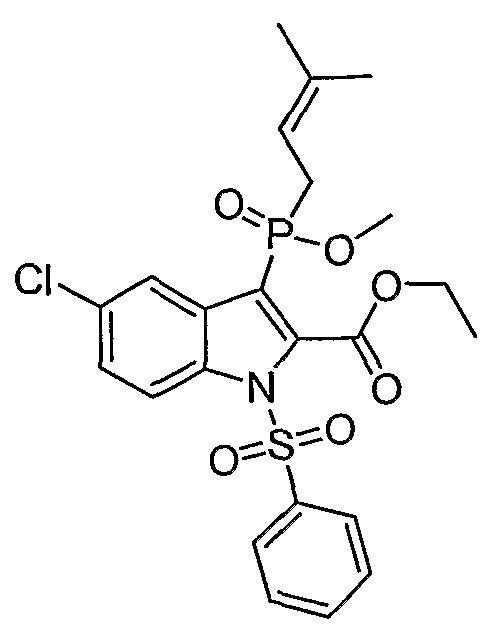
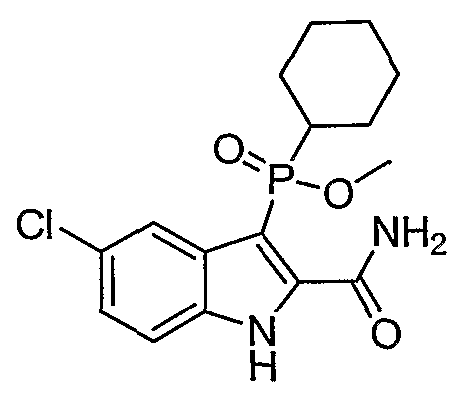
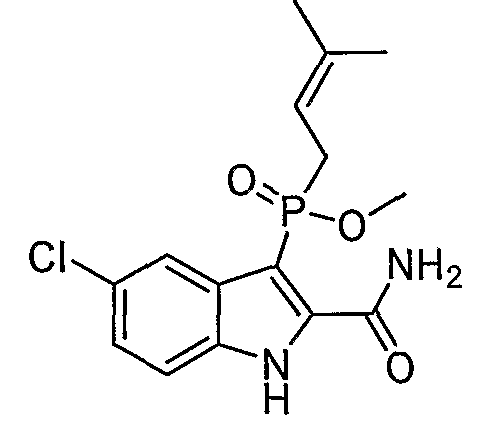
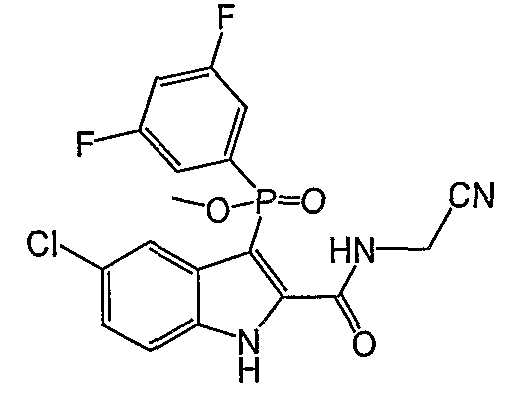
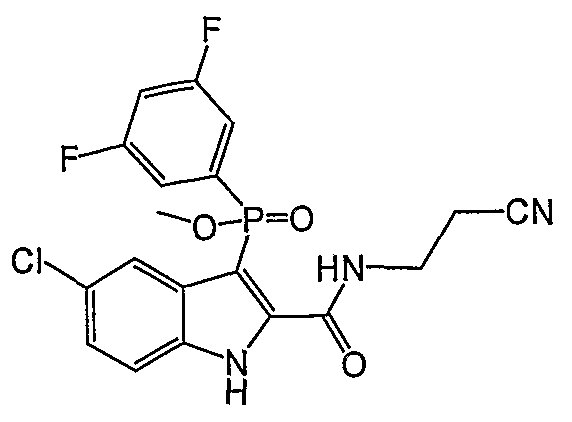
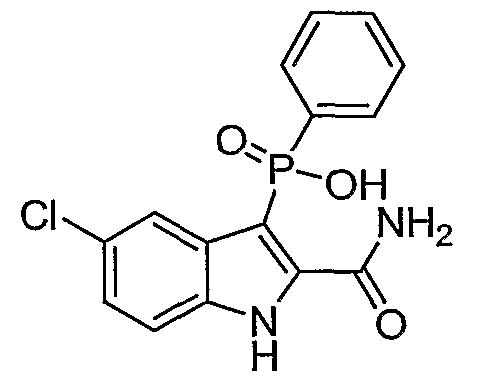
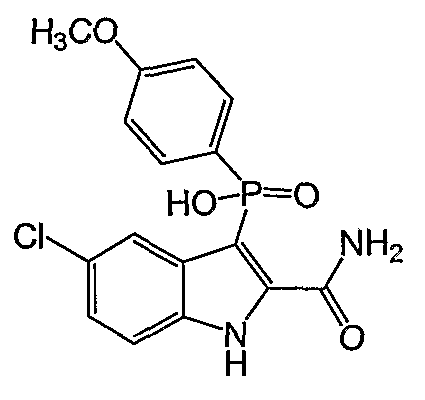
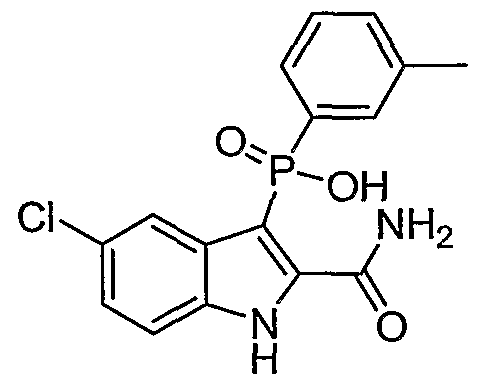
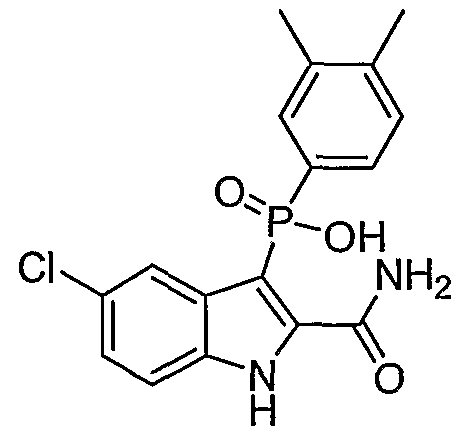
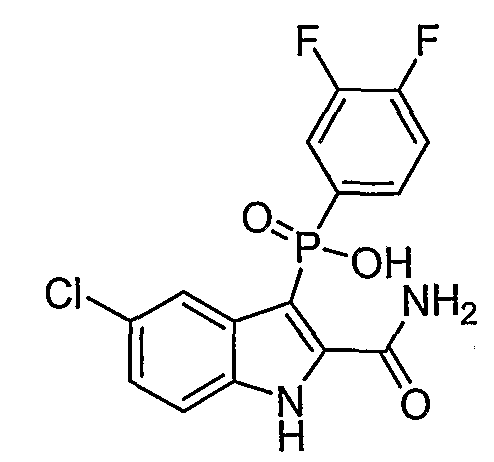
Следующие примеры назначены для иллюстрации изобретения, и никоим образом не ограничивают сферу действия изобретения.
ПРИМЕРЫ
Х. Синтез соединений
Общий способ синтеза
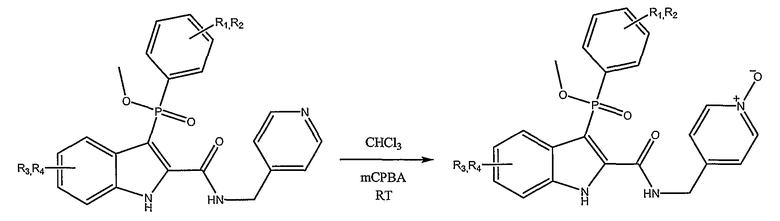
Эксперимент:
Предшественник пиридина растворяли в хлороформе (или в CH2Cl2) при перемешивании при комнатной температуре; м-хлорпероксибензойную кислоту добавляли, и реакционную смесь оставляли для перемешивания в течение ночи (~15 часов).
Смесь разбавляли дихлорметаном и экстрагировали смесью насыщенного K2CO3/H2O (1/3).
Водный слой экстрагировали три раза дихлорметаном. Объединенный органический слой высушивали над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. (ТСХ: дихлорметан/метанол = 9/1). Неочищенный продукт затем очищали методом хроматографии.
Соединения синтезировали:
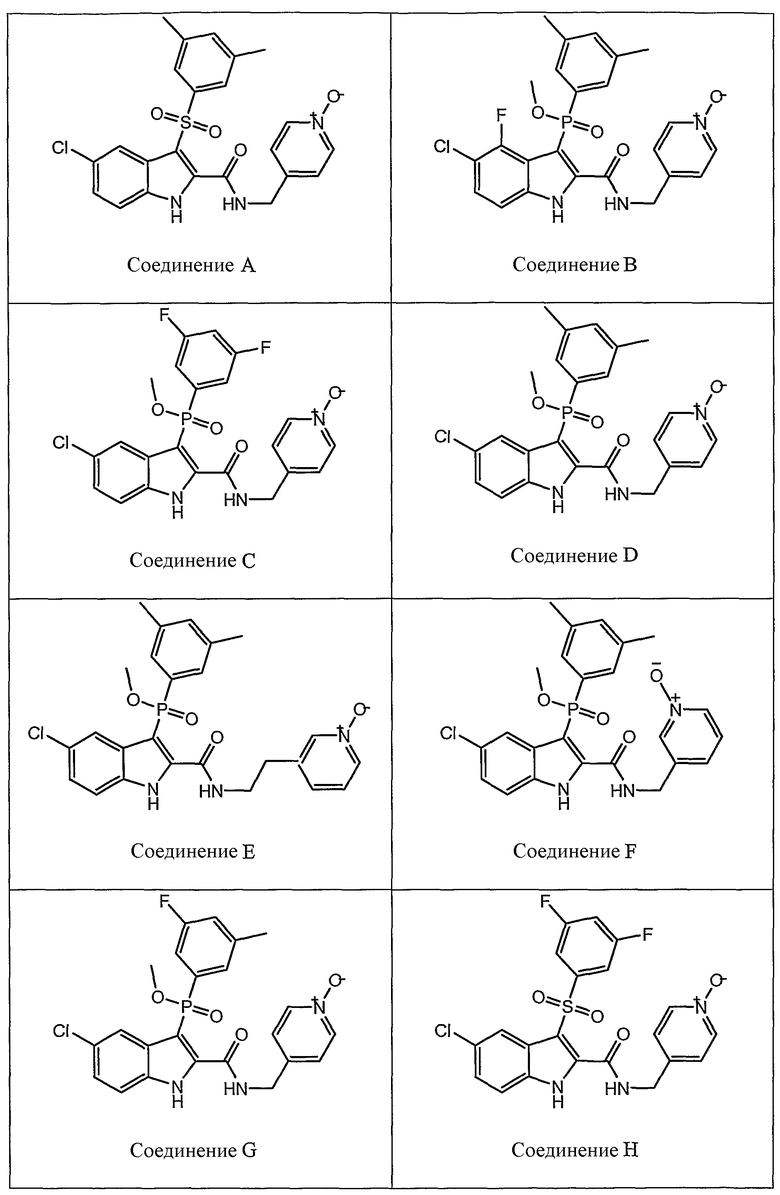
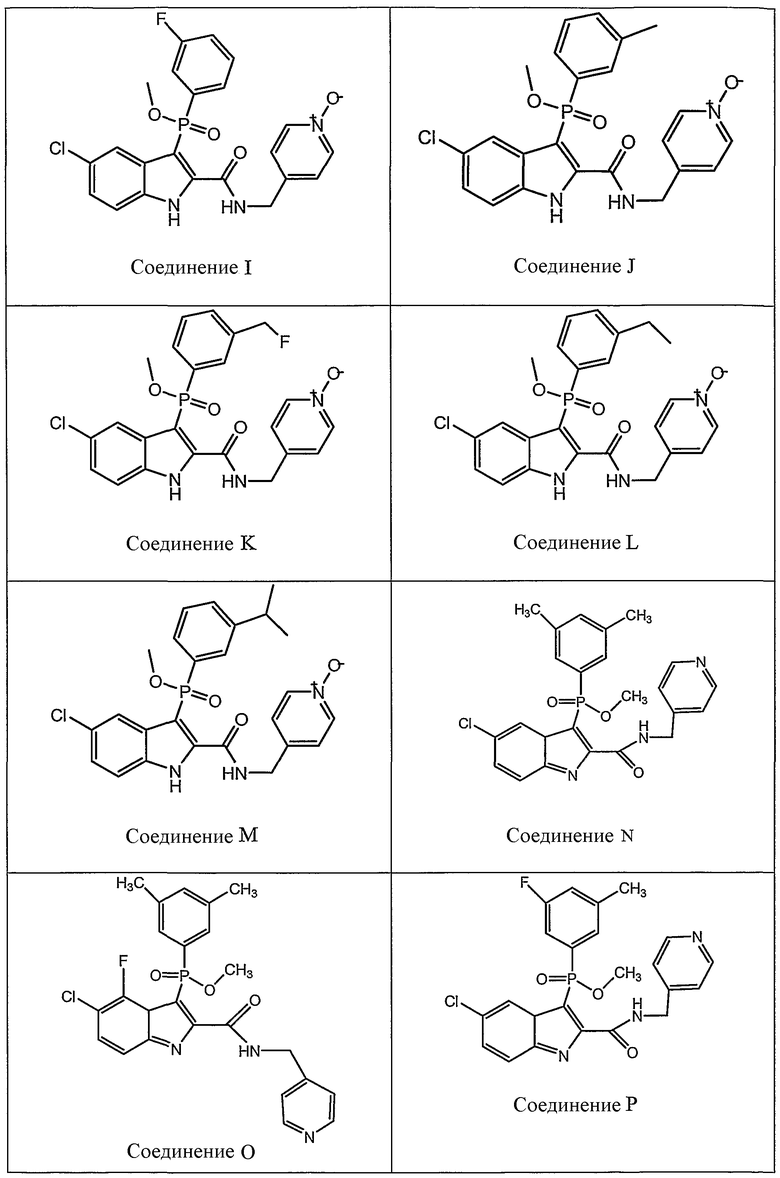
Пример 1. Этил 3-бром-5-хлор-1-(фенилсульфонил)-1Н-индол-2-карбоксилат
а) Синтез этил 5-хлор-1-(фенилсульфонил)-1Н-индол-2-карбоксилата в качестве исходного вещества (на основании работы Silvestri R., De Martino G., La Regina G., Artico M., Massa S., Vargiu L., Mura M., Loi A.-G., Marceddu T., La Colla P. J. Med. Chem. 2003, 46:2482-2493):
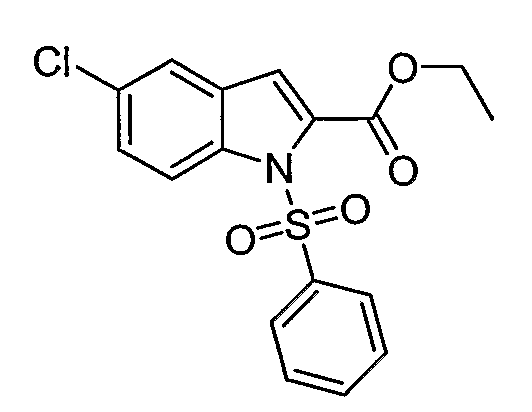
К перемешиваемому и охлажденному (0°С) раствору этил-5-хлориндол-2-карбоксилата (1,052 г, 4,70 ммоль) в DMF (25 мл) в атмосфере N2 добавляли по каплям NaH (60% в масле, 230 мг, 5,64 ммоль). После окончания выделения газа добавляли фенилсульфонилхлорид (0,72 мл, 5,64 ммоль). Реакционную смесь перемешивали в течение 1 часа (контроль с помощью ТСХ, элюент: дихлорметан). Небольшое количество воды добавляли и выпаривали DMF. Неочищенный остаток растворяли в EtOAc и промывали водой и солевым раствором. После высушивания и выпаривания растворителя соединение очищали методом хроматографии на силикагеле (элюент: циклогексан/EtOAc от 9/1 до 7/3), чтобы получить защищенный индол (1,547 г, выход 90%). Не совсем белое твердое вещество; 1H ЯМР (d6-ДМСО) δ 1,30 (т, J=7,2 Гц, 3H), 4,35 (кв, J=7,2 Гц, 2H), 7,37 (с, 1H), 7,53 (дд, J=2,2 и 9,1 Гц), 7,62-7,77 (м, 3H), 7,80 (д, J=2,2 Гц, 1H), 7,99 (м, 2H), 8,06 (д, J=9,1 Гц); МС (ESI, El+) m/z=364 (MH+).
b) Синтез промежуточного этил 3-бром-5-хлор-1-(фенилсульфонил)-1Н-индол-2-карбоксилата:
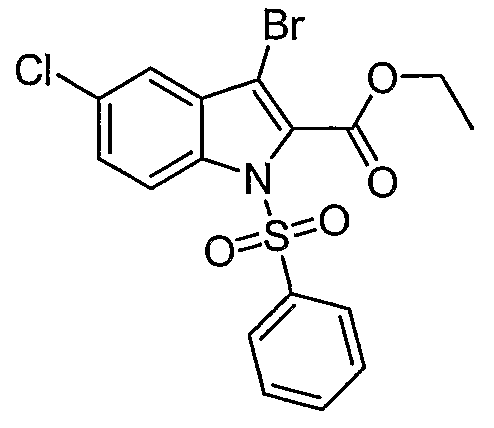
К перемешиваемому раствору этил 5-хлор-1-(фенилсульфонил)-1Н-индол-2-карбоксилата (4,83 г, 13,27 ммоль) в DMF (40 мл) в атмосфере N2 добавляли раствор брома (1,3 мл, 26,54 ммоль) в DMF (10 мл). Реакционную смесь перемешивали при RT (комнатной температуре) 4 часа, добавляли воду (150 мл) и экстрагировали дихлорметаном (3×100 мл). Органический слой промывали насыщенным раствором Na2SO4, высушивали и выпаривали, чтобы получить неочищенное, желтое масло. Очистка методом хроматографии на силикагеле (элюент: циклогексан/EtOAc 9/1) давала 3-бромированный индол (5,548 г, выход 93%). Не совсем белое твердое вещество; 1H ЯМР (d6-ДМСО) δ 1,37 (т, J=7,2 Гц, 3H), 4,48 (кв, J=7,2 Гц, 2H), 7,59-7,68 (м, 4H), 7,77 (м, 1H), 7,96-8,09 (м, 3H); МС (ESI, El+) m/z=442-444 (MH+).
Способ А: Обычная методика синтеза этил 5-хлор-3-(диалкоскифосфорил)-1-(фенилсульфонил)-1Н-индол-2-карбоксилата и этил 5-хлор-3-[алкокси(фенил)фосфорил]-1-(фенилсульфонил)-1Н-индол-2-карбоксилата
К перемешиваемому и охлажденному (-90°С) раствору этил-3-бром-5-хлор-1-(фенилсульфонил)-1Н-индол-2-карбоксилата (0,50 ммоль) в безводном THF (2,5 мл) в атмосфере N2 добавляли по каплям n-BuLi (2,5 М в гексане, 0,24 мл, 0,60 ммоль). После 5-минутной экспозиции при -90°С, соответствующий хлорфосфорный реагент (0,60 ммоль) добавляли по каплям при той же самой температуре. Реакционную смесь оставляли для нагревания вплоть до комнатной температуры в течение 3 часов (контроль методом ТСХ, элюент: дихлорметан/EtOAc 9/1). Затем добавляли воду (5 мл). Экстракция EtOAc (3×20 мл), высушивание и выпаривание давали неочищенное масло, которое очищали методом хроматографии на силикагеле.
Пример 2. Этил 5-хлор-3-(диэтоксифосфорил)-1-(фенилсульфонил)-1Н-индол-2-карбоксилат
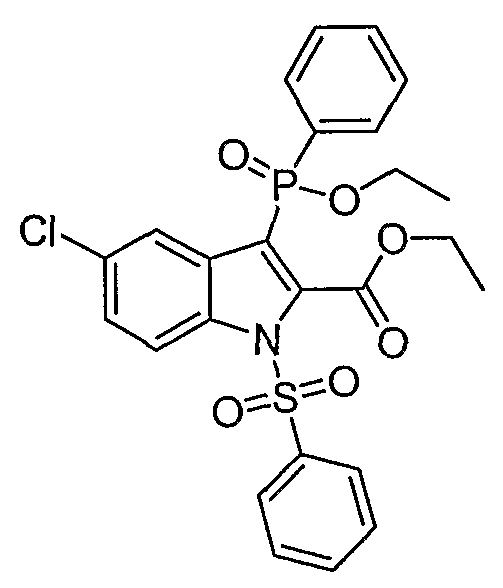
Способ А: Очистка методом хроматографии на силикагеле (элюент: дихлорметан/EtOAc от 9/1 до 8/2) давала требуемый индол (176 мг, выход 71%). Белое твердое вещество; 1H ЯМР (d6-ДМСО, 300 МГц) δ 1,19 (т, J=7,1 Гц, 6H), 1,39 (т, J=7,1 Гц, 3H), 3,99-4,09 (м, 4H), 4,46 (кв, J=7,1 Гц, 2H), 7,77 (дд, J= 2,1 и 8,7 Гц, 1H), 7,67-7,82 (м, 4H), 8,07-8,12 (м, 2H); 31P ЯМР (d6-ДМСО, 101 MHz) δ 9,7; МС (ESI, El+) m/z=500 (MH+).
Пример 3. Этил 5-хлор-3-[этокси(фенил)фосфорил]-1-(фенилсульфонил)-1Н-индол-2-карбоксилат
а) Синтез промежуточного этилгидрофенилфосфонохлоридата осуществляли по Smith A.B. III, Ducry L., Corbett, R.M., Hirschmann R. Org. Lett. 2000, 2:3887-3890:
i) Синтез диэтилфенилфосфоната:
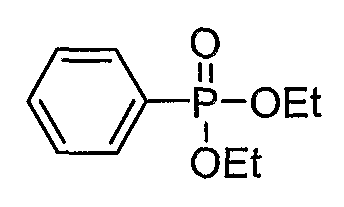
Бесцветное масло; 1H ЯМР (CDCl3, 250 МГц) δ 1,33 (т, J=7,1 Гц, 6H), 4,05-4,25 (м, 4H), 7,46-7,57 (м, 3H), 7,78-7,87 (м, 2H), 31P ЯМР (CDCl3, 101 МГц) δ 19,3.
ii) Синтез этилгидрофенилфосфоната:
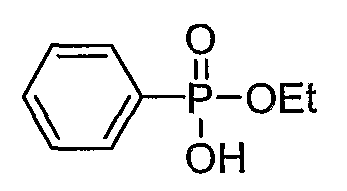
Бесцветное масло; 1Н ЯМР (CDCl3, 300 МГц) δ 1,32 (т, J=7,3 Гц, 3H), 4,08 (кв, J=7,3 Гц, 2H), 7,42-7,56 (м, 3H), 7,79-7,86 (м, 2H), 10,67 (шир.с, 1H). 31P ЯМР (CDCl3, 101 МГц) δ 21,3.
iii) Синтез этилгидрофенилфосфонохлоридата, имеющего следующие физические характеристики:
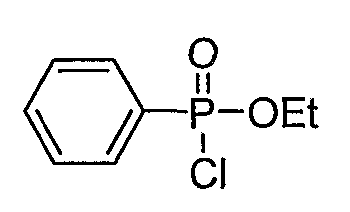
31P ЯМР (CDCl3, 101 MHz) δ 10,20 и 10,24.
b) Синтез конечного продукта этил 5-хлор-3-[этокси(фенил)фосфорил]-1-(фенилсульфонил)-1Н-индол-2-карбоксилата:
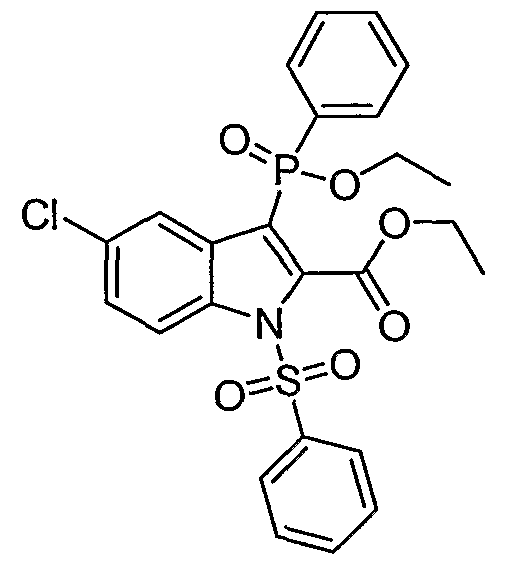
Способ А: Очистка методом хроматографии на силикагеле (элюент: дихлорметан/EtOAc 9/1) давала дебромированный индол (318 мг) и потом требуемый индол (326 мг, выход 41%). Бесцветное масло; 1H ЯМР (d6-ДМСО, 300 МГц) δ 1,27 (т, J=7,1 Гц, 3H), 1,36 (т, J=7,1 Гц, 3H), 4,03 (м, 2H), 4,38 (кв, J=7,1 Гц, 2H), 7,51-7,83 (м, 11H), 8,05-8,11 (м, 3H); 31P ЯМР (d6-ДМСО, 101 МГц) δ 23,3; МС (ESI, El+) m/z=532 (MH+).
Пример 4. Этил 5-хлор-3-[этокси(3,5-диметилфенил)фосфорил]-1-(фенилсульфонил)-1Н-индол-2-карбоксилат
а) Синтез промежуточного диэтил 3,5-диметилфенилфосфоната осуществляли по способу, описанному Hirao T., Masunaga T., Oshiro Y., Agawa T. Synthesis 1981, 56-57.
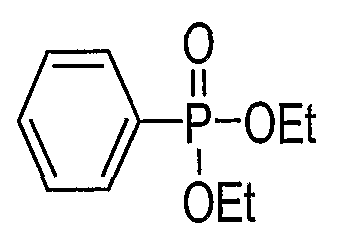
Очистка методом хроматографии на силикагеле (элюент: циклогексан/EtOAc 6/4) давала продукт (1,625 г, выход 61%) в виде бесцветного масла; 1Н ЯМР (CDCl3, 300 МГц) δ 1,33 (т, J=7,0 Гц, 6H), 2,35 (с, 6H), 4,02-4,18 (м, 4H), 7,18 (с, 1H), 7,40 (с, 1H), 7,45 (с, 1H); 31P ЯМР (CDCl3, 101 МГц) δ 20,3.
Другие промежуточные соединения синтезировали согласно примеру 3 (i, ii и iii).
b) Синтез этил 5-хлор-3-[этокси(3,5-диметилфенил)фосфорил]-1-(фенилсульфонил)-1Н-индол-2-карбоксилата:
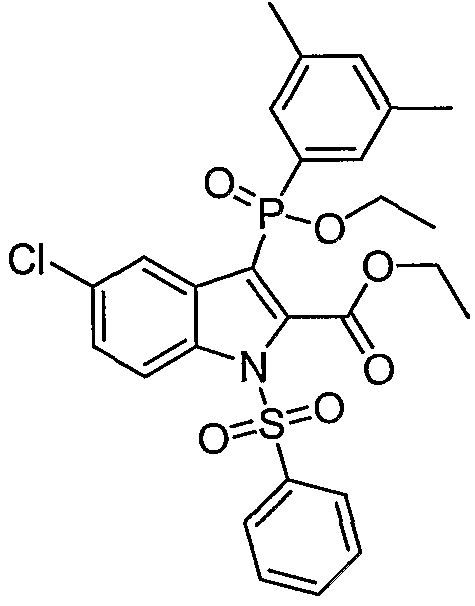
Способ А: Очистка методом хроматографии на силикагеле (элюент: дихлорметан/EtOAc 95/5) давала продукт (750 мг, выход 56%) в виде светло-желтого твердого вещества; 1H ЯМР (d6-ДМСО, 300 МГц) δ 1,27 (т, J=7,1 Гц, 3H), 1,36 (т, J=7,1 Гц, 3H), 2,30 (с, 6H), 3,94-4,06 (м, 2H), 4,44 (кв, J=7,1 Гц, 2H), 7,25 (с, 1H), 7,39 (с, 1H), 7,42 (с, 1H), 7,53 (дд, J=2,1 и 9,0 Гц, 1H), 7,65-7,71 (м, 2H), 7,77-7,82 (м, 2H), 8,05-8,11 (м, 3H); 31P ЯМР (d6-ДМСО, 101 МГц) δ 23,6; МС (ESI, El+) m/z=560 (MH+).
Пример 5. Этил 5-хлор-3-[метокси(фенил)фосфорил]-1-(фенилсульфонил)-1Н-индол-2-карбоксилат
а) Синтез диметилфенилфосфоната:
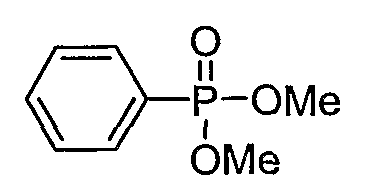
К раствору бензолфосфонил-дихлорида (1 мл, 6,35 ммоль) в безводном дихлорметане (25 мл) добавляли по каплям при 0°С этанол (1,12 мл, 19,04 ммоль), за которым следовал триэтиламин (2,65 мл, 19,04 ммоль). Реакционную смесь перемешивали при комнатной температуре 2 часа. Реакционную смесь промывали раствором HCl 1 н. (50 мл). Водный слой экстрагировали дихлорметаном. Объединенные органические фазы высушивали и концентрировали при пониженном давлении. Неочищенное масло очищали методом хроматографии на силикагеле (Элюент: циклогексан/EtOAc 6/4), чтобы получить диметилфенилфосфонат в виде бесцветного масла (1,110 г, выход 82%). 1H ЯМР (CDCl3, 300 МГц) δ 3,76 (д, J=11,1 Гц, 3H), 7,44-7,58 (м, 3H), 7,76-7,84 (м, 2H); 31P ЯМР (CDCl3, 1 01 МГц) δ 22,2.
Другие промежуточные соединения синтезировали согласно примеру 3 (i, ii и iii).
b) Синтез конечного продукта этил 5-хлор-3-[метокси(фенил)фосфорил]-1-(фенилсульфонил)-1Н-индол-2-карбоксилата:
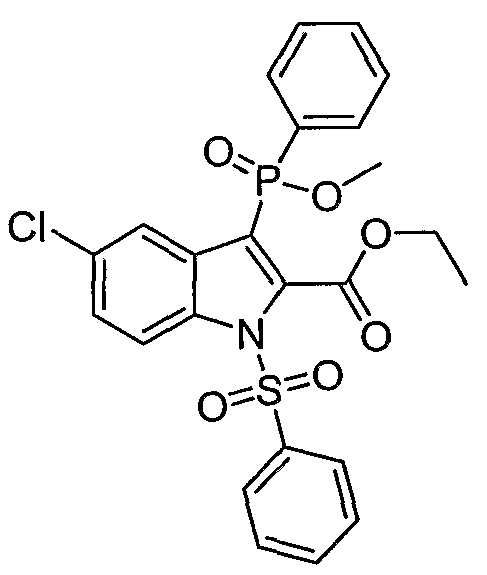
Способ А: Бесцветное масло; 1H ЯМР (CDCl3, 300 МГц) δ 1,45 (т, J=7,2 Гц, 3H), 3,80 (д, J=11,4 Гц,3H), 4,54 (кв, J=7,2 Гц, 2H), 7,36 (дд, J=2,1 и 9,0 Гц, 1H), 7,47-7,67 (м, 6H), 7,84-7,96 (м, 4H), 8,09-8,12 (м, 2H); 31P ЯМР (CDCl3, 101 МГц) δ 26,7; МС (ESI, El+) m/z=518 (MH+).
Пример 6. Этил 2-(аминокарбонил)-5-хлор-1Н-индол-3-ил-(фенил)фосфоната
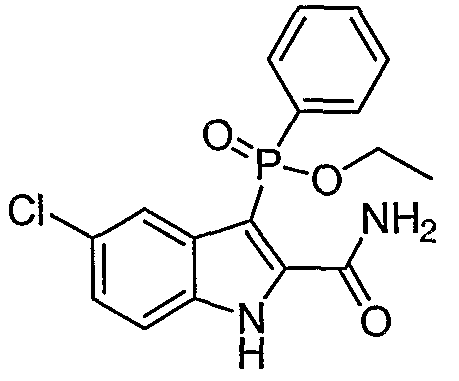
Этил-5-хлор-3-[этокси(фенил)фосфорил]-1-(фенилсульфонил)-1Н-индол-2-карбоксилат (268 мг, 0,50 ммоль) растворяли в насыщенном растворе аммиака в метаноле (5 мл) в трубчатом автоклаве. Трубку нагревали при облучении микроволнами при давлении при 65°С (максимальная мощность 100 Вт, устройство для обнаружения СЕМ) в течение 2 часов. После выпаривания растворителей очистка методом хроматографии на силикагеле (элюент: дихлорметан/MeOH от 95/5 до 9/1) давала требуемый карбоксамидиндол (107 мг, выхол 81%). Белое твердое вещество; 1H ЯМР (d6-ДМСО, 300 МГц) δ 1,34 (т, J=7,1 Гц, 3H), 4,05 (м, 1H), 4,20 (м, 1H), 7,32 (дд, J=2,1 и 8,7 Гц, 1H), 7,49-7,61 (м, 5H), 7,68-7,75 (м, 2H), 8,02 (шир.с, 1H), 10,27 (шир.с, 1H), 12,77 (шир.с, 1H); 31P ЯМР (d6-ДМСО, 101 МГц) δ 31,1; МС (ESI, El+) m/z=363 (MH+).
Пример 7. Этил 2-(аминокарбонил)-5-хлор-1Н-3-ил-(3,5-диметилфенил)фосфонат
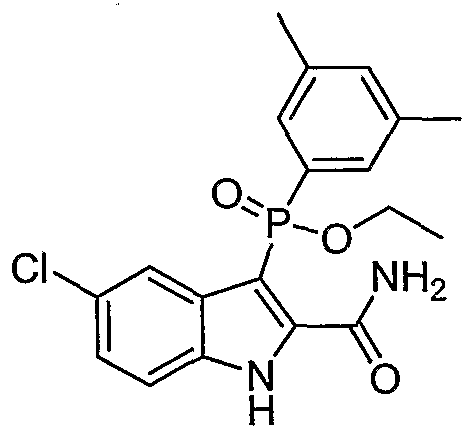
Проводили такую же методику, как описано в примере 5. Белое твердое вещество; 1H ЯМР (d6-ДМСО, 300 МГц) δ 1,32 (т, J=7,0 Гц, 3H), 2,26 (с, 6H), 3,90-4,03 (м, 1H), 4,09-4,22 (м, 1H), 7,21 (с, 1H), 7,29-7,33 (м, 3H), 7,57 (дд, J=1,8 и 9,0 Гц, 1H), 7,60 (дд, J=1,8 Гц, 1H), 7,99 (шир.с, 1H), 10,3 (шир.с, 1H), 12,7 (шир.с, 1H); 31P ЯМР (d6-ДМСО, 101 МГц) δ 31,3; МС (ESI, El+) m/z=391 (MH+).
Пример 8. Метил 2-(аминокарбонил)-5-хлор-1Н-индол-3-ил-(фенил)фосфинат
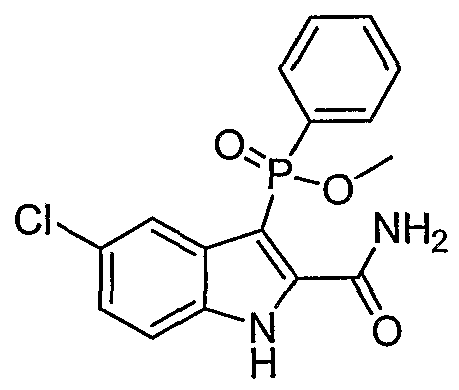
Проводили такую же методику, как описано в примере 5. Бледно-желтое твердое вещество; 1H ЯМР (CDCl3, 300 МГц) δ 3,85 (д, J=11,4 Гц, 3H), 6,08 (шир.с, 1H), 7,30 (дд, J=2,0 и 9,0 Гц, 1H), 7,36-7,56 (м, 4H), 7,68 (д, J=1,8 Гц, 1H), 7,73-7,81 (м, 2H), 10,78 (шир.с, 1H), 10,03 (шир.с, 1H); 31P ЯМР (CDCl3, 101 МГц) δ 33,3; МС (ESI, El+) m/z=349(MH+).
Пример 9: Биологическая активность в отношении штаммов ВИЧ, с устойчивостью к лекарственным средствам
В одном осуществлении эффективность анти-ВИЧ соединения оценивали in vitro быстрым, чувствительным и автоматизированным способом, который включает в себя восстановление бромида 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия (МТТ). Линию ВИЧ-трансформированных клеток, которая является высоко пермиссивной и избирательной в отношении ВИЧ-инфекции, например, такую как Т-4 клеточная линия, МТ-4, выбирали как линию клеток-мишеней (Koyanagi et al., Int. J. Cancer, 1985, 36:445-451). Восстановление in situ бромида 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия (МТТ), которое определяли спектрофотометрически, является стандартом, по которому оценивают жизнеспособность как псевдозараженных клеток, так и ВИЧ-инфицированных клеток. Ингибирование ВИЧ-индуцированного цитопатического эффекта служит в качестве конечной точки. 50% цитотоксическую концентрацию (CC50 в мкМ) определяли как концентрацию соединения, которая снижает оптическую плотность псевдоинфицированного контрольного образца на 50%. Процент эффективаности анти-ВИЧ соединения рассчитывали по формуле (выражали как %):
(ODВИЧ тестируемого соединения)-(ODконтроль)/(ODпсевдоинфиц. клетки)-(ODконтроль)
Здесь, (ODВИЧ тестируемого соединения) представляет собой оптическую плотность, установленную для определенного количества тестируемого соединения в ВИЧ-инфицированных клетках; (ODконтроль) представляет собой оптическую плотность, установленную для необработанных ВИЧ-инфицированных, контрольных клеток; и (ODпсевдоинфицированных клеток) представляет собой оптическую плотность, установленную для контрольных, псевдоинфицированных клеток, которые не обрабатывали. Величины оптической плотности обычно определяли при 540 нм. Дозу анти-ВИЧ тестируемого соединения, которая обеспечивает 50% защиту в соответствии с предшествующей формулой, определяли как 50% ингибиторную концентрацию (IC50 в мкМ). Индекс селективности (SI) определяли как соотношение СС50 к IC50.
В другом осуществлении анализ ELISA p24 использовали, чтобы определить эффективность анти-ВИЧ соединения. Названный иммуноанализ репликации вируса позволяет определять количество присутствующего вирусного капсидного (ядерного) антигена р24, и коммерчески предоставляется фирмами, например, такими как Coulter Corporation/Immunotech, Inc.® (Westbrook, MI).
Следующие осуществления включают в себя исследование обратной транскриптазы, в котором оценивают количество вирусной репликации, используя систему гомополимер поли-rA:матричный праймер олиго-dT, которая количественно определяет включение в клетки тритированного монофосфата тимидина методами подсчета импульсов (Southern Research Institute, University of Alabama, Birmingham, AL); исследование синцитиального ингибирования, в котором используют CEM-SS, HeLa-CD4, или HeLa-CD4-LTR-b-галактозидазные клетки, имеющие иммунофлуоресцентный, хемилюминесцентный или колометрический концевой фрагмент; и исследование ингибирования прикрепления и слияния, в котором утилизируют индикаторные клеточные линии, и количественное определение с помощью хемилюминисцентной, колориметрической или микроскопической оценки (Southern Research Institute, University of Alabama, Birmingham, AL).
В одном осуществлении индольные соединения данного изобретения не проявляли перекрестной резистентности с другими ненуклеозидными ингибиторами обратной транскриптазы (NNRTI) в том смысле, что соединения данного изобретения демонстрировали EC50 (в молярной концентрации) для мутантного штамма ВИЧ приблизительно ниже, чем концентрация 50, 25, 10 или 1 мкМ. В обычном осуществлении, NNRTI демонстрировали EC50 для мутантного штамма ВИЧ приблизительно ниже 5, 2,5, 1 или 0,1 мкМ концентрации. Степень перекрестной резистентности относительно штамма ВИЧ, резистентного к лекарственному средству, определяли, оценивая EC50 требуемого соединения оксо-пиримидина на мутантном вирусе-мишени, то есть резистентном к лекарственному средству.
Поэтому в другом важном осуществлении данного изобретения представлен способ лечения пациента с перекрестно резистентным ВИЧ, который включает в себя введение эффективного для лечения ВИЧ количества соединения индола, его соли, пролекарства, стереоизомера или таутомера.
Биологическая активность относительно штаммов ВИЧ, резистентных к лекарственному средству
В одном осуществлении фенилиндолы данного изобретения не проявляли перекрестной резистентности к другим ненуклеозидным ингибиторам обратной транскриптазы (NNRTI) в том смысле, что они демонстрировали EC50 (в молярной концентрации) для мутантного штамма ВИЧ приблизительно ниже 50, 25, 10 или 1 молярной концентрации. В обычном осуществлении ненуклеозидные ингибиторы обратной транскриптазы (NNRTI) демонстрировали EC50 для мутантного штамма ВИЧ приблизительно ниже 5, 2,5, 1 или 0,1 мкМ концентрации. Степень перекрестной резистентности относительно штамма ВИЧ, резистентного к лекарственному средству, легко определяли, оценивая EC50 требуемого индола на мутантном вирусе-мишени, то есть резистентном к лекарственному средству.
Поэтому в другом важном осуществлении данного изобретения представлен способ лечения пациента с перекрестно резистентным ВИЧ, который включает в себя введение эффективного для лечения ВИЧ количества соединения фенилиндола или его пролекарства или соли.
Таблица 3
Данные энзиматического исследования
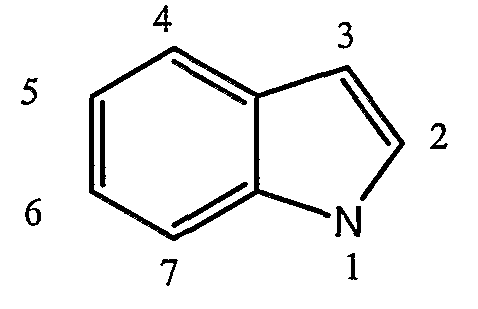
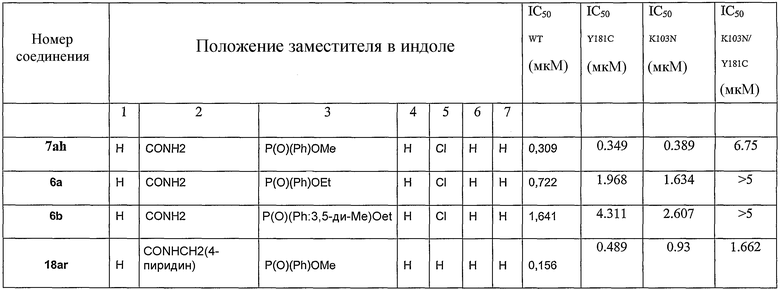
Таблица 4
Клеточный анализ с применением клеток ВН-1
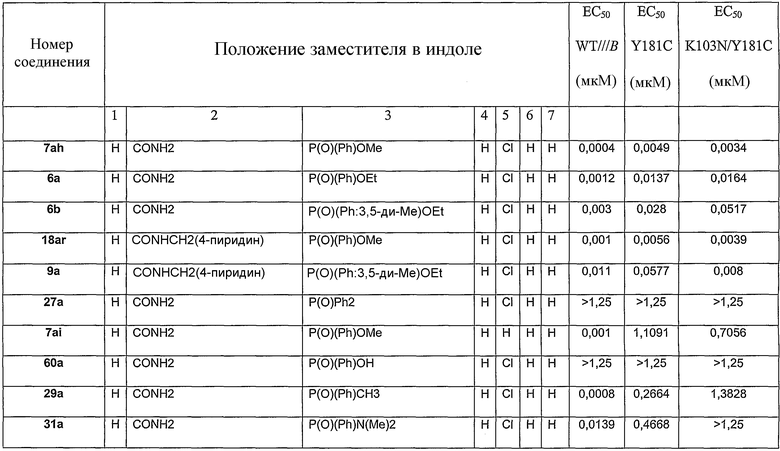
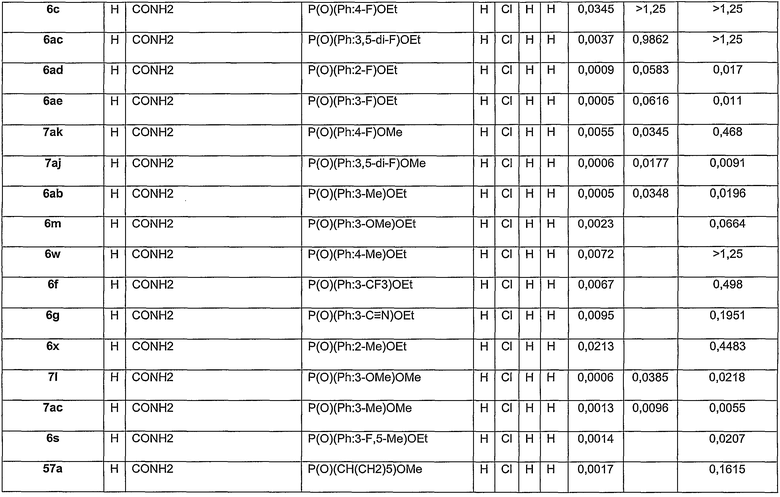
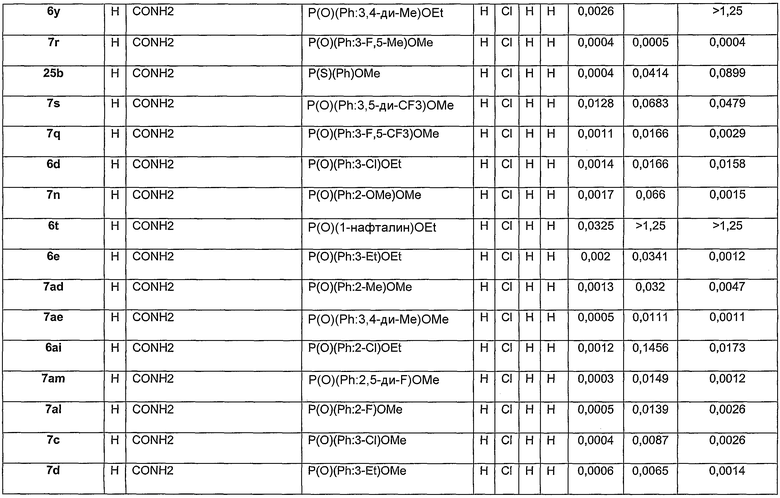
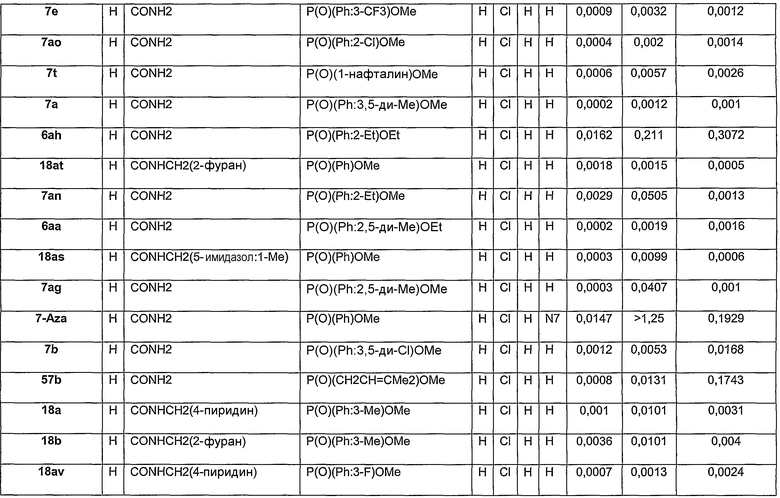
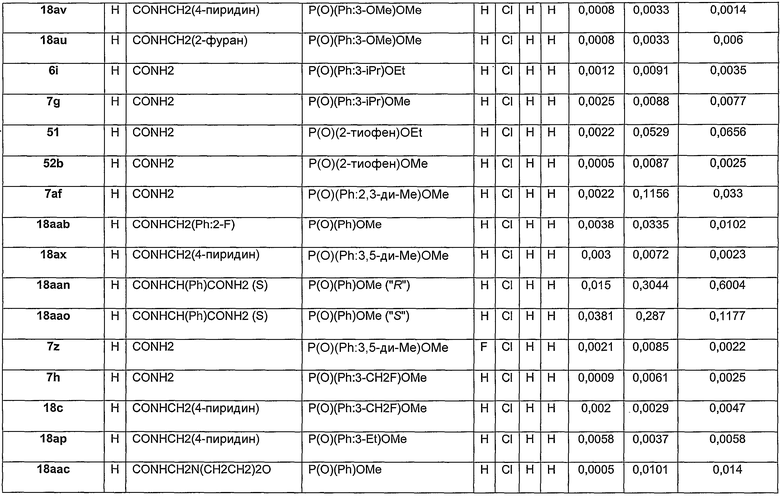
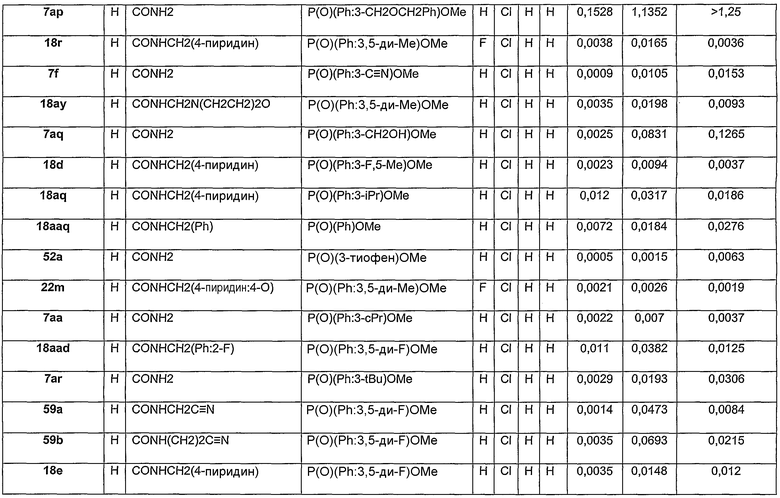
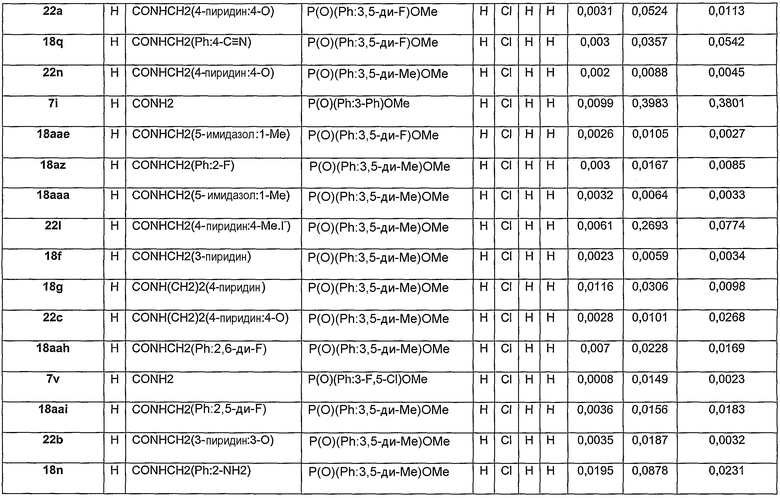
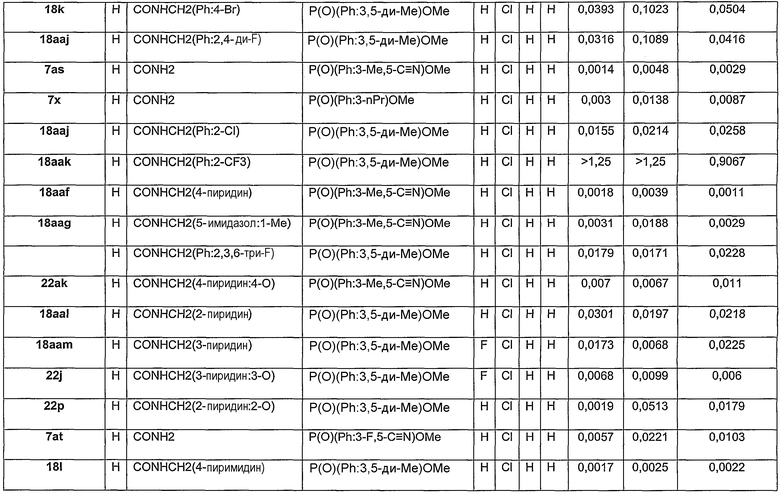
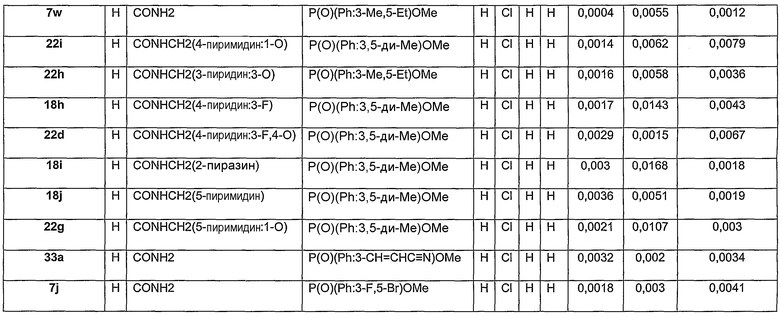
Ph означает фенил, Me означает метил, и Et означает этил. Относительная растворимость (при OD 600 нм) соединений колеблется приблизительно от 75 мкМ/мл для соединения № 5 до > 1000 мкМ/мл для соединений №№ 7-11. Исследование связывания цитохрома-Р450, проведенное для соединения № 3, указало на связывание 15,87 мкМ, а исследование на клетках MDRC4 и CNDO с тем же самым соединением по сравнению с другими мутантными формами, например, такими как K103N/M184V/NAMS и K103N/Y181C/M184V/NAMS, дало значения EC50 0,0013-0,4466 мкМ.
Токсикология
1. рН-Зависимая растворимость в воде
Растворимость в воде каждого соединения определяли общепринятым способом при встряхивании сосуда при насыщающей концентрации 1 мМ. Сосуд (флакон) встряхивали в течение 3 часов при температуре окружающей среды и потом центрифугировали. Супернатант исследовали методом ВЭЖХ с УФ-детекцией для определения растворимости. Вообще, более высокая растворимость в воде оказывается более желательной для кандидата на лекарственное средство.
2. Связывание белков плазмы человека
Связывание белков плазмы человека определяли, используя способ уравновешивающего диализа. Диализ проводили с цельной плазмой человека при 37°С приблизительно в течение 6 часов при концентрации лекарственного средства 1 мкМ. В конце диализа образцы буфера из буферного окружения диализованных клеток отбирали и исследовали с помощью LC/MS/MS (ЖХ/МС/МС) относительно свободной концентрации лекарственного средства. Для NNRTI более низкое связывание белка является более желательным.
3. Двунаправленная САСО-2-проницаемость
Цель данного исследования заключалась в определении классификации двунаправленной проницаемости и ограниченного утечкой потенциала всасывания тестируемого соединения в системе монослоя Сасо-2-клеток. Обычно исследование включало в себя измерение неспецифического связывания с Transwell-аппаратом в буфере исследования рН 7,4, оценку двунаправленной проницаемости тестируемого соединения через монослой Сасо-2-клеток, оценку апикального-до-базолатерального транспорта, оценку базолатерального-до-апикального транспорта и исследование целостности монослоя. Высокая проницаемость и отсутствие утечки позволило предположить, что интестинальная проницаемость, как полагают, не должна являться ограничивающим фактором для перорального всасывания у человека.
4. Ингибирование CYP450
Скрининг ингибирования CYP450 in vitro предусматривает предсказание возможных взаимодействий лекарство-лекарство. Чтобы определить, ингибирует ли тестируемое соединение активность определенного фермента Р450, изменения в метаболизме Р450-специфического субстрата микросомами печени человека определяли при отличающихся концентрациях тестируемого соединения. Эффективность и порядок степени ингибирования можно оценивать при определении величин IC50 для отдельного изофермента. Для NNRTI более высокие величины IC50 будут означать меньшую степень ингибирования и, таким образом, меньшую вероятность взаимодействия лекарство-лекарство у человека.
Ингибирование CYP3A4 тестировали, используя набор для высоко производительного ингибиторного скрининга CYP3A4/BFC (BD Biosciences), ингибирование CYP2D6 тестировали, используя набор для высоко производительного ингибиторного скрининга CYP2D6/AMMC (BD Biosciences) и ингибирование CYP2C9 тестировали, используя набор для исследования P450-Glo™ (Promega).
5. Метаболическая стабильность в микросомах печени in vitro
Исследование метаболической стабильности является оценкой стабильности тестируемого соединения в биологическом матриксе. Результаты являются важными с точки зрения понимания и предсказания механизмов элиминации тестируемого соединения. CYP450-зависимый метаболизм лекарственного средства также может значительно отличаться от одного вида к другому. Оценка in vitro метаболизма лекарственного средства микросомами печени многих видов позволяет сравнивать метаболизм у животных с метаболизмом у человека. Это может способствовать идентификации наиболее соответствующих животных моделей для изучения PK и токсикологии. Метаболическую стабильность тестируемого соединения оценивали in vitro в микросомах печени крысы, собаки, обезьяны и человека. 10 мкМ тестируемого соединения пре-инкубировали в течение 5 минут при 37°С с 1 мг/мл микросом печени в 0,1 М трис-буфере, рН 7,4, содержащем 5 мМ MgCl2 и 0,1 мМ EDTA. После пре-инкубации добавляли NaDPH (конечная концентрация 3 мМ), чтобы начать реакцию, и образцы инкубировали в течение 0 и 1 или 2 часов. После окончания реакции супернатант исследовали методом ВЭЖХ-УФ или ЖХ/МС/МС для установления исчезновения исходного соединения и образования метаболита(ов). % Оставшегося исходного соединения соответствовал соотношению площади пика образца 1 или 2 часа к образцу с 0 временем. Вообще, более низкий метаболизм (более высокая величина % исходного соединения) является более желательным.
6. Метаболизм в микросомах печени in vitro - метаболический путь
Биотрансформацию фазы I тестируемого соединения оценивали в данном исследовании. Образцы из эксперимента по метаболической стабильности исследовали с помощью ЖХ/МС/МС для метаболической характеристики и идентификации. Структуры метаболитов выясняли на основании многочисленных экспериментов МС/МС, таких как полный скан, скан нейтральной потери и скан ионов продукта. Метаболические пути затем постулировали на основании структур основных метаболитов. Что касается соединений из фосфинатной серии, N-окисление концевого кольца пиридина является преобладающим метаболическим путем с последующим окислением группы диметилфенила, где метильная группа(ы) гидроксилировалась, потом окислялась до альдегида и, наконец, до карбоновой кислоты. Выяснение метаболических путей является важным для понимания механизма элиминации тестируемого соединения и способствует разработке новых молекул с улучшенными характеристиками DM-PK.
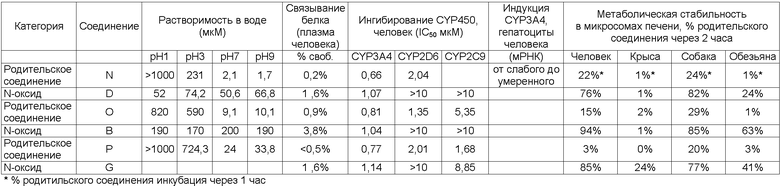
7. РК и пероральная биодоступность у крысы и собаки
Фармакокинетику тестируемого соединения оценивали на крысах Sprague-Dawley и гончих собаках. Типичное исследование РК включает в себя введение средства 2-3 животным через единичную болюс-инъекцию IV в концентрации 1 мг/кг, а другим 3 животным через единичное пероральное чреззондовое кормление в концентрации 5 мг/кг. Образцы крови брали в различные временные точки в течение 24-часового периода. Плазму отделяли и исследовали относительно тестируемого соединения и его метаболита(ов) с помощью ЖХ/МС/МС. Параметры РК рассчитывали по кривой концентрация плазмы - время, используя некомпартментальный способ. Пероральную биодоступность (F) рассчитывали по доза-нормализованным величинам AUC из перорального и IV введения. Более высокие величины пероральной биодоступности являются более подходящими.
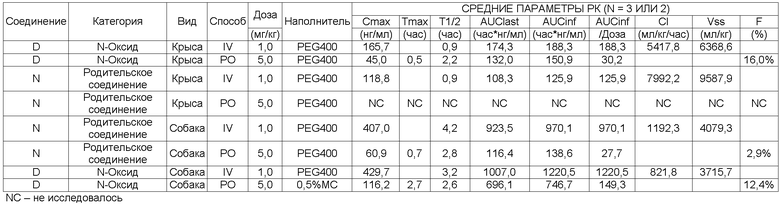
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ ПИРРОЛЫ, АКТИВНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2013 |
|
RU2666538C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2013 |
|
RU2667788C2 |
| 3-ЗАМЕЩЕННЫЕ ОКСИНДОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ КАЛИЙНЫХ КАНАЛОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ | 1996 |
|
RU2165925C2 |
| АНТАГОНИСТЫ АРИЛСУЛЬФОНАМИДА CCR3 | 2010 |
|
RU2539591C2 |
| ПОЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2557059C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2013 |
|
RU2654336C2 |
| 1,2,5-ТИАДИАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ ИНДОЛИЛАЛКИЛ-ПИРИМИДИНИЛ-ПИПЕРАЗИНОВ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1996 |
|
RU2165420C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2001 |
|
RU2340611C2 |
| ПРОИЗВОДНЫЕ АНТРАНИЛОВОЙ КИСЛОТЫ ИЛИ ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ НА ИХ ОСНОВЕ | 1994 |
|
RU2128644C1 |
| НОВЫЙ ПИРИМИДИНОВЫЙ НУКЛЕОЗИД ИЛИ ЕГО СОЛЬ | 2006 |
|
RU2395517C2 |
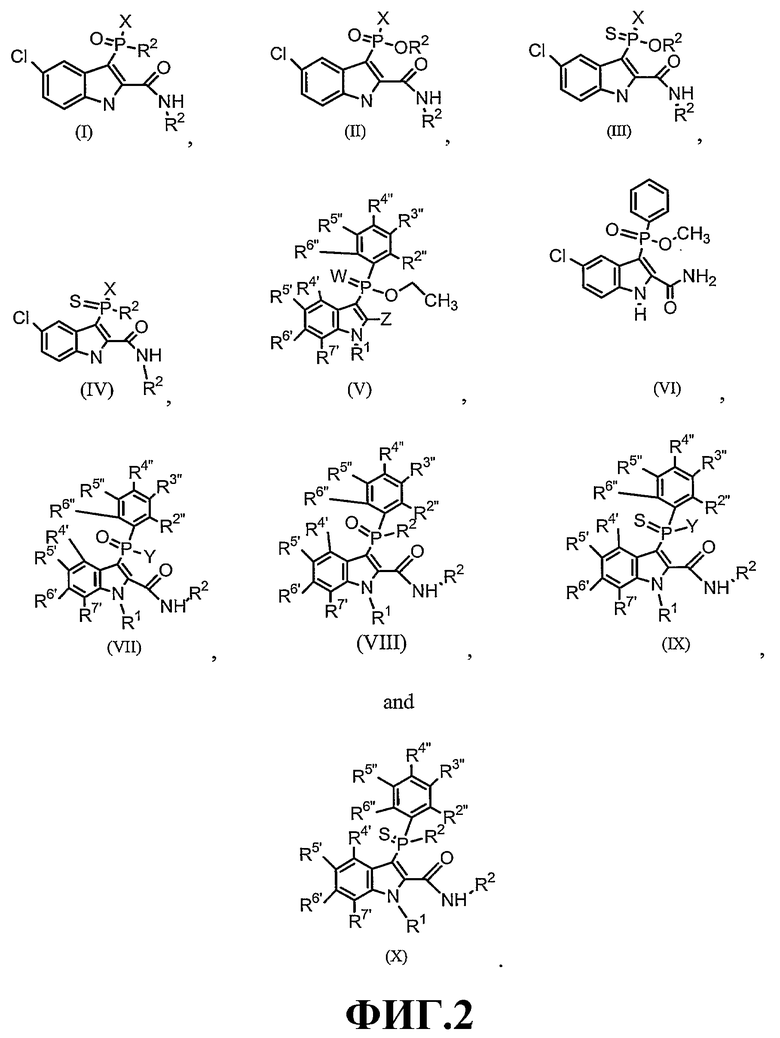
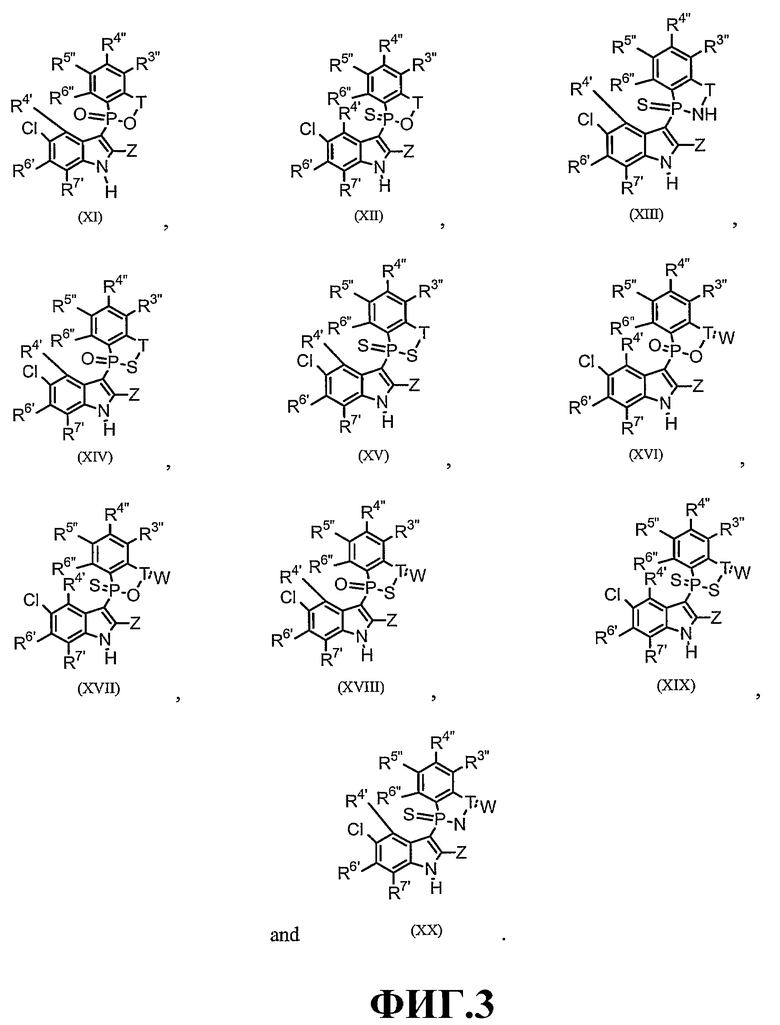
Настоящее изобретение относится к фосфоиндолам формул (А) и (В), и их применению для лечения ретровирусных инфекций, особенно ВИЧ-инфекции, в том числе в виде фармацевтически приемлемых солей, N-оксидов, четвертичных аминов, стереохимических изомеров и таутомеров
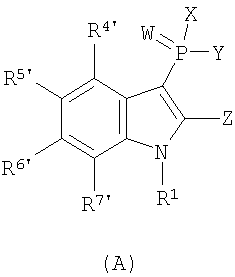 и
и 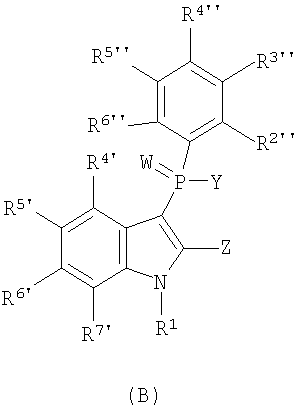
где Z представляет собой C(=O)-NH2; X - необязательно замещенный фенил; Y представляет собой О-алкил; R6′ и R7′ представляют собой Н; W может представлять собой О или S; R5′ может представлять собой галоген, метил, этил или CF3; R4′ может представлять собой Н, галоген, метил, этил или CF3; R1 может представлять собой Н или S(O)2-Ph; R2″, R3″, R4″, R5″ и R6″ могут представлять собой Н, галоген, CN, ОН, алкокси, SH, алкилтио, фенил, CF3, СН2ОН, алкил, галогеналкил, цианоалкил, гидроксиалкил, бензилоксиалкил, алкинил, алкенил, цианоалкинил, цианоалкенил. Технический результат - разработка новых противовирусных препаратов. 4 н. и 24 з.п. ф-лы, 3 ил., 5 табл.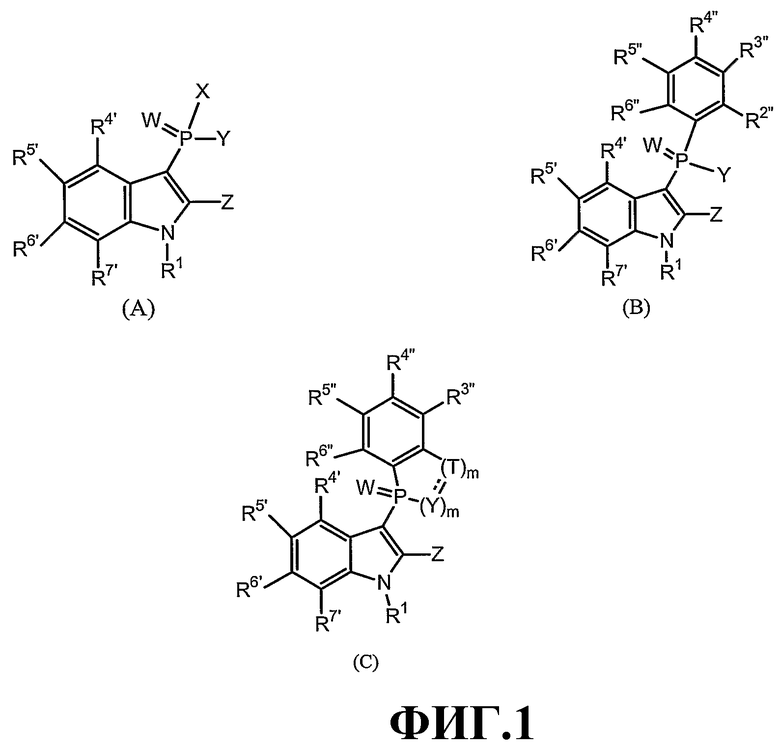
1. Соединение формулы (А):
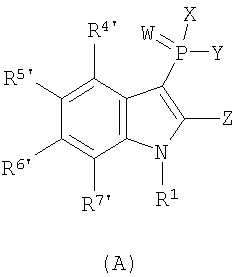
или его фармацевтически приемлемая соль, N-оксид, четвертичный амин, стереохимический изомер или таутомер,
где X представляет собой необязательно замещенный фенил, где указанное необязательное замещение включает один или более: гетероциклил, являющийся 5-членным моноциклом, содержащим 1-3 гетероатомов, выбранных из О, S и N; фенил, галоген, -CN, С3-6 циклоалкил, алкокси, гидроксил; С1-6 алкил, который необязательно может быть замещен галогеном, -CN, гидроксилом или бензилоксилом; или С2-6 алкинил или С2-6 алкенил, который необязательно может быть замещен -CN;
Y представляет собой О-алкил;
W представляет собой О или S;
каждый R1, R4′, R6′ и R7′ независимо представляет собой Н;
R5′ представляет собой галоген; и
Z представляет собой C(=O)-NH2;
2. Соединение по п.1 формулы (А):

или его фармацевтически приемлемая соль, N-оксид, четвертичный амин, стереохимический изомер или таутомер,
где X представляет собой необязательно замещенный фенил, где указанное необязательное замещение включает один или более: гетероциклил, являющийся 5-членным моноциклом, содержащим 1-3 гетероатомов, выбранных из О, S и N; фенил, галоген, -CN, С3-6 циклоалкил, алкокси, гидроксил; С1-6 алкил, который необязательно может быть замещен галогеном, -CN, гидроксилом или бензилоксилом; или С2-6 алкинил или С2-6 алкенил, который необязательно может быть замещен -CN;
Y представляет собой О-алкил;
W представляет собой О;
каждый R1, R4′, R6′ и R7′ независимо представляет собой Н;
R5′ представляет собой галоген; и
Z представляет собой C(=O)-NH2;
3. Соединение по п.1, в котором R5′ представляет собой хлор.
4. Соединение по п.1, в котором Y представляет собой -О-С1-6алкил.
5. Соединение по п.1, выбранное из группы, состоящей из:
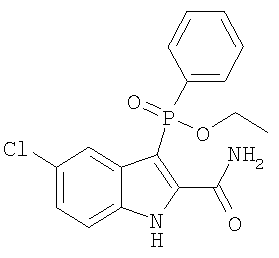
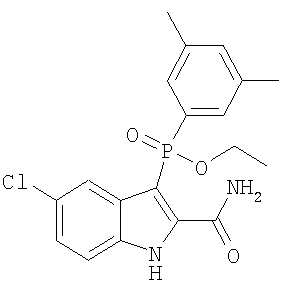 и
и 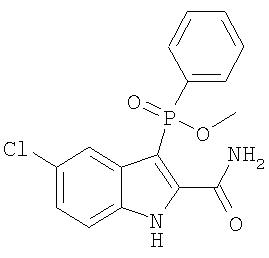 .
.
6. Соединение по п.1, представляющее собой:
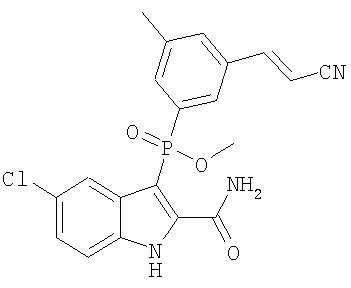 .
.
7. Соединение формулы (В):
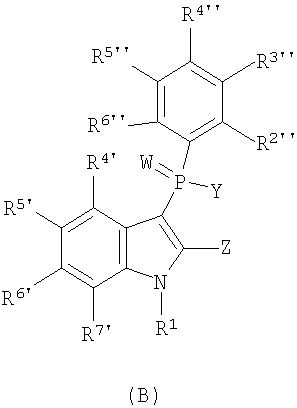
или его фармацевтически приемлемая соль, N-оксид, четвертичный амин, стереохимический изомер или таутомер,
где Y представляет собой О-алкил;
W представляет собой О;
R1 представляет собой Н, S(O)2-R3;
R3 представляет собой фенил;
каждый R6′ и R7′ независимо представляет собой Н;
каждый R4′ и R5′ независимо представляет собой Cl, F, Br, I, метил, этил или CF3;
Z представляет собой С(=O)-NH2;
каждый R2″, R3″, R4″, R5″ и R6″ независимо представляет собой Н, галоген, CN, OR2, SR2, фенил, CF3, СН2ОН; С1-6 алкил, который необязательно может быть замещен галогеном, CN, гидроксилом или бензилоксилом; или С2-6 алкинил или С2-6 алкенил, который необязательно может быть замещен CN; и
каждый R2 независимо представляет собой Н или алкил.
8. Соединение по п.7, в котором каждый R2″, R4″ и R6″ независимо представляет собой Н; и
каждый R3″ и R5″ независимо представляет собой галоген, CN, OR2, SR2, фенил, CF3; C1-6 алкил, который необязательно может быть замещен галогеном, CN, гидроксилом или бензилоксилом; или С2-6 алкинил или С2-6 алкенил, который необязательно может быть замещен CN.
9. Соединение по п.7, представляющее собой:
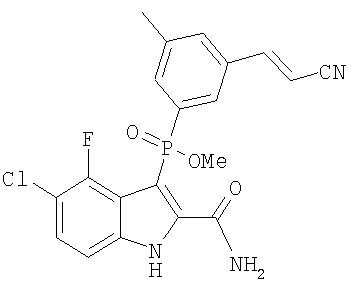 .
.
10. Фармацевтическая композиция для лечения или профилактики ВИЧ-инфекции у хозяина необязательно в виде восстановительной терапии, содержащая соединение по любому одному из пп.1-9 или его фармацевтически приемлемую соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем.
11. Фармацевтическая композиция для лечения или профилактики ВИЧ-инфекции у хозяина необязательно в виде восстановительной терапии, содержащая соединение по любому одному из пп.1-9 или его фармацевтически приемлемую соль, стереоизомер, таутомер, N-оксид или четвертичный амин в сочетании с по меньшей мере одним другим анти-ВИЧ средством, необязательно с фармацевтически приемлемым носителем или разбавителем, где другое анти-ВИЧ средство выбирают из группы, состоящей из протеазного ингибитора, ингибитора ВИЧ-интегразы, ингибитора хемокина, ингибитора обратной транскриптазы, аналога пирофосфата или ингибитора слияния-связывания.
12. Фармацевтическая композиция по п.11, в которой другое анти-ВИЧ средство представляет собой ингибитор обратной транскриптазы.
13. Фармацевтическая композиция по п.12, в которой ингибитор обратной транскриптазы индуцирует мутацию лизина 103→аспарагин и/или тирозина 181→цистеин в обратной транскриптазе ВИЧ.
14. Соединение по п.1 или его фармацевтически приемлемая соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем для применения при лечении или профилактики ВИЧ-инфекции у хозяина.
15. Соединение по п.6 или его фармацевтически приемлемая соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем для применения при лечении или профилактики ВИЧ-инфекции у хозяина.
16. Соединение по п.7 или его фармацевтически приемлемая соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем для применения при лечении или профилактики ВИЧ-инфекции у хозяина.
17. Соединение по п.9 или его фармацевтически приемлемая соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем для применения при лечении или профилактики ВИЧ-инфекции у хозяина.
18. Соединение по п.1 или его фармацевтически приемлемая соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем для применения в сочетании и/или при чередовании по меньшей мере с одним другим анти-ВИЧ средством для лечения или профилактики ВИЧ-инфекции у хозяина.
19. Соединение по п.6 или его фармацевтически приемлемая соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем для применения в сочетании и/или при чередовании по меньшей мере с одним другим анти-ВИЧ средством для лечения или профилактики ВИЧ-инфекции у хозяина.
20. Соединение по п.7 или его фармацевтически приемлемая соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем для применения в сочетании и/или при чередовании по меньшей мере с одним другим анти-ВИЧ средством для лечения или профилактики ВИЧ-инфекции у хозяина.
21. Соединение по п.9 или его фармацевтически приемлемая соль, стереоизомер, таутомер, N-оксид или четвертичный амин необязательно с фармацевтически приемлемым носителем или разбавителем для применения в сочетании и/или при чередовании по меньшей мере с одним другим анти-ВИЧ средством для лечения или профилактики ВИЧ-инфекции у хозяина.
22. Соединение по любому одному из пп.18-21, в котором другое анти-ВИЧ средство представляет собой ингибитор обратной транскриптазы.
23. Соединение по п.22, в котором ингибитор обратной транскриптазы индуцирует мутацию лизина 103→аспарагин и/или тирозина 181→цистеин в обратной транскриптазе ВИЧ.
24. Соединение по любому одному из пп.14-21, при котором ВИЧ имеет мутацию лизина 103→аспарагин и/или тирозина 181→цистеин в обратной транскриптазе ВИЧ.
25. Соединение по любому одному из пп.14-21, при котором ВИЧ резистентен к одному или более ингибитору(ам) обратной транскриптазы.
26. Соединение по любому одному из пп.14-21 для восстановительной терапии при лечении или профилактике ВИЧ-инфекции у хозяина.
27. Соединение по любому одному из пп.14-21, в котором хозяином является человек.
28. Соединение по п.26, в котором хозяином является человек.
| АНАЛОГИ Δ-ИЗОТАКСОЛА, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2142950C1 |
| HORWITZ J.P | |||
| ET AL | |||
| Journal of medical chemistry, 1970, vol.13, №5, 1024-1025 | |||
| TSOU K.C | |||
| ET AL | |||
| Journal of medical chemistry, 1970, vol.13, №4, 765-768 | |||
| TSOU K.C | |||
| ET AL | |||
| Journal of medical chemistry, 1972, vol.15, №12, 1221-1224 | |||
| MARCH L.C | |||
| ET AL | |||
| Journal of heterocyclic chemistry, 1970, vol.7, | |||
Авторы
Даты
2010-06-27—Публикация
2005-09-16—Подача