Текст описания приведен в факсимильном виде. 





















































































































































































































































































































































































































| название | год | авторы | номер документа |
|---|---|---|---|
| НИКОТИНОВЫЕ ИММУНОНАНОТЕРАПЕВТИЧЕСКИЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА | 2009 |
|
RU2487712C2 |
| НАЦЕЛИВАНИЕ НА АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ ИММУНОНАНОТЕРАПЕВТИЧЕСКИХ СРЕДСТВ | 2009 |
|
RU2497542C2 |
| ОПРЕДЕЛЕНИЕ ДОЗЫ ДЛЯ ИММУНОТЕРАПЕВТИЧЕСКИХ СРЕДСТВ | 2017 |
|
RU2771717C2 |
| СИСТЕМА И СПОСОБ ПОЛУЧЕНИЯ И ХРАНЕНИЯ АКТИВИРОВАННЫХ ЗРЕЛЫХ ДЕНДРИТНЫХ КЛЕТОК | 2011 |
|
RU2575978C2 |
| МУТАНТНЫЕ ПОЛИПЕПТИДЫ СУАА И ПРОИЗВОДНЫЕ ПОЛИПЕПТИДОВ, ПОДХОДЯЩИЕ ДЛЯ ДОСТАВКИ ИММУНОГЕННЫХ МОЛЕКУЛ В КЛЕТКУ | 2010 |
|
RU2585216C2 |
| ВВЕДЕНИЕ ДЕНДРИТНЫХ КЛЕТОК, ПОДВЕРГНУТЫХ ЧАСТИЧНОМУ СОЗРЕВАНИЮ IN VITRO, ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2003 |
|
RU2348418C2 |
| ВНУТРИКЛЕТОЧНЫЙ ДОМЕН БЕЛКА HER-2/NEU ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ МАЛИГНИЗАЦИЙ | 1996 |
|
RU2236461C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА И ДРУГИХ ВНУТРИКЛЕТОЧНЫХ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ И ВАКЦИНА, ПОЛУЧЕННАЯ ПО НАЗВАННОМУ СПОСОБУ | 2001 |
|
RU2262950C2 |
| ИММУНОСТИМУЛИРУЮЩИЕ G, U-СОДЕРЖАЩИЕ ОЛИГОРИБОНУКЛЕОТИДЫ | 2003 |
|
RU2302865C2 |
| ИММУНОТЕРАПЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ОСНОВЕ ДРОЖЖЕЙ-MUC1 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2642300C2 |
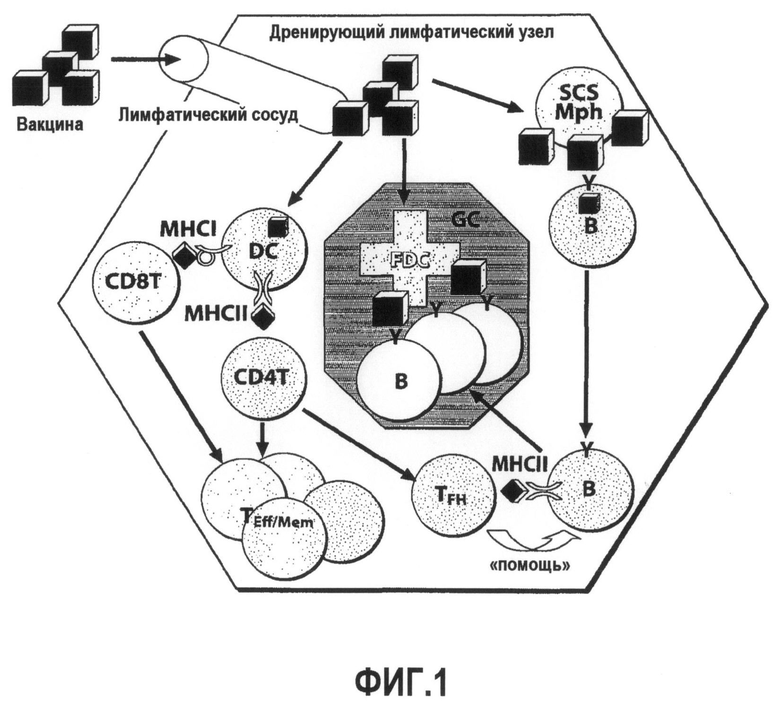


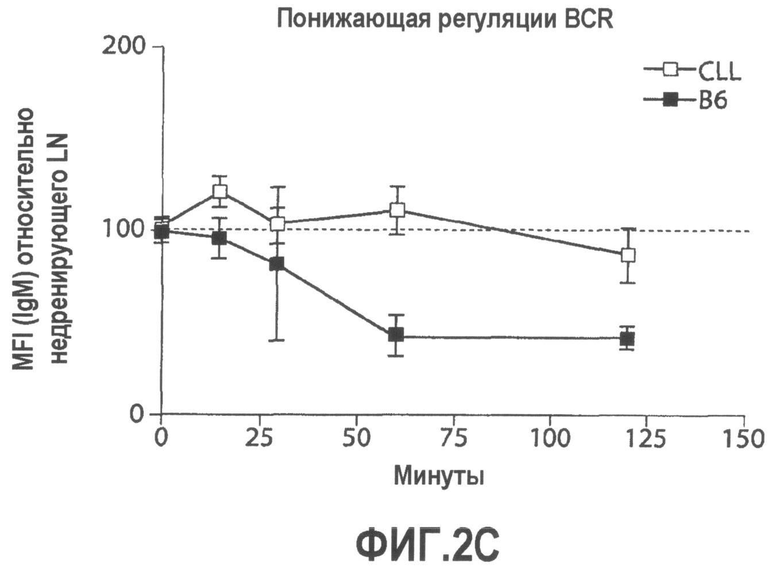
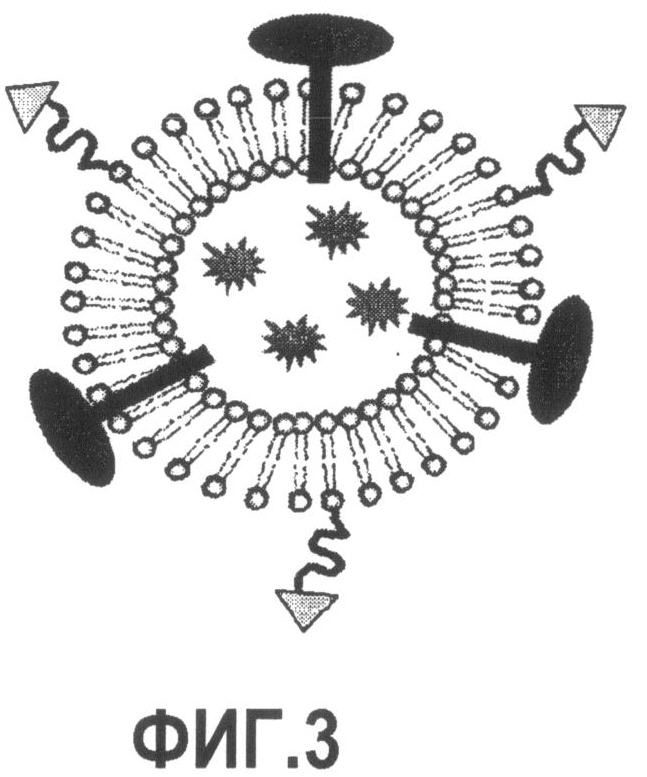
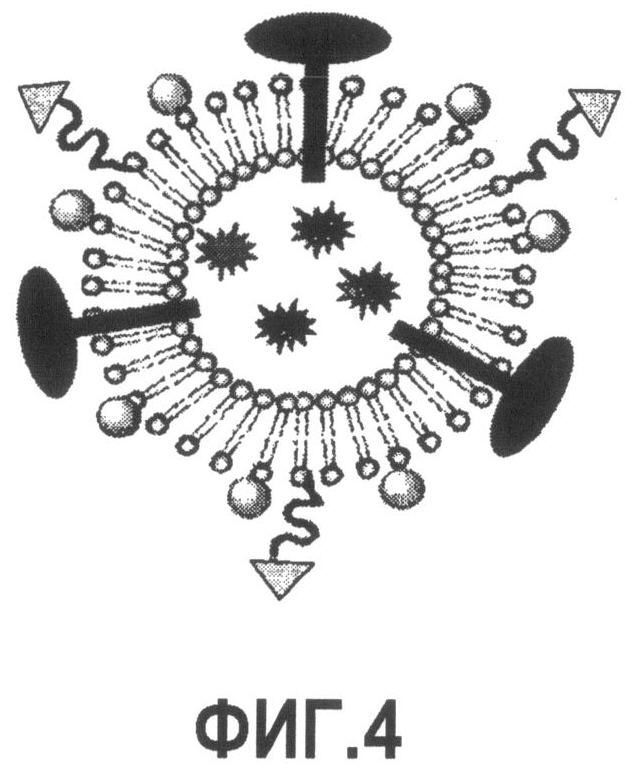
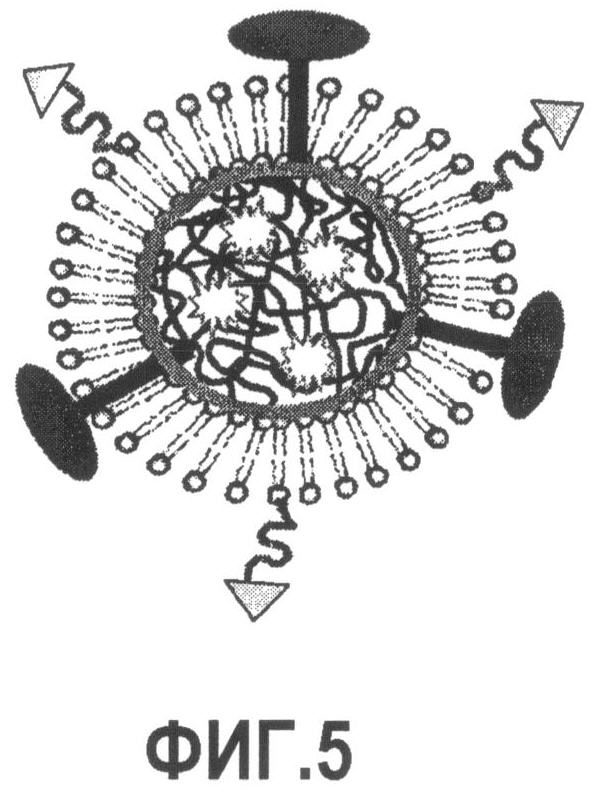



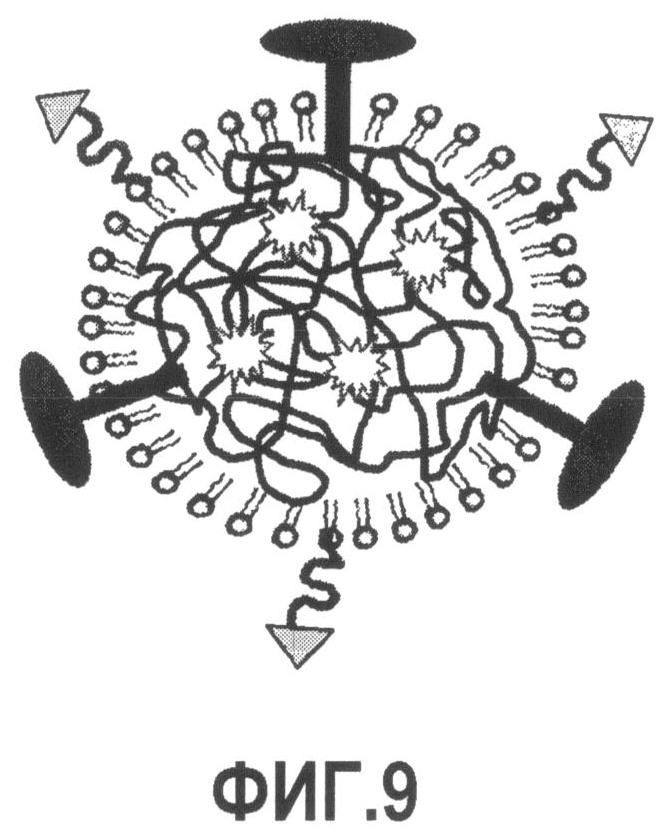
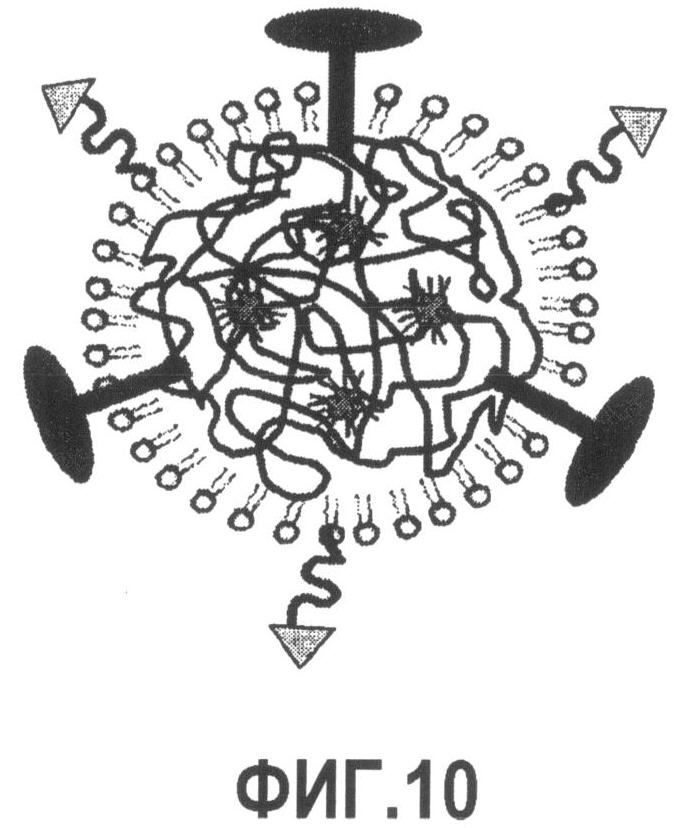
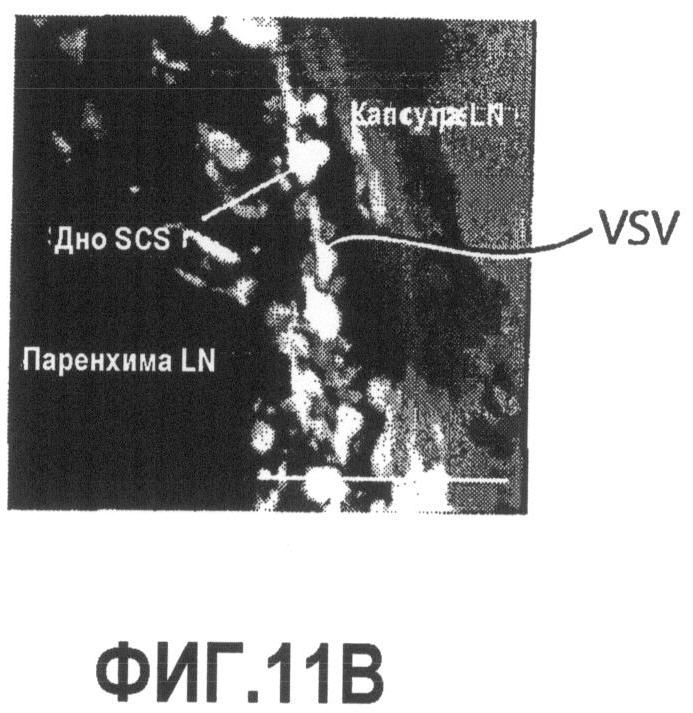


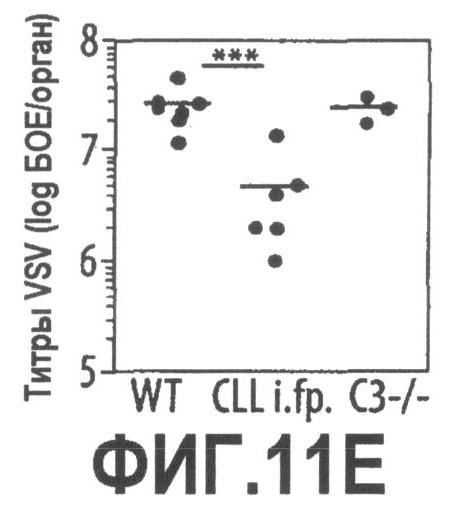
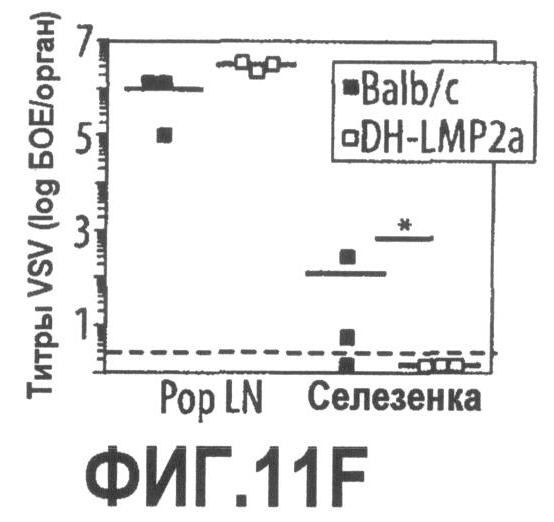
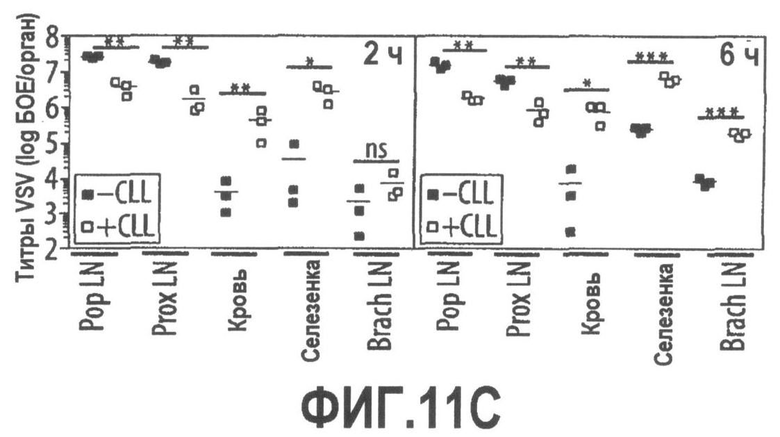
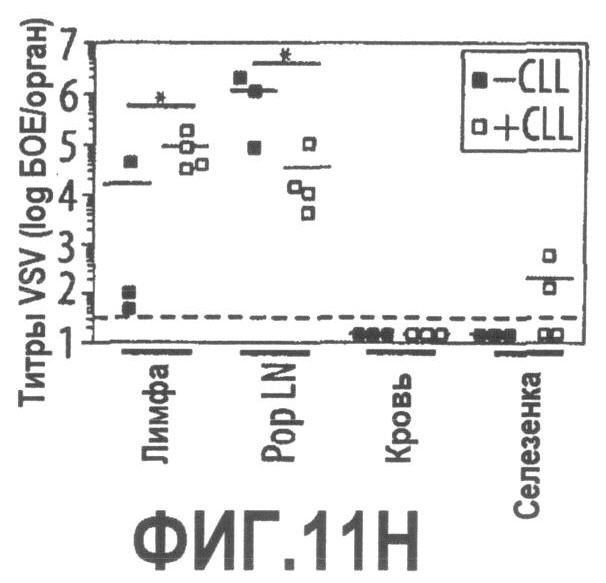
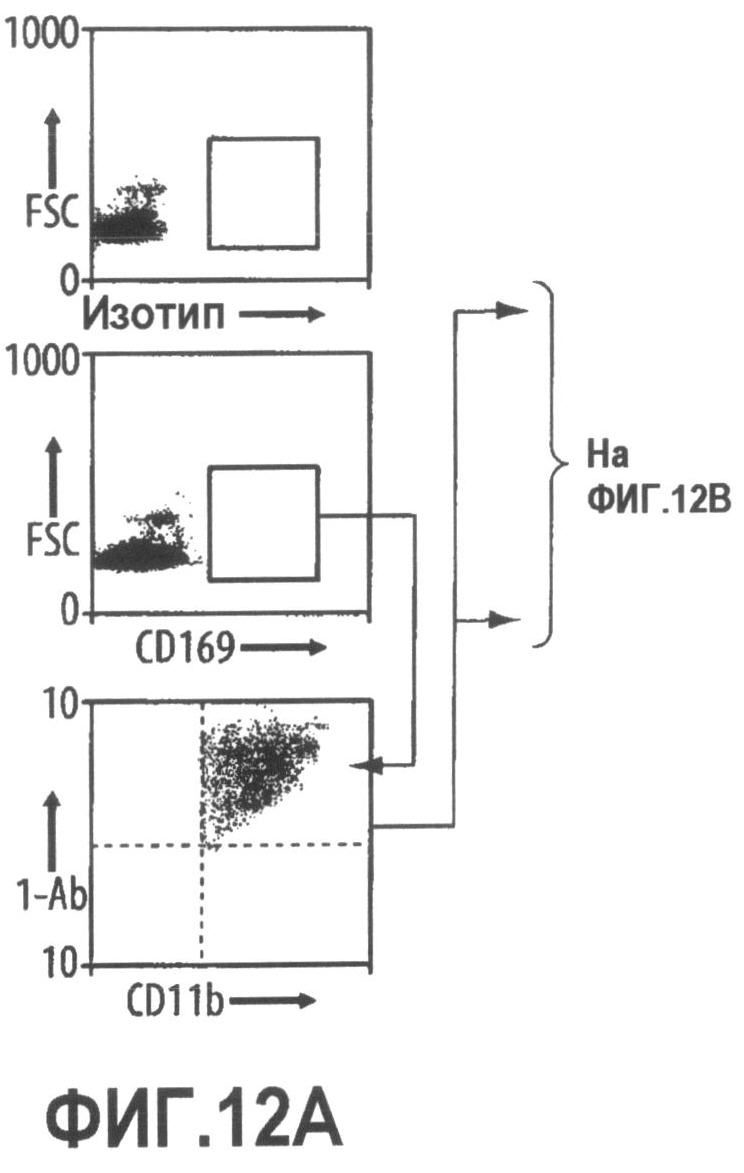


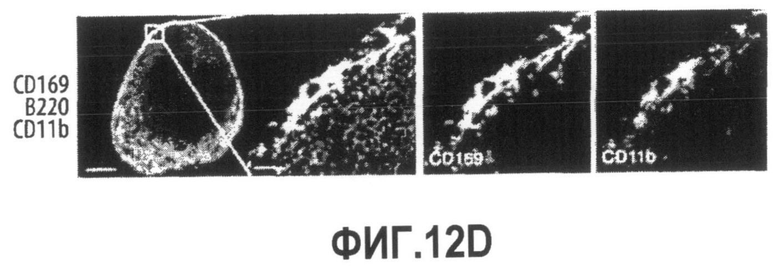

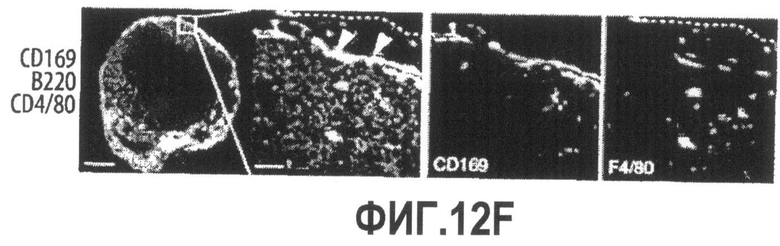
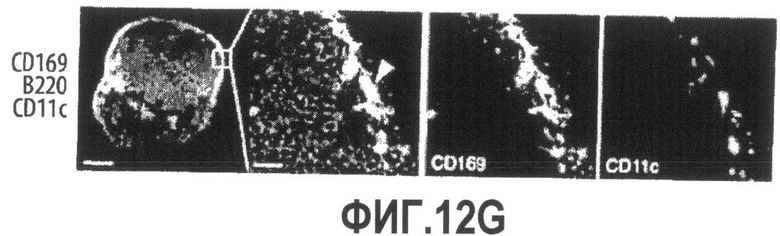
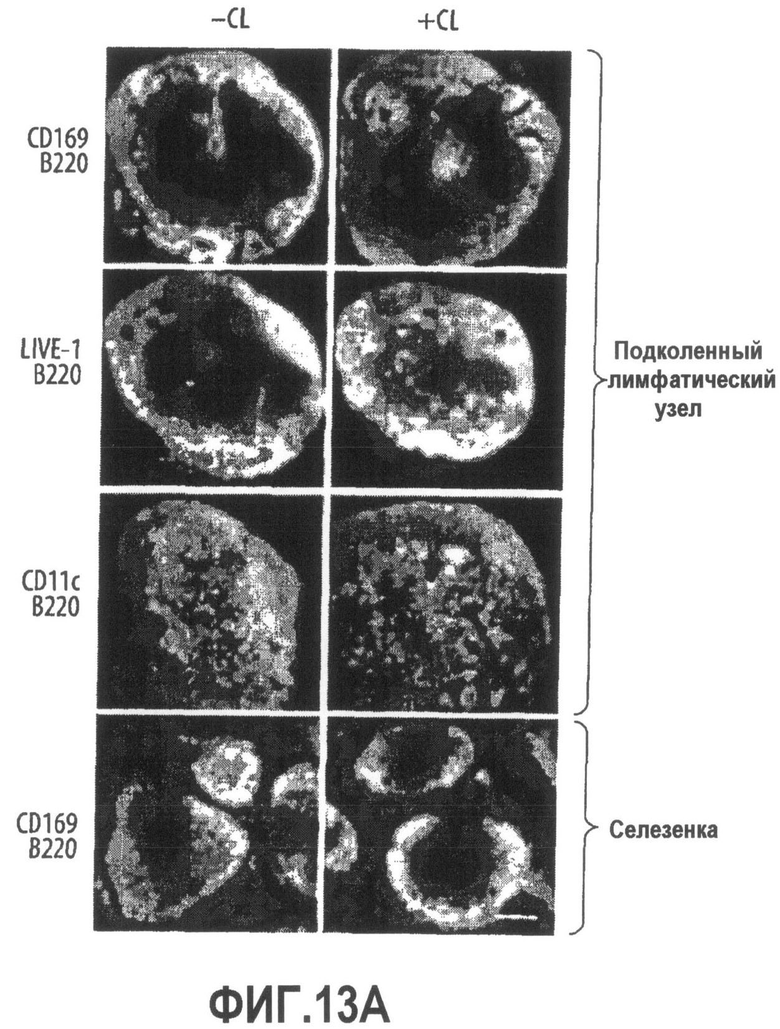


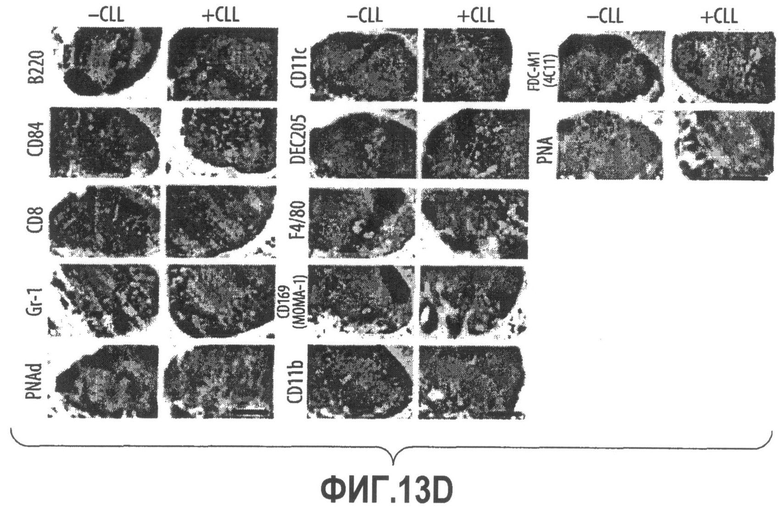
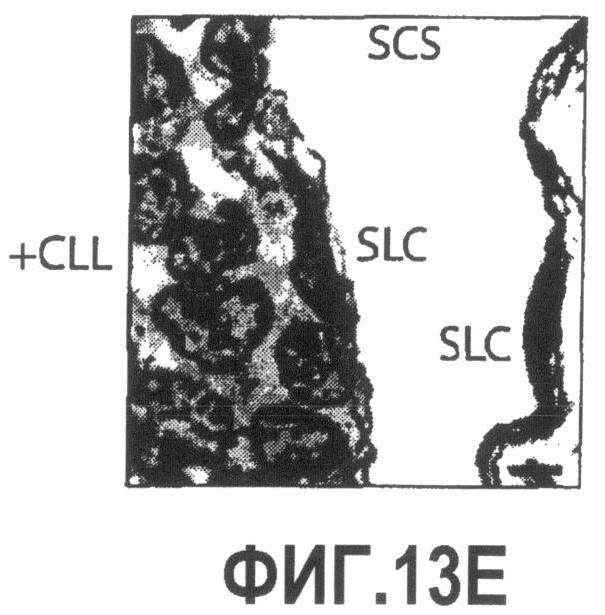


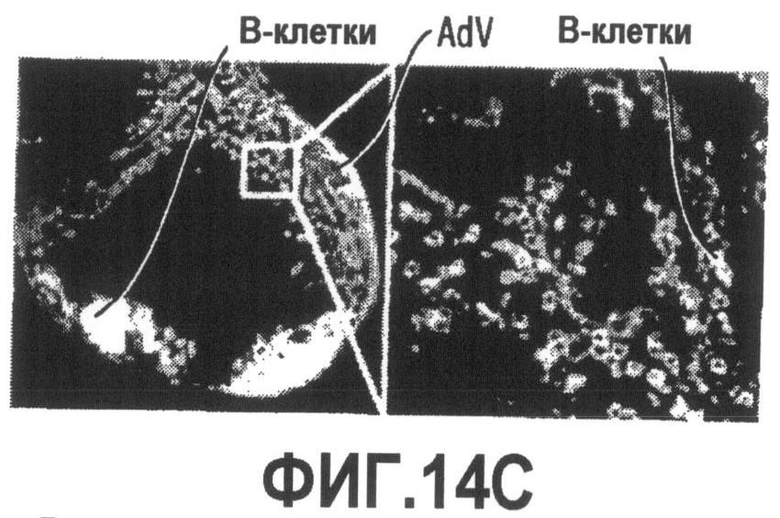


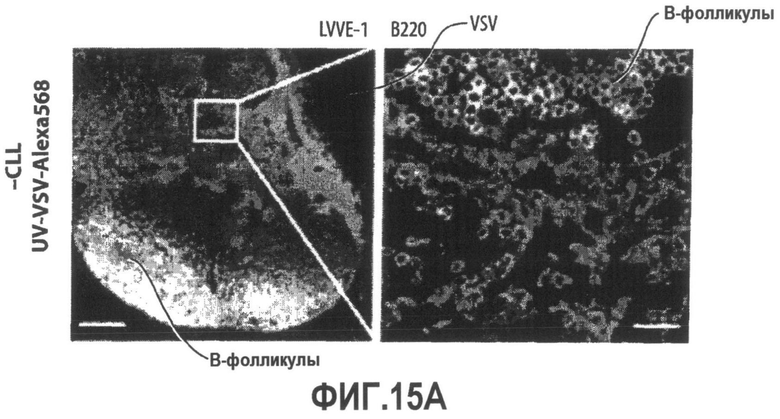


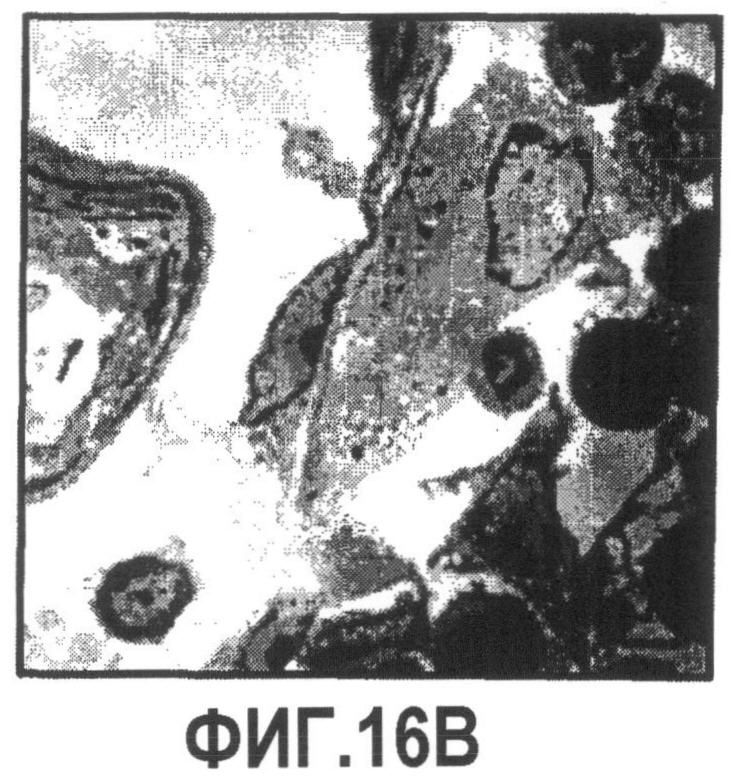
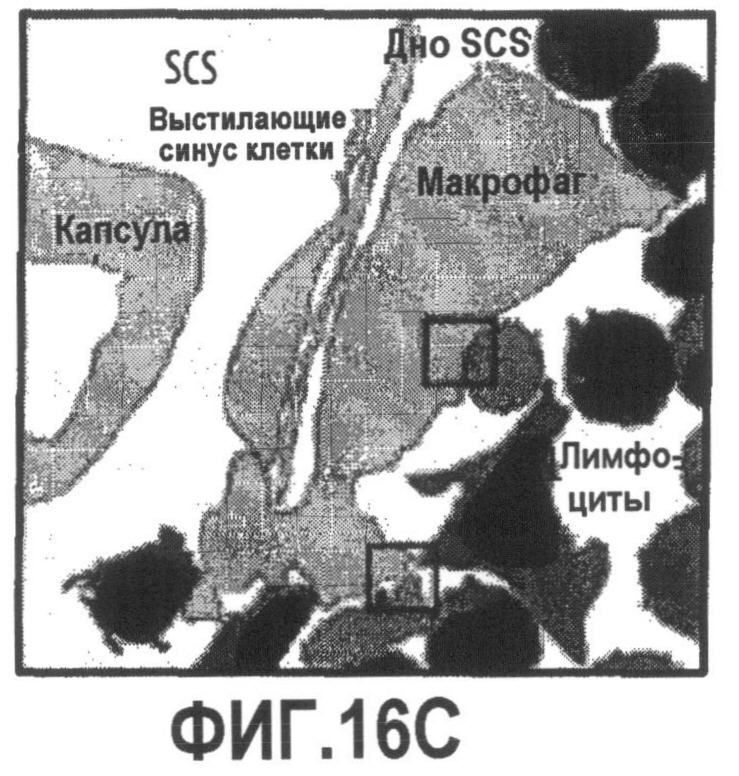
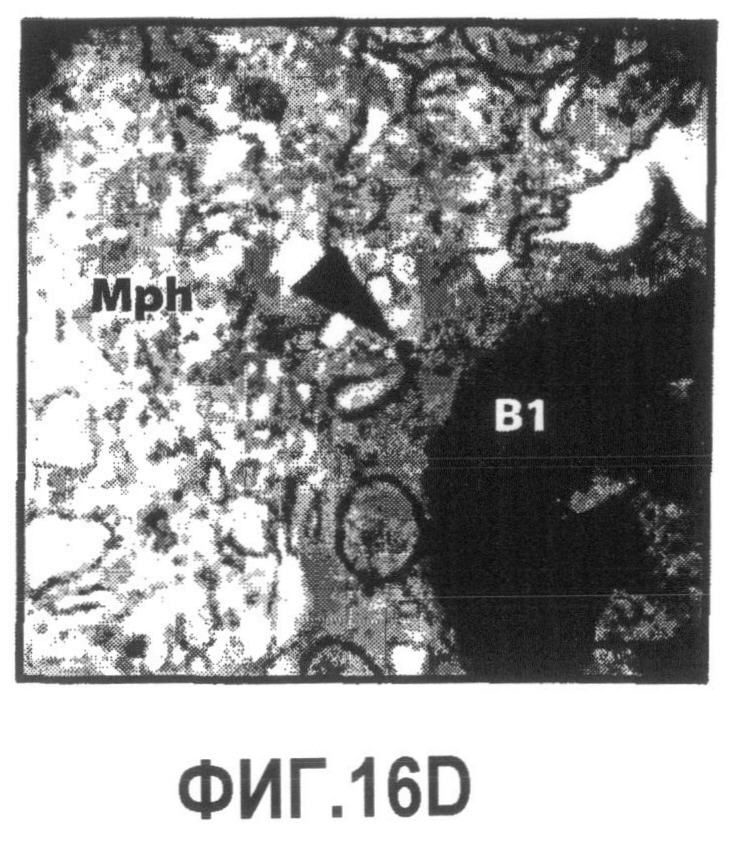


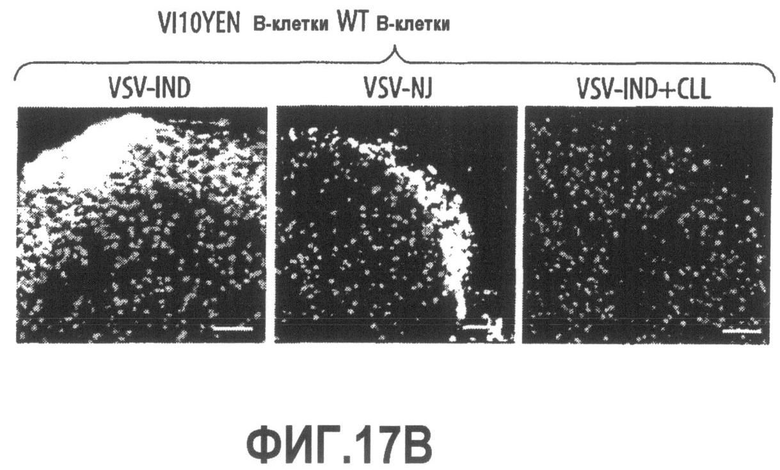
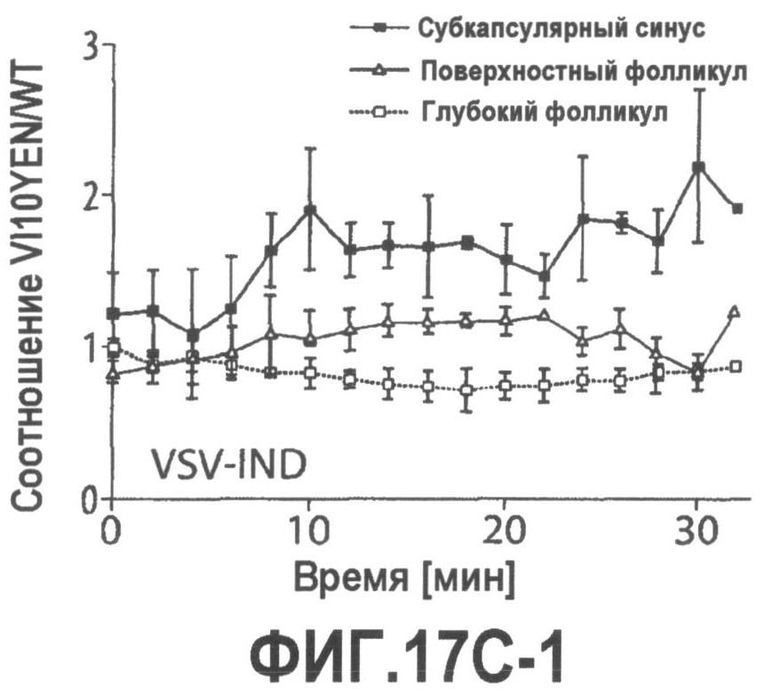



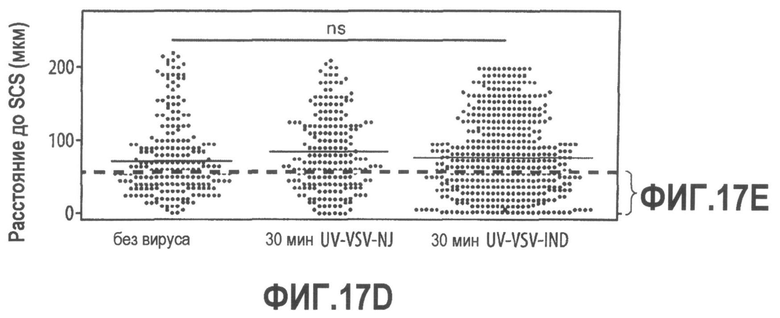
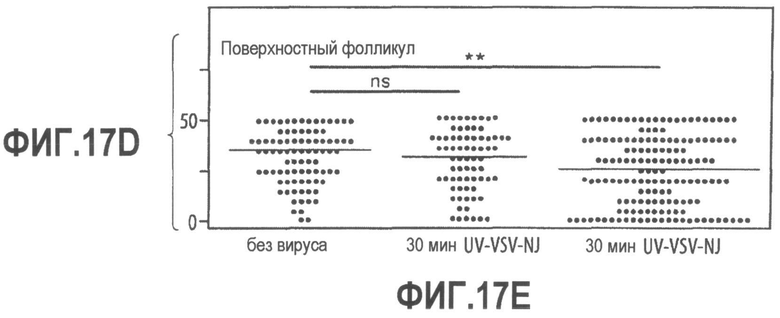
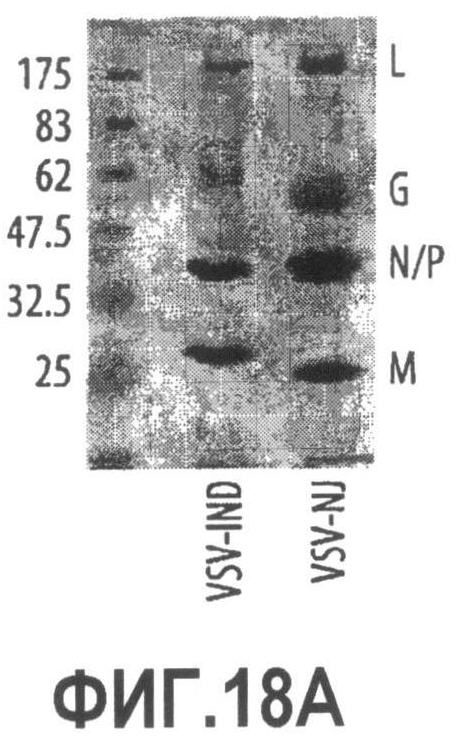
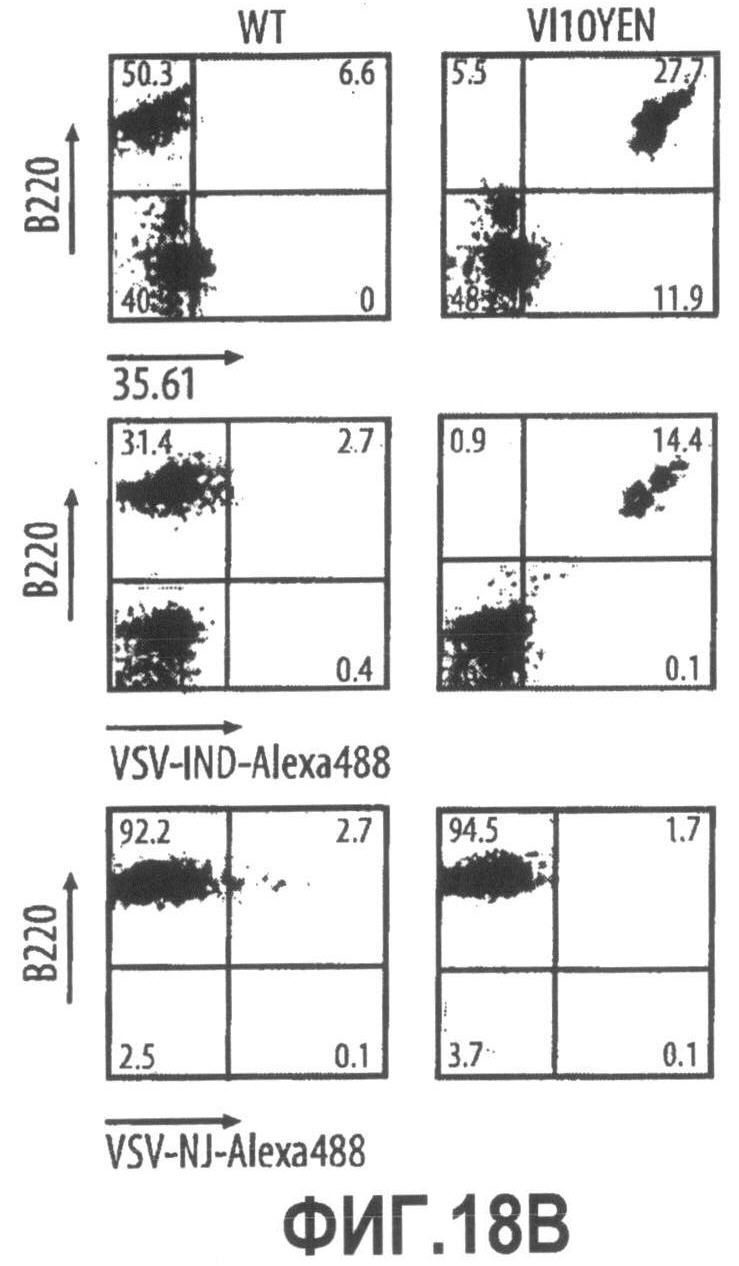
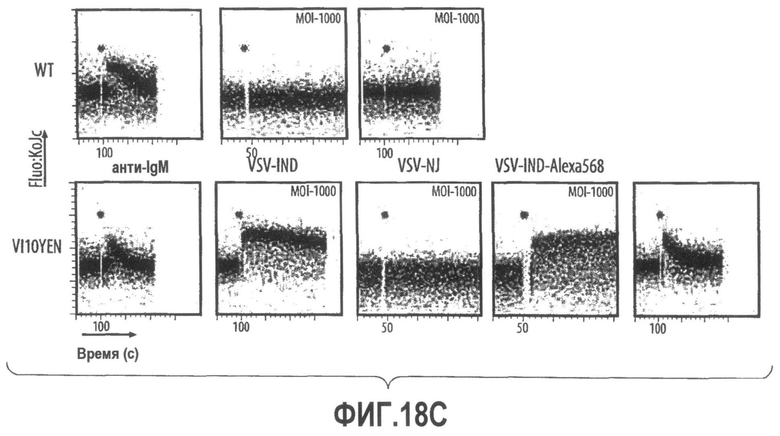
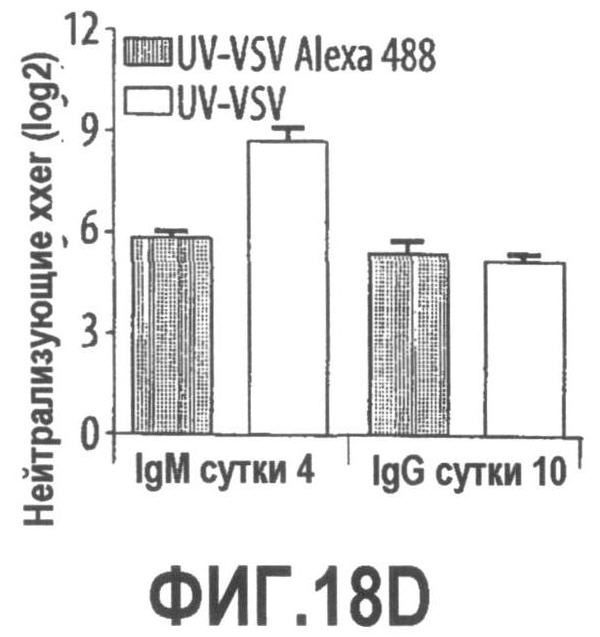
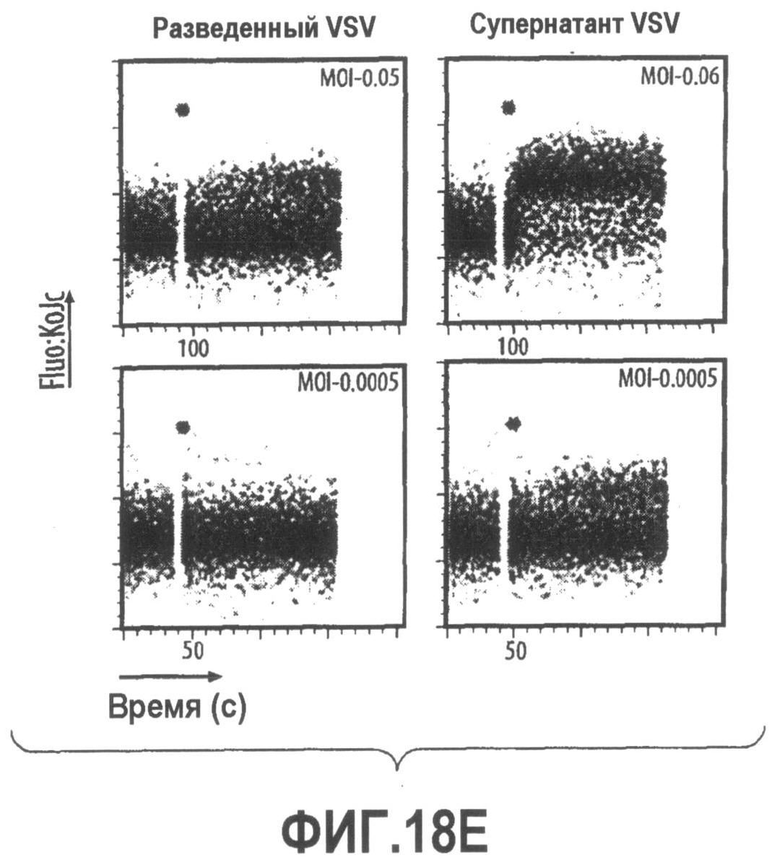
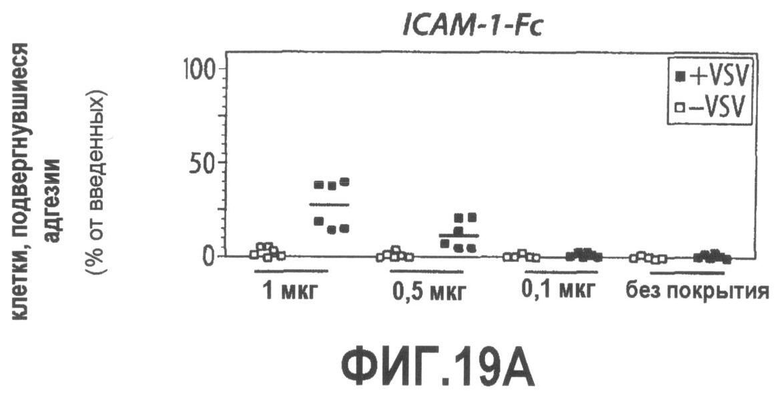
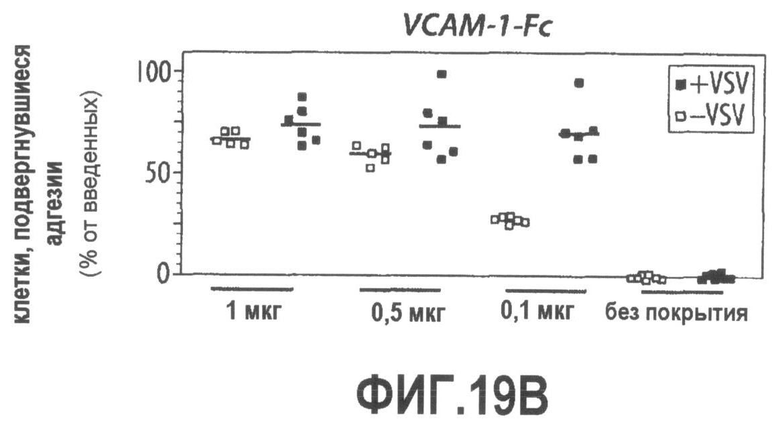
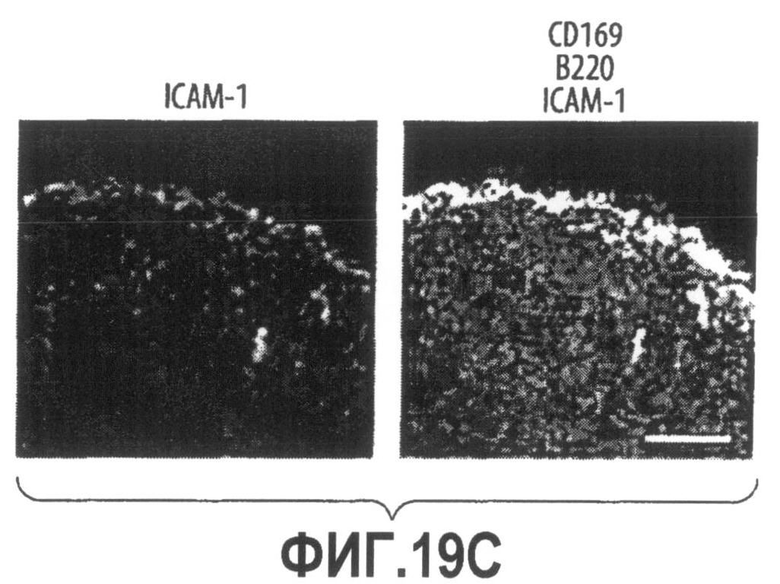


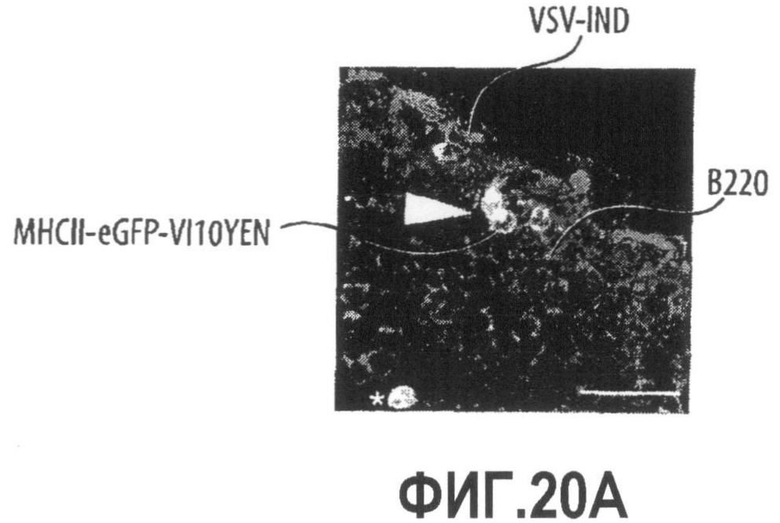
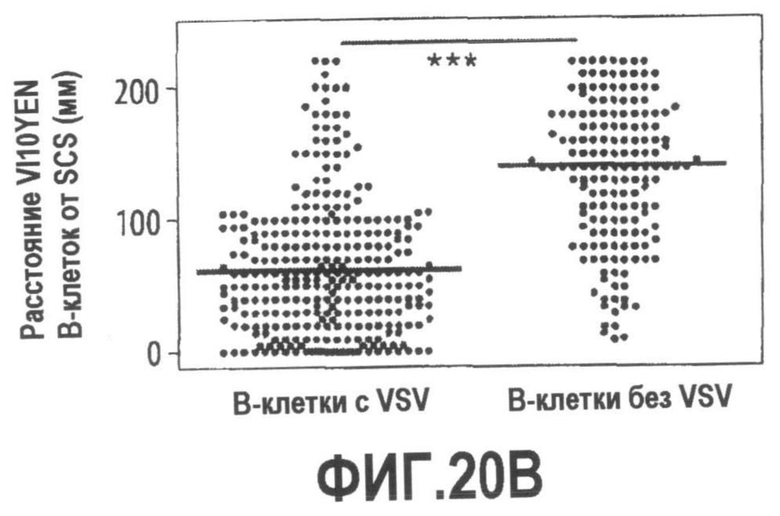
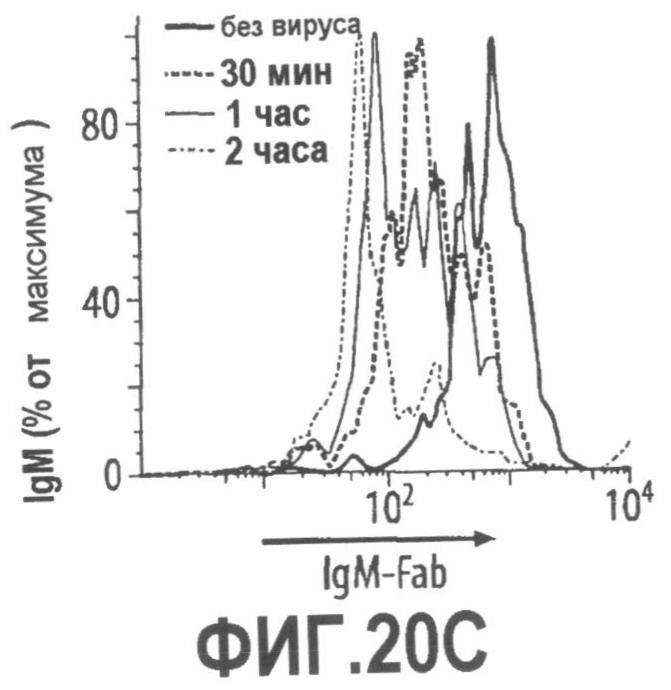
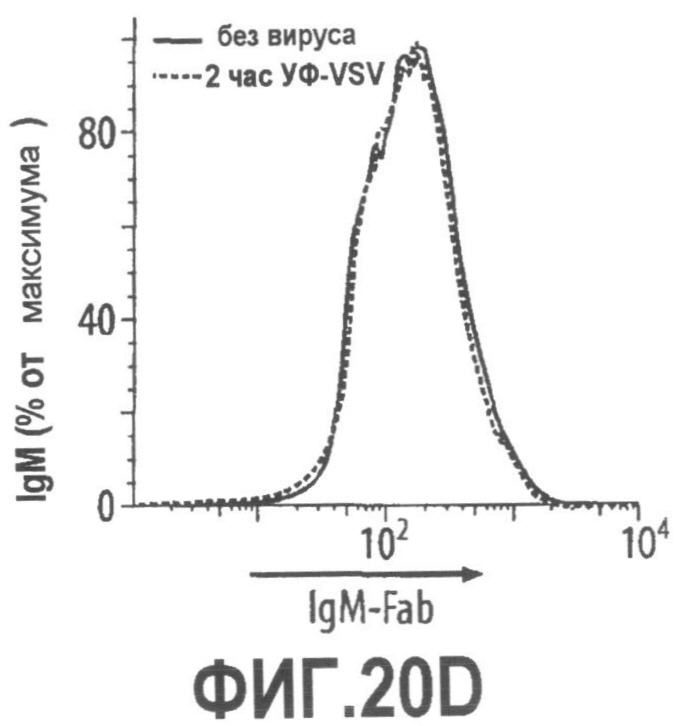
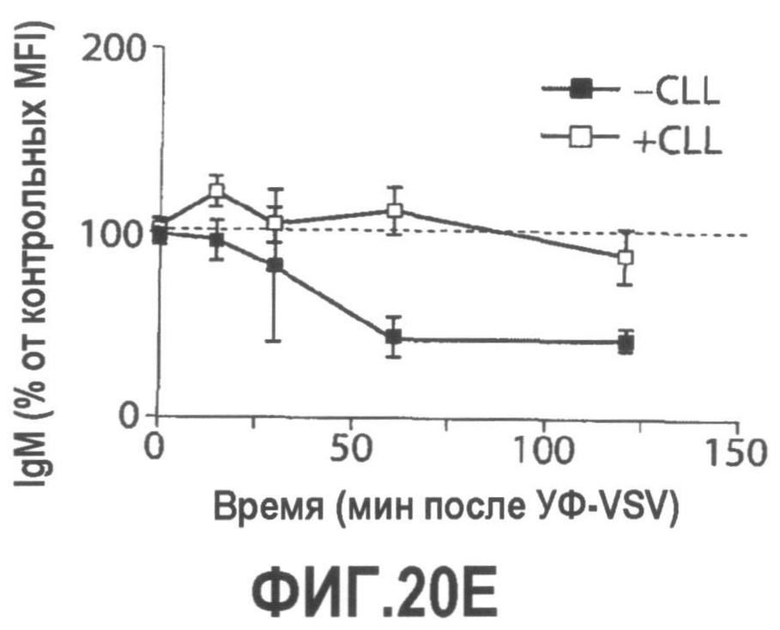
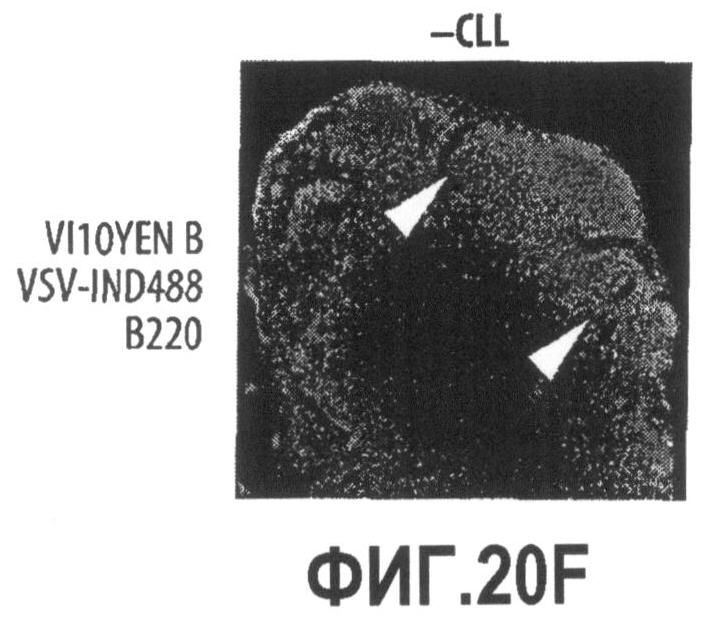

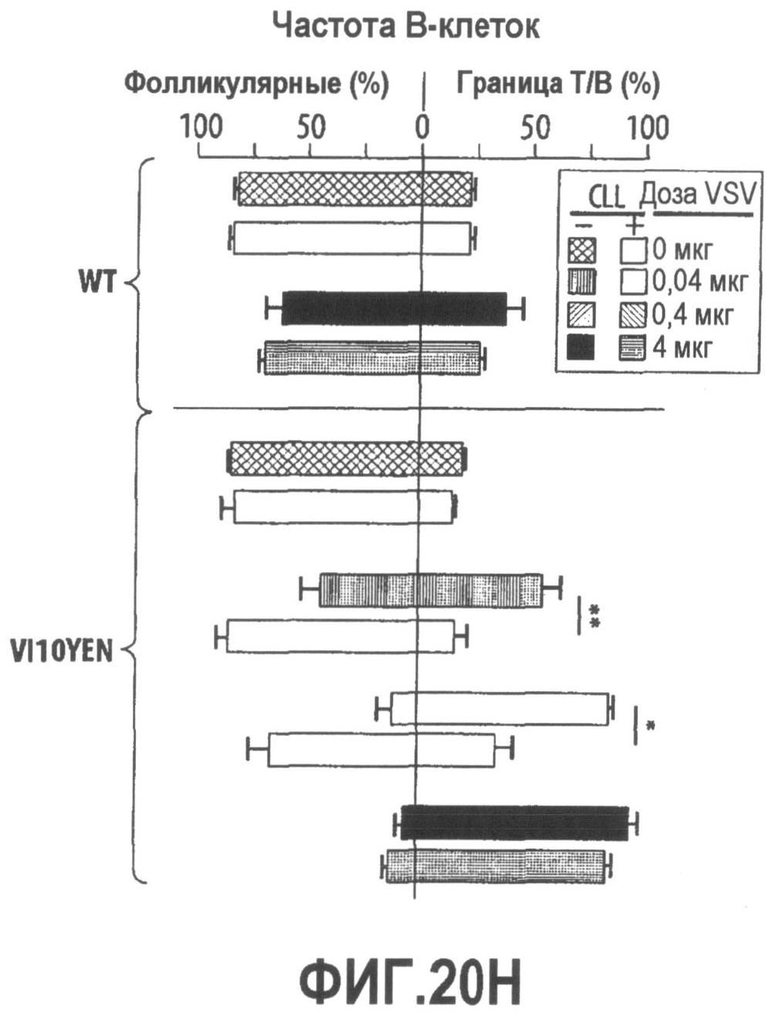

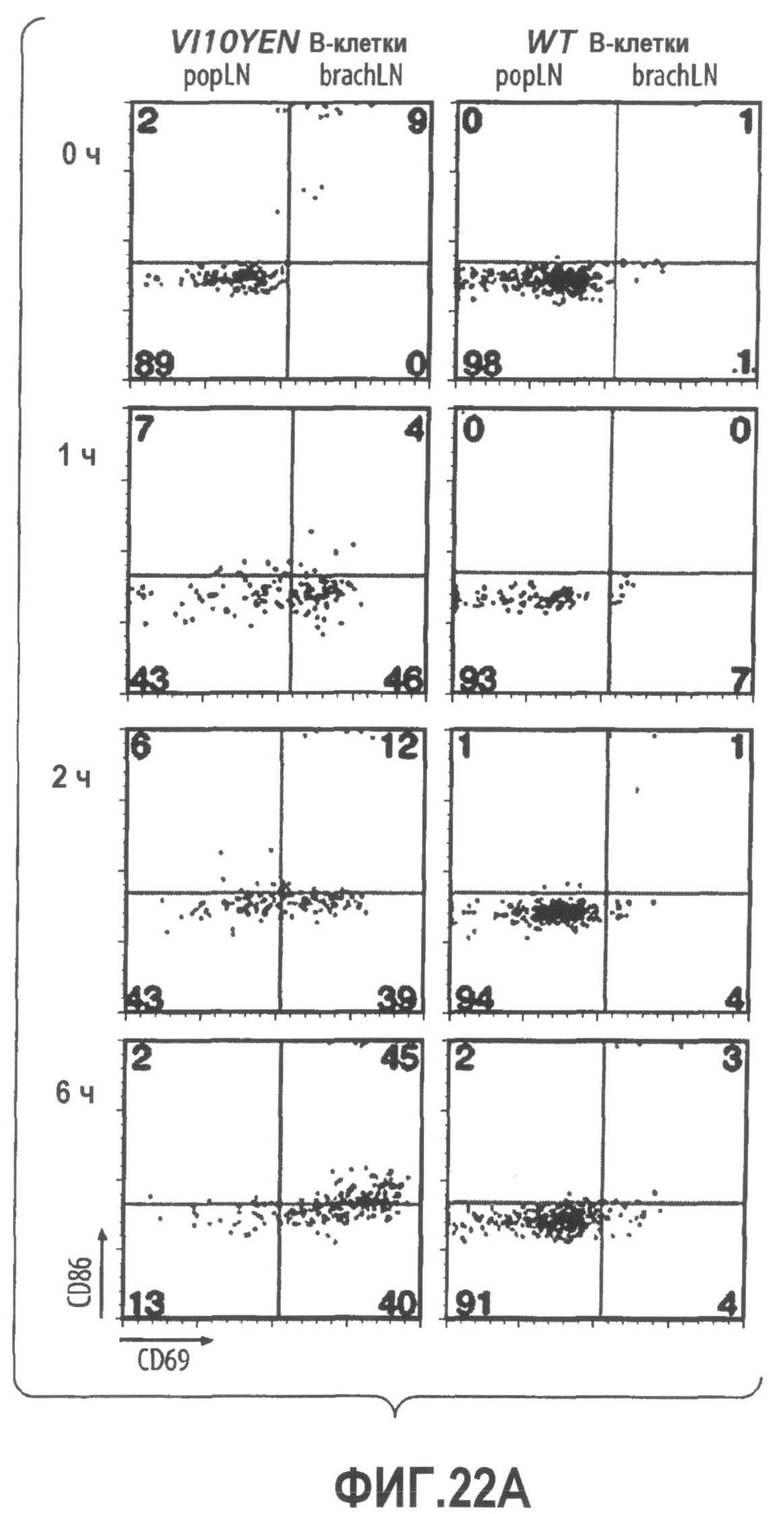


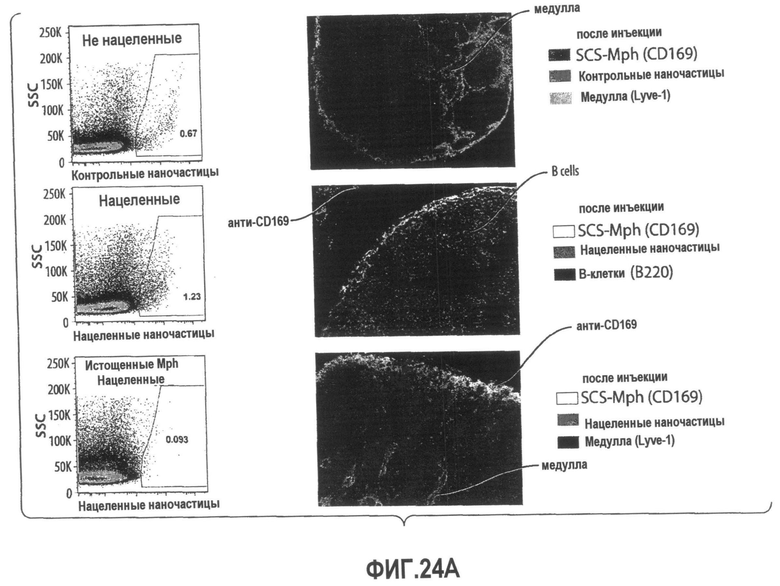


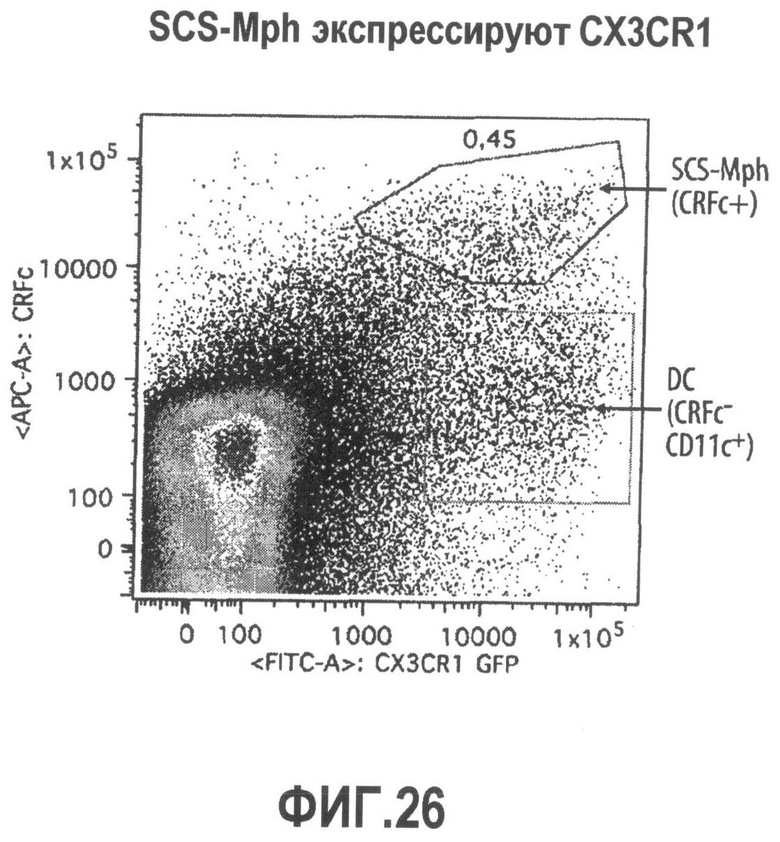

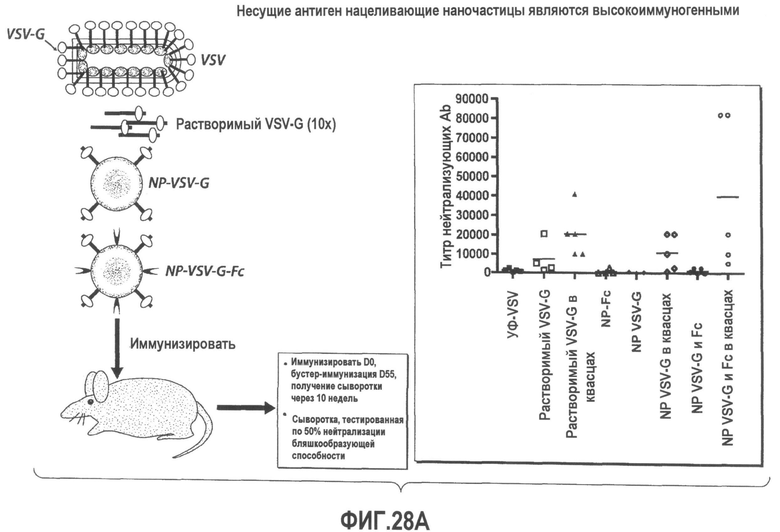
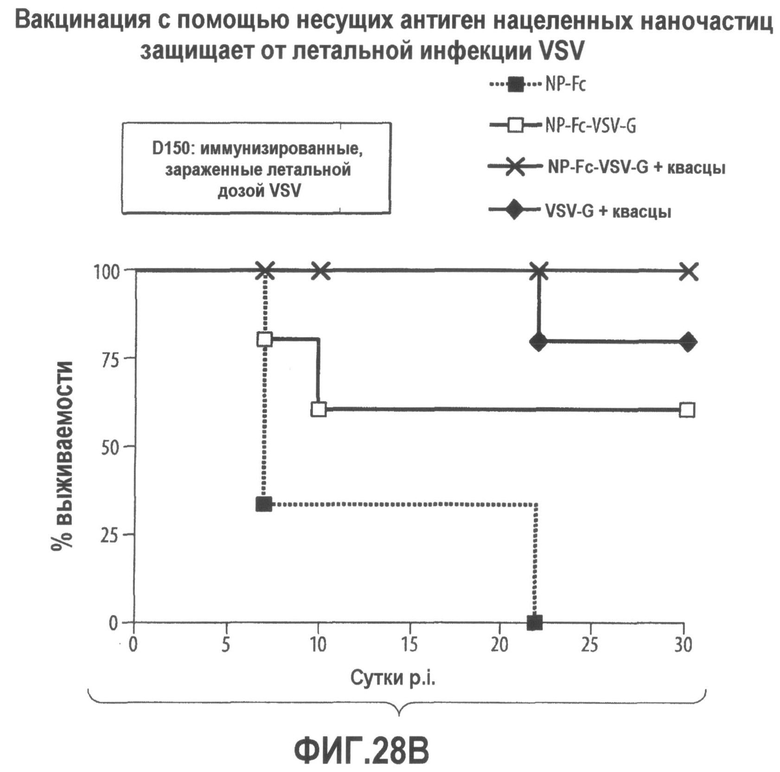
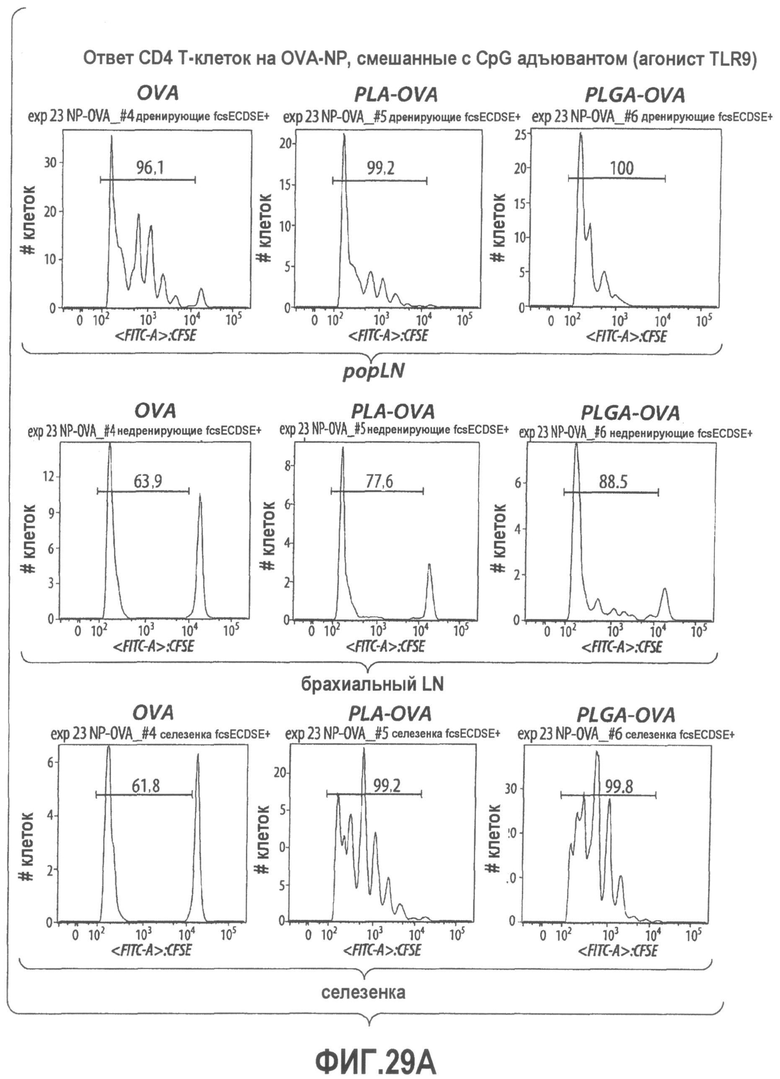




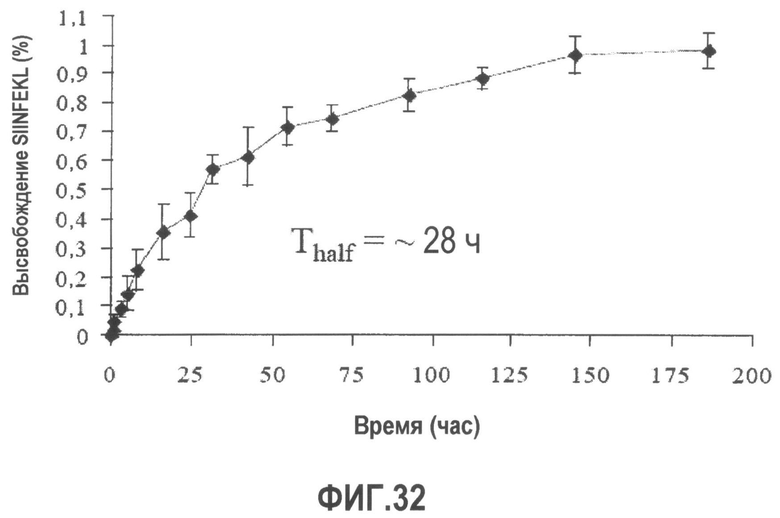
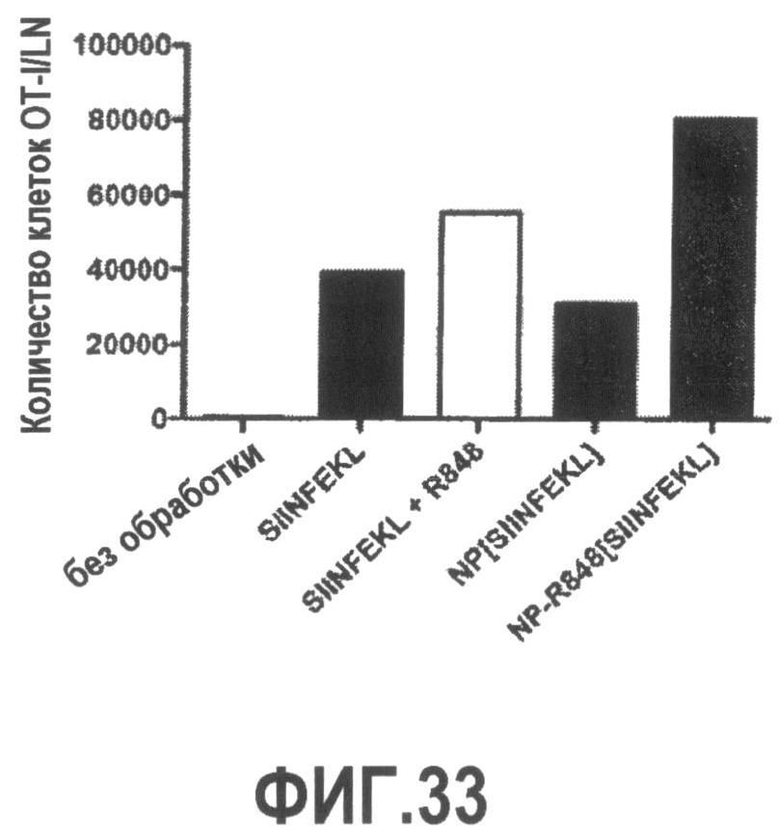

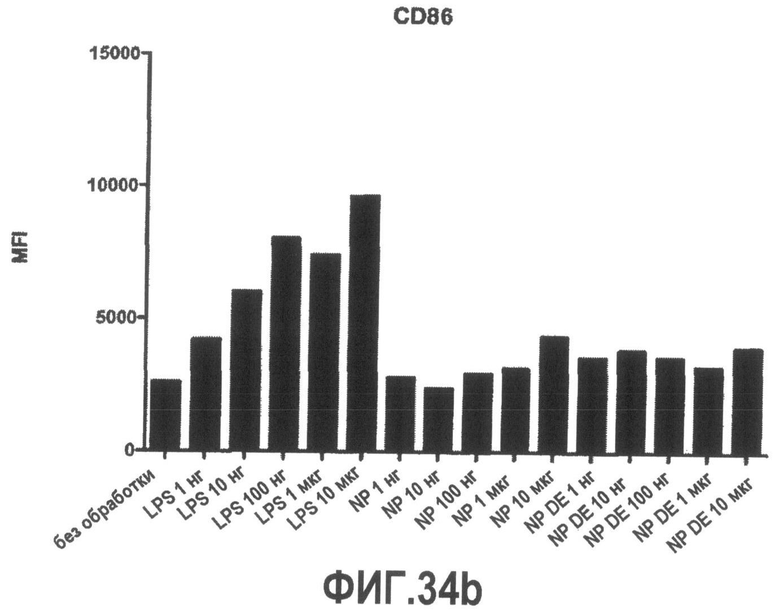

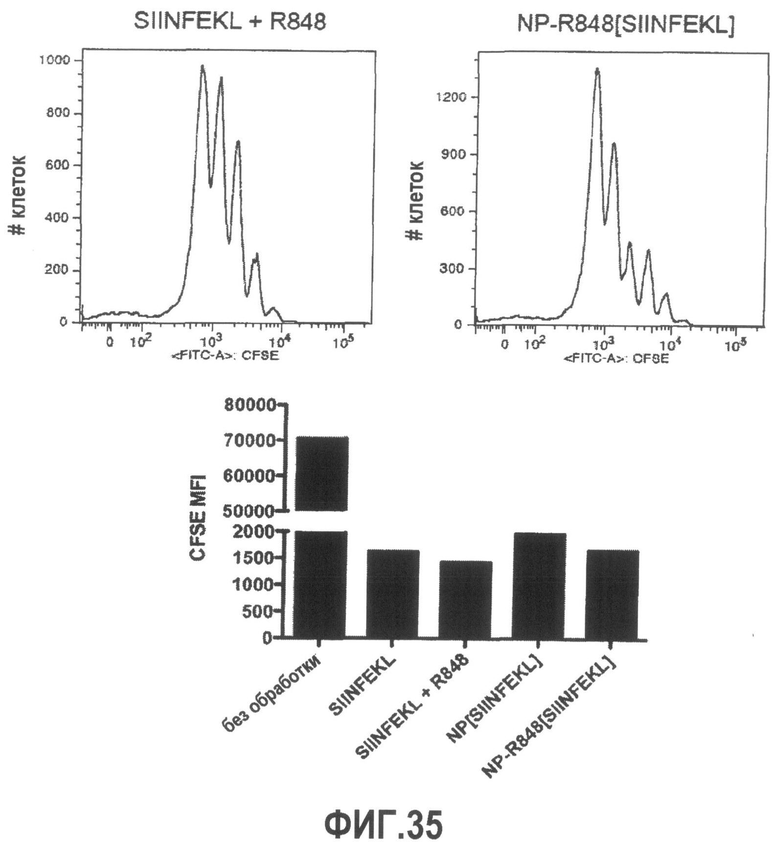





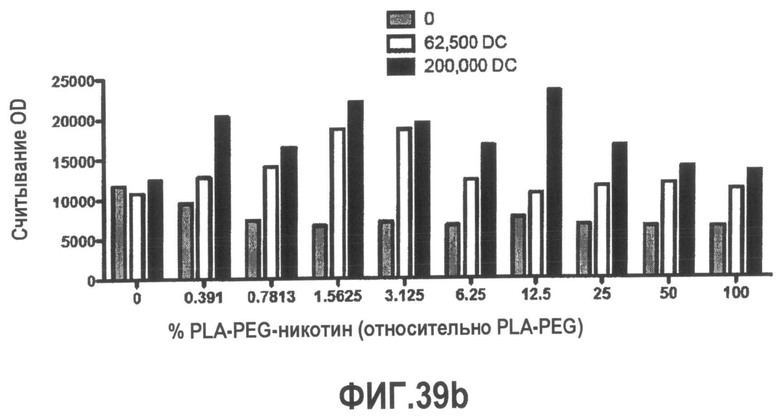

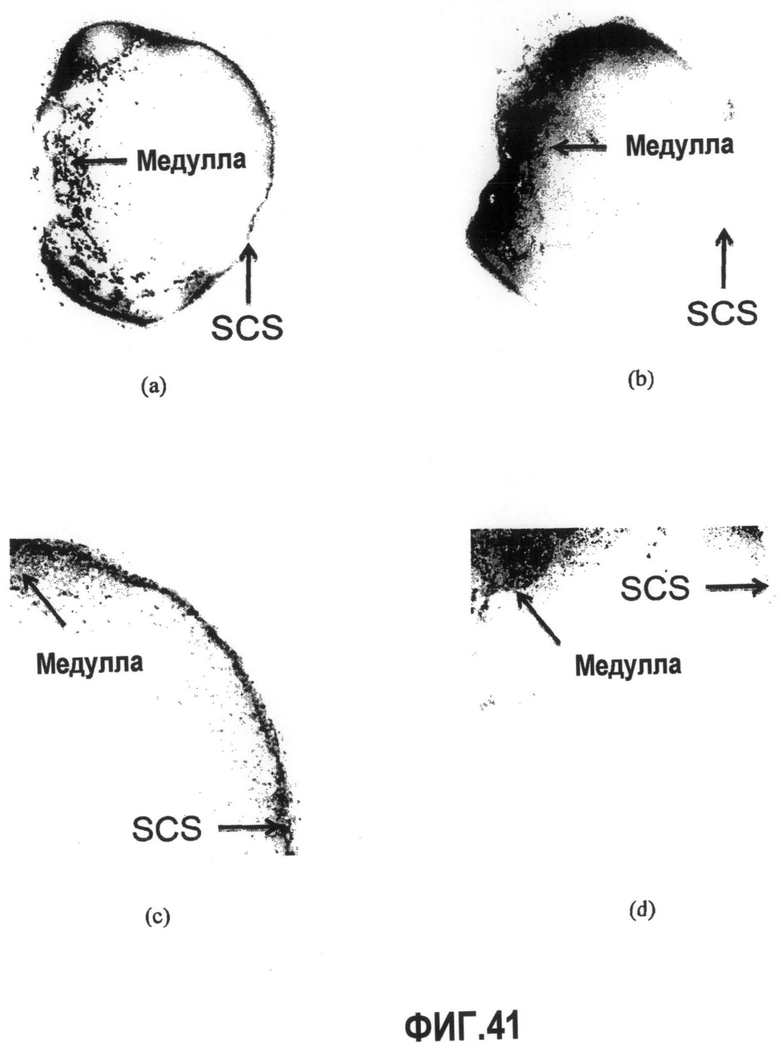
Группа изобретений относится к медицине, а именно к композициям и способам для доставки наноносителей к клеткам иммунной системы, способным стимулировать иммунный ответ в Т-клетках и/или в В-клетках. Композиция содержит полимерные наноносители, содержащие иммунофункциональную поверхность, сформированную из массива связывающих групп, причем массив связывается с дендритными клетками или макрофагами субкапсулярного синуса с высокой авидностью и низкой афинностью по сравнению со связыванием антител, и фармацевтически приемлемый эксципиент. В некоторых вариантах осуществления иммуностимулирующая группа представляет собой адъювант. Изобретение касается также способа введения композиции для пролиферации Т-клеток у пациента. Группа изобретений обеспечивает возможность наноносителям доставлять иммуностимулирующие и иммуномодулирующие средства к В-клеткам и/или Т-клеткам и усиливать иммунный ответ системы. 3 н. и 32 з.п. ф-лы, 20 пр., 40 ил.
1. Композиция для модуляции иммунной системы, содержащая i) полимерные синтетические наноносители, содержащие иммунофункциональную поверхность, сформированную из массива связующих групп, причем массив связывается с дендритными клетками или макрофагами субкапсулярного синуса с высокой авидностью и низкой афинностью по сравнению со связыванием антител, и ii) фармацевтически приемлемый эксципиент.
2. Композиция по п.1, содержащая иммуностимулирующее средство.
3. Композиция по п.1, содержащая полипептид, поддающийся представлению посредством МНС класса I, MHC класса II или CD-I, связанный с иммунофункциональной поверхностью, связанный со второй поверхностью наноносителя или инкапсулированный в наноносителе.
4. Композиция по п.1, где иммунофункциональная поверхность содержит множество групп, которые присутствуют с плотностью, равной или большей, чем плотность, необходимая для получения по меньшей мере 10% от максимальной иммобилизации, наблюдаемой для моноклонального антитела (МАb) в анализе связывания антигенпредставляющих клеток (АРС).
5. Композиция по п.4, содержащая иммуностимулирующее средство, причем половина максимальной плотности связывания для иммуностимулирующего средства по меньшей мере в два раза превышает половину максимальной плотности связывания для МАb, и иммуностимулирующее средство присутствует с плотностью, равной или большей, чем плотность, необходимая для получения по меньшей с мере 20% от максимальной иммобилизации, наблюдаемой для МАb в анализе связывания АРС.
6. Композиция по п.5, где половина максимальной плотности связывания для иммуностимулирующего средства по меньшей мере в четыре раза превышает половину максимальной плотности связывания для МАb.
7. Композиция по п.4, где анализ связывания АРС включает:
(a) получение серий субстратов, обладающих покрытиями из функциональной группы при сериях плотности покрытия поверхности, где функциональная группа является способной связывать рецепторы поверхности дендритных клеток (DC) или макрофагов субкапсулярного синуса;
(b) приведение в контакт серий субстратов и суспензий отдельных клеток DC или макрофагов субкапсулярного синуса в течение предопределенного периода времени;
(c) удаление несвязавшихся АРС с серией субстратов и фиксация связавшихся АРС на сериях субстратов;
(d) количественное определения числа связавшихся АРС на единицу площади поверхности для каждого субстрата в сериях субстратов;
(e) нанесение на график результатов (d) против плотности покрытия функциональной группы;
(f) получение значения для максимальной иммобилизации посредством определения максимального числа связавшихся АРС на единицу площади поверхности для серий субстратов и
(g) получение значения для половины максимальной плотности связывания посредством определения плотности покрытия поверхности, обеспечивающей 50% от максимума.
8. Композиция по п.4, где MAb представляет собой анти-CD1c (BDCA-I) клон AD5-8E7 или антитело крысы к CD169 мыши, клон 3D6.112, изотип IgG2a.
9. Композиция по п.2, где иммуностимулирующее средство представляет собой агонист Toll-подобного рецептора (TLR).
10. Композиция по п.1, где агонист TLR представляет собой агонист TLR-1, TLR-2, TLR-3, TLR-4, TLR-5, TLR-6, TLR-7, TLR-8, TLR-9 или TLR-10.
11. Композиция по п.2, где иммуностимулирующее средство выбрано из интерлейкина, интерферона, цитокина и адъюванта.
12. Композиция по п.1, где композиция является способной обеспечивать усиленную пролиферацию Т-клеток у пациента-человека.
13. Композиция по п.1, где композиция вызывает созревание дендритных клеток при введении пациенту-человеку.
14. Композиция по п.1, где наноносители содержат два или более различных полипептида, поддающихся представлению МНС класса I, МНС класса II или CD-1.
15. Композиция по п.1, где композиция содержит два или более иммуностимулирующих средства.
16. Композиция по п.15, где композиция содержит два или более агониста Toll-подобного рецептора (TLR).
17. Композиция по п.15, где композиция содержит один агонист Toll-подобного рецептора (TLR) и один неагонист TLR.
18. Композиция по п.17, где неагонист TLR представляет собой группу, индуцирующую передачу сигнала через инфламмасому, CD40 или рецептор цитокина.
19. Композиция по п.3, где полипептид, поддающийся представлению посредством МНС класса I, выбран из антигенов, SIINFEKL, GP33, Core 18-27 и MAGE.
20. Композиция по п.3, где полипептид, поддающийся представлению посредством МНС класса II, выбран из антигенов, OVA323-339, GP61, MAGE-A4 280-299, токсоида столбняка, токсоида дифтерии и пептида PADRE.
21. Композиция по п.3, где полипептид, поддающийся представлению CD-1, выбран из липидных антигенов, миколовой кислоты, сульфолипидов, липофосфогликана, диацилглицеринов, гликосфинголипидов, альфа-галактозилцерамида, изоглоботригексозилцерамида и ганглиозида GD3.
22. Композиция по п.1, дополнительно содержащая иммуномодулирующее средство, выбранное из В-клеточных антигенов, Т-клеточных антигенов, белков, пептидов, углеводов, гликопротеинов, гликопептидов, протеогликанов, инактивированных организмов и вирусов, убитых организмов и вирусов, генетически измененных организмов или вирусов, антигенов грибов, простейших, и/или паразитических организмов и экстрактов клеток.
23. Способ улучшения иммунного ответа на группы, формирующие иммунофункциональную поверхность на носителе, включающий:
введение пациенту первой дозы композиции по п.1 и
введение пациенту первой последующей дозы композиции по п.1 в период времени после введения первой дозы.
24. Способ по п.23, где период времени представляет собой интервал от 1 суток до 1 года.
25. Способ по п.23, где первая доза композиции вызывает пролиферацию Т-клеток у пациента.
26. Способ по п.23, где через одну неделю после введения начальной дозы концентрация антигенспецифических Т-клеток в крови пациента по меньшей мере в 10 превышает концентрацию Т-клеток, узнающих неродственный антиген, для которого у пациента не существует иммунологической памяти.
27. Способ по п.26, где неродственный антиген представляет собой бычий сывороточный альбумин.
28. Способ по п.23, где через одну неделю после введения первой последующей дозы концентрация антигенспецифических Т-клеток в крови пациента по меньшей мере в 10 превышает концентрацию Т-клеток, узнающих неродственный антиген, для которого у пациента не существует иммунологической памяти.
29. Способ по п.28, где неродственный антиген представляет собой бычий сывороточный альбумин.
30. Композиция для модуляции иммунной системы, содержащая:
(1) наноноситель, имеющий по меньшей мере одну поверхность, где первая поверхность наноносителя содержит множество групп в количестве, эффективном для обеспечения гуморального ответа на группы;
(2) иммуностимулирующую группу;
(3) полипептид, поддающийся представлению посредством МНС класса I, МНС класса II или CD-1; и
(4) фармацевтически приемлемый эксципиент.
31. Композиция по п.30, где группы присутствуют в количестве, эффективном для обеспечения основанного на авидности связывания для связывания с антигенпредставляющими клетками млекопитающих.
32. Композиция по п.30, где диаметр наноносителей превышает 100 нм.
33. Композиция по п.30, где фармацевтически приемлемый эксципиент выбран из растворителей, диспергентов, разбавителей или других жидких носителей, веществ, способствующих диспергированию или суспендированию, изотонических средств, загустителей или эмульгаторов, консервантов, твердых связующих веществ и лубрикантов.
34. Композиция по п.30, где композиция нацелена на дендритные клетки.
35. Композиция по п.30, где композиция, по существу, не активирует комплемент.
| WO 2007098254 А2, 30.08.2007 | |||
| US 2004022840 A1, 05.02.2004 | |||
| RU 2006142094 А, 20.06.2008 | |||
| WO 2007086911 А2, 20.06.2008. |
Авторы
Даты
2013-10-27—Публикация
2009-10-09—Подача