Изобретение относится к химической отрасли промышленности и касается синтеза полициклических азотсодержащих гетероароматических соединений. Изобретение может найти применение в биомедицинских исследованиях и в фармакологии, в разработке новых красителей для тканей, пластических масс, в органической электронике при разработке фоточувствительных и светоизлучающих устройств и в других областях техники.
Гетероароматические полициклические соединения представляют интерес для науки и техники как перспективные красители [1 - патент Германии DE 10157034 А1, 2003], материалы для формирования зарядово-инжектирующих и зарядово-транспортных слоев в органических светоизлучающих диодах (ОСИДах) [2 - Y. Shirota, H. Kageyama, Chem. Rev. 2007, 107, 953-1010], электролюминесцентные материалы для ОСИДов [3 - J.M. Hancock, А.Р. Gifford, Y. Zhu, Y. Lou, S.A. Jenekhe, Chem. Mater. 2006, 18, 4924-4932] материалы для электрофотографических систем [G. Henkel, L. Feiler, W. Haiizel, патент Германии DE 3001936 C2] и фоточувствительные материалы для органических фото детекторов и солнечных батарей [4 - П.А. Трошин, Д.К. Сусарова, Р.Н. Любовская, В.Ф. Разумов «Органические фотодетекторы: краткий обзор», глава 10 в монографии "Наноструктурированные материалы для запасания и преобразования энергии" Иваново: Ивановский государственный университет, 2009. - 451 с.]. Большой интерес представляет использование разнообразных полициклических молекул в разработке новых лекарственных препаратов [5 - L.M. Wilhelmsson, N. Kingi, J. Bergman, J. Med. Chem. 2008, 51, 7744-7750]. Приведенные примеры однозначно показывают практическую ценность гетероароматических полициклических соединений.
Задачей данного изобретения является получение новой группы полициклических конденсированных азотсодержащих соединений, имеющих ценные электронные свойства. Задача решается разработкой тетрацианозамещенных 1,4,9b-триазафеналенов общей формулы 1, а именно:
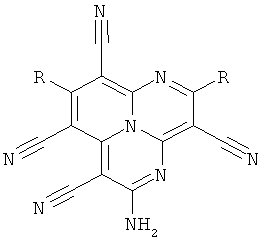
где в общей формуле 1 заместитель R означает:
- фенильный радикал состава C6H4X, X является заместителем в бензольном ядре и представляет собой нитрогруппу (NO2), атом галогена (F, Cl, Br, I), углеводородный радикал С1-С4 или фрагмент простого эфира -OR1 (R1 - углеводородный радикал С1);
- нафтильный радикал состава C10H7;
- пятичленный ароматический гетероциклический радикал состава C4H3S, где S -- атом серы.
Заявляемые тетрацианозамещенные 1,4,9b-триазафеналены, описывающиеся общей формулой (1), являются новой, ранее неизвестной группой органических соединений. Предполагается, что эти соединения найдут применение в фармакологических исследованиях для разработки лекарственных препаратов различного спектра действия. В то же время перспективным может быть использование полученных соединений в органической электронике в качестве полупроводниковых материалов.
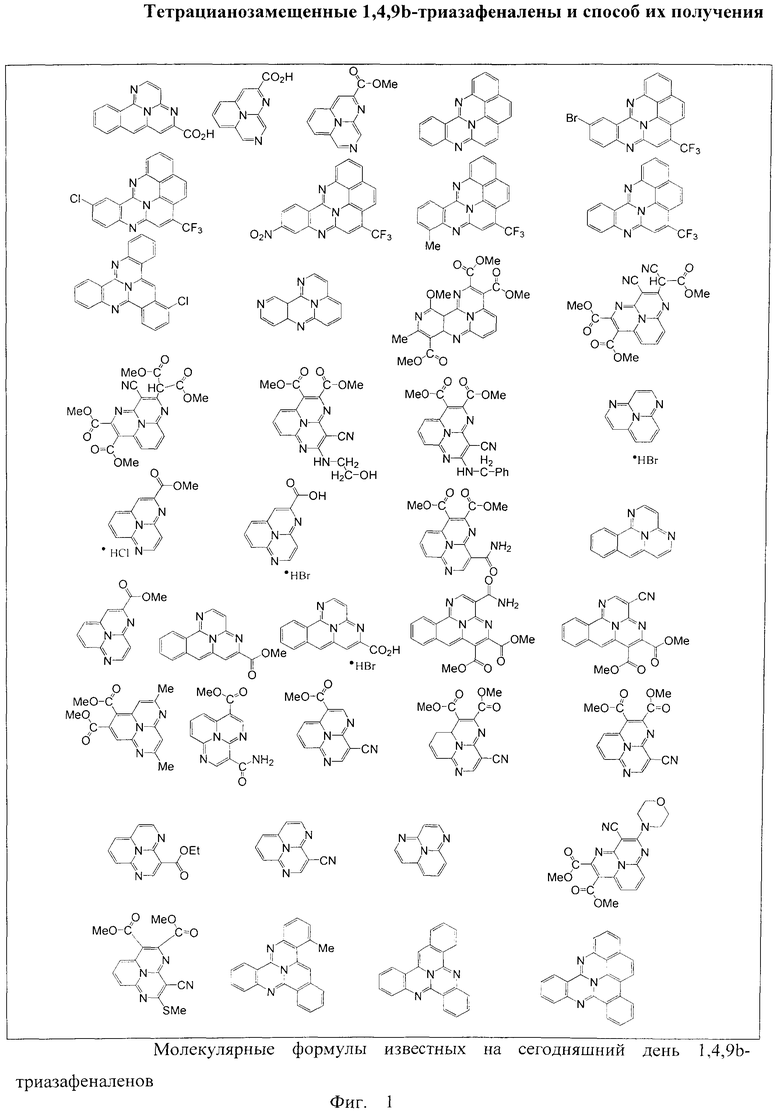
Прототипами заявляемых тетрацианозамещенных 1,4,9b-триазафеналенов является группа 1,4,9b-триазафеналенов, не содержащих заместителей CN, как, например, соединение формулы 2 [6 - Y. Matsuda, Y. Tominaga, H. Awaya, K. Kurata, K. Kato, H. Gotou, Yakugaku Zasshi 1987, 107(5), 344], а также 1,4,9b-триазафеналены, содержащие одну цианогруппу, например, формулы 3 [6, 7 - Y. Matsuda, H. Gotou, K. Katou, H. Matsumoto, Chemical & Pharmaceutical Bulletin, 1989, 37(5), 1188]. Молекулярные формулы всех известных на сегодняшний день соединений с 1,4,9b-триазафеналеновым фрагментом представлены на Фиг.1.
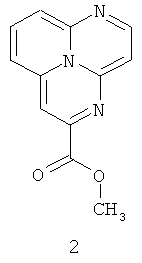
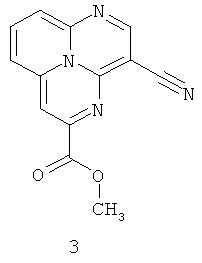
Заявляемые тетрацианозамещенные 1,4,9b-триазафеналены общей формулы 1 имеют ряд принципиальных отличий от известного прототипа:
1) в соединениях общей формулы 1 имеются четыре заместителя CN, которых нет в молекулах известных в литературе аналогов;
2) в соединениях общей формулы 1 имеется первичная аминогруппа, которой нет в структурах известных в литературе аналогов;
Таким образом, тетрацианозамещенные 1,4,9b-триазафеналены общей формулы 1 являются новой группой соединений, которые могут найти практическое использование в различных областях науки и техники ввиду своего большого сродства к электрону, индуцированного присутствием четырех цианогрупп, и необычных оптических свойств, проявляемых этими соединениями (см. ниже).
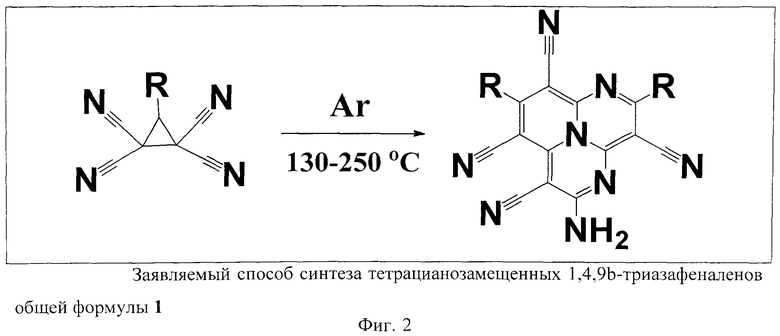
Задачи данного изобретения также решаются разработкой способа получения тетрацианозамещенных 1,4,9b-триазафеналенов общей формулы 1. Он основан на термической конденсации тетрацианоциклопропанов при кипячении в 1,2-дихлорбензоле или другом органическом растворителе с температурой кипения от 130 до 250°С (Фиг.2). Исходные тетрацианоциклопропаны можно легко получить из соответствующих карбонильных соединений и малононитрила в присутствии молекулярного брома, йода или N-бромосукцинимида в качестве окислителя [8 - M.N. Elinson, A.N. Vereshchagin, N.О. Stepanov, A.I. Ilovaisky, A. Ya. Vorontsov, G.I. Nikishin, Tetrahedron 2009, 65, 6057].
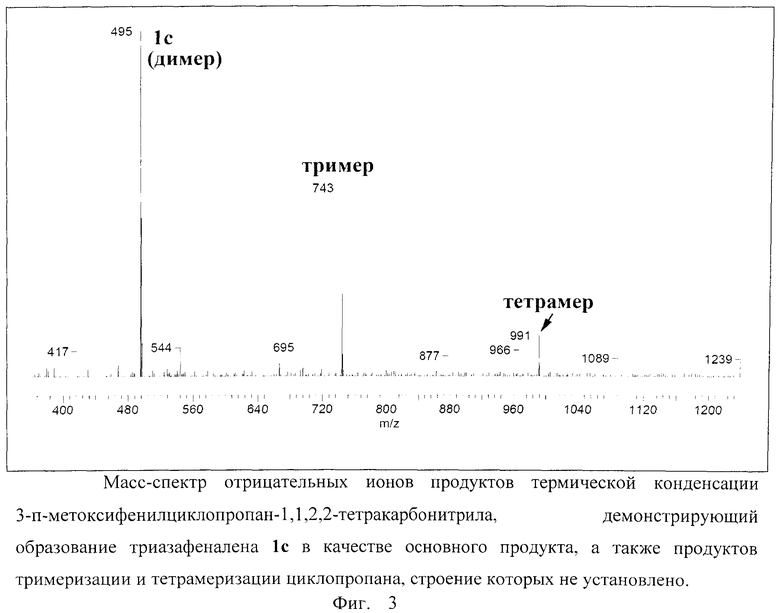
Конденсация тетрацианоциклопропанов с образованием 1,4,9b-триазафеналенов общей формулы 1 протекает наиболее гладко в тех случаях, когда заместитель R является ароматическим фрагментом. Выходы целевых продуктов достигают 50-60% при времени реакции около 20-30 часов. Заметим, что 1,4,9b-триазафеналены 1 формально являются димерами тетрацианоциклопропанов. Помимо них в реакции образуются также продукты тримеризации и тетрамеризации циклопропанов, идентифицированные с использованием масс-спектрометрии (Фиг.3). Молекулярное строение тримеров и тетрамеров остается неустановленным.
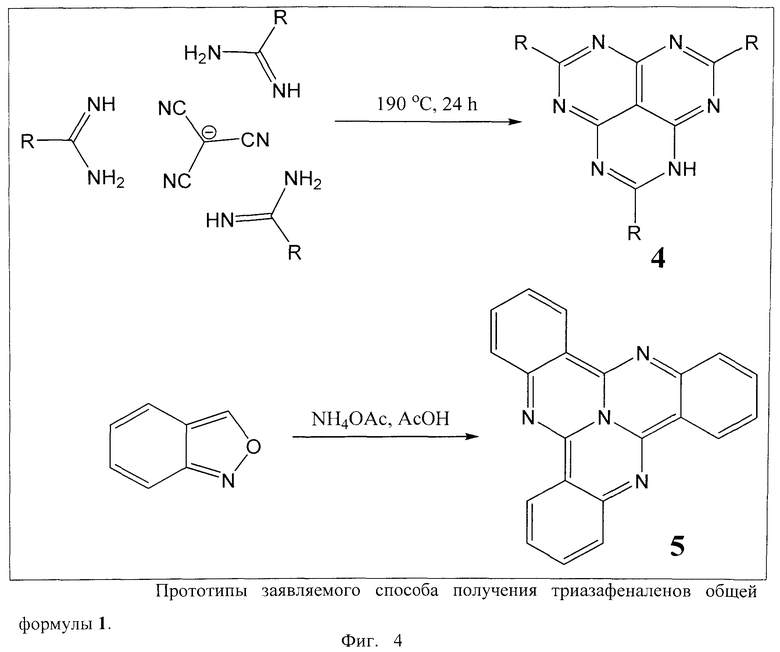
Отдаленным аналогом заявляемого способа получения 1,4,9b-триазафеналенов общей формулы 1 является реакция конденсации амидин гидрохлоридов и трицианометильного аниона, приводящая к образованию гексаазафеналенов общей формулы 4 (Фиг.4) [9 - S. Suzuki, K. Fukui, A. Fuyuhiro, K. Sato, T. Takui, K. Nakasuji, Y. Morita, Org. Lett. 2010, 12, 5036-5039]. Прототипом заявляемого способа получения 1,4,9b-триазафеналенов общей формулы 1 является реакция тримеризации бензоизоксазолов с образованием тетраазофеналенов (трициклохиназолинов) общей формулы 5 (Фиг.4) [10 - S. Kumar, D.S.S. Rao, S.K. Prasad, J. Mater. Chem., 1999, 9, 2751].
Заявляемый способ получения тетрацианозамещенных 1,4,9b-триазафеналенов общей формулы 1 имеет ряд принципиальных отличий от протипа:
1) в качестве исходных соединений используются тетрацианоциклопропаны, а не бензоизоксазолы, как в описанном в литературе прототипе [10 - S. Kumar, D.S.S. Rao, S.K. Prasad, J. Mater. Chem., 1999, 9, 2751];
2) в качестве продуктов реакции образуются триазафеналены, а не тетраазафеналены, как в описанном прототипе.
Таким образом, заявляемый способ отличается принципиальной новизной и большой практической ценностью учитывая, что он открывает путь к получению новой обширной группы соединений с ценными оптическими свойствами (см. ниже). Важность этого способа состоит также в том, что целевые триазафеналены можно получать в одну стадию из сравнительно доступных исходных реагентов. Описанные в литературе синтезы триазафеналенов представляют собой многостадийные синтезы, в которых используются редкие и дорогостоящие реагенты [6-7].
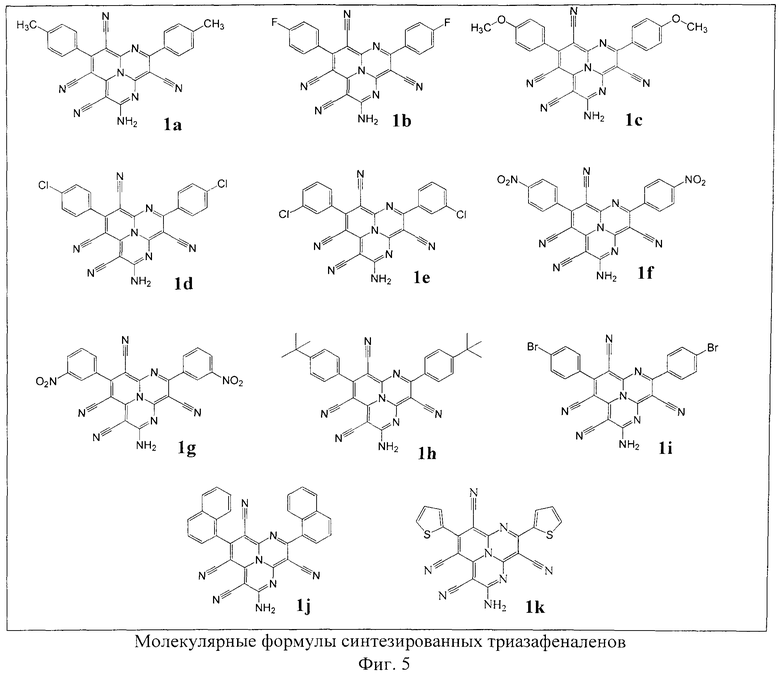
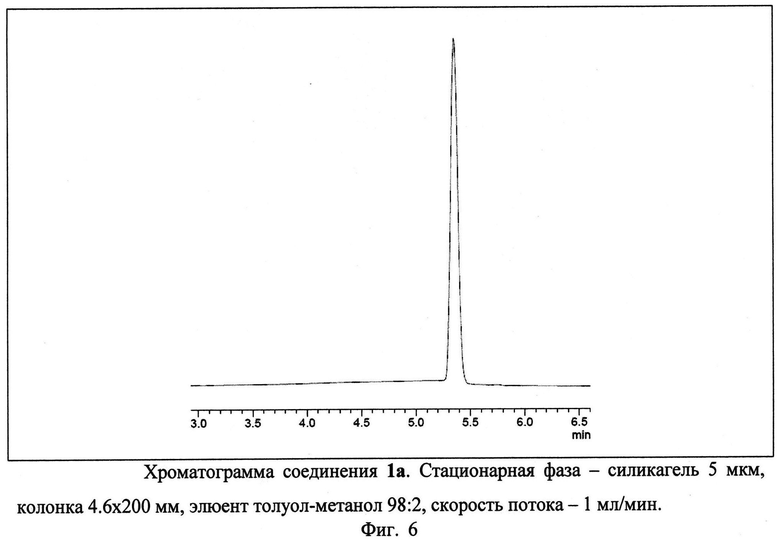
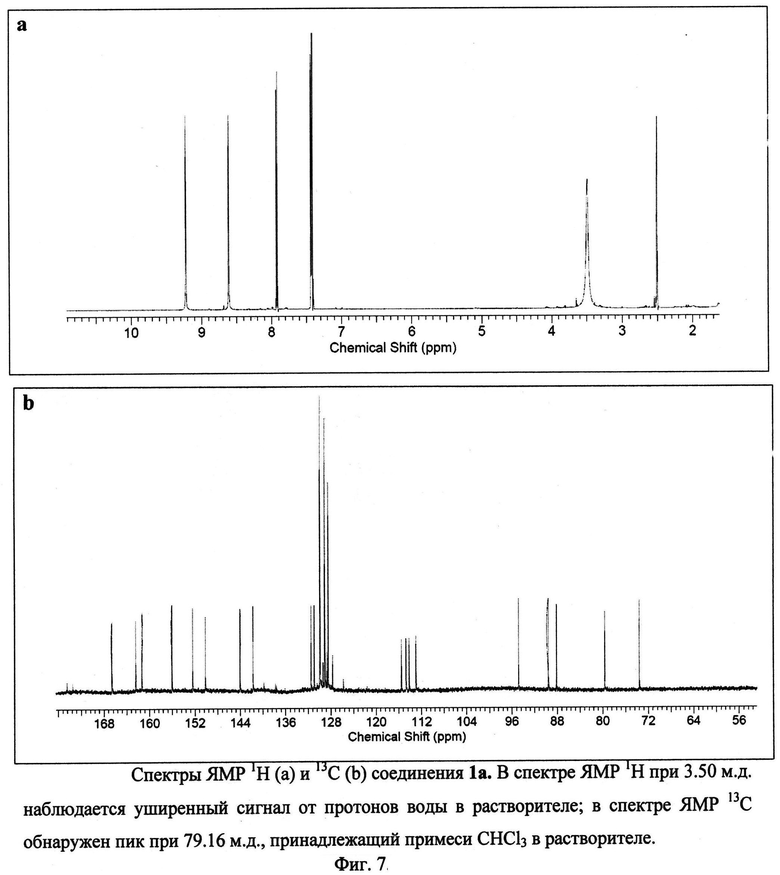
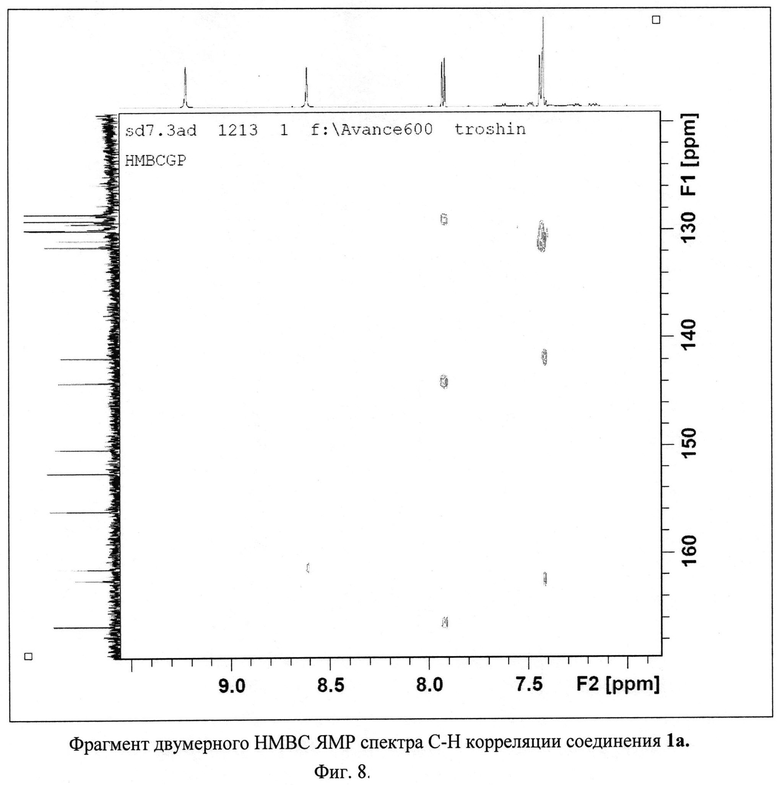
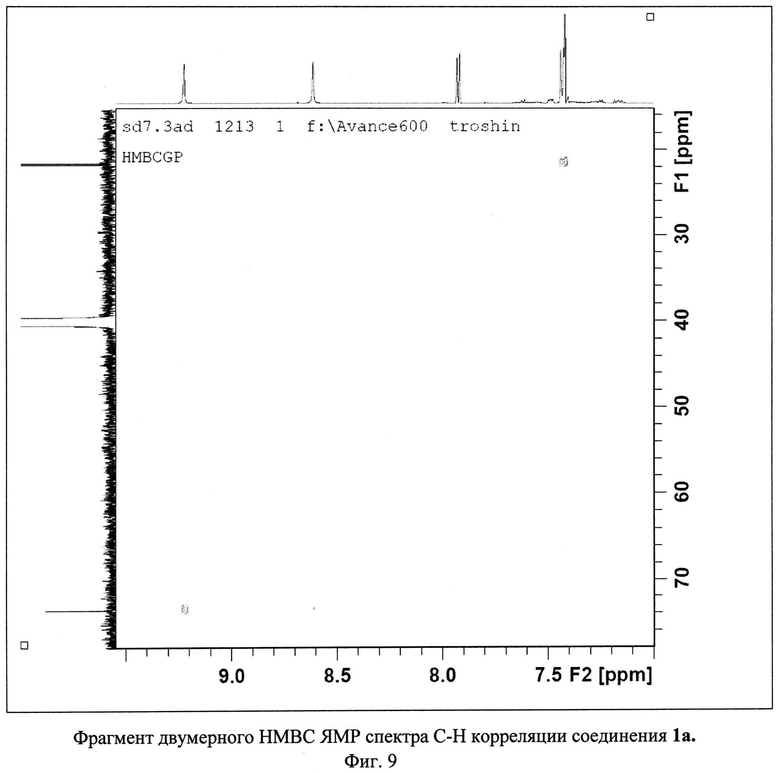
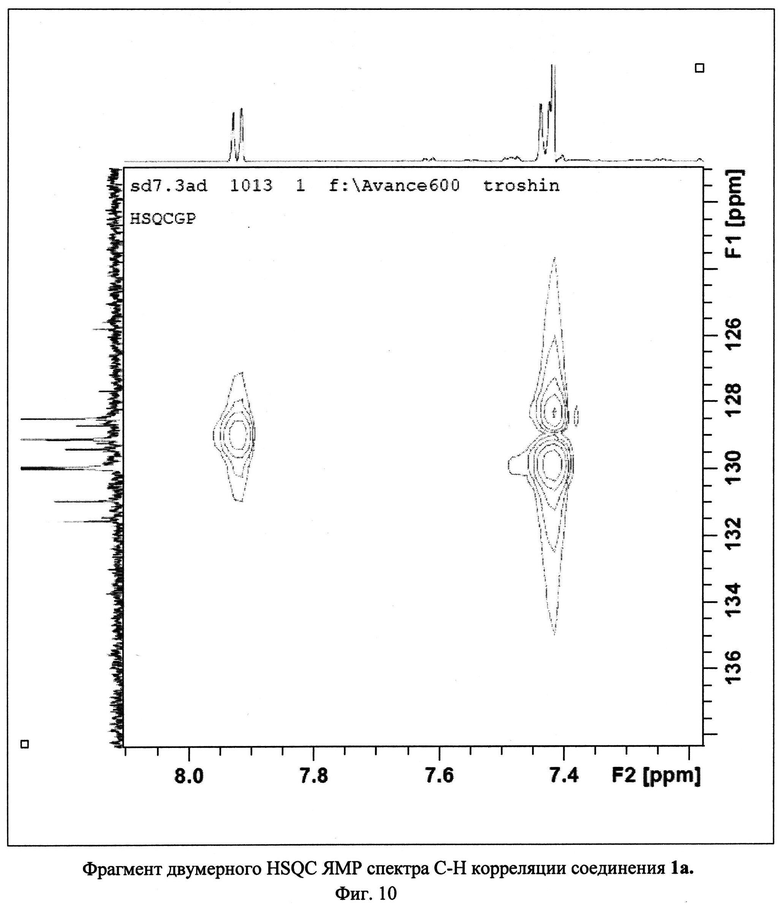
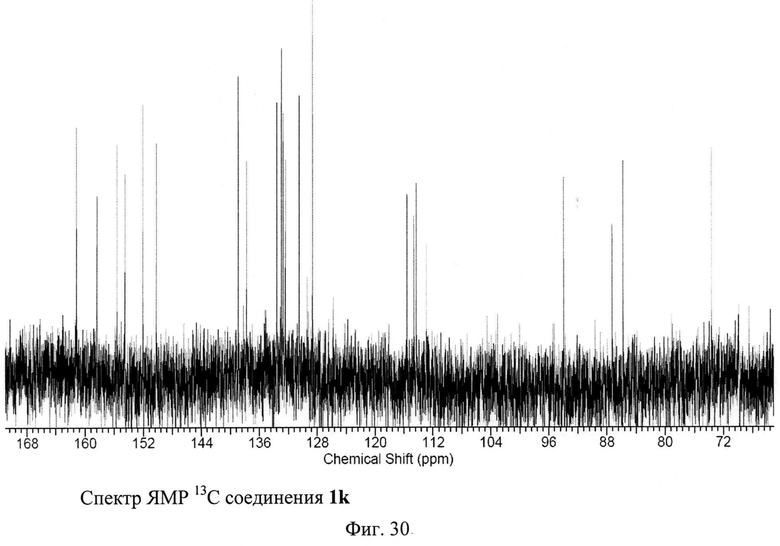
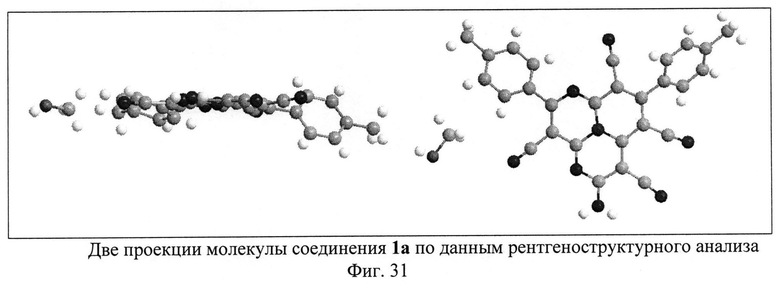
Изобретение иллюстрируется многими примерами синтезированных тетрацианозамещенных 1,4,9b-триазафеналенов, молекулярные формулы которых представлены на Фиг.5. Высокая чистота триазафеналенов подтверждена хроматографическими методами (высокоэффективная жидкостная хроматография, Фиг.6). Состав и строение полученных соединений подтверждено методами ЯМР-спектроскопии на ядрах 1Н и 13С, двумерными спектрами Н-Н и С-Н корреляции и данными электроспрей масс-спектрометрии (Фиг.7-30). Для ключевого соединения 1а были получены монокристаллы, что позволило установить его строение с использованием рентгеноструктурного анализа. Две проекции молекулы 1,4,9b-триазафеналена 1а представлены на Фиг.31.
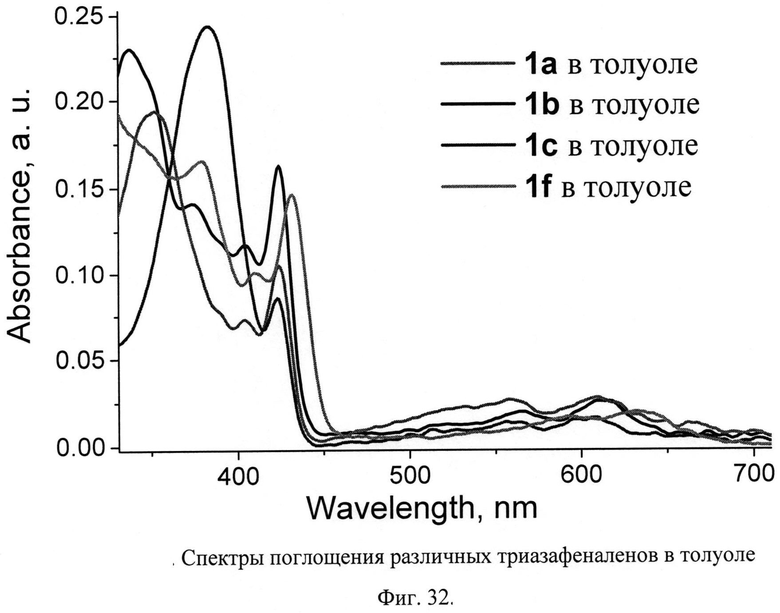
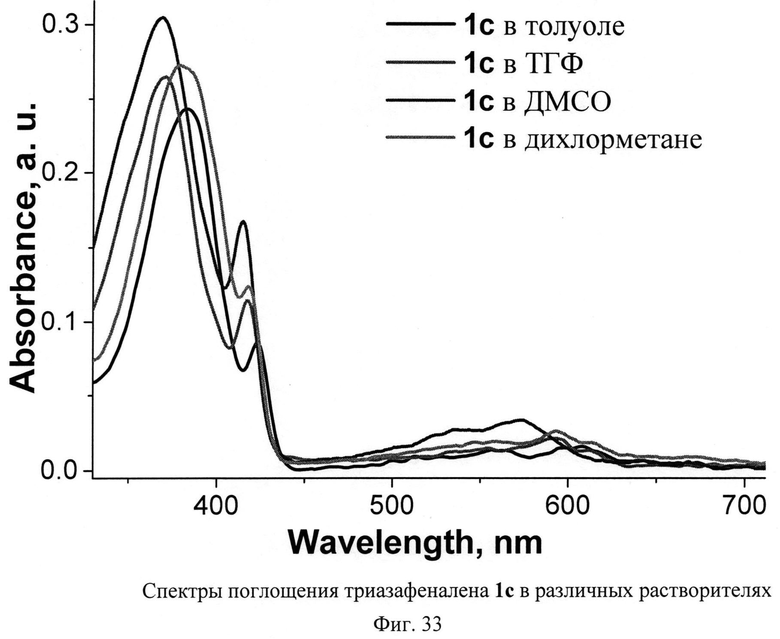
Крайне интересными оказались оптические спектры соединений. В спектрах поглощения всех тетрацианозамещенных триазафеналенов (Фиг.32-33) была обнаружена интенсивная полоса в коротковолновой части спектра, которая меняет свое положение от 330 до 390 нм в зависимости от природы заместителей в триазафеналеновом цикле. Следующая по интенсивности полоса также чувствительна к особенностям строения триазафеналенов и проявляется для разных соединений в диапазоне 420-430 нм. Имеется также четкая полоса поглощения при 400-410 нм. Наиболее интересной особенностью спектров поглощения триазафеналенов является наличие очень широкой полосы при 450-700 нм. Эта полоса закрывает собой весь видимый диапазон, что придает триазафеналенам яркую окраску в растворах и в тонких пленках. Заметим, что описанные в литературе тетрааза- и гексаазафеналены являются бесцветными или слабоокрашенными соединениями. Поэтому яркая окраска заявляемых нами тетрацианозамещенных 1,4,9b-триазафеналенов общей формулы 1 является их важнейшей отличительной особенностью. По-видимому, появление широкой полосы в видимой части спектра связано с внутримолекулярным переносом заряда в этих соединениях, индуцированным присутствием четырех электронодефицитных цианогрупп и электронодонорной аминогруппы в молекулах соединений формулы 1.
Обнаружено, что положение полос в спектрах поглощения триазафеналенов сильно меняется в зависимости от растворителя, в котором проводится измерение спектра. Подобное явление сольватохромизма лежит в основе многих практических приложений, в частности в разработке индикаторов для оптохемосенсорных систем, предназначенных для обнаружения примесей тех или иных органических соединений в газах и жидкостях.
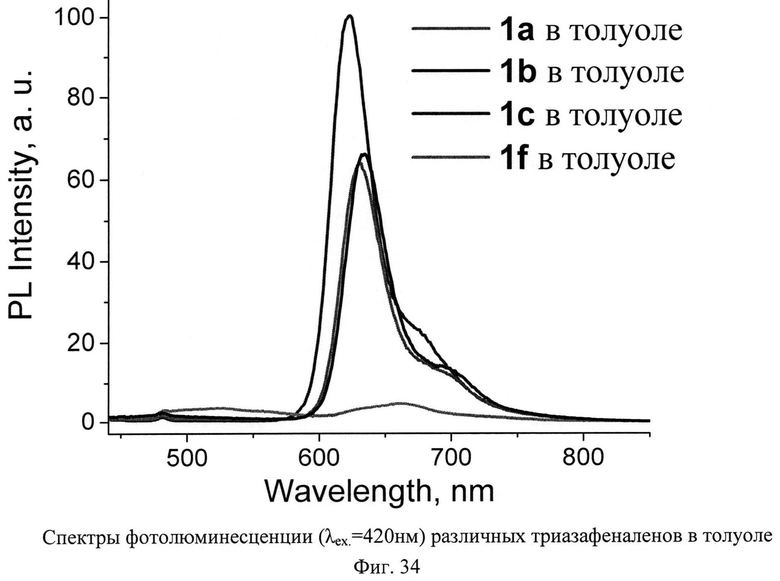
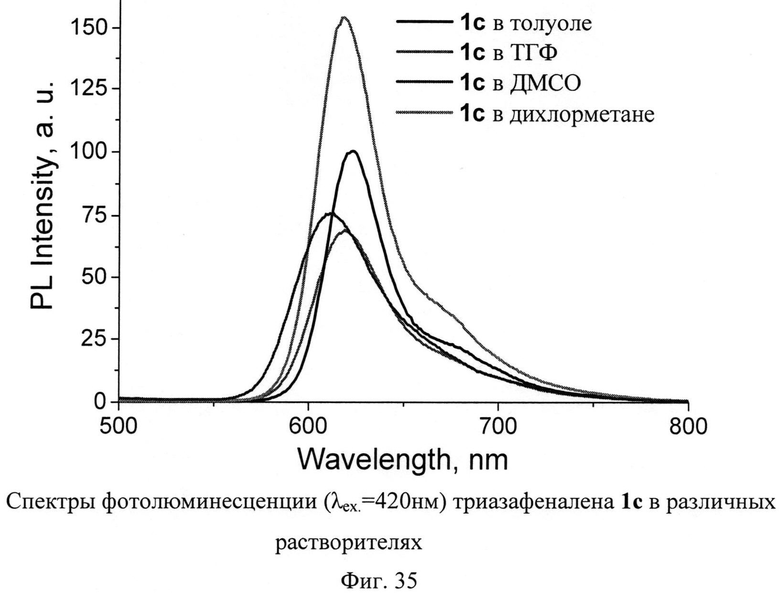
В то же время почти все триазафеналены демонстрируют интенсивную красную фотолюминесценцию. В спектрах фотолюминесценции наблюдается лишь узкие полосы с максимумом 620-635 нм и шириной у основания около 100 нм (Фиг.34-35). Положение максимума также сдвигается на 5-10 нм в зависимости от того, в каком растворителе регистрируется спектр фотолюминесценции. Более того, интенсивность люминесценции также сильно меняется в зависимости от растворителя. Сольватохромизм в спектрах фотолюминесценции является редким явлением, которое интенсивно изучается с целью разработки оптохемосенсоров нового поколения. В таких оптохемосенсорах используются флуоресцентные красители в качестве индикаторов, реагирующих на присутствие тех или иных аналитов. Обнаруженные свойства триазафеналенов указывают на перспективы их испытания и возможно также последующего практического использования в качестве флуоресцентных индикаторов для оптохемосенсоров нового поколения.
Более того, люминесцентные свойства тетрацианозамещенных триазафеналенов позволяют их использовать в качестве материалов для светоизлучающих диодов, о чем свидетельствует пример 11.
Заявляемое изобретение иллюстрируется, но не ограничивается, следующими примерами:
Пример 1. Синтез 4-амино-2,8-ди(4-метилфенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1а.
Исходный 3-п-толилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 2.16 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1а элюировали смесью толуол-метанол в соотношении 99.6:0.4 по объему. Выход продукта 1а составил 57% от теоретического (285 мг).
ЯМР 1Н (600 МГц, ДМСО-D6), δ=2.41 (s, 6H), 7.42 (m, 6H), 7.92 (d, 2H), 8.61 (s, 1Н), 9.23 (s, 1H) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=21.51, 21.69, 73.57, 79.64, 88.14, 89.54, 94.86, 112.97, 114.17, 114.72, 115.55, 127.69, 128.47, 128.65, 129.08, 129.37, 129.9, 129.94, 130.92, 131.49, 141.78, 144.07, 150.21, 152.44, 156.04, 161.35, 162.41, 166.61 м. д.
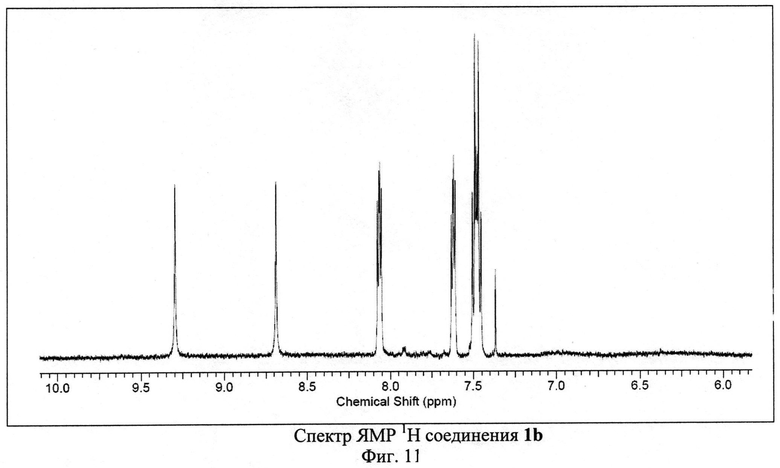
Пример 2. Синтез 4-амино-2,8-ди(4-фторфенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1b.
Исходный 3-п-фторфенилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 2.12 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1b элюировали смесью толуол-метанол в соотношении 99.8:0.2 по объему. Выход продукта 1b составил 23% от теоретического (115 мг).
ЯМР 1Н (600 МГц, ДМСО-D6), δ=7.47 (m, 4H), 7.62 (d, 2H), 8.06 (d, 2H) 8.69 (s, 1Н), 9.30 (s, 1Н) м. д.
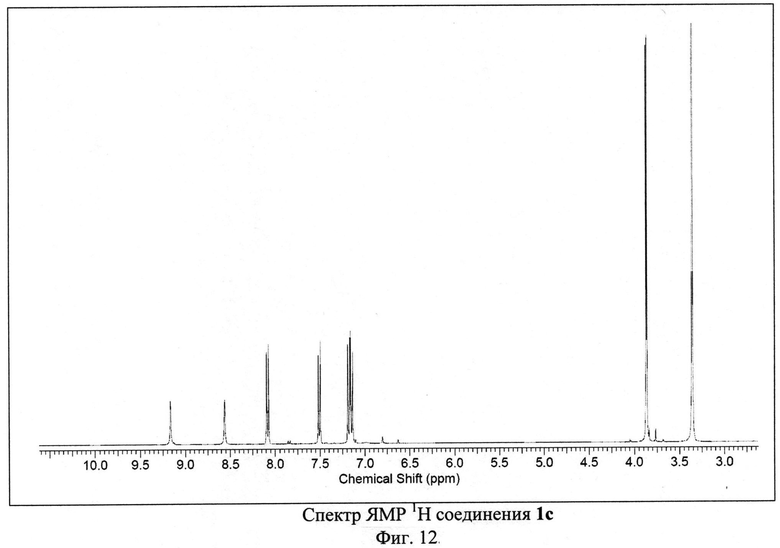
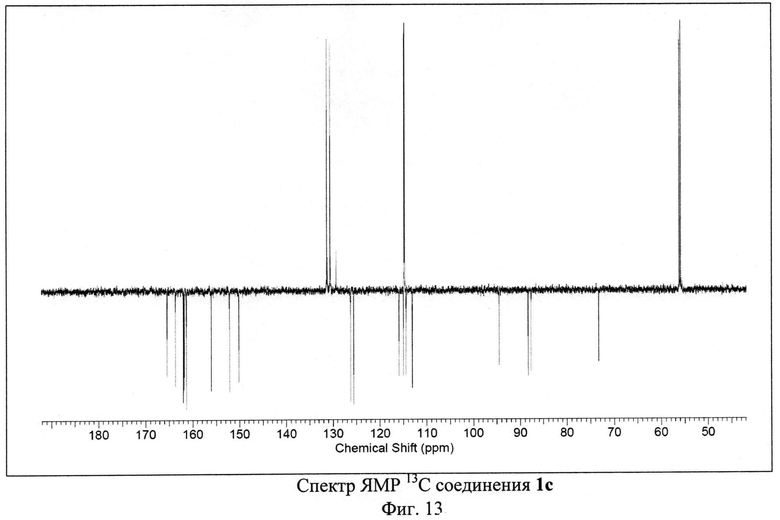
Пример 3. Синтез 4-амино-2,8-ди(4-метоксифенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1с.
Исходный 3-п-метоксифенилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 2.02 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1 с элюировали смесью толуол-метанол в соотношении 99.6:0.4 по объему. Выход продукта 1 с составил 29% от теоретического (145 мг).
ЯМР 1Н (600 МГц, ДМСО-D6), δ=3.87 (s, 6H), 7.16 (m, 4H), 7.51 (d, 2H), 8.10 (d, 2Н), 8.56 (s, 1H), 9.17 (s, 1H) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=55.92, 56.18, 73.33, 87.74, 88.36, 94.55, 113.09, 114.43, 114.74, 114.84, 115, 115.91, 125.62, 126.26, 129.32, 130.62, 131.18, 131.35, 150.19, 152.18, 156.08, 161.37, 161.85, 162.01, 163.7, 165.48 м. д.
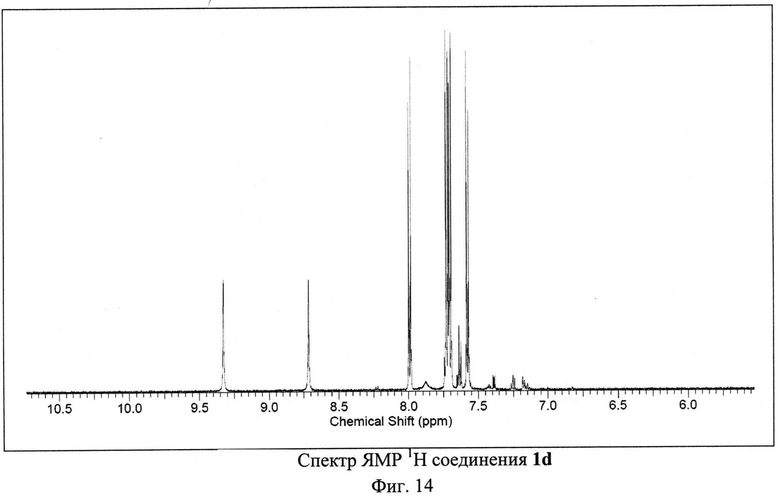
Пример 4. Синтез 4-амино-2,8-ди(4-хлорфенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1d.
Исходный 3-п-хлорфенилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 1.98 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1d элюировали смесью толуол-метанол в соотношении 99.2:0.8 по объему. Выход продукта 1d составил 27% от теоретического (135 мг).
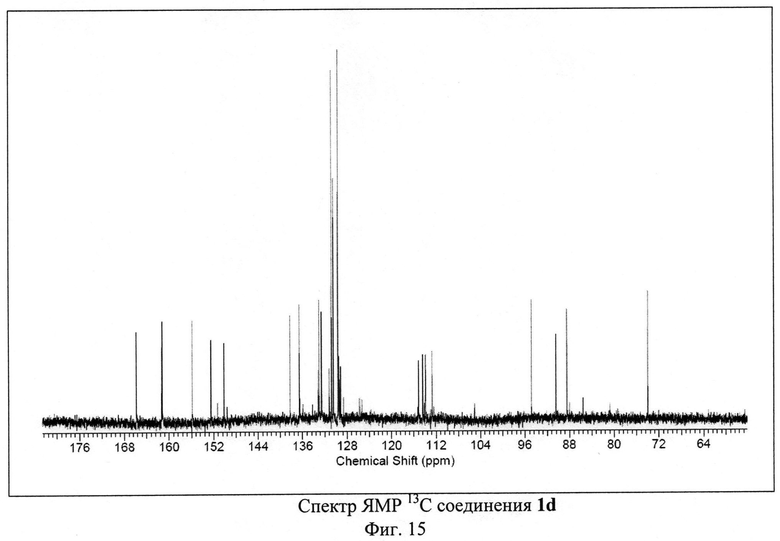
ЯМР 1Н (600 МГц, ДМСО-D6), δ=7.58 (d, 2Н), 7.70 (m, 4Н), 7.981 (d, 2Н), 8.72 (s, 1H), 9.33 (s, 1H) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=74.02, 88.47, 90.45, 94.89, 112.77, 113.92, 114.43, 115.18, 129.18, 129.57, 129.68, 130.48, 130.81, 131.24, 132.61, 133.01, 133.21, 136.57, 138.28, 150.16, 152.53, 155.9, 161.24, 161.36, 165.84 м. д.
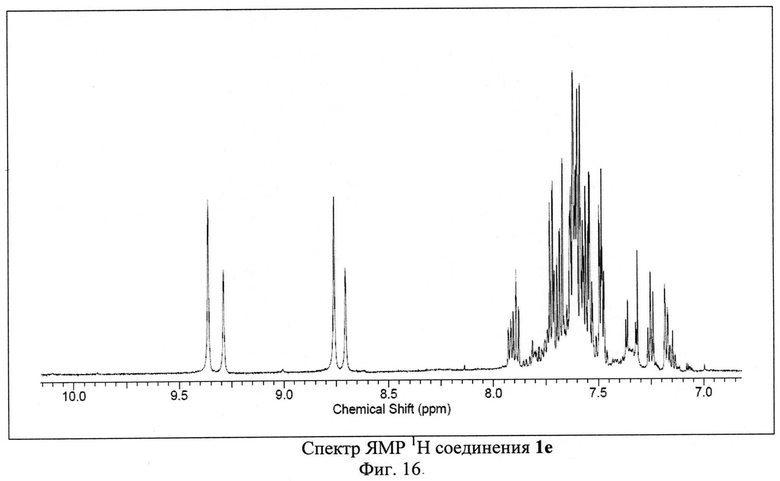
Пример 5. Синтез 4-амино-2,8-ди(3-хлорфенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1е.
Исходный 3-м-хлорфенилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 1.98 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1е элюировали смесью толуол-метанол в соотношении 98.8:1.2 по объему. Выход продукта 1е составил 19% от теоретического (95 мг).
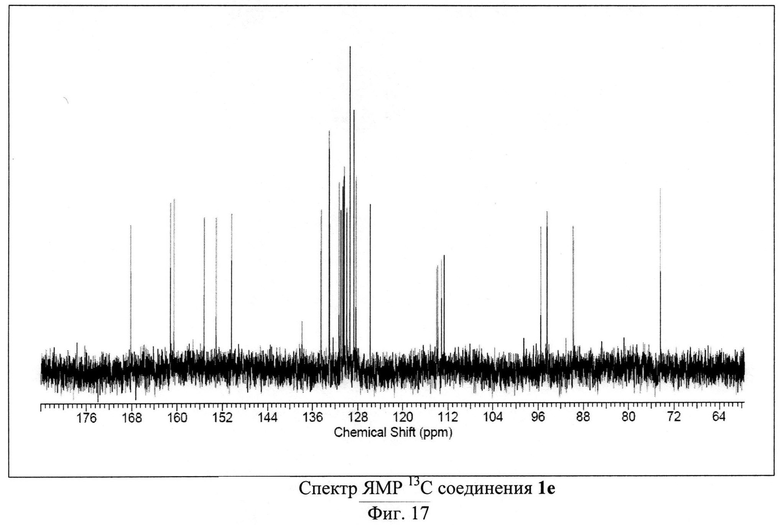
ЯМР 1Н (600 МГц, ДМСО-D6), δ=7.7-8.0 (m, 8Н), 8.75 (m, 1H), 9.33 (m, 1Н) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=73.95, 89.27,93.92,95.03, 112.18, 112.67, 113.31, 113.52, 127.79, 128.2, 129.44, 129.88, 130.07, 130.11, 130.46, 130.77, 132.46, 132.53, 133.96, 149.87, 152.57, 154.75, 160.07, 160.7, 167.66 м. д.
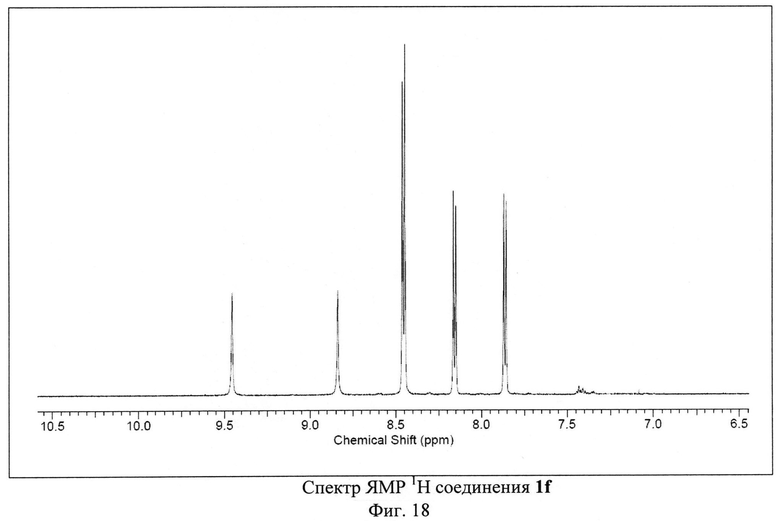
Пример 6. Синтез 4-амино-2,8-ди(4-нитрофенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1f.
Исходный 3-п-нитрофенилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 1.90 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1f элюировали смесью толуол-метанол в соотношении 99.2:0.8 по объему. Выход продукта 1f составил 21% от теоретического (105 мг).
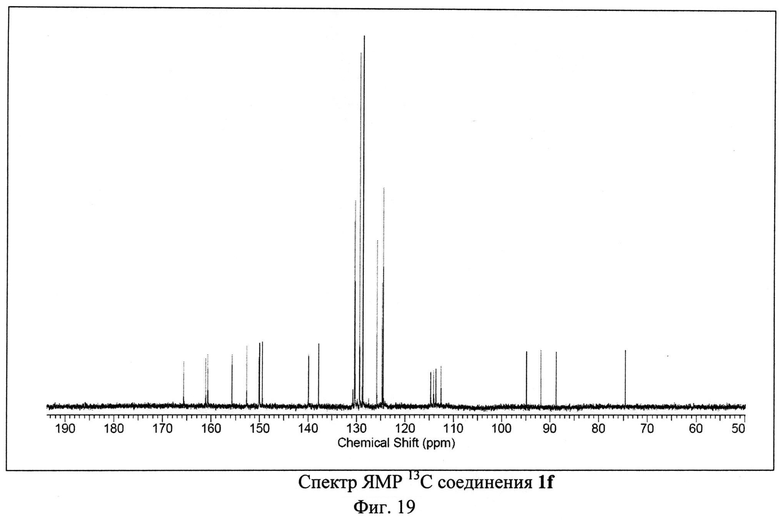
ЯМР 1Н (600 МГц, ДМСО-D6), δ=7.86 (d, 2H), 8.15 (d, 2H), 8.45 (m, 4H) 8.84 (s, 1H), 9.46 (s, 1H) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=74.55, 88.76, 91.92, 94.89, 112.56, 113.63, 114.08, 114.69, 124.52, 124.72, 125.78, 128.67, 129.37, 130.29, 130.41, 137.81, 139.87, 139.92, 149.47, 150.06, 150.17, 152.74, 155.72, 160.75, 161.17, 165.67 м. д.
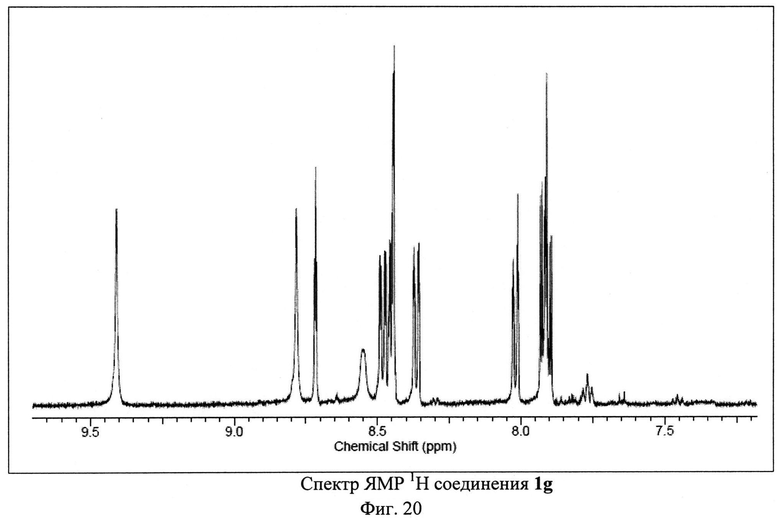
Пример 7. Синтез 4-амино-2,8-ди(3-нитрофенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1g.
Исходный 3-м-нитрофенилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 1.90 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1g элюировали смесью толуол-метанол в соотношении 98.6:1.4 по объему. Выход продукта 1g составил 27% от теоретического (135 мг).
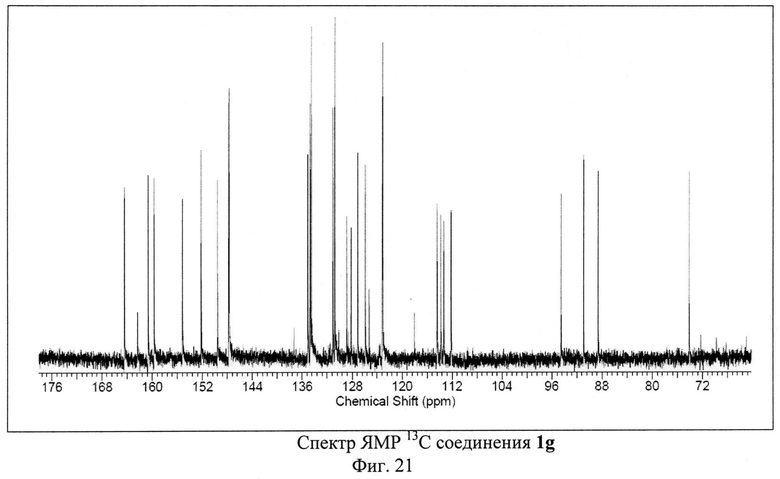
ЯМР 1Н (600 МГц, ДМСО-D6), δ=7.91 (m, 2Н), 8.02 (m, 1Н), 8.36 (m, 1Н), 8.45 (m, 2Н), 8.48 (m, 1H), 8.72 (t, 1H), 8.78 (s, 1H), 9.41 (s, 1H) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=74.14, 88.63, 90.95, 94.56, 112.17, 113.35, 113.81, 114.41, 123.1, 123.16, 125.91, 127.1, 130.76, 131.07, 134.51, 134.69, 134.73, 135.1, 147.72, 147.8, 149.57, 152.21, 155.19, 159.72, 160.63, 164.42 м. д.
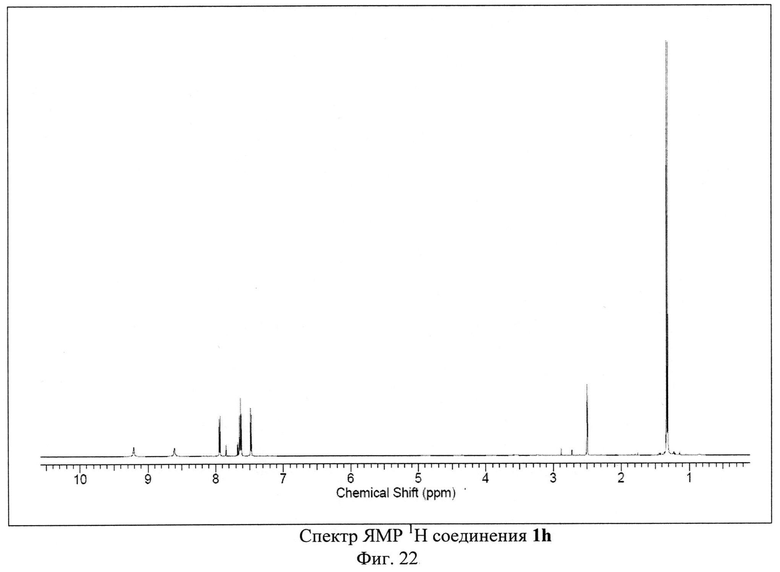
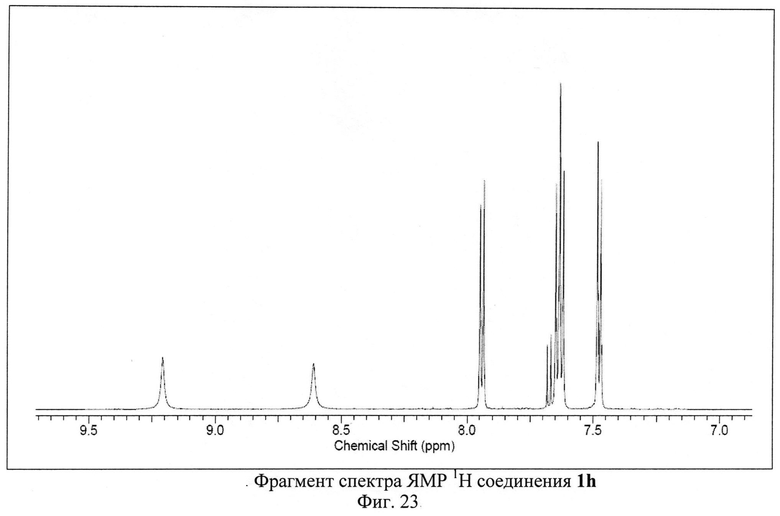
Пример 9. Синтез 4-амино-2,8-ди(4-трет-бутилфенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1h.
Исходный 3-п-трет-бутилфенилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 1.82 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1h элюировали смесью толуол-метанол в соотношении 99.2:0.8 по объему. Выход продукта 1h составил 28% от теоретического (140 мг).
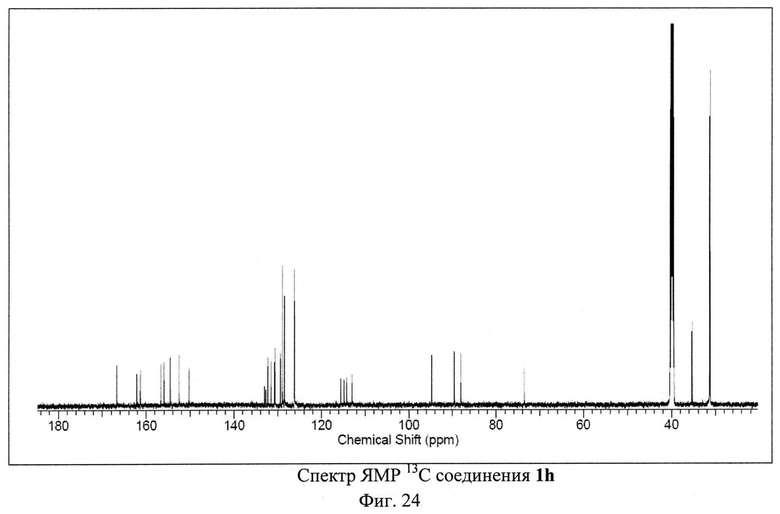
ЯМР 1Н (600 МГц, ДМСО-D6), δ=1.32 (s, 9H), 1.33 (s, 9H), 7.48 (m, 2H), 7.63 (m, 4Н), 7.93 (d, 2H), 8.61 (s, 1H), 9.21 (s, 1H) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=31.23, 31.38, 35.26, 35.43, 73.6, 88.08, 89.64, 94.76, 112.99, 114.22, 114.79, 115.57, 126.17, 126.23, 128.49, 128.96, 129.38, 130.63, 130.8, 131.57, 132.26, 133.05, 150.31, 152.54, 154.56, 156, 156.67, 161.38, 162.18, 166.71, 164.42 м. д.
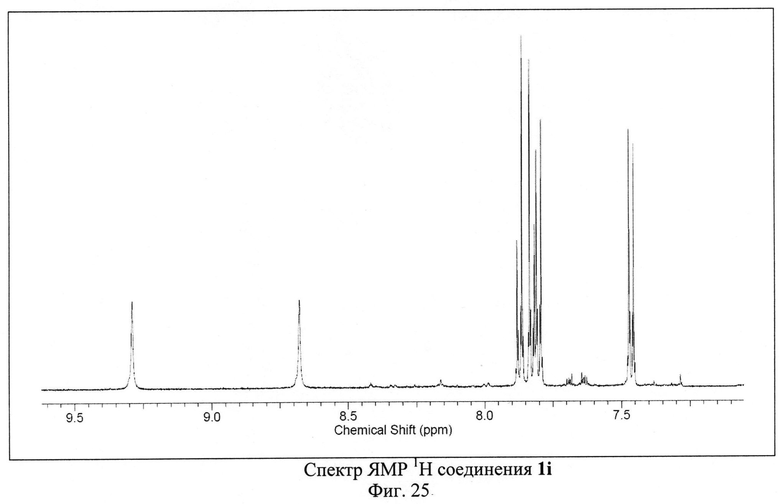
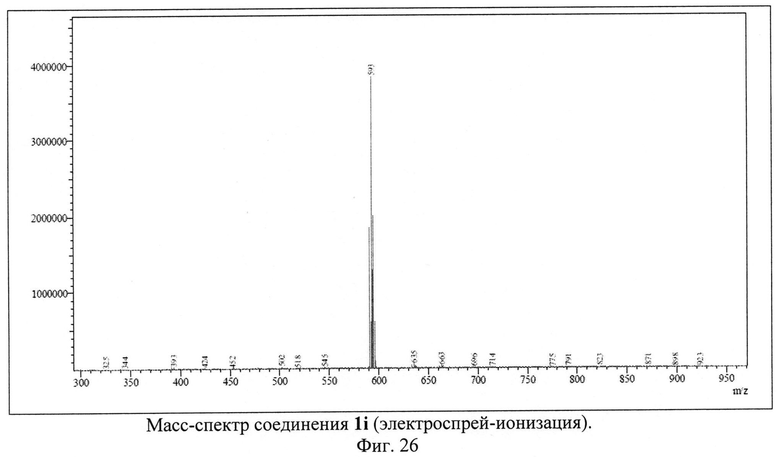
Пример 9. Синтез 4-амино-2,8-ди(4-бромофенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1i.
Исходный 3-п-бромфенилциклопропан-1,1,2,2-тетракарбонитрил (500 мг, 1.68 ммоль) растворили в 50 мл 1,2-дихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 30-40 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1i элюировали смесью толуол-метанол в соотношении 99.2:0.8 по объему. Выход продукта 1i составил 57% от теоретического (285 мг).
ЯМР 1Н (600 МГц, ДМСО-D6), δ=7.46 (m, 2Н), 7.84 (m, 6Н), 8.68 (s, 1H), 9.29 (s, 1Н) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=74.07, 88.49, 90.45, 94.93, 112.6, 113.72, 114.18, 114.98, 123.6, 124.16, 125.23, 127.18, 130.16, 130.53, 132.53, 133.44, 135.32, 150.19, 152.6, 155.96, 161.37, 161.41, 166.02 м.д.
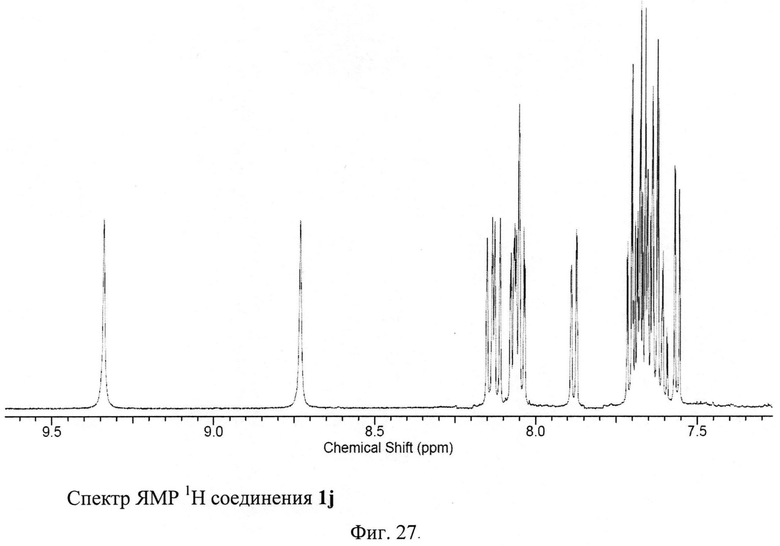
Пример 10. Синтез 4-амино-2,8-ди(2-нафтил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена lj.
Исходный 3-(2-нафтил)циклопропан-1,1,2,2-тетракарбонитрил (500 мг, 1.86 ммоль) растворили в 50 мл 1,2,4-трихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 8 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1j элюировали смесью толуол-метанол в соотношении 99.4:0.6 по объему. Выход продукта 1j составил 37% от теоретического (185 мг).
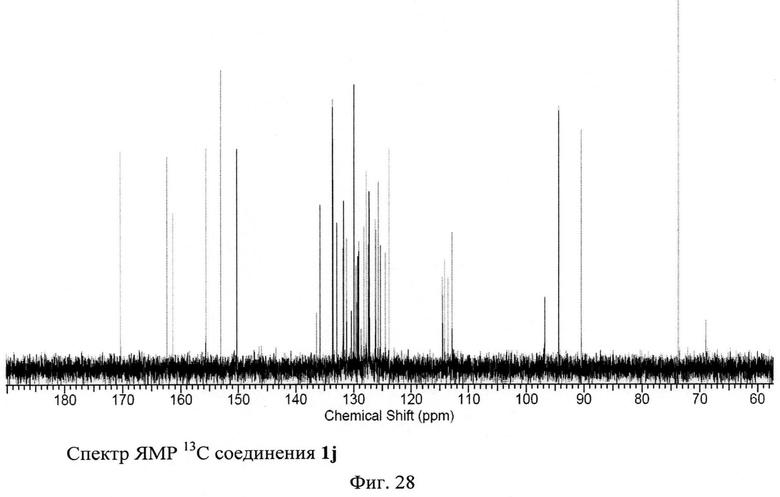
ЯМР 1Н (600 МГц, ДМСО-D6), δ=7.55-7.72 (m, 8H), 7.87 (d, 1H), 8.05 (m, 3H), 8.13 (m, 2Н), 8.73 (s, 1H), 9.34 (s, 1H) м. д. ЯМР 13С (125 МГц, ДМСО-D6) δ=73.73, 90.46, 94.37, 96.79, 112.89, 113.58, 114.21, 114.56, 123.82, 124.48, 125.7, 126.11, 126.25, 127.25, 127.31, 127.44, 127.8, 129.28, 129.6, 129.9, 131.23, 131.72, 131.86, 132.88, 133.54, 133.62, 135.81, 150.27, 153.02, 155.65, 161.35, 162.39, 170.38 м.д.
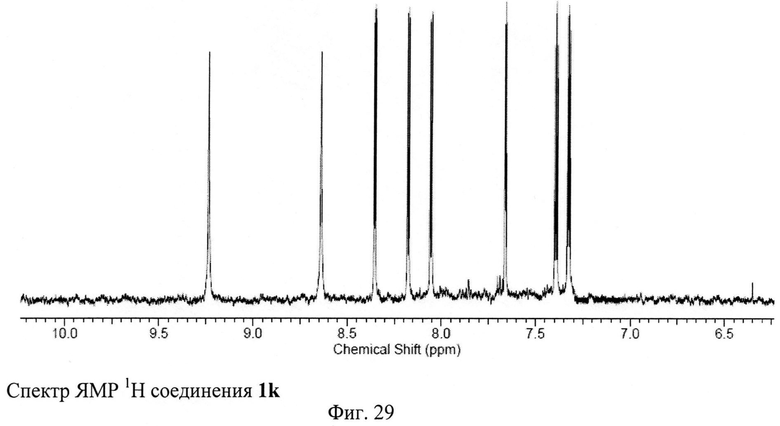
Пример 11. Синтез 4-амино-2,8-ди(2-тиенил)-3,6,7,9-тетрациано-1,4,9b-триазафеналена 1j.
Исходный 3-(2-тиенил)циклопропан-1,1,2,2-тетракарбонитрил (500 мг, 2.23 ммоль) растворили в 50 мл 1,2,4-трихлорбензола. Полученный раствор кипятили с обратным холодильником в атмосфере аргона в течение 8 часов. Цвет реакционной смеси изменялся от бесцветного к ярко-красному и затем к темно-коричневому. После окончания синтеза реакционную смесь охлаждали и фильтровали через бумажный фильтр. Фильтрат концентрировали на роторном испарителе. Полученный остаток растворяли в толуоле и наносили на хроматографическую колонку с силикагелем (Acros Organics, 40-60 µ, 60 Å). Целевой продукт 1k элюировали смесью толуол-метанол в соотношении 99.4:0.6 по объему. Выход продукта 1k составил 14% от теоретического (70 мг).
ЯМР 1Н (600 МГц, ДМСО-D6), δ=7.33 (m, 1H), 7.39 (m, 1H), 7.66 (dd, 1H), 8.06 (dd, 1Н), 8.18 (dd, 1H), 8.36 (dd, 1H), 8.64 (s, 1H), 9.24 (s, 1H) м. д. ЯМР 13С (150 МГц, ДМСО-D6) δ=73.68, 85.81, 87.29, 93.94, 112.94, 114.33, 114.65, 115.61, 128.68, 130.52, 132.43, 132.74, 132.97, 133.61, 137.78, 138.93, 150.22, 152.05, 154.52, 155.65, 158.37, 161.20 м. Д.
Пример 12. Использование соединения 1а в качестве материала для органических светоизлучающих диодов.
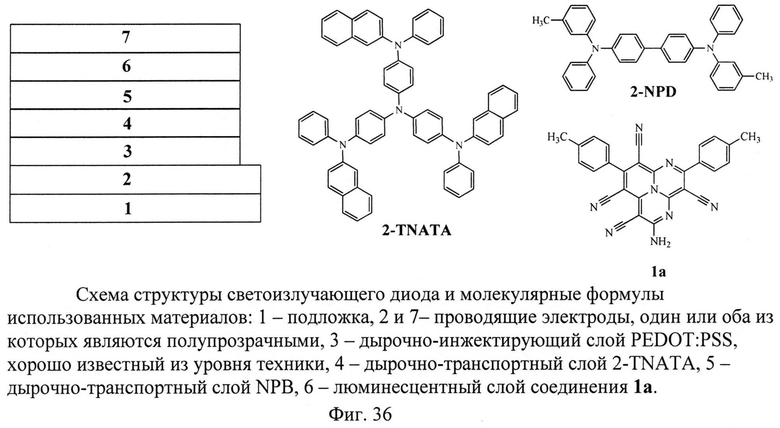
В камере, встроенной внутри аргонового бокса, на подложку с проводящим слоем ITO и дырочно-инжектирующим слоем PEDOT-PSS при давлении 10-6 мБар последовательно напыляли дырочно-транспортные слои 2-TNATA (60 нм) и 2-NPD (15 нм), а также слой электролюминесцентного материала - триазафеналена 1а (15 нм). Поверх органических слоев напыляли металлический кальциевый катод (150 нм) (Фиг.36).
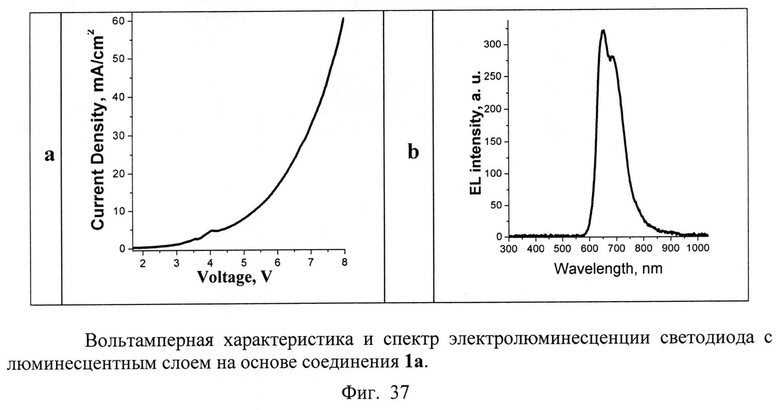
Изготовленный ОСИД начинает излучать красный свет при приложенных напряжениях около 3.5 В, тогда как при напряжении 8.0 В его яркость составляет около 1000 кд/м2 (Фиг.37). Эффективность устройства по току невысока, но может быть улучшена путем оптимизации структуры ОСИДа и молекулярной структуры светоизлучающего материала.
| название | год | авторы | номер документа |
|---|---|---|---|
| Донорно-акцепторные олигомеры с фенилдициановинильными заместителями на основе трифениламина и способ их получения | 2015 |
|
RU2667362C2 |
| Способ получения пирроло[3,4-с]хинолинов | 2022 |
|
RU2802332C1 |
| 4,5-БИС-(1',2':3',4'-ДИ-О-ИЗОПРОПИЛИДЕН-α-D-ГАЛАКТОПИРАНОЗО-6'-ИЛ)ФТАЛОНИТРИЛ | 2009 |
|
RU2409585C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛ 3-АЦИЛ-4-ЦИАНО-5-(ДИЦИАНОМЕТИЛЕН)-2-ГИДРОКСИ-2,5-ДИГИДРО-1H-ПИРРОЛ-2-КАРБОКСИЛАТОВ | 2018 |
|
RU2700928C2 |
| НОВЫЕ N-МОДИФИЦИРОВАННЫЕ 5-МЕТИЛ-2'-ДЕЗОКСИЦИТИДИНЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКОЗНУЮ АКТИВНОСТЬ | 2021 |
|
RU2766333C1 |
| Эффективный способ получения производных гидразинофенола | 2020 |
|
RU2759291C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АМИНО-8-ГИДРОКСИ-1,6-ДИОКСО-2,7-ДИАЗАСПИРО[4.4]НОН-3-ЕН-4-КАРБОНИТРИЛОВ | 2012 |
|
RU2495040C1 |
| Донорно-акцепторные сопряженные молекулы и способ их получения | 2014 |
|
RU2624820C2 |
| 6,7-ДИГИДРО-5H-ПИРИДО[2,3-C]ПИРИДАЗИНОВЫЕ ПРОИЗВОДНЫЕ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ БЕЛКОВ BCLXL И ПРОАПОПТОТИЧЕСКИХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2020 |
|
RU2832191C2 |
| СПОСОБ ПОЛУЧЕНИЯ 6-ИМИНО-2,7-ДИОКСАБИЦИКЛО[3.2.1]ОКТАН-4,4,5-ТРИКАРБОНИТРИЛОВ | 2014 |
|
RU2545459C1 |
Описываются новые полициклические азотсодержащие гетероароматические соединения - тетрацианозамещенные 1,4,9b-триазафеналены общей формулы 1
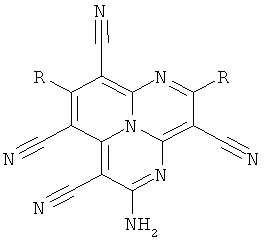
где R означает
- фенил, замещенный NO2, галогеном, С1-4алкилом или группой -OR1, где R1 - метил,
- нафтил или
- гетероарил состава C4H3S, и способ их получения исходя из соответствующих R-замещенных 1,1,2,2-тетрацианоциклопропанов при их кипячении в 1,2-дихлорбензоле. Описываемые соединения могут быть использованы в качестве флуоресцентных индикаторов для оптохемосенсоров нового поколения или в качестве материала для светоизлучающих диодов. 2 н.п. ф-лы, 12 пр., 37 ил.
1. Тетрацианозамещенные 1,4,9b-триазафеналены общей формулы 1, а именно:
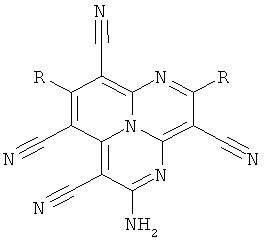
где в общей формуле 1 R означает:
фенильный радикал состава С6Н4Х, где X является заместителем в бензольном ядре и представляет собой нитрогруппу (NO2), атом галогена (F, Cl, Br, I), углеводородный радикал C1-C4 или фрагмент простого эфира -OR1 (R1-углеводородный радикал С1);
нафтильный радикал состава С10Н7;
пятичленный ароматический гетероциклический радикал состава C4H3S, где S - атом серы.
2. Способ получения тетрацианозамещенных 1,4,9b-триазафеналенов общей формулы 1 из 1,1,2,2-тетрацианоциклопропанов при их кипячении в 1,2-дихлорбензоле.
| ПРОИЗВОДНЫЕ 1, 3, 4-ТРИАЗАФЕНАЛЕНА И 1, 3, 4, 6-ТЕТРААЗАФЕНАЛЕНА, ОБЛАДАЮЩИЕ СВОЙСТВАМИ ИНГИБИТОРА ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА ТИРОЗИНКИНАЗЫ | 2004 |
|
RU2346946C2 |
| RU 2004104464 А, 10.08.2005 | |||
| Устройство фазовой автоподстройки частоты | 1985 |
|
SU1383498A1 |
| Направляющее устройство для токарноревольверного станка | 1975 |
|
SU653031A1 |
| US 7329667 В2, 12.02.2008. | |||
Авторы
Даты
2013-11-20—Публикация
2011-07-20—Подача