Область техники
Настоящее изобретение относится к омега-3 липидным соединениям общей формулы (I):

Изобретение также относится к фармацевтическим композициям и липидным композициям, содержащим такие соединения, и к таким соединениям для применения их в качестве лекарственных средств, в частности, для лечения сердечно-сосудистых и метаболических заболеваний.
Предпосылки создания изобретения
Пищевые полиненасыщенные жирные кислоты (PUFA)(ПНЖК) влияют на многообразные физиологические процессы, оказывая воздействие на нормальное состояние здоровья и на хронические заболевания, как например, регуляция уровней липидов плазмы крови, сердечно-сосудистые и иммунные функции, действие инсулина, и развитие нейронов и зрительная функция. Прием внутрь ПНЖК (обычно в виде сложных эфиров, например, в виде глицеридов или фосфолипидов) будет приводить к их распределению практически в каждой клетке организма, воздействуя на состав и функцию мембраны, синтез эйкозаноидов, передачу сигнала в клетке и регуляцию экспрессии генов.
Колебания в распределении различных жирных кислот/липидов по различным тканям, в дополнение к специфическому относительно клетки липидному метаболизму, а также экспрессия регулируемых жирными кислотами факторов транскрипции, вероятно, играют важную роль в установлении того, как клетки реагируют на изменения состава ПНЖК. (Benatti, P. et al, J. Am. Coll. Nutr. 2004, 23, 281).
ПНЖК или их метаболиты, как было показано, модулируют транскрипцию генов путем взаимодействия с несколькими ядерными рецепторами. Существуют активируемые пролифераторами пероксисом рецепторы (PPAR), печеночный ядерный фактор-4 (HNF-4), X-рецептор печени (LXR) и рецептор 9-цис-ретиноевой кислоты (ретиноевый X-рецептор, RXR). Обработка ПНЖК также может способствовать регуляции относительного количества многих факторов транскрипции в ядре, включая SREBP, NFkB, c/EBPβ и HIF-1α. Указанные эффекты не обусловлены прямым связыванием жирной кислоты с фактором транскрипции, а скорее включаются механизмы, которые оказывают влияние на содержание факторов транскрипции в ядре.
Регуляция транскрипции генов посредством ПНЖК оказывает сильные воздействия на клеточный и тканевый метаболизм и создает возможность вероятного объяснения вовлечения взаимодействий нутриент-ген в возникновение и предотвращение или ослабление заболеваний, таких как ожирение, диабет, сердечно-сосудистые нарушения, иммунно-воспалительные заболевания и злокачественные заболевания (Wahle, J., et al., Proceedings of the Nutrition Society, 2003, 349).
Было показано, что рыбий жир, богатый омега-3 полиненасыщенными жирными кислотами, эйкозапентаеновой кислотой (ЕРА) и докозагексаеновой кислотой (DHA), снижает риск сердечно-сосудистых заболеваний, отчасти, путем снижения концентрации триглицеридов в крови. Указанный благоприятный эффект является результатом, главным образом, комбинированного действия процессов ингибирования липогенеза путем уменьшения SPEBP-1 и стимуляции окисления жирных кислот путем активации PPAR-α в печени.
Было показано, что омега-3 ПНЖК в рыбьем жире улучшают прогноз некоторых хронических воспалительных заболеваний, характеризующихся аккумуляцией лейкоцитов и опосредованным лейкоцитами повреждением ткани, включая атеросклероз, IgA нефропатию, воспалительное заболевание кишечника, ревматоидный артрит, псориаз, и т.д. (Mishra, A., Arterioscler. Thromb. Vasc. Biol., 2004, 1621).
Вследствие их ограниченной устойчивости in vivo и отсутствия их биологической специфичности, ПНЖК не достигли широкого применения в качестве терапевтических средств. Химические модификации омега-3 полиненасыщенных жирных кислот были осуществлены несколькими исследовательскими группами для изменения или увеличения их метаболических эффектов.
Например, гиполипидемические эффекты ЕРА были усилены путем введения метила или этила в α-положение этилового сложного эфира ЕРА. (Vaagenes et al. Biochemical Pharm. 1999, 58, 1133).
В последней работе, опубликованной L. Larsen (Larsen, L. et al., Lipids, 2005, 40, 49), авторы показали, что α-метильные производные ЕРА и DHA повышали активацию ядерного рецептора PPARa и, тем самым, экспрессию L-FABP по сравнению с ЕРА/DHA. Авторы полагают, что замедленный катаболизм указанных α-метильных производных ПНЖК вносит вклад в повышение их воздействия.
Ядерные рецепторы (NR) составляют большое и высококонсервативное семейство факторов транскрипции, активированных лигандами, которые регулируют различные биологические процессы, такие как развитие, метаболизм и репродукция. Признано, что лиганды для указанных рецепторов могут быть использованы в лечении общих заболеваний, таких как атеросклероз, диабет, ожирение и воспалительные заболевания. Как таковые, NR стали важными мишенями лекарственных средств, и идентификация новых лигандов NR является предметом многочисленных исследований.
Активность многих ядерных рецепторов контролируется путем связывания небольших, липофильных лигандов, которые включают гормоны, метаболиты, такие как жирные кислоты, желчные кислоты, продукты окисления холестерина и ксено- и эндобиотики. Ядерные рецепторы могут связываться как мономеры, гомодимеры, или RXR гетеродимеры с ДНК.
Фактор транскрипции NF-kB является индуцируемым эукариотическим фактором транскрипции Rel-семейства. Он является главным компонентом в последовательности реакций стресса, который регулирует активацию генов раннего ответа, вовлеченных в экспрессию воспалительных цитокинов, молекул адгезии, белков теплового шока, циклооксигеназ, липооксигеназ и окислительно-восстановительных ферментов.
Zhao, G. et al (Biochemical and Biophysical Research Comm., 2005, 909) предположил, что противовоспалительные эффекты ПНЖК в моноцитах ТНР-1 человека опосредуются, отчасти, путем ингибирования активации фактора транскрипции NF-kB посредством активации PPAR-γ. Другие исследователи предположили, что противовоспалительное действие ПНЖК опосредуется через ингибирование активации NF-kB, зависимое от PPAR-α.
Для того чтобы проанализировать и оценить результаты, в настоящее время проводится обширное исследование в области ПНЖК, и, в частности омега-3 полиненасыщенных жирных кислот. Однако их фармацевтический потенциал все еще не полностью оценен, и поэтому до сих пор сохраняется необходимость дальнейшей оценки и разработки таких соединений для повышения их применимости в медицине.
Сущность изобретения
Одной целью настоящего изобретения является предоставление омега-3 липидных соединений, обладающих фармацевтической активностью.
Данная цель достигается омега-3 липидным соединением формулы (I):

где
- R1 и R2 являются одинаковыми или разными и могут быть выбраны из группы заместителей, состоящей из атома водорода, гидроксигруппы, алкильной группы, атома галогена, алкоксигруппы, ацилоксигруппы, ацильной группы, алкенильной группы, алкинильной группы, арильной группы, алкилтиогруппы, алкоксикарбонильной группы, карбоксигруппы, алкилсульфинильной группы, алкилсульфонильной группы, аминогруппы и алкиламиногруппы;
- X представляет собой карбоновую кислоту или ее производное, карбоксилат, ангидрид карбоновой кислоты или карбоксамид,
- Y является C16-C22 алкеном с двумя или более двойными связями, имеющими E- и/или Z-конфигурацию,
или его любым фармацевтически приемлемым комплексом, солью, сольватом или пролекарством,
при условии, что:
- R1 и R2 не являются одновременно атомом водорода или атомом фтора; и
- соединение формулы (I) не является:
- 2-замещенной (все-Z)-4,7,10,13,16,19-докозагексаеновой кислотой в виде карбоновой кислоты, карбоксилата, ангидрида карбоновой кислоты или карбоксамида;
- (все-Z)-2-метил-5,8,11,14,17 эйкозапентаеновой кислотой или ее этиловым эфиром;
- (все-Z)-2-этил-5,8,11,14,17 эйкозапентаеновой кислотой или ее этиловым эфиром;
- (все-Z)-2,2-диметил-5,8,11,14,17 эйкозапентаеновой кислотой или ее этиловым эфиром;
- (все-Z)-2-бензил-5,8,11,14,17 эйкозапентаеновой кислотой или ее этиловым эфиром;
или
- (все-Z)-2-гидрокси-9,12,15-октадекатриеновой кислотой или ее этиловым эфиром;
- (все-Z)-2-карбокси-6,9,12,15,18,21-тетракозагексаеновой кислотой;
- этил (все-Z)-2-этоксикарбонил-6,9,12,15,18,21-тетракозагексаеноатом.
В частности, настоящее изобретение относится к омега-3 липидным соединениям формулы (I), где:
Y является C16-C20 алкеном с 2-6 двойными связями;
Y является C16-C20 алкеном с 2-6 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации;
Y является C16-C20 алкеном с 3-5 двойными связями;
Y является C16-C20 алкеном с 3-5 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации;
Y является C20 алкеном с 5 двойными связями в Z-конфигурации;
Y является C20 алкеном с 5 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации;
Y является C16 алкеном с 3 двойными связями в Z-конфигурации; или
Y является C16 алкеном с 3 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации.
Изобретение также относится к солям соединения формулы (I). Такие соли могут быть представлены
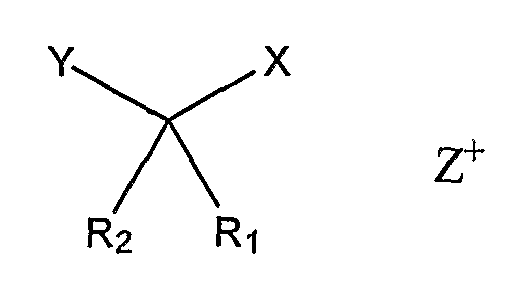
где Х является СОО-,
Z выбирают из группы, состоящей из Li+, Na+, K+, NH4 +,
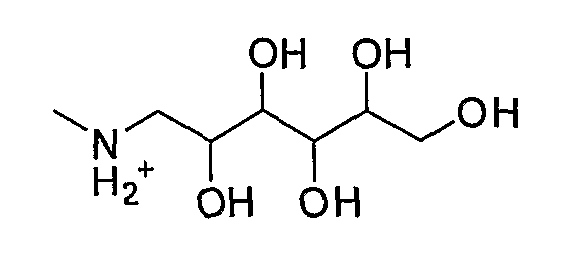
Меглумина,
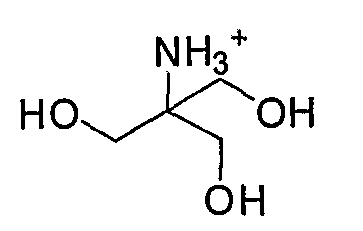
Трис(гидроксиметил)аминометана,
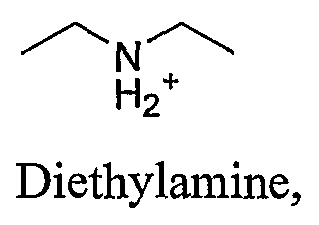
Диэтиламина,
и
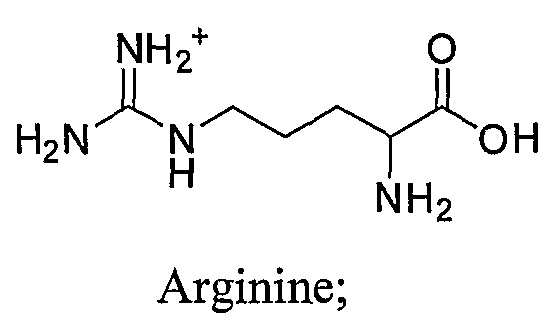
Аргинина;
или соединением
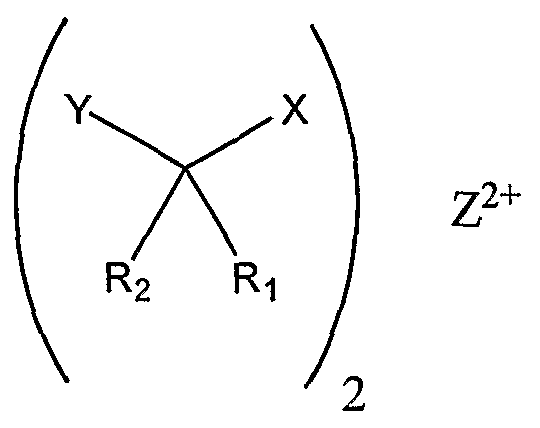
где Х=СОО-,
Z2+ выбирают из группы, состоящей из Mg2+, Ca2+,
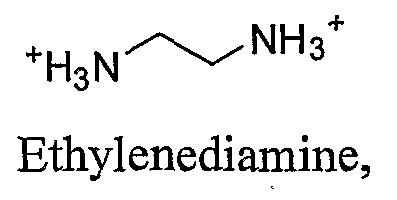
Этилендиамина,
и
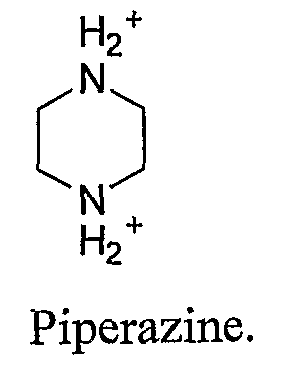
Пиперазина.
Другой характерной солью является
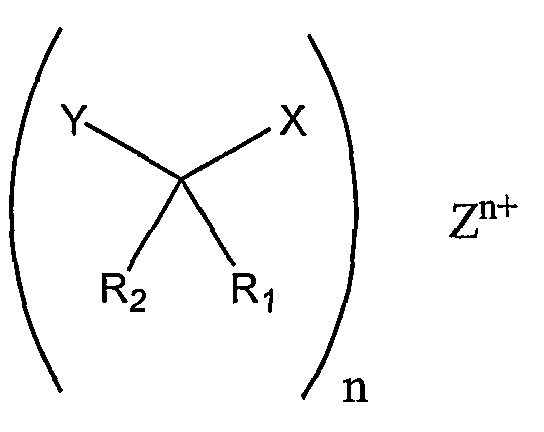
где Х является СОО-,
Zn+ является
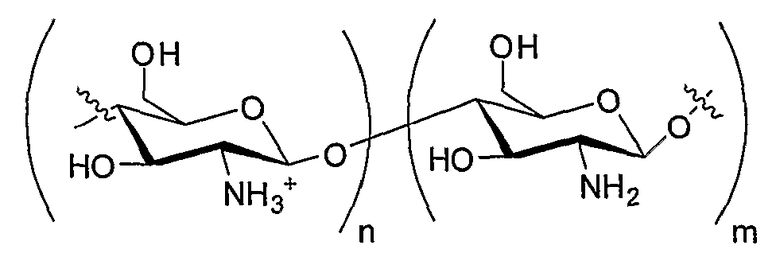
Хитозаном.
Кроме того, настоящее изобретение относится к соединениям формулы (I), где Х является карбоновой кислотой в виде фосфолипида. Такие соединения могут быть представлены следующими формулами,
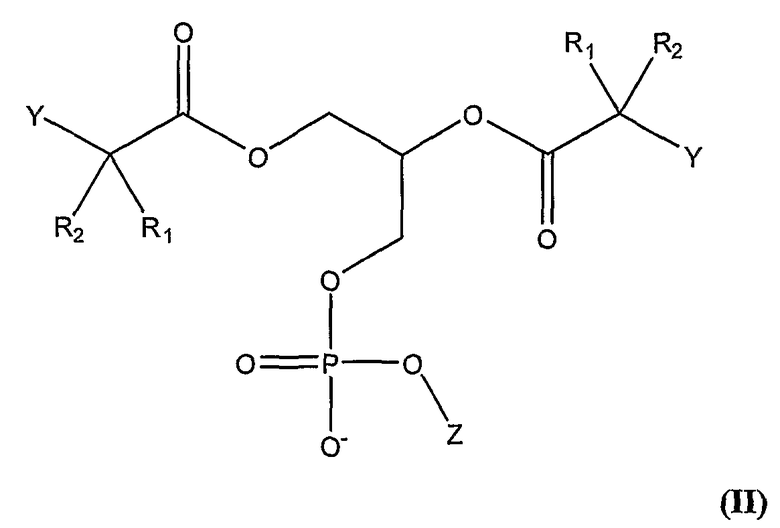
где
Z является
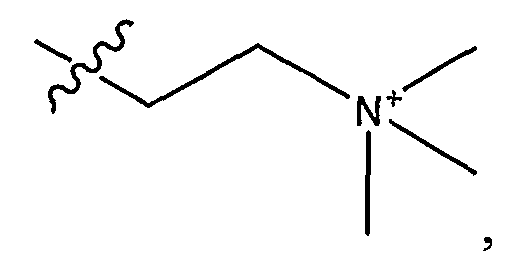
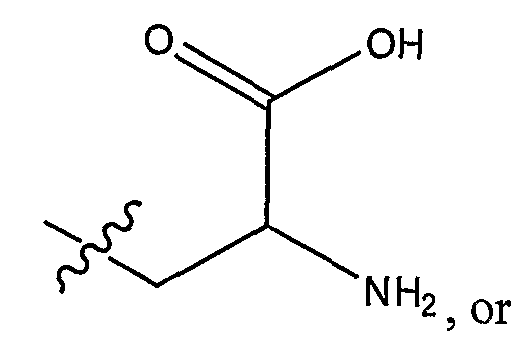 или
или
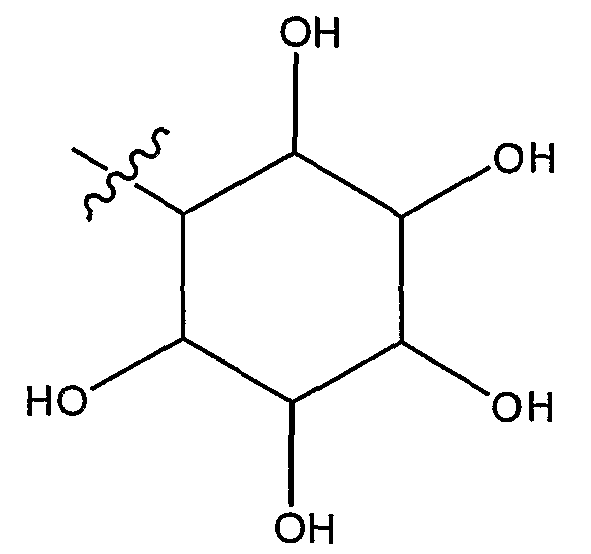
и
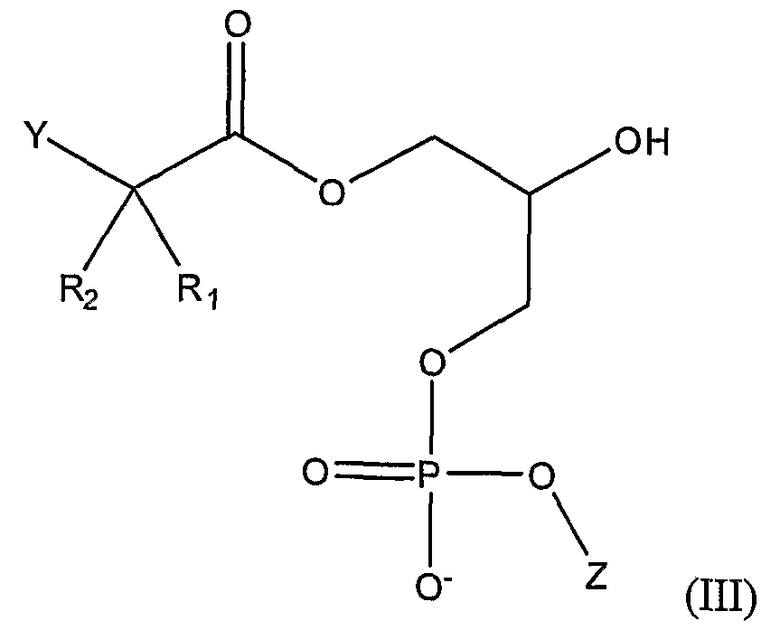
где
Z является

 или
или

или
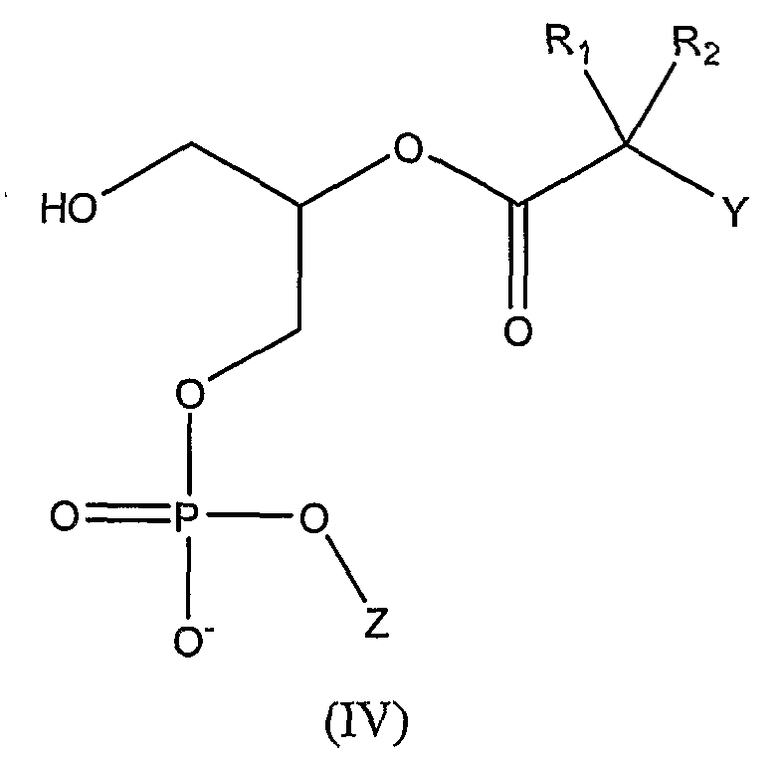
где
Z является

 или
или

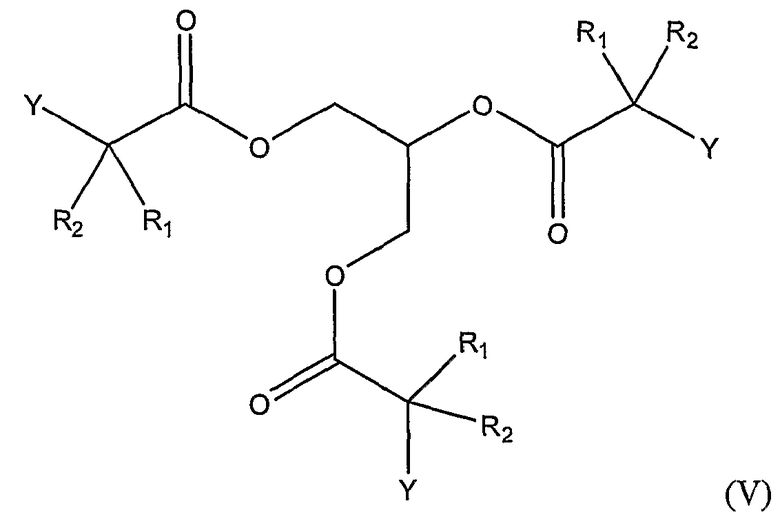
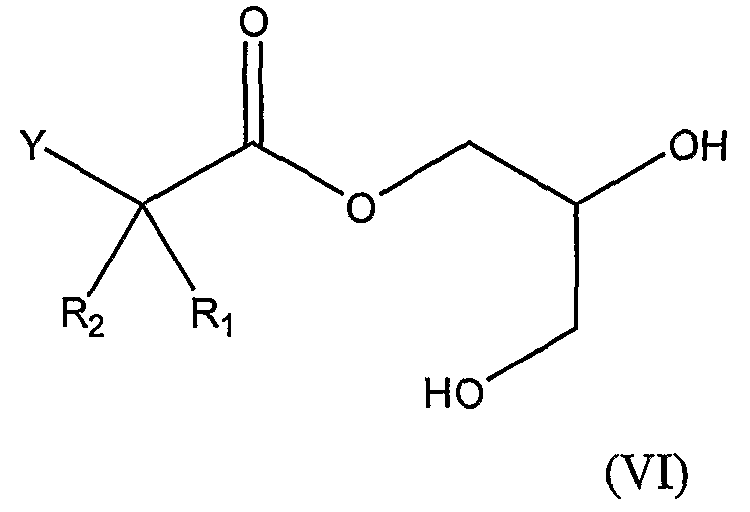
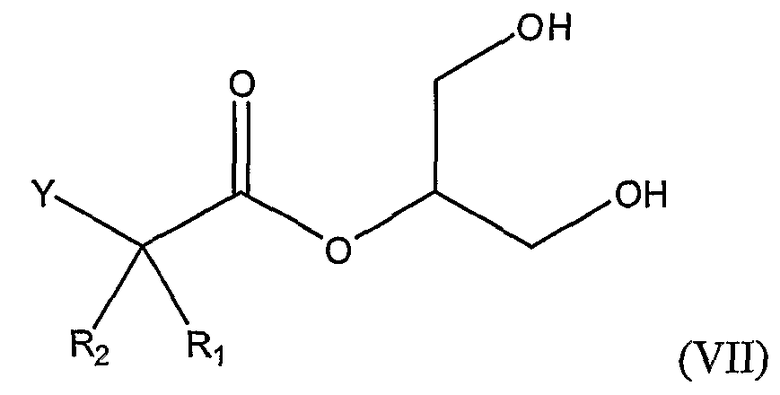
Соединения формулы (I), где Х является карбоновой кислотой в виде триглицерида, 1-моноглицерида и 2-моноглицерида также включены в настоящее изобретение. Указанные соединения представлены в описании формулами (V), (VI) и (VII), соответственно.
Точнее, настоящее изобретение относится к омега-3 липидному соединению, выбранному из группы, состоящей из:
- (все-Z)-9,12,15-октадекатриеновой кислоты
- (все-Z)-6,9,12,15-октадекатетраеновой кислоты
- (все-Z)-7,10,13,16,19-докозапентаеновой кислоты
- (все-Z)-11,14,17-эйкозатриеновой кислоты
- (все-Z)-6,9,12,15,18,21-тетракозагексаеновой кислоты
- (4E, 8Z, 11Z, 14Z, 17Z)-4,8,11,14,17-эйкозапентаеновой кислоты
- (5Е, 8Z, 11Z, 14Z, 17Z)-5,8,11,14,17-эйкозапентаеновой кислоты
- (все-Z)-8,11,14,17-эйкозатетраеновой кислоты
- (4E, 7Z, 10Z, 13Z, 16Z, 19Z)-4,7,10,13,16,19-докозагексаеновой кислоты
в виде карбоновой кислоты или ее производного, карбоксилата, ангидрида карбоновой кислоты или карбоксамида,
или к его любому фармацевтически приемлемому комплексу, соли, сольвату или пролекарству;
где указанное соединение замещено у углерода 2, считая от функциональной группы омега-3 липидного соединения, по крайней мере, одним заместителем, выбранным из группы, состоящей из:
атома водорода, гидроксигруппы, алкильной группы, атома галогена, алкоксигруппы, ацилоксигруппы, ацильной группы, алкенильной группы, алкинильной группы, арильной группы, алкилтиогруппы, алкоксикарбонильной группы, карбоксигруппы, алкилсульфинильной группы, алкилсульфонильной группы, аминогруппы и алкиламиногруппы;
при условии, что омега-3 липидное соединение не является
- замещенным двумя атомами водорода
- (все-Z)-2-карбокси-6,9,12,15,18,21-тетракозагексаеновой кислотой
- этил (все-Z)-2-этоксикарбонил-6,9,12,15,18,21-тетракозагексаеноатом
- (все-Z)-2-гидрокси-9,12,15-октадекатриеновой кислотой, или ее этиловым эфиром.
Примеры солей упомянутых выше соединений включают
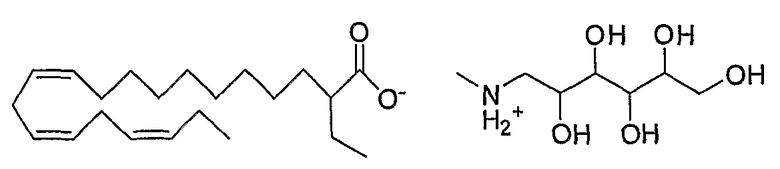
меглуминовую соль (все-Z)-2-этил-11,14,17-эйкозатриеновой кислоты,
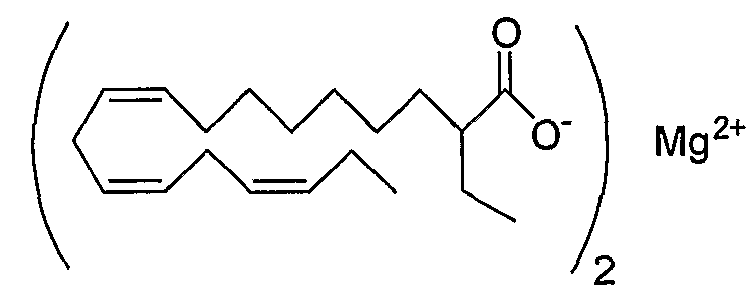
магниевую соль (все-Z)-2-этил-9,12,15-октадекатриеновой кислоты,
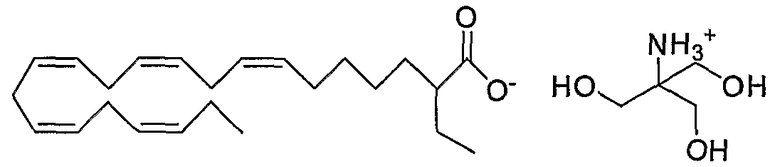
трис(гидроксиметил)аминометановую соль (все-Z)-2-этил-7,10,13,16,19-докозапентаеновой кислоты,
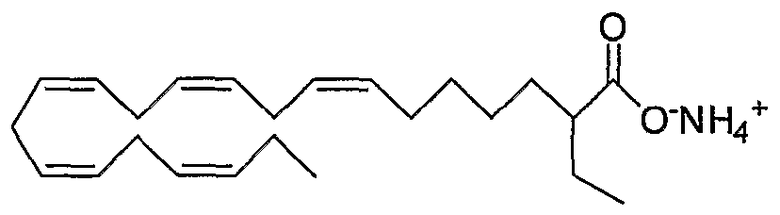
аммониевую соль (все-Z)-2-этил-7,10,13,16,19-докозапентаеновой кислоты.
Кроме того, настоящее изобретение относится к омега-3 липидному соединению, которое получено из (все-Z)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА). Такое соединение может быть представлено следующей формулой
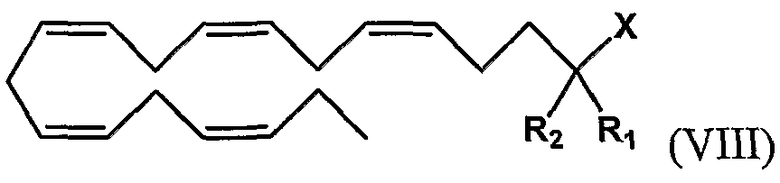
в виде карбоновой кислоты или ее производного, карбоксилата, ангидрида карбоновой кислоты или карбоксамида, представленного Х
или к его любому фармацевтически приемлемому комплексу, соли, сольвату или пролекарству, где
- R1 и R2 являются одинаковыми или разными и могут быть выбраны из группы, состоящей из атома водорода, гидроксигруппы, С3-С7 алкильной группы, атома галогена, алкоксигруппы, ацилоксигруппы, ацильной группы, алкенильной группы, алкинильной группы, алкилтиогруппы, алкоксикарбонильной группы, карбоксигруппы, алкилсульфинильной группы, алкилсульфонильной группы, аминогруппы и алкиламиногруппы, при условии, что R1 и R2 не являются одновременно атомом водорода. Обычно, R1 и R2 выбирают из атома водорода, С3-С7 алкильной группы, алкоксигруппы, алкилтиогруппы, аминогруппы, алкиламиногруппы, алкоксикарбонильной группы и карбоксигруппы. Точнее, R1 и R2 выбирают из атома водорода, С3-С7 алкильной группы, предпочтительно пропила, С1-С7 алкоксигруппы, предпочтительно метокси, эпокси или пропокси, С1-С7 алкилтиогруппы, предпочтительно метилтио, этилтио или пропилтио, аминогруппы, С1-С7 алкиламиногруппы, предпочтительно этиламино- или диэтиламиногруппы, С1-С7 алкоксикарбонильной группы и карбоксигруппы.
- Соединение замещено у углерода 2, считая от функциональной группы омега-3 липидного соединения, двумя заместителями, представленными R1 и R2, выбранными из группы, состоящей из гидроксигруппы, алкильной группы, атома галогена, алкоксигруппы, ацилоксигруппы, ацильной группы, алкенильной группы, алкинильной группы, арильной группы, алкилтиогруппы, алкоксикарбонильной группы, карбоксигруппы, алкилсульфинильной группы, алкилсульфонильной группы, аминогруппы и алкиламиногруппы, при условии, что указанное выше соединение не является 2,2,-диметил-5,8, 11,14,17-эйкозапентаеновой кислотой. Обычно, R1 и R2 выбирают из алкильной группы, алкоксигруппы, алкилтиогруппы, аминогруппы, алкиламиногруппы, алкоксикарбонильной группы и карбоксигруппы. Точнее, R1 и R2 выбирают из С1-С7 алкильной группы, предпочтительно метила, этила или пропила, С1-С7 алкоксигруппы, предпочтительно метокси, этокси или пропокси, С1-С7 алкилтиогруппы, предпочтительно метилтио, этилтио или пропилтио, аминогруппы, С1-С7 алкиламиногруппы, предпочтительно этиламино или диэтиламино, С1-С7 алкоксикарбонильной группы и карбоксигруппы.
В соединениях формул (I) и (VIII), Х обычно представляет собой карбоксилат или карбоновую кислоту. Однако Х может быть производным карбоновой кислоты в виде фосфолипида или три-, ди- или моноглицерида.
Кроме того, настоящее соединение относится к омега-3 липидному соединению, которое получено из (все-Z)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА), представленному формулой (VIII)
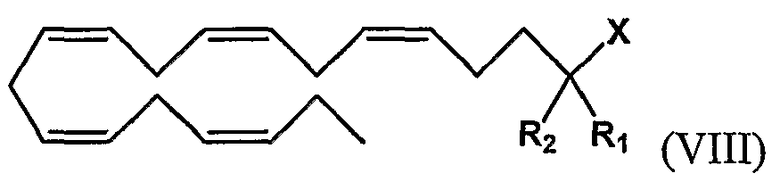
в виде фосфолипида, три-, ди- или моноглицерида, карбоксилата, ангидрида карбоновой кислоты или карбоксамида, представленного Х,
или к его любому фармацевтически приемлемому комплексу, соли, сольвату или пролекарству,
где R1 и R2 являются одинаковыми или разными и могут быть выбраны из группы, состоящей из атома водорода, гидроксигруппы, алкильной группы, атома галогена, алкоксигруппы, ацилоксигруппы, ацильной группы, алкенильной группы, алкинильной группы, арильной группы, алкилтиогруппы, алкоксикарбонильной группы, карбоксигруппы, алкилсульфинильной группы, алкилсульфонильной группы, аминогруппы и алкиламиногруппы, при условии, что R1 и R2 не являются одновременно атомом водорода. Соединение формулы (VIII) не является любым одним из
- (все-Z)-2-метил-5,8,11,14,17-эйкозапентаеновой кислоты или ее этилового эфира;
- (все-Z)-2-этил-5,8,11,14,17-эйкозапентаеновой кислоты или ее этилового эфира;
- (все-Z)-2,2-диметил-5,8,11,14,17-эйкозапентаеновой кислоты или ее этилового эфира.
Обычно, R1 и R2 являются одинаковыми или различными и выбранными из атома водорода, алкильной группы, алкоксигруппы, алкилтиогруппы, аминогруппы, алкиламиногруппы, алкоксикарбонильной группы и карбоксигруппы. Точнее, R1 и R2 выбирают из атома водорода, C1-C7 алкильной группы, предпочтительно метила, этила или пропила, C1-C7 алкоксигруппы, предпочтительно метокси, этокси или пропокси, C1-C7 алкилтиогруппы, предпочтительно метилтио, этилтио или пропилтио, аминогруппы, C1-C7 алкиламиногруппы, предпочтительно этиламино или диэтиламино, C1-C7 алкоксикарбонильной группы и карбоксигруппы.
В соединениях формулы (VIII), представленной выше, Х может представлять собой карбоксилат или карбоновую кислоту. Однако группа Х может быть представлена карбоновой кислотой в виде фосфолипида согласно формулам (II), (III) и (IV), описанным выше. Примеры таких соединений включают:
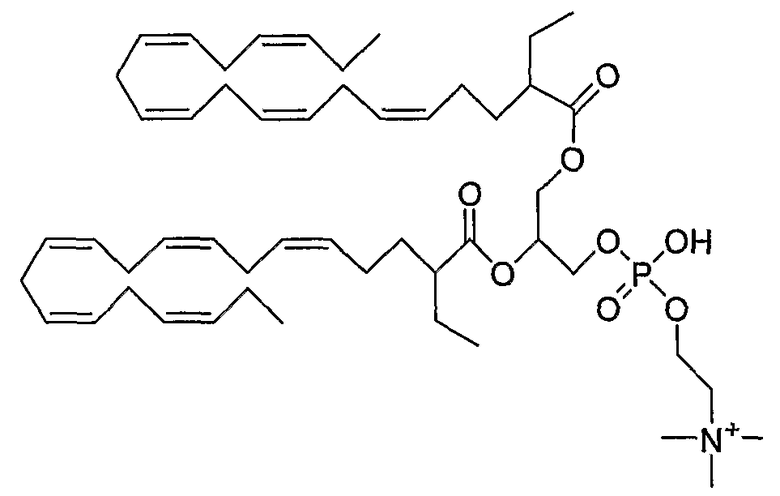
1,2-Ди((все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицеро-3-фосфохолин,
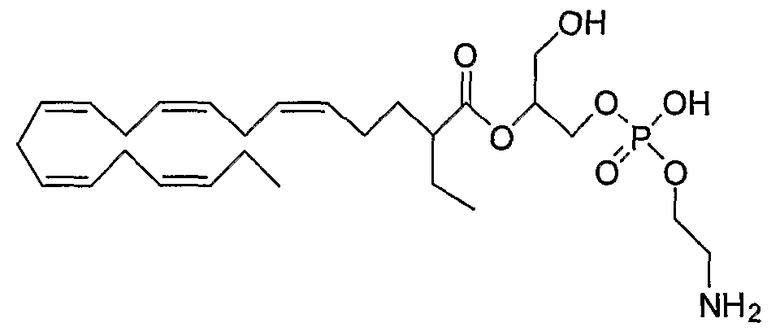
2-(все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил-sn-глицеро-3-фосфоэтаноламин
Кроме того, группа Х также может быть представлена карбоновой кислотой в виде триглицерида согласно формуле (V), представленной выше. Примером такого соединения является
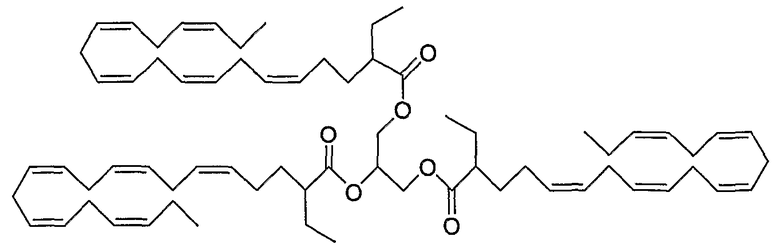
1,2,3-трис((все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицерин.
Группа Х также может быть представлена карбоновой кислотой в виде 2-моноглицерида формулы (VII). Примером такого соединения является
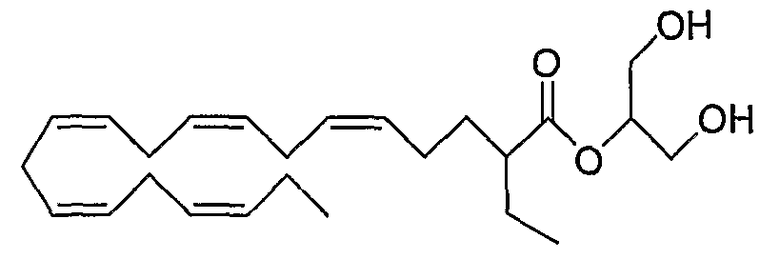
2-((все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицерин
В соединении согласно изобретению, указанная выше алкильная группа может быть выбрана из группы, состоящей из метила, этила, н-пропила, изопропила, н-бутила, изобутила, втор-бутила и н-гексила; указанным выше атомом галогена может быть фтор; указанная выше алкоксигруппа может быть выбрана из группы, состоящей из метокси, этокси, пропокси, изопропокси, втор-бутокси, фенокси, бензилокси, OCH2CF3 и OCH2CH2OCH3; указанная выше алкенильная группа может быть выбрана из группы, состоящей из аллила, 2-бутенила и 3-гексенила; указанная выше алкинильная группа может быть выбрана из группы, состоящей из пропаргила, 2-бутинила и 3-гексинила; указанная выше арильная группа может быть выбрана из бензильной группы и замещенной бензильной группы; указанная выше алкилтиогруппа может быть выбрана из группы, состоящей из метилтио, этилтио, изопропилтио и фенилтио; указанная выше алкоксикарбонильная группа может быть выбрана из группы, состоящей из метоксикарбонила, этоксикарбонила, пропоксикарбонила и бутоксикарбонила; указанная выше алкилсульфинильная группа может быть выбрана из группы, состоящей из метансульфинила, этансульфинила и изопропансульфинила; указанная выше алкилсульфонильная группа может быть выбрана из группы, состоящей из метансульфонила, этансульфонила и изопропансульфонила; и указанная выше алкиламиногруппа может быть выбрана из группы, состоящей из метиламино, диметиламино, этиламино и диэтиламино.
Производным карбоновой кислоты может быть фосфолипид или три-, ди- или моноглицерид, т.е. соединение согласно изобретению может существовать в виде фосфолипида, три-, ди- или моноглицерида или в виде свободной кислоты.
Согласно настоящему изобретению, указанная выше карбоксилатная группа может быть выбрана из группы, состоящей из этилкарбоксилата, метилкарбоксилата, н-пропилкарбоксилата, изопропилкарбоксилата, н-бутилкарбоксилата, втор-бутилкарбоксилата и н-гексилкарбоксилата, и указанная выше карбоксамидная группа может быть выбрана из группы, состоящей из первичного карбоксамида, N-метилкарбоксамида, N,N-диметилкарбоксамида, N-этилкарбоксамида и N,N-диэтилкарбоксамида.
Примерами соединений согласно изобретению являются такие соединения, у которых Х является этилкарбоксилатом, и Y является С16 алкеном с 3 двойными связями, прерываемыми метиленовой группой, имеющими Z-конфигурацию в положениях 9, 12 и 15, где:
одной из групп R1 и R2 является метил, и другой является атом водорода;
одной из групп R1 и R2 является этил, и другой является атом водорода;
одной из групп R1 и R2 является пропил, и другой является атом водорода;
одной из групп R1 и R2 является метокси, и другой является атом водорода;
одной из групп R1 и R2 является этокси, и другой является атом водорода;
одной из групп R1 и R2 является пропокси, и другой является атом водорода;
одной из групп R1 и R2 является тиометил, и другой является атом водорода;
одной из групп R1 и R2 является тиоэтил, и другой является атом водорода;
одной из групп R1 и R2 является тиопропил, и другой является атом водорода;
одной из групп R1 и R2 является этиламино, и другой является атом водорода;
одной из групп R1 и R2 является диэтиламино, и другой является атом водорода; или
одной из групп R1 и R2 является амино, и другой является атом водорода.
Другими примерами соединений согласно изобретению являются такие соединения, у которых Х является этилкарбоксилатом, и Y является С20 алкеном с 5 двойными связями, прерываемыми метиленовой группой, имеющими Z-конфигурацию в положениях 7, 10, 13, 16 и 19, где:
одной из групп R1 и R2 является метил, и другой является атом водорода;
одной из групп R1 и R2 является этил, и другой является атом водорода;
одной из групп R1 и R2 является пропил, и другой является атом водорода;
одной из групп R1 и R2 является метокси, и другой является атом водорода;
одной из групп R1 и R2 является этокси, и другой является атом водорода;
одной из групп R1 и R2 является пропокси, и другой является атом водорода;
одной из групп R1 и R2 является тиометил, и другой является атом водорода;
одной из групп R1 и R2 является тиоэтил, и другой является атом водорода;
одной из групп R1 и R2 является тиопропил, и другой является атом водорода.
В омега-3 липидном соединении формулы (I) согласно настоящему изобретению, R1 и R2 могут быть одинаковыми или различными. Когда указанные группы являются различными, соединения формулы (I) могут существовать в стереоизомерных формах. Надо понимать, что изобретение охватывает все оптические изомеры соединений формулы (I) и их смеси, включая рацематы. Поэтому, настоящее изобретение включает, когда R1 отличается от R2, соединения формулы (I), которые являются рацемическими или энантиомерно чистыми, либо в виде (S)-, либо в виде (R)-энантиомера.
Настоящее изобретение также относится к омега-3 соединению формулы (I) для применения в качестве лекарственного средства или для диагностических целей, например, для позитрон-эмиссионной томографии (РЕТ).
Кроме того, настоящее изобретение относится к фармацевтической композиции, содержащей омега-3 липидное соединение формулы (I). Фармацевтическая композиция может содержать фармацевтически приемлемый носитель, эксципиент или разбавитель или любую их комбинацию, и походящим образом составлена для перорального введения, например, в виде капсулы или пакета-саше. Подходящей суточной дозой соединения формулы (I) является от 1 мг до 10 г указанного соединения; от 50 мг до 1 г указанного соединения или от 50 мг до 200 мг указанного соединения.
Настоящее изобретение также относится к липидной композиции, содержащей омега-3 липидное соединение формулы (I). Подходящим является, когда, по меньшей мере, 60% масс. или, по меньшей мере, 80% масс. липидной композиции составляет указанное соединение. Липидная композиция также может включать жирные кислоты, выбранные из (все-Z)-5,8,11,14,17-эйкозапентаеновой кислоты (EPA), (все-Z)-4,7,10,13,16,19-докозагексаеновой кислоты (DHA), (все-Z)-6,9,12,15,18-генэйкозапентаеновой кислоты (HPA) и/или (все-Z)-7,10,13,16,19-докозапентаеновой кислоты (DPA) или их производных, т.е. представленных в их альфа-замещенной форме, и/или фармацевтически приемлемый антиоксидант, например, токоферол.
Кроме того, изобретение относится к применению омега-3 липидного соединения формулы (I) для получения лекарственного средства для:
- активации или модуляции, по меньшей мере, одной из изоформ рецептора (PPAR) человека, активируемого пролифераторами пероксисом, где указанный активируемый пролифераторами пероксисом рецептор (PPAR) является активируемым пролифераторами пероксисом рецептором (PPAR)α и/или γ.
- лечения и/или предотвращения периферической инсулинорезистентности и/или состояния диабета.
- снижения уровня инсулина плазмы, глюкозы в крови и/или триглицеридов сыворотки.
- лечения и/или предотвращения диабета 2 типа.
- предотвращения и/или лечения повышенных уровней триглицеридов и/или не-HDL-холестерина (не-ЛПВП), LDL-холестерина (ЛПНП) и VLDL-холестерина (ЛПОНП).
- предотвращения и/или лечения гиперлипидемического состояния, например, гипертриглицеридемии (HTG).
- повышения уровней HDL (ЛПВП) в сыворотке человека.
- лечения и/или предотвращения ожирения или состояния избыточной массы тела.
- уменьшения массы тела и/или предотвращения прибавления в массе тела.
- лечения и/или предотвращения заболевания жировой инфильтрации печени, например, неалкогольной печени (NAFLD).
- лечения инсулинорезистентности, гиперлипидемии и/или ожирения или состояния избыточной массы тела.
- получения лекарственного средства для лечения и/или предотвращения воспалительного заболевания или состояния.
Изобретение также относится к соединению формулы (I) для лечения и/или предотвращения состояний, перечисленных выше, и к способам лечения и/или предотвращения перечисленных выше состояний, включающим введение млекопитающему, нуждающемуся в этом, фармацевтически активного количества соединения формулы (I).
Кроме того, настоящее изобретение охватывает способы получения омега-3 липидных соединений формулы (I).
Подробное описание изобретения
В исследовательской работе, приведшей к настоящему изобретению, удивительным образом было обнаружено, что омега-3 липидные соединения, представленные общей формулой (I), имеют высокую аффинность к ядерным рецепторам семейства PPAR.
Известно, что PPARα является самым разнородным из рецепторов PPAR, взаимодействуя с насыщенными и ненасыщенными жирными кислотами. Рецептор PPARδ взаимодействует с насыщенными и ненасыщенными жирными кислотами, хотя и менее эффективно, чем PPARα. Рецептор PPARγ имеет самый ограниченный профиль связывания с жирными кислотами, взаимодействуя наиболее эффективно с ПНЖК и только слабо с мононенасыщенными жирными кислотами (Xu et al., Molecular Cell, 1999, 397-403).
Действие ПНЖК на указанные ядерные рецепторы обусловлено не только структурой и аффинностью жирных кислот к рецептору. Факторы, влияющие на уровни составляющих внутриклеточных неэтерифицированных жирных кислот (NEFA)(НЭЖК), представляются также важными. На указанный пул НЭЖК оказывает воздействие концентрация экзогенных жирных кислот, поступающих в клетку, и количество эндогенных синтезированных жирных кислот, их удаление через включение в липиды, а также их пути окисления. (Pawar, A. & Jump, DB, Journal of Biological Chem., 2003, 278, 35931).
Согласно изобретению, введение, по меньшей мере, одного заместителя в α-положение различных полиненасыщенных жирных кислот приводит к накоплению производных жирных кислот в пуле НЭЖК скорее, чем включение в нейтральные липиды или окисление указанных жирных кислот. Омега-3 липидные соединения согласно настоящему изобретению накапливаются во внутриклеточном пуле НЭЖК и запускают механизм действия локальных ядерных рецепторов в большей степени, чем незамещенные жирные кислоты.
Различные заместители ПНЖК согласно изобретению будут приводить к различной аффинности производных к ядерным рецепторам и, в частности, к рецепторам PPAR. Изменения в аффинности к различным рецепторам в дополнение к различному набору кофакторов, приводят к изменениям биологической активности указанных α-замещенных липидных производных формулы (I).
Поскольку ПНЖК аккумулируются по-разному в различных тканях, указанные выше модифицированные ПНЖК имеют потенциальную способность выступать в качестве тканеспецифических лигандов ядерных рецепторов. Поскольку многие из ядерных рецепторов распределяются по-разному в различных тканях, представляется важным разработать лиганды, которые in vivo могут быть направлены на определенные клетки для связывания и активирования рецептора-мишени.
Помимо того, что производные согласно изобретению являются лучшими лигандами ядерных рецепторов, они не легко деградируют посредством α- и β-окисления, как природные ПНЖК, благодаря замещению в α-положении.
Номенклатура и терминология
Жирные кислоты являются углеводородами с прямой цепью, имеющие карбоксильную (СООН) группу у одного конца (α) и (обычно) метильную группу у другого (ω)-конца. В физиологии, жирные кислоты называют по положению первой двойной связи от ω-конца. Термин ω-3 (омега-3) означает, что первая двойная связь присутствует как третья углерод-углеродная связь от концевой СН3-группы (ω) углеродной цепи. В химии, нумерация атомов углерода начинается от α-конца.
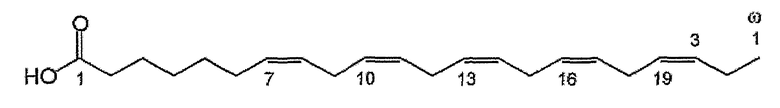
Как используют в описании, выражение “двойные связи, прерываемые метиленовой группой” относится к случаю, когда метиленовая группа расположена между отдельными двойными связями в углеродной цепи омега-3 липидного соединения.
В данном описании, термины “2-замещенный”, замещенный в положении 2 и “замещенный у углерода 2, считая от функциональной группы омега-3 липидного соединения” относятся к замещению у атома углерода, обозначенного 2 в соответствии с упомянутой выше нумерацией углеродной цепи. Альтернативно, такое замещение может быть названо “альфа-замещение”.
В данном описании, термин “омега-3 липидное соединение” (соответствующий ω-3 или n-3) относится к липидному соединению, имеющему первую двойную связь у третьей углерод-углеродной связи от ω-конца углеродной цепи, как определено выше.
Основной идеей настоящего изобретения является омега-3 липидное соединение формулы (I):

где
- R1 и R2 являются одинаковыми или разными и могут быть выбраны из группы заместителей, состоящей из атома водорода, гидроксигруппы, алкильной группы, атома галогена, алкоксигруппы, ацилоксигруппы, ацильной группы, алкенильной группы, алкинильной группы, арильной группы, алкилтиогруппы, алкоксикарбонильной группы, карбоксигруппы, алкилсульфинильной группы, алкилсульфонильной группы, аминогруппы и алкиламиногруппы;
- X представляет собой карбоновую кислоту или ее производное, карбоксилат, ангидрид карбоновой кислоты или карбоксамид; и
- Y является C16-C22 алкеном с двумя или более двойными связями, имеющими E- и/или Z-конфигурацию.
Получающееся соединение является альфа-замещенным омега-3 липидным соединением, т.е. омега-3 липидным соединением, замещенным в положении 2 у атома углерода углеродной цепи, считая от карбонильного конца. Точнее, получающееся соединение является альфа-замещенной полиненасыщенной омега-3 жирной кислотой, которая может быть представлена как карбоновая кислота или ее производное, как карбоксилат, как ангидрид карбоновой кислоты или как карбоксамид. Авторы настоящего изобретения удивительным образом обнаружили, что следующие омега-3 жирные кислоты являются особенно подходящими как замещенными в альфа-положении, как приведено в формуле (I):
- (все-Z)-9,12,15-октадекатриеновая кислота
- (все-Z)-6,9,12,15-октадекатетраеновая кислота
- (все-Z)-7,10,13,16,19-докозапентаеновая кислота
- (все-Z)-11,14,17-эйкозатриеновая кислота
- (все-Z)-6,9,12,15,18,21-тетракозагексаеновая кислота
- (4E, 8Z, 11Z, 14Z, 17Z)-4,8,11,14,17-эйкозапентаеновая кислота
- (5Е, 8Z, 11Z, 14Z, 17Z)-5,8,11,14,17-эйкозапентаеновая кислота
- (все-Z)-8,11,14,17-эйкозатетраеновая кислота
- (4E, 7Z, 10Z, 13Z, 16Z, 19Z)-4,7,10,13,16,19-докозагексаеновая кислота.
Среди возможных заместителей, перечисленных выше, низшие алкильные группы, в частности, метильные и этильные группы, оказались чрезвычайно пригодными для достижения желаемой фармацевтической активности. Другими чрезвычайно пригодными заместителями являются низшие алкилтиогруппы и низшие алкиламиногруппы, например, имеющие 1-3 атома углерода. Замещение либо R1-группы, либо R2-группы одним из указанных подходящих заместителей, в то время как другая группа является водородом, как полагают, предоставит наиболее эффективный результат.
(все-Z)-5,8,11,14,17-Эйкозапентаеновая кислота (ЕРА) является другой омега-3 жирной кислотой, которая оказалась пригодной для замещения в альфа-положении кислоты, как предложено согласно настоящему изобретению. Для ЕРА, подходящими заместителями являются низшие алкилтиогруппы и низшие алкиламиногруппы, например, имеющие 1-3 атома углерода. По аналогии с описанным выше, замещение либо R1-группы, либо R2-группы одним из указанных заместителей, в то время как другая группа является водородом, как полагают, предоставит наиболее эффективный результат. Случай, когда обе группы R1 и R2 являются этилом, представляет собой другое подходящее замещение ЕРА.
Предпочтительные омега-3 липидные соединения согласно настоящему изобретению разделены на следующие категории A-F:
Категория А - (все-Z)-9,12,15-октадекатриеновая кислота (альфа-линоленовая кислота, ALA) в виде карбоновой кислоты или ее производного, карбоксилата, ангидрида карбоновой кислоты или карбоксамида, замещенная в положении 2:
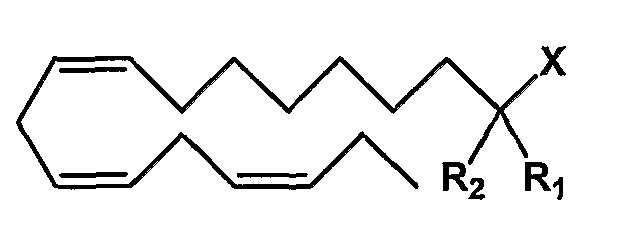
Y=С16 алкен с 3 двойными связями в Z-конфигурации в положениях 9, 12 и 15;
Категория В - (все-Z)-7,10,13,16,19-докозапентаеновая кислота (клупанодоновая кислота, DPA) в виде карбоновой кислоты или ее производного, карбоксилата, ангидрида карбоновой кислоты или карбоксамида, замещенная в положении 2:
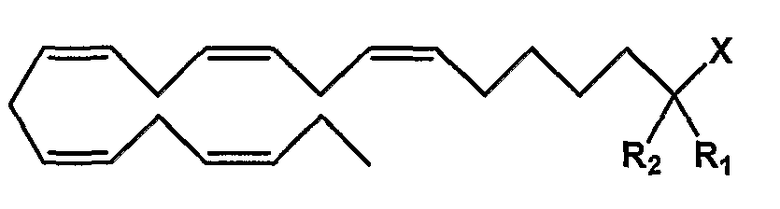
Y=С20 алкен с 5 двойными связями в Z-конфигурации в положениях 7, 10, 13, 16 и 19;
Категория С - (все-Z)-11,14,17-эйкозатриеновая кислота в виде карбоновой кислоты или ее производного, карбоксилата, ангидрида карбоновой кислоты или карбоксамида, замещенная в положении 2:
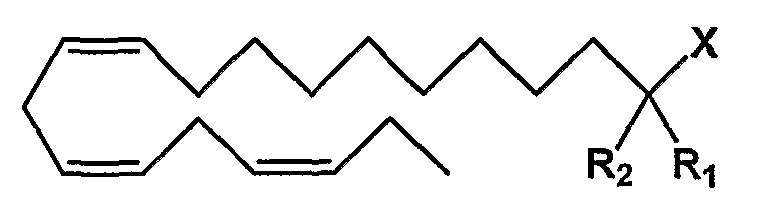
Y=С18 алкен с 3 двойными связями в Z-конфигурации в положениях 11, 14 и 17;
Категория D - (4Е, 8Z, 11Z, 14Z, 17Z)-эйкозапентаеновая кислота в виде карбоновой кислоты или ее производного, карбоксилата, ангидрида карбоновой кислоты или карбоксамида, замещенная в положении 2:
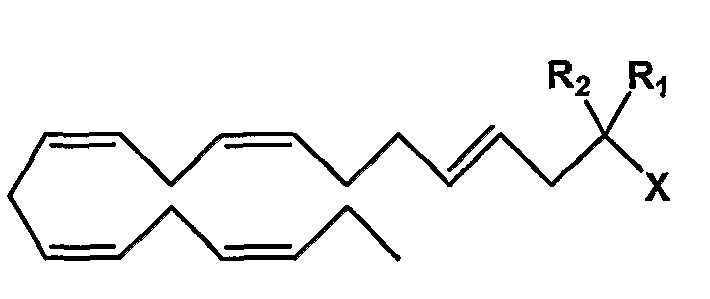
Y=С18 алкен с 5 двойными связями в положениях 4, 8, 11, 14 и 17, где двойные связи в положении 8, 11, 14 и 17 имеют Z-конфигурацию, и двойная связь в положении 4 имеет Е-конфигурацию;
Категория Е - (все-Z)-5,8,11,14,17-эйкозапентаеновая кислота (ЕРА) в виде карбоновой кислоты или ее производного, карбоксилата, ангидрида карбоновой кислоты или карбоксамида, замещенная в положении 2:
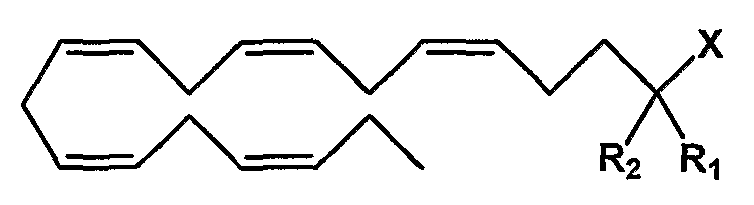
Y=С18 алкен с 5 двойными связями в Z-конфигурации в положениях 5, 8, 11, 14 и 17;
Категория F - (4E, 7Z, 10Z, 13Z, 16Z, 19Z)-докозагексаеновая кислота (транс-DHA) в виде карбоновой кислоты или ее производного, карбоксилата, ангидрида карбоновой кислоты или карбоксамида, замещенная в положении 2:
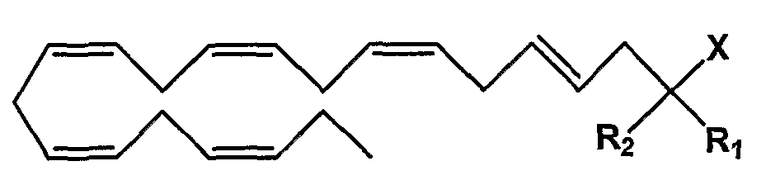
Y=С20 алкен с 6 двойными связями в положениях 4, 7, 10, 13, 16 и 19, где двойные связи в положении 7, 10, 13, 16 и 19 имеют Z-конфигурацию, и двойная связь в положении 4 имеет Е-конфигурацию.
Отдельными примерами предпочтительных омега-3 липидных соединений согласно изобретению являются:
Категория А - примеры (1)-(12):
Для всех примеров (1)-(12):
Х = этилкарбоксилат
Y=С16 алкен с 3 двойными связями в Z-конфигурации в положениях 9, 12 и 15

Этил (все-Z)-2-метил-9,12,15-октадекатриеноат (1)
R1 = метил и R2 = атом водорода, или
R2 = метил и R1 = атом водорода
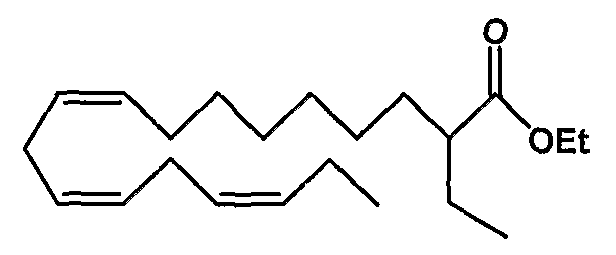
Этил (все-Z)-2-этил-9,12,15-октадекатриеноат (2)
R1 = этил и R2 = атом водорода, или
R2 = этил и R1 = атом водорода
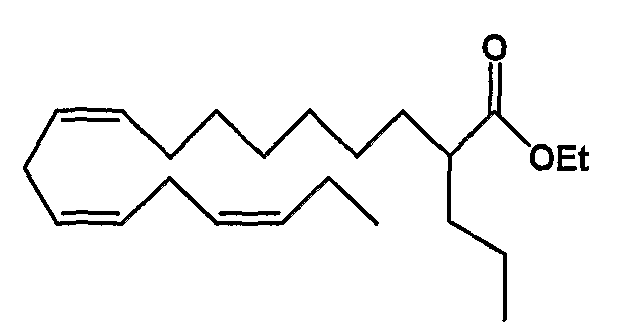
Этил (все-Z)-2-пропил-9,12,15-октадекатриеноат (3)
R1 = пропил и R2 = атом водорода, или
R2 = пропил и R1 = атом водорода
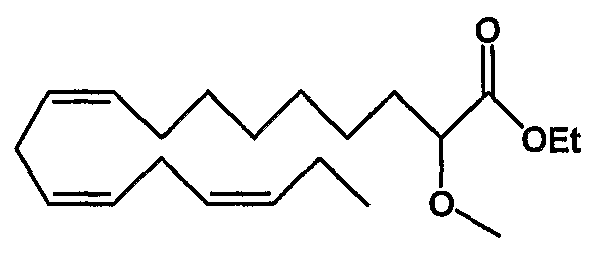
Этил (все-Z)-2-метокси-9,12,15-октадекатриеноат (4)
R1 = метокси и R2 = атом водорода, или
R2 = метокси и R1 = атом водорода
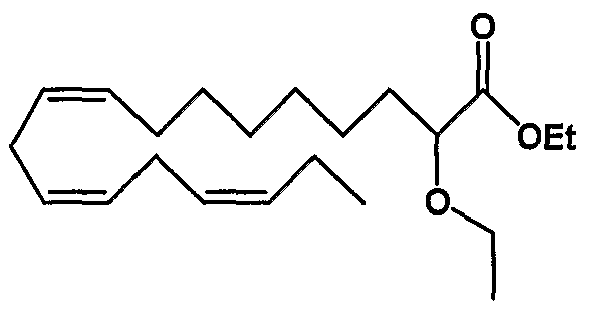
Этил (все-Z)-2-этокси-9,12,15-октадекатриеноат (5)
R1 = этокси и R2 = атом водорода, или
R2 = этокси и R1 = атом водорода
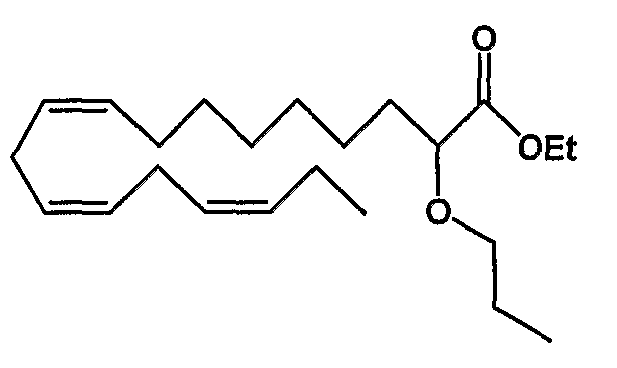
Этил (все-Z)-2-пропокси-9,12,15-октадекатриеноат (6)
R1 = пропокси и R2 = атом водорода, или
R2 = пропокси и R1 = атом водорода
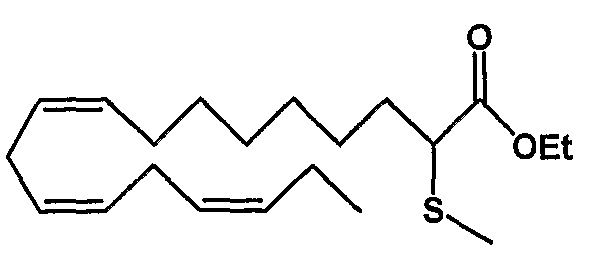
Этил (все-Z)-2-тиометил-9,12,15-октадекатриеноат (7)
R1 = метилтио и R2 = атом водорода, или
R2 = метилтио и R1 = атом водорода
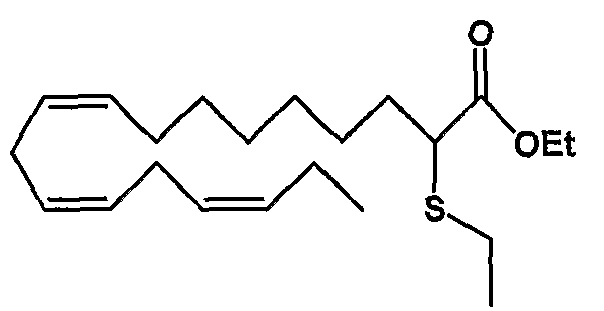
Этил (все-Z)-2-тиоэтил-9,12,15-октадекатриеноат (8)
R1 = этилтио и R2 = атом водорода, или
R2 = этилтио и R1 = атом водорода
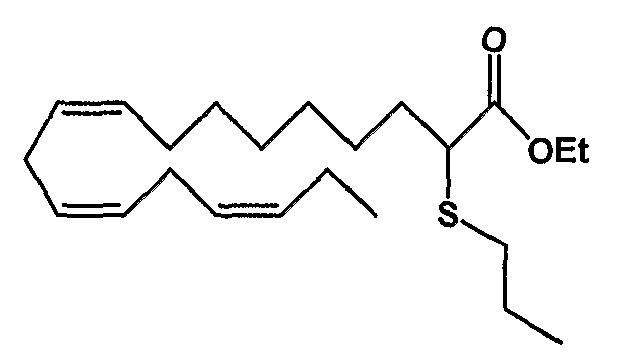
Этил (все-Z)-2-тиопропил-9,12,15-октадекатриеноат (9)
R1 = пропилтио и R2 = атом водорода, или
R2 = пропилтио и R1 = атом водорода
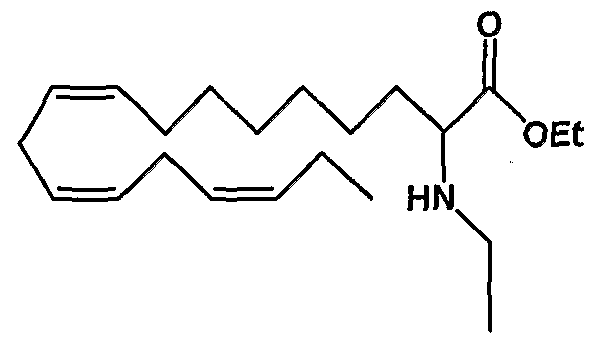
Этил (все-Z)-2-этиламино-9,12,15-октадекатриеноат (10)
R1 = этиламино и R2 = атом водорода, или
R2 = этиламино и R1 = атом водорода
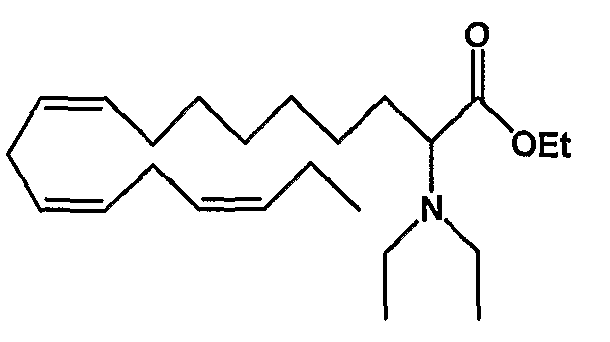
Этил (все-Z)-2-диэтиламино-9,12,15-октадекатриеноат (11)
R1 = диэтиламино и R2 = атом водорода, или
R2 = диэтиламино и R1 = атом водорода
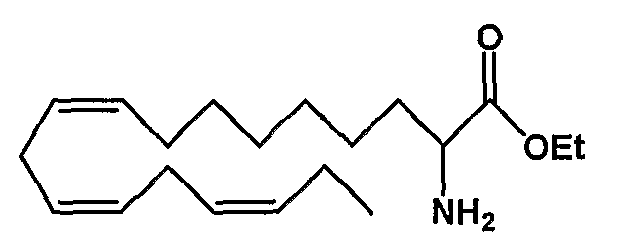
Этил (все-Z)-2-амино-9,12,15-октадекатриеноат (12)
R1 = амино и R2 = атом водорода, или
R2 = амино и R1 = атом водорода
Категория В - примеры (13)-(21):
Для всех примеров (13)-(21):
Х = этилкарбоксилат
Y=С20 алкен с 5 двойными связями в Z-конфигурации в положениях 7, 10, 13, 16 и 19
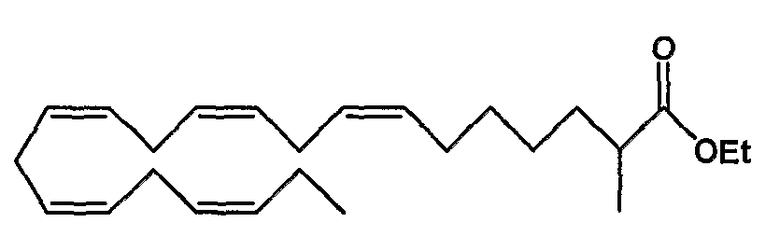
Этил (все-Z)-2-метил-7,10,13,16,19-докозапентаеноат (13)
R1 = метил и R2 = атом водорода, или
R2 = метил и R1 = атом водорода
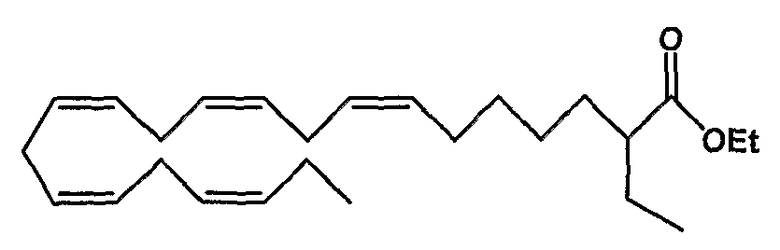
Этил (все-Z)-2-этил-7,10,13,16,19-докозапентаеноат (14)
R1 = этил и R2 = атом водорода, или
R2 = этил и R1 = атом водорода
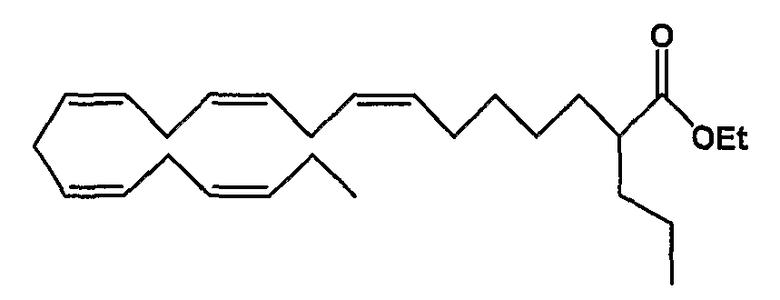
Этил (все-Z)-2-пропил-7,10,13,16,19-докозапентаеноат (15)
R1 = пропил и R2 = атом водорода, или
R2 = пропил и R1 = атом водорода
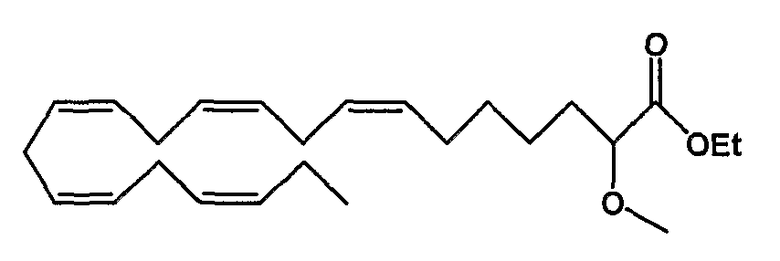
Этил (все-Z)-2-метокси-7,10,13,16,19-докозапентаеноат (16)
R1 = метокси и R2 = атом водорода, или
R2 = метокси и R1 = атом водорода
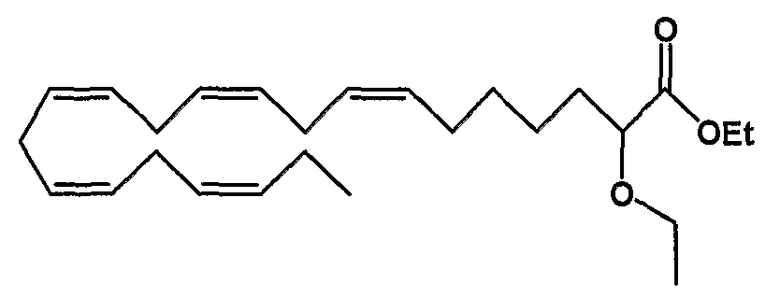
Этил (все-Z)-2-этокси-7,10,13,16,19-докозапентаеноат (17)
R1 = этокси и R2 = атом водорода, или
R2 = этокси и R1 = атом водорода
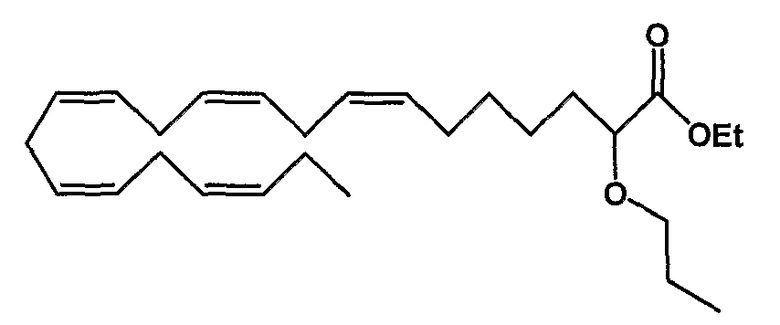
Этил (все-Z)-2-пропокси-7,10,13,16,19-докозапентаеноат (18)
R1 = пропокси и R2 = атом водорода, или
R2 = пропокси и R1 = атом водорода
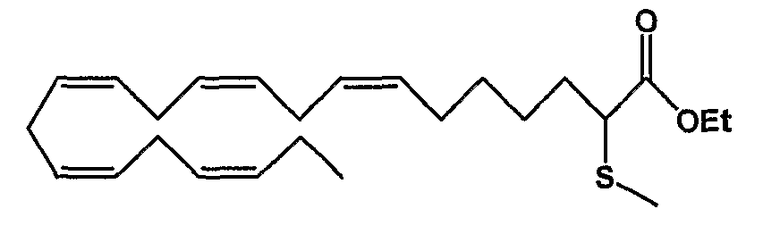
Этил (все-Z)-2-тиометил-7,10,13,16,19-докозапентаеноат (19)
R1 = метилтио и R2 = атом водорода, или
R2 = метилтио и R1 = атом водорода

Этил (все-Z)-2-тиоэтил-7,10,13,16,19-докозапентаеноат (20)
R1 = этилтио и R2 = атом водорода, или
R2 = этилтио и R1 = атом водорода
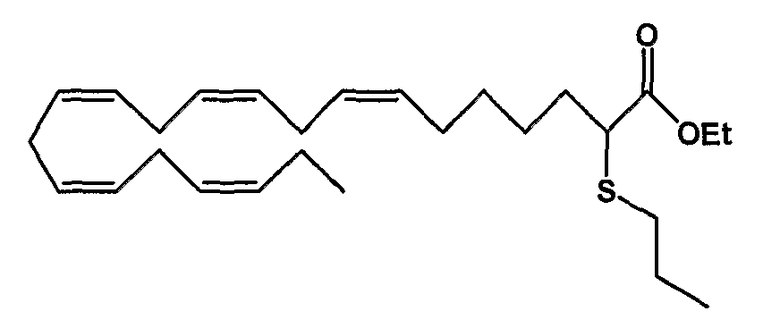
Этил (все-Z)-2-тиопропил-7,10,13,16,19-докозапентаеноат (21)
R1 = пропилтио и R2 = атом водорода, или
R2 = пропилтио и R1 = атом водорода
Категория С - примеры (23)-(24) и (27)-(35):
Для всех примеров (23)-(24) и (27)-(35):
Y=С18 алкен с 3 двойными связями в Z-конфигурации в положениях 11, 14 и 17
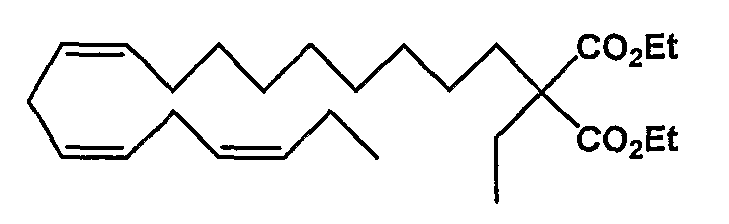
Этил (все-Z)-2-этил,2-этоксикарбонил-11,14,17-эйкозатриеноат (23)
R1 = этоксикарбонил и R2 = этил, или
R2 = этоксикарбонил и R1 = этил
Х = этилкарбоксилат
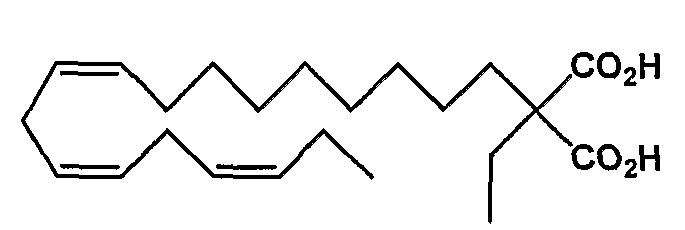
(все-Z)-2-этил,2-карбокси-11,14,17-эйкозатриеновая кислота (24)
R1 = карбокси и R2 = этил, или
R2 = карбокси и R1 = этил
Х = уксусная кислота
Для всех примеров (27)-(35):
Х = этилкарбоксилат
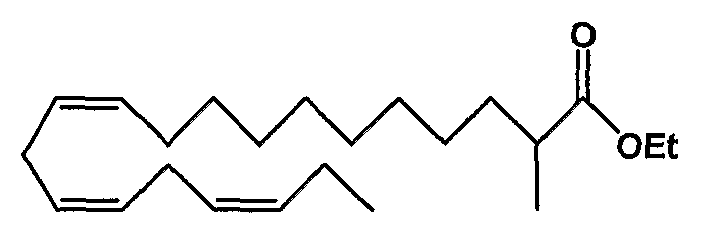
Этил (все-Z)-2-метил-11,14,17-эйкозатриеноат (27)
R1 = метил и R2 = атом водорода, или
R2 = метил и R1 = атом водорода
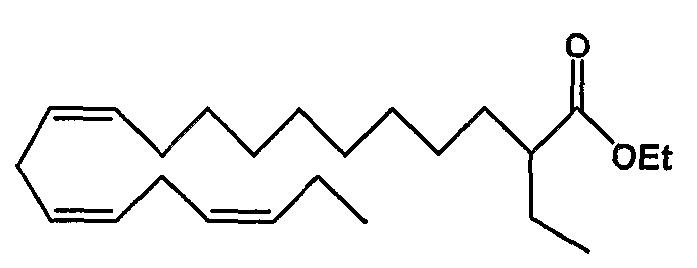
Этил (все-Z)-2-этил-11,14,17-эйкозатриеноат (28)
R1 = этил и R2 = атом водорода, или
R2 = этил и R1 = атом водорода
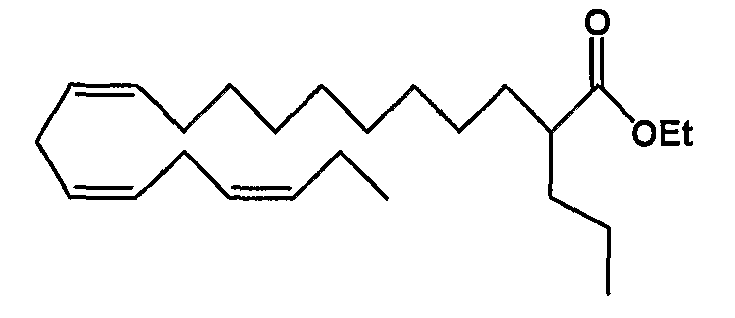
Этил (все-Z)-2-пропил-11,14,17-эйкозатриеноат (29)
R1 = пропил и R2 = атом водорода, или
R2 = пропил и R1 = атом водорода
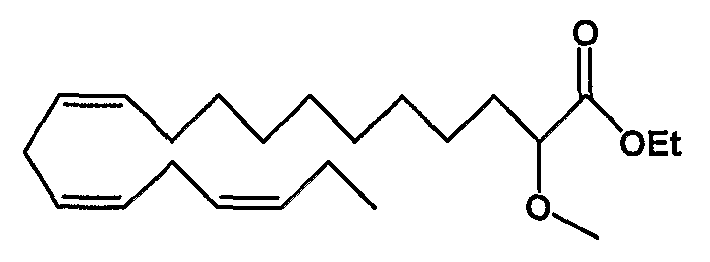
Этил (все-Z)-2-метокси-11,14,17-эйкозатриеноат (30)
R1 = метокси и R2 = атом водорода, или
R2 = метокси и R1 = атом водорода
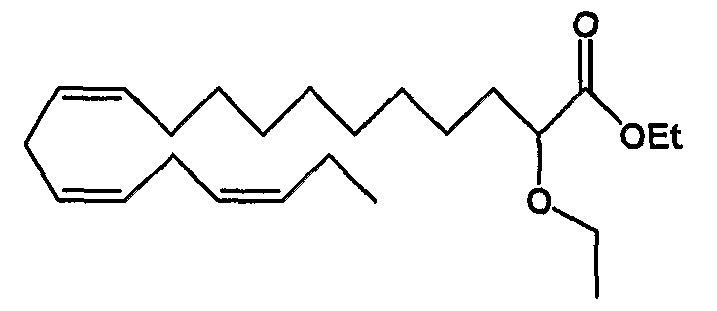
Этил (все-Z)-2-этокси-11,14,17-эйкозатриеноат (31)
R1 = этокси и R2 = атом водорода, или
R2 = этокси и R1 = атом водорода
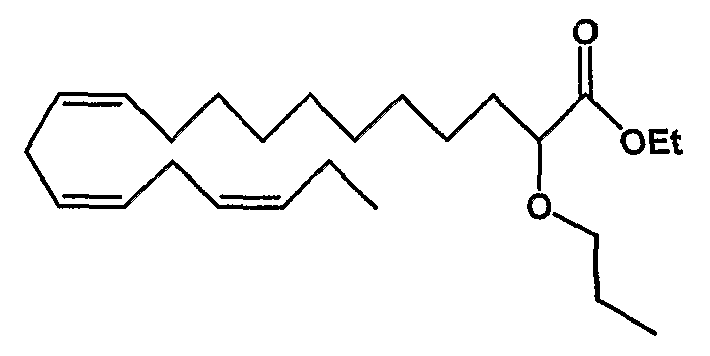
Этил (все-Z)-2-пропокси-11,14,17-эйкозатриеноат (32)
R1 = пропокси и R2 = атом водорода, или
R2 = пропокси и R1 = атом водорода
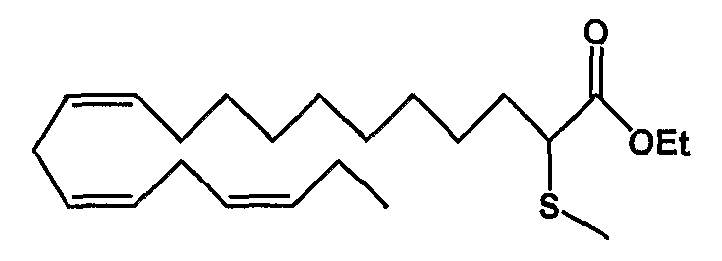
Этил (все-Z)-2-тиометил-11,14,17-эйкозатриеноат (33)
R1 = метилтио и R2 = атом водорода, или
R2 = метилтио и R1 = атом водорода
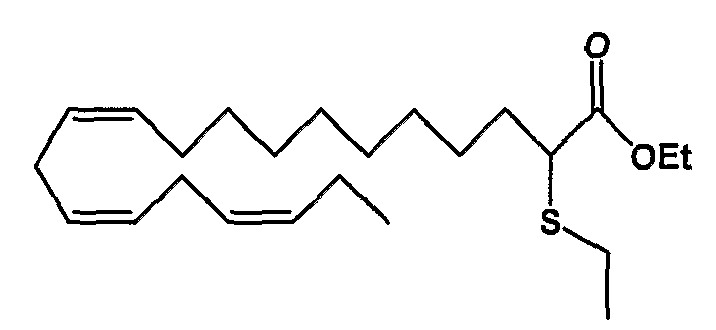
Этил (все-Z)-2-тиоэтил-11,14,17-эйкозатриеноат (34)
R1 = этилтио и R2 = атом водорода, или
R2 = этилтио и R1 = атом водорода
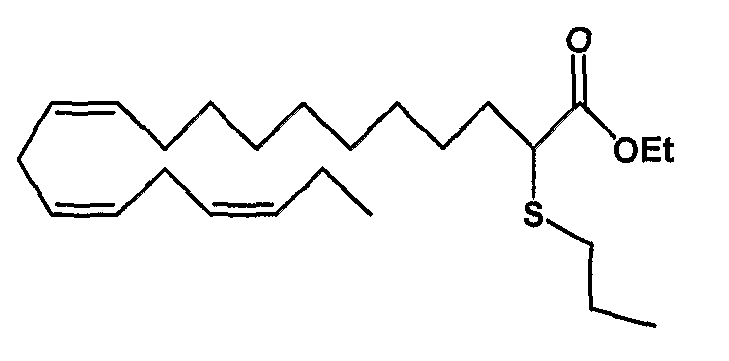
Этил (все-Z)-2-тиопропил-11,14,17-эйкозатриеноат (35)
R1 = пропилтио и R2 = атом водорода, или
R2 = пропилтио и R1 = атом водорода
Категория D - примеры (36)-(44):
Для всех примеров (36)-(44):
Y=С18 алкен с 5 двойными связями в положениях 4, 8, 11, 14 и 17, где двойные связи в положениях 8, 11, 14 и 17 имеют Z-конфигурацию, и двойная связь в положении 4 имеет Е-конфигурацию
Х = этилкарбоксилат
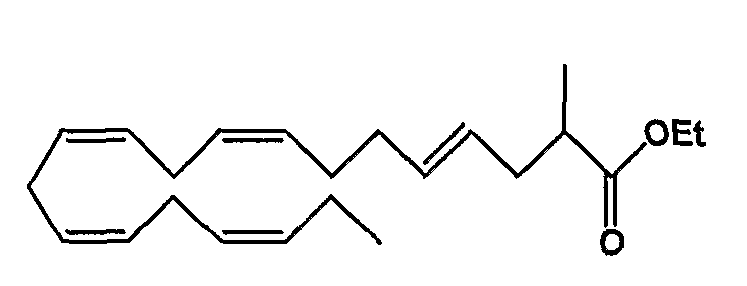
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-метил-4,8,11,14,17-эйкозапентаеноат (36)
R1 = метил и R2 = атом водорода, или
R2 = метил и R1 = атом водорода
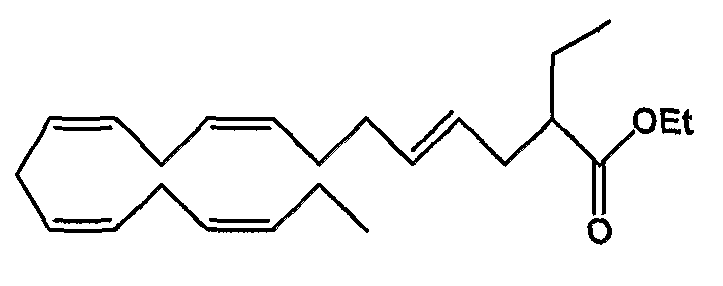
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-этил-4,8,11,14,17-эйкозапентаеноат (37)
R1 = этил и R2 = атом водорода, или
R2 = этил и R1 = атом водорода
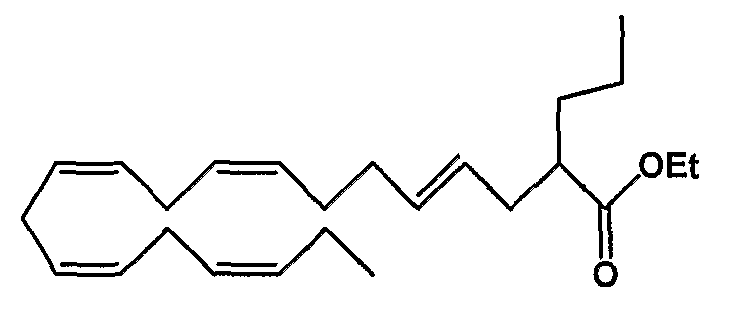
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-пропил-4,8,11,14,17-эйкозапентаеноат (38)
R1 = пропил и R2 = атом водорода, или
R2 = пропил и R1 = атом водорода
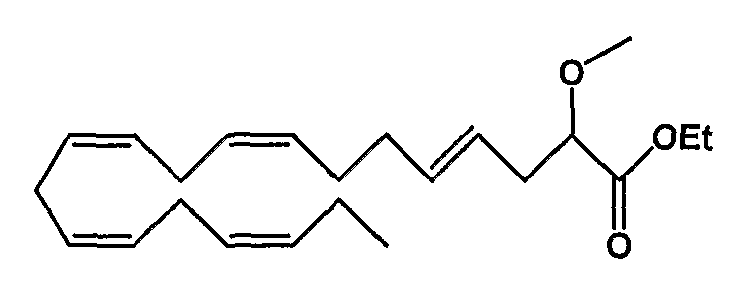
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-метокси-4,8,11,14,17-эйкозапентаеноат (39)
R1 = метокси и R2 = атом водорода, или
R2 = метокси и R1 = атом водорода
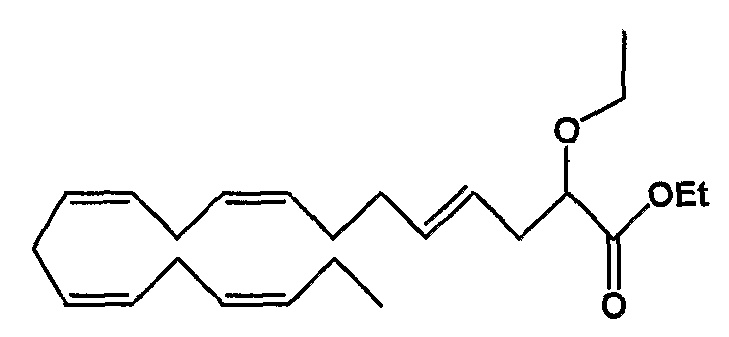
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-этокси-4,8,11,14,17-эйкозапентаеноат (40)
R1 = этокси и R2 = атом водорода, или
R2 = этокси и R1 = атом водорода
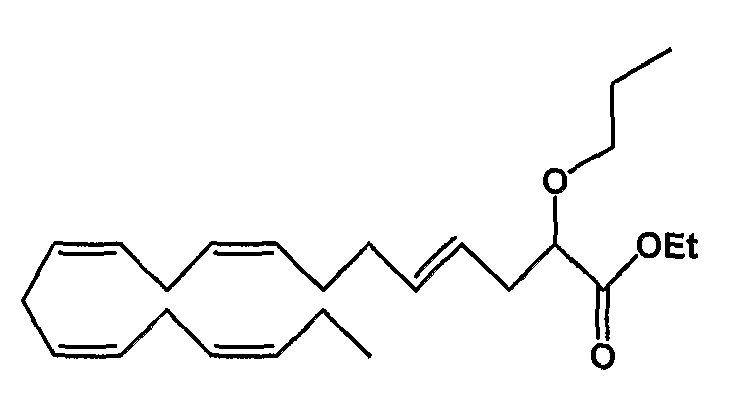
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-пропокси-4,8,11,14,17-эйкозапентаеноат (41)
R1 = пропокси и R2 = атом водорода, или
R2 = пропокси и R1 = атом водорода
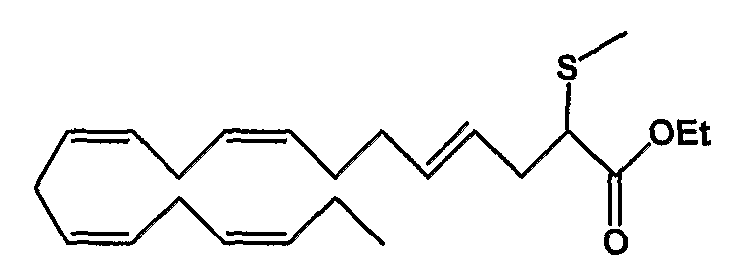
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-тиометил-4,8,11,14,17-эйкозапентаеноат (42)
R1 = метилтио и R2 = атом водорода, или
R2 = метилтио и R1 = атом водорода
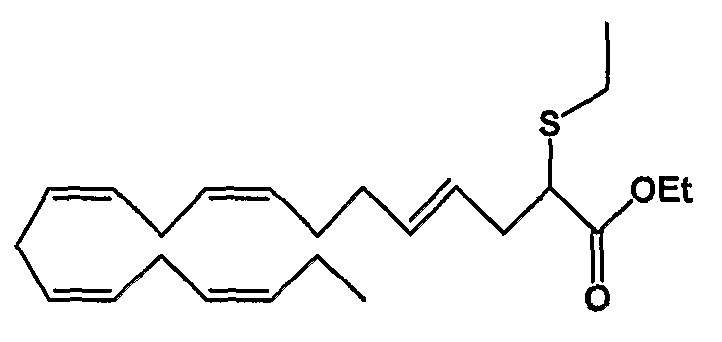
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-тиоэтил-4,8,11,14,17-эйкозапентаеноат (43)
R1 = этилтио и R2 = атом водорода, или
R2 = этилтио и R1 = атом водорода
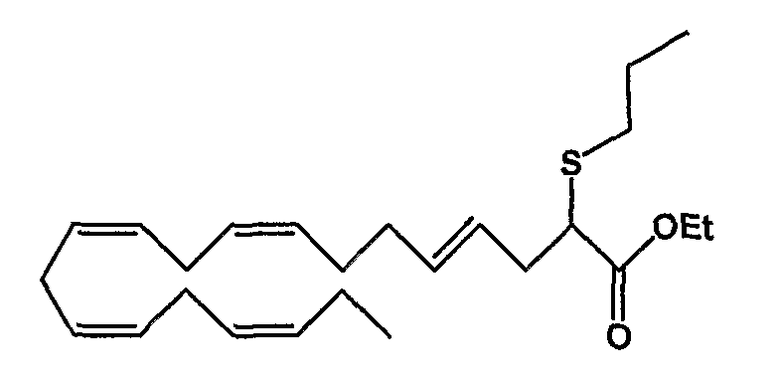
Этил (4Е, 8Z, 11Z, 14Z, 17Z)-2-тиопропил-4,8,11,14,17-эйкозапентаеноат (44)
R1 = пропилтио и R2 = атом водорода, или
R2 = пропилтио и R1 = атом водорода
Категория Е - примеры (45)-(50):
Для всех примеров (45)-(50):
Х = этилкарбоксилат
Y=С18 алкен с 5 двойными связями в Z-конфигурации в положениях 5, 8, 11, 14 и 17
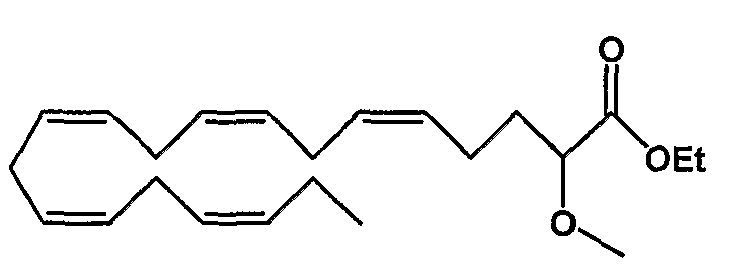
Этил (все-Z)-2-метокси-5,8,11,14,17-эйкозапентаеноат (45)
R1 = метокси и R2 = атом водорода, или
R2 = метокси и R1 = атом водорода
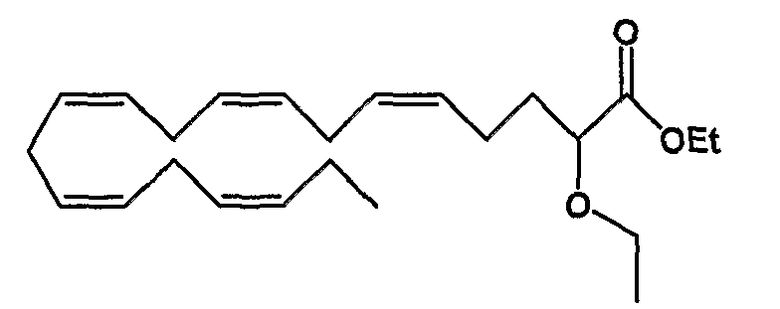
Этил (все-Z)-2-этокси-5,8,11,14,17-эйкозапентаеноат (46)
R1 = этокси и R2 = атом водорода, или
R2 = этокси и R1 = атом водорода
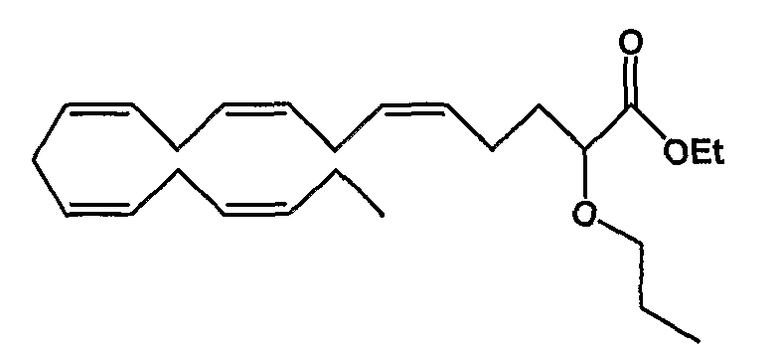
Этил (все-Z)-2-пропокси-5,8,11,14,17-эйкозапентаеноат (47)
R1 = пропокси и R2 = атом водорода, или
R2 = пропокси и R1 = атом водорода
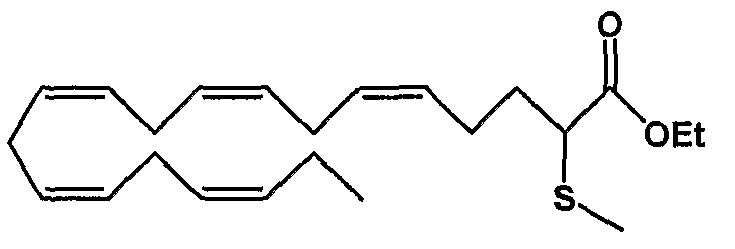
Этил (все-Z)-2-тиометил-5,8,11,14,17-эйкозапентаеноат (48)
R1 = метилтио и R2 = атом водорода, или
R2 = метилтио и R1 = атом водорода
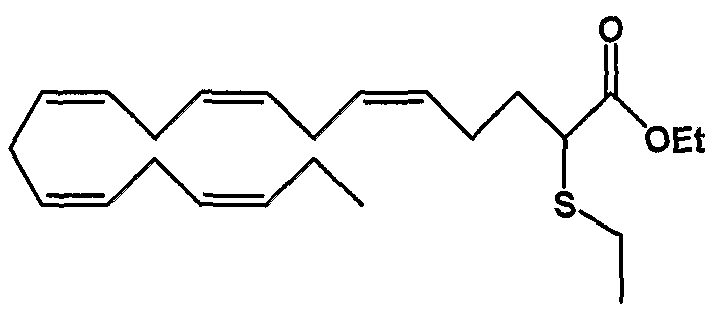
Этил (все-Z)-2-тиоэтил-5,8,11,14,17-эйкозапентаеноат (49)
R1 = этилтио и R2 = атом водорода, или
R2 = этилтио и R1 = атом водорода
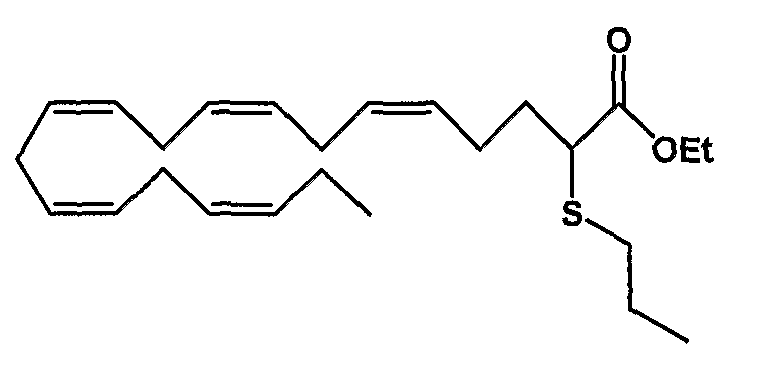
Этил (все-Z)-2-тиопропил-5,8,11,14,17-эйкозапентаеноат (50)
R1 = пропилтио и R2 = атом водорода, или
R2 = пропилтио и R1 = атом водорода
Категория F - примеры (51)-(59):
Для всех примеров (51)-(59):
Х = этилкарбоксилат
Y=С20 алкен с 6 двойными связями в положениях 4, 7, 10, 13, 16 и 19, где двойные связи в положениях 7, 10, 13, 16 и 19 имеют Z-конфигурацию, и двойная связь в положении 4 имеет Е-конфигурацию
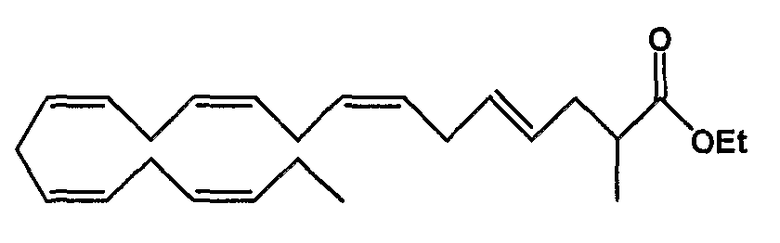
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-метил-4,7,10,13,16,19-докозагексаеноат (51)
R1 = метил и R2 = атом водорода, или
R2 = метил и R1 = атом водорода
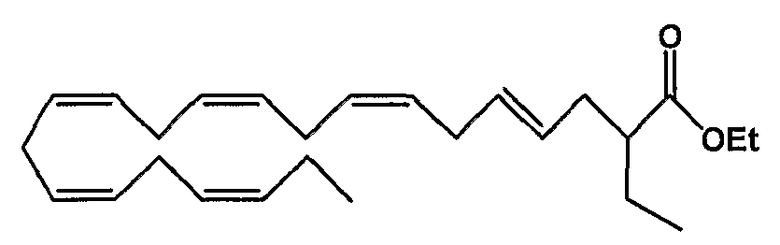
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-этил-4,7,10,13,16,19-докозагексаеноат (52)
R1 = этил и R2 = атом водорода, или
R2 = этил и R1 = атом водорода
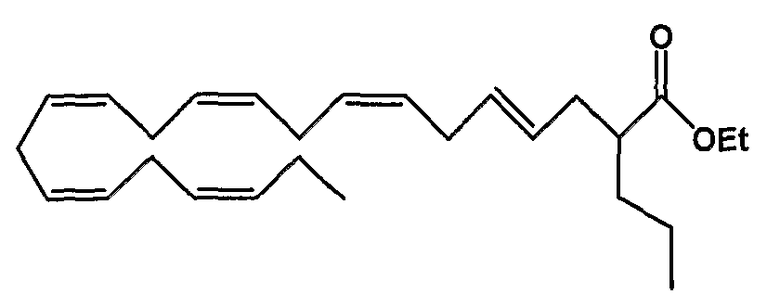
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-пропил-4,7,10,13,16,19-докозагексаеноат (53)
R1 = пропил и R2 = атом водорода, или
R2 = пропил и R1 = атом водорода
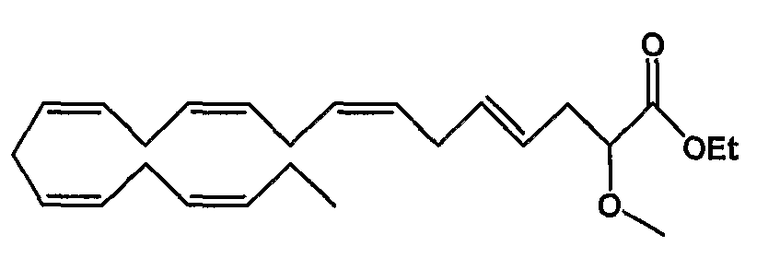
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-метокси-4,7,10,13,16,19-докозагексаеноат (54)
R1 = метокси и R2 = атом водорода, или
R2 = метокси и R1 = атом водорода
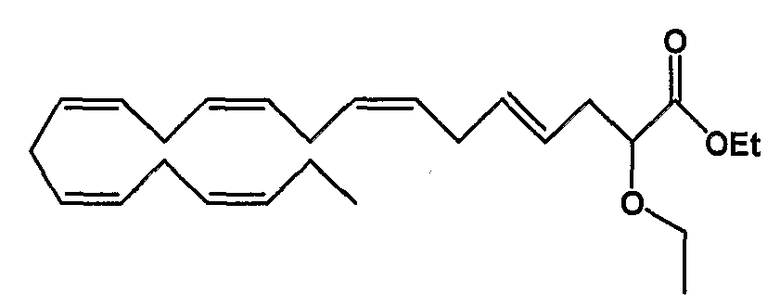
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-этокси-4,7,10,13,16,19-докозагексаеноат (55)
R1 = этокси и R2 = атом водорода, или
R2 = этокси и R1 = атом водорода
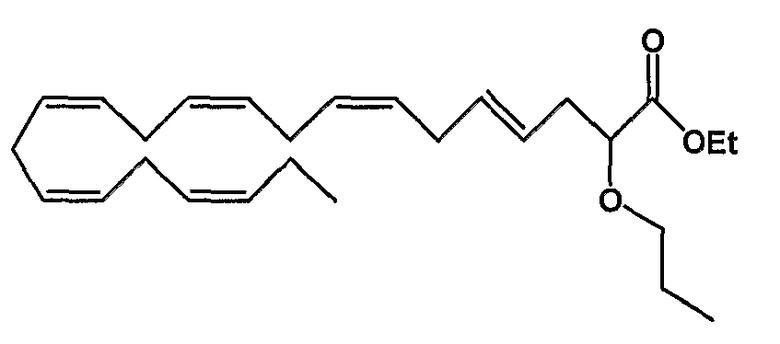
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-пропокси-4,7,10,13,16,19-докозагексаеноат (56)
R1 = пропокси и R2 = атом водорода, или
R2 = пропокси и R1 = атом водорода
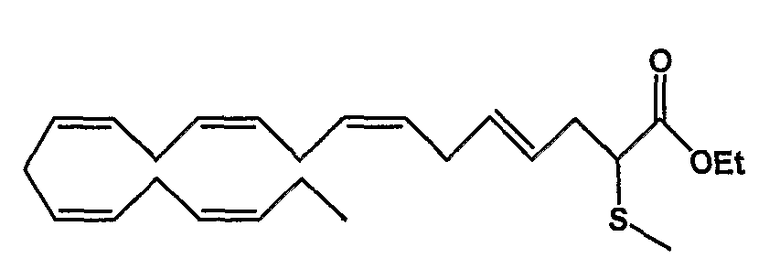
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-тиометил-4,7,10,13,16,19-докозагексаеноат (57)
R1 = метилтио и R2 = атом водорода, или
R2 = метилтио и R1 = атом водорода
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-тиоэтил-4,7,10,13,16,19-докозагексаеноат (58)
R1 = этилтио и R2 = атом водорода, или
R2 = этилтио и R1 = атом водорода
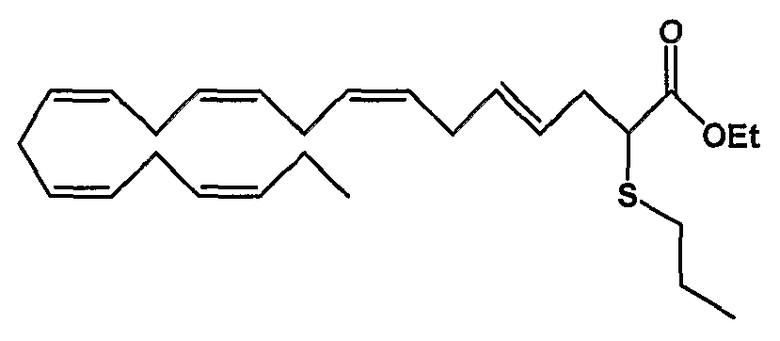
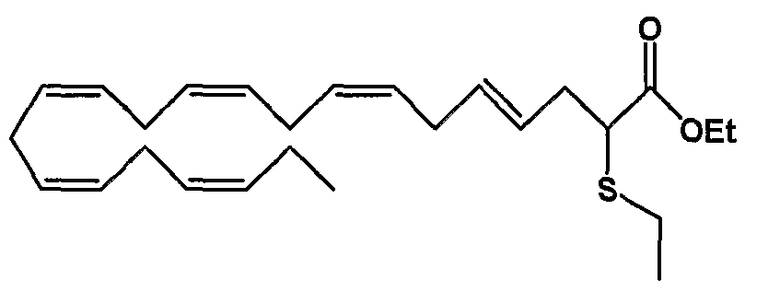
Этил (4Е, 7Z, 10Z, 13Z, 16Z, 19Z)-2-тиопропил-4,7,10,13,16,19-докозагексаеноат (59)
R1 = пропилтио и R2 = атом водорода, или
R2 = пропилтио и R1 = атом водорода
Другие примеры соединений согласно изобретению
Дополнительные предпочтительные соединения включают следующие соединения/промежуточные соединения:
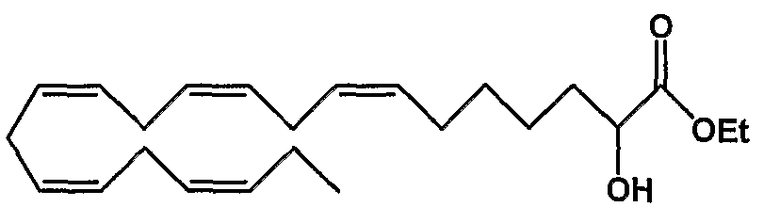
Этил (все-Z)-2-гидрокси-7,10,13,16,19-докозапентаеноат (65)
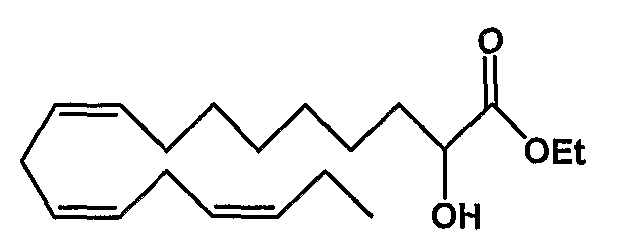
Этил (все-Z)-2-гидрокси-9,12,15-октадекатриеноат (61)
Соединения согласно категориям от A до F могут быть представлены в виде солей, в виде три-, ди- и моноглицеридов и фосфолипидов, как описано ранее.
Следует понимать, что настоящее изобретение охватывает все возможные фармацевтически приемлемые комплексы, сольваты или пролекарства омега-3 липидных соединений формулы (I).
“Пролекарства” являются веществами, которые могут обладать или не могут обладать фармакологической активностью как таковой, но могут быть введены (таким способом, как перорально или парентерально) и, следовательно, подвергнуты биоактивации (например, метаболизировать) в организме с образованием средства согласно настоящему изобретению, являющегося фармакологически активным.
“Фармацевтически активное количество” относится к количеству, которое приведет к желаемым фармакологическим и/или терапевтическим эффектам, т.е. количество омега-3 липидного соединения, которое является эффективным для достижения намеченной цели. Хотя требования отдельного больного могут изменяться, определение оптимальных диапазонов эффективных количеств омега-3 липидного соединения находится в компетентности специалиста в данной области техники. Обычно, режим дозирования для лечения состояния соединениями и/или композициями согласно данному изобретению выбирают в соответствии с рядом факторов, включающих тип, возраст, вес, пол, питание и медицинское состояние больного.
Под “лекарственным средством” подразумевают омега-3 липидное соединение формулы (I) в любом виде, подходящем для применения в медицинских целях, например, в виде лекарственного средства, фармацевтического средства или продукта, диетического продукта, продукта питания или пищевой добавки.
“Лечение” включает любое терапевтическое применение, которое может благоприятно воздействовать на человека или отличного от человека млекопитающего. Лечение, как человека, так и в области ветеринарии, входит в объем настоящего изобретения. Лечение может быть направлено на существующее состояние или на профилактику.
Омега-3 липидные соединения формулы (I) могут быть использованы как таковые, но обычно их вводят в виде фармацевтической композиции, в которой соединения формулы (I) (активный ингредиент) находятся в ассоциации с фармацевтически приемлемым носителем, эксципиентом или разбавителем (включая их комбинации).
Приемлемые носители, эксципиентом и разбавители для терапевтического использования хорошо известны в фармацевтической области и могут быть выбраны на основе предназначенного способа введения и стандартной фармацевтической практики. Примеры охватывают связующие вещества, лубриканты, суспендирующие средства, средства для покрытия, солюбилизирующие средства, консерванты, смачивающие средства, эмульгаторы, подсластители, красители, вкусовые ароматизирующие вещества, душистые вещества, буферы, суспендирующие средства, стабилизирующие средства и/или соли.
Фармацевтическая композиция согласно изобретению предпочтительно составлена для перорального введения человеку или животному. Фармацевтическая композиция также может быть составлена для введения любым другим способом, где активные ингредиенты могут быть эффективно поглощены и утилизированы, например, внутривенным, подкожным, внутримышечным, внутриназальным, ректальным, вагинальным или местным способом.
В отдельном варианте осуществления изобретения, фармацевтическая композиция сформирована в виде капсулы, которая также может быть микрокапсулой, образующей порошок или пакет-саше. Капсула может быть ароматизированной. Данный вариант осуществления изобретения включает капсулу, где капсула и инкапсулированная композиция согласно изобретению является ароматизированной. Благодаря ароматизации, капсула становится более привлекательной для пользователя. Что касается упомянутых выше целей терапевтического использования, вводимые дозировки, конечно, будут изменяться в зависимости от используемого соединения, способа введения, желаемого лечения и указанного нарушения.
Фармацевтическая композиция может быть составлена для предоставления суточной дозировки, например, от 5 мг до 10 г; от 50 мг до 1 г или от 50 мг до 200 г омега-3 липидного соединения. Под суточной дозировкой подразумевают дозировку на 24 часа.
Вводимые дозировки, конечно, будут изменяться в зависимости от используемого соединения, способа введения, желаемого лечения и указанного нарушения. Обычно, лечащий врач определяет фактическую дозировку, которая будет наиболее подходящей для отдельного субъекта. Отдельный дозовый уровень и частота дозировки для любого отдельного больного могут изменяться и будут зависеть от ряда факторов, включающих активность отдельного используемого соединения, метаболической устойчивости и продолжительности действия указанного соединения, возраста, массы тела, общего здоровья, пола, питания, способа и времени введения, скорости выведения, комбинации лекарственных средств, тяжести отдельного состояния и терапии, которой подвергается индивидуум. Омега-3 липидное соединение и/или фармацевтическая композиция согласно настоящему изобретению могут быть введены в соответствии с режимом от 1 до 10 раз в день, например, один или два раза в день. Что касается перорального и парентерального способа введения человеку, суточный уровень дозировки средства может быть в виде одной дозы или в виде разделенных доз.
Дальнейший аспект настоящего изобретения относится к липидной композиции, содержащей омега-3 липидные соединения формулы (I). Липидная композиция может содержать в диапазоне от 60 до 100% масс. омега-3 липидных соединений формулы (I), причем все проценты масс. основаны на общей массе липидной композиции. Например, по меньшей мере, 60%, по меньшей мере, 70%, по меньшей мере, 80% или, по меньшей мере, 95% масс. липидной композиции составляют омега-3 липидные соединения формулы (I).
Липидная композиция также может содержать, по меньшей мере, одну из жирных кислот (все-Z)-5,8,11,14,17-эйкозапентаеновую кислоту (ЕРА), (все-Z)-4,7,10,13,16,19-докозагексаеновую кислоту (DHA), (все-Z)-6,9,12,15,18-генэйкозапентаеновую кислоту (НРА), (все-Z)-7,10,13,16,19-докозапентаеновую кислоту (DPA, n-3), (все-Z)-8,11,14,17-эйкозатетраеновую кислоту (ЕТА, n-3), (все-Z)-4,7,10,13,16-докозапентаеновую кислоту (DPA, n-6) и/или (все-Z)-5,8,11,14-эйкозатетраеновую кислоту (ARA) или их производные, т.е. присутствующие в виде их альфа-замещенных соединений.
В отдельных вариантах осуществления изобретения, липидная композиция является фармацевтической композицией, пищевой композицией или композицией для диетического питания.
Липидная композиция также может содержать эффективное количество фармацевтически приемлемого антиоксиданта, например, токоферола или смеси токоферолов, в количестве вплоть до 4 мг на г, например, от 0,05 до 0,4 мг на г токоферолов от общей массы липидной композиции.
Омега-3 соединения и композиции согласно изобретению являются пригодными для лечения широкого диапазона заболеваний и состояний, как будет описано подробнее ниже.
Существует два основных типа сахарного диабета. Одним типом является диабет 1 типа, который известен как инсулинзависимый сахарный диабет (IDDM), и другим является диабет 2 типа, который известен как инсулиннезависимый сахарный диабет (NIDDM). Диабет 2 типа связан с ожирением/избыточной массой тела и отсутствием физической нагрузки, во многих случаях характеризуется постепенным началом заболевания, обычно у взрослых, и вызван снижением чувствительности тканей к действию инсулина, так называемой периферической инсулинорезистентностью. Это приводит к компенсаторному увеличению продукции инсулина. Указанную стадию до развития полностью сформировавшегося диабета 2 типа называют метаболическим синдромом, и она характеризуется гиперинсулинемией, инсулинорезистентностью, ожирением, отсутствием толерантности к глюкозе, гипертензией, аномальными липидами крови, гиперкоагулопатией, дислипидемией и воспалением. Таким образом, настоящее изобретение относится к применению омега-3 липидного соединения формулы (I) для получения лекарственного средства для лечения и/или предотвращения мультиметаболического синдрома, названного “метаболическим синдромом”, и связанных с ним состояний, упомянутых выше. В более позднем периоде, когда выработка инсулина тормозится, развивается сахарный диабет 2 типа. В одном варианте осуществления изобретения, соединения формулы (I) могут быть применены для лечения диабета 2 типа.
Омега-3 липидные соединения формулы (I) также могут быть применены для лечения других типов диабета, выбранных из группы, состоящей из вторичного диабета, такого как панкреатический диабет, экстрапанкреатический диабет/диабет, индуцированный эндокринными нарушениями или лекарственными средствами, или из исключительных форм диабета, таких как липоатрофический, миатонический или заболевание, вызванное нарушением рецепторов инсулина.
Соответственно, омега-3 липидные соединения формулы (I), как определено в описании выше, могут активировать ядерные рецепторы, предпочтительно PPAR (пролифераторами пероксисом активируемый рецептор) α и/или γ.
Омега-3 липидные соединения формулы (I) также могут быть использованы для лечения и/или предотвращения ожирения. Обычно, ожирение связано с повышенной инсулинорезистентностью, и тучные люди подвергаются высокому риску развития диабета 2 типа, который является основным фактором риска развития сердечно-сосудистых заболеваний. Ожирение является хроническим заболеванием, которым поражается все возрастающая часть населения в западных сообществах, и оно связано, не только с социальной проблемой, но также со снижением продолжительности жизни и многочисленными проблемами, например, сахарным диабетом, инсульнорезистентностью и гипертензией. Настоящее изобретение, таким образом, способствует удовлетворению в давно испытываемой потребности в лекарственном средстве, которое будет снижать общую массу тела, или количество жировой ткани, предпочтительно у тучных людей, приводя к идеальной массе тела без значительных неблагоприятных побочных эффектов.
Кроме того, неалкогольная жировая инфильтрация печени является общим состоянием, связанным с метаболическим синдромом. Точнее, жировая инфильтрация печени первоначально связана с гиперинсулинемией и инсулинорезистентностью. В одном варианте осуществления изобретения, омега-3 липидное соединение формулы (I) может действовать как чувствительное к инсулину средство и снижать жировую дегенерацию печени.
Кроме того, жировая инфильтрация печени встречается в двух основных формах - алкогольной и неалкогольной. Оба термина выражают накопление жира в печени с различной степенью повреждения печени, воспаления и фиброза. Диапазон заболевания жировой инфильтрации печени изменяется от простого стеатоза (признанный неопасным и непрогрессирующим) до стеатогепатита (жировая дегенерация печени с повреждением клеток печени и воспалением), до нарастающего фиброза и цирроза печени. Все указанные состояния включены в предотвращение и/или лечение омега-3 липидным соединением формулы (I) согласно изобретению.
Кроме того, омега-3 липидные соединения формулы (I), как определено в описании, являются чрезвычайно полезными для лечения и профилактики множества факторов риска, известных для сердечно-сосудистых заболеваний, таких как гипертензия, гипертриглицеридемия и высокая активность комплекса фактора коагуляции VII и фосфолипида. Омега-3 липидные соединения формулы (I) могут быть использованы для лечения повышенных уровней липидов в крови человека, действуя в качестве снижающих уровни липида лекарственных средств.
Настоящее изобретение также относится к применению омега-3 липидного соединения формулы (I) для получения лекарственного средства для снижения уровня триглицеридов в крови млекопитающих и/или повышения уровней HDL-холестерина (ЛПВП) в сыворотке больного человека.
В другом аспекте, настоящее изобретение относится к применению омега-3 липидного соединения формулы (I) для получения лекарственного средства или фармацевтического средства для лечения и/или предотвращения, по меньшей мере, одного из атеросклероза или IgA нефропатии, профилактики множества факторов риска сердечно-сосудистых заболеваний, сердечной недостаточности, мерцательной аритмии и/или постмиокардиального инфаркта, удара, церебральных или преходящих ишемических нарушений, связанных с атеросклерозом некоторых артерий, лечением ТВС или HIV (ВИЧ) и лечением HTG у больных ВИЧ.
В одном варианте осуществления изобретения, настоящее изобретение также относится к применению омега-3 липидного соединения формулы (I) для получения лекарственного средства или фармацевтического средства для лечения и/или предотвращения псориаза, рассеянного склероза и/или ревматоидного артрита.
Омега-3 липидные соединения формулы (I) или композиции, включающие омега-3 липидные соединения формулы (I), являются, по меньшей мере, одним из активаторов или модуляторов рецептора (PPAR)α, γ и/или δ человека, активированного пролифераторами пероксисом. Как было известно ранее, рецептор PPARα является более “неразборчивым” в сравнении с PPARγ, что означает, что рецептор PPARα связывается с большим рядом жирных кислот в качестве лигандов в сравнении с PPARγ. Однако поскольку больные с метаболическим синдромом или диабетом 2 типа, обычно, являются тучными или имеют избыточную массу тела, и в крови которых содержатся патологические липиды, в основном, повышенные уровни триглицеридов и низкие уровни холестерина высокой плотности (ЛПВП-хол), то активация рецептора PPARα представляется важной. Поэтому, в более специфическом варианте осуществления изобретения, соединение формулы (I) является селективным активатором или модулятором рецептора (PPAR)α человека, активируемого пролифераторами пероксисом. Кроме того, идеальное лекарственное средство для лечения метаболического синдрома или диабета 2 типа может действовать в качестве лиганда обоих указанных рецепторов. Таким образом, настоящее изобретение относится к применению соединения формулы (I) в качестве двойного активатора или модулятора активируемого пролифераторами пероксисом рецептора (PPAR) человека, α/γ и/или α/δ, предпочтительно активатора или модулятора PPAR α/γ. Настоящее изобретение также включает случай, когда соединения формулы (I) являются пан-агонистами PPAR (т.е. агонистами альфа-, бета- и гамма-рецепторов).
Способы получения соединений согласно изобретению
Омега-3 липидное соединение формулы (I), где R1 (или R2) является водородом, может быть получено следующими способами (схема 1). Омега-3 липидные соединения, представленные общей формулой (I), где R1 является водородом, и R2 означает С1-С6 алкильную группу, бензил, галоген, алкенил, алкинил, получают путем взаимодействия длинноцепочечного полиненасыщенного сложного эфира с сильным ненуклеофильным основанием, подобным литийдиизопропиламину, гексаметилдисилазиду калия/натрия или KH/NaH в ДМФА, в растворителе, таком как тетрагидрофуран, диэтиловый эфир при температуре от -60 до -78°С с получением сложного эфира енола (способ 1).
Способ I
Схема 1: R3 = алкильная группа (метил, этил, пропил)
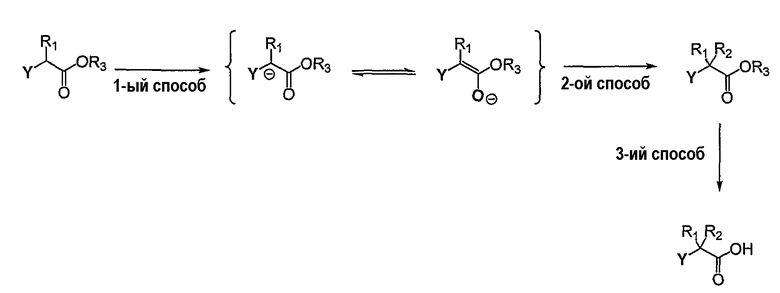
Указанный сложный эфир енолат взаимодействует с электрофильным реагентом, подобным галоидному алкилу, представленному йодистым этилом, бензилхлоридом, галоидангидриду карбоновой кислоты, представленному ацетилхлоридом, бензоилбромидом, ангидриду карбоновой кислоты, представленному уксусным ангидридом, или электрофильному галогенирующему реагенту, представленному N-фторбензолсульфонимидом (NFSI), N-бромсукцинимидом или йодом и т.д., с получением замещенного производного (способ 2). 2-Галогензамещенные производные соединения могут взаимодействовать с нуклеофильным реагентом, таким как тиолы, с получением 2-алкилтио-производных соединений.
Сложный эфир далее гидролизуется в растворителе, подобном этанолу или метанолу, до производного соединения карбоновой кислоты путем добавления основания, подобного гидроксиду лития/натрия/калия, в воде при температурах между 15°С и температурой образования флегмы.
Конденсация Кляйзена длинноцепочечного полиненасыщенного сложного эфира происходит во время обработки эфира сильным основанием. (Продукт конденсации может обладать интересующей биологической активностью. Таким образом, в одном варианте осуществления изобретения раскрыты продукт конденсации (промежуточное соединение), упомянутый выше, а также применение данного продукта для лечения и/или предотвращения заболеваний согласно настоящему изобретению).
Кроме того, в другом варианте осуществления изобретения, соединения, представленные общей формулой (I), синтезируют следующими способами (схема 2).
Способ II:
Схема 2: R3 = алкильная группа (метил, этил, пропил)
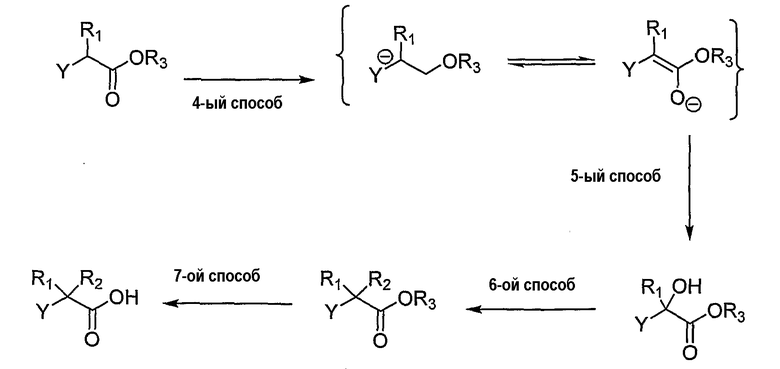
Соединения, представленные общей формулой (I), где R1 является водородом, и R2 означает гидроксигруппу, алкоксигруппу, ацилоксигруппу, получают путем взаимодействия длинноцепочечного полиненасыщенного сложного эфира с сильным ненуклеофильным основанием, подобным литийдиизопропиламину или гексаметилдисилазиду калия/натрия в растворителе, таком как тетрагидрофуран, диэтиловый эфир при температурах от -60 до -78°С с получением сложного эфира енола (способ 4). Данный сложный эфир енола взаимодействует с источником кислорода, подобным диметилдиоксирану, 2-(фенилсульфонил)-3-фенилоксазиридину, молекулярному кислороду с различными вспомогательными веществами, подобными триметилфосфиту, или различными катализаторами, подобными комплексу Ni(II), с получением сложного эфира альфа-гидроксикислоты (способ 5). При реакции вторичного спирта с основанием, подобным натрийгидриду, в растворителе, подобном ТГФ или ДМФА, образуется алкоголят, который взаимодействует с различными электрофильными реагентами, например, алкилйодидом, метилйодидом, этилйодидом; бензилбромидом или галоидангидридом карбоновой кислоты, например, ацетилхлоридом, бензоилбромидом (способ 6). Сложный эфир гидролизуется в растворителе, подобном этанолу или метанолу, до производного карбоновой кислоты путем добавления основания, подобного гидроксиду лития/натрия/калия в воде при температурах между 15°С и температурой образования флегмы (способ 7).
Сложный эфир альфа-гидроксикислоты является пригодным промежуточным соединением для введения других функциональных групп в α-положение согласно изобретению. Гидроксильная функция может быть активирована путем превращения в галоид или тозилат до взаимодействия с различными нуклеофилами, подобными аммиаку, аминам, тиолам и т.д. Реакция Мицунобу также применима для превращения гидроксильной группы в другие функциональные группы. (Mitsunobu, O., Synthesis, 1981, 1).
Соединения, представленные общей формулой (I), где R1 является водородом, и R2 означает алкил, фенил, гидроксиметил, карбоксил, алкоксикарбонил, гидрокси, алкоксигруппу, ацилокси, могут быть получены путем взаимодействия длинноцепочечного полиненасыщенного тозилата, мезилата или галоида с диалкилмалонатом или замещенными диалкилмалонатами. Способ III, схема 3. Гидролиз диэфира и декарбоксилирование приводят к альфа-замещенным продуктам.
Способ III
Схема 3
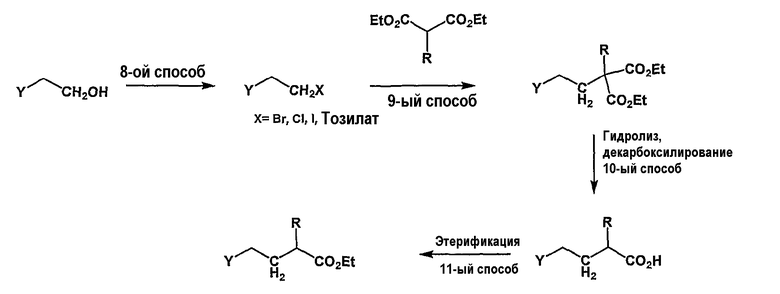
Длинноцепочечные полиненасыщенные тозилаты, используемые в способе III, могут быть получены из соответствующего длинноцепочечного полиненасыщенного спирта. Такие спирты могут быть получены непосредственно из сложных эфиров карбоновых кислот природных ненасыщенных жирных кислот: альфа-линоленовой кислоты, конъюгированной линоленовой кислоты, эйкозапентаеновой кислоты и т.д., путем реакции восстановления посредством восстанавливающего реагента, подобного литийалюминийгидриду или диизобутилалюминийгидриду при температуре от -10 до 0°С. Используя спирт, полученный из этил (все-Z)-5,8,11,14,17-эйкозапентаеноата в последовательности реакций, описанных в способе III, могут быть получены 2-замещенные производные DPA. Спирты также могут быть получены путем деградации полиненасыщенных жирных кислот EPA и DHA, как описано Holmeide et al. (J. Chem. Soc., Perkin Trans. 1, 2000, 2271). В данном случае способ можно начинать с очищенной EPA или DHA, но также его можно начинать с рыбьего жира, содержащего EPA и DHA в смеси. Причиной тому является то, что DHA реагирует быстрее в реакции йодолактонизации, чем ЕРА, с образованием йод-δ-лактона (Corey et al., Proc. Natl. Acad. Sci. USA, 1983, 3581, Wright et al., J. Org. Chem., 1987, 4399, Kuklev et al., Phytochemistry, 1992, 2401). (все-Z)-3,6,9,12,15-Октадекапентаенол может быть получен из DHA способом, описанным в указанной выше литературе. Используя указанный выше спирт в качестве реагента в способах III, могут быть получены 2-замещенные производные ЕРА.
Комбинируя способ III со способом I, можно получить дизамещенные производные.
Способ IV
Соединения формулы (I), где Х является карбоновой кислотой в виде фосфолипида, могут быть получены следующими способами.
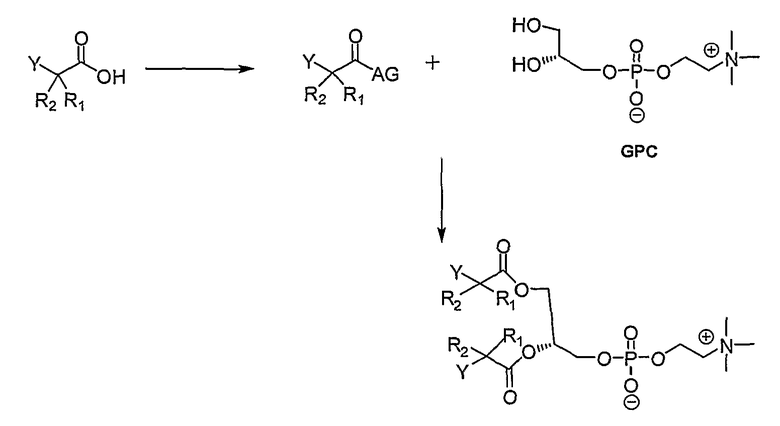
Ацилирование sn-глицеро-3-фосфохолина (GPC) активированной жирной кислотой, такой как имидазолиды жирной кислоты, является стандартной процедурой в синтезе фосфатидилхолина. Обычно, синтез осуществляют в присутствии ДМСО-аниона с ДМСО в качестве растворителя (Hermetter; Chemistry and Physics of lipids, 1981, 28, 111). Sn-Глицеро-3-фосфохолин, как аддукт кадмия(II), также может взаимодействовать с имидазолидом активированной жирной кислотой в присутствии DBU (1,8-диазабицикло[5.4.0]ундек-7-ен) с получением фосфатидилхолина соответствующей жирной кислоты (международная заявка номер РСТ/GB2003/002582). Ферментативное трансфосфатидилирование может привести к трансформации фосфатидилхолина в фосфатидилэтаноламин (Wang et al., J. Am. Chem. Soc., 1993, 115, 10487).
Полиненасыщенные соединения, содержащие фосфолипиды, могут быть получены различными путями, главным образом, химическим синтезом фосфолипидов, как описано, ферментативной этерификацией и трансэтерификацией фосфолипидов или ферментативным трансфосфатидилированием фосфолипидов. (Hosokawa, J. Am. Oil Chem. Soc. 1995, 1287, Lilja-Hallberg, Biocatalysis, 1994, 195). В случае применения ферментов, предпочтительным вариантом осуществления изобретения является соединение формулы (I), где R1 или R2 представляет собой водород.
Соединения формулы (I), где Х является карбоновой кислотой в виде триглицерида, могут быть получены следующими способами. Избыток новой жирной кислоты может быть сочетан с глицерином с использованием диметиламинопиридина (DMAP) и 2-(1H-бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфата (HBTU).
Соединения формулы (I), где Х является карбоновой кислотой в виде диглицерида, могут быть получены реакцией жирной кислоты (2 эквивалента) с глицерином (1 эквивалент) в присутствии 1,3-дициклогексилкарбодиимида (DCC) и 4-диметиламинопиридина (DMAP).
Соединения формулы (I), где Х является карбоновой кислотой в виде моноглицерида, могут быть получены следующими способами. Ацилирование 1,2-O-изопропилиден-sn-глицерина жирной кислотой с использованием DCC и DMAP в хлороформе приводит к монодиеноилглицерину. Удаление защитной изопропилиденовой группы может быть осуществлено путем обработки защищенного глицерина кислотой (HCl, уксусная и т.д.) (O'Brian, J. Org. Chem., 1996, 5914).
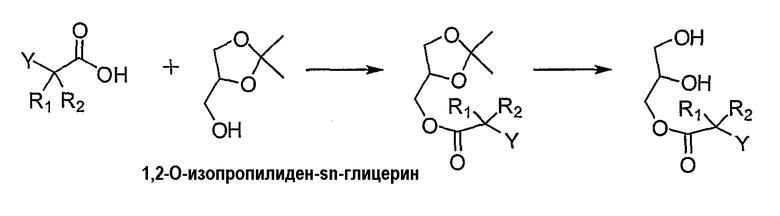
Существует несколько общих синтетических способов получения моноглицеридов с жирной кислотой в 2-положении. В одном способе используют этерификацию жирной кислоты глицидолом в присутствии хлоргидрата 1-(3-диметиламинопропил)-3-этилкарбодиимида (EDC) и 4-диметиламинопиридина (DMAP) с получением глицидильного производного. Обработкой глицидильного производного трифторуксусным ангидридом (TFAA) перед трансэтерификацией получают моноглицерид (Parkkari et al, Bioorg. Med. Chem. Lett. 2006, 2437).
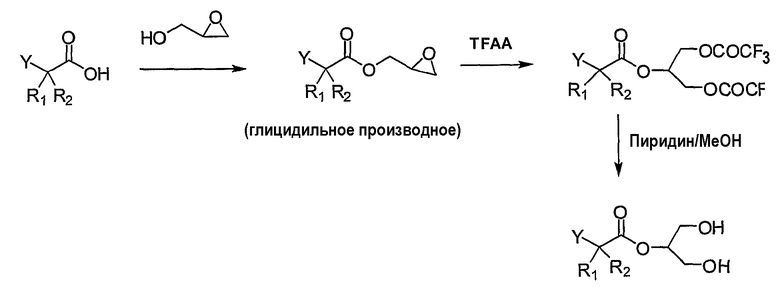
Другие общие способы получения моно-, ди- и триглицеридов производных жирных кислот описаны в Международной патентной заявке, РСТ/FR02/02831.
Также возможно использовать ферментативные способы (реакции с липазой) для превращения жирных кислот в моно-, ди-, триглицерид. 1,3-Региоспецифическая липаза из гриба Mucor miehei может быть использована для получения триглицеридов или диглицеридов из полиненасыщенных жирных кислот и глицерина. Другая липаза, нерегиоспецифическая липаза дрожжей Candida antartica является высокоэффективной в образовании триглицеридов из полиненасыщенных жирных кислот (Haraldsson, pharmazie, 2000, 3). Для данной ферментативной реакции, предпочтительным вариантом осуществления изобретения является соединение формулы I, где R1 и R2 являются водородом.
Протоколы синтеза
Изобретение будет описано подробнее посредством следующих примеров, которые не должны рассматриваться как ограничивающие изобретение. В следующих примерах структуры были подтверждены ЯМР и масс-спектрометрией (МС). Спектры ЯМР были записаны в CDCl3. Величины J даны в Гц.
Этил (все-Z)-2-этил-7,10,13,16,19-докозапентаеноат (14)
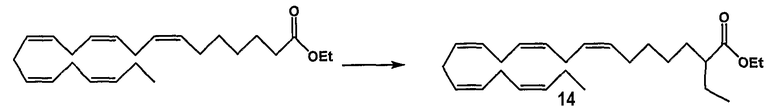
Бутиллитий (0,96 мл, 1,54 ммоль, 1,6 М в гексане) добавляли по каплям к перемешиваемому раствору диизопропиламина (0,23 мл, 1,60 ммоль) в сухом ТГФ (5 мл) в атмосфере N2 при 0°C. Образовавшийся раствор перемешивали при 0°С в течение 20 мин, охлаждали до -78°С и перемешивали дополнительные 10 мин до добавления по каплям этил (все-Z)-7,10,13,16,19-докозапентаеноата (0,50 г, 1,40 ммоль) в сухом ТГФ (5 мл) в течение 10 мин. Раствор зеленого цвета перемешивали при -78°С в течение 10 мин до добавления этилйодида (0,16 мл, 2,09 ммоль). Образовавшийся раствор оставляли до достижения температуры окружающей среды в течение одного часа, распределяли между водой (10 мл) и гептаном (10 мл). Водный слой экстрагировали гептаном (20 мл), и объединенный органический слой промывали 1 М HCl и сушили (Na2SO4). Концентрирование при пониженном давлении и очистка флэш-хроматографией (гептан:EtOAc 98:2) привели к 0,37 г (68%) указанного в заголовке соединения 14 в виде бесцветного масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,83-0,99 (м, 6H), 1,20-1,60 (м, 11H), 2,05 (м, 4H), 2,19 (м, 1H), 2,81 (м, 8H), 4,11 (кв, 2H), 5,35 (м, 10H);
13C-ЯМР (50 МГц, CDCl3) δ 11,72, 14,18, 14,28, 20,47, 25,43, 25,45, 25,54, 26,99, 29,45, 30,22, 31,91, 37,70, 47,19, 59,82, 85,73, 126,94, 127,72, 127,79, 127,85, 128,05, 128,09, 128,36, 128,44, 129,97, 176,17;
МС (электрораспыление): 409,3 [M+Na].
Этил (все-Z)-2-гидрокси-7,l0,13,16,19-докозапентаеноат (65)
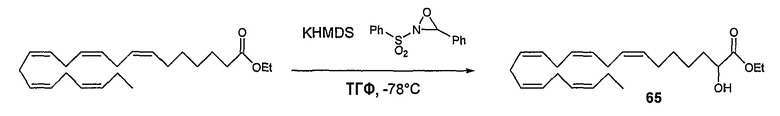
Раствор KHMDS (533,9 мг, 2,68 ммоль) в ТГФ, 10 мл, охлаждали до -78°C в атмосфере N2 до добавления по каплям раствора (все-Z)-7,10,13,16,19-докозапентаеноата (478,8 мг, 1,33 ммоль) в ТГФ, 2,5 мл. Смесь перемешивали при -78°С в течение 30 минут до добавления по каплям раствора транс-2-(фенилсульфонил)-3-фенилоксазиридина (реагент Дэвиса) (525,3 мг, 2,01 ммоль) в ТГФ, 1,5 мл. Реакционную смесь перемешивали при -78°С в течение 1 часа 50 минут до гашения реакции насыщенным раствором NH4Cl, 20 мл, после нагревания до комнатной температуры смесь экстрагировали диэтиловым эфиром, 50 мл×2, органическую фазу промывали насыщенным раствором соли, 20 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме. Полученный сырой продукт подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан/EtOAc (100:1)-(95:5), с получением 293 мг (59%) продукта 65 в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,95 (т, J=7,5 Гц, 3H), 1,28 (т, J=7,1 Гц, 3H), 1,38-1,46 (м, 4H), 1,49-1,81 (м, 2H), 2,02-2,13 (м, 4H), 2,76-2,85 (м, 9H), 4,12 (дд, J=2,5, 6,9 Гц, 1H), 4,22 (кв, J=7,1 Гц, 2H), 5,32-5,41 (м, 10H).
13C ЯМР (50 МГц, CDCl3) δ 14,1, 14,2, 20,4, 24,4, 25,5, 25,6, 27,0, 29,3, 34,3, 61,5, 70,3, 127,0, 127,8, 127,87, 127,92, 128,08, 128,15, 128,4, 128,5, 129,9, 132,0, 175,3 (2 сигнала невидимы).
МС (электрораспыление): 397 [M+Na]+.
Этил (все-Z)-2-этокси-7,10,13,16,19-докозапентаеноат (17)
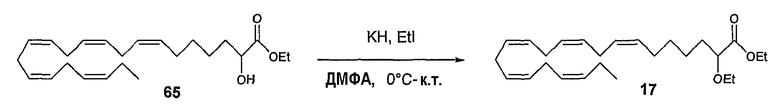
Суспензию 35% КН (92,4 мг, 0,806 ммоль КН) в ДМФА, 3 мл, охлаждали в атмосфере N2 до 0°С, и добавляли по каплям раствор этил (все-Z)-2-гидрокси-7,10,13,16,19-докозапентаеноата (65) (101 мг, 0,27 ммоль) в ДМФА, 2 мл. Смесь перемешивали в течение 30 минут при 0°С до добавления EtI (0,22 мл, 2,73 ммоль). Затем, смесь оставляли медленно достигать комнатной температуры и перемешивали в течение 4 часов. Реакцию гасили насыщенным раствором NH4Cl, 20 мл, и экстрагировали диэтиловым эфиром, 50 мл×2. Органическую фазу промывали насыщенным раствором соли, 20 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме и подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан:EtOAc (100:1)-(95:5), с получением 19,4 мг (18%) продукта 17 в виде бесцветной жидкости.
1Н ЯМР (300 МГц, CDCl3) δ 0,95 (т, J=7,5 Гц, 3H), 1,20 (т, J=7,0 Гц, 3H), 1,26 (т, J=7,1 Гц, 3H), 1,31-1,47 (м, 5H), 1,66-1,72 (м, 2H), 2,03-2,11 (м, 5H), 2,77-2,84 (м, 6H), 3,33-3,47 (м, 1H), 3,55-3,65 (м, 1H), 3,78 (т, J=6,4 Гц, 1H), 4,14-4,22 (м, 2H), 5,27-5,39 (м, 10H).
13C ЯМР (75 МГц, CDCl3) δ 14,3, 15,2, 20,6, 25,0, 25,5, 25,6 (2 сигнала), 27,0, 29,3, 32,9, 60,6, 65,9, 79,0, 127,0, 127,9 (2 сигнала), 128,0, 128,1, 128,2, 128,4, 128,5, 130,0, 132,0, 173,2 (2 сигнала невидимы).
МС (электрораспыление): 425 [M+Na]+.
(все-Z)-2-Этокси-7,10,13,16,19-докозапентаеновая кислота (69)
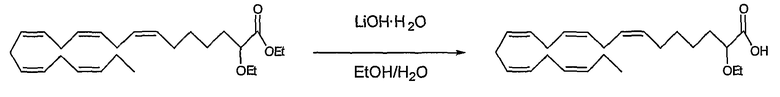
К раствору этил (все-Z)-2-этокси-7,10,13,16,19-докозапентаеноата (17) (66,1 мг, 0,164 ммоль) в EtOH (5 мл) добавляли раствор LiOH·H2O (57,7 мг, 1,38 ммоль) в воде (5 мл). Реакционную смесь перемешивали в атмосфере N2 при 80°С в течение 19½ часов. После охлаждения, 1 М HCl добавляли (до рН~1). Полученную смесь экстрагировали диэтиловым эфиром (50 мл), сушили (MgSO4) и упаривали в вакууме с получением 55 мг (90%) указанного в заголовке соединения в виде светло-желтого масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,95 (т, J=7,5 Гц, 3H), 1,24 (т, J=7,0 Гц, 3H), 1,38-1,41 (м, 4H), 1,75-1,85 (м, 2H), 2,03-2,13 (м, 4H), 2,80-2,83 (м, 8H), 3,46-3,71 (м, 2H), 3,88 (т, J=5,8 Гц, 1H), 5,23-5,44 (м, 10H).
МС (электрораспыление): 373 [M-Н]-.
Этил (все-Z)-2-этил-9,12,15-октадекатриеноат (2)
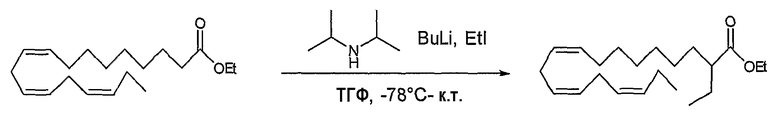
К раствору диизопропиламина (265 мкл, 1,88 ммоль) в сухом ТГФ, 5 мл, в атмосфере N2 при 0°С добавляли по каплям 1,6 М BuLi в гексане (1,15 мл, 1,84 ммоль). Полученную смесь перемешивали при -78°С в течение 20 минут до добавления по каплям раствора этил (все-Z)-9,12,15-октадекатриеноата (502 мг, 1,64 ммоль) в ТГФ, 5 мл. Полученную реакционную смесь перемешивали в течение 30 минут при -78°С до добавления по каплям EtI (0,20 мл, 2,48 ммоль). Охлаждающую баню отставляли, реакционную смесь перемешивали в течение 3 часов 45 минут до гашения реакции водой, 25 мл, и экстрагировали диэтиловым эфиром, 50 мл×2. Органическую фазу промывали 1 М HCl (водн.), 20 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме. Полученный сырой продукт подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан/EtOAc (100:1), с получением 216 мг (39%) этил (все-Z)-2-этил-9,12,15-октадекатриеноата (2) в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,84 (т, J=7,4 Гц, 3H), 0,93 (т, J=7,5 Гц, 3H), 1,21 (т, J=7,1 Гц, 3H), 1,25 (м, 8H), 1,33-1,65 (м, 4H), 2,02 (кв, J=7,0 Гц, 4H), 2,13-2,27 (м, 1H), 2,76 (т, J=5,6 Гц, 4H), 4,10 (кв, J=7,1 Гц, 2H), 5,20-5,41 (м, 6H).
13C ЯМР (50 МГц, CDCl3) δ 11,7, 14,2, 14,3, 20,5, 25,4, 25,5, 27,1, 27,3, 29,0, 29,4, 29,5, 32,0, 47,2, 59,8, 127,0, 127,6, 128,1, 130,1, 131,8, 176,2 (2 сигнала невидимы)
МС (электрораспыление): 357 [M+Na]+.
(все-Z)-2-Этил-9,12,15-октадекатриеновая кислота (70)
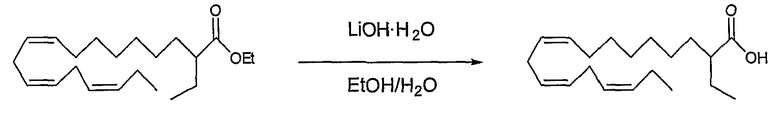
К раствору этил (все-Z)-2-этил-9,12,15-октадекатриеноата (2) (111 мг, 0,312 ммоль) в EtOH (10 мл) добавляли раствор LiOH·H2O (108 мг, 2,57 ммоль) в воде (10 мл). Реакционную смесь перемешивали в атмосфере N2 при 80°С в течение 15 часов. После охлаждения, добавляли 1 M HCl (до pH ~2). Образовавшуюся смесь экстрагировали диэтиловым эфиром (50 мл), сушили (MgSO4) и упаривали в вакууме с получением 81 мг (79%) указанного в заголовке соединения в виде желтого масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,83-0,99 (м, 6H), 1,20-1,29 (м, 8H), 1,41-1,78 (м, 4H), 1,99-2,13 (м, 4H), 2,21-2,30 (м, 1H), 2,76-2,82 (м, 4H), 5,23-5,44 (м, 6H).
МС (электрораспыление): 305 [M-Н]-.
Этил (все-Z)-2-йод-9,12,15-октадекатриеноат (60)
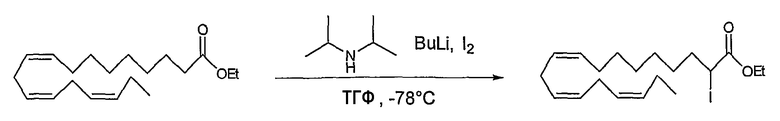
К раствору диизопропиламина (322 мкл, 2,28 ммоль) в сухом ТГФ, 5 мл, в атмосфере N2 при 0°С добавляли по каплям 1,6 М BuLi в гексане (1,25 мл, 2,0 ммоль). Образовавшуюся смесь перемешивали при -78°С в течение 20 минут до добавления по каплям раствора этил (все-Z)-9,12,15-октадекатриеноата (501 мг, 1,63 ммоль) в ТГФ, 5 мл. Полученную реакционную смесь желтого цвета перемешивали в течение 35 минут при -78°С до добавления по каплям раствора I2 (704 мг, 2,77 ммоль) в ТГФ, 5 мл. Реакционную смесь перемешивали при -78°С в течение 25 минут до гашения реакции 1 M HCl, 20 мл, и экстрагировали гептаном, 50 мл. Органическую фазу промывали 10% Na2S2O3 (водн.), 25 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме. Полученный сырой продукт подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан/EtOAc (100:1), с получением 152 мг (22%) этил (все-Z)-2-йод-9,12,15-октадекатриеноата (60) в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,95 (т, J=7,5 Гц, 3H), 1,25 (т, J=7,1 Гц, 3H), 1,30 (м, 8H), 1,89-2,09 (м, 6H), 2,78 (т, J=5,5 Гц, 4H), 4,13-4,28 (м, 3H), 5,25-5 (м, 6H).
13C ЯМР (50 МГц, CDCl3) δ 13,7, 14,2, 20,5, 21,4, 25,5, 25,6, 27,1, 28,5, 28,9, 26,3, 29,4, 36,0, 61,6, 127,0, 127,8, 128,2, 128,3, 130,1, 131,9, 171,4.
МС (электрораспыление): 455 [M+Na]+.
Этил (все-Z)-2-тиометил-9,12,15-октадекатриеноат (7)
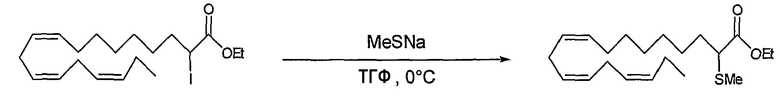
Этил (все-Z)-2-йод-9,12,15-октадекатриеноат (60) (146 мг, 0,338 ммоль) растворяли в ТГФ, 5 мл, и охлаждали до 0°С в атмосфере N2 до добавления MeSNa. Реакционную смесь перемешивали при 0°С в течение 1 часа до разбавления ее гептаном, 50 мл, промывали водой, 2×20 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме. Полученный сырой продукт подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан/EtOAc (100:1)-(95:5), с получением 110 мг (92%) этил (все-Z)-2-тиометил-9,12,15-октадекатриеноата (7) в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,94 (т, J=7,5 Гц, 3H), 1,23 (т, J=7,1 Гц, 3H), 1,29 (м, 8H), (м, 1H), (м, 1H), 2,09 (c, 3H), 1,97-2,13 (м, 8H), 2,77 (т, J=5,6 Гц, 4H), 3,12 (дд, J=6,8, 8,3 Гц, 1H), 4,17 (кв, J=7,1 Гц, 2H), 5,26-5,37 (м, 6H).
13C ЯМР (50 МГц, CDCl3) δ 13,7, 14,2, 20,5, 25,5, 25,6, 27,1, 27,2, 28,97, 29,04, 29,4, 30,6, 47,3, 60,9, 127,1, 127,7, 128,17, 128,23, 130,1, 131,9, 172,4 (1 сигнал невидим).
МС (электрораспыление): 375 [M+Na]+.
Этил (все-Z)-2-гидрокси-9,12,15-октадекатриеноат (61)
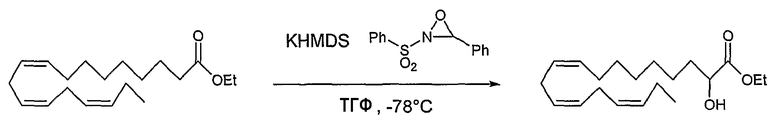
Раствор KHMDS (5,24 г, 26,2 ммоль) в ТГФ, 100 мл, охлаждали до -78°С в атмосфере N2 до добавления по каплям раствора этил (все-Z)-9,12,15-октадекатриеноата (4,01 г, 13,1 ммоль) в ТГФ, 25 мл. Смесь перемешивали при -78°С в течение 30 минут до добавления по каплям раствора транс-2-(фенилсульфонил)-3-фенилоксазиридина (реагент Дэвиса) (5,13 г, 19,6 ммоль) в ТГФ, 15 мл. Реакционную смесь перемешивали при -78°С в течение 1½ часов до гашения реакции насыщенным раствором NH4Cl, 30 мл, после нагревания до комнатной температуры смесь экстрагировали диэтиловым эфиром, 100 мл×2, органическую фазу промывали насыщенным раствором соли, 30 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме. Полученный сырой продукт подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан/EtOAc (100:1)-(95:5), с получением 2,67 г (63%) этил (все-Z)-2- гидрокси-9,12,15-октадекатриеноата (61) в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,92 (т, J=7,5 Гц, 3H), 1,24 (т, J=7,1 Гц, 3H), 1,28 (м, 8H), 1,53-1,75 (м, 2H), 1,96-2,10 (м, 4H), 2,76 (т, J=5,6 Гц, 5H), 4,11 (дд, J=4,0, 6,7 Гц, 1H), 4,19 (кв, J=7,1 Гц, 2H), 5,22-5,41 (м, 6H).
13C ЯМР (50 МГц, CDCl3) δ 14,09, 14,14, 20,4, 24,6, 25,4, 25,5, 27,1, 29,0, 29,1, 29,4, 34,3, 61,4, 70,3, 127,0, 127,7, 128,11, 128,14, 130,1, 131,8, 175,3.
МС (электрораспыление): 345 [M+Na]+.
Этил (все-Z)-2-этокси-9,12,15-октадекатриеноат (5)
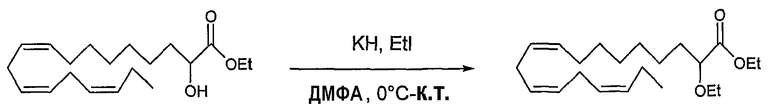
Суспензию 35% КН (84,3 мг, 0,735 ммоль КН) в ДМФА, 2 мл, охлаждали в атмосфере N2 до 0°С, и раствор этил (все-Z)-2-гидрокси-9,12,15-октадекатриеноата (61) (119,7 мг, 0,37 ммоль) в ДМФА, 2 мл, добавляли по каплям. Смесь перемешивали в течение 30 минут при 0°С до добавления EtI (0,15 мл, 1,87 ммоль). Затем, смесь оставляли медленно достигать комнатной температуры и перемешивали в течение ночи. Реакцию гасили насыщенным раствором NH4Cl, 20 мл, и реакционную смесь экстрагировали диэтиловым эфиром, 50 мл×2. Органическую фазу промывали насыщенным раствором соли, 20 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме и подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан:EtOAc (100:1)-(95:5), получая 31,5 мг (24%) продукта 5 в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,95 (т, J=7,5 Гц, 3H), 1,20 (т, J=7,0 Гц, 3H), 1,22-1,30 (м, 11H), 1,63-1,71 (м, 2H), 1,98-2,12 (м, 4H), 2,78 (т, J=5,5 Гц, 4H), 3,33-3,45 (м, 1H), 3,52-3,64 (м, 1H), 3,78 (т, J=6,4 Гц, 1H), 4,12-4,24 (м, 2H), 5,27-5,40 (м, 6H).
13C ЯМР (50 МГц, CDCl3) δ 14,2, 15,1, 20,5, 25,2, 25,5, 25,6, 27,2, 29,0, 29,1, 29,2, 29,5, 33,0, 60,6, 65,9, 79,0, 127,1, 127,7, 128,2 (2 сигнала), 130,2, 131,9, 173,3.
МС (электрораспыление): 373 [M+Na]+.
Этил (все-Z)-2-фталимид-9,12,15-октадекатриеноат (62)
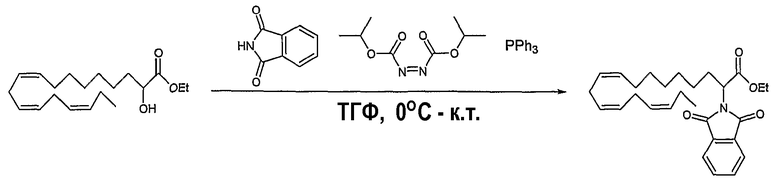
Раствор этил (все-Z)-2-гидрокси-9,12,15-октадекатриеноата (61) (176,8 мг, 0,548 ммоль), фталимида (97,6 мг, 0,663 ммоль) и трифенилфосфина (178,3 мг, 0,680 ммоль) в ТГФ охлаждали до 0°С в атмосфере N2 до добавления диизопропилазодикарбоксилата (DIAD) (128 мкл, 0,660 ммоль). Охлаждающую баню отставляли, и смесь перемешивали в течение 22 часов. Реакционную смесь упаривали в вакууме и подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан:EtOAc (95:5)-(4:1), с получением 153,8 мг (62%) этил (все-Z)-2-фталимид-9,12,15-октадекатриеноата (62) в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,92 (т, J=7,5 Гц, 3H), 1,18 (т, J=7,1 Гц, 3H), 1,29 (м, 8H), 1,97-2,10 (м, 4H), 2,17-2,24 (м, 2H), 2,72-2 ,79 (м, 4H), 4,17 (кв, J=7,1 Гц, 2H), 4,79 (дд, J=9,6, 6,0 Гц, 1H), 5,24-5,35 (м, 6H), 7,68-7,74 (м, 2H), 7,79-7,85 (м, 2H).
13C ЯМР (50 МГц, CDCl3) δ 14,0, 14,2, 20,4, 25,4, 25,5, 26,2, 27,0, 28,5, 28,8, 28,9, 29,4, 52,3, 61,6, 123,4, 127,0, 127,6, 128,11, 128,16, 130,1, 131,7, 131,8, 134,0, 167,6, 169,3.
МС (электрораспыление): 474 [M+Na]+.
Этил (все-Z)-2-амино-9,12,15-октадекатриеноат (12)
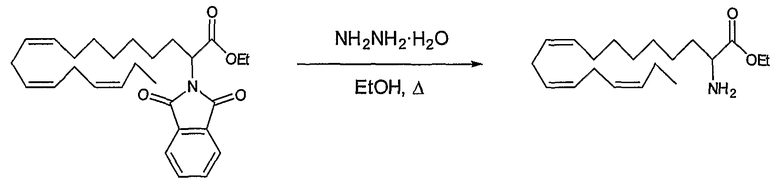
К раствору этил (все-Z)-2-фталимид-9,12,l5-октадекатриеноата (62) (104,6 мг, 0,232 ммоль) в EtOH, 4 мл, добавляли гидрат гидразина (17 мкл, 0,35 ммоль), и смесь кипятили с обратным холодильником в атмосфере N2 в течение 15 часов. Реакционную смесь охлаждали, упаривали в вакууме и подвергали флэш-хроматографии на силикагеле, элюируя смесью CH2C12:2M NH3 в MeOH (97,5:2,5), с получением 58,4 мг (78%) этил (все-Z)-2-амино-9,12,15-октадекатриеноата (12) в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,92 (т, J=7,5 Гц, 3H), 1,21 (т, J=7,1 Гц, 3H), 1,27 (м, 8H), 1,37-1,69 (м, 4H), 1,95-2,09 (м, 4H), 2,74 (т, J=5,6 Гц, 4H), 3,36 (ушир.c, 1H), 4,11 (кв, J=7,1 Гц, 2H), 5,22-5,37 (м, 6H).
13C ЯМР (50 МГц, CDCl3) δ 14,1 (2 C), 20,4, 25,4, 25,45, 25,49, 27,1, 29,0, 29,2, 29,4, 34,8, 54,3, 60,6, 127,0, 127,6, 128,11, 128,15, 130,1, 131,8, 176,1.
МС (электрораспыление): 322 [M+H]+, 344 [M+Na]+.
Этил (все-Z)-2-диэтиламино-9,12,15-октадекатриеноат (10) и этил (все-Z)-2-этиламино-9,12,15-октадекатриеноат (11)
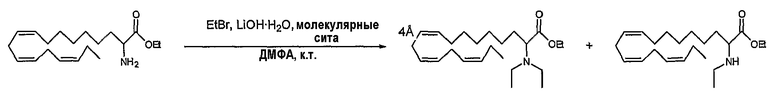
К смеси этил (все-Z)-2-амино-9,12,15-октадекатриеноата (12) (551,7 мг, 1,72 ммоль), LiOH·H2O (144,6 мг, 3,45 ммоль) и молекулярных сит 4Å (507 мг) в ДМФА, 4 мл, добавляли этилбромид (2,6 мл, 34,8 ммоль), и образовавшуюся смесь перемешивали при температуре окружающей среды в течение 46 часов. Смесь разбавляли диэтиловым эфиром, 100 мл, и фильтровали. Органическую фазу промывали 1 M NaOH, 20 мл, и насыщенным раствором соли, 20 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме и подвергали флэш-хроматографии на силикагеле, элюируя смесью гептан:EtOAc (95:5)-CH2Cl2:2M NH3 в MeOH (98:2), с получением 357 мг (55%) диэтиламино-производного сложного эфира 10 в виде бесцветной жидкости и 161 мг (27%) этиламино-производного сложного эфира 11 в виде жидкости желтого цвета.
Этил (все-Z)-2-диэтиламино-9,12,15-октадекатриеноат (10)
1Н ЯМР (200 МГц, CDCl3) δ 0,93 (т, J=7,5 Гц, 3H), 0,99 (т, J=7,1 Гц, 6H), 1,22 (т, J=7,1 Гц, 3H), 1,27 (м, 8H), 1,51-1,70 (м, 2H), 1,96-2,11 (м, 4H), 2,43 (секстет, J=6,8 Гц, 2H), 2,66 (кв, J=7,3 Гц, 2H), 2,71-2,79 (м, 4H), 3,28 (т, J=7,4 Гц, 1H), 4,10 (кв, J=7,1 Гц, 2H), 5,22-5,38 (м, 6H).
13C ЯМР (50 МГц, CDCl3) δ 13,9, 14,2, 14,4, 20,5, 25,4, 25,5, 26,3, 27,1, 29,1, 29,3, 29,5, 29,9, 44,4, 59,7, 63,0, 127,0, 127,6, 128,2 (2C), 130,2, 131,8, 173,5.
МС (электрораспыление): 378 [M+H]+, 400 [M+Na]+.
Этил (все-Z)-2-этиламино-9,12,15-октадекатриеноат (11)
1Н ЯМР (200 МГц, CDCl3) δ 0,91 (т, J=7,5 Гц, 3H), 1,02 (т, J=1,1 Гц, 3H), 1,24 (м, 11H), 1,55 (м, 3H), 1,94-2,08 (м, 4H), 2,35-2,65 (м, 2H), 2,73 (т, J=5,6 Гц, 4H), 3,14 (т, J=6,6 Гц, 1H), 4,11 (кв, J=7,1 Гц, 2H), 5,17-5,38 (м, 6H).
13C ЯМР (50 МГц, CDCl3) δ 14,1, 14,2, 15,2, 20,4, 25,4, 25,5, 25,6, 27,0, 28,9, 29,2, 29,4, 33,5, 42,3, 60,3, 61,3, 127,0, 127,6, 128,09, 128,11, 130,1, 131,8, 175,5.
МС (электрораспыление): 350 [M+H]+, 372 [M+Na]+.
(все-Z)-4,7,10,13,16,19-докозагексаенол (63)
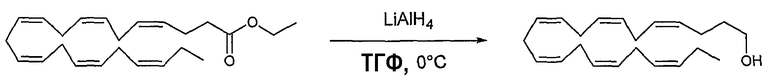
Раствор этил (все-Z)-4,7,10,13,16,19-докозагексаеноата (10,72 г, 30,0 ммоль) в ТГФ, 30 мл, добавляли по каплям к суспензии LiAlH4 в THH, 140 мл, в атмосфере N2 при 0°С. Образовавшуюся смесь перемешивали при 0°С в течение 50 минут до гашения реакции водой, 50 мл, добавляли 1 M HCl, 100 мл, и перемешивали при комнатной температуре в течение 1 часа. Фазы разделяли, и водную фазу экстрагировали диэтиловым эфиром, 100 мл×2. Органическую фазу промывали 1M HCl, 50 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме с получением 8,56 г (91%) (все-Z)-4,7,10,13,16,19-докозагексаенола (63) в виде бесцветной жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 1,00 (т, J=7,5 Гц, 3H), 1,63-1,73 (м, 2H), 1,83 (ушир.c, 1H), 2,04-2,24 (м, 4H), 2,88 (ушир.c, 10H), 3,67 (т, J=6,4 Гц, 2H), 5,41 (ушир.c, 12H).
(все-Z)-4,7,10,13,16,19-докозагексаентозилат (64)
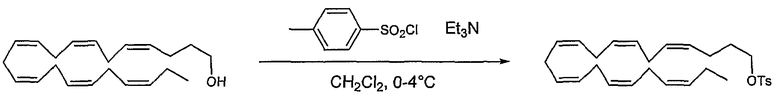
Раствор (все-Z)-4,7,10,13,16,19-докозагексаенола (63) (8,50 г, 27,0 ммоль) и тозилхлорида (5,41 г, 28,4 ммоль) в сухом CH2Cl2, 30 мл, охлаждали до 0°С до добавления Et3N (4,15 мл, 29,8 ммоль). Реакционную смесь помещали в холодильник. Через 17 часов, добавляли дополнительное количество тозилхлорида (774 мг, 4,06 ммоль) и Et3N (565 мкл, 4,06 ммоль), и смесь помещали в холодильник на 21½ часов. Реакционную смесь выливали в воду со льдом и экстрагировали CH2Cl2, 50 мл×2, и упаривали в вакууме. Остаток растворяли в гептане, 100 мл, промывали водой, 30 мл, 1M HCl, 30 мл×2, и насыщенным раствором соли, 30 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме. К остатку добавляли пиридин, 1,6 мл, и воду, 1,25 мл, и перемешивали при комнатной температуре в течение 1 часа. Смесь разбавляли гептаном, 100 мл, и промывали водой, 25 мл, 1 M HCl, 25 мл×2, насыщенным раствором соли, 25 мл, сушили (Na2SO4), фильтровали и упаривали в вакууме с получением 10,27 г (81%) тозилата 64 в виде бесцветного масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,94 (т, J=7,5 Гц, 3H), 1,61-1,75 (м, 2H), 1,97-2,12 (м, 4H), 2,41 (c, 3H), 2,70-2,89 (м, 10H), 4,00 (т, J=6,4 Гц, 2H), 5,27-5,38 (м, 12H), 7,31 (д, 2H), 7,76 (д, 2H).
МС (электрораспыление): 491 [M+Na]+.
(все-Z)-9,12,15-октадекатриенол (66)
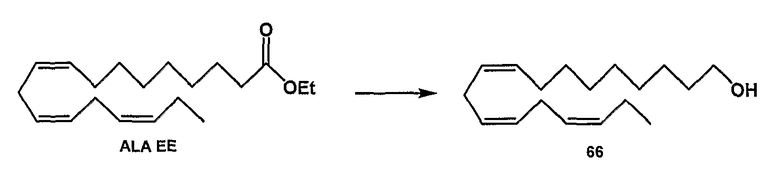
К перемешиваемой суспензии LAH (0,130 г, 3,43 ммоль) в сухом ТГФ (10 мл), которую держали при 0°С в инертной атмосфере, добавляли по каплям раствор этил (все-Z)-9,12,15- октадекатриеноата (1,0 г, 3,26 ммоль) в сухом ТГФ (15 мл). Образовавшийся раствор перемешивали при 0°С в течение одного часа, добавляли 10% раствор NH4Cl (15 мл) и фильтровали через невысокий слой целита. Целит промывали водой (10 мл) и гептаном (20 мл), и слои разделяли. Водный слой экстрагировали гептаном (20 мл), и объединенные органические слои промывали насыщенным раствором соли (20 мл) и сушили (MgSO4). Синтез привел к 0,78 г (91%) (все-Z)-9,12,15-октадекатриенола (66) в виде бесцветного масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,95 (т, 3Н), 1,20-1,35 (м, 10Н), 1,48-1,58 (м, 2Н), 1,98-2,09 (м, 4Н), 2,76-2,82 (м, 4Н), 5,23-5,44 (м, 6Н);
МС (электрораспыление): 287,3 [M+Na]+.
(все-Z)-9,12,15-октадекатриентозилат (67)

К перемешиваемому раствору (все-Z)-9,12,15-октадекатриенола (66) (0,78 г, 2,95 ммоль) в сухом CH2Cl2 (15 мл), который держали при 0°С в инертной атмосфере, добавляли толуол-4-сульфонилхлорид (1,12 г, 5,90 ммоль) и Et3N (0,82 мл, 5,90 ммоль). Образовавшийся раствор перемешивали при 0°С в течение пяти часов и затем в течение 66 часов при температуре окружающей среды. Смесь выливали в воду со льдом (40 мл), и слои разделяли. Водный слой экстрагировали CH2Cl2 (20 мл), и объединенный органический слой концентрировали. К сырому продукту добавляли 2 мл пиридина и 1,6 мл воды, и смесь перемешивали при температуре окружающей среды в течение 30 минут. Гептан (70 мл) добавляли, и органический слой промывали водой (30 мл), 1M HCl (30 мл) и насыщенным раствором соли (30 мл). Сушка (MgSO4) и концентрирование при пониженном давлении привели к 0,68 г (55%) тозилата 67 в виде бесцветного масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,91 (т, 3H), 1,15-1,35 (м, 10H), 1,53-1,60 (м, 2H), 1,98-2,12 (м, 4H), 2,43 (c, 3H), 2,70-2,80 (м, 4H), 5,22-5,40 (м, 6H), 7,31 (д, 2H), 7,76 (д, 2H);
МС (электрораспыление): 441,2 [M+Na].
Этил (все-Z)-2-этил-2-этоксикарбонил-ll,14,17-эйкозатриеноат (23)
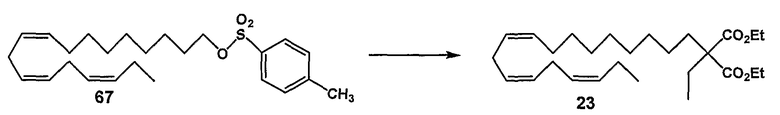
К перемешиваемой суспензии NaH (60%, 0,098 г, 2,44 ммоль) в сухом ТГФ (15 мл) и сухом ДМФА (3 мл), которую держали при 0°С в инертной атмосфере, добавляли по каплям диэтил этилмалонат (0,61 мл, 3,25 ммоль). Образовавшуюся смесь перемешивали при 0°С в течение десяти минут, доводили температуру до температуры окружающей среды и перемешивали еще 20 минут. Тозилат 67 (0,68 г, 1,62 ммоль) в сухом ТГФ (3 мл) добавляли, с последующим добавлением NaI (0,098 г, 0,65 ммоль). Затем, образовавшийся раствор перемешивали при 70°С в течение четырех часов, охлаждали и распределяли между 10% NH4Cl (30 мл) и гептаном (30 мл). Водный слой экстрагировали гептаном (20 мл), и объединенный органический слой промывали насыщенным раствором соли (30 мл) и сушили (Na2SO4). Данный синтез привел к 0,70 г (количественный выход) указанного в заголовке соединения 23 в виде бесцветного масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,91 (т, 3H), 1,18-1,30 (м, 19H), 1,80-2,10 (м, 10H), 2,75-2,81 (м, 4H), 4,16 (м, 4H), 5,28-5,38 (м, 6H);
МС (электрораспыление): 457,3 [M+Na].
(все-Z)-2-этил,2-карбокси-ll,14,17-эйкозатриеновая кислота (24)
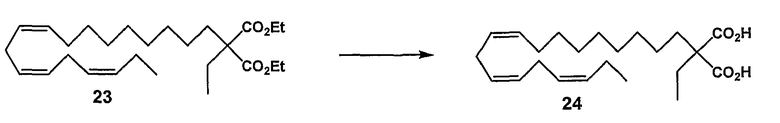
Этил (все-Z)-2-этил,2-этоксикарбонил-11,14,17-эйкозатриеноат (23) (0,70 г, 1,61 ммоль) растворяли в 96% этаноле (20 мл) и добавляли 5M KOH (2,6 мл, 13 ммоль). Образовавшуюся смесь перемешивали при кипячении с обратным холодильником в течение 19 часов, охлаждали и концентрировали при пониженном давлении. К полученному сырому продукту добавляли 1M HCl (20 мл) и экстрагировали дважды диэтиловым эфиром (30 мл). Объединенный органический слой промывали насыщенным раствором соли (30 мл) и сушили (MgSO4). Концентрирование при пониженном давлении привело к 0,60 г (количественный выход) указанного в заголовке соединения 24 в виде светло-коричневого масла.
МС (электрораспыление): 377,2 [M-H].
(все-Z)-2-этил-ll,14,17-эйкозатриеновая кислота (68)
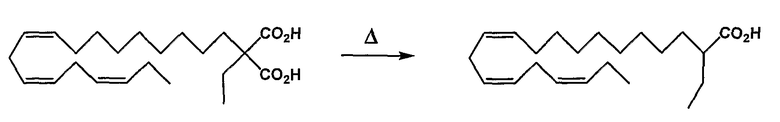
Чистую (все-Z)-2-этил,2-карбокси-11,14,17-эйкозатриеновую кислоту (24) (0,60 г, 1,59 ммоль) в инертной атмосфере нагревали при 160°С в течение двух часов, охлаждали и очищали флэш-хроматографией (гептан:EtOAc 9:1, затем 4:1). Данная процедура привела к 0,33 г (62%) указанной в заголовке (все-Z)-2-этил-l1,14,17-эйкозатриеновой кислоты (68) в виде бесцветного масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,84-0,99 (м, 8H), 1,15-1,35 (м, 10H), 1,35-1,70 (м, 4H), 2,00-2,15 (м, 4H), 2,20-2,30 (м, 1H), 2,75-2,85 (м, 4H), 5,25-5,45 (м, 6H);
МС (электрораспыление): 333,2 [M-H].
Этил (все-Z)-2-этил-ll,14,17-эйкозатриеноат (28)
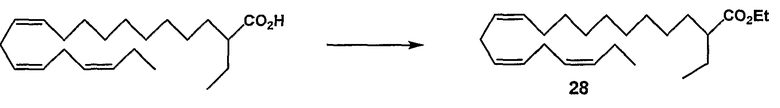
(все-Z)-2-Этил-l1,14,17-эйкозатриеновую кислоту (0,15 г, 0,45 ммоль) растворяли в абсолютном EtOH (5 мл), добавляли по каплям концентрированную H2SO4 и перемешивали при кипячении с обратным холодильником в инертной атмосфере в течение 18 часов. Смесь охлаждали, концентрировали и очищали флэш-хроматографией (гептан:EtOAc 95:5). Данная процедура привела к 0,13 г (80%) указанного в заголовке соединения 28 в виде бесцветного масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,85 (т, 3H), 0,94 (т, 3H), 1,18-1,34 (м, 13H), 1,45-1,59 (м, 4H), 1,97-2,08 (м, 4H), 2,25 (м, 1H), 2,74-2,85 (м, 4H), 4,09 (кв, 4H), 5,24-5,42 (м, 6H);
13C ЯМР (50 МГц, CDCl3) δ 11,76, 14,21, 14,30, 20,49, 25,46, 25,56, 27,18, 27,37, 29,22, 29,41, 29,42, 29,50, 29,59, 32,06, 47,29, 59,83, 127,06, 127,59, 128,18, 128,21, 130,27, 131,85, 176,33;
МС (электрораспыление): 385,3 [M+Na]+.
2-((все-Z)-2-Этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицерин (71)
Стадия 1: Глицидил (все-Z)-2-этил-5,8,11,14,17-
эйкозапентаеноат
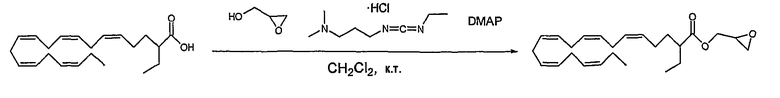 Раствор (все-Z)-2-этил-5,8,11,14,17-эйкозапентаеновой кислоты (1,00 г, 3,03 ммоль), глицидола (167 мкл, 2,52 ммоль), хлоргидрата N-этил-N'-(3-диметиламинопропил)карбодиимида (585 мг, 3,05 ммоль) и DMAP (372 мг, 3,05 ммоль) в сухом CH2Cl2 (10 мл) перемешивали в течение 18 часов в атмосфере N2 при комнатной температуре. Смесь упаривали в вакууме. Остаток очищали флэш-хроматографией на силикагеле, элюируя смесью гептан - гептан:EtOAc (95:5), с получением 647 мг (55%) указанного в заголовке продукта в виде слегка желтой жидкости.
Раствор (все-Z)-2-этил-5,8,11,14,17-эйкозапентаеновой кислоты (1,00 г, 3,03 ммоль), глицидола (167 мкл, 2,52 ммоль), хлоргидрата N-этил-N'-(3-диметиламинопропил)карбодиимида (585 мг, 3,05 ммоль) и DMAP (372 мг, 3,05 ммоль) в сухом CH2Cl2 (10 мл) перемешивали в течение 18 часов в атмосфере N2 при комнатной температуре. Смесь упаривали в вакууме. Остаток очищали флэш-хроматографией на силикагеле, элюируя смесью гептан - гептан:EtOAc (95:5), с получением 647 мг (55%) указанного в заголовке продукта в виде слегка желтой жидкости.
1Н ЯМР (200 МГц, CDCl3) δ 0,85-0,99 (м, 6H), 1,42-1,80 (м, 5H), 2,03-2,09 (м, 4H), 2,28-2,42 (м, 1H), 2,60-2,64 (м, 1H), 2,79-2,82 (м, 8H), 3,14-3,21 (м, 1H), 3,88-3,97 (м, 1H), 4,36-4,46 (м, 1H), 5,23-5,51 (м, 10H).
МС (электрораспыление): 409 [M+Na]+
Стадия 2: 1,3-ди(трифторацетат)-2-((все-Z)-2-этил-5,8, 11,14,17-эйкозапентаеноил)-sn-глицерин
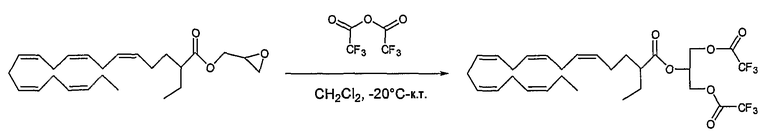
Раствор глицидил (все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноата (641 мг, 1,66 ммоль) в сухом свободном от спирта CH2Cl2 (6,5 мл) охлаждали до -20°С в атмосфере N2. Раствор ангидрида трифторуксусной кислоты (TFAA) (0,93 мл, 6,69 ммоль) в сухом CH2Cl2 (6,5 мл) добавляли по каплям. Охлаждающую баню отставляли, и смесь перемешивали в течение 70 минут. Растворитель и непрореагировавший TFAA упаривали в вакууме (t<40°C), и остаток растворяли в толуоле (15 мл), и раствор пропускали через слой силикагеля (16,5 г), элюируя толуолом (350 мл). Данный синтез привел к 607 мг (61%) сырого указанного в заголовке продукта в виде желтого масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,83-0,99 (м, 6H), 1,54-1,67 (м, 4H), 1,99-2,13 (м, 4H), 2,27-2,38 (м, 1H), 2,63-2,82 (м, 8H), 4,44 (дд, J=11,8 Гц, 5,7 Гц, 2H), 4,62(дд, J=11,9 Гц, 4,1 Гц, 2H), 5,20-5,45 (м, 11H).
Стадия 3: 2-((все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицерин
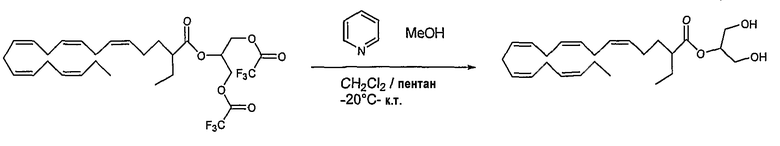
Раствор 1,3-ди(трифторацетат)-2-((все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицерина (607 мг, 1,02 ммоль) в смеси пентан/CH2Cl2 (2:1, 10 мл) охлаждали до -20°С в атмосфере N2. Раствор пиридина (0,83 мл, 10,3 ммоль) и MeOH (0,62 мл, 15,3 ммоль) в смеси пентан/CH2Cl2 (2:1, 9 мл) добавляли по каплям. Охлаждающую баню отставляли, и смесь перемешивали в течение 4 часов. Полученную смесь упаривали в вакууме. Флэш-хроматографией на силикагеле, элюируя смесью гептан - гептан:EtOAC 1:1 получали 352 мг (86%) указанного в заголовке продукта в виде слегка желтого масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,86-0,99 (м, 6H), 1,43-1,81 (м, 4H); 1,94 (ушир.c, 2H), 2,02-2,13 (м, 4H), 2,29-2,43 (м, 1H), 2,79-2,83 (м, 8H), 3,81 (д, J=4,8 Гц, 4H), 4,89-4,98 (м, 1H), 5,22-5,43 (м, 10H).
МС (электрораспыление): 427 [M+Na]+
1,2,3-трис((все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицерин (72)
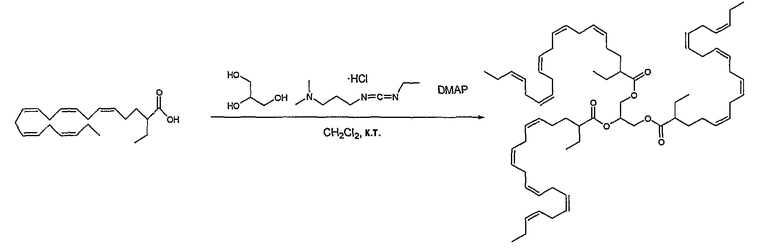
(все-Z)-2-Этил-5,8,11,14,17-эйкозапентаеновую кислоту (501 мг, 1,52 ммоль), DMAP (185 мг, 1,52 ммоль), хлоргидрат N-этил-N'-(3-диметиламинопропил)карбодиимида (295 мг, 1,54 ммоль) и сухой CH2Cl2 (5 мл) добавляли к раствору глицерина (31,6 мг, 0,343 ммоль) в ДМФА (2 мл). Образовавшуюся смесь перемешивали в течение 17½ часов в атмосфере N2 при комнатной температуре. Диэтиловый эфир (50 мл) добавляли, и образовавшуюся смесь промывали 1M HCl (20 мл) и насыщенным раствором соли (20 мл), сушили (Na2SO4) и упаривали в вакууме. Повторной флэш-хроматографией на силикагеле с элюцией смесью гептан - гептан:EtOAc (100:1)-(95:5) получали 206 мг (58%) указанного в заголовке продукта в виде бесцветного масла.
1Н ЯМР (200 МГц, CDCl3) δ 0,83-0,99 (м, 18H), 1,43-1,77 (м, 12H), 1,98-2,13 (м, 12H), 2,23-2,37 (м, 3H), 2,77-2,85 (м, 24H), 4,04-4,18 (м, 2H), 4,28-4,42 (м, 2H), 5,23-5,49 (м, 31H).
МС (электрораспыление): 1051 [M+Na]+.
Соединения, перечисленные в таблицах 1-3, могут быть получены подобно примерам, описанным выше:
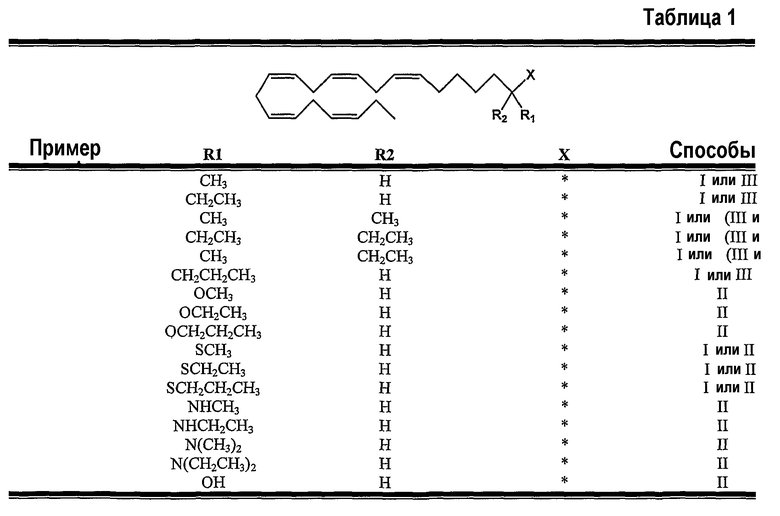
Случай, когда R1 и R2 являются обратными, также включен. ∗ случаи, где Х представляет собой карбоновую кислоту или ее производное, карбоксилат, ангидрид карбоновой кислоты или карбоксамид.
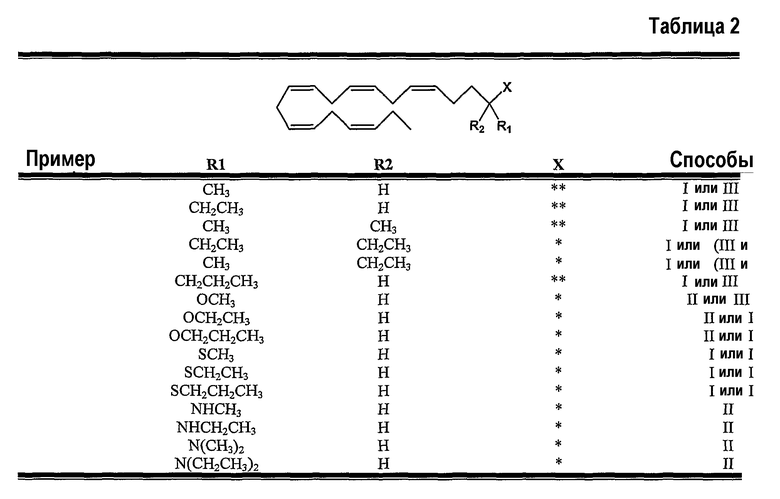
Случай, когда R1 и R2 являются обратными, также включен; ∗ случаи, где Х представляет собой карбоновую кислоту или ее производное, карбоксилат, ангидрид карбоновой кислоты или карбоксамид; ∗∗ случаи, где Х представляет собой ангидрид карбоновой кислоты, карбоксамид, моно-, ди- или триглицерид или фосфолипид.
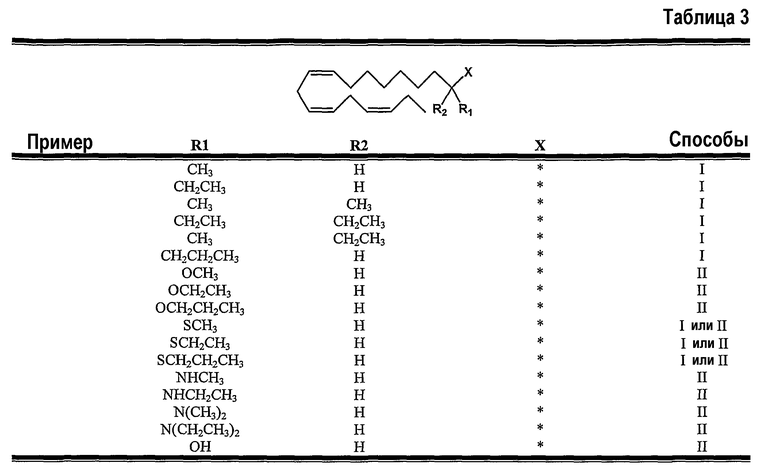
Случай, когда R1 и R2 являются обратными, также включен. ∗ случаи, где Х представляет собой карбоновую кислоту или ее производное, карбоксилат, ангидрид карбоновой кислоты или карбоксамид.
Изобретение не должно ограничиваться представленными вариантами осуществления изобретения и примерами.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ЛИПИДНЫЕ СОЕДИНЕНИЯ | 2007 |
|
RU2509071C2 |
| КОНЪЮГИРОВАННЫЕ ЛИПИДНЫЕ ПРОИЗВОДНЫЕ | 2007 |
|
RU2480447C2 |
| СТРУКТУРНО УСИЛЕННЫЕ ЖИРНЫЕ КИСЛОТЫ, СОДЕРЖАЩИЕ КИСЛОРОД, ДЛЯ ЛЕЧЕНИЯ НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА | 2018 |
|
RU2820995C2 |
| ПРОИЗВОДНЫЕ ДОКОЗАГЕКСАЕНОВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2006 |
|
RU2441061C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА КАК ИНГИБИТОРЫ 11-БЕТА-ГИДРОКСИСТЕРОИДДЕГИДРОГЕНАЗЫ-1 | 2003 |
|
RU2360910C2 |
| НОВЫЕ ФОСФОНАМИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2314314C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛА С ИНГИБИРУЮЩЕЙ ГИСТОНДЕАЦЕТИЛАЗУ АКТИВНОСТЬЮ | 2005 |
|
RU2416600C2 |
| ПРОИЗВОДНЫЕ ЭФИРА ГЕТЕРОАРИЛКАРБОНОВОЙ КИСЛОТЫ | 2013 |
|
RU2664544C2 |
| ПРОИЗВОДНЫЕ НЕЙРАМИНОВОЙ КИСЛОТЫ, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ИЛИ ИХ СЛОЖНЫЕ ЭФИРЫ, А ТАКЖЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СИАЛИДАЗУ-ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ | 1997 |
|
RU2124509C1 |
| ЦИКЛИЧЕСКИЕ АМИНОПРОИЗВОДНЫЕ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ЗАБОЛЕВАНИЙ | 1997 |
|
RU2163596C2 |
Изобретение относится к новым омега-3 липидным соединениям общей формулы (I) или к их любой фармацевтически приемлемой соли, где в формуле (I): R1 и R2 являются одинаковыми или разными и могут быть выбраны из группы заместителей, состоящей из атома водорода, гидроксигруппы, С1-С7алкильной группы, атома галогена, C1-С7алкоксигруппы, С1-С7алкилтиогруппы, С1-С7алкоксикарбонильной группы, карбоксигруппы, аминогруппы и С1-С7алкиламиногруппы; Х представляет собой карбоновую кислоту или ее карбоксилат, выбранный из этилкарбоксилата, метилкарбоксилата, н-пропилкарбоксилата, изопропилкарбоксилата, н-бутилкарбоксилата, втор-бутилкарбоксилата или н-гексилкарбоксилата, карбоновую кислоту в форме триглицерида, диглицерида, 1-моноглицерида или 2-моноглицерида, или карбоксамид, выбранный из первичного карбоксамида, N-метилкарбоксамида, N,N-диметилкарбоксамида, N-этилкарбоксамида или N,N-диэтилкарбоксамида; и Y является С16-С22 алкеном с двумя или более двойными связями, имеющими Е- и/или Z-конфигурацию. Также описаны фармацевтические и липидные композиции, содержащие такие соединения, для применения в качестве лекарственных средств, в частности для лечения и/или предотвращения периферической инсулинорезистентности и/или состояния диабета, например диабета 2 типа, повышенных уровней триглицеридов и/или уровней не-HDL холестерина, LDL холестерина и VLDL холестерина, гиперлипидемического состояния, например, гипертриглицеридемии (НТО), ожирения или состояния избыточной массы тела, заболевания жировой инфильтрации печени, например неалкогольной жировой инфильтрации печени (NAFLD) или воспалительного заболевания или состояния.

10 н. и 50 з.п. ф-лы, 3 табл., 65 пр.
1. Омега-3 липидное соединение формулы (I):

где
- R1 и R2 являются одинаковыми или разными и могут быть выбраны из группы заместителей, состоящей из атома водорода, гидроксигруппы, C1-С7алкильной группы, атома галогена, С1-С7алкоксигруппы, С1-С7алкилтиогруппы, С1-С7алкоксикарбонильной группы, карбоксигруппы, аминогруппы и С1-С7алкиламиногруппы;
- Х представляет собой карбоновую кислоту или ее карбоксилат, выбранный из этилкарбоксилата, метилкарбоксилата, н-пропилкарбоксилата, изопропилкарбоксилата, н-бутилкарбоксилата, втор-бутилкарбоксилата или н-гексилкарбоксилата, карбоновую кислоту в форме триглицерида, диглицерида, 1-моноглицерида или 2-моноглицерида, или карбоксамид, выбранный из первичного карбоксамида, N-метилкарбоксамида, N,N-диметилкарбоксамида, N-этилкарбоксамида или N,N-диэтилкарбоксамида; и
- Y является C16-C22 алкеном с двумя или более двойными связями,
имеющими Е- и/или Z-конфигурацию
или его любая фармацевтически приемлемая соль,
при условии, что:
- R1 и R2 не являются одновременно атомом водорода или атомом фтора;
и
- соединение формулы (I) не является:
- 2-замещенной (4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаеновой кислотой в виде карбоновой кислоты, карбоксилата, диглицерида, триглицерида или карбоксамида;
- (5Z,8Z,11Z,14Z,17Z)-2-метилэйкоза-5,8,11,14,17-пентаеновой кислотой, ее этиловым эфиром или ее 4-(трет-бутил)фениловым эфиром;
- (5Z,8Z,11Z,14Z,17Z)-2-этилэйкоза-5,8,11,14,17-пентаеновой кислотой, ее этиловым эфиром или ее мезитиловым эфиром;
- (5Z,8Z,11Z,14Z,17Z)-2,2-диметилэйкоза-5,8,11,14,17-пентаеновой кислотой, ее этиловым эфиром или ее 4-(трет-бутил)фениловым эфиром;
- (5Z,8Z,11Z,14Z,17Z)-метизил 2,2-диэтилэйкоза-5,8,11,14,17-пентаеноатом;
- (5Z,8Z,11Z,14Z,17Z)-2-бензилэйкоза-5,8,11,14,17-пентаеновой кислотой или ее этиловым эфиром;
- (9Z,12Z,15Z)-2-гидроксиоктадека-9,12,15-триеновой кислотой, ее метиловым эфиром или ее этиловым эфиром;
- диэтил 2-((3Z,6Z,9Z,12Z,15Z)-октадека-3,6,9,12,15-пентаен-1-ил)малонатом;
- диэтил 2-((5Z,9Z,12Z)-октадека-5,9,12-триен-1-ил)малонатом;
- диэтил 2-((6Z,9Z,12Z,15Z)-октадека-6,9,12,15-тетраен-1-ил)малонатом;
- диэтил 2-((5Z,8Z,11Z,14Z)-эйкоза-5,8,11,14-тетраен-1-ил)малонатом;
- диэтил 2-((5Z,8Z,11Z,14Z,15Z)-эйкоза-5,8,11,14,15-пентаен-1-ил)малонатом;
- этил (4Z,7Z,10Z,13Z,16Z,19Z)-2,2-диэтилдокоза-4,7,10,13,16,19-гексаеноатом.
2. Соединение по п.1, где Y является С16-С20 алкеном с 2-6 двойными связями, например 2-6 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации.
3. Соединение по п.1, где Y является С16-С20 алкеном с 3-5 двойными связями, например, 3-5 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации.
4. Соединение по п.1, где Y является С20 алкеном с 5 двойными связями в Z-конфигурации, например, 5 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации.
5. Соединение по п.1, где Y является C16 алкеном с 3 двойными связями в Z-конфигурации, например, 3 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации.
6. Соединение по п.1, выбранное из следующих категорий:
Категория А - (все-Z)-9,12,15-октадекатриеновая кислота (альфа-линоленовая кислота, ALA)
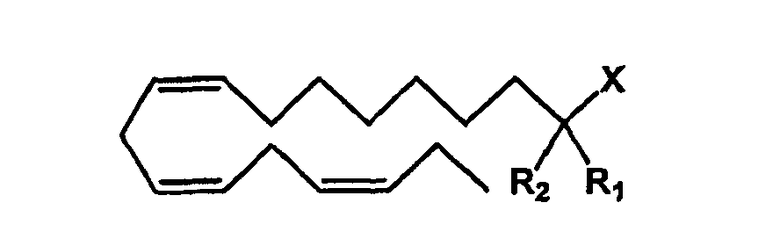
Y=C16 алкен с 3 двойными связями в Z-конфигурации в положениях 9, 12 и 15;
Категория В - (все-Z)-7,10,13,16,19-докозапентаеновая кислота (клупанодоновая кислота, DPA)
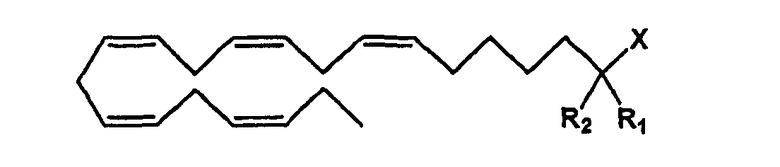
Y=C20 алкен с 5 двойными связями в Z-конфигурации в положениях 7, 10, 13, 16 и 19;
Категория С - (все-Z)-11,14,17-эйкозатриеновая кислота
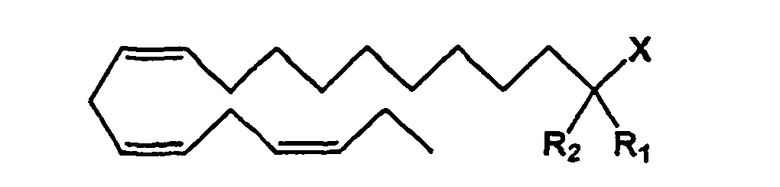
Y=C18 алкен с 3 двойными связями в Z-конфигурации в положениях 11, 14 и 17;
Категория D - (4E,8Z,11Z,14Z,17Z)-эйкозапентаеновая кислота
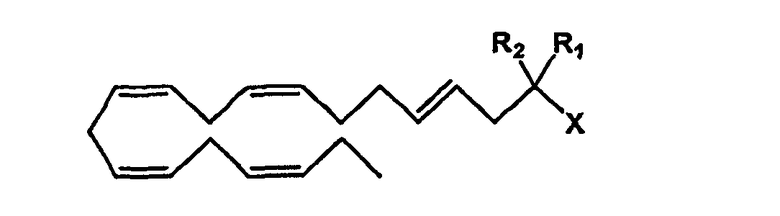
Y=C18 алкен с 5 двойными связями в положениях 4, 8, 11, 14 и 17, где двойные связи в положении 8, 11, 14 и 17 находятся в Z-конфигурации, и двойная связь в положении 4 находится в Е-конфигурации;
Категория Е - (все-Z)-5,8,11,14,17-эйкозапентаеновая кислота (ЕРА)
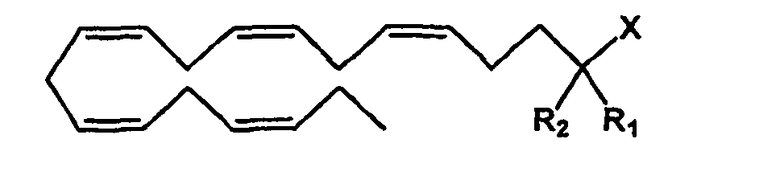
Y=C18 алкен с 5 двойными связями в Z-конфигурации в положениях 5, 8, 11, 14 и 17;
Категория F - (4Е,7Z,10Z,13Z,16Z,19Z)-докозагексаеновая кислота (транс-DHA)
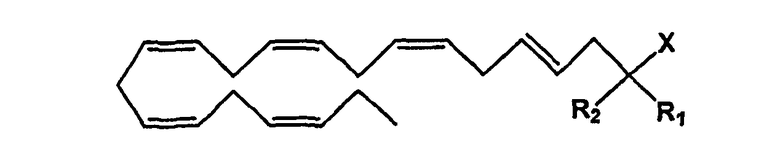
Y=C20 алкен с 6 двойными связями в положениях 4, 7, 10, 13, 16 и 19, где двойные связи в положении 7, 10, 13, 16 и 19 находятся в Z-конфигурации, и двойная связь в положении 4 находится в Е-конфигурации.
7. Соединение по любому из пп.1-6 в виде соли
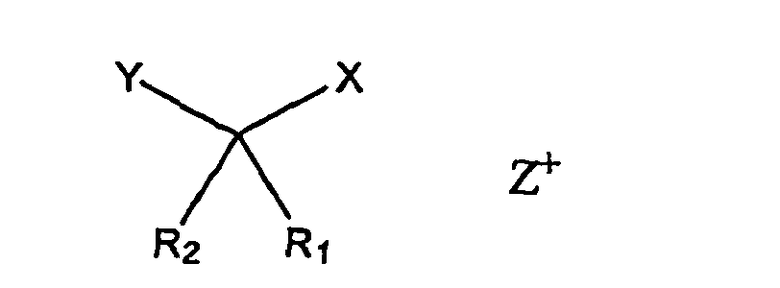
где X является COO-,
Z выбирают из группы, состоящей из Li+, Na+, K+, NH4 +,
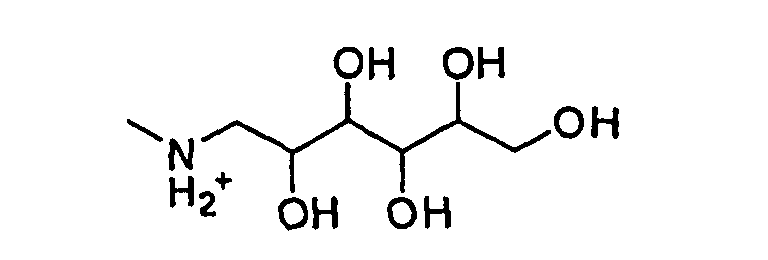
Меглумина,
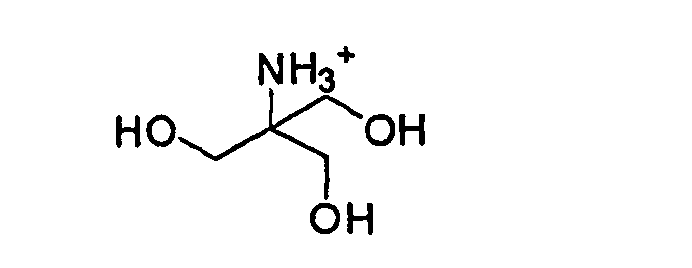
Трис(гидроксиметил)аминометана,
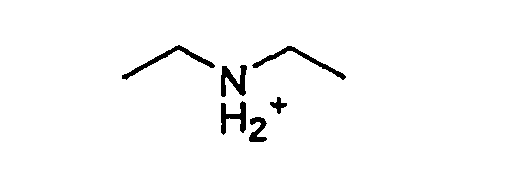
Диэтиламина, и
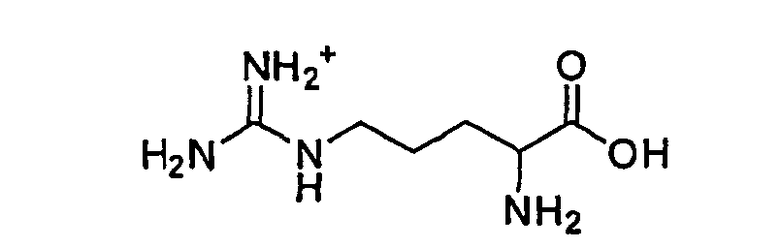
Аргинина; или
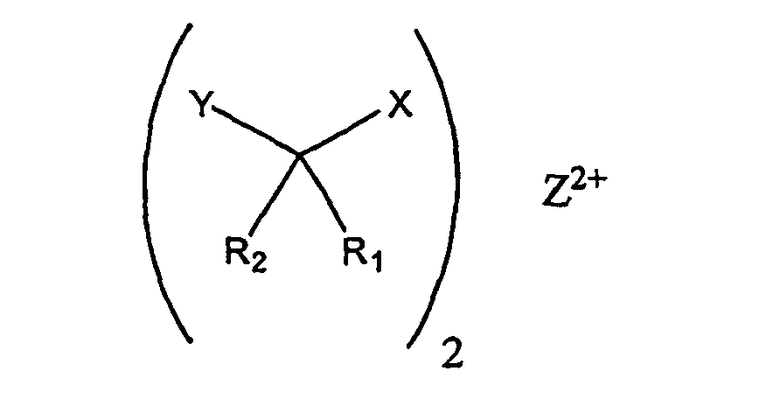
где Х=СОО-,
Z2+ выбирают из группы, состоящей из Mg2+, Ca2+,
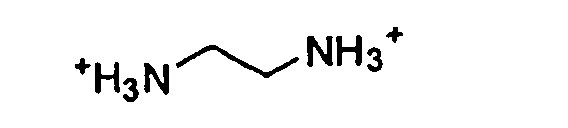
Этилендиамина, и
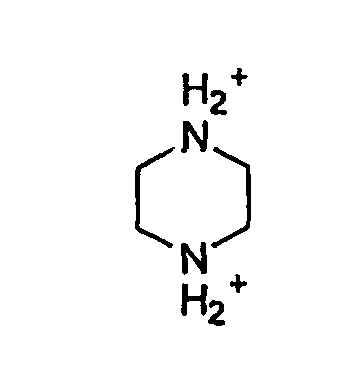
Пиперазина; или
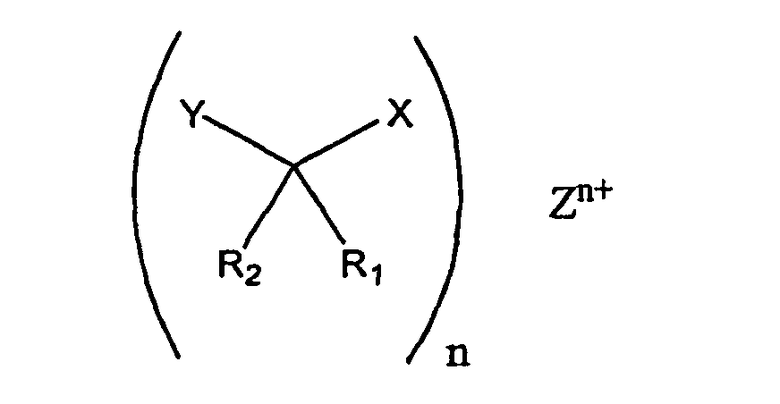
где Х является СОО-,
Zn+ является

Хитозаном.
8. Соединение по п.7, где указанное выше соединение выбирают из: меглуминовой соли (все-Z)-2-этил-11,14,17-эйкозатриеновой кислоты
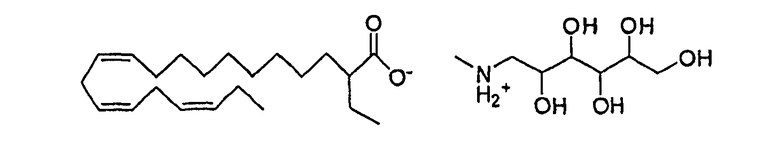
магниевой соли (все-Z)-2-этил-11,14,17-октадекатриеновой кислоты
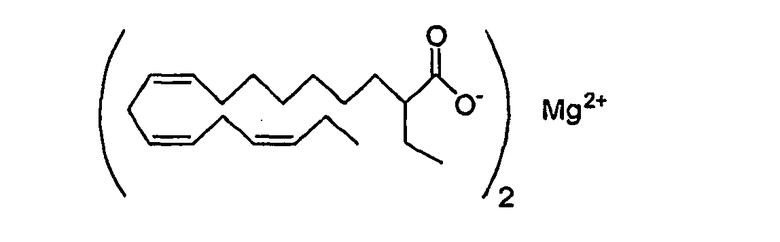
(все-Z)-2-этил-7,10,13,16,19-докозапентаеновой кислоты трис(гидроксиметил)аминометановой соли
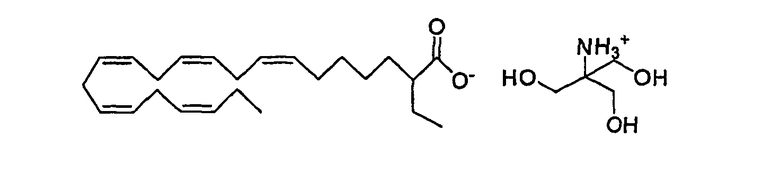
(все-Z)-2-этил-7,10,13,16,19-докозапентаеновой кислоты аммониевой соли
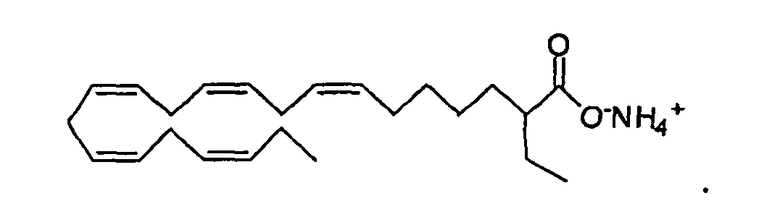
9. Соединение по любому из пп.1-6, где указанным производным карбоновой кислоты является три-, ди- или моноглицерид.
10. Соединение по п.9, где Х является карбоновой кислотой в виде триглицерида, представленное формулой (V):
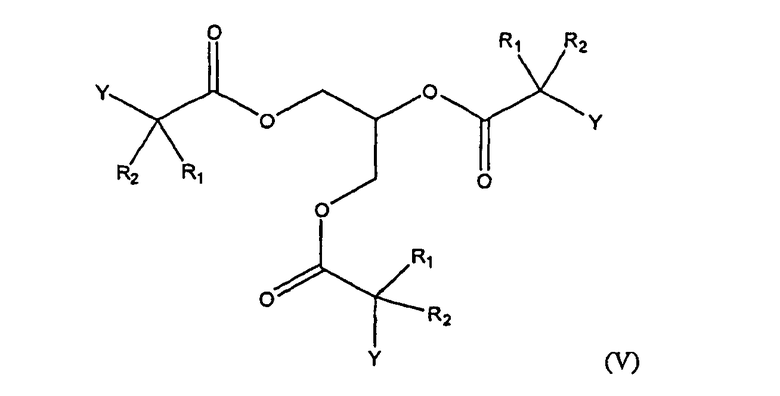
или, где Х является карбоновой кислотой в виде 1-моноглицерида, представленное формулой (VI)
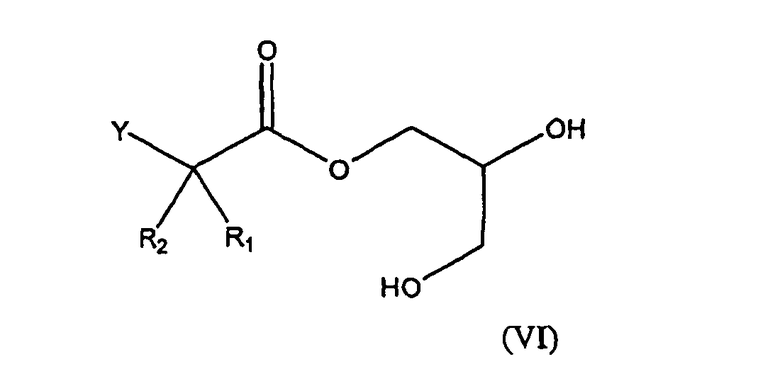
или, где Х является карбоновой кислотой в виде 2-моноглицерида, представленное формулой (VII)
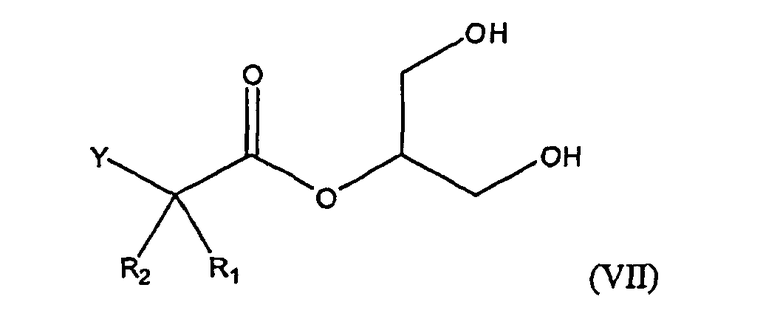
11. Омега-3 липидное соединение, выбранное из группы, состоящей из:
- (все-Z)-6,9,12,15-октадекатетраеновой кислоты
- (все-Z)-6,9,12,15,18,21-тетракозагексаеновой кислоты
- (все-Z)-8,11,14,17-эйкозатетраеновой кислоты
в виде карбоновой кислоты или ее карбоксилата, выбранного из этилкарбоксилата, метилкарбоксилата, н-пропилкарбоксилата, изопропилкарбоксилата, н-бутилкарбоксилата, втор-бутилкарбоксилата или н-гексилкарбоксилата, карбоновой кислоты в форме триглицерида, диглицерида, 1-моноглицерида или 2-моноглицерида, или карбоксамида, выбранного из первичного карбоксамида, N-метилкарбоксамида, N,N-диметилкарбоксамида, N-этилкарбоксамида или N,N-диэтилкарбоксамида;
или его любая фармацевтически приемлемая соль;
где указанное выше соединение замещено у углерода 2, считая от функциональной группы омега-3 липидного соединения, по крайней мере, одним заместителем, выбранным из группы, состоящей из:
атома водорода, гидроксигруппы, C1-C7 алкильной группы, атома галогена, C1-C7 алкоксигруппы, С1-С7алкилтиогруппы, C1-C7 алкоксикарбонильной группы, карбоксигруппы, аминогруппы и C1-C7 алкиламиногруппы;
при условии, что омега-3 липидное соединение не является:
- замещенным двумя атомами водорода
- (все-Z)-2-карбокси-6,9,12,15,18,21-тетракозагексаеновой кислотой
- этил (все-Z)-2-этоксикарбонил-6,9,12,15,18,21-тетракозагексаеноатом
- диэтил 2-((6Z,9Z,12Z,15Z)-октадека-6,9,12,15-тетраен-1-ил)малонатом.
12. Омега-3 липидное соединение, которое выбрано из:
(все-Z)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА), представленное формулой (VIII)
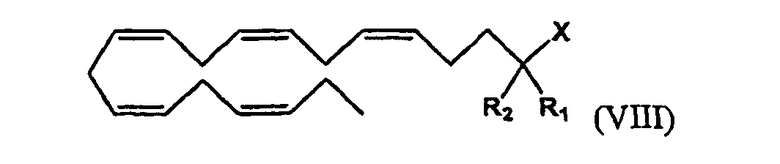
в виде карбоновой кислоты или ее карбоксилата, выбранного из этилкарбоксилата, метилкарбоксилата, н-пропилкарбоксилата, изопропилкарбоксилата, н-бутилкарбоксилата, втор-бутилкарбоксилата или н-гексилкарбоксилата, карбоновой кислоты в форме триглицерида, диглицерида, 1-моноглицерида или 2-моноглицерида, или карбоксамида, выбранного из первичного карбоксамида, N-метилкарбоксамида, N,N-диметилкарбоксамида, N-этилкарбоксамида или N,N-диэтилкарбоксамида, представленного X, или его фармацевтически приемлемая соль, где R1 и R2 являются одинаковыми или разными и могут быть выбраны из группы заместителей, состоящей из атома водорода, С3-С7 алкильной группы, C1-C7 алкоксигруппы, C1-C7 алкилтиогруппы, C1-C7 алкоксикарбонильной группы, карбоксигруппы, аминогруппы и C1-C7 алкиламиногруппы,
при условии, что R1 и R2 не являются одновременно атомом водорода; и липидное соединение не является диэтил 2-((3Z,6Z,9Z,12Z,15Z)-октадека-3,6,9,12,15-пентаен-1-ил)малонатом.
13. Соединение по п.12, где R1 и R2 выбирают из группы, состоящей из атома водорода, С3-С7 алкильной группы, например, пропила, C1-C7 алкоксигруппы, например, метокси, этокси или пропокси, C1-C7 алкилтиогруппы, например, метилтио, этилтио или пропилтио, аминогруппы, C1-C7 алкиламиногруппы, например, этиламино или диэтиламино, C1-C7 алкоксикарбонильной группы и карбоксигруппы.
14. Омега-3 липидное соединение, которое выбрано из:
(все-Z)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА), представленное формулой (VIII)
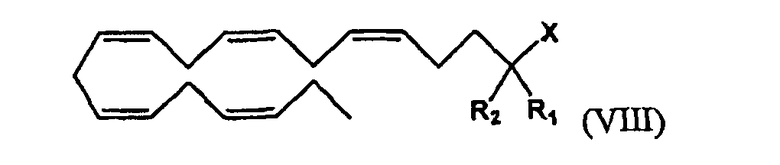
в виде карбоновой кислоты или ее карбоксилата, выбранного из этилкарбоксилата, метилкарбоксилата, н-пропилкарбоксилата, изопропилкарбоксилата, н-бутилкарбоксилата, втор-бутилкарбоксилата или н-гексилкарбоксилата, карбоновой кислоты в форме триглицерида, диглицерида, 1-моноглицерида или 2-моноглицерида, или карбоксамида, выбранного из первичного карбоксамида, N-метилкарбоксамида, N,N-диметилкарбоксамида, N-этилкарбоксамида или N,N-диэтилкарбоксамида, представленного X,
или его фармацевтически приемлемая соль,
где указанное выше соединение замещено у углерода 2, считая от функциональной группы омега-3 липидного соединения, двумя заместителями, представленными R1 и R2, выбранными из C1-C7 алкильной группы,
при условии, что указанное выше соединение не является 2,2-диметил-5,8,11,14,17-эйкозапентаеновой кислотой, ее этиловым эфиром или ее 4-(трет-бутил)фениловым эфиром; или (все-Z)-мезитил 2,2-диэтил-5,8,11,14,17-эйкозапентаеноатом.
15. Соединение по п.14, где R1 и R2 выбирают из группы, состоящей из C1-C7 алкильной группы, например, метила, этила или пропила.
16. Омега-3 липидное соединение по любому из пп.11-15, где указанным производным карбоновой кислоты является три-, ди- или моноглицерид.
17. Омега-3 липидное соединение, которое является три- или моноглицеридом
(все-Z)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА), представленным формулой (VIII)
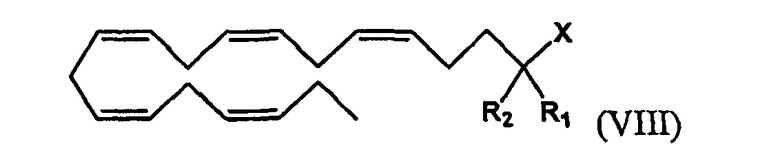
где три- или моноглицерид представлен X,
или его любая фармацевтически приемлемая соль,
где R1 и R2 являются одинаковыми или разными и могут быть выбраны из группы, состоящей из атома водорода, C1-C7 алкильной группы, при условии, что
- R1 и R2 не являются одновременно атомом водорода.
18. Соединение по п.17, где R1 и R2 выбирают из группы, состоящей из атома водорода, C1-C7 алкильной группы, например, метила, этила или пропила.
19. Соединение по п.17, где указанное соединение выбирают из 1,2,3-трис((все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицерина
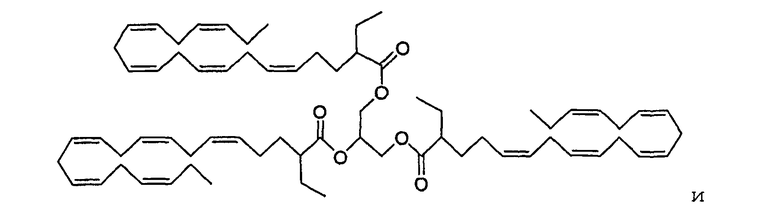
2-((все-Z)-2-этил-5,8,11,14,17-эйкозапентаеноил)-sn-глицерина
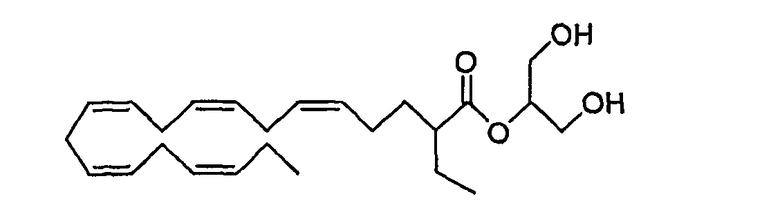
20. Соединение по любому из пп.1, 11, 12 или 14, где указанную карбоксилатную группу выбирают из группы, состоящей из этилкарбоксилата, метилкарбоксилата, н-пропилкарбоксилата, изопропилкарбоксилата, н-бутилкарбоксилата, втор-бутилкарбоксилата и н-гексилкарбоксилата.
21. Соединение по любому из пп.1, 11, 12 или 14, где Х является этилкарбоксилатом.
22. Соединение по любому из пп.1, 11, 14 или 17, где указанную алкильную группу выбирают из группы, состоящей из метила, этила, н-пропила, изопропила, н-бутила, изобутила, втор-бутила и н-гексила.
23. Соединение по п.12, где указанную алкильную группу выбирают из группы, состоящей из н-пропила, изопропила, н-бутила, изобутила, втор-бутила и н-гексила.
24. Соединение по любому из пп.1 или 11, где указанным атомом галогена является фтор.
25. Соединение по любому из пп.1, 11 или 12, где указанную выше алкоксигруппу выбирают из группы, состоящей из метокси, этокси, пропокси, изопропокси, втор-бутокси, OCH2CF3 и ОСН2СН2ОСН3.
26. Соединение по любому из пп.1, 11 или 12, где указанную алкилтиогруппу выбирают из группы, состоящей из метилтио, этилтио и изопропилтио.
27. Соединение по любому из пп.1, 11, 12 или 14, где указанную выше карбоксамидную группу выбирают из группы, состоящей из первичного карбоксамида, N-метилкарбоксамида, N,N-диметилкарбоксамида, N-этилкарбоксамида и N,N-диметилкарбоксамида.
28. Соединение по п.1, где Y является C16 алкеном с 3 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации, одной из групп R1 и R2 является метил, этил или пропил, и другой является атом водорода.
29. Соединение по п.1, где Y является C16 алкеном с 3 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации, одной из групп R1 и R2 является метокси, этокси или пропокси, и другой является атом водорода.
30. Соединение по п.1, где Y является C16 алкеном с 3 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации, одной из групп R1 и R2 является тиометил, тиоэтил или тиопропил, и другой является атом водорода.
31. Соединение по п.1, где Y является C16 алкеном с 3 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации, одной из групп R1 и R2 является этиламино, диэтиламино, и другой является атом водорода.
32. Соединение по п.1, где Y является C16 алкеном с 3 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации, одной из групп R1 и R2 является амино, и другой является атом водорода.
33. Соединение по любому из пп.28-32, где двойные связи расположены у положений 9, 12 и 15 указанного омега-3 липидного соединения.
34. Соединение по п.1, где Y является С20 алкеном с 5 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации, одной из групп R1 и R2 является метил, этил или пропил, и другой является атом водорода.
35. Соединение по п.1, где Y является С20 алкеном с 5 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации, одной из групп R1 и R2 является метокси, этокси или пропокси, и другой является атом водорода.
36. Соединение по п.1, где Y является C20 алкеном с 5 двойными связями, прерываемыми метиленовой группой, в Z-конфигурации, одной из групп R1 и R2 является тиометил, тиоэтил или тиопропил, и другой является атом водорода.
37. Соединение по любому из пп.34-36, где двойные связи расположены у положений 7, 10, 13, 16 и 19 указанного омега-3 липидного соединения.
38. Соединение по п.1, где Х является этилкарбоксилатом.
39. Соединение по п.1, 12, 14, 17, где R1 и R2 являются разными.
40. Соединение по п.39 в рацемической форме.
41. Соединение по п.40 в виде R-стереоизомера.
42. Соединение по п.40 в виде S-стереоизомера.
43. Соединение по любому из пп.1-42 для применения в лечении и/или предотвращении состояния, связанного с усилением функций, по меньшей мере, одной из изоформ рецептора (PPAR) человека, активируемого пролифератором пероксисом.
44. Соединение по п.43, где указанным выше активируемым пролифератором пероксисом рецептором (PPAR) является рецептор (PPAR) а и/или у, активируемый пролифератором пероксисом.
45. Соединение по любому из пп.1-42 для применения в лечении и/или предотвращении периферической инсулинорезистентности и/или состояния диабета, например, диабета 2 типа, повышенных уровней триглицеридов и/или уровней не-HDL холестерина, LDL холестерина и VLDL холестерина, гиперлипидемического состояния, например, гипертриглицеридемии (HTG), ожирения или состояния избыточной массы тела, заболевания жировой инфильтрации печени, например, неалкогольной жировой инфильтрации печени (NAFLD) или воспалительного заболевания или состояния.
46. Соединение по любому из пп.1-42 для применения в снижении уровней инсулина плазмы крови, глюкозы в крови и/или триглицеридов сыворотки, для применения в повышении уровней HDL сыворотки у человека или для применения в снижении массы тела и/или для предотвращения прибавления в массе тела.
47. Соединение по любому из пп.1-42 для применения в качестве PPAR-активирующего или модулирующего лекарственного средства.
48. Фармацевтическая композиция для активации или модуляции, по меньшей мере, одной из изоформ рецептора человека, активируемого пролифераторами пероксисом (PPAR), содержащая эффективное количество соединения по любому из пп.1-42 и фармацевтически приемлемый носитель, эксципиент или разбавитель или любую их комбинацию.
49. Фармацевтическая композиция по п.48, составленная для перорального введения, например, в виде капсулы, пакета-саше или твердой дозированной формы.
50. Фармацевтическая композиция по п.48, составленная для получения суточной дозы от 1 мг до 10 г, например, от 50 мг до 1 г, например, от 50 мг до 200 мг указанного выше соединения.
51. Фармацевтическая композиция по любому из пп.48-49 для применения в качестве PPAR-активирующего или модулирующего лекарственного средства.
52. Пищевая липидная композиция, содержащая эффективное количество омега-3 липидного соединения по любому из пп.1-42.
53. Пищевая липидная композиция по п.52, где, по меньшей мере, 60%, например, по меньшей мере, 80 мас.% липидной композиции составляет указанное соединение.
54. Пищевая липидная композиция по любому из пп.52-53, также содержащая жирные кислоты, выбранные из (все-Z)-5,8,11,14,17-эйкозапентаеновой кислоты (ЕРА), (все-Z)-4,7,10,13,16,19-докозагексаеновой кислоты (DHA), (все-Z)-6,9,12,15,18-генэйкозапентаеновой кислоты (НРА) и/или (все-Z)-7,10,13,16,19-докозапентаеновой кислоты (DPA).
55. Пищевая липидная композиция по п.54, где указанные жирные кислоты присутствуют в виде их альфа-замещенных форм.
56. Пищевая липидная композиция по п.52, также содержащая фармацевтически приемлемый антиоксидант, например, токоферол.
57. Применение соединения по любому из пп.1-42 для получения лекарственного средства для активации или модуляции, по меньшей мере, одной из изоформ рецептора человека, активируемого пролифератором пероксисом (PPAR).
58. Применение по п.57, где указанным выше активируемым пролифератором пероксисом рецептором (PPAR) является рецептор (PPAR) α и/или γ, активируемый пролифератором пероксисом.
59. Применение соединения по любому из пп.1-42 для получения лекарственного средства для лечения и/или предотвращения периферической инсулинорезистентности и/или состояния диабета, например, диабета 2 типа, повышенных уровней триглицеридов и/или уровней не-HDL-холестерина (не-ЛПВП), LDL-холестерина (ЛПНП) и VLDL-холестерина (ЛПОНП), гиперлипидемического состояния, например, гипертриглицеридемии (HTG), ожирения или состояния избыточной массы тела, заболевания жировой инфильтрации печени, например, неалкогольной жировой инфильтрации печени (NAFLD) или воспалительного заболевания или состояния.
60. Применение соединения по любому из пп.1-42 для получения лекарственного средства для снижения уровней инсулина в плазме, глюкозы в крови и/или триглицеридов в сыворотке, для повышения уровней HDL в сыворотке человека или для снижения массы тела и/или для предотвращения избыточной массы тела.
| US 4264517 А, 28.04.1981 | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| Куклев и др | |||
| «Синтез С-элонгированных полиненасыщенных жирных кислот» БИООРГАНИЧЕСКАЯ ХИМИЯ, 1996, т.22, №3, сс.219-222, RN 181213-50-3 | |||
| LARSEN L.N | |||
| ET AL.: «Alfa- and Beta-Alkyl-Substituted Eicosapentaenoic Acids» BIOCHEMICAL | |||
Авторы
Даты
2014-02-20—Публикация
2007-11-01—Подача