[001] Ангиогенез представляет собой процесс, в ходе которого новые кровеносные сосуды могут расти из существующей сосудистой сети. Такой процесс может возникать в организме при заживлении ран, например, восстановлении кровотока в поврежденном участке ткани, например, при травме кисти. Однако, избыточный ангиогенез может быть инициирован при специфических патологических состояниях, таких как опухоль, возрастная дегенерация желтого пятна (ВДЖП), ревматоидный артрит, псориаз и т.д. В таких обстоятельствах может существовать тенденция к нежелательному образованию новых кровеносных сосудов с возникновением патологических тканей, которые питаются и повреждают нормальные ткани. Например, раковые клетки могут попадать в кровоток посредством новых кровеносных сосудов и проникать в нормальные ткани.
[002] VEGF (сосудистый эндотелиальный фактор роста) и его рецептор VEGFR-2 (также называется KDR, рецептор, содержащий домен вставки киназы) может образовывать основной путь для образования новых кровеносных сосудов. Было показано, что ингибирование KDR может вызывать апоптоз эндотелиальных клеток, что в последующем блокирует процесс ангиогенеза (Rubin М. Tuder, Chest, 2000; 117:281). Таким образом, ингибиторы KDR могут применяться для лечения связанных с ангиогенезом расстройств.
[003] FGF (фактор роста фибробластов) представляет собой проангиогенетическую молекулу, также как и VEGF. В ходе ангиогенеза, считается, что VEGF является критическим для процесса неоваскуляризации, и ось FGF (фактор роста фибpoблacтoв)/FGFR (рецептор фактора роста фибробластов) играет роль в функциональном созревании новых сосудов. Кроме того, аберрантная активация членов семейства FGF и их родственные рецепторы были найдены при многих видах рака, таких как рак молочной железы, мочевого пузыря и предстательной железы. Уровни FGFR1 и их партнеры связывания FGF1, FGF2, FGF8b и FGF17 также повышены. В опухолях других типов FGFR1 принимает участие как онкоген, экспрессия которого повышена по сравнению с нормальной тканью. Таким образом, блокада проведения сигнала FGF/FGFR может оказывать благоприятное действие при лечении рака, сопровождающегося активацией FGF/FGFR.
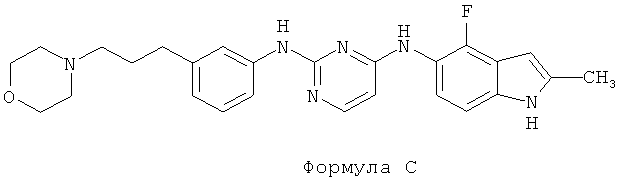
[004] В данном описании раскрыто соединение Формулы А, например, N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамид и/или его фармацевтически приемлемая соль.
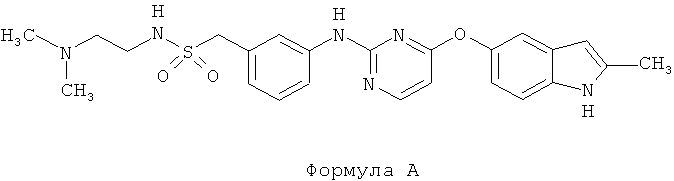
N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамид
[005] Также в данном описании раскрыта фармацевтическая композиция, содержащая по меньшей мере один фармацевтически приемлемый носитель и соединение формулы А и/или по меньшей мере одну его фармацевтически приемлемую соль.
[006] Также в данном описании раскрыт способ лечения субъекта, для которого установлена потребность в лечении по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства, который включает введение указанному субъекту, который в этом нуждается, эффективного количества соединения Формулы А и/или его фармацевтически приемлемой соли.
[007] Твердофазные кристаллические формы I и II соединения Формулы А открыты и раскрыты в данном описании. Способность соединения существовать в более чем одной кристаллической структуре или форме известна как полиморфизм. Многие соединения неожиданно могут существовать в форме полиморфных кристаллов и те же самые соединения также могут существовать в твердофазном аморфном состоянии. До открытия полиморфизма было совершенно непредсказуемым (1) будет ли конкретное соединение проявлять полиморфизм, (2) как получить любые из таких неизвестных полиморфов и (3) какие свойства, например, стабильность, будут присущи любым из таких неизвестных полиморфов. См., например, J. Bernstein "Polymorphism in Molecular Crystals", Oxford University Press, (2002).
[008] Вследствие того, что свойства любого твердого материала зависят от структуры, а также собственно от природы соединения, различные твердофазные формы соединения могут и часто демонстрируют отличные физические и химические свойства. Различия в химических свойствах могут быть определены множеством аналитических способ ов, которые применяются для характеристики, анализа и сравнения. И такие различия в химических свойствах в конечном итоге могут использоваться для различия между твердофазными формами, которые могут быть обнаружены. Кроме того, различия физических свойств, таких как растворимость или биодоступность твердофазных форм вещества, могут быть важны при введении фармацевтического соединения в препараты. Таким образом, новые кристаллические и аморфные твердофазные формы вещества в случае фармацевтически пригодных соединений, таких как соединение Формулы А, могут быть важны при разработке таких пригодных соединений.
[009] Также в данном описании раскрыта новая форма соединения Формулы А, обозначенная как Форма I //-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамида.
[010] Также в данном описании раскрыты способы получения Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[011] Также в данном описании раскрыта фармацевтическая композиция, содержащая по меньшей мере один фармацевтически приемлемый носитель и Форму I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамида.
[012] Также в данном описании раскрыт способ лечения субъекта, для которого установлена потребность в лечении по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства, который включает введение указанному субъекту, который в этом нуждается, эффективного количества Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[013] Также в данном описании раскрыта другая новая форма соединения Формулы А, обозначенная как Форма II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[014] Также в данном описании раскрыты способы получения Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[015] Также в данном описании раскрыта фармацевтическая композиция, содержащая по меньшей мере один фармацевтически приемлемый носитель и Форму II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамида.
[016] Также в данном описании раскрыт способ лечения субъекта, для которого установлена потребность в лечении по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства, который включает введение указанному субъекту, который в этом нуждается, эффективного количества Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[017] На фиг.1 показана рентгенограмма порошка Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, где на горизонтальной оси (ось x) нанесен угол дифракции 2 тета, а на вертикальной оси (ось у) нанесена интенсивность (количество импульсов).
[018] На фиг.2 показана полученная с помощью дифференциального сканирующего калориметра (ДСК) термограмма Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2- ил)амино)фенил)метансульфонамида, где на горизонтальной оси (ось x) нанесена температура (°C), а на вертикальной оси (ось у) нанесен поток тепла (мВт).
[019] На фиг.3 показан спектр в инфракрасной области с Фурье-преобразованием (FT-IR) Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, где на горизонтальной оси (ось x) нанесена длина волны (см-1), а на вертикальной оси (ось у) нанесена интенсивность трансмиссии.
[020] На фиг.4 показана термогравиметрическая (TG) кривая Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, где на горизонтальной оси (ось x) нанесена температура (°C), а на вертикальной оси (ось у) нанесен процент массы (%).
[021] На фиг.5 показана рентгенограмма порошка Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, где на горизонтальной оси (ось x) нанесен угол дифракции 2 тета, а на вертикальной оси (ось у) нанесена интенсивность (количество импульсов).
[022] На фиг.6 показана полученная с помощью дифференциального сканирующего калориметра (ДСК) термограмма Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, где на горизонтальной оси (ось x) нанесена температура (°C), а на вертикальной оси (ось у) нанесен поток тепла (мВт).
[023] На фиг.7 показан спектр в инфракрасной области с Фурье-преобразованием (FT-IR) Формы II N-2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, где на горизонтальной оси (ось x) нанесена длина волны (см-1), а на вертикальной оси (ось у) нанесена интенсивность трансмиссии.
[024] На фиг.8 показана термогравиметрическая (TG) кривая Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, где на горизонтальной оси (ось x) нанесена температура (°C), а на вертикальной оси (ось у) нанесен процент массы (%).
[025] Следующие сокращения и термины имеют указанные значения в данном описании:
[026] Термин "новая форма" в данном описании обозначает кристаллические формы (Форму I и Форму II) соединения Формулы А, аморфные формы соединения Формулы А, а также их смеси. "Кристаллическая форма" и "полиморф" могут применяться в данном описании взаимозаменяемым образом.
[027] Термин "соединение Формулы А" или "N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамид" эквивалентен соединению с химической структурой Формулы А (также называется "Соединение А"):
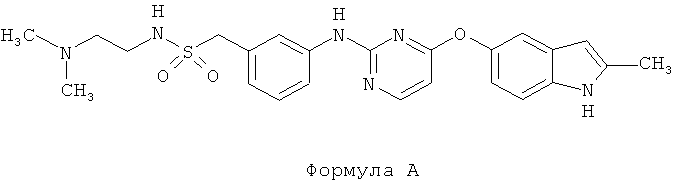
[028] Термин "раствор" обозначает подходящую для целей изобретения, раскрытого в данном описании, смесь одного или более растворенных веществ в одном или более растворителей. Раствор предназначен включать гомогенные смеси, а также гетерогенные смеси, такие как суспензии или другие смеси, содержащие суспензию нерастворимого (нерастворенного) материала. [029] Термин "органический растворитель" в широком смысле предназначен обозначать любой подходящий органический растворитель для целей раскрытого в данном описании изобретения.
[030] Термин "органический растворитель, в котором растворяется вещество", обозначает любой органический растворитель, который является подходящим в силу своей способности растворять субстрат, полностью или частично, в подходящих условиях, таких как подходящее количество и подходящая температура, например, комнатная температура или повышенная температура.
[031] Термин "органический растворитель, в котором не растворяется вещество" обозначает любой подходящий органический растворитель, в котором растворимость субстрата меньше, чем в органическом растворителе, в котором растворяется вещество.
[032] "Фармацевтические приемлемые соли" включают, не ограничиваясь ими, соли с неорганическими кислотами, такие как гидрохлорат, гидробромат, фосфат, дифосфат, сульфат, сульфинат, нитрат и т.п. соли; а также соли с органической кислотой, такие как малат, малеат, манделат, фумарат, тартрат, сукцинат, цитрат, аспартат, глутамат, атролактат, глюконат, пропионат, лактат, камфорсульфонат, метансульфонат, этансульфонат, нафталинсульфонат, n-толуолсульфонат, 2-гидроксиэтилсульфонат, гидроксибутират, бензоат, салицилат, стеарат и алканоат, например, ацетат, HOOC-(CH2)n-COOH, где n равно 0-4, и т.п. соли. Подобным образом фармацевтически приемлемые катионы включают, не ограничиваясь ими, натрий, калий, кальций, алюминий, литий и аммоний.
[033] Кроме того, если описанное здесь соединение получают в виде кислотно-аддитивной соли, свободное основание может быть получено путем подщелачивания раствора кислотно-аддитивной соли. И наоборот, если продукт находится в форме основно-аддитивной соли, в частности, фармацевтически приемлемая аддитивная соль может быть получена путем растворения свободного основания в подходящем органическом растворителе с обработкой раствора кислотой в соответствии с обычными методиками получения кислотно-аддитивной соли основного соединения. Специалистам в данной области будут известны различные методологии синтеза, которые могут применяться в пределах шаблонного экспериментирования для получения нетоксичных фармацевтически приемлемых аддитивных солей.
[034] Термин "эффективное количество" соединения Формулы А, в том числе новой формы, описанной здесь, обозначает количество, при введении субъекту с установленной потребностью, такому как пациент-человек или негуманоидный пациент, эффективное для облегчения симптомов или остановки прогрессирования по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства.
[035] Предложен N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамид Формулы А (Соединение А)
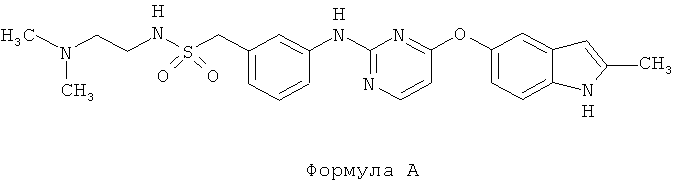
и/или его фармацевтически приемлемые соли.
[036] Также предложена фармацевтическая композиция, содержащая по меньшей мере один фармацевтически приемлемый носитель и соединение Формулы А, и/или его фармацевтически приемлемые соли. [037] Соединение Формулы А может быть синтезировано в соответствии с приведенной ниже схемой.
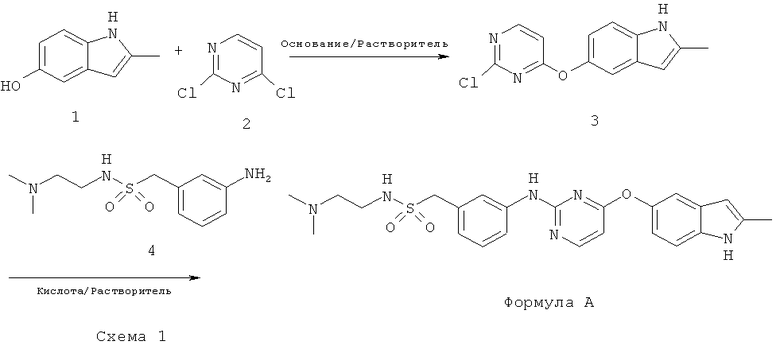 Стадия 1: Синтез 5-((2-хлорпиримидин-4-ил)окси)-2-метил-1H-индола (соединение 3)
Стадия 1: Синтез 5-((2-хлорпиримидин-4-ил)окси)-2-метил-1H-индола (соединение 3)
[038] Названное в заголовке соединение 3 может быть получено реакцией 5-гидроксил-2-метил-индола (соединение 1) с 2,4-дихлорпиримидином (соединение 2) в присутствии основания, такого как, не ограничиваясь этим, NaHCO3, КОН, NaOH, К2СO2, КНСO3, диизопропилэтиламин (ДИПЭА), пиридин, триэтиламин (ТЭА) или триметиламин, в растворителе, таком как, не ограничиваясь этим, ацетонитрил, N,N-диметилформамид (ДМФА), диоксан, тетрагидрофуран (ТГФ). Реакция может быть проведена при подходящей температуре, например, при температуре в интервале от 0 до 60°C.
Стадия 2: Синтез N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида (соединение Формулы А)
[039] Названное в заголовке соединение Формулы А может быть синтезировано как неочищенный продукт соединения Формулы А реакцией Соединения 3 с 1-(3-аминофенил)-N-(2-(диметиламино)этил)метансульфонамидом (Соединение 4) в присутствии кислоты, такой как, не ограничиваясь ими, уксусная кислота, муравьиная кислота, HCl, H2SO4, толуолсульфоновая кислота, трифторуксусная кислота или кислая этансульфоновая кислота, и в растворителе, таком как, не ограничиваясь ими, N,N-диметилформамид (ДМФА), ацетонитрил, тетрагидрофуран, этанол, изопропанол или толуол. Реакция может быть проведена при подходящей температуре, например, при температуре в интервале от 40 до 100°C.
[040] Неочищенный продукт соединения Формулы А может быть дополнительно очищен хроматографией на силикагеле, высокоэффективной жидкостной хроматографией, кристаллизацией или другими подходящими способами.
[041] Неочищенный продукт соединения Формулы А также может быть очищен перекристаллизацией с использованием растворителя, такого как, не ограничиваясь ими, N-метилпирролидон, дихлорметан, толуол, N,N-диметилформамид или смесь N,N-диметилформамид/толуол.
[042] Также предложены новые формы N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[043] В некоторых вариантах воплощения описанные здесь новые формы могут быть идентифицированы с помощью одного или более твердофазных способов анализа. Например, Форма I и/или Форма II могут быть охарактеризованы, например, в соответствии с одним или более следующих способов: рентгеноструктурный анализ порошка, одноячеечные константы, полученные для одиночного кристалла, спектроскопия в инфракрасной области с Фурье-преобразованием, данные кривой дифференциальной сканирующей калориметрии (ДСК) и термогравиметрическая кривая. И если характеристика с помощью любого из указанных способов согласуется с существованием Формы I и/или Формы II, это не означает, что данные какого-либо другого способа не будут согласоваться с таким существованием.
[044] В некоторых вариантах воплощения описанная здесь новая форма может быть охарактеризована в соответствии с рентгенограммой порошка. Однако в данной области известно, что интенсивность и/или измеренные пики на рентгенограмме различных партий новой формы могут варьировать, например, вследствие различий в экспериментальных условиях и/или предпочтительных ориентациях. И, в соответствии с точностью прибора, ошибка измерения значения 2θ составляет ±0,2 2θ. Но, нивелируя экспериментальные и расчетные ошибки и такие принципы, как предпочтительная ориентация, специалист в данной области может получить достаточную информацию относительно данных рентгенограммы, приведенных в данном описании, для идентификации Формы I и Формы II без необходимости полностью полагаться на все приведенные данные рентгенограммы.
Форма I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида
[045] Предложена Форма I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[046] В некоторых вариантах воплощения рентгенограмма порошка Формы I, описанной здесь, может содержать пики (2θ), некоторые из которых имеют приблизительно следующие значения: 7,0, 8,0 и 8,6, каждый из углов дифракции ±0,2° (2θ). В некоторых вариантах воплощения рентгенограмма порошка Формы I, описанная здесь, может содержать пики (2θ), некоторые из которых имеют приблизительно следующие значения: 7,0, 8,0, 8,6, 11,0, 11,8, каждый из углов дифракции ±0,2° (2θ). В некоторых вариантах воплощения дифрактограмма Формы I, описанной в данном документе, может быть в существенной мере подобной той, что показана на фиг.1.
[047] В некоторых вариантах воплощения Форма I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида может быть охарактеризована с помощью ИК-спектра с Фурье-преобразованием (FT-IR). Например, также предлагается вариант Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамида, где спектр FT-IR демонстрирует пики приблизительно при 2781,4, 1218,2, 1163,1, 1124,5, 1114,8, 1085,7, 984,9, 705,0, 500,7 и 434,8 см-1. В некоторых вариантах воплощения FT-IR спектр Формы I, описанной здесь, может быть в существенной мере подобным тому, что показан на фиг.3.
[048] В некоторых вариантах воплощения Форма I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида может быть охарактеризована в соответствии с термограммой ДСК. Например, предлагается вариант Формы I, описанной здесь, где термограмма ДСК в существенной мере подобна показанной на фиг.2. Например, также предлагается вариант воплощения Формы I, описанной здесь, где термограмма ДСК содержит эндотермические пики приблизительно при 167-169°C.
[049] В некоторых вариантах воплощения Форма I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида может быть охарактеризована термогравиметрическим анализом (ТГА). Например, предлагается вариант воплощения Формы I, описанной здесь, где ТГА показывает Форму I, описанную здесь, в виде безводной или неразведенной формы. См. фиг.4.
[050] В некоторых вариантах воплощения Форма I в существенной мере свободна от Формы II и аморфной формы соединения Формулы А. Например, Форма I составляет по меньшей мере 99 масс.%, по меньшей мере 95 масс.%, по меньшей мере 90 масс.% или по меньшей мере 80%, масс., свободна от Формы II и аморфной формы соединения Формулы А. В качестве еще одного примера, Форма I по меньшей мере на 70 масс.% или по меньшей мере на 60 масс.% свободна от Формы II и аморфной формы соединения Формулы А. В качестве еще одного примера, Форма I по меньшей мере более чем на 50 масс.%, свободна от Формы II и аморфной формы соединения Формулы А.
Способы получения Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида
Способ А
[051] Также предложен способ получения Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, который включает:
(1) смешивание N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1 Я-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида Формулы А по меньшей мере с одним органическим растворителем, в котором данное вещество растворяется, и далее кипячение смеси с обратным холодильником с получением раствора;
(2) охлаждение раствора до комнатной температуры, например медленное охлаждение; и
(3) выделение Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[052] В некоторых вариантах воплощения по меньшей мере один подходящий органический растворитель, в котором растворяется вещество, выбран из протонных растворителей и апротонных растворителей. В некоторых вариантах воплощения протонные растворители представляют собой спирты, такие как метанол, этанол, изопропанол, н-бутанол, и спирты, содержащие менее 6 атомов углерода, дополнительно, в том числе метанол, этанол и изопропанол. В некоторых вариантах воплощения апротонные растворители выбраны из ацетона, ацетонитрила, N,N-диметилформамида, толуола, дихлорметана и этилацетата.
[053] В некоторых вариантах воплощения раствор охлаждают до комнатной температуры, например, медленно охлаждают при перемешивании, таком как перемешивание со средней скоростью, например со скоростью перемешивания от 50 до 200 об/мин.
[054] В некоторых вариантах воплощения количество по меньшей мере одного растворителя, в котором растворяется вещество, составляет от 10 до 60 объемов (мл) на 1 единицу массы (г) соединения Формулы А, используемого на стадии (1).
Способ Б
[055] Также предложен альтернативный способ получения Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил), который включает:
(1) смешивание N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида по меньшей мере с одним органическим растворителем, в котором растворяется данное вещество, и последующее кипячение смеси с обратным холодильником с получением первого раствора;
(2) добавление по меньшей мере одного органического растворителя, в котором данное вещество не растворяется, к первому раствору при температуре кипения с обратным холодильником с получением второго раствора;
(3) остывание второго раствора, например, медленное охлаждение до комнатной температуры; и
(4) выделение Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[056] В некоторых вариантах воплощения по меньшей мере один растворитель, в котором растворяется вещество, является таким, как описано выше. В некоторых вариантах воплощения по меньшей мере один растворитель, в котором растворяется вещество, выбран из метанола, этанола, ацетона, ацетонитрила и N,N-диметилформамида.
[057] В некоторых вариантах воплощения подходящий растворитель, в котором не растворяется вещество, в зависимости от условий, выбран из воды, гептанов, гексанов и других насыщенных углеводородных растворителей, содержащих менее 9 атомов углерода; этилацетата и других сложных эфиров органических кислот, содержащих менее 8 атомов углерода; трет-бутилметилового эфира и других эфиров, содержащих менее 6 атомов углерода; и толуола. В некоторых вариантах воплощения по меньшей мере один растворитель, в котором не растворяется вещество, выбран из воды, гептанов, гексанов и этилацетата.
[058] В некоторых вариантах воплощения объемное соотношение по меньшей мере одного растворителя, в котором растворяется вещество, и по меньшей мере одного растворителя, в котором не растворяется вещество, варьирует от 1:3 до 5:1.
[059] В некоторых вариантах воплощения количество по меньшей мере одного растворителя, в котором растворяется вещество, используемого в данном альтернативном способе, также составляет от 10 до 60 объемов (мл) на 1 единицу массы (г) соединения Формулы А, используемого на стадии (1).
Форма II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамид.
[060] Также предлагается Форма II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[061] В некоторых вариантах воплощения Форма II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида может быть охарактеризована в соответствии с рентгенограммой порошка. В некоторых вариантах воплощения рентгенограмма порошка Формы II, описанной здесь, может содержать пики (2θ), некоторые из которых имеют приблизительно следующие значения: 6,8, 9,8, 10,5 и 10,7, где каждый из углов дифракции составляет ±0,2° (2θ). В некоторых вариантах воплощения рентгенограмма порошка Формы II, описанной в данном документе, может содержать пики (2θ), некоторые из которых имеют приблизительно следующие значения: 6,8, 9,8, 10,5, 10,7, 13,6, 15,0, где каждый из углов дифракции составляет ±0,2° (2θ). В некоторых вариантах воплощения рентгенограмма порошка Формы II, описанной здесь, может быть в существенной мере подобной той, что показана на фиг.5. Но, нивелируя экспериментальные и расчетные ошибки, и такие принципы, как предпочтительная ориентация, специалист в данной области может получить достаточную информацию относительно данных рентгенограммы порошка, приведенных здесь, для идентификации Формы II, без необходимости полностью полагаться на все приведенные данные рентгенограммы.
[062] В некоторых вариантах воплощения Форма II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида может быть охарактеризована в соответствии с ИК-спектром с Фурье-преобразованием (FT-IR). Например, также предлагается вариант воплощения Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, для которого спектр FT-IR демонстрирует пики на длинах волн приблизительно 2770,3, 1216,3, 1166,3, 1115,8, 1089,8, 986,5, 872,5, 695,5, 520,5, 456,0 см-1. В некоторых вариантах воплощения спектр FT-IR Формы II, описанной здесь, может быть в существенной мере подобным показанному на фиг.7.
[063] В некоторых вариантах воплощения Форма II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида может быть охарактеризована в соответствии с термограммой ДСК. Например, предлагается вариант воплощения Формы II, описанной здесь, где термограмма ДСК в существенной мере подобна показанной на фиг.6. Например, также предлагается вариант воплощения Формы II, описанной в данном документе, где ДСК содержит эндотермические пики при температуре приблизительно 160-162°C. См. фиг.6.
[064] В некоторых вариантах воплощения Форма II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида может быть охарактеризована термогравиметрическим анализом (ТГА). Например, предлагается вариант воплощения Формы II, описанной в данном документе, где ТГА указывает на Форму II, описанную здесь, как безводную или неразведенную форму. См. фиг.8.
[065] В некоторых вариантах воплощения Форма II в существенной мере свободна от Формы I и аморфной формы соединения Формулы А. Например, Форма II по меньшей мере на 99 масс.%, по меньшей мере на 95 масс.%, по меньшей мере на 90 масс.% или по меньшей мере на 80 масс.%, свободна от Формы I и аморфной формы соединения Формулы А. Далее, например, Форма II по меньшей мере на 70 масс.% или по меньшей мере на 60 масс.%, свободна от Формы I и аморфной формы соединения Формулы А. Еще, например, Форма II по меньшей мере более чем на 50 масс.%, свободна от Формы I и аморфной формы соединения Формулы А.
Способ получения Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамид
Способ Б
[066] Также предложен способ получения Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, который включает
(1) смешивание N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида по меньшей мере с одним растворителем, в котором растворяется вещество, и нагревание смеси до кипения с обратным холодильником с получением первого раствора;
(2) добавление по меньшей мере одного растворителя, в котором не растворяется вещество, к первому раствору при температуре кипения с обратным холодильником с получением второго раствора;
(3) охлаждение второго раствора, например, до 0-5°C, например, при скорости охлаждения 1-40°C/мин.; и
(4) выделение Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[067] В некоторых вариантах воплощения раствор охлаждают до 0-5°C при скорости охлаждения 1-40°C/мин при перемешивании.
[068] В некоторых вариантах воплощения по меньшей мере один подходящий органический растворитель, в котором растворяется вещество, выбран из протонных растворителей и апротонных растворителей. В некоторых вариантах воплощения протонные растворители представляют собой спирты, такие как метанол, этанол, изопропанол, н-бутанол, и спирты, содержащие менее 6 атомов углерода, такие как метанол, этанол и изопропанол. В некоторых вариантах воплощения апротонные растворители выбраны из ацетона, ацетонитрила, N,N-диметилформамида, толуола, дихлорметана и этилацетата.
[069] В некоторых вариантах воплощения подходящие спирты выбраны из метанола и этанола. В некоторых вариантах воплощения апротонные растворители выбраны из ацетона, ацетонитрила, этилацетата и N,N-диметилформамида.
[070] В некоторых вариантах воплощения соотношение по массе соединения Формулы А к объему по меньшей мере одного растворителя, в котором растворяется вещество, варьирует от 0,03:1 до 0,08:1 (г/мл).
Способ Г
[071] Также предлагается альтернативный способ получения Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, который включает:
(1) смешивание N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида по меньшей мере с одним растворителем, в котором растворяется вещество, и кипячение смеси с обратным холодильником с получением раствора;
(2) охлаждение раствора с последующим внесением затравки Формы II, описанной здесь, в охлажденный раствор;
(3) охлаждение раствора с затравкой до комнатной температуры; и
(4) выделение Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
[072] В некоторых вариантах воплощения раствор на стадии (2) медленно охлаждают до 45-55°C перед внесением затравки.
[073] В некоторых вариантах воплощения затравку Формы II добавляют к раствору при перемешивании.
[074] В некоторых вариантах воплощения раствор с затравкой охлаждают до комнатной температуры, давая ему постоять при комнатной температуре.
[075] В некоторых вариантах воплощения по меньшей мере один подходящий органический растворитель, в котором растворяется вещество, выбирают из протонных растворителей и апротонных растворителей. В некоторых вариантах воплощения протонные растворители представляют собой спирты, такие как метанол, этанол, изопропанол, н-бутанол, и спирты, содержащие менее 6 атомов углерода, такие как метанол, этанол и изопропанол.
В некоторых вариантах воплощения апротонные растворители выбраны из ацетона, ацетонитрила, N,N-диметилформамида, толуола, дихлорметана и этилацетата.
[076] В некоторых вариантах воплощения подходящие спирты выбраны из метанола и этанола. В некоторых вариантах воплощения апротонные растворители выбраны из ацетона, ацетонитрила, этилацетата и N,N-диметилформамида
[077] В некоторых вариантах воплощения затравку Формы II добавляют к раствору при перемешивании.
[078] В некоторых вариантах воплощения соотношение по массе соединения Формулы А к объему по меньшей мере одного растворителя, в котором растворяется вещество, варьирует от 0,03:1 до 0,08:1 (г/мл).
[079] В некоторых вариантах воплощения количество затравки Формы II варьирует от 0,01 до 0,5 масс.%, относительно массы N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, используемого на стадии (1). В некоторых вариантах воплощения количество затравки Формы II составляет 0,5 масс.%, относительно массы ЛЧ2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, используемого на стадии (1).
[080] Все описанные в данном описании способы получения Формы I или Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида необязательно могут дополнительно включать еще одну стадию между стадией (1) и стадией (2), где полученный на стадии (1) раствор фильтруют в горячем состоянии для удаления нерастворимых частиц. Во избежание осаждения в ходе любой стадии горячего фильтрования воронку для фильтрования можно нагреть в ходе или перед началом фильтрования. Образующийся в ходе горячего фильтрования осадок можно снова растворить путем нагревания фильтратов перед выполнением следующей операции.
Фармацевтическая композиция и способы лечения
[081] В некоторых вариантах воплощения по меньшей мере один активный фармацевтический ингредиент, выбранный из соединения Формулы А (Соединения А) и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, может быть пригоден для лечения по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанное с ангиогенезом расстройство. В некоторых вариантах воплощения связанные с ангиогенезом расстройства выбраны из возрастной дегенерации желтого пятна и различных видов рака. Различные виды рака, как описано в данном документе, включают, не ограничиваясь ими, рак печени, рак легкого, рак головы и шеи, рак молочной железы, рак мочевого пузыря, рак ободочной и прямой кишки, рак желудка, рак поджелудочной железы, рак яичника, рак предстательной железы, рак почки и саркому.
[082] В некоторых вариантах воплощения способ лечения субъекта, страдающего по меньшей мере одним видом рака и/или по меньшей мере одним связанным с ангиогенезом заболеванием, с установленной потребностью в лечении такого заболевания, включает введение указанному субъекту с установленной потребностью в лечении эффективного количества по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, для лечения указанного по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства.
[083] В некоторых вариантах воплощения способ лечения субъекта, страдающего по меньшей мере одним заболеванием, отвечающим на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства, с установленной потребностью в лечении, включает введение указанному субъекту с установленной потребностью в лечении эффективного количества Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида для лечения указанного по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства.
[084] В некоторых вариантах воплощения способ лечения субъекта, страдающего по меньшей мере одним заболеванием, отвечающим на ингибирование FGFR1, таким как рак, и/или по меньшей мере одним заболеванием, отвечающим на ингибирование KDR, таким как связанные с ангиогенезом расстройства, с установленной потребностью в лечении, таким образом, включает введение указанному субъекту с установленной потребностью в лечении эффективного количества Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида для лечения указанного по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства.
[085] В некоторых вариантах воплощения способ лечения субъекта, страдающего по меньшей мере одним заболеванием, отвечающим на ингибирование FGFR1, таким как рак, и/или по меньшей мере одним заболеванием, отвечающим на ингибирование KDR, таким как связанные с ангиогенезом расстройства, с установленной потребностью в лечении, таким образом, включает введение указанному субъекту с установленной потребностью в лечении эффективного количества фармацевтической композиции, содержащей: по меньшей мере один фармацевтически приемлемый носитель и соединение Формулы А и/или его фармацевтически приемлемые соли для обеспечения указанного лечения.
[086] В некоторых вариантах воплощения способ лечения субъекта, страдающего по меньшей мере одним заболеванием, отвечающим на ингибирование FGFR1, таким как рак, и/или по меньшей мере одним заболеванием, отвечающим на ингибирование KDR, таким как связанные с ангиогенезом расстройства, с установленной потребностью в лечении, таким образом, включает введение указанному субъекту с установленной потребностью в лечении эффективного количества фармацевтической композиции, содержащей: по меньшей мере один фармацевтически приемлемый носитель и Форму I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил) для обеспечения указанного лечения.
[087] В некоторых вариантах воплощения способ лечения субъекта, страдающего по меньшей мере одним заболеванием, отвечающим на ингибирование FGFR1, таким как рак, и/или по меньшей мере одним заболеванием, отвечающим на ингибирование KDR, таким как связанные с ангиогенезом расстройства, с установленной потребностью в лечении, таким образом, включает введение указанному субъекту с установленной потребностью в лечении эффективного количества фармацевтической композиции, содержащей: по меньшей мере один фармацевтически приемлемый носитель и Форму II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида для обеспечения указанного лечения.
[088] Количество по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, эффективное для достижения целевого биологического эффекта, может зависеть от множества факторов, например, предусмотренное применение, способ введения и клиническое состояние пациента. Суточная доза, например, может варьировать от 0,1 мг до 3 г/сутки (например, от 0,5 мг до 2 г /сутки, еще, например, от 100 мг до 1 г/сутки). Однодозовые препараты, которые можно вводить перорально, включают, например, таблетки или капсулы.
[089] Для лечения вышеупомянутых состояний по меньшей мере один активный фармацевтический ингредиент, выбранный из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, может применяться в качестве собственно соединения, но типично каждый из них будет применяться в форме фармацевтической композиции с одним или более приемлемых носителей/вспомогательных веществ. Характерные примеры носителей/вспомогательных веществ должны быть совместимы с другими ингредиентами композиции и не должны быть опасными для здоровья больного. Носитель/вспомогательное вещество может представлять собой твердое вещество или жидкость, или оба, и может быть введен в препарат с соединением Формулы А, таким как Форма I и/или Форма И, приведенные в данном описании, в однодозовой форме, такой как таблетка, которая может содержать от 0,05 масс.% до 95 масс.%, оединения Формулы А, приведенного в данном описании. Фармацевтические композиции, приведенные в данном описании, могут быть получены известными в области фармации способами, например, включающими смешивание ингредиентов с фармакологически приемлемыми носителями и/или вспомогательными веществами, и/или разбавителями.
[090] В некоторых вариантах воплощения характерные примеры носителей/вспомогательных веществ могут включать, не ограничиваясь ими: микрокристаллическую целлюлозу, лактозу, натрия цитрат, кальция карбонат, дикальция фосфат, глицин, дезинтегранты, такие как крахмал, натрия поперечно-сшитая карбоксиметилцеллюлоза, композитные силикаты и полиэтиленгликоль с высокой молекулярной массой, связующие агенты для грануляции (такие как поливинилпирролидон, сахароза, желатин и аравийская камедь) и любриканты (такие как магния стеарат, глицерин и тальк).
[091] В некоторых вариантах воплощения по меньшей мере один активный фармацевтический ингредиент, выбранный из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, может быть объединен по меньшей мере с одним компонентом, таким как носитель и/или вспомогательное вещество, и/или разбавитель, выбранным из подсластителей, ароматизаторов с ненавязчивым запахом, окрашенных материалов, красителей и эмульгаторов.
[092] В некоторых вариантах воплощения Форма I или Форма II, приведенная в данном описании, может не быть введена в препарат с одним или более фармацевтически приемлемых разбавителей. В других вариантах воплощения Форма I или Форма II, приведенная в данном описании, может быть превращена, полностью или частично, в одну или более других форм, в том числе нетвердофазных, при введении в препарат с одним или более фармацевтически приемлемых носителей/разбавителей/вспомогательных веществ. Примеры носителей/разбавителей/вспомогательных веществ включают, не ограничиваясь ими, воду, этанол, пропиленгликоль, глицерин и их смеси. В некоторых вариантах воплощения Форма I или Форма II, приведенная в данном описании, может быть растворена при введении в фармацевтическую композицию. Соответственно, в случаях такого «растворения» Форма I или Форма II не существует больше в соответствующей кристаллической форме в фармацевтической композиции.
[093] В некоторых вариантах воплощения по меньшей мере один активный фармацевтический ингредиент, выбранный из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, может быть введен в подходящую лекарственную форму.
[094] Фармацевтические композиции, приведенные в данном описании, могут быть пригодны для орального и перорального применения (например, сублингвально), хотя подходящий способ введения может зависеть в каждом отдельном случае от природы и тяжести состояния, подлежащего лечению, и от природы по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, применяемого в каждом случае для получения фармацевтической композиции. Также предлагаются препараты с покрытием и препараты замедленного высвобождения с покрытием. Возможно получение препаратов, устойчивых к действию кислоты и желудочного сока. Подходящие устойчивые к действию желудочного сока покрытия включают целлюлозы ацетат фталат, поливинилацетатфталат, гидроксипропилметилцеллюлозы фталат, анионные полимеры метакриловой кислоты и метилметакрилат.
[095] Подходящие фармацевтические композиции для перорального введения, приготовленные из по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, могут находиться в форме отдельных единиц, таких как, например, капсулы, саше и таблетки, в том числе таблетки для рассасывания, каждые из которых могут быть получены с определенным количеством по меньшей мере одного активного фармацевтического ингредиента, описанного здесь, а также в форме, выбранной из порошков, гранул, растворов, суспензий в водной или неводной жидкости и эмульсий масло-в-воде и вода-в-масле. Такие композиции, как указано выше, могут быть получены любым подходящим способом получения фармацевтических препаратов, таким как способы, включающие стадию, где обеспечивается контакт по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, и носителя (который может состоять из одного или более дополнительных ингредиентов, в том числе разбавителей и вспомогательных веществ). Композиции в целом могут быть получены путем однородного и гомогенного смешивания по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, с жидкостью и/или тонко измельченным твердым веществом носителя, после чего продукту может быть придана форма. Таким образом, например, таблетка может быть получена прессованием или формованием порошка или гранул по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, при необходимости, с одним или более дополнительных ингредиентов. Прессованные таблетки могут быть получены путем таблетирования по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, в форме свободно насыпанного вещества, такого как, например, порошок или гранулы, при необходимости в смеси со связующим агентом, улучшающим скольжение средством, инертным разбавителем и/или одним (или более) поверхностно-активных/диспергирующих агентов в подходящем аппарате. Формованные таблетки могут быть получены путем формования по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, в форме порошка с последующим увлажнением инертным жидким разбавителем в подходящем аппарате. Композиции также могут быть получены путем влажной грануляции. Таким образом, например, композиция может быть получена путем влажной грануляции при смешивании по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, с одним или более необязательных дополнительных ингредиентов, подходящим растворителем и связующим агентом для получения влажного гранулята, сушки влажного гранулята и помола сухого гранулята. Способ может дополнительно включать добавление по меньшей мере одного любриканта к сухому молотому грануляту и прессование сухого молотого гранулята с получением таблеток. Необязательные дополнительные ингредиенты могут включать, например, по меньшей мере один разбавитель и/или по меньшей мере один дезинтегрант. Подходящим растворителем может быть вода. В некоторых вариантах воплощения разбавитель выбран из кальция карбоната, кальция фосфата (двухосновного и/или трехосновного), кальция сульфата, порошкообразной целлюлозы, декстратов, декстрина, фруктозы, каолина, лактитола, безводной лактозы, моногидрата лактозы, мальтозы, маннита, микрокристаллической целлюлозы, сорбита, сахарозы и крахмала. В некоторых вариантах воплощения разбавитель может присутствовать в количестве от приблизительно 35% до приблизительно 90% массы таблетки. В некоторых вариантах воплощения связующий агент может быть выбран из акациевой камеди, альгиновой кислоты, карбомера, натрия карбоксиметилцеллюлозы, декстрина, этилцеллюлозы, желатина, глюкозы, гуаровой камеди, гидроксипропилцеллюлозы, мальтозы, метилцеллюлозы, полиэтиленоксида и повидона. В некоторых примерных вариантах воплощения связующий агент присутствует в количестве от приблизительно 0,5% до приблизительно 5% массы таблетки. В других примерных вариантах воплощения вышеупомянутые препараты содержат приблизительно 0,05-5 г по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, на милилитр или грамм препарата.
[096] Композиции, раскрытые в данном описании, могут применяться местно или вводиться системно.
[097] Фармацевтические композиции, пригодные для перорального (сублингвального) введения, могут включать таблетки для рассасывания, которые могут быть приготовлены из по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, с применением ароматизатора, который обычно выбирают из сахарозы, аравийской камеди, трагакантовой камеди и пастилок.
[098] Фармацевтические композиции, описанные здесь, также могут быть пригодными для парентерального введения, ингаляцией спрея или с помощью имплантируемого резервуара. Твердые носители, например, крахмал, лактоза, микрокристаллическая целлюлоза, алюминия силикат, жидкие носители, например, вода для инъекций, поливиниловый спирт, неионные поверхностно-активные вещества и кукурузное масло, а также любые ингредиенты, подходящие для предусмотренного способа введения. Другие вспомогательные вещества, широко применяемые в фармацевтической рецептуре, включают красители, консерванты, средства для коррекции вкуса и антиоксиданты, такие как витамин Е, витамин А, бутилгидрокситолуол и бутилированный гидроксианизол.
[099] Соединение Формулы А, такое как Форма I или Форма II, описанное в данном документе, также может вводиться интраперитонеально. Также раствор и суспензия соединения могут быть получены растворением или суспендированием соединения в воде, содержащей подходящие поверхностно-активные вещества. Диспергированные суспензии могут быть получены при использовании глицерина, полиэтиленгликоля (ПЭГ) или их смеси с подходящими маслами. Консерванты могут быть добавлены в такие препараты для предупреждения роста микроорганизмов в ходе применения.
[0100] Инъекционный препарат включает раствор или суспензию стерильного порошка в стерильной воде. Во всех случаях такие препараты должны быть стерилизованы и легко извлекаться из шприца, а также должны быть стабильными в условиях производства и хранения и, насколько это возможно, свободны от загрязнения и влияния микроорганизмов. Носители могут представлять собой растворители или диспергирующие агенты и включают воду, спирт и некоторые подходящие масла.
[0101] По меньшей мере один активный фармацевтический ингредиент, выбранный из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, также может вводиться в комбинации с одним или более других активных ингредиентов. При введении в комбинации активные ингредиенты могут быть введены в препараты как отдельные композиции, которые вводят одновременно или последовательно в различные моменты времени, или активные ингредиенты могут быть введены в однодозовой форме, т.е. как единая композиция, при условии, что активные ингредиенты в такой единой однодозовой форме не будут несовместимы с другими активными ингредиентами или компонентами лекарственной формы или при объединении не будут возникать другие нежелательные эффекты.
[0102] В некоторых вариантах воплощения по меньшей мере один активный фармацевтический ингредиент, выбранный из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, может быть введен с одним или более других известных средств для лечения по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, такого как рак, и/или по меньшей мере одного заболевания, отвечающего на ингибирование KDR, такого как связанные с ангиогенезом расстройства.
[0103] Выражение "сопутствующая терапия" (или "комбинированная терапия") или "в комбинации с" в данном описании определяет применение по меньшей мере одного активного фармацевтического ингредиента, выбранного из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, как описано здесь, и одного или более других активных ингредиентов, таких как, например, антинеопластические средства. В данном описании термин "антинеопластическое средство" обозначает любое средство, которое вводят больному раком субъекту для целей лечения рака. Не ограничивающие примеры антинеопластических средств включают: радиотерапию, иммунотерапию, повреждающие ДНК химиотерапевтические агенты и химиотерапевтические агенты, которые нарушают репликацию клеток.
[0104] Не ограничивающие примеры повреждающих ДНК химиотерапевтических агентов включают ингибиторы топоизомеразы I (например, иринотекан, топотекан, камптотецин и их аналоги или метаболиты, а также доксорубицин); ингибиторы топоизомеразы II (например, этопозид, тенипозид и даунорубицин); алкилирующие агенты (например, мелфалан, хлорамбуцил, бусульфан, тиотепа, ифосфамид, кармустин, ломустин, семустин, стрептозоцин, дакарбазин, метотексан, митомицин С и циклофосфамид); интеркаляторы ДНК (например, цисплатин, оксалиплатин и карбоплатин); интеркаляторы ДНК и генераторы свободных радикалов, такие как блеомицин; и миметики нуклеозидов (например, 5-фторурацил, капецитабин, гемцитабин, флударабин, цитарабин, меркаптопурин, тиогуанин, пентостатин и гидроксимочевина).
[0105] Химиотерапевтические средства, которые нарушают репликацию клетки, включают: паклитаксел, доцетаксел и родственные аналоги; винкристин, винбластин и родственные аналоги; талидомид и родственные аналоги (например, СС-5013 и СС-4047); ингибиторы протеинтирозинкиназы (например, иматиниб мезилат и гефтиниб); ингибиторы протеасомы (например, бортезомиб); ингибиторы NF-каппа В, в том числе ингибиторы I каппа В киназы; антитела, связывающие с чрезмерно экспрессируемыми при раке белками, которые, таким образом, регулируют вниз репликацию клеток (например, трастузумаб, ритуксимаб, цетуксимаб и бевацизумаб); и другие ингибиторы белков или ферментов, которые, как доказано, регулируются вверх, чрезмерно экспрессируются или активируются при различных видах рака, ингибирование которых регулирует вниз репликацию клеток.
[0106] При сопутствующей терапии введение каждого из активных ингредиентов может происходить последовательно в схеме с получением благоприятного эффекта комбинации лекарственных средств; и/или сопутствующее введение вышеупомянутых соединений может проводиться в существенной мере одновременно (например, в виде единой лекарственной формы, такой как капсула, содержащей фиксированное соотношение активных ингредиентов, или в виде нескольких отдельных капсул для каждого активного ингредиента и т.д.).
[0107] Таким образом, описанные в данном документе способы не ограничиваются последовательностью введения; по меньшей мере один активный фармацевтический ингредиент, выбранный из соединения Формулы А и/или его фармацевтически приемлемой соли, и Форм I и II соединения Формулы А, описанных здесь, может быть введен до, одновременно или после введения одного или более других активных ингредиентов. [0108] Предложены следующие неограничивающие примеры.
Эксперименты
[0109] Все реагенты, за исключением промежуточных соединений, используемые в данном описании, являются коммерчески доступными. Все названия соединений, за исключением реагентов, образованы с помощью ChemBioDraw Ultra 12,0.
[0110] Если не указано иное, рентгенограммы порошка получены с использованием рентгеновского дифрактометра Bruker D8 ADVANCE, с генерацией радиоволн источником СuKa при 40 мА и 40 кВ, а прибор может работать в интервале 2θ 3-45° с шагом сканирования 0,02° и скоростью сканирования 4°/мин.
[0111] Термический анализ ДСК выполняли на приборе ДСК PerkinElmer 7, где для продувания использовали азот со скоростью потока 50 мл/мин. Образцы исследовали в гофрированных алюминиевых чашках. Приборы калибровали для температуры с использованием индия. Исследование образцов для экспериментов ДСК осуществляли обычным способом со скоростью нагревания 5-10°C/мин в интервале температуры от 25 до 200°C.
[0112] ИК-спектры регистрировали с помощью спектрометра MagnaTI-IR750 (NICOLET), из каждого образца прессованием получали диски KBr.
[0113] Термогравиметрические (TG) кривые, которые могут быть использованы для определения изменений массы материалов как функции температуры, получали с использованием Perkin-Elmer Thermal ТГА7 и N2 для продувания со скоростью потока 50 мл/мин., скорость нагревания составляла 10°C/мин.
Пример 1
Синтез N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида
Стадия 1: Синтез 5-((2-хлорпиримидин-4-ил)окси)-2-метил-1Н-индола (Соединение 3):
[0114] В 3-горлую круглодонную колбу емкостью 50 л, оборудованную механической мешалкой, воронкой для добавления и термометром, помещают 2-метил-1H-индол-5-ол (соединение 1, 3 кг), безводный ацетонитрил (9 л) и калия карбонат (4,2 кг). Реакционную смесь охлаждают до 0-5°C при перемешивании в атмосфере азота N2. Раствор 2,4-дихлорпиримидина (Соединение 2, 3,05 кг в 9 л ацетонитрила) добавляют к реакционной смеси по каплям, поддерживая внутреннюю температуру реакционной смеси в интервале от 0 до 5°C. После завершения добавления реакционной смеси дают нагреться до температуры в интервале от 5 до 10°C напротяжении периода 4-8 часов. После завершения реакции реакционную смесь при перемешивании выливают в 54 л дистиллированной воды в реакторе емкостью 100 л и перемешивают еще в течение 1 часа при комнатной температуре. Осадок отделяют фильтрацией, а остаток на фильтре промывают чистой водой с получением Соединения 3 (5,7 кг).
Стадия 2: Синтез N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида (Соединение Формулы А):
[0115] В 3-горлую круглодонную колбу емкостью 10 л, оборудованную механической мешалкой и термометром, помещают Соединение 3 (1,05 кг), 1-(3-аминофенил)-N-(2-(диметиламино)этил)метансульфонамид (Соединение 4, 1,06 кг), n-толуолсульфоновую кислоту (0,86 кг) и N,N-диметилформамид (5,25 л). Реакционную смесь осторожно нагревают до температуры в интервале от 55 до 65°C и перемешивают при указанной температуре в течение 16-20 час. После завершения реакции реакционную смесь охлаждают до комнатной температуры и порциями перенося в 5% водный раствор калия карбоната. После завершения добавления полученную суспензию перемешивают еще в течение 1-2 часов. Неочищенный продукт отделяют фильтрацией, а и влажный остаток на фильтре переносят в реактор емкостью 200 л.
[0116] В реактор добавляют толуол (104 кг) и суспензию кипятят с обратным холодильником для удаления воды с использованием ловушки Дина-Старка. После удаления воды, раствор упаривают до конечного объема 30-40 л при сниженном давлении, охлаждают до 15-20°C. Продукт собирают и сушат с получением названного в заголовке соединения (Соединение Формулы А, 1,07 кг). Далее полученный материал может быть использован для получения новых форм соединения Формулы А, таких как Форма I и/или Форма II.
Пример 2
Исследование in vitro активности ингибирования KDR киназы
[0117] Исследованные соединения:
- N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамид (Соединение Формулы А1
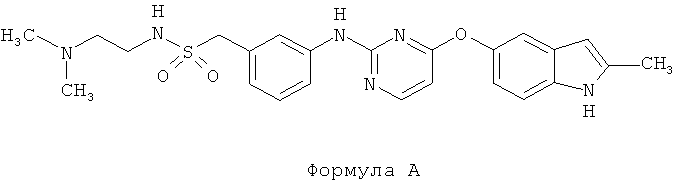
- N-метил-1-(3-((4-((2-метил-1Н-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамид (Соединение Формулы В)
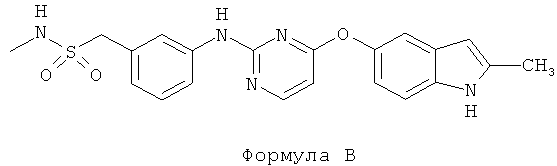
- N4 -(4-фтор-2-метил-1H-индол-5-ил)-N2-(3-(2-
морфолиноэтокси)фенил)пиримидин-2,4-диамин (Соединение Формулы С)
[0118] Способность перечисленных выше 3 соединений ингибировать KDR киназу исследовали с использованием набора для анализа Z-Lyte.
Материалы и способы:
[0119] Пептид Z'-LYTE™ Tyrl (Invitrogen, кат. №PV3190) использовали для анализа активности вышеперечисленных соединений в качестве ингибиторов KDR киназы. Система анализа содержала 300 нг/мл рекомбинантного каталитического домена KDR человека, 10 мкМ АТФ, 1 мкМ субстрата пептида и исследуемое соединение в серии концентраций на 384-луночном планшете (Thermo Labsystems, кат. №7805); общий объем составлял 10 мкл. Ингибирование фермента проводили при комнатной температуре (25°C) в течение 1 часа при встряхивании, с последующим добавлением 5 мкл усилителя, и инкубировали еще в течение 1 часа при комнатной температуре и встряхивании. 5 мкл останавливающего раствора добавляли для остановки реакции. Активность исследуемого соединения, ингибирующую KDR киназу, вычисляли на основе способа, рекомендованного производителем. Значения IC50 активности ингибирования KDR киназы вычисляли с использованием программного обеспечения XLfit.
Способ анализа:
[0120] (1) Разведение исследуемых соединений: каждое из вышеуказанных 3 соединений растворяют в ДМСО для получения 10 мкМ запасного раствора и хранят при температуре -20°C в морозильной камере. Запасной раствор перед использованием разбавляют 8% ДМСО до концентрации, в 4 раза превышающей целевую концентрацию для анализа.
[0121] (2) 1,33× буфер анализа: Разбавляют 5× буфер анализа ddH2O до 1,33× буфер анализа.
[0122] (3) Разведение каталитического домена KDR киназы (KDR CD): разбавляют оригинальный запасной раствор KDR CD 1,33× буфер анализа в 10 раз. Отбирают аликвоты по 5 мкл/флакон и хранят при температуре -80°C. Следует избегать повторного замораживания и оттаивания.
[0123] (4) Смесь киназа/субстрат: добавляют запасной раствор KDR CD и пептид Tyrl к 1,33× буфер анализа с получением смеси, содержащей 0,6 нг/мкл KDR CD, и разбавленный в 250 раз пептид Tyrl. Выдерживают смесь на льду до использования.
[0124] (5) Смесь для контрольной лунки СЗ: разбавляют фосфо-пептидный субстрат 1,33× буфер анализа в 250 раз. Осторожно перемешивают и выдерживают на льду.
[0125] (6) Раствор АТФ: разбавляют 10 мМ запасной АТФ раствор ddH2O в 250 раз. Получают 40 мкМ раствора АТФ и отбирают аликвоты по 100 мкл/флакон, и хранят при температуре -20°C.
[0126] (7) Ингибирование киназы: добавляют следующие компоненты по очереди на 384-луночный планшет. Лунки в двойном повторении исследуют для каждой концентрации каждого исследуемого соединения, и среднее значение используют для вычисления.
[0127] а) Добавляют 2,5 мкл разбавленного раствора исследуемого соединения, полученного на стадии (1) во все лунки, за исключением контрольных лунок C1, С2 и С3. Добавляют 2,5 мкл 8% ДМСО вместо раствора исследуемого соединения в контрольные лунки C1, С2, С3.
[0128] б) Добавляют 5 мкл смеси киназа-субстрат, полученной на стадии (4) во все лунки, в том числе в контрольные лунки С1 и С2, но не в лунку С3. 5 мкл смеси С3, полученной на стадии (5), добавляют в контрольную лунку С3.
[0129] в) Добавляют 2,5 мкл 40 мкМ раствора АТФ, полученного на стадии (6) во все лунки, в том числе в контрольную лунку С2, но не в лунки С1 и С3. 2,5 мкл 1,33× буфер анализа добавляют в контрольные лунки С1 и С3 вместо раствора АТФ.
[0130] г) Планшет коротко центрифугируют со скоростью 1000 об/мин для осаждения всех компонентов реакции в лунке. Запечатывают планшет алюминиевой фольгой и дают реакции протекать при комнатной температуре (25°C) в течение 1 часа при встряхивании (250 об/мин).
[0131] д) Разведение раствора усилителя (непосредственно перед использованием): в соответствии с рекомендациями производителя разбавляют запасной раствор усилителя проявляющим буфером для разбавления в 128 раз.
[0132] е) Усиление флуоресценции: добавляют 5 мкл/лунку разбавленного раствора усилителя во все лунки, коротко центрифугируют со скоростью 1000 об./мин., снова запечатывают планшет и дают реакции протекать при комнатной температуре в течение еще 1 часа при встряхивании.
[0133] ж) Добавляют 5 мкл/лунку останавливающего раствора во все лунки, коротко центрифугируют со скоростью 1000 об/мин. Перемешивают при комнатной температуре в течение 2 минут при встряхивании и считывают сигнал флуоресценции на приборе Victor3 (Perkin Elmer) при длине волны возбуждения 400 нм, эмиссии - 445 нм/530 нм.
[0134] Вычисление активности ингибирования KDR киназы:
(1) Вычисление ER (соотношение эмиссии):
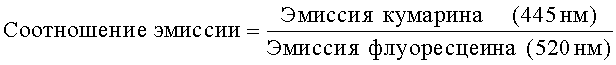
(2) Вычисление скорости фосфорилирования (%)
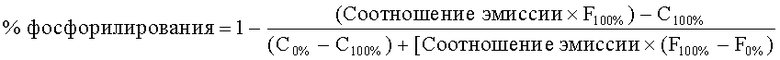
где
Соотношение эмиссии=соотношение кумарин/флуоресцеин в лунках с образцом
С100%=средний уровень сигнала эмиссии кумарина от 100% фос. контроля (С3, 445 нм).
С0%=средний уровень сигнала эмиссии кумарина от 0% фос. контроля (С1, 445 нм).
F100%=средний сигнал эмиссии флуоресцеина от 100% фос. контроля (С3, 520 нм).
F0%=средний сигнал эмиссии флуоресцеина от 0% фос. контроля (С1, 520 нм).
[0135] На основе приведенных выше условий анализа определена активность ингибирования KDR киназы соединениями Формулы А, В и С.
[0136] Результаты: значения 1С5о активности ингибирования KDR киназы для соединений Формулы А, В, С составляют 0,021 мкМ, 0,038 мкМ и 0,111 мкМ, соответственно.
Пример 3
Исследовании in vitro активности ингибирования FGFR1 киназы
[0137] В анализе активности FGFR1 киназы использовали технологию Transcreener FP (Bellbrook Labs). Реакцию киназы проводили на 96-луночных половинных черных планшетах (Greiner, кат. №675076). В каждую лунку добавляли 5 мкл исследуемого соединения в 5% ДМСО, 10 мкл 0,3 нг/мкл FGFR1 киназы (Invitrogen, PV3146), разбавленной буфером анализа. Реакцию инициировали добавлением 10 мкл 62,5 нг/мкл поли (Glu:Tyr, 4:1) субстрата (Sigma, Р0275) и 25 мкмоль/л смеси АТФ, после чего инкубировали в течение 60 минут при комнатной температуре. Конечные условия анализа киназы были следующими: 10 мкМ АТФ, 0,12 нг/мкл FGFR1 киназы, 25 нг/мкл субстрата, 53,6 ммоль/л HEPES (pH 7,5), 21,6 ммоль/л MgCl2, 0,536 ммоль/л MnCl2, 1 ммоль/л дитиотрейтола (ДТТ) и 0,01% Тритон Х-100, 1% ДМСО.
[0138] В то же время получали стандартную кривую АДФ. Стандартная кривая имитировала реакцию киназы в отсутствие исследуемого соединения, киназы и липидного субстрата. Стандартная кривая включала точки 12 концентраций и в целом [АТФ+АДФ] простиралась от 10 мкМ до 0,01 мкМ. 5 мкл 5% ДМСО и 10 мкл буфера анализа добавляли вместо исследуемого соединения и FGFR1 киназы, соответственно. Другие условия были такими же, как описано выше.
[0139] После протекания реакции в течение 60 минут при комнатной температуре добавляли 25 мкл реагента из набора Transcreener Kinase Kit - Смесь для обнаружения АДФ (Bellbrook Labs), и реакция протекала еще в течение 1,0 часа. Затем планшеты считывали на приборе Tecan Infinite F500 на длине волны возбуждения 610 нм и эмиссии 670 нм. Стандартную кривую получали с использованием программного обеспечения Origin 8,0. Ингибирующее влияние исследуемого соединения на выработку АДФ вычисляли на основе концентрации АДФ, рассчитанной с помощью стандартной кривой. Значения IC50 получали с использованием программного обеспечения XLfit 2,0. Результаты
Пример 4: Анализ hERG
4.1 Культура клеток
[0140] Для данного исследования использовали клеточную линию СНО, стабильно трансфицированную кДНК hERG и экспрессирующую каналы hERG. Клетки культивировали в среде, содержащей:
Модифицированную Дульбекко-среду Игла (DMEM/F12)
10% (об/об) инактивированной нагреванием сыворотки телячьего эмбриона (СТЭ)
1% (об/об) пенициллина/стрептомицина
500 мкг/мл реактива Geneticin® (G418)
[0141] Перед началом анализа клетки собирали с помощью Accumax (Innovative Cell Technologies).
[0142] Для регистрации электрофизиологических данных использовали следующие растворы.
4.2 Раствор
4.3 Система регистрации
[0144] Регистрацию цельных клеток осуществляли с использованием прибора 700 В (Axon Instruments). Для клеток устанавливали гальванический зажим при потенциале удерживания -80 мВ. Ток hERG активировали деполяризацией при +20 мВ в течение 2 с, после чего ток поворачивали в обратную сторону к -50 мВ на 2 с для устранения инактивации и наблюдали деактивацию остаточного тока. Первую стадию при -50 мВ использовали в качестве фонового значения для измерения пиковой амплитуды остаточного тока.
4.4 Обработка и разведение соединения
[0145] Готовили запасной раствор исследуемого соединения в 10 мМ ДМСО в стеклянном флаконе. Запасной раствор энергично перемешивали в течение 10 мин. при комнатной температуре. Запасной раствор разбавляли в стеклянном флаконе с использованием Внешнего раствора; разведение готовили не раньше, чем за 30 мин. перед использованием. Равные количества ДМСО (0,1%) присутствовали в конечном разведении.
4.5 Электрофизиологические методики
[0146] После достижения цельноклеточной конфигурации состояние клеток контролировали в течение 90 с для оценки стабильности и промывали Внешним раствором в течение 66 с. Далее описанный выше протокол напряжения применяли к клеткам каждые 20 с напротяжении всей методики. Только стабильные клетки с зарегистрированными параметрами выше порога использовали в методике исследования соединения.
[0147] Внешний раствор, содержащий 0,1% ДМСО (растворитель), наносили на клетки для получения фонового значения. После стабилизации тока в течение 3 мин. наносили исследуемое соединение. Раствор исследуемого соединения добавляли в 4 стадии, и клетки выдерживали в исследуемом растворе до тех пор, пока влияние соединения не достигало фазы плато или не более 6 мин. Далее добавляли положительный контроль (10 нМ цизаприда). Проводили промывание внешним раствором до тех пор, пока восстановление тока не достигало фазы плато.
4.6 Анализ данных
[0148] Данные анализировали с использованием Clampfit (оба от Axon Instruments) и Origin 7 (Originlab Corporation).
[0149] Соединение Формулы С ингибировало ток hERG со значением IC50 0,547 мкМ, тогда как соединение Формулы А ингибировало hERG со значением IC50 6,8 мкМ.
Пример 5: Исследование фармакокинетики (ФК)
[0150] Методика эксперимента: Фармакокинетику исследуемого соединения изучали на самцах мышей ICR (n=6 для каждой группы, масса 20-30 г) после однократного внутривенного (в/в) и перорального (п/о) введения в дозе 2,5 и 10 мг/кг, соответственно. Для в/в введения соединение растворяли в смеси ДМСО (0,25%)-солютол (10%)-этанол (10%)-физиологический раствор соли (79,75%) в концентрации 0,25 мг/мл. При пероральном введении готовили препарат (1 мг/мл) в 0,5% КМЦ-Na. После в/в или п/о введения образцы крови отбирали из глазной вены в точках времени 0 (до введения дозы), 5, 15, 30 мин. и 1, 1,5, 2, 4, 8, 24 часа, проводили антикоагулянтную обработку с помощью гепарина-Na. После центрифугирования образцов плазму отделяли, а белок осаждали ацетонитрилом (содержащим внутренний стандарт). Далее концентрацию исследуемого соединения в полученных образцах плазмы определяли способом ЖХ/МС/МС.
[0151] Результаты: После перорального введения в дозе 10 мг/кг значения AUC и Cmax Соединения В составляли 26 нг/мл час и 20 нг/мл, соответственно. При пероральном введении такой же дозы (10 мг/кг) значения AUC и Сmax Соединения А составляли 397 нг/мл час и 138 нг/мл, соответственно. Как можно увидеть, после перорального введения мышам соединение Формулы А продемонстрировало намного более высокую степень контакта для плазмы, т.е. более высокие значения AUC и Сmax, чем Соединение В.
[0152] В следующих примерах 6-10 показаны различные способы получения Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
Получение Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида
Пример 6
[0153] Соединение Формулы А (151 мг) растворяют в 3 мл этанола при нагревании и перемешивании. Раствор фильтруют в горячем состоянии для удаления нерастворимых частиц. Фильтрат нагревают еще в течение 5 минут с получением прозрачного раствора и затем медленно охлаждают до комнатной температуры при перемешивании. При комнатной температуре смесь перемешивают еще в течение 4 часов со средней скоростью перемешивания (100 об/мин). Осадок отделяют фильтрацией и сушат при 60°C, выдерживая при этой температуре в течение 2 часов под вакуумом, с получением белого кристаллического порошка (Форма I, 136 мг), Тпл (ДСК): 166,6-168,2°C.
[0154] Полученная рентгенограмма порошка Формы I показана на фиг.1. Она содержит пики (2θ), выбранные из тех, которые имеют следующие значения: 7,1, 8,0, 8,7, 11,1, 11,8, где каждый из углов дифракции составляет ±0,2° (2θ) и где характерные пики (2θ) идентифицированы как 7,1, 8,0 и 8,7.
[0155] Исследование способом ДСК показало, что температура плавления полученной Формы I составляла 166,6-168,2°C.
Пример 7
[0156] Соединение Формулы А (152 мг) растворяют в 3 мл ацетонитрила при нагревании и перемешивании. Перемешивание и нагревание продолжают до полного растворения. Нерастворимые частицы удаляют фильтрацией в горячем состоянии. Фильтрат кипятят с обратным холодильником в течение 5 минут с получением прозрачного раствора и затем дают остыть до комнатной температуры при перемешивании со средней скоростью (100 об/мин).
[0157] Затем суспензию перемешивают еще в течение 2 часов, осадок отделяют фильтрацией и сушат при температуре 60°C в вакуумной печи в течение 4 часов с получением продукта Формы I (113 мг, выход 74,3%).
[0158] Рентгенограмма порошка является в значительной степени сходной с рентгенограммой Формы I, полученной в Примере 5.
Пример 8
[0159] Соединение Формулы А (141,8 мг) растворяют в 8 мл толуола при нагревании и перемешивании. Перемешивание и нагревание продолжают до полного растворения. Затем смеси дают остыть до комнатной температуры при перемешивании со средней скоростью (100 об/мин). После этого суспензию перемешивают еще в течение 2 часов, осадок отделяют фильтрацией и сушат при температуре 60°C в вакуумной печи в течение 4 часов с получением продукта Формы I (86 мг).
[0160] Рентгенограмма порошка в существенной мере сходна с рентгенограммой продукта Формы I, полученной в Примере 5.
Пример 9
[0161] Соединение А (150 мг) растворяют в 2,5 мл ацетона при нагревании и перемешивании. Нерастворимые частицы удаляют горячей фильтрацией. Фильтрат кипятят с обратным холодильником в течение 5 минут с получением прозрачного раствора. Далее к раствору добавляют 2,5 мл воды. По окончании добавления раствору дают остыть до комнатной температуры при перемешивании со средней скоростью (100 об/мин).
[0162] Суспензию перемешивают в течение 4 часов. Осадок отделяют фильтрацией и сушат при температуре 60°C в вакуумной печи с получением продукта Формы I (123 мг). Температура плавления (по данным ДСК): 165,6-167,5°C.
[0163] Рентгенограмма порошка полученного продукта в существенной мере сходна с рентгенограммой продукта Формы I, полученной в Примере 5.
Пример 10
[0164] Соединение А (180,3 мг) растворяют в 6,0 мл метанола при нагревании и перемешивании. Перемешивание и нагревание продолжают до полного растворения. Нерастворимые частицы удаляют фильтрацией в горячем состоянии. Фильтрат кипятят с обратным холодильником в течение 5 минут с получением прозрачного раствора. К полученному раствору медленно добавляют гептан (6,0 мл). По окончании добавления смесь упаривают до конечного объема 10 мл и затем дают остыть до комнатной температуры.
[0165] Осадок отделяют фильтрацией и сушат при температуре 60°C в вакуумной печи с получением продукта Формы I (118 мг).
[0166] Рентгенограмма порошка является в существенной мере сходной с рентгенограммой Формы I, полученной в Примере 6.
[0167] В следующих примерах 11-12 показаны различные способы получения Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
Получение Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида
Пример 11
[0168] Соединение А (2,4 г) растворяют в 35 мл ацетона при нагревании и перемешивании. Перемешивание и нагревание продолжают до полного растворения. Нерастворимые частицы удаляют фильтрацией в горячем состоянии. Фильтрат кипятят с обратным холодильником в течение 5 минут с получением прозрачного раствора. Затем к раствору добавляют гептан (20 мл) при перемешивании. После окончания добавления смесь быстро охлаждают до 0-5°C при перемешивании. При указанной температуре смесь перемешивают еще в течение 4 часов.
[0169] Осадок отделяют фильтрацией и сушат при 60°C, выдерживая при этой температуре в течение 2 часов в вакуумной печи, с получением продукта Формы II (2,0 г, выход 83,3%), Тпл (ДСК): 160,3-161,6°C.
[0170] Рентгенограмма порошка полученной Формы II показана на фиг.5. Она содержит пики (29), некоторые из которых имеют приблизительно следующие значения: 6,8, 9,8, 10,5, 10,7, 13,6, 15,0, где каждый из углов дифракции составляет ±0,2° (2θ) и где характерные пики (29) идентифицированы как 6,8, 9,8, 10,5 и 10,7.
Пример 12
[0171] Соединение А (17 г) растворяют в 425 мл этанола при нагревании и перемешивании. Перемешивание и нагревание продолжают до полного растворения. Нерастворимые частицы удаляют фильтрацией в горячем состоянии. Фильтрат кипятят с обратным холодильником в течение 5 минут с получением прозрачного раствора. Раствор охлаждают до 50°C и добавляют 0,34 г (2% масса/массу) затравки Формы II. По окончании добавления раствору дают остыть до комнатной температуры. Смесь перемешивают еще в течение 4 часов при комнатной температуре, осадок отделяют фильтрацией и сушат при температуре 60°C в вакуумной печи с получением 15 г продукта кристаллической Формы II, выход 88,0%.
[0172] Рентгенограмма порошка является в существенной мере сходной с рентгенограммой продукта Формы II, полученной в Примере 11.
[0173] Измерение ДСК показало, что температура появления Формы II составляла 160,3°C с пиком при 161,6°C.
Пример 13
Исследования гигроскопичности Формы I и Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида
[0174] Гигроскопичность Формы I и Формы II исследовали по способу насыщенного раствора соли.
[0175] Приблизительно по 1 г образцов Формы I и Формы II, соответственно, аккуратно взвешивали, и образцы помещали в эксикатор, содержащий насыщенный раствор NaCl. Эксикатор закрывали и оставляли на 10 дней при температуре 25°C. Затем образцы извлекали и снова взвешивали, после чего рассчитывали увеличение массы.
[0176] Обнаружено, что образец Формы I не гигроскопичен, и для него увеличение массы до 92,5% относительной влажности составляло менее 0,1%. Обнаружено, что образец Формы II слегка гигроскопичен с увеличением массы менее 1%. Образцы Формы I и Формы II после исследования анализировали с помощью рентгеновского дифрактометра; обнаружено, что полученные дифрактограммы сравнимы с дифрактограммами, представленными на фиг.1 и 5, соответственно.
[0177] Результаты анализа гигроскопичности показывают, что как Форма I, так и Форма II являются стабильными в исследуемых условиях влажности, а легкая поверхностная абсорбция влаги не изменяет кристаллической формы. Таким образом, Форма I и Форма II могут быть использованы в фармацевтическом продукте для применения, описанного здесь.
Пример 14
Сравнение термодинамической стабильности
[0178] Суспензию смеси Формы I и Формы II в метаноле перемешивали при 60°C, выдерживая при этой температуре в течение 20 часов. Далее суспензию фильтровали сквозь воронку Бюхнера с бумажным диском и сушили в вакуумной печи. Высушенный образец далее анализировали способом рентгеноструктурного анализа порошка, и было обнаружено, что дифрактограмма является сравнимой с представленной на фиг.1.
[0179] Характерные пики дифракции Формы II не были обнаружены на полученной рентгеноструктурной дифрактограмме, что является свидетельством превращения Формы II в суспензии в Форму I в ходе процесса суспендирования, причем Форма I является с физической и/или термодинамической точки зрения более стабильной, чем Форма II в трансформирующихся условиях.
[0180] Таким образом, Форма I также может быть получена путем превращения Формы II в подходящих растворителях.
[0181] Результаты:
- Форма I является стабильной как в условиях высокой влажности, так и в растворителях для перекристаллизации, и может быть получена в промышленном масштабе,
- Форма II может быть использована в качестве промежуточного соединения для получения Формы I, которая может использоваться в качестве подходящей твердофазной кристаллической формы в фармацевтической лекарственной форме. При этом Форма II также может использоваться в лекарственной форме благодаря ее высокой стабильности.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2712187C2 |
| ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 2008 |
|
RU2455994C2 |
| Гетероциклические соединения в качестве ингибиторов киназы RET | 2017 |
|
RU2742115C2 |
| ПРОИЗВОДНЫЕ ГИДАНТОИНА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ММР | 2007 |
|
RU2463301C2 |
| ПРОИЗВОДНЫЕ БИЦИКЛИЧЕСКИХ АМИНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ ТИРОЗИНКИНАЗЫ | 2007 |
|
RU2465275C2 |
| Новое производное пиридо [3,4-d] пиримидин-8-она, обладающее ингибирующей протеинкиназы активностью, и фармацевтическая композиция для предупреждения, облегчения или лечения рака, содержащее указанное выше | 2020 |
|
RU2780168C1 |
| 2,6-ЗАМЕЩЕННЫЕ-4-МОНОЗАМЕЩЕННЫЙ АМИНО-ПИРИМИДИНЫ КАК АНТАГОНИСТЫ РЕЦЕПТОРА ПРОСТАГЛАНДИНА D2 | 2005 |
|
RU2417990C2 |
| ПРОИЗВОДНЫЕ 4-АМИНО-6-ФЕНИЛПИРРОЛО[2,3] ПИРИМИДИНА, ОБЛАДАЮЩИЕ ИНГИБИРУЮЩИМ ДЕЙСТВИЕМ В ОТНОШЕНИИ ДЕЙСТВИЯ ТИРОЗИНКИНАЗЫ, ИХ ПРИМЕНЕНИЕ И СПОСОБЫ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2002 |
|
RU2318826C2 |
| 6-АРИЛ-4-МОРФОЛИН-1-ИЛПИРИДОНЫ, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ РАКА ИЛИ ДИАБЕТА | 2017 |
|
RU2754664C2 |
| СОЕДИНЕНИЯ ПИРИМИДИНА И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ РАКА | 2019 |
|
RU2807277C2 |
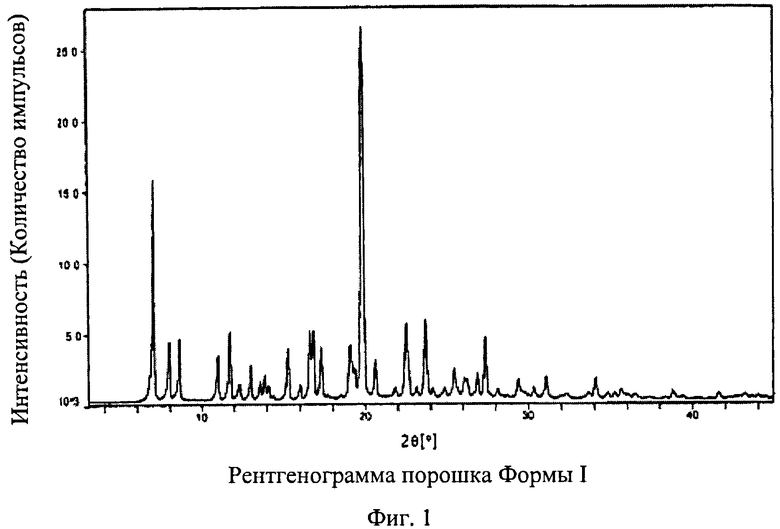
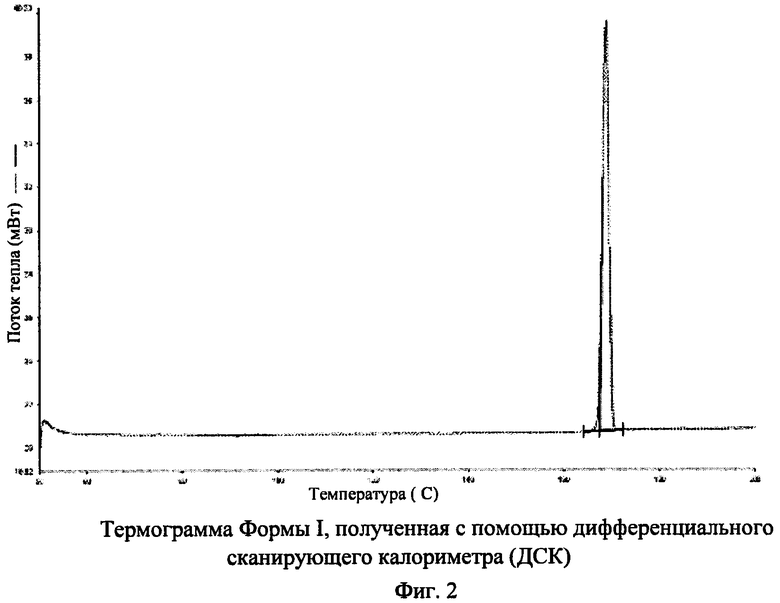
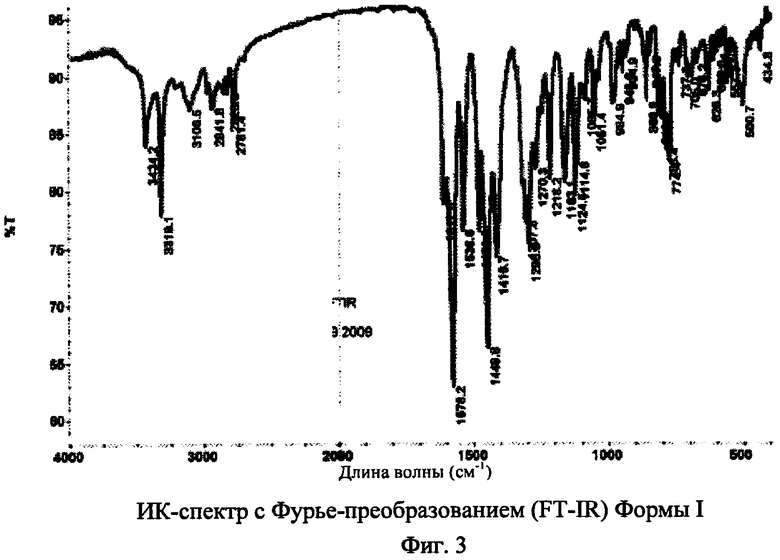
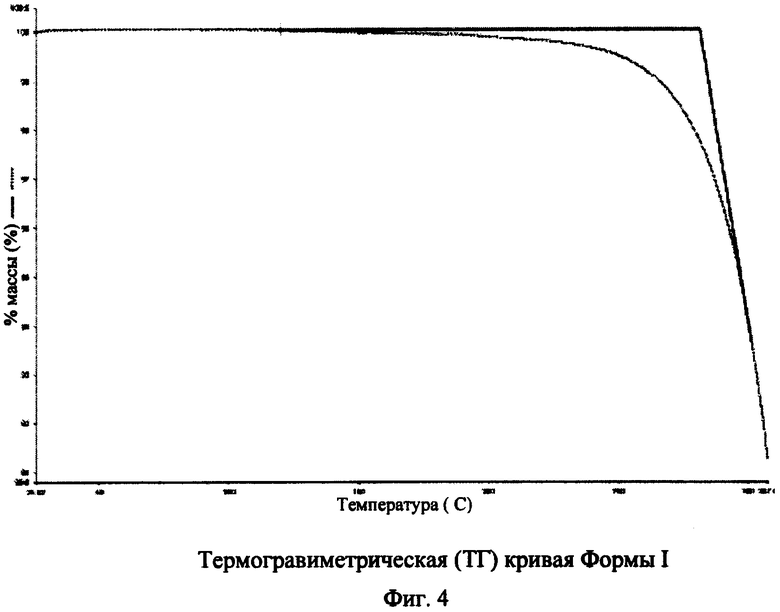
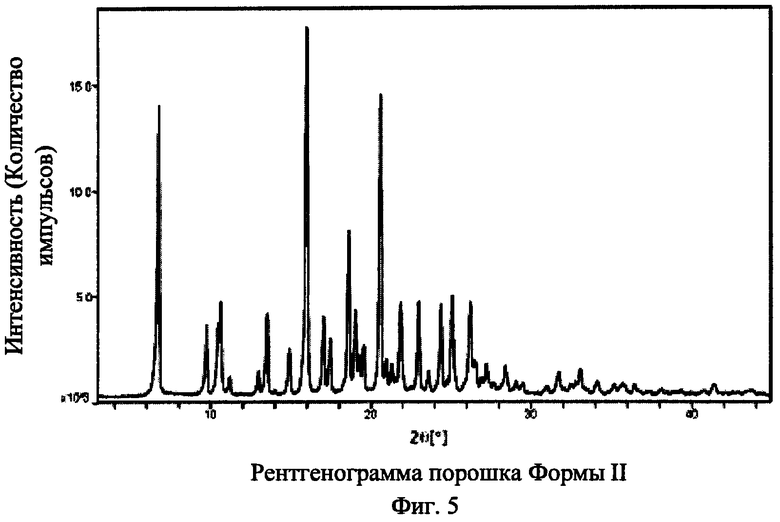
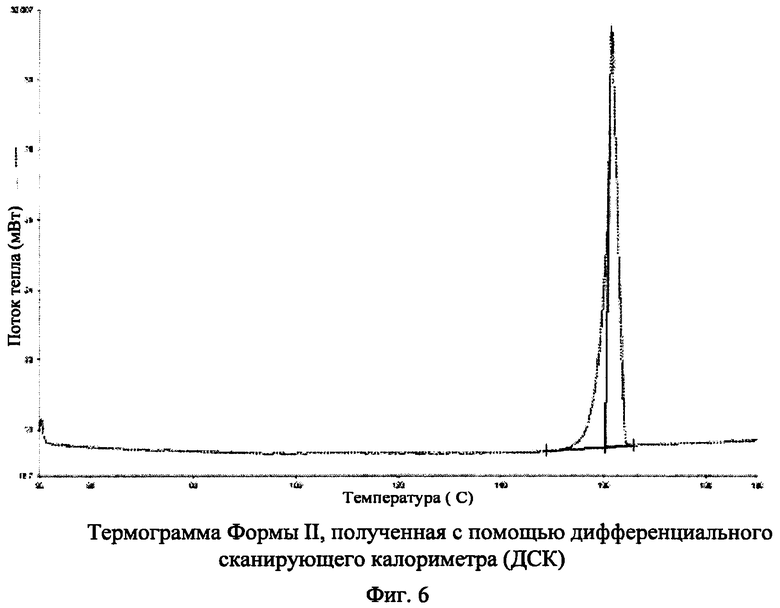
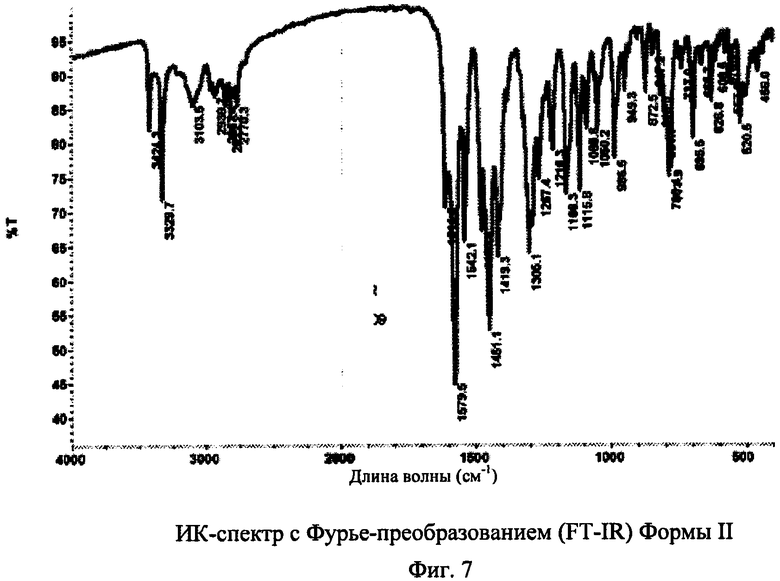
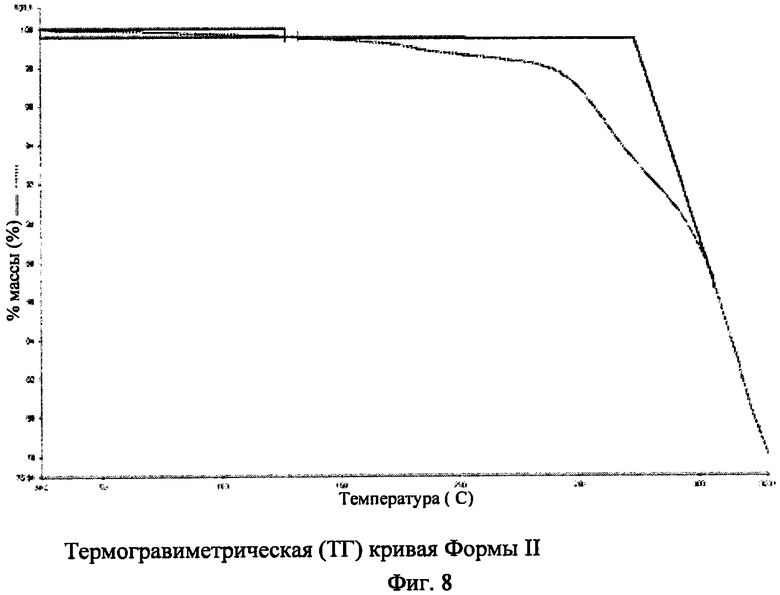
Изобретение относится к новому соединению- N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1Н-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамиду формулы А и/или его фармацевтически приемлемой соли, которые обладают свойствами ингибитора KDR и/или FGFR1 киназы. Соединения могут найти применение для лечения расстройств, связанных с ангиогенезом, опосредованным KDR, таких как рак и возрастная дегенерация желтого пятна, либо различных раковых заболеваний, отвечающих на ингибирование FGFR1. Соединение (А) соответствует нижеуказанной структурной формуле
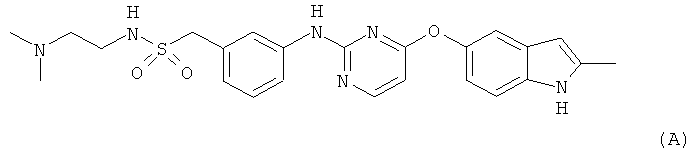
Изобретение также относится к кристаллическим формам I и II указанного соединения А и способам их получения, фармацевтическим композициям и способу лечения. 16 н. и 22 з.п. ф-лы, 8 ил., 14 пр.
1. N-(2-(Диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамид
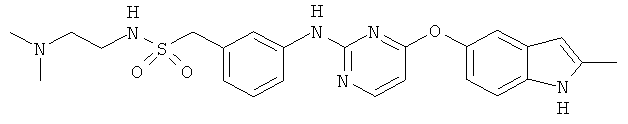
и/или его фармацевтически приемлемая соль.
2. Фармацевтическая композиция, обладающая свойствами ингибитора KDR и/или FGFRI киназы, содержащая по меньшей мере один фармацевтически приемлемый носитель и эффективное количество N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида
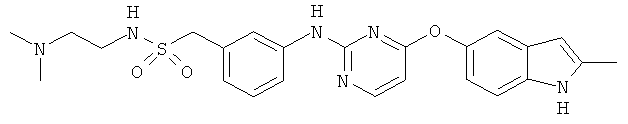 ,
,
и/или его фармацевтически приемлемой соли.
3. Форма I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, которая характеризуется порошковой дифракционной рентгенограммой, содержащей пик, который имеет значение угла 2θ, равное 8,0±0,2.
4. Форма I по п.3, отличающаяся тем, что Форма I по существу свободна от аморфной формы N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, а также по существу свободна от Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
5. Способ получения Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.3, включающий:
(1) смешивание N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида по меньшей мере с одним органическим растворителем, в котором растворяется данное вещество, и последующее нагревание смеси до температуры кипения с обратным холодильником с получением раствора;
(2) охлаждение раствора до комнатной температуры; и
(3) выделение Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
6. Способ по п.5, отличающийся тем, что по меньшей мере один органический растворитель, в котором растворяется вещество, выбирают из спиртов и апротонных растворителей.
7. Способ по п.5, отличающийся тем, что спирты выбирают из метанола, этанола и изопропанола.
8. Способ по п.5, отличающийся тем, что апротонные растворители выбирают из ацетона, ацетонитрила, этилацетата, толуола, дихлорметана и N,N-диметилформамида.
9. Способ получения Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.3, включающий:
(1) смешивание N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида по меньшей мере с одним растворителем, в котором растворяется вещество, и последующее нагревание смеси до температуры кипения с обратным холодильником с получением первого раствора;
(2) добавление по меньшей мере одного органического растворителя, в котором данное вещество не растворяется, к первому раствору при температуре кипения с обратным холодильником с получением второго раствора;
(3) остывание второго раствора при комнатной температуре; и
(4) выделение Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
10. Способ по п.9, отличающийся тем, что по меньшей мере один растворитель, в котором растворяется вещество, выбирают из метанола, этанола, ацетона, ацетонитрила и N-диметилформамида.
11. Способ по п.9, отличающийся тем, что по меньшей мере один растворитель, в котором не растворяется вещество, выбирают из воды, гептана, гексана и этилацетата.
12. Способ по п.9, отличающийся тем, что объемное соотношение по меньшей мере одного растворителя, в котором растворяется вещество, и по меньшей мере одного растворителя, в котором не растворяется вещество, варьирует от 1:3 до 5:1.
13. Фармацевтическая композиция, обладающая свойствами ингибитора KDR и/или FGFRI киназы, содержащая по меньшей мере один фармацевтически приемлемый носитель и эффективное количество Формы I N-(1-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида.
14. Форма II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, которая характеризуется порошковой дифракционной рентгенограммой, содержащей пик, который имеет значение угла 29, равное 9,8±0,2.
15. Форма II по п.14, отличающаяся тем, что Форма II в существенной мере свободна от аморфной формы соединения Формулы А, а также в существенной мере свободна от Формы I соединения Формулы А.
16. Способ получения Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.14, включающий:
(1) смешивание N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида по меньшей мере с одним растворителем, в котором растворяется вещество, и нагревание смеси с обратным холодильником с получением первого раствора;
(2) добавление по меньшей мере одного растворителя, в котором не растворяется вещество, к первому раствору при температуре кипения с обратным холодильником с получением второго раствора;
(3) охлаждение второго раствора до 0-5°С при скорости охлаждения 1-40°С/мин; и
(4) выделение Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.14.
17. Способ по п.16, отличающийся тем, что по меньшей мере один растворитель, в котором растворяется вещество, выбирают из спиртов и апротонных растворителей.
18. Способ по п.17, отличающийся тем, что спирты выбирают из метанола и этанола.
19. Способ по п.17, отличающийся тем, что апротонные растворители выбирают из ацетона, ацетонитрила, этилацетата, толуола, дихлорметана и N,N-диметилформамида.
20. Способ получения Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.14, включающий:
(1) смешивание N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида по меньшей мере с одним растворителем, в котором растворяется вещество, и нагревание смеси до кипения с обратным холодильником с получением раствора;
(2) охлаждение раствора, с последующим внесением затравки Формы II в указанный охлажденный раствор;
(3) охлаждение указанного раствора с затравкой до комнатной температуры, и
(4) выделение Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.14.
21. Способ по п.20, отличающийся тем, что раствор медленно охлаждают до 45-55°С.
22. Способ по п.20, отличающийся тем, что раствор с затравкой медленно охлаждают до комнатной температуры.
23. Способ по п.20, отличающийся тем, что по меньшей мере один растворитель, в котором растворяется вещество, выбирают из спиртов и апротонных растворителей.
24. Способ по п.23, отличающийся тем, что спирты выбирают из метанола и этанола.
25. Способ по п.23, отличающийся тем, что апротонные растворители выбирают из ацетона, ацетонитрила, этилацетата, толуола, дихлорметана и N,N-диметилформамида.
26. Фармацевтическая композиция, обладающая свойствами ингибитора KDR и/или FGFRI киназы, содержащая по меньшей мере один фармацевтически приемлемый носитель и эффективное количество Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.14.
27. Способ лечения субъекта, нуждающегося в лечении по меньшей мере одного связанного с ангиогенезом расстройства, опосредованного KDR активностью, включающий введение указанному субъекту, который в этом нуждается, эффективного количества N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида и/или его фармацевтически приемлемых солей.
28. Способ по п.27, отличающийся тем, что по меньшей мере одно связанное с ангиогенезом расстройство выбирают из рака и возрастной дегенерации желтого пятна.
29. Способ лечения субъекта, нуждающегося в лечении по меньшей мере одного связанного с ангиогенезом расстройства, опосредованного KDR активностью, включающий введение указанному субъекту, который в этом нуждается, эффективного количества Формы I N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.3.
30. Способ по п.29, отличающийся тем, что по меньшей мере одно связанное с ангиогенезом расстройство выбирают из рака и возрастной дегенерации желтого пятна.
31. Способ лечения субъекта, нуждающегося в лечении по меньшей мере одного связанного с ангиогенезом расстройства, опосредованного KDR активностью, который включает введение указанному субъекту, который в этом нуждается, эффективного количества Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида, охарактеризованной в п.14.
32. Способ по п.31, отличающийся тем, что по меньшей мере одно связанное с ангиогенезом расстройство выбрано из рака и возрастной дегенерации желтого пятна.
33. Способ лечения субъекта с установленной потребностью в лечении по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, который включает введение указанному субъекту, который в этом нуждается, эффективного количества N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)метансульфонамида и/или его фармацевтически приемлемых солей.
34. Способ по п.33, отличающийся тем, что по меньшей мере одно заболевание выбрано из различных видов рака, отвечающих на ингибирование FGFR1.
35. Способ лечения субъекта с установленной потребностью в лечении по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, который включает введение указанному субъекту, который в этом нуждается, эффективного количества Формы 1N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)- метансульфонамида, охарактеризованного в п.3.
36. Способ по п.35, отличающийся тем, что по меньшей мере одно заболевание выбрано из различных видов рака, отвечающих на ингибирование FGFR1.
37. Способ лечения субъекта с установленной потребностью в лечении по меньшей мере одного заболевания, отвечающего на ингибирование FGFR1, включающий введение указанному субъекту, который нуждается в лечении, эффективного количества Формы II N-(2-(диметиламино)этил)-1-(3-((4-((2-метил-1H-индол-5-ил)окси)пиримидин-2-ил)амино)фенил)-метансульфонамида, охарактеризованной в п.14.
38. Способ по п.37, отличающийся тем, что по меньшей мере одно заболевание выбрано из различных видов рака, отвечающих на ингибирование FGFR1.
| CN 101289444 A, 22.10.2008 | |||
| US 20080255172 A1, 16.10.2008 | |||
| ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ, ОБЛАДАЮЩИЕ АКТИВНОСТЬЮ В ОТНОШЕНИИ МСН | 2005 |
|
RU2373197C2 |
Авторы
Даты
2014-02-20—Публикация
2010-11-23—Подача