Изобретение относится к области биотехнологии и может быть использовано в технологии производства тест-систем для иммуноферментного анализа.
Иммуноферментный анализ является одним из высокочувствительных методов лабораторной диагностики. Он широко используется в медицинских лабораториях для определения в сыворотке крови различных макромолекул (антигенов, гормонов), вирусов и т.д. Предприятия-производители тест-систем для иммуноферментного анализа выпускают готовые наборы для постановки ИФА, в состав которых входят все необходимые компоненты. Примерами таких тест-систем являются, например, тест-системы, описанные в приложениях 1 и 2 к Приказу №214 Министерства здравоохранения РФ О разрешении медицинского применения медицинских иммунологических препаратов от 14 июня 2000 г. или в Приложениях 1 и 2 к Приказу №118 Министерства здравоохранения РФ О разрешении медицинского применения медицинских иммунологических препаратов от 15 апреля 1998 г. В качественных системах используются позитивные и негативные контроли, которые заведомо содержат и не содержат аналиты (антитела либо антигены). В количественных системах используются калибраторы - образцы с известной концентрацией искомых макромолекул, которые позволяют определить концентрацию тех или иных антигенов или антител в анализируемой сыворотке. Контрольные образцы представляют собой жидкие окрашенные реагенты, которые используются в постановке анализа согласно процедурам, описанным в инструкциях по использованию наборов. Как правило, положительный и отрицательный контроли вносятся в определенном объеме в несколько лунок планшета, после чего инкубируются так же, как исследуемые образцы. В количественных системах используются жидкие калибраторы, которые по инструкции так же вносятся в лунки планшета в определенном объеме и затем инкубируются так же, как исследуемые образцы. По оптической плотности в лунках планшета с контролями по окончании анализа судят о правильности прохождения реакции. В количественном анализе по оптической плотности калибраторов строится калибровочная кривая, посредством которой определяются концентрации аналитов в образцах сыворотки.
Постановка контролей либо калибраторов очень важна. Любой анализ должен сопровождаться постановкой контроля. В противном случае анализ является невалидным, а полученные результаты недостоверными. При постановке большого количества образцов ставится от 3 до 8 положительных и отрицательных контролей. Для этого используются лунки планшета с иммуносорбентом. Таким образом, количество образцов крови, которое можно поставить с помощью одного набора, уменьшается. При дробном использовании набора это количество снижается еще больше, так как при постановке даже одной сыворотки необходим контроль. Если разбить один набор на 3 постановки, то количество лунок, занимаемых контролем, увеличивается втрое. Постановка с калибраторами снижает количество свободных лунок для одного анализа образцов на 10 - 12. Таким образом, недостатком известных из уровня техники способов является небольшое количество образцов, которое можно поставить с использованием одного набора.
Из уровня техники известны способы изготовления контрольных панелей для тест-систем (см. например, патент РФ 2265028 С2, опубликованный 27.11.2005, или патент РФ 2346282 С2, опубликованный 10.02.2009). Согласно данным документам изготавливают контрольные панели сывороток для контроля качества диагностики гепатита В. При этом референс-панели лиофильно высушивают.
Кроме того, из уровня техники известен патент РФ 2181893 С1, опубликованный 27.04.2002, в котором раскрыт способ получения референс-панели для контроля качества тест-систем и вакцин против гепатита В. Данный способ взят авторами настоящего изобретения за прототип.
При производстве иммуноферментных диагностических систем для определения специфических антител, например антител к возбудителям инфекционных заболеваний, аутоантител, антител к специфическим маркерам, в качестве позитивного контрольного образца традиционно используются образцы сыворотки крови человека, содержащие определяемые антитела (аналиты) от пациентов с перенесенным или текущим патологическим процессом (инфекционным заболеванием, аллергией или злокачественными новообразованиями). Образование специфических антител является ответной реакцией организма на циркулирование биологических агентов, вызвавших данное инфекционное заболевание или патологический процесс. Таким образом, еще одной проблемой известных тест-систем является проблема инфекционной опасности.
Решением проблемы инфекционной опасности использования контрольных образцов в иммуноферментных тест-системах, а также проблемы расходования иммуносорбента для постановки контрольных образцов в анализе может быть добавление в набор дополнительных лунок иммуносорбента, которые будут использоваться для постановки контролей либо калибраторов. Для удобства эти дополнительные лунки изначально содержат, либо не содержат, контрольные образцы в высушенном виде. Во время постановки требуется лишь внести в эти лунки раствор для разведения сывороток или блокирующий раствор, который используется в данном тесте.
Еще одним недостатком известных тест-систем является их неуниверсальность. Для определения различных инфекций необходимы различные тест-системы.
В основу настоящего изобретения поставлена следующая задача: создание универсальных положительных и отрицательных контрольных образцов, инкорпорированных именно в лунках рабочего планшета, используемых в иммуноферментном анализе, чувствительность, специфичность и стабильность которых не отличается от жидких аналогов.
Задача решается разработанным способом получения универсальных инкорпорированных контрольных образцов для использования при постановках всех иммуноферментных тест-систем для определения инфекций группы TORCH, в которую входят токсоплазмоз, краснуха, цитомегаловирус и герпес.
Заявлен способ получения инкорпорированных контрольных образцов для иммуноферментных тест-систем для определения инфекций группы TORCH, включающий:
A) приготовление раствора для разведения сыворотки, представляющего собой фосфатно-солевой буфер с 2%-ным содержанием бычьего сывороточного альбумина с добавлением проклина 300 и 10%-ного раствора азида,
Б) подготовку сыворотки доноров для отрицательного контроля, причем сыворотка не содержит антитела к токсоплазме, цитомегаловирусу, вирусам простого герпеса и краснухи, HBsAg, антитела к ВИЧ-1,2, вирусу гепатита С, где отобранные сыворотки крови осветляют центрифугированием при температуре 4-8 градусов С,
B) разведение сыворотки, полученной на этапе Б), в растворе для разведения для получения жидкого отрицательного контроля,
Г) подготовку сыворотки доноров для положительного контроля, причем сыворотка содержит антитела к токсоплазме, цитомегаловирусу, вирусам простого герпеса и краснухи, где отобранные сыворотки крови осветляют центрифугированием при температуре 4-8 градусов С,
Д) разведение сыворотки, полученной на этапе Г), в растворе для разведения для получения жидкого положительного контроля,
Е) внесение жидких контрольных образцов в лунки планшета,
Ж) лиофильную сушку положительного и отрицательного контроля,
3) маркировку положительного контроля красным цветом, а отрицательного контроля - зеленым.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Получение инкорпорированного в лунке рабочего планшета отрицательного контрольного образца тест-системы для определения в сыворотке антител к TORCH-инфекциям.
Получение жидкого контрольного отрицательного образца.
Приготовление раствора для разведения отрицательной сыворотки
Готовится 100 мл фосфатно-солевого буфера с 2%-ным содержанием БСА (бычий сывороточный альбумин) (Sigma Cat # A3059). К полученному раствору добавляется 0,1 мл проклина300, 1 мл 10% раствора азида. В приготовленную среду добавляется негативная сыворотка или плазма.
В качестве отрицательного контрольного образца (К-) используют сыворотки доноров, не содержащих антитела к токсоплазме, цитомегаловирусу, вирусам простого герпеса и краснухи, не содержащие HBsAg, антитела к ВИЧ-1,2 и вирусу гепатита С, инактивированные прогреванием в течение 45 мин при 56°С. Отобранные для приготовления К- сыворотки крови осветляют 50-минутным центрифугированием при 18000 об/мин на рефрижераторной центрифуге при температуре от 4 до 8°С, после чего разводят на среде, состоящей из ФСР (консерванты - проклин и азид).
Сыворотка разводится в растворе в соотношении 1 к 100. Жидкий контроль вносится в нужные лунки планшета в объеме 100 мл, после чего лиофильно высушивается.
Лиофильная сушка проводится согласно стандартной процедуре, описанной, например, в патенте №RU 2179726 от 20.02.2002.
Приготовление инкорпорированных положительных образцов или калибраторов производится аналогично. В качестве позитивного контрольного образца используют сыворотки доноров, содержащих антитела к токсоплазме, цитомегаловирусу, вирусам простого герпеса и краснухи, и вносят в раствор для разведения в нужном объеме. Жидкие К+ или калибраторы вносятся в лунки планшета по 100 мл и лиофильно высушиваются (см. выше).
Для идентификации положительного и отрицательного контролей лунки, в которые были внесены и высушены образцы, маркируются красным и зеленым цветом.
В дальнейшем такие контроли и калибраторы можно использовать в необходимом количестве для конкретной постановки. Необходимо отделить нужное количество лунок от стрипа и поместить в рамку. Далее процедура проходит согласно инструкции. В лунки с контрольными образцами вносится раствор для разведения сывороток или блокирующий раствор, после чего проводятся все те же манипуляции, что с анализируемыми образцами крови.
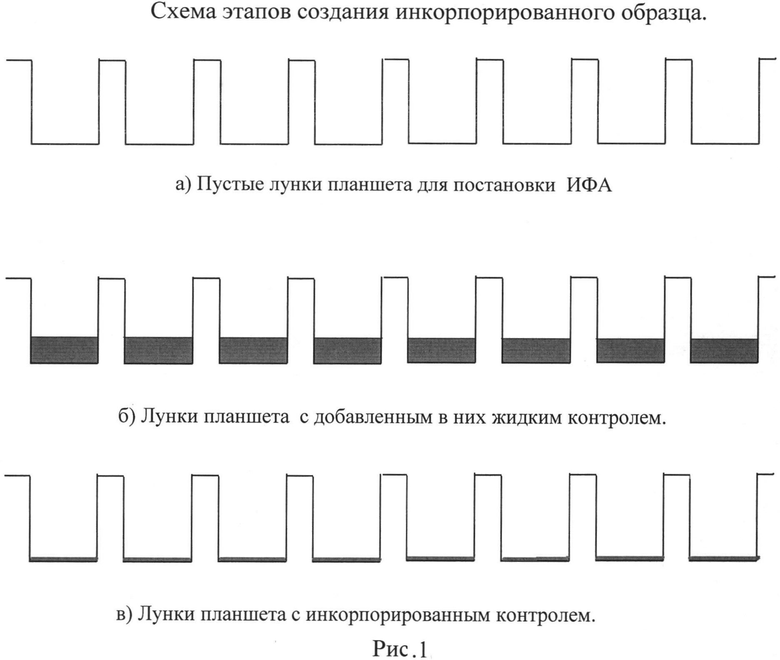
Схематично процесс производства инкорпорированного образца представлен на рисунке 1.
Благодаря наличию консервантов в буфере для разведения контрольных образцов инкорпорированные контроли стабильны в течение всего срока годности тест-систем. Исследования показали, что стабильность и специфичность инкорпорированных контрольных образцов аналогичны этим показателям жидких контрольных образцов. Результаты приведены в таблицах 1 и 2.
На основании вышеизложенного можно сделать вывод, что преимущества заявленного способа получения контрольных образцов заключаются в следующем.
1. Удобство использования потребителем лунок с сухим контролем. Исчезает необходимость переноса контрольных образцов, содержащих и не содержащих инфицированную сыворотку из специальных флаконов в лунки рабочего планшета. В случае с инкорпорированными контролями требуется просто добавить в лунку блокирующий раствор, в котором разводятся все остальные анализируемые сыворотки.
2. Безопасность постановок тест-системы. Необходимость переноса жидких положительных образцов в лунки планшета несет потенциальную возможность контактирования с инфицированным материалом, поскольку в качестве позитивного контрольного образца традиционно используются образцы сыворотки крови человека, содержащие определяемые антитела (аналиты) от пациентов с перенесенным или текущим патологическим процессом.
3. Экономия основных лунок планшета при постановке ИФА. Наборы иммуноферментных тест-систем комплектуются дополнительными стрипами с инкорпорированными контрольными образцами, что дает возможность не использовать в наборе жидкие контрольные образцы и использовать дробную постановку без ущерба для количества анализируемых сывороток.
4. Удобство при производстве иммуноферментных тест-систем. Универсальные положительные и отрицательные контрольные инкорпорированные образцы могут быть одинаковыми и использоваться при постановках всех иммуноферментных тест-систем для определения инфекций группы ToRCH.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОДНОВРЕМЕННОГО ДЕТЕКТИРОВАНИЯ АНТИТЕЛ КЛАССА G К АНТИГЕНАМ ВОЗБУДИТЕЛЕЙ TORCH-ИНФЕКЦИЙ С ИСПОЛЬЗОВАНИЕМ ИММУНОЧИПА | 2014 |
|
RU2545792C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К ОППОРТУНИСТИЧЕСКИМ ИНФЕКЦИЯМ В ЛИКВОРЕ ДЕТЕЙ | 2012 |
|
RU2488822C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ВРОЖДЕННЫХ ИНФЕКЦИЙ | 2013 |
|
RU2532382C1 |
| ТЕСТ-СИСТЕМА ДЛЯ ОДНОВРЕМЕННОЙ ДЕТЕКЦИИ ГУМОРАЛЬНЫХ МАРКЕРОВ ИНФИЦИРОВАНИЯ ГЕРПЕСВИРУСАМИ ЧЕЛОВЕКА | 2019 |
|
RU2724897C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ АДЕНОВИРУСНОГО КЕРАТОКОНЪЮНКТИВИТА | 2011 |
|
RU2470591C1 |
| ТЕСТ-СИСТЕМА ИММУНОФЕРМЕНТНАЯ ДЛЯ ОПРЕДЕЛЕНИЯ КОКЛЮШНЫХ АНТИТЕЛ В СЫВОРОТКАХ КРОВИ ЧЕЛОВЕКА И ЖИВОТНЫХ | 2015 |
|
RU2582959C1 |
| СПОСОБ ДИАГНОСТИКИ АУТОИММУННЫХ ПОРАЖЕНИЙ ПЕЧЕНИ У БОЛЬНЫХ ХРОНИЧЕСКИМИ ГЕПАТИТАМИ | 2003 |
|
RU2247387C1 |
| ТЕСТ-СИСТЕМА ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К HBs-АНТИГЕНУ И БЛОКАТОР В ТЕСТ-СИСТЕМЕ | 2001 |
|
RU2206095C1 |
| Мозаичный рекомбинантный полипептид, содержащий фрагменты белков вируса гепатита Е 1 и 3 генотипов в одной полипептидной цепи, предназначенный для использования в тест-системах, применяемых в серодиагностике гепатита Е | 2020 |
|
RU2754791C1 |
| ИММУНОФЕРМЕНТНАЯ ТЕСТ-СИСТЕМА ДЛЯ ОПРЕДЕЛЕНИЯ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В И СПОСОБ ОПРЕДЕЛЕНИЯ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСНОГО ГЕПАТИТА В | 2006 |
|
RU2325655C9 |
Изобретение относится к биотехнологии, в частности к иммуноферментным анализам, и представляет собой способ получения инкорпорированных контрольных образцов для иммуноферментных тест-систем для определения инфекций группы TORCH. Способ включает приготовление раствора для разведения сыворотки, подготовку сыворотки доноров для отрицательного контроля с последующим разведением раствором для разведения, причем сыворотка не содержит антитела к токсоплазме, цитомегаловирусу, вирусам простого герпеса и краснухи, HBsAg, антитела к ВИЧ-1,2, вирусу гепатита С, подготовку сыворотки доноров для положительного контроля с последующим ее разведением раствором для разведения, причем сыворотка содержит антитела к токсоплазме, цитомегаловирусу, вирусам простого герпеса и краснухи, внесение жидких контрольных образцов в лунки планшета, лиофильную сушку положительного и отрицательного контроля, маркировку положительного контроля красным цветом, а отрицательного контроля - зеленым. Заявленное изобретение позволяет получить универсальные контрольные образцы для всех тест-систем для определения инфекции группы TORCH, инкорпорированные в лунках рабочего планшета, удобные в использовании и безопасные. 1 ил., 2 табл., 1 пр.
Способ получения инкорпорированных контрольных образцов для иммуноферментных тест-систем для определения инфекций группы TORCH, включающий:
A) приготовление раствора для разведения сыворотки, представляющего собой фосфатно-солевой буфер с 2%-ным содержанием бычьего сывороточного альбумина с добавлением проклина 300 и 10%-ного раствора азида,
Б) подготовку сыворотки доноров для отрицательного контроля, причем сыворотка не содержит антитела к токсоплазме, цитомегаловирусу, вирусам простого герпеса и краснухи, HBsAg, антитела к ВИЧ-1,2, вирусу гепатита С, где отобранные сыворотки крови осветляют центрифугированием при температуре 4-8 градусов С,
B) разведение сыворотки, полученной на этапе Б) в растворе для разведения для получения жидкого отрицательного контроля,
Г) подготовку сыворотки доноров для положительного контроля, причем сыворотка содержит антитела к токсоплазме, цитомегаловирусу, вирусам простого герпеса и краснухи, где отобранные сыворотки крови осветляют центрифугированием при температуре 4-8 градусов С,
Д) разведение сыворотки, полученной на этапе Г) в растворе для разведения для получения жидкого положительного контроля,
Е) внесение жидких контрольных образцов в лунки планшета,
Ж) лиофильную сушку положительного и отрицательного контроля,
З) маркировку положительного контроля красным цветом, а отрицательного контроля - зеленым.
| СПОСОБ ПОЛУЧЕНИЯ РЕФЕРЕНС-ПАНЕЛИ ДЛЯ КОНТРОЛЯ КАЧЕСТВА ТЕСТ-СИСТЕМ И ВАКЦИН ПРОТИВ ГЕПАТИТА В | 1999 |
|
RU2181893C2 |
| ИММУНОФЕРМЕНТНАЯ ТЕСТ-СИСТЕМА ДЛЯ ОПРЕДЕЛЕНИЯ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В И СПОСОБ ОПРЕДЕЛЕНИЯ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСНОГО ГЕПАТИТА В | 2006 |
|
RU2325655C9 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОНТРОЛЬНОЙ ПАНЕЛИ СЫВОРОТОК AY ЭНД AD СУБТИПОВ HBsAg ДЛЯ КОНТРОЛЯ КАЧЕСТВА ДИАГНОСТИКИ ГЕПАТИТА B | 2003 |
|
RU2265028C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОНТРОЛЬНЫХ ПАНЕЛЕЙ СЫВОРОТОК ДЛЯ КОНТРОЛЯ КАЧЕСТВА ДИАГНОСТИКИ ГЕПАТИТА В | 1999 |
|
RU2179726C2 |
Авторы
Даты
2014-02-27—Публикация
2012-12-25—Подача