Область техники
Изобретение относится к медицине, в частности, к клинической лабораторной диагностике, иммунохимии и касается диагностики инфекций, вызываемых патогенными для человека герпесвирусами, методом линейного иммунного блоттинга (ЛИБ), который является разновидностью твердофазного иммуноферментного анализа (ИФА), наиболее используемого при диагностике различных вирусных, бактериальных и других инфекций.
Уровень техники
Согласно современной классификации, семейство Herpesviridae в настоящее время включает около 120 видов ДНК-вирусов, подразделяемых на 3 подсемейства: а-, (3- и у-герпесвирусов [1]. Восемь представителей герпесвирусов патогенны для человека; из подсемейства а-герпесвирусов к их числу относят: вирусы простого герпеса 1 и 2 типа (ВПГ-1 и ВПГ-2, или herpes simplex virus type 1 and 2 - HSV-1 и HSV-2, или human herpes virus type 1 and 2 - HHV-1 и HHV-2) и вирус ветряной оспы и опоясывающего герпеса (ВВО, или вирус Варицелла-Зостер - ВВЗ, или varicella zoster virus - VZV, или HHV-3), из (3-подсемейства - цитомегаловирус (ЦМВ, или cytomegalovirus - CMV, или HHV-5), вирус герпеса 6 типа (HHV-6), являющийся возбудителем внезапной экзантемы и ассоциирующийся с синдромом хронической усталости и вирус герпеса 7 типа (HHV-7), также выявляемый у больных с синдромом хронической усталости; из у-подсемейства - вирус Эпштейна-Барр (ВЭБ, или Epstein Barr virus - EBV, или HHV-4) и вирус герпеса 8 типа (HHV-8), причастный к возникновению саркомы Капоши. Известны также вирусы герпеса животных, способные поражать человека и вызывать энцефаломиелиты со смертельным исходом [2].
По данным ВОЗ, обусловленные герпесвирусами заболевания занимают 2 место после гриппа как причина смерти от вирусных инфекций, и этот показатель достигает 15,8% [3]. О высоком уровне распространения герпесвирусов в человеческой популяции свидетельствуют данные отдельных эпидемиологических исследований, в которых установлено, что к 18 годам более 90% жителей городов инфицированы одним или несколькими видами герпесвирусов, и у 50% инфицированных ежегодно наблюдают клинические рецидивы заболевания, в связи с отсутствием формирования к ним защитного иммунитета [4-5].
Герпесвирусы очень активно проявляют себя у лиц с иммунодефицитными состояниями (их относят к оппортунистическим инфекциям), приводя к клиническим поражениям разных систем органов, развитию нейроинфекции с высоким уровнем инвалидизации (50%) и летальных исходов (20%) [6-7]. Многие герпесвирусы также обладают высокой онкогенной активностью, это доказано для HSV, CMV, EBV, HHV-8 и, возможно, HHV-6 [8].
Представителей герпесвирусов (HSV, CMV) относят к возбудителям инфекций TORCH-группы, так как при заражении беременных они способны приводить к развитию внутриутробных инфекций, поражениям эмбрионов, гибели плодов и новорожденных [6-7, 9].
Герпесвирусы способны поражать практически все ткани и системы органов хозяина, где они непрерывно или циклично размножаются, обеспечивая постоянную готовность к клиническому обострению инфекционного процесса (персистенция). Как правило, герпесвирусы пожизненно сохраняются в морфологически и иммунохимически изменённой форме в нервных клетках регионарных (по отношению к месту первичного внедрения) ганглиев чувствительных нервов (латенция).
Инфицирование герпесвирусами нередко протекает в субклинических формах, или клинические проявления не имеют специфических признаков, позволяющих установить этиологический диагноз.
На инфицирование герпесвирусами иммунная система человека реагирует выработкой специфических антител разных классов, но это не обеспечивает полной элиминации вирусов из макроорганизма. Выработка вируснейтрализующих антител поддерживается в течение всей последующей жизни человека, иногда в довольно высоких титрах, что препятствует проявлению инфекции, но и не предупреждает возникновение клинических рецидивов при ослаблении иммунной защиты [10-12].
Спектр клинических проявлений при герпесвирусных инфекциях зависит от локализации патологического процесса, его распространенности, состояния иммунной системы больного и антигенного субтипа вируса. Заболевания, обусловленные HSV, CMV и EBV рассматривают как СПИД-индикаторные в связи с их частым обнаружением при этой патологии; установлено, что многие HHV могут активировать находящийся в стадии провируса ВИЧ и являются кофакторами прогрессирования ВИЧ-инфекции и СПИД [13].
В последние годы активно изучаются различные аспекты эпидемиологии, клиники и профилактики инфекций, вызванных относительно малоизвестными герпесвирусами человека: HHV-6, HHV-7 и HHV-8 [14]. Предполагается участие HHV-6 в этиологии рака, хронических демиелинизирующих заболеваний центральной нервной системы, рассеянного склероза, синдрома хронической усталости, внезапных экзантем у детей [15].
Современная лабораторная диагностика герпесвирусных инфекций у человека включает: вирусологический, молекулярно-биологический и серологические методы, каждый из которых имеет свои показания и ограничения в применении. Иммунохимическое исследование антител к герпесвирусам в ИФА особенно важно при обследовании лиц со сниженной иммунной защитой (на фоне терапии цитостатиками, системными кортикостероидами, при лучевой терапии, а также у лиц с ВИЧ-инфекцией). Наиболее распространенным методом исследования, доступным для большинства клинических лабораторий является иммуноферментный анализ, позволяющий достаточно надежно оценивать наличие гуморального ответа организма на текущую или имевшуюся в анамнезе герпесвирусную инфекцию или их сочетание [16]. Одним из современных вариантов ИФА является иммунный блоттинг - выявление наличия или отсутствия антител к отдельным антигенам возбудителя, позволяющий выявлять не только сам факт инфицирования, но и оценивать стадию развития инфекции.
Наиболее близкими по осуществлению аналогами являются иммуно-сорбенты для линейного ИБ, содержащие сорбированные на твердой фазе специфические иммунодоминантные антигены одного или нескольких возбудителей.
Прототипом изобретения является тест-система, содержащая мультиантигенный иммуносорбент для линейного иммуноблоттинга, который включает одновременно несколько специфических антигенов разных видов возбудителей TORCH-инфекций («Лайн-Блот TORCH-Профиль»): клеточного паразита {Toxoplasma gondii) и вирусов {Rubella virus, CMV, HSV-1 и HSV-2), нанесенных в виде антигенных линий на тест-полосках из нитроцеллюлозной мембраны (стрипах).
Для нанесения на нитроцеллюлозную мембрану с целью получения иммуносорбента были подобраны следующие очищенные нативные и рекомбинантные антигены основных возбудителей TORCH-инфекций:
~ нативный антиген токсоплазмы (Toxoplasma gondii) и рекомбинантный аналог антигена токсоплазмы р30;
~ нативный антиген вируса краснухи (Rubella virus);
~ рекомбинантный аналог мозаичного антигена цитомегаловируса (CMV), содержащий иммунодоминантные последовательности белков рр150, рр52, рр28 и gB;
~ рекомбинантные аналоги антигена G1 вируса простого герпеса 1 типа (HSV-1) и антигена G2 вируса простого герпеса 2 типа (HSV-2). Кроме этого, на иммуносорбенте нанесены:
~ международный стандарт ВОЗ Anti-Rubella Immunoglobulin, Human (NIBSC, code RUBI-1-94), представляющий собой иммуноглобулины человека класса G к вирусу краснухи - в концентрации 15-20 МЕ/мл (линия "Rub. Cut off);
~ три контрольные линии, две из которых ("0,5+" и "2,0+") содержат иммуноглобулины человека класса G или М в разных концентрациях для калибровки результатов исследования, и одна линия (Кво - контроль внесения образца) содержит антитела к IgG/IgM человека для контроля внесения образца [17].
Недостатком прототипа является использование антигенов только трех типов герпесвирусов, что не охватывает весь спектр возбудителей герпесвирусных инфекций человека. Для получения более полной информации о серологической реактивности в отношении всех 8 патогенных для человека типов герпесвирусов у обследуемого лица требуется выполнение не менее 5 дополнительных исследований в формате ИФА, при этом каждый соответствующий набор реагентов имеет особенности калибровки по показателям аналитической и диагностической чувствительности и эффективности.
Раскрытие сущности изобретения
Технической задачей изобретения явилась разработка тест системы для одновременной детекции гуморальных маркеров инфицирования герпесвирусами человека и способа ее получения, при этом тест система содержит иммуносорбент в виде тест-полосок (стрипов), на который в определенном порядке нанесены и иммобилизированы антигены основных герпесвирусов человека, что позволяет в формате линейного иммуноблоттинга проводить клиническое лабораторное исследование образцов биоматериала человека с одномоментным выявлением специфических гуморальных маркеров инфицирования каждым из 8 видов герпесвирусов (антител классов М или G).
Эта задача достигается за счет подбора наиболее специфичных антигенов герпесвирусов человека, определения оптимальной сорбционной концентрации каждого антигена для разработки технологии их нанесения и иммобилизации на тест-полосках из нитроцеллюлозной мембраны, предназначенных для последующего использования в линейном иммуноб лоттинге.
Новый оригинальный состав и технология получения предполагает поэтапное нанесение калиброванных растворов рекомбинантных и очищенных нативных антигенов 8 типов герпесвирусов человека на нитроцеллюлозную мембрану и обеспечение условий их устойчивой иммобилизации.
Таким образом, заявлена тест-система для одновременной детекции антител класса G к антигенам патогенных для человека типов герпесвирусов методом линейного иммуноблотинга, включающая иммуносорбент в виде тест-полосок из нитроцеллюлозной мембраны, на каждой из которых в виде отдельных линий нанесены следующие антигены:
гес антиген gG-1 HSV-1;
гес антиген gG-2 HSV-2;
нативный антиген VZV;
гес антиген gE VZV;
гес антигены EBV: ядерный - EBNA (Epstein Barr Nuclear Antigen), ранний - EA (Early Antigen) и капсидный - VCA (Viral Capsid Antigen);
гес мозаичный антиген CMV, содержащий последовательности белков рр150, рр52, рр28 и gB;
гес большой структурный фосфопротеин (Large structural protein) U11 вируса HHV-6;
гес гликопротеин В (gB) вируса HHV-7;
гес мозаичный антиген HHV-8, содержащий последовательности белков ORF65 и ORF8 (К8).
Кроме этого, дополнительно на каждой тест-полоске имеются участки для маркировки, в частности, для нанесения идентифицирующего номера.
Также дополнительно каждая тест-полоска содержит контрольную линию - контроль внесения образца (Кво), предназначенную для контроля внесения биологического образца, представлена антивидовыми антителами к IgG человека.
Техническими результатами заявляемого изобретения являются:
замена нескольких лабораторных исследований в формате ИФА по определению в биологических образцах специфических антител класса G к каждому типу герпесвируса (до 8-9 самостоятельных ИФА исследований) одним диагностическим исследованием в формате линейного иммуноблоттинга;
унификация методики лабораторного исследования напряженности гуморального иммунного ответа на каждый включенный в иммуносорбент антиген определенного типа герпесвируса;
возможность одновременного выявления антител класса G ко всем патогенным для человека типам герпесвирусов, что достигается за счет использования в иммуносорбенте антигенов всех 8 возбудителей герпесвирусных инфекций человека;
использование в линейном иммуноблоттинге минимального количества биологического материала по сравнению с несколькими постановками ИФА;
экономия трудовых затрат специалистами лабораторной медицины при замене 8-9 постановок ИФА одним исследованием в формате линейного иммуноблоттинга.
В процессе изучения научной литературы (как российской, так и зарубежной) по герпесвирусам, патогенным для человека, сложилось представление о том, какие из антигенов, представляют наибольшую диагностическую ценность.
При изучении литературы по вирусам простого герпеса 1 и 2 типа было установлено, что гуморальный ответ человека в первую очередь вырабатывается к типоспецифическому антигену gG (gG-1 ВПГ-1 и gG-2 ВПГ-2) [18, 19], причем перекрестной реактивности между gG-1 ВПГ-1 и gG-2 ВПГ-2 установлено не было [20]. Поэтому данные антигены стали использовать при создании иммуноферментных тест-систем, предназначенных для диагностики инфекции, вызываемой ВПГ-1 и ВПГ-2 (герпетической инфекции), в том числе и для дифференциации этих двух типов ВПГ [21].
Данные литературы послужили основанием для включения в состав иммуносорбента разрабатываемой тест-системы рекомбинантных антигенов gG-1 ВПГ-1 и gG-2 ВПГ-2.
При изучении литературы по вирусу Варицелла-Зостер было установлено, что данный вирус содержит несколько высокоспецифичных антигенов (gH, gE, gB, gL), выявление антител к которым имеет одинаково значимую диагностическую ценность [22, 23]. На основании этих данных было принято решение о включении в состав иммуносорбента разрабатываемой тест-системы антигенной линии, представленной нативным лизатом (антигеном) ВВЗ, содержащим все специфические белки вируса. Однако ввиду того, что все герпесвирусы схожи по строению, возможно появление перекрестных реакций при выявлении антител к отдельным видам семейства. Так, известно, что антитела к некоторым антигенам вируса ветряной оспы могут перекрестно реагировать с антигенами вируса простого герпеса первого типа [24]. Исключением является антиген gE ВВЗ [25]. В связи с этим с целью дифференциации ВВЗ от ВПГ-1 было принято решение о включении в иммуносорбент дополнительной линии, представленной антигеном gE ВВЗ.
При изучении литературы по вирусу Эпштейна-Барр было установлено, что IgG к ядерному антигену (EBNA - Epstein Barr Nuclear Antigen) появляются в крови человека через несколько недель после появления клинических признаков и сохраняются на протяжении всей жизни. IgG к раннему антигену (ЕА - Early Antigen) появляются с первой недели болезни и служат маркером острой инфекции. IgG к капсидному антигену (VCA - Viral Capsid Antigen) появляются обычно (но не всегда) через несколько недель после инфицирования и сохраняются пожизненно [26]. Эти данные послужили основанием для включения в состав иммуносорбента всех трех вышеназванных антигенов вируса Эпштейна-Барр.
При изучении литературы по цитомегаловирусу было установлено, что наиболее диагностически значимыми антигенами являются фосфопротеины рр150, рр52, рр28 и гликопротеин gp55 (gB) [27]. IgG к рр150 обычно вырабатываются при каждом случае ЦМВИ, по мере развития инфекционного процесса появляются IgG к белку рр28. Наличие IgG к антигенам рр52 и gB является свидетельством давно прошедшей (более 6 месяцев) инфекции [28]. На основании этих данных было принято решение о включении в состав иммуносорбента линии, представленной смесью всех значимых рекомбинантных антигенов ЦМВ (рр150, рр52, рр28 и gp55 (gB)).
При изучении литературы по вирусу герпеса человека 6 типа (HHV-6) было установлено, что HHV-6 бывает двух видов: HHV-6A (нейровирулентный) и HHV-6B (вызывающий заболевание «детская розеола») [29, 30, 31]. При этом наиболее иммуногенным антигеном является антиген с молекулярной массой 101 килодальтон (кДа), гомологичный для обоих видов вируса и лишенный перекрестной реактивности с HHV-7 [32]. Данный антиген был выбран для нанесения линии HHV-6 на иммуносорбенте.
При изучении литературы по вирусу герпеса человека 7 типа (HHV-7) было установлено, что гликопротеин В (gB) является высококонсервативным среди отдельных штаммов HHV-7 и индуцирует специфический иммунный ответ человека. Кроме того, данный антиген не дает перекрестной реакции с антигенами других герпесвирусов [33]. На этом основании гликопротеин В (gB) был выбран для включения в состав иммуносорбента.
При изучении литературы по вирусу герпеса человека 8 типа (HHV-8) было установлено, что наиболее диагностически значимыми антигенами являются белки ORF65 и ORF8 (К8). По мере развития HHV-8-инфекции происходит нарастание титров IgG к ORF65. Использование антигена К8 обеспечивает высокую чувствительность и специфичность исследования, поскольку у К8 нет гомолога среди других герпесвирусов, а значит - нет потенциальной перекрестной реакции с антителами против других герпесвирусов [34]. В связи с этим было принято решение о включении в состав иммуносорбента линии, представленной мозаичным антигеном, содержащим иммунодоминантные последовательности белков ORF65 и ORF8 (К8) HHV-8.
Осуществление изобретения
Сущность изобретения заключается в получении диагностической тест-системы путем изготовления иммуносорбента, включающего диагностически значимые антигены 8 видов герпесвирусов человека (гес антиген gG-1 HSV-1; гес антиген gG-2 HSV-2; нативный антиген VZV; гес антиген gE VZV; гес антигены EBV: ядерный - EBNA, ранний - ЕА и капсидный - VCA; гес мозаичный антиген CMV, содержащий последовательности белков рр150, рр52, рр28 и gB; гес большой структурный фосфопротеин Ul1 вируса HHV-6; гес гликопротеин В (gB) вируса HHV-7; гес мозаичный антиген HHV-8, содержащий последовательности белков ORF65 и ORF8 (К8)), приготовлении раствора для разведения образцов - РРО, 10-кратного концентрата промывочного раствора - ПРхЮ, конъюгата, а также комплектации тест-системы.
Краткое описание таблиц
Табл. 1. Интенсивность окрашивания антигенных линий.
Табл. 2. Исследование чувствительности разработанной тест-системы «Лайн-Блот ВГЧ-профиль-IgG» в сравнении с тест-системой-прототипом «Лайн-Блот ТОRСН-Профиль- IgG».
*Тест-система-прототип «Лайн-Блот ТОRСН - Профиль- IgG» не предполагает выявление IgG к ВВЗ, ВЭБ, ВГЧ-6, ВГЧ-7, ВГЧ-8 (выделено серым цветом)
Табл. 3. Исследование специфичности разработанной тест-системы «Лайн-Блот ВГЧ-профиль-IgG» в сравнении с тест-системой-прототипом «Лайн-Блот ТОRСН - Профиль IgG».
Изобретение в частных случаях осуществления поясняется следующими примерами.
Пример 1
1. Изготовление иммуносорбента.
Иммуносорбент (стрипы из нитроцеллюлозной мембраны) готовят непосредственным нанесением антигенов HSV-1, HSV-2, VZV, EBV, CMV, HHV-6, HHV-7, HHV-8 на нитроцеллюлозную мембрану.
1.1. Подготовка мембран.
Подготовить необходимое количество нитроцеллюлозных мембран размером 10x20 см.
Приготовить 10-кратный концентрат фосфатно-солевого буферного раствора (ФСБх10).
Состав на 1 л раствора:
- натрий фосфорнокислый 2-замещенный 12-водный (Na2HPO4x12H2O)-9,3 г;
- натрий фосфорнокислый 1-замещенный 2-водный (Na2HPO4x2H2O) -0,65 г;
- натрий хлористый (NaCl) - 59,5 г;
- мертиолят натрия - 0,7 г;
- вода очищенная 2-й ступени - 1000 мл.
С помощью мерного цилиндра внести в колбу 500 мл воды очищенной. Внести в емкость с водой навески солей, перемешать на магнитной мешалке до полного растворения, довести объем раствора до 700 мл водой очищенной, перемешать 10-15 мин.
Измерить рН раствора, (требуемое значение рН 7,3+0,2). При необходимости довести рН с помощью 2-молярного раствора гидроокиси натрия до требуемого значения.
Приготовить однократное разведение ФСБх1 путем разбавления ФСБх10 водой очищенной, исходя из потребности 50 мл ФСБх1 на 1 мембрану.
Перелить готовый раствор по 500 мл в лотки и поместить туда же нитроцеллюлозные мембраны по 9 шт. в 1 лоток. Инкубировать на шейкере-качалке 15 мин. Далее мембраны выложить на фильтровальную бумагу и сушить в ламинарном шкафу в течение 55-65 мин при температуре 18-24°С или оставить на рабочем столе и сушить в течение 80-100 мин при температуре 18-24°С.
1.2. Приготовление рабочих разведений антигенов HSV-1, HSV-2, VZV, EBV, CMV, HHV-6, HHV-7, HHV-8 и антител против IgG.
Приготовить карбонат-бикарбонатный буфер (КББ).
Состав (на 1 л раствора):
- натрия углекислого - 1,6 г;
- натрия углекислого кислого - 3,0 г;
- натрия азида - 0,2 г;
- воды очищенной 2-й ступени - до 1000 мл.
С помощью мерного цилиндра внести рассчитанный объем воды очищенной в колбу, внести в емкость навески солей, перемешать на магнитной мешалке до полного растворения солей. Проверить рН раствора, норма 9,4-9,6. Если рН раствора не соответствует данному значению, КББ готовить заново.
Исходя из исходной белковой концентрации антигенов, рабочей концентрации антигенов и общего объема рабочего разведения каждого антигена (зависит от количества мембран), рассчитать объем КББ и количество каждого антигена, необходимые для приготовления заданных объемов рабочих разведений.
Пример расчета:
Исходная белковая концентрация антигена - 3 мг/мл
Объем рабочего разведения антигена в КББ - 2000 мкл (на 36 мембран).
Рабочая концентрация антигена - 0,1 мг/мл.
2000×0,1/3 = 66,7 мкл антигена нужно взять.
2000-66,7 = 1933,3 мкл КББ нужно взять.
Таким же образом приготовить рабочее разведение антител против IgG человека (контроль внесения образца) в растворе КББ.
Рабочие разведения готовить непосредственно перед сорбцией.
1.3. Нанесение рабочих разведений антигенов на мембрану (сорбция)
Нанесение рабочих разведений антигенов на мембрану может быть выполнено вручную с помощью капиллярно-поршневого устройства или с помощью машины для капиллярного нанесения линий.
При ручном нанесении заполнить капиллярно-поршневое устройство рабочим разведением антигена и с помощью линейки нанести на мембрану полосу этого разведения в соответствии со стандартной схемой нанесения антигенов HSV-1, HSV-2, VZV, EBV, CMV, HHV-6, HHV-7, HHV-8 и контрольной линии Кво (контроль внесения образца).
Стандартная схема нанесения антигенов антигенов HSV-1, HSV-2, VZV, EBV, CMV, HHV-6, HHV-7, HHV-8 и контрольной линии Кво на стрип:
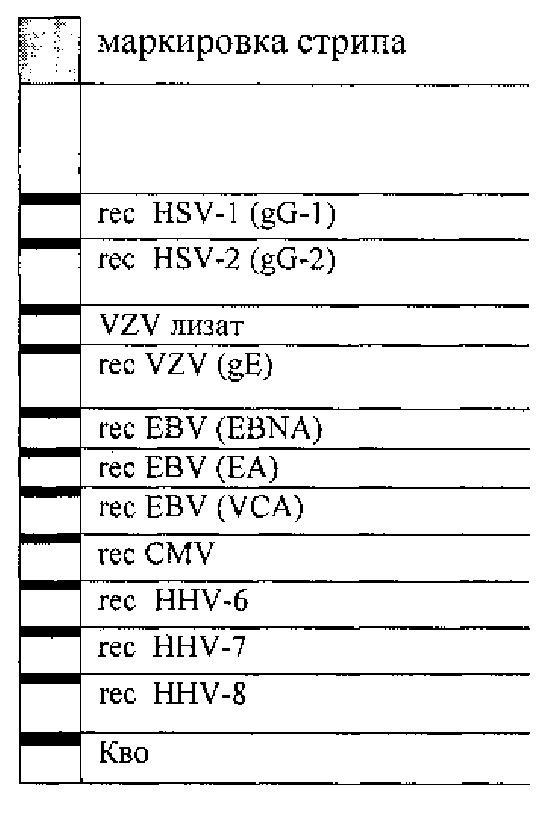
Мембраны с нанесенными антигенами поместить на полки холодильника, застеленные фильтровальной бумагой и выдержать при температуре 2-8°С в течение 18-24 ч.
1.4. Блокировка мембран Приготовить блокирующий раствор (БР). Состав (на 1 л раствора):
- БСА - 10,0 г;
- ФСБ×10 - 100 мл;
- вода очищенная - 900 мл.
Налить БР в лотки по 500 мл. Аккуратно перенести туда же с помощью пинцета мембраны с нанесенными антигенами по 9 шт.
Поместить лоток на шейкер-качалку и выдержать 55-65 мин при интенсивности покачивания 40 об/мин и температуре 18-24°С, после чего отмыть мембраны от БР водой очищенной до полного исчезновения пены на их поверхностях.
1.5. Сушка мембран и нарезка на стрипы
Для предварительного удаления влаги аккуратно пинцетом поместить отмытые мембраны на 5 мин на сложенные вдвое листы фильтровальной бумаги при температуре 18-24°С. Надрезать каждую мембрану полосками шириной 3 мм при помощи специального резака, оставляя неразрезанной ее верхнюю часть для маркировки стрипов.
Надрезанные мембраны сушить в ламинарном шкафу в течение 3-3,5 ч при 18-24°С.
С каждой мембраны получается 48-52 стрипов, что представляет 2 иммуносорбента по 24 стрипа. Используя липкую ленту с нанесенными на нее порядковыми номерами (маркировка), промаркировать полученные стрипы, для чего маркировку наклеить на неразрезанную часть мембраны таким образом, чтобы каждая цифра маркировки приходилась на середину маркируемого стрипа, после чего обрезать верхнюю часть мембраны над маркировкой. Промаркированные стрипы разрезать ножницами. Стрипы одной мембраны с помощью пинцета аккуратно поместить по 24 штуки (№№ 1-24) в пластиковый контейнер-пробирку.
1.6. Контроль иммуносорбента в ИБ
Каждую новую серию иммуносорбента проконтролировать в ИБ путем исследования сывороток стандартных панелей, содержащих и не содержащих антитела к антигенам HSV-1, HSV-2, VZV, EBV, CMV, HHV-6, HHV-7, HHV-8. Новую серию иммуносорбента считать пригодной для использования при соответствии результатов исследования образцов их паспортным характеристикам.
1.7. Маркировка и хранение иммуносорбента
На каждую пробирку со стрипами наклеить этикетку с указанием сведений, требуемых ТУ на набор. До комплектации набора хранить пробирки с иммуносорбентом при температуре 2-8°С не более 12 мес.
2. Приготовление раствора для разведения образцов (РРО)
2.1. Приготовление 10-кратного концентрата трис-солевого буферного раствора (ТСБх10)
Состав (на 1 л раствора):
- трис-(оксиметил)-аминометан – 24,20 г;
- натрий хлористый – 234,0 г;
- азид натрия – 0,10 г;
- твин-20 – 10,0 мл;
- вода очищенная 2-й ступени - до 1000 мл.
С помощью мерного цилиндра внести в колбу воду очищенную в объеме, равном 0,8 заданного объема раствора, внести навески трис-(оксиметил)-аминометана и натрия хлористого, перемешать до полного растворения реактивов, проверить рН. рН должен составлять 7,4-7,6. При необходимости рН скорректировать с помощью концентрированной соляной кислоты (на 500 мл раствора расходуется 7-20 мл кислоты). Внести в емкость с раствором навеску азида натрия, перемешать до полного растворения соли; с помощью дозатора пипеточного внести рассчитанный объем твин-20, довести объем раствора до заданного водой, перемешать на магнитной мешалке 15 мин. Полученный ТСБх10 профильтровать через обеззоленный фильтр или фильтр из фильтровальной бумаги.
2.2. Приготовление РРО
Состав (на 1 л раствора):
- ТСБх10 – 80 мл;
- казеин натриевая соль – 3,00 г;
- хлорацетамид – 2,00 г;
- концентрат блокирующего раствора (КБР) - 180 мл;
- нормальная козья сыворотка – 65 мл;
- паранитрофенол – 0,10 г;
- бромфенола синего натриевая соль – 0,10 г;
- вода очищенная – 675 мл;
С помощью мерного цилиндра внести в колбу рассчитанный объем ТСБх10, внести в емкость навески казеина и хлорацетамида, перемешать на магнитной мешалке 15 мин до полного растворения. С помощью мерного цилиндра внести в емкость рассчитанные объемы воды очищенной, КБР и нормальной козьей сыворотки, перемешать 30 мин, внести в емкость навески паранитрофенола и бромфенола синего натриевой соли, перемешать 30 мин до полного растворения.
2.3. Розлив, маркировка и хранение РРО
Провести розлив РРО по флаконам, укупорку и маркировку флаконов в соответствии с требованиями ТУ на набор. Маркированные флаконы до использования при комплектации хранить при 2-8°С не более 6 мес.
3. Приготовление 10-кратного концентрата промывочного раствора (ПРх10)
3.1. Приготовление 10-кратного концентрата промывочного раствора (ПРх10)
Состав (на 1 л раствора):
- вода очищенная – 1000 мл;
- трис-(оксиметил)-аминометан – 24,20 г;
- натрия хлористого – 234,0 г;
- мертиолята натрия - 0,10 г;
- твин-20 – 10,0 мл
- 4-нитрофенол – 0,10 г.
С помощью мерного цилиндра внести в колбу рассчитанный объем воды очищенной, внести навески трис-(оксиметил)-аминометана и натрия хлористого, перемешать на магнитной мешалке до полного растворения, проверить рН. рН должен составлять 7,4-7,6. При необходимости рН скорректировать с помощью концентрированной соляной кислоты (на 500 мл раствора расходуется 10,0-12,0 мл кислоты). Внести в емкость с раствором навески мертиолята и 4-нитрофенола, с помощью дозатора пипеточного внести рассчитанный объем твин-20, перемешать 15 мин. Полученный ПРх10 профильтровать через обеззоленный фильтр или фильтр из фильтровальной бумаги.
3.2. Розлив, маркировка и хранение ПРх10
Провести розлив ПРх10 по флаконам, укупорку и маркировку флаконов в соответствии с требованиями ТУ на набор. Маркированные флаконы до использования при комплектации хранить при 2-8°С не более 6 мес.
4. Приготовление конъюгата
4.1. Приготовление конъюгата
Состав (на 1 л раствора):
- стабилизирующий раствор для антител – 1000 мл;
- конъюгат антител козы к IgG человека, меченных щелочной фосфатазой, - 0,03 мг;
- бромфеноловый синий – 0,001 г.
С помощью мерного цилиндра внести в колбу рассчитанный объем стабилизирующего раствора для антител, всыпать навеску бромфенолового синего, с помощью дозатора пипеточного внести в емкость конъюгат антител козы к IgG человека, меченных щелочной фосфатазой. Перемешать на магнитной мешалке в течение 15 мин.
4.2. Розлив, маркировка и хранение конъюгата
Провести розлив конъюгата по флаконам, укупорку и маркировку флаконов в соответствии с требованиями ТУ на набор. Маркированные флаконы до использования при комплектации хранить при 2-8°С не более 1 мес.
5. Розлив, маркировка и хранение субстратного раствора (CP)
Субстратный раствор (5-бром-4-хлор-3-индолилфосфат и нитроголубой тетразолий) поставляется в готовом виде. Провести розлив CP по флаконам, укупорку и маркировку флаконов в соответствии с требованиями ТУ на набор. Маркированные флаконы до использования при комплектации хранить при 2-8°С не более 6 мес.
6. Комплектация тест-системы
Собрать из кроя коробки, поместить в них вкладыши и разместить в коробках маркированные компоненты тест-системы в следующем количестве:
Иммуносорбент - 24 стрипа в пластмассовом контейнере;
РРО-1 фл. (30 мл);
ПРх10 - 1 фл. (50 мл);
Конъюгат - 1 фл. (45 мл);
CP - 1 фл. (45 мл).
В каждую коробку вложить инструкцию по применению, бланк протокола, бланк потребителя, пинцет и 3 планшета-ванночки для проведения анализа по 8 ячеек в полиэтиленовом пакете.
Авторам не известны технические решения, имеющие совокупность признаков, подобную заявляемому изобретению. Следовательно, предлагаемое изобретение отвечает критерию - новизна.
Использование при получении иммуносорбента наиболее диагностически значимых антигенов герпесвирусов 8 типов (гес антиген gG-1 HSV-1; гес антиген gG-2 HSV-2; нативный антиген VZV; гес антиген gE VZV; гес антигены EBV: ядерный - EBNA, ранний - ЕА и капсидный - VCA; гес мозаичный антиген CMV, содержащий последовательности белков рр150, рр52, рр28 и gB; гес большой структурный фосфопротеин U11 вируса HHV-6; гес гликопротеин В (gB) вируса HHV-7; гес мозаичный антиген HHV-8, содержащий последовательности белков ORF65 и ORF8 (К8)) позволяет увеличить чувствительность анализа в отношении выявления антител класса G к герпесвирусам, позволяет выявить антитела к полному спектру патогенных для человека герпесвирусов, а также дифференцировать разные типы герпесвирусов за счет подбора антигенов с минимальной перекрестной реактивностью.
Тест-система для одновременного мультиплексного выявления антител класса G к антигенам возбудителей герпесвирусных инфекций человека: вируса простого герпеса 1 и 2 типов, вируса Варицелла-Зостер, вируса Эпштейна-Барр, цитомегаловируса, вирусов герпеса человека 6-го, 7-го и 8-го типов методом линейного иммуноблоттинга "Лайн-Блот ВГЧ профиль", получаемая по предлагаемому способу, найдет широкое применение в здравоохранении, в частности, в клинических лабораториях, для проведения иммунохимического и иммунологического анализа. Следовательно, предлагаемое изобретение отвечает критерию промышленной применимости.
Способ применения тест-системы осуществляется следующим образом.
Пример 2.
Проведение анализа с использованием тест-системы, полученной по предлагаемому способу.
Проведение анализа методом линейного иммуноблоттинга
1. Необходимое число стрипов (один стрип на каждый исследуемый образец) осторожно по одному извлечь из контейнера пинцетом и поместить в канавки ванночки маркированной стороной вверх. Плотно закрыть контейнер с неиспользованными стрипами и поместить его для последующего хранения при температуре от 2 до 8°С.
2. В канавки ванночки со стрипами внести по 1 мл РРО, выдержать 3-5 мин при покачивании на шейкере-качалке с частотой качания 40-50 об/мин при температуре от 18 до 25°С.
3. Отдельными наконечниками внести по 20 мкл исследуемых образцов сывороток или плазмы крови.
4. Заклеить занятые канавки клейкой пленкой или закрыть крышкой. Поместить ванночку на шейкер. Инкубировать 2 ч при температуре от 18 до 25°С.
5. После инкубации удалить жидкость из канавок ванночки, используя автоматическую пипетку или вакуумный насос, в емкость, содержащую дезинфицирующий раствор.
6. Промыть каждый стрип 4 раза рабочим (однократным) промывочным раствором, внося в каждую канавку по 2 мл раствора. При первой промывке раствор удалить из канавок, как указано в п. 5, сразу после внесения. При последующих трех промывках после внесения промывочного раствора выдерживать ванночку по 5 мин на шейкере. Удаление промывочного раствора проводить, как указано в п.5.
7. Во все использованные канавки ванночки внести по 1,0 мл конъюгата.
8. Инкубировать в течение 30 мин при температуре от 18 до 25°С на шейкере-качалке.
9. После инкубации удалить жидкость из канавок ванночки, как указано в п. 5. Промыть стрипы, как указано в п.6.
10. Внести во все использованные канавки по 1,0 мл субстратного раствора. Инкубировать 15 мин на шейкере-качалке в защищенном от света месте при температуре от 18 до 25°С.
11. Для остановки реакции удалить субстратный раствор, как указано в п. 5. Промыть стрипы 4 раза, внося в канавки по 2 мл воды очищенной и выдерживая ванночку в течение 1 мин на шейкере. Воду удалять, как указано в п. 5.
12. Поместить стрипы между двумя листами фильтровальной бумаги маркированной стороной вверх и выдержать в защищенном от света месте до полного высыхания, после чего зарегистрировать результаты.
Регистрация и учет результатов
Полученные результаты учитывать только при условии, что контрольная линия внесения образца (Кво) окрашена. В противном случае исследование необходимо повторить, поскольку неокрашенная линия Кво означает отсутствие образца.
Присутствие в образце сыворотки (плазмы) крови человека антител к антигенам герпесвирусов обнаруживается по появлению окрашенных антигенных полос, соответствующих отдельным герпесвирусам.
В зависимости от наличия и интенсивности окрашивания антигенных линий результаты делятся на положительные, неопределенные и отрицательные (табл. 1).
При получении неопределенного результата рекомендуется провести повторное исследование; если в нем вновь будет получен неопределенный результат, рекомендуется взятие крови через 3-4 недели с проведением нового исследования на выявление антител к данному возбудителю.
Окрашивание антигенной линии гес EBV ЕА говорит о недавнем инфицировании организма вирусом Эпштейна-Барр.
Пример 3.
В отделе перспективных разработок ЗАО «ЭКОлаб» были приготовлены опытно-экспериментальные серии разработанного набора реагентов «Лайн-Блот ВГЧ-профиль-IgG».
Проведенные испытания с использованием тест-системы по настоящему изобретению «Лайн-Блот ВГЧ-профиль-IgG» и тест-системы-прототипа «Лайн-Блот TORCH-Профиль-IgG» показали более высокую чувствительность первой, поскольку тест-система-прототип не предполагает выявление антител к вирусу Варицелла-Зостер (ВВЗ), вирусу герпеса 6 типа (ВГЧ-6), вирусу Эпштейна-Барр (ВЭБ), вирусу герпеса 7 типа (ВГЧ-7) и вирусу герпеса 8 типа (ВГЧ-8). Результаты исследования чувствительности и специфичности разработанной тест-системы в сравнении с тест-системой-прототипом отражены в табл. 2 и 3.
В качестве референсного материала при оценке чувствительности разработанной тест-системы были исследованы сыворотки стандартных панелей положительных образцов предприятия ЗАО «ЭКОлаб», содержащих IgG к индивидуальным белкам ВПГ-1 (С0П+-ВПГ-1-G - 12 образцов), ВПГ-2 (C0n+-BПГ-2-G - 12 образцов), ВВЗ (CОП+-BB3-G - 12 образцов), ВЭБ (CОП+-BЭБ-G - 12 образцов), ЦМВ (COП+-ЦMB-G - 12 образцов), ВГЧ-6 (СОП+-ВГЧ-6-G - 12 образцов), ВГЧ-7 (СОП+-ВГЧ-7-G - 12 образцов) и ВГЧ-8 (СОП+-ВГЧ-8-G- 12 образцов). Указанные стандартные панели изготовлены из образцов сыворотки крови человека, полученных в коммерческой лаборатории «ИНВИТРО», с положительным результатом по наличию IgG к ВПГ-1, ВПГ-2, ВВЗ, ВЭБ, ЦМВ, ВГЧ-6, ВГЧ-7 и ВГЧ-8 соответственно. Дополнительно полученные образцы были верифицированы в иммуноферментных тест-системах производства ЗАО «ЭКОлаб»: «ИФА-ВПГ-1-IgG», «ИФА-ВПГ-2-IgG», «ИФА-Ветряная оспа-IgG», «ИФА-Эпштейн-Барр-IgG», «ИФА-ЦМВ-IgG», «ИФА-ВГЧ-6-IgG», «ИФА-ВГЧ-7-IgG» и «ИФА-ВГЧ-8-IgG» соответственно.
В качестве референсного материала при оценке специфичности разработанной тест-системы были исследованы сыворотки стандартных панелей положительных образцов предприятия ЗАО «ЭКОлаб», не содержащих IgG к индивидуальным белкам ВПГ-1 (СОП--ВПГ-1-G - 12 образцов), ВПГ-2 (СОП--ВПГ-2-G - 12 образцов), ВВЗ (СОП--BBЗ-G - 12 образцов), ВЭБ (СОП--BЭБ-G - 12 образцов), ЦМВ (СОП--ЦMB-G - 12 образцов), ВГЧ-6 (СОП--ВГЧ-6-G - 12 образцов), ВГЧ-7 (СОП--ВГЧ-7-G - 12 образцов) и ВГЧ-8 (СОП--ВГЧ-8-G - 12 образцов). Указанные стандартные панели изготовлены из образцов сыворотки крови человека, полученных в коммерческой лаборатории «ИНВИТРО», с отрицательным результатом по наличию IgG к ВПГ-1, ВПГ-2, ВВЗ, ВЭБ, ЦМВ, ВГЧ-6, ВГЧ-7 и ВГЧ-8 соответственно. Дополнительно полученные образцы были верифицированы в иммуноферментных тест-системах производства ЗАО «ЭКОлаб»: «ИФА-ВПГ-1-IgG», «ИФА-ВПГ-2-IgG», «ИФА-Ветряная оспа-IgG», «ИФА-Эпштейн-Барр-IgG», «ИФА-ЦМВ-IgG», «ИФА-ВГЧ-6-IgG», «ИФА-ВГЧ-7-IgG» и «ИФА-ВГЧ-8-IgG» соответственно.
Список источников информации
1. Davison A., Eberle R., Ehlers В., Hayward G., McGeoch D., Minson A., Pellett Ph., Roizman В., Studdert M., Thiry E. The order Herpesvirales // Arch of Virology. - 2009(Jan). - Vol. 154, №1. -P. 171-177.
2. Richard J. Herpesviruses / Chapter 68 in Medical Microbiology, 4th ed. -Whitley: University of Texas Medical Branch at Galveston, 1996.
3. Мурзич A.B., Голубев M.A. Герпетическая инфекция // Южно-Российский медицинский журнал. – 1998. - №3 [Электронный ресурс]: https://medi.ru/info/6380/ (дата обращения: 19.02.2020).
4. Gottlieb S.L., Douglas J.M.Jr., Schmid D.S. et al. Project RESPECT Study Group. Seroprevalence and correlates of herpes simplex virus type 2 infection in five sexually transmitted-disease clinics // J Infect Dis. - 2002. - Vol. 186.-P. 1381-1389.
5. Staras S.A., Dollard S.C., Radford K.W., Flanders W.D., Pass R.F., Cannon M.J. Seroprevalence of cytomegalovirus infection in the United States, 1988-1994 // Clin Infect Dis. - 2006(Nov). - Vol. 43, №9. - P. 1143-1151.
6. Кускова Т.К., Белова Е.Г. Семейство герпесвирусов на современном этапе // Лечащий врач. – 2004. - №5 [Электронный ресурс]: http://www.lvrach.ru/2004/05/4531295 (дата обращения: 19.02.2020).
7. Шульженко А. Е., Викулов Г. X., Тутушкина Т. В. Герпетические инфекции - настоящее и будущее // Трудный пациент. - 2003. - Т.1. - №4. -С. 6-15.
8. Новикова Е.В., Яковлева Л.С., Стенина В.Н., Гурцевич В.Э. Обнаружение и клинико-морфологическая характеристика опухолей желудка, ассоциированных с вирусом Эпштейна-Барр // Русский журнал ВИЧ/СПИД и родственные проблемы. – 1999. – ТЗ. - №1. – С. 28-33.
9. Логутова Л.С., Новикова СВ., Бочарова И.И. Оптимизация ведения беременных с высоким инфекционным риском // РМЖ. - 2015. - Т.23. - №1. -С. 6.
10. Баринский И.Ф. Герпесвирусные инфекции – иммунодефицитные заболевания XXI века // Актуальные проблемы герпесвирусных инфекций. -2004. – С. 5-7.
11. Самгин М.А., Халдин А.А. Простой герпес (дерматологические аспекты). – М.: МЕДпресс-информ, 2002. – 160 с.
12. Исаков В.А., Ермоленко Д.К., Ермоленко Е.И. Герпесвирусные и папилломавирусные инфекции. / В кн.: Аковбян В.А., Прохоренков В.И., Соколовский Е.В. [ред.] «Инфекции, передаваемые половым путем». – М.: Медиа Сфера, 2007. – С. 448-513.
13. Рахманова А.Г., Пригожкина В.К., Неверов В.А. Инфекционные болезни: Руководство для врачей общей практики. - М.-СПб.: ССЗ, 1995. -304 с.
14. Ward К.М., Andrews N.J., Verity СМ., Miller Е. Human herpesviruses-6 and -7 each cause significant neurological morbidity in Britain and Ireland // Arch Dis Child. - 2005. - Vol. 90. - №6. - P. 619-623.
15. Калугина М.Ю., Каражас H.B., Рыбалкина Т.Н., Бошьян Р.Е., Ермакова Т.М., Тебеньков А.В. Актуальность диагностики инфекции, вызванной вирусом герпеса человека 6-го // Детские инфекции. – 2012. - №1. –С. 60-63.
16. Лабораторная диагностика инфекционных вирусных заболеваний. 2-е издание // Коллектив авторов СПб ГУЗ «Городской диагностический центр (вирусологичекий)», Экспертная лаборатория Минздрава РФ. – СПб: [б.и.], 2004. – 94 с.
17. Марданлы С.Г., Арсеньева В.А., Амелина Е.А., Марданлы С.С., Ротанов С.В. Применение метода линейного иммуноблоттинга для определения антител классов G и М к основным возбудителям инфекций TORCH-группы // Справочник заведующего КДЛ. – 2015. - №9. – С. 4-13.
18. Ashley R., Militoni J. Use of densitometric analysis for interpreting HSV serologies based on Western blot // J. Virol. Methods. – 1987. – Vol. 18. – P. 159-168.
19. Lee F. K., Coleman R. M., Pereira L., Bailey P. D., Tatsuno M., Nahmias A. J. Detection of herpes simplex virus type 2-specific antibody with glycoprotein G // J. Clin. Microbiol. – 1985. – Vol. 22, №4. – P. 641-644.
20. Gorander S., Svennerholm В., Liljeqvist J. Secreted portion of
glycoprotein g of herpes simplex virus type 2 is a novel antigen for type-
discriminating serology // Journal of Clinical Microbiology. – 2003. – Vol. 41,
№8. – P. 3681-3686.
21. Laboratory diagnosis of sexually transmitted infections, including human immunodeficiency virus / edited by Magnus Unemo… [et al.]. - Chapter 9. Herpes simplex virus (HSV) infections. - World Health Organization. - 2013. - P. 93-106.
22. Kutinova L., Hainz P., Ludvikova V., Maresova L., Nemeckova S. Immune response to vaccinia virus recombinants expressing glycoproteins gE, gB, gH, and gL of varicella-zoster virus // Virology. - 2001. - Vol. 280. - P. 211-220.
23. Montalvo E.A., Parmley R.T., Grose C. Structural analysis of the varicella-zoster virus gp98-gp62 complex: posttranslational addition of N-linked and O-linked oligosaccharide moieties // J. Virol. - 1985. - Vol. 53. - P. 761-770.
24. Edson СМ., Hosier B.A., Respess R.A., Waters D.J., Thorley-Lawson D.A. Cross-reactivity between herpes simplex virus glycoprotein В and a 63,000-dalton varicella zoster virus envelope glycoprotein // J. Virol. - 1985. - Vol. 56. -P. 333-336.
25. Grahn A., Studahl M., Nilsson S. et al. Varicella-zoster virus (VZV) glycoprotein E is a serological antigen for detection of intrathecal antibodies to VZV in central nervous system infections, without cross-reaction to herpes simplex virus 1 // Clin. Vaccine Immunol. - 2011. - Vol. 18, №8. - P. 1336-1342.
26. Human Herpesviruses: Biology, Therapy, and Immunoprophylaxis / Eds A. Arvin, G. Campadelli-Fiume et al. - Cambridge: Cambridge University Press, 2007: 1432.-P. 929-935.
27. Tomtishen J. P. III. Cytomegalovirus Tegument Proteins and the Development of Novel Antiviral Therapeutics // Manifestations of Cytomegalovirus Infection / Edited by Price P., Makwana N. and Brunt S. –Chapter 7. – InTech, 2013. – P. 111-131.
28. Маркина М.В., Романов В.В. Иммуноблот в диагностике инфекционных заболеваний. Новые возможности. Практическое руководство по интерпретации полученных результатов [Электронный ресурс]. URL: http://www.labdiagnostic.rn/docs/specialists/immunobloM (дата обращения: 19.02.2020).
29. Adams M.J., Carstens Е.В. Ratification vote on taxonomic proposals to the International Committee on Taxonomy of Viruses // Archives of virology. - 2012. -Vol. 157, №7. - P. 1411-1422.
30. De Bolle L., Van Loon J., De Clercq E., Naesens L. Quantitative analysis of human herpesvirus 6 cell tropism // Journal of medical virology. - 2005. - Vol. 75, № 1. - P. 76-85.
31. Alvarez-Lafuente R., Garcia-Montojo M., De las Heras V., Bartolome M., Arroyo R. Clinical parameters and HHV-6 active replication in relapsing-remitting multiple sclerosis patients // Journal of clinical virology : the official publication of the Pan American Society for Clinical Virology.- 2006. - Vol. 37, Suppl 1. - P. 24-26.
32. Black J.B., Schwarz T.F., Patton J.L., Kite-Powell K., Pellett P.E., Wiersbitzky S., Bruns R., Muller C., Jager G., Stewart J. Evaluation of immunoassays for detection of antibodies to human herpesvirus 7 // Clin. Diagn. Lab. Immunol. – 1996. - №3. – P. 79-83.
33. Franti M., Aubin J.T., De Saint-Maur G., Kosuge H., Yamanishi K., Gautheret-Dejean A., Garbarg-Chenon A., Huraux J.M., Agut H. Immune reactivity of human sera to the glycoprotein В of human herpesvirus 7 // J. Clin. Microbiol. – 2002. - №40. – P. 44-51.
34. Corchero J.L., Mar E.C., Spira T.J., Pellett P.E., Inoue N. Comparison of Serologic Assays for Detection of Antibodies against Human Herpesvirus 8 // Clin. Diagn. Lab. Immunol. - 2001. - №8. - P. 913-921.
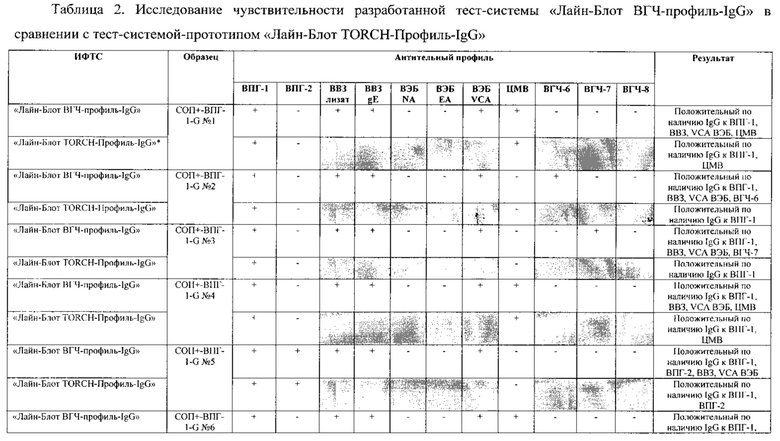
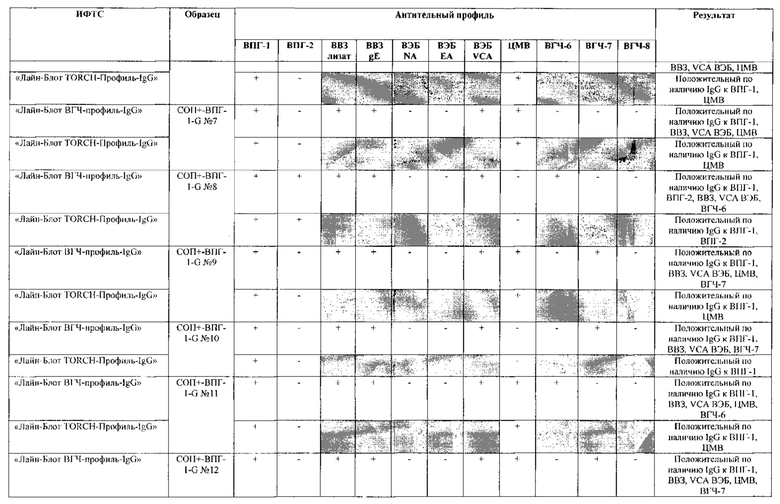
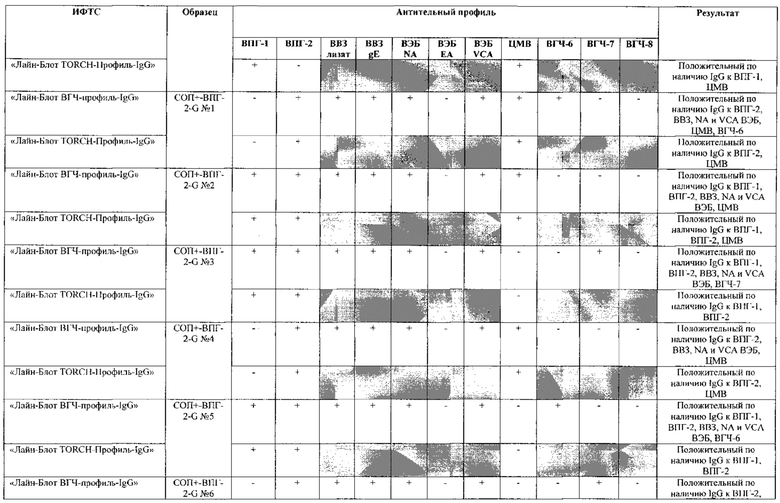
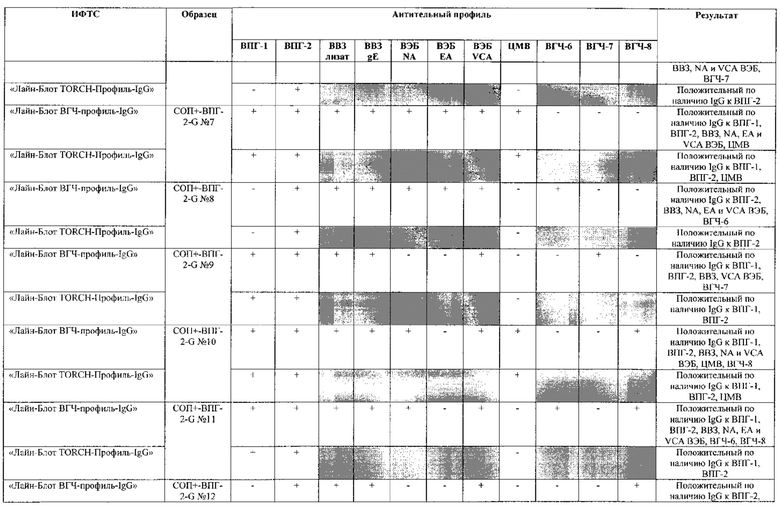
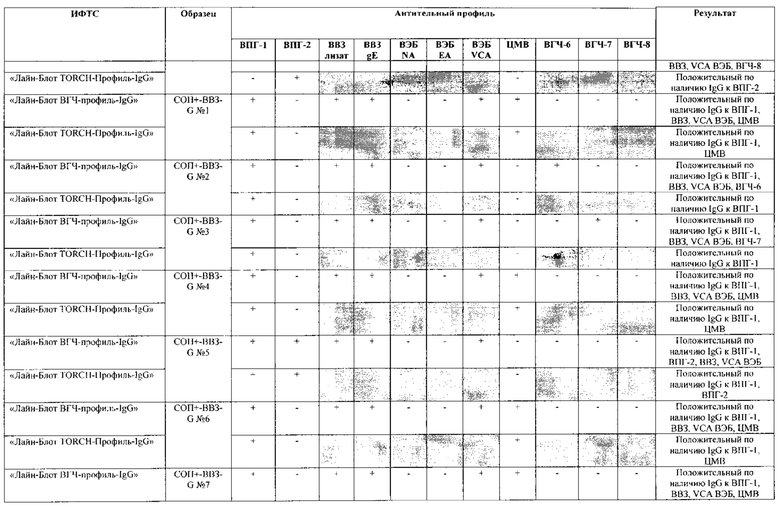
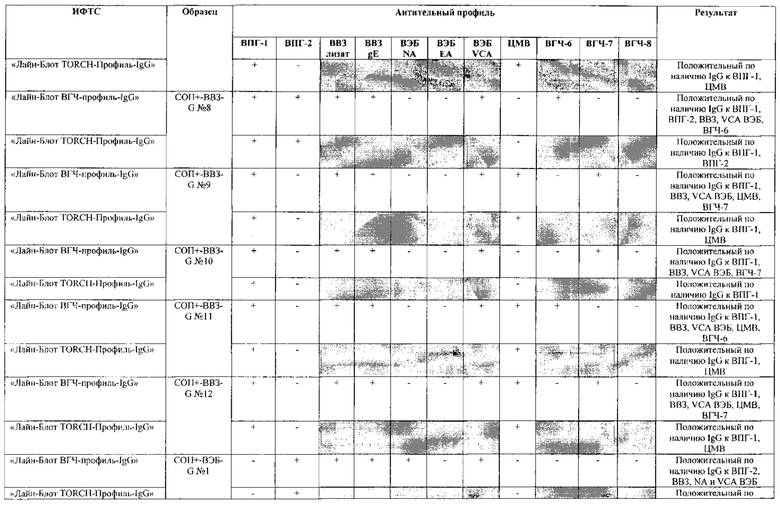

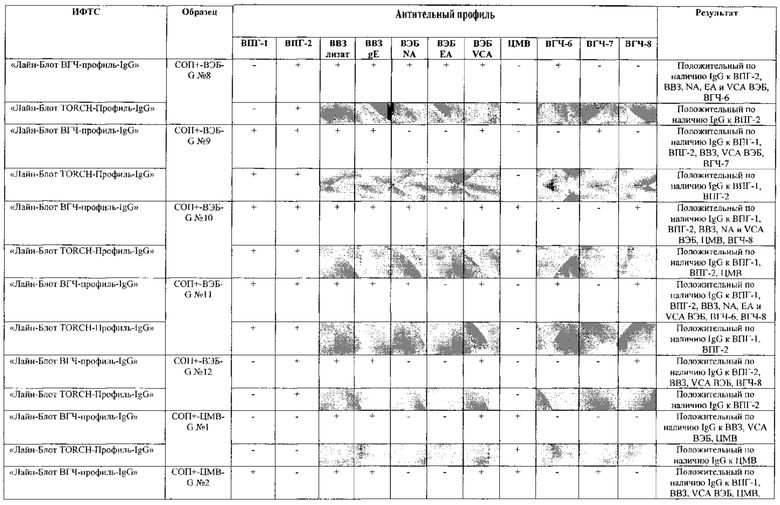
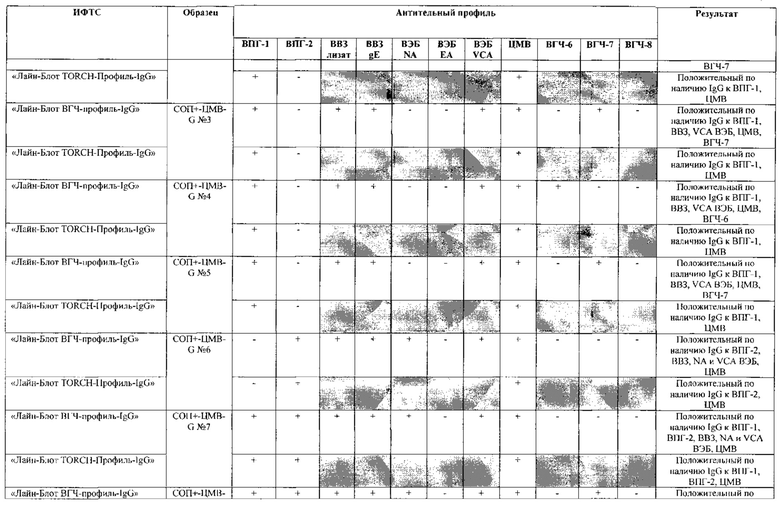
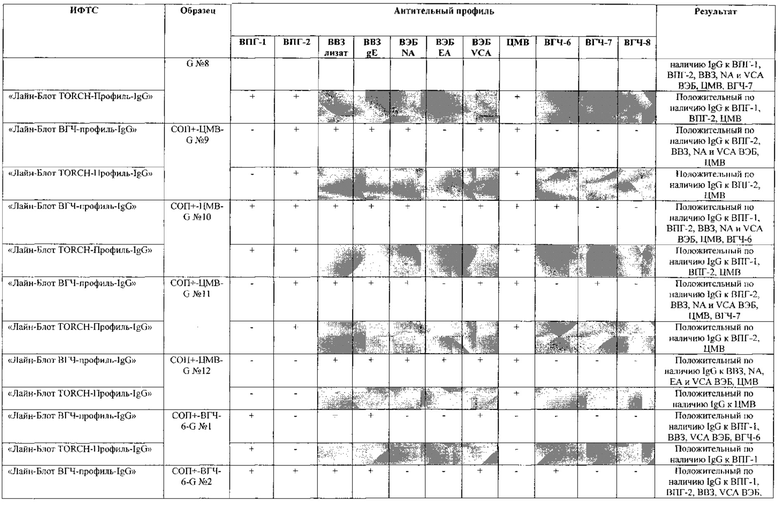
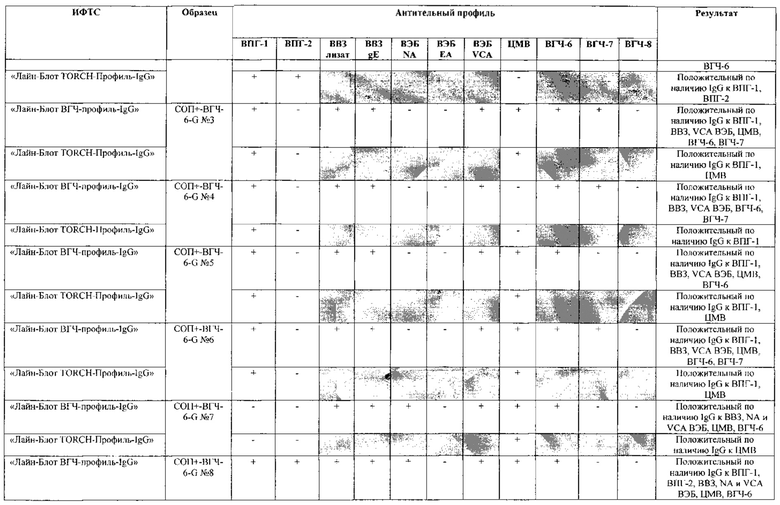
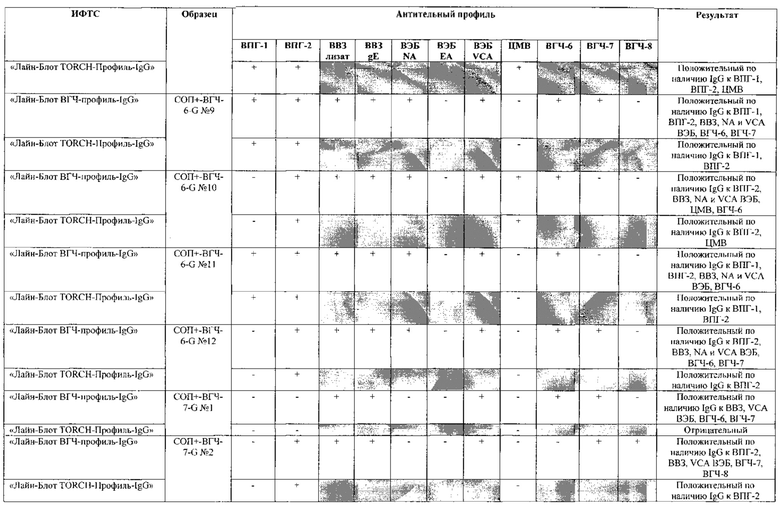
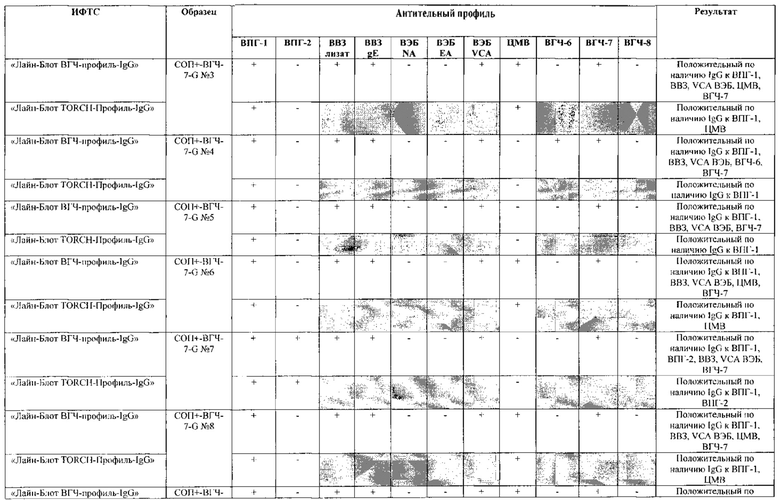
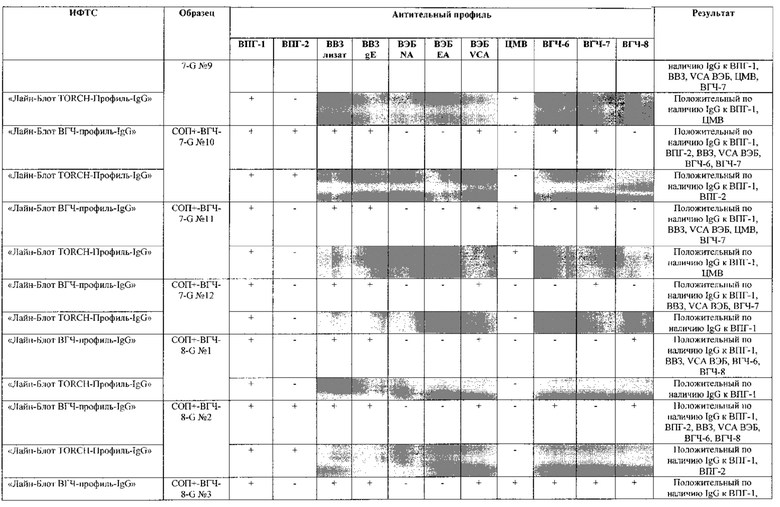
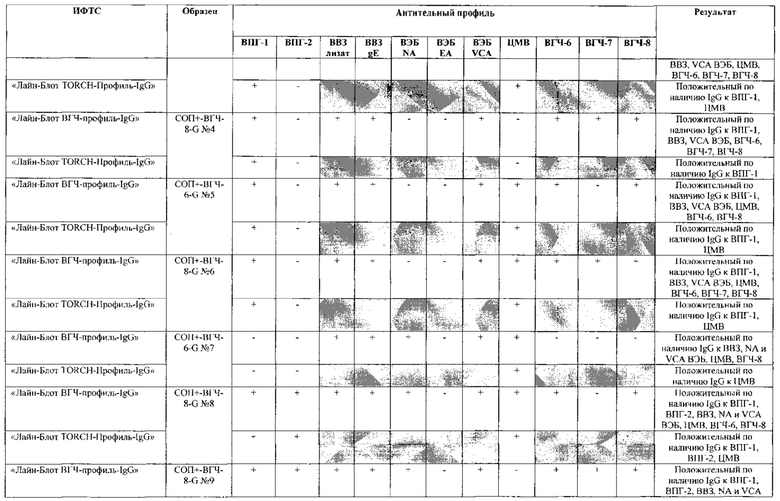
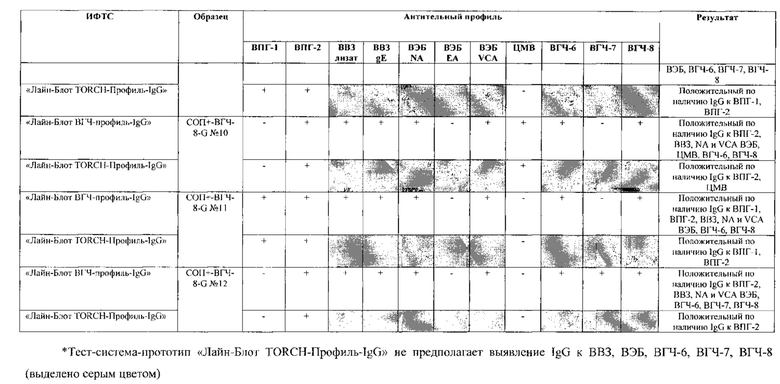
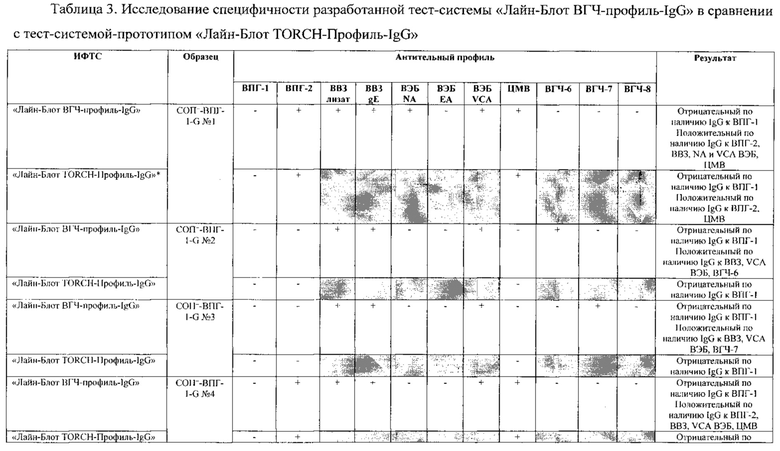
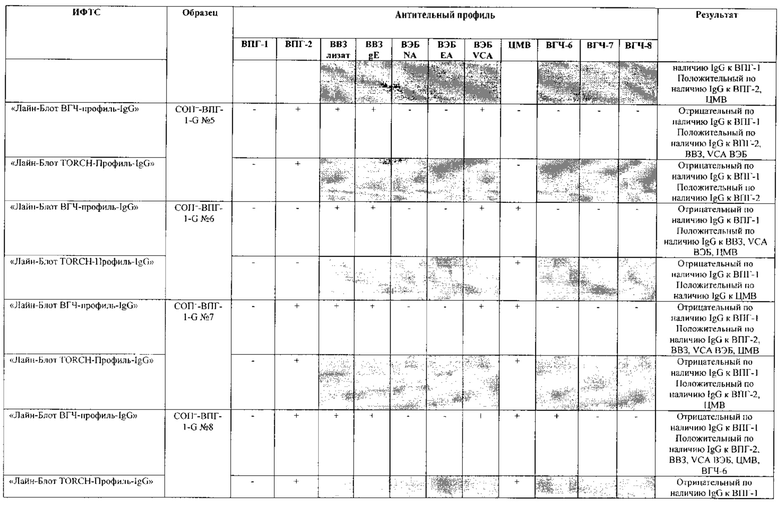
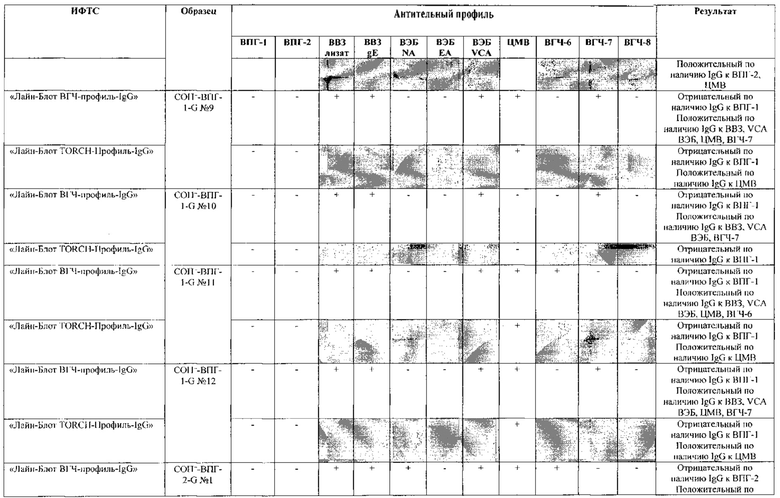
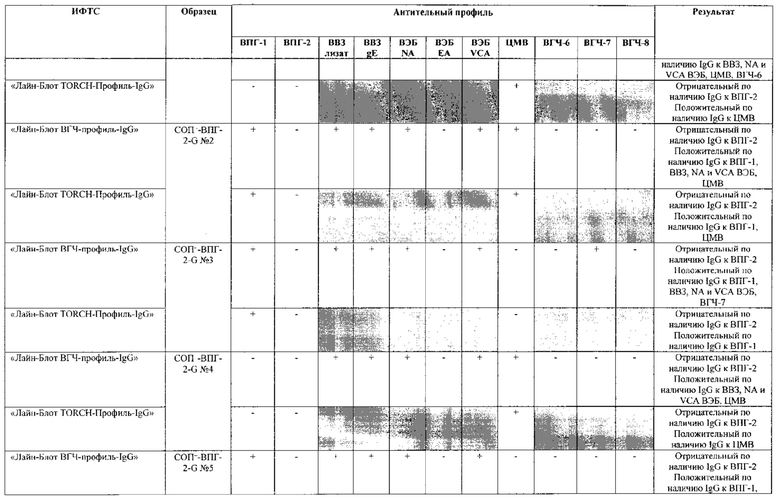
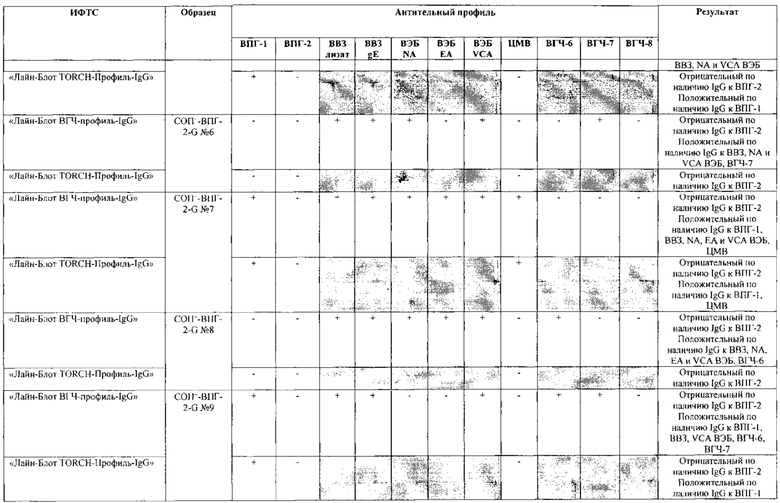
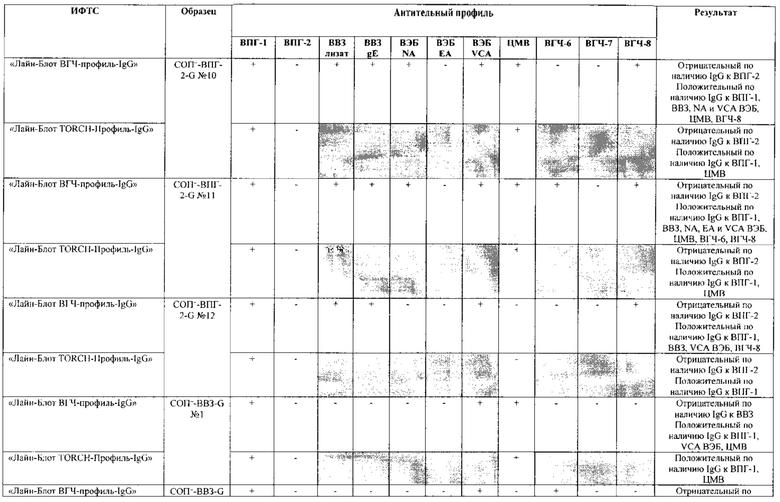

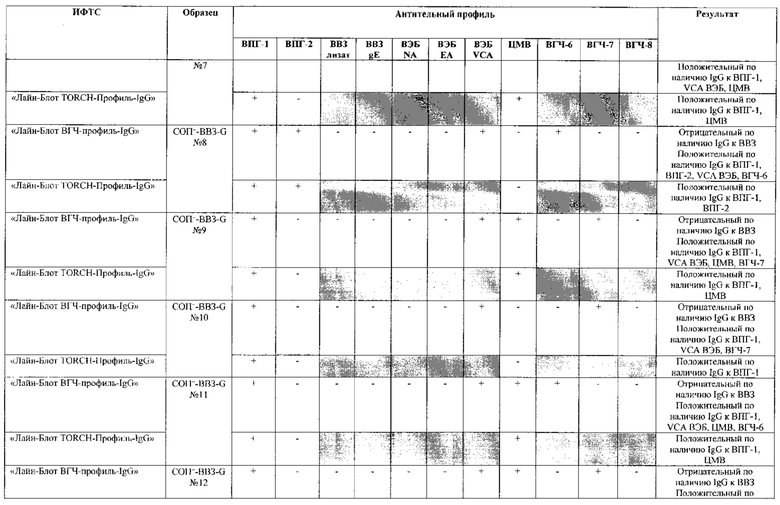
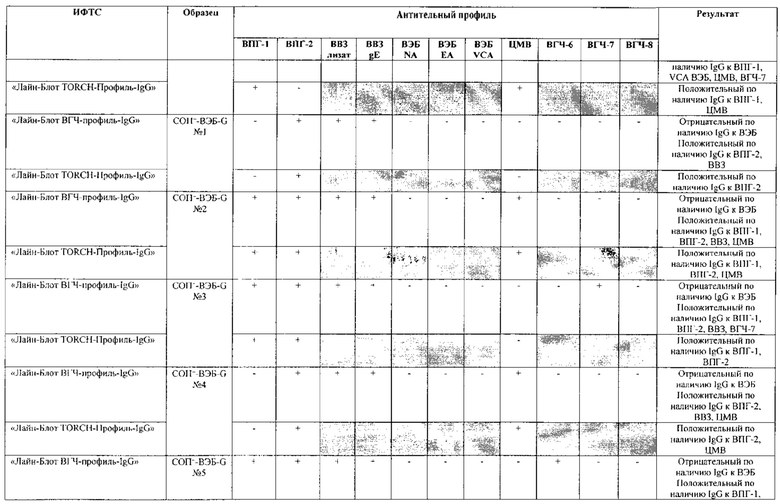
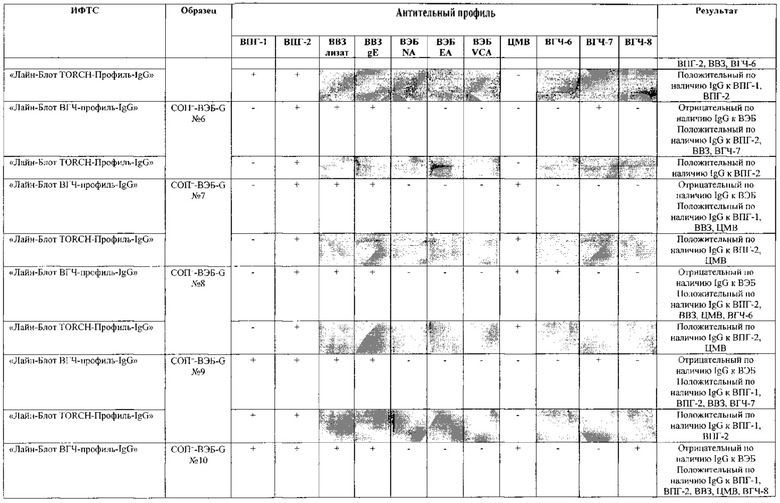
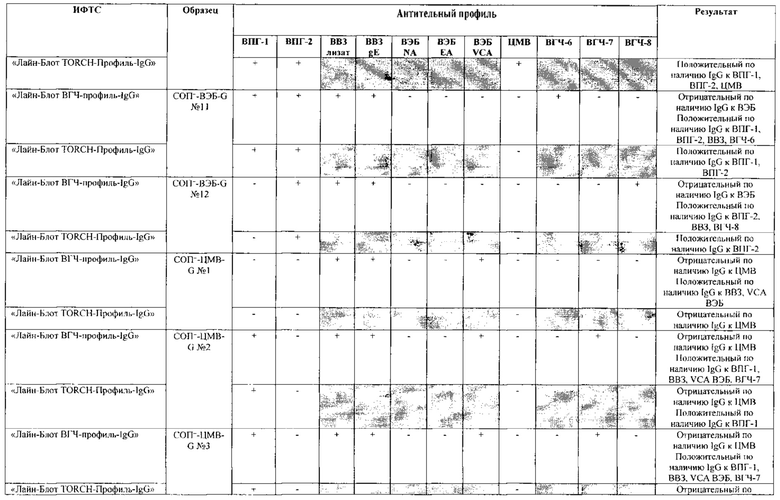
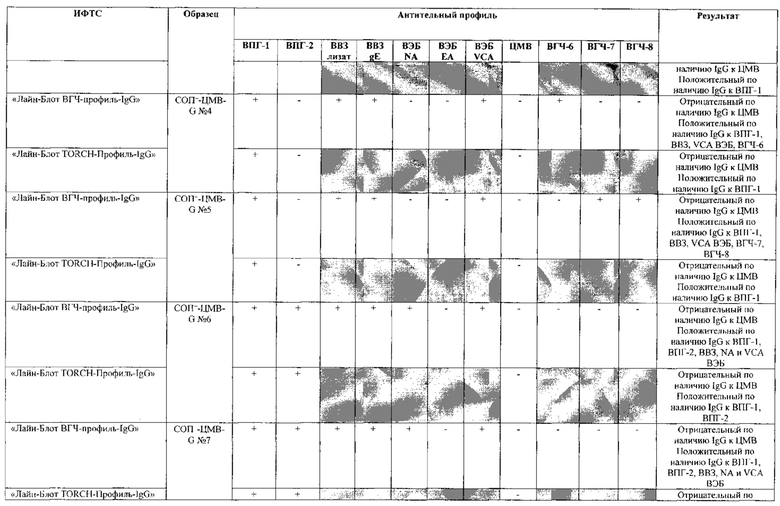
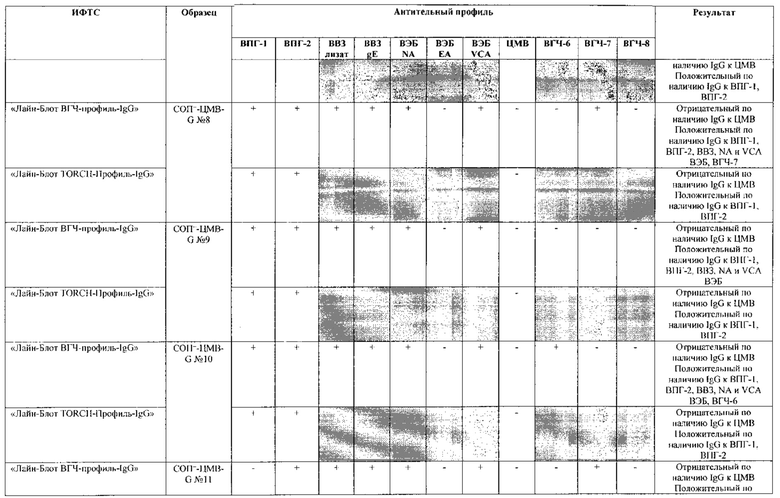
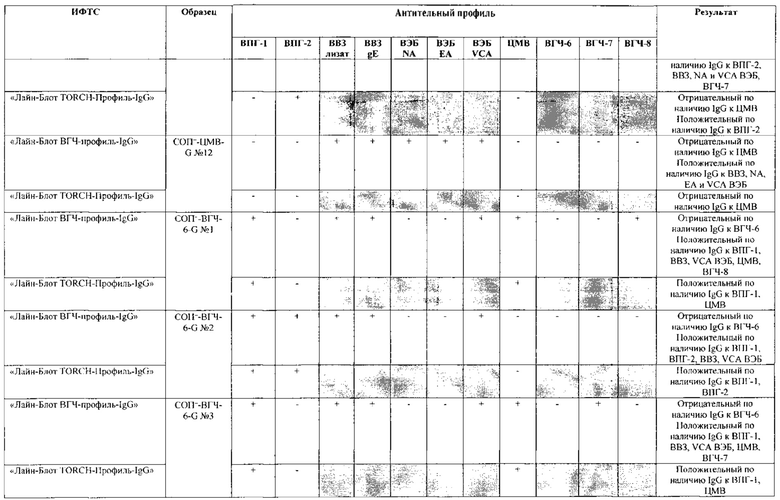
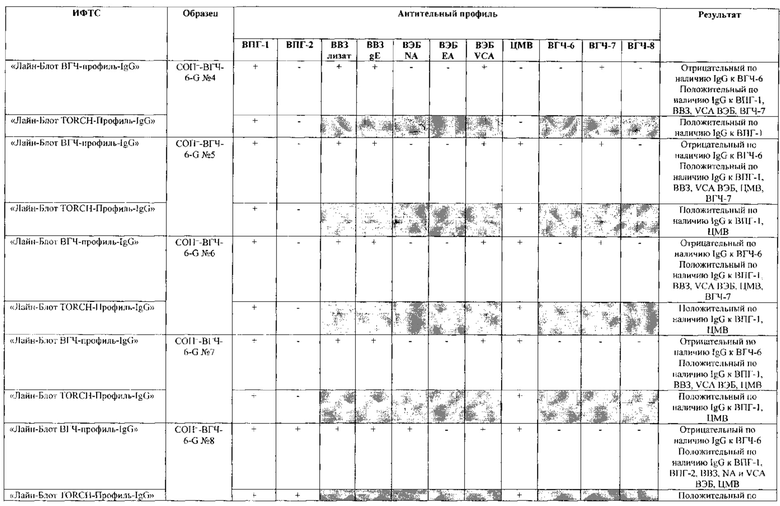
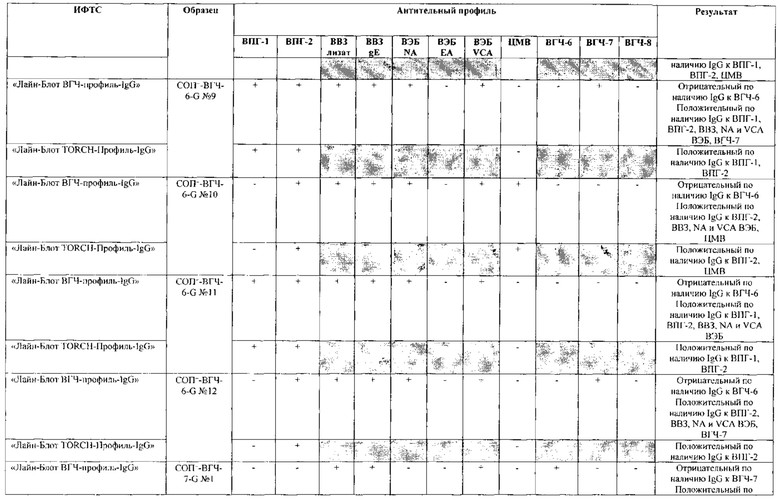
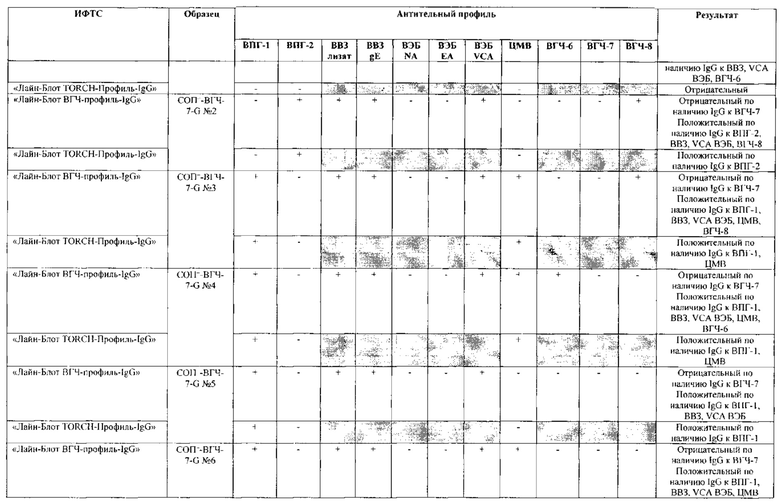
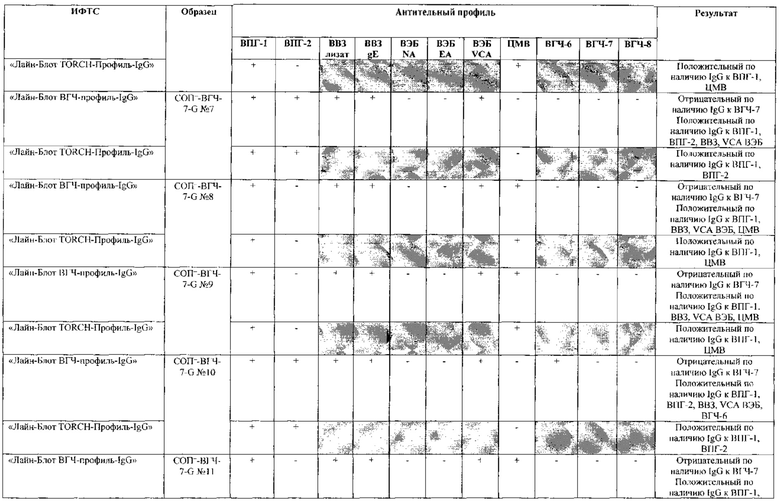
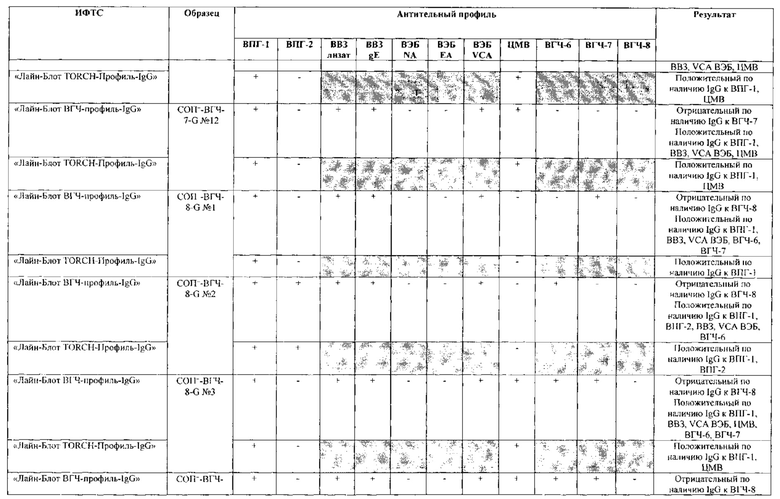
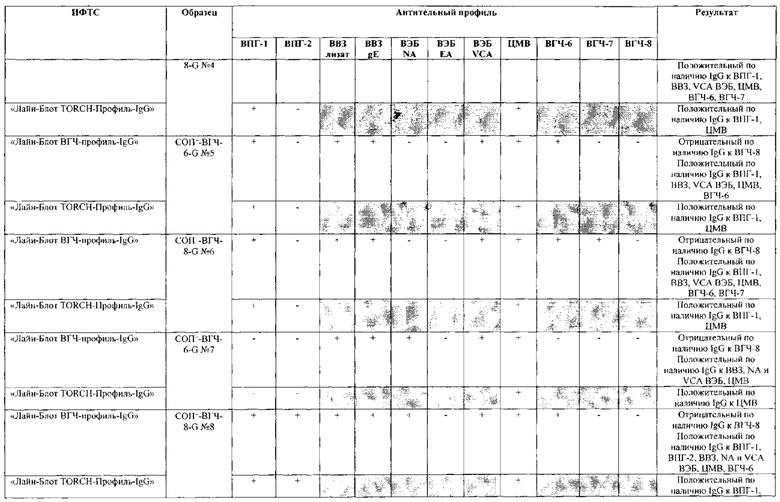
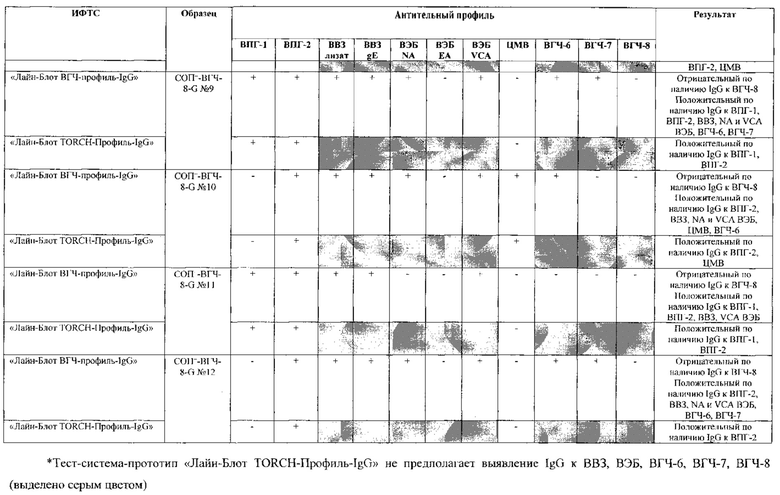
Как следует из табл. 2 и 3, по результатам проведенных испытаний в обеих тест-системах было получено полное совпадение итоговых оценок исследованных образцов в отношении выявления IgG к ВПГ-1, ВПГ-2 и ЦМВ. Также получено полное совпадение оценок сывороток стандартных панелей, полученных в исследовании разработанной тест-системы «Лайн-Блот ВГЧ-профиль-IgG», с их исходными характеристиками.
Таким образом, за счет расширения спектра антигенов (включение в состав иммуносорбента антигенов ВВЗ, ВЭБ, ВГЧ-6, ВГЧ-7, ВГЧ-8) разработанная тест-система «Лайн-Блот ВГЧ-профиль-IgG» обладает более высокой чувствительностью, чем тест-система-прототип «Лайн-Блот ТОRСН-Профиль-IgG», которая не предполагает выявление IgG к ВВЗ, ВЭБ, ВГЧ-6, ВГЧ-7, ВГЧ-8.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТЕСТ-СИСТЕМЫ ДЛЯ ДИАГНОСТИКИ ЦИТОМЕГОВИРУСНОЙ ИНФЕКЦИИ МЕТОДОМ ИММУНОБЛОТТИНГА | 2013 |
|
RU2545785C2 |
| СПОСОБ ОДНОВРЕМЕННОГО ДЕТЕКТИРОВАНИЯ АНТИТЕЛ КЛАССА G К АНТИГЕНАМ ВОЗБУДИТЕЛЕЙ TORCH-ИНФЕКЦИЙ С ИСПОЛЬЗОВАНИЕМ ИММУНОЧИПА | 2014 |
|
RU2545792C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОСОРБЕНТА ДЛЯ ДИАГНОСТИКИ ВИРУСА ПРОСТОГО ГЕРПЕСА 1 ТИПА | 2013 |
|
RU2528896C1 |
| Набор для выявления антител классов M и G к нуклеокапсиду (Nc) и рецепторсвязывающему домену спайк белка коронавируса SARS-CoV-2 | 2023 |
|
RU2808765C2 |
| Композиция для профилактики заболеваний, вызываемых цитомегаловирусной инфекцией | 2015 |
|
RU2616245C2 |
| СПОСОБ ДИАГНОСТИКИ ГЕРПЕСВИРУСНЫХ ЗАБОЛЕВАНИЙ ГЛАЗ | 2006 |
|
RU2400756C2 |
| Способ дифференциальной диагностики герпесвирусной микст-инфекции | 2020 |
|
RU2739854C1 |
| СТАБИЛИЗИРОВАННЫЙ КАРДИОЛИПИНОВЫЙ АНТИГЕН ДЛЯ РЕАКЦИИ МИКРОПРЕЦИПИТАЦИИ ПРИ ДИАГНОСТИКЕ СИФИЛИСА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2633087C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АВИДНОСТИ ИММУНОГЛОБУЛИНОВ КЛАССА G К ВИРУСУ ГЕРПЕСА 6 ТИПА | 2015 |
|
RU2596794C1 |
| Способ диагностики периода инфекционного заболевания, вызванного вирусом varicella zoster у детей | 2016 |
|
RU2629335C1 |
Изобретение относится к медицине, в частности к клинической лабораторной диагностике. Раскрыта тест-система для одновременной детекции гуморальных маркеров инфицирования герпесвирусами человека, включающая иммуносорбент в виде тест-полосок (стрипов), на каждой из которых в виде отдельных линий нанесены следующие антигены: гес антиген gG-1 HSV-1; гес антиген gG-2 HSV-2; нативный антиген VZV; гес антиген gE VZV; гес антигены EBV: ядерный - EBNA (Epstein Barr Nuclear Antigen), ранний - EA (Early Antigen) и капсидный - VCA (Viral Capsid Antigen); гес мозаичный антиген CMV, содержащий последовательности белков рр150, рр52, рр28 и gB; гес большой структурный фосфопротеин (Large structural protein) Ul1 вируса HHV-6; гес гликопротеин В (gB) вируса HHV-7; гес мозаичный антиген HHV-8, содержащий последовательности белков ORF65 и ORF8 (К8). Изобретение обеспечивает замену нескольких лабораторных исследований в формате ИФА одним диагностическим исследованием, возможность одновременного выявления антител класса G ко всем патогенным для человека типам герпесвирусов, использование минимального количества биологического материала по сравнению с несколькими постановками ИФА и экономию трудовых затрат специалистами лабораторной медицины. 2 з.п. ф-лы, 3 табл., 3 пр.
1. 1. Тест-система для одновременной детекции гуморальных маркеров инфицирования герпесвирусами человека методом линейного иммуноблотинга, включающая иммуносорбент в виде тест-полосок (стрипов), на каждой из которых в виде отдельных линий нанесены следующие антигены:
- гес антиген gG-1 HSV-1;
- гес антиген gG-2 HSV-2;
- нативный антиген VZV;
- гес антиген gE VZV;
- гес антигены EBV: ядерный – EBNA (Epstein Barr Nuclear Antigen), ранний – EA (Early Antigen) и капсидный – VCA (Viral Capsid Antigen);
-гес мозаичный антиген CMV, содержащий последовательности белков рр150, рр52, рр28 и gB;
- гес большой структурный фосфопротеин (Large structural protein) Ul1 вируса HHV-6;
- гес гликопротеин В (gB) вируса HHV-7;
- гес мозаичный антиген HHV-8, содержащий последовательности белков ORF65 и ORF8 (К8).
2. Тест-система по п.1, отличающаяся тем, что дополнительно на тест-полоске имеются участки для маркировки, в частности нанесения идентифицирующего номера.
3. Тест-система по п.1, отличающаяся тем, что тест-полоска содержит контрольную линию - контроль внесения образца.
| МАРДАНЛЫ С.Г | |||
| и др | |||
| Синхронная детекция серологических маркеров основных герпесвирусных инфекций // Инфекционные болезни | |||
| Гастроэнтерология, 2017, N.1, стр.25-30 | |||
| SPIRA T.J | |||
| et al | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
Авторы
Даты
2020-06-26—Публикация
2019-04-24—Подача