Изобретение относится к области медицины, а именно к онкологии, к иммуногенетическим исследованиям и может быть использовано для прогнозирования возникновения злокачественных новообразований у детей при нарушении иммунологического гемостаза.
Заболеваемость детей злокачественными опухолями в России за последние 10 лет увеличилось на 20% и достигла 4,25. В настоящее время в России насчитывается около 12500 детей до 15 лет находящихся под врачебным наблюдением по поводу злокачественных новообразований всех локализаций. Россию можно отнести к странам с высоким уровнем заболеваемости детской онкологической патологией. Солидные злокачественные новообразования, включая опухоли ЦНС, занимают второе место в структуре заболеваемости детей злокачественными опухолями, на их долю по данным различных отечественных и зарубежных авторов приходится от 48,5 до 54% от всей онкопатологии.
Известен «Способ прогнозирования течения онкологических заболеваний» (см. патент №2018835 от 11.11.90. Биол. №16 от 30.08.94). Сущность изобретения заключается в том, что в лимфоцитах и нейтрофилах крови определяют содержание гистамина в течение 4-5 суток, рассчитывают отношение первого показателя ко второму и при значении более 0,9 прогнозируют осложнение течения заболевания в виде появления рецидивов и метастазов. Недостаток данного способа заключается в его не специфичности для рака щитовидной железы, так как данный показатель может повышаться и при других локализаций рака, а также вирусных заболеваниях как показатель неспецифической стимуляции Т-клеточного звена иммунитета.
Известен «Способ дифференциальной диагностики злокачественных опухолей щитовидной железы у детей и подростков» (см. патент №23 00106 от 27 мая 2007 года. Биол. №15), выбранный нами в качестве прототипа. Сущность изобретения заключается в том, что у детей и подростков с узловыми образованиями щитовидной железы до начала лечения определяют антигены главного комплекса гистосовместимости и при выявлении антигенов: А10,В7,В35, а также неполном фенотипе по локусам HLA - А и HLA - В диагностируют паппилярный рак щитовидной железы без присоединения аутоиммунного компонента и выполняют радикальное оперативное вмешательство, а при отсутствии данных антигенов диагностируют фолликулярный вариант опухоли и выполняют органносохранные операции.
Известный способ позволяет выбрать наиболее эффективный и адекватный метод хирургического лечения при различных диагностических показателях рака щитовидной железы у детей и подростков, однако он не может быть использован в качестве прогностического фактора возникновения и развития злокачественных солидных опухолей у детей и подростков.
Целью изобретения является выявление иммуногенетических ассоциаций антигенов главного комплекса гистосовместимости с наличием солидных злокачественных опухолей у детей.
Поставленная цель достигается тем, что у детей и подростков с солидными опухолями определяют антигены главного комплекса гистосовместимости путем серологического типирования I и II класса HLA типирования PCS-SSP и прогнозируют группы риска возникновения злокачественных опухолей у детей и подростков при повышении частоты антигенов HLA A26 у детей с нефробластомой и герминогенными опухолями, повышение частоты HLA В13 при нейробластоме, а также частоты HLA DRB1 13 при нефробластоме.
Изобретение «Способ прогнозирования развития злокачественных солидных опухолей у детей и подростков» является новым, так как оно неизвестно в медицине в области лабораторной диагностики, а именно, при иммуногенетическом исследовании в онкопатологии, для прогнозирования развития солидных злокачественных опухолей у детей и подростков.
Возникновение злокачественных новообразований становится возможным при нарушении иммунологического гомеостаза. Развитие недостаточности функций иммунной системы находится под контролем генов иммунного ответа, ассоциированных, в сою очередь, с антигенами гистосовместимости. Следовательно, существует взаимосвязь онкозаболеваний с антигенами системы HLA.
Таким образом, совокупность представленных нами существенных признаков не известна из уровня медицины в области иммуногенетических исследований в онкологии для планирования эффективных методов лечения.
У детей с солидными злокачественными опухолями проводят HLA типирование I и II класса HLA типирования PCS-SSP.
Новизна представленного изобретения заключается в том, что у детей и подростков с солидными злокачественными опухолями определяют антигены главного комплекса гистосовместимости. При повышении частоты антигенов HLA A26 у детей с нефробластомой и герминогенными опухолями, повышение частоты HLA В 13 при нейробластоме, а так же повышение частоты антигенов HLA DRB1 13 при нейробластома и нефробластоме - данные группы детей можно отнести к группам риска возникновения данных злокачественных опухолей.
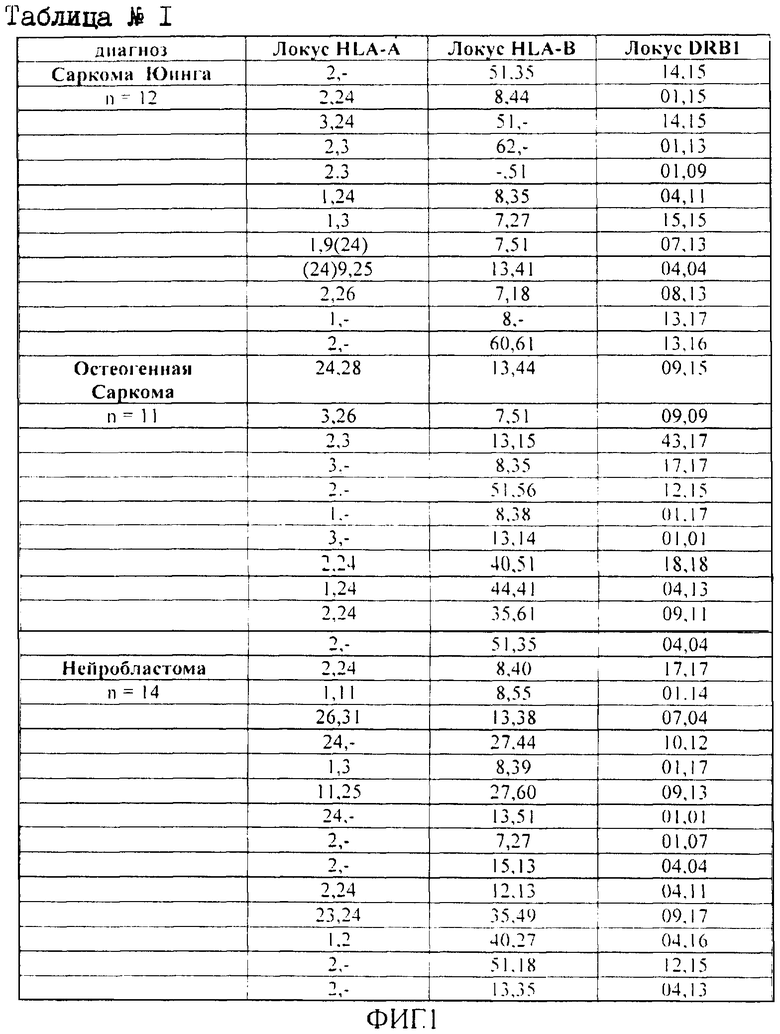
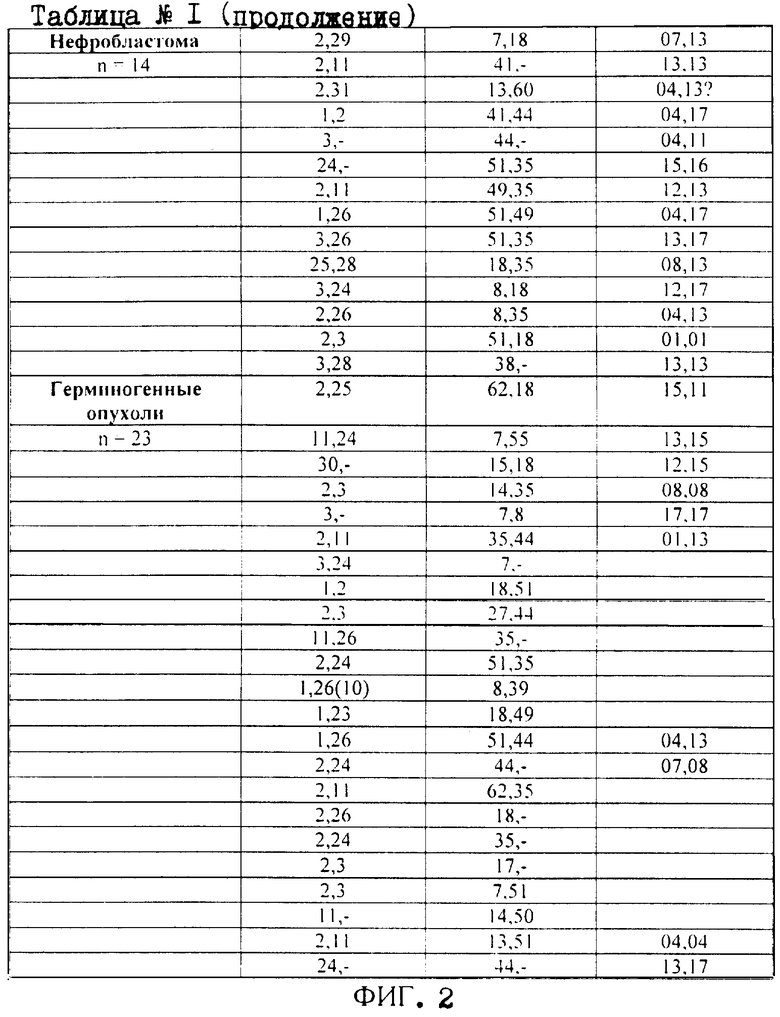
Изобретение «Способ прогнозирования развития злокачественных солидных опухолей у детей и подростков» является промышленно применимым, так как может быть использован в здравоохранении, детских медицинских учреждениях онкологического профиля, диспансерах, научно-исследовательских онкологических институтах. Способ прогнозирования развития злокачественных солидных опухолей у детей и подростков выполнялся следующим образом: было проведено у 74 пациентов ОДО РНИОИ определение антигенов HLA I и II класса, контрольную группу составили доноры ГУЗ СПК РО в количестве 1215 доноров (I класс) и 128 доноров (II класс). Сводные данные представлены в таблице №1 и таблица №1 (продолжение) (HLA - фенотип больных детей с солидными злокачественными опухолями, ФИГ.1, ФИГ.2).
Серологическое типирование осуществляли в стандартном лимфоцитотоксическом тесте, предложенном Национальным институтом здоровья в Бетезде (NIH - метод), для определения HLA - антигенов I класса, локусов А и В. В качестве гистотипирующих стандартов использовали сыворотки Всероссийского банка гистотипирующих реагентов Санкт - Петербургского НИИ гематологии и переливании крови.
Генотипирование аллельных вариантов HLA II класса (DRBI - локус), проводили методом полимеразной цепной реакции с использованием панели праймеров фирмы «НПФ ДИК - Технология» (Москва).
Анализируя данные таблицы (HLA - фенотип больных детей с солидными злокачественными опухолями, ФИГ.1, ФИГ.2) выявлено: при нейробластоме повышение частоты антигенов HLA А24 - 35,71% (контроль - 16,46%), В8 - 21,42% (контроль - 10,86%), В 13 - 35,71% (контроль - 11,6%), В 27 - 28,57% (контроль - 10,74%), В 60 - 14,28% (контроль - 6,34%), достоверно повышена только частота антигена В 13 (%2 - 6,02, р<0,05). При нефробластоме наблюдается повышение частоты антигенов А26 - 21,42% (контроль - 5,35%), В51 - 28,57% (контроль - 12,35%), В 18 - 28,57% (контроль - 13,5%), В 35 - 35,71% (контроль - 14,9%), В 41 - 14,28% (контроль - 4,12), достоверно повышена только частота антигена А26 (χ2 - 6,85, р<0,05). У пациентов с Саркомой Юинга значительно повышена частота антигенов А24 - 41,66% (контроль - 16,46%), В51 - 33,33% (контроль - 12,35%), В61 - 8,33% (контроль - 2,47%). У пациентов с остеогенной саркомой повышена частота этих же антигенов: А24 - 36,36% (контроль - 16,46%), В51 - 36,36% (контроль - 12,35%), В61 - 9,0% (контроль - 2,47%). Так же отмечено повышение частоты В13, В56, В35 (27,27%, 9,0%, 27,27%) по сравнению с контролем (11,6%, 1,97%, 14,9%); снижена частота антигенов В7 - 9,0% (контроль - 19,67%), однако эти различия не достоверны. Число гомозигот по HLA - А локусу в группе с остеогенной саркомой составило 5 случаев, число гомозигот у пациентов с саркомой Юинга - 7. При герминогенных опухолях повышена частота антигенов А24 - 26,09% (контроль - 16,46%), А26 - 17,39% (контроль - 5,35%), A11 - 26,09% (контроль - 12,59%), В51 - 21,74% (контроль - 12,35%), В18 - 21,74% (контроль - 12,35%), В39 - 4,34% (контроль - 1,73%), В50 - 4,34% (контроль - 1,24%), В55 - 4,34%(контроль - 0,82%). Достоверные различия по сравнению с контрольной группой отмечены в частоте встречаемости антигена А26 (χ2 - 3,98, р<0,05). При проведении типирования генов HLA II класса в группе с нейробластомой было выявлено повышение частоты HLA DRB1 04 - 35,71% (контроль - 18,75%), DRB1 09 - 14,28% (контроль - 6,25%), DRB1 12 - 14,28% (контроль - 7,81%), DRB1 14 - 7,14% (контроль - 3,9%). При нефробластоме наблюдается повышение частоты DRB1 04 - 35,71% (контроль - 18,75%) и достоверно повышена частота DRB1 13 - 57,14% (χ2 - 4,45, р<0,05). При саркоме Юинга отмечается повышение частоты специфичностей: DRB1 14 - 16,67% (в контроле - 3,9%), так же повышена частота DRB1 15. У больных с остеогенной саркомой отмечено повышение частоты специфичностей: DRB1 03 - 45,45% (контроль - 22,65%) и DRB1 09 - 27,27%. У больных с герминогенными опухолями повышена частота DRB1 08 - 20,0% (контроль - 7,8%), DRB1 13 - 40,0% (контроль - 29,68%), DRB1 15 - 30,0% (контроль - 21,88%).
За период с 2010 по 2011 г. нами было обследовано 74 пациента (12 пациентов с саркомой Юинга, 11 пациентов с остеогенной саркомой, 14 пациентов с нейробластомой, 14 пациентов с нефробластомой, 23 пациента с герминогенными опухолями). Средний возраст больных составил: с саркомой Юинга - 11,8 года, остеогенная саркома - 17,1 года, нейробластомой - 4,7 года, нефробластомой - 4,8 года, герминогенные опухоли - 14,2 года. Заболевание начиналось в среднем в возрасте: с саркомой Юинга - 11,6 года, остеогенная саркома - 16,4 года, нейробластомой - 4,4 года, нефробластомой -4,2 года, герминогенные опухоли - 10,6 года. Из них при саркоме Юинга - 9 мальчиков, 3 девочки, при остеогенной саркоме - 7 мальчиков, 4 девочек, нейробластома - 8 мальчиков, 6 девочек, нефробластома - 9 мальчиков, 5 девочек, герминогенные опухоли - 10 мальчиков, 13 девочек.
HLA - фенотип больных детей с солидными злокачественными опухолями. ФИГ.1. и ФИГ.2.
Как видно из данных ФИГ.1 и ФИГ.2, в материалах заявки мы представили таблицу №1 и Таблица №1 (продолжение) фенотипов (HLA I и II классов) детей и подростков с солидными злокачественными опухолями. В зависимости от присутствия в фенотипе пациента антигена А26 у детей с нефробластомой и герминогенными опухолями, В 13 при нейробластоме, HLA DRB1 13 при нейробластоме и нефробластоме и учитывая достоверное повышение их частоты по сравнению с группой популяционного контроля, этих детей можно отнести к группам риска возникновения данных злокачественных опухолей.
Возможность осуществления изобретения «Способ прогнозирования развития злокачественных солидных опухолей у детей и подростков» подтверждается следующими историями болезни.
1. Больная И., 2007 г.р., история болезни №18505/ю, поступила в отделение детской онкологии 5.10.09 с диагнозом: Нейробластома крестцовой области с прорастанием мышц тазового дна, инфильтрацией клетчатки малого таза, St IV. Высокая группа риска, кл.группа.2. 10.09.09 была проведена операция - удаление опухоли малого таза. ГА пересмотрен в РНИОИ №1 1454-1 1468 от 29.09.09 - ганглионейробластома. Пересмотр Г.А. №68253-9/09 от 6.10.09 - нейробластома G 3, рядом с опухолью расположен нервный ганглий. Выполнено исследование главного комплекса гистосовместимости: HLA-фенотип (I и II класса): А24, А-; В13, В51, DRB1 01, 01. наличие антигенов В13 свидетельствует о предрасположенности ребенка к нейробластоме.
2. Больная И, 2002 г.р., история болезни №3444/ю, поступила в отделение детской онкологии 25.02.09 с диагнозом: нефробластома слева, St I.II, кл. группа.2. 12.09.08 была проведена операция - нефрэктомия слева. Г.А. №8109-14 (пересмотр РНИОИ) - нефробластома, аденоматозный (железистый) вариант. Выполнено исследование главного комплекса гистосовместимости: HLA - фенотип (I и II класса): A3, А26; В51, В35, DRB1 13, 17, что свидетельствует о предрасположенности ребенка к нейробластома.
Технико-экономическая эффективность «Способ прогнозирования развития злокачественных солидных опухолей у детей и подростков» заключается в том, что при выявлении ассоциативной связи антигенов главного комплексам гистосовместимости с развитием злокачественных процессов в детском возрасте в дальнейшем может выполняться скрининговая программа раннего выявления патологии в общеврачебной сети и в патронажной системе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ЗАБРЮШИННЫХ ОПУХОЛЕЙ У ДЕТЕЙ И ПОДРОСТКОВ | 2009 |
|
RU2420239C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ У ДЕТЕЙ И ПОДРОСТКОВ | 2005 |
|
RU2300106C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ УЗЛОВЫХ ОБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ У ДЕТЕЙ И ПОДРОСТКОВ | 2004 |
|
RU2285923C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ГЕНЕРАЛИЗАЦИИ ПРОЦЕССА ПРИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЯХ КОСТЕЙ | 2010 |
|
RU2427323C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ГЕНЕРАЛИЗАЦИИ ПРОЦЕССА У ДЕТЕЙ И ПОДРОСТКОВ С КОСТНЫМИ САРКОМАМИ | 2004 |
|
RU2282195C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ГЕНЕТИЧЕСКОЙ ПРЕДРАСПОЛОЖЕННОСТИ К ТУБЕРКУЛЕЗУ ОРГАНОВ ДЫХАНИЯ У ДЕТЕЙ | 2009 |
|
RU2398230C1 |
| СПОСОБ И СИСТЕМЫ ДЛЯ ПРОГНОЗИРОВАНИЯ СПЕЦИФИЧЕСКИХ ДЛЯ HLA КЛАССА II ЭПИТОПОВ И ОХАРАКТЕРИЗАЦИИ CD4+ T-КЛЕТОК | 2019 |
|
RU2826261C2 |
| СПОСОБЫ EX VIVO ЭКСПАНСИИ ЕСТЕСТВЕННЫХ КЛЕТОК-КИЛЛЕРОВ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2814083C2 |
| УНИВЕРСАЛЬНЫЕ АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2809113C2 |
| БИОИНФОРМАТИКА | 2021 |
|
RU2836005C1 |
Изобретение относится к области лабораторной диагностики, а именно иммуногенетическим исследованиям в онкологии, и может быть использовано для прогнозирования развития нефробластомы у детей и подростков. Способ прогнозирования риска развития нефробластомы у детей и подростков включает определение ангигенов главного комплекса гистосовместимости и отличается тем, что определяют путем серологического типирования антигены главного комплекса гистосовместимости I и II класса HLA методом PCS-SSP, прогнозируют группы риска развития нефробластомы при наличии антигенов HLA A26 и антигенов DRBI 13. Перспективность данного способа заключается в его простоте и эффективности. 2 ил.
Способ прогнозирования риска развития нефробластомы у детей и подростков, включающий определение антигенов главного комплекса гистосовместимости, отличающийся тем, что определяют путем серологического типирования антигены главного комплекса гистосовместимости I и II класса HLA методом PCS-SSP, прогнозируют группы риска развития нефробластомы при наличии антигенов HLA A26 и антигенов DRBI 13.
| УСТРОЙСТВО ДЛЯ БОРЬБЫ С ОТЛОЖЕНИЯМИ ПАРАФИНА НА ТРУБЧАТЫХ ПОВЕРХНОСТЯХ | 1996 |
|
RU2110669C1 |
| EP 1889922 A1, 20.02.2008 | |||
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ У ДЕТЕЙ И ПОДРОСТКОВ | 2005 |
|
RU2300106C1 |
| US 20100092983 A1, 15.04.2010. | |||
Авторы
Даты
2014-02-27—Публикация
2011-06-17—Подача