Настоящее изобретение относится к применению определенных производных имидазохинолина и пиридина для лечения VEGF-зависимых заболеваний или для получения фармацевтических композиций для применения в лечении данных заболеваний, к способам применения определенных производных имидазохинолина и пиридина для лечения данных заболеваний у теплокровного животного, в частности человека, к фармацевтическим составам, содержащим определенные производные имидазохинолина и пиридина, для лечения данных заболеваний и к определенным производным имидазохинолина и пиридина для применения в лечении данных заболеваний.
Было обнаружено, что определенные производные имидазохинолина и пиримидина, описанные в W02006/122806 и W007/084786, соответственно, как модулирующие биологическую активность РI3-киназ, способны блокировать биологические эффекты, связанные с активацией VEGF-рецепторов, при помощи родственных лигандов. Таким образом, эти соединения пригодны для лечения VEGF-стимулируемых ангиогенных заболеваний.
Синдромы, для которых установлена или предполагается молекулярная связь с осью VEGFR/VEGF, описаны, например, в «P.Carmeliet and RK Jain; Angiogenesis in cancer and other diseases, Nature 2000; 407: 249-257», а также в «SM Weiss and DA Cheresh; Pathophysiological consequences ofVEGF-induced vascular permeability. Nature 2005, 437:4697-50», которые полностью, включая все упомянутые в них ссылки, включены в настоящую заявку посредством ссылки, и представляют собой следующие:
- ревматоидный артрит
- синовит
- деструкцию костей и хрящей
- остеомиелит
- разрастание паннуса
- образование остеофитов
- гепатит
- пневмонию
- гломерулонефрит
- астму
- носовые полипы
- состояния после трансплантации
- образования в печени
- ретинопатию недоношенных
- возрастную макулярную дегенерацию
- диабетическую ретинопатию
- хроидальные и другие внутриглазные заболеваний
- лейкомаляцию
- тироидит
- гипертрофию щитовидной железы
- лимфопролиферативные заболевания
- саркому Капоши
- гематологические злокачественные новообразования (например, гемангиому)
- ожирение
- повреждения спинного мозга
- острый инфаркт миокарда
- отеки легких, мозга и сетчатки глаза
или любую другую их комбинацию.
Современная антиангиогенная терапия нацелена или на связывание лигандов (посредством конкуренции с антагонистом или фиксации эндогенного лиганда или экспрессией растворимой формы рецептора) с родственными рецепторами, экспрессированными на поверхности клеток эндотелия, образующих кровеносные сосуды (например, связывание VEGF с VEGFR1, 2 или 3); или на подавление путем активации рецепторов при помощи ингибиторов с малой молекулярной массой, блокирующих киназную активность рецептора(-ов) тирозинкиназы (например, блокада активации VEGFR1, 2 или 3). Ранее были описаны другие стратегии, нацеленные на активирование эндогенного и природного ингибитора VEGF-индуцированного пути, в клетках эндотелия, или на атаку уже существующей сосудистой системы VEGF-токсиновым конъюгатом. Ингибиторы PI3K проявляют свои антиангиогенные свойства при блокировании распространения VEGF-индуцированного сигнала, будучи связанными с VEGFR1, 2 или 3, Путь PI3K/Akt является важным нижележащим эффектором VEGFR, поскольку он требуется для выживания и пролиферации эндотелиальных клеток in vitro и in vivo (HP Gerber et al.. Vascular Endothelial Growth Factor Regulates Endothelial Cell Survival through the Phosphatidylinositol 3'-kinase/Akt Signal Transduction Pathway, J Biol Chem 1998; 273(46); 30336-30343; Y Fujio Y and К Wash, Akt Mediates Cytoprotection of Endothelial Cells by Vascular Endothelial Growth Factor in an Anchorage-dependent Manner. J Biol Chem 1999; 274(23):16349- 16354; LE Benjamin and E Keshet E. Conditional switching of vascular endothelial growth factor (VEGF) expression in tumors: Induction of endothelial cell shedding and regression ofhemangioblastoma-like vessels by VEGF withdrawal. PNAS 1997; 94(16):8761-8766; TL Phung et al. Pathological angiogenesis is induced by sustained АКТ signaling and inhibited by rapamycin. Cancer Cell 2006; 10(2); 159-170). Показано, что ингибиторы PI3K аннулируют VEGF-индуцированную пролиферацию и выживаемость («V Dayanir et al., Identification of Tyrosine Residues in Vascular Endothelial Growth Factor Receptor-2/FLK-l Involved in Activation ofPhosphatidylinositol 3-Kinase and Cell Proliferation. J Biol Chem 2001: 276(21): 17686-17692 »), поскольку считается, что путь перехвата PI3K оказывает значительное влияние на разрегулированную функцию сосудов (АК Olsson et al., Nature Review Molecular Cellular Biology, 2006; vol 7,359-371).
Определенные производные имидазохинолина, подходящие для настоящего изобретения, их получение и содержащие их подходящие фармацевтические составы описаны в WО 2006/122806 и включают соединения формулы I:
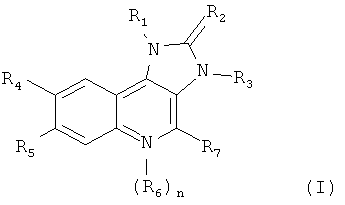 ,
,
в которой
R1 представляет собой нафтил или фенил, где упомянутый фенил замещен одним или двумя заместителями, независимо выбранными из группы, включающей галоген; (низш.)алкил, незамещенный или замещенный галогеном, цианогруппой, имидазолилом или триазолилом; циклоалкил; аминогруппу, замещенную одним или двумя заместителями, независимо выбранными из группы, включающей (низш.)алкил, (низш.)алкилсульфонил, (низш.)алкоксигруппу и (низш.)алкокси(низш.)алкиламиногруппу; пиперазинил, незамещенный или замещенный одним или двумя заместителями, независимо выбранными из группы, включающей (низш.)алкил и (низш.)алкилсульфонил; 2-оксопирролидинил; (низш.)алкокси(низш.)алкил; имидазолил; пиразолил; и триазолил;
R2 представляет собой О или S;
R3 представляет собой (низш.)алкил;
R4 представляет собой пиридил, незамещенный или замещенный галогеном, цианогруппой, (низш.)алкилом, (низш.)алкоксигруппой или пиперазинилом, незамещенным или замещенным (низш.)алкилом; пиримидинил, незамещенный или замещенный (низш.)алкоксигруппой; хинолинил, незамещенный или замещенный галогеном; хиноксалинил; или фенил, замещенный алкоксигруппой;
R5 представляет собой водород или галоген;
n равно 0 или 1;
R6 представляет собой оксидогруппу;
при условии, что если n=1, N-атом, содержащий радикал R6, имеет положительный заряд;
R7 представляет собой водород или аминогруппу;
или их таутомеры, фармацевтически приемлемые соли, гидраты или сольваты.
Радикалы и символы, используемые для определения соединения формулы I, имеют те же значения, что раскрыты в публикации WО 2006/122806, которая включена в настоящую заявку посредством ссылки.
Предпочтительными соединениями настоящего изобретения являются соединения, описанные в WО 2006/122806 и выбранные из группы, включающей;
2-метил-2-[4-(3-метил-2-оксо-8-пиридин-4-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-{4-[8-(5-метоксипиридин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}-2-метилпропионитрил;
2-{4-[8-(5-метоксипиридин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил] фенил}-2-метилпропионитрил;
2-метил-2-{4-[3-метил-2-оксо-8-(6-пиперазин-1-илпиридин-3-ил)-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}пропионитрил;
2-метил-2-(4-{3-метил-8-[2-(4-метилпиперазин-1-ил)пиридин-4-ил]-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил}фенил)пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо [4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-{4-[8-(2-фторхинолин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил] фенил}-2-метилпропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-хинолин-6-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-хинолин-5-ил-2,3-дигидроимидазо [4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-8-хиноксалин-6-ил-2,3-дигидроимидазо[4,5-с]хинолин-1 -ил)фенил]пропионитрил;
2-этил-2-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо [4,5-с]хинолин-1-ил)фенил]бутиронитрил;
2-этил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо [4,5-с]хинолин-1-ил)фенил]бутиронитрил;
1-[3-фтор-4-(2-оксопирролидин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-фтор-4-(2-оксопирролидин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(2-оксопирролидин-1-ил)фенил]-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(2-оксопирролидин-1-ил)фенил]-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-{4-[бис(2-метоксиэтил)амино]-3-фторфенил}-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-{4-[бис(2-метоксиэтил)амино]-3-фторфенил}-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-{4-[бис(2-метоксиэтил)амино]фенил}-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-{4-[бис(2-метоксиэтил)амино]фенил}-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-нафталин-2-ил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-нафталин-2-ил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-хлорфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-(2-хлорфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-о-толил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-о-толил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-этилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-(2-этилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(2-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(2-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-фтор-2-метилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-фтор-2-метилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(2-хлор-4-фторфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-(2-хлор-4-фторфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-(3-хлорфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-(3-хлорфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(3-трифторметилфенил)-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-метоксиметилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-метоксиметилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(2-метоксиэтил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(2-метоксиэтил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(2-метоксиэтил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(2-метоксиэтил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
2-метил-2-[4-(3-метил-2-оксо-5-окси-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-метил-2-[4-(3-метил-2-оксо-5-окси-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-[4-(7-фтор-3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил;
2-[4-(7-фтор-3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил;
N-мeтил-N-[4-(3-мeтил-2-oкco-8-пиpидин-3-ил-2,3-дигидpoимидaзo[4,5-с]хинолин-1-ил)фенил]метансульфонамид;
трет-бутиловый эфир метил[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]карбаминовой кислоты;
метил[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]амид этансульфоновой кислоты;
метил[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]амид этансульфоновой кислоты;
N-этил-N-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]метансульфонамид;
N-этил-N-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]метансульфонамид;
2-[4-(3-этил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил;
1-[3-фтор-4-(4-метансульфонилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-фтор-4-(4-метансульфонилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-фтор-4-пиперазин-1-илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-фтор-4-пиперазин-1-илфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(4-метилпиперазин-1 -ил)фенил]-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(4-метилпиперазин-1-ил)фенил]-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[2-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1 -[2-хлор-4-(4-метилпиперазин-1 -ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-2-метилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-2-метилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиразол-1-илфенил)-8-хинолин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
3-метил-1-(4-пиразол-1-илфенил)-8-пиридин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(4-[1,2,4]триазол-1-илфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(4-[1,2,4]триазол-1-илфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-[4-(4-метилпиперазин-1-ил)-3-трифторметилфенил]-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3 -метил-1-[4-(4-метилпиперазин-1-ил)-3-трифторметилфенил]-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1 -илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-[4-(4-метилпиперазин-1-ил)-3-трифторметилфенил]-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-[4-(4-метилпиперазин-1-ил)-3-трифторметилфенил]- 1,3-дигидроимидазо [4,5 -с]хинолин-2-он;
1-[2-хлор-4-(4-метилпиперазин-1-ил)фенил]-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-[2-хлор-4-(4-метилпиперазин-1-ил)фенил]-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-хиноксалин-6-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиперазин-1 -ил-3 -трифторметилфенил)-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-8-пиридин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-8-хиноксалин-6-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(цис-3,5-диметилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-[3-хлор-4-(цис-3,5-диметилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-этилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-этилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-изопропилпиперазин-1-ил)фенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-изопропилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-изопропилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-изопропилпиперазин-1-ил)фенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(4-этилпиперазин-1-ил)-3-трифторметилфенил]-3-метил-8-пиридин-З3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(4-этилпиперазин-1-ил)-3-трифторметилфенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(4-этилпиперазин-1-ил)-3-трифторметилфенил]-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-[4-(4-этилпиперазин-1-ил)-3-трифторметилфенил]-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо [4,5-с] хинолин-2-он;
3-метил-8-(6-пиперазин-1-илпиридин-3-ил)-1-(3-трифторметилфенил)-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(3-трифторметилфенил)-1,3-дигидроимидазо [4,5-с]хинолин-2-он;
1-(3-хлор-4-имидазол-1-илфенид)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-имидазол-1-илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
2-метил-2-[4-(3-метил-8-хинолин-3-ил-2-тиоксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил;
2-метил-2-{4-[3-метил-8-(2-метилпиридин-4-ил)-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}пропионитрил;
5-{1-[4-(цианодиметилметил)фенил]-3-метил-2-оксо-2,3-дигидро-1Я-имидазо[4,5-с]хинолин-8-ил}пиридин-2-карбонитрил;
2-[4-(4-амино-3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]-2-метилпропионитрил;
1-[4-(3-метил-2-оксо-8-пиридин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]циклопропанкарбонитрил;
1-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]циклопропанкарбонитрил;
1-{4-[8-(6-метоксипиридин-3-ил)-3-метил-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]фенил}циклопропанкарбонитрил;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(4-метилпиперазин-1-ил)фенил]-3-метил-8-хиноксалин-6-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-8-(2-метоксипиримидин-5-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-пиперазин-1-ил)фенил]-3-метил-8-пиримидин-6-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-ил)фенил)-8-(2-метоксипиримидин-5-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-пиримидин-5-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-пиперазин-1-илфенил)-3-метил-8-(2-метилпиридин-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(цис-3,5-диметилпиперазин-1-ил)фенил]-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[3-хлор-4-(цис-3,5-диметилпиперазин-1-ил)фенил]-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(цис-3,5-диметилпиперазин-1-ил)-3-трифторметилфенил]-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-[4-(цис-3,5-диметилпиперазин-1-ил)-3-трифторметилфенил]-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(2-метоксипиримидин-5-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-8-пиримидин-5-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
5-[3-метил-2-оксо-1-(4-пиперазин-1-ил-3-трифторметилфенил)-2,3-дигидро-1H-имидазо[4,5-с]хинолин-8-ил]пиридин-2-карбонитрил;
3-метил-8-(2-метилпиридин-4-ил)-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(3,4-диметоксифенил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
5-[3-метил-2-оксо-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-2,3-дигидро-1H-имидазо[4,5-с]хинолин-8-ил]пиридин-2-карбонитрил;
8-(6-фторпиридин-3-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(2,6-диметоксипиридин-3-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиримидин-5-ил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(2-метоксипиримидин-5-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(2,4-диметоксипиримидин-5-ил)-3-метил-1-(4-[1,2,4]триазол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
8-(5-метоксипиридин-3-ил)-3-метил-1-(4-пиразол-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-[1,2,4]триазол-1-илфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(3-хлор-4-[1,2,4]триазол-1-илфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-3-трифторметилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-3-трифторметилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-3-трифторметилфенил)-8-(6-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-ил-3-трифторметилфенил)-8-(5-метоксипиридин-3-ил)-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-пиридин-3-ил-1-(4-[1,2,4]триазол-1-илметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
3-метил-8-хинолин-3-ил-1-(4-[1,2,4]триазол-1-илметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
1-(4-имидазол-1-илметилфенил)-3-метил-8-пиридин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он и
1-(4-имидазол-1-илметилфенил)-3-метил-8-хинолин-3-ил-1,3-дигидроимидазо[4,5-с]хинолин-2-он;
или их таутомеры, фармацевтически приемлемые соли, гидраты или сольваты.
Особенно предпочтительным соединением настоящего изобретения является 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрил. Синтез 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрила описан в примере 1 заявки WО 2006/122806 (соединение А).
Другим предпочтительным соединением настоящего изобретения является 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-он. Синтез 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-рна описан в примере 86 заявки WО 2006/122806 (соединение Б).
Определенные производные пиримидина, подходящие для настоящего изобретения, их получение и содержащие их подходящие фармацевтические составы описаны в WО 07/084786 и включают соединения формулы II
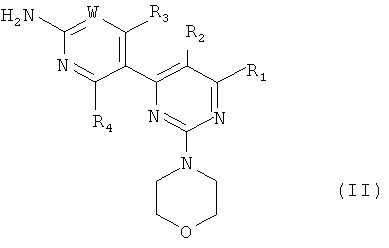 ,
,
или их стереоизомеры, таутомеры или фармацевтически приемлемые соли, где W представляет собой С, Rw или N, где Rw выбран из группы, включающей:
(1) водород,
(2) цианогруппу,
(3) галоген,
(4) метил,
(5) трифторметил,
(6) сульфонамидогруппу;
R1 выбран из группы, включающей:
(1) водород,
(2) цианогруппу,
(3) нитрогруппу,
(4) галоген,
(5) замещенный или незамещенный алкил,
(6) замещенный или незамещенный алкенил,
(7) замещенный или незамещенный алкинил,
(8) замещенный или незамещенный арил,
(9) замещенный или незамещенный гетероарил,
(10) замещенный или незамещенный гетероциклил,
(11) замещенный или незамещенный циклоалкил,
(12) -COR1a,
(13) -CO2R1a,
(14) -CONR1aR1b,
(15) -NR1aR1b,
(16) -NR1aCOR1b,
(17) -NR1aSO2R1b,
(18) -OCOR1a,
(19) -OR1a,
(20) -SR1a,
(21) -SOR1a,
(22) -SO2R1aH
(23) -SO2NR1aR1b
где R1a и R1b независимо выбраны из группы, включающей:
(а) водород,
(б) замещенный или незамещенный алкил,
(в) замещенный или незамещенный арил,
(г) замещенный или незамещенный гетероарил,
(д) замещенный или незамещенный гетероциклил и (е) замещенный или незамещенный циклоалкил,
R2 выбран из группы, включающей:
(1) водород,
(2) цианогруппу,
(3) нитрогруппу,
(4) галоген,
(5) гидроксигруппу,
(6) аминогруппу,
(7) замещенный или незамещенный алкил,
(8) -СОR2а и
(9) -NR2aCOR2b,
где R2a и R2b независимо выбраны из группы, включающей:
(а) водород и
(б) замещенный или незамещенный алкил;
R3 выбран из группы, включающей;
(1) водород,
(2) цианогруппу,
(3) нитрогруппу,
(4) галоген,
(5) замещенный или незамещенный алкил,
(6) замещенный или незамещенный алкенил,
(7) замещенный или незамещенный алкинил,
(8) замещенный или незамещенный арил,
(9) замещенный или незамещенный гетероарил,
(10) замещенный или незамещенный гетероциклил,
(11) замещенный или незамещенный циклоалкил,
(12) -СОR3а.
(13) -NR3aR3b,
(14) -NR3aCOR3b.
(15) -NR3aSO2R3b,
(16) -ОR3а,
(17) -SR3a,
(18) -SOR3a,
(19) -SO2R3а и
(20) -SO2NR3aR3b,
где R3а и R3b независимо выбраны из группы, включающей:
(а) водород,
(б) замещенный или незамещенный алкил,
(в) замещенный или незамещенный арил,
(г) замещенный или незамещенный гетероарил,
(д) замещенный или незамещенный гетероциклил и (е) замещенный или незамещенный циклоалкил и R4 выбран из группы, включающей:
(1) водород и
(2) галоген.
Радикалы и символы, используемые для описания соединения формулы II, имеют те же значения, что и раскрытые в публикации W007/084786, которая включена в настоящую заявку посредством ссылки.
Предпочтительными соединениями настоящего изобретения являются соединения, специально описанные в WО 07/084786. Особенно предпочтительным соединением настоящего изобретения является 5-(2,6-диморфолин-4-ил-пиримидин-4-ил)-4-трифторметилпиридин-2-иламин (соединение В). Синтез 5-(2,6-диморфолин-4-ил-пиримидин-4-ил)-4-трифторметилпиридин-2-иламина описан в примере 10 заявки WО 07/084786.
В соответствии с настоящим изобретением лечение:
- ревматоидного артрита
- синовита
- деструкции костей и хрящей
- остеомелита
- разрастания паннуса
- образования остеофитов
- гепатита
- пневмонии
- гломерулонефрита
- астмы
- носовых полипов
- состояний после трансплантации
- образований в печени
- ретинопатии недоношенных
- возрастной макулярной дегенерации
- диабетической ретинопатии
- хориодальных и других глазных заболеваний
- лейкомаляции
- тироидита
- гипертрофии щитовидной железы
- лимфопролиферативных заболеваний
- саркомы Капоши
- гематологических злокачественных новообразований (например, гемангиомы)
- ожирения
- повреждения спинного мозга
- острого инфаркта миокарда
- отеков легких, мозга и сетчатки глаза
или любой другой их комбинации, соединениями формулы I и II является наиболее предпочтительным.
В частности, настоящее изобретение относится к способу лечения VEGF-стимулированного ангиогенного заболевания, включающему введение нуждающемуся в этом теплокровному животному терапевтически эффективного количества определенного производного имидазохинолина формулы I, особенно предпочтительно 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрила (соединение А) или 8-(6-метоксипиридин-3 -ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она (соединение Б), или определенного производного пиридина формулы II, особенно предпочтительно 5-(2,6-диморфолин-4-ил-пиримидин-4-ил)-4-трифторметилпиридин-2-иламина (соединение В).
Кроме того, настоящее изобретение относится к применению определенного производного имидазохинолина формулы I, особенно предпочтительно 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрила (соединение А) или 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она (соединение Б), или определенного производного пиридина формулы II, особенно предпочтительно 5-(2,6-диморфолин-4-ил-пиримидин-4-ил)-4-трифторметилпиридин-2-иламина (соединение В), для получения фармацевтического состава для лечения VEGF-стимулированного ангиогенного заболевания или новообразования, или заболевания, резистентного к агентам, направленным на представителей семейства VEGF и/или VEGFR.
Резистентность к лечению модуляторами VEGF и/или VEGFR может приобретаться по различным механизмам при воздействии указанным VEGF-и/или VEGFR-модулятором.
В частности, настоящее изобретение относится к лечению заболевания или новообразования, зависящего от VEGF или обладающего резистентностью при лечении модулятором оси VEGF/VEGFR, соединением формулы I, особенно предпочтительно 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрилом (соединение А) или 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-оном (соединение Б), или формулы II, особенно предпочтительно 5-(2,6-диморфолин-4-ил-пиримидин-4-ил)-4-трифторметилпиридин-2-иламином (соединение В) или их фармацевтически приемлемыми солями. Возможными агентами, направленными на ось VEGF/VEGFR, являются, например, бевацизумаб, ранибизумаб, AVE0005, HuMV833, 2C3, СВО-Р11, сутент, сорафениб, ваталаниб, зактима, мидостаурин, ангиозим,, AG-013736, лестаутиниб, СР-547,632, СЕР-7055, KRN633, NVP-АЕЕ788, IMC-1211, ZK260253, семаксаниб, Е-7107, AS-3, Cand5 и РТС-299.
Соединение формулы (I) или (II) также может быть использовано для лечения VEGF-стимулированных ангиогенных заболеваний в комбинации с другими активными соединениями, например, в комбинации со вспомогательными агентами, как описано в W02006/122806 и W007/084786, более предпочтительно с агентами, направленными на VEGF или VEGFR, такими как, но без ограничения, анти-VEGF бевацизумаб, анти-VEGF ранибизумаб, AVE0005, анти-VEGF HuMV833, анти-VEGF 2СЗ, СВО-Р11, сутент, сорафениб, ваталаниб, зактима, мидостаурин, ангиозим, AG-013736, лестаутиниб, СР-547,632, СЕР-7055, KRN633, NVP-AEE788, IMC-1211, ZK260253, семаксаниб, Е-7107, AS-3, Cand5 и РТС-299; и ингибиторами HSP90 CNF1010, CNF2024, танеспимицином, алвеспимицином, IPI504, SNX5422 и NVP-AUY922.
Термин «комбинация» в рамках настоящего изобретения означает либо фиксированную комбинацию в одной дозированной лекарственной форме, либо набор частей для совместного введения, в котором соединение формулы (I) и партнер комбинации могут быть введены независимо в одно и тоже время или отдельно в течение периода времени, за который партнеры комбинации проявят совместный, например, синергетический эффект.
Соединение формулы (I) может быть введено само по себе или в комбинации с одним или несколькими другими терапевтическими соединениями. Возможная комбинационная терапия принимает вид фиксированных комбинаций, или введения соединения по настоящему изобретению и одного или более иного терапевтического соединения, поочередно или независимо одно от другого, или же совместное введение фиксированных комбинаций и одного или более других терапевтических соединений.
Дозировка активного ингредиента зависит от различных факторов, включающих, вид, возраст, массу, пол и медицинское состояние пациента, тяжесть заболевания, тип введения, функционирование почек и печени человека и конкретного используемого соединения. Терапевт, клиницист или ветеринар среднего уровня легко сможет определить и назначить эффективное количество лекарственного средства, которое требуется для предотвращения, противодействия или остановки развития состояния. Оптимальная точность в подборе концентрации лекарственного средства в диапазоне, обеспечивающем эффективность, требует режима, основанного на кинетике доступности лекарственного средства к целевым участкам, что включает рассмотрение распределения, установления равновесной концентрации и выведения лекарственного средства.
Соединения настоящего изобретения могут быть введены любым традиционным способом, в частности, парентерально, например, в виде растворов или суспензий для инъекций, энтерально, например, перорально, в виде таблеток или капсул, топически, например, в форме лосьонов, гелей, мазей или кремов, или в виде назальной или суппозитарной формы. Топическое нанесение, например, осуществляется на кожу. Другой формой топического введения является нанесение на глаза. Фармацевтические композиции, содержащие соединение настоящего изобретения вместе с, по меньшей мере, одним фармацевтически приемлемым носителем или разбавителем, могут быть получены обычным путем посредством смешивания с фармацевтически приемлемым носителем или разбавителем.
Фармацевтические композиции содержат эффективное количество для лечения одного из вышеуказанных расстройств, соединения формулы I или его N-оксида или таутомера, вместе с фармацевтически приемлемыми носителями, пригодными для топического, энтерального, например, перорального или ректального, или парэнтерального введения, и которые могут быть органическими или неорганическими, твердыми или жидкими. Существуют фармацевтические композиции, используемые для перорального введения, в особенности, таблетки или желатиновые капсулы, которые содержат активный ингредиент вместе с разбавителями, например, лактозой, декстрозой, маннитом и/или глицерином, и/или смазочные вещества и/или полиэтиленгликоль. Таблетки могут также содержать связующие вещества, например, алюмосиликат магния, крахмалы, такие как пшеничный, кукурузный или рисовый крахмал, желатин, метилцеллюлозу, натрий карбоксиметилцеллюлозу и/или поливинилпирролидон, и, при желании, вещества-разрыхлители, например, крахмалы, агар, альгиновую кислоту или ее соли, такие как альгинат натрия, и/или выделяющие газ смеси, или адсорбенты, красители, подсластители и ароматизаторы. Также возможно использовать фармакологически активные соединения настоящего изобретения в форме парэнтерально вводимых композиций или же в форме инфузионных растворов. Фармацевтические композиции могут быть стерилизованы и/или могут содержать эксципиенты, например, консерванты, стабилизаторы, увлажнители и/или эмульгаторы, растворители, соли для регулирования осмотического давления и/или буферы. Фармацевтические композиции настоящего изобретения, которые, при желании, могут содержать другие фармакологически активные вещества, получают известным образом, например, при помощи простого смешивания, гранулирования, получения лекарственных средств со сладким наполнителем, растворения или процессов лиофилизации, и содержат примерно от 1% до 99%, особенно предпочтительно от примерно 1% до примерно 20% активного ингредиента(-ов).
Краткое описание фигур
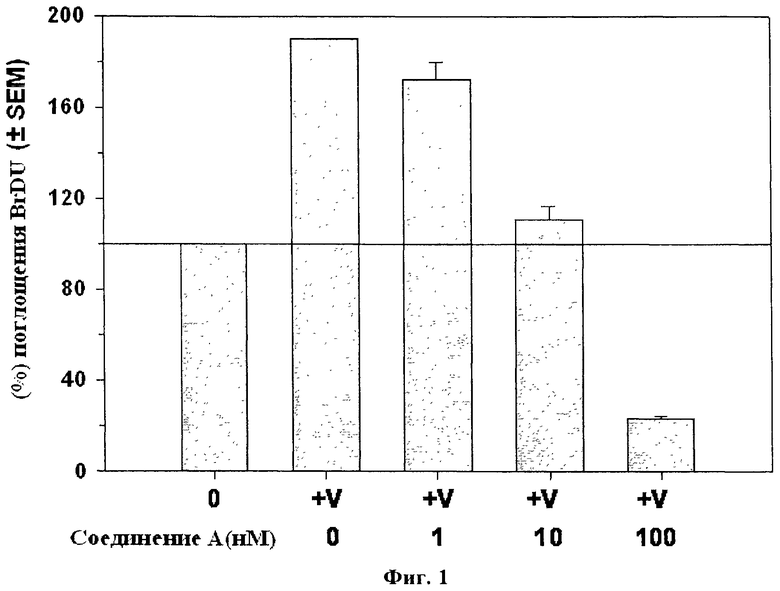
На фиг.1 показано влияние соединения А на VEGF-индуцированную пролиферацию. Клетки HUVEC высеивают, выдерживают в малосывороточной среде, содержащей (V) или не содержащей (0) VEGF и BrDU, и инкубируют с увеличением концентраций соединения А в течение 24 ч. Пролиферацию эндотелиальных клеток измеряют по количественному содержанию введенного BrDU. Проводят четыре независимых эксперимента с n=3 ячейки на группу*, р=<0,05 (ANOVA-Dunnett's) над базовой линией, обработанные VEGF образцы сравнения (представлены горизонтальной линией).
Рентгеновская дифрактограмма.
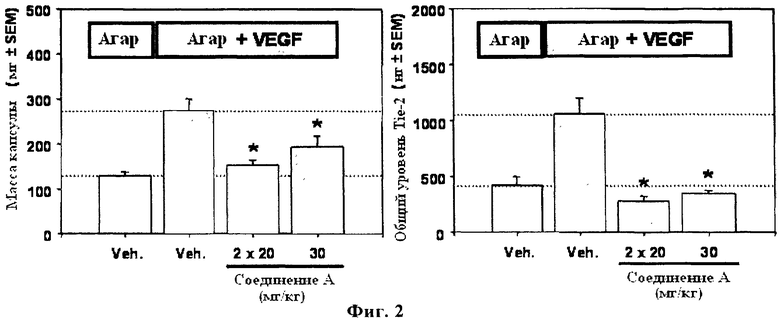
На фиг.2 показано влияние соединения А на VEGF-индуцированную неоваскуляризацию in vivo. Мышам FVB, с имплантированной тефлоновой агаровой камерой только с агаром (агар) или с VEGF 165 (агар+VEGF) в концентрации 2 мг/мл, вводят перорально соединение А или плацебо (Veh, все ячейки) в течение 4 дней при указанных дозировках и режиме. Животных умерщвляют спустя 24 ч после последней дозы, для количественного определения VEGF-индуцированной неоваскуляризованной ткани (левая панель), и содержания Tie-2 no ELISA (правая панель). *, р=<0,05 (ANOVA-Dunnett's) по сравнению с обработанными VEGF образцами сравнения,
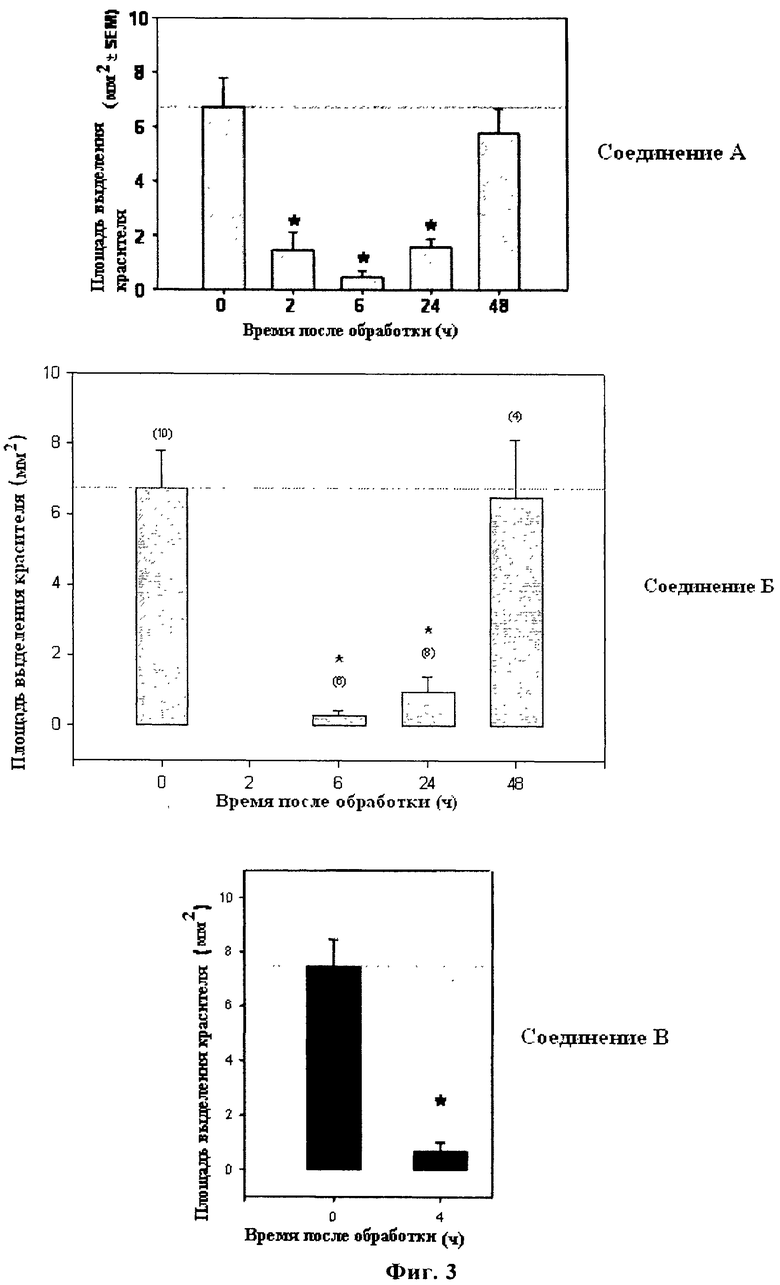
Фиг.3: Влияние соединения А, Б и В на VEGF-индуцированную проницаемость in vivo. Мышам FVB, которым предварительно, в указанное время, перорально ввели или соединение А (30 мг/кг), или соединение Б (7,5 мг/кг), или соединение В (50 мг/кг), внутривенно вводят синий Эванса и спустя 30 мин делают инъекцию VEGF в ухо. Затем мышей умерщвляют, и измеряют область выделения красителя. *, р=<0,05.
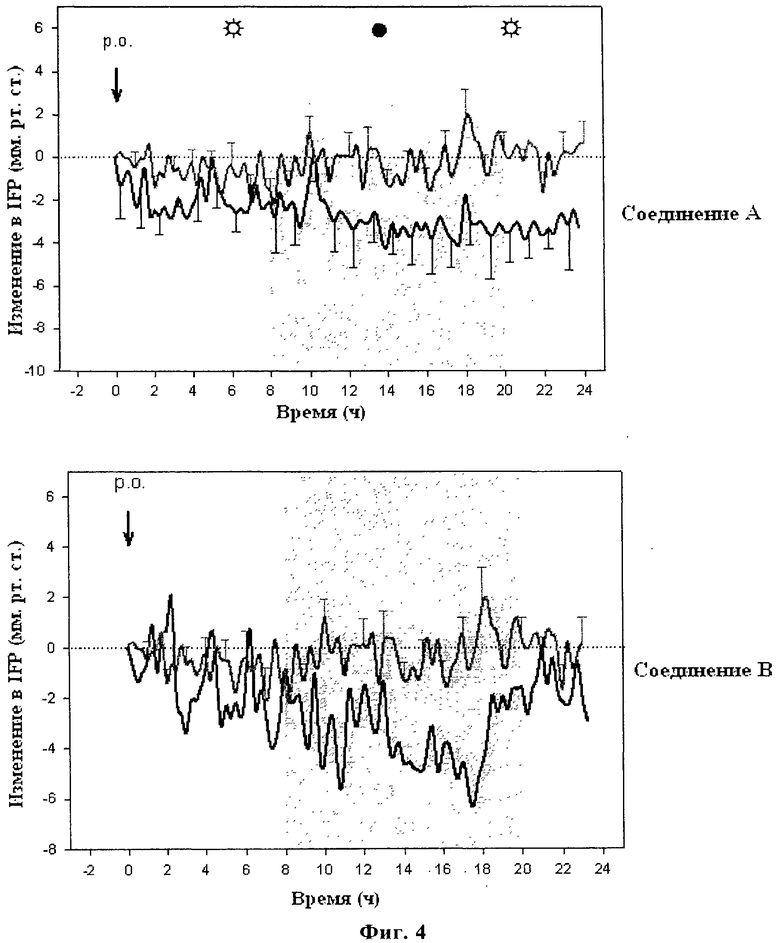
Фиг.4: Влияние соединения А и В на внутрижидкостное давление в опухоли. Крысам, с ортотопически трансплаттированной опухолью BN472, имеющим чувствительный к давлению катетер, вставленный в опухоль, единовременно перорально вводят соединение А (30 мг/кг - верхняя панель, темная линия), или соединение В (2,5 мг/кг, нижняя панель, темная линия), или же плацебо (обе панели - серая линия). IFP регистрируют в течение 24 ч и строят график отклонений (дельту) (верхняя панель, темные линии: необработанные животные; серая линия/обработка проведена, как указано над графиком).
Примеры
Эффективность соединений формулы (I) и (II) и их солей может быть продемонстрирована следующим образом:
Пример 1: анализ пролиферации HUVEC
Влияние на VEGF-индуцированную пролиферацию HUVEC исследуют с использованием набора для введения BrdU (Biotrak Cell Proliferation Elisa System V.2, Amersham, England). Субконфлюентный слой HUVEC высеивают при плотности 5х10 клеток на ячейку в 96-ячеечные планшеты, заполненные 1,5% желатином, и затем инкубируют при 37°С в присутствии 5% СО2 в питательной среде, содержащей 5% FBS (PromoCell, Switzerland). По истечении 24-х ч питательную среду заменяют базальной средой, содержащей 1,5% FBS. По истечении еще 24-х ч среду обновляют и добавляют соединение или контроль растворителем. В то же время добавляют человеческий фактор роста VEGFigs (10 нг/мл). По истечении 24-х ч инкубирования добавляют BrdU-меченный раствор и клетки инкубируют еще 24 ч перед фиксацией, блокадой и добавлением меченного пероксидазой антитела BrdU. Связывание антитела определяют с использованием субстрата 3,3'5,5'-тетраметилбензидина, который образует окрашенный продукт, количество которого измеряют на спектрофотометре при 450 нм.
Пример 2: анализ ангиогенеза камеры-импланта in vivo
Стерильные тканевые камеры, изготовленные из перфторалкокси-Teflon®, заполняют 500 мкл жидкого агара (0,8% масс./об.), содержащего 20 ед/мл гепарина (Novo Nordisk A/S, Bagsvaerd, Denmark), с или без фактора роста (VEGF165; 2 мкг/мл) и имплантируют в стерильных условиях в дорсальную поверхность самок мышей (FVB; Charles River Laboratories, les Oncins, France). Обработку начинают за 4-6 дней до имплантации камеры, а затем каждый день назначенными дозами в течение 3-х дней. После этого камеры из животных удаляют, а образовавшуюся васкуляризированную ткань удаляют и взвешивают. Образцы тканей гомогенизируют в буфере RlPA (50 мМ Tris-HCl, 121 мМ NaCl, 1 мМ ЭДТА, 6 мМ EGTA, 1% NP-40, 20 мМ NaF, 1 мМ Pefabloc SC, 1 мМ Na3V04), центрифугируют 1 ч при 7000 об/мин и надосадочную жидкость отфильтровывают с использованием 0,45 мкм шприцевого фильтра (Acrodisc® GF, Gelman Sciences, Ann Arbor, MI, USA). Для определения уровня Tie-2 96-ячеечные планшеты Nunc (Naperville, IL) Maxisorp заполняют захватывающим антителом - анти-Тiе-2 АВ33 (UBI, Hauppauge, NY), с концентрацией 2 мкг/мл (100 мкл/ячейку), и выдерживают в течение ночи при 4°С. Затем ячейки промывают TPBS (Tween 80 PBS) и блокируют инкубированием с 3% Top-Block (Juro, Lucerne, Switzerland) в течение 2-х ч при комнатной температуре. Добавляют 300 мг протеинового лизата и инкубируют еще 2 ч, а затем ячейки три раза промывают перед добавлением козьего антимышиного антитела Tie-2 (R&D Systems, Minneapolis, MN; 0,5 мкг/мл) и конъюгированного с щелочным фосфатом антикозьего антитела (Sigma, St. Louis, МО; разбавление 1:6,000) в TPBS+0,1%Top-Block в течение 1 ч при комнатной температуре. Комплексы антитела Tie-2 определяют по завершении инкубирования с использованием п-нитрофенилфосфатного субстрата (Sigma). Поглощающую способность спектро-фотометрической реакции определяют с использованием считывающего устройства ELISA при 405 нм. В качестве стандарта используют рекомбинантный человеческий внеклеточный домен Tie-2, скомбинированный с постоянными областями IgGI (sTie-2Fc) человека, растворенный в буферном растворе RIPA в концентрации от 0,1 до 300 нг/ячейка.
Пример 3: анализ VEGF-индуцированной проницаемости (анализ Майлса) 200 мкл синего Эванса (0,5%) вводят в хвостовую вену самкам мышей линии FVB. Тридцать минут спустя мышей анастезируют (3% изофлурана в О2, Forene, Abbott AG, Cham, Switzerland), а затем помещают на операционный стол, температуру которого поддерживают на уровне 39°С. Уши мышей растягивают на стальном конусе, снабженном двусторонним стикером, для выделения дорсальной поверхности. Затем при помощи микроскопа вводят под кожу гиподермальную иглу (30G) между первым и вторым нервно-сосудистым пучком уха и углубляют на 4-5 мм. После этого микролитровым шприцем (250 мкл, Hamilton, Bonaduz, Switzerland) вводят 2 мкл VEGF164 (10 нг/мл), с образованием субдермального пузыря. Краситель синий Эванса, связанный, с сывороточным альбумином, будет вытекать в областях повышенной капиллярной проницаемости, генерируя видимое голубое пятно, позволяющее измерить проницаемость сосудов. Область внутрикожного введения фотографируют 30 мин после инъекции у всех животных.
VEGF-опосредованную проницаемость сосудов определяют посредством измерения площади (мм2) красителя, вытекшего в область введения VEGF, с использованием вспомогательного программного обеспечения для анализа изображений (система визуализации KS-400 3.0, Zeiss, Germany).
Пример 4: Давление интерстициальной жидкости опухоли IFP опухолей BN472 измеряют у находящихся в сознании, свободно перемещающихся крыс, находящихся в своей клетке, при помощи адаптированной, целиком имплантируемой миниатюрной системы радиотелеметрии, включающей 4 основных компонента: имплантируемый передатчик (AM unit, модель TLM-PAC10, объем: 1,1 см, масса: 1,4 г), непрерывно считывающий и передающий информацию о животном, одно приемное устройство, расположенное под клеткой, матричный интерфейс для координирования сигналов и компьютерную систему получения данных для сбора, анализа и хранения данных. Передатчик имплантируют в стерильных условиях в бок животного при анестезии изофлуораном (3% изофлурана в О2). Животных в бессознательном состоянии помещают на нагретую поверхность и бреют им брюшную область. Вентральную поверхность брюшины получают, смазывая кожу хирургическим скрабом на основе повидон-йода. У лежащих на спине животных в середине брюшины делают разрез около 30 мм и кожу отделяют от пристеночной мускулатуры воздушного кармана. Затем в карман помещают стерильный передатчик, и измерительный катетер вводят подкожно в опухолевую область (самую нижнюю жировую прослойку молочной железы). Чувствительный к давлению катетер вводят в опухоль (на глубину 4-5 мм), и фиксируют в месте введения тканевым клеем Vetbond (фирмы 3М). Наличие жидкостной связи между наконечником чувствительного к давлению катетера и опухолью определяют по слабой пульсации подводящих трубок, соединяющих катетер с телеметрическим датчиком при помощи зажима. Имплантация катетера считается успешной, если показания до и после такого теста различаются не более чем на 1 мм рт.ст. Однако в большинстве имплантированных опухолей волнообразные кривые внутриопухолевых IFP-пульсаций давления могут быть легко зарегистрированы с высоким разрешением, что только сильнее подтверждает правильность расположения сенсорного катетера. Общее время операции по имплантированию телеметрического датчика составляет около 20 мин. Постоперационное обезболивание проводят с использованием двух подкожных инъекций по 0,05 мг/кг бупренорфина (Temgesic®, Reckitt and Colman), непосредственно после операции и спустя 8-12 ч. В ходе операции животное в бессознательном состоянии помещают на мягкий материал в чистой клетке с неограниченным количеством воды. Для поддержания температуры тела используют внешнюю нагревательную лампу. Животным дают 2 суток на восстановление после операции перед тем, как начать сбор каких-либо физиологических данных, IFP для всех животных записывают непрерывно в течение 24 часов до 10 дней, и анализируют 10-секундными циклами с перерывом в 1 мин и частотой дискретизации 500 Гц. Площади под кривой (ППК), записанные в течение 24 часов после обработки, рассчитывают с использованием метода трапеции.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИМИДАЗОХИНОЛИНЫ В КАЧЕСТВЕ ДВОЙНЫХ ИНГИБИТОРОВ ЛИПИДКИНАЗЫ И mTOR | 2008 |
|
RU2478387C2 |
| ПРИМЕНЕНИЕ ИМИДАЗОХИНОЛИНОВ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ЗАВИСИМЫХ ОТ EGFR, ИЛИ ЗАБОЛЕВАНИЙ С ПРИОБРЕТЕННОЙ РЕЗИСТЕНТНОСТЬЮ К АГЕНТАМ, КОТОРЫЕ СВЯЗЫВАЮТСЯ С ЧЛЕНАМИ СЕМЕЙСТВА EGFR | 2008 |
|
RU2481838C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМБИНАЦИИ, ВКЛЮЧАЮЩИЕ ПРОИЗВОДНЫЕ ПИРИДО [4,3-d]ПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРА HSP90 И ИНГИБИТОРА HER2 | 2009 |
|
RU2532375C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ SMOOTHENED ДЛЯ ЛЕЧЕНИЯ СВЯЗАННЫХ С ПУТЕМ HEDGEHOG НАРУШЕНИЙ | 2009 |
|
RU2519200C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ АКТИВНОСТИ КАННАБИНОИДНОГО РЕЦЕПТОРА 1 | 2005 |
|
RU2431635C2 |
| КОМБИНАЦИИ ИНГИБИТОРА HSP90 | 2009 |
|
RU2519673C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОИЗВОДНЫЕ БЕНЗОДИАЗЕПИНА И ИНГИБИТОР БЕЛКА СЛИЯНИЯ RSV | 2005 |
|
RU2388476C2 |
| ПРОИЗВОДНЫЕ 2,3-ДИГИДРО-6-НИТРОИМИДАЗО [2, 1-b] ОКСАЗОЛА | 2003 |
|
RU2326121C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, ПРИМЕНЕНИЕ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ И СПОСОБ ИНГИБИРОВАНИЯ АКТИВНОСТИ КАТЕПСИНА S | 2001 |
|
RU2317988C2 |
| ПРОИЗВОДНЫЕ ДИГИДРОБЕНЗОДИАЗЕПИН-2-ОНА ДЛЯ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ НАРУШЕНИЙ | 2003 |
|
RU2315764C2 |
Изобретение относится к области фармацевтики и медицины и касается применения 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-с]хинолин-1-ил)фенил]пропионитрила или 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она для получения фармацевтического состава для лечения VEGF-стимулированного ангиогенного заболевания, способа лечения VEGF-стимулированного ангиогенного заболевания и применения указанных соединений для лечения данных заболеваний с высокой эффективностью. 3 н. и 2 з.п. ф-лы, 4 ил., 4 пр.
1. Применение соединения, которое представляет собой 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-c]хинолин-1-ил)фенил]пропионитрил или 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-c]хинолин-2-он или их фармацевтически приемлемые соли для получения фармацевтического состава для лечения VEGF-стимулированного ангиогенного заболевания, выбранного из группы, состоящей из ревматоидного артрита, синовита, деструкции костей и хрящей, остеомиелита, разрастания паннуса, образования остеофитов, носовых полипов, образования в печени, ретинопатии недоношенных, возрастной макулярной дегенерации, диабетической ретинопатии, хориодальных и других внутриглазных заболеваний, лейкомаляции, тиреоидита, гипертрофии щитовидной железы, лимфопролиферативных заболеваний, саркомы Капоши, гемангиом, ожирения, повреждения спинного мозга, острого инфаркта миокарда, отека легких, мозга и сетчатки глаза, или любых их комбинаций.
2. Применение по п.1, где соединение представляет собой 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-c]хинолин-1-ил)фенил]пропионитрил или его фармацевтически приемлемую соль.
3. Применение по п.1, где соединение представляет собой 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-c]хинолин-2-он или его фармацевтически приемлемую соль.
4. Способ лечения VEGF-стимулированного ангиогенного заболевания, выбранного из группы, состоящей из ревматоидного артрита, синовита, деструкции костей и хрящей, остеомиелита, разрастания паннуса, образования остеофитов, носовых полипов, образования в печени, ретинопатии недоношенных, возрастной макулярной дегенерации, диабетической ретинопатии, хориодальных и других внутриглазных заболеваний, лейкомаляции, тиреоидита, гипертрофии щитовидной железы, лимфопролиферативных заболеваний, саркомы Капоши, гемангиом, ожирения, повреждения спинного мозга, острого инфаркта миокарда, отека легких, мозга и сетчатки глаза, или любых их комбинаций, включающий введение терапевтически эффективного количества соединения 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-c]хинолин-1-ил)фенил]пропионитрила или 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-c]хинолин-2-она по п.1 или их фармацевтически приемлемых солей нуждающемуся в этом теплокровному животному.
5. Применение соединения 2-метил-2-[4-(3-метил-2-оксо-8-хинолин-3-ил-2,3-дигидроимидазо[4,5-c]хинолин-1-ил)фенил]пропионитрила или 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-пиперазин-1-ил-3-трифторметилфенил)-1,3-дигидроимидазо[4,5-c]хинолин-2-она по п.1 или их фармацевтически приемлемой соли для лечения VEGF-стимулированного ангиогенного заболевания, выбранного из группы, состоящей из ревматоидного артрита, синовита, деструкции костей и хрящей, остеомиелита, разрастания паннуса, образования остеофитов, носовых полипов, образования в печени, ретинопатии недоношенных, возрастной макулярной дегенерации, диабетической ретинопатии, хориодальных и других внутриглазных заболеваний, лейкомаляции, тиреоидита, гипертрофии щитовидной железы, лимфопролиферативных заболеваний, саркомы Капоши, гемангиом, ожирения, повреждения спинного мозга, острого инфаркта миокарда, отека легких, мозга и сетчатки глаза, или любых их комбинаций.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| ПРОИЗВОДНЫЕ 2-АМИНОНИКОТИНАМИДА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ VEGF-РЕЦЕПТОРА ТИРОЗИНКИНАЗЫ | 2001 |
|
RU2296124C2 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНА В КАЧЕСТВЕ ИНГИБИТОРОВ АНГИОГЕНЕЗА | 2000 |
|
RU2262935C2 |
Авторы
Даты
2014-03-20—Публикация
2009-03-24—Подача