Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения фенил-замещенного гетероциклического производного используя новый способ сочетания между фенильным производным и гетероциклическим производным, при использовании катализатора переходного металла. Более подробно, настоящее изобретение относится к превосходному способу получения фенил-замещенного гетероциклического производного или его промежуточного соединения, которое применяют в качестве ингибитора ксантин оксидазы, используемого в качестве терапевтического агента для подагры, гиперурикемии и тому подобного.
Уровень техники
Причиной подагры является гиперурикемия, и после ремиссии приступа подагры проводят лечение лекарствами, чтобы облегчить гиперурикемию. Терапевтические агенты для гиперурикемии ориентировочно разделяют на средство, способствующее выведению мочевой кислоты и ингибитор синтеза мочевой кислоты (ингибитор ксантин оксидазы), и выбирают, соответственно, в зависимости от состояния и степени состояния.
Ингибиторы ксантин оксидазы (XOD) включают производные 2-фенилтиазола (PTLs с 1 по 6, NPL 1), производные 3-фенилизотиазола (PTLs 7 и 8), производные фенилпиразола (PTL с 9 по 11), производные 2-фенилоксазола (PTL 12) и фенил-гетероарильные производные (PTL 13). Способы получения, описанные в патентной литературе, приведенные в PTLs с 1 по 12, представляют собой способы, где гетероциклические кольца образованы способами получения, включающими ряд последовательных реакций и таким образом, включают большое количество стадий. Способ получения, описанный в PLT 13, представляет собой способ, где структура образована прямым сочетанием фенильного кольца с гетероциклическим кольцом и таким образом, включает небольшое количество стадий. Однако в данном способе необходимо приготовить соединения бора и, следовательно, это приводит к более высокой стоимости. Таким образом, указанный способ не является удовлетворительным с точки зрения способа получения с низкой стоимостью, включающего небольшое количество стадий.
В качестве способа, чтобы связать C-H связь на гетероциклическом кольце 2 непосредственно с фенильным кольцом без использования соединений бора, были описаны реакции сочетания при использовании, в качестве катализатора палладия (NPLs 2 до 10), родия (NPL 11), иридия (NPL 12), меди (NPL 13), никеля (NPL 14 и 15), кобальта (NPL 16), палладия-меди (NPL 17 to 19), и палладия-серебра (NPL 20). Среди них, способ получения, использующий никелевый катализатор отнесен к способу синтеза фенил-замещенного гетероциклического производного, который является ингибитором ксантин оксидазы (NPL 9). Однако не было описано примера, где фенил-замещенное гетероциклическое производное настоящего изобретения было синтезировано, при использовании металлического катализатора иного, чем никелевый катализатор. Кроме того, ни одна из реакций не является удовлетворительной, с точки зрения, ограничения субстрата, стоимости и выхода.
Список ссылок
Патентная литература
[PTL 1] Международная публикация No. WO 92/09279
[PTL 2] Патент Японии, выложенная публикация No. H6-293746
[PTL 3] Патент Японии, выложенная публикация No. H6-329647
[PTL 4] Патент Японии, выложенная публикация No. H6-345724
[PTL 5] Патент Японии, выложенная публикация No. H10-139770
[PTL 6] Патент Японии, выложенная публикация No. H11-60552
[PTL 7] Патент Японии, выложенная публикация о. S57-85379
[PTL 8] Патент Японии, выложенная публикация No. H6-211815
[PTL 9] Патент Японии, выложенная публикация No. S59-95272
[PTL 10] Международная публикация No. WO 98/18765
[PTL 11] Патент Японии, выложенная публикация No. H10-310578
[PTL 12] Патент Японии, выложенная публикация No. H6-65210
[PTL 13] Международная публикация No. WO 2007/097403
Не патентная литература
[NPL 1] Heterocycles, 1998:47, 857
[NPL 2] J. Am. Chem. Soc., 2003:125, 1700
[NPL 3] J. Am. Chem. Soc., 2006:128, 16496
[NPL 4] Angew. Chem., Int. Ed. 2007:46, 7996
[NPL 5] J. Org. Chem., 2009:74, 1826
[NPL 6] Org. Lett, 2009:10(13), 2909
[NPL 7] Tetrahedron Letters, 2008:49(6), 1045
[NPL 8] Tetrahedron Letters, 2003:59(30), 5685
[NPL 9] Bull. Chem. Soc. Jpn, 1998:71, 467
[NPL 10] Chem. A. Eur. J., 2009:15(6), 1337
[NPL 11] J. Am. Chem. Soc., 2008:130, 14926
[NPL 12] Chem. Comm, 2004, 1926
[NPL 13] J. Am. Chem. Soc., 2007:129(41), 12404
[NPL 14] Org. Lett., 2009:11(8), 1733
[NPL 15] Org. Lett., 2009:11(8), 1737
[NPL 16] Org. Lett., 2003:5(20), 3607
[NPL 17] Tetrahedron, 2007:63(9), 1970
[NPL 18] Org. Lett., 2004:6(12), 2011
[NPL 19] J. Am. Chem. Soc., 2003:125, 1700
[NPL 20] Angew. Chem. Int. Ed., 2007:46, 7996
Раскрытие изобретения
Техническая задача
Задача настоящего изобретения заключается в том, чтобы предложить превосходный коротко-стадийный способ получения, который отличается от ранее известных способов получения, указанных выше, фенил-замещенного гетероциклического производного или его промежуточного соединения, производного являющегося ингибитором ксантин оксидазы, используемого в качестве терапевтического агента для подагры, гиперурикемии и тому подобное.
Решение задачи
Авторы настоящего изобретения провели кропотливую исследовательскую работу в отношении указанной выше задачи и, как результат, обнаружили, что фенильное кольцо фенильного производного и C-H связь на гетероциклическом производном могут быть связаны непосредственно, с высокой селективностью, при использовании соединения переходного металла.
То есть, настоящее изобретение относится к следующему:
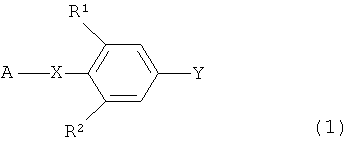
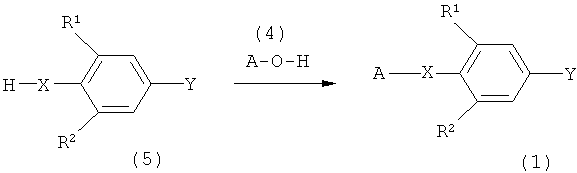
[1] Способу, включающему взаимодействие соединения, представленного следующей формулой (I):
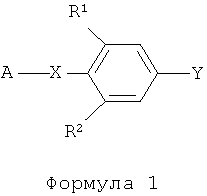
В формуле (1) R1 представляет собой атом водорода или атом галогена; R2 представляет собой атом водорода, цианогруппу, нитрогруппу, атом галогена, формильную группу или галогенметильную группу; А представляет собой атом водорода, C1 до C8 алкильную группу, C3 до C6 циклоалкильную группу, фенильную группу, атом фтора (только когда Х представляет связь) или защитную группу для гидроксильной группы (только когда Х представляет атом кислорода), где А может быть замещено 1 до 3 заместителями, такой заместитель, представляющий группу, выбран из группы, состоящей из атома галогена, C1 до C4 алкильной группы, C1 до C4 алкоксигруппы, C1 до C4 алкилтиогруппы, C3 до C6 циклоалкильной группы, фенильной группы, феноксигруппы и пиридильной группы; Х представляет собой связь (только когда А представляет фенильную группу или атом фтора) или атом кислорода; и Y представляет собой уходящую группу
и соединения, представленного следующей формулой (2):
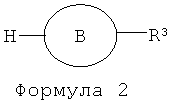
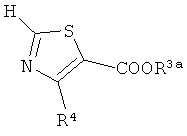
В формуле (2) H представляет собой атом водорода; и В представляет собой группу, выбранную из следующих формул:
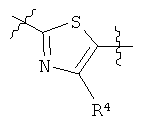 ,
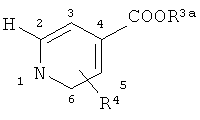
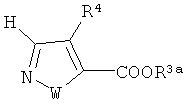
, 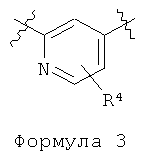 или
или 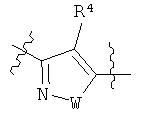
где R3 представляет собой COOR3a или COR3b; R3a представляет собой атом водорода, C1 до C4 алкильную труппу или защитную группу сложноэфирного типа для карбоксильной группы; R3b представляет собой защитную группу амидного типа для карбоксильной группы, защитную группу образующую амид с соседней карбонильной группой; R4 представляет собой атом водорода, атом галогена или C1 до C4 алкильную группу; и W представляет собой атом кислорода или атом серы)
в присутствии соединения переходного металла, для того чтобы получить фенил-замещенное гетероциклическое производное, представленное следующей формулой (3):
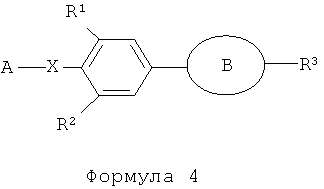
где в формуле (3), A, X, R1 и R2 являются такими, как определено в формуле (1); и B и R3 являются такими, как определено в формуле (2)).
[2] Способ получения по [1], где A представляет C1 до C5 алкильную группу.
[3] Способ получения по [1], где A представляет изобутильную группу.
[4] Способ получения по любому из с [1] по [3], где X представляет атом кислорода.
[5] Способ получения по любому из с [1] по [4], где R' представляет атом водорода.
[6] Способ получения по любому из с [1] по [5], где R2 представляет цианогруппу.
[7] Способ получения по любому из с [1] по [6], где Y представляет собой атом галогена, -OCO2-(C1 до C4 алкильную группу), -OCO2-(фенильную группу), -OSO2-(C1 до C4 алкильную группу), -OSO2-Сфенильную группу) или диазониевую группу, где в Y, C1 до C4 алкильная группа, может быть замещена от 1 до 3 атомами галогена и фенильная группа, может быть замещена от 1 до 3 атомами галогена или C1 до C4 алкильными группами.
[8] Способ получения по любому из с [1] по [7], где B представлен следующей группой:
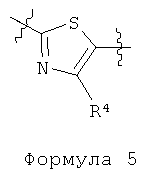
[9] Способ по любому из с [1] по [8], где R представляет метальную группу.
[10] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет нуль-валентную медь или соль одновалентной меди.
[11] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет нуль-валентный палладий или соль одно- или дивалентного палладия.
[12] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет нуль-валентный палладий или соль дивалентного палладия.
[13] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет нуль-валентный кобальт или соль дивалентного кобальта.
[14] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет иодид меди (I) (CuI).
[15] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет ацетат палладия (II) (Pd(OAc)2), пропионат палладия (II) (Pd(O(C=O)CH2CH3)2), 2-метилпропаноат палладия (II) (Pd(O(C=O)CH(CH3)2)2, пивалат палладия (Pd(OPiv)2), хлорид палладия (II) (PdCl2), бромид палладия (I) (Pd2Br2) или гидроксид палладия (II) (Pd(OH)2).
[16] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет ацетат палладия (II) (Pd(OAc)2), пропионат палладия (II) (Pd(O(C=O)CH2CH3)2), 2-метилпропаноат палладия (II) (Pd(O(C=O)CH(CH3)2)2 или пивалат палладия (Pd(OPiv)2).
[17] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет ацетат палладия (II) (Pd(OAc)2), хлорид палладия (II) (PdCl2) или гидроксид палладия (II) (Pd(OH)2).
[18] Способ получения по любому из с [1] по [9], где соединение переходного металла представляет ацетат кобальта (II) (Co(ОАс)2).
[19] Способ получения по любому из с [1] по [18], где лиганд, способный к координированию соединения переходного металла дополнительно присутствует в течение хода реакции.
[20] Способ получения по [19], где лиганд представляет трифенилфосфин, три(трет-бутил)фосфин, ди(трет-бутил)метилфосфин, трет-бутилдициклогексилфосфин, ди(трет-бутил)циклогексилфосфин, три(пиклогексил)фосфин, 2-дициклогексилфосфино-1,6'-диизопропокси-1,1'-бифенил, 2-дициклогексилфосфино-2',4',6'-триизопропил-1,1'-бифенил-2-дициклогексилфосфиноциклогексилфосфино-2',4',6'-триизопропил-1,1'-бифенил, фенантролин, 1,1'-бис(дифенилфосфино)ферроцен или его соли.
[21] Способ получения по [19], где лиганд представляет трифенилфосфин, три(трет-бутил)фосфин, ди(трет-бутил)метилфосфин, трет-бутилдициклогексилфосфин, ди(трет-бутил)циклогексилфосфин, три(циклогексил)фосфин), фенантролин или 1,1'-бис(дифенилфосфино)ферроцен.
[22] Способ получения по [19], где лиганд представляет трифенилфосфин, фенантролин или 1,1'-бис(дифенилфосфино)ферроцен.
[23] Способ получения по [19], где лиганд представляет лиганд фосфинового типа.
[24] Способ получения по [23], где лиганд представляет три(трет-бутил)фосфин, трет-бутилдициклогексилфосфин, ди(трет-бутил)метилфосфин, ди(трет-бутил)циклогексилфосфин, три(циклогексил)фосфин, 2-дициклогексилфосфино-2',6'-диизопропокси-1,1'-бифенил, 2-дициклогексилфосфино-2',4',6' -тиризопропил-1,1'-бифенил или его соль.
[25] Способ получения по [23], где лиганд представляет три(трет-бутил)фосфин, трет-бутилдициклогексилфосфин, ди(трет-бутил)метилфосфин, ди(трет-бутил)циклогексилфосфин или три(циклогексил)фосфин.
[26] Способ получения по любому из с [1] по [25], где основание дополнительно присутствует в течение хода реакции.
[27] Способ получения по [26], где основание представляет трет-бутоксид лития.
[28] Способ получения по [26], где основание представляет карбонат калия или карбонат цезия.
[29] Способ получения по любому из с [1] по [28], где соль серебра дополнительно присутствует в течение хода реакции.
[30] Способ получения по [29], где соль серебра представляет карбонат серебра.
[31] Способ получения по любому из с [1] по [30], где C1 до C12 карбоновая кислота или ее соль дополнительно присутствуют в течение хода реакции.
[32] Способ получения по любому из с [1] по [30], где C1 до C6 карбоновая кислота или ее соль дополнительно присутствует в течение хода реакции.
[33] Способ получения по [32], где карбоновая кислота или ее соль представляют 2- метилпропановую кислоту, пивалевую кислоту или ее соль.
[34] Способ получения по [32], где карбоновая кислота или ее соль представляют пивалевую кислоту.
Преимущества изобретения
В соответствии с настоящим изобретением, фенил-замещенное гетероциклическое производное (соединение, представленное формулой (3)) может быть получено в способе, включающем небольшое количество стадий за счет того, что фенольное производное (соединение, представленное формулой (1)) и гетероциклическое производное (соединение, представленное формулой (2)) подвергают реакции селективного сочетания при использовании катализатора переходного металла.
Более того, так как способ включает небольшое количество стадий, возможно получить фенил-замещенное гетероциклическое производное (соединение, представленное формулой (3)) с высоким выходом и низкой стоимостью.
Осуществление изобретения
Описание вариантов осуществления
Термины, используемые отдельно или в комбинации, в настоящем изобретении будут объяснены далее. Если не указано иначе, толкование каждого заместителя должно быть общим для каждой позиции. В дополнение, комбинация заместителей и переменных допустима, только когда такая комбинация приводит к химически стабильному соединению. Когда заместитель сам по себе является замещенным двумя или более группами, такое множество групп может существовать на том же самом или отличном атоме углерода до тех пор, пока образуют стабильную структуру.
В настоящем изобретении, «атом галогена» означает атом фтора, атом хлора, атом брома или атом йода.
В настоящем изобретении, "C1 до C8 алкильная группа" означает линейную или разветвленную насыщенную алифатическую группу, содержащую от 1 до 8 атомов углерода и включает, например, метальную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, трет-бутильную группу, н-пентильную группу, изопентильную группу, неопентильную группу, 1-метилпропильную группу, н-гексильную группу, изогексильную группу, 1,1-диметилбутильную группу, 2,2-диметилбутильную группу, 3,3-диметилбутильную группу, н-гептильную группу, н-октильную группу и тому подобное.
В настоящем изобретении, "C1 до C4 алкоксигруппа" означает группу, состоящую из "C1 до C4 алкильной группы" и оксигруппы. Примеры включают метоксигруппу, этоксигруппу, н-пропилоксигруппу, изопропилоксигруппу, н-бутилоксигруппу, изобутилоксигруппу, трет-бутилоксигруппу и тому подобное.
В настоящем изобретении, "C3 до C6 циклоалкильная группа" означает циклическую алкильную группу, содержащую от 3 до 6 атомов углерода, и включает, например, циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу и тому подобное.
В настоящем изобретении, "C1 до C4 алкилтиогруппа" означает группу, состоящую из "C1 до C4 алкильной группы" и тиогруппы. Примеры включают метилтиогруппу, этилтиогруппу, н-пропилтиогруппу, изопропилтиогруппу, н-бутилтиогруппу, изобутилтиогруппу, трет-бутилтиогруппу и тому подобное.
В настоящем изобретении, "галогенметильная группа" означает метальную группу, замещенную одним или более атомами галогена и включает, например, трифторметильную группу, дифторметильную группу, фторметильную группу, трихлорметильную группу, дихлорметильную группу, хлорметильную группу, трибромметильную группу, дибромметильную группу, бромметильную группу и тому подобное.
В настоящем изобретении, "уходящая группа" означает атом или группу атомов, которые уходят из реакционного субстрата в реакции замещения, реакции отщепления или тому подобное. Такая уходящая группа включает, например, атом галогена, -OCO2-(C1 до C4 алкильную группу), -OCO2-(фенильную группу), -OSO2-(C1 до C4 алкильную группу), -OSO2-(фенильную группу), диазониевую группу (-N+≡N) или тому подобное. Кроме того, C1 до C4 алкильная группа и фенильная группа, которые составляют уходящую группу, могут быть замещены 1 до 3 атомами галогена и 1 до 3 атомами галогена или C1 до C4 алкильными группами, соответственно. Однако настоящее изобретение этим не ограничено.
"Защитная группа для гидроксильной группы" означает группу, которая защищает гидроксильную группу. Такая "защитная группа для гидроксильной группы" является хорошо известной в уровне технике и классифицированной на защитную группу простоэфирного типа, защитную группу типа простого силильного эфира, защитную группу сложноэфирного типа, защитную группу карбонатного типа, защитную группу фосфинового типа, защитную группу сульфонатного типа и тому подобное. Примеры включают группы, описанные в качестве защитной группы фенола и тому подобное в Т.W. Greene и Р.G.M. Wuts, "Protective Groups in Organic Synthesis (3rd Ed., 1994) (4th Ed., 2006)" и тому подобное, такие как бензилоксиметильная группа, метоксиэтоксиметильная группа, фенилтиометильная группа, фенацилметильная группа, 4-бромфенацилметильная группа, циклопропилметильная группа, аллильная группа, пропаргиловая группа, циклогексильная группа, бензильная группа, орто-нитробензильная группа, 4-(диметиламино)карбонилбензильная группа, 4-метилсульфинилбензильная группа, 9-антранилметильная группа, 4-picoryl group, триметилсилильная группа, трет-бутилдиметилсилильная группа, трет-бутилдифенилсилильная группа, триизопропилсилильная группа, формильная группа, -(C=O)-(C1 до C4 алкильная группа), бензоильная группа, 4-оксопентаноильная группа, пивалоильная группа, группа сложного метилового эфира, 1-адамантилоксикарбонильная группа, трет-бутоксикарбонильная группа, 4-метилсульфинилбензилоксикарбонильная группа, 2,4-диметилпент-3-илоксикарбонильная группа, 2,2,2-трихлорэтоксикарбонильная группа, винилоксикарбонильная группа, бензилоксикарбонильная группа, -(C=O)NH-(C1 до C4 алкильная группа), метансульфонильная группа, толуолсульфонильная группа и тому подобное. Однако настоящее изобретение не ограничено группами, проиллюстрированными здесь, и любая группа может быть выбрана, если она использована в качестве защитной группы для гидроксильной группы. Здесь, защитную группу для гидроксильной группы в качестве А используют как таковую, когда Х представляет атом кислорода. Например, когда бензильная группа является защитной группой, А-Х- соответствует PhCH2-O-.
"Защитная группа сложноэфирного типа для карбоксильной группы" в настоящем изобретении означает группу, которая защищает карбоксильную группу за счет присоединения к атому кислорода карбоксильной группы, которая должна быть защищена, и образования сложного эфира. Такая "защитная группа сложноэфирного типа для карбоксильной группы" включает группы, описанные в качестве защитной группы сложноэфирного типа для карбоксильной группы в Т.W. Greene and P.G.M. Wuts, "Protective Groups in Organic Synthesis (3rd Ed.,1994) (4th Ed., 2006)," такие как C1 до C6 алкильную группу, 9-флуоренилметильную группу, метоксиметильную группу, метилтиометильную группу, тетрагидропиранильную группу, тетрагидрофуранильную группу, метоксиэтоксиметильную группу, 2-(триметилсилил)этоксиметильную группу, бензилоксиметильную группу, пивалоилоксиметильную группу, фенилацетоксиметильную группу, триизопропилсилилметильную группу, пара-бромфенацильную группу, α-метилфенацильную группу, пара-метоксифенацильную группу, децильную группу, карбоксамидометильную группу, пара-азобензокарбоксамидометильную группу, N-фталимидометильную группу, 2,2,2-трихлорэтильную группу, 2-галогенэтильную группу, ω-хлоралкильную группу, 2-(триэтилсилил)этильную группу, 2-метилтиоэтильную группу, 1,3-дитианил-2-метильную группу, 2-(пара-нитрофенилсульфенил)этильную группу, 2-(пара-толуолсульфонил)этильную группу, 2-(2'-пиридил)этильную группу, 2-(пара-метоксифенил)этильную группу, 2-(дифенилфосфино)этильную группу, 1-метил-1-фенилэтильную группу, 2-(4-ацетил-2-нитрофенил)этильную группу, 2-цианоэтильную группу, дициклопропилметильную группу, циклопентильную группу, циклогексильную группу, аллильную группу, металлильную группу, 2-метилбут-3-ен-2-ильную группу, 3-метилбут-2-(пренильную) группу, 3-бутен-1-ильную группу, 4-(триметилсилил)-2-бутен-1-ильную группу, циннамильную группу, α-метилциннамильную группу, проп-2-инильную (пропаргиловую) группу, фенильную группу, 2,6-диметилфенильную группу, 2,6-диизопропилфенильную группу, 2,6-ди(трет-бутил)-4-метилфенильную группу, 2,6-ди(трет-бутил)-4-метоксифенильную группу, пара-(метилтио)фенильную группу, пентафторфенильную группу, бензильную группу, трифенилметильную группу, дифенилметильную группу, бис(орто-нитрофенил)метильную группу, 9-антранилметильную группу, 2-(9,10-диоксо)антранилметильную группу, 5-дибензосуберильную группу, 1-пиренилметильную группу, 2-(трифторметил)-6-хромонилметильную группу, 2,4,6-триметилбензильную группу, пара-бромбензильную группу, орто-нитробензильную группу, пара-нитробензильную группу, пара-метоксибензильную группу, 2,6-диметоксибензильную группу, 4-(метилсульфинил)бензильную группу, 4-сульфобензильную группу, 4-азидометоксибензильную группу, пиперониловую группу, 4-piconyl group, пapa-бензильную группу, триметилсилильную группу, триэтилсилильную группу, трет-бутилдиметилсилильную группу, изопропилдиметилсилильную группу, фенилдиметилсилильную группу, ди(трет-бутил)метилсилильную группу, триизопропилсилильную группу, C1 до C6 алкилтиогруппу, оксазольную группу, 2-алкил-1,3-оксазолиновую группу, 4-алкил-5-оксо-1,3-оксазолидиновую группу, 2,2-бистрифторметил-4-алкил-5-оксо-1,3 -оксазолидиновую группу, 5 -алкил-4-оксо-1,3-диоксолановую группу, диоксаноновую группу и тому подобное. Однако настоящее изобретение не ограничено группами, проиллюстрированными здесь, и любая группа может быть выбрана, если она использована в качестве защитной группы для карбоксильной группы.
"Защитная группа амидного типа для карбоксильной группы" в настоящем изобретении означает группу, которая защищает карбоксильную группу за счет присоединения к карбонильному атому углерода карбоксильной группы, которая должна быть защищена, и образования амида. Такая "защитная группа амидного типа для карбоксильной группы" включает группы, описанные в качестве защитной группы для карбоксильной группы в Т.W. Greene and P.G.M. Wuts, "Protective Groups in Organic Synthesis (3rd Ed., 1994) (4th Ed., 2006)," такая как N,N-диметиламиногруппа, пирролидинильная группа, пиперидинильная группа, 5,6-дигидрофенантридильная группа, орто-нитрофениламиногруппа, N-7-нитроиндолильная группа, N-8-нитро-l,2,3,4-тетрагидрохинолильная группа, N-фенилгидразильная группа, N,N'-диизопропилгидразильная группа и тому подобное. Однако настоящее изобретение не ограничено группами, проиллюстрированными здесь, и любая аминогруппа может быть выбрана, если она использована в качестве защитной группы для карбоксильной группы.
В настоящем изобретении, "C" такой как в "C1" и тому подобное, представляет собой атом углерода и цифра, которая следует за ним, представляет количество атомов углерода. Например, "C1 до C6" представляет интервал количества атомов углерода от 1 до 6. Естественно, в настоящем изобретении, когда количество атомов углерода является разным, соответствующая группа является отличной. Например, "C1 до C4 алкильная группа" означает группу, содержащую от 1 до 4 атомов углерода среди алкильных групп, определенных "C1 до C8 алкильной группой". Толкование количества атомов углерода в других группах является тем же самым.
"Диазониевая группа" в настоящем изобретении может образовывать соль. Такая соль включает фторидную соль, хлоридную соль, бромидную соль, иодидную соль, тетрафторборатную соль и тому подобное.
Сокращения, использованные в настоящем изобретении представляют следующее:
TfO: трифторметансульфонилоксигруппа, MsO: метансульфонилоксигруппа, TsO: толуолсульфонилоксигруппа, Me: метильная группа, Et: этильная группа, n-Pr; н-пропильная группа, i-Pr: изопропильная группа, i-Bu: изобутильная группа, t-Bu: трет-бутильная группа, MeO: метоксигруппа, Ph: фенильная группа, ОАс: ацетилоксигруппа, 4-MeO-Ph: 4-метоксифенильная группа, Cy: циклогексильная группа, Piv: пивалоильная группа.
Настоящее изобретение относится к способу, включающему взаимодействие соединения, представленного следующей формулой (I):
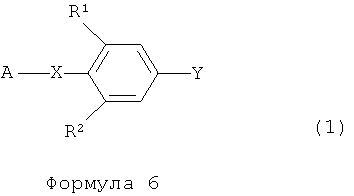
и соединения, представленного следующей формулой (2):
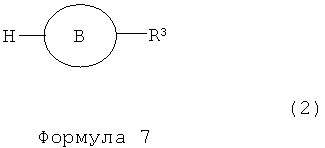
в присутствии соединения переходного металла, для того чтобы получить фенил-замещенное гетероциклическое производное, представленное следующей формулой (3):
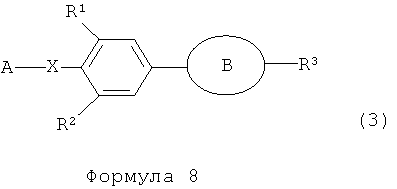
В формулах (1) и (3), R1 представляет собой атом водорода или атом галогена.
"Атом галогена" в R1 представляет, предпочтительно, атом хлора или атом фтора, более предпочтительно, атом фтора.
В целом, R1 представляет, предпочтительно, атом водорода.
В формулах (1) и (3), R2 представляют собой атом водорода, цианогруппу, нитрогруппу, атом галогена, формильную группу или галогенметильную группу.
"Атом галогена" в R2 представляет, предпочтительно, атом брома.
"Галогенметильная группа" в R2 представляет, предпочтительно, хлорметильную группу, дихлорметильную группу, трихлорметильную группу или трифторметильную группу.
В целом, R2 представляет, предпочтительно, цианогруппу, нитрогруппу или формильную группу и прежде всего, цианогруппа является предпочтительной.
В формулах (1) и (3), A представляет собой атом водорода, C1 до C6 алкильную группу, C3 до C6 циклоалкильную группу, фенильную группу, атом фтора (только когда Х представляет связь), или защитную группу для гидроксильной группы (только когда Х представляет атом кислорода). Здесь, защитную группу для гидроксильной группы в качестве A, используют как таковую, когда Х представляет атом кислорода. Например, когда защитная группа представляет бензильную группу, A-X- представляет собой PhCH2-O-.
Более того, А может быть замещен от 1 до 3 заместителями, такой заместитель представляющий группу, выбран из группы, состоящей из атома галогена, C1 до C4 алкильной группы, C1 до C4 алкоксигруппы, C1 до C4 алкилтиогруппы, C3 до C6 циклоалкильной группы, фенильной группы, феноксигруппы и пиридильной группы.
"C1 до C9 алкильная группа" в А представляет, предпочтительно, метальную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, трет-бутильную группу, н-пентильную группу, изопентильную группу или неопентильную группу. В целом, предпочтительно, представляет изобутильную группу или неопентильную группу; более предпочтительно, представляет изобутильную группу.
В целом, A представляет, предпочтительно, C1 до C5 алкильную группу.
В формулах (1) и (3), X представляет собой связь (только когда A представляет фенильную группу или атом фтора) или атом кислорода. В целом, атом кислорода является предпочтительным.
В формуле (1), Y представляет собой уходящую группу. В целом, предпочтительно, представляет атом галогена, -OCO2-(C1 до C4 алкильную группу), -OCO2-(фенильную группу), -OSO2-(C1 до C4 алкильную группу), -OSO2-(фенильную группу) или диазониевую группу.
Когда уходящая группа в качестве Y представляет "-OCO2-(C1 до C4 алкильную группу)" или "-OSO2-(C1 до C4 алкильную группу)", такая "C1 до C4 алкильная группа" в Y представляет, предпочтительно, метальную группу.
Когда уходящая группа, в качестве Y, представляет "-OCO2-(C1 до C4 алкильную группу)" или "-OSO2-(C1 до C4 алкильную группу)", такая "C1 до C4 алкильная группа" в Y может быть замещена 1 до 3 атомами галогена. Такой "атом галогена" представляет, предпочтительно, атом фтора. Особенно предпочтительно, что группа замещена тремя атомами фтора.
Когда уходящая группа, в качестве Y, представляет "-OCO2-(фенильную группу)" или "-OSO2-(фенильную группу)", такая "фенильная группа" в Y может быть замещенной 1 до 3 атомами галогена или C1 до C4 алкильными группами. Такая "C1 до C4 алкильная группа" представляет, предпочтительно, метальную группу.
Когда уходящая группа в качестве Y представляет "атом галогена", "атом галогена" представляет, предпочтительно, атом йода, атом брома или атом хлора. В целом, атом йода или атом брома является предпочтительным.
"Диазониевая группа" может образовывать соль. Когда уходящая группа, в качестве Y, представляет "диазониевую группу", соль "диазониевой группы" представляет, предпочтительно, тетрафторборат.
В целом, Y представляет, предпочтительно, атом йода, атом брома, трифторметансульфонилокси или тому подобное.
В формуле (2), H представляет собой атом водорода.
В формулах (2) и (3), B представляет собой группу, выбранную из следующих формул. Между тем, связь с правой стороны каждой из следующих формул предназначена для связывания с R3; и связь с левой стороны предназначена для связывания с атомом водорода в формуле (2) и фенильной группой в формуле (3):
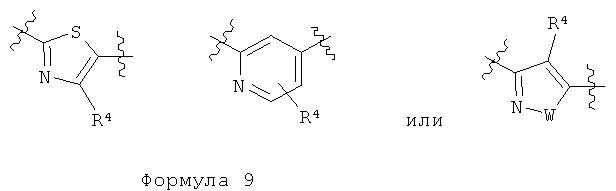 ,
,
В целом, следующая группа является предпочтительной:
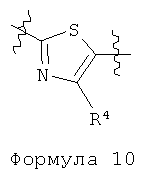
В формулах (2) и (3), R3 представляет собой COOR3b или COR3b.
R3a представляет собой атом водорода, C1 до C4 алкильную группу или защитную группу сложноэфирного типа для карбоксильной группы. Здесь, защитная группа сложноэфирного типа для карбоксильной группы в качестве R3a защищает карбоксильную группу, которую R3a замещает.
Например, R3a, предпочтительно, представляет атом водорода или C1 до C4 алкильную группу.
R3b представляет защитную группу амидного типа для карбоксильной группы, которая образует амид с соседней карбонильной группой.
В целом, R3 представляет, предпочтительно, COOR3a.
В формулах (2) и (3), R4 представляет атом водорода, атом галогена или C1 до C4 алкильную группу.
"Атом галогена" в R4 представляет, предпочтительно, атом фтора.
"C1 до C4 алкильная группа" в R4 представляет, предпочтительно, метальную группу.
В целом, R4 представляет, предпочтительно, C1 до C4 алкильную группу. В основном, метальная группа является предпочтительной.
В формулах (2) и (3), W представляет собой атом кислорода или атом серы.
В формуле (3), значение A, X, R1 и R2 и их предпочтительных групп является, соответственно, тем же самым значением, как и в формуле (1); и значение B и R3 и их предпочтительных групп является тем же самым значением, как в формуле (2).
Конкретные примеры соединений, представленных формулой (1), и конкретные примеры соединений, представленных формулой (2), приведены в таблицах с 1 по 4 и таблицах с 5 по 7, соответственно. Однако, соединения, представленные формулой (1) и формулой (3) не ограничиваются такими конкретными примерами.
Способ получения настоящего изобретения характеризуется тем, что соединение переходного металла используют в качестве катализатора. В способе получения настоящего изобретения, переходные металлы в используемых соединениях переходного металла являются другими металлами, чем никель и включают медь, палладий, кобальт, железо, родий, рутений, иридий и тому подобное. В целом, медь, палладий или кобальт является предпочтительным. Медь включает нуль-валентную Cu(0), одновалентную Cu(I) и дивалентную Cu(II), где предпочтительной является нуль-валентная Cu(0) или одновалентная Cu(I). Палладий является предпочтительно нуль-валентным Pd(0), одновалентным Pd(I) или дивалентным Pd(II). Кобальт включает нуль-валентный Co(0), одновалентный Co(I), дивалентный Co(II) и тривалентный Co(III), где предпочтительным является нуль-валентный Co(0), одновалентный Co или дивалентный Co (II). Железо включает нуль-валентное Fe(0), дивалентное Fe(II) и тривалентное Fe(III), где предпочтительным является дивалентное Fe(II) или тривалентное Fe(III). Родий является предпочтительно нуль-валентным Rh(0) или одновалентным Rh(I). Рутений является предпочтительно нуль-валентным Ru(0) или дивалентным Rh(II). Иридий включает нуль-валентный Ir(0), одновалентный Ir(I), дивалентный Ir(II), тривалентный Ir(III) и тетравалентный Ir(IV), где предпочтительным является тривалентный Ir(III).
Соль Cu(I) включает хлорид меди(I), бромид меди (I), иодид меди(I), ацетат меди(I), тетрафторборат меди, тиофен-2-карбоксилат меди, ее гидраты, смеси и тому подобное.
Соль Cu(II) включает фторид меди (II), хлорид меди (II), бромид меди (II), иодид меди (II), ацетат меди (II), формиат меди (II), гидроксид меди (II), нитрат меди (II), карбонат меди (II), ацетилацетонат меди (II), борат меди (II), оксалат меди (II), фталат меди (II), тартрат меди (II), трифторметансульфонат меди (II), бензоат меди(II), ее гидраты, смеси и тому подобное.
В целом, предпочтительным является иодид меди (I) (CuI).
Соль Pd(I) включает дибром-дипалладий (I), ее гидрат и тому подобное.
Соль Pd(II) включает ацетат палладия (II), пропионат палладия (II), бутаноат палладия (II), 2-метилпропаноат палладия(II), 3-метилбутаноат палладия(II), 2-метилбутаноат палладия (II), 2-этилбутаноат палладия (II), пивалат палладия (II), 3,3-диметилбутаноат палладия (II), 2,2,3,3-тетраметилбутаноат палладия (II), трифторацетат палладия (II), нитрат палладия (II), хлорид палладия (II), бромил палладия(II), иодид палладия (II), ацетилацетонат палладия (II), перхлорат палладия (II), цитрат палладия (II), оксалат палладия (II), циклогексанбутират палладия (II), бензоат палладия (II), стеарат палладия (II), сульфамат палладия (II), карбонат палладия (II), тиоцианат палладия (II), трифторметансульфонат палладия (II), бис(4-диэтиламинодитиобензил)палладия(II) палладия (II), цианид палладия (II), фторид палладия (II), борид палладия (II), борат палладия (II), гипофосфит палладия (II), сульфатноаммонийный палладий (II), гидроксид палладия (II), циклопентадиенил палладия (II), ее гидраты, смеси и тому подобное. В целом, предпочтительным является ацетат палладия (II) (Pd(OAc)2), пропионат палладия (II) (Pd(O(C=O)CH2CH3)2), 2-метилпропаноат палладия (II) (Pd(O(C=O)CH(CH3)2)2, пивалат палладия (II) (Pd(OPiv)2), хлорид палладия (II) (PdCl2), бромид палладия(I) (Pd2Br2) гидроксид палладия (II) (Pd(OH)2); особенно предпочтительным является ацетат палладия (II) (Pd(OAc)2), пропионат палладия (II) (Pd(O(C=O)CH2CH3)2), 2-метилпропаноат палладия (II) (Pd(O(C=O)CH(CH3)2)2, или пивалат палладия (Pd(OPiv)2).
Соль кобальта (II) включает ацетат кобальта (II), нитрат кобальта (II), хлорид кобальта(II), бромид кобальта (II), иодид кобальт (II), ацетилацетонат кобальта (II), перхлорат кобальта (II), цитрат кобальта (II), оксалат кобальта (II), фумарат кобальта (II), глюконат кобальта (II), бензоат кобальта (II), лактат кобальта(II), стеарат кобальта (II), сульфамат кобальта, карбонат кобальта (II), тиоцианат кобальта (II), фторид кобальта (II), фосфат кобальта (II), сульфат кобальта (II), гидроксид кобальта (II), сульфид кобальта (II), ее гидраты, смеси и тому подобное. В целом, предпочтительным является ацетат кобальта (II) (Co(ОАс)2).
Соль кобальта (III) включает фторид кобальта (III), хлорид кобальта (III), бромид кобальта (III), иодид кобальта (III), ацетилацетонат кобальта (III), сульфат кобальта (III), нитрат кобальта (III), фосфат кобальта (III), перхлорат кобальта(III), цитрат кобальта (III), ее гидраты, смеси и тому подобное.
Соль железа (II) включает фторид железа (II), хлорид железа (II), бромид железа (II), иодид железа (II), сульфат железа (II), нитрат железа (II), оксалат (II), фумарат железа(II), ацетат железа (II), лактат железа (II), глюконат (II), бензоат железа (II), стеарат железа (II), ацетилацетонат железа (II), сульфид железа(II), ее гидраты, смеси и тому подобное.
Соль железа(III) включает фторид железа(III), хлорид железа(III), бромид железа (III), иодид железа(III), сульфат железа(III), фосфат железа(III), перхлорат железа (III), ее гидраты, смеси и тому подобное.
Соль родия (I) включает хлорид родия(I), ее гидраты, смеси и тому подобное.
Соль рутения (II) включает хлорид рутения(II), ее гидраты, смеси и тому подобное.
Соль иридия(III) включает хлорид иридия(III), бромид иридия(III), ацетат иридия (III), карбонил иридия(III), (ацетилацетонато)иридий(III), калий гексахлориридат(III), калий пентахлорнитрозилиридат(III), 2,4-пентадионат иридия (III), димер дихлорида (пентаметилциклопентадиенил)иридия(III), димер дихлор(пентаметилциклопентадиенил)иридия(III), димер гидрохлорида (пентаметилциклопентадиенил)иридия, ее гидраты, смеси и тому подобное.
Соединения переходного металла могут быть использованы в виде смеси.
Среди приведенных соединений переходного металла, особо предпочтительной разновидностью металла является палладий.
В качестве настоящих соединений переходного металла, могут быть использованы соединения, к которым лиганды были скоординированы заранее. В качестве таких соединений переходного металла, содержащего координированные лиганды, могут быть указаны, например, следующие соединения переходного металла. Однако настоящее изобретение ими не ограничено.
Формула 11
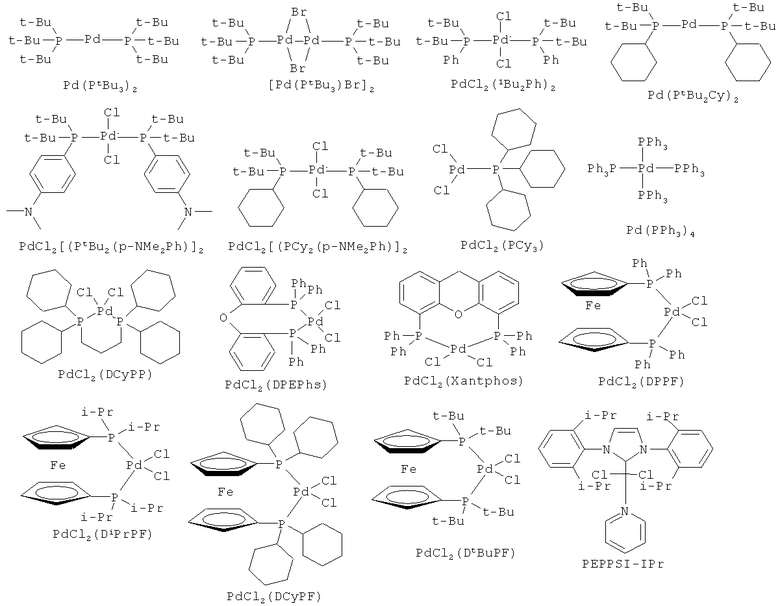
В способе получения настоящего изобретения, лиганд, который может координировать переходный металл может присутствовать вместе с соединением переходного металла. Присутствие лиганда, который может координировать к соединению переходного металла в реакции, способствует сочетанию фенильного кольца фенильного производного и связь C-H на гетероциклическом производном может быть присоединена с высокой селективностью, приводящей к более высокому выходу соединения, представленному формулой (3). Такой лиганд, использованный в способе настоящего изобретения, включает группу карбоновой кислоты, группу амида, группу фосфина, группу оксима, группу сульфида, группу сульфоновой кислоты, группу 1,3-дикетона, группу основания Шиффа, группу оксазолина, группу диамина, группу углеводорода, монооксид углерода, группу карбена и тому подобное. Однако настоящее изобретение не ограничено ими. Координационный атом в лиганде включает атом азота, атом фосфора, атом кислорода, атом серы и тому подобное. В качестве лиганда, присутствуют монодентатный лиганд, имеющий координационный атом в одном положении и полидентатный лиганд, имеющий координационные атомы в двух и более положениях. Что касается углеводородного класса, монооксида углерода и класса карбена, то координационный атом представляет атом углерода. Данные лиганды могут быть использованы в виде солей.
Монодентатный лиганд включает лиганд фосфинового типа, представленный PR5R6R7 (где R5, R6 и R7 каждый независимо представляет C1 до C8 алкильную группу, C1 до C4 алкоксигруппу, C3 до C8 циклоалкильную группу, фенильную группу, бифенильную группу, феноксигруппу и фурильную группу. Данная C3 до C8 циклоалкильная группа может быть дополнительно замещена C1 до C4 алкильной группой. Фенильная группа может быть дополнительно замещена метильной группой, группой сульфоновой кислоты или их солями. Бифенильная группа может быть дополнительно замещена, каждая независимо, C1 до C4 алкильной группой, C1 до C4 алкоксигруппой и диметиламиногруппой), триэтиламином, пиридином и тому подобное.
Лиганд фосфинового типа представленный PR5R6R7, включает например, трет-бутилдициклогексилфосфин, изобутилдициклогексилфосфин, (н-бутил)дициклогексилфосфин, изопропилдициклогексилфосфин, (н-пропил)дициклогексилфосфин, этилдициклогексилфосфин, метилдициклогексилфосфин, циклопропилдициклогексилфосфин, циклобутилдициклогексилфосфин, трет-бутилдициклооктилфосфин, трет-бутилдициклогептилфосфин, трет-бутилдициклопентилфосфин, трет-бутилдициклобутилфосфин, трет-бутилдициклопропилфосфин, триэтилфосфин, три(н-пропил)фосфин, три(изопропил)фосфин, три(трет-бутил)фосфин, три(н-бутил)фосфин, три(н-октил)фосфин, три(циклооктил)фосфин, три(циклогептил)фосфин, три(циклогексил)фосфин, три(циклопентил)фосфин, три(циклобутил)фосфин, три(циклопропил)фосфин, ди(трет-бутил)метилфосфин, ди(трет-бутил)этилфосфин, ди(трет-бутил)н-пропилфосфин, ди(трет-бутил)изопропилфосфин, ди(трет-бутил)н-бутилфосфин, ди(трет-бутил)изобутилфосфин, ди(трет-бутил)неопентилфосфин, трифенилфосфин, три(орто-толил)фосфин, три(мезитил)фосфин, три(фенокси)фосфин, три(2-фурил)фосфин, триметоксифосфин, триэтоксифосфин, три(н-пропилокси)фосфин, три(изопропилокси)фосфин, три(н-бутилокси)фосфин, три(изобутилокси)фосфин, три(трет-бутилокси)фосфин, ди(трет-бутил)циклогексилфосфин, ди(изобутил)циклогексилфосфин, ди(н-бутил)циклогексилфосфин, ди(изопропил)циклогексилфосфин, ди(н-пропил)циклогексилфосфин, диэтилциклогексилфосфин, диметилциклогексилфосфин, ди(трет-бутил)циклопентилфосфин, ди(изобутил)циклопентилфосфин, ди(н-бутил)циклопентилфосфин, ди(изопропил)циклопентилфосфин, ди(н-пропил)циклопентилфосфин, диэтилциклопентилфосфин, диметилциклопентилфосфин, ди(трет-бутил)циклооктилфосфин, ди(трет-бутил)циклогептилфосфин, ди(трет-бутил)циклопентилфосфин, ди(трет-бутил)циклобутилфосфин, ди(трет-бутил)циклопропилфосфин, диметилфенилфосфин, диэтилфенилфосфин, ди(н-пропил)фенилфосфин, ди(изопропил)фенилфосфин, ди(н-бутил)фенилфосфин, ди(изобутил)фенилфосфин, ди(трет-бутил)фенилфосфин, ди(циклооктил)фенилфосфин, дициклогептилфенилфосфин, дициклогексилфенилфосфин, дициклопентилфенилфосфин, дициклобутилфенилфосфин, дициклопропилфенилфосфин, дициклогексил(пара-толил)фосфин, дициклогексил(орто-толил)фосфин, дициклогексил(пара-толил)фосфин, дициклогексил(2,4,6-триметилфенил)фосфин, метилдифенилфосфин, этилдифенилфосфин, (н-пропил)дифенилфосфин, изопропилдифенилфосфин, (н-бутил)дифенилфосфин, изобутилдифенилфосфин, (трет-бутил)дифенилфосфин, циклооктилдифенилфосфин, циклогептилдифенилфосфин, циклогексилдифенилфосфин, циклопентилдифенилфосфин, циклобутилдифенилфосфин, циклопропилдифенилфосфин, бис(пара-сульфонатофенил)фенилфосфин калия, cBRIDP, BippyPhos, TrippyPhos, XPhos (2-дициклогексилфосфино-2',4',6'-триизопропил-1,1'-бифенил), t-Bu-XPhos, JohnPhos, Cy-JohnPhos, MePhos, t-Bu-MePhos, DavePhos, t-Bu-DavePhos, SPhos, RuPhos (2-дициклогексилфосфино-2',6'-диизопропокси-1,1'-бифенил), cataCXium A, cataCXium ABn, cataCXium PtB, cataCXium PCy, cataCXium POMetB, cataCXium POMeCy, cataCXium PIntB, cataCXium PInCy, cataCXium PICy, Q-Phos, JOSIPHOS, и тому подобное, и их смеси.
Формула 12
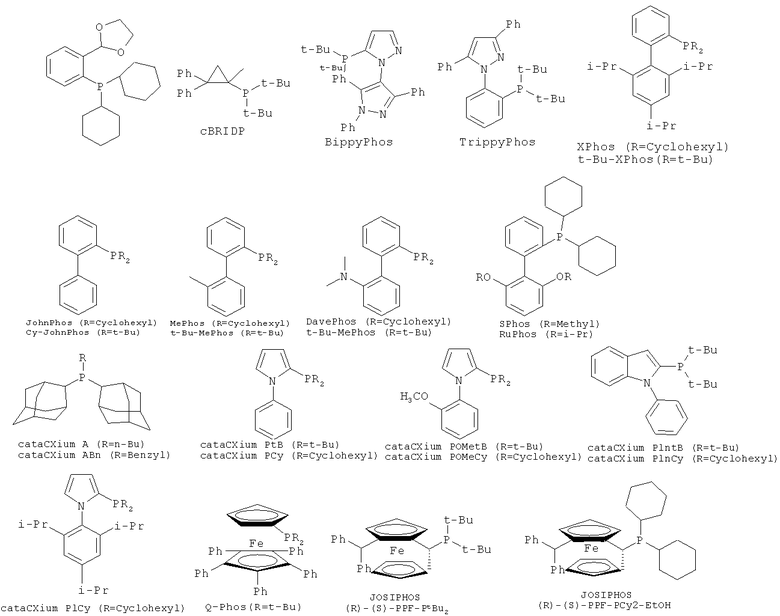
Бидендатный лиганд включает 2,2'-бипиридил, 4,4'-(трет-бутил)бипиридил, фенантролин, 2,2'-бипиримидил, 1,4-диазабицикло[2.2.2]октан, 2-(диметиламино)этанол, тетраметилэтилендиамин, N,N-диметилэтилендиамин, N,N'-диметилэтилендиамин, 2-аминометилпиридин, (NE)-N-(пиридин-2-илметилиден)анилин, 1,1'-бис(дифенилфосфино)ферроцен, 1,1'-бис(трет-бутил)ферроцен, дифенилфосфинометан, 1,2-бис(дифенилфосфино)этан, 1,3-бис(дифенилфосфино)пропан, 1,5-бис(дифенилфосфино)пентан, 1,2-бис(дипентафторфенилфосфино)этан, 1,2-бис(дициклогексилфосфино)этан, 1,3-(дициклогексилфосфино)пропан, 1,2-бис(ди-трет-бутилфосфино)этан, 1,3-бис(ди-трет-бутилфосфино)пропан, 1,2-бис(дифенилфосфино)бензол, 1,5-циклооктадиен, BINAP, BIPHEMP, PROPHOS, DIOP, DEGUPHOS, DIPAMP, DuPHOS, NORPHOS, PNNP, SKEWPHOS, BPPFA, SEGPHOS, CHIRAPHOS, DPEphos, Xantphos, и тому подобное, и их смеси.
Формула 13
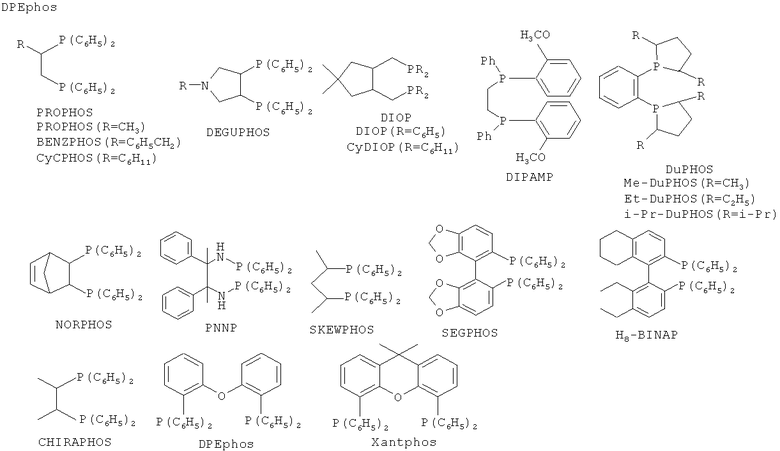
BINAP включает его производные и конкретные примеры включают 2,2'-бис(дифенилфосфино)-1,1'-бинафтил, 2,2'-бис(ди-пара-толилфосфино)-1,1'-бинафтил, 2,2'-бис(ди-пара-трет-бутилфенилфосфино)-1,1'-бинафтил, 2,2'-бис(ди-мета-толилфосфино)-1,1'-бинафтил, 2,2'-бис(ди-3,5-диметилфенилфосфино)-1,1'-бинафтил, 2,2'-бис(ди-пара-метоксифенилфосфино)-1,1'-бинафтил, 2,2'-бис(дициклопентилфосфино)-1,1'-бинафтил, 2,2'-бис(дициклогексилфосфино)-1,1'-бинафтил, 2-ди(р-нафтил)фосфино-2'-дифенилфосфино-1,1'-бинафтил, 2-дифенилфосфино-2'-ди(пара-трифторметилфенил)фосфино-1,1'-бинафтил и тому подобное.
BIPHEMP включает его производные и конкретные примеры включают 2,2'-диметил-6,6'-бис(дифенилфосфино)-1,1'-бифенил, 2,2'-диметил-6,6'-бис(дициклогексилфосфино)-1,1'-бифенил, 2,2'-диметил-4,4'-бис(диметиламино)-6,6'-бис(дифенилфосфино)-1,1'-бифенил, 2,2',4,4'-тетраметил-6,6'-бис(дифенилфосфино)-1,1'-бифенил, 2,2'-диметокси-6,6'-бис(дифенилфосфино)-1,1'-бифенил, 2,2',3,3'-тетраметокси-6,6'-бис(дифенилфосфино)-1,1'-бифенил, 2,2',4,4'-тетраметил-3,3'-диметокси-6,6'-бис(дифенилфосфино)-1,1'-бифенил, 2,2'-диметил-6,6'-бис(ди-пара-толилфосфино)-1,1'-бифенил, 2,2'-диметил-6,6'-бис(ди-пара-трет-бутилфенилфосфино)-1,1'-бифенил, 2,2',4,4'-тетраметил-3,3'-диметокси-6,6'-бис(ди-пара-метоксифенилфосфино)-1,1'-бифенил и тому подобное.
Лиганд, используемый в реакции настоящего изобретения, может быть использован в виде соли. Такая соль включает, например, соль соляной кислоты, соль бромистоводородной кислоты, соль тетрафторборной кислоты, и тому подобное.
Когда используют палладиевый катализатор, данный лиганд представляет, предпочтительно, лиганд фосфинового типа. В целом, лиганд фосфинового типа представленный PR5R6R7, является предпочтительным. Конкретно, предпочтительным является три(трет-бутил)фосфин, три(циклогексил)фосфин, трет-бутилдициклогексилфосфин, ди(трет-бутил)циклогексилфосфин, ди(трет-бутил)метилфосфин, 2-дициклогексилфосфино-2',6'-диизопропокси-1,1'-бифенил, 2-дициклогексилфосфино-2',4',6'-триизопропил-1,1'-бифенил или их соли; более предпочтительным, является три(трет-бутил)фосфин, ди(трет-бутил)циклогексилфосфин или их соли, и особенно предпочтительным является ди(трет-бутил)циклогексилфосфин.
Когда лиганд координирован заранее, предпочтительный лиганд может быть использован при таком же координировании к палладию.
Лиганд может быть использован в виде смеси. Более того, лиганд может быть использован при таком же координировании к соединению переходного металла, заранее. В дополнении, лиганд, используемый в реакции настоящего изобретения, может быть не использован в зависимости от обстоятельств.
В способе получения настоящего изобретения, основание может быть использовано вместе с соединением переходного металла. При использовании вместе с основанием, выход настоящего соединения, представленного формулой (3) может быть улучшен. Такое основание, используемое в способе получения настоящего изобретения, не является особо ограниченным, но предпочтительно, в целом, представляет гидрид лития, гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, карбонат цезия, фторид калия, фторид цезия, трикалий фосфат, ацетат натрия, ацетат калия и тому подобное; металлическая соль C1 до C6 алкоксида (литиевая соль, натриевая соль, калиевая соль и магниевая соль); C1 до C6 алкил анионная металлическая соль (литиевая соль, натриевая соль, калиевая соль и магниевая соль); тетра(C1 до C4 алкил)аммонийная соль (фторидная соль, хлоридная соль, и бромидная соль), диизопропилэтиламин, трибутиламин, N-метилморфолин, диазабициклоундецен, диазабициклооктан, имидазол; или тому подобное.
В "металлической соли C1 до C6 алкоксида (литиевая соль, натриевая соль, калиевая соль и магниевая соль)", используемой в качестве основания в способе получения настоящего изобретения, "C1 до C6 алкоксид" включает метоксид, этоксид, н-пропоксид, изопропоксид, н-бутоксид, изобутоксид, трет-бутоксид, н-пентоксид, изопентоксид, неопентоксид, 1-метилпропоксид, н-гексоксид, изогексоксид, 1,1- диметилбутоксид, 2,2-диметилбутоксид, 3,3-диметилбутоксид и тому подобное. Кроме того, могут быть использованы их смеси.
В "C1 до C6 алкил анионной металлической соли (литиевая соль, натриевая соль, калиевая соль и магниевая соль)", используемой в качестве основания, в реакции настоящего изобретения, "C1 до C6 алкиланион" включает метил анион, этил анион, н-пропил анион, изопропил анион, н-бутил анион, изобутил анион, трет-бутил анион, н-пентил анион, изопентил анион, неопентил анион, 1-метилпропил анион, н-гексил анион, изогексил анион, 1,1-диметилбутил анион, 2,2-диметилбутил анион и тому подобное. Кроме того, могут быть использованы их смеси.
Когда используют палладиевый катализатор, основание представляет, предпочтительно, карбонат калия, бикарбонат калия, карбонат цезия или фторид тетра(н-бутил)аммония; особо предпочтительны, карбонат калия или карбонат цезия.
Когда используют медный катализатор, предпочтительным основанием является фосфат калия. Когда используют кобальтовый катализатор, предпочтительным основанием является фторид цезия.
В зависимости от обстоятельств, основание, используемое в настоящей реакции, может не использоваться.
В способе получения настоящего изобретения, восстанавливающий агент, который восстанавливает переходный металл, может быть использован вместе с соединением переходного металла. Например, может быть указан цинк и тому подобное.
В способ получения настоящего изобретения, может быть добавлена соль серебра. Кроме того, соль серебра может дополнительно улучшить выход соединения, представленного формулой (3). Такая соль серебра включает, например, карбонат серебра, и тому подобное.
В способ получения настоящего изобретения может быть добавлена C1 до C4 карбоновая кислота или ее соль. Добавление C1 до C12 карбоновой кислоты или ее соли может улучшить выход соединения, представленного формулой (3) и/или скорость реакции. Данные C1 до C12 карбоновые кислоты и их соли могут быть использованы в виде смеси. C1 до C12 карбоновая кислота содержит 1 до 12 атомов углерода, включая атом углерода карбоксильной группы и может содержать атом галогена, оксогруппу и простую эфирную связь. Примеры включают муравьиную кислоту, уксусную кислоту, пропионовую кислоту, бутановую кислоту, 2-метилпропановую кислоту, пентановую кислоту, 3-метилбутановую кислоту, 2-метилбутановую кислоту, пивалевую кислоту, 3,3-диметилбутановую кислоту, 2-метилпентановую кислоту, 2-метилгексановую кислоту, 2-метилгептановую кислоту, пентанкарбоновую кислоту, гексановую кислоту, 4- метилпентановую кислоту, 3.3-диметилбутановую кислоту, 2-этилбутановую кислоту, 2-метилпентановую кислоту, 3-метилпентановую кислоту, 2,2-диметилбутановую кислоту, 2,3-диметилбутановую кислоту, гептановую кислоту, 2-метилгексановую кислоту, 3-метилгексановую кислоту, 4-метилгексановую кислоту, 5-метилгексановую кислоту, 2,2-диметилпентановую кислоту, 2,3,3-триметилбутановую кислоту, октановую кислоту, 2-пропилпентановую кислоту, 2-этилгексановую кислоту. 2-метилгептановую кислоту, 3-метилгептановую кислоту, 4-метилгептановую кислоту, 6-метилгептановую кислоту, 2,2-диметилгептановую кислоту, 3-метилгептановую кислоту, 2,2-диэтилбутановую кислоту, 2,2,4-триметилпентановую кислоту, 2-метилоктановую кислоту, 2-метилундекановую кислоту, 2-метилнонановую кислоту, α-метилкоричную кислоту, циклопропилуксусную кислоту, 3-циклопропилпропионовую кислоту, циклобутилуксусную кислоту, циклопентилуксусную кислоту, циклогексилуксусную кислоту, циклопентилпропионовую кислоту, (2-метилциклопентил)уксусную кислоту, циклопентанкарбоновую кислоту, 3-оксоциклопентанкарбоновую кислоту, циклопропанкарбоновую кислоту, циклобутанкарбоновую кислоту, циклогексанкарбоновую кислоту, циклогептанкарбоновую кислоту, 1-метилциклопропанкарбоновую кислоту, 2-метилциклопропанкарбоновую кислоту, 2,2-диметилциклопропанкарбоновую кислоту, 2,2,3,3-тетраметилциклопропанкарбоновую кислоту, 2-октилциклопропанкарбоновую кислоту, 1-(4-метилфенил)-1-циклопропанкарбоновую кислоту, 2-пара-толилциклопропанкарбоновую кислоту, 1 -(2-фторфенил)циклопропанкарбоновую кислоту, 1-(3-фторфенил)циклопропанкарбоновую кислоту, 1-(4-фторфенил)циклопропанкарбоновую кислоту, 1-(4-хлорфенил)циклопропанкарбоновую кислоту, 1-(3-хлорфенил)циклопропанкарбоновую кислоту, 2-(4-хлорфенил)циклопропанкарбоновую кислоту, 1-(2,4-дихлорфенил)циклопропанкарбоновую кислоту, 1-(3,4-дихлорфенил)циклопропанкарбоновую кислоту, 2-фтор-2-фенилциклопропанкарбоновую кислоту, 1-(4-метоксифенил)циклопропанкарбоновую кислоту, 2-(4-(трет-бутил)фенил)циклопропанкарбоновую кислоту, 2,2-дифторциклопропанкарбоновую кислоту, 2,2-дихлорциклопропанкарбоновую кислоту, 2-хлор-2-фторциклопропанкарбоновую кислоту, 1-трифторметилциклопропанкарбоновую кислоту, 2,2-дихлор-1-метилциклопропанкарбоновую кислоту, циклопропан-1,1-дикарбновую кислоту, 2,2'-оксидиуксусную кислоту, 1,2-диметилциклопропандикарбоновую кислоту, 4-метилциклобутанкарбоновую кислоту, 4-этилциклопропанкарбоновую кислоту, 3-метоксициклобутанкарбоновую кислоту, 3-хлорциклобутанкарбоновую кислоту, 4-хлорбутанкарбоновую кислоту, 3-оксоциклобутанкарбоновую кислоту, 3,3- диметилциклобутанкарбоновую кислоту, 1-метилциклопентанкарбоновую кислоту, 3-циклопентенкарбоновую кислоту, 1-метилциклопентанкарбоновую кислоту, 1-метилциклогексанкарбоновую кислоту, 4-метилциклогексанкарбоновую кислоту, 2-метилциклогексанкарбоновую кислоту, 3-метилциклогексанкарбоновую кислоту, циклооктанкарбоновую кислоту, спиро[2.2]пентан-1-карбоновую кислоту, спиро[2.3]гексан-1-карбоновую кислоту, бицикло[4.1.0]гептан-7-карбоновую кислоту, трицикло[3.2.1.0*2,4*]октан-3-карбоновую кислоту, бицикло[6.1.0]нонан-9-карбоновую кислоту, бицикло[2.2.1]гептан-1-карбоновую кислоту, бицикло[2.2.1]гептан-2-карбоновую кислоту, 7,7-диметилтрицикло[2.2.1.0(2,6)]гептан-1-карбоновую кислоту, 5-норборнен-2-карбоновую кислоту, норборнан-2-карбоновую кислоту, 1-адамантанкарбоновую кислоту, 3-метиладамантан-1-карбоновую кислоту, 3-фторадамантан-1-карбоновую кислоту, 3,5-диметиладамантан-1-карбоновую кислоту, 3-этиладамантан-1-карбоновую кислоту, 3-хлорадамантан-1-карбоновую кислоту, 3,5,7-триметиладамантан-1-карбоновую кислоту, 3-бромадамантан-1 -карбоновую кислоту, 5-бром-3-метиладамантан-1 -карбоновую кислоту, 5-бром-3-этиладамантан-1-карбоновую кислоту, тетрагидрофуран-2-карбоновую кислоту, тетрагидрофуран-3-карбоновую кислоту, тетрагидропиран-4-карбоновую кислоту, тетрагидропиран-3-карбоновую кислоту, метоксиуксусную кислоту, трихлоруксусную кислоту, дихлоруксусную кислоту, хлоруксусную кислоту, фторуксусную кислоту, 2-фтор-2-метилпропановую кислоту, дифторуксусную кислоту, 2-хлорпропановую кислоту, 3-фторпропионовую кислоту, 2-фторпропионовую кислоту, 2-хлорпропионовую кислоту, 3-хлорпропионовую кислоту, 2-хлорбутановую кислоту, 3-хлорбутановую кислоту, 4-хлорбутановую кислоту, 2-хлор-2-метилпропановую кислоту, 3-хлор-2,2-диметилпропановую кислоту, 5-хлорпентановую кислоту, 2-хлор-3-метилбутановую кислоту, дихлоруксусную кислоту, 1-фтор-1-хлоруксусную кислоту, 2,2-дифторпропионовую кислоту, 2,2-дифторбутановую кислоту, 2,2-дихлорпропионовую кислоту, 2,3-дихлорпропионовую кислоту, хлордифторуксусную кислоту, трифторуксусную кислоту, 3,3,3-трифторпропионовую кислоту, 2-метил-4,4,4-трифторбутановую кислоту, 4,4,4-трифторбутановую кислоту, 2,2,3,3-тетрафторпропионовую кислоту, 2,3,3,3-тетрафторпропионовую кислоту и тому подобное. Однако настоящее изобретение не ограничивается этим.
Такая C1 до C 12 карбоновая кислота, предпочтительно, является карбоновой кислотой, где атом углерода в α-положении карбоксильной группы не является атомом углерода на ароматическом кольце, более предпочтительной, является карбоновая кислота, которая может содержать атом галогена или простую эфирную связь. Примеры включают уксусную кислоту, пропионовую кислоту, 2-метилпропановую кислоту, 2- этилбутановую кислоту, пивалевую кислоту, циклопропановую кислоту, 2,2,3,3-тетраметилциклопропановую кислоту, циклопентановую кислоту, 1-адамантанкарбоновую кислоту, 2-хлор-2-метилпропановую кислоту, тетрагидрофуран-2-карбоновую кислоту 2,2'-оксидиуксусную кислоту, циклопропан-1,1-дикарбоновую кислоту и тому подобное.
В целом, предпочтительной, является карбоновая кислота, содержащая одну карбоксильную группу. Примеры включают уксусную кислоту, пропионовую кислоту, 2-метилпропановую кислоту, 2-этилбутановую кислоту, пивалевую кислоту, циклопропановую кислоту, 2,2,3,3-тетраметилциклопропановую кислоту, циклопентановую кислоту, 1-адамантанкарбоновую кислоту, 2-хлор-2-метилпропановую кислоту, тетрагидрофуран-2-карбоновую кислоту и тому подобное.
Кроме того, более предпочтительной является карбоновая кислота, у которой число атомов водорода, связанных с атомом углерода в α-положении карбоксильной группы равно 0 или 1. Примеры включают 2-метилпропановую кислоту, 2-этилбутановую кислоту, пивалевую кислоту, циклопропановую кислоту, 2,2,3,3-тетраметилциклопропановую кислоту, циклопентановую кислоту, 1-адамантанкарбоновую кислоту, 2-хлор-2-метилпропановую кислоту, тетрагидрофуран-2-карбоновую кислоту и тому подобное.
Особенно, более предпочтительной является карбоновая кислота, содержащая только атомы углерода и атомы водорода, за исключением карбоксильной группы. Примеры включают 2-метилпропановую кислоту, 2-этилбутановую кислоту, пивалевую кислоту, циклопропановую кислоту, 2,2,3,3-тетраметилциклопропановую кислоту, циклопентановую кислоту, 1-адамантанкарбоновую кислоту, и тому подобное.
Более, особенно предпочтительной, является карбоновая кислота, содержащая 1 до 8 атомов углерода, более предпочтительной является карбоновая кислота, содержащая 1 до 6 атомов углерода. Примеры включают 2-метилпропановую кислоту, 2-этилбутановую кислоту, пивалевую кислоту, циклопропановую кислоту, циклопентановую кислоту и тому подобное. Даже более, особенно предпочтительной, является 2-метилпропановая кислота или пивалевая кислота.
C1 до C12 карбоновая кислота, используемая в реакции настоящего изобретения, может быть использована в виде соли. Такая соль включает, например, соли щелочного металла, такие как натриевая соль, калиевая соль, литиевая соль и тому подобное; соли щелочноземельного металла, такие как кальциевая соль, магниевая соль и тому подобное; металлические соли, такие как соль алюминия, соль железа и тому подобное; неорганические соли, такие как аммонийная соль и тому подобное; органические соли, такие как аминные соли, включающие t-octylamine salt (третичная октиламинная соль), дибензиламинную соль, морфолиновую соль, глюкозаминную соль, соль сложного алкилового эфира фенилглицина, этилендиаминную соль, N-метилглюкаминную соль, гуанидиновую соль, диэтиламинную соль, триэтиламинную соль, дициклогексиламинную соль, N,N'-дибензилэтилендиаминную соль, хлорпрокаиновую соль, прокаиновую соль, диэтаноламинную соль, N-бензилфениламинную соль, пиперазиновую соль, тетраметиламмонийную соль, трис(гидроксиметил)аминометановую соль и тому подобное.
C1 до C12 карбоновая кислота и ее соль, используемые в реакции настоящего изобретения, как правило, могут быть использованы в качестве добавки. Однако если они являются коммерчески доступными, как таковые, или их легко приготовить в качестве солей карбоновой кислоты соединений переходного металла (например, пропионат палладия (II)), могут быть использованы карбоксилаты переходного металла.
Способ получения настоящего изобретения может быть проведен в широком интервале температур. Интервал равен, обычно, от 0°C до 200°C, предпочтительно, от 0°C до 150°C. Кроме того, реакцию осуществляют, предпочтительно, при нормальном давлении, но можно проводить при повышенном давлении или пониженном давлении. Время реакции равно от 0,1 до 72 часов, предпочтительно, от 0,1 до 48 часов. Реакция может быть проведена в воздухе, но желательно, проводить реакцию в газовой атмосфере, не оказывающей негативного влияния на реакцию, такой как аргоновый газ, азотный газ и тому подобное. Более того, настоящая реакция может быть подвержена микроволновому облучению.
Растворитель, используемый в способе получения настоящего изобретения, включает алифатические углеводороды (гексан, циклогексан, гептан и тому подобное), алифатические галогенированные углеводороды (дихлорметан, хлороформ, четыреххлористый углерод, дихлорэтан и тому подобное), ароматические углеводороды (бензол, толуол, мезителен, хлорбензол и тому подобное), простые эфиры (диэтиловый эфир, дибутиловый эфир, диметоксиэтан (DME), циклопентилметиловый эфир (CPME), трет-бутилметиловый эфир, тетрагидрофуран, диоксан и тому подобное), сложные эфиры (этилацетат, этилпропионат и тому подобное), амиды кислоты (диметилформамид (DMF), диметилацетамид (DMA), N-метилпирролидон (NMP) и тому подобное), нитрилы (ацетонитрил, пропионитрил и тому подобное), диметилсульфоксид (DMSO), смесь указанных растворителей и тому подобное.
В способе получения настоящего изобретения, количество используемого соединения формулы (2) может быть в диапазоне от 1 моль% до 1000 моль% относительно соединения формулы (1). Диапазон равен, предпочтительно, 50 моль% до 200 моль%, более предпочтительно, 80 моль% до 120 моль%.
В способе настоящего изобретения, количество используемого соединения переходного металла и лиганда может быть в диапазоне 100 моль% или меньше относительно соединения формулы (1) или соединения формулы (2). Предпочтительно, количество равно в диапазоне 20 моль% или меньше. Лиганд может быть не использован в зависимости от обстоятельств.
В способе получения настоящего изобретения, количество используемого основания может быть в диапазоне 1000 моль% или меньше относительно соединения формулы (1) или соединения формулы (2). Предпочтительно, количество равно в диапазоне 500 моль% или меньше.
В способе получения настоящего изобретения, количество используемого растворителя может быть 1000 кратным или меньше веса соединения формулы (1) или соединения формулы (2). Количество равно, предпочтительно, 100 кратным или меньше, более предпочтительно, 20 кратным или меньше.
Порядок введения соединения формулы (1), соединения формулы (2), соединения переходного металла, лиганда, основания, C1 до C12 карбоновой кислоты и растворителя, которые используют в способе получения настоящего изобретения, является необязательным. Самый лучший порядок может быть выбран в зависимости от комбинации используемых реагентов.
В способе получения настоящего изобретения, количество используемой C1 до C12 карбоновой кислоты может быть 50000 моль% или меньше, относительно используемого соединения переходного металла. Количество является, предпочтительно, 5000 моль% или меньше, более предпочтительно 1000 моль% или меньше, особо предпочтительно, 500 моль% или меньше.
В способе настоящего изобретения, количество используемой соли серебра равно 500 моль% или меньше относительно соединения формулы (1). Предпочтительно, количество равно 200 моль% или меньше.
"Моль%" обозначает концентрацию конкретного вещества, полученную делением количества молей конкретного вещества на 100 моль соответствующего вещества.
Соединение, представленное формулой (1), которое используют в способе получения настоящего изобретения, может быть получено следующими способами.
Способ синтеза (I):
Формула 14
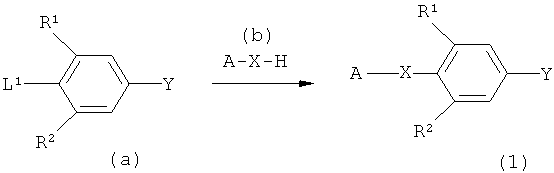
В реакционном уравнении, Х представляет собой атом кислорода; R1, R2, А и Y являются такими, как они обозначены в формуле (1); L1 представляет уходящую группу и включает атом галогена, метансульфонилоксигруппу трифторметансульфонилоксигруппу, пара-толуолсульфонилоксигруппу и тому подобное.
Конкретно, соединение, представленное формулой (1), может быть получено взаимодействием соединения (a) с соединением (b) в присутствии подходящего основания в подходящем растворителе, при подходящих температурных условиях.
Используемый растворитель не является особо ограниченным и включает, например, алифатические углеводороды (гексан, циклогексан, гептан и тому подобное), алифатические галогенированные углеводороды (дихлорметан, хлороформ, четыреххлористый углерод, дихлорэтан и тому подобное), ароматические углеводороды (бензол, толуол, ксилол, хлорбензол, мезитилен и тому подобное), простые эфиры (диэтиловый эфир, дибутиловый эфир, диметоксиэтан (DME), циклопентилметиловый эфир (CPME), тетрагидрофуран, диоксан и тому подобное), сложные эфиры (этилацетат, этилпропионат и тому подобное), амиды кислоты (диметилформамид (DMF), диметилацетамид (DMA), N-метилпирролидон (NMP) и тому подобное), нитрилы (ацетонитрил, пропионитрил и тому подобное), диметилсульфоксид (DMSO), вода, смешанные вышеуказанные растворители, и тому подобное.
Используемое основание включает, например, гидрид лития, гидрид натрия, гидрид калия, гидроксид натрия, карбонат натрия, карбонат калия, карбонат цезия, фторид калия, фторид цезия, трикалий фосфат, ацетат натрия, ацетат калия и тому подобное; металлическая соль C1 до C6 алкоксида (литиевая соль, натриевая соль и калиевая соль); C1 до C6 алкил анионная металлическая соль (литиевая соль, натриевая соль и калиевая соль); диизопропилэтиламин, трибутиламин, N-метилморфолин, диазабициклоундецен, диазабициклооктан, имидазол и тому подобное.
Например, синтез может быть проведен со ссылкой на ссылочный пример настоящего изобретения или "Bioorg. Med. Chem. Lett., 2004:14, pp.2547-2550," и т.д.
Способ синтеза (2):
Формула 15
В реакционном уравнении, Х представляет собой атом кислорода; R1, R2, А и Y являются такими, как они определены в формуле (1). Данная реакция может быть осуществлена при использовании реакции Мицунобу (Mitsunobu). Например, в присутствии диэтилазодикарбксилата (DEAD), диизопропилазодикарбоксилата (DIAD), 1,1'-(азодикарбонил)дипиперидина (ADDP), 1,1'-азобис(N,N-диметилформамид) (TMAD), или тому подобное, и в присутствии трифенилфосфина, трибутилфосфина или тому подобное, реакция может быть осуществлена в растворителе, таком как, тетрагидрофуран, диэтиловый эфир, 1,2-диметоксиэтан, дихлорметан, толуол или тому подобное, при температуре в пределах от 0°C до 150°C.
Соединение, представленное формулой (1), может быть получено реакцией, использующей реакцию Мицунобу (Mitsunobu) и похожими реакциями, описанными в Bull. Chem. Soc. Jpn., 1967:40, p.2380; Synthesis, 1981, p.1; и Org. React., 1992:42, p.335.
Кроме вышесказанного, соединение, представленное формулой (1) также может быть синтезировано с использованием существующих общих способов синтеза простого эфира. Например, синтез может быть выполнен согласно общим текстам учебников по синтезам органической химии, такие как Jikken Kagaku Koza 4th ed., No.20, "Organic Synthesis II Alcohol/Amine," Ed. Chemical Society of Japan (Maruzen Co., Ltd.), pp.187-205, и тому подобное.
Среди соединений, представленных формулой (2), соединения, содержащие тиазольное кольцо в качестве В, являются коммерчески доступными в некоторых случаях, но они могут быть синтезированы со ссылкой, например, на следующую схему:
Формула 16
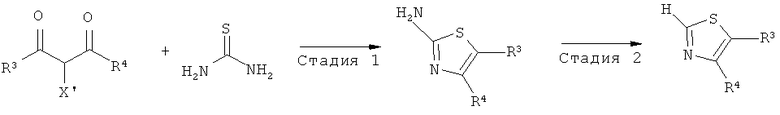
В реакционной схеме, описанной выше, R3 и R4 являются такими, как они определены в формуле (2) настоящего изобретения. X' представляет атом галогена.
Производное 2-аминотиазола в соответствии с реакцией циклизации тиазола стадии 1, может быть синтезировано согласно Pharmaceutical Chemistry Journal, 2007:41, pp.105-108; Pharmaceutical Chemistry Journal, 2001:35, pp.96-98; WO 2005/075435; WO 2005/026137; и тому подобное. Реакция стадии 2 может быть выполнена согласно Journal of Heterocyclic Chemistry, 1985:22, pp.1621-1630; Journal of the Chemical Society, Perkin Transactions 1: Organic and Bio-Organic Chemistry, 1982:1, pp.159-164; и Bioorganic & Medicinal Chemistry Letters, 2008:18, pp.6231-6235. Кроме того, производное тиазола, представленное формулой (2), может быть синтезировано согласно, например, на WO 2002/051849 и WO 2001/062250.
Среди соединений, представленных формулой (2), различные соединения, содержащие кольцо пиридина в качестве В, являются коммерчески доступными. Также как наличие в продаже, методы синтеза указанных соединений являются широко описанными и, таким образом, они могут быть синтезированы при использовании известных методов.
Среди соединений, представленных формулой (2), соединения, содержащие изоксазольное кольцо или изотиазольное кольцо [в формуле (2), W представляет атом кислорода или атом серы] являются коммерчески доступными в некоторых случаях. Однако они могут быть синтезированы согласно, например, способам, описанным в Tetrahedron Letters, 1968, pp.5209-5213; Synthesis, 1970, pp.344-350; Angewandte Chemie, 1967:79, pp.471-472; и Chemische Berichte, 1973:106, pp.3291-3311.
Примеры
Далее, настоящее изобретение будет описано конкретно, ссылаясь на примеры, и т.д. Однако следует понимать, что объем настоящего изобретения, не ограничен каким либо значением приведенных примеров.
В настоящих примерах, анализ и очистку выполнили с использованием следующего оборудования и ему подобного:
TCX (TLC): силикагель Е. Merck 60 F254 (0.25 мм)
Флэш колоночная хроматография: Biotage Flash, Si40
Препаративная тонкослойная хроматография ((ПТСХ)PTLC): силикагель Merck 60 F254 (1 мм)
Жидкостная хроматография/Масс спектрометрия (LC/MS):
Аналитическая система: SHIMAZU LCMS-2010A
Программное обеспечение: LCMS Solution
Экспериментальные условия:
Колонка: Phenomenex Gemini 3 мкм 4.6 мм ×30 мм
Скорость потока: 1.2 мл/мин
Температура измерения: 40°C
A-растворитель: 5% MeCN/95% H2O+0.05% ТФУК (TFA)
B-растворитель: 95% MeCN/5% H2O+0.05% ТФУК (TFA)
MS-метод: ESI+
ESI напряжение: 4.5 KV
Температура источника: 130°C
Температура десольватации: 320°C
Использована система двойной колонны
Ядерный магнитный резонанс (NMR): JEOL JNM-AL400 (1H 400 MHz)
Величина сдвига H-ЯМР представлена в м.д. относительно величины сдвига тетраметилсилана (δ 0.0 м.д.) в качестве стандарта. Данные представлены со следующими сокращениями:
s = синглет, d=дуплет, dd = двойной дуплет, t = триплет, q=квартет, m = мультиплет, br = расширенный сигнал.
Кроме того, в 1H-NMR спектре, в ссылочных примерах и примерах, протонный сигнал карбоновой кислоты может быть не установлен в некоторых случаях, в зависимости от условий измерения, таких как, растворитель и тому подобное.
Ссылочный пример 1
Синтез трет-бутил-4-метилтиазол-5-карбоксилата
Формула 17
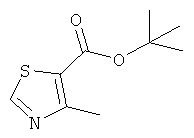
Смесь 4-метил-5-тиазолкарбоновой кислоты (1.36 г, 9,48 ммоль) и тионил хлорида (28,7 мл) перемешивали при 80°C в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении, удаляя тионил хлорид, и полученный сырой продукт сушили при пониженном давлении. К раствору полученного сырого вещества в дихлорметане (5,68 мл), добавляли трет-бутанол (2.84 мл) и пиридин (16,9 мл), и смесь перемешивали при 60°C всю ночь. После того, как реакция была завершена, реакционную смесь концентрировали при пониженном давлении. К полученному сырому материалу добавляли насыщенный водный раствор карбоната натрия и этил ацетата. После отделения этилацетата, выполняли экстракцию, снова добавляя этилацетат к насыщенному водному раствору бикарбоната натрия. Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. После удаления сульфата магния фильтрацией, растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали хроматографией на силикагеле (гексан/этилацетат=85/15) чтобы получить указанное в заголовке соединение (964 мг). Выход 51%.
1H-NMR (400 MHz, CDCl3): δ 8.72 (s, 1 H), 2.74 (s, 3H), 1.58 (s, 9 H).
Ссылочный пример 2
Синтез 5-йодо-2-изобутоксибензонитрил
Формула 18
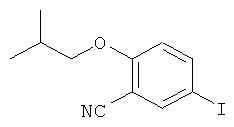
Раствор 2-метил-1-пропанола (0,56 мл, 6,06 ммоль) в N,N-диметилформамиде (10 мл) охлаждали до 0°C и добавляли к нему гидрид натрия (242 мг, 60% суспензия в минеральном масле, 6,06 ммоль) в маленьких порциях. Мутную реакционную смесь перемешивали при 0°C в течение 5 минут и температуру поднимали до 23°C. Затем, смесь перемешивали при комнатной температуре в течение 10 минут и снова охлаждали до 0°C. К реакционной смеси добавляли 2-фтор-5-йодбензонитрил (1,0 г, 4,04 ммоль) и затем, подогретую до комнатной температуры, реакционную смесь перемешивали в течение 1,5 часов. После того, как реакция была завершена, добавляли воду (20 мл) к реакционной смеси, которую экстрагировали этилацетатом (3×30 мл). Объединенные органические фазы, промывали насыщенным водным раствором хлорида натрия (3×30 мл) и затем, сушили над безводным сульфатом магния. После удаления сульфата магния фильтрацией, растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали хроматографией на силикагеле (гексан/этилацетат=98/2), чтобы получить названное в заголовке соединение (950 мг). Выход 78%.
1H-NMR (400 MHz, CDCl3): δ 7.81 (d, J=2.2 Hz, 1 H), 7.76 (dd, J=8.8 Hz, 2.2 Hz, 1H), 6.72 (d, J=8.8 Hz, 1 H), 3.80 (d, J=6.3 Hz, 2H), 2.21-2.11 (m, 1 H), 1.06 (d, J=6.8 Hz, 6 H).
Ссылочный пример 3
Синтез 5-бром-2-изобутоксибензонитрил
Формула 19
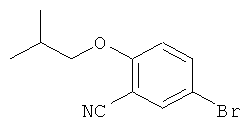
Суспензию гидрида натрия (1,46 г, 60% суспензия в минеральном масле, 37,5 ммоль) в N,N-диметилформамиде (50 мл) охлаждали до 0°C и затем, 2-метил-1-пропанол (3,47 мл, 37,5 ммоль) добавляли в маленьких порциях. Реакционную смесь перемешивали при комнатной температуре в течение 20 минут. Смесь охлаждали снова до 0°C, 2-фтор-5-бромбензонитрил (5,00 г, 25,0 ммоль) добавляли к смеси в маленьких порциях и затем, реакционную смесь перемешивали при комнатной температуре в течение 15 часов. После того как реакция была завершена, воду (100 мл) добавляли к реакционной смеси, которую затем экстрагировали этилацетатом (3×100 мл). Органические фазы объединяли, промывали насыщенным водным раствором хлорида натрия (2×50 мл), и затем, сушили над безводным сульфатом натрия. После удаления сульфата натрия фильтрацией, растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали хроматографией на силикагеле (гексан/этилацетат=9/1), чтобы получить указанное в заголовке соединение (6.04 г). Выход 95%.
1H-NMR (400MHz, CDCl3): δ 7.65 (d, J=2.4 Hz, 1 H), 7.60 (d, J=9.0 Hz, 2.4 Hz, 1 H), 6.84 (d, J=8.8 Hz, 1 H), 3.81 (d, J=6.6 Hz, 2H), 2.22-2.12 (m, 1 H), 1.06 (d, J=6.6 Hz, 6 H).
Пример 1
Синтез трет-бутил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилат
Формула 20

где mol% CuI - мол.% CuI; 2.0 equiv tert-BuOLi - 2,0 эквив. трет-BuOLi; DMF - ДМФА; min - мин.; Y. - Выход
В реакционный сосуд добавляли трет-бутил-4-метилтиазол-5-карбоксилат (49,8 мг, 0,25 ммоль), полученный в ссылочном примере 1, 5-йод-2-изобутоксибензонитрил (112,9 мг, 0,375 ммоль), полученный в ссылочном примере 2 и безводный N,N-диметилформамид (1,25 мл). После добавления трет-бутоксилития (40,0 мг, 0,5 ммоль) и йодида меди(I) (9,5 мг, 0,05 ммоль) к смеси в атмосфере азота, реакционную смесь нагревали до 140°C и перемешивали в течение 30 минут. После того как реакция была завершена, реакционную смесь охлаждали до комнатной температуры. Воду добавляли к реакционной смеси, которую затем экстрагировали этилацетатом. Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия и сушили над сульфатом магния. После удаления сульфата магния фильтрацией, органический растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали тонкослойной хроматографией на силикагеле (гексан/этилацетат=4/1), чтобы получить указанное в заголовке соединение (29,2 мг). Выход 31%.
1H-NMR (400MHz, CDCl3): δ 8.16 (d, J=2.4 Hz, 1 H), 8.08 (dd, J=8.8 Hz, 2.4 Hz, 1 H), 7.00 (d, J=8.8 Hz, 1 H), 3.89 (d, J=6.8 Hz, 2 H), 2.73 (s, 3 H), 2.24-2.16 (m, 1 H), 1.59 (s, 9 H), 1.09 (d, J=6.8 Hz, 6 H).
Пример 2
Синтез трет-бутил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилат
Формула 21

где mol% - мол.%; equiv - эквив.; hr - час.; Y. - Выход
В реакционный сосуд добавляли трет-бутил-4-метилтиазол-5-карбоксилат (49,8 мг, 0,25 ммоль), полученный в ссылочном примере 1, 5-йод-2-изобутоксибензонитрил (112,9 мг, 0,375 ммоль), полученный в ссылочном примере 2 и воду (0.5 мл). В атмосфере азота, комплекс хлорида палладия (II) с бидентатным 1,Г-бис(дифенилфосфино)ферроценом [PdCl2(dppf)] (20,7 мг, 0,025 ммоль), трифенилфосфин (39,3 мг, 0,15 ммоль) и карбонат серебра (138,4 мг, 0,5 ммоль) добавляли и затем, реакционную смесь нагревали до 60°C и перемешивали в течение 24 часов. После того как реакция была завершена, реакционную смесь охлаждали до комнатной температуры. Этилацетат (2,5 мл) добавляли к реакционной смеси, и нерастворимое вещество отделяли фильтрацией и фильтрат промывали этилацетатом. Фильтрат экстрагировали этилацетатом дважды. Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия и высушивали над сульфатом магния. После удаления сульфата магния фильтрацией, органический растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали тонкослойной хроматографией на силикагеле (гексан/этилацетат=3/1), чтобы получить названное в заголовке соединение (87,6 мг). Выход 94%.
1H-NMR (400MHz, CDCl3): δ 8.16 (d, J=2.4 Hz, 1 H), 8.08 (dd, J=8.8 Hz, 2.4 Hz, 1 H), 7.00 (d, J=8.8 Hz, 1H), 3.89 (d, J=6.8 Hz, 2 H), 2.73 (s, 3 H), 2.24-2.16 (m, 1 H), 1.59 (s, 9 H), 1.09 (d, J=6.8 Hz, 6 H).
Пример 3
Синтез трет-бутил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилат
Формула 22

где mol% - мол.%; equiv - эквив.; toluene - толуол; hr - час.; Y. - Выход
В тестовый трубчатый реакционный сосуд (50 мл) добавляли трет-бутил-4-метилтиазол-5-карбоксилат (598 мг, 3,0 ммоль), полученный в ссылочном примере 1, 5-бром-2-изобутоксибензонитрил (762 мг, 3,0 ммоль), полученный в ссылочном примере 3, ацетат палладия (67,4 мг, 0,30 ммоль), три(циклогексил)фосфин (168 мг, 0,60 ммоль), карбонат цезия (1,95 г, 6,0 ммоль) и толуол (11 мл). Затем, реакционный сосуд заполняли азотом, нагревали до 120°C в условиях герметической изоляции и реакционную смесь перемешивали в течение 19 часов. После того, как реакция была завершена, этилацетат (30 мл) добавляли к реакционной смеси и нерастворимое вещество удаляли фильтрацией. К фильтрату добавляли 0,1 моль/л соляной кислоты (20 мл) и органическую фазу экстрагировали и отделяли. Далее, водную фазу экстрагировали этилацетатом (20 мл). Объединенные органические фазы промывали водой (30 мл) и насыщенным водным раствором хлорида натрия (30 мл) и сушили над сульфатом натрия. После удаления сульфата натрия фильтрацией, органический растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали хроматографией с силикагелем (гексан/этилацетат=7/1), чтобы получить указанное в заголовке соединение (930 мг). Выход 83%.
1H-NMR (400 MHz, CDCl3): δ 8.16 (d, J=2.44 Hz, 1 H), 8.08 (dd, J=8.78 Hz, 2.20 Hz, 1 H), 7.00 (d, J=8.78 Hz, 1 H), 3.90 (d, J=6.59 Hz, 2H), 2.73 (s, 3 H), 2.25-2.16 (m, 1 H), 1.59 (s, 9 H),1.09(d, J=6.83 Hz, 6 H).
Пример 4
Синтез трет-бутил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилата
Формула 23

где mol% - мол.%; equiv - эквив.; hr - час.; Y. - Выход
В тестовый трубчатый реакционный сосуд добавляли трет-бутил-4-метилтиазол-5-карбоксилат (180 мг, 0,903 ммоль), полученный в ссылочном примере 1, 5-бром-2-изобутоксибензонитрил (230 мг, 0,903 ммоль), полученный в ссылочном примере 3, гидроксид палладия (31,7 мг, 0,045 ммоль), три(циклогексил)фосфин (12,7 мг, 0,045 ммоль), карбонат калия (250 мг, 1,81 ммоль), йодид меди (172 мг, 0,903 ммоль) и диметилсульфоксид (3,0 мл). Затем реакционный сосуд заполняли азотом, нагревали до 120°C в условиях герметичной изоляции и реакционную смесь перемешивали в течение 20 часов. После того, как реакция была завершена, этилацетат (10 мл) и воду (10 мл) добавляли к реакционной смеси и полученную в результате смесь перемешивали при комнатной температуре в течение 30 минут. Раствор отфильтровывали через Celite и указанный слой Celite промывали этилацетатом (20 мл) и водой (10 мл). Органическую фазу отделяли от фильтрата и водную фазу экстрагировали дополнительно этилацетатом (20 мл). Объединенные органические фазы промывали насыщенным водным раствором хлорида натрия (10 мл) и сушили над сульфатом натрия. После удаления сульфата натрия фильтрованием, органический растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали хроматографией с силикагелем (гексан/этилацетат=49/1 до 4/1), чтобы получить сырой продукт, указанного в заголовке соединения (188 мг). После растворения продукта снова в этаноле (3 мл) при нагревании (80°C), раствор охлаждали до 10°C и осажденное твердое вещество отделяли фильтрованием и промывали этанолом (2 мл). Твердое вещество сушили при комнатной температуре при пониженном давлении, чтобы получить указанное в заголовке соединение (132 мг). Выход 39%.
1H-NMR (400MHz, CDCl3): δ 8.17 (d, J=2.20Hz, 1H), 8.08 (dd, J=8.90Hz, 2.32Hz, 1H), 7.00 (d, J=9.02Hz, 1H), 3.90 (d, J=6.59Hz, 2H), 2.73 (s, 3H), 2.24-2.15 (m, 1H), 1.59 (s, 9H),1.09(d, J=6.83Hz, 6H).
Пример 5
Синтез трет-бутил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилат
Формула 24
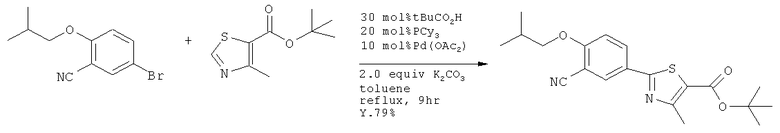
где mol% - мол.%; equiv - эквив.; toluene - толуол; reflux - кипячение с обратным холодильником; hr - час.; Y. - Выход
В реакционный сосуд добавляли трет-бутил-4-метилтиазол-5-карбоксилат (598 мг, 3,0 ммоль), полученный в ссылочном примере 1, 5-бром-2-изобутоксибензонитрил (762 мг, 3,0 ммоль), полученный в примере 3, ацетат палладия (67,4 мг, 0,30 ммоль), три(циклогексил)фосфин (168 мг, 0,60 ммоль), карбонат калия (829 мг, 6,0 ммоль), толуол (10 мл) и пивалевую кислоту (92 мг, 0,90 ммоль). Затем, реакционную смесь перемешивали при комнатной температуре в течение 30 минут в атмосфере азота, и в течение дополнительных 9 часов кипятили с обратным холодильником. После того, как реакция была завершена, воду (20 мл) и этилацетат (20 мл) добавляли к реакционной смеси и органическую фазу экстрагировали и отделяли. Далее, водную фазу экстрагировали этилацетатом (20 мл). Объединенные органические фазы сушили над сульфатом магния. После удаления сульфата магния фильтрацией, органический растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали хроматографией с силикагелем (гексан/этилацетат=100/0 до 0/100), чтобы получить указанное в заголовке соединение (880 мг). Выход 79%.
1H-NMR (400MHz, CDCl3): δ 8.16 (d, J=2.20 Hz, 1 H), 8.08 (dd, J=8.78 Hz, 2.20 Hz, 1 H), 7.00 (d, J=8.78 Hz, 1 H), 3.90 (d, J=6.34 Hz, 2 H), 2.73 (s, 3 H), 2.25-2.15 (m, 1 H), 1.59 (s, 9 H), 1.09 (d, J=6.59 Hz, 6 H).
Пример 6
Синтез этил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилат
Формула 25
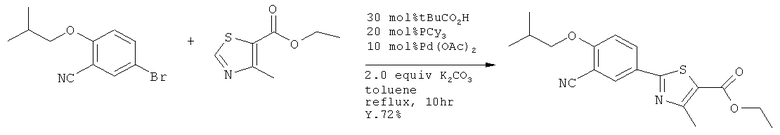
где mol% - мол.%; equiv - эквив.; toluene - толуол; reflux - кипячение с обратным холодильником; hr - час.; Y. - Выход
В реакционный сосуд добавляли этил-4-метилтиазол-5-карбоксилат (514 мг, 3,0 ммоль), 5-бром-2-изобутоксибензонитрил (762 мг, 3,0 ммоль), полученный в примере 3, ацетат палладия (67,4 мг, 0,30 ммоль), три(циклогексил)фосфин (168 мг, 0,60 ммоль), карбонат калия (829 мг, 6,0 ммоль), толуол (10 мл) и пивалевую кислоту (92 мг, 0,90 ммоль). Затем, реакционную смесь перемешивали при комнатной температуре в течение 30 минут в атмосфере азота, и в течение дополнительных 10 часов нагревали с обратным холодильником. После того, как реакция была завершена, воду (20 мл) и этилацетат (20 мл) добавляли к реакционной смеси и органическую фазу экстрагировали и отделяли. Далее, водную фазу экстрагировали этилацетатом (20 мл). Объединенные органические фазы сушили над сульфатом магния. После удаления сульфата магния фильтрацией, органический растворитель концентрировали при пониженном давлении. Полученный сырой продукт очищали хроматографией с силикагелем (гексан/этилацетат=100/0 до 0/100), чтобы получить указанное в заголовке соединение (734 мг). Выход 71%.
1H-NMR (400MHz, CDCl3): δ 8.18 (d, J=2.44 Hz, 1 H), 8.09 (dd, J=8.78 Hz, 2.20 Hz, 1 H), 7.01 (d, J=8.78 Hz, 1 H), 4.36 (q, J=7.07 Hz, 2 H), 3.90 (d, J=6.34 Hz, 2 H), 2.77 (s, 3 H), 2.26-2.16 (m, 1 H), 1.39 (t, J=7.19 Hz, 3 H), 1.09 (d, J=6.83 Hz, 6 H).
Пример 7
Синтез трет-бутил-2-(3-циано-4-изобутилфенил)-4-метилтиазол-5-карбоксилат
Формула 26
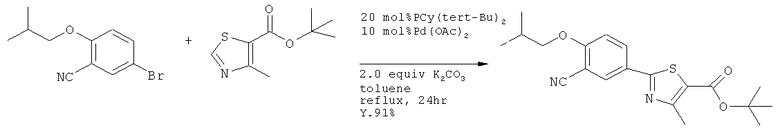
где mol% - мол.%; equiv - эквив.; toluene - толуол; reflux - кипячение с обратным холодильником; hr - час.; Y. - Выход
В реакционный сосуд добавляли трет-бутил-4-метилтиазол-5-карбоксилат (598 мг, 3,0 ммоль), полученный в ссылочном примере 1, 5-бром-2-изобутоксибензонитрил (801 мг, 3,15 ммоль), полученный в ссылочном примере 3, ацетат палладия (67,4 мг, 0,30 ммоль), ди(трет-бутил)циклогексилфосфин (137 мг, 0,60 ммоль), карбонат калия (829 мг, 6,0 ммоль) и толуол (10 мл). Затем, реакционную смесь перемешивали при комнатной температуре в течение 30 минут и в течение дополнительных 24 часов, в атмосфере азота, нагревали с обратным холодильником. После того, как реакция была завершена, воду (15 мл) и этилацетат (20 мл) добавляли к реакционной смеси и органическую фазу экстрагировали и отделяли. Далее, водную фазу экстрагировали этилацетатом (20 мл). Объединенные органические фазы сушили над сульфатом магния. После удаления сульфата магния фильтрацией, органический растворитель концентрировали при пониженном давлении, чтобы получить сырой продукт. После растворения сырого продукта при добавлении толуола (1 мл) и нагревании до 70°C, добавляли гептан (9 мл) при 70°C и полученную в результате смесь оставляли охлаждаться до комнатной температуры, и затем охлаждали до 0°C.Осажденное твердое вещество отделяли фильтрацией, промывали гептаном (20 мл), чтобы получить, указанное в заголовке соединение (611 мг, 1,64 ммоль). Далее, фильтрат концентрировали при пониженном давлении и, полученный сырой продукт очищали хроматографией с силикагелем (гексан/этилацетат=100/0 до 0/100), чтобы получить указанное в заголовке соединение (405 мг, 1,09 ммоль). Выход 91%.
1H-NMR (400MHz, CDCl3): δ 8.17(d, J=2.20Hz, 1H), 8.09 (dd, J=8.90 Hz, 2.32 Hz, 1 H), 7.00 (d, J=8.78 Hz, 1 H), 3.90 (d, J=6.34 Hz, 2 H), 2.73 (s, 3H), 2.24-2.17 (m, 1H), 1.59 (s, 9H), 1.09 (d, J=6.83 Hz, 6 H).
Пример 8
Синтез этил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилат
Формула 27
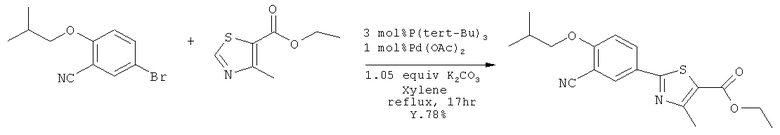
где mol% - мол.%; equiv - эквив.; Xylene - ксилол; reflux - кипячение с обратным холодильником; hr - час.; Y. - Выход
В реакционный сосуд добавляли этил-4-метилтиазол-5-карбоксилат (1,71 г, 10,0 ммоль), 5-бром-2-изобутоксибензонитрил (2,54 мг, 10,0 ммоль), полученный в ссылочном примере 3, ацетат палладия (22,4 мг, 0,10 ммоль), соль тетрафторборной кислоты три(трет-бутил)фосфина (87,0 мг, 0,30 ммоль), карбонат калия (1,45 г, 10,5 ммоль) и ксилол (10 мл). Затем, реакционную смесь перемешивали при комнатной температуре в течение 30 минут и в течение дополнительных 17 часов в атмосфере азота нагревали с обратным холодильником. После того, как реакция была завершена, реакционную смесь отфильтровывали еще горячей и фильтрационный слой промывали толуолом и дихлорметаном. Фильтрат концентрировали при пониженном давлении и полученный сырой продукт очищали, чтобы получить указанное в заголовке соединение (2,69 г). Выход 78%.
1H-NMR (400 MHz, CDCl3): δ 8.18 (d, J=2.44 Hz, 1 H), 8.09 (dd, J=8.78 Hz, 2.20 Hz, 1 H), 7.01 (d, J=8.78 Hz, 1 H), 4.36 (q, J=7.07 Hz, 2 H), 3.90 (d, J=6.34 Hz, 2H), 2.77 (s, 3 H), 2.26-2.16 (m, 1 H), 1.39 (t, J=7.19 Hz, 3 H), 1.09 (d, J=6.83 Hz, 6 H).
Пример 9
Синтез этил-2(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилат
Формула 28
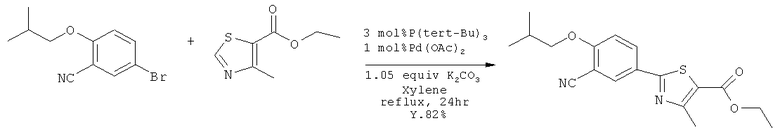
где mol% - мол.%; equiv - эквив.; Xylene - ксилол; reflux - кипячение с обратным холодильником; hr - час.; Y. - Выход
В реакционный сосуд добавляли этил-4-метилтиазол-5-карбоксилат (1,71 г, 10,0 ммоль), 5-бром-2-изобутоксибензонитрил (2,69 мг, 10,5 ммоль), полученный в ссылочном примере 3, ацетат палладия (22,4 мг, 0,10 ммоль), ди(трет-бутил)циклогексилфосфина (68,5 мг, 0,30 ммоль), карбонат калия (1,45 г, 10,5 ммоль) и ксилол (10 мл). Затем, реакционную смесь перемешивали при комнатной температуре в течение 30 минут и в течение дополнительных 24 часов в атмосфере азота нагревали с обратным холодильником. После того, как реакция была завершена, реакционную смесь фильтровали еще горячей и фильтрационный слой промывали толуолом и дихлорметаном. Фильтрат концентрировали при пониженном давлении и полученный сырой продукт очищали, чтобы получить указанное в заголовке соединение (2,83 г). Выход 82%.
1H-NMR (400 MHz, CDCl3): δ 8.18 (d, J=2.44 Hz, 1 H), 8.09 (dd, J=8.78 Hz, 2.20 Hz, 1 H), 7.01 (d. J=8.78 Hz, 1 H), 4.36 (q, J=7.07 Hz, 2 H), 3.90 (d, J=6.34 Hz, 2 H), 2.77 (s, 3 H), 2.26-2.16 (m, 1 H), 1.39 (t, J - 7.19 Hz, 3 H), 1.09 (d, J=6.83 Hz, 6 H).
Пример 10
Синтез трет-бутил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилата
Формула 29
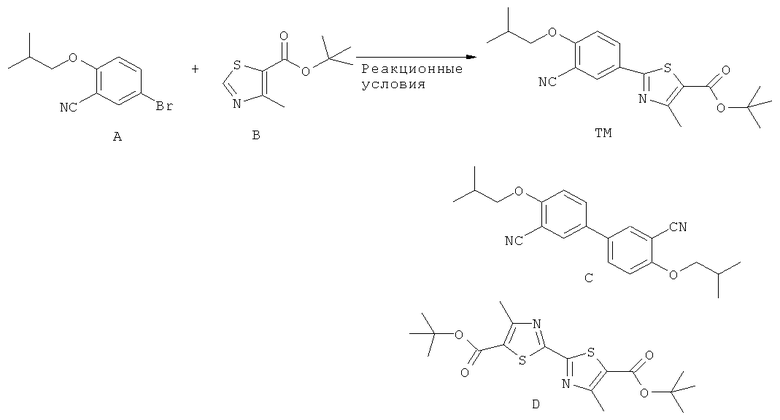
В тестовый трубчатый реакционный сосуд (10 мл) добавляли трет-бутил-4-метилтиазол-5-карбоксилат (59,8 мг, 0,3 ммоль), полученный в ссылочном примере 1, 5-бром-2-изобутоксибензонитрил (76,2 мг, 0,3 ммоль), полученный в ссылочном примере 3, ацетат палладия (6,7 мг, 0,030 ммоль), лиганд, основание (0,60 ммоль) и растворитель (1 мл). Затем, реакционный сосуд заполняли азотом, нагревали до 120°C в условиях герметической изоляции, и реакционную смесь перемешивали. После того, как реакция была завершена, часть реакционной смеси разбавляли ДМСО и полученный раствор измеряли ВЭЖХ. Общий % площади ВЭЖХ соединений А до D и ТМ был определен как 100% и расчетный выход целевого вещества был рассчитан из % площади ВЭЖХ целевого вещества. Вычисление расчетного выхода целевого вещества из % площади ВЭЖХ осуществляли определением соответствующих значений в следующей формуле вычисления.
Выход ТМ (%)=общее количество ТМ (моль)/[{общее количество В (моль)+общее количество D (моль) × 2+общее количество ТМ (моль)}/2+{общее количество A (моль) + общее количество (C) × 2+общее количество ТМ (моль)}/2] × 100
Общее количество каждого соединения (моль)=значение площади ВЭЖХ (mAU)/ значение площади ВЭЖХ на моль каждого соединения (mAU/моль)
Высокоэффективная жидкостная хроматография:
Аналитическая система: G1315A Hewlett Packard Series 1100
Программное обеспечение: ChemStation for LC 3D
Экспериментальные условия:
Колонка: Imtakt Cadenza CD-C18 4.6×100 мм
Поток: 1.0 мл/мин
Длина волны: 254 нм
Температура: 40°C
A-растворитель: 5% MeCN/95% H2O+0.05% TFA (ТФУК)
B-растворитель: 95% MeCN/5% H2O+0.05% TFA (ТФУК)
Градиент:
0-1 мин 10% B-растворитель
1-7 мин 10-50% B-растворитель
7-14 мин 0-80% B-растворитель
14-16 мин 80-100% B-растворитель
16-20 мин 100% B-растворитель
20-22 мин 100-10% B-растворитель
22-25 мин 10% B-растворитель
Результаты в настоящем примере показывают следующее.
Таблица 9
Эксперимент No.
Реакционные условия
Растворитель
Основание
Лиганд
Добавка
Температура
Время реакции
Вычисленный выход
Сокращения в таблице обозначают следующее:
DME: Диметоксиэтан
NMP: N-метилпирролидон
EA: Этилацетат
CPME: Циклопентилметиловый эфир
HBF4: Тетрафторборная кислота
dppp: 1,1'-бис(дифенилфосфино)пропан
dppe: 1,1'-бис(дифенилфосфино)этан
dppb: 1,1'-бис(дифенилфосфино)бутан
dppf: 1,1'-бис(дифенилфосфино)ферроцен
PCy3: Трициклогексилфосфин
PivOH: Пивалевая кислота n-Oct.: н-октил
Пример 11
Синтез этил-2-(3-циано-4-изобутоксифенил)-4-метилтиазол-5-карбоксилат
Формула 30
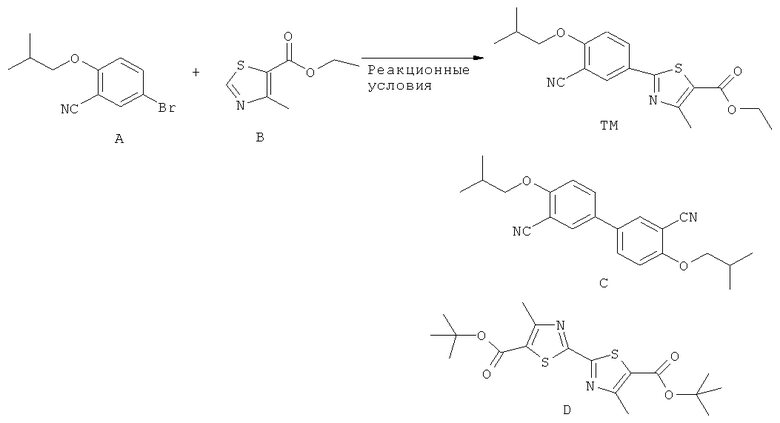
В тестовый трубчатый реакционный сосуд (10 мл) добавляли этил-4-метилтиазол-5-карбоксилат (85,5 мг, 0,5 ммоль), 5-бром-2-изобутоксибензонитрил (127,1 мг, 0,5 ммоль), полученный в ссылочном примере 3, разновидность палладия, лиганд, основание (1,0 ммоль), добавку (0,15 ммоль) и растворитель (1,7 мл). Затем реакционный сосуд заполняли азотом, нагревали до 120°C в условиях герметической изоляции и реакционную смесь перемешивали. После того, как реакция была завершена, часть реакционной смеси разбавляли ДМСО и полученный раствор измеряли ВЭЖХ. Общий % площади ВЭЖХ соединений А до D и ТМ был определен как 100%, и вычисленный выход целевого вещества вычислили из % площади ВЭЖХ целевого материала. Результаты представлены в таблице 10.
Высокоэффективная жидкостная хроматография:
Аналитическая система: G1315A Hewlett Packard Series 1100
Программное обеспечение: ChemStation for LC 3D
Экспериментальные условия:
Колонка: Phenomenex Luna Phenyl-Hexyl Sum 4.6×100 mm
Поток: 1.0 мл/мин
Длина волны: 240 нм
Температура: 40°C
A-Растворитель: 5%MeCN/95%H2O+0.05%TFA (ТФУК)
B-растворитель: 95%MeCN/5%H2O+0.05%TFA (ТФУК)
Градиент:
0-1 мин 10% B-растворитель
1-14 мин 10-70% B-растворитель
14-24 мин 70-80% B-растворитель
24-25 мин 80-100% B-растворитель
25-30 мин 100% B-растворитель
30-32 мин 100-10% В-растворитель
32-35 мин 10% B-растворитель
Таблица 10
Эксперимент No.
Реакционные условия
Растворитель
Основание
Лиганд
Добавка
Температура
Время реакции
Вычисленный выход
Сокращения в таблице обозначают следующее:
AcOH: уксусная кислота
EtCO2H: пропионовая кислота
i-PrCO2H: 2-метилпропановая кислота
Пример 12
Синтез этил-2-(3-циано-4-изобутоксифенил')-4-метилтиазол-5-карбоксилата
Формула 31
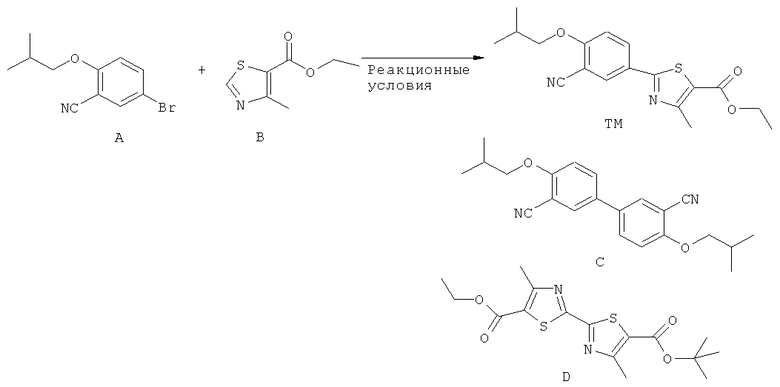
В трубчатый реакционный сосуд (20 мл) добавляли этил-4-метилтиазол-5-карбоксилат (381,2 мг, 1,5 ммоль), 5-бром-2-изобутоксибензонитрил (256,8 мг, 1,5 ммоль), полученный в ссылочном примере 3, ацетат палладия (6,7 мг, 0,030 ммоль), ди(трет-бутил)циклогексилфосфин (13,7 мг, 0,060 ммоль), карбонат калия (414,6 мг, 3,0 ммоль), добавку (0,45 ммоль) и ксилол (5,0 мл). Затем реакционный сосуд заполняли азотом, нагревали до 120°C в условиях герметической изоляции и реакционную смесь перемешивали в течение 5 часов. После того, как реакция была завершена, часть реакционной смеси разбавляли ДМСО и полученный раствор измеряли ВЭЖХ. Общий % площади ВЭЖХ соединений А до D и ТМ был определен как 100%, и вычисленный выход целевого вещества был вычислен из % площади ВЭЖХ целевого материала. Результаты представлены в таблице 11.
Высокоэффективная жидкостная хроматография:
Аналитическая система: G1315A Hewlett Packard Series 1100
Программное обеспечение: ChemStation for LC 3D
Экспериментальные условия:
Колонка: Phenomenex Luna Phenyl-Hexyl 5 um 4.6×100 mm
Поток: 1.0 mL/min
Длина волны: 240 нм
Температура: 40°C
A-растворитель: 5% MeCN/95% H2O+0.05% TFA (ТФК)
B-растворитель: 95% MeCN/5% H2O+0.05% TFA (ТФК)
Градиент:
0-1 мин 10% В-растворитель
1-14 мин 10-70% B-растворитель
14-24 мин 70-80% B-растворитель
24-25 мин 80-100% B-растворитель
25-30 мин 100% B-растворитель
30-32 мин 100-10% B-растворитель
32-35 мин 10% B-растворитель
Таблица 11
Эксперимент No.
Реакционные условия
Растворитель
Основание
Лиганд
Добавка
Температура
Время реакции
Вычисленный выход
Сокращения в таблице обозначают следующее:
CyPrCO2H: циклопропанкарбоновая кислота
tetraMeCyPrCO2H: 2,2,3,3-тетраметилциклопропанкарбоновая кислота
CyPnCO2H: циклопентанкарбоновая кислота
1-ad-CO2H: 1-адамантанкарбоновая кислота
CyPenteneCO2H: 3-циклопентенкарбоновая кислота
3-THFCO2H: тетрагидрофуран-3-карбоновая кислота
Промышленная применимость
Новый способ сочетания настоящего изобретения, где производное фенила, представленное формулой (1) и гетероциклическое производное, представленное формулой (2) сочетают в присутствии соединения переходного металла, чтобы получить фенил-замещенное гетероциклическое производное, представленное формулой (3), применяют для получения ингибитора ксантин оксидазы, который представляет собой терапевтический агент при гиперурикемии, или его промежуточного соединения, в способе, включающим небольшое количество стадий и следовательно, с высоким выходом и низкой стоимостью.


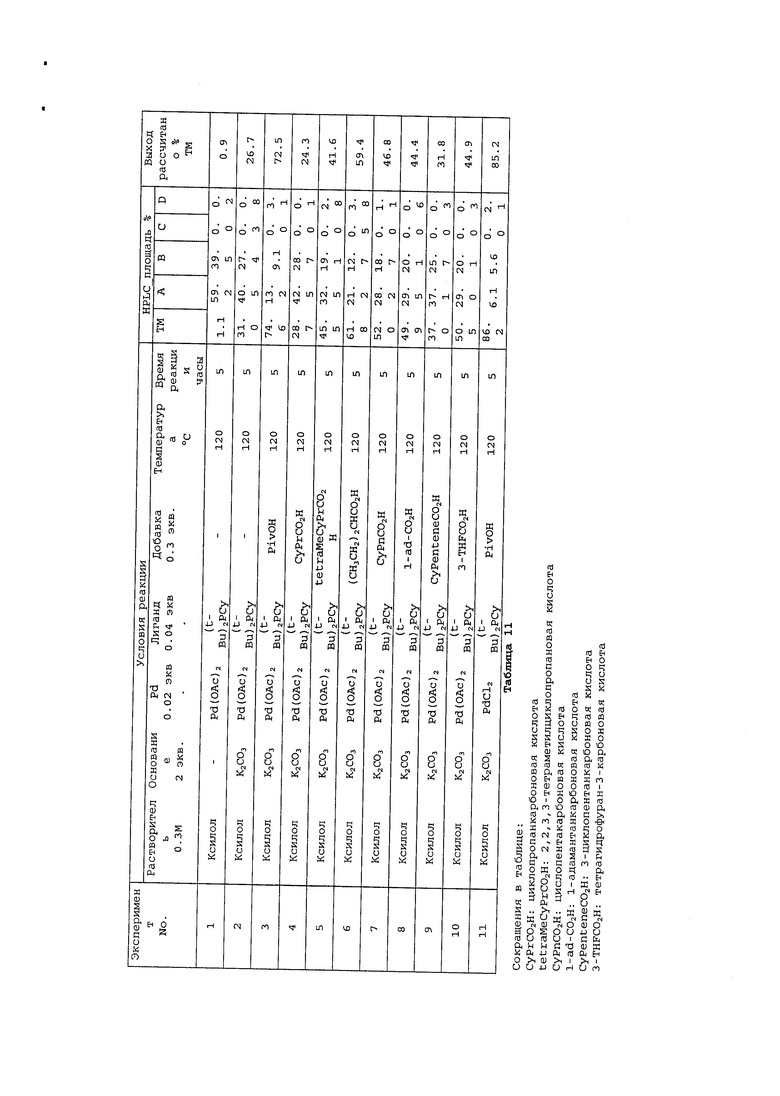
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛЗАМЕЩЕННОГО ГЕТЕРОЦИКЛИЧЕСКОГО ПРОИЗВОДНОГО ПОСРЕДСТВОМ СПОСОБА СОЧЕТАНИЯ С ИСПОЛЬЗОВАНИЕМ СОЕДИНЕНИЯ ПАЛЛАДИЯ | 2011 |
|
RU2563459C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2006 |
|
RU2382781C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-ФЕНИЛПИРАЗОЛ-1-КАРБОКСАМИДОВ | 2005 |
|
RU2397165C2 |
| ПРОИЗВОДНЫЕ АМИДИНОФЕНИЛАЛАНИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРОИЗВОДНЫЕ АМИДИНОФЕНИЛАЛАНИНА, ОБЛАДАЮЩИЕ АНТИКОАГУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1992 |
|
RU2088591C1 |
| ФАРМАЦЕВТИЧЕСКОЕ СОЕДИНЕНИЕ | 2015 |
|
RU2719446C2 |
| ПРОИЗВОДНЫЕ АМИДОВ ПИРАЗОЛГЛИКОЛЕВОЙ КИСЛОТЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1992 |
|
RU2090560C1 |
| СПОСОБ ПОЛУЧЕНИЯ [(3-ГИДРОКСИПИРИДИН-2-КАРБОНИЛ)АМИНО]АЛКАНОВЫХ КИСЛОТ, СЛОЖНЫХ ЭФИРОВ И АМИДОВ | 2012 |
|
RU2602083C2 |
| СПОСОБ ПОЛУЧЕНИЯ [(3-ГИДРОКСИПИРИДИН-2-КАРБОНИЛ)АМИНО]АЛКАНОВЫХ КИСЛОТ, СЛОЖНЫХ ЭФИРОВ И АМИДОВ | 2012 |
|
RU2764667C2 |
| ЗАМЕЩЕННОЕ АНИЛИДНОЕ ПРОИЗВОДНОЕ ПИРАЗОЛКАРБОНОВОЙ КИСЛОТЫ ИЛИ ЕГО СОЛЬ, ЕГО ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ, АГЕНТ ДЛЯ ПРИМЕНЕНИЯ В СЕЛЬСКОМ ХОЗЯЙСТВЕ И САДОВОДСТВЕ И ЕГО ПРИМЕНЕНИЕ | 2006 |
|
RU2375348C1 |
| ФТОРАЛКИЛИРУЮЩИЙ АГЕНТ | 2015 |
|
RU2716008C2 |
Изобретение относится к способу, включающему взаимодействие соединения, представленного следующей формулой (1), где R1 представляет собой атом водорода или атом галогена; R2 представляет собой атом водорода, цианогруппу, нитрогруппу, атом галогена, формильную группу или галогенметильную группу; A представляет собой атом водорода, C1-C8 алкильную группу, C3-C6 циклоалкильную группу, фенильную группу, атом фтора (только когда X представляет собой связь), или защитную группу для гидроксильной группы (только когда X представляет собой атом кислорода), где A может быть замещено от 1 до 3 заместителями, такой заместитель, представляющий группу, выбран из группы, состоящей из атома галогена, С1-C4 алкильной группы, C1-C4 алкоксигруппы, C1-C4 алкилтиогруппы, C3-C6 циклоалкильной группы, фенильной группы, феноксигруппы и пиридильной группы; X представляет собой связь (только когда A представляет собой фенильную группу или атом фтора) или атом кислорода; и Y представляет собой уходящую группу и соединения, представленного следующей формулой (2): H представляет атом водорода; R3 представляет собой COOR3a или COR3b; R3a представляет собой атом водорода, C1-C4 алкильную группу или защитную группу сложноэфирного типа для карбоксильной группы; R3b представляет собой защитную группу амидного типа для карбоксильной группы, защитную группу образующую амид с соседней карбонильной группой; R4 представляет собой атом водорода, атом галогена или C1-C4 алкильную группу; в присутствии соединения переходного металла, выбранного из группы, состоящей из палладия нулевой валентности и соли моно- и дивалентного палладия и (n) лиганда фосфинового типа, способного к координированию соединения переходного металла, чтобы получить фенил-замещенное гетероциклическое производное, представленное следующей формулой (3), где A, X, R1 и R3 являются такими, как определено в формуле (1); и R3 и R4 являются такими, как определено в формуле (2). Технический результат - способ получения фенил-замещенного гетероциклического производного с небольшим количеством стадий, высоким выходом и низкой стоимостью. 16 з.п. ф-лы, 11 табл., 15 пр.
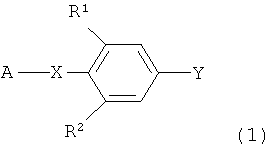
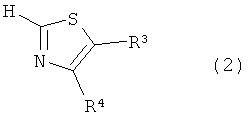
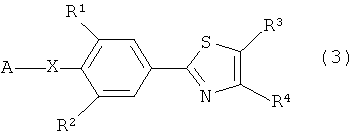
1. Способ, включающий взаимодействие соединения, представленного следующей формулой (1):

где R1 представляет собой атом водорода или атом галогена; R2 представляет собой атом водорода, цианогруппу, нитрогруппу, атом галогена, формильную группу или галогенметильную группу; A представляет собой атом водорода, C1-C8 алкильную группу, C3-C6 циклоалкильную группу, фенильную группу, атом фтора (только когда X представляет собой связь), или защитную группу для гидроксильной группы (только когда X представляет собой атом кислорода), где A может быть замещено от 1 до 3 заместителями, такой заместитель, представляющий группу, выбран из группы, состоящей из атома галогена, C1-C4 алкильной группы, C1-C4 алкоксигруппы, C1-C4 алкилтиогруппы, C3-C6 циклоалкильной группы, фенильной группы, феноксигруппы и пиридильной группы; X представляет собой связь (только когда A представляет собой фенильную группу или атом фтора) или атом кислорода; и Y представляет собой уходящую группу и соединения, представленного следующей формулой (2):

H представляет атом водорода;
R3 представляет собой COOR3a или COR3b; R3a представляет собой атом водорода, C1-C4 алкильную группу или защитную группу сложноэфирного типа для карбоксильной группы; R3b представляет собой защитную группу амидного типа для карбоксильной группы, защитную группу образующую амид с соседней карбонильной группой; R4 представляет собой атом водорода, атом галогена или C1-C4 алкильную группу;
в присутствии соединения переходного металла, выбранного из группы, состоящей из палладия нулевой валентности и соли моно- и дивалентного палладия и
(ii) лиганда фосфинового типа, способного к координированию соединения переходного металла
чтобы получить фенилзамещенное гетероциклическое производное, представленное следующей формулой (3):

где A, X, R1 и R2 являются такими, как определено в формуле (1); и
R3 и R4 являются такими как определено в формуле (2).
2. Способ по п.1, где A представляет C1-C5 алкильную группу.
3. Способ по п.1, где A представляет изобутильную группу.
4. Способ по п.1, где X представляет атом кислорода.
5. Способ по п.1, где R1 представляет атом водорода.
6. Способ по п.1, где R2 представляет цианогруппу.
7. Способ по п.1, где Y представляет собой атом галогена, -OCO2-(C1 до C4 алкильную группу), -OCO2-(фенильную группу), -OSO2-(C1 до С4 алкильную группу), -OSO2-(фенильную группу) или диазониевую группу, где в Y C1-C4 алкильная группа может быть замещена 1 до 3 атомами галогена и фенильная группа может быть замещена 1 до 3 атомами галогена или C1-C4 алкильными группами.
8. Способ по п.1, где R4 представляет метильную группу.
9. Способ по п.1, где соединение переходного металла представляет ацетат палладия (II) (Pd(OAc)2), пропионат палладия (II) (Pd(O(C=O)CH2CH3)2), 2-метилпропаноат палладия (II) (Pd(O(C=O)CH(CH3)2)2), пивалат палладия (Pd(OPiv)2), хлорид палладия (II) (PdCl2), бромид палладия (I) (Pd2Br2), или гидроксид палладия (II) (Pd(OH)2).
10. Способ по п.1, где соединение переходного металла представляет ацетат палладия (II) (Pd(OAc)2), пропионат палладия (II) (Pd(O(C=O)CH2CH3)2), 2-метилпропаноат палладия (II) (Pd(O(C=O)CH(CH3)2)2), или пивалат палладия (Pd(OPiv)2).
11. Способ по п.1, где лиганд фосфинового типа представляет три(трет-бутил)фосфин, ди(трет-бутил)метилфосфин, трет-бутилдициклогексилфосфин, ди(трет-бутил)циклогексилфосфин, три(циклогексил)фосфин, 2-дициклогексилфосфино-2',6'-диизопропокси-1,1'-бифенил, 2-дициклогексилфосфино-2',4',6'-триизопропил-1,1'-бифенил или его соль.
12. Способ по п.1, где основание дополнительно присутствует в течение хода реакции.
13. Способ по п.12, где основание представляет карбонат калия, бикарбонат калия, карбонат цезия или фторид тетра-н-бутиламмония.
14. Способ по п.1, где соль серебра дополнительно присутствует в течение хода реакции.
15. Способ по п.14, где соль серебра представляет карбонат серебра.
16. Способ по п.1, где C1 до C12 карбоновая кислота или ее соль дополнительно присутствуют в течение хода реакции.
17. Способ по п.16, где карбоновая кислота или ее соль представляют 2-метилпропановую кислоту, пивалевую кислоту или ее соль.
| Способ безлюдной выемки крутых пластов угля | 1990 |
|
SU1783116A1 |
| EP 1992361 A1, 30.08.2007 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Design of tunable light emission and liquid crystalline characteristics", J | |||
| AM | |||
| CHEM | |||
| SOC, 2003, vol.125, p.1700-1701 | |||
| Julien Roger et al.: "Ligand-free palladium-catalyzed direct | |||
Авторы
Даты
2014-03-27—Публикация
2010-02-26—Подача