Настоящее изобретение относится к замещенным пиразолкарбоксанилидным производным или к их солям, к их промежуточным соединениям и к агентам для сельского хозяйства, в частности к инсектицидам или акарицидам, содержащим указанные соединения в качестве активного ингредиента, и к способу их применения.
Обычно замещенные пиразолкарбоксамидные производные, сходные с настоящим изобретением, как известно, полезны в качестве инсектицидов, фунгицидов или акарицидов для сельского хозяйства (например, заявки на патент Японии JP-A-2003-48878, JP-A-2004-189738 и JP-A-2004-269515). В заявке на патент Японии JP-A-2003-48878 описаны замещенные пиразолкарбоксанилидные производные. Однако заместители в анилиновом остатке по большей части ограничиваются заместителями в положении 2, заместитель в положении 3 представляет собой только метильную группу, и соединение, описываемое в настоящем изобретении, где алкильная группа, имеющая 2 или более атомов углерода, введена в положении 3, не включено в список указанных соединений. Более того, форма с метильной группой в положении 3, конкретно описанная в ней, не показывает акарицидной активности. В заявке на патент Японии JP-A-2004-189738 описаны замещенные пиразолкарбоксанилидные производные. Однако заместители в анилиновом остатке ограничиваются алкоксигруппой, алкилтиогруппой и алкиламиногруппой, и соединение, описываемое в настоящем изобретении, где алкильная группа, имеющая 2 или более атомов углерода, непосредственно введена в положение 3, даже не включено в указанный список соединений. В заявке на патент Японии JP-A-2004-269515 описаны замещенные пиразолкарбоксамидные производные. Однако описано только амидное соединение с гетероциклиламином, и замещенные пиразолкарбоксанилидные производные настоящего изобретения не описаны.
При выращивании сельскохозяйственных и садовых растений вред, наносимый вредными насекомыми, по-прежнему остается серьезной проблемой, и разработка новых агентов для сельского хозяйства, в частности разработка инсектицидов и акарицидов, является желательной вследствие генерирования вредных насекомых, устойчивых к известным агентам и тому подобное. Поскольку являются востребованными различные сельскохозяйственные работы, экономящие труд, вследствие увеличения численности пожилых работников сельского хозяйства, требуется также создание агентов для сельского хозяйства со свойствами, пригодными для таких сельскохозяйственных работ с экономией труда, в частности инсектицидов и акарицидов.
Авторы настоящего изобретения продолжили широкие исследования по разработке новых агентов для сельского хозяйства, в частности инсектицидов и акарицидов, и обнаружили, что в широком диапазоне соединений, описанных в указанном выше предшествующем уровне, замещенные пиразолкарбоксанилидные производные, представленные формулой (I), где пиразольное кольцо выбрано как остаток гетероциклической карбоновой кислоты, и конкретный заместитель введен в анилиновый остаток в положении 3, демонстрируют превосходный контролирующий эффект в качестве акарицидов, как правило, не предсказуемый по содержанию, описанному в указанных выше ссылках на предшествующий уровень. Кроме того, авторы обнаружили, что промежуточные соединения указанного соединения, то есть замещенные анилиновые производные, представленные формулой (II), и 1,3-диметил-5-трифторметилпиразол-4-карбоновая кислота или ее соль являются новыми соединениями, неизвестными в ссылках на предшествующий уровень, и являются полезными в качестве промежуточных соединений для получения различных производных, обладающих физиологической активностью, таких как фармацевтические препараты, пестициды и тому подобное, и таким образом завершили настоящее изобретение.
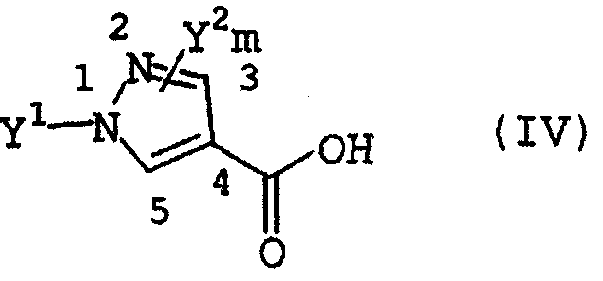
Соответственно, настоящее изобретение относится к замещенным пиразолкарбоксанилидным производным, представленным формулой (I):
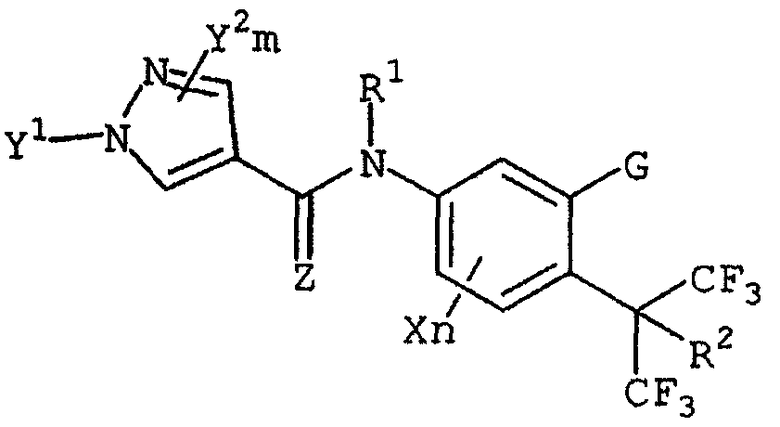 (I)
(I)
где R1 представляет собой 1a) атом водорода, 2a) C1-C8алкильную группу, 3a) галогенС1-C6алкильную группу, 4a) C1-C6алкилкарбонильную группу, 5a)
галогенС1-C6алкилкарбонильную группу, 6a) C2-C6алкенилкарбонильную группу, 7a) галогенС2-C6алкенилкарбонильную группу, 8a) C1-C6алкилкарбонилС1-C6алкильную группу, 9a) C3-C6циклоалкильную группу, 10a) галогенС3-C6циклоалкильную группу, 11a) C3-C6циклоалкилC1-C6алкильную группу, 12a) галогенС3-C6циклоалкилC1-C6алкильную группу, 13a) C2-C6алкенильную группу, 14a) галогенС2-C6алкенильную группу, 15a) C2-C6алкинильную группу, 16a) галогенС2-C6алкинильную группу, 17a) C1-C10алкоксиС1-C6алкильную группу, 18a) галогенС1-C6алкоксиС1-C6алкильную группу, 19a) C2-C6алкенилоксиС1-C6алкильную группу, 20a) C1-C6алкоксиС1-C6алкоксиС1-C6алкильную группу, 21a) C1-C6алкилтиоС1-C6алкильную группу, 22a) галогенС1-C6алкилтиоС1-C6алкильную группу, 23a) C1-C6алкилсульфинилС1-C6алкильную группу, 24a) галогенС1-C6алкилсульфинилС1-C6алкильную группу, 25a) C1-C6алкилсульфонилС1-C6алкильную группу 26a) галогенС1-C6алкилсульфонилС1-C6алкильную группу, 27a)
моноС1-C6алкиламиноС1-C6алкильную группу, 28a) диС1-C6алкиламиноС1-C6алкильную группу, где алкильные группы являются одинаковыми или различными, 29a) фенилС1-C6алкоксиС1-C6алкильную группу, 30a) замещенную фенилС1-C6алкоксиС1-C6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 31a) C1-C16алкоксикарбонильную группу, 32a) C1-C6алкоксиС1-C6алкоксикарбонильную группу, 33a) галогенС1-C6алкоксикарбонильную группу, 34a) C2-C6алкенилоксикарбонильную группу, 35a) C1-C6алкилтиокарбонильную группу, 36a) моноС1-C6алкиламинокарбонильную группу, 37a) диС1-C6алкиламинокарбонильную группу, где алкильные группы являются одинаковыми или различными, 38a) C1-C6алкоксикарбонилС1-C6алкильную группу, 39a) C1-C6алкилсульфонильную группу, 40a) галогенС1-C6алкилсульфонильную группу, 41a) цианоС1-C6алкильную группу, 42a) фенилС1-C6алкильную группу, 43a) замещенную фенилС1-C6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 44a) фенилкарбонильную группу, 45a) замещенную фенилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o)
диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 46a) гетероциклилкарбонильную группу, 47a) замещенную гетероциклилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o)
диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 48a) феноксикарбонильную группу, 49a) замещенную феноксикарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 50a) феноксиС1-C6алкилкарбонильную группу, 51a) замещенную феноксиС1-C6алкилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 52a) фенилсульфонильную группу, 53a) замещенную фенилсульфонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 54a) диС1-C6алкилфосфоногруппу, где алкильные группы являются одинаковыми или различными, 55a) диС1-C6алкилфосфонотиогруппу, где алкильные группы являются одинаковыми или различными, 56a) N-C1-C6алкил-N-C1-C6алкоксикарбониламинотиогруппу, 57a) N-C1-C6алкил-N-C1-C6алкоксикарбонилС1-C6алкиламинотиогруппу, 58a) диС1-C6алкиламинотиогруппу, где алкильные группы являются одинаковыми или различными, 59a) C3-C6циклоалкилкарбонильную группу, 60a) галогенС3-C6циклоалкилкарбонильную группу, 61a) C1-C6алкилC3-C6циклоалкилкарбонильную группу, 62a) галогенС1-C6алкилC3-C6циклоалкилкарбонильную группу, 63a) фенилС1-C6алкилкарбонильную группу, 64a) замещенную фенилС1-C6алкилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o)
диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 65a) фенилС3-C6циклоалкилкарбонильную группу, 66a) замещенную фенилС3-C6циклоалкилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 67a) C3-C6циклоалкилC1-C6алкилкарбонильную группу, 68a) C1-C6алкоксиС1-C6алкилкарбонильную группу, 69a) галогенС3-C6циклоалкилC1-C6алкилкарбонильную группу, 70a) феноксиС1-C6алкоксикарбонильную группу, 71a) замещенную феноксиС1-C6алкоксикарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 72a) C1-C6алкилкарбонилоксиС1-C6алкильную группу, 73a) C1-C6алкилкарбонилС1-C6алкилкарбонильную группу или 74a) C1-C6алкоксикарбонилС1-C6алкилкарбонильную группу;
R2 представляет собой 1b) атом водорода, 2b) атом галогена, 3b) C1-C6алкильную группу, 4b) галогенС1-C6алкильную группу, 5b) цианогруппу, 6b) гидроксигруппу, 7b) C1-C6алкоксигруппу, 8b) галогенС1-C6алкоксигруппу, 9b) C1-C6алкоксиС1-C3алкоксигруппу, 10b) галогенС1-C6алкоксиС1-C3алкоксигруппу, 11b) C1-C6алкилтиоС1-C3алкоксигруппу, 12b) галогенС1-C6алкилтиоС1-C3алкоксигруппу, 13b) C1-C6алкилсульфинилС1-C3алкоксигруппу, 14b)
галогенС1-C6алкилсульфинилС1-C3алкоксигруппу, 15b) C1-C6алкилсульфонилС1-C3алкоксигруппу, 16b) галогенС1-C6алкилсульфонилС1-C3алкоксигруппу, 17b) моноС1-C6алкиламиноС1-C3алкоксигруппу, 18b) диС1-C6алкиламиноС1-C3алкоксигруппу, где алкильные группы являются одинаковыми или различными, 19b) C1-C6алкилтиогруппу, 20b) галогенС1-C6алкилтиогруппу, 21b) C1-C6алкилсульфинильную группу, 22b) галогенС1-C6алкилсульфинильную группу, 23b) C1-C6алкилсульфонильную группу, 24b) галогенС1-C6алкилсульфонильную группу, 25b) аминогруппу, 26b) моноС1-C6алкиламиногруппу, 27b) диС1-C6алкиламиногруппу, где алкильные группы являются одинаковыми или различными, 28b) феноксигруппу, 29b) замещенную феноксигруппу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 30b) фенилтиогруппу, 31b) замещенную фенилтиогруппу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 32b) фенилсульфинильную группу, 33b) замещенную фенилсульфинильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, j) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 34b) фенилсульфонильную группу, 35b) замещенную фенилсульфонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 36b) фенилС1-C6алкоксигруппу или 37b) замещенную фенилС1-C6алкоксигруппу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы;
G представляет собой 1c) C2-C10алкильную группу, 2c) галогенС2-C10алкильную группу, 3c) C3-C10алкенильную группу, 4c) галогенС3-C10алкенильную группу, 5c) C3-C10алкинильную группу, 6c) галогенС3-C10алкинильную группу, 7c) C3-C10циклоалкильную группу, 8c) замещенную C3-C10циклоалкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) C1-C6алкильной группы и c) галогенС1-C6алкильной группы, 9c) C3-C10циклоалкенильную группу, 10c) замещенную C3-C10циклоалкенильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) C1-C6алкильной группы и c) галогенС1-C6алкильной группы, 11c) C3-C8циклоалкилC1-C6алкильную группу или 12c) галогенС3-C8циклоалкилC1-C6алкильную группу;
Z представляет собой атом кислорода или атом серы;
X могут быть одинаковыми или различными и представляют собой 1d) атом водорода, 2d) атом галогена, 3d) цианогруппу, 4d) нитрогруппу, 5d) C1-C6алкильную группу или 6d) галогенС1-C6алкильную группу;
Y1 представляет собой 1e) атом водорода, 2e) C1-C6алкильную группу, 3e) галогенС1-C6алкильную группу, 4e) C2-C6алкенильную группу, 5e) галогенС2-C6алкенильную группу, 6e) C2-C6алкинильную группу, 7e) галогенС2-C6алкинильную группу, 8e) C1-C6алкоксиС1-C6алкоксиС1-C6алкильную группу, 9e) гидроксиС1-C6алкильную группу, 10e) C1-C6алкилкарбонилоксиС1-C6алкильную группу, 11e) C3-C6циклоалкильную группу, 12e) галогенС3-C6циклоалкильную группу, 13e) C3-C6циклоалкилC1-C6алкильную группу, 14e) галогенС3-C6циклоалкилC1-C6алкильную группу, 15e) C1-C6алкилсульфонильную группу, 16e) галогенС1-C6алкилсульфонильную группу, 17e) C1-C6алкилтиоС1-C6алкильную группу, 18e) галогенС1-C6алкилтиоС1-C6алкильную группу, 19e) C1-C6алкилсульфинилС1-C6алкильную группу, 20e) галогенС1-C6алкилсульфинилС1-C6алкильную группу, 21e) C1-C6алкилсульфонилС1-C6алкильную группу, 22e) галогенС1-C6алкилсульфонилС1-C6алкильную группу, 23e) моноС1-C6алкиламиноС1-C6алкильную группу, 24e) диС1-C6алкиламиноС1-C6алкильную группу, где алкильные группы являются одинаковыми или различными, 25e) фенильную группу, 26e) замещенную фенильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы;
Y2 могут быть одинаковыми или различными и представляют собой 1f) атом водорода, 2f) атом галогена, 3f) цианогруппу, 4f) нитрогруппу, 5f) гидроксильную группу, 6f) меркаптогруппу, 7f) аминогруппу, 8f) карбоксильную группу, 9f) C1-C6алкильную группу, 10f) галогенС1-C6алкильную группу, 11f) C2-C6алкенильную группу, 12f) галогенС2-C6алкенильную группу, 13f) C2-C6алкинильную группу, 14f) галогенС2-C6алкинильную группу, 15f) триС1-C6алкилсилилС2-C6алкинильную группу, где алкильные группы являются одинаковыми или различными, 16f) фенилС2-C6алкинильную группу, 17f) C1-C6алкоксиС1-C6алкоксиС1-C6алкильную группу, 18f) гидроксиС1-C6алкильную группу, 19f) C1-C6алкилкарбонилоксиС1-C6алкильную группу, 20f) C3-C6циклоалкильную группу, 21f) галогенС3-C6циклоалкильную группу, 22f) C3-C6циклоалкилC1-C6алкильную группу, 23f) галогенС3-C6циклоалкилC1-C6алкильную группу, 24f) C1-C6алкоксигруппу, 25f) галогенС1-C6алкоксигруппу, 26f) C1-C6алкоксиС1-C6алкоксигруппу, 27f) галогенС1-C6алкоксиС1-C6алкоксигруппу, 28f) фенилС1-C6алкоксигруппу, 29f) C1-C6алкоксиС1-C6алкильную группу, 30f) галогенС1-C6алкоксиС1-C6алкильную группу, 31f) C1-C6алкилтиогруппу, 32f) галогенС1-C6алкилтиогруппу, 33f) C1-C6алкилсульфинильную группу, 34f) галогенС1-C6алкилсульфинильную группу, 35f) C1-C6алкилсульфонильную группу, 36f) галогенС1-C6алкилсульфонильную группу, 37f) С1-C6алкилтиоС1-C6алкильную группу, 38f) галогенС1-C6алкилтиоС1-C6алкильную группу, 39f) C1-C6алкилсульфинилС1-C6алкильную группу, 40f) галогенС1-C6алкилсульфинилС1-C6алкильную группу, 41f) C1-C6алкилсульфонилС1-C6алкильную группу, 42f) галогенС1-C6алкилсульфонилС1-C6алкильную группу, 43f) моноС1-C6алкиламиногруппу, 44f) диС1-C6алкиламиногруппу, где алкильные группы являются одинаковыми или различными, 45f) фениламиногруппу, 46f) моноС1-C6алкиламиноС1-C6алкильную группу, 47f) диС1-C6алкиламиноС1-C6алкильную группу, где алкильные группы являются одинаковыми или различными, 48f) фенильную группу, 49f) замещенную фенильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 50f) феноксигруппу, 51f) замещенную феноксигруппу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 52f) гетероциклическую группу или 53f) замещенную гетероциклическую группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы;
m равно 1 или 2; и
n равно целому числу от 1 до 3,
их солям и агентам для сельского хозяйства, содержащим соединение в качестве активного ингредиента, и к способам их применения.
В дополнение, настоящее изобретение также относится к замещенным анилиновым производным, представленным формулой (II), которые являются промежуточными соединениями:
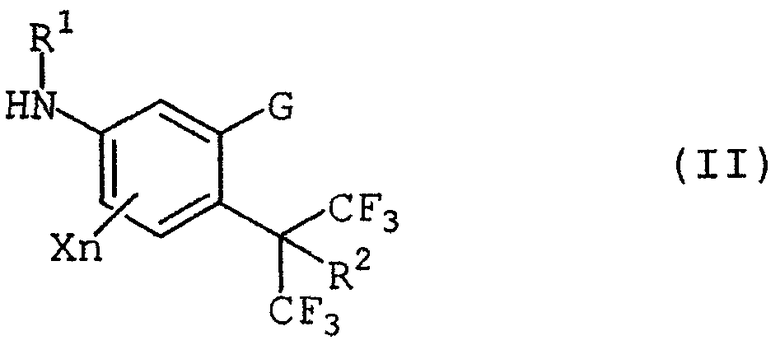
где R1 представляет собой 1a) атом водорода, 2a) C1-C8алкильную группу, 3a) галогенС1-C6алкильную группу, 4a) C1-C6алкилкарбонильную группу, 5a) галогенС1-C6алкилкарбонильную группу, 6a) C2-C6алкенилкарбонильную группу, 7a) галогенС2-C6алкенилкарбонильную группу, 8a) C1-C6алкилкарбонилС1-C6алкильную группу, 9a) C3-C6циклоалкильную группу, 10a) галогенС3-C6циклоалкильную группу, 11a) C3-C6циклоалкилC1-C6алкильную группу, 12a) галогенС3-C6циклоалкилC1-C6алкильную группу, 13a) C2-C6алкенильную группу, 14a) галогенС2-C6алкенильную группу, 15a) C2-C6алкинильную группу, 16a) галогенС2-C6алкинильную группу, 17a) C1-C10алкоксиС1-C6алкильную группу, 18a) галогенС1-C6алкоксиС1-C6алкильную группу, 19a) C2-C6алкенилоксиС1-C6алкильную группу, 20a) C1-C6алкоксиС1-C6алкоксиС1-C6алкильную группу, 21a) C1-C6алкилтиоС1-C6алкильную группу, 22a) галогенС1-C6алкилтиоС1-C6алкильную группу, 23a) C1-C6алкилсульфинилС1-C6алкильную группу, 24a) галогенС1-C6алкилсульфинилС1-C6алкильную группу, 25a) C1-C6алкилсульфонилС1-C6алкильную группу, 26a) галогенС1-C6алкилсульфонилС1-C6алкильную группу, 27a) моноС1-C6алкилaмино C1-C6алкильную группу, 28a) диС1-C6алкиламиноС1-C6алкильную группу, где алкильные группы являются одинаковыми или различными, 29a) фенилС1-C6алкоксиС1-C6алкильную группу, 30a) замещенную фенилС1-C6алкоксиС1-C6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 31a) C1-C16алкоксикарбонильную группу, 32a) C1-C6алкоксиС1-C6алкоксикарбонильную группу, 33a) галогенС1-C6алкоксикарбонильную группу, 34a) C2-C6алкенилоксикарбонильную группу, 35a) C1-C6алкилтиокарбонильную группу, 36a) моноС1-C6алкиламинокарбонильную группу, 37a) диС1-C6алкиламинокарбонильную группу, где алкильные группы являются одинаковыми или различными, 38a) C1-C6алкоксикарбонилС1-C6алкильную группу, 39a) C1-C6алкилсульфонильную группу, 40a) галогенС1-C6алкилсульфонильную группу, 41a) цианоС1-C6алкильную группу, 42a) фенилС1-C6алкильную группу, 43a) замещенную фенилС1-C6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 44a) фенилкарбонильную группу, 45a) замещенную фенилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 46a) гетероциклилкарбонильную группу, 47a) замещенную гетероциклилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 48a) феноксикарбонильную группу, 49a) замещенную феноксикарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 50a) феноксиС1-C6алкилкарбонильную группу, 51a) замещенную феноксиС1-C6алкилкарбонильную группу имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 52a) фенилсульфонильную группу, 53a) замещенную фенилсульфонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 54a) диС1-C6алкилфосфоногруппу, где алкильные группы являются одинаковыми или различными, 55a) диС1-C6алкилфосфонотиогруппу, где алкильные группы являются одинаковыми или различными, 56a) N-C1-C6алкил-N-C1-C6алкоксикарбониламинотиогруппу, 57a) N-C1-C6алкил-N-C1-C6алкоксикарбонилС1-C6алкиламинотиогруппу, 58a) диС1-C6алкиламинотиогруппу, где алкильные группы являются одинаковыми или различными, 59a) C3-C6циклоалкилкарбонильную группу, 60a) галогенС3-C6циклоалкилкарбонильную группу, 61a) C1-C6алкилC3-C6циклоалкилкарбонильную группу, 62a) галогенС1-C6алкилC3-C6циклоалкилкарбонильную группу, 63a) фенилС1-C6алкилкарбонильную группу, 64a) замещенную фенилС1-C6алкилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 65a) фенилС3-C6циклоалкилкарбонильную группу, 66a) замещенную фенилС3-C6циклоалкилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, 1) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 67a) C3-C6циклоалкилC1-C6алкилкарбонильную группу, 68a) C1-C6алкоксиС1-C6алкилкарбонильную группу, 69a) галогенС3-C6циклоалкилC1-C6алкилкарбонильную группу, 70a) феноксиС1-C6алкоксикарбонильную группу, 71a) замещенную феноксиС1-C6алкоксикарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 72a) C1-C6алкилкарбонилоксиС1-C6алкильную группу, 73a) C1-C6алкилкарбонилС1-C6алкилкарбонильную группу или 74a) C1-C6алкоксикарбонилС1-C6алкилкарбонильную группу;
R2 представляет собой 1b) атом водорода, 2b) атом галогена, 3b) C1-C6алкильную группу, 4b) галогенС1-C6алкильную группу, 5b) цианогруппу, 6b) гидроксигруппу, 7b) C1-C6алкоксигруппу, 8b) галогенС1-C6алкоксигруппу, 9b) C1-C6алкоксиС1-C3алкоксигруппу, 10b) галогенС1-C6алкоксиС1-C3алкоксигруппу, 11b) C1-C6алкилтиоС1-C3алкоксигруппу, 12b) галогенС1-C6алкилтиоС1-C3алкоксигруппу, 13b) C1-C6алкилсульфинилС1-C3алкоксигруппу, 14b) галогенС1-C6алкилсульфинилС1-C3алкоксигруппу, 15b) C1-C6алкилсульфонилС1-C3алкоксигруппу, 16b) галогенС1-C6алкилсульфонилС1-C3алкоксигруппу, 17b) моноС1-C6алкиламиноС1-C3алкоксигруппу, 18b) диС1-C6алкиламиноС1-C3алкоксигруппы, где алкильные группы являются одинаковыми или различными, 19b) C1-C6алкилтиогруппу, 20b) галогенС1-C6алкилтиогруппу, 21b) C1-C6алкилсульфинильную группу, 22b) галогенС1-C6алкилсульфинильную группу, 23b) C1-C6алкилсульфонильную группу, 24b) галогенС1-C6алкилсульфонильную группу, 25b) аминогруппу, 26b) моноС1-C6алкиламиногруппу, 27b) диС1-C6алкиламиногруппу, где алкильные группы являются одинаковыми или различными, 28b) феноксигруппу, 29b) замещенную феноксигруппу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 30b) фенилтиогруппу, 31b) замещенную фенилтиогруппу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 32b) фенилсульфинильную группу, 33b) замещенную фенилсульфинильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 34b) фенилсульфонильную группу, 35b) замещенную фенилсульфонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 36b) фенилС1-C6алкоксигруппу или 37b) замещенную фенилС1-C6алкоксигруппу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы;
G представляет собой 1c) C2-C10алкильную группу, 2c) галогенС2-C10алкильную группу, 3c) C3-C10алкенильную группу, 4c) галогенС3-C10алкенильную группу, 5c) C3-C10алкинильную группу, 6c) галогенС3-C10алкинильную группу, 7c) C3-C10циклоалкильную группу, 8c) замещенную C3-C10циклоалкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) C1-C6алкильной группы и c) галогенС1-C6алкильной группы, 9c) C3-C10циклоалкенильную группу, 10c) замещенную C3-C10циклоалкенильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) C1-C6алкильной группы и c) галогенС1-C6алкильной группы, 11e) C3-C8циклоалкилC1-C6алкильную группу или 12c) галогенС3-C8циклоалкилC1-C6алкильную группу;
X могут быть одинаковыми или различными и представляют собой 1d) атом водорода, 2d) атом галогена, 3d) цианогруппу, 4d) нитрогруппу, 5d) C1-C6алкильную группу или 6d) галогенС1-C6алкильную группу;
n равно целому числу от 1 до 3,
к их солям и к 1,3-диметил-5-трифторметилпиразол-4-карбоновой кислоте и к ее солям.
В определениях замещенного пиразолкарбоксанилидного производного формулы (I) и замещенного анилинового производного формулы (II) настоящего изобретения, "галоген", "C1-C6алкил", "C1-C6алкоксил", "C2-C6алкенил", "C2-C6алкинил" или "гетероциклическая группа" и тому подобное, каждый из заместителей имеет следующее значение.
"Галоген" или "атом галогена" означает атом хлора, атом брома, атом йода или атом фтора.
"C1-C6алкил" представляет собой алкил с линейной и разветвленной цепью, имеющий 1-6 атомов углерода, такой как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, трет-пентил, 2-метилбутил, 1-этилпропил, н-гексил, 2-этилбутил и тому подобное.
"C1-C6алкил" представляет собой алкил с линейной и разветвленной цепью, имеющий 1-8 атомов углерода, такой как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, трет-пентил, 2-метилбутил, 1-этилпропил, н-гексил, 2-этилбутил, н-гептил, н-октил, 2-этилгексил и тому подобное.
"C2-C10алкил" представляет собой алкил с линейной и разветвленной цепью, имеющий 2-10 атомов углерода, такой как этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, трет-пентил, 2-метилбутил, н-гексил, 2-этилбутил, 1-этилпропил, н-гептил, н-октил, 2-этилгексил, н-нонил, н-децил и тому подобное.
"C3-C6циклоалкил" представляет собой циклический алкил, имеющий 3-6 атомов углерода, такой как циклопропил, циклобутил, циклопентил, циклогексил и тому подобное.
"C3-C8циклоалкил" представляет собой циклический алкил, имеющий 3-8 атомов углерода, такой как циклопропил, циклобутил, циклопентил, циклогексил, циклооктил и тому подобное.
"C3-C10циклоалкил" представляет собой циклический алкил, имеющий 3-10 атомов углерода, такой как циклопропил, циклобутил, циклопентил, циклогексил, циклооктил, циклодецил и тому подобное.
"C3-C10циклоалкенил" представляет собой циклический алкенил, имеющий 3-10 атомов углерода, такой как циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклооктенил, циклодеценил и тому подобное.
"C1-C3алкокси" представляет собой алкокси, где ее алкильный остаток представляет собой алкил с линейной и разветвленной цепью, имеющий 1-3 атома углерода, такую как метокси, этокси, пропокси, изопропокси и тому подобное.
"C1-C6алкокси" представляет собой алкокси, где алкильный остаток представляет собой указанный выше "C1-C6алкил", такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентилокси, изопентилокси, неопентилокси, трет-пентилокси, 2-метилбутокси, 1-этилпропокси, гексилокси, 2-этилбутокси и тому подобное.
"C1-C10алкокси" представляет собой алкокси, где алкильный остаток представляет собой алкил с линейной и разветвленной цепью, имеющий 1-10 атомов углерода, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентилокси, изопентилокси, неопентилокси, трет-пентилокси, 2-метилбутокси, 1-этилпропокси, гексилокси, 2-этилбутокси, н-гептилокси, н-октилокси, 2-этилгексилокси, н-нонилокси, н-децилокси и тому подобное.
"C1-C16алкокси" представляет собой алкокси, где алкильный остаток представляет собой алкил с линейной и разветвленной цепью, имеющий 1-16 атомов углерода, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентилокси, изопентилокси, неопентилокси, трет-пентилокси, 2-метилбутокси, 1-этилпропокси, гексилокси, 2-этилбутокси, н-гептилокси, н-октилокси, 2-этилгексилокси, н-нонилокси, н-децилокси, н-ундецилокси, н-додецилокси, н-тридецилокси, н-тетрадецилокси, н-пентадецилокси, н-гексадецилокси и тому подобное.
"C2-C6алкенил" представляет собой алкенил с линейной и разветвленной цепью, имеющий 2-6 атомов углерода, который имеет по меньшей мере одну двойную связь, такой как винил, 1-пропенил, аллил, 1-бутенил, 2-бутенил, 3-бутенил, 2-пентенил, 2-метил-1-пропенил, 2,4-пентадиенил, 3-гексенил и тому подобное.
"C3-C10алкенил" представляет собой алкенил с линейной и разветвленной цепью, имеющий 3-10 атомов углерода, который имеет по меньшей мере одну двойную связь, такой как 1-бутенил, 2-бутенил, 3-бутенил, 2-пентенил, 2,4-пентадиенил, 3-гексенил, 3-гептенил, 3-октенил, 3-ноненил, 3-деценил и тому подобное.
"C2-C6алкинил" представляет собой алкинил с линейной и разветвленной цепью, имеющий 2-6 атомов углерода, который имеет по меньшей мере одну тройную связь, такой как этинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 2-пентинил, 3-гексинил и тому подобное.
"C3-C10алкинил" представляет собой алкинил с линейной и разветвленной цепью, имеющий 3-10 атомов углерода, который имеет по меньшей мере одну тройную связь, такой как 1-бутинил, 2-бутинил, 3-бутинил, 2-пентинил, 3-гексинил, 3-гептинил, 3-октинил, 3-нонинил, 3-децинил и тому подобное.
Числа в "C2-C6", "C3-C10" и тому подобное, показывают диапазон числа атомов углерода, такой как 2-6 атомов углерода и 3-10 атомов углерода.
Кроме того, рассмотренные выше определения могут применяться к группам, к которым присоединены приведенные выше заместители. Например, "галогенС1-C6алкил" означает алкильную группу с линейной или разветвленной цепью, имеющую 1-6 атомов углерода, которая замещена одним или несколькими одинаковыми или различными атомами галогена, такую как хлорметил, 2-хлорэтил, 2,2,2-трихлорэтил, 3-хлорпропил, 2-хлор-1,1-диметилэтил, 1-бром-1-метилэтил, дифторметил, трифторметил, 2,2,2-трифторэтил, перфторгексил и тому подобное.
"Гетероциклическая группа" и "гетероциклил" представляют собой 5- или 6-членные гетероциклические группы, имеющие один или несколько гетероатомов, выбранных из атома кислорода, атома серы и атома азота, включая, например, пиридильную группу, пиридин-N-оксидную группу, пиримидинильную группу, фурильную группу, тетрагидрофурильную группу, тиенильную группу, тетрагидротиенильную группу, тетрагидропиранильную группу, тетрагидротиопиранильную группу, оксазолильную группу, изоксазолильную группу, оксадиазолильную группу, тиазолильную группу, изотиазолильную группу, тиадиазолильную группу, имидазолильную группу, триазолильную группу и пиразолильную группу.
Соль замещенного пиразолкарбоксанилидного производного, представленного формулой (I) настоящего изобретения, включает соль щелочного металла (лития, натрия, калия и тому подобное); соль щелочно-земельного металла (кальция, магния и тому подобное); соль аммония и соль органического амина (метиламина, триэтиламина, диэтаноламина, пиперидина, пиридина и тому подобное) или кислотно-аддитивную соль. Кислотно-аддитивная соль включает, например, карбоксилат, такой как ацетат, пропионат, оксалат, трифторацетат, бензоат и тому подобное; сульфонат, такой как метансульфонат, трифторметансульфонат, п-толуолсульфонат и тому подобное; соль неорганической кислоты, такую как гидрохлорид, сульфат, нитрат, карбонат и тому подобное.
В замещенных пиразолкарбоксанилидных производных, представленных формулой (I) настоящего изобретения, R1 предпочтительно представляет собой 1a) атом водорода, 2a) C1-C6алкильную группу, 3a) галогенС1-C6алкильную группу, 4a) C1-C6алкилкарбонильную группу, 5a) галогенС1-C6алкилкарбонильную группу, 6a) C2-C6алкенилкарбонильную группу, 13a) C2-C6алкенильную группу, 17a) C1-C10алкоксиС1-C6алкильную группу, 18a) галогенС1-C6алкоксиС1-C6алкильную группу, 19a) C2-C6алкенилоксиС1-C6алкильную группу, 20a) C1-C6алкоксиС1-C6алкоксиС1-C6алкильную группу, 29a) фенилС1-C6алкоксиС1-C6алкильную группу, 30a) замещенную фенилС1-C6алкоксиС1-C6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 31a) C1-C16алкоксикарбонильную группу, 32a) C1-C6алкоксиС1-C6алкоксикарбонильную группу, 33a) галогенС1-C6алкоксикарбонильную группу, 34a) C2-C6алкенилоксикарбонильную группу, 35a) C1-C6алкилтиокарбонильную группу, 42a) фенилС1-C6алкильную группу, 43a) замещенную фенилС1-C6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 44a) фенилкарбонильную группу, 45a) замещенную фенилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 46a) гетероциклилкарбонильную группу, 47a) замещенную гетероциклилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 48a) феноксикарбонильную группу, 49a) замещенную феноксикарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 50a) феноксиС1-C6алкилкарбонильную группу, 51a) замещенную феноксиС1-C6алкилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 52a) фенилсульфонильную группу, 53a) замещенную фенилсульфонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 58a) диС1-C6алкиламинотиогруппу, где алкильные группы являются одинаковыми или различными, 59a) C3-C6циклоалкилкарбонильную группу, 61a) C1-C6алкилС3-C6циклоалкилкарбонильную группу, 63a) фенилС1-C6алкилкарбонильную группу, 64a) замещенную фенилС1-C6алкилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 65a) фенилС3-C6циклоалкилкарбонильную группу, 66a) замещенную фенилС3-C6циклоалкилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из a) атома галогена, b) цианогруппы, c) нитрогруппы, d) C1-C6алкильной группы, e) галогенС1-C6алкильной группы, f) C1-C6алкоксигруппы, g) галогенС1-C6алкоксигруппы, h) C1-C6алкилтиогруппы, i) галогенС1-C6алкилтиогруппы, j) C1-C6алкилсульфинильной группы, k) галогенС1-C6алкилсульфинильной группы, l) C1-C6алкилсульфонильной группы, m) галогенС1-C6алкилсульфонильной группы, n) моноС1-C6алкиламиногруппы, o) диС1-C6алкиламиногруппы, где алкильные группы являются одинаковыми или различными, и p) C1-C6алкоксикарбонильной группы, 68a) C1-C6алкоксиС1-C6алкилкарбонильную группу, 73a) C1-C6алкилкарбонилС1-C6алкилкарбонильную группу или 74a) C1-C6алкоксикарбонилС1-C6алкилкарбонильную группу, и более предпочтительно, 1a) атом водорода, 4a) C1-C6алкилкарбонильную группу, 5a) галогенС1-C6алкилкарбонильную группу, 17a) C1-C10алкоксиС1-C6алкильную группу, 18a) галогенС1-C6алкоксиС1-C6алкильную группу, 31a) C1-C16алкоксикарбонильную группу, 33a) галогенС1-C6алкоксикарбонильную группу или 68a) C1-C6алкоксиС1-C6алкилкарбонильную группу.
R2 предпочтительно представляет собой 1b) атом водорода, 2b) атом галогена, 6b) гидроксигруппу, 7b) C1-C6алкоксигруппу или 8b) галогенС1-C6алкоксигруппу, и более предпочтительно, 1b) атом водорода или 7b) C1-C6алкоксигруппу.
G предпочтительно представляет собой 1c) C2-C10алкильную группу, 3c) C3-C10алкенильную группу или 11e) C3-C8циклоалкилC1-C6алкильную группу, и более предпочтительно, 1c) C2-C10алкильную группу.
X предпочтительно представляет собой 1d) атом водорода, 2d) атом галогена или 5d) C1-C6алкильную группу, и более предпочтительно, 1d) атом водорода.
Z предпочтительно представляет собой атом кислорода.
Y1 предпочтительно представляет собой 2e) C1-C6алкильную группу, 3e) галогенС1-C6алкильную группу или 4e) C2-C6алкенильную группу, и более предпочтительно, 2e) C1-C6алкильную группу.
Y2 предпочтительно представляет собой 1f) атом водорода, 2f) атом галогена, 9f) C1-C6алкильную группу, 10f) галогенС1-C6алкильную группу или 31f) C1-C6алкилтиогруппу, и более предпочтительно, 1f) атом водорода, 2f) атом галогена, 9f) C1-C6алкильную группу или 10) галогенС1-C6алкильную группу.
m предпочтительно равно 2.
В дополнение, соль замещенного анилинового производного, представленного формулой (II), предпочтительно представляет собой кислотно-аддитивную соль, включая, например, карбоксилат, такой как ацетат, пропионат, оксалат, трифторацетат, бензоат и тому подобное; сульфонат, такой как метансульфонат, трифторметансульфонат, п-толуолсульфонат и тому подобное; соль неорганической кислоты, такую как гидрохлорид, сульфат, нитрат, карбонат и тому подобное.
Соль 1,3-диметил-5-трифторметилпиразол-4-карбоновой кислоты настоящего изобретения включает соль щелочного металла (лития, натрия, калия и тому подобное); соль щелочноземельного металла (кальция, магния и тому подобное); соль аммония и соль органического амина (метиламина, триэтиламина, диэтаноламина, пиперидина, пиридина и тому подобное).
Замещенное пиразолкарбоксанилидное производное, представленное формулой (I), или его промежуточное соединение, то есть замещенное анилиновое производное, представленное формулой (II), настоящего изобретения, может иметь один или несколько асимметричных центров в структурной формуле, и кроме того, могут присутствовать два или более оптических изомеров и диастереомеров. Как следствие, настоящее изобретение полностью охватывает каждый оптический изомер и смеси с любым их соотношением. В дополнение, замещенное пиразолкарбоксанилидное производное, представленное формулой (I), настоящего изобретения может иметь два типа геометрических изомеров, полученных из двойной связи C-C в структурной формуле. Настоящее изобретение охватывает все геометрические изомеры и смеси, содержащие их, при любом соотношении. Кроме того, настоящее изобретение охватывает их гидраты.
Репрезентативные способы получения замещенного пиразолкарбоксанилидного производного, представленного формулой (I), и замещенного анилинового производного, представленного формулой (II), как его промежуточного соединения, иллюстрируется ниже, но настоящее изобретение не должно рассматриваться как ограничиваемое ими.
Способ получения 1
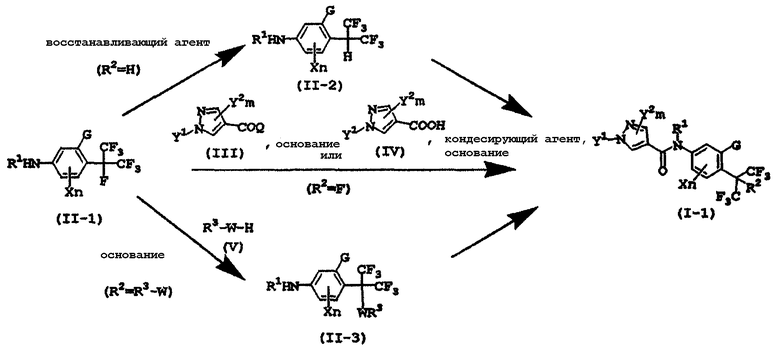
(где G, R1, X, n, Y1, Y2 и m являются такими, как определено выше, и R3 представляет собой атом водорода, C1-C6алкильную группу, галогенС1-C6алкильную группу, фенильную группу, замещенную фенильную группу или фенилС1-C4алкильную группу; W представляет собой -O-, -S- или -N(R4)-, где R4 представляет собой атом водорода, C1-C6алкильную группу, галогенС1-C6алкильную группу, фенильную группу, замещенную фенильную группу или фенилС1-C4алкильную группу, и Q представляет собой атом галогена или C1-C6алкоксильную группу).
Среди замещенных пиразолкарбоксанилидных производных, представленных формулой (I), замещенное пиразолкарбоксанилидное производное (I-1), где Z представляет собой O, и R2 представляет собой атом водорода, атом фтора или WR3, где W и R3 являются такими, как определено выше, может быть получено путем взаимодействия анилинового производного, представленного формулами (II-1)-(II-3), с галоидангидридом пиразолкарбоновой кислоты или эфиром пиразолкарбоновой кислоты, представленной формулой (III), в присутствии или в отсутствие основания, в инертном растворителе, или путем взаимодействия анилинового производного, представленного формулами (II-1)-(II-3), с пиразолкарбоновой кислотой, представленной формулой (IV), в присутствии конденсирующего агента, в присутствии или в отсутствие основания, в инертном растворителе, и могут быть использованы любые обычные способы получения амидов.
Анилиновое производное, представленное формулой (II-2), может быть получено восстановлением анилинового производного, представленного формулой (II-1), в присутствии восстанавливающего агента, в инертном растворителе.
Анилиновое производное, представленное формулой (II-3), может быть получено путем взаимодействия анилинового производного, представленного формулой (II-1), со спиртовым производным, тиольным производным или аминовым производным, представленным формулой (V), в присутствии или в отсутствие основания, в инертном растворителе.
Формула (II-1) → формула (II-2)
Пример восстанавливающего агента, который может быть использован в настоящей реакции, включает гидриды металлов, такие как литийалюминийгидрид, борогидрид лития, борогидрид натрия, диизобутилалюминийгидрид, натрий-бис-(2-метоксиэтокси)алюминийгидрид и тому подобное, металл, такой как литий и тому подобное, или соли металлов и тому подобное. Количество восстанавливающего агента, который может быть использован, выбирают соответствующим образом в пределах от эквивалентного количества до избыточного количества по отношению к анилиновому производному, представленного формулой (II-1).
Примеры инертного растворителя, который может быть использован в настоящей реакции и может быть любым, пока он заметно не тормозит ход настоящей реакции, включают ароматические углеводороды, такие как бензол, толуол, ксилол и тому подобное; галогенированные углеводороды, такие как метиленхлорид, хлороформ, четыреххлористый углерод и тому подобное; галогенированные ароматические углеводороды, такие как хлорбензол, дихлорбензол и тому подобное; простые эфиры с прямой цепью или циклические, такие как простой диэтиловый эфир, диоксан, тетрагидрофуран и тому подобное, или диметилсульфоксид и тому подобное, и такие инертные растворители могут быть использованы по отдельности или в комбинации двух или нескольких видов.
Температура реакции может находиться в пределах от комнатной температуры до температуры кипения инертного растворителя, который может быть использован, и время реакции может находиться в пределах от нескольких минут до 50 часов, в зависимости от масштаба реакции и температуры реакции.
После завершения реакции желаемое соединение может быть выделено из реакционной смеси обычными методами, и желаемое соединение может быть подвергнуто очистке с использованием перекристаллизации или колоночной хроматографии и тому подобное, если это необходимо. Желаемое соединение может быть использовано на последующей стадии реакции без выделения из реакционной смеси.
Формула (II-1) → формула (II-3)
Пример основания, которое может быть использовано в настоящей реакции, включает гидриды металлов, такие как гидрид лития, гидрид натрия, гидрид калия и тому подобное; алкоголяты металлов, такие как метоксид натрия, этоксид натрия, трет-бутоксид калия и тому подобное; и металлоалкилы, такие как н-бутиллитий, втор-бутиллитий, трет-бутиллитий и тому подобное. Количество основания, которое может быть использовано, может быть выбрано соответствующим образом, в пределах от эквивалентного количества до избыточного количества по отношению к анилиновому производному, представленному формулой (II-1).
Примеры инертного растворителя, который может быть использован в настоящей реакции и может быть любым, пока он заметно не тормозит ход настоящей реакции, включают ароматические углеводороды, такие как бензол, толуол, ксилол и тому подобное; спирты, такие как метанол, этанол и тому подобное; простые эфиры с прямой цепью или циклические, такие как простой диэтиловый эфир, 1,2-диметоксиэтан, диоксан, тетрагидрофуран и тому подобное, и такие инертные растворители могут быть использованы по отдельности или в комбинации двух или нескольких видов.
Температура реакции может находиться в пределах от -70°C до температуры кипения инертного растворителя, который может быть использован, и время реакции может находиться в пределах от нескольких минут до 50 часов, в зависимости от масштаба реакции и температуры реакции.
После завершения реакции, желаемое соединение может быть выделено из реакционной смеси обычными методами, и желаемое соединение может быть подвергнуто очистке с использованием перекристаллизации или колоночной хроматографии и тому подобное, если это необходимо. Желаемое соединение может быть использовано на последующей стадии реакции без выделения из реакционной смеси.
Формула (II-1), (II-2) или (II-3) → формула (I-1)
Примеры конденсирующего агента, который может быть использован в настоящей реакции, включают диэтилцианофосфат (DEPC), карбонилдиимидазол (CDI), 1,3-дициклогексилкарбодиимид (DCC), хлорформиаты, 2-хлор-1-метилпиридиниййодид и тому подобное.
В качестве основания, которое может быть использовано в настоящей реакции, включено неорганическое основание или органическое основание, и примеры неорганического основания включают гидроксиды щелочного металла, такие как гидроксид натрия, гидроксид калия и тому подобное; гидриды щелочного металла, такие как гидрид натрия, гидрид калия и тому подобное; соли щелочного металла и спирта, такие как этоксид натрия, трет-бутоксид калия и тому подобное; карбонаты, такие как карбонат натрия, карбонат калия, бикарбонат натрия и тому подобное; и пример органических оснований включает триэтиламин, пиридин, DBU и тому подобное. Количество основания, которое может быть использовано, может быть выбрано в пределах от эквивалентного количества до избыточного количества по отношению к производному пиразолкарбоновой кислоты, представленному формулой (III) или (IV).
Примеры инертного растворителя, который может быть использован в настоящей реакции и может быть любым, пока он заметно не тормозит хода настоящей реакции, включают ароматические углеводороды, такие как бензол, толуол, ксилол и тому подобное; галогенированные углеводороды, такие как метиленхлорид, хлороформ, четыреххлористый углерод и тому подобное; галогенированные ароматические углеводороды, такие как хлорбензол, дихлорбензол и тому подобное; простые эфиры с прямой цепью или циклические, такие как простой диэтиловый эфир, диоксан, тетрагидрофуран и тому подобное; сложные эфиры, такие как этилацетат и тому подобное; амиды, такие как диметилформамид, диметилацетамид и тому подобное; диметилсульфоксид; 1,3-диметил-2-имидазолидинон; ацетон, метилэтилкетон и тому подобное. Такие инертные растворители могут быть использованы по отдельности или в комбинации двух или нескольких видов.
Поскольку настоящая реакция является эквимолярной реакцией, каждый реагент может быть использован в равном молярном количестве, однако любой из реагентов также может быть использован в избытке. Температура реакции может находиться в пределах от комнатной температуры до температуры кипения инертного растворителя, который может быть использован, и время реакции может находиться в пределах от нескольких минут до 48 часов, в зависимости от масштаба реакции и температуры реакции.
После завершения реакции желаемое соединение может быть выделено из реакционной смеси обычными методами, и желаемое соединение может быть подвергнуто очистке с использованием перекристаллизации или колоночной хроматографии и тому подобное, если это необходимо.
Анилиновое производное, представленное формулой (II-1), в качестве исходного вещества настоящей реакции, может быть получено в соответствии со способом получения, описанным в заявках на патент Японии JP-A-11-302233, JP-A-2001-122836 или JP-A-2006-8675.
Производное пиразолкарбоновой кислоты, представленное формулами (III) или (IV), может быть получено в соответствии с несколькими способами, описанными в известной литературе (например, Aust. J. Chem., 1983, 36, 135-147, Synthesis, 1986, 753-755, заявки на патент Японии JP-A-52-87168, JP-A-63-452 64, JP-A-1-106866 и тому подобное).
Способ получения 2

(где G, R1, R2, X, n, Y1, Y2 и m являются такими, как определено выше).
Среди замещенных пиразолкарбоксанилидных производных, представленных формулой (I), замещенное пиразолкарбоксанилидное производное (1-2), где Z представляет собой S, может быть получено путем взаимодействия анилидного производного, представленного (I-1), с реагентом Лоуссона в соответствии с известным способом (Tetrahedron Lett., 21 (42), 4061 (1980)).
Способ получения 3
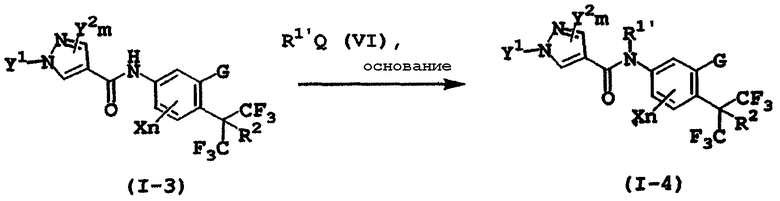
(где G, R2, X, n, Y1, Y2, m и Q являются такими, как определено выше, и R1' является таким, как определено выше, за исключением атома водорода).
Среди замещенных пиразолкарбоксанилидных производных, представленных формулой (I), замещенное пиразолкарбоксанилидное производное (I-4), где R1 является иным, чем атом водорода, может быть получено путем взаимодействия амидного производного, представленного формулой (I-3), с галогенидным производным или сложноэфирным производным, представленным формулой (VI), в присутствии или в отсутствие основания, в инертном растворителе.
Примеры основания, которое может быть использовано в настоящей реакции, включают гидроксиды металлов, такие как гидроксид натрия, гидроксид калия и тому подобное; карбонаты, такие как карбонат натрия, карбонат калия, бикарбонат натрия и тому подобное; гидриды металлов, такие как гидрид лития, гидрид натрия, гидрид калия и тому подобное; алкоголяты металлов, такие как метоксид натрия, этоксид натрия, трет-бутоксид калия и тому подобное; алкилметаллы, такие как н-бутиллитий, втор-бутиллитий, трет-бутиллитий и тому подобное. Количество основания, которое может быть использовано, может быть выбрано соответствующим образом в пределах от эквивалентного количества до избыточного количества по отношению к амидному производному, представленному формулой (I-3).
Примеры инертного растворителя, который может быть использован в настоящей реакции и может быть любым, пока он заметно не тормозит ход настоящей реакции, включают ароматические углеводороды, такие как бензол, толуол, ксилол и тому подобное; спирты, такие как метанол, этанол и тому подобное; простые эфиры с прямой цепью или циклические, такие как простой диэтиловый эфир, 1,2-диметоксиэтан, диоксан, тетрагидрофуран и тому подобное; амиды, такие как диметилформамид, диметилацетамид и тому подобное; диметилсульфоксид; 1,3-диметил-2-имидазолидинон и тому подобное. Такие инертные растворители могут быть использованы по отдельности или в комбинации двух или нескольких видов.
Температура реакции может находиться в пределах от -70°C до температуры кипения инертного растворителя, который может быть использован, и время реакции может находиться в пределах от нескольких минут до 50 часов, в зависимости от масштаба реакции и температуры реакции.
После завершения реакции желаемое соединение может быть выделено из реакционной смеси обычными методами, и желаемое соединение может быть подвергнуто очистке с использованием перекристаллизации или колоночной хроматографии и тому подобное, если это необходимо.
Способ получения 4
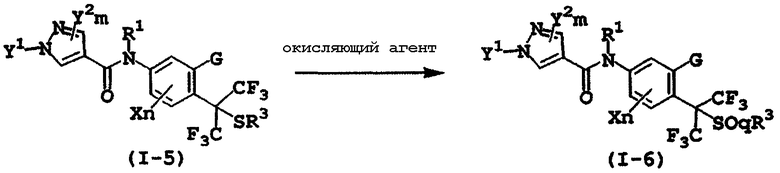
(где G, R1, R3, X, n, Y1, Y2 и m являются такими, как определено выше, и q равно 1 или 2).
Замещенные пиразолкарбоксанилидные производные, представленные формулой (I-6), могут быть получены путем взаимодействия сульфидного производного, представленного формулой (I-5), которое может быть получено по способу получения 1, с окисляющим агентом, в присутствии инертного растворителя.
Примеры инертного растворителя, который может быть использован в настоящей реакции, включают галогенированные углеводороды, такие как метиленхлорид, хлороформ и тому подобное; ароматические углеводороды, такие как толуол, ксилол и тому подобное; галогенированные ароматические углеводороды, такие как фторбензол, хлорбензол, дихлорбензол и тому подобное; кислоты, такие как уксусная кислота и тому подобное; спирты, такие как метанол, этанол, пропанол и тому подобное.
Примеры окисляющего агента включают м-пероксихлорбензойную кислоту, перуксусную кислоту, метапериодат калия, гидроперсульфат калия (оксон), перекись водорода и тому подобное. Количество окисляющего агента, который может быть использован, может быть выбрано соответствующим образом в пределах от 0,5 до 3 эквивалентов по отношению к сульфидному производному, представленному формулой (I-5).
Температура реакции может находиться в пределах от -50°C до температуры кипения инертного растворителя, который может быть использован, и время реакции может находиться в пределах от нескольких минут до 24 часов, в зависимости от масштаба реакции и температуры реакции.
После завершения реакции желаемое соединение может быть выделено из реакционной смеси обычными методами, и желаемое соединение может быть подвергнуто очистке с использованием перекристаллизации или колоночной хроматографии и тому подобное, если это необходимо.
Конкретные соединения замещенных пиразолкарбоксанилидных производных, представленных формулой (I), проиллюстрированы в таблицах 1 и 2, конкретные соединения замещенных анилиновых производных, представленных формулой (II), проиллюстрированы в таблице 3, и замещенные производные пиразолкарбоновой кислоты, представленные формулой (IV), проиллюстрированы в таблице 4, однако настоящее изобретение не должно рассматриваться как ограничиваемое ими.
В столбце "свойство" таблицы 1 и таблицы 2 показана температура плавления (°C) или коэффициент преломления (nD(°C)) и для соединений, описанных как аморфные или пастообразные, их данные 1H-ЯМР показаны в таблице 5. В таблицах, "n-" означает нормальный, и "i-" означает изо, "t-" означает третичный, "c-" означает цикло, "Me" означает метильную группу, "Et" означает этильную группу, "Pr" означает пропильную группу, "Bu" означает бутильную группу, "Pen" означает пентильную группу, "Hex" означает гексильную группу, "Ph" означает фенильную группу, "Bn" означает бензильную группу, "Ac" означает ацетильную группу и "Pyr" означает пиразинильную группу.
Формула (I-4)
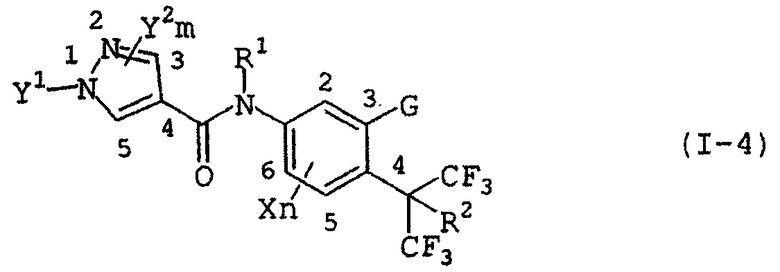
(Xn=H)
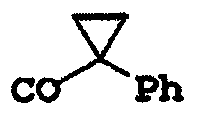
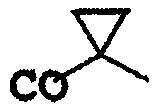
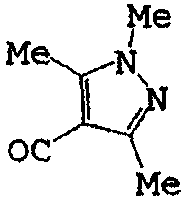
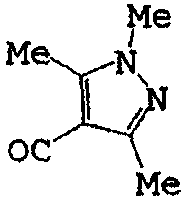
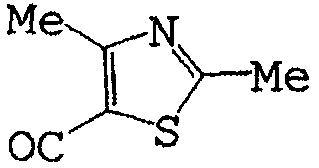
Формула (I-4)

(Y
1
=Me)
Формула (II)
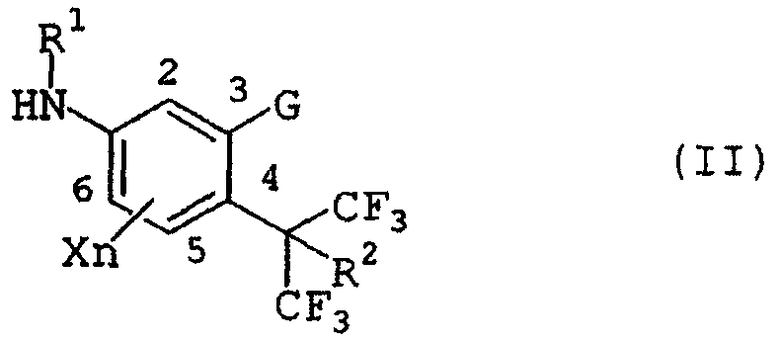
(R
1
=H)
Формула (IV)
Инсектициды или акарициды для сельского хозяйства, содержащие замещенное пиразолкарбоксанилидное производное, представленное формулой (I), или соль настоящего изобретения в качестве активного ингредиента, являются полезными для борьбы с различными вредными насекомыми, такими как вредные насекомые для сельского хозяйства, вредные насекомые для сохраняемого зерна, вредные санитарные насекомые, нематоды и тому подобное, которые приносят вред необрушенному рису, фруктовым деревьям, растениям другим сельскохозяйственным культурам, цветам и декоративным растениям, и тому подобное. Они имеют заметное инсектицидное воздействие, например, на LEPIDOPTERA, включая листовертку фруктовых деревьев (Adoxophes orana fasciata), малую чайную листовертку (Adoxophyes sp.), плодожорку маньчжурскую яблонную (Grapholita inopinata), листовертку восточную персиковую (Grapholita molesta), плодожорку соевую (Leguminivora glycinivorella), листовертку тутовую (Olethreutes mori), листовертку чайную (Caloptilia thevivora), Caloptilia sp. (Caloptilia zachrysa), яблонную минирующую моль (Phy Honor yet er ringonie11a), горностаевую моль (Spulerrina astaurota), репницу (Piers rapae crucivora), гусеницу листовертки-почкоеда табачного (Heliothis sp.), плодожорку яблонную (Laspey resia pomonella), моль капустную (Plutella xylostella), побеговую моль бурую (Argyresthia conjugella), побеговую моль персиковую (Carposina niponensis), рисовую пьявицу (Chilo_ suppressalis), рисовую листовертку (Cnaphalocrocis medinalis), огневку шоколадную (Ephestia elutella), тутовую огневку (Glyphodes pyloalis), стеблевую рисовую огневку (Scirpophaga incertulas), толстоголовку рисовую (Parnara guttata), рисовую совку (Pseudaletia separata), огневку розовую (Sesamia inferens), совку литуру (Spodoptera litura), совку малую (Spodoptera exigua) и тому подобное;
HEMIPTERA, включая цикадку шеститочечную (Macrosteles fascifrons), весеннюю рисовую цикадку (Nephotettix cincticepts), бурую рисовую цикадку (Nilaparvata lugens), белоспинную рисовую цикадку (Sogatella furcifera), восточную листоблошку (Diaphorina citri), белокрылку полосатую (Aleurolibus taonabae), табачную белокрылку (Bemisia tabaci), белокрылку тепличную (Trialeurodes vaporariorum), тлю горчичную листовую (Lipaphis erysimi), зеленую персиковую тлю (Myzus persicae), ложнощитовку восковую (Ceroplastes ceriferus), пульвинарию цитрусовую (Pulvinaria aurantii), щитовку японскую камфорную (Pseudaonidia duplex), щитовку калифорнийскую (Corastockaspis perniciosa), восточную цитрусовую щитовку (Unaspis yanonensis) и тому подобное;
TYLENCHIDA, включая хрущика блестяще-рыжего (Anomala rufocuprea), японского жука (Popillia japonica), точильщика табачного малого (Lasioderma serricorne), древогрыза темно-бурого (Lyctus brunneus), коровку крапчатую (Epilachna vigintiotopunctata), китайскую зерновку (Callosobruchus chinensis), овощного долгоносика (Listroderes costirostris), кукурузного долгоносика (Sitophilus zeamais), долгоносика-цветоеда хлопкового (Anthonomus grandis), долгоносика рисового водяного (Lissorhoptrus oryzophilus), листоеда тыквенного (Aulacophora femoralis), листоеда рисового (Ouleraa oryzae), жука-блошку полосатую (Phyllotreta striolata), большого соснового лубоеда (Tomicus piniperda), колорадского жука (Leptinotarsa decemlineata), зерновку бобовую мексиканскую (Epilachna varivestis), кукурузных жуков (Diabrotica sp.) и тому подобное;
DIPTERA, включая муху дынную (Dacus(Zeugodacus) cucurbitae), муху восточную фруктовую (Dacus(Bactrocera) dorsalis), рисовую минирующую моль (Agnomyza oryzae), муху луковую (Delia antiqua), муху ростковую (Delia platura), галлицы (Asphondylia sp.) и тому подобное;
TYLENCHIDA, включая корневые нематодыe (Pratylenchus sp.), цистообразующие картофельные нематоды (Globodera rostochiensis), корневые галловые нематоды (Meloidogyne sp.), цитрусовые нематоды (Tylenchulus semipenetrans), Aphelenchus sp. (Aphelenchus avenae), хризантемную нематоду (Aphelenchoides ritzemabosi) и тому подобное; и
ACARINA, включая красного цитрусового клеща (Panonychus citri), красного плодового клеща (Panonychus ulna), красного паутинного клеща (Tetranychus cinnabarinus), клеща Канзавы (Tetranychus Kanzawai Kishida), клещика паутинного двупятнистого (Tetranychus urticae Koch), красного чайного галлового клеща (Acaphylla theae), красного цитрусового галлового клеща (Aculops pelekassi), ложного красного клещика (Calacarus carinatus), грушевого галлового клеща (Epitrimerus pyri) и тому подобное.
Замещенное пиразолкарбоксанилидное производное, представленное формулой (I), или его соли, настоящего изобретения предпочтительно используется в качестве инсектицидов или акарицидов для сельского хозяйства. Однако соединение демонстрирует превосходное контролирующее воздействие против различных вредных насекомых, таких как вредные насекомые для леса и древесины, вредные насекомые для животноводства, санитарные вредные насекомые и тому подобное, и могут быть использованы в качестве агентов для борьбы с вредителями в различных широких областях. Примеры вредных насекомых включают: Tabanidae, такие как Tabanus rufidens Bigot; Muscidae, такие как муха комнатная (Musca domestica uicina MACQUART); Gasterophilidae, такие как желудочные оводы (Gasterophilus intestinalis); Hypodermatidae, такие как овод бычий (Hypoderma bovis L.); Phoridae, такие как Megaselia spiracularis; Culicidae, такие как бледный кулекс (Culex pipiens pallens), Anopheles sinensis, тигровый комар (Aedes albopictus) и Aedes japonicus; Pulicidae, такие как блоха кошачья (Ctenocephalides felis), блоха собачья (Ctenocephalides canis), блоха человечья (Pulex irritans); Ixodidae, такие как Ixodes ovatus Neumann; Lymantriidae, такие как Euproctis similes; Rhynchophoridae, такие как рисовый долгоносик (Sitophilus zeamais); Vespidae, такие как Vespa simillima xanthoptera Cameron; Blattellidae, такие как рыжие тараканы (Blattela germanica); Blattidae, такие как таракан американский (Periplaneta americana) и Periplaneta japonica; Pthiridae, такие как вши (Phthirus pubis); Termitidae, такие как японские термиты (Reticulitermes speratus) и домашние термиты (Coptotermes formosanus); и Ixodidae, такие как Ixodes persulcatus; и Macronyssidae, такие как тропические крысиные клещи (Ornithonyssus bacoti).
Агенты для сельского хозяйства, в частности инсектициды или акарициды для сельского хозяйства, содержащие замещенное пиразолкарбоксанилидное производное, представленное формулой (I), или его соль настоящего изобретения в качестве активного ингредиента, обладают заметным контролирующим воздействием на приведенных выше вредных насекомых, которые приносят вред сельскохозяйственным растениям на рисовых чеках, суходольным сельскохозяйственным растениям, фруктовым деревьям, растениям и другим сельскохозяйственным культурам, цветам и декоративным растениям и тому подобное. По этой причине, желаемое воздействие инсектицидов для сельского хозяйства настоящего изобретения может быть продемонстрировано путем нанесения агентов на рисовые чеки, на поле, фруктовые деревья, растения, другие сельскохозяйственные культуры, семена цветов и декоративных растений, воду в рисовых чеках, черенки и листья или на почву, в то время года, когда ожидается появление вредных насекомых, перед их появлением или во время, когда подтверждается их появление.
Растения, для которых может использоваться агент для сельского хозяйства настоящего изобретения, не являются конкретно ограниченными и включают, например, растения, показанные ниже.
Зерновые культуры (например, рис (Oryza sativa), ячмень (Hordeum vulgare), пшеницу (Triticum aestivuro L.), рожь (Secale cereale), овес (Avena), маис (Zea mays L.), гаолян и тому подобное); бобовые (соевые бобы, фасоль лучистую, конские бобы, фасоль, арахис и тому подобное); фруктовые деревья и плоды (яблоки, плоды цитрусовых, груши, виноград, персики, сливы, вишни, грецкий орех, миндаль, банан, клубнику и тому подобное); овощи (капусту, томаты, шпинат, брокколи, салат-латук, лук, лук-батун, зеленый перец и тому подобное); корнеплоды (морковь, картофель, потаты, редис, корень лотоса, репу и тому подобное); технические сельскохозяйственные культуры (хлопок, лен (Linum usitatissimum), бумажную шелковицу(Broussonetia kasinoki SIEB), эджвортию бумагоносную (Edgeworthia papyrifera), рапс (Brassica napus L.), свеклу (Beta vulgaris), хмель, сахарный тростник (Saccharum officinarum), сахарную свеклу (Beta vulgaris var. saccharifera), оливки, каучук, кофе, табак, чай и тому подобное); тыквенные (тыкву, огурец, арбуз, дыню и тому подобное); траву (садовую траву, сорго, тимофеевку луговую, клевер, люцерну и тому подобное); траву (зойсию японскую, жестковолосистые травы и тому подобное); растения для пряностей (лаванду (Lavandula officinalis CHAIX), розмарин, тимьян, петрушку, перец, имбирь и тому подобное); и цветы (хризантемы, розы, орхидеи и тому подобное).
Недавно стали развиваться генномодифицированные рекомбинантные сельскохозяйственные культуры (растения, стойкие к гербицидам, растения, стойкие к вредным насекомым, у которых инкорпорирован ген генерирования инсектицидного токсина, стойкие к заболеваниям растения, у которых инкорпорирован ген продуцирования индуктора стойкости к заболеваниям, растения с улучшенным вкусом, растения с улучшенными свойствами консервирования, растения с улучшенной урожайностью и тому подобное), технология с использованием половых феромонов насекомых (химикалии, разрушающие феромоны листоверток, капустной совки и тому подобное), IPM (встроенного контроля вредителей) с использованием природных врагов насекомых, и композиции пестицидов настоящего изобретения могут быть использованы в комбинации или в системе вместе с такими технологиями.
Агент для сельского хозяйства настоящего изобретения, как правило, приготавливается в удобных для использования формах, в соответствии с обычным способом приготовления агрохимикалиев.
То есть, замещенное пиразолкарбоксанилидное производное, представленное формулой (I), или соль настоящего изобретения и, необязательно, вспомогательное вещество смешивают с подходящим для использования инертным носителем в соответствующей пропорции и приготавливаются в форме соответствующего препарата, такого как суспензия, эмульгируемый концентрат, растворимый концентрат, смачиваемый порошок, диспергируемые в воде гранулы, гранулы, мелкодисперсный порошок, таблетки, упаковка или тому подобное, путем растворения, диспергирования, суспендирования, смешивания, импрегнации, адсорбции или прилипания.
Инертный носитель, используемый в настоящем изобретении, может быть либо твердым, либо жидким. В качестве материала, используемого в качестве твердого носителя, могут быть приведены соевая мука, зерновая мука, древесная мука, мука из коры, опилки, порошкообразные табачные черенки, измельченные в порошок скорлупки грецких орехов, отруби, порошкообразная целлюлоза, жмых, смолы, такие как порошкообразные синтетические полимеры и тому подобное, глины (например, каолин, бентонит и кислотная глина), тальки (например, тальк и пирофиллит), порошки или хлопья окиси кремния (например, диатомовая земля, кремниевый песок, слюда и белый углерод [синтетическая высокодисперсная кремниевая кислота, называемая также мелкодисперсной гидратированной окисью кремния или гидратированной кремниевой кислотой, некоторые коммерчески доступные продукты содержат силикат кальция в качестве главного компонента]), неорганические или минеральные порошки, такие как активированный уголь, порошкообразная сера, пемза, кальцинированная диатомовая земля, измельченный кирпич, зола, песок, карбонат кальция, фосфат кальция и тому подобное, пластиковые носители, такие как полиэтилен, полипропилен, поли(винилиденхлорид) и тому подобное, химические удобрения (например, сульфат аммония, фосфат аммония, нитрат аммония, мочевина и хлорид аммония) и компост. Такие носители могут быть использованы по отдельности или в виде смеси двух или более их видов.
Материал, используемый в качестве жидкого носителя, выбирают из материалов, которые сами растворяют или которые, даже без такого растворения, способны к диспергированию активного ингредиента с помощью адъюванта. Ниже представлены конкретные примеры жидкого носителя, который может быть использован по отдельности или в виде смеси двух или нескольких видов: вода, спирты (например, метанол, этанол, изопропанол, бутанол и этиленгликоль), кетоны (например, ацетон, метилэтилкетон, метилизобутилкетон, диизобутилкетон и циклогексанон), простые эфиры (например, простой этиловый эфир, диоксан, целлосолв, простой дипропиловый эфир и тетрагидрофуран), алифатические углеводороды (например, керосин и минеральные масла), ароматические углеводороды (например, бензол, толуол, ксилол, растворитель нафта и алкилнафталины), галогенированные углеводороды (например, дихлорэтан, хлороформ, четыреххлористый углерод и хлорбензол), сложные эфиры (например, этилацетат, диизопропилфталат, дибутилфталат и диоктилфталат), амиды (например, диметилформамид, диэтилформамид и диметилацетамид), нитрилы (например, ацетонитрил) и диметилсульфоксид.
Ниже представлены конкретные примеры адъюванта, который используется в зависимости от предназначения или по отдельности, или в комбинации двух или нескольких видов, или, в некоторых случаях, может не использоваться вообще.
Для эмульгирования, диспергирования, растворения и/или смачивания соединения в качестве активного ингредиента используется поверхностно-активное вещество. В качестве поверхностно-активного вещества могут быть приведены простые полиоксиэтиленалкиловые эфиры, простые полиоксиэтиленалкилариловые эфиры, сложные полиоксиэтиленовые эфиры высших жирных кислот, полиоксиэтиленрезонаты, полиоксиэтиленсорбитанмонолаурат, полиоксиэтиленсорбитан моноолеат, алкиларилсульфонат, продукты конденсации нафталинсульфоновых кислот, лигнинсульфонаты и сложные сульфатные эфиры высших спиртов.
Кроме того, для стабилизации дисперсии соединения в качестве активного ингредиента, чтобы сделать его липким и/или связать его, также могут быть использованы адъюванты, приведенные ниже, а именно могут быть использованы такие адъюванты как казеин, желатин, крахмал, метилцеллюлоза, карбоксиметилцеллюлоза, аравийская камедь, поли(виниловые спирты), терпентин, масло из высевок, бентонит и лигнинсульфонаты.
Для улучшения сыпучести твердого продукта могут быть использованы следующие адъюванты, а именно, такие как воски, стеараты, алкилфосфаты и тому подобное.
Адъюванты, такие как продукты конденсации нафталинсульфоновых кислот и поликонденсаты фосфатов, могут быть использованы в качестве активатора пластификации для диспергируемых продуктов.
Адъюванты, такие как силиконовые масла, также могут быть использованы в качестве противовспенивающего агента.
Адъюванты, такие как 1,2-бензизотиазолин-3-он, п-хлор-м-ксиленол, бутил-п-гидроксибензоат, также могут быть добавлены в качестве консерванта.
Кроме того, если это необходимо, могут быть добавлены также функциональные распределяющие агенты, усилители активности, такие как ингибитор метаболического разложения, подобный пиперонилбутоксиду, агенты антифризы, такие как пропиленгликоль, антиоксиданты, такие как BHT, поглотители ультрафиолета и другие добавки.
Содержание соединения в качестве активного ингредиента может изменяться при необходимости, и соединение в качестве активного ингредиента может быть использовано в пропорции, выбранной соответствующим образом, в пределах от 0,01 до 90 частей массовых на 100 частей агентов для сельского хозяйства. Например, в мелкодисперсных порошках или гранулах подходящее для использования содержание соединения в качестве активного ингредиента составляет от 0,01 до 50 мас.%. В эмульгируемом концентрате или смачиваемых порошках оно также составляет от 0,01 до 50 мас.%.
Агент для сельского хозяйства настоящего изобретения используется для борьбы с разнообразными вредными насекомыми следующим образом: его применяют к сельскохозяйственной культуре, на которой, как ожидается, появятся вредные насекомые, или к такому месту, где появление и рост вредных насекомых является нежелательным, как таковой или после соответствующего разбавления водой или суспендирования в воде или тому подобном, в количестве, эффективном для борьбы с вредными насекомыми.
Применяемая дозировка агента для сельского хозяйства настоящего изобретения изменяется в зависимости от различных факторов, таких как цель, вредные насекомые, с которыми должны бороться, состояния роста растения, тенденция к появлению вредных насекомых, погода, условия окружающей среды, форма препарата, способ нанесения, место нанесения и время нанесения. Она может выбираться соответствующим образом в пределах от 0,001 г до 10 кг, предпочтительно от 0,01 г до 1 кг (в терминах соединения в качестве активного ингредиента) на 10 аров, в зависимости от целей.
Агент для сельского хозяйства настоящего изобретения может использоваться в смеси с другими инсектицидами, акарицидами, нематоцидами, фунгицидами, биотическими пестицидами для сельского хозяйства или подобным, для расширения как спектра контролируемых видов вредных насекомых, так и периода времени, когда возможно эффективное нанесение, или для уменьшения дозировки. Кроме того, инсектицид для сельского хозяйства настоящего изобретения может использоваться в смеси с гербицидами, регуляторами роста растений, удобрениями или подобным, в зависимости от ситуаций с применением.
В качестве других инсектицидов, акарицидов и нематоцидов для сельского хозяйства, которые используют для указанной выше цели, могут быть приведены такие инсектициды, акарициды и нематоциды для сельского хозяйства, как этион, трихлорфон, метамидофос, ацефат, дихлорвос, мевинфос, монокротофос, малатион, диметоат, формотион, мекарбам, вамидотион, тиометон, дисульфотон, оксидепрофос, налед, метилпаратион, фенитротион, цианофос, пропафос, фентион, протиофос, профенофос, изофенфос, темефос, фентоат, диметилвинфос, хлорфенвинфос, тетрахлорвинфос, фоксим, изоксатион, пираклофос, метидатион, хлорпирифос, хлорпирифосметил, пиридафентион, диазинон, пиримифосметил, фосалон, фосмет, диоксабензофос, хиналфос, тербуфос, этопрофос, кадусафос, месульфенфос, спиродиклофен, метафлумизон, флубендиамид, DPS (NK-0795), фосфокарб, фенамифос, изоамидофос, фостиазат, исазофос, этопрофос, фентион, фостиетан, дихлофентион, тионазин, сульпрофос, фенсульфотион, диамидафос, пиретрин, аллетрин, праллетрин, ресметрин, перметрин, тефлутрин, бифентрин, фенпропатрин, циперметрин, α-циперметрин, цигалотрин, λ- цигалотрин, дельтаметрин, акринатрин, фенвалерат, эсфенвалерат, циклопротрин, этофенпрокс, галфенпрокс, силафлуофен, флуцитринат, флувалинат, меторнил, оксамил, тиодикарб, алдикарб, аланикарб, картап, метолкарб, ксиликарб, пропоксур, феноксикарб, фенобукарб, этиофенкарб, фенотиокарб, бифеназат, BPMC, карббарил, принтикарб, карбофуран, карбосульфан, фуратиокарб, бенфуракарб, альдоксикарб, диафентиоурон, дифлубензурон, тефлубензурон, гексафлумурон, новалурон, луфенурон, флуфеноксурон, хлорфлуазурон, фенбутатин оксид, гидроксид трициклогексилолова, олеат натрия, олеат калия, метопрен, гидропрен, бинапакрил, амитраз, дикофол, керзен, хлорбензилат, бромпропилат, тетрадифон, бенсультап, бензоксимат, тебуфенозид, метоксифенозид, пиридалил, хромафенозид, пропаргит, ацехинозил, эндосульфан, диофенолан, хлорфенапил, фенпироксимат, тольфенпирад, фипронил, тебуфенпирад, триазамат, этоксазол, гекситиахокс, никотин сульфат, нитенпирам, ацетамиприд, тиаклоприд, имидаклоприд, тиаметоксам, клотианидин, динотефуран, флуазинам, пирипроксифен, гидраметилнон, пиримидифен, пиридабен, циромазин, TPIC (трипропил изоцианурат), пиметрозин, клофентезин, бупрофедин, тиоциклам, фензахин, хинометионат, индоксакарб, комплексы полинактина, милбемектин, абамектин, емамектин-бензоат, спинозад, BT (Bacillus thuringiensis), азадирактин, ротенон, гидроксипропил крахмал, левамизол гидрохлорид, метам-натрий, морантель татрат, дазомет, трихламид, пастеуриа пенетранс, Monacrosporium-phymatophagum и тому подобное.
В качестве фунгицидов для сельского хозяйства, используемых для такой же цели, как указано выше, могут быть приведены такие фунгициды для сельского хозяйства, как сера, сернистая известь, основной сульфат меди, ипробенфос, эдифенфос, толклофос-метил, тирам, полкарбамат, зинеб, манеб, манкозеб, пропинеб, тиофанат, тиофанатметил, беномил, иминоктадин ацетат, иминокутадин альбецилат, мепронил, флутоланил, пенцикурон, фураметпил, тифузамид, металаксил, оксадиксил, капропамид, дихлофлунамид, флусульфамид, хлорталонил, крезоксим-метил, феноксанил, химексазол, этридиазол, фторимид, процимидон, винклозолин, ипродион, триадимефон, битертанол, трифлумизол, ипконазол, флуконазол, пропиконазол, дифеноконазол, миклобутанил, тетраконазол, гексаконазол, тебуконазол, тиадинил, имибенконазол, проклораз, пефуразоат, ципроконазол, изопротиолан, фенаримол, пириметанил, меранипирим, пирифенокс, флуазинам, трифорин, дикломезин, азоксистробин, тиадиазин, каптан, пробеназол, ацибензолар-S-метил, фталид, трициклазол, пирохилон, хинометионат, оксолиновая кислота, дитианон, касугамицин, валидомицин, полиоксин, бластицидин, стрептомицин и тому подобное.
Подобным образом, в качестве гербицидов, могут быть приведены такие гербициды, как глифосат, сульфосат, глифосинат, биалафос, бутамифос, эспрокарб, просулкарб, бентиокарб, пирибутикарб, асулам, линурон, димрон, изоурон, бенсульфурон метил, циклосульфамурон, циносульфурон, пиразосульфурон этил, азимсульфурон, имазосульфурон, тенилхлор, алахлор, претилахлор, кломепроп, этобензанид, мефенацет, пендиметалин, бифенокс, ацифлурфен, лактфен, цигалофор-бутил, иоксинил, бромбутид, аллоксидим, сетоксидим, напропамид, инданофан, пиразолат, бензофенап, пирафлуфен-этил, имазапил, сульфентразон, кафенстрол, бентоксазон, оксадиазон, паракуат, дикуат, пириминобак, симазин, атразин, диметаметрин, триазифлам, бенфлесат, флутиацет-метил, хизалофор-этил, бентазон, пероксид кальция и тому подобное.
Относительно биотических пестицидов, такое же воздействие, как указано выше, может ожидаться при использовании агента для сельского хозяйства настоящего изобретения в смеси, например, с вирусными препаратами, приготовленными из вируса ядерного полиэдроза (NPV), вируса гранулеза (GV), вируса цитоплазматического полиэдроза (CPV), вируса энтомопокс (EPV) и тому подобное; с микробными пестицидами, используемыми в качестве инсектицидов или нематицидов, такими как Monacrosporium phymatophagum, Steinernema carpocapsae, Steirxernema kushidai, Pasteuria penetrans и тому подобное; микробными пестицидами, используемыми в качестве фунгицидов, такими как Trichoderma lignorum, Agrobacterium radiobactor, непатогенная Erwinia carotovora, Bacillus subtilis и тому подобное; и биотическими пестицидами, используемыми в качестве гербицидов, такими как Xanthomonas campestris и тому подобное.
В дополнение, агент для сельского хозяйства настоящего изобретения может использоваться в сочетании с биотическими пестицидами, включая природных врагов, таких как осы-паразиты (Encarsia formosa), осы-паразиты (Aphidius colemani), галлообразующие насекомые (Aphidoletes aphidimyza), осы-паразиты (Diglyphus isaea), клещи-паразиты (Dacnusa sibirica), хищные клещики (Phytoseiulus persimilis), хищные клещики (Amblyseius cucumeris), хищные клопы (Orius sauteri) и тому подобное; микробными пестицидами, такими как Beauveria brongniartii, и тому подобное; и феромонами, такими как (Z)-10-тетрадеценилацетат, (E,Z)-4,10-тетрадекадиенилацетат, (Z)-8-додеценилацетат, (Z)-11-тетрадеценилацетат, (Z)-13-икозен-10-он и тому подобное.
Примеры
Замещенные пиразолкарбоксанилидные производные, представленные формулой (I), и замещенное анилиновое производное, представленное формулой (II), и замещенная пиразолкарбоновая кислота, представленная формулой (IV), которые являются промежуточными соединениями настоящего изобретения, описаны далее со ссылками на примеры, которые не должны рассматриваться в качестве ограничивающих.
Пример 1
Получение 1,3-диметил-5-трифторметилпиразол-4-карбоновой кислоты (соединение № 4-1)
4-Йод-1,3-диметил-5-трифторметилпиразол (8,7 г, 30 ммоль) растворяют в тетрагидрофуране (87 мл) и медленно добавляют раствор (1,6М, 28 мл) н-бутиллития в гексане в атмосфере аргона при охлаждении смесью сухой лед/ацетон (не выше -60°C). После перемешивания при -70°C в течение 30 мин смесь постепенно нагревают до комнатной температуры, продувая ее диоксидом углерода. Реакционную смесь выливают в воду, органический слой удаляют и водный слой подкисляют хлористоводородной кислотой. Водный слой экстрагируют этилацетатом. Органический слой промывают водой, сушат над сульфатом магния и концентрируют при пониженном давлении. Полученные неочищенные кристаллы промывают гексаном, с получением желаемого соединения (4,67 г) в виде кристаллов.
Выход 74%.
Свойство: температура плавления 124-125,5°C.
Пример 2
Получение N-{3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,5-диметил-3-трифторметилпиразол-4-карбоксамида (соединение № 1-211)
1,5-Диметил-3-трифторметилпиразол-4-карбоновую кислоту (2,09 г, 10 ммоль) растворяют в тионилхлориде и смесь нагревают при кипячении с обратным холодильником в течение 3 час. Смесь концентрируют при пониженном давлении с получением 1,5-диметил-3-трифторметилпиразол-4-карбонилхлорида. Полученный карбонилхлорид добавляют к раствору 3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]анилина (3,29 г, 10 ммоль) и триэтиламина (3,03 г, 30 ммоль) в тетрагидрофуране (30 мл) и смесь нагревают при кипячении с обратным холодильником в течение 2 час. Реакционную смесь разбавляют этилацетатом, промывают водой и сушат над сульфатом магния. После концентрирования при пониженном давлении полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=1:1), с получением желаемого соединения (3,64 г) в виде кристаллов.
Выход 70%.
Свойство: температура плавления 138-139°C.
Пример 3
Получение N-метоксиметил-N-{3-изобутил-4-[1-Inэтокси-2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,5-диметил-3-трифторметилпиразол-4-карбоксамида (соединение № 1-222)
Гидрид натрия (32 мг, 60%, 0,8 ммоль) суспендируют в тетрагидрофуране (10 мл) и добавляют по каплям раствор N-{3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,5-диметил-3-трифторметилпиразол-4-карбоксамида (250 мг, 0,48 ммоль) в тетрагидрофуране (5 мл). После перемешивания при комнатной температуре в течение 30 мин добавляют раствор простого хлорметилметилового эфира (64 мг, 0,8 ммоль) в тетрагидрофуране (2 мл) и смесь перемешивают в течение 5 час. Реакционную смесь выливают в разбавленную хлористоводородную кислоту и экстрагируют этилацетатом. Органический слой промывают водой, сушат над сульфатом магния, концентрируют при пониженном давлении и полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=2:1) с получением желаемого соединения (238 мг).
Выход: 88%.
Свойство: nD 1,4669 (22,4°C).
Пример 4
Получение 2-метил-5-н-пропил-4-[1,2,2,2-тетрафтор-1-(трифторметил)этил]анилина (соединение № 3-1)
5-н-Пропил-2-метиланилин (14,9 г, 0,1 моль) разбавляют смешанным растворителем (300 мл) простой трет-бутилметиловый эфир-вода (1:1) и последовательно добавляют гептафторизопропилйодид (29,6 г, 0,1 моль), гидросульфат тетрабутиламмония (3,4 г, 0,01 моль), бикарбонат натрия (8,4 г, 0,1 моль) и дитионит натрия (17 г, 0,1 моль). Смесь перемешивают в течение ночи при комнатной температуре. Реакционную смесь разбавляют гексаном, промывают дважды 3 н хлористоводородной кислотой и промывают водным раствором бикарбоната натрия и насыщенным раствором соли. Органический слой сушат над сульфатом магния и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле (гексан:этилацетат=5:1) с получением желаемого соединения (28,5 г).
Выход: 90%.
Свойство: 1H-ЯМР [CDCl3/TMS, значение δ (м.д.)] 7,09 (с, 1H), 6,54 (с, 1H), 3,76 (ушир.с, 2H), 2,63 (м, 2H), 2,13 (м, 3H), 1,58 (м, 2H), 0,96 (т, 3H).
Пример 5
Получение 4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]-2-метил-5-н-пропиланилина (соединение № 3-3)
2-Метил-5-н-пропил-4-[1,2,2,2-тетрафтор-1-(трифторметил)этил]анилин (1,6 г, 5 ммоль) растворяют в 28% растворе (9,6 г) метоксида натрия в метаноле и смесь нагревают при кипячении с обратным холодильником в течение 3 час. После того как ей дают возможность охладиться, реакционную смесь выливают в воду со льдом и экстрагируют этилацетатом. Органический слой промывают водой, сушат над сульфатом магния и концентрируют при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=5:1) с получением желаемого соединения (1,31 г).
Выход: 79%.
Свойство: 1H-ЯМР [CDCl3/TMS, значение δ (м.д.)] 7,10 (с, 1H), 6,66 (с, 1H), 3,72 (ушир.с, 2H), 3,42 (с, 3H), 2,84 (м, 2H), 2,14 (с, 3H), 1,61 (м, 2H), 1,00 (т, 3H).
Пример 6
Получение 2-метил-5-н-пропил-4-[2,2,2-трифтор-1-(трифторметил)этил]анилина (соединение № 3-2)
2-Метил-5-н-пропил-4-[1,2,2,2-тетрафтор-1-(трифторметил)этил]анилин (1,6 г, 5 ммоль) растворяют в диметилсульфоксиде (20 мл), добавляют небольшими порциями борогидрид натрия (378 мг, 10 ммоль) и смесь перемешивают при 60°C в течение 5 час. Добавляют лед небольшими порциями к реакционной смеси и затем добавляют уксусную кислоту по каплям. Реакционную смесь разбавляют этилацетатом, органический слой промывают 4 раза водой, сушат над сульфатом магния и концентрируют при пониженном давлении, с получением желаемого соединения (1,47 г).
Выход: 99%.
Свойство: 1H-ЯМР [CDCl3/TMS, значение δ (м.д.)] 7,18 (с, 1H), 6,54 (с, 1H), 4,45-4,20 (ушир., 2H), 4,27 (м, 1H), 2,50 (дд, 2H), 2,14 (с, 3H), 1,57 (м, 2H), 0,98 (т, 3H).
Пример 7
Получение N-{4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]-2-метил-5-н-пропилфенил}-1,3,5-триметилпиразол-4-карбоксамида (соединение № 2-15)
1,3,5-Триметилпиразол-4-карбонилхлорид (172 мг, 1 ммоль), 4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]-2-метил-5-н-пропиланилин (329 мг, 1 ммоль) и триэтиламин (303 мг, 3 ммоль) растворяют в тетрагидрофуране (10 мл) и смесь нагревают при кипячении с обратным холодильником в течение 3 час. Реакционную смесь разбавляют этилацетатом и промывают водой. Органический слой сушат над безводным сульфатом магния и концентрируют при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=1:2), с получением желаемого соединения (360 мг).
Выход: 77%.
Свойство: температура плавления 132-134°C.
Пример 8
Получение N-ацетил-N-{4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]-2-метил-5-н-пропилфенил}-1,3,5-триметилпиразол-4-карбоксамида (соединение № 2-16)
Гидрид натрия (32 мг, 60%, 0,8 ммоль) суспендируют в тетрагидрофуране (10 мл) и добавляют по каплям раствор N-{4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]-2-метил-5-н-пропилфенил}-1,3,5-триметилпиразол-4-карбоксамида (250 мг, 0,53 ммоль) в тетрагидрофуране (5 мл). После перемешивания при комнатной температуре в течение 30 мин добавляют раствор уксусного ангидрида (80 мг, 0,78 ммоль) в тетрагидрофуране (2 мл) и смесь перемешивают в течение одного дня. Реакционную смесь выливают в разбавленную хлористоводородную кислоту и смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над сульфатом магния, концентрируют при пониженном давлении и полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=1:3) с получением желаемого соединения (139 мг).
Выход: 52%.
Свойство: nD1,4905 (25,9°C).
Пример 9
Получение N-{2-метил-5-н-пропил-4-[2,2,2-трифтор-1-(трифторметил)этил]фенил-2-метил-5-н-пропилфенил}-1,3,5-триметилпиразол-4-карбоксамида (соединение № 2-13)
По методике примера 7, за исключением того, что 2-метил-5-н-пропил-4-[2,2,2-трифтор-1-(трифторметил)этил]анилин используют вместо 4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]-2-метил-5-н-пропиланилина, реакцию осуществляют в течение 3 час с получением желаемого соединения.
Выход: 66%.
Свойство: температура плавления 128-131°C.
Пример 10
Получение N-{3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,3,5-триметилпиразол-4-карбоксамида (соединение № 1-155)
1,3,5-триметилпиразол-4-карбонилхлорид (3,93 г, 22,8 ммоль), 3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]анилин (5,0 г, 15,2 ммоль) и триэтиламин (3,07 г, 30,4 ммоль) растворяют в тетрагидрофуране (100 мл) и смесь нагревают при кипячении с обратным холодильником в течение 5 час. Реакционную смесь разбавляют этилацетатом и промывают водой. Органический слой сушат над безводным сульфатом магния и концентрируют при пониженном давлении. Полученные неочищенные кристаллы промывают простым эфиром с получением желаемого соединения (5,62 г).
Выход: 80%.
Свойство: температура плавления 189-190°C.
Пример 11
Получение N-этоксиметил-N-{3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,3,5-триметилпиразол-4-карбоксамида (соединение № 1-145)
Гидрид натрия (29 мг, 60%, 0,73 ммоль) суспендируют в тетрагидрофуране (10 мл) и добавляют по каплям раствор N-{3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,3,5-триметилпиразол-4-карбоксамида (260 мг, 0,48 ммоль) в тетрагидрофуране (5 мл). После перемешивания при комнатной температуре в течение 30 мин добавляют раствор простого хлорметилэтилового эфира (70 мг, 0,73 ммоль) в тетрагидрофуране (2 мл) и смесь перемешивают в течение одного дня. Реакционную смесь выливают в разбавленную хлористоводородную кислоту и смесь экстрагируют этилацетатом. Органический слой промывают водой, сушат над сульфатом магния, концентрируют при пониженном давлении и полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=1:3) с получением желаемого соединения (200 мг).
Выход: 69%.
Свойство: nD1,4892 (22,4°C).
Пример 12
Получение N-изобутилоксикарбонил-N-{3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,3,5-триметилпиразол-4-карбоксамида (соединение № 1-152)
Гидрид натрия (29 мг, 60%, 0,73 ммоль) суспендируют в тетрагидрофуране (10 мл) и добавляют по каплям раствор N-{3-изобутил-4-[1-метокси-2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,3,5-триметилпиразол-4-карбоксамида (260 мг, 0,48 ммоль) в тетрагидрофуране (5 мл). После перемешивания при комнатной температуре в течение 30 мин добавляют раствор изобутилхлоркарбоната (100 мг, 0,73 ммоль) в тетрагидрофуране (2 мл) и смесь перемешивают в течение одного дня. Реакционную смесь выливают в разбавленную хлористоводородную кислоту и экстрагируют этилацетатом. Органический слой промывают водой, сушат над сульфатом магния, концентрируют при пониженном давлении и полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=1:1) с получением желаемого соединения (280 мг).
Выход: 91%.
Свойство: nD 1,4829 (22,3°C).
Пример 13
Получение N-{3-изобутил-4-[2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,3,5-триметилпиразол-4-карбоксамида (соединение № 1-123)
1,3,5-Триметилпиразол-4-карбонилхлорид (2,09 г, 10,0 ммоль), 3-изобутил-4-[2,2,2-трифтор-1-(трифторметил)этил]анилин (2,0 г, 6,69 ммоль) и триэтиламин (1,35 г, 13,4 ммоль) растворяют в тетрагидрофуране (60 мл) и смесь нагревают при кипячении с обратным холодильником в течение 5 час. Реакционную смесь разбавляют этилацетатом и промывают водой. Органический слой сушат над безводным сульфатом магния, концентрируют при пониженном давлении и полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=1:3) с получением желаемого соединения (2,41 г).
Выход: 77%.
Свойство: температура плавления 148-151°C.
Пример 14
Получение N-ацетил-N-{3-изобутил-4-[2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,3,5-триметилпиразол-4-карбоксамида (соединение № 1-125)
Гидрид натрия (38 мг, 60%, 0,96 ммоль) суспендируют в тетрагидрофуране (10 мл) и добавляют по каплям раствор N-{3-изобутил-4-[2,2,2-трифтор-1-(трифторметил)этил]фенил}-1,3,5-триметилпиразол-4-карбоксамида (300 мг, 0,64 ммоль) в тетрагидрофуране (5 мл). После перемешивания при комнатной температуре в течение 30 мин добавляют раствор ацетилхлорида (75 мг, 0,96 ммоль) в тетрагидрофуране (2 мл) и смесь перемешивают в течение одного дня. Реакционную смесь выливают в разбавленную хлористоводородную кислоту и экстрагируют этилацетатом. Органический слой промывают водой, сушат над сульфатом магния, концентрируют при пониженном давлении и полученный остаток очищают колоночной хроматографией на силикагеле (гексан:этилацетат=1:3) с получением желаемого соединения (90 мг).
Выход: 28%.
Свойство: nD 1,5021 (22,5°C).
Сравнительный пример получения 1
4-йод-1,3-диметил-5-трифторметилпиразол
Йод (30 г) растворяют в 60% серной кислоте (дымящая, 80 г) и медленно добавляют 1,3-диметил-5-трифторметилпиразол (13,12 г, 80 ммоль) при охлаждении на льду. Смесь перемешивают при 0°C в течение 2 час. Реакционную смесь выливают в воду со льдом и экстрагируют этилацетатом. Органический слой промывают водным тиосульфатом натрия и насыщенным раствором соли, сушат над сульфатом магния и концентрируют при пониженном давлении. Полученные неочищенные кристаллы промывают гексаном с получением желаемого соединения (20 г) в виде кристаллов.
Выход 86%.
Свойство: 1H-ЯМР [CDCl3/TMS, значение δ (м.д.)] 3,98 (с, 3H), 2,26 (с, 3H).
Конкретные примеры приготовления и пример исследования настоящего изобретения описаны ниже, но они не должны рассматриваться как ограничивающие объем настоящего изобретения.
Как использовано в примерах, термины "часть" и "части" являются частями по массе.
Пример приготовления 1
или табл.2
алкилбензолсульфоната кальция
Эмульгируемый концентрат приготавливают путем однородного перемешивания указанных выше ингредиентов для растворения.
Пример приготовления 2
или табл.2
Мелкодисперсный порошок приготавливают путем однородного перемешивания и измельчения указанных выше ингредиентов.
Пример приготовления 3
или табл.2
Гранулы приготавливают путем однородного смешивания указанных выше ингредиентов и замешивания полученной смеси вместе с соответствующим количеством воды с последующим гранулированием и сушкой.
Пример приготовления 4
или табл.2
Смачиваемый порошок приготавливают путем однородного смешивания и измельчения указанных выше ингредиентов.
Пример исследования 1:
Акарицидное действие на клещик паутинный двупятнистый (Tetranychus urticae)
Диск листа фасоли обыкновенной диаметром 2 см помещают на влажную фильтровальную бумагу. Десять взрослых самцов клещика паутинного двупятнистого инокулируют на каждый диск листа и опыляют 50 мл исследуемого раствора, полученного путем разбавления препарата, содержащего каждое из соединений, перечисленных в табл.1 или табл.2, в качестве активного ингредиента, для установления каждой из концентраций при 500 ч./млн, 50 ч./млн и 5 ч./млн. Через два дня после обработки считают выживших клещей. Скорректированную смертность вычисляют с помощью следующего уравнения, и акарицидную активность оценивают в соответствии с критерием, показанным ниже. Эксперимент осуществляют двукратно при условиях, при 25°C.
Критерий:
A --- Скорректированная смертность 100%
B --- Скорректированная смертность 99-90%
C --- Скорректированная смертность 89-80%
D --- Скорректированная смертность 79-50%
В качестве сравнительных соединений используют соединения №№ 1-163 и 1-164, описанные в заявке на патент Японии JP-A-2003-48878.
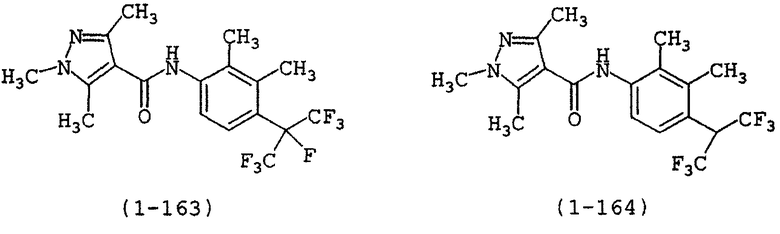
В результате приведенного выше исследования соединения №№ 1-1, 1-3, 1-4, 1-6, 1-8, 1-10, 1-12, 1-13, 1-15, 1-16, (1-25)-(1-28), 1-31, (1-34)-(1-37), 1-45, (1-47)-(1-49), (1-51)-(1-54), 1-56, 1-57, 1-59, 1-67, (1-69)-(1-72), (1-74)-(1-76), 1-89, (1-101)-(1-114), (1-120)-(1-160), (1-176)-(1-225), 1-228, 1-234, 1-246, 1-258, 1-260, 1-266, 1-270, 1-282, 1-285, 1-294, (1-306)-(1-325), (1-327)-(1-332), (1-335)-(1-337), (1-339)-(1-342), (1-344)-(1-358), (1-361)-(1-373), (1-375)-(1-380), (1-382)-(1-384), (1-386)-(1-389), (1-391)-(1-394), 1-396, (1-399)-(1-406), (1-412)-(1-416), (1-420)-(1-423), (1-425)-(1-427), (1-429)-(1-433), (1-435)-(1-439), (1-441)-(1-445), 1-448, (1-450)-(1-452), (1-454)-(1-463), (1-467)-(1-470), 1-473, 1-477, 1-478, (1-482)-(1-487), (1-489)-(1-493), (1-496)-(1-502), 1-510, 1-514, 1-515, 1-518, 1-519, (1-523)-(1-527), 1-531, (1-539)-(1-541), (1-546)-(1-549), 2-13, (2-15)-(2-17), (2-21)-(2-23), 2-25, 2-34, (2-36)-(2-39), (2-41)-(2-43) и 2-45 настоящего изобретения показывают активность A при любой концентрации, 500 ч./млн, 50 ч./млн и 5 ч./млн, и соединения №№ 1-23, 1-32, 1-78, 1-173, 1-284, 1-326, 1-334, 1-338, 1-343, 1-385, (1-397)-(1-398), 1-408, 1-410, 1-417, 1-440, 1-447, 1-449, 1-464, 1-472, 1-475, 1-476, 1-479, 1-480, (1-504)-(1-506), 1-509, 1-521, 1-529, 1-530, 1-533, 1-542, (2-26)-(2-33), 2-40 и 2-46 показывают активность A при любой концентрации, 500 ч./млн и 50 ч./млн. В противоположность этому, оба контрольные соединения не показывают акарицидной активности даже при концентрации 500 ч./млн.
В соответствии с настоящим изобретением, могут быть получены агенты для сельского хозяйства, в частности, инсектициды и акарициды, обладающие превосходными свойствами по сравнению с обычными технологиями.
Настоящая заявка основывается на заявках на патент №№ 234405/2005, 322531/2005 и 114937/2006, поданных в Японии, содержание которых включено в данное описание посредством ссылок.
Хотя настоящее изобретение показано и описано со ссылками на его предпочтительные варианты осуществления, специалистам в данной области будет понятно, что могут быть произведены различные изменения в форме и в деталях без отклонения от объема настоящего изобретения, охваченного прилагаемой формулой изобретения.
Все патенты, патентные публикации и другие публикации, идентифицированные или приведенные в данном описании, включены посредством ссылок во всей их полноте.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ N-(4-ПИРИДИЛ)НИКОТИНАМИД ИЛИ ЕГО СОЛЬ | 2018 |
|
RU2785399C2 |
| КОНДЕНСИРОВАННЫЕ 11-ЧЛЕННЫЕ СОЕДИНЕНИЯ И СОДЕРЖАЩИЕ ИХ СЕЛЬСКОХОЗЯЙСТВЕННЫЕ/САДОВОДЧЕСКИЕ ФУНГИЦИДЫ | 2015 |
|
RU2693458C2 |
| КОНДЕНСИРОВАННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ, СОДЕРЖАЩЕЕ ОКСИМНУЮ ГРУППУ, ИЛИ ЕГО СОЛЬ, СЕЛЬСКОХОЗЯЙСТВЕННЫЙ И САДОВОДЧЕСКИЙ ИНСЕКТИЦИД, ВКЛЮЧАЮЩИЙ УКАЗАННОЕ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ, И СПОСОБ ПРИМЕНЕНИЯ ИНСЕКТИЦИДА | 2017 |
|
RU2745412C2 |
| N-(1,2,5-ОКСАДИАЗОЛ-3-ИЛ)БЕНЗАМИДЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2010 |
|
RU2554349C9 |
| СРЕДСТВО ДЛЯ БОРЬБЫ С ВРЕДИТЕЛЯМИ | 2013 |
|
RU2641295C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ТРИФТОРМЕТИЛЬНЫХ ХАЛКОНОВ | 2009 |
|
RU2502720C2 |
| СОЕДИНЕНИЕ АНТРАНИЛАТА КИСЛОТЫ, ЕГО СОЛЬ, ФУНГИЦИД, ВКЛЮЧАЮЩИЙ ЭТО СОЕДИНЕНИЕ, И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2720996C2 |
| КОНДЕНСИРОВАННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ, ИМЕЮЩЕЕ ЦИКЛОАЛКИЛПИРИДИЛЬНУЮ ГРУППУ, ИЛИ ЕГО СОЛЬ, СЕЛЬСКОХОЗЯЙСТВЕННЫЙ И САДОВЫЙ ИНСЕКТИЦИД, ВКЛЮЧАЮЩИЙ ЭТО СОЕДИНЕНИЕ, И СПОСОБ ПРИМЕНЕНИЯ ЭТОГО ИНСЕКТИЦИДА | 2016 |
|
RU2676760C1 |
| ИЗОКСАЗОЛИНОВЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В БОРЬБЕ С ВРЕДИТЕЛЯМИ | 2008 |
|
RU2461546C2 |
| МЕЗОИОННЫЕ ПИРИДО[1,2-a]ПИРИМИДИНОВЫЕ ПЕСТИЦИДЫ | 2011 |
|
RU2585616C2 |
Описываются замещенные пиразолкарбоксанилидные производные формулы (I), где R1 представляет собой Н, алкил, алкилкарбонил, алкенилкарбонил, фенилалкил, фенилкарбонил; R2 представляет собой Н, галоген, алкокси; G представляет собой алкил, алкенил; Z представляет собой О; Х представляет собой Н, галоген, алкил; Y1 представляет собой алкил, алкенил; Y2 представляет собой галоген, C1-С6алкил, m равно 1 или 2; и n равно 1, и их соли, акарицид для сельского хозяйства, в качестве которого используют пиразолкарбоксанилидные производные формулы (I) и способ его применения. Описывается также промежуточное соединение формулы (II) и 1,3-диметил-5-трифторметилпиразол-4-карбоновая кислота. Техническим результатом является получение новых акарицидов, полезных в сельском хозяйстве. 5 н. и 7 з.п. ф-лы, 5 табл.
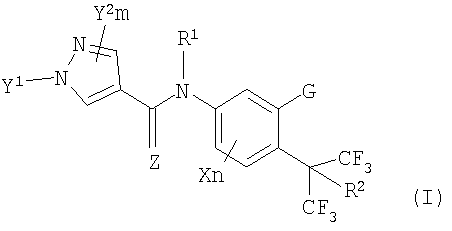
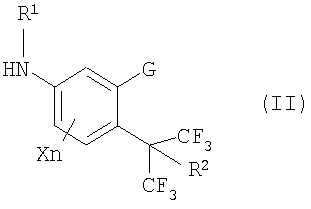
1. Замещенное пиразолкарбоксанилидное производное, представленное формулой (I):
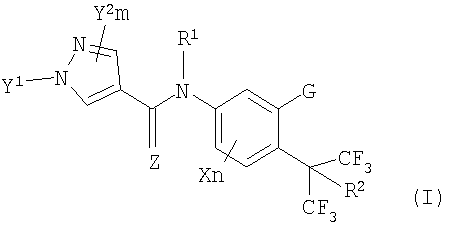
где R1 представляет собой 1а) атом водорода, 2а) С1-С8алкильную группу. 3а) галогенС1-С6алкильную группу, 4а) C1-С6алкилкарбонильную группу, 5а) галогенС1-С6алкилкарбонильную группу, 6а) С2-С6алкенилкарбонильную группу, 13а) C2-С6алкенильную группу, 17а) С1-С10алкоксиС1-С6алкильную группу, 18а) галогенС1-С6алкоксиС1-С6алкильную группу, 19а) С2-С6алкенилоксиС1-С6алкильную группу, 20а) C1-С6алкоксиС1-Сбалкокси C1-С6алкильную группу, 29а) фенилС1-С6алкоксиС1-С6алкильную группу, 31а) С1-С16алкоксикарбонильную группу, 32а) С1-С6алкоксиС1-С6алкоксикарбонильную группу, 33а) галогенС1-С6алкоксикарбонильную группу, 34а) С2-С6алкенилоксикарбонильную группу, 35а) C1-С6алкилтиокарбонильную группу, 42а) фенилС1-С6алкильную группу, 43а) замещенную фенилС1-С6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, с) нитрогруппы и d) C1-С6алкильной группы, 44а) фенилкарбонильную группу, 45а) замещенную фенилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, с) нитрогруппы, d) C1-С6алкильной группы, е) галогенС1-С6алкильной группы и f) C1-С6алкоксигруппы, 47а) замещенную гетероциклилкарбонильную группу, выбранную из пиразинкарбонильной группы, пиразолкарбонильной группы, тиофенкарбонильной группы и тиазолкарбонильной группы, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из d) C1-С6алкильной группы, 48а) феноксикарбонильную группу, 50а) феноксиС1-С6алкилкарбонильную группу, 53а) замещенную фенилсульфонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, 58а) диС1-С6алкиламинотиогруппу, где алкильные группы являются одинаковыми или различными, 59а) С3-С6циклоалкилкарбонильную группу, 61а) C1-С6алкилС3-С6циклоалкилкарбонильную группу, 63а) фенилС1-С6алкилкарбонильную группу, 65а) фенилС3-С6циклоалкилкарбонильную группу, 68а) С1-С6алкоксиС1-С6алкилкарбонильную группу, 72а) С1-С6алкилкарбонилоксиС1-С6алкильную группу, 73а) C1-С6алкилкарбонилС1-С6алкилкарбонильную группу или 74а) С1-С6алкоксикарбонилС1-С6алкилкарбонильную группу;
R2 представляет собой 1b) атом водорода, 2b) атом галогена или 7b) C1-С6алкоксигруппу;
G представляет собой 1 с) С2-С10алкильную группу, 3с) С3-С10алкенильную группу или 11 с) С3-С8циклоалкилС1-С6алкильную группу;
Z представляет собой атом кислорода;
Х могут быть одинаковыми или различными и представляют собой Id) атом водорода, 2d) атом галогена или 5d) C1-С6алкильную группу;
Y1 представляет собой 2е) C1-С6алкильную группу, 3е) галогенС1-С6алкильную группу или 4е) С2-С6алкенильную группу;
Y2 могут быть одинаковыми или различными и представляют собой 2f) атом галогена,
9f) C1-С6алкильную группу, 10f) галогенС1-С6алкильную группу или 31f) C1-С6алкилтиогруппу;
m равно 1 или 2; и
n равно 1,
или его соль.
2. Замещенное пиразолкарбоксанилидное производное по п.1, где R1 представляет собой 1а) атом водорода, 2а) С1-С8алкильную группу, 3а) галогенС1-С6алкильную группу, 4а) C1-С6алкилкарбонильную группу, 5а) галогенС1-С6алкилкарбонильную группу, 6а) С2-С6алкенилкарбонильную группу, 13а) С2-С6алкенильную группу, 17а) С1-С10алкоксиС1-С6алкильную группу, 18а) галогенС1-С6алкоксиС1-С6алкильную группу, 19а) С2-С6алкенилоксиС1-С6алкильную группу, 20а) С1-С6алкоксиС1-С6алкокси C1-С6алкильную группу, 29а) фенилС1-С6алкоксиС1-С6алкильную группу, 31а) С1-С16алкоксикарбонильную группу, 32а) С1-С6алкоксиС1-С6алкоксикарбонильную группу, 33а) галогенС1-С6алкоксикарбонильную группу, 34а) С2-С6алкенилоксикарбонильную группу, 35а) C1-С6алкилтиокарбонильную группу, 42а) фенилС1-С6алкильную группу, 43а) замещенную фенилС1-С6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, с) нитрогруппы и d) C1-С6алкильной группы, 44а) фенилкарбонильную группу, 45а) замещенную фенилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, с) нитрогруппы, d) C1-С6алкильной группы, е) галогенС1-С6алкильной группы и f) C1-С6алкоксигруппы, 47а) замещенную гетероциклилкарбонильную группу, выбранную из пиразинкарбонильной группы, пиразолкарбонильной группы, тиофенкарбонильной группы и тиазолкарбонильной группы, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из d) C1-С6алкильной группы, 48а) феноксикарбонильную группу, 50а) феноксиС1-С6алкилкарбонильную группу, 53а) замещенную фенилсульфонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, 58а) диС1-С6алкиламинотиогруппу, где алкильные группы являются одинаковыми или различными, 59а) С3-С6циклоалкилкарбонильную группу, 61 а) C1-С6алкилС3-С6циклоалкилкарбонильную группу, 63а) фенилС1-С6алкилкарбонильную группу, 65а) фенилС3-С6циклоалкилкарбонильную группу, 68а) C1-С6алкоксиС1-С6алкилкарбонильную группу, 73а) С1-С6алкилкарбонилС1-С6алкилкарбонильную группу или 74а) С1-С6алкоксикарбонилС1-С6алкилкарбонильную группу, или его соль.
3. Замещенное пиразолкарбоксанилидное производное по п.1 или 2, где R2 представляет собой 1b) атом водорода, 2b) атом галогена или 7b) C1-С6алкоксигруппу.
4. Замещенное пиразолкарбоксанилидное производное по п.1 или 2, где G представляет собой 1 с) С2-С10алкильную группу, 3с) С3-С10алкенильную группу или 11 с) С3-С8циклоалкилС1-С6алкильную группу, или его соль.
5. Замещенное пиразолкарбоксанилидное производное по п.1 или 2, где Х представляет собой 1d) атом водорода, 2d) атом галогена или 5d) C1-С6алкильную группу, или его соль.
6. Замещенное пиразолкарбоксанилидное производное по п.1 или 2, где Z представляет собой атом кислорода;
Y1 представляет собой 2е) C1-С6алкильную группу, 3е) галогенС1-С6алкильную группу или 4е) С2-С6алкенильную группу;
Y2 могут быть одинаковыми или различными и представляют собой 2f) атом галогена,
9f) C1-С6алкильную группу, 10f) галогенС1-С6алкильную группу или 31f) C1-С6алкилтиогруппу, или его соль.
7. Замещенное пиразолкарбоксанилидное производное по п.1, где R1 представляет собой 1а) атом водорода, 4а) C1-С6алкилкарбонильную группу, 5а) галогенС1-С6алкилкарбонильную группу, 17а) С1-С10алкоксиС1-С6алкильную группу, 18а) галогенС1-С6алкоксиС1-С6алкильную группу, 31а) С1-С16алкоксикарбонильную группу, 33а) галогенС1-С6алкоксикарбонильную группу или 68а) С1-С6алкоксиС1-С6алкилкарбонильную группу;
R2 представляет собой 1b) атом водорода или 7b) C1-С6алкоксигруппу;
G представляет собой 1с) С2-С10алкильную группу;
Z представляет собой атом кислорода;
Х представляет собой 1d) атом водорода;
Y1 представляет собой 2е) C1-С6алкильную группу;
Y2 могут быть одинаковьми или различными и представляют собой 2f) атом галогена,
9f) C1-С6алкильную группу или 10f) галогенС1-С6алкильную группу или его соль.
8. Акарицид для сельского хозяйства, содержащий замещенное пиразолкарбоксанилидное производное по пп.1-7 или его соль в качестве активного ингредиента.
9. Способ применения акарицида для сельского хозяйства, который включает обработку целевого растения или почвы эффективным количеством акарицида для сельского хозяйства по п.8 для борьбы с вредными организмами на полезных растениях.
10. Замещенное анилиновое производное, представленное формулой (II):
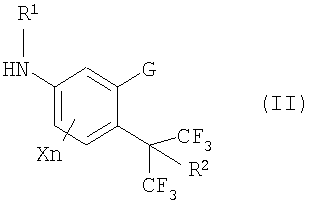
R1 представляет собой 1а) атом водорода, 2а) С1-С8алкильную группу, 3а) галогенС1-С6алкильную группу, 4а) С1-С6алкилкарбонильную группу, 5а) галогенС1-С6алкилкарбонильную группу, 6а) С2-С6алкенилкарбонильную группу, 13а) С2-С6алкенильную группу, 17а) С1-С10алкоксиС1-С6алкильную группу, 18а) галогенС1-С6алкоксиС1-С6алкильную группу, 19а) С2-С6алкенилоксиС1-С6алкильную группу, 20а) C1-С6алкоксиС1-С6алкокси C1-С6алкильную группу, 29а) фенилС1-С6алкоксиС1-С6алкильную группу, 31а) С1-С16алкоксикарбонильную группу, 32а) С1-С6алкоксиС1-С6алкоксикарбонильную группу, 33а) галогенС1-С6алкоксикарбонильную группу, 34а) С2-С6алкенилоксикарбонильную группу, 35а) C1-С6алкилтиокарбонильную группу, 42а) фенилС1-С6алкильную группу, 43а) замещенную фенилС1-С6алкильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, с) нитрогруппы и d) C1-С6алкильной группы, 44а) фенилкарбонильную группу, 45 а) замещенную фенилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, с) нитрогруппы, d) C1-С6алкильной группы, е) галогенС1-С6алкильной группы и f) C1-С6алкоксигруппы, 47а) замещенную гетероциклилкарбонильную группу, выбранную из пиразинкарбонильной группы, пиразолкарбонильной группы, тиофенкарбонильной группы и тиазолкарбонильной группы, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из d) C1-С6алкильной группы, 48а) феноксикарбонильную группу, 50а) феноксиС1-С6алкилкарбонильную группу, 53а) замещенную фенилсульфонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, 58а) диС1-С6алкиламинотиогруппу, где алкильные группы являются одинаковыми или различными, 59а) С3-С6циклоалкилкарбонильную группу, 61а) C1-С6алкилС3-С6циклоалкилкарбонильную группу, 63а) фенилС1-С6алкилкарбонильную группу, 65а) фенилС3-С6циклоалкилкарбонильную группу, 68а) С1-С6алкоксиС1-С6алкилкарбонильную группу, 72а) С1-С6алкилкарбонилоксиС1-С6алкильную группу, 73а) C1-С6алкилкарбонилС1-С6алкилкарбонильную группу или 74а) С1-С6алкоксикарбонилС1-С6алкилкарбонильную группу;
R2 представляет собой 1b) атом водорода, 2b) атом галогена или 7b) C1-С6алкоксигруппу;
G представляет собой 1с) С2-С10алкильную группу, 3с) С3-С10алкенильную группу или 11с) С3-С8циклоалкилСгСбалкильную группу;
Х могут быть одинаковыми или различными и представляют собой 1d) атом водорода, 2d) атом галогена или 5d) C1-С6алкильную группу;
n равно 1,
или его соль.
11. Замещенное анилиновое производное по п.10, где R1 представляет собой 1а) атом водорода, 2а) C1-С6алкильную группу, 3а) галогенС1-С6алкильную группу, 4а) C1-С6алкилкарбонильную группу, 5а) галогенС1-С6алкилкарбонильную группу, 17а) C1-С6алкоксиС1-С6алкильную группу, 18а) галогенС1-С6алкоксиС1-С6алкильную группу, 31а) С1-С16алкоксикарбонильную группу, 33а) галогенС1-С6алкоксикарбонильную группу, 44а) фенилкарбонильную группу или 45а) замещенную фенилкарбонильную группу, имеющую на кольце один или несколько одинаковых или различных заместителей, выбранных из а) атома галогена, b) цианогруппы, с) нитрогруппы, d) C1-С6алкильной группы, е) галогенС1-С6алкильной группы и f) C1-С6алкоксигруппы;
R2 представляет собой 1b) атом водорода, 2b) атом галогена или 7b) C1-С6алкоксигруппу;
G представляет собой 1с) С2-С10алкильную группу; и
Х представляет собой 1d) атом водорода или 5d) C1-С6алкильную группу, или его соль.
12. 1,3-Диметил-5-трифторметилпиразол-4-карбоновая кислота или его соль.
| RU 2003134631 А, 10.05.2005 | |||
| СПОСОБ ТЕЛЕУПРАВЛЕНИЯ РАКЕТОЙ | 2013 |
|
RU2537124C1 |
| EP 1253128 A1, 30.10.2002 | |||
| US 6316503 B1, 13.11.2001 | |||
| Устройство для резки проката | 1981 |
|
SU1006102A1 |
| УСТРОЙСТВО ОБРАБОТКИ ИНФОРМАЦИИ, ВСПОМОГАТЕЛЬНЫЙ СЕРВЕР ОБРАБОТКИ ИНФОРМАЦИИ И СИСТЕМА ОБРАБОТКИ ИНФОРМАЦИИ | 2007 |
|
RU2395113C1 |
| КАРБАНИЛИДЫ И СРЕДСТВО ДЛЯ БОРЬБЫ С НАСЕКОМЫМИ И ПАТОГЕННЫМИ ГРИБАМИ НА ИХ ОСНОВЕ | 1997 |
|
RU2194704C2 |
Авторы
Даты
2009-12-10—Публикация
2006-08-11—Подача