Сорбционное извлечение ионов железа из кислых хлоридных растворов относится к области извлечения веществ с использованием сорбентов и может быть использовано в цветной и черной металлургии, а также для очистки промышленных и бытовых стоков.
Известно применение катионитов и анионитов в гидрометаллургии для очистки растворов соответственно от катионов и анионов металлов [Г.М.Вольдман, А.Н.Зеликман. Теория гидрометаллургических процессов. М., Металлургия. 1993. С.263-267].
Однако применение анионитов для извлечения катионов металлов недостаточно исследовано и представляет интерес для нахождения дополнительных возможностей селективного извлечения ионов металлов из растворов сложного состава.
Наиболее близким техническим решением является извлечение ионов железа из солянокислых растворов экстракцией трибутилфосфатом [Материалы VII Международной конференции «Устойчивое развитие горных территорий в условиях глобальных изменений», Владикавказ. 2010. Воропанова Л.А., Барвинюк Н.Г., Суладзе З.А. Экстракция ионов железа из водных растворов трибутилфосфатом при переработке природного и техногенного сырья]. Лучшие результаты получены из 3 М раствора соляной кислоты при соотношении О:В=1:4 и содержании в растворе, г/дм3: 5,6 Fe (III) и 150 NaCl.
Недостатком способа является то, что не указаны возможности сорбционного извлечения железа из кислых хлоридных растворов.
Задачей, на решение которой направлено заявленное изобретение, является нахождение оптимальных условий для сорбции ионов железа на анионитах марок АМ-2б и АМП.
Техническим результатом, который может быть достигнут при осуществлении изобретения, является эффективная сорбция ионов железа на анионитах.
Этот технический результат достигается тем, что извлечение ионов железа осуществляют из солянокислых растворов, насыщенных хлоридами щелочных и щелочноземельных металлов, сорбцией при температуре 70-80°С на анионитах марок АМП, содержащих обменные группы
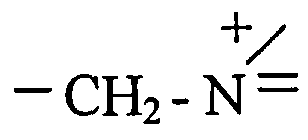
и АМ-2б, содержащих обменные группы

Сущность способа заключается в том, что ионы железа в солянокислых растворах образуют устойчивые анионные комплексы, которые могут быть извлечены из раствора на анионитах.
Известно, что хлоридная гидрометаллургия находит применение в процессах выщелачивания полиметаллических концентратов. Использование соляной кислоты вследствии повышенной ее способности к комплексообразованию интересно в схемах, включающих сорбционно-экстракционную технологию разделения металлов.
Примеры конкретного выполнения способа.
Рассмотрены возможности использования анионитов марок АМП и АМ-2б для извлечения хлоридных анионных комплексов железа из солянокислых растворов.
Пористый анионит АМ-2б смешанной основности со сферическими гранулами получен аминированием ХМС стирола и ДВБ смесью диметил- и триметиламинов. Крупность гранул 0,63-1,60 мм; удельный объем набухшей смолы 2,7-3,2 см3/г; удельная поверхность 50-100 м2/г; общий объем пор 0,80-0,87 см3/г, механическая прочность 98-99%; ПОЕ 3,3-3,7 мг-экв/г. Обменные группы

Гелевый высокоосновный анионит АМП со сферическими гранулами получен аминированием ХМС стирола и 3,5-4,0% ДВБ пиридином. Круп-ность гранул 0,63-1,60 мм; удельный объем набухшей смолы 2,7-2,9 см3/г; механическая прочность 98-99%; ПОЕ 3,3-3,7 мг-экв/г. Обменные группы:
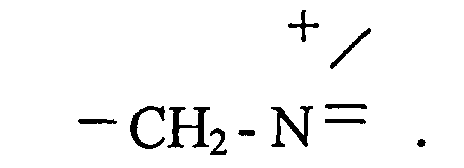
Сорбцию ионов железа осуществляли при 70-80°С из насыщенных хлоридами щелочных (NaCl) и щелочноземельных (CaCl2) металлов растворов, подкисленных до 40 г/дм3 HCl.
Объем раствора 50 см3, масса сухого сорбента 1 г.
Предварительно сорбенты в течение суток выдерживали в дистиллированной воде.
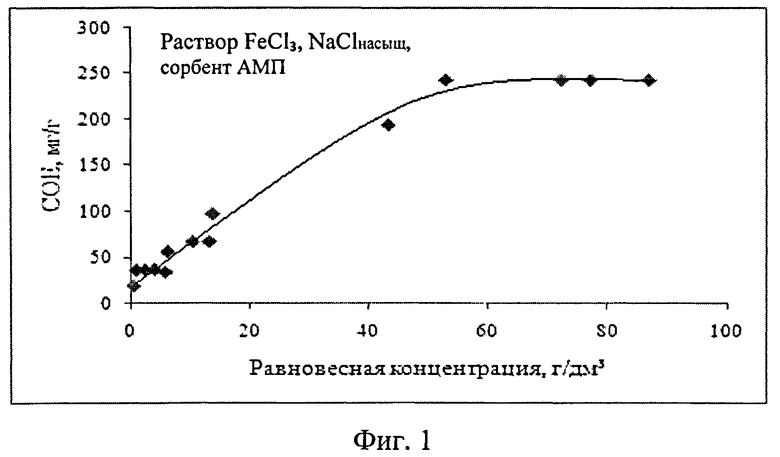
Пример 1 (табл.1, опыты 1-16; фиг.1).
В табл.1, опыты 1-16, даны результаты сорбции ионов железа при использовании сорбента марки АМП. Сорбцию осуществляли из солянокислых растворов FeCl3, содержащих хлорид натрия.
На фиг.1 даны изотермы сорбции в виде зависимостей СОЕ, мг/г, от равновесной концентрации сорбируемых ионов, полученных в условиях опытов 1-16, табл.1.
Максимальные показатели сорбции получены за время 30 мин в следующих условиях:
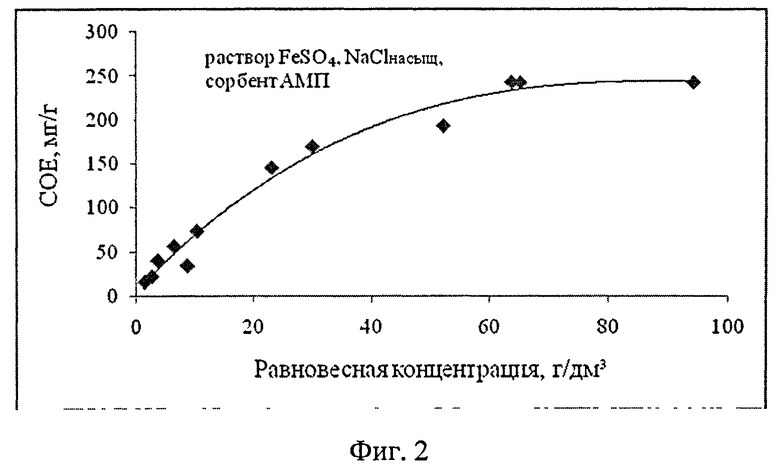
Пример 2 (табл.1, опыты 17-36; фиг.2 и 3).
В табл.1, опыты 17-36, даны результаты сорбции при использовании сорбентов марок АМП и АМ-2б. Сорбцию ионов металлов FeSO4 и FeCl3 осуществляли из солянокислых растворов, насыщенных хлоридом натрия и содержащих 40 г/дм3 HCl.
На фиг.2 даны изотермы сорбции в виде зависимостей СОЕ, мг/г, от равновесной концентрации сорбируемых ионов, полученных в условиях опытов 17-27, табл.1.
На фиг.3 даны изотермы сорбции в виде зависимостей СОЕ, мг/г, от равновесной концентрации сорбируемых ионов, полученных в условиях опытов 28-34, табл.1.
Максимальные показатели сорбции получены за время 15-30 мин в следующих условиях:
Пример 3 (табл.1).
В табл.1, опыты 37-39, даны результаты сорбции при использовании сорбентов марки АМП и АМ-2б. Сорбцию ионов FeCls осуществляли из солянокислых растворов, насыщенных хлоридами кальция, содержащих 40 г/дм3 HCl.
Максимальные показатели сорбции получены за время 15-30 мин в следующих условиях:
Пример 4 (табл.2).
В табл.2 даны результаты сорбции при использовании сорбентов марки АМП. Сорбцию ионов металлов FeSO4 и FeCl3 осуществляли из солянокислых растворов, насыщенных хлоридами натрия и кальция, содержащих 20-40 г/дм3 HCl. Извлечение железа осуществляли в процессе 5-10 циклов сорбции - десорбции.
Из данных табл.2 следует, что извлечение ионов железа увеличивается с увеличением концентрации HCl и числа циклов сорбции - десорбции.
По сравнению с прототипом показаны возможности эффективной сорбции ионов железа из кислых хлоридных растворов на анионитах марок АМП и АМ-2б.
чение,1мас.%
40 г/дм3 HCl,
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ МЕДИ (II) ИЗ КИСЛЫХ РАСТВОРОВ | 2008 |
|
RU2393245C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ СВИНЦА Pb ИЗ КИСЛЫХ РАСТВОРОВ | 2008 |
|
RU2393244C1 |
| СОРБЦИОННОЕ ИЗВЛЕЧЕНИЕ ИОНОВ КОБАЛЬТА ИЗ КИСЛЫХ ХЛОРИДНЫХ РАСТВОРОВ | 2012 |
|
RU2514242C1 |
| СОРБЦИОННОЕ ИЗВЛЕЧЕНИЕ ИОНОВ ЦИНКА ИЗ КИСЛЫХ ХЛОРИДНЫХ РАСТВОРОВ | 2008 |
|
RU2389551C1 |
| СПОСОБ СОРБЦИИ ИОНОВ РЕНИЯ (VII) ИЗ ВОДНОГО РАСТВОРА | 2009 |
|
RU2405845C2 |
| СЕЛЕКТИВНОЕ ИЗВЛЕЧЕНИЕ ИОНОВ РЕНИЯ (VII) ИЗ ВОДНЫХ РАСТВОРОВ КАТИОНОВ МЕТАЛЛОВ | 2009 |
|
RU2405846C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ ЖЕЛЕЗА (III) ИЗ ВОДНОГО РАСТВОРА | 2009 |
|
RU2394776C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ МАРГАНЦА (VII) ИЗ РАСТВОРА | 2005 |
|
RU2288963C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ НИОБИЯ ИЗ ФТОРСОДЕРЖАЩЕГО ВОДНОГО РАСТВОРА | 2010 |
|
RU2421531C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ НИОБИЯ (V) ИЗ ФТОРСОДЕРЖАЩЕГО ВОДНОГО РАСТВОРА | 2010 |
|
RU2430173C1 |

Сорбционное извлечение ионов железа из кислых хлоридных растворов относится к области извлечения веществ с использованием сорбентов и может быть использовано в цветной и черной металлургии, а также для очистки промышленных и бытовых стоков. Извлечение ионов железа осуществляют сорбцией на анионитах из солянокислых растворов, насыщенных хлоридами щелочных и щелочноземельных металлов, при температуре 70-80°С. При этом сорбцию ведут на анионитах, выбранных из марок: АМП, содержащего обменные группы , и АМ-2б, содержащего обменные группы
, и АМ-2б, содержащего обменные группы 
Способ извлечения ионов железа из солянокислых растворов, насыщенных хлоридами щелочных и щелочноземельных металлов, отличающийся тем, что извлечение осуществляют сорбцией при температуре 70-80°С на анионитах, выбранных из марок: АМП, содержащего обменные группы
 ,
,
и АМ-2б, содержащего обменные группы
 .
.
| Способ очистки растворов,содержащих цветные металлы,от железа | 1984 |
|
SU1235957A1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ ЖЕЛЕЗА (III) ИЗ ВОДНОГО РАСТВОРА | 2009 |
|
RU2394776C1 |
| СПОСОБ СОРБЦИОННОГО ИЗВЛЕЧЕНИЯ ЖЕЛЕЗА ИЗ РАСТВОРОВ НИТРАТНЫХ СОЛЕЙ | 2011 |
|
RU2453368C1 |
| GB 1466150 A, 02.03.1977 | |||
| WO 9922933 A1, 14.05.1999 | |||
| US 4952321 A, 28.08.1990 | |||
| US 2004000523 A1, 01.01.2004 | |||
| WO 2011156255 A2, 15.12.2011/ | |||
Авторы
Даты
2014-04-27—Публикация
2012-09-28—Подача