Изобретение относится к экологии и токсикологии и может быть использовано для оценки токсичности воды и донных отложений Азовского и Черного морей как в условиях хозяйственной деятельности, так и в аварийных ситуациях.
Известно, что при действии различных экологических факторов и антропогенных загрязнений на водные экосистемы в первую очередь изменяется фотосинтетическая активность клеток фотосинтезирующих организмов. Эти изменения в дальнейшем приводят к изменениям во всех остальных звеньях экосистемы.
Для оценки токсичности вод Азово-Черноморского бассейна используются штамм люминесцирующих бактерий Ph. phosphoreum (Cohn) Ford (И.Ю.Малыгина, А.М.Кацев. Светящиеся бактерии Черного и Азовского морей. Экология моря. 2003. Вып. 64) (1), бактериальный тест «Эколюм», разработанный в России (ТУ 6-09-20-236-93, МГУ, Москва) (2), штаммы бактерий Vibrio fischeri ВКПМ В-9579 (Патент на изобретение РФ №2346035. МКИ C12N 1/20 2007) (3) и Vibrio fischeri ВКПМ В-9580 (Патент на изобретение РФ №2342434 МКИ C12N 1/20) (4). Эти штаммы выделены из воды Черного моря. Биотестирование основано на чувствительности биолюминесцентных бактерий к действию токсикантов, присутствующих в воде и донных отложениях морских водоемов. В известных способах оценка токсичности основана на определении изменения интенсивности биолюминесценции бактерий при воздействии токсических веществ, присутствующих в анализируемой пробе, по сравнению с контролем. Однако содержание бактериальных культур требовательно к условиям культивирования, необходимо их частое пересевание, что приводит к большим затратам труда и средств. Кроме того, известны случаи утраты штаммом биолюминесцентной активности (свойств) в процессе хранения.
Для контроля морских вод Азово-Черноморского бассейна, кроме бактериальных клеток, можно использовать другие организмы, например клетки водорослей. Водоросли, как и все автотрофы, играют жизненно важную роль в пищевой сети экосистемы. Нарушение токсинами их физиологической активности, равно как и самой структуры альгоценоза, имеют серьезные последствия для экосистем. Методы исследования фитопланктона, основанные на измерении флуоресценции, в настоящее время находят широкое применение как в лабораторных условиях на экспериментальных культурах водорослей, так на водоемах, в полевых условиях. Измеряя флуоресценцию фитопланктона, можно рассчитать концентрацию хлорофилла у микроводорослей (Гольд В.М., Гаевский Н.А., Шатров И.Ю., Попельницкий В.А., Рубцов С.А. Опыт использования флуоресценции для дифференциальной оценки содержания хлорофилла а у планктонных водорослей// Гидробиол. журн. 1986. Т. 22, №3) (5).
Известен способ определения токсичности воды (АС СССР №1405745 МКИ А01K 61/00, G01N 33/18) (6), в котором контролируют изменение интенсивности выхода пигментов в среду под действием токсических соединений, где в качестве пигментсодержащего тест-объекта используют морские красные водоросли рода Callithamnion. Стандартными международными методами биотестирования морской воды, разработанными под эгидой ISO (International Standard Organization), являются тест-системы с использованием микроводорослей Phaeodactylum tricornutum и Skeletonema costatum (Water quality - Algal growth inhibition test with Skeletonema costatum and Phaeodactylum tricornutum. Draft International Standard ISO/DIS 10253.2. 1994. 12 p.) (7).
Анализы на микроводорослях дают статистическое преимущество перед многими тест-объектами, так как можно легко использовать большее количество клеток, требуются намного меньшие объемы проб и время тестирования, содержание запасных культур, вследствие их редкого пересевания и низкой требовательности к условиям культивирования, не требует больших затрат труда и средств. Процесс тестирования легко автоматизировать.
Наиболее близким решением является выбранный в качестве прототипа способ оценки токсичности жидкости (авт.свид. СССР №1515105 МКИ G01N 33/18) (8), предусматривающий культивирование фотосинтетического тест-объекта, возбуждение свечения тест-объекта и определение флуоресцентных характеристик, по изменению которых судят о токсичности контролируемой жидкости.
При использовании водорослей для оценки токсичности морских вод в различных морях не всегда достигается адаптация тест-объекта к конкретным водам, что снижает достоверность полученных результатов. В частности, при оценке токсичности природных вод, не соответствующих естественному гидрохимическому составу воды, в которой выращивалась культура тест-объекта, реакция этого тест-объекта может расцениваться как токсическое воздействие исследуемой воды. Поэтому поиск тест-объектов в Азовском и Черном морях был направлен на подбор микроводорослей, которые могли бы служить в качестве тест-объекта загрязнителей вод Азовского и Черного морей.
Задача, решаемая изобретением, - расширение числа тест-объектов для оценки токсичности морских вод Азово-Черноморского бассейна, а также повышение достоверности информации при оценке токсичности среды. Поставленная задача достигается тем, что в известном способе, включающем помещение флуоресцирующих тест-объектов в контрольные и анализируемые пробы, облучение возбуждающим светом, определение флуоресцентных характеристик, по изменению которых судят о токсичности контролируемой среды, согласно изобретению, качестве тест-объектов используют микроводоросли вида Scenedesmus apiculatus, которые предварительно выделяют из экологически чистого района исследуемого водоема.
Использование в качестве тест-объекта микроводоросли Scenedesmus apiculatus расширяет число тест-объектов для оценки токсичности морских вод Азово-Черноморского бассейна и удешевляет тестирование.
При этом использование в качестве тест-объекта аборигенных водорослей Scenedesmus apiculatus, выделенных из экологически чистых районов Азовского и Черного морей как наиболее адаптированных к среде исследуемых водоемов, позволит снизить ошибки и значительно повысить чувствительность флуоресцентного биотестирования.
Совокупность отличительных признаков описываемого способа обеспечивает достижение поставленной задачи.
Сравнение прототипа с заявляемым решением показало, что указанные выше признаки являются отличительными, в связи с чем заявляемый способ соответствует критерию "новизны".
Способ осуществляется следующим образом.
Из экологически чистых районов Азовского и Черного морей отбирают пробы воды. Методами многократных разведений и пересевов из отобранных проб выделяют зеленую водоросль вида Scenedesmus apiculatu, которую используют в качестве тест-объекта. Суспензии микроводорослей помещают в контрольные (без токсикантов) пробы и анализируемые пробы. Воздействуют на пробы возбуждающими импульсами света для возбуждения флуоресценции тест-объектов. Определяют флуоресцентные характеристики тест-объектов, по изменению которых судят о токсичности анализируемых проб.
Пример 1. Из экологически чистых районов Азовского и Черного морей в мае-июне 2008 г., т.е. в период активной вегетации основных видов микроводорослей, были отобраны пробы воды. В этот период в Азовском и Черном морях вегетируют водоросли 7 отделов: Cyanophyta, Chrysophyta, Bacillariophyta, Dinophyta, Cryptophyta, Chlorophyta, Euglenophyta. Методами многократных разведений и пересевов из отобранных проб было выделено 5 альгологически и бактериологически чистых культур отдельных видов зеленых и сине-зеленых водорослей. По таксономической принадлежности 3 выделенных штамма относились к сине-зеленым водорослям (Cyanophyta), и 2 штамма - к зеленым водорослям (Chlorophyta). Сине-зеленые водоросли определены как Oscillatoria laetevirens (Crouan) Gom. (=Phormidium laetevirens (Crouan et Gom.) Anagn. et. Kom.), Oscillatoria Agardhii Gom. (=Planktothrix Agardhii (Gom.) Anagn. et. Kom.) и Snowella rosea (Snow) Elenkin; зеленые - как Oocystis borgei Snow и Scenedesmus apiculatus (W. et W.) Chod. Выделенные штаммы водорослей были подготовлены к спектральному анализу. Суспензии микроводорослей поместили в контрольные (без токсикантов) пробы воды. Спектры флуоресценции растворов, содержащих микроводоросли, регистрировали на спектрофлуорофотометре RF-5301PC фирмы Shimadzu (Япония). С помощью программы Panorama fluorescence 1.1 в режиме сканирования (2D synchro measurement) был проведен анализ спектров возбуждения и люминесценции и по результатам их синхронизации для каждого штамма выбраны длины волн с характерными максимумами возбуждения.
На следующем этапе работы определяли чувствительность выделенных культур микроводорослей к действию стандартных токсикантов. Оценку чувствительности проводили по относительному различию в интенсивности биолюминесценции контрольной и опытной проб. Суспензию микроводорослей вносили в пробы с бихроматом калия K2Cr2O7 (концентрации раствора от 0.001 до 100 мг/л), сульфатом меди CuSO4 (концентрации от 0.0001 до 100 мг/л) и фенолом (5-1500 мг/л). Время экспозиции составляло от 10 до 30 мин. Отклик микроводорослей на воздействие выбранных токсикантов исследовали, возбуждая свечение в области максимумов, установленных для каждого штамма водоросли. При этом регистрировали спектры флуоресценции, фиксируя изменения интенсивности свечения при установленных максимумах эмиссии.
По результатам исследований чувствительности всех выделенных культур микроводорослей к действию стандартных токсикантов - бихромату калия (K2Cr2O7), сульфату меди (CuSO4) и фенолу были отобраны наиболее чувствительные (перспективные для биотестирования) виды микроводорослей Scenedesmus apiculatus и Snowella rosea.
Изменение чувствительности выделенных видов микроводорослей при воздействии стандартных токсикантов и интенсивность флуоресценции (в условных единицах свечения, УЕС) микроводорослей Scenedesmus apiculatus и Snowella rosea в опыте даны в табл.1, 2, 3.
Из таблицы 1 видно, что под влиянием K2Cr2O7 (0.01-10 мг/л) (ПДК 0.05 мг/л) интенсивность флуоресценции (λвозб. 220 нм, λэмисс. 366 нм) культуры Scenedesmus apiculatus снижалась максимально до 45-50% от контрольного уровня (в зависимости от времени экспозиции и условий флуориметрии).
Для культуры Snowella rosea в присутствии таких же концентраций K2Cr2O7 установлено максимальное увеличение интенсивности флуоресценции до 60% (λвозб. 340 нм, λэмисс. 440 нм).
Более высокие концентрации K2Cr2O7 (на уровне 50-100 мг/л) на 45-99% подавляли флуоресценцию обеих культур водорослей.
Из таблицы 2 видно, что в растворах CuSO4 (0.01-10 мг/л) Scenedesmus apiculatus проявлял аналогичную чувствительность, о чем свидетельствовало снижение интенсивности флуоресценции (λвозб. 220 нм, λэмисс.366 нм) максимально на 50% от контрольного уровня. В растворе с концентрацией CuSO4 100 мг/л наблюдалось практически полное тушение флуоресценции суспензии Scenedesmus apiculatus.
Под влиянием низких концентраций CuSO4 (0.0001-1.0 мг/л) спектры флуоресценции Snowella rosea заметно не изменялись. Максимально высокая индукция свечения (до 25% от контроля, λвозб. 340 нм, λэмисс. 440 нм) зарегистрирована в растворе CuSO4 с концентрацией 1.0 мг/л. Экспозиция водоросли в культуральной среде с CuSO4 в концентрации 10 и 100 мг/л вызывает тушение свечения на 25 и 30%. Следовательно, чувствительность культуры Snowella rosea к CuSO4 была приблизительно в 2 раза ниже, чем Scenedesmus apiculatus.
Из таблицы 3 видно, что фенол в концентрации 5 мг/л ингибировал флуоресценцию Scenedesmus apiculatus (λвозб. 220 нм, λэмисс. 366 нм) на 10-55%, а в растворе с содержанием фенола 50 мг/л тушение флуоресценции достигало почти 100%. В то же время, Snowella rosea проявляла низкую чувствительность к фенолу: интенсивность флуоресценции в 1.5 раза ингибировала лишь концентрация фенола 1000 мг/л.
Пример 2. Для сравнительной оценки чувствительности использовали характеристику ЕС50 (effective concentration) - концентрацию вещества, вызывающую 50%-ное снижение биолюминесценции суспензии микроводорослей.
Использование показателя ЕС50 (эффективная концентрация токсиканта, снижающая люминесценцию на 50%) позволило сравнить чувствительность выделенных водорослей Scenedesmus apiculatus и Snowella rosea с чувствительностью биолюминесцентных бактерий Е. coli РТ-5, Ph. phosphoreum (Cohn) Ford и штаммов аборигенных бактерий Vibrio fischeri ВКПМ В-9579 и Vibrio fischeri ВКПМ В-9580, выделенных из воды Азовского и Черного морей (таблица 4).
Сравнение чувствительности аборигенных микроводорослей к исследованным токсическим веществам (табл.4) показало в 2 раза более высокую чувствительность микроводоросли Scenedesmus apiculatus по сранению с чувствительностью Snowella rosea. Поэтому для тестирования в качестве тест-объекта была выбрана микроводоросль Scenedesmus apiculatus.
Сравнение чувствительности аборигенной микроводоросли Scenedesmus apiculatus по средним значениям EC50 к исследованным токсическим веществам показало, что Scenedesmus apiculatus более чувствителен, чем штамм Ph. phosphoreum (Cohn) Ford. В частности, в среднем он примерно на порядок более чувствителен к K2Cr2O7. Так, величина EC50 у микроводоросли Scenedesmus apiculatus по бихромату калия находится в диапазоне концентраций от 10 до 50 мг/л, а для Ph. phosphoreum составляет 250 мг/л.
По фенолу величина EC50 для микроводоросли Scenedesmus apiculatus составила 5-30 мг/л, что также на порядок ниже, чем EC50 для Ph. phosphoreum.
Сравнение чувствительности микроводоросли Scenedesmus apiculatus к токсическим веществам с чувствительностью lux-штамма E.coli РТ-5 показало аналогичные результаты, за исключением CuSO4. Микроводоросль Scenedesmus apiculatus более чувствительна к K2Cr2O7, (~ в 5 раз), а также к фенолу (примерно на порядок), но уступает по чувствительности к CuSO4 (~ в 4 раза).
Полученные данные свидетельствуют о перспективности использования микроводоросли Scenedesmus apiculatus для определения токсичности водных сред.
Пример 3. Проводили проверку чувствительности используемой в качестве тест-объекта водоросли вида Scenedesmus apiculatus, выделенной из воды Черного и Азовского морей. Из экологически чистых районов Азовского и Черного морей были отобраны пробы воды. В них помещали микроводоросли Scenedesmus apiculatus, отобранные из разных морей.
Как показали исследования, культуры Scenedesmus apiculatus из разных морей, помещенные в «родные» и «неродные» среды, отличались интенсивностью флуоресценции (λвозб. 220 нм, λэмисс. 366 нм) в пределах 12-17% в зависимости от условий экспозиции (таблица 5).
Таким образом, аборигенные водоросли, помещенные в «неродную» среду, показывали в 2-3 раза большие отклонение уровня флуоресценции от такового у микроводорослей, помещенных в «родную» среду. Такое отклонение может искажать результаты измерения токсичности проб в «неродной» среде, что указывает на необходимость использования аборигенных микроводорослей (как наиболее адаптированных к условиям данного водоема) в практике биотестирования воды и водных экстрактов донных отложений.
Пример 4. Были проведены эксперименты по определению токсичности компонентов среды (вода, донные отложения) Черного моря с использованием аборигенной микроводоросли Scenedesmus apiculatus в качестве тест-объекта. Были исследованы 3 пробы воды и 3 пробы донных отложений, отобранных в районе с высоким антропогенным загрязнением (акватория черноморского порта). Для подготовки экстрактов донных отложений в качестве растворителя использовали чистую морскую воду Черного моря, предварительно профильтрованную через бактериальный фильтр, в весовом соотношении 10:1 с высушенным при комнатной температуре грунтом. Пробы донных отложений встряхивали на орбитальном шейкере при 65 об/мин при комнатной температуре в течение одного часа и затем отстаивали до оседания взвеси. Отстоявшиеся экстракты фильтровали через сифон (капроновая сеть №76) и использовали в дальнейших исследованиях токсичности.
Токсичность воды и водных экстрактов донных отложений определяли по изменению интенсивности флуоресценции Scenedesmus apiculatus (λвозб. 220 нм, λэмисс. 366 нм) относительно контроля (чистая морская вода Черного моря). Время экспозиции - 10 мин. При этом отклонение интенсивности свечения в тестируемой пробе относительно контроля (как в сторону уменьшения, так и в сторону увеличения) менее 20% свидетельствует об отсутствии токсичности, от 20 до 30% - о слабой токсичности, от 30 до 50% - умеренной токсичности, свыше 50% - об острой токсичности.
Результаты исследований приведены в таблице 6.
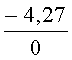
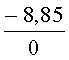
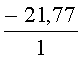



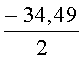

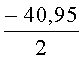
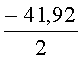
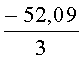
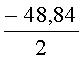
По результатам тестирования, снижение интенсивности флуоресценции относительно контроля в пробах воды №1, 2 и 3 в зависимости от времени экспозиции, составило, соответственно, -4.27 - -8.85%; -21.77 - -10.67% и -8.52 - -13.42%, что в соответствии с представленной выше шкалой, характеризует пробы воды №1 и 3 как не токсичные, пробу №2, в зависимости от условий тестирования - как не токсичную - слабо токсичную.
Интенсивность флуоресценции в экстрактах донных отложений №1,2 и 3 в зависимости от времени экспозиции снизилась относительно контроля соответственно на -34.49 - -34.86%, -40.95 - -41.92% и -52.09 - - 48.84%. По результатам флуориметрии донные отложения №1 и 2 оцениваются, таким образом, как умеренно токсичные, проба №3 - как остро токсичная. Полученные результаты тестирования свидетельствуют об умеренной токсичности проб донных отложений №1 и 2 и острой токсичности - пробы №3. В пробе донных отложений №3, по аналитическим данным, отмечались максимально высокие для исследованной акватории порта содержания нефтепродуктов (32.6 г/кг сухого грунта), АПАВ (91 мг/кг), фенола (4.1 мг/кг) и полициклических ароматических углеводородов (1010 мкг/кг).
Испытание метода биотестирования воды и донных отложений, отобранных в районе с высоким антропогенным загрязнением (морской порт) с использованием Scenedesmus apiculatus в качестве тест-объекта, позволило по изменению интенсивности флуоресценции (λэмисс. 366 нм) установить токсичность проб воды и донных отложений. При этом значения токсичности для проб воды были ниже, чем для экстрактов донных отложений и в ряде случаев коррелировали с содержанием в пробах поверхностно-активных веществ, нефтепродуктов и фенола.
В целом высокая чувствительность выделенных культур водорослей к испытанным токсикантам и апробация метода биотестирования на основе Scenedesmus apiculatus в акватории Черного моря свидетельствуют о перспективности использования выделенных культур микроводорослей в качестве тест-объектов для определения токсичности компонентов среды морских водоемов в условиях комплексного антропогенного загрязнения.
Разрабатываемый метод биотестирования может применяться как для экспресс-оценки содержания токсических веществ в жидкостях, например, при сбросах в окружающую среду сточных (сбросных) вод, так и для непрерывного контроля токсичности окружающей среды, в том числе при аварийных случаях и неблагоприятных экологических ситуациях.
Заявляемый способ определения токсичности выгодно отличается от подобных систем более высокой чувствительностью к токсикантам (возможна регистрация токсического эффекта токсиканта на уровне его ПДК для воды рыбохозяйственного водоема), экспресс-реакцией (результаты анализа регистрируются в течение часа), безинерционностью (свет, возбуждающий флуоресценцию, мало меняет физиологическое состояние тест-объекта), низкой стоимостью анализа.
Литература
1. И.Ю.Малыгина, А.М.Кацев. Светящиеся бактерии Черного и Азовского морей. Экология моря. 2003. Вып. 64.
2. ТУ 6-09-20-236-93
3. Патент на изобретение РФ №2346035. МКИ C12N 1/20.
4. Патент на изобретение РФ №2342434 МКИ C12N 1/20.
5. Гольд В.М., Гаевский Н.А., Шатров И.Ю., Попельницкий В.А., Рубцов С.А. Опыт использования флуоресценции для дифференциальной оценки содержания хлорофилла у планктонных вддорослей//Гидробиол. журн. 1986. Т. 22, №3.
6. Авторское свидетельство СССР №1405745, МПК А01K 61/00, G01N 33/18.
7. Water quality - Algal growth inhibition test with Skeletonema costatum and Phaeodactylum tricornutum. Draft International Standard ISO/DIS 10253.2. 1994. 12p.
8. Авторское свидетельство СССР №1515105 МКИ G01N 33/18 (прототип).
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ VIBRIO AQUAMARINUS, СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ПРОБ С ЕГО ПОМОЩЬЮ И ТЕСТ-КУЛЬТУРА ДЛЯ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ПРОБ | 2012 |
|
RU2534819C2 |
| ШТАММ БАКТЕРИЙ VIBRIO FISCHERI, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ТЕСТ-КУЛЬТУРЫ ДЛЯ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ОБЪЕКТОВ ОКРУЖАЮЩЕЙ СРЕДЫ | 2007 |
|
RU2342434C1 |
| ШТАММ БАКТЕРИЙ Vibrio fischeri, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ТЕСТ-КУЛЬТУРЫ ДЛЯ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ОБЪЕКТОВ ОКРУЖАЮЩЕЙ СРЕДЫ | 2007 |
|
RU2346035C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ КОНТАКТНОЙ ЗОНЫ "ГРУНТ-ВОДА" | 2007 |
|
RU2358264C2 |
| Термофильный штамм водоросли Chlorella vulgaris Beijer для оперативного биотестирования токсичности водных сред | 2023 |
|
RU2819768C1 |
| СПОСОБ БИОТЕСТИРОВАНИЯ ТОКСИЧНОСТИ ВОДНОЙ СРЕДЫ | 2011 |
|
RU2462707C1 |
| Способ полевого биотестирования поверхностных вод на загрязненность нефтью и нефтепродуктами | 2023 |
|
RU2813895C1 |
| СПОСОБ БИОТЕСТИРОВАНИЯ ПРИРОДНЫХ, СТОЧНЫХ ВОД И ВОДНЫХ РАСТВОРОВ | 2001 |
|
RU2222003C2 |
| Способ оценки токсичности жидкости | 2018 |
|
RU2682673C1 |
| СПОСОБ БИОТЕСТИРОВАНИЯ ТОКСИЧНОСТИ ВОД И ВОДНЫХ РАСТВОРОВ | 2011 |
|
RU2482474C2 |
(57) Изобретение относится к области экологии и предназначено для оценки токсичности воды и донных отложений Азовского и Черного морей. Способ включает помещение флуоресцирующих тест-объектов в контрольные и анализируемые пробы, облучение возбуждающим светом, определение флуоресцентных характеристик, по изменению которых судят о токсичности контролируемой среды. В качестве тест-объектов используют микроводоросли вида Scenedesmus apiculatus, которые предварительно выделяют из экологически чистых районов исследуемых водоемов. Использование заявленного способа позволяет быстро и точно дать оценку токсичности вод и донных отложений Азовского и Черного морей. 6 табл., 4 пр.
Способ оценки токсичности компонентов среды Азовского и Черного морей включающий помещение флуоресцирующих тест-объектов в контрольные и анализируемые пробы, облучение возбуждающим светом, определение флуоресцентных характеристик, по изменению которых судят о токсичности контролируемой среды, отличающийся тем, что в качестве тест-объектов используют микроводоросли вида Scenedesmus apiculatus, которые предварительно выделяют из экологически чистых районов исследуемых водоемов.
| САКСОНОВ М.Н | |||
| И ДР | |||
| Влияние ряда токсикантов на люминесценцию клеток водорослей// XII Международная школа-cеминар по люминесценции и лазерной физике, 26-31 июля 2010, Иркутск, 2010, с.188, 189 | |||
| Способ оценки токсичности жидкости | 1987 |
|
SU1515105A1 |
| ШТАММ БАКТЕРИЙ Vibrio fischeri, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ТЕСТ-КУЛЬТУРЫ ДЛЯ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ОБЪЕКТОВ ОКРУЖАЮЩЕЙ СРЕДЫ | 2007 |
|
RU2346035C1 |
| CN102465167 A, 23.05.2012 | |||
Авторы
Даты
2014-06-10—Публикация
2013-05-08—Подача