Область техники, к которой относится изобретение
Предоставлена фармацевтическая композиция в виде разовой пероральной дозы, содержащая а) леводопу или ее соли в количестве от приблизительно 50 мг до приблизительно 300 мг в форме пролонгированного высвобождения, b) карбидопу или ее соли в количестве от приблизительно 10 мг до приблизительно 100 мг в форме пролонгированного высвобождения и с) энтакапон или его соли в количестве от приблизительно 100 мг до приблизительно 1000 мг в форме продолжительного высвобождения, необязательно с другими фармацевтически приемлемыми эксципиентами. Изобретение также относится к способу получения подобных композиций.
Уровень техники
Энтакапон, ингибитор катехин-O-метилтрансферазы (СОМТ), используется при лечении болезни Паркинсона в качестве вспомогательного средства к терапевтическому лечению леводопой/карбидопой. Химическое название энтакапона - (Е)-2-циано-3-(3,4-дигидрокси-5-нитрофенил)-N,N-диэтил-2-пропенамид. Его эмпирическая формула C14H15N3O5, а структурная формула
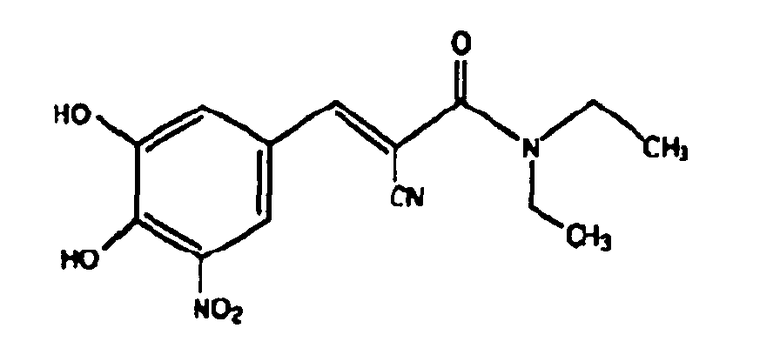
Карбидопа, ингибитор декарбоксилирования ароматических аминокислот, представляет собой кристаллическое соединение белого цвета, малорастворимое в воде. Его химическое название -(-)-L-(α-гидразино-(α-метил-β-(3,4-дигидроксибензол)пропионовая кислота. Его эмпирическая формула C10H14N2O4, а его структурная формула

Леводопа, ароматическая аминокислота, представляет собой кристаллическое соединение белого цвета, малорастворимое в воде. Его химическое название (-)-L-α-амино-β-(3,4-дигидроксибензол)пропионовая кислота. Его эмпирическая формула С9Н11NO4, а его структурная формула

В патентах США №№6500867 и 6797732 описаны пероральные твердые таблетированные композиции, содержащие энтакапон, леводопу и карбидопу или их фармацевтически приемлемые соли или гидраты и фармацевтически приемлемый эксципиент.
В патенте США 7094427 и патенте США 20040166159 описана композиция, содержащая компонент немедленного высвобождения и пролонгированного высвобождения.
В патенте США 20080051459 описан способ лечения болезни Паркинсона, включающий в себя введение фармацевтически эффективного количества композиции, содержащей леводопу.
В патенте США 20070275060 описана таблетка пролонгированного высвобождения, включающая в себя композицию пролонгированного высвобождения, содержащую леводопу, и композицию немедленного или быстрого высвобождения, содержащую карбидопу.
В WO 07/073702 описана многослойная таблетка, обеспечивающая три различных профиля высвобождения.
В патенте США 20060173074 описан способ лечения синдрома беспокойных ног у млекопитающего.
Энтакапон доступен в виде композиции немедленного высвобождения под торговой маркой Comtan®. Продажная концентрация составляет 200 мг.
Тройное сочетание леводопы, карбидопы и энтакапона доступно в виде композиции немедленного высвобождения различной концентрации. Например, Stalevo® 50 (содержащая 12,5 мг карбидопы, 50 мг леводопы и 200 мг энтакапона), Stalevo® 75 (содержащая 18,75 мг карбидопы, 75 мг леводопы и 200 мг энтакапона), Stalevo® 100 (содержащая 25 мг карбидопы, 100 мг леводопы и 200 мг энтакапона), Stalevo® 125 (содержащая 31,2575 мг карбидопы, 125 мг леводопы и 200 мг энтакапона), Stalevo® 150 (содержащая 37,5 мг карбидопы, 150 мг леводопы и 200 мг энтакапона) и Stalevo® 200 (содержащая 50 мг карбидопы, 200 мг леводопы и 200 мг энтакапона).
Болезнь Паркинсона представляет собой медленно прогрессирующее заболевание, симптомы которого усугубляются со временем. Поэтому симптомы будут изменяться и развиваться. Характер симптомов может варьироваться для каждого человека. Однако по прошествии ряда лет некоторые люди могут увидеть изменения в том, как их лекарственное средство контролирует их симптомы. Эти изменения общеизвестны как двигательные флуктуации. Со временем симптомы начинают возвращаться, перед тем как пора принимать следующую дозу лекарства леводопы. Данное изменение в симптомах называют «изнашиванием». Как только «изнашивание» становится заметным, промежуток времени для хорошего отклика на леводопу (известный как время «включения») уменьшается, а время слабого отклика на леводопу (известного как время «выключения») может увеличиться.
На ранних стадиях заболевания мозг способен запасать достаточное количество допамина. Это позволяет равномернее высвобождать допамин в мозге. Кроме того, это обеспечивает более постоянное контролирование симптомов. Однако по мере того как болезнь Паркинсона усугубляется, в мозге становится меньше клеток, которые могут поглощать леводопу и запасать ее в виде допамина для высвобождения при низких концентрациях. Вследствие этой пониженной способности запасать допамин в мозге симптомы могут возвращаться после более коротких периодов времени (например, «изнашивание»). Если кому-то со сниженной способностью запасать допамин дают слишком много леводопы, это может привести к побочным эффектам (например, дискинезии).
Есть возможность лучше контролировать данные симптомы за счет изменения или регулирования лечения. Как только возникают данные двигательные флуктуации, могут появиться прочие нежелательные побочные эффекты. Они включают в себя непроизвольные движения, известные как дискинезия (например, движения скручивания/поворота) или дистония (например, продолжительный мышечный спазм). У пациентов, получающих лечение от болезни Паркинсона, часто могут развиваться двигательные флуктуации, характеризуемые недостаточностью конца лечения, дискинезией и акинезией при пиковой дозе, при терапевтическом лечении леводопой (изнашивание), при котором пациенты страдают от непредсказуемых колебаний от подвижности к неподвижности. Более чем у 50% пациентов с болезнью Паркинсона после терапевтического лечения леводопой развиваются двигательные ответные флуктуации (явление «изнашивания»). Симптомы изнашивания включают в себя брадикинезию, дистонию, дрожания, пониженную ловкость рук, парестезию, мышечную боль, ослабление голоса.
Предполагается, что эффект «изнашивания» можно свести к минимуму у пациентов при помощи режима лечения, который обеспечивает свойства менее быстрого растворения и приведет к более равномерному профилю леводопы в плазме крови. При введении в сочетании с леводопой энтакапон повышает биодоступность леводопы, способствуя ее прохождению через гематоэнцефалический барьер. Поэтому энтакапон принят в качестве вспомогательного средства при лечении леводопой болезни Паркинсона. Однако дозу доступного в настоящее время препарата леводопы и энтакапона, то есть Stalevo®, дают восемь раз в день. Частая дозировка данных препаратов связана с более флуктуирующими концентрациями энтакапона в плазме. Кроме того, данный режим не способствует приверженности пациента лечению.
Кроме того, наблюдалось, что пациенту крайне неудобно одновременно принимать таблетку Sinemet CR и Comtan несколько раз в день, что приводит к неподверженности пациента лечению, особенно в случае пациента с болезнью Паркинсона. Кроме того, в литературе также предполагают, что если три данных ингредиента - энтакапон, карбидопа и леводопа - находятся вместе, это приводит к снижению биодоступности энтакапона и леводопы. Поэтому в коммерчески доступном препарате Stalevo значительная часть карбидопы содержится отдельно от леводопы и энтакапона. Кроме того, в литературе также сообщается о дестабилизации препарата с тройной комбинацией в присутствии микрокристаллической целлюлозы.
Следовательно, есть необходимость в способствующей приверженности пациента лечению композиции энтакапона и/или тройной комбинации, включающей в себя леводопу, карбидопу и энтакапон, которая будет растворяться медленно и обеспечит более равномерный профиль в плазме крови у пациентов с режимом лечения энтакапоном или леводопой/энтакапоном/карбидопой.
Сущность изобретения
В одном из аспектов данного изобретения предоставлена разовая пероральная дозированная фармацевтическая композиция, содержащая а) леводопу или ее соли в количестве от приблизительно 50 мг до приблизительно 300 мг в форме пролонгированного высвобождения, b) карбидопу или ее соли в количестве от приблизительно 10 мг до приблизительно 100 мг в форме пролонгированного высвобождения и с) энтакапон или его соли в количестве от приблизительно 100 мг до приблизительно 1000 мг в форме немедленного высвобождения, необязательно с другими фармацевтически приемлемыми эксципиентами.
В следующем общем аспекте данного изобретения предоставлен способ лечения болезни Паркинсона у млекопитающего, включающий в себя введение нуждающемуся в этом млекопитающему разовой пероральной дозированной фармацевтической композиции, содержащей а) леводопу или ее соли в количестве от приблизительно 50 мг до приблизительно 300 мг в форме пролонгированного высвобождения, b) карбидопу или ее соли в количестве от приблизительно 10 мг до приблизительно 100 мг в форме пролонгированного высвобождения и с) энтакапон или его соли в количестве от приблизительно 100 мг до приблизительно 1000 мг в форме немедленного высвобождения, необязательно с другими фармацевтически приемлемыми эксципиентами.
В следующем общем аспекте данного изобретения предоставлен способ уменьшения явления «изнашивания» у пациентов с болезнью Паркинсона, включающий в себя введение нуждающемуся в этом пациенту разовой пероральной дозированной фармацевтической композиции, содержащей а) леводопу или ее соли в количестве от приблизительно 50 мг до приблизительно 300 мг в форме пролонгированного высвобождения, b) карбидопу или ее соли в количестве от приблизительно 10 мг до приблизительно 100 мг в форме пролонгированного высвобождения и с) энтакапон или его соли в количестве от приблизительно 100 мг до приблизительно 1000 мг в форме немедленного высвобождения, необязательно с другими фармацевтически приемлемыми эксципиентами.
В следующем общем аспекте данного изобретения предоставлен способ получения разовой пероральной дозированной фармацевтической композиции, содержащей а) леводопу или ее соли в количестве от приблизительно 50 мг до приблизительно 300 мг в форме пролонгированного высвобождения, b) карбидопу или ее соли в количестве от приблизительно 10 мг до приблизительно 100 мг в форме пролонгированного высвобождения и с) энтакапон или его соли в количестве от приблизительно 100 мг до приблизительно 1000 мг в форме немедленного высвобождения, где указанный способ включает в себя: а) нанесения покрытия или смешивание леводопы, карбидопы с фармацевтически приемлемыми регулирующими скорость полимерами, b) энтакапона с одним или более фармацевтически приемлемыми эксципиентами, с) перемешивание смеси со стадии а) и b) и переведение ее в подходящую дозированную форму.
Варианты осуществления данной фармацевтической композиции могут включать в себя один или более следующих признаков. Например, фармацевтически приемлемые эксципиенты могут включать в себя один или более из числа наполнителей, связывающих веществ, смазывающих веществ, подслащивающих агентов, окрашивающих и вкусовых агентов, глидантов, дезинтегрирующих веществ и так далее.
Подробности одного или более вариантов осуществления данного изобретения представлены в приведенном ниже описании. Прочие признаки, объекты и преимущества изобретения будут ясны из описания и формулы изобретения.
Подробное описание изобретения
Работая над композициями леводопы, энтакапона и карбидопы, авторы изобретения заметили, что составление из леводопы или карбидопы препарата в форме пролонгированного высвобождения дает возможность непрерывно высвобождать леводопу или карбидопу в течение длительного периода времени. Таким образом, композиция пролонгированного высвобождения поддерживает продолжительное высвобождение леводопы и карбидопы, приводя, таким образом, к нефлуктуирующим постоянным концентрациям леводопы и карбидопы в плазме крови. Кроме того, это приводит к уменьшению явления «изнашивания», которое наблюдается у пациентов с болезнью Паркинсона вследствие флуктуирующих концентраций в плазме.
Кроме того, авторы изобретения неожиданно обнаружили, что Sinemet CR и Comtan можно объединить в виде фиксированной комбинации разовой пероральной дозы, не влияя на биодоступность любого из активных компонентов в присутствии другого. Даже микрокристаллическую целлюлозу можно также использовать в данной комбинации фиксированной дозы без оказания какого-либо дестабилизирующего влияния на композицию фиксированной дозы. Кроме того, данная комбинация фиксированной дозы приводит к увеличению приверженности пациента лечению.
Использованный в настоящем описании термин «пролонгированное высвобождение» относится к определенному высвобождению лекарственного средства в течение определенного периода времени, который может продолжаться от 4 ч до 24 ч или более.
Пролонгированного высвобождения в фармацевтической композиции можно добиться за счет одного или более покрытий, или внедрения в матрицу с использованием гидрофильных или гидрофобных полимеров, или за счет соединения с ионообменными смолами. Кроме того, пролонгированного высвобождения можно добиться также при помощи технологии осмотического перорального высвобождения.
Одна таблетка указанной композиции не проявляет существенного различия в скорости и/или степени абсорбции энтакапона по сравнению с 2-4 таблетками 200 мг энтакапона немедленного высвобождения, коммерчески доступного в виде Comtan®, и леводопы и карбидопы по сравнению с одной таблеткой Sineret®CR, вводимой с интервалом 3-4 часа.
«Биоэквивалентность» устанавливают по 90% доверительному интервалу (CI) в пределах от 0,80 до 1,25 как для Смакс, так и для AUC согласно регулирующим нормативам Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (USFDA) или по 90% CI для AUC в пределах от 0,80 до 1,25 и 90% CI для Смакc в пределах от 0,70 до 1,43 согласно регулирующим нормативам европейского ЕМЕА.
Используемый здесь термин «доверительный интервал» относится к обычному значению, известному специалисту в данной области. Доверительный интервал относится к статистическому интервалу с определенной вероятностью того, что заданный параметр попадет в данный интервал.
Используемый здесь термин «ковариация» относится к обычному значению, известному специалисту в данной области. Она представляет собой статистическую меру вариации двух случайных переменных, которые наблюдают или измеряют в один и тот же средний период времени. Эта мера равна продукту отклонений соответствующих значений двух данных переменных от их соответствующих средних значений.
Фармацевтическая композиция пролонгированного высвобождения может включать в себя одно или более из числа таблетки, двухслойной таблетки, трехслойной таблетки, таблетки в таблетке, капсулы, порошка, пластинки, таблетки в виде капсулы, гранул, шариков, гранул в капсуле, минитаблеток, минитаблеток в капсуле, шариков в капсуле, саше и так далее.
Леводопа, карбидопа или энтакапон могут находиться в форме порошка, гранул, пилюль, шариков, микротаблеток, минитаблеток и кристаллов.
Количество энтакапона в данных фармацевтических композициях изменяется от приблизительно 100 до приблизительно 1000 мг. Количество леводопы в данных фармацевтических композициях изменяется от приблизительно 50 до приблизительно 300 мг. Количество карбидопы в данных фармацевтических композициях изменяется от приблизительно 10 до приблизительно 100 мг.
Подходящие регулирующие скорость гидрофильные или гидрофобные полимеры включают в себя один или более из числа поливинилацетата, ацетата целлюлозы, ацетата-бутирата целлюлозы, ацетата-пропионата целлюлозы, этилцеллюлозы, жирной кислоты, эфира жирной кислоты, алкилового спирта, воска, шеллака, смолы, зеина (проламина кукурузы), повидона, коллидона SR, поли(мет)акрилата, микрокристаллической целлюлозы или поли(этиленоксида), солей полиуроновой кислоты, простых эфиров целлюлозы, ксантановой камеди, трагакантовой камеди, карайи, гуаровой камеди, аравийской камеди, геллановой камеди, камеди рожкового дерева, солей щелочных металлов альгиновой кислоты или пектиновой кислоты, альгината натрия, альгината калия, альгината аммония, гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, карбоксивиниловых полимеров, полимеризованного желатина, шеллака, сополимеров метакриловой кислоты типа С NF, бутирата-фталата целлюлозы, гидрофталата целлюлозы, пропионата-фталата целлюлозы, фталата поливинилацетата (PVAP), ацетата-фталата целлюлозы (CAP), ацетата-тримеллитата целлюлозы (CAT), фталата гидроксипропилметилцеллюлозы, ацетата гидроксипропилметилцеллюлозы, сукцината диоксипропилметилцеллюлозы, карбоксиметилэтилцеллюлозы (СМЕС), ацетата-сукцината гидроксипропилметилцеллюлозы (HMPCAS) и полимеров и сополимеров акриловой кислоты типа метилакрилата, этилакрилата, метилметакрилата и/или этилметакрилата с сополимерами эфиров акриловой и метакриловой кислоты (Eudragit NE, Eudragit RL, Eudragit RS) и так далее. Полимер можно использовать в количестве от 0,1-50% от массы композиции.
Фармацевтическая композиция пролонгированного высвобождения может включать в себя один или более фармацевтически приемлемых эксципиентов. Фармацевтически приемлемые эксципиенты могут включать в себя разбавители, связывающие вещества, дезинтегрирующие вещества, поверхностно-активные вещества, смазывающие вещества, глиданты и так далее.
Подходящее связывающее вещество может представлять собой одно или более из числа повидона, крахмала, стеариновой кислоты, камедей, гидроксипропилметилцеллюлозы и так далее. Связывающее вещество можно использовать в количестве от 0,1% до 40% от массы композиции.
Подходящий разбавитель может представлять собой одно или более из числа микрокристаллической целлюлозы, маннита, фосфата кальция, сульфата кальция, каолина, сухого крахмала, сахарной пудры и так далее. Разбавитель можно использовать в количестве от 1 до 50% от массы композиции.
Подходящий дезинтегрирующий агент может представлять собой одно или более из числа крахмала, кроскармеллозы натрия, кросповидона, гликолята крахмала натрия и так далее. Дезинтегрирующий агент можно использовать в количестве от 2-20% от массы композиции.
Подходящее смазывающее вещество может представлять собой одно или более из числа стеарата магния, стеарата цинка, стеарата кальция, стеариновой кислоты, стеарилфумарата натрия, гидрированного растительного масла, глицерилбегената и так далее. Смазывающее вещество можно использовать в количестве от 0,1-5% от массы композиции.
Подходящий глидант может представлять собой один или более из числа коллоидного оксида кремния, талька, кукурузного крахмала и так далее. Глидант можно использовать в количестве от 0,1-5% от массы композиции.
Данную фармацевтическую композицию можно получить, смешивая энтакапон с фармацевтически приемлемыми эксципиентами для получения смеси энтакапона. Леводопу и карбидопу можно смешать с одним или более фармацевтически приемлемыми полимерами и эксципиентами для получения смеси леводопы-карбидопы. Смесь энтакапона и смесь леводопы-карбидопы можно смешать с фармацевтически приемлемыми эксципиентами и перевести в подходящую дозированную форму.
Далее изобретение иллюстрировано следующими примерами, которые предоставлены только для иллюстрации изобретения и не ограничивают рамок изобретения. Некоторые модификации и эквиваленты будут очевидны специалистам в данной области, и подразумевается, что они входят в рамки данного изобретения.
Примеры
Композиция порций приведена в таблицах с 1 по 23. Следующие составы являются представительными для предпочтительных композиций изобретения. Получение примера подробно описано далее.
Пример I
Таблица 1. Фармацевтическая композиция изобретения.
Методика
Слой/порция энтакапона
Энтакапон и маннит совместно измельчали и просеивали. Кукурузный крахмал, кроскармеллозу натрия и гликолят крахмала натрия совместно просеивали по отдельности. Вещества помещали в гранулятор и перемешивали. Повидон растворяли в очищенной воде и гранулировали с перемешанным веществом. Гранулированное содержимое сушили. Стеарат магния просеивали и смешивали с высушенными гранулами.
Слой/порция леводопы и карбидопы
Леводопу, карбидопу и микрокристаллическую целлюлозу совместно просеивали и перемешивали. Повидон растворяли в очищенной воде и гранулировали с упомянутым выше перемешанным содержимым. Гранулированное содержимое сушили. Стеарат магния просеивали с поливинилпирролидоном и перемешивали с высушенными гранулами.
Прессование
И слой/порцию энтакапона, и слой/порцию леводопы и карбидопы прессовали в двухслойные таблетки или в таблетку в таблетке с энтакапоном, окружающим вложенную таблетку леводопы-карбидопы.
Таблица 2. Данные относительно растворения композиции, полученной в соответствии с примером I.
В таблице 2 приведены данные относительно растворения части леводопы и карбидопы из композиции, полученной согласно составу, приведенному в таблице 1. В таблице 3 приведены данные относительно растворения части энтакапона из композиции, полученной согласно составу, приведенному в таблице 1. Для определения скорости высвобождения лекарственного вещества энтакапона использовали прибор USP 2 типа (50 об/мин), в котором в качестве среды использовали 900 мл фосфатного буфера с рН 5,5 при 37°С±0,5°С. Кроме того, для определения скорости высвобождения лекарственного вещества леводопы и карбидопы использовали прибор USP 2 типа (50 об/мин), в котором в качестве среды использовали 900 мл 0,1 N НСl при 37°С±0,5°С.
Пример II
Таблица 4. Фармацевтическая композиция изобретения.
Методика
Слой/порция энтакапона
Энтакапон и маннит совместно измельчали и просеивали. Кукурузный крахмал, кроскармеллозу натрия и гликолят крахмала натрия совместно просеивали отдельно. Вещества помещали в гранулятор и перемешивали. Повидон растворяли в очищенной воде и гранулировали с перемешанным веществом. Гранулированное содержимое сушили. Стеарат магния просеивали и смешивали с высушенными гранулами.
Слой/порция леводопы и карбидопы
Леводопу, карбидопу и микрокристаллическую целлюлозу совместно просеивали и перемешивали. Повидон растворяли в очищенной воде и гранулировали с упомянутым выше перемешанным содержимым. Гранулированное содержимое сушили. Стеарат магния просеивали с поливинилпирролидоном и перемешивали с высушенными гранулами.
Прессование
И слой/порцию энтакапона, и слой/порцию леводопы и карбидопы прессовали в двухслойные таблетки или в таблетку в таблетке с энтакапоном, окружающим вложенную таблетку леводопы-карбидопы.
Данные относительно растворения композиции, полученной в соответствии с примером II.
В таблице 5 приведены данные относительно растворения композиции, полученной в соответствии с составом, приведенным в таблице 4. В таблице 6 приведены данные относительно растворения части энтакапона из композиции, полученной согласно составу, приведенному в таблице 4.
Для определения скорости высвобождения лекарственного вещества энтакапона использовали прибор USP 2 типа (50 об/мин), в котором в качестве среды использовали 900 мл фосфатного буфера с рН 5,5 при 37°С±0,5°С. Кроме того, для определения скорости высвобождения лекарственного вещества леводопы и карбидопы использовали прибор USP 2 типа (50 об/мин), в котором в качестве среды использовали 900 мл 0,1 N НСl при 37°С±0,5°С.
Пример III
Таблица 7. Фармацевтическая композиция изобретения.
Методика
Слой/порция энтакапона
Энтакапон и маннит совместно измельчали и просеивали. Повидон, кросповидон и маннит совместно просеивали отдельно. Вещества смешивали, получая массу. Стеарат магния просеивали и смешивали с упомянутой выше массой. Массу прессовали и измельчали. Стеарат магния и тальк просеивали отдельно и смешивали с измельченным веществом.
Слой/порция леводопы и карбидопы
Леводопу, карбидопу и микрокристаллическую целлюлозу совместно просеивали и перемешивали. Повидон растворяли в очищенной воде и гранулировали с упомянутым выше перемешанным содержимым. Гранулированное содержимое сушили. Стеарат магния просеивали с поливинилпирролидоном и перемешивали с высушенными гранулами.
Прессование
И слой/порцию энтакапона, и слой/порцию леводопы и карбидопы прессовали в двухслойные таблетки или в таблетку в таблетке с энтакапоном, окружающим вложенную таблетку леводопы-карбидопы.
Пример IV
Таблица 8. Фармацевтическая композиция изобретения.
Методика
Слой/порция энтакапона
Энтакапон и маннит совместно измельчали и просеивали. Повидон, кросповидон и маннит совместно просеивали отдельно. Вещества смешивали, получая массу. Стеарат магния просеивали и смешивали с упомянутой выше массой. Массу прессовали и измельчали. Стеарат магния и тальк просеивали отдельно и смешивали с измельченным веществом.
Слой/порция леводопы и карбидопы
Леводопу, карбидопу и микрокристаллическую целлюлозу совместно просеивали и перемешивали. Повидон растворяли в очищенной воде и гранулировали с упомянутым выше смешанным содержимым. Гранулированное содержимое сушили. Стеарат магния просеивали с поливинилпирролидоном и перемешивали с высушенными гранулами.
Прессование
И слой/порцию энтакапона, и слой/порцию леводопы и карбидопы прессовали в двухслойные таблетки или в таблетку в таблетке с энтакапоном, окружающим вложенную таблетку леводопы-карбидопы.
Пример V
Таблица 9. Фармацевтическая композиция изобретения.
Методика
Слой/порция энтакапона
Леводопу, карбидопу, гидроксипропилцеллюлозу и маннит совместно просеивали и перемешивали. Повидон К90 растворяли в изопропиловом спирте и хлористом метилене. Массу со стадии 1 гранулировали с использованием раствора со стадии 2 и сушили гранулы. К полученным гранулам добавляли стеарат магния и прессовали смазанные гранулы, получая ядра таблеток.
Внешние гранулы IR энтакапона
Энтакапон и маннит совместно просеивали. Гликолят крахмала натрия, кроскармеллозу натрия, кукурузный крахмал совместно просеивали. Повидон К30 растворяли в очищенной воде и использовали для гранулирования массы со стадии 1. Гранулы сушили. Гликолят крахмала натрия просевали через подходящее сито и добавляли к описанным выше гранулам. К описанной выше смеси добавляли стеарат магния.
Прессование
Таблетку в таблетке, состоящую из внутренних ядер таблеток LC ER и внешних гранул IR энтакапона, прессовали при помощи подходящего аппарата для прессования.
В таблице 11 приведены данные относительно растворения композиции, полученной в соответствии с составом, приведеннsм в таблице 9. Для определения скорости высвобождения лекарственного вещества энтакапона использовали прибор USP 2 типа (50 об/мин), в котором в качестве среды использовали 900 мл фосфатного буфера с рН 5,5 при 37°С±0,5°С. Кроме того, для определения скорости высвобождения лекарственного вещества леводопы и карбидопы использовали прибор USP 2 типа (50 об/мин), в котором в качестве среды использовали 900 мл 0,1 N НСl при 37°С±0,5°С.
Биоданные (состояние голодания)
Для энтакапона -
Для карбидопы -
Для леводопы -
В таблице 12 представлен биопрофиль энтакапона IR; в таблице 13 представлен биопрофиль карбидопы ER; в таблице 14 представлен биопрофиль леводопы ER, полученных согласно примеру V в условиях голодания по сравнению с контрольным продуктом Comtan® 200 мг + одна таблетка Sinemet CR (производитель: Merck; леводопа 200 + карбидопа 50 мг ER таблетка). Схема исследования включает в себя двойное перекрестное исследование биоэквивалентности на 15 нормальных взрослых субъектах в условиях получения пищи.
Пример VI
Таблица 15. Фармацевтическая композиция изобретения.
Методика
Внутреннее LC-ER ядро таблетки
Леводопу, карбидопу, гидроксипропилцеллюлозу и маннит совместно просеивали и смешивали. Сополимер метакриловой кислоты растворяли в изопропиловом спирте и хлористом метилене. Массу со стадии 1 гранулировали с использованием раствора со стадии 2 и сушили гранулы. К полученным гранулам добавляли стеарат магния и перемешивали. Массу со стадии 4 гранулировали с использованием подходящих штампов, получая ядра таблеток.
Внешние гранулы IR энтакапона
Энтакапон и маннит перемешивали и измельчали. Гликолят крахмала натрия, кроскармеллозу натрия, кукурузный крахмал совместно просеивали и перемешивали. Повидон К30 растворяли в очищенной воде. Массу со стадии 7 гранулировали с использованием раствора со стадии 8 и гранулы сушили. Гликолят крахмала натрия добавляли к массе со стадии 9 и перемешивали. Стеарат магния добавляли к массе со стадии 10 и перемешивали.
Прессование
Дозированную форму таблетки в таблетке получали при использовании внутренних ядер LC ER таблеток и внешних гранул IR энтакапона при помощи подходящего аппарата для прессования.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ЭНТАКАПОНА ИЛИ ЕГО СОЛЕЙ ПРОЛОНГРИРОВАННОГО ВЫСВОБОЖДЕНИЯ | 2009 |
|
RU2540465C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ЭНТАКАПОНА, ЛЕВОДОПЫ И КАРБИДОПЫ С УЛУЧШЕННОЙ БИОДОСТУПНОСТЬЮ | 2009 |
|
RU2485947C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ПЕРОРАЛЬНЫЕ ДОЗИРОВАННЫЕ ФОРМЫ ПРОЛЕКАРСТВА ЛЕВОДОПЫ И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2537137C2 |
| КОМПОЗИЦИИ ДЛЯ НЕПРЕРЫВНОГО ВВЕДЕНИЯ ИНГИБИТОРОВ ДОПА-ДЕКАРБОКСИЛАЗЫ | 2010 |
|
RU2559083C9 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2014 |
|
RU2677278C2 |
| СПОСОБЫ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2004 |
|
RU2342929C2 |
| КОМПОЗИЦИИ ДЛЯ НЕПРЕРЫВНОГО ВВЕДЕНИЯ ИНГИБИТОРОВ ДОПА-ДЕКАРБОКСИЛАЗЫ | 2010 |
|
RU2678839C2 |
| Режим введения для нитрокатехолов | 2011 |
|
RU2639131C2 |
| НОВАЯ КОМПОЗИЦИЯ ЛАПАТИНИБА В ВИДЕ ТВЕРДОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2019 |
|
RU2821950C2 |
| ПРОТИВОТУБЕРКУЛЕЗНАЯ СТАБИЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ ДИСПЕРГИРУЕМОЙ ТАБЛЕТКИ, СОДЕРЖАЩЕЙ ГРАНУЛИРОВАННЫЙ ИЗОНИАЗИД И ГРАНУЛИРОВАННЫЙ РИФАПЕНТИН, И СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ | 2014 |
|
RU2694056C2 |
Предложена группа изобретений, включающая фармацевтическую композицию, способ ее получения, способ лечения болезни Паркинсона и способ уменьшения явлений «изнашивания» у данных больных с ее введением. Фармацевтическая композиция в виде разовой пероральной дозы для лечения болезни Паркинсона состоит из смеси а) леводопы или ее соли в количестве от 50 мг до 300 мг в форме пролонгированного высвобождения, b) карбидопы или ее соли в количестве от 10 мг до 100 мг в форме пролонгированного высвобождения, где пролонгированное высвобождение достигается за счет нанесения покрытия или смешивания леводопы и карбидопы с одним или более регулирующими скорость полимерами, и с) энтакапона или его соли в количестве от 100 мг до 1000 мг в форме немедленного высвобождения, необязательно с другими фармацевтически приемлемыми эксципиентами. Технический результат: группа изобретений способствует приверженности пациента лечению, ее применение приводит к неколеблющемуся уровню активных агентов в крови и к снижению частоты ее введения. Это обеспечивает снижение явления изнашивания у больных болезнью Паркинсона. Кроме того, дополнительный технический результат, достигаемый композицией, состоит в ее стабильности в условиях высокой температуры и влажности. 4 н. и 5 з.п. ф-лы, 15 табл.
1. Фармацевтическая композиция в виде разовой пероральной дозы для лечения болезни Паркинсона, где композиция состоит из смеси a) леводопы или ее соли в количестве от приблизительно 50 мг до приблизительно 300 мг в форме пролонгированного высвобождения, b) карбидопы или ее соли в количестве от приблизительно 10 мг до приблизительно 100 мг в форме пролонгированного высвобождения, где пролонгированное высвобождение достигается за счет нанесения покрытия или смешивания леводопы и карбидопы с одним или более регулирующими скорость гидрофильными или гидрофобными полимерами, и с) энтакапона или его соли в количестве от приблизительно 100 мг до приблизительно 1000 мг в форме немедленного высвобождения с другими фармацевтически приемлемыми эксципиентами, где композиция необязательно содержит один или более фармацевтически приемлемых эксципиентов.
2. Способ лечения болезни Паркинсона у млекопитающего, включающий в себя введение нуждающемуся в этом млекопитающему разовой пероральной дозированной фармацевтической композиции по п.1.
3. Способ уменьшения явления «изнашивания» у пациентов с болезнью Паркинсона, включающий в себя введение нуждающемуся в этом пациенту разовой пероральной дозированной фармацевтической композиции по п.1.
4. Способ получения разовой пероральной дозированной фармацевтической композиции по п.1, где указанный способ включает в себя: a) нанесение покрытия или смешивание леводопы, карбидопы с одним или более фармацевтически приемлемыми регулирующими скорость гидрофильными или гидрофобными полимерами, b) смешивание энтакапона с одним или более фармацевтически приемлемыми эксципиентами, c) перемешивание смеси со стадии a) и b) и переведение ее в подходящую дозированную форму.
5. Композиция по п.1, где данная композиция представляет собой одно или более из числа таблетки, двухслойной таблетки, трехслойной таблетки, капсулы, порошка, пластинки, таблетки в виде капсулы, гранул, шариков, гранул в капсуле, минитаблеток, минитаблеток в капсуле, шариков в капсуле и саше.
6. Композиция по п.1, в которой фармацевтически приемлемые регулирующие скорость гидрофильные или гидрофобные полимеры включают в себя один или более из числа поливинилацетата, ацетата целлюлозы, ацетата-бутирата целлюлозы, ацетата-пропионата целлюлозы, этилцеллюлозы, жирной кислоты, эфира жирной кислоты, алкилового спирта, воска, шеллака, смолы, зеина (проламина кукурузы), повидона, коллидона SR, поли(мет)акрилата или поли(этиленоксида), солей полиуроновой кислоты, простых эфиров целлюлозы, ксантановой камеди, трагакантовой камеди, карайи, гуаровой камеди, аравийской камеди, геллановой камеди, камеди рожкового дерева, солей щелочных металлов альгиновой кислоты или пектиновой кислоты, альгината натрия, альгината калия, альгината аммония, гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, карбоксивиниловых полимеров, полимеризованного желатина, шеллака, сополимеров метакриловой кислоты типа C NF, бутирата-фталата целлюлозы, гидрофталата целлюлозы, пропионата-фталата целлюлозы, фталата поливинилацетата (PVAP), ацетата-фталата целлюлозы (CAP), ацетата-тримеллитата целлюлозы (CAT), фталата гидроксипропилметилцеллюлозы, ацетата гидроксипропилметилцеллюлозы, сукцината диоксипропилметилцеллюлозы, карбоксиметилэтилцеллюлозы (СМЕС), ацетата-сукцината гидроксипропилметилцеллюлозы (HMPCAS) и полимеров и сополимеров акриловой кислоты типа метилакрилата, этилакрилата, метилметакрилата и/или этилметакрилата с сополимерами эфиров акриловой и метакриловой кислоты (Eudragit NE, Eudragit RL, Eudragit RS).
7. Фармацевтическая композиция по п.1, в которой одна таблетка указанной композиции не проявляет существенного различия в скорости и/или степени абсорбции энтакапона по сравнению с 2-4 таблетками 200 мг энтакапона немедленного высвобождения, коммерчески доступного в виде Comtan® CR, и отсутствует существенное различие в скорости и/или степени абсорбции леводопы и карбидопы по сравнению с одной таблеткой Sinemet®, вводимой с интервалом 3-4 часа.
8. Способ лечения по п.2, где одна таблетка указанной композиции не проявляет существенного различия в скорости и/или степени абсорбции энтакапона по сравнению с 2-4 таблетками 200 мг энтакапона немедленного высвобождения, коммерчески доступного в виде Comtan® CR, и отсутствует существенное различие в скорости и/или степени абсорбции леводопы и карбидопы по сравнению с одной таблеткой Sinemet®, вводимой с интервалом 3-4 часа.
9. Способ уменьшения явления «изнашивания» по п.3, где одна таблетка указанной композиции не проявляет существенного различия в скорости и/или степени абсорбции энтакапона по сравнению с 2-4 таблетками 200 мг энтакапона немедленного высвобождения, коммерчески доступного в виде Comtan® CR, и отсутствует существенное различие в скорости и/или степени абсорбции леводопы и карбидопы по сравнению с одной таблеткой Sinemet®, вводимой с интервалом 3-4 часа.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| КЛИНОВАЯ ДЫШЛОВАЯ ГОЛОВКА | 1919 |
|
SU4503A1 |
| AHTILA S | |||
| et al | |||
| Effect of entecapone, a COMT inhibitor, on the pharmacokinetics and metabolism of levodopa after administration of controlled-release levodopa-carbidopa in volunteers | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
Авторы
Даты
2014-06-10—Публикация
2009-08-22—Подача