Изобретение относится к медицине, а именно к созданию лекарственных средств природного происхождения и может быть использовано для лечения доброкачественной гиперплазии предстательной железы (ДГПЖ).
ДГПЖ является одним из наиболее частых заболеваний мужчин пожилого возраста [Аляев Ю.Г., Винаров А.З., Локшин К.Л., Спивак Л.Г. Новое в консервативной терапии больных гиперплазией предстательной железы // Consilium medicum. - 2008. - №4. - С.45-49]. Гистологические признаки ДГПЖ обнаруживаются более чем у 40% мужчин старше 50 лет и 90% мужчин старше 80 лет. Клинические симптомы заболевания диагностируются у большинства мужчин старше 50 лет [Dhingra N., Bhagwat D. Benign prostatic hyperplasia: an overview of existing treatment // Ind. J. Pharmacol. - 2011. - Vol.43, N 1. - P.6-12]. По данным эпидемиологических исследований, проведенных в России, частота ДГПЖ увеличилась с 11,3% среди 40-50-летних до 81,4% у 80-летних мужчин [Рациональная фармакотерапия в урологии / Под ред. Н.А. Лопаткина, Т.С. Перепановой. - М.: Литтерра, 2006. - С.30-42].
Известно применение гомеопатического препарата рододендрона для лечения доброкачественных опухолей [Пат. РФ №2207868]. Его недостатком является необходимость индивидуального подбора дозы для каждого больного, что затрудняет применение в амбулаторной практике.
Известно применение отвара корня солодки голой для лечения хронического простатита [Пат. РФ №2058152]. Недостатками данного средства являются нестойкая при хранении и неудобная для приготовления лекарственная форма, слабый симптоматический эффект при хроническом простатите без терапевтического воздействия на патогенез заболевания, что не исключает возникновение рецидивов.
Известно применение препарата растительного происхождения для лечения простатита и аденомы предстательной железы в виде комплексной терапии, включающей средства для перорального и ректального применения [Пат. РФ №2275929]. Данное средство оказывает противовоспалительное действие, но не тормозит пролиферативные процессы в предстательной железе. Лечебный эффект при доброкачественной гиперплазии предстательной железы наступает только при сочетанном приеме средства внутрь и ректальном введении в форме клизм, что создает неудобства для амбулаторных больных.
Известно лечебно-профилактическое средство «Простанорм» для лечения простатитов, уретритов и других воспалительных заболеваний мочеполовой сферы, включающее корень солодки голой, траву зверобоя продырявленного, траву золотарника канадского, корни с корневищами эхинацеи пурпурной, взятые в равных пропорциях [Пат РФ №2098119]. Это средство также оказывает только противовоспалительный эффект и не обладает антипролиферативным действием при доброкачественной гиперплазии предстательной железы.
Для лечения и профилактики ДГПЖ применяют более 10 групп лекарственных средств, хотя доказана терапевтическая эффективность только α-адреноблокаторов, ингибитора 5α-редуктазы финастерида и растительных средств - экстрактов американской вееролистной пальмы Serenoa repens (пермиксон, простамол) и камерунской сливы Pygeum africanum (трианол) [Рациональная фармакотерапия в урологии / Под ред. Н.А. Лопаткина, Т.С. Перепановой. - М.: Литтерра, 2006. - С.30-42].
В свете сказанного актуальным является поиск препаратов, обладающих комплексным влиянием на регуляторные механизмы, запускающие каскад физиологических изменений, которые приводят к возникновению такой серьезной патологии как ДГПЖ.
Наиболее близким к предлагаемому решению является средство по патенту CN101884759, взятое в качестве прототипа.
Задача изобретения - расширение арсенала средств природного происхождения на основе отечественного сырья, эффективных при лечении ДГПЖ.
Технический результат достигается тем, что в качестве антипролиферативного средства используют липиды пантов марала.
Экстракцию липидов из пантов марала осуществляют смесью растворителей этанол : этилацетат : вода при их соотношении, мас.ч., 1:1:1 и соотношении сырье : экстрагент 1:10 мас.ч. тремя последовательными мацерациями по 4 ч. каждая. Полученный экстракт концентрируют в вакуумном выпарном аппарате и досушивают в испарителе.
Эксперименты проводили на 120 аутбредных белых крысах самцах позднего репродуктивного возраста (8-10 мес) массой 500-550 г, выращенных в конвенциональных условиях в клинике лабораторных животных НИИ фармакологии СО РАМН. Антипролиферативное влияние липидов пантов марала оценивали на модели ДГПЖ, вызванной ежедневным внутрибрюшинным введением сульпирида (эглонил, раствор в ампулах, Sanofi-Winthrop Industrie, Франция) в дозе 40 мг/кг в течение 60 сут. На протяжении эксперимента крысам вводили в желудок липиды пантов марала в виде суспензии на 1% крахмальной слизи в дозах 10, 30, 60 мг/кг. В качестве референтного препарата применяли экстракт Serenoa repens пермиксон (Pierre Fabre Medicament Production, Франция) в дозе 50 мг/кг (по экстракту Serenoa repens). Контрольные животные получали 1% крахмальную слизь. Через 60 сут крыс декапитировали под эфирным наркозом. Взвешивали переднюю, боковую и заднюю доли предстательной железы. Для гистологического исследования боковую и заднюю доли фиксировали 10% нейтральным формалином, депарафинированные срезы окрашивали гематоксилином-эозином. В гомогенатах боковой и задней долей предстательной железы определяли содержание белка, диеновых конъюгатов, скорость образования малонового диальдегида, количество восстановленного глутатиона, активность селензависимой глутатионпероксиазы и супероксиддисмутазы. В плазме крови анализировали содержание пролактина, тестостерона и 5α-дигидротестостерона иммунофлуоресцентным методом (наборы DRG International, США).
Статистическую обработку результатов проводили методом парных сравнений с использованием непараметрического критерия Вилкоксона-Манна-Уитни при вероятности ошибочного вывода, не превышающей 5% (р≤0,05).
Сульпирид, блокируя рецепторы D2 дофамина в тубероинфундибулярной системе, значительно увеличивает секрецию стимулятора пролиферации предстательной железы пролактина с развитием экспериментальной ДГПЖ. При введении сульпирида в течение 60 сут масса передней доли предстательной железы не изменялась, масса боковой и задней долей и весовые коэффициенты (отношение массы железы к массе тела животных) становились в 1,8-2,1 раза больше, чем у интактных животных (табл.1). При гистологическом исследовании предстательной железы определялись увеличенное число ацинусов с папиллярным разрастанием эпителия в форме сосочков. Строма между ацинусами содержала большое количество гипертрофированных гладких мышц, грубых коллагеновых волокон, была инфильтрирована нейтрофилами, лимфоцитами, макрофагами, тучными клетками. Расширенный просвет ацинусов заполнялся ацидофильной массой и нейтрофилами. В гомогенатах боковой и задней долей предстательной железы в 1,6 раза увеличивалось содержание белка и активировалось перекисное окисление липидов на фоне ингибирования антиперекисной защиты. Содержание диеновых конъюгатов повышалось в 2,1 раза по сравнению с их количеством в норме, продукция малонового диальдегида в присутствии аскорбата ускорялась в 2,2 раза, после добавления NADP·H - в 2,7 раза. Содержание восстановленного глутатиона, активность глутатионпероксидазы и супероксиддисмутазы уменьшались в 1,7-2,2 раза. В сыворотке крови крыс с экспериментальной ДГПЖ содержание пролактина возрастало в 5,8 раза, 5α-дигидротестостерона - в 1,5 раза, количество тестостерона снижалось в 3,2 раза (табл.2).
Липиды пантов марала в дозах 10, 30 и 60 мг/кг и экстракт Serenoa repens в дозе 50 мг/кг эффективно препятствовали прогрессированию экспериментальной ДГПЖ, вызванной инъекциями сульпирида у крыс самцов позднего репродуктивного возраста. В дозе 10 мг/кг липиды пантов марала и экстракт Serenoa repens снижали массу боковой и задней долей предстательной железы в 1,4-1,5 раза, хотя она оставалась в 1,3-1,4 раза больше, чем в норме. В дозах 30 и 60 мг/кг липиды пантов марала уменьшали массу боковой и задней долей в 1,8-2,1 раза, при этом масса становилась такой же, как у интактных животных. Весовые коэффициенты снижались в 1,8-2,1 раза. Антипролиферативное действие липидов пантов марала в дозах 30 и 60 мг/кг превосходило эффект экстракта Serenoa repens (табл.1).
Для углубленного исследования антипролиферативного действия при модели ДГПЖ липиды пантов марала вводили в дозе 30 мг/кг. Под влиянием экспериментальной терапии липидами пантов марала в ткани боковой и задней долей предстательной железы сокращалась площадь эпителиальных структур на фоне расширения просвета ацинусов. Ткань предстательной железы состояла из отдельных железок, разделенных узкими пучками соединительной ткани с гладкомышечными клетками, коллагеновыми и эластическими волокнами нормального строения. Клеточная инфильтрация интерстиция отсутствовала, в ацинусах не определялись лейкоциты. При введении экстракта Serenoa repens сохранялась умеренная лимфоцитарно-макрофагальная инфильтрация. В гомогенатах боковой и задней долей предстательной железы экспериментальная терапия липидами пантов марала сопровождалась снижением содержания белка в 1,5 раза, при действии экстракта Serenoa repens - в значительно меньшей степени, в 1,3 раза (табл.2).
Липиды пантов марала оказывали выраженное антиоксидантное действие. В гомогенатах боковой и задней долей предстательной железы содержание продуктов перекисного окисления липидов и показатели антиперекисной защиты - количество восстановленного глутатиона, активность глутатионпероксидазы и супероксиддисмутазы нормализовались. Содержание диеновых конъюгатов уменьшалось в 2,2 раза, продукция аскорбат- и NADP·H-зависимого малонового диальдегида замедлялась в 1,8-2,1 раза, содержание глутатиона, активность глутатионпероксидазы и супероксиддисмутазы повышались в 1,5-2 раза по сравнению с показателями при модели ДГПЖ. При введении экстракта Serenoa repens интенсивность липопероксидации снижалась в 1,4-1,8 раза, активность антиперекисной защиты возрастала в 1,3-1,5 раза (различия с эффектами липидов пантов марала достоверны только для содержания диеновых конъюгатов). Скорость продукции малонового диальдегида превышала скорость в норме в 1,4-1,5 раза, содержание восстановленного глутатиона, активность глутатионпероксидазы и супероксиддисмутазы оставались сниженными в 1,4 раза (табл.2).
В крови крыс, получавших липиды пантов марала, содержание пролактина снижалось втрое по сравнению с уровнем гормона у крыс, которым вводили только сульпирид, но оно в 1,9 раза превышало норму. При введении экстракта Serenoa repens содержание в крови пролактина уменьшалось в меньшей степени - в 1,5 раза, оставаясь в 3,8 раза выше нормы и вдвое больше, чем при введении липидов пантов марала. Содержание мужских половых гормонов в крови крыс, защищенных липидами пантов марала и экстрактом Serenoa repens, изменялось в одинаковой степени и становилось близким к количеству гормонов у интактных животных - содержание тестостерона повышалось в 2,2-2,6 раза, 5α-дигидротестостерона - снижалось в 1,5-1,7 раза по сравнению с количеством этих гормонов, измеренном при введении одного сульпирида (табл.2).
Таким образом, при модели ДГПЖ, вызванной введением стимулятора секреции пролактина сульпиридом крысам самцам позднего репродуктивного возраста, липиды пантов марала в эффективной дозе 30 мг/кг и экстракт Serenoa repens в дозе 50 мг/кг, препятствовали развитию гиперплазии боковой и задней долей предстательной железы, разрастанию ее эпителия и воспалительной инфильтрации. Оба препарата оказывали выраженное антиоксидантное действие и изменяли в сторону нормы гормональный баланс. При экспериментальной ДГПЖ липиды пантов в большей степени, чем экстракт Serenoa repens, сдерживали увеличение массы боковой и задней долей предстательной железы, продукцию первичных продуктов липопероксидации - диеновых конъюгатов и развитие гиперпролактинемии.
Судя по росту уровня тестостерона и снижению количества 5α-дигидротестостерона, в крови крыс, получавших на фоне инъекций сульпирида липиды пантов марала, этот препарат ингибирует 5α-редуктазу и тормозит восстановление тестостерона в 5α-дигидротестостерон - стимулятор пролиферации ткани предстательной железы. В механизме антипролиферативного эффекта липидов пантов марала большое значение имеет антиоксидантное действие. Продукты липопероксидации стимулируют пролиферацию эпителия и соединительной ткани в предстательной железе.
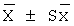
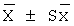
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИПРОЛИФЕРАТИВНОЕ СРЕДСТВО | 2012 |
|
RU2482857C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2574014C2 |
| Малотоксичные 1,3,4-оксадиазольные производные дезоксихолевой кислоты с простатопротекторным и противовоспалительным действием | 2023 |
|
RU2819604C1 |
| СПОСОБ И СРЕДСТВО ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2019 |
|
RU2764850C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ ПАТОЛОГИЙ ПРОСТАТЫ | 2017 |
|
RU2750992C2 |
| 1,2,4-Оксадиазольные производные дезоксихолевой кислоты, обладающие простатопротекторным действием, гипохолестеринемической и противовоспалительной активностями | 2020 |
|
RU2750488C1 |
| Средство для профилактики и лечения доброкачественной гиперплазии предстательной железы | 2016 |
|
RU2612268C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ПРОСТАТИТА И ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2020 |
|
RU2751342C1 |
| СРЕДСТВО (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ХИМИОПРОФИЛАКТИКИ ПРЕДРАКА И РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2012 |
|
RU2571818C2 |
| КОМПОЗИЦИЯ С КВЕРЦЕТИНОМ, ЛИКОПИНОМ И НАРИНГИНОМ ДЛЯ ПРОФИЛАКТИКИ ХРОНИЧЕСКОГО ПРОСТАТИТА - СИНДРОМА ХРОНИЧЕСКОЙ ТАЗОВОЙ БОЛИ | 2023 |
|
RU2835864C1 |
Изобретение относится к медицине, а именно к средству для лечения доброкачественной гиперплазии предстательной железы. Антипролиферативное средство для лечения доброкачественной гиперплазии предстательной железы, которое содержит липиды пантов марала, полученные экстракцией пантов марала смесью растворителей этанол : этилацетат : вода при определенных условиях. Вышеописанное средство эффективно для лечения доброкачественной гиперплазии предстательной железы. 2 табл.
Антипролиферативное средство для лечения доброкачественной гиперплазии предстательной железы на основе экстрактов из сырья животного происхождения, отличающееся тем, что оно содержит липиды пантов марала, полученные экстракцией смеси растворителей этанол: этилацетат : вода при их соотношении, мас.ч., 1:1:1 и соотношении сырье : экстрагент 1:10.
| CN 101884759 A, 17.11.2010 | |||
| Велкорнин | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Пантолечение | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| CN 102100845 A, 22.06.2011 | |||
| Рациональная фармакотерапия | |||
Авторы
Даты
2014-06-20—Публикация
2011-11-23—Подача