Область изобретения
Изобретение относится к области антимикробных средств и к соединениям, способным повышать эффективность антимикробных средств. Такие усилители могут быть использованы для повышения эффективности антимикробных средств в различных областях, включая, например, усовершенствование эффективности антимикробных средств для лечения состояний ротовой полости, возникающих из-за присутствия патогенных микроорганизмов (например, гингивит, зубной налет и т.п.). Изобретение также относится к способам получения таких соединений, композициям, которые содержат такие соединения, и к применению соединений и композиций в способах лечения микробных инфекций и других расстройств, вызываемых патогенными микроорганизмами.
Уровень техники
Разнообразные недомогания человека возникают из-за патогенных микроорганизмов, которые включают бактерии, вирусы и грибы. Присутствие таких патогенных микроорганизмов ведет к септицемии, серьезным инфекциям верхних и нижних дыхательных путей, ЦНС, менингиту, внутриабдоминальной ткани, включая брюшину, мочеполовой тракт, кожные и мягкие ткани, и к разнообразным другим инфекциям, таким как системный микоз, кандидоз, включая инфекции, вызываемые дерматофитами. В течение последних 100 лет достигнут значительный прогресс в борьбе с болезнями, вызываемыми большим семейством микробов, с применением многочисленных терапевтических средств различного химического и биологического характера, которые стали доступными в качестве средств для краткосрочного и долгосрочного лечения. Такие антимикробные средства включают аминогликозиды, пенициллины, цефалоспорины, макролиды, гликопептиды, фторозамещенные хинолоны, тетрациклины, противотуберкулезные лекарства первой и второй линии, средства против проказы, противовирусные средства, полиеновые, триазоловые и имидазоловые антигрибковые средства, сочетания типа производных пиримидина и триметоприма и сульфаметоксизола.
Постоянное применение антибиотиков в больничных условиях привело к появлению бактериальных популяций, которые являются резистентными ко многим антибиотикам. Такие популяции включают условно-патогенные микроорганизмы, которые могут и не быть сильно вирулентными, но которые являются по существу резистентными к множеству антибиотиков. Такие бактерии часто заражают ослабленных или иммунологически "скомпрометированных" пациентов (то есть обладающих недостаточным иммунитетом вследствие. Появление резистентных популяций включает также щтаммы бактериальных разновидностей, которые являются хорошо известными патогенами, которые прежде были восприимчивы к антибиотикам. Вновь приобретенная резистентность, как правило, обусловлена мутациями DNA или резистентными плазмидами (R плазмиды) или придающими резистентность транспозонами, переносимыми от другого организма. Инфекции тем или иным типом бактериальной популяции, естественно резистентных условно-патогенных микроорганизмов или резистентных к антибиотикам патогенных бактерий трудно поддаются лечению современными антибиотиками. Необходимы новые антибиотические молекулы, которые могут преодолеть механизмы резистентности.
С годами бактерии развивают различные механизмы для преодоления действия антибиотиков. Эти механизмы резистентности могут быть специфическими для молекулы или для семейства антибиотиков или могут быть неспецифическими и могут быть вовлечены в резистентность к неродственным антибиотикам. Специфические механизмы включают разложение лекарства, инактивацию лекарства ферментативной модификацией и изменение лекарственной мишени (B.G. Spratt, Science 264:388 (1994)). Существуют, однако, более общие механизмы лекарственной резистентности, в которых доступ антибиотика к целевому месту предотвращается или уменьшается путем уменьшения переноса антибиотика в клетку или путем увеличения оттока лекарства из клетки во внешнюю среду. Оба механизма могут снижать концентрацию лекарства на целевом месте и давать возможность бактериям выживать в присутствии одного или нескольких антибиотиков, которые иначе могли бы подавлять или убивать бактериальные клетки. Некоторые бактерии используют оба механизма, объединяя низкую проницаемость стенки клетки (включающей мембраны) с активным оттоком антибиотиков. (H. Nikaido, Science 264:382-388 (1994)).
Снижение проницаемости внешней мембраны путем или уменьшения количества поринов, или уменьшения количества конкретных разновидностей поринов может снижать восприимчивость штамма к широкому диапазону антибиотиков, благодаря уменьшенной скорости поступления антибиотиков в клетки. Однако для большинства антибиотиков полупериоды достижения равновесного состояния являются настолько короткими, что антибиотик может оказать свой эффект, если отсутствует другой механизм. Насосы оттока являются примером такого другого механизма. Однажды в цитоплазме или периплазме лекарство может быть перенесено обратно во внешнюю среду. Этот перенос опосредуется насосами оттока, которые созданы протеинами. Различные насосы могут выводить специфически лекарство или группу лекарств, например система Nor-A, которая переносит хинолоны, или Tet A, которая переносит тетрациклины, или они могут создавать отток большого разнообразия молекул, так, например, как некоторые насосы оттока у Pseudomonas aeruginosa. Как правило, насосы оттока имеют цитоплазматический компонент, и требуется энергия для переноса молекул наружу из клетки. Некоторые насосы оттока имеют второй цитоплазматический мембранный протеин, который распространяет влияние в периплазму.
Многокомпонентные насосы оттока, принадлежащие в основном к членам семейства типа, регулирующего резистентность (RND), обнаруженные главным образом в грамотрицательных бактериях, включают MDR насосы AcrAB-TolC и MexAB-OprM от E. coli и Pseudomonas aeruginosa. Взаимодействие между насосами оттока может обеспечивать либо аддитивные, либо мультипликативные воздействия на лекарственную резистентность (A. Lee et al., J. of Bacteriology, 2000, 182:3142). Насосы MexAB-OprM, MexCD-OprJ, MexEF-OprN, MexXY-OprM, AcrAB-TolC, AcrEF, MarA, SoxS и/или Tet известны как присутствующие в грамотрицательных организмах, таких как P. aeruginosa и E. coli и рассматриваются в последних публикациях и журналах, таких как Webber and Piddock, J. of Antimicrobial Chemother, 2003, 51:39-11; Bambeke et al., J. of Antimicrobial Chemother, 2003, 51:1055-1056; Xian Zhi Li et al., Journal of Antimicrob. Chemother., 2000, 45:433-436; O. Lomovskaya Li et al., Antimicrob. Agents and Chemother., 1999, 43:1340-1346.
Биопленка является структурированной группой микроорганизмов, инкапсулированных в собственном создаваемом ими матриксе. Биопленки обычно прилипают к живой или инертной поверхности. В организме человека или животного биопленки могут образовываться или на внутренней, или на внешней поверхности. Биопленки, как было обнаружено, оказываются вовлеченными в широкое разнообразие микробных инфекций в организме и, следовательно, вызывают некоторые состояния, включая инфекции мочевого тракта, инфекции среднего уха, образование зубного налета и гингивит.
Микроорганизмы, присутствующие в биопленке, имеют свойства, существенно отличающиеся от свойств свободно плавающих микроорганизмов тех же видов. Это происходит потому, что полимерный экстрацеллюлярный матрикс, защищая микроорганизмы от окружающей среды, дает возможность микроорганизмам объединяться и взаимодействовать различными путями, которые недоступны для свободно плавающих микроорганизмов. Эти сложные сообщества микроорганизмов представляют собой нечто уникальное в том отношении, что они часто являются резистентными по отношению к классическим средствам антимикробного контроля. Бактерии, живущие в биопленке, обнаруживают повышенную резистентность к антибиотикам, потому что плотный экстрацеллюлярный матрикс и внешний слой клеток защищают внутреннюю часть биопленки от воздействий антибиотиков. Поэтому известные антимикробные средства не будут оказывать того же воздействия на бактерии, присутствующие в биопленке.
Таким образом, клеточные факторы, влияющие на перенос (как активный, так и пассивный перенос) антибиотиков (и антибактериальных средств) в бактериальные клетки, являются важными компонентами антибиотической резистентности для многих бактериальных видов. Существует потребность в соединениях и композициях, которые повышают эффективность антимикробных средств, даже когда эффективность антимикробного средства может быть ухудшена антибиотической резистентностью.
Сущность изобретения
Данное изобретение направлено на разрешение таких проблем, и применение продуктов по данному изобретению предполагает режим низкого дозирования, который обеспечивает улучшенное терапевтическое действие по сравнению с действием стандартной дозы одного лекарства.
Особенность изобретения в том, чтобы обеспечить фармацевтические композиции, содержащие соединения по изобретению. Один вариант осуществления включает композицию, которая содержит по меньшей мере одно из соединений формулы 1-4 и дополнительно может также включать антибиотическое или антимикробное соединение. Еще одна особенность изобретения относится к способу лечения инфекций с применением соединений по изобретению или содержащих их композиций. Лечение предусматривает пероральное, парентеральное введение и/или местное применение эффективного количества соединения по изобретению или его композиций или отдельно, или в сочетании с антибиотическим или антимикробным средством или с двумя или несколькими соединениями по данному изобретению.
Данное изобретение относится к применению синтетических халконов в качестве усилителей антимикробных (или антибактериальных) средств. Более конкретно изобретение относится к халконам и композициям, содержащим халконы, выбранные из группы, состоящей из таких членов, как 3-(4"-гидрокси-3"-метоксифенил)-1-(2'-гидрокси-5'-метоксифенил)проп-2-ен-1-он (СК-1 - формула 2), 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-он (СК-4 - формула 1), 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-он (СК-14 - формула 3), 3-(2",5"-диметоксифенил)-1-(1Н-пиррол-2-ил)проп-2-ен-1-он (СК-16 - формула 4) и их смесей.
Описание предпочтительных вариантов осуществления
Следует понимать, что подробное описание и конкретные примеры, хотя и показывают варианты осуществления изобретения, предназначены только для целей пояснения и не предназначены для ограничения сферы действия изобретения.
Следующие определения и неограничительные рекомендации следует иметь в виду при рассмотрении описания данного изобретения, изложенного в данной заявке. Используемые здесь заголовки (такие как "Область изобретения", "Уровень техники" и "Сущность изобретения") предназначены только для общей организации предметов обсуждения в раскрытии изобретения и не предназначены для ограничения раскрытия изобретения или какого-либо его аспекта. В частности, предмет обсуждения, раскрытый в разделе "Уровень техники", может включать аспекты технологии в сфере действия изобретения и может не давать повторения предшествующего опыта. Предмет обсуждения, раскрытый в разделе "Сущность изобретения", не является исчерпывающим или полным раскрытием всего объема изобретения или каких-либо его вариантов осуществления. Классификация или обсуждение материала в разделе данного описания, как имеющего конкретное применение (например, как являющегося "активным" ингредиентом или ингредиентом "носителя") сделаны для удобства и не следует делать умозаключение, что материал должен обязательно или единственным образом функционировать в соответствии с его классификацией в данном описании, когда его используют в любой заданной композиции.
Цитирование ссылок в данном описании не означает признание факта, что эти ссылки являются предшествующим опытом или имеют какое-либо отношение к патентоспособности изобретения, раскрытого в данной заявке. Любое обсуждение ссылок, цитируемых в разделе "Уровень техники", предназначается только для того, чтобы обеспечить общее краткое изложение утверждений, сделанных авторами ссылок, и не составляет допущения в отношении точности содержания таких ссылок.
Описание и конкретные примеры, хотя и указывают варианты осуществления изобретения, предназначены только для целей пояснения и не предназначены для ограничения сферы действия изобретения. Более того, перечисление разнообразных вариантов осуществления, имеющих установленные характерные особенности, не предназначено для исключения других вариантов осуществления, имеющих дополнительные характерные особенности, или других вариантов осуществления, включающих различные сочетания установленных характерных особенностей. Конкретные примеры приведены в целях пояснения, как осуществлять и применять композиции и способы по данному изобретению и, если подробно не установлено иное, не предназначены для того, чтобы давать представление о том, что данные варианты осуществления данного изобретения могут или не могут быть осуществлены или испытаны.
Используемые в данном описании слова "предпочтительный" и "предпочтительно" относятся к вариантам осуществления изобретения, которые приносят конкретную пользу в конкретных обстоятельствах. Однако другие варианты осуществления также могут быть предпочтительными в тех же самых или других обстоятельствах. Кроме того, приведение одного или нескольких вариантов осуществления не подразумевает, что другие варианты осуществления не полезны, и не предназначено для исключения других вариантов осуществления из объема изобретения. В дополнение, композиции и способы могут содержать, состоять по существу из или состоять из элементов, описанных в данной заявке.
Используемое здесь слово "включают" и его варианты предназначены быть неограничительными, так что перечисление объектов в списке не означает исключения других подобных объектов, которые могут быть также полезными в материалах, композициях, устройствах и способах по данному изобретению.
Используемый в данном описании термин "около", когда прилагается к величине или параметру композиции или способа по данному изобретению, указывает, что расчет или измерение величины допускает некоторую легкую погрешность без существенного влияния на химические или физические неотъемлемые признаки композиции или способа. Если, по какой-то причине, погрешность, обозначаемая "около", является по-другому непонятной в ее обычном значении, тогда используемый в данном описании термин "около" указывает возможное отклонение вплоть до 5% по величине.
Все упоминаемые в данном описании композиционные процентные доли даны по массе от всей композиции, если не указано иное.
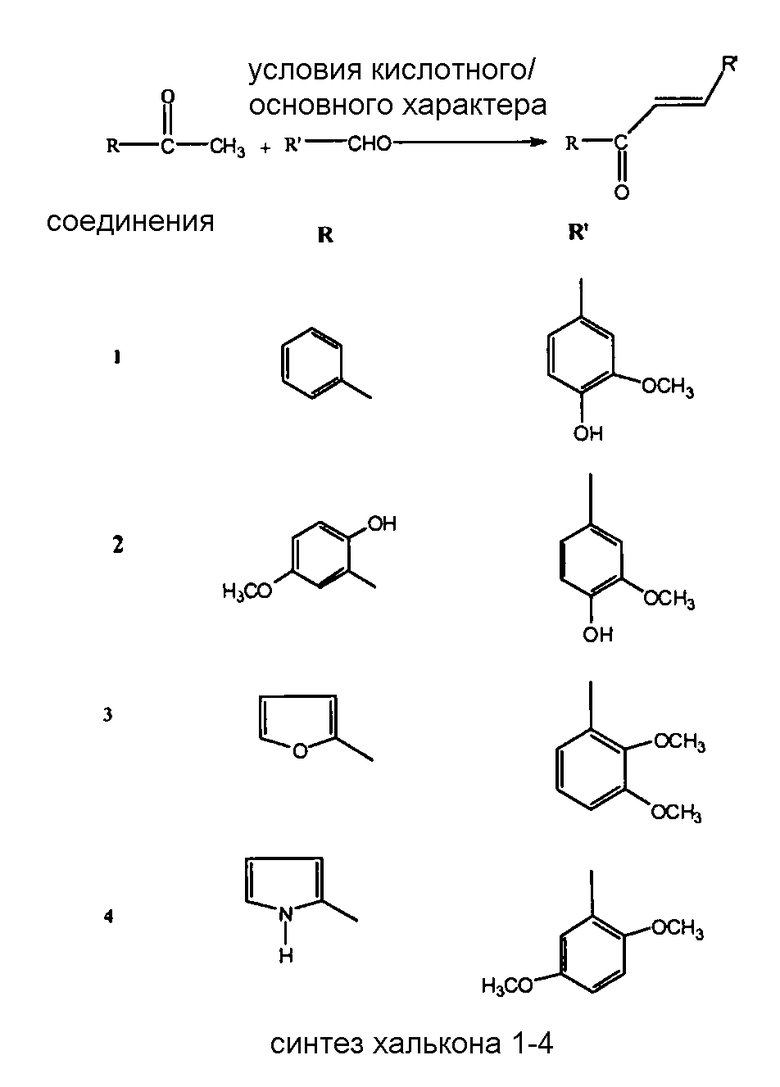
Данные варианты осуществления включают композиции, содержащие халконы, 3-(4"-гидрокси-3"-метоксифенил)-1-(2'-гидрокси-5'-метоксифенил)проп-2-ен-1-он (СК-1 - формула 2), 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-он (СК-4 - формула 1), 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-он (СК-14 - формула 3), 3-(2",5"-диметоксифенил)-1-(1Н-пиррол-2-ил)проп-2-ен-1-он (СК-16 - формула 4) и их смеси. Как предполагается, указанные соединения и композиции, когда объединены с различными противоинфекционными средствами, имеют свойства усиления эффективности при скрининге in vitro с использованием бактерий, вирусов и дрожжей. Указанные соединения и композиции были также действенными при испытаниях in vivo с использованием моделей на мышах и морских свинках, зараженных микроорганизмами. Структуры халконов предпочтительных вариантов осуществления приведены в таблице ниже, которая поясняет синтез соединений.
О соединениях по данному изобретению не было сообщений как о применимых для усиления биоэффективности лекарств, в частности противоинфекционных лекарств, таких как описанные в данной заявке. Синтез соединений осуществляют путем сочетания различных химических стадий, известных в технологии синтеза. Обычный специалист в этой области будет способен синтезировать соединения, описанные в вариантах осуществления, с использованием предоставленных рекомендаций.
Производные халкона формулы 2, то есть 3-(4"-гидрокси-3"-метоксифенил)-1-(2'-гидрокси-5'-метоксифенил)проп-2-ен-1-он и 1, то есть 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-он синтезировали путем конденсации производных ацетофенона с замещенными ароматическими альдегидами в щелочных или кислотных условиях, тогда как в случае соединений 3 и 4 конденсация была между замещенным ароматическим альдегидом и 2-ацетилфураном и замещенными ароматическими альдегидами и 2-ацетилпирролом соответственно. Синтез и структура соединений формул 1-4 схематически показаны ниже.
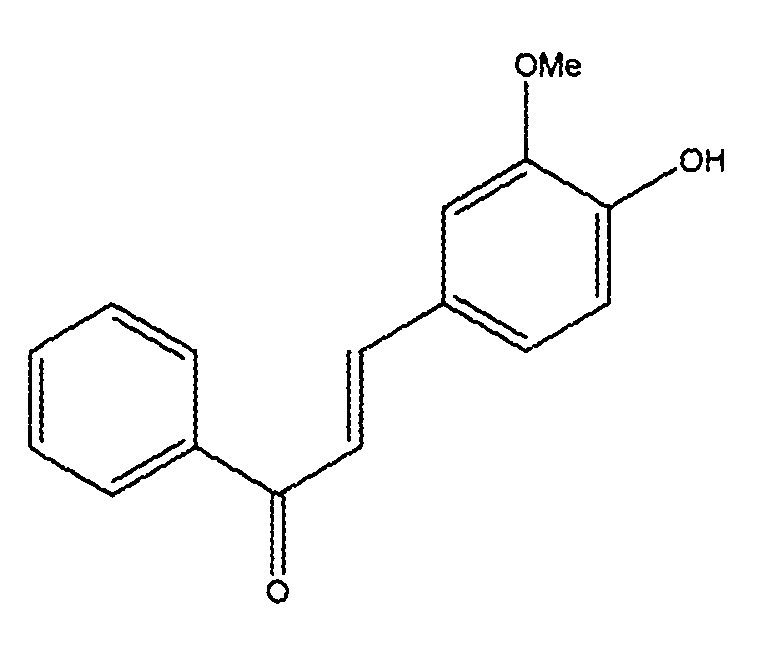
В качестве пояснительного примера, химическая структура соединения 1, 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-она, называемого также фенил-3-метокси-4-гидроксистирил кетон, является следующей:
Без намерения ограничиться какой-либо теорией или образом действий, можно предположить, что указанные соединения ингибируют клеточные насосы оттока у бактерий или других микробов. Такие насосы оттока экспортируют субстратные молекулы из цитоплазмы зависимым от энергии образом, и экспортируемые субстратные молекулы могут включать антибактериальные средства или другие антимикробные средства и дезинфицирующие средства. Такие ингибиторы насосов оттока применимы, например, для лечения микробных инфекций путем уменьшения экспорта совместно введенного антимикробного средства или путем предотвращения экспорта соединения, синтезируемого микробами (например, бактериями), чтобы сделать возможным или улучшить их рост. Примером уменьшения экспорта такого соединения является ингибирование доступности железа для микроба путем уменьшения экспорта сидерофоров. Пока без намерения быть связанными какой-либо теорией действия, соединения по изобретению могут также усиливать эффективность некоторых антибактериальных средств путем ингибирования образования биопленки и/или путем разрушения биопленки. Поэтому соединения и композиции, как представляется, применимы для предотвращения состояний, вызываемых образованием биопленки. Таким образом, данное изобретение также относится к композициям, которые включают такие соединения, и способам лечения микробных инфекций, состояний, вызываемых присутствием патогенных микроорганизмов, и состояний, вызываемых образованием биопленки.
Следовательно, характерная особенность изобретения - предоставить способ подавления роста бактерий или грибов, содержащий контактирование указанных бактерий или грибов с соединением халкона по изобретению в присутствии антибактериального или противогрибкового средства в концентрации ниже минимальной ингибирующей концентрации (MIC) для указанных бактерий или грибов.
Дополнительная характерная особенность изобретения - предоставить способы лечения инфекций у людей и животных, вызываемых восприимчивыми и резистентными микробными штаммами, с применением антимикробного средства и соединения халкона по изобретению в количестве, эффективном для уменьшения антибиотической резистентности, или в количестве, достаточном для ингибирования образования и/или для разрушения биопленки, где соединение халкона повышает восприимчивость микроба к антимикробному средству.
Другая характерная особенность изобретения относится к способу профилактической терапии человека или животного, содержащему введение указанному человеку или животному при риске микробной инфекции соединения халкона по изобретению, где соединение снижает патогенность микроба в организме человека или животного.
Другая характерная особенность изобретения относится к способу профилактической терапии человека или животного, содержащему введение указанному человеку или животному при риске микробной инфекции антимикробного средства и соединения халкона по изобретению, где соединение повышает восприимчивость микроба к антимикробному средству.
Другая характерная особенность изобретения относится к способу лечения с применением соединения халкона по изобретению путем введения, системно или местно, соединения пораженному болезнью человеку или животному, исключая тем самым токсичные эффекты, связанные со смесями соединений по изобретению.
Другой характерной особенностью изобретения является усиление антимикробной активности антимикробного средства против микроба путем контактирования микроба с антимикробным средством и соединением халкона по изобретению.
Используемый в данном раскрытии термин "лекарство" относится к химическому веществу, которое способно влиять на патофизиологию организма и может быть применено для лечения или профилактики болезни. Лекарства включают многие классы соединений, включая, но без ограничения указанными, аминогликозид, пенициллины, цефалоспорины и другие β-лактамные средства, макролиды, гликопептиды, фторхинолоны, тетрациклины, противотуберкулезные лекарства первой и второй линии, средства против проказы, противовирусные средства, полиеновые, триазоловые и имидазоловые соединения и сочетания типа пиримидинов, сульфаметоксазола, фенольные соединения, такие как триклозан, магнолол и его производные, хонокиол и его производные, соединения четвертичного аммониевого основания, такие как хлорил цетилпиридиния. Лекарства могут быть пролекарством, активируемой или метаболизируемой формой, состоящей из заряженных, незаряженных, гидрофильных, гидрофобных или цвиттер-ионных частиц, которая обеспечивает их поступление путем простой диффузии, опосредуемого носителем переноса, зависимого или независимого от энергетических потребностей, через ионные и/или управляемые импульсами напряжения каналы.
Особенно предпочтительные производные халкона формулы 1-4 выбраны из следующего набора соединений, полученных способами, описанными в примерах. Одно или несколько производных халкона могут быть использованы в вариантах осуществления, приведенных в данном описании.
1. 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-он
2. 3-(4"-гидрокси-3"-метоксифенил)-1-(2'-гидрокси-5'-метоксифенил)проп-2-ен-1-он
3. 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-он
4. 3-(2",5"-диметоксифенил)-1-(1Н-пиррол-2-ил)проп-2-ен-1-он
5. 1-(2-фурил)-3-(3,4-диметоксифенил)проп-2-ен-1-он
6. 1-(2-фурил)-3-фенилпроп-2-ен-1-он
7. 1-(2-фурил)-3-(3,4,5-метилендиокси фенил)проп-2-ен-1-он
8. 1-(2-фурил)-3-(3-гидрокси-метокси фенил)проп-2-ен-1-он
9. 1-(2-фурил)-3-(3-нитрофенил)проп-2-ен-1-он
10. 1-(2-фурил)-3-(3-гидроксифенил)проп-2-ен-1-он
11. 1-(2-фурил)-3-(4,5-нитрофенил)проп-2-ен-1-он
12. 1-(2-фурил)-3-(3,6-дихлорфенил)проп-2-ен-1-он
13. 1-(2-фурил)-3-(2,3-диметоксифенил)проп-2-ен-1-он
14. 1-(2-фурил)-3-(2,5-диметоксифенил)проп-2-ен-1-он
15. 3-(4-нитрофенил)-1-(1Н-пиррол-2-ил)пропенон
16. 3-(3-нитрофенил)-1-(1Н-пиррол-2-ил)пропенон
17. 3-(2,5-дихлорфенил)-1-(1Н-пиррол-2-ил)пропенон
18. 3-(2,3-диметоксифенил)-1-(1Н-пиррол-2-ил)пропенон
19. 3-(2,3-дихлорфенил)-1-(1Н-пиррол-2-ил)пропенон
20. 3-(2,6-дихлорфенил)-1-(1Н-пиррол-2-ил)пропенон
Особенно подходящими примерами микроба, подходящего для применения с соединением халкона предпочтительных вариантов осуществления, являются патогенные бактериальные виды, такие как Streptococcus pneumoniae, Streptococcus pyogenes, Pseudomonas aeruginosa, Escherischia coli, Staphylococcus aureus, Streptococcus mutans, Actinomycetes viscosus, Fusobacterium nucleatum, Porphyromonas gingivalis, которые могут быть по существу резистентными к обычно используемым антибактериальным средствам. Представляется, что подвергание указанных бактерий воздействию соединения халкона по изобретению может значительно снизить экспорт антибактериального средства из внутренности клетки или экспорт сидерофоров. Например, были сообщения о сверхэкспрессии мультилекарственного транспортера NorA для штаммов S. aureus, для фторхинолоновой резистентности in vitro (Kaatz and Seo, Antimicrobial agents and Chemother., 1997, 41:2733-2737). Следовательно, если другое антибактериальное средство вводят в сочетании с соединением халкона по изобретению, антибактериальное средство, который иначе поддерживался бы при очень низкой внутриклеточной концентрации процессом экспорта, может аккумулироваться до концентрации, которая будет ингибировать рост бактериальных клеток. Это ингибирование роста может происходить или из-за бактериостатической, или из-за бактерицидной активности в зависимости от конкретного используемого антибактериального средства. Хотя P. aeruginosa является примером подходящей бактерии, другие бактериальные и микробные виды, включая те, которые описаны выше, могут содержать подобные широкосубстратные насосы, которые активно экспортируют разнообразные антимикробные средства и, следовательно, также могут быть подходящими мишенями.
Поэтому, поясняя полезность соединений халкона по изобретению, можно предположить, что ингибирование насоса оттока Streptococcus pneumoniae, Streptococcus pyogenes, Pseudomonas aeruginosa, Escherischia coli, Staphylococcus aureus, Streptococcus mutans, Actinomycetes viscosus, Fusobacterium nucleatum, Porphyromonas gingivalis позволит достичь одного или нескольких из следующих эффектов: 1 штаммы Streptococcus pneumoniae, Streptococcus pyogenes, Pseudomonas aeruginosa, Escherischia coli, Staphylococcus aureus, Streptococcus mutans, Actinomycetes viscosus, Fusobacterium nucleatum, Porphyromonas gingivalis станут восприимчивыми к антибиотикам, которые не могли бы применяться для лечения соответствующих бактериальных инфекций, или станут более восприимчивыми к антибиотикам, которые ингибируют соответствующий бактериальный рост; 2 штаммы Streptococcus pneumoniae, Streptococcus pyogenes, Pseudomonas aeruginosa, Escherischia coli, Staphylococcus aureus, Streptococcus mutans, Actinomycetes viscosus, Fusobacterium nucleatum, Porphyromonas gingivalis станут более восприимчивыми к антибиотикам, применяемым в настоящее время для лечения соответствующих бактериальных инфекций; 3 вирулентность Streptococcus pneumoniae, Streptococcus pyogenes, Pseudomonas aeruginosa, Escherischia coli, Staphylococcus aureus, Streptococcus mutans, Actinomycetes viscosus, Fusobacterium nucleatum, Porphyromonas gingivalis будет ослаблена, потому что доступность незаменимого несущего сидерофор элемента будет затруднена, и 4 ингибирование насосов или одного из компонентов насосов может быть фатальным или предотвращающим рост.
Достижение даже одного из указанных эффектов обеспечивает потенциальное терапевтическое лечение заражений указанными бактериями. Некоторые или все из указанных эффектов также могут быть достигнуты с такими микробами, и поэтому они также являются подходящими мишенями для обнаружения или применения ингибиторов насосов оттока. Так, термин "микробы" включает, например, бактерии, грибы, дрожжи и простейших.
Как указано, бактерия, которая должна быть ингибирована путем применения соединения халкона по изобретению, может быть из других бактериальных групп или видов, такие бактериальные группы видов, включают, но без ограничения перечисленным, следующие:

Термин "насос оттока" относится к трансмембранной белковой упорядоченной структуре, которая экспортирует субстратные молекулы из цитоплазмы или периплазмы клетки зависимым от энергии образом. Так, насос оттока обычно будет находиться в цитоплазматической мембране клетки (остов цитоплазматической мембраны). В грамположительной бактерии насос может распространяться в периплазматическое пространство, и также может быть часть насоса оттока, которая распространяется во внешнюю мембрану.
"Ингибитором насоса оттока" является соединение, которое специфически влияет на способность насоса оттока экспортировать его нормальный субстрат или другие соединения, такие как антибиотики. Ингибитор сам может иметь существенную антимикробную (например, антибактериальную) активность, но по меньшей мере значительная часть релевантной активности соответствует активности ингибирования насоса оттока. Особый интерес в вариантах осуществления представляют соединения, которые ингибируют экспорт или активность насосов оттока, которые имеют широкий субстратный диапазон, который включает антибактериальные средства.
В другом аспекте изобретение относится к способу лечения микробной инфекции, например бактериальной инфекции, у животного введением животному, страдающему от такой инфекции, одного или нескольких соединений халкона, которые описаны выше, в количестве, достаточном для снижения активности насоса оттока, или в количестве, достаточном для ингибирования образования биопленки и/или для разрушения биопленки.
В предпочтительном варианте осуществления соединение халкона является соединением, которое снижает патогенность микроба. Такое снижение патогенности может быть достигнуто, например, путем создания помехи приобретением существенного бактериального элемента, путем ингибирования переноса сидерофоров или путем ингибирования образования или разрушения биопленки. Патогенность может быть также снижена уменьшением или удалением микробных продуктов, которые вызывают эффекты, повреждающие ткани организма-хозяина. Другие способы снижения патогенности, однако, также охвачены этим аспектом.
В некоторых предпочтительных вариантах осуществления микробная инфекция или расстройство могут быть из-за бактерий любого из бактериальных видов, указанных выше, но особенно из-за включающих Streptococcus pneumoniae, Pseudomonas aeruginosa, Escherischia coli, Staphylococcus aureus. Такие расстройства, когда они присутствуют в ротовой полости, включают, например, гингивит, зубное гниение, образование зубного налета и тому подобное.
В связанном с этим аспекте данное изобретение относится к способу лечения животного, страдающего от микробной инфекции, путем введения животному соединения халкона по изобретению в количестве, достаточном для усиления активности антимикробного средства, вводимого вместе с соединением халкона. В этом аспекте соединение халкона может быть соединением, которое снижает in vivo жизнестойкость микроба, замешанного в инфекции. Путем снижения in vivo жизнестойкости (микроба) инфицированное животное может быстрее очистить свой организм от инфекции, или микробы могут быть даже уничтожены. В конкретных вариантах осуществления животное является млекопитающим. Также в конкретных вариантах осуществления микроб может быть одним из разнообразных патогенных бактериальных видов, особенно включающих те, которые перечислены выше.
В соответствующем аспекте изобретение относится к способу лечения микробной инфекции у животного, особенно у млекопитающего, путем лечения животного, страдающего от такой инфекции, антимикробным средством и соединением халкона по изобретению, которое повышает восприимчивость микроба в отношении антимикробного средства. Таким образом, микроб, замешанный в инфекции, может быть обработан с применением антимикробного средства в меньших количествах или может быть обработан антимикробным средством, который не является терапевтически эффективным, когда его применяют в отсутствие соединения халкона. Так, этот способ лечения является особенно подходящим для лечения инфекций, при которых применяют одно антимикробное средство, из-за необходимости высоких уровней дозирования (которые могут вызывать нежелательные побочные эффекты) или из-за нехватки каких-либо клинически эффективных антимикробных средств. Однако он также является подходящим для лечения инфекций, вовлекающих микробы, которые восприимчивы к конкретным антимикробным средствам, как путь для снижения дозирования таких конкретных средств. Это может уменьшить риск побочных эффектов, но может также снизить эффект селекции высоко резистентных микробов, являющийся результатом соответствующего высокого уровня применения конкретного антимикробного средства. В конкретном варианте осуществления микроб является бактерией, которая, например, может быть какой-либо из групп или видов, указанных выше. Также в конкретных вариантах осуществления могут быть использованы различные антибактериальные средства. К ним относятся хинолоны, тетрациклины, гликопептиды, аминогликозиды, бета-лактамы, рифамицины, кумермицины, макролиды и хлорамфеникол.
В конкретных вариантах осуществления антибиотик указанных классов может быть, например, одним из следующего:
Бета-лактамные антибиотики
Имипенем, меропенем, санефтринем, биапенем, цефаклор, цефадроксил, цефамандол, цефатризин, цефазедон, цефазолин, цефиксим, цефменоксим, цефодизим, цефоницид, цефоперазон, цефоранид, цефотаксим, цефотиам, цефпимизол, цефпирамид, цефподоксим, цефсулодин, цефтазидим, цефтерам, цефтезол, цефтибутен, цефтизоксим, цефтриазон, цефурозим, цефузонам, цефаацетерил, цефалексин, цефалоглицин, цефалоридин, цефалотин, цефапирин, цефрадин, цефметазол, цефокситин, цефотетан, азтреонам, карумонам, фломоксеф, моксалактам, амидиноциллин, амоксициллин, амициллин, азлоциллин, карбенициллин, бензилпенициллин, карфециллин, клоксациллин, диклоксациллин, метиклилоин, мезлоциллин, нафциллин, оксациллин, пенициллин G, пиперациллин, сулбенициллин, темоциллин, тикарциллин, цефдиторен, SC004, KY-020, цефдинир, цефтибутен, FK-312, S-1090, CP-0467, BK-218, FK-037, DQ-2556, FK-518, цефозопран, МЕ1228, КР-736, СР-6232, Ro 09-1227, OPC-20000, LY206763, макролиды, азитромицин, кларитромицин, эритромицин, олеандомицин, рокитамицин, розарамицин, рокситромицин, тролеандомицин, телитромицин и другие кетолиды. Хинолоны амифлоксацин, циноксацин, ципрофлоксацин, эноксацин, флероксацин, флумекуин, лоМефлоксацин, налидиксовая кислота, норфлоксацин, офлоксацин, левофлоксацин, оксолиновая кислота, перфлоксацин, дифлоксацин, марбофлоксацин, розоксацин, темафлоксацин, тосуфлоксацин, спарфлоксацин, клинафлоксацин, тровафлоксацин, алатрофлоксацин, грепафлоксацин, моксифлоксацин, гатифлоксацин, гемифлоксацин, надифлоксацин, PD131628, PD140248, Q-35, AM-1155, NM394, T-3761, руфлоксацин, OPC-17116, DU-6859a (идентивицированы в Sato, K. et al., 1992, Antimicrob. Agents Chemother. 37:2212 18).
Тетрациклины
Хлортетрациклин, демеклоциклин, доксициклин, лимециклин, метациклин, миноциклин, окситетрациклин, тетрациклин, аминоглкозиды, амикацин, арбекацин, бутирозин, дибекацин, фортимицины, гентамицин, канамицин, нетилмицин, рибостаницин, сизомицин, спектиномицин, стрептомицин, тобрамицин, клиндамицин, линкомицин.
Оксазолидиноны
Линезолид, эперезолид
О каждом из указанных соединений сообщалось в литературе. Другие антибиотические соединения, которые могут быть идентифицированы, также могут быть использованы с соединениями халкона по данному изобретению.
В контексте ответной реакции микроба, такого как бактерия, на антимикробное средство термин "восприимчивость" относится к чувствительности микроба к присутствию антимикробного средства. Так, увеличить восприимчивость означает, что микроб будет ингибироваться более низкой концентрацией антимикробного средства в среде, окружающей микробные клетки. Это эквивалентно выражению, что микроб является более чувствительным к антимикробному средству. В большинстве случаев минимальную ингибирующую концентрацию (MIC) такого антимикробного средства полагается уменьшать.
Данное изобретение относится также к способу усиления антимикробной активности антимикробного средства против микроба, в котором такой микроб приводят в контакт с соединением халкона по изобретению, например не-тетрациклин-специфическим соединением халкона, и антибактериальным средством. Таким образом, этот способ делает антимикробное средство более эффективным против клетки, которая экспрессирует насос оттока, или против клетки, вовлекаемой в образование биопленки, когда клетку обрабатывают сочетанием антимикробного средства и соединения халкона. В конкретных вариантах осуществления микроб является бактерией или грибом, такими как какие-либо из указанных выше; антибактериальное средство может быть выбран из числа структурных классов антибиотиков, включая, например, бета-лактамы, гликопептиды, аминогликозиды, хинолоны, тетрациклины, рифамицины, кумермицины, макролиды и хлорамфеникол. В конкретных вариантах осуществления антибиотик указанных классов может быть таким, как установлено выше.
В дополнительном аспекте данное изобретение относится к фармацевтическим композициям эффективным для лечения заражения животного, например млекопитающего, микробом, таким как бактерия или гриб. Композиция включает фармацевтически приемлемый носитель и соединение халкона, которое описано выше. В предпочтительных вариантах осуществления такие композиции содержат соединения халкона, которые сами по себе являются эффективными антимикробными средствами, даже в отсутствие другого антибактериального средства (то есть имеют собственную антимикробную активность). Таким образом, фармацевтическая композиция, включающая такие соединения халкона, может быть использована или одна, или в сочетании с другим антимикробным средством.
Также в предпочтительных вариантах осуществления, соединения халкона в фармацевтических композициях этого аспекта усиливают эффективность антимикробного средства, так что такие композиции будут использоваться, как правило, в сочетании с другим таким антимикробным средством. Изобретение также относится к фармацевтическим композициям, подобным образом эффективным для лечения инфекции млекопитающего, где композиции включают соединение халкона и антимикробное средство. Изобретение также относится к антимикробным составам, которые включают антимикробное средство, соединение халкона по изобретению и носитель. В предпочтительных вариантах осуществления антимикробное средство является антибактериальным средством.
"Носитель" или "наполнитель" является соединением или материалом, используемым для облегчения введения соединения, например, для повышения растворимости соединения. Твердые носители включают, например, крахмал, лактозу, дикальций фосфат, сахарозу и каолин. Жидкие носители включают, например, стерильную воду, буферы, неионогенные поверхностно-активные вещества и пищевые масла, такие как масло, арахисовое и кунжутное масла. В дополнение в состав могут быть введены различные адъюванты, такие как традиционно применяемые в этой области. Эти и другие такие соединения описаны в литературе, например, в Merck Index, Merck & Company, Rahway, N. J. Соображения по поводу введения различных компонентов в фармацевтические композиции описаны, например, в Gilman et al. (Eds.) (1990); Goodman and Gilman': The Pharmacological Basis of Therapeutics, 8. sup.th Ed., Pergamon Press.
В дополнительном аспекте изобретение относится к способу получения фармацевтической композиции, содержащему идентификацию соединения халкона типа, описанного выше в таблице, формулы 1-4; синтез соединения и приготовление фармацевтической композиции, содержащей соединение. Соединение халкона может иметь химическую структуру, которая описана выше. Фармацевтическая композиция может также содержать один или несколько антибактериальных средств, например, таких как идентифицированные выше, и один или несколько носителей, разбавителей и наполнителей. Кроме того, в предпочтительных вариантах осуществления, соединение халкона является активным против микроба, например бактерии, как установлено выше.
Идентификация соединений халкона
Идентификацию соединений халкона, имеющих структуры, которые описаны для данного изобретения, проводили, применяя методы скрининга, известные специалистам в области биологических технологий и описанные подробно ниже. Однако могут быть применены и другие методы скрининга для обнаружения ингибиторов насосов оттока. Была подвергнута скринигу библиотека синтетических химикатов и идентифицированы некоторые соединения, которые эффективно ингибируют соответствующие насосы оттока Staphylococcus aureus 1199В (сверхэкпрессирование NorA), Staphylococcus aureus SA-K2192 (сверхэкпрессирование TetK) и Staphylococcus aureus SA-K2191 (сверхэкпрессирование MsrA).
Метод шахматной доски:
Метод шахматной доски является наиболее часто применяемым методом для оценки антимикробных сочетаний in vitro. Термин "шахматная доска" относится к системе рапределения (пробирок или лунок титрационного микропланшета), образованной множественными разбавлениями двух испытуемых лекарств (Eliopoulos GM, Moellering RC. Antimicrobial Combinations, in: Antibiotics in Laboratory Medicine: USA: Williams & Wilkins). В данном исследовании шахматная доска составлена из колонок, в которых каждая пробирка (или лунка) содержит одно и то же количество стандартного лекарства (антибактериального/противогрибкового/противотуберкулезного/противовирусного), разбавленного по оси х, и рядов, в которых каждая пробирка (или лунка) содержит одно и то же количество усилителя, который разбавлен по оси y. Как результат, каждый квадрат в шахматной доске (который представляет собой одну пробирку/лунку планшета) содержал уникальное сочетание стандартного лекарства и усилителя. Диапазон концентраций стандартного лекарства в данном исследовании был от 64 мкг/мл до 0,03 мкг/мл, тогда как усилитель испытывали в диапазоне от 500 мкг/мл до 0,2 мкг/мл. Эта методика шахматной доски может быть осуществлена с жидкой или полутвердой (агаровой) средой.
Агаровый метод:
В агаровом методе агар (Mueller Hinton agar, Middlebrook 7H10 agar) автоклавировали и давали ему возможность остыть до 55-50°С. Сочетание стандартного лекарства и усилителя добавляли к агару. Последовательные двукратные разбавления каждого стандартного лекарства и усилителя готовили в подходящих растворителях. Чтобы обеспечивать желательные концентрации и агара, и лекарств и исключить эффект растворителя, объем добавленного к агару растворителя (содержащего стандартное лекарство или усилитель) поддерживали небольшим (то есть ≤5% от всего объема). После того как агаровые пластины отливали и давали им возможность высохнуть, бактерии, которые должны были быть испытаны, наносили на поверхность агара реплицирующим устройством, сконструированным так, чтобы доставлять стандартный инокулят (приблизительно 104 КОЕ/пятно). Пластины инкубировали при 37°С в течение 24 ч (3 недели в случае Micobacterium tuberculosis).
Бульонный метод:
Указанный метод шахматной доски осуществляли также с жидкой средой в формате титрационного микропланшета. Этот метод применяли для исследования сочетания антибактериального/противогрибкового/антивирусного лекарств с усилителем.
Скрининг соединений халкона in vivo
Ингибиторы бактериальных насосов оттока вначале в основном характеризуют in vitro. Те, которые показывают эффективное ингибирование насоса (насосов) и которые проявляют синергическую активность с антибиотиками, отбирают для оценки in vivo. Испытание эффективности будет проводиться с использованием стандарных процедур. Первичная оценка эффективности может быть осуществлена с использованием мышиной модели септицемии (Yun et al., Journal of Antimicrob. Chemother., 2002, 46: 3071-3074). В этой модели супра-летальную дозу бактерий используют для контрольного заражения грызунов. Лечение начинают, изменяя время обработки или дозу антибиотика или и то и другое. В этих экспериментах изменяют дозы и антибиотика, и ингибитора насоса оттока. На позитивный результат указывает значительное усиление защиты от летальной инфекции при сочетании усилителя (ингибитора насоса оттока) и антибиотика против одного антибиотика.
Фармацевтические композиции и способы введения
Конкретное соединение, идентифицированное выше, может быть введено пациенту либо само по себе, либо в сочетании с антимикробным, например антибактериальным средством, или в фармацевтических композициях, где его смешивают с подходящим носителем (носителями) или разбавителем (разбавителями). Сочетание соединения халкона с антимикробным средством может быть по меньшей мере двух различных типов. В одном количество соединения халкона объединяют с количеством антимикробного средства в смеси, например в растворе или порошкообразной смеси. В таких смесях относительные количества соединения халкона и антимикробного средства могут изменяться, как свойственно специфическому сочетанию и предполагаемой обработке. Во втором типе сочетания соединение халкона и антимикробное средство могут быть ковалентно связаны таким образом, что связанные молекулы могут отщепляться внутри клетки. Однако термин "в сочетании" может также относится к другим возможностям, включая последовательное введение соединения халкона и антимикробного средства. В дополнение, соединение халкона и/или другой антимикробное средство могут быть введены в пролекарственных формах, то есть соединение вводят в форме, которая модифицируется внутри клетки с образованием функциональной формы. При лечении пациента, проявляющего представляющее интерес расстройство, вводят терапевтически эффективное количество средства или средств, таких как эти. Терапевтически эффективная доза относится к такому количеству соединения (соединений), которое имеет результатом облегчение симптомов или продление жизни пациента и может включать устранение микробной инфекции.
Токсичность и терапевтическая эффективность таких соединений могут быть определены стандартными фармацевтическими процедурами на клеточных культурах или подопытных животных, например, для определения ID50 (дозы летальной для 50% популяции) и ED50 (дозы терапевтически эффективной для 50% популяции). Дозовое соотношение между токсичным и терапевтическим эффектами является терапевтическим показателем и может быть выражено как отношение ID50/ED50. Соединения, которые обнаруживают большие терапевтические показатели, предпочтительны. Данные, полученные из этих анализов клеточных культур и исследований на животных, могут быть использованы при формулировании диапазона дозирования для применения для людей. Дозировка таких соединений лежит предпочтительно в диапазоне циркулирующих в крови концентраций, которые включают ED50 с малой токсичностью или нетоксичные. Дозировка может изменяться в этом диапазоне в зависимости от дозировки и используемой дозированной формы и используемого пути введения. Предпочтительно, чтобы терапевтическая концентрация соединения халкона в сыворотке была в пределах от 0,1 до 100 мкг/мл.
В случае средства для чистки зубов или композиции для профилактики заболеваний ротовой полости, соединения, описанные в данной заявке, могут быть введены с соответствующим антибактериальным средством, средством против зубного налета, средством против твердых зубных отложений, средством против зубного камня и другими активными веществами для профилактики заболеваний ротовой полости, а также сочетаниями указанных активных веществ. Композиции могут быть в форме зубной пасты, зубного порошка, геля, полоскания, пастилки, жевательной резинки, пленки и тому подобного. Любоей подходящее антибактериальное средство может быть использовано, включая натуральные антибактериальные средства, синтетические средства и тому подобное. Композиции средства для чистки зубов обычно содержат антибактериальное средство, соединение халкона, абразив, увлажнитель и орально приемлемый носитель. Соответствующие количества компонентов могут изменяться, и специалисты в этой области способны составить подходящие композиции средства для чистки зубов, используя приводимые в данном описании рекомендации.
Антимикробное средство в композиции по данному изобретению конкретно не ограничено и может быть выбрано из следующих, таких как галогенированный дифениловый простой эфир (триклозан), травяные экстракты или эфирные масла (например, розмариновый экстракт, тимол, ментол, эвкалиптол, метилсалицилат), антисептики на основе бисгуанида (например, хлоргексидин, алексидин или октенидин), фенольные антисептики, гексетидин, повидониод, делмопинол, салифлюор, ионы металлов и их соли (например, хлорид цинка, лактат цинка, цитрат цинка, оксид цинка, фторид олова (II) и хлорид олова (II)), сангвинарин, прополис, средства оксигенирования (например, пероксид водорода, забуференный пероксиборат натрия или пероксикарбонат), хлорид цетилпиридиния, экстракт магнолии, магнолол, хонокиол, 5,5'-дибутил-2,2'-диол, пропил хонокиол, сложные эфиры бороновой кислоты и их смеси. Средства против прикрепления, такие как солрол, также могут быть включены, а также средства, диспергирующие зубной налет, такие как ферменты (папаин, глюкоамилаза и т.п.).
Обнаружено, что применение соединений халкона по изобретению в сочетании с антимикробными средствами может значительно усиливать эффективность антимикробного средства. Усиление эффективности может иметь результатом применение более низких концентраций антимикробных средств для достижения такого же или подобного эффекта, достигаемого, когда используют одни антимикробные средства. Количество антимикробного средства может быть уменьшено где-нибудь на величину от 10% до более чем 50% его концентрации, когда его использовали одного без соединения халкона, предпочтительно от 10% до 75%, более предпочтительно от около 10% до около 50%.
В варианте осуществления, который изложен подробно где-то в данном описании, сочетание обоих и соединения халкона, предпочтительно 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-она, и антимикробного средства обеспечивает синергический эффект при ингибировании образования биопленки и/или при разрушении биопленки. Обнаружено неожиданное уменьшение концентрации уничтожения биопленки (ВЕС50), которая является наименьшей концентрацией, при которой наблюдается более чем 50% уменьшение биомассы по отношению к контролю. ВЕС50 соединения халкона и антимикробных средств является более низкой, когда их испытывают вместе в отношении ингибирования биопленки, по сравнению с тем, когда их испытывают раздельно.
Таким образом, в предпочтительном варианте осуществления соединение халкона имеет ВЕС50 в присутствии антимикробного средства 50% или менее, более предпочтительно 30% или менее, наиболее более предпочтительно 25% или менее, по сравнению с ВЕС50 соединения халкона в отсутствие антимикробного средства. Соединение халкона предпочтительно имеет ВЕС50 в присутствии антимикробного средства от 0,1 м.д. до 40 м.д., более предпочтительно от 0,2 м.д. до 30 м.д.
В предпочтительном варианте осуществления антимикробное средство имеет ВЕС50 в присутствии соединения халкона 75% или менее, более предпочтительно 50% или менее, по сравнению с ВЕС50 антимикробного средства одного (в отсутствие соединения халкона). ВЕС50 антимикробного средства в присутствии соединения халкона зависит от конкретного антимикробного средства, используемого в композиции. Антимикробное средство обычно может иметь ВЕС50 30 м.д. в присутствии соединения халкона. Антимикробное средство предпочтительно имеет ВЕС50 20 м.д. или менее, более предпочтительно 6 м.д. или менее, наиболее предпочтительно 2 м.д. или менее, в присутствии соединения халкона. В одном варианте осуществления, где антимикробным средством является триклозан, триклозан имеет ВЕС50 от 5 м.д. до 3 м.д. в присутствии соединения халкона, более предпочтительно ВЕС50 от 0,75 м.д. до 1,5 м.д., тогда как ВЕС50 одного триклозана находится в пределах от около 1,5 до около 2,5 м.д.
В различных вариантах осуществления данного изобретения, где носитель композиции для профилактики заболеваний ротовой полости является твердым или пастообразным, оральная композиция предпочтительно содержит приемлемый для зубов абразивный материал, который служит либо для полирования зубной эмали, либо обеспечивает отбеливающий эффект. Неограничительные примеры включают кремнеземистые абразивы, такие как силикагели и осажденные кремнеземы. Коммерческие варианты осуществления включают ZEODENT® 115, продаваемый J.M. Huber, Edison, New Jersey, United States of America, и SILODENT® XWA, SILODENT® 783 или SILODENT® 650 XWA от Davisob Chemical Division of W. R. Grace & Co., New York, New York, United States of America и кремнеземистые абразивы SORBOSIL®, продаваемые PQ Corporation, Malvern, PA, United States of America. Другие применимые абразивы для средств для чистки зубов включают, без ограничения, метафосфат натрия, метафосфат калия, трикальций фосфат, дигидратированный дикальций фосфат, силикат алюминия, прокаленный оксид алюминия, бентонит или другие кремнистые материалы или их сочетания.
Абразив присутствует в эффективном количестве. В вариантах осуществления, где оральная композиция находится в твердой или пастообразной форме, абразивный материал, как правило, составляет от около 10% до около 99% оральной композиции. В некоторых вариантах осуществления полирующий материал присутствует в количествах от около 10% до около 75% (например, от около 10% до около 40% или от около 15% до около 30%) в зубной пасте и от около 70% до около 99% в зубном порошке.
В еще одном варианте осуществления композиция по изобретению содержит по меньшей мере один увлажнитель, применимый, например, для предотвращения затвердевания зубной пасты, когда она открыта для доступа воздуха. Может быть использован орально приемлемый увлажнитель, включая, но без ограничения, многоатомные спирты, такие как глицерин, сорбит, ксилит и низкомолекулярные PEG. Большинство увлажнителей выполняют также функцию подсластителей. Один или несколько увлажнителей необязательно присутствуют в общем количестве от около 1% до около 70%, например от около 1% до около 50%, от около 2% до около 25% или от около 5% до около 15% по массе композиции.
В еще одном варианте осуществления композиция по изобретению содержит по меньшей мере одно поверхностно-активное вещество, применимое, например, для того, чтобы придать совместимость другим компонентам композиции и тем самым обеспечить улучшенную стабильность, чтобы способствовать очистке зубной поверхности за счет детергентности и обеспечить пену при взбалтывании, например, во время нанесения щеткой композиции для чистки зубов по изобретению. Может быть использовано любое орально приемлемое поверхностно-активное вещество, большинство из которых является анионогенными, неионогенными или амфотерными. Подходящие анионогенные поверхностно-активные вещества включают, без ограничения, растворимые в воде соли С8-20 алкилсульфаты, сульфированные моноглицериды С8-20 жирных кислот, саркозинаты, таураты и тому подобное. Пояснительные примеры этих и других классов включают натрий лаурил сульфат, натриевую соль кокосового моноглицерид сульфоната, натрий лаурил саркозинат, натрий лаурил изетионат, натрий лаурет карбоксилат и натрий додецил бензолсульфонат. Подходящие неионогенные поверхностно-активные вещества включают, без ограничения, полоксамеры, сложные эфиры полиоксиэтилен сорбитана, этоксилаты жирных спиртов, этоксилаты алкилфенола, третичные амин оксиды, третичные фосфин оксиды, диалкил сульфоксиды и тому подобное. Подходящие амфотерные поверхностно-активные вещества включают, без ограничения, производные С8-20 алифатических вторичных и третичных аминов, имеющие анионную группу, такую как карбоксилат, сульфат, сульфонат, фосфат или фосфонат. Подходящим примером является кокоамидопропил бетаин. Одно или несколько поверхностно-активных веществ необязательно присутствуют в общем количестве от около 0,01% до около 10%, например от около 0,05% до около 5% или от около 0,1% до около 2% по массе композиции.
В другом варианте осуществления композиция содержит орально приемлемое средство против зубного камня. Один или несколько таких средств могут присутствовать. Подходящие средства против зубного камня включают, без ограничения, фосфаты и полифосфаты (например, пирофосфаты), полиаминопропансульфоновую кислоту (AMPS), тригидрат цитрата цинка, полипептиды, такие как полиаспарагиновая и полиглутаминовая кислоты, полиолефин сульфонаты, полиолефин фосфаты, дифосфонаты, такие как азациклоалкан-2,2-дифосфонаты (например, азациклогептан-2,2-дифосфоновая кислота), N-метил азациклопентан-2,3-дифосфоновая кислота, этан-1-гидрокси-1,1-дифосфоновая кислота (EHDP) и этан-1-амино-1,1-дифосфонат, фосфоноалкан карбоновые кислоты и соли каких-либо указанных средств, например соли щелочных металлов и аммония. Применимые неорганические фосфатные и полифосфатные соли включают, иллюстративно, одноосновные, двухосновные и трехосновные фосфаты натрия, триполифосфат натрия (STPP), тетраполифосфат, моно-, ди-, три- и тетранатрий пирофосфаты, динатрий дигидроген фосфат, триметафосфат натрия, гексаметафосфат натрия и тому подобное, где натрий необязательно может быть замещен калием или аммонием. Другие применимые средства против зубного камня включают поликарбоксилатные полимеры. Они включают полимеры и/или сополимеры мономеров, которые содержат группы карбоновых кислот, таких как акриловая кислота, метакриловая кислота и малеиновая кислота и/или ангидрид. Неограничительные примеры включают сополимеры поливинил метилового простого эфира/малеинового ангидрида (PVME/MA), такие как те, которые доступны под названием GANTREZ® от ISP, Wayne, New Jersey, United States of America. Дополнительные другие применимые средства против зубного камня включают пассиваторы, включающие гидроксикарбоновые кислоты, такие как лимонная, фумаровая, яблочная, глутаровпая и щавелевая кислоты и их соли, и аминополикарбоновые кислоты, такие как этилендиаминтетрауксуная кислота (EDTA). Один или несколько средств против зубного камня необязательно присутствуют в композиции в эффективном против зубного камня общем количестве обычно от около 0,01% до около 50%, например от около 0,05% до около 25% или от около 0,1% до около 15% по массе.
В различных вариантах осуществления система потив зубного камня содержит смесь триполифосфата натрия (STPP) и тетранатрий пирофосфата (TSPP). В различных вариантах осуществления отношение TSPP к STPP находится в пределах от около 1:2 до около 1:4. В предпочтительном варианте осуществления первый активный против зубного камня ингредиент, TSPP, присутствует в количестве от около 1% до около 2,5%, и второй активный против зубного камня ингредиент, STPP, присутствует в количестве от около 1 до около 10%.
В различных вариантах осуществления система потив зубного камня дополнительно содержит синтетический анионогенный поликарбоксилатный полимер. В одном варианте осуществления синтетический анионогенный поликарбоксилат присутствует в количестве от около 0,1% до около 5%. В другом варианте осуществления синтетический анионогенный поликарбоксилат присутствует в количестве от около 0,5% до около 1,5%, наиболее предпочтительно от около 1% композиции для профилактики заболеваний ротовой полости. В одном варианте осуществления по данному изобретению система против зубного камня содержит сополимер малеинового ангидрида и метил винилового простого эфира, такой как, например, GANTREZ® S-97, продукт, который обсуждался выше.
В различных вариантах осуществления отношение TSPP к STPP к синтетическому анионогенному поликарбоксилату находится в пределах от около 5:10:1 до около 5:20:10 (или 1:4:2). В одном варианте осуществления система потив зубного камня композиции для профилактики заболеваний ротовой полости содержит TSPP, STPP и поликарбоксилат как сополимер малеинового ангидрида и метил винилового простого эфира при соотношении около 1:7:1. В неограничительном варианте осуществления система потив зубного камня состоит по существу из TSPP, присутствующего в количестве от около 0,5% до около 2,5%, STPP, присутствующего в количестве от около 1% до около 10%, и сополимера малеинового ангидрида и метил винилового простого эфира, присутствующего в количестве от около 0,5% до около 1,5%.
В еще одном варианте осуществления композиция по изобретению содержит по меньшей мере один загуститель, применимый, например, для придания композиции желательной конситенции и/или желательного ощущения в ротовой полости. Может быть использован любой орально приемлемый загуститель, включая, без ограничения, карбомеры, известные также как карбоксивинилоые полимеры, каррагеннаны, известные также как ирландский мох, и более конкретно ι-каррагеннан (йота-каррагеннан), целлюлозные полимеры, такие как гидроксиэтилцеллюлоза, карбоксиметилцеллюлоза (CMC) и их соли, например СМС натрий, натуральные камеди, такие как карайя, ксантан, гуммиарабик и трагакант, коллоидальный смешанный силикат магния и алюминия, коллоидальный кремнезем и тому подобное. Один или несколько загустителей необязательно присутствуют в общем количестве от около 0,01% до около 15%, например от около 0,1% до около 10% или от около 0,2% до около 5% по массе композиции.
В еще одном варианте осуществления композиция по изобретению содержит по меньшей мере один модификатор вязкости, применимый, например, для ингибирования осаждения или разделения ингредиентов или для промотирования повторной диспергируемости при взбалтывании жидкой композиции. Может быть использован любой орально приемлемый модификатор вязкости, включая, без ограничения, минеральное масло, петролатум, глины и органомодифицированные глины, кремнезем и тому подобное. Один или несколько модификаторов вязкости необязательно присутствуют в общем количестве от около 0,01% до около 10%, например от около 0,1% до около 5% по массе композиции.
В другом варианте осуществления композиция содержит орально приемлемый источник фторидных ионов. Один или несколько таких источников могут присутствовать. Подходящие источники фторидных ионов включают фторидные, монофторфосфатные и фторсиликатные соли и фториды аминов, включая олафлур (N'-октадецил-триметилендиамин-N,N,N'-трис(2-этанол)дигидрофторид). Может быть использована любая такая соль, которая является орально приемлемой, включая, без ограничения, соли щелочных металлов (например, калия, натрия), аммония, олова (II) и индия и тому подобное. Обычно используют растворимые в воде высвобождающие фторид соли. Одна или несколько высвобождающих фторид солей необязательно присутствуют в общем количестве, обеспечивающем от около 100 до около 20000 м.д., от около 200 до около 5000 м.д. или от около 500 до около 2500 м.д. фторидных ионов. Когда фторид натрия является единственной высвобождающей фторид солью, фторид натрия в композиции может представлять, для пояснения, от около 0,01% до около 5%, от около 0,05% до около 1% или от около 0,1% до около 0,5% по массе.
Другие компоненты включают, без ограничения, ароматизаторы, красители и другие активные ингредиенты, такие как антиоксиданты и противовоспалительные средства. Компоненты вводят в состав оральных композиций согласно известным процедурам.
Зубные пасты и гели содержат значительные количества увлажнителей и, обычно, абразивное соединение или соединения для чистки зубов. Они введены в состав с различными активными ингредиентами, такими как средства против кариеса, соединение против зубного налета, противовоспалительные средства и тому подобное, в дополнение к антибактериальному соединению и ингибитору насоса оттока.
Полоскания и промывания для ротовой полости содержат ингибиторы насоса оттока и антибактериальные средства в жидком носителе, таком как вода или смесь вода/этанол. Как правило, композиции содержат значительное количество растворителя вплоть до 98 или 99% по массе. Активное соединение (I) необязательно вводят в состав вместе с поверхностно-активными веществами, красителями, ароматизаторами и другими активными ингредиентами.
Орально приемлемым разбавителем или носителем в пастилке, шарике или таблетке является не вызывающий кариеса твердый растворимый в воде многоатомный спирт (полиол), такой как маннит, ксилит, сорбит, мальтит, гидрогенизированный гидролизат крахмала, гидрогенизированная глюкоза, гидрогенизированные дисахариды, гидрогенизированные полисахариды и тому подобное, в количестве от около 85% до около 95% всей композиции. Эмульгаторы, такие как глицерин, и таблетирующие смазки в малых количествах от около 0,1% до 5% могут быть введены в состав таблетки, шарика или пастилки для облегчения получения таблеток, шариков и пастилок. Подходящие смазки включают растительные масла, такие как кокосовое масло, стеарат магния, стеарат алюминия, тальк, крахмал и карбовакс. Подходящие не вызывающие кариеса камеди включают каппа каррагеннан, карбоксиметилцеллюлозу, гидроксиэтилцеллюлозу и тому подобное.
Пастилка, шарик или таблетка необязательно могут быть покрыты кроющим материалом, таким как воски, шеллак, карбоксиметилцеллюлоза, сополимер полиэтилен/малеиновый ангидрид или каппа каррагеннан, чтобы дополнительно увеличить время растворения таблетки или пастилки во рту. Непокрытая таблетка или пастилка медленно растворяются, обеспечивая замедленную скорость высвобождения активных ингредиентов в течение около 3-5 минут. Соответственно, твердые дозированные композиции таблетки, шарика или пастилки по данному варианту осуществления позволяют достичь относительно более продолжительного периода контакта зубов в ротовой полости с антибактериальным средством и ингибитором насоса оттока по данному изобретению.
Составы жевательных резинок обычно содержат гуммиоснову, один или несколько пластифицирующих средств, по меньшей мере один подсластитель и по меньшей мере один ароматизатор в дополнение к антибактериальному соединению и соединениям ингибиторам насоса оттока. Предпочтительно это камедь без сахара.
Материалы гуммиосновы хорошо известны в технике и включают натуральные или синтетические гуммиосновы. Типичные натуральные камеди или эластомеры включают такие как чикл, натуральный каучук, желутонг, балата, гуттаперча, лечи каспи, сорва, гуттакай, кронгум и перилло или их смеси. Типичные синтетические камеди или эластомеры включают бутадиен-стироловые сополимеры, полиизобутилен и изобутилен-изопреновые сополимеры. Гуммиоснову вводят в состав жевательного гуммипродукта в концентрации от около 10% до около 40% и предпочтительно от около 20% до около 35%.
Пластифицирующие/смягчающие средства включают, без ограничения, желатин, воски и их смеси в количествах от около 0,1% до около 5%. Подслащивающий ингредиент, применимый при осуществлении на практике данного изобретения, может быть выбран их широкого разнообразия материалов и включает те же самые исскусственные и полиоловые подсластители, которые используются при приготовлении таблеток, шариков и пастилок. Полиоловые подсластители, такие как сорбит и мальтит, представлены в жевательной гуммикомпозиции по данному изобретению в количествах от около 40% до около 80% и предпочтительно от около 50% до около 75%. В неограничительном варианте осуществления искусственный подсластитель представлен в композиции жевательной резинки по данному изобретению в количествах от около 0,1% до около 2% и предпочтительно от около 0,3% до около 1%.
Предпочтительные варианты осуществления теперь будут пояснены со ссылкой на следующие неограничительные примеры.
Пример 1
Получение 3-(4"-гидрокси-3"-метоксифенил)-1-(2'-гидрокси-5'-метоксифенил)проп-2-ен-1-она (СК-1)
2-Гидрокси-5-метокси ацетофенон (10 г, 0,06 моль) и 3-метокси-4-гидрокси бензальдегид (10 г, 0,06 моль) добавляли к раствору 6 г гидроксида натрия в 30 мл дистиллированной воды в 250 мл круглодонной колбе при 0°С. Температуру реакции поддерживали ниже 15°С с периодическим взбалтыванием в течение 200 ч. Реакционную смесь нейтрализовали 5% водным раствором HCl в условиях охлаждения льдом. Нейтрализованную смесь экстрагировали хлороформом и очищали колоночной хроматографией с использованием силикагеля, получая соединение 2, т. пл. 121,5°С.
1Н ЯМР: δ 3,84 (с, 3Н), δ 3,97 (с, 3Н), δ 6,96 (м, 2Н), δ 7,14(м, 2Н), δ 7,24 (д, 1Н) δ 7,39 (шир.с, 1Н), δ 7,44 (д, 1Н, J=15,31 Гц,), δ 7,86 (д, 1Н, J=15,31 Гц)
Пример 2
Получение 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-она (СК-4)
3-Метокси-4-гидроксибензальдегид (20 г, 0,132 моль) добавляли к раствору ацетофенона (20 г, 0,125 моль), растворенного в уксусной кислоте (20 мл) в круглодонной колбе при постоянном перемешивании. Температуру реакции поддерживали ниже 15°С с периодическим взбалтыванием в течение 200 ч. Реакционную смесь выливали в охлаждаемую льдом воду и продукт экстрагировали хлороформом. Экстракт в хлороформе перегоняли при пониженном давлении и остаток подвергали хроматографии на геле SiO2, получая соединение 1, т. пл. 91°С.
1Н ЯМР: δ 3,94 (с, 3Н), δ 6,96 (д, 1Н, J=8,11 Гц), δ 7,13 (д, 1Н, J=1,78 Гц), δ 7,22 (дд, 1Н, J=8,11 Гц и 1,78 Гц), δ 7,37 (д, 1Н, J=15,30 Гц), δ 7,50 (м, 2Н), δ 7,57 (м, 1Н), δ 7,75 (д, 1Н, J=15,30 Гц), δ 8,01 (м, 2Н).
Пример 3
Получение 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-она (СК-14)
2,3-Диметоксибензальдегид (4,69 г, 0,018 моль) добавляли к раствору ацетилфурана (2 г, 0,018 моль) в метаноле (10 мл) в круглодонной колбе. К этому раствору добавляли 10% водный раствор NaOH (4 мл) при перемешивании. Температуру реакции поддерживали ниже 15°С и перемешивание продолжали в течение 24 ч. Реакционную смесь затем выливали в энергично перемешиваемую охлаждаемую льдом воду и продукт фильтровали. Перекристаллизацию продукта осуществляли с этанолом, т. пл. 109,8°С.
1Н ЯМР: δ 3,80 (с, 3Н), δ 3,88 (с, 3Н), δ 6,69 (дд, 1Н, J=3,56 и 1,99 Гц), δ 7,00 (шир.с, 3Н), δ 7,54 (шир.с, 1Н), δ 7,60 (д, 1Н, J=15,80 Гц), δ 7,84 (шир.с, 1Н), 8,14 (д, 1Н, J=15,80 Гц).
Пример 4
Получение 3-(2",5"-диметоксифенил)-1-(1Н-пиррол-2-ил)проп-2-ен-1-она (СК-16)
2,5-Диметоксибензальдегид (0,76 г, 0,004 моль) добавляли к раствору ацетилпиррола (0,5 г, 0,004 моль) в метаноле (10 мл) в 100 мл Rb (круглодонной колбе). К этому раствору добавляли 10% водный раствор NaOH (2 мл) при перемешивании. Температуру реакции поддерживали ниже 15°С и перемешивание продолжали в течение 15 ч. Реакционную смесь затем выливали в энергично перемешиваемую охлаждаемую льдом воду и продукт фильтровали. Перекристаллизацию продукта осуществляли с этилацетатом, т. пл. 122,6°С.
1Н ЯМР: δ 3,86(с, 6Н), δ 6,35 (шир.с, 1Н), δ 6,96 (д, 1Н, J=6,35 Гц), δ 7,17 (м, 3Н), δ 7,28 (шир.с, 1Н), δ 7,42 (д, 1Н, J=15,90 Гц), δ 8,11 (д, 1Н, J=15,90 Гц).
Пример 5
Снижение MIC ципрофлоксацина против Staphylococcus aureus 1199В (сверхэкспрессия NorA) при использовании в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4)
Минимальную ингибирующую концентрацию (MIC) ципрофлоксацина одного и в сочетании с указанным соединением халкона определяли против Staphylococcus aureus 1199В, используя метод, описанный в программе исследования. Снижение MIC ципрофлоксацина вплоть до шестнадцатикратного наблюдали в сочетании с соединением халкона при 50 мкг/мл (таблица 1).
MIC ципрофлоксацина одного и в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4) против Staphylococcus aureus 1199В (сверхэкспрессия NorA)
конц (мкг/мл)
против Staphylococcus aureus 1199В
Пример 6
Снижение MIC тетрациклина против Staphylococcus aureus SA-K2192 (сверхэкспрессия TetK) при использовании в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4)
Минимальную ингибирующую концентрацию (MIC) тетрациклина одного и в сочетании с указанным соединением халкона определяли против Staphylococcus aureus SA-K2192, используя метод, описанный в программе исследования. Снижение MIC тетрациклина вплоть до восьмикратного наблюдали в сочетании с соединением халкона при 50 мкг/мл (таблица 2).
MIC тетрациклина одного и в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4) против Staphylococcus aureus SA-K2192 (сверхэкспрессия TetK)
конц (мкг/мл)
против Staphylococcus aureus SA-K2192
Пример 7
Снижение MIC тетрациклина против Staphylococcus aureus SA-K2192 (сверхэкспрессия MsrA) при использовании в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4)
Минимальную ингибирующую концентрацию (MIC) эритромицина одного и в сочетании с указанным соединением халкона определяли против Staphylococcus aureus SA-K2192, используя метод, описанный в программе исследования. Снижение MIC эритромицина вплоть до восьмикратного наблюдали в сочетании с соединением халкона при 50 мкг/мл (таблица 3).
MIC эритромицина одного и в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4) против Staphylococcus aureus SA-K2192 (сверхэкспрессия MsrA)
конц (мкг/мл)
против Staphylococcus aureus SA-K2191
Пример 8
Снижение MIC ципрофлоксацина против Staphylococcus aureus 1199В (сверхэкспрессия NorA) при использовании в сочетании с 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-оном (СК-14)
Минимальную ингибирующую концентрацию (MIC) ципрофлоксацина одного и в сочетании с указанным соединением халкона определяли против Staphylococcus aureus 1199В, используя метод, описанный в программе исследования. Снижение MIC ципрофлоксацина вплоть до восьмикратного наблюдали в сочетании с соединением халкона при 50 мкг/мл (таблица 4).
MIC ципрофлоксацина одного и в сочетании с 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-оном (СК-14) против Staphylococcus aureus 1199В (сверхэкспрессия NorA)
конц .(мкг/мл)
против Staphylococcus aureus 1199В
Пример 9
Снижение MIC тетрациклина против Staphylococcus aureus SA-K2192 (сверхэкспрессия TetK) при использовании в сочетании с 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-оном (СК-14)
Минимальную ингибирующую концентрацию (MIC) тетрациклина одного и в сочетании с указанным соединением халкона определяли против Staphylococcus aureus SA-K2192, используя метод, описанный в программе исследования. Снижение MIC ципрофлоксацина вплоть до четырехкратного наблюдали в сочетании с соединением халкона при 50 мкг/мл (таблица 5).
MIC тетрациклина одного и в сочетании с 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-оном (СК-14) против Staphylococcus aureus SA-K2192 (сверхэкспрессия TetK)
конц.(мкг/мл)
Пример 10
Снижение MIC тетрациклина против Staphylococcus aureus SA-K2192 (сверхэкспрессия MsrA) при использовании в сочетании с 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-оном (СК-14)
Минимальную ингибирующую концентрацию (MIC) эритромицина одного и в сочетании с указанным соединением халкона определяли против Staphylococcus aureus SA-K2191, используя метод, описанный в программе исследования. Снижение MIC эритромицина вплоть до четырехкратного наблюдали в сочетании с соединением халкона при 50 мкг/мл (таблица 6).
MIC эритромицина одного и в сочетании с 3-(2",3"-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-оном (СК-14) против Staphylococcus aureus SA-K2191 (сверхэкспрессия MsrA)
конц.(мкг/мл)
Пример 11
Усиление активности триклозана против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum при использовании в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4)
Минимальную ингибирующую концентрацию (MIC) триклозана одного и в сочетании с указанным соединением халкона определяли против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum, используя метод, описанный в программе исследования. Снижение MIC триклозана от четырех- до восьмикратного наблюдали в сочетании с соединением халкона (таблица 7).
(MIC) триклозана одного и в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4) против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum
Пример 12
Усиление активности магнолола против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum при использовании в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4)
Минимальную ингибирующую концентрацию (MIC) магнолола одного и в сочетании с указанным соединением халкона определяли против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum, используя метод, описанный в программе исследования. Снижение MIC магнолола вплоть до шестнадцатикратного наблюдали в сочетании с соединением халкона (таблица 8).
MIC магнолола одного и в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4) против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum
Пример 13
Усиление активности 5,5'-дибутилбифенил-2,2'-диола против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum при использовании в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4)
Минимальную ингибирующую концентрацию (MIC) 5,5'-дибутилбифенил-2,2'-диола одного и в сочетании с указанным соединением халкона определяли против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum, используя метод, описанный в программе исследования. Снижение MIC 5,5'-дибутилбифенил-2,2'-диола от двух- до четырехкратного наблюдали в сочетании с соединением халкона (таблица 9).
(MIC) 5,5'-дибутилбифенил-2,2'-диола одного и в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4) против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum
Пример 14
Усиление активности хонокиола против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum при использовании в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4)
Минимальную ингибирующую концентрацию (MIC) хонокиола одного и в сочетании с указанным соединением халкона определяли против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum, используя метод, описанный в программе исследования. Снижение MIC хонокиола от четырех- до восьмикратного наблюдали в сочетании с соединением халкона (таблица 10).
(MIC) хонокиола одного и в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4) против Streptococcus mutans, Actinomyces viscosus и Fusobacterium nucleatum
Пример 15
Уменьшение потребности в дозе ципрофлоксацина при использовании его в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4) на мышиной модели системной инфекции
Исследование проводили, чтобы увидеть in vivo ответную реакцию на ципрофлоксацин в сочетании с указанным ингибитором насоса оттока. Швейцарских мышей-альбиносов инфицировали внутривенно Staphylococcus aureus АТСС 29213 (107 КОЕ/мышь). Инфицированных мышей разделяли на группы, и каждая группа состояла из 6 мышей. Лечение состояло из одной дозы сразу после инфицирования с последующей дозой через промежуток времени 6 ч. Результат регистрировали каждый день как число живых особей. Мышей наблюдали семь дней и ED50 определяли после семи дней наблюдения. Показатель ED50 для ципрофолксацина был 9,2 мг/кг и в сочетании с СК-4 ED50 для ципрофолксацина уменьшался до 5,86 мг/кг.
Пример 16
Уменьшение концентрации уничтожения биопленки (ВЕС50) для антибактериальных средств, когда их используют в сочетании с 3-(4'-гидрокси-3'-метоксифенил)-1-фенил-проп-2-ен-1-оном (СК-4)
Соединение СК-4 вначале испытывали, чтобы определить, имеет ли оно собственную антимикробную эффективность. Анализ MIC проводили на двух известных антибактериальных средствах, а также СК-4, используя A. viscosus в качестве индикаторного организма. Результаты показаны в таблице 11 ниже:
Из указанной таблицы ясно видно, что СК-4 имеет значительно более высокую MIC чем два обычно используемых антибактериальных средства (триклозан и хлорид цетилпиридиния (СРС)). Это означает, что один СК-4 не является сильным антибактериальным средством и будет, при уровнях, используемых в составах, вносить очень малый вклад в общую антибактериальную эффективность.
Actinomyces viscosus (АТСС #35037) выращивали в трех повторениях в соевом бульоне, обогащенном 0,6% дрожжевым экстрактом (TSB-YE), при 37°С, статическая культура. Для анализов смешанных видов источником бактерий был культуральный хемостат непрерывного действия, инокулированный A. viscosus, Lactpbacillus casei (АТСС #334), Streptococcus oralis (АТСС #35037), Fusobacterium nucleatum (АТСС #10953) и Veilonella parvula (АТСС #17745). Эту смешанную культуру поддерживали при 37°С в специализированной комплексной среде в культуральном хемостате непрерывного действия.
Анализы MIC проводили, используя A. viscosus в качестве индикаторного организма. Соединения, которые должны быть испытаны, размещали в сдвоенных рядах первой колонки стерильного 96-луночного культурального планшета. Двукратные последовательные разбавления осуществляли в 0,5х TSB поперек планшета. Бактерию A. viscosus выращивали в течение ночи в TSB-YE при 37°С, статическая культура. Полученные за ночь культуры бактерии разбавляли до OD610 ~0,4 в 0,5х TSB. Эквивалентный объем бактерии к испытуемому раствору добавляли в каждую лунку 96-луночного планшета. Планшеты инкубировали в течение ночи при 37°С, позволяя происходить бактериальному росту. OD610 всего планшета считывали на ридере микропланшетов Perkin Ellner En Vision. Величины оптической плотности для парных лунок усредняли и сравнивали с величинами для лунок, содержащих только бактерии в одной среде. Величины MIC определяли как концентрацию активного вещества в последней лунке, в которой рост бактерии был ингибирован по отношению к контролям среды. Все планшеты содержали два ряда триклозана в качестве положительного контроля.
Чтобы оценить биоусиливающую способность СК-4, проводили испытания ингибирования образования биопленки отдельными видами. Представляющие интерес активные вещества размещали в первой колонке стерильного 384-луночного культурального планшета и последовательные двукратные разбавления в 0,5х TSB осуществляли поперек планшета. Первые культуры размножения бактерии A. viscosus выращивали в течение ночи в TSB-YE. Культуры разбавляли до OD610 ~0,2 в 0,5х TSB и помещали в лунки, содержащие последовательные разбавления активных веществ. Планшеты инкубировали а течение 24 часов при 37°С и обеспечивали возможность роста и образования биопленки.
После инкубирования супернатанты удаляли из планшета и оставшиеся биопленки окрашивали 0,3% крезиловым фиолетовым по Грам. Окрашенные планшеты считывали на ридере микропланшетов Perkin Elmer En Vision для оптической плотности при 590 нм. Величины оптической плотности сравнивали с оптической плотностью лунок, обработанных только средой, и результаты представлены как процентное уменьшение образования биопленки относительно контроля среды. ВЕС50 определяют как наименьшую концентрацию, при которой происходит более чем 50% уменьшение плотности биопленки (как зарегистрировано по оптической плотности красителя, используемого для окрашивания биопленки) относительно контроля только со средой. Соединение с более низкой ВЕС50 считается более эффективным, чем соединение с более высокой величиной. Результаты показаны в таблице 12 ниже для разнообразных известных антибактериальных средств.
ВЕС50 антибактериальных средств одних и с СК-4
Результаты этого эксперимента показывают, что добавление СК-4 имеет потенциальную возможность существенно и неожиданно увеличивать эффективность нескольких антимикробных соединений, несмотря на отсутствие у него собственной какой-либо значительной активности. Эффект был особенно сильным для хлорида цетилпиридиния (СРС), который имел результатом приблизительно 4кратное снижение ВЕС50 по сравнению с одним СРС, позволяя таким образом применять значительно более низкие концентрации антимикробного вещества для достижения той же антибактериальной эффективности (вплоть до 75% менее СРС при применении вместе с СК-4).
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ 4- ИЗОПРОПИЛ-3- МЕТИЛФЕНОЛ И ИОНЫ ЦИНКА | 2010 |
|
RU2535010C2 |
| Композиция, содержащая антибиотик и диспергирующее средство или антиадгезивный агент | 2011 |
|
RU2739249C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИБИОТИК И ДИСПЕРГИРУЮЩЕЕ СРЕДСТВО ИЛИ АНТИАДГЕЗИВНЫЙ АГЕНТ | 2011 |
|
RU2607660C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ВНЕКЛЕТОЧНОГО МЕТАБОЛИТА BACILLUS COAGULANS И ЕГО БИОЛОГИЧЕСКИЕ ПРИМЕНЕНИЯ | 2014 |
|
RU2617965C2 |
| ПРЕБИОТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА, СОДЕРЖАЩИЕ КАРБОНОВЫЕ КИСЛОТЫ | 2013 |
|
RU2673473C2 |
| СПОСОБЫ УХОДА ЗА ПОЛОСТЬЮ РТА С ИСПОЛЬЗОВАНИЕМ САХАРИДА В КАЧЕСТВЕ ПРЕБИОТИКА | 2013 |
|
RU2691408C2 |
| АНТИМИКРОБНЫЕ КОМПОЗИЦИИ | 2013 |
|
RU2694758C2 |
| ГАЛОГЕНИРОВАННЫЕ БИФЕНОЛЫ В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2010 |
|
RU2549543C2 |
| КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2009 |
|
RU2526913C2 |
| ИНГИБИРОВАНИЕ ОРГАНИЗМОВ БИОПЛЕНКИ | 2010 |
|
RU2548786C2 |
Изобретение относится к области антимикробных средств и касается композиций, содержащих антимикробный агент и соединение, которое является эффективным для усиления действия антимикробного агента. Композиция для предотвращения и/или лечения заболеваний ротовой полости содержит носитель, антимикробное средство и соединение, выбранное из группы халконов, состоящей из 3-(4′-гидрокси-3′-метоксифенил)-1-(2′-гидрокси-5′-метоксифенил)проп-2-ен-1-она, 3-(4′-гидрокси-3′-метоксифенил)-1-фенил-проп-2-ен-1-она, 3-(2″,3″-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-она, 3-(2″,5″-диметоксифенил)-1-(1Н-пиррол-2-ил)проп-2-ен-1-она и их смесей. Композиция предпочтительно выполнена в форме средства для чистки зубов. Использование вышеуказанных халконов в сочетании с антимикробными средствами значительно усиливает эффективность антимикробных средств. 14 з.п. ф-лы, 12 табл., 16 пр.
1. Композиция для предотвращения и/или лечения заболеваний ротовой полости, содержащая носитель, антимикробное средство и соединение, выбранное из группы, состоящей из 3-(4′-гидрокси-3′-метоксифенил)-1-(2′-гидрокси-5′-метоксифенил)проп-2-ен-1-она, 3-(4′-гидрокси-3′-метокси-фенил)-1-фенил-проп-2-ен-1-она, 3-(2″,3″-диметоксифенил)-1-фуран-2-ил-проп-2-ен-1-она, 3-(2″,5″-диметоксифенил)-1-(1Н-пиррол-2-ил)проп-2-ен-1-она и их смесей.
2. Композиция по п.1, где композиция находится в форме средства для чистки зубов, выбранного из группы, состоящей из зубной пасты, зубного порошка, геля, полоскания, пастилки, жевательной резинки, пленки и их смесей.
3. Композиция по п.2, где антимикробное средство содержит антибактериальное средство.
4. Композиция по п.3, где антибактериальное средство выбрано из группы, состоящей из хинолона, бета-лактама, хлорамфеникола, гликопептида, аминогликозида, макролида, рифамицина, оксазолидонона, кумермицина, полифенольного средства, триклозана, соединения четвертичного аммония, соединения цинка, сложного эфира бороновой кислоты и их смесей.
5. Композиция по п.4, где полифенольным средством является триклозан, или содержит магнолол или его производные, или содержит хонокиол или его производные.
6. Композиция по п.4, где соединением четвертичного аммония является хлорид цетилпиридиния.
7. Композиция по п.1, где соединением является 3-(4′-гидрокси-3′-метоксифенил)-1-фенил-проп-2-ен-1-он.
8. Композиция по п.1 для лечения микробной инфекции, посредством местного введения в ротовую полость млекопитающего, нуждающегося в этом.
9. Композиция по п.8, где микробная инфекция вызвана бактерией.
10. Композиция но п.9, где композиция находится в форме средства для чистки зубов, выбранного из группы, состоящей из зубной пасты, зубного порошка, геля, полоскания, пастилки, жевательной резинки, пленки и их смесей.
11. Композиция по п.8, где антимикробное средство включает антибактериальное средство.
12. Композиция по п.11, где антибактериальное средство выбрано из группы, состоящей из хинолона, бета-лактама, хлорамфеникола, гликопептида, аминогликозида, макролида, рифамицина, оксазолидонона, кумермицина, полифенольного средства, триклозана, соединения четвертичного аммония, соединения цинка, сложного эфира бороновой кислоты и их смесей.
13. Композиция по п.12, где полифенольным средством является триклозан, или содержит магнолол или его производные, или содержит хонокиол или его производные.
14. Композиция по п.12, где соединением является 3-(4′-гидрокси-3′-метоксифенил)-1-фенил-проп-2-ен-1-он.
15. Композиция по п.8, при использовании которой количество микробов в ротовой полости снижается.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| BATOVSKA D | |||
| et al | |||
| Examination of growth inhibitory properties of synthetic chalcones for which antibacterial activity was predicted | |||
| EUROPEAN JOURNAL OF MEDICAL CHEMISTRY | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Упаковочный сосуд | 1924 |
|
SU2211A1 |
| EP 1764363 A2, 21.03.2007 | |||
| JP 2003171274 A, 17.06.2003 | |||
| Производные халкона в качестве антибактериальных средств | 1977 |
|
SU677262A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
Авторы
Даты
2014-06-27—Публикация
2009-12-18—Подача