(54) ПРОИЗВОДНЫЕ ХАЛКОНА В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ
го натра, содержащего 3,4 г NaOH. Образуется осадок желтого цвета.
После 2 ч непрерывного перемешивания реакционную смесь оставляют на 12 ч, после чего вылнвают в холодную воду и подкисляют 20%-ным раствором серной кислоты до рН 5. Выпавшнй осадок желтого цвета фильтруют и промывают холодной водой.
Выход 61%, т. пл. 166-167° С (е./ОН).
Найдено, %: С 56,36, Н 4,40, Вг 22,15, N 3,90.
CirHisOsBr.
Вычислено, %: С 56,35, Н 4,42, Вг 22,10, N 3,86.
УФ-спектр: Я:,,.,-; 344, 2,60 нм (еЮН).
МК-спбктр: 1650, 1600, 1480 см-.
Пример 2. 4-нитро-2, 4-диокси-5бромхалкон.
В 20 мл 96%-ного этилового спирта растворяют 1,7 г бромрезацетофенона и при перемешивании добавляют 1,1 г л-нитробензальдегида. При непрерывном перемешивании к реакционной смеси добавляют 5 мл водного раствора едкого натра, содержаш.его 3,4 г NaOH. Образуется осадок желтого цвета. После 2 ч непрерывного перемешивания реакционную смесь оставляют на 12 ч, после чего выливают в ледяную воду и подкисляют 20%-ным раствором серной кислоты до рН 4,5. Выпавший осадок л елтого цвета фильтруют и промывают водой.
Выход 55%, т. пл. 165° С (еЮН).
Найдено, %: С 49,50, Н 2,76, N 3,80, Вг 22,06.
CisHioOsBr.
Вычислено, %: С 49,45, Н 2,74, N 3,84, Вг 21,98.
УФ-спектр: л ,„ах 344, 267 нм.
ИК-спектр: 1660, 1610, 1480 CM™.
Пример 3. 2,2,4-триокси-3-метокси5-бромхалкон.
В 20 мл 96%-ного этилового спирта растворяют 1,7 г бромрезацетофенона и 1,12 г о-ркси-ж-метоксибензальдегида. При непрерывном перемешивании к реакционной смеси добавляют 6 мл водного раствора едкого натра, содержащего 3,7 г NaOH. Образуется осадок желтого цвета.
Реакционную смесь непрерывно перемешивают в течение 2 ч, после чего оставляют на 16 ч, а затем вылив.ают в 100 мл ледяной воды и П)0 дкисляют 20%-ны;м раствором серной кислоты до рН 5. .Выпавший осадок желтого цвета фильтруют и промывают холодной водой до нейтральной реакции.
Выход 69%, т. пл. 168° С (еЮН).
Найдено, %: С 52,51, Н 3,60, Вг 22,00.
CieHi OgBr.
Вычислено, %; С 52,60, Н 3,56, Вг 21,91; УФ-спектр: А,,ах 344, 259 нм.
HTf-nnPTfTn- IKfi. Ifil. 14«n f-Mпример 4. 3,2,4-триокси-4-метокси5-бромхалкон.
В 20 мл 96%-ного этилового спирта растворяют 1,7 г бромрезацетофенона и 1,Л/2 г .«-окси-л-метоксибензальдегида. При непрерывном перемешивании к реакционной смеси добавляют 6 мл водного раствора едкого натра, содержащего 3,7 г NaOH.
Образ1уется осадо|к желтого цвета. Реакционн}ю смесь непрерывно перемешивают в течение 2 ч, после чего оставляют на 16 ч, а затем выливают в 100 мл ледяной воды Н подкисляют 20%-ным раствором серной кислоты до рН 5. Выпавший осадок желтого цвета фильтруют и промывают холодной водой до нейтральной реакции.
Т. пл. 161° С (еЮН).
Найдено, %: С 52,55, Н 3,52, Вг 22,08. CieHisOsBr.
Вычислено, %: С 52,60, Н 3,56, Вг 21,91.
УФ-спектр: 344, 259 нм.
ИК-спектр: 1665, 1620, 1492 см-.
П р И м е р 5. 3,4-диметокси-2Ч-диокси5-бромхалкон.
В 20 мл 96%-ного этилового спирта растворяют 1,7 г бромрезацетофенона и 1,22 г 3,4-диметокси1бензальдегида. При непрерывном перемешивании к реакционной смеси добавляют 5 мл водного раствора едкого натра, содержащего 3,4 г NaOH. Образуется осадок желтого цвета. После 2 ч непрерывного перемешивания реакционную смесь оставляют на 12 ч, после чего выливают в холодную воду и подкисляют 20%ным раствором серной кислоты до рН 5. Выпавший осадок отфильтровывают и промывают холодной водой. Выход 93%, т. пл. 145° С.
Найдено %: С 53,90, Н 4,00, Вг 21,00. CirHisOgBr.
Вычислено, %: С 53,82, Н 3,95, Вг 21,10. УФ-спектр: А,тач 344, 259 нм (еЮН). ИК-спектр: 1650, 1600, 1480 см-.
Пример 6. 4,2,4-триакси-3-карбокси5-бромхалкон получают из 1,7 г бромрезацетофенона и 1,22 г 5-альдегидосалициловой кислоты в условиях, аналогичных при.меру 5, с выходом 75%. Т. пл. 150° С (40% водный еЮН).
Найдено, %: С 50,90, Н 2,86, Вг 21,05.
Вычислено, %: С 50,66, Н 2,90, Вг 21,10. УФ-спектр: Я„,ах 334, 259 нм.
ИК-спектр 1660, 1(590, il485 .
Исследование предложенных соединений на антибактериальную активность.
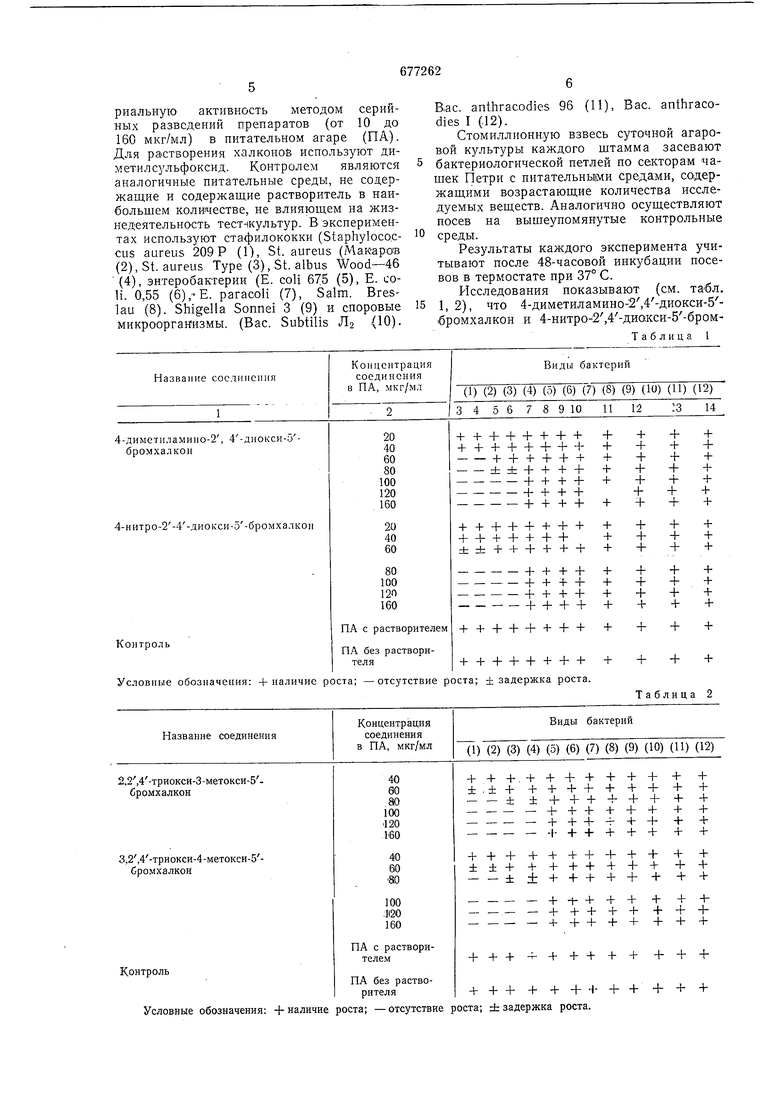
4-диметиламино-24 - диокси - 5 - бромхалкон (а),4-нитро-24-диокси-5 - бромхалкон(б),2,2,4- триокси-3 - метокси-5-бромхалкон (в), 3,2,4-триокси-4-метокси-5-бром.. хал;кон (г), 3,4 - диметокси - 2,4-диокси-5бромхалкон (д), 4,2,4-трнокси-3-карбокси 1-(ллпилуя rrwoH (f иплпрггУют игя янтибяктрриальную активность методом серийных разведений препаратов (от 10 до 160 мкг/мл) в питательном агаре (ПА). Для растворения халконоб используют диметилсульфоксид. Контролем являются аналогичные питательные среды, не содержащие и содержащие растворитель в наибольщем количестве, не влияющем на жизнедеятельность тестнкультур. В экспериментах используют стафилококки (StaphylococCUS aureus 209 Р (1), St. aureus (Макаров (2), St. aureus Type (3), St. albus Wood-46 (4), энтеробактерии (E. coli 675 (5), E. coli. 0,55 (6),-E. paracoli (7), Salm. Breslau (8). Shigella Sonnei 3 (9) и споровые микроорганизмы. (Вас. Subtilis Я (Ю).
В.ас. anthracodies 96 (11), Вас. anthracodies I (12).
Стомиллионную взвесь суточной агаровой культуры каждого щтамма засевают бактериологической петлей по секторам чашек Петри с питательньвми средами, содержащими возрастающие количества исследуемых веществ. Аналогично осуществляют посев на вышеупомянутые контрольные среды.
Результаты каждого эксперимента учитывают после 48-часовой инкубации посевов в термостате при 37° С.
Исследования показывают (см. табл. 1, 2), что 4-диметиламино-2,4-диокси-5бромхалкон и 4-нитро-2,4-дио;кси-5-бромТаблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Производные халкона в качестве противовоспалительных и капилляроукрепляющих средств | 1979 |
|
SU750960A1 |
| Производные халкона в качестве антибактериальных средств | 1976 |
|
SU593425A1 |
| Производные 4-карбоксивиниленхалкона, обладающие антигрибковой активностью | 1988 |
|
SU1571982A1 |
| Производные @ -амира-3-он-12-ен-28-овой кислоты, обладающие антибактериальной активностью по отношению к Вас.SUвRILIS L-2 и Вас.ceReUS(VaR.аNтнRасоIDеS)96 | 1984 |
|
SU1325881A1 |
| Производные халкона в качестве противовоспалительных и капилляроукрепляющих средств | 1978 |
|
SU694009A1 |
| Способ получения этил 3-(3-гидрокси-1,4-диоксо-1,4-дигидронафталин-2-ил)-2,5,10-триоксо-10b-фенил-1,2,3,5,10,10b-гексагидро-3аН-нафто[2',3':4,5]фуро[3,2-b]пиррол-3а-карбоксилатов | 2017 |
|
RU2643372C1 |
| Способ получения -гомостероидов | 1976 |
|
SU689621A3 |
| Способ получения производных прегнановой кислоты | 1974 |
|
SU622411A3 |
| Способ получения 6,6,9 -трифторпрегнанов | 1971 |
|
SU492079A3 |
| Способ получения -гомостероидов | 1975 |
|
SU634676A3 |

Условные обозначения: + наличие роста; -отсутствие
Условные обозначения: -{- наличие роста; - отсутствие роста; db задержка роста.
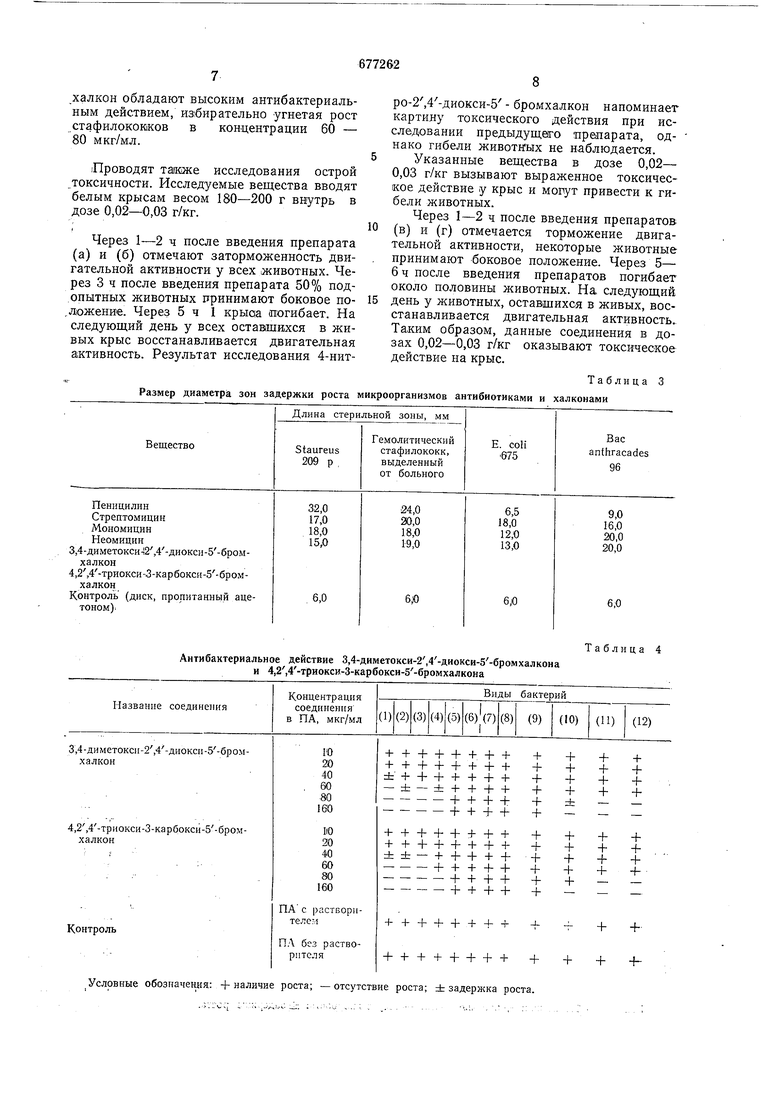
Таблица 2 роста; ± задержка роста
халкон обладают высоким антибактериальным действием, избирательно угнетая рост стафилокок1ков в концентрации 60 - 80 мкг/мл.
Проводят также исследования острой токсичности. Исследуемые вещества вводят белым крысам весом 180-200 г внутрь в дозе 0,02-0,03 г/кг.
Через 1-2 ч после введения препарата (а) и (б) отмечают заторможенность двигательной активности у всех животных. Через 3 ч после введения препарата 50% подопытных животных принимают боковое по„ложение. Через 5 ч 1 крыоа погибает. На следующий день у всех оставщкхся в живых крыс восстанавливается двигательная активность. Результат исследования 4-нитРазмер диаметра зон задержки роста микроорганизмов
Антибактериальное действие 3,4-диметокси-2,4-диокси-5-бромхалкона и 4,2,4-триокси-3-карбокси-5-бромхалкона
Условные обозначения: -f-наличие роста; -отсутствие роста; ± задержка роста.
ро-2,4-диокси-5 - бромхалкон напоминает картину токсического действия при исследовании предыдущего препарата, однако гибели животных не наблюдается.
Указанные вещества в дозе 0,02- 0,03 г/кг вызывают выраженное токсическое действие у крыс и могут привести к гибели животных.
Через I-2 ч после введения препаратов (в) и (г) отмечается торможение двигательной активности, некоторые животные принимают боковое положение. Через 5- 6 ч после введения препаратов погибает около половины животных. На следующий день у животных, оставшихся в живых, восстанавливается двигательная активность. Таким образом, данные соединения в дозах 0,02-0,03 г/кг оказывают токсическое действие на крыс.
Таблица 3
Таблица 4 антибиотиками и халконами Биологические испытания также показывают, что полученные халконы (д, е) обладают высоким антибактериальным действием на некоторые микроорганизмы при концентрации препарата в питательной среде равной 40-60 мкг/мл. Результаты испытаний на антибактериальную активность представлены в табл. 3 и 4. Исследования острой токсичности показывают, что 3,4-ди метокси-2,4-диокси-5бромхалкон и 4,2,4-триокси-3-карбокси-5бромхалкон малотоксичны. LDso для данных препаратов для крыс -0,05 г/кг. Формула изобретения Производные халкона общей формулы где при RI-Н, Н2 Кз-ОСНз; или при RI-Н, R2-СООН, Нз-ОН; или при RI-ОН, R2-ОСНз, R3-Н; или при RI-Н, R2-ОН, Rs-ОСНз; или при Ri R2-Н, Ra-N, N0, в качестве антибактериальных средств. Источники информации, принятые во внимание при экспертизе: 1. S. Н. Dandegaonker und Revanker. Arch. Pharm und Ber. Deutsch Pharmaz. Ges, 1967, beru 300, 11, c;. 897. 2. Авторское свидетельство СССР по заявке № 2356309/23-04, кл. С 07 С 49/02, 11.05.76.
Авторы
Даты
1982-04-30—Публикация
1977-12-28—Подача