Ссылки на родственные заявки на патенты
Данная заявка на патент представляет собой подачу обычной заявки на основе предварительной заявки на патент США №61920567, поданной 24 декабря 2013 в отношении изобретения, озаглавленного "СПОСОБ ПРОДУКЦИИ ЧАСТИЧНО ОЧИЩЕННЫХ ВНЕКЛЕТОЧНЫХ ПРОДУКТОВ МЕТАБОЛИЗМА BACILLUS COAGULANS И ИХ БИОЛОГИЧЕСКИЕ ПРИМЕНЕНИЯ".
Предшествующий уровень техники
Область изобретения
Изобретение в общем относится к антимикробным действиям пробиотических препаратов. Конкретно настоящее изобретение относится к: (1) способу получения частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банк, и которому присвоен номер штамма MTCC 5856), демонстрирующему 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050 и (2) антимикробному профилю указанного препарата внеклеточного метаболита против панели микробных патогенов, включая синергические антимикробные действия препарата при комбинировании с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis. Также показано, что препарат внеклеточного метаболита отдельно или комбинация указанного препарата внеклеточного метаболита и смеси консервантов синергическим образом ингибирует образование микробной биопленки.
Описание предшествующего уровня техники
В области техники известны внеклеточные продукты Bacillus coagulans, содержащие супернатант или фильтрат культуры штамма Bacillus coagulans, подходящие для местного применения на кожу или слизистые оболочки млекопитающего, и, таким образом, которые можно использовать для ингибирования роста бактерий, дрожжей, грибов, вирусов и их комбинаций (US 6905692, "Topical compositions containing probiotic Bacillus bacteria, spores, and extracellular products and uses thereof"). Настоящее изобретение относится к дополнительной очистке внеклеточных компонентов культуры пробиотических Bacillus coagulans SBC37-01 (депонированной в Коллекцию типовых культур микроорганизмов и Генетический банк, и которой присвоен номер штамма МТСС 5856) с получением концентрированного препарата внеклеточного метаболита, который демонстрирует повышенные антимикробные действия по сравнению с самим супернатантом и в комбинации с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis, способ получения которой раскрыт в US 2010/120911.
Основная задача настоящего изобретения заключается в том, чтобы раскрыть:
1) Способ продукции частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банке, и которому присвоен номер штамма МТСС 5856), демонстрирующего 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans АТСС 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans АТСС 7050.
2) Антимикробный профиль указанного препарата внеклеточного метаболита против панели микробных патогенов, включая синергические антимикробные действия препарата при комбинировании с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
3) Ингибирующее в отношении микробной биопленки действие указанного препарата внеклеточного метаболита отдельно или в комбинации с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
Настоящее изобретение удовлетворяет вышеуказанным задачам и обеспечивает дополнительные преимущества.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретение описан
(1) Способ продукции частично очищенного препарата внеклеточного метаболита из пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банк, и которому присвоен номер штамма MTCC 5856), демонстрирующего 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050;
(2) Антимикробный профиль указанного препарата внеклеточного метаболита против панели микробных патогенов, включая синергические антимикробные действия препарата при комбинировании с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis, и
(3) Ингибирующее в отношении микробной биопленки действие указанного препарата внеклеточного метаболита отдельно или в комбинации с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
(4) Антимикробная активность и антикислотогенное действие против адгезированных S. mutans в не растворимых в воде глюканах указанного препарата внеклеточного метаболита самого по себе или в комбинации с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
В настоящем изобретении предложены следующие преимущества.
1) Раскрыт способ очистки для продукции частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банк, и которому присвоен номер штамма MTCC 5856), демонстрирующего 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050;
2) Раскрыт антимикробный профиль частично очищенного препарата против панели микробных патогенов, включая синергические антимикробные действия указанного частично очищенного внеклеточного препарата при комбинировании с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
3) Раскрыт ингибирующий микробную биопленку потенциал указанного препарата внеклеточного метаболита самого по себе или в комбинации с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
4) Раскрыта антимикробная активность и антикислотогенное действие против адгезированных S. mutans в не растворимых в воде глюканах указанного препарата внеклеточного метаболита отдельно или в комбинации с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
Другие особенности и преимущества настоящего изобретения будут понятны из следующего более подробного описания в сочетании с сопутствующими графическими материалами, которые в качестве примера иллюстрируют принцип изобретения.
Краткое описание чертежей
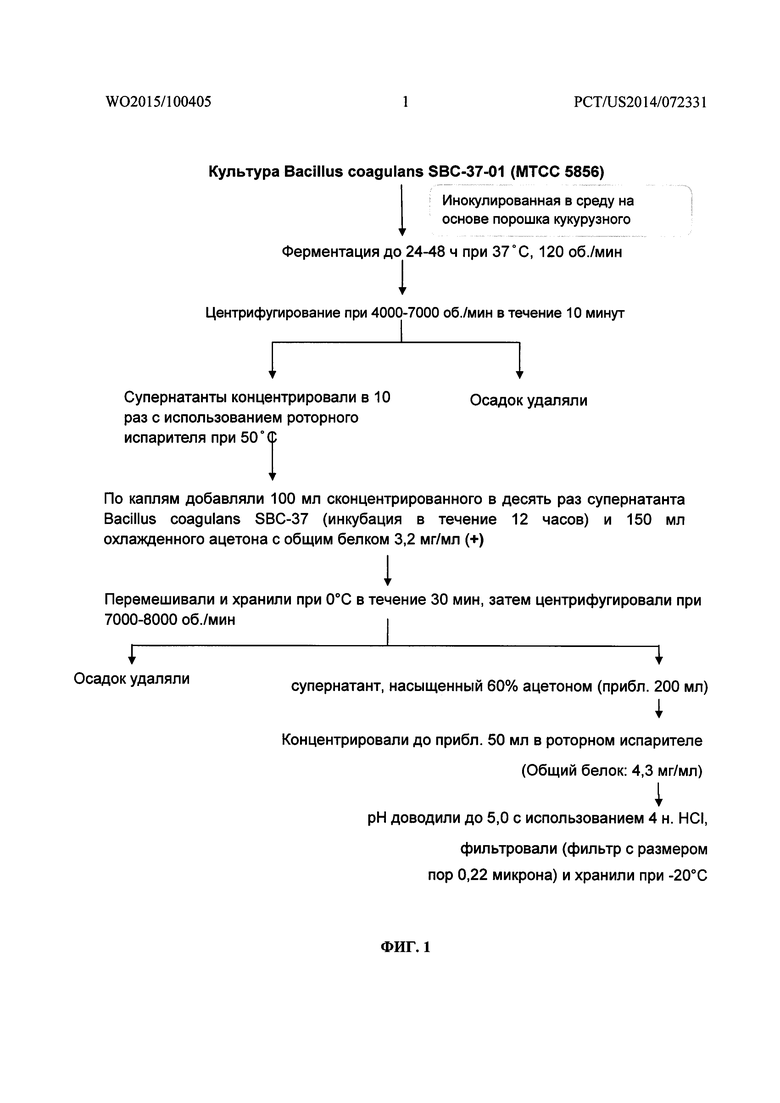
На Фиг. 1 показана блок-схема способа очистки для получения частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банк, и которому присвоен номер штамма MTCC 5856), демонстрирующего 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050.
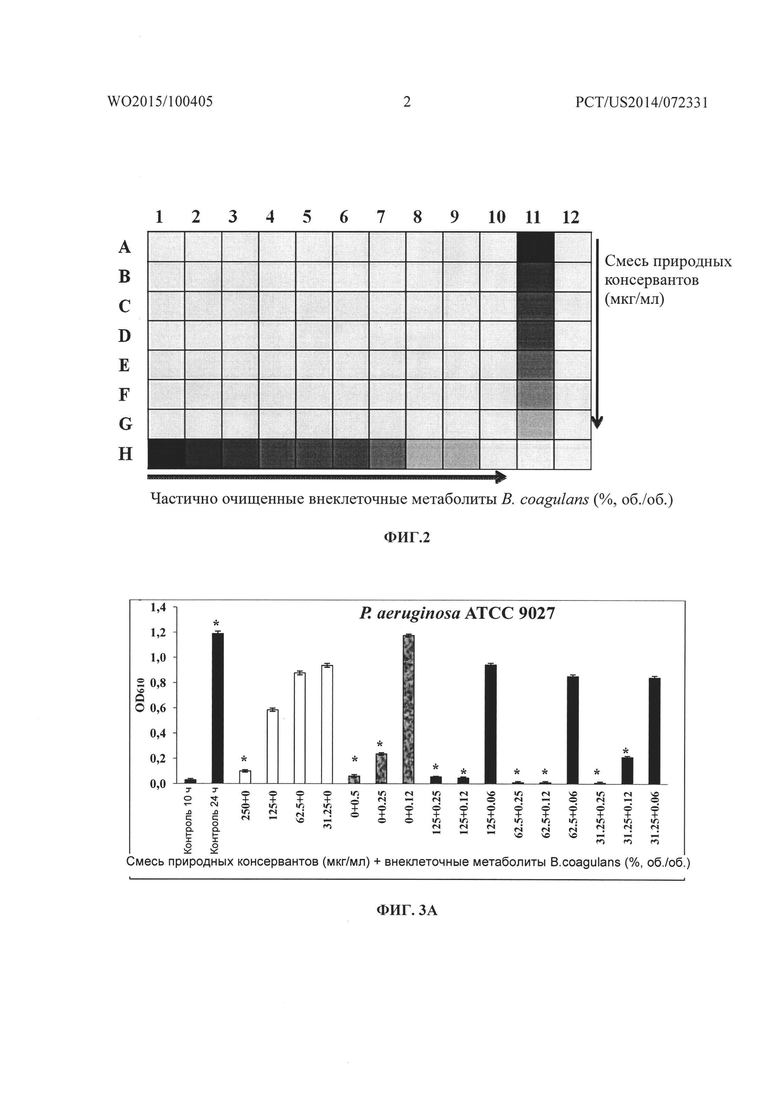
На Фиг. 2 показана схема «шахматной доски» микроразведения средой для синергических антимикробных исследований.
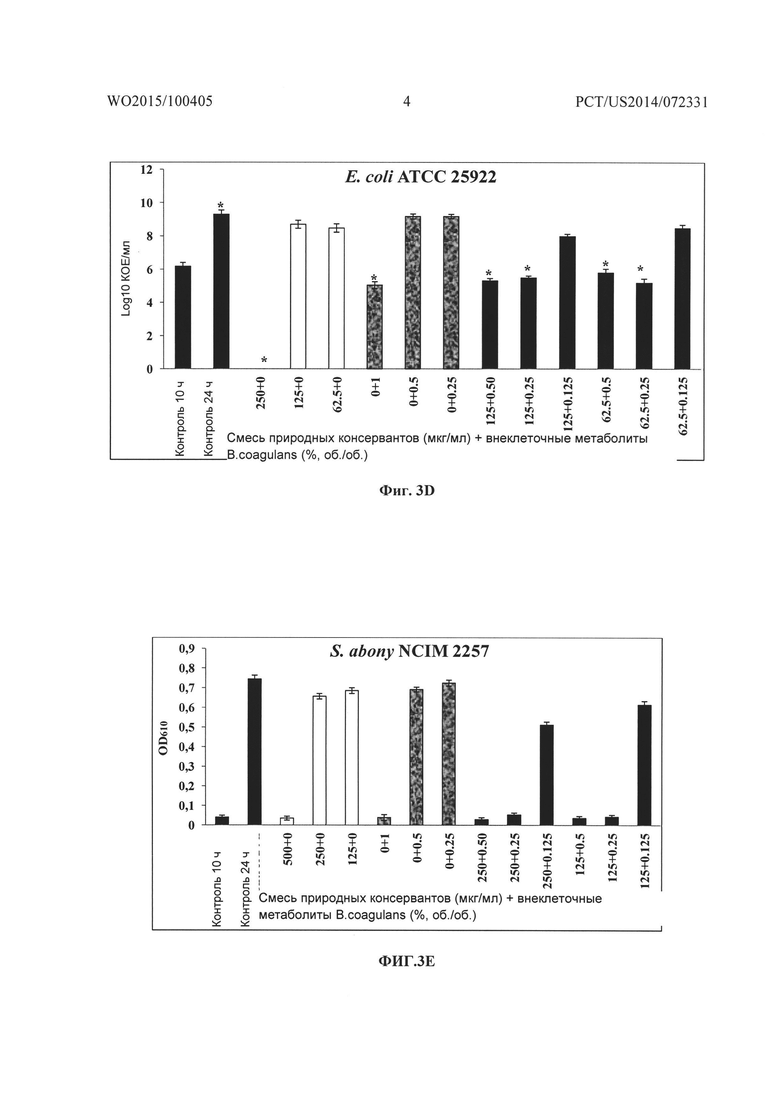
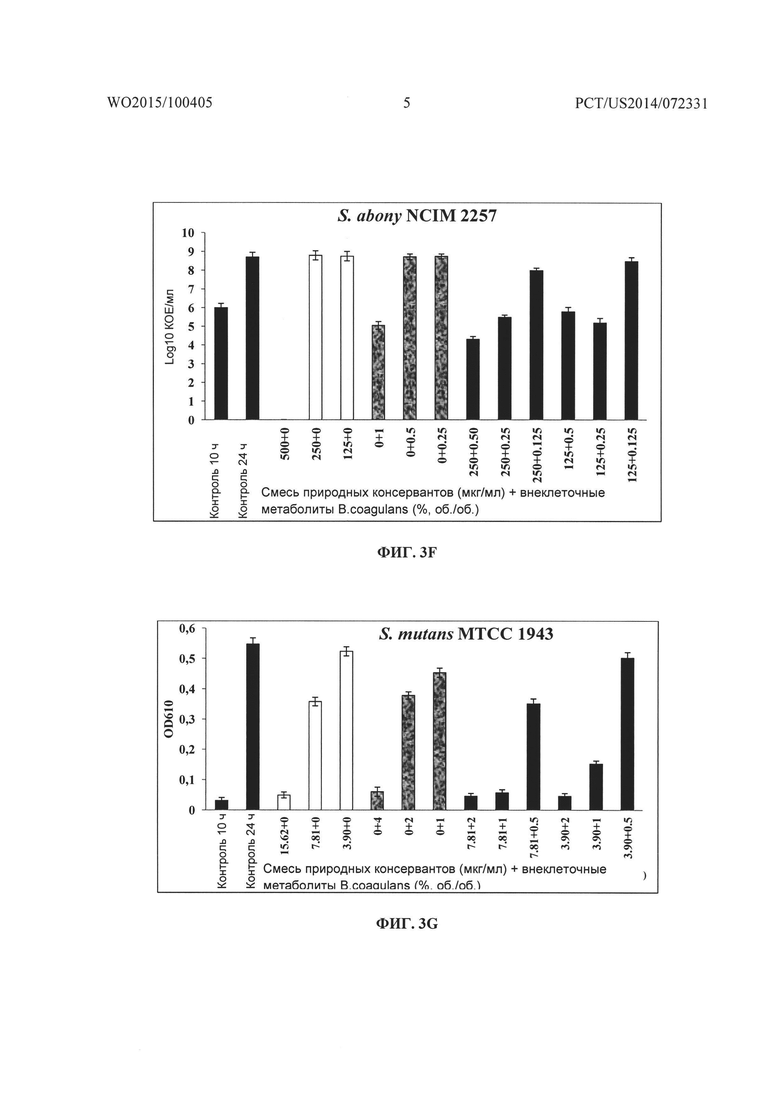
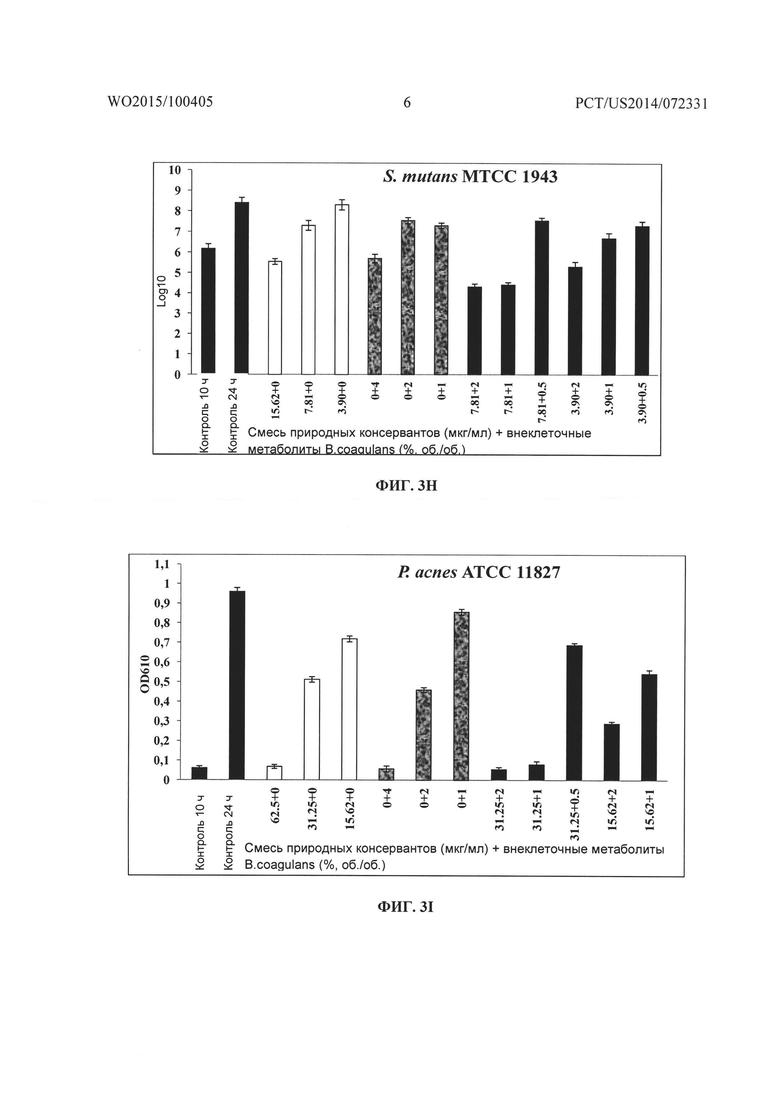
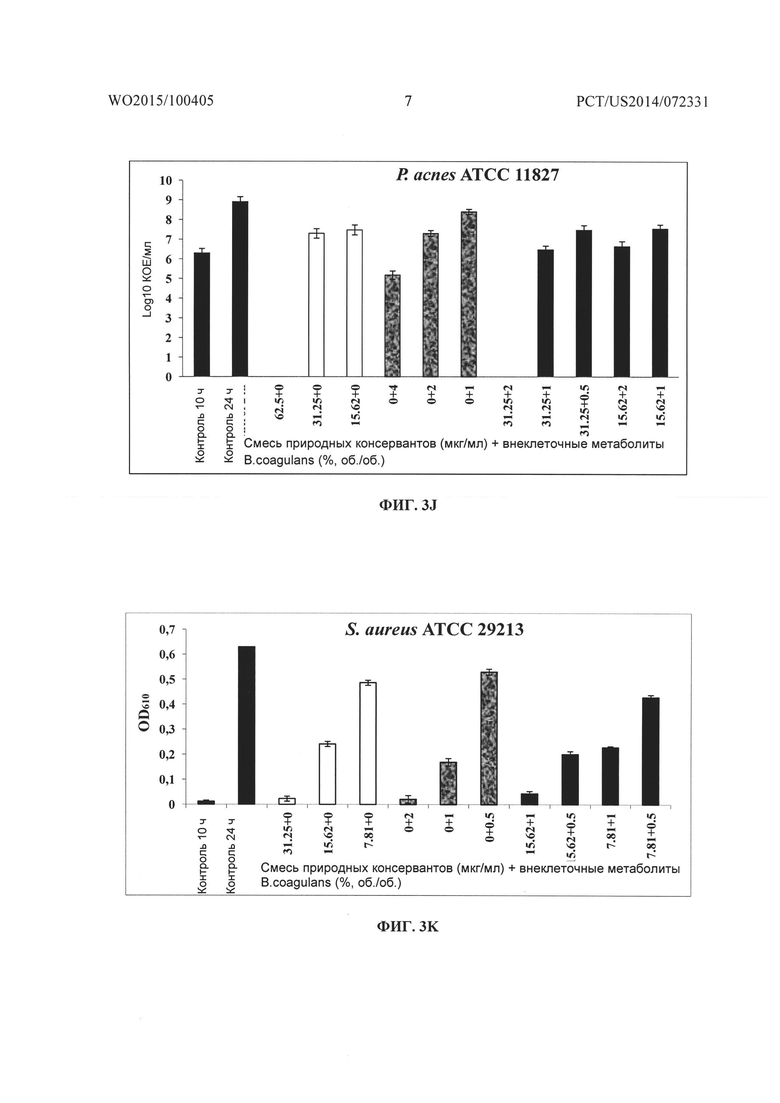
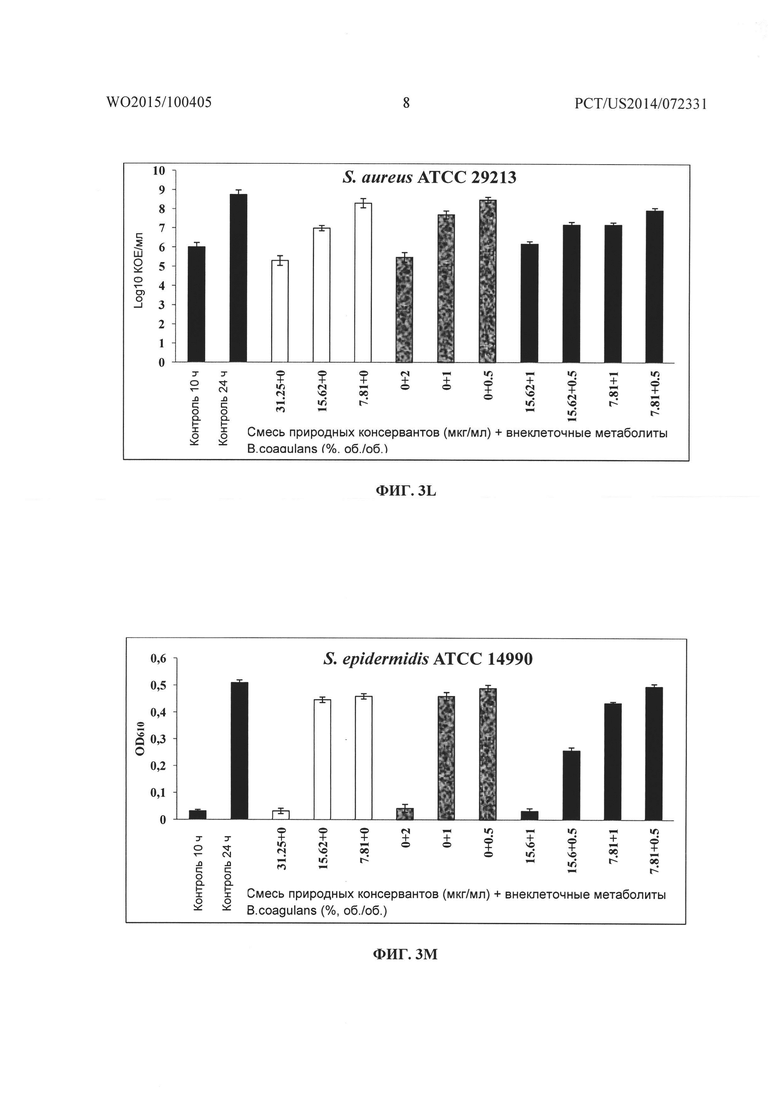
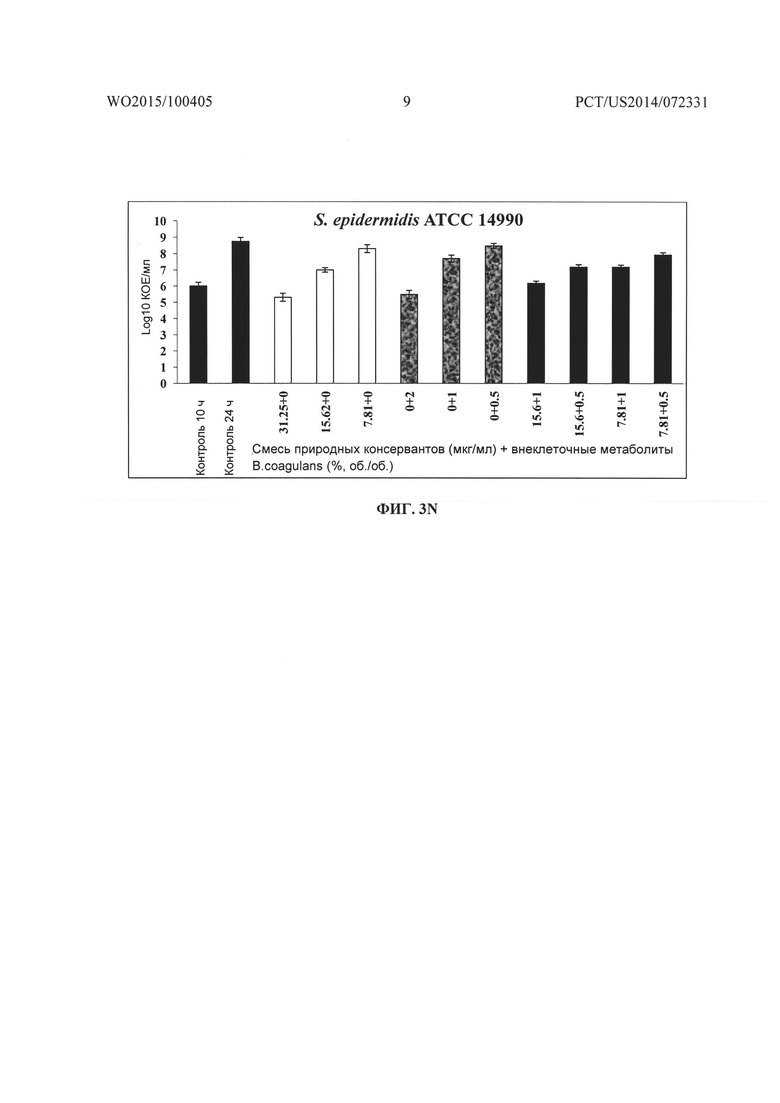
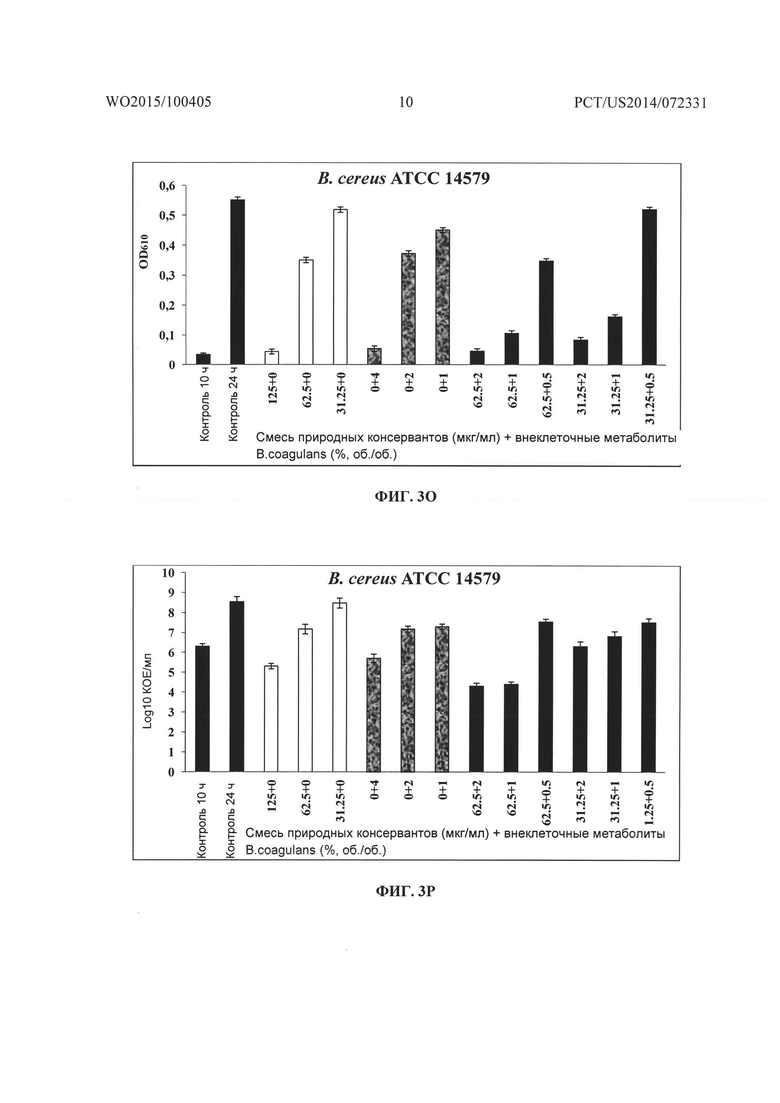
На Фиг. 3A-3B, 3C-3D, 3E-3F, 3G-3H, 3I-3J, 3K-3L, 3M-3N, 3O-3P соответственно показано графическое представление действия смеси природных консервантов и внеклеточных метаболитов B. coagulans MTCC 5856 отдельно и в комбинации на рост и жизнеспособность Pseudomonas aeruginosa ATCC 9027, Escherichia coli ATCC 25922, Salmonella abony NCIM 2257, Streptococcus mutans MTCC 1943, Propionibacterium acnes ATCC 11827, Staphylococcus aureus ATCC 29213, Staphlococcus epidermidis ATCC 14990 и Bacillus cereus ATCC 14579.
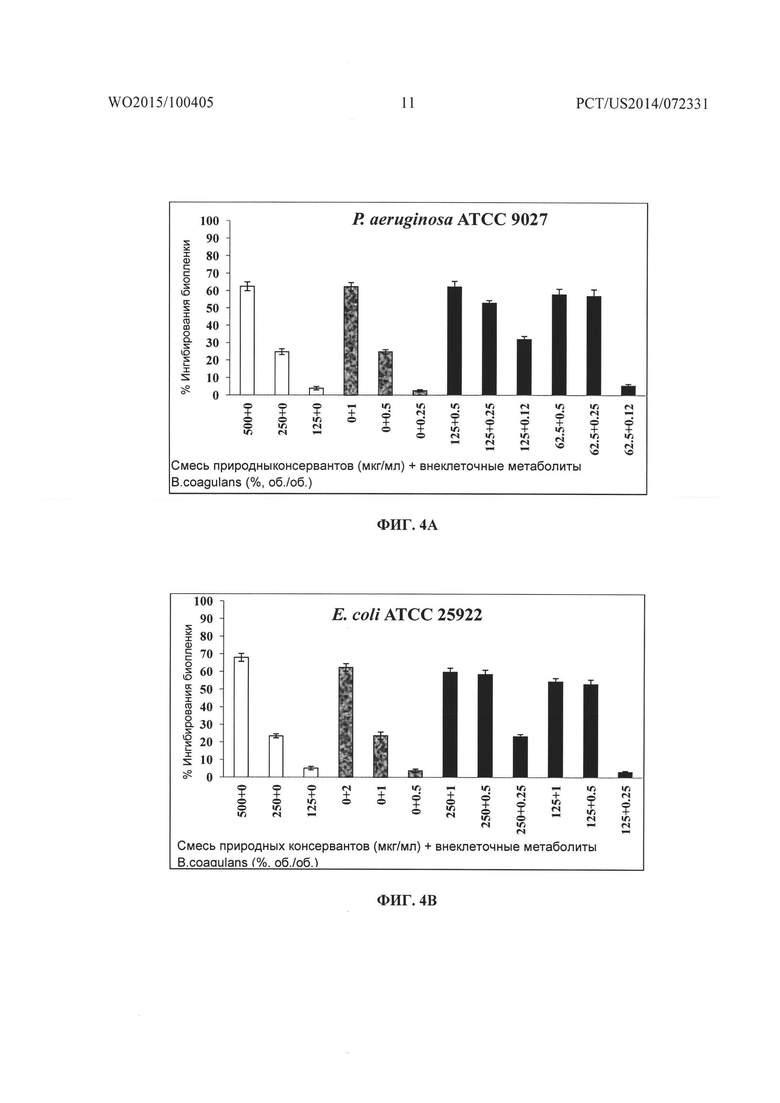
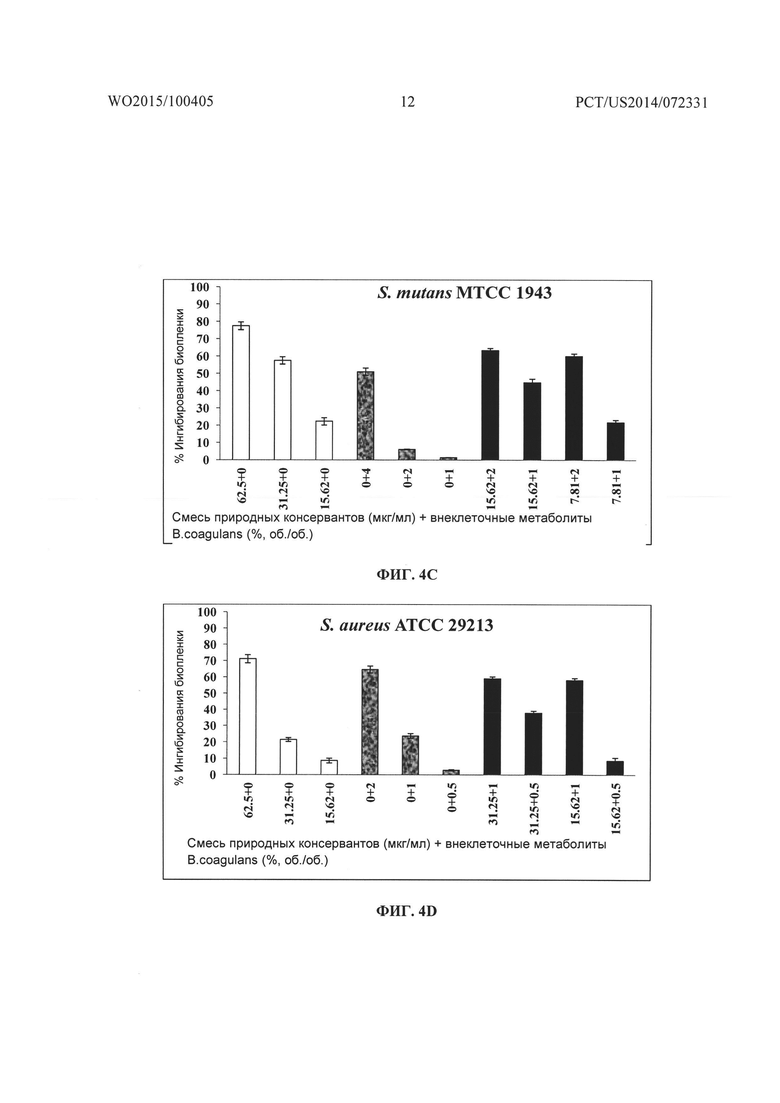
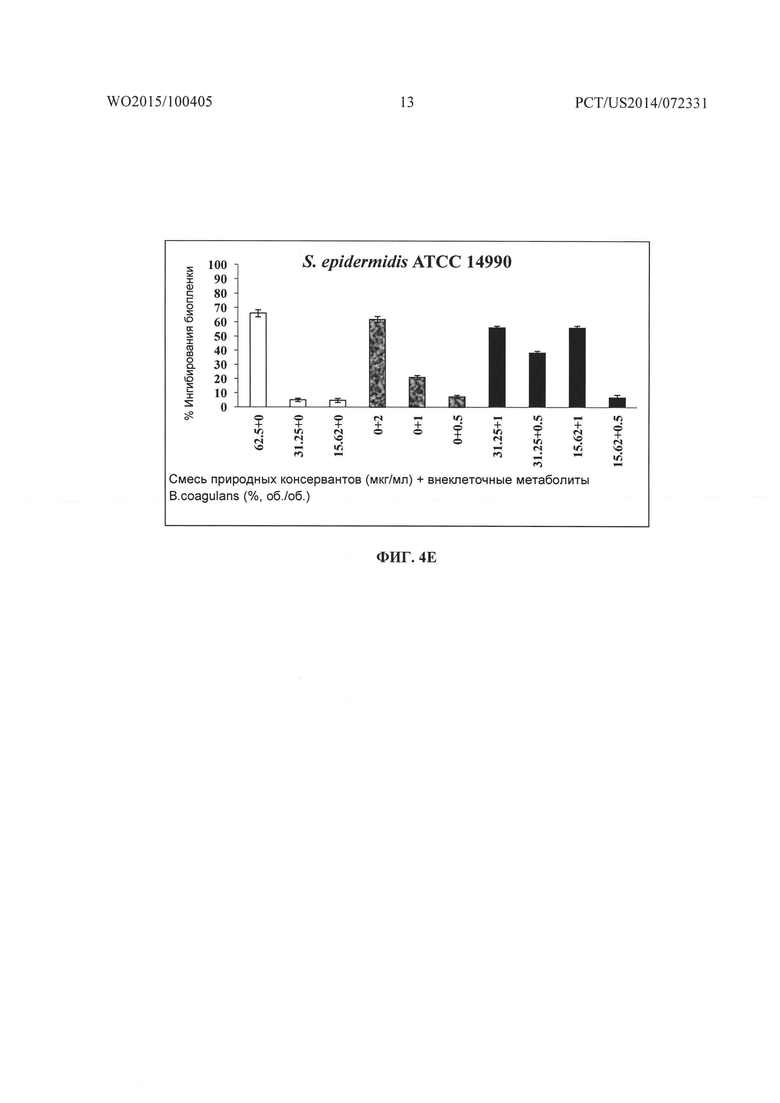
На Фиг. 4A, 4B, 4C, 4D и 4E соответственно показано графическое представление действия смеси природных консервантов и внеклеточных метаболитов В. coagulans MTCC 5856 отдельно и в комбинации на образование биопленки Pseudomonas aeruginosa ATCC 9027, Escherichia coli ATCC 25922, Streptococcus mutans MTCC 1943, Staphylococcus aureus ATCC 29213 и Staphylococcus epidermidis ATCC 14990.
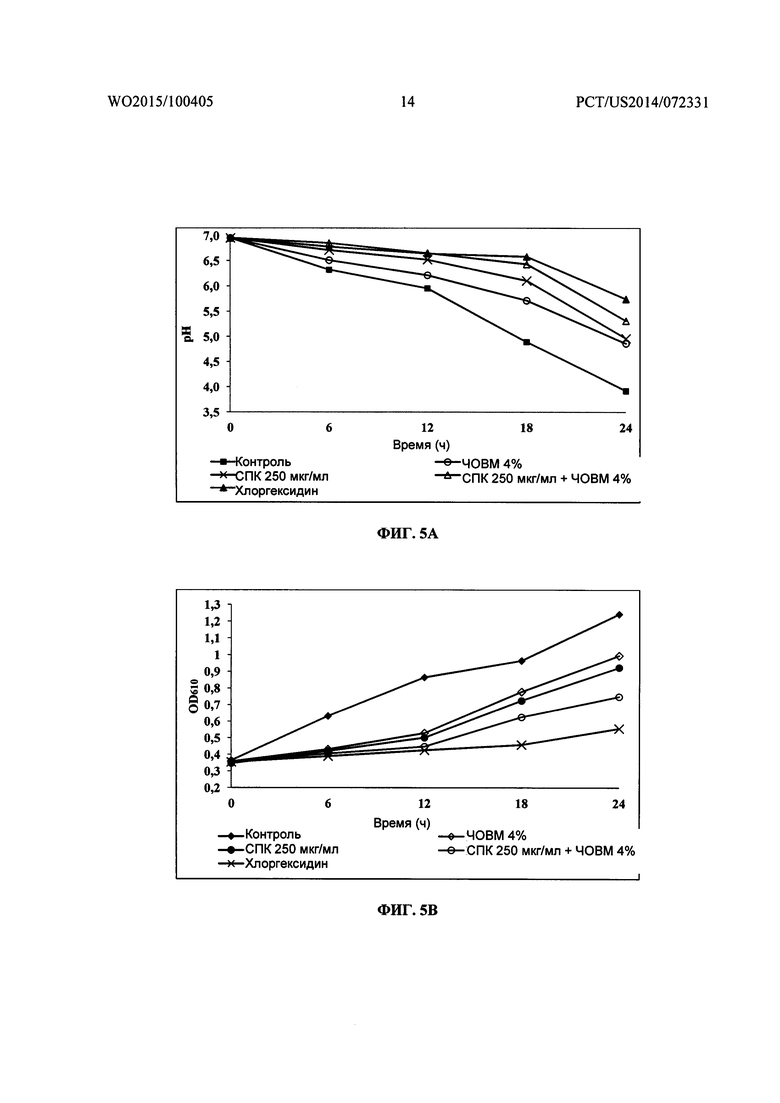
На Фиг. 5А и 5B соответственно показано графическое представление действия смеси природных консервантов и внеклеточных метаболитов В. coagulans MTCC 5856 на рост/снижение pH и образование не растворимых в воде глюканов биопленки S. mutans MTCC 1943 в присутствии 2% сахарозы.
Подробное описание наиболее предпочтительного варианта воплощения
В наиболее предпочтительном варианте воплощения настоящее изобретение относится к способу очистки для получении частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банк, и которому присвоен номер штамма MTCC 5856), демонстрирующего 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050, причем указанный способ очистки включает стадии:
1. Инокуляции культуры Bacillus coagulans MTCC 5856, демонстрирующей 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050, в 1,0 литре бульонной питательной среды дрожжевого экстракта с глюкозой и ацетатом (HiMedia, Мумбай, Индия) или бульонной питательной среды MRS, содержащей 0,5% твина-80, или в среды на основе порошка кукурузного экстракта;
2. Проведения ферментации в инокулированной на стадии 1 среде в течение 24-48 ч при 37°C и 120 об/мин;
3. Центрифугирования ферментативного бульона со стадии 2 при 4000-7000 об/мин;
4. Концентрирования супернатантов со стадии 3 в 10 раз с использованием роторного испарителя при 50°C.
5. Добавления по каплям 150 мл охлажденного ацетона к 100 мл сконцентрированных в десять раз супернатантов со стадии 4, с последующим перемешиванием;
6. Инкубирования смеси со стадии 5 при 0°C в течение 30 минут с последующим центрифугированием при 7000-8000 об/мин;
7. Удаления осадка, полученного на стадии 6, и сбора 60% насыщенного ацетоном супернатанта (приблизительно 200 мл).
8. Концентрирования насыщенного ацетоном супернатанта со стадии 7 до 50 мл при помощи роторного испарителя.
9. Доведения pH до 5,0 при использовании 4 н. HCl, фильтрования (фильтр с размером пор 0,22 микрона; Millex, Millipore, Индия) и хранения при -20°C до дальнейшего применения.
10. Лиофилизации/сушки распылением/сушки на поддоне супернатанта со стадии 8.
В еще одном наиболее предпочтительном варианте воплощения настоящее изобретение относится к способу микробиологического контроля, причем указанный способ включает стадию приведения в контакт эффективных концентраций частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банк, и которому присвоен номер штамма MTCC 5856), демонстрирующего 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050, и микробную клетку-мишень. В более конкретных вариантах воплощения микробная клетка может представлять собой клетку, выбранную из группы, содержащей Pseudomonas aeruginosa, Escherichia coli, Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus mutans, Propionibacterium acnes, Bacillus cereus и Salmonella abony.
В еще одном наиболее предпочтительном варианте воплощения настоящее изобретение относится к способу микробиологического контроля, причем указанный способ включает стадию приведения в контакт микробной клетки с эффективными концентрациями препарата, состоящего по существу из частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банк, и которому присвоен номер штамма MTCC 5856), демонстрирующего 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050, и синергической смеси консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis. В более конкретных вариантах воплощения микробная клетка может представлять собой клетку, выбранную из группы, содержащей Pseudomonas aeruginosa, Escherichia coli, Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus mutans, Propionibacterium acnes, Bacillus cereus и Salmonella abony.
В еще одном наиболее предпочтительном варианте воплощения настоящее изобретение также относится к способу ингибирования образования микробной биопленки, причем указанный способ включает стадию приведения в контакт продуцирующих биопленку микробных клеток и препарата, состоящего по существу из частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans SBC37-01 (депонированного в Коллекцию типовых культур микроорганизмов и Генетический банк, и которому присвоен номер штамма MTCC 5856), демонстрирующего 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans ATCC 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans ATCC 7050, отдельно или указанного препарата, скомбинированного с синергической смесью консервантов, содержащей приблизительно 61% масс./масс. тимола, приблизительно 38% монолаурина и приблизительно 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
Следующие примеры в настоящем описании представлены для иллюстрации вариантов воплощения настоящего изобретения.
Пример 1
Микроорганизмы и условия культивирования
Бактериальные штаммы, используемые в этом исследовании, включали Streptococcus mutans MTCC 1943, Staphylococcus aureus ATCC 29213, Staphylococcus epidermidis ATCC 14990, Escherichia coli ATCC 25922, Pseudomonas aeruginosa ATCC 9027, Salmonella abony NCIM 2257 и Bacillus cereus ATCC 14579. Референтные штаммы приобретены в ATCC (Американская коллекция типовых культур, Манассас, Вашингтон, США), MTCC (IMTECH, Чандигарх, Индия) и NCIM (Национальная коллекция промышленных микроорганизмов, Пуне, Индия). S. mutans и P. acnes поддерживали на агаре с сердечно-мозговым экстрактом (BHI; Difco Laboratories, Детройт, Мичиган, США) и усиленном клостридиальном агаре (RCA; HiMedia, Мумбай, Индия) соответственно. S. aureus, S. epidermidis Е. coli, P. aeruginosa, S. abony и В. cereus поддерживали на триптиказо-соевом агаре (Difco Laboratories) при 37°C. S. mutans и P. acnes инкубировали в анаэробных условиях (80% N2, 10% H2 и 10% CO2) при 37°C до 48 ч в анаэробной камере (Coy Laboratory Products Inc, Мичиган). Bacillus coagulans SBC37-01, используемый в исследовании, был описан и депонирован в Коллекцию типовых культур микроорганизмов, Чандигарх, Индия, и штамм был обозначен как Bacillus coagulans MTCC 5856.
Способ
Способ «шахматной доски» для исследования синергического действия
Представляет собой наиболее часто используемый способ для оценки антимикробных комбинаций in vitro. Термин "шахматная доска" относится к схеме (пробирок или лунок микротитровального планшета), получаемой множественными разведениями двух тестируемых лекарств (Eliopoulos GM, Moellering RC: Antimicrobial combinations. In Antibiotics in laboratory medicine. Edited by Lorian V. Baltimore, The Williams & Wilkins Co; 1991: 432-492). В настоящем исследовании шахматная доска состояла из столбцов, в которой каждая пробирка (или лунка) содержит то же самое количество частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans MTCC 5856, разведенного вдоль оси X (ряды), в которых каждая пробирка (или лунка) содержит то же самое количество смеси консервантов, разведенной вдоль оси Y (Фиг. 2). В результате каждая клетка на шахматной доске (которая соответствует одной пробирке/лунке или планшету) содержала уникальную комбинацию частично очищенного препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans MTCC 5856 и смеси консервантов. Диапазон концентраций смеси консервантов в настоящем исследовании составлял от 2000 мкг/мл до 31,25 мкг/мл и в некоторых случаях меньше, тогда как частично очищенный препарат внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans MTCC 5856 тестировали в диапазоне от 8% (об./об.) до 0,015% (об./об.). Этот способ с использованием шахматной доски можно осуществить с жидкими или полутвердыми (агаровыми) средами. Бульон BHI и бульон RC использовали для S. mutans и P. acnes соответственно, и планшеты инкубировали в анаэробных условиях (80% N2, 10% H2 и 10% CO2) при 37°C до 48 ч в анаэробной камере. Среду Мюллера-Хинтона (Difco) использовали для S. aureus, S. epidermidis Е. coli, P. aeruginosa, S. abony и В. cereus, и планшеты инкубировали при 37°C в течение 18 ч.
Кинетика подавления
Исследования подавления в зависимости от времени смесью консервантов и частично очищенным препаратом внеклеточного метаболита штамма Bacillus coagulans MTCC 5856 проводили против P. aeruginosa, Е. coli, S. aureus S. epidermidis, S. mutans, P. acnes, B. cereus и Salmonella abony, и оценивали с использованием способа с построением кривой зависимости подавления от времени, как описано ранее (Eliopoulus GM, Moellering RCJ. Antimicrobial combinations. In: Lorian V, ed. Antibiotics in Laboratory Medicine, 4th edn. Baltimore: Williams & Wilkins, 1996; 330-6). Бактериальную суспензию в своей логарифмической фазе (1×106 КОЕ/мл) использовали в качестве инокулума. Смесь консервантов и частично очищенный препарат внеклеточного метаболита штамма Bacillus coagulans MTCC 5856 тестировали по отдельности и в комбинации в различных концентрациях, определенных при анализе с использованием шахматной доски. Клеточную популяцию, выраженную в виде КОЕ/мл, определяли при помощи способа серийного разведения в трех параллелях на соответствующих средах и инкубировали в соответствующих условиях роста. Подсчет количества жизнеспособных микроорганизмов и определение поглощения (OD610) осуществляли в 0 момент (необработанный контроль), и после 24 ч инкубации при 37°C. Подсчет количества жизнеспособных микроорганизмов выражали в Log10 КОЕ/мл, а поглощение выражали в виде величины OD при 610 нм.
Анализы чувствительности биопленки
Ингибирующее биопленку действие смеси консервантов и частично очищенного препарата внеклеточного метаболита штамма Bacillus coagulans MTCC 5856 по отдельности и в комбинации исследовали по сравнению с S. mutans, Е. coli, S. aureus S. epidermidis и P. aerugenosa при помощи способа микроразведения (Wei et al. Journal of Antimicrob. Chemother. 2006. 57: 1100-1109). Этот способ был аналогичным способу для пассивноплавающих клеток с использованием шахматной доски. Для анализа биопленки S. mutans использовали бульон BHI, дополненный 2% сахарозой. В случае других организмов в исследовании использовали TSB, дополненный 2% глюкозой. Бактериальные суспензии готовили из суточной культуры, и мутность суспензии доводили до оптической плотности при 610 нм (A610), равной 0,7 (1×109 КОЕ/мл). Диапазон концентраций смеси консервантов в настоящем исследовании составлял от 2000 мкг/мл до 31,25 мкг/мл и в некоторых случаях меньше, тогда как частично очищенный препарат внеклеточного метаболита штамма Bacillus coagulans MTCC 5856 тестировали в диапазоне от 8% (об./об.) до 0,015% (об./об.). Сорок микролитров свежего питательного бульона добавляли в каждую лунку, а затем в каждую лунку планшета добавляли по 60 мкл указанной выше суспензии. Последнее приводило в результате к окончательному инокулуму 6×107 КОЕ/мл в каждой лунке; после инкубации при 37°C в течение 48 ч культуральный супернатант из каждой лунки отбирали и пассивноплавающие клетки удаляли путем промывания лунок физиологическим раствором, забуференным фосфатом (PBS; pH 7,2). Биопленку фиксировали метанолом в течение 15 мин и затем сушили на воздухе при комнатной температуре. Лунки высушенного планшета окрашивали 0,1% (масс./об.) кристаллического фиолетового (Sigma Chemical Co., Сент-Луис, Миссури) в течение 10 мин и тщательно промывали водой до тех пор, пока лунки с отрицательным контролем не окажутся бесцветными. Образование биопленки количественно оценивали путем добавления 200 мкл 95% этанола к клеткам, окрашенным кристаллическим фиолетовым, и при регистрации поглощения при 595 нм (A595). Процент ингибирования биопленки рассчитывали с использованием уравнения (A595 биопленки, обработанной тестируемым агентом/A595 необработанного контроля) × 100. Культуру без тестируемого агента использовали в качестве необработанного контроля.
Антимикробная активность против адгезированных S. mutans в нерастворимом в воде глюкане
Образование не растворимого в воде глюкана S. mutans MTCC 1943 осуществляли в соответствии с ранее описанным способом (Katsura et al., Antimicrob. Agents Chemother. 2001. 45: 3009-3013). Кратко, аликвоты 100 мкл культуры S. mutans MTCC 1943 (приблизительно 1×108 клеток/мл) инокулировали в 10 мл свежего бульона BHI, содержащего 2% сахарозу (масс./об.) в тестируемых пробирках, и инкубировали при 37°C в течение 24 ч при наклоне 30°. Жидкость, содержащую пассивноплавающие клетки, осторожно удаляли. Не растворимый в воде глюкан, содержащий клетки S. mutans MTCC 1943, осторожно промывали 10 мл стерильной воды и ресуспендировали в 10 мл фосфатного буфера (10 мМ, pH 5,0), содержащего смесь консервантов и частично очищенный препарат внеклеточного метаболита штамма Bacillus coagulans MTCC 5856 по отдельности и в комбинации, с последующей инкубацией при 37°C в течение 5 мин. Хлоргексидин 0,12% (об./об.) (Sigma Chemical Co., Сент-Луис, Миссури) использовали в качестве внутреннего контроля в исследовании. Смесь вновь осторожно промывали стерильным физиологическим раствором (0,89% NaCl, масс./об.), а затем обработанные клетки ресуспендировали в 10 мл бульона BHI, содержащего 2% сахарозу (масс./об.). После инкубации клеток при 37°C в течение 6, 12, 18 и 24 ч количество кислоты, продуцируемой культурой, измеряли с использованием pH-метра. Жидкость, содержащую свободные клетки S. mutans MTCC, осторожно удаляли. Не растворимый в воде глюкан ресуспендировали в 10 мл 1 н. раствора NaOH и гомогенизировали; мутность измеряли при 610 нм.
Результаты:
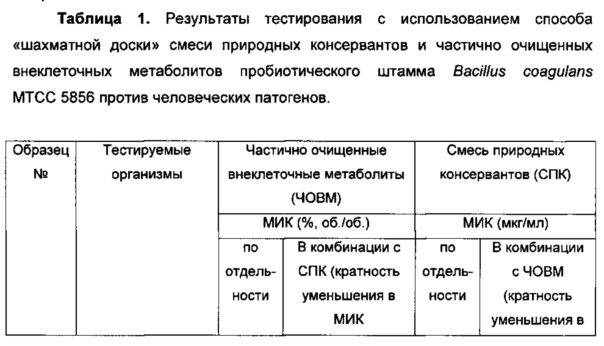
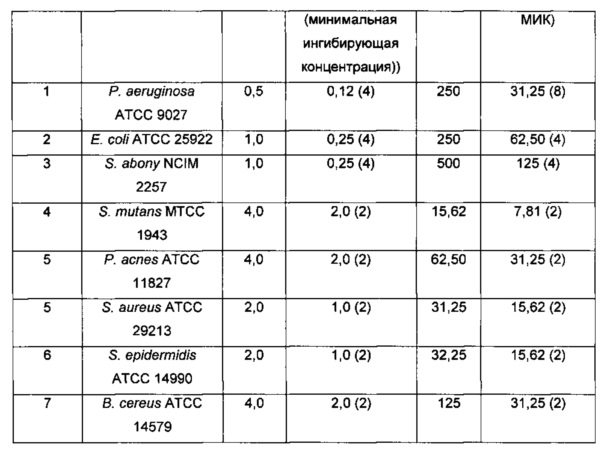
Таблица 1 демонстрирует кратное уменьшение человеческих микробных патогенов при приведении в контакт с композициями А, содержащими только частично очищенные внеклеточные метаболиты (ЧОВМ) или смесь природных консервантов (СПК); и с композициями Б, включающими как частично очищенные внеклеточные метаболиты (ЧОВМ), так и смесь природных консервантов (СПК). Можно отметить, что композиции, включающие как частично очищенные внеклеточные метаболиты (ЧОВМ), так и смесь природных консервантов (СПК), вызывают значимое восьмикратное уменьшение патогена Pseudomonas aeruginosa и четырехкратное уменьшение патогена Escherichia coli.
Несмотря на то, что изобретение описано со ссылкой на предпочтительный вариант воплощения, специалисту в данной области техники понятно, что изобретение не ограничивается этим. Более того, объем изобретения должен интерпретироваться только в комбинации с формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОЗАГРЯЗНЯЮЩИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ BACILLUS COAGULANS | 2018 |
|
RU2745755C1 |
| СИНЕРГИЧЕСКИЕ СЕЛЕНОПЕПТИДНЫЕ ПРЕПАРАТЫ ДЛЯ ЗАЩИТЫ ДЕРМАЛЬНЫХ СОСОЧКОВЫХ КЛЕТОК | 2012 |
|
RU2606752C2 |
| Новый пробиотический препарат на основе консорциума спорообразующих бактерий для аквакультуры и животных и способ его получения | 2022 |
|
RU2799554C1 |
| ХАЛКОНЫ В КАЧЕСТВЕ УСИЛИТЕЛЕЙ АНТИМИКРОБНЫХ СРЕДСТВ | 2009 |
|
RU2521252C2 |
| ЭКСТРАКТ КОРЫ МАГНОЛИИ В КАЧЕСТВЕ ГИДРОФОБНОГО ЛИГАНДА ДЛЯ ПРЕИМУЩЕСТВЕННОГО УДАЛЕНИЯ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ ИЗ РОТОВОЙ ПОЛОСТИ | 2016 |
|
RU2744578C2 |
| КОМПОНЕНТЫ НА ОСНОВЕ МИКРООРГАНИЗМА РОДА BACILLUS ДЛЯ ИНГИБИРОВАНИЯ ИЛИ ЗАМЕДЛЕНИЯ РОСТА ENTEROCOCCUS SPP. У ЖИВОТНЫХ | 2017 |
|
RU2789148C2 |
| Бесклеточная культуральная жидкость на основе штамма Bacillus subtilis, консервант для силоса и полифункциональное средство для растений с фунгицидными, бактерицидными и ростстимулирующими свойствами | 2017 |
|
RU2665547C1 |
| СРЕДСТВО ДЛЯ СЕЛЕКТИВНОГО ВЛИЯНИЯ НА БИОПЛЕНКООБРАЗОВАНИЕ МИКРООРГАНИЗМАМИ | 2016 |
|
RU2646488C2 |
| АКТИВНАЯ БИОЛОГИЧЕСКАЯ СУБСТАНЦИЯ "ИНГАЛИПТ АКТИВ ПЛЮС" (INGALIPTUM ACTIVE PLUS), ПОЛУЧЕННЫЙ НА ЕЁ ОСНОВЕ ПРЕПАРАТ МЕСТНОГО ДЕЙСТВИЯ | 2016 |
|
RU2639562C1 |
| КАЛЕБИН А ПРИ ЖИРОВОМ ГЕПАТОЗЕ | 2015 |
|
RU2643297C2 |

Группа изобретений относится к биотехнологии. Предложены способ получения препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans MTCC 5856, способы контроля роста и жизнеспособности микробных патогенов, способ ингибирования образования микробной биопленки, а также способ предупреждения дальнейшего накопления биопленки Streptococcus mutans и обусловленного этим снижения рН. Инокулируют культуру Bacillus coagulans МТСС 5856 в бульонной питательной среде. Проводят ферментацию, центрифугируют ферментативный бульон, концентрируют супернатант, добавляют охлажденный ацетон и перемешивают, инкубируют с последующим центрифугированием, собирают насыщенный ацетоном 60% супернатант, концентрируют при помощи роторного испарителя, доводят рН до 5, фильтруют и хранят при -20°С либо проводят лиофилизацию или сушку распылением, или сушку на поддоне. Полученный препарат внеклеточного метаболита Bacillus coagulans MTCC 5856 отдельно или в комбинации с синергетической смесью консервантов ингибирует рост Pseudomonas aeruginosa, Escherichia coli, Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus mutans, Propionibacterium acnes, Bacillus cereus и Salmonella abony и образование микробной биопленки. Смесь консервантов содержит приблизительно 61% масс./масс. тимола, 38% монолаурина и 1% масс./масс. магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis. 5 н.п. ф-лы, 25 ил., 1 табл., 1 пр.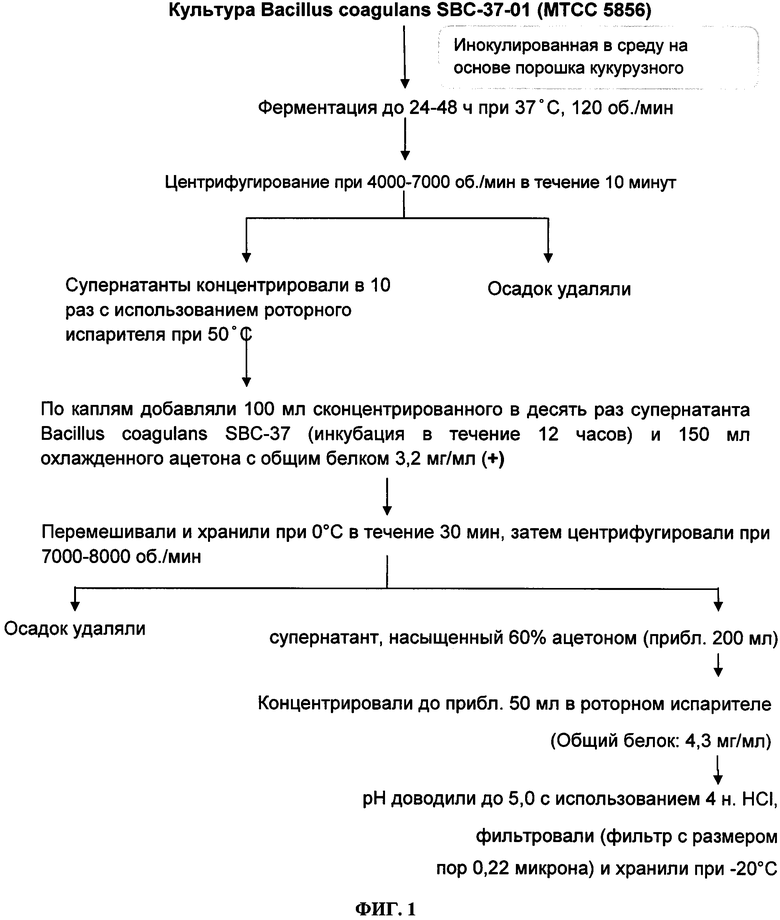
1. Способ получения препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans, депонированного в МТСС под номером 5856, причем указанный способ включает следующие стадии:
a) инокуляция культуры Bacillus coagulans МТСС 5856, демонстрирующей 99% генетической гомологии с известными бактериальными штаммами Bacillus coagulans АТСС 31284, Bacillus coagulans NBRC 3887 и Bacillus coagulans АТСС 7050, в 1,0 л бульонной питательной среды дрожжевого экстракта с глюкозой и ацетатом или бульонной питательной среды MRS, содержащей 0,5% твин-80 или среды на основе порошка кукурузного экстракта;
b) проведение ферментации в инокулированной на стадии а) среде в течение 24-48 ч при 37°С и 120 об/мин;
c) центрифугирование ферментативного бульона, полученного на стадии b), при 4000-7000 об/мин;
d) концентрирование супернатантов, полученных на стадии с), в 10 раз с использованием роторного испарителя при 50°С;
e) добавление по каплям 150 мл охлажденного ацетона к 100 мл сконцентрированных в десять раз супернатантов, полученных на стадии d), с последующим перемешиванием;
f) инкубирование смеси, полученной на стадии е), при 0°С в течение 30 минут с последующим центрифугированием при 7000-8000 об/мин;
g) удаление осадка, полученного на стадии f), и сбор насыщенного ацетоном 60% супернатанта;
h) концентрирование насыщенного ацетоном супернатанта, полученного на стадии g), до 50 мл при помощи роторного испарителя;
i) доведение рН до 5,0 при использовании 4 н. HCl, фильтрование и хранение при -20°С до дальнейшего применения;
j) лиофилизация/сушка распылением/сушка на поддоне супернатанта, полученного на стадии h).
2. Способ контроля роста и жизнеспособности микробных патогенов, включающий стадию приведения в контакт эффективных концентраций препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans, депонированного в МТСС под номером 5856, полученного способом по п. 1, и микробной клетки-мишени, представляющей собой клетку, выбранную из группы, содержащей Pseudomonas aeruginosa, Escherichia coli, Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus mutans, Propionibacterium acnes, Bacillus cereus и Salmonella abony.
3. Способ контроля роста и жизнеспособности микробных патогенов, включающий стадию приведения в контакт микробной клетки с эффективными концентрациями препарата, состоящего по существу из препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans, депонированного в МТСС под номером 5856, полученного способом по п. 1, и синергической смеси консервантов, содержащей приблизительно 61 масс./масс.% тимола, приблизительно 38% монолаурина и приблизительно 1 масс./масс.% магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis, где микробная клетка представляет собой клетку, выбранную из группы, содержащей Pseudomonas aeruginosa, Escherichia coli, Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus mutans, Propionibacterium acnes, Bacillus cereus и Salmonella abony.
4. Способ ингибирования образования микробной биопленки, включающий стадию приведения в контакт продуцирующих биопленку микробных клеток и препарата, состоящего по существу из препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans, депонированного в МТСС под номером 5856, полученного способом по п. 1, отдельно или в комбинации с синергической смесью консервантов, содержащей приблизительно 61 масс./масс.% тимола, приблизительно 38% монолаурина и приблизительно 1 масс./масс.% магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis, где продуцирующая биопленку микробная клетка представляет собой клетку, выбранную из группы, содержащей Pseudomonas aeruginosa, Escherichia coli, Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus mutans.
5. Способ предупреждения дальнейшего накопления биопленки Streptococcus mutans и обусловленного этим снижения рН в присутствии сахарозы, включающий стадию приведения в контакт продуцирующего биопленку/бляшки Streptococcus mutans и препарата, состоящего по существу из препарата внеклеточного метаболита пробиотического бактериального штамма Bacillus coagulans, депонированного в МТСС под номером 5856, полученного способом по п. 1, отдельно или в комбинации с синергической смесью консервантов, содержащей приблизительно 61 масс./масс.% тимола, приблизительно 38% монолаурина и приблизительно 1 масс./масс.% магнолола, полученного из сверхкритических жидких экстрактов Magnolia officinalis.
| US 20040197277 A1, 07.10.2004 | |||
| RIAZI S | |||
| et al | |||
| "Characterization of lactosporin, a novel antimicrobial protein produced by Bacillus coagulans ATCC 7050", Journal of applied microbiology, 2009, v.106, no.4, p.1370-1377 | |||
| MAJEED M | |||
| et al | |||
| "Bacillus coagulans: Probiotic of choice Introduction", Prebiotics/probiotics, NutraCos, 2012, p.19-21 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| US 2010120911 A1, 13.05.2010 | |||
| ШТАММ BACILLUS COAGULANS SIM-7 DSM 14043 ДЛЯ ПОЛУЧЕНИЯ L(+)-ЛАКТАТА И СПОСОБ ПОЛУЧЕНИЯ L(+)-ЛАКТАТА | 2002 |
|
RU2288263C2 |
| ШТАММ БАКТЕРИЙ BACILLUS COAGULANS - ПРОДУЦЕНТ ЭНДОНУКЛЕАЗЫ РЕСТРИКЦИИ, УЗНАЮЩЕЙ И РАСЩЕПЛЯЮЩЕЙ ПОСЛЕДОВАТЕЛЬНОСТЬ НУКЛЕОТИДОВ 5'-GATNNNNATC-3' | 1994 |
|
RU2057806C1 |
Авторы
Даты
2017-04-28—Публикация
2014-12-24—Подача